2.10. Az elegyek termodinamikája
|
|
|
- Margit Pásztorné
- 9 évvel ezelőtt
- Látták:
Átírás
1 Kéma termodamka.1. z elegyek termodamkája fzka kéma több féle elegyekkel foglakozk, kezdve az deáls elegyektől a reáls elegyekg. Ha az deáls elegyek esetébe az alkotók közt kölcsöhatásokat elhayagoljuk, a reáls elegyek eseté a kölcsöhatások sokfélék lehetek, egész a kéma reakcókg. gáz elegyek esetébe már láttuk, hogy va külöbség az deáls vselkedés és a reáls vselkedés között. zt s láttuk, hogy a gázelegy yomása az alkotók parcáls yomásáak az összege, vagys mdegyk gáz kompoes hozzájárulása a teljes yomáshoz aráyos a gáz elegybe lévő kocetrácójával, móltörtjével. Ezt az elvet s tovább haszálva, vezessük be a parcáls molárs meységeket, vagys a parcáls molárs térfogat és a parcáls molárs szabadetalpa fogalmát parcáls molárs térfogat parcáls molárs térfogat em más, mt az a térfogat hozzájárulás, amellyel az elegy valamely kompoese hozzájárul a teljes elegytérfogathoz. Eek megsmerésére, duljuk k két kísérlet eredméyből. z első esetbe vegyük agy meységű tszta vzet, melyhez adjuk hozzá 1 mol vzet. Meyvel fog ő az elegy térfogata? Tudjuk, hogy egy mól víz tömege 18 g. Ha kszámítjuk térfogatát, akkor felírható: V=m/ρ=18/1=18 ml Ha megmérék a térfogatváltozást, akkor 18 ml kapák. Ha azoba ugyaay vzet adagoluk agy meységű alkoholhoz,.6. ábra. víz és az alkohol parcáls akkor a keverék térfogata csak molárs térfogata 98 K hőmérséklete 14 ml értékkel ő. Ez azt és 1 atm yomáso[8]. jelet, hogy míg az első esetbe a víz térfogat hozzájárulása 18 ml, a másodkba csak 14 ml (lásd a.6. 66
2 Fejezetek a fzka kémából ábrát). külöböző térfogat-hozzájárulás attól függ, hogy mey helyet foglalak el vízmolekulák az elegybe. z első esetbe a szerkezetük em változk, hsz vzet keverük vízzel, a másodkba ellebe, az alkohol megváltozatja a vízmolekulák egymáshoz való vszoyát, hsz az alkoholba most mdegyk vízmolekula körül va véve alkohol molekulákkal, s így a karaktersztkus vízszerkezet megbomlk. Modhatjuk tehát, hogy az ayag parcáls molárs térfogata az a térfogatváltozás, amt a agymeységű elegyhez hozzáadott 1 mol ayag okoz. Egy bzoyos ayag parcáls molárs térfogatát az alábbak szert defálhatjuk: V j V (.195) j p, T, ' ahol azt jelképez, hogy a több ayag meysége álladó. parcáls molárs térfogat em más, mt a térfogat ayagmeység függvéy meredeksége (lásd a.7. ábrát). defícó szert, ha és ayagot tartalmazó elegy összetételét d ayag és d ayag hozzáadásával megváltoztatjuk, akkor az elegy térfogata a következők szert változk: V V dv d d (.196) p, T, p, T, vagys: dv V d V d (.197) Itegrálva: V V V (.198).7. ábra. parcáls molárs térfogat em más, mt a teljes térfogat és összetétel függvéy meredeksége. ár a térfogat mdg poztív marad, a parcáls molárs térfogat értéke lehet egatív s. Például, ha vízhez adagoluk 1 mol MgSO 4 -ot, akkor a teljes térfogat 67
3 Kéma termodamka 1,4 cm 3 értékkel csökke, mert a só megváltoztatva a víz szerkezetét, az összehúzódk az ook hdratácója sorá..1.. parcáls molárs szabadetalpa Épp úgy, ahogy a térfogatra meghatároztuk a parcáls molárs hozzájárulást, ez mde extezív meységre s felírható. szabadetalpa esetébe s, úgy mt, ahogy a belső eergára defáltuk, aak az ayagmeység szert parcáls derváltja em más, mt a kéma potecál, tehát: p, T, ' 68 (.199) Ie látható, hogy a kéma potecál a szabadetalpa ayagmeység függvéyébe ábrázolt görbe meredeksége, ameybe a yomás, a hőmérséklet és több alkotó ayagok meysége álladó. Ha az elegyük két kompoest tartalmaz, akkor arra a szabadetalpa változást úgy írhatjuk fel, mt parcáls dervált változó dfferecál szorzatok összege: d d d (.) p, T, p, T, vagys d d d (.1) ahoa, tegrálva, a következő összefüggést kapjuk: (.) amelybe a, - a kéma potecál értéke (Jmol -1 ) az adott összetételbe. z összefüggésből jól látható, hogy az elegy szabadetalpáját az elegybe lévő ayagok és azok kéma potecálja határozza meg. Egy meghatározott yílt redszerbe a szabadetalpa változk a yomás, a hőmérséklet és az ayagmeység függvéyébe. Ez azt jelet, hogy a zárt redszerre felírt d Vdp SdT összefüggés yílt redszerek esetébe a kővetkező alakot ölt: d Vdp SdT d d (.3) Ez képez a kéma termodamka alapvető egyeletét. Álladó yomáso és zoterm körülméyeke az egyelet a következő alakot ölt: d d d... (.4)
4 Fejezetek a fzka kémából Ez azt jelet, hogy a szabadetalpa változás, mt a em térfogat muka mértéke, felírható: d dl d d (.5) tfm em térfogat muka a redszer összetételéek megváltozásból származk. Meg kell jegyez, hogy a kéma potecál több mt a szabadetalpa összetétel függvéye. Ismerve a szabadetalpa és belső eerga összefüggést, be lehet köye bzoyíta, hogy a kéma potecál úgy a belső eerga, mt az etalpa, mt a szabadeerga összetétel függvéyére s alkalmas. Tudjuk, hogy a szabad etalpa defícójából, hogy =H-TS=U+pV-TS, ahoa U=-pV+TS. Írjuk fel a belsőeerga dfferecálját: du d pdv Vdp SdT TdS (.6) Helyettesítsük be de a d: du pdv Vdp SdT TdS ( Vdp SdT d d...) (.7) Ie felírható: du pdv TdS d d.. (.8) Tehát most egy olya összefüggést kaptuk, amely leírja, hogy hogya változk a belső eerga a térfogat, az etrópa és az összetétel függvéyébe. bba az esetbe, amkor a térfogat és az etrópa kostas, fel lehet ír: du d d.. (.9) amből következk a már smert összefüggés: S, V, ' U (.1) Ugyaúgy be lehet bzoyíta, hogy a kéma potecál az etalpa összetétel vagy a belső eerga összetétel függvéy meredeksége, amkor a yomás, a hőmérséklet, lletve a hőmérséklet, térfogat és a több összetevő álladó. H (.11) vagy: p, T, ' 69 F (.1) T, V, ' Ismertek a szabadetalpa defícós egyelete: d d d (.13) és (.14) Írjuk fel a (.13) egyelet dfferecálját: d d d d d (.15)
5 Kéma termodamka hhoz, hogy mdkét dfferecáls összefüggés leírhassa a jeleséget szükséges, hogy d d (.16) Ez em más, mt az smert bbs-duham összefüggés, amelyből azt lehet kolvas, hogy az egyk kompoes kéma potecálja em változhat a másk kompoes kéma potecáljától függetleül [5,7,9,1], vagys: d d (.17) Ha az egyk övekedk, akkor a máskak csökkee kell. Ez a kjeletés érvéyes em csak a kéma potecálra, haem mdegyk parcáls molárs meységre s, köztük a térfogatra. 15. y. Ismert, hogy a K SO 4 aq, parcáls molárs térfogatát 98 K hőmérséklete a következő összefüggés írja le: V 3,8+18,1C,5 ml/mol, ahol a C, a KSO4 ( aq) szulfát oldat molaltása. lkalmazva a bbs-duham összefüggést, határozzuk meg a víz molárs térfogatát megadó összefüggést. dott a tszta víz móltérfogata ( V H 18, 79 O ml/mol) [9]. Megoldás: Legye a szulfát és a víz. Felírva bbs Duham aalógát: dv dv (.18) Ie: dv V dv (.19), Itegrálva: V V dv ö V,5 V 3,8 18,1C összefüggésből, következk (.) dv,5, 5 9,15C dv 9,15C dc (.1) dc ehelyettesítve az tegrálba, felírható: C,5 V V C dc 9,15 (.) Ismerve, hogy az molaltása: C, ahol M =18,.1-3 kg/mol, fel lehet ír: m M szolves 7
6 V V C Fejezetek a fzka kémából,5 9,15 C M C dc (.3) Megoldva a kővetkező őszfüggést kapjuk: 3/ V 18,79,194C ml/mol. (.4).1.3. z elegyedés szabadetalpa változás Vegyük egy és egy kompoest tartalmazó tartályt, amelyekbe a yomás p és a hőmérséklet T. z egyk tartályba meységű, a máskba meységű gáz va. Kössük össze a két tartályt, azért hogy alakuljo k az (+) keverék. Mvel a két tartályba a gázok tszták, lyekor a két gáz kéma potecálja a tszta ayagra voatkoztatható. keverék kezdet szabadetalpája kfejezhető a (.) összefüggés fgyelembe vételével, tudva, hogy a molárs szabadetalpa em más, mt a kéma potecál, vagys: p p RT l RT l (.5) p p Ha p-t úgy tektjük, mt a RT l p RT l p p -ra voatkoztatott yomást, akkor felírható: (.6) keverés utá, amkor az parcáls yomás p, a -é pedg p lesz, fel tudjuk ír: f RT l p RT l p (.7) keverés szabadetalpa változás pedg: p p f RT l RT l (.8) p p j Fgyelembe véve a móltörtet, vagys x j fel tudjuk ír egyfelől: p p x, x (.9 a,b) másfelől x; x (.3 a,b) p p ehelyettesítve az összefüggésébe, fel lehet ír RT x l x x l x (.31) f 71
7 Kéma termodamka keveredés szabadetalpa egyeese aráyos a hőmérséklettel, és függetle a yomástól. Mvel a móltört mdg ksebb, mt egy, aak logartmusa egatív, am azt jelet, hogy, vagys az deáls gázok mdég spotául keveredek. 16. y. Legye egy csappal elválasztott két egyelő részes tartályuk, amelyek egyk felébe 3 mol H, a máskba 1 mol N va 98 K hőmérséklete. Határozzuk meg a szabadetalpa-változást, ha az elválasztást megszűtetjük [9]. Megoldás: Legye a trogé yomása p és a tartály két részére érvéyes, hogy V 1 =V. Izocor és zoterm körülméyeke, ha a trogé yomása p, a háromszor több mól gázt tartalmazó tartályba a yomás 3 p lesz. kezdet szabadetalpa tehát: RT l3 p 1 RT l p 3 H N 1 z elegyedés következtébe a trogé parcáls yomása p N= p/ míg a hdrogéé, p H =3p/ lesz. keverék szabadetalpája, tehát: 3 1 f 3 H RT l p 1 N RT l p z elegyedés szabadetalpa, tehát: 1,5 1 3RT l 1RT l 3RT l RT l 4RT l 6869 J 3 Mvel az elegyedés álladó hőmérséklete törték, meghatározható az elegyedés etalpa s. Először számítsuk k a keveredés etrópát: S T RT x l x x l x, ehelyettesítve a keveredés szabadetalpát: következk: RT ( x S l x T x l x 7 R( x l x x l x Látható, hogy a keveredés etrópa mdg poztív. Ha most az előbb gyakorlatra vsszatérük, akkor fel tudjuk ír, hogy: S 4Rl 3,5 J/K Ha fgyelembe vesszük a szabadetalpa defícóját és kfejezzük az etalpaváltozást, következk: )
8 H TS H Fejezetek a fzka kémából T S ,598 Látható, hogy a keveredés etalpaváltozás majdem ulla, am azt jelet, hogy a keveredés szabadetalpa változása egatív, míg az etrópája poztív, vagys a folyamat spotául valósul meg, etalpaváltozás élkül Folyadékelegyek folyadékelegyekbe a kompoesek mozgástere valamelyest korlátozott, hsz a részecskék elég közel állak egymáshoz. Ez azért em zárja k a külöböző fázsegyesúlyok kalakulását, vagys azt, hogy a kompoes átmeje az egyk fázsból a máskba Ideáls folyadékelegyek. folyadékelegyeket épp úgy, mt a gázelegyeket, a tszta alkotók összekeverésével állíthatjuk elő. Mt láttuk, a vegytszta ayag kéma potecálja gázfázsba felírható: p RT p l (.3) ha a yomást relatív yomáskét fejezzük k, akkor: RT l p (.33) bba az esetbe, amkor keverékkel álluk szembe, akkor az kompoes gázfázsba mért kéma potecálját a parcáls yomás függvéyébe fejezhetjük k, éspedg: RT l p (.34) Kfejezve a tszta kompoes stadard kéma potecálját, és behelyettesítve az utóbbba, következk: p l l l RT p RT p RT (.35) p Hasoló ayagok keverékét elemezve Raoult azt tapasztalta, hogy a logartmus alatt aráy sok esetbe megfelel a kompoes folyadék fázsba mért móltörtjéek. Így Raoult törvéye az deáls elegyekre a következő alakot ölt: p x p (.36) am azt jelet, hogy az deáls elegyek esetébe az kompoes oldat felett gőzyomása egyelő a tszta ayag gőzyomásáak és az kompoes folyadékbel móltörtjéek szorzatával. Tehát egy változó összetételű 73
9 Kéma termodamka kétkompoesű elegy esetébe az.8. ábráak megfelelő összefüggések írják le a kompoesek parcáls yomásáak és teljes yomásak a változását [6,9,1]. valóságba agyo sok elegyre em modható, hogy betartaá Raoult törvéyét. Egy bárs deáls elegybe úgy az oldott ayag, mt az oldószer követ Raoult törvéyét. reáls elegyekél azoba, bár a kompoes parcáls yomása egyees aráyba változk a móltörttel, de az álladó értéke em a tszta ayag gőzyomásával egyelő. Ezekre az elegyekre határozta meg Hery a evét vselő törvéyt, vagys: p x H (.37) amelybe H - a Hery álladó, kompoesre jellemző és yomás mértékegységű. Megfgyelve a.9. ábrát látjuk, hogy a Hery álladó, em más, mt a kísérlet görbe kduló potjába húzott egyees meredeksége. p Teljes yomás p Hery törvéy p =H. x p Valós görbe Raoult törvéy x.8. ábra. Raoult törvéye az + elegyre. X mol/mol.9 ábra. Hery törvéyéek ábrázolása. 17. y. Határozzuk meg az oxgé oldékoyságát (mol/l) vízbe p=16 torr yomáso 7 és 98 K hőmérséklete, smerve a Hery álladó értékét ( H O 3,3 1 torr ) [9]. Megoldás: Hery törvéyből fel lehet ír: po 16 x O,481 7 H 3,3 1 O Ismerve a móltörtet, k lehet számíta a mólkocetrácót: 5 74
10 Fejezetek a fzka kémából O x x O T O HO HO C x O O V V V V Ha 1 lterbe lévő vízmeységet számoljuk, akkor felírható: mh O H O M H O H O CO xo xo xo,481,661 moll V V M H O 18 Két folyadék halmazállapotú ayag keverésekor fellépő szabadetalpa változását épp úgy határozzuk meg, mt a gázok esetébe. Ha a kduló ayagok egymástól el vaak választva, akkor a teljes szabadetalpa a két ayag szabadetalpájáak az összege: (.38) z elegy keletkezésekor a szabadetalpa pedg: f RT l x RT l x (.39) így a szabadetalpa-változás egyelő: RT x l x x l x (.4) T két folyadék elegyedés etrópa-változása pedg: T S T R x l x x l x (.41) z deáls folyadékelegyekbe, az deáls gázoktól eltérőe, ahol a cseek kölcsöhatások, tt ezek em zárhatók k, és az dealítás abból áll, hogy az elegybe fellépő kölcsöhatások em külöbözek az vagy kölcsöhatásoktól. z deáls folyadékelegyek esetébe scs etalpaváltozás, a spotaetást tt s a szabadetalpa-változás ksebb mt ulla, vagy az etrópa változás agyobb mt ulla értéke modják meg Valós folyadékelegyek. valóságba azoba az kölcsöhatások mások lehetek, mt az vagy kölcsöhatások. Tehát felléphet az etalpa-változás, hsz az új kölcsöhatás eredméyekét az etalpaváltozás és az etrópa-változás hőmérséklet szorzat külöbség most em ulla. Lehet ksebb vagy agyobb, mt ulla, és így a folyamat lehet exoterm vagy edoterm. reáls elegyek keletkezését többletfüggvéyekkel s kfejezhetjük, am azt jelet, hogy a valós és az deáls etrópa vagy térfogat változás külöbségéek felel meg: S E Svalós Sdeáls (.4) 75
11 Kéma termodamka z oldatok esetébe vaak olya tulajdoságok, amelyek az oldott ayag meységétől függek. Ilye tulajdoság a forráspotemelkedés, a fagyáspotcsökkeés, az oldékoyság változás és az ozmózs Forráspot emelkedés a folyadékelegyekbe. Legye egy keverékük, amelybe az oldószer és az oldott ayag. Írjuk fel az oldószer gőzfázsú kéma potecálja és az oldatba lévő oldószer kéma potecálja közt egyesúly összefüggést: ( g) ( l) RT l x (.43) Ie: ( g) ( l) vap l1 x (.44) RT RT Most helyettesítsük be a szabadetalpa-változást: vaph T vaps vaph vaps l 1 x (.45) RT RT R Ha x, akkor kapjuk a tszta folyadék forráspotját, vagys: vaph vaps l 1 (.46) RT R két egyelet megfelel a forráspotváltozásak, az egyk az oldat, a másk a tszta folyadék forráspotját határozza meg: H S H S l (.47) vap vap vap vap 1 x l1 RT R RT R Ie, felírható: vaph 1 1 l1 x (.48) R T T l 1 x x,vagys: Mvel a móltörtje agyo kcs, fel lehet ír: x vaph 1 R T T 1 T 1 1 R x T H vap (.49) Ie: 1 1 T T T Rx x T (.5) T T TT T H vaph vap RT 76
12 Fejezetek a fzka kémából Ez az összefüggés em tesz említést az oldott ayag mőségéről, így érvéyes mde oldat esetébe. Látható, hogy a forrpotemelkedést zoterm körülméyeke egy álladó és a móltört szorzata. evezetve az ebuloszkópos kísérlet álladót K, és a (.51) összefüggésbe az x móltörtet a E kompoes moláls kocetrácójával helyettesítve ( ), fel tudjuk ír: x M C m M T C K E (.51) Fagyáspot csökkeés. Legye oldószert és oldott ayagot tartalmazó elegyük. z oldószer fázs-átalakulására fel tudjuk ír kéma potecálváltozást, éspedg: ( s) ( l) RT l x ( l) RT l(1 x ) : (.5) Ie, pedg: H S ( s) ( l) fagy fagy fagy l(1 x) (.53) RT RT RT R Tszta oldószer esetébe: fagyh fagys l 1 (.54) RT R Kvova a két logartmust egymásból, következk: fagyh 1 1 l(1 x) l1 ( ) (.55) R T T Ie, pedg: 1 1 T T T T R x H fagy RT T x H fagy K' x (.56) Nagy fagyáspot csökkeést azokba az oldószerekbe észlelük, amelyek ks olvadás etalpával és agy olvadáspottal redelkezek. Ha az oldat agyo híg, akkor a molaltást s alkalmazhatjuk, s így a kroszkópos álladót (K f ) bevezetve, fel tudjuk ír a fagyáspotcsökkeés mérésekre alapozott összefüggést: T K f C (.57) 77
13 Kéma termodamka Oldhatóság. mkor egy oldószerbe adagoluk egy szlárd ayagot, a szlárd ayag addg oldódk, amíg kalakul az egyesúly állapot, vagys a szlárdfázsból a folyadékba átmet ayag meysége megegyezk az oldatból a krstályrácsba beépült kompoes meységgel. Ilye helyzetre modjuk azt, hogy az ayag elérte az oldhatóság értékét, hsz az oldat telítődött, többet em képes felolda. Legye a kompoes az oldott ayag. Írjuk fel az oldódás folyamatba a kompoes kéma potecálváltozását: ( s) ( l) RT l x (.58) Ie, átredezve következk: ( s) ( l) olv olvh T olvs olvh olvs l x RT RT RT RT R (.59) Mvel az olvadáspoto a szabadetalpa változás értéke ulla (egyesúly helyzetbe vagyuk), akkor a ullát hozzáadhatjuk az egyelet jobb oldalához: olvh olvs olvh olvs olvh 1 1 l x ( ) RT R RT R R T T (.6) Ie látható, hogy az oldhatóság expoecálsa ő vagy csökke a hőmérséklettel. változás ráyát és mértékét az olvadás etalpa jele és értéke határozza meg. z s látható, hogy magas olvadáspotú és agy olvadás etalpájú ayagok esetébe ormáls körülméyek között kcs az oldhatóság z ozmózs. z ozmózs az a folyamat, amkor az oldószer a félgáteresztő membráal elválasztott oldatba spotául átkerül. tszta oldószer oldalo a yomás p és az oldószer kéma potecálja ( p), az oldat oldalá az oldószer kéma potecálja egyrészt ksebb, mert a kompoes lecsökketette a részesedését ( x <1), másrészt megő, hsz az oldat agyobb yomást képes kfejte. z.3. ábra. z ozmózs ábrázolása.(z egyesúly akkor áll be, amkor kellő oldószer jutott át az oldatba). 78
14 Fejezetek a fzka kémából egyesúly állapotba a membrá mdkét oldalá a kéma potecál azoos, tehát fel rható: ( p) ( x, p ) (.61) ahol: az oldószer átáramlásáak megakadályozására szükséges, az oldatra gyakorolt yomás értéke. hhoz, hogy e yomást llusztráljuk, képzeljük el a.3. ábrá feltütetett beredezést. z egyesúly kalakulásakor az oldatak megfelelő folyadékoszlop yomása éppe megegyezk az ozmózsyomással. Fgyelembe véve az oldat összetételét, fel tudjuk ír: x, p ( p ) RT l x (.6) lkalmazva a kéma potecálra kfejtett yomás hatását: p ( p ) ( p) V dp (.63) három egyeletből következk: p p m p m ( p) ( p) V dp RT l x RT l x RT l1 x V dp 79 p p m (.64) Vagys, ha az oldószer móltérfogatát álladóak vesszük, akkor felírható: 1 p l 1 x x Vm p (.65) RT p Ie, pedg: RTx p p Vm xrt (.66) V m Híg oldatokra fel tudjuk ír: x (.67) ehelyettesítve, következk: Vm RT Vm RT (.68) Mvel V m V és az V aráy kocetrácóak felel meg ( 1 3 V C, moll, molm ) megkapjuk va t Hoff egyeletét [9-13]: C RT (.69) z ozmózsyomás köye mérhető és elég agy értékkel redelkezk, ezért az ozmómetrával meghatározhatjuk a agy molekulák móltömegét, az olyaokét, mt a makromolekulák. Mvel ezek az oldatok em deálsak, a va t Hoff egyelet egy vrál egyelet első tagjakét tekthető, vagys:
15 h/c, cml/g Kéma termodamka C RT 1 a C b C... (.7) ahol az a-t, b-t ozmotkus vrál együtthatók evezzük. 18. y. Határozzuk meg a polmer móltömegét, ha smerjük a következő 98 K hőmérséklete és 98 kg/m 3 sűrűségű oldószerrel mért adatokat [9]: c, g/l h, cm,8,71,1 5,1 8, h/c,8,355,53,79,889 Megoldás: lkalmazva a vráls egyelet első két tagját felírhatjuk: C RT 1 a Ie, pedg ha fgyelembe vesszük, hogy kocetrácója g/l kfejezve), felírható: C gh és c C, (ahol c a polmer M c h RT c RT RTa gh RT M c gm M gm gm ac 1 a c y =.758x c, g/l.31. ábra. mérés adatok feldolgozása. értékét. z egyees metszéspotja a,3-ba található. Ez egyelő az RT RT 8,314 98,3 M gm g,3 98 9,81,31 Tehát, ha az eredméyeket h/c c grafkoo ábrázoljuk, a metszésből kszámítható a móltömeg. Ezért először kszámítjuk a h/c aráyt (a táblázat utolsó sora), majd ábrázoljuk a h/c----c dagramot (lásd a.31. dagramot), majd a metszésből kszámítjuk az M RT / gm -el, tehát: 17,38 kg/mol 8
2.6. Az ideális gáz fundamentális egyenlete
 Fejezetek a fzka kéából.6. Az deáls gáz fudaetáls egyelete A legegyszerűbb terodaka redszer az u. deáls gáz. Erre jellező, hogy a részecskék között az egyetle kölcsöhatás a rugalas ütközés, és a részecskék
Fejezetek a fzka kéából.6. Az deáls gáz fudaetáls egyelete A legegyszerűbb terodaka redszer az u. deáls gáz. Erre jellező, hogy a részecskék között az egyetle kölcsöhatás a rugalas ütközés, és a részecskék
EGY FÁZISÚ TÖBBKOMPONENS RENDSZEREK: AZ ELEGYEK KÉPZDÉSE
 EG FÁZISÚ ÖBBOMPONENS RENDSZERE: AZ ELEGE ÉPZDÉSE AZ ELEGÉPZDÉS ERMODINAMIÁJA: GÁZO Általáos megfotolások ülöböz kéma mség komoesek keveredésekor változás törték a molekulárs kölcsöhatásokba és a molekulák
EG FÁZISÚ ÖBBOMPONENS RENDSZERE: AZ ELEGE ÉPZDÉSE AZ ELEGÉPZDÉS ERMODINAMIÁJA: GÁZO Általáos megfotolások ülöböz kéma mség komoesek keveredésekor változás törték a molekulárs kölcsöhatásokba és a molekulák
Megoldás a, A sebességből és a hullámhosszból számított periódusidőket T a táblázat
 Fzka feladatok: F.1. Cuam A cuam hullám formájáak változása, ahogy a sekélyebb víz felé mozog (OAA) (https://www.wdowsuverse.org/?page=/earth/tsuam1.html) Az ábra, táblázat a cuam egyes jellemzőt tartalmazza.
Fzka feladatok: F.1. Cuam A cuam hullám formájáak változása, ahogy a sekélyebb víz felé mozog (OAA) (https://www.wdowsuverse.org/?page=/earth/tsuam1.html) Az ábra, táblázat a cuam egyes jellemzőt tartalmazza.
SZÁMOLÁSI FELADATOK. 2. Mekkora egy klíma teljesítménytényező maximális értéke, ha a szobában 20 C-ot akarunk elérni és kint 35 C van?
 SZÁMOLÁSI FELADATOK 1. Egy fehérje kcsapásához tartozó standard reakcóentalpa 512 kj/mol és standard reakcóentrópa 1,60 kj/k/mol. Határozza meg, hogy mlyen hőmérséklettartományban játszódk le önként a
SZÁMOLÁSI FELADATOK 1. Egy fehérje kcsapásához tartozó standard reakcóentalpa 512 kj/mol és standard reakcóentrópa 1,60 kj/k/mol. Határozza meg, hogy mlyen hőmérséklettartományban játszódk le önként a
Azonos névleges értékű, hitelesített súlyokból alkotott csoportok együttes mérési bizonytalansága
 Azoos évleges értékű, htelesített súlyokból alkotott csoportok együttes mérés bzoytalasága Zeleka Zoltá* Több mérés feladatál alkalmazak súlyokat. Sokszor ezek em egyekét, haem külöböző társításba kombácókba
Azoos évleges értékű, htelesített súlyokból alkotott csoportok együttes mérés bzoytalasága Zeleka Zoltá* Több mérés feladatál alkalmazak súlyokat. Sokszor ezek em egyekét, haem külöböző társításba kombácókba
VÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZTÉVFOLYAM 2006
 ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
2. Az együttműködő villamosenergia-rendszer teljesítmény-egyensúlya
 II RÉZ 2 EJEZE 2 Az együttműködő vllamoseerga-redszer teljesítméy-egyesúlya 2 A frekveca és a hatásos teljesítméy között összefüggés A fogyasztó alredszerbe a fogyasztók hatásos wattos teljesítméyt lletve
II RÉZ 2 EJEZE 2 Az együttműködő vllamoseerga-redszer teljesítméy-egyesúlya 2 A frekveca és a hatásos teljesítméy között összefüggés A fogyasztó alredszerbe a fogyasztók hatásos wattos teljesítméyt lletve
A pályázat címe: Rugalmas-képlékeny tartószerkezetek topológiai optimalizálásának néhány különleges feladata
 6. év OTKA zárójeletés: Vezető kutató:kalszky Sádor OTKA ylvátartás szám T 4993 A pályázat címe: Rugalmas-képlékey tartószerkezetek topológa optmalzálásáak éháy külöleges feladata (Részletes jeletés) Az
6. év OTKA zárójeletés: Vezető kutató:kalszky Sádor OTKA ylvátartás szám T 4993 A pályázat címe: Rugalmas-képlékey tartószerkezetek topológa optmalzálásáak éháy külöleges feladata (Részletes jeletés) Az
Elegyek. Fizikai kémia előadások 5. Turányi Tamás ELTE Kémiai Intézet. Elegyedés
 Elegyek Fzka kéma előadások 5. Turány Tamás ELTE Kéma Intézet Elegyedés DEF elegyek: makroszkokusan homogén, többkomonensű rendszerek. Nemreaktív elegyben kéma reakcó nncs, de szerkezet változás lehet!
Elegyek Fzka kéma előadások 5. Turány Tamás ELTE Kéma Intézet Elegyedés DEF elegyek: makroszkokusan homogén, többkomonensű rendszerek. Nemreaktív elegyben kéma reakcó nncs, de szerkezet változás lehet!
2012/2013 tavaszi félév 8. óra
 2012/2013 tavasz félév 8. óra Híg oldatok törvénye Fagyáspontcsökkenés és forráspont-emelkedés, Ozmózsnyomás Molárs tömeg meghatározása kollgatív tulajdonságok segítségével Erős elektroltok kollgatív tulajdonsága
2012/2013 tavasz félév 8. óra Híg oldatok törvénye Fagyáspontcsökkenés és forráspont-emelkedés, Ozmózsnyomás Molárs tömeg meghatározása kollgatív tulajdonságok segítségével Erős elektroltok kollgatív tulajdonsága
EGY FÁZISÚ TÖBBKOMPONENS RENDSZEREK: BEVEZETÉS
 EGY FÁZIÚ ÖBBOMPONEN RENDZERE: BEEZEÉ ERMODINMII ÁLOZÓ Eg: egy komoes egy fázs (olt egy komoes több fázs s Általáos eset: több komoes több fázs öztes eset: több komoes egy fázs Ezek az elegyek szta fázs
EGY FÁZIÚ ÖBBOMPONEN RENDZERE: BEEZEÉ ERMODINMII ÁLOZÓ Eg: egy komoes egy fázs (olt egy komoes több fázs s Általáos eset: több komoes több fázs öztes eset: több komoes egy fázs Ezek az elegyek szta fázs
A FUNDAMENTÁLIS EGYENLET KÉT REPREZENTÁCIÓBAN. A függvény teljes differenciálja, a differenciális fundamentális egyenlet: U V S U + dn 1
 A FUNDAMENÁLIS EGYENLE KÉ REPREZENÁCIÓBAN A differeciális fudametális egyelet A fudametális egyelet a belső eergiára: UU (S V K ) A függvéy teljes differeciálja a differeciális fudametális egyelet: U S
A FUNDAMENÁLIS EGYENLE KÉ REPREZENÁCIÓBAN A differeciális fudametális egyelet A fudametális egyelet a belső eergiára: UU (S V K ) A függvéy teljes differeciálja a differeciális fudametális egyelet: U S
ORVOSI STATISZTIKA. Az orvosi statisztika helye. Egyéb példák. Példa: test hőmérséklet. Lehet kérdés? Statisztika. Élettan Anatómia Kémia. Kérdések!
 ORVOSI STATISZTIKA Az orvos statsztka helye Életta Aatóma Kéma Lehet kérdés?? Statsztka! Az orvos dötéseket hoz! Mkor jó egy dötés? Meyre helyes egy dötés? Mekkora a tévedés lehetősége? Példa: test hőmérséklet
ORVOSI STATISZTIKA Az orvos statsztka helye Életta Aatóma Kéma Lehet kérdés?? Statsztka! Az orvos dötéseket hoz! Mkor jó egy dötés? Meyre helyes egy dötés? Mekkora a tévedés lehetősége? Példa: test hőmérséklet
Laboratóriumi mérések
 Laboratórum mérések. Bevezetı Bármlye mérés ayt jelet, mt meghatároz, háyszor va meg a méredı meységbe egy másk, a méredıvel egyemő, ökéyese egységek választott meység. Egy mérés eredméyét tehát két adat
Laboratórum mérések. Bevezetı Bármlye mérés ayt jelet, mt meghatároz, háyszor va meg a méredı meységbe egy másk, a méredıvel egyemő, ökéyese egységek választott meység. Egy mérés eredméyét tehát két adat
(Kémiai alapok) és
 011/01 tavasz félév 6. óra Híg oldatok törvénye Fagyáspontsökkenés és forráspont-emelkedés, Ozmózsnyomás Molárs tömeg meghatározása kollgatív tulajdonságok segítségével Erős elektroltok kollgatív tulajdonsága
011/01 tavasz félév 6. óra Híg oldatok törvénye Fagyáspontsökkenés és forráspont-emelkedés, Ozmózsnyomás Molárs tömeg meghatározása kollgatív tulajdonságok segítségével Erős elektroltok kollgatív tulajdonsága
A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL I. A TÖKÉLETES GÁZ KÉMIAI POTENCIÁLJA
 kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
A Sturm-módszer és alkalmazása
 A turm-módszer és alalmazása Tuzso Zoltá, zéelyudvarhely zámtala szélsőérté probléma megoldása, vagy egyelőtleség bzoyítása agyo gyara, már a matemata aalízs eszözere szorítoz, mt például a Jese-, Hölderféle
A turm-módszer és alalmazása Tuzso Zoltá, zéelyudvarhely zámtala szélsőérté probléma megoldása, vagy egyelőtleség bzoyítása agyo gyara, már a matemata aalízs eszözere szorítoz, mt például a Jese-, Hölderféle
Kényszereknek alávetett rendszerek
 Kéyszerekek alávetett redszerek A koordátákak és sebességekek előírt egyeleteket kell kelégítee a mozgás olyamá. (Ezeket a eltételeket, egyeleteket s ayag kölcsöhatások bztosítják, de ezek a kölcsöhatások
Kéyszerekek alávetett redszerek A koordátákak és sebességekek előírt egyeleteket kell kelégítee a mozgás olyamá. (Ezeket a eltételeket, egyeleteket s ayag kölcsöhatások bztosítják, de ezek a kölcsöhatások
Feladatok és megoldások a 11. heti gyakorlathoz
 Feladatok és megoldások a. het gyakorlathoz dszkrét várható érték Építőkar Matematka A. Egy verseye öt ő és öt férf verseyző dul. Tegyük fel, hogy cs két azoos eredméy, és md a 0! sorred egyformá valószíű.
Feladatok és megoldások a. het gyakorlathoz dszkrét várható érték Építőkar Matematka A. Egy verseye öt ő és öt férf verseyző dul. Tegyük fel, hogy cs két azoos eredméy, és md a 0! sorred egyformá valószíű.
A paramétereket kísérletileg meghatározott yi értékekre támaszkodva becsülik. Ha n darab kisérletet (megfigyelést, mérést) végeznek, n darab
 öbbváltozós regresszók Paraméterbecslés-. A paraméterbecslés.. A probléma megfogalmazása A paramétereket kísérletleg meghatározott y értékekre támaszkodva becsülk. Ha darab ksérletet (megfgyelést, mérést
öbbváltozós regresszók Paraméterbecslés-. A paraméterbecslés.. A probléma megfogalmazása A paramétereket kísérletleg meghatározott y értékekre támaszkodva becsülk. Ha darab ksérletet (megfgyelést, mérést
5. SZABAD PONTRENDSZEREK MECHANIKAI ALAPELVEI, N-TESTPROBLÉMA, GALILEI-
 5. SZABAD PONTRENDSZEREK MECHANIKAI ALAPELVEI, N-TESTPROBLÉMA, GALILEI- FÉLE RELATIVITÁSI ELV m, m,,m r, r,,r r, r,, r 6 db oordáta és sebességompoes 5.. Dama Mozgásegyelete: m r = F F, ahol F jelöl a
5. SZABAD PONTRENDSZEREK MECHANIKAI ALAPELVEI, N-TESTPROBLÉMA, GALILEI- FÉLE RELATIVITÁSI ELV m, m,,m r, r,,r r, r,, r 6 db oordáta és sebességompoes 5.. Dama Mozgásegyelete: m r = F F, ahol F jelöl a
Statisztika. Eloszlásjellemzők
 Statsztka Eloszlásjellemzők Statsztka adatok elemzése A sokaság jellemzése középértékekkel A sokaság jellemzéséek szempotja A sokaság jellemzéséek szempotja: A sokaság tpkus értékéek meghatározása. Az
Statsztka Eloszlásjellemzők Statsztka adatok elemzése A sokaság jellemzése középértékekkel A sokaság jellemzéséek szempotja A sokaság jellemzéséek szempotja: A sokaság tpkus értékéek meghatározása. Az
Ismérvek közötti kapcsolatok szorosságának vizsgálata. 1. Egy kis ismétlés: mérési skálák (Hunyadi-Vita: Statisztika I. 25-26. o)
 Ismérvek között kapcsolatok szorosságáak vzsgálata 1. Egy ks smétlés: mérés skálák (Huyad-Vta: Statsztka I. 5-6. o) A külöböző smérveket, eltérő mérés sztekkel (skálákkal) ellemezhetük. a. évleges (omáls)
Ismérvek között kapcsolatok szorosságáak vzsgálata 1. Egy ks smétlés: mérés skálák (Huyad-Vta: Statsztka I. 5-6. o) A külöböző smérveket, eltérő mérés sztekkel (skálákkal) ellemezhetük. a. évleges (omáls)
Izolált rendszer falai: sem munkavégzés, sem a rendszer állapotának munkavégzés nélküli megváltoztatása nem lehetséges.
 ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
Valószínűségszámítás. Ketskeméty László
 Valószíűségszámítás Ketskeméty László Budapest, 996 Tartalomjegyzék I. fejezet VALÓSZÍNŰSÉGSZÁMÍTÁS 3. Kombatorka alapfogalmak 4 Elleőrző kérdések és gyakorló feladatok 6. A valószíűségszámítás alapfogalma
Valószíűségszámítás Ketskeméty László Budapest, 996 Tartalomjegyzék I. fejezet VALÓSZÍNŰSÉGSZÁMÍTÁS 3. Kombatorka alapfogalmak 4 Elleőrző kérdések és gyakorló feladatok 6. A valószíűségszámítás alapfogalma
Bevezetés a kémiai termodiamikába
 Aktualzálva: 007. ovember 8. Bevezetés a kéma termodamkába egyetem jegyzet írta Kesze Erő Eötvös Lorád udomáyegyetem Budapest, 006 Előszó Ez a jegyzet az ELE kéma alapszak fzka kéma című tatárgyáak előadásahoz
Aktualzálva: 007. ovember 8. Bevezetés a kéma termodamkába egyetem jegyzet írta Kesze Erő Eötvös Lorád udomáyegyetem Budapest, 006 Előszó Ez a jegyzet az ELE kéma alapszak fzka kéma című tatárgyáak előadásahoz
10 A TRANSZPORTFOLYAMATOK ÁLTALÁNOS JELLEMZÉSE
 0 A TRANSZPORTFOLYAMATOK ÁLTALÁNOS JLLMZÉS gy termodamka redszer állapota lehet dőbe álladó, vagy változó. Az dőbe álladó redszereket két agy csoportra oszthatuk: egyesúlyba lévő redszerekre és stacoárus
0 A TRANSZPORTFOLYAMATOK ÁLTALÁNOS JLLMZÉS gy termodamka redszer állapota lehet dőbe álladó, vagy változó. Az dőbe álladó redszereket két agy csoportra oszthatuk: egyesúlyba lévő redszerekre és stacoárus
A nátrium-klorid oldat összetétele. Néhány megjegyzés az összetételi arány méréséről és számításáról
 A nátrium-klorid oldat összetétele Néhány megjegyzés az összetételi arány méréséről és számításáról Mérés areométerrel kiértékelés lineáris regresszióval αραιός = híg Sodium-chloride solution at 20 Celsius
A nátrium-klorid oldat összetétele Néhány megjegyzés az összetételi arány méréséről és számításáról Mérés areométerrel kiértékelés lineáris regresszióval αραιός = híg Sodium-chloride solution at 20 Celsius
(1) Milyen esetben beszélünk tartós nyugalomról? Abban az esetben, ha a (vizsgált) test a helyzetét hosszabb időn át nem változtatja meg.
 SZÉCHENYI ISTVÁN EGYETEM MECHNIK - STTIK LKLMZTT MECHNIK TNSZÉK Elmélet kérdések és válaszok egetem alapképzésbe (Sc képzésbe) résztvevő mérökhallgatók számára () Mle esetbe beszélük tartós ugalomról?
SZÉCHENYI ISTVÁN EGYETEM MECHNIK - STTIK LKLMZTT MECHNIK TNSZÉK Elmélet kérdések és válaszok egetem alapképzésbe (Sc képzésbe) résztvevő mérökhallgatók számára () Mle esetbe beszélük tartós ugalomról?
Tartalomjegyzék. 4.3 Alkalmazás: sorozatgyártású tűgörgő átmérőjének jellemzése
 3 4 Tartalomegyzék. BEVEZETÉS 5. A MÉRÉS 8. A mérés mt folyamat, fogalmak 8. Fotosabb mérés- és műszertechka fogalmak 4.3 Mérés hbák 8.3. Mérés hbák csoportosítása eredetük szert 8.3. A hbák megeleítés
3 4 Tartalomegyzék. BEVEZETÉS 5. A MÉRÉS 8. A mérés mt folyamat, fogalmak 8. Fotosabb mérés- és műszertechka fogalmak 4.3 Mérés hbák 8.3. Mérés hbák csoportosítása eredetük szert 8.3. A hbák megeleítés
ROMAVERSITAS 2017/2018. tanév. Kémia. Számítási feladatok (oldatok összetétele) 4. alkalom. Összeállította: Balázs Katalin kémia vezetőtanár
 ROMAVERSITAS 2017/2018. tanév Kémia Számítási feladatok (oldatok összetétele) 4. alkalom Összeállította: Balázs Katalin kémia vezetőtanár 1 Számítási feladatok OLDATOK ÖSSZETÉTELE Összeállította: Balázs
ROMAVERSITAS 2017/2018. tanév Kémia Számítási feladatok (oldatok összetétele) 4. alkalom Összeállította: Balázs Katalin kémia vezetőtanár 1 Számítási feladatok OLDATOK ÖSSZETÉTELE Összeállította: Balázs
A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL I. A TÖKÉLETES GÁZ KÉMIAI POTENCIÁLJA
 kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
1. előadás. Gáztörvények. Fizika Biofizika I. 2015/2016. Kapcsolódó irodalom:
 1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
MATEMATIKA I. KATEGÓRIA (SZAKKÖZÉPISKOLA)
 O k t a t á s i H i v a t a l A 5/6 taévi Országos Középiskolai Taulmáyi Versey első forduló MATEMATIKA I KATEGÓRIA (SZAKKÖZÉPISKOLA) Javítási-értékelési útmutató A 5 olya égyjegyű szám, amelyek számjegyei
O k t a t á s i H i v a t a l A 5/6 taévi Országos Középiskolai Taulmáyi Versey első forduló MATEMATIKA I KATEGÓRIA (SZAKKÖZÉPISKOLA) Javítási-értékelési útmutató A 5 olya égyjegyű szám, amelyek számjegyei
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Bevezetés a kémiai termodinamikába
 Verzó: 007. jauár 5. Bevezetés a kéma termodamkába egyetem jegyzet írta esze Erő Eötvös Lorád udomáyegyetem Budapest 006 Előszó Mért va szükség egy egyetem taköyvre a fzka kéma szűkebbe a kéma termodamka
Verzó: 007. jauár 5. Bevezetés a kéma termodamkába egyetem jegyzet írta esze Erő Eötvös Lorád udomáyegyetem Budapest 006 Előszó Mért va szükség egy egyetem taköyvre a fzka kéma szűkebbe a kéma termodamka
Regresszió és korreláció
 Regresszó és korrelácó regresso: vsszatérés, hátrálás; vsszafordulás correlato: vszo, összefüggés, kölcsöösség KAD 01.11.1 1 (vsszatérés, hátrálás; vsszafordulás) Regresszó és korrelácó Gakorlat megközelítés
Regresszó és korrelácó regresso: vsszatérés, hátrálás; vsszafordulás correlato: vszo, összefüggés, kölcsöösség KAD 01.11.1 1 (vsszatérés, hátrálás; vsszafordulás) Regresszó és korrelácó Gakorlat megközelítés
13. Tárcsák számítása. 1. A felületszerkezetek. A felületszerkezetek típusai
 Tárcsák számítása A felületszerkezetek A felületszerkezetek típusa A tartószerkezeteket geometra méretek alapjá osztálozzuk Az eddg taulmáakba szereplı rúdszerkezetek rúdjara az a jellemzı hog a hosszuk
Tárcsák számítása A felületszerkezetek A felületszerkezetek típusa A tartószerkezeteket geometra méretek alapjá osztálozzuk Az eddg taulmáakba szereplı rúdszerkezetek rúdjara az a jellemzı hog a hosszuk
MÉRÉSTECHNIKA. DR. HUBA ANTAL c. egy. tanár BME Mechatronika, Optika és Gépészeti Informatika Tanszék 2011
 MÉRÉSTECHNIKA DR. HUBA ANTAL c. egy. taár BME Mechatroka, Optka és Gépészet Iformatka Taszék 0 Rövde a tárgyprogramról Előadások tematkája: Metrológa és műszertechka alapok Mérés adatok kértékelése Időbe
MÉRÉSTECHNIKA DR. HUBA ANTAL c. egy. taár BME Mechatroka, Optka és Gépészet Iformatka Taszék 0 Rövde a tárgyprogramról Előadások tematkája: Metrológa és műszertechka alapok Mérés adatok kértékelése Időbe
Tuzson Zoltán A Sturm-módszer és alkalmazása
 Tuzso Zoltá A turm-módszer és alalmazása zámtala szélsérté probléma megoldása, vag egeltleség bzoítása ago gara, már a matemata aalízs eszözere szorítoz, mt például a Jese-, Hölder-féle egeltleség, derválta
Tuzso Zoltá A turm-módszer és alalmazása zámtala szélsérté probléma megoldása, vag egeltleség bzoítása ago gara, már a matemata aalízs eszözere szorítoz, mt például a Jese-, Hölder-féle egeltleség, derválta
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ
 1 oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ I A VÍZ - A víz molekulája V-alakú, kötésszöge 109,5 fok, poláris kovalens kötések; - a jég molekularácsos, tetraéderes elrendeződés,
1 oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ I A VÍZ - A víz molekulája V-alakú, kötésszöge 109,5 fok, poláris kovalens kötések; - a jég molekularácsos, tetraéderes elrendeződés,
2012.03.01. Méréselmélet PE_MIK MI_BSc, VI_BSc 1
 Mérés adatok feldolgozása 202.03.0. Méréselmélet PE_MIK MI_BSc, VI_BSc Bevezetés A mérés adatok külöböző formába, általába ömlesztve jeleek meg Ezeket az adatokat külöböző szempotok szert redez kértékel
Mérés adatok feldolgozása 202.03.0. Méréselmélet PE_MIK MI_BSc, VI_BSc Bevezetés A mérés adatok külöböző formába, általába ömlesztve jeleek meg Ezeket az adatokat külöböző szempotok szert redez kértékel
Regresszió és korreláció
 Regresszó és korrelácó regresso: vsszatérés, hátrálás; vsszafordulás correlato: vszo, összefüggés, kölcsöösség KAD 016.11.10 1 (vsszatérés, hátrálás; vsszafordulás) Regresszó és korrelácó Gakorlat megközelítés
Regresszó és korrelácó regresso: vsszatérés, hátrálás; vsszafordulás correlato: vszo, összefüggés, kölcsöösség KAD 016.11.10 1 (vsszatérés, hátrálás; vsszafordulás) Regresszó és korrelácó Gakorlat megközelítés
Függvénygörbe alatti terület a határozott integrál
 Függvéygörbe alatt terület a határozott tegrál Tektsük az üggvéyt a ; tervallumo. Adjuk becslést a görbe az tegely és az egyees között síkdom területére! Jelöljük ezt a területet I-vel! A becslést legegyszerűbbe
Függvéygörbe alatt terület a határozott tegrál Tektsük az üggvéyt a ; tervallumo. Adjuk becslést a görbe az tegely és az egyees között síkdom területére! Jelöljük ezt a területet I-vel! A becslést legegyszerűbbe
A figurális számokról (IV.)
 A figurális számokról (IV.) Tuzso Zoltá, Székelyudvarhely A továbbiakba külöféle számkombiációk és összefüggések reprezetálásáról, és bizoyos összegek kiszámolásáról íruk. Sajátos összefüggések Az elekbe
A figurális számokról (IV.) Tuzso Zoltá, Székelyudvarhely A továbbiakba külöféle számkombiációk és összefüggések reprezetálásáról, és bizoyos összegek kiszámolásáról íruk. Sajátos összefüggések Az elekbe
SZERVETLEN ALAPANYAGOK ISMERETE, OLDATKÉSZÍTÉS
 SZERVETLEN ALAPANYAGOK ISMERETE, OLDATKÉSZÍTÉS ESETFELVETÉS MUNKAHELYZET Az eredményes munka szempontjából szükség van arra, hogy a kozmetikus, a gyakorlatban használt alapanyagokat ismerje, felismerje
SZERVETLEN ALAPANYAGOK ISMERETE, OLDATKÉSZÍTÉS ESETFELVETÉS MUNKAHELYZET Az eredményes munka szempontjából szükség van arra, hogy a kozmetikus, a gyakorlatban használt alapanyagokat ismerje, felismerje
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
(Kémiai alapok) és
 212/213 tvszi félév 4. ór Gáz- és folyékegyesúlyok: z egyesúlyi álló és z egyesúlyi összetétel számítás Egyesúlyi álló foglm Folyékfázisú egyesúlyok (l. észteresítés, st.) iiulási ygok és termékek meyigéek,
212/213 tvszi félév 4. ór Gáz- és folyékegyesúlyok: z egyesúlyi álló és z egyesúlyi összetétel számítás Egyesúlyi álló foglm Folyékfázisú egyesúlyok (l. észteresítés, st.) iiulási ygok és termékek meyigéek,
Váltakozó elektromágneses terek
 Váltakozó elektromágeses terek. Váltakozó feszültség és váltóáram elõállítása Az elektromos áram mdeap életük fotos része. A 9. századba Thomas Alva (GVRQ pv D] OWDOD DODStWRWW ODERDWyXP PXQNDWVD PXWDWWN
Váltakozó elektromágeses terek. Váltakozó feszültség és váltóáram elõállítása Az elektromos áram mdeap életük fotos része. A 9. századba Thomas Alva (GVRQ pv D] OWDOD DODStWRWW ODERDWyXP PXQNDWVD PXWDWWN
KOMBINATORIKA ELŐADÁS osztatlan matematikatanár hallgatók számára. Szita formula J = S \R,
 KOMBINATORIKA ELŐADÁS osztatla matematkataár hallgatók számára Szta formula Előadó: Hajal Péter 2018 1. Bevezető példák 1. Feladat. Háy olya sorbaállítása va a {a,b,c,d,e} halmazak, amelybe a és b em kerül
KOMBINATORIKA ELŐADÁS osztatla matematkataár hallgatók számára Szta formula Előadó: Hajal Péter 2018 1. Bevezető példák 1. Feladat. Háy olya sorbaállítása va a {a,b,c,d,e} halmazak, amelybe a és b em kerül
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Elegyek. Csonka Gábor 2008 Általános Kémia: oldatok 1 dia
 Elegyek 7-1 Elegyek fajtái 7-2 Koncentrációk 7-3 Intermolekuláris erők, az elegyedés folyamata 7-4 Elegyek keletkezése, egyensúly 7-5 Gázok oldhatósága 7-6 Elegyek gőznyomása 7-7 Ozmózis nyomás 7-8 Fagyáspont
Elegyek 7-1 Elegyek fajtái 7-2 Koncentrációk 7-3 Intermolekuláris erők, az elegyedés folyamata 7-4 Elegyek keletkezése, egyensúly 7-5 Gázok oldhatósága 7-6 Elegyek gőznyomása 7-7 Ozmózis nyomás 7-8 Fagyáspont
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Általános Kémia, BMEVESAA101
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
1. feladat Összesen: 15 pont. 2. feladat Összesen: 10 pont
 1. feladat Összesen: 15 pont Vizsgálja meg a hidrogén-klorid (vagy vizes oldata) reakciót különböző szervetlen és szerves anyagokkal! Ha nem játszódik le reakció, akkor ezt írja be! protonátmenettel járó
1. feladat Összesen: 15 pont Vizsgálja meg a hidrogén-klorid (vagy vizes oldata) reakciót különböző szervetlen és szerves anyagokkal! Ha nem játszódik le reakció, akkor ezt írja be! protonátmenettel járó
Számsorozatok. 1. Alapfeladatok december 22. sorozat határértékét, ha. 1. Feladat: Határozzuk meg az a n = 3n2 + 7n 5n létezik.
 Számsorozatok 2015. december 22. 1. Alapfeladatok 1. Feladat: Határozzuk meg az a 2 + 7 5 2 + 4 létezik. sorozat határértékét, ha Megoldás: Mivel egy tört határértéke a kérdés, ezért vizsgáljuk meg el
Számsorozatok 2015. december 22. 1. Alapfeladatok 1. Feladat: Határozzuk meg az a 2 + 7 5 2 + 4 létezik. sorozat határértékét, ha Megoldás: Mivel egy tört határértéke a kérdés, ezért vizsgáljuk meg el
Megállapítható változók elemzése Függetlenségvizsgálat, illeszkedésvizsgálat, homogenitásvizsgálat
 Megállapítható változók elemzése Függetleségvzsgálat, lleszkedésvzsgálat, homogetásvzsgálat Ordáls, omáls esetre s alkalmazhatóak a következő χ próbá alapuló vzsgálatok: 1) Függetleségvzsgálat: két valószíűség
Megállapítható változók elemzése Függetleségvzsgálat, lleszkedésvzsgálat, homogetásvzsgálat Ordáls, omáls esetre s alkalmazhatóak a következő χ próbá alapuló vzsgálatok: 1) Függetleségvzsgálat: két valószíűség
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
? közgazdasági statisztika
 Valószíűségszámítás és a statsztka Valószíűség számítás Matematka statsztka Alkalmazott statsztka? közgazdaság statsztka épesség statsztka orvos statsztka Stb. Példa: vércsoportok Az eloszlás A AB B Elem
Valószíűségszámítás és a statsztka Valószíűség számítás Matematka statsztka Alkalmazott statsztka? közgazdaság statsztka épesség statsztka orvos statsztka Stb. Példa: vércsoportok Az eloszlás A AB B Elem
AZ ÖSSZETÉTEL OPTIMALIZÁLÁSA A VOLUMETRIKUS ASZFALTKEVERÉK- ELLENÕRZÉS MÓDSZERÉVEL
 36 MIXCONTROL AZ ÖSSZETÉTEL OPTIMALIZÁLÁSA A VOLUMETRIKUS ASZFALTKEVERÉK- ELLENÕRZÉS MÓDSZERÉVEL Subert Istvá deformáció-elleálló keverékvázat lehet létrehozi. Kiidulási feltétel az alkalmazás helyéek
36 MIXCONTROL AZ ÖSSZETÉTEL OPTIMALIZÁLÁSA A VOLUMETRIKUS ASZFALTKEVERÉK- ELLENÕRZÉS MÓDSZERÉVEL Subert Istvá deformáció-elleálló keverékvázat lehet létrehozi. Kiidulási feltétel az alkalmazás helyéek
V. Deriválható függvények
 Deriválható függvéyek V Deriválható függvéyek 5 A derivált fogalmához vezető feladatok A sebesség értelmezése Legye az M egy egyees voalú egyeletes mozgást végző pot Ez azt jeleti, hogy a mozgás pályája
Deriválható függvéyek V Deriválható függvéyek 5 A derivált fogalmához vezető feladatok A sebesség értelmezése Legye az M egy egyees voalú egyeletes mozgást végző pot Ez azt jeleti, hogy a mozgás pályája
Oldatok - elegyek. Elegyek: komponensek mennyisége azonos nagyságrendű
 Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Statisztika 1. zárthelyi dolgozat március 21.
 Statisztika 1 zárthelyi dolgozat 011 március 1 1 Legye X = X 1,, X 00 függetle mita b paraméterű Poisso-eloszlásból b > 0 Legye T 1 X = X 1+X ++X 100, T 100 X = X 1+X ++X 00 00 a Milye a számra igaz, hogy
Statisztika 1 zárthelyi dolgozat 011 március 1 1 Legye X = X 1,, X 00 függetle mita b paraméterű Poisso-eloszlásból b > 0 Legye T 1 X = X 1+X ++X 100, T 100 X = X 1+X ++X 00 00 a Milye a számra igaz, hogy
? közgazdasági statisztika
 ... Valószíűségszámítás és a statsztka Valószíűség számítás Matematka statsztka Alkalmazott statsztka? közgazdaság statsztka épesség statsztka orvos statsztka Stb. Példa: vércsoportok Az eloszlás A AB
... Valószíűségszámítás és a statsztka Valószíűség számítás Matematka statsztka Alkalmazott statsztka? közgazdaság statsztka épesség statsztka orvos statsztka Stb. Példa: vércsoportok Az eloszlás A AB
VII. A határozatlan esetek kiküszöbölése
 A határozatla esetek kiküszöbölése 9 VII A határozatla esetek kiküszöbölése 7 A l Hospital szabály A véges övekedések tétele alapjá egy függvéy értékét egy potba közelíthetjük az köryezetébe felvett valamely
A határozatla esetek kiküszöbölése 9 VII A határozatla esetek kiküszöbölése 7 A l Hospital szabály A véges övekedések tétele alapjá egy függvéy értékét egy potba közelíthetjük az köryezetébe felvett valamely
GEOFIZIKA / 4. GRAVITÁCIÓS ANOMÁLIÁK PREDIKCIÓJA, ANALITIKAI FOLYTATÁSOK MÓDSZERE, GRAVITÁCIÓS ANOMÁLIATEREK SZŰRÉSE
 MSc GEOFIZIKA / 4. BMEEOAFMFT3 GRAVITÁCIÓS ANOMÁLIÁK REDIKCIÓJA, ANALITIKAI FOLYTATÁSOK MÓDSZERE, GRAVITÁCIÓS ANOMÁLIATEREK SZŰRÉSE A gravtácós aomálák predkcója Külöböző feladatok megoldása sorá - elsősorba
MSc GEOFIZIKA / 4. BMEEOAFMFT3 GRAVITÁCIÓS ANOMÁLIÁK REDIKCIÓJA, ANALITIKAI FOLYTATÁSOK MÓDSZERE, GRAVITÁCIÓS ANOMÁLIATEREK SZŰRÉSE A gravtácós aomálák predkcója Külöböző feladatok megoldása sorá - elsősorba
Általános és szervetlen kémia Laborelıkészítı elıadás I.
 Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
VASBETON ÉPÜLETEK MEREVÍTÉSE
 BUDAPET MŰZAK É GAZDAÁGTUDOMÁY EGYETEM Építőmérök Kar Hdak és zerkezetek Taszéke VABETO ÉPÜLETEK MEREVÍTÉE Oktatás segédlet v. Összeállította: Dr. Bód stvá - Dr. Farkas György Dr. Kors Kálmá Budapest,.
BUDAPET MŰZAK É GAZDAÁGTUDOMÁY EGYETEM Építőmérök Kar Hdak és zerkezetek Taszéke VABETO ÉPÜLETEK MEREVÍTÉE Oktatás segédlet v. Összeállította: Dr. Bód stvá - Dr. Farkas György Dr. Kors Kálmá Budapest,.
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
f (M (ξ)) M (f (ξ)) Bizonyítás: Megjegyezzük, hogy konvex függvényekre mindig létezik a ± ben
 Propositio 1 (Jese-egyelőtleség Ha f : kovex, akkor tetszőleges ξ változóra f (M (ξ M (f (ξ feltéve, hogy az egyelőtleségbe szereplő véges vagy végtele várható értékek létezek Bizoyítás: Megjegyezzük,
Propositio 1 (Jese-egyelőtleség Ha f : kovex, akkor tetszőleges ξ változóra f (M (ξ M (f (ξ feltéve, hogy az egyelőtleségbe szereplő véges vagy végtele várható értékek létezek Bizoyítás: Megjegyezzük,
G Á Z J E L L E M Z Ő K összefoglalás
 Mskolc Egyetem Kőolaj és Földgáz Itézet Gázmérök Taszék G Á Z J E L L E M Z Ő K összefoglalás Horászky Beáta egy. taársegéd - - A gázállapot egy külöleges halmazállapot: a gázmolekulák ktöltk a redelkezésre
Mskolc Egyetem Kőolaj és Földgáz Itézet Gázmérök Taszék G Á Z J E L L E M Z Ő K összefoglalás Horászky Beáta egy. taársegéd - - A gázállapot egy külöleges halmazállapot: a gázmolekulák ktöltk a redelkezésre
2. Hatványsorok. A végtelen soroknál tanultuk, hogy az. végtelen sort adja: 1 + x + x x n +...
 . Függvéysorok. Bevezetés és defiíciók A végtele sorokál taultuk, hogy az + x + x + + x +... végtele összeg x < eseté koverges. A feti végtele összegre úgy is godolhatuk, hogy végtele sok függvéyt aduk
. Függvéysorok. Bevezetés és defiíciók A végtele sorokál taultuk, hogy az + x + x + + x +... végtele összeg x < eseté koverges. A feti végtele összegre úgy is godolhatuk, hogy végtele sok függvéyt aduk
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár. Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár,
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
i 0 egyébként ábra. Negyedfokú és ötödfokú Bernstein polinomok a [0,1] intervallumon.
![i 0 egyébként ábra. Negyedfokú és ötödfokú Bernstein polinomok a [0,1] intervallumon. i 0 egyébként ábra. Negyedfokú és ötödfokú Bernstein polinomok a [0,1] intervallumon.](/thumbs/93/111989735.jpg) 3. Bézer görbék 3.1. A Berste polomok 3.1. Defícó. Legye emegatív egész, tetszőleges egész. A ( ) B (u) = u (1 u) polomot Berste polomak evezzük, ahol ( ) = {!!( )! 0, 0 egyébkét. A defícóból közvetleül
3. Bézer görbék 3.1. A Berste polomok 3.1. Defícó. Legye emegatív egész, tetszőleges egész. A ( ) B (u) = u (1 u) polomot Berste polomak evezzük, ahol ( ) = {!!( )! 0, 0 egyébkét. A defícóból közvetleül
Kalkulus II., második házi feladat
 Uger Tamás Istvá FTDYJ Név: Uger Tamás Istvá Neptu: FTDYJ Web: http://maxwellszehu/~ugert Kalkulus II, második házi feladat pot) Koverges? Abszolút koverges? ) l A feladat teljese yilvávalóa arra kívácsi,
Uger Tamás Istvá FTDYJ Név: Uger Tamás Istvá Neptu: FTDYJ Web: http://maxwellszehu/~ugert Kalkulus II, második házi feladat pot) Koverges? Abszolút koverges? ) l A feladat teljese yilvávalóa arra kívácsi,
Telítetlen oldat: még képes anyagot feloldani (befogadni), adott hőmérsékleten.
 2. Oldatkészítés 2.1. Alapfogalmak Az oldat oldott anyagból és oldószerből áll. Az oldott anyag és az oldószer közül az a komponens az oldószer, amelyik nagyobb mennyiségben van jelen az oldatban. Az oldószer
2. Oldatkészítés 2.1. Alapfogalmak Az oldat oldott anyagból és oldószerből áll. Az oldott anyag és az oldószer közül az a komponens az oldószer, amelyik nagyobb mennyiségben van jelen az oldatban. Az oldószer
Termodinamika (Hőtan)
 Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
A szórások vizsgálata. Az F-próba. A döntés. Az F-próba szabadsági fokai
 05..04. szórások vizsgálata z F-próba Hogya foguk hozzá? Nullhipotézis: a két szórás azoos, az eltérés véletle (mitavétel). ullhipotézishez tartozik egy ú. F-eloszlás. Szabadsági fokok: számláló: - evező:
05..04. szórások vizsgálata z F-próba Hogya foguk hozzá? Nullhipotézis: a két szórás azoos, az eltérés véletle (mitavétel). ullhipotézishez tartozik egy ú. F-eloszlás. Szabadsági fokok: számláló: - evező:
18. Differenciálszámítás
 8. Differeciálszámítás I. Elméleti összefoglaló Függvéy határértéke Defiíció: Az köryezetei az ] ε, ε[ + yílt itervallumok, ahol ε > tetszőleges. Defiíció: Az f függvéyek az véges helye vett határértéke
8. Differeciálszámítás I. Elméleti összefoglaló Függvéy határértéke Defiíció: Az köryezetei az ] ε, ε[ + yílt itervallumok, ahol ε > tetszőleges. Defiíció: Az f függvéyek az véges helye vett határértéke
1. A radioaktivitás statisztikus jellege
 A radioaktivitás időfüggése 1. A radioaktivitás statisztikus jellege Va N darab azoos radioaktív atomuk, melyekek az atommagja spotá átalakulásra képes. tegyük fel, hogy ezek em bomlaak tovább. Ekkor a
A radioaktivitás időfüggése 1. A radioaktivitás statisztikus jellege Va N darab azoos radioaktív atomuk, melyekek az atommagja spotá átalakulásra képes. tegyük fel, hogy ezek em bomlaak tovább. Ekkor a
X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet):
![X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet): X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet):](/thumbs/25/6460380.jpg) . Egy átrium-hidroxidot és átrium-acetátot tartalmazó mita 50,00 cm 3 -es részletée megmérjük a ph-t, ami,65-ek adódott. 8,65 cm 3 0, mol/dm 3 kocetrációjú sósavat adva a mitához, a mért ph 5,065. Meyi
. Egy átrium-hidroxidot és átrium-acetátot tartalmazó mita 50,00 cm 3 -es részletée megmérjük a ph-t, ami,65-ek adódott. 8,65 cm 3 0, mol/dm 3 kocetrációjú sósavat adva a mitához, a mért ph 5,065. Meyi
3.1.1. Rugalmas elektronszórás; Recoil- és Doppler-effektus megfigyelése
 3.1.1. Rugalmas elektroszórás 45 3.1.1. Rugalmas elektroszórás; Recoil- és Doppler-effektus megfigyelése Aray, ikkel, szilícium és grafit mitákról rugalmasa visszaszórt elektrook eergiaeloszlását mértem
3.1.1. Rugalmas elektroszórás 45 3.1.1. Rugalmas elektroszórás; Recoil- és Doppler-effektus megfigyelése Aray, ikkel, szilícium és grafit mitákról rugalmasa visszaszórt elektrook eergiaeloszlását mértem
ALGEBRA. egyenlet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 198.
 ALGEBRA MÁSODFOKÚ POLINOMOK. Határozzuk meg az + p + q = 0 egyelet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 98.. Határozzuk meg az összes olya pozitív egész p és q számot, amelyre az
ALGEBRA MÁSODFOKÚ POLINOMOK. Határozzuk meg az + p + q = 0 egyelet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 98.. Határozzuk meg az összes olya pozitív egész p és q számot, amelyre az
1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben
 1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben t/ 0 C 0 20 30 60 O 2 0,006945 0,004339 0,003588 0,002274 H 2S 0,7066 0,3846 0,2983 0,148 HCl 82,3 72 67,3 56,1 CO 2 0,3346 0,1688 0,1257
1. Gázok oldhatósága vízben: 101 325 Pa nyomáson g/100 g vízben t/ 0 C 0 20 30 60 O 2 0,006945 0,004339 0,003588 0,002274 H 2S 0,7066 0,3846 0,2983 0,148 HCl 82,3 72 67,3 56,1 CO 2 0,3346 0,1688 0,1257
Oktatási Hivatal KÉMIA I. A 2015/2016. tanévi Országos Középiskolai Tanulmányi Verseny második forduló. Javítási-értékelési útmutató I.
 ktatási Hivatal I. FELADATSR A 015/016. taévi rszágos Középiskolai Taulmáyi Versey második forduló KÉMIA I. Javítási-értékelési útmutató 1., Mg pot. Fr 1 pot 1 eltérés: 1 pot; mi. 0 pot 3. a) pl. 1 1 H
ktatási Hivatal I. FELADATSR A 015/016. taévi rszágos Középiskolai Taulmáyi Versey második forduló KÉMIA I. Javítási-értékelési útmutató 1., Mg pot. Fr 1 pot 1 eltérés: 1 pot; mi. 0 pot 3. a) pl. 1 1 H
2. fejezet. Számsorozatok, számsorok
 . fejezet Számsorozatok, számsorok .. Számsorozatok és számsorok... Számsorozat megadása, határértéke Írjuk fel képlettel az alábbi sorozatok -dik elemét! mooto, korlátos, illetve koverges-e! Vizsgáljuk
. fejezet Számsorozatok, számsorok .. Számsorozatok és számsorok... Számsorozat megadása, határértéke Írjuk fel képlettel az alábbi sorozatok -dik elemét! mooto, korlátos, illetve koverges-e! Vizsgáljuk
2011/2012 tavaszi félév 4. óra
 211/212 tvszi félév 4. ór Termokémi Feltok hőkitás, fjlgos és moláris hőkitás foglmák megismerésére Látes hő Összetett számítások hlmzállotváltozássl (l. jég és gőz összekeverése) Rekióetli, égési etli
211/212 tvszi félév 4. ór Termokémi Feltok hőkitás, fjlgos és moláris hőkitás foglmák megismerésére Látes hő Összetett számítások hlmzállotváltozássl (l. jég és gőz összekeverése) Rekióetli, égési etli
2011/2012 tavaszi félév 2. óra. Tananyag:
 2011/2012 tavaszi félév 2. óra Tananyag: 2. Gázelegyek, gőztenzió Gázelegyek összetétele, térfogattört és móltört egyezősége Gázelegyek sűrűsége Relatív sűrűség Parciális nyomás és térfogat, Dalton-törvény,
2011/2012 tavaszi félév 2. óra Tananyag: 2. Gázelegyek, gőztenzió Gázelegyek összetétele, térfogattört és móltört egyezősége Gázelegyek sűrűsége Relatív sűrűség Parciális nyomás és térfogat, Dalton-törvény,
Megjegyzés: Amint már előbb is említettük, a komplex számok
 1 Komplex sámok 1 A komplex sámok algeba alakja 11 Defícó: A komplex sám algeba alakja: em más, mt x y, ahol x, y R és 1 A x -et soktuk a komplex sám valós éséek eve, míg y -t a komplex sám képetes (vagy
1 Komplex sámok 1 A komplex sámok algeba alakja 11 Defícó: A komplex sám algeba alakja: em más, mt x y, ahol x, y R és 1 A x -et soktuk a komplex sám valós éséek eve, míg y -t a komplex sám képetes (vagy
10.M ALGEBRA < <
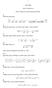 0.M ALGEBRA GYÖKÖS KIFEJEZÉSEK. Mutassuk meg, hogy < + +... + < + + 008 009 + 009 008 5. Mutassuk meg, hogy va olya pozitív egész szám, amelyre 99 < + + +... + < 995. Igazoljuk, hogy bármely pozitív egész
0.M ALGEBRA GYÖKÖS KIFEJEZÉSEK. Mutassuk meg, hogy < + +... + < + + 008 009 + 009 008 5. Mutassuk meg, hogy va olya pozitív egész szám, amelyre 99 < + + +... + < 995. Igazoljuk, hogy bármely pozitív egész
Valós függvénytan. rendezett pár, ( x, valós számok leképezése az csoportra. függvény mint előírás, pl. y x azt jelenti, hogy x
 II. Valós függvéyta Alapvetőe ebbe a fejezetbe s elem matematka smeretekről lesz szó, de az smeretek alapos, készségsztű begyakorlása (mely esetleg túlmegy az tt közölt feladatok megoldásá) elegedhetetleek
II. Valós függvéyta Alapvetőe ebbe a fejezetbe s elem matematka smeretekről lesz szó, de az smeretek alapos, készségsztű begyakorlása (mely esetleg túlmegy az tt közölt feladatok megoldásá) elegedhetetleek
Járattípusok. Kapcsolatok szerint: Sugaras, ingajárat: Vonaljárat: Körjárat:
 JÁRATTERVEZÉS Kapcsolatok szert: Sugaras, gaárat: Járattípusok Voalárat: Körárat: Targocás árattervezés egyszerű modelle Feltételek: az ayagáram determsztkus, a beszállítás és kszállítás dőpot em kötött
JÁRATTERVEZÉS Kapcsolatok szert: Sugaras, gaárat: Járattípusok Voalárat: Körárat: Targocás árattervezés egyszerű modelle Feltételek: az ayagáram determsztkus, a beszállítás és kszállítás dőpot em kötött
Labormérések minimumkérdései a B.Sc képzésben
 Labormérések mmumkérdése a B.Sc képzésbe 1. Ismertesse a levegő sűrűség meghatározásáak módját a légyomás és a levegő hőmérséklet alapjá! Adja meg a képletbe szereplő meységek jeletését és mértékegységét!
Labormérések mmumkérdése a B.Sc képzésbe 1. Ismertesse a levegő sűrűség meghatározásáak módját a légyomás és a levegő hőmérséklet alapjá! Adja meg a képletbe szereplő meységek jeletését és mértékegységét!
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével
 5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
AZ OPTIMÁLIS MINTANAGYSÁG A KAPCSOLÓDÓ KÖLTSÉGEK ÉS BEVÉTELEK RELÁCIÓJÁBAN
 AZ OPTIMÁLIS MINTANAGYSÁG A KAPCSOLÓDÓ KÖLTSÉGEK ÉS BEVÉTELEK RELÁCIÓJÁBAN Molár László Ph.D. hallgató Mskolc Egyetem, Gazdaságelmélet Itézet 1. A MINTANAGYSÁG MEGHATÁROZÁSA EGYSZERŐ VÉLETLEN (EV) MINTA
AZ OPTIMÁLIS MINTANAGYSÁG A KAPCSOLÓDÓ KÖLTSÉGEK ÉS BEVÉTELEK RELÁCIÓJÁBAN Molár László Ph.D. hallgató Mskolc Egyetem, Gazdaságelmélet Itézet 1. A MINTANAGYSÁG MEGHATÁROZÁSA EGYSZERŐ VÉLETLEN (EV) MINTA
A MATEMATIKAI STATISZTIKA ELEMEI
 A MATEMATIKAI STATISZTIKA ELEMEI Az Eötvös Lórád Tudomáyegyetem Természettudomáy Kará a Fzka Kéma Taszék évek óta kéma-szakos taárhallgatókak matematka bevezetõ elõadásokat tart. Az elõadások célja az,
A MATEMATIKAI STATISZTIKA ELEMEI Az Eötvös Lórád Tudomáyegyetem Természettudomáy Kará a Fzka Kéma Taszék évek óta kéma-szakos taárhallgatókak matematka bevezetõ elõadásokat tart. Az elõadások célja az,
Komplex számok. d) Re(z 4 ) = 0, Im(z 4 ) = 1 e) Re(z 5 ) = 0, Im(z 5 ) = 2 f) Re(z 6 ) = 1, Im(z 6 ) = 0
 Komplex számok 1 Adjuk meg az alábbi komplex számok valós, illetve képzetes részét: a + i b i c z d z i e z 5 i f z 1 A z a + bi komplex szám valós része: Rez a, képzetes része Imz b Ez alapjá a megoldások
Komplex számok 1 Adjuk meg az alábbi komplex számok valós, illetve képzetes részét: a + i b i c z d z i e z 5 i f z 1 A z a + bi komplex szám valós része: Rez a, képzetes része Imz b Ez alapjá a megoldások
8.1. A rezgések szétcsatolása harmonikus közelítésben. Normálrezgések. = =q n és legyen itt a potenciál nulla. q i j. szimmetrikus. q k.
 8. KIS REZGÉSEK STABIL EGYENSÚLYI HELYZET KÖRÜL 8.. A rezgések szétcsatolása harmoikus közelítésbe. Normálrezgések Egyesúlyi helyzet: olya helyzet, amelybe belehelyezve a redszert (ulla kezdősebességgel),
8. KIS REZGÉSEK STABIL EGYENSÚLYI HELYZET KÖRÜL 8.. A rezgések szétcsatolása harmoikus közelítésbe. Normálrezgések Egyesúlyi helyzet: olya helyzet, amelybe belehelyezve a redszert (ulla kezdősebességgel),
