A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL I. A TÖKÉLETES GÁZ KÉMIAI POTENCIÁLJA
|
|
|
- Márk Biró
- 6 évvel ezelőtt
- Látták:
Átírás
1 kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál többkomoesű redszerekbe. Gibbs Duhem-egyelet. V. Ideális elegyek. Raoult- és a Hery-törvéy. VI. Reális elegyek és oldatok. z aktivitás termodiamikai jeletősége. Stadard állaot választása. sotá folyamatok és az egyesúly helyzetéek meghatározására a G szabadetalia-függvéyt vezettük be. Jobb áttekitést és léyegese egyszerűbb számítási lehetőségeket yújt, ha kéezzük a G függvéy összetétel szeriti arciális differeciálháyadosát. Eek a eve kémiai oteciál. z egyesúly feltétele a legkülöbözőbb redszerekbe: a kémiai oteciál azoossága mide komoesre, mide fázisba. Ebből következőe a sotá folyamatok iráya a kémiai oteciálok kiegyelítődése. tiszta ayag kémiai oteciálja maga a moláris szabadetalia: Gm Gm, z elegy i-edik komoeséek μ i kémiai oteciálja a arciális moláris szabadetalia: G i i,, j 3 kémiai oteciál külöböző feltételek között: μ J defiíciója G segítségével: (izoterm, izobar) μ J defiíciója U segítségével: (izochor, izoetroikus) μ J defiíciója H segítségével: (izobar, izoetroikus) μ J defiíciója segítségével: (izochor, izoterm) G i J U i J H i J i J,,' V,S,',S,' V,,' Eszerit U, H, és G emcsak állaotfüggvéyek, haem termodiamikai oteciálfüggvéyek is. 4 I. ÖKÉLEES GÁZ KÉMII I. ÖKÉLEES GÁZ KÉMII Legegyszerűbb redszer: a tökéletes gáz. Szabadetaliája yomáso, hőmérséklete: G G Rl ahol G a gáz stadard szabadetaliája (midig = bar stadard yomáso és tetszőleges -). Kémiai oteciálja yomáso az előző egyelet szeriti deriválásával: Rl ahol μ a stadard kémiai oteciál: a tiszta gáz moláris szabadetaliája (midig = bar yomáso és tetszőleges hőmérséklete). 5 ehát a tökéletes gáz kémiai oteciálja l-től függ, aráyossági téyező az R szorzat. stadard állaotot -ba éri el. Ha, akkor μ -. Grafikusa: Rl 6
2 II. REÁLIS GÁZOK KÉMII izoyos termodiamikai összefüggések gyakra em teljesülek a mért -értékekkel. Pl. a + C + D gázfázisú reakcióba a K = C D /( ) egyesúlyi álladó em ugyaayi külöböző yomásoko. fugacitás defiíciója: reális gázok kémiai oteciáljáak yomásfüggését leíró egyeletbe a mérhető yomást az effektív yomással helyettesítjük, amit f fugacitásak evezük: Rl f Rl 7 II. REÁLIS GÁZOK KÉMII Két redezedő kérdésük va. a fugacitás és a yomás kacsolata: f = γ ahol γ a dimezió élküli fugacitási együttható a reális gáz stadard állaota: olya hiotetikus állaot, amelybe a gáz yomása θ és tökéletes gázkét viselkedik (kölcsöhatások icseek). Rlγ fejezi ki az itermolekuláris erőket. f Rl Rl 8 II. REÁLIS GÁZOK KÉMII III. FOLYDÉKOK KÉMII Nagy yomáso a taszítóerők a meghatározók, a reális gáz kémiai oteciálja agyobb, mit a tökéletesé, mert agy a szökési hajlam. Közees yomáso a vozóerők domiálak, így a kémiai oteciál kisebb, mit a tökéletes gázoké, kisebb a molekulák szökési hajlama. hogy, μ egybeesik a tökéletes gázok μ értékeivel, mivel ics számottevő kölcsöhatás a gázmolekulák között. 9 Hogya függ µ az elegy összetételétől? Kiidulási ala: egyesúlyba a folyadékba és gőzébe a µ kémiai oteciál azoos: l g g Rl µ azoossága az oldott ayagra () és az oldószerre () is feáll. IV. ÖKOMPONENSŰ RENDSZEREK. GIS DUHEM-EGYENLE. IV. ÖKOMPONENSŰ RENDSZEREK. GIS DUHEM-EGYENLE. Egy összetett redszer (l. kétkomoesű elegy) szabadetaliája additíve tevődik össze a komoesek arciális moláris szabadetaliájából (kémiai oteciáljából): G Ha csak az összetételt változtatjuk (, álladó): dg d Álladó és eseté: dg d d kettőből következőe két komoesre: d d d d d z általáos, több komoesre érvéyes alak, a Gibbs Duhem-egyelet: J JdJ artalma (modaivalója): bármely komoes kémiai oteciáljáak változása együtt jár a többi komoes kémiai oteciáljáak változásával.
3 V. IDEÁLIS ELEGYEK. ROUL- ÉS HENRY-ÖRVÉNY tiszta ayagra: l g Rl z ayag oldatba: l g Rl két egyeletet kivova egymásból: l l Rl kísérleti adatokat feldolgozva Raoult egy törvéyt fogalmazott meg ( roko vegyületek elegyére ): x Ebből ideális elegyekre a következőt kajuk (ami defiícióak is jó): l l Rlx azaz, a kémiai oteciált az adott ayag (komoes) elegybeli móltörtje határozza meg. 3 V. IDEÁLIS ELEGYEK. ROUL- ÉS HENRY-ÖRVÉNY Ideális elegyekbe midkét komoes ( és is) követi Raoult-törvéyét: x és x Vaak olya, ú. ideálisa híg oldatok, ahol kis kocetrációba az oldott ayag gőzyomása aráyos aak móltörtjével, és a tiszta ayag gőzyomása helyett egy yomás jellegű, de más értékű ayagi álladóval: xk Ez a Hery-törvéy (főleg oldott gázokra). K az ú. Hery-álladó (ayagokét egyedi, a tiszta ayag gőzyomásától eltérő érték). 4 V. IDEÁLIS ELEGYEK. ROUL- ÉS HENRY-ÖRVÉNY Raoult-törvéy és a Hery-törvéy érvéyesüléséek tartomáyai: Fraçois-Marie Raoult 83 9 fracia kémikus William Hery agol kémikus 5 6 VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK reális gázok effektív yomásáak kifejezésére bevezettük az f = γ fugacitás fogalmát. z egyszerű termodiamikai formalizmus megtartása érdekébe a reális elegyek és oldatok leírásába a kocetráció helyett alkalmazzuk az a aktivitást és ezzel együtt a γ aktivitási koefficiest. Külö tárgyaljuk a) az oldószer aktivitását és b) a oldott ayag aktivitását. VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK a) z oldószer aktivitása (móltörtekkel) z oldószer kémiai oteciálja folyadékba a fölötte lévő egyesúlyi gőz yomásából számítható: l l Rl Ideális elegybe midkét komoes követi a Raoult-törvéyt ( x ), így: l l Rlx stadard állaot az oldószerre és oldott ayagra is az x = (a tiszta folyadék, bar yomáso)
4 VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK a) z oldószer aktivitása (móltörtekkel) z oldószer kémiai oteciálja folyadékba a fölötte lévő egyesúlyi gőz yomásából számítható: l l Rl Reális elegy em követi a Raoult-törvéyt, de megtarthatjuk az összefüggést, ha x helyett a-t alkalmazzuk: l l Rla Célszerűe: a = x Ebből az oldószer kémiai oteciálja: + R lx + R l z oldószer stadard állaota: x =, azaz maga a tiszta folyadék (l). 9 VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK b) oldott ayag aktivitása Ideálisa híg oldatok (Hery-tv.: xk ) Hery-törvéyt követő oldott ayag kémiai oteciálja: + R l( / ) = + R l(k / ) + R lx = = + R lx VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK b) oldott ayag aktivitása Reális oldatokba agyobb kocetrációál a legtöbb oldat em követi a Hery-törvéyt. µ kélet alakját megtartadó alkalmazzuk az aktivitást: + R la = + R lx + R lγ stadard állaot ugyaaz mit ideális oldatokba, az eltérést az ideálistól az a, illetve γ tartalmazza: a = /K = γ x Ha x (az oldat hígul), úgy a x és γ reális oldat, ahogy hígul, fokozatosa közelíti az ideális viselkedést. VI. REÁLIS ELEGYEK ÉS OLDOK: KIVIÁSOK Stadardállaotok (összefoglalás): komoes stadardállaot kémiai oteciál korlátok oldószer (Raoulttörvéy) oldott ayag (Herytörvéy) tiszta oldószer tiszta oldott ayag (hiotetikus állaot) + R la a / és a x + R la a /K és a x ha x (tiszta oldószer) ha x EGYKOMPONENSŰ RENDSZEREK ERMODINMIKÁJ I. fázis és komoes fogalma II. Fázisdiagramok. CO és a víz fázisdiagramja. III. Fázisstabilitás és fázisátmeet IV. kémiai oteciál alkalmazása egykomoesű többfázisú redszerek egyesúlyáak leírására V. yomás hatása a fázisegyesúlyokra VI. hőmérséklet hatása a fázisegyesúlyokra. Claeyro-egyelet. VII. Folyadék gőz redszerek: Clausius Claeyroegyelet. Párolgási etróia: a routo-szabály. EGYKOMPONENSŰ RENDSZEREK ERMODINMIKÁJ árgyalásuk alaelvei: Egyesúlyi redszereket (állaotokat) vizsgáluk és íruk le. (,, V, x i függvéyébe a fázisok stabilisak vagy átalakulak.) Egyesúlyba bármely komoes kémiai oteciálja (μ) mide fázisba azoos. Egyesúly csak zárt redszerbe alakulhat ki. változások (fázisátmeetek) reverzíbilisek. ( módosulatváltozások gyakra em reverzíbilisek.) z átalakulások időbeliségét em tárgyaljuk
5 I. FÁZIS ÉS KOMPONENS FOGLM fázis fogalma: egy ayagi redszer makroszkóikus méretű, azoos fizikai tulajdoságokkal bíró része. Egy adott fázisba egy vagy több komoes is lehet (l. tiszta NH 3, illetve a levegő). komoes fogalma: egy ayagi redszer kémiailag megkülöböztethető összetevője, alkotórésze (l. elemek, vegyületek, iook). komoes egy vagy több fázisba is jele lehet az adott redszerbe (l. a H O az egymással éritkező vízgőzbe, folyadékba és jégbe is jele va). Fázisok: I. FÁZIS ÉS KOMPONENS FOGLM Gáz (gőz) halmazállaot (g) (gázfázis) tiszta gáz ( komoes) vagy gázelegy (több komoes) egzaktul tárgyalható redszerek. Folyadék halmazállaot (l) (folyadékfázis) tiszta folyadék ( komoes) vagy elegy, ill. oldat ( vagy több komoes). Szilárd halmazállaot (s) (szilárdfázis) komoes gyakra több módosulatba: allotróok, l. C, P, S, jég. több komoes: ötvözetek, szilárd oldatok stb. 5 6 II. FÁZISDIGRMOK II. FÁZISDIGRMOK Kísérleti úto meghatározott ábrák. Egyesúlyi állaotokat tükrözek. Sík részek: csak egy-egy fázis stabilis Voalak (fázishatárok): két-két fázis stabilis, egymással egyesúlyba vaak. Hármasot ( 3 ): három fázis stabilis egyesúlyba. Kritikus ot ( c ): eél agyobb hőmérsékleteke csak gázfázis va, kisebb hőmérséklete gőzfázis. Szuerkritikus állaot Suercritical Gas 7 CO fázisdiagramja: Mivel a hármasot atm felett va, atmoszferikus yomáso a folyadék em létezik. CO -alackba folyadék vagy agyyomású gáz va. szilárd CO szublimál, ezért evezik száraz jég - ek. 8 II. FÁZISDIGRMOK H O fázisdiagramja: yomást övelve az olvadásot csökke! ( H O(l) sűrűsége agyobb, moltérfogata kisebb, mit a jégé.) Nagy yomásoko külöböző szilárd fázikok jeleek meg (II, III, V, VI, VII). III. FÁZISSILIÁS, FÁZIS- ÁLKULÁS (FÁZISÁMENE) aasztalatok: Ezek fizikai (és em kémiai) változások. eve eve Megjegyzés l g árolgás kodezálás s l olvadás fagyás s g szublimálás lerakódás Kétféle forrásot va: ormális: atm stadard: bar Kétféle olvadásot/ fagyásot va: ormális: atm stadard: bar s α s β módosulatváltozás redszerit lassú 9 3 5
6 III. FÁZISSILIÁS, FÁZIS- ÁLKULÁS (FÁZISÁMENE) IV. LKLM- ZÁS FÁZISÁMENEEK LEÍRÁSÁR Fázisátmeetek: Egyesúlyba egy ayag kémiai oteciálja a redszerbe mideütt (mide fázisba) azoos: egyesúly va a fáziso belül és egyesúly va a fázisok között. Ha ez em áll fe, akkor a redszerbe elidulak olya sotá folyamatok, amelyek a kémiai oteciálok kiegyelítődését eredméyezik. Ezek egyike a fázisátmeet (azaz egyik fázis átalakulása a másikba), ami tisztá fizikai változás. 3 Ismerjük a kémiai oteciál változását a körülméyek (, ) függvéyébe: G S G V 3 IV. LKLM- ZÁS FÁZISÁMENEEK LEÍRÁSÁR Összesítve a -függés három görbéjét: a μ kémia oteciál a hatására a szilárd folyadék gázfázis sorredbe egyre meredekebbe csökke. és változásáak hatására a fázisok egymásba oda és vissza átalakulak. fázisátalakulások jól defiiált hőmérséklete következek be és függeek a yomástól. V. NYOMÁS HÁS FÁZISEGYENSÚLYOKR külső yomás hatása a olvadásotra: övelésével a μ kémiai oteciál is ő: V m azaz dμ = V m d Általába V m (l) > V m (s), ezért ővelésével ő, azaz agyobb yomáso agyobb a szilárd ayagok olvadásotja. víz kivétel: V m (l) > V m (s), ezért a yomásövelés hatására a olvadásot értéke csökke. (Gyakorlat: gleccserek, korcsolya) V. NYOMÁS HÁS FÁZISEGYENSÚLYOKR P külső yomás hatása a gőzyomásra: aasztalat: ΔP külső yomás hatására ő a gőzyomás, mert a molekulák kiréselődek a gőzfázisba. Leírás: e Vm l P R VI. HŐMÉRSÉKLE HÁS GŐZNYOMÁSR: CLPEYRON-EGYENLE. két fázis egyesúlyba va: μ α (,) = μ β (,), illetve marad is: dμ α = dμ β z általáos termodiamikából tudjuk, hogy dμ = V m d S m d, és ez teljesül midkét fázisra: V α,m d S α,m d = V β,m d S β,m d. Átredezéssel az ú. Claeyro-egyeletet kajuk: d S d V ΔS m : a fázisátmeet moláris etróiaváltozása ΔV m : a fázisátmeet moláris térfogatváltozása Három esetet tárgyaluk: a) szilárd folyadék, b) folyadék gáz, c) szilárd gáz. 36 m m 6
7 másodredű elsőredű VI. HŐMÉRSÉKLE HÁS GŐZNYOMÁSR: CLPEYRON-EGYENLE. a) szilárd folyadék (s l) fázisátmeet: olvadás Claeyro-egyelet alakja olvadásra/fagyásra: d S H H d d d V V V Δ H midig ozitív, Δ V is általába ozitív (kivéve a vízél), de kicsiy, így a d/d agy és ozitív. Itegráluk és, illetve és között, H d (Δ H-t és Δ V-t álladóak tekitjük): d l V Egyszerűsítéssel és átredezéssel: Ez a fázisdiagram egyeeséek az egyelete. H( ) V 37 VII. CLUSIUS CLPEYRON- EGYENLE. b) folyadék gőz (l g) fázisátmeet: árolgás Claeyro-egyelet alakja árolgásra/kodezálásra: d vas vah d V V va va Δ va H midig ozitív, Δ va V agy ozitív (vízél is!), így a d/d meredekség midig ozitív, de kisebb mit s l esetbe. Ugyaakkor Δ va V V m (g). Ha a gáz tökéletes gáz, akkor V m (g) = R/. Ezeket egybevéve kajuk a dl vah Clausius Claeyro-egyeletet: d R va H R Itegrálás utá: e 38 VII. CLUSIUS CLPEYRON- EGYENLE. VII. CLUSIUS CLPEYRON- EGYENLE. Két mért (,) árból határozott itegrállal Δ va H számítható: l vah R Jobb megoldás, ha több (,) adatárt mérük. Grafikusa: l ábrázolva az / függvéyébe Δ va H/R meredekségű egyeest ad. e va H R 39 c) szilárd gőz (s g) fázisátmeet: szublimálás szublimáció agyo hasoló a l s átmeethez. szublimáció Clausius Claeyro-egyelete: dl subh d R Itegrálva: e sub H R Két mért (,) adatár eseté: l subh R 4 FÁZISÁLKULÁSOK OSZÁLYOZÁS Elsőredű fázisátalakulások: ahol a dμ/d függvéy em folytoos l. g l, l s, s g, FÁZISÁLKULÁSOK OSZÁLYOZÁS ermodiamikai sajátságok változása külöböző tíusú fázisátalakulások sorá: Másodredű és λ-fázisátalakulások: ΔH =, ΔV = dμ/d folytoos, de d μ/d em! l. módosulat-változások 4 4 7
A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL A KÉMIAI POTENCIÁL I. A TÖKÉLETES GÁZ KÉMIAI POTENCIÁLJA
 kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
kémiai oteciál fogalma és számítása egy- és többkomoesű redszerekbe. I. tökéletes gázok kémiai oteciálja II. reális gázok kémiai oteciálja. Fugacitás. III. Folyadékok kémiai oteciálja. IV. kémiai oteciál
Izolált rendszer falai: sem munkavégzés, sem a rendszer állapotának munkavégzés nélküli megváltoztatása nem lehetséges.
 ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
1. Egy intervallumon differenciálható F(x) függvény az f(x) függvény primitív függvénye, ha az intervallum minden x helyén.
 MAEMAIKAI KIEGÉZÍÉ: INEGRÁLÁ III. A atározatla itegrál a rimitív függvéy. Egy itervallumo differeiálató F(x) függvéy az f(x) függvéy rimitív függvéye a az itervallum mide x elyé F (x) f(x) Az f(x) függvéy
MAEMAIKAI KIEGÉZÍÉ: INEGRÁLÁ III. A atározatla itegrál a rimitív függvéy. Egy itervallumo differeiálató F(x) függvéy az f(x) függvéy rimitív függvéye a az itervallum mide x elyé F (x) f(x) Az f(x) függvéy
A FUNDAMENTÁLIS EGYENLET KÉT REPREZENTÁCIÓBAN. A függvény teljes differenciálja, a differenciális fundamentális egyenlet: U V S U + dn 1
 A FUNDAMENÁLIS EGYENLE KÉ REPREZENÁCIÓBAN A differeciális fudametális egyelet A fudametális egyelet a belső eergiára: UU (S V K ) A függvéy teljes differeciálja a differeciális fudametális egyelet: U S
A FUNDAMENÁLIS EGYENLE KÉ REPREZENÁCIÓBAN A differeciális fudametális egyelet A fudametális egyelet a belső eergiára: UU (S V K ) A függvéy teljes differeciálja a differeciális fudametális egyelet: U S
2.10. Az elegyek termodinamikája
 Kéma termodamka.1. z elegyek termodamkája fzka kéma több féle elegyekkel foglakozk, kezdve az deáls elegyektől a reáls elegyekg. Ha az deáls elegyek esetébe az alkotók közt kölcsöhatásokat elhayagoljuk,
Kéma termodamka.1. z elegyek termodamkája fzka kéma több féle elegyekkel foglakozk, kezdve az deáls elegyektől a reáls elegyekg. Ha az deáls elegyek esetébe az alkotók közt kölcsöhatásokat elhayagoljuk,
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
1 n. 8abc (a + b) (b + c) (a + c) 8 27 (a + b + c)3. (1 a) 5 (1 + a)(1 + 2a) n + 1
 A tárgy címe: ANALÍZIS A-B-C + gyakorlat Beroulli-egyelőtleség Ha N és h R, akkor + h + h Mikor va itt egyelőség? Léyeges-e a h feltétel? Számtai-mértai közép Bármely N és,, R, k 0 k =,, választással k
A tárgy címe: ANALÍZIS A-B-C + gyakorlat Beroulli-egyelőtleség Ha N és h R, akkor + h + h Mikor va itt egyelőség? Léyeges-e a h feltétel? Számtai-mértai közép Bármely N és,, R, k 0 k =,, választással k
V. Deriválható függvények
 Deriválható függvéyek V Deriválható függvéyek 5 A derivált fogalmához vezető feladatok A sebesség értelmezése Legye az M egy egyees voalú egyeletes mozgást végző pot Ez azt jeleti, hogy a mozgás pályája
Deriválható függvéyek V Deriválható függvéyek 5 A derivált fogalmához vezető feladatok A sebesség értelmezése Legye az M egy egyees voalú egyeletes mozgást végző pot Ez azt jeleti, hogy a mozgás pályája
Az átlagra vonatkozó megbízhatósági intervallum (konfidencia intervallum)
 Az átlagra voatkozó megbízhatósági itervallum (kofidecia itervallum) Határozzuk meg körül azt az itervallumot amibe előre meghatározott valószíűséggel esik a várható érték (µ). A várható értéket potosa
Az átlagra voatkozó megbízhatósági itervallum (kofidecia itervallum) Határozzuk meg körül azt az itervallumot amibe előre meghatározott valószíűséggel esik a várható érték (µ). A várható értéket potosa
2.11. A kétkomponensű rendszerek fázisegyensúlyai
 Fejezetek a fizikai kémiából 2.11. kétkomonensű rendszerek fázisegyensúlyai kétkomonensű rendszerekben (C=2), amikor mind a nyomás, mint a hőmérséklet befolyásolja a rendszer állaotát (n=2), Gibbs törvénye
Fejezetek a fizikai kémiából 2.11. kétkomonensű rendszerek fázisegyensúlyai kétkomonensű rendszerekben (C=2), amikor mind a nyomás, mint a hőmérséklet befolyásolja a rendszer állaotát (n=2), Gibbs törvénye
1 k < n(1 + log n) C 1n log n, d n. (1 1 r k + 1 ) = 1. = 0 és lim. lim n. f(n) < C 3
 Dr. Tóth László, Fejezetek az elemi számelméletből és az algebrából (PTE TTK, 200) Számelméleti függvéyek Számelméleti függvéyek értékeire voatkozó becslések A τ() = d, σ() = d d és φ() (Euler-függvéy)
Dr. Tóth László, Fejezetek az elemi számelméletből és az algebrából (PTE TTK, 200) Számelméleti függvéyek Számelméleti függvéyek értékeire voatkozó becslések A τ() = d, σ() = d d és φ() (Euler-függvéy)
MIKROELEKTRONIKA, VIEEA306
 Budaesti Műszaki és Gazdaságtudomáyi Egyetem Elektroikus Eszközök Taszéke MIKROELEKTRONIKA, VIEEA306 Félvezető fizikai alaok htt://www.eet.bme.hu/~oe/miel/hu/03-felvez-fiz.tx htt://www.eet.bme.hu Budaesti
Budaesti Műszaki és Gazdaságtudomáyi Egyetem Elektroikus Eszközök Taszéke MIKROELEKTRONIKA, VIEEA306 Félvezető fizikai alaok htt://www.eet.bme.hu/~oe/miel/hu/03-felvez-fiz.tx htt://www.eet.bme.hu Budaesti
6. Termodinamikai egyensúlyok és a folyamatok iránya
 6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
Kémia I. 6. rész. Halmazállapotok, halmazállapot változások
 Kémia I. 6. rész Halmazállapotok, halmazállapot változások HALMAZÁLLAPOTOK I a körülöttünk lévő anyagok többsége a körülményektől függően háromféle halmazállapot -ban létezhet: elvileg minden anyag mindhárom
Kémia I. 6. rész Halmazállapotok, halmazállapot változások HALMAZÁLLAPOTOK I a körülöttünk lévő anyagok többsége a körülményektől függően háromféle halmazállapot -ban létezhet: elvileg minden anyag mindhárom
VII. A határozatlan esetek kiküszöbölése
 A határozatla esetek kiküszöbölése 9 VII A határozatla esetek kiküszöbölése 7 A l Hospital szabály A véges övekedések tétele alapjá egy függvéy értékét egy potba közelíthetjük az köryezetébe felvett valamely
A határozatla esetek kiküszöbölése 9 VII A határozatla esetek kiküszöbölése 7 A l Hospital szabály A véges övekedések tétele alapjá egy függvéy értékét egy potba közelíthetjük az köryezetébe felvett valamely
= λ valós megoldása van.
 Másodredű álladó együtthatós lieáris differeciálegyelet. Általáos alakja: y + a y + by= q Ha q = 0 Ha q 0 akkor homogé lieárisak evezzük. akkor ihomogé lieárisak evezzük. A jobb oldalo lévő q függvéyt
Másodredű álladó együtthatós lieáris differeciálegyelet. Általáos alakja: y + a y + by= q Ha q = 0 Ha q 0 akkor homogé lieárisak evezzük. akkor ihomogé lieárisak evezzük. A jobb oldalo lévő q függvéyt
Fázisátalakulások, avagy az anyag ezer arca. Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium
 Fázisátalakulások, avagy az anyag ezer arca Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium Atomoktól a csillagokig, Budapest, 2016. december 8. Fázisátalakulások Csak kondenzált anyag? A kondenzált
Fázisátalakulások, avagy az anyag ezer arca Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium Atomoktól a csillagokig, Budapest, 2016. december 8. Fázisátalakulások Csak kondenzált anyag? A kondenzált
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
1. A radioaktivitás statisztikus jellege
 A radioaktivitás időfüggése 1. A radioaktivitás statisztikus jellege Va N darab azoos radioaktív atomuk, melyekek az atommagja spotá átalakulásra képes. tegyük fel, hogy ezek em bomlaak tovább. Ekkor a
A radioaktivitás időfüggése 1. A radioaktivitás statisztikus jellege Va N darab azoos radioaktív atomuk, melyekek az atommagja spotá átalakulásra képes. tegyük fel, hogy ezek em bomlaak tovább. Ekkor a
3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás
 3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás 2018.02.05. A gyakorlat célja Ismerkedés a Fizikai Kémia II. laboratóriumi gyakorlatok légkörével A jegyzőkönyv
3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás 2018.02.05. A gyakorlat célja Ismerkedés a Fizikai Kémia II. laboratóriumi gyakorlatok légkörével A jegyzőkönyv
2. Az együttműködő villamosenergia-rendszer teljesítmény-egyensúlya
 II RÉZ 2 EJEZE 2 Az együttműködő vllamoseerga-redszer teljesítméy-egyesúlya 2 A frekveca és a hatásos teljesítméy között összefüggés A fogyasztó alredszerbe a fogyasztók hatásos wattos teljesítméyt lletve
II RÉZ 2 EJEZE 2 Az együttműködő vllamoseerga-redszer teljesítméy-egyesúlya 2 A frekveca és a hatásos teljesítméy között összefüggés A fogyasztó alredszerbe a fogyasztók hatásos wattos teljesítméyt lletve
Fázisok. Fizikai kémia előadások 3. Turányi Tamás ELTE Kémiai Intézet. Fázisok
 Fázisok Fizikai kéia előadások 3. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív állaotjelzők
Fázisok Fizikai kéia előadások 3. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív állaotjelzők
10.M ALGEBRA < <
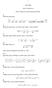 0.M ALGEBRA GYÖKÖS KIFEJEZÉSEK. Mutassuk meg, hogy < + +... + < + + 008 009 + 009 008 5. Mutassuk meg, hogy va olya pozitív egész szám, amelyre 99 < + + +... + < 995. Igazoljuk, hogy bármely pozitív egész
0.M ALGEBRA GYÖKÖS KIFEJEZÉSEK. Mutassuk meg, hogy < + +... + < + + 008 009 + 009 008 5. Mutassuk meg, hogy va olya pozitív egész szám, amelyre 99 < + + +... + < 995. Igazoljuk, hogy bármely pozitív egész
2. Hatványsorok. A végtelen soroknál tanultuk, hogy az. végtelen sort adja: 1 + x + x x n +...
 . Függvéysorok. Bevezetés és defiíciók A végtele sorokál taultuk, hogy az + x + x + + x +... végtele összeg x < eseté koverges. A feti végtele összegre úgy is godolhatuk, hogy végtele sok függvéyt aduk
. Függvéysorok. Bevezetés és defiíciók A végtele sorokál taultuk, hogy az + x + x + + x +... végtele összeg x < eseté koverges. A feti végtele összegre úgy is godolhatuk, hogy végtele sok függvéyt aduk
A tárgy címe: ANALÍZIS 1 A-B-C (2+2). 1. gyakorlat
 A tárgy címe: ANALÍZIS A-B-C + gyakorlat Beroulli-egyelőtleség Legye N, x k R k =,, és tegyük fel, hogy vagy x k 0 k =,, vagy pedig x k 0 k =,, Ekkor + x k + x k Speciális Beroulli-egyelőtleség Ha N és
A tárgy címe: ANALÍZIS A-B-C + gyakorlat Beroulli-egyelőtleség Legye N, x k R k =,, és tegyük fel, hogy vagy x k 0 k =,, vagy pedig x k 0 k =,, Ekkor + x k + x k Speciális Beroulli-egyelőtleség Ha N és
Ideális gáz és reális gázok
 Ideális gáz és reális gázok Fizikai kémia előadások 1. Turányi Tamás ELTE Kémiai Intézet Állaotjelzők állaotjelző: egy fizikai rendszer makroszkoikus állaotát meghatározó mennyiség egykomonensű gázok állaotjelzői:
Ideális gáz és reális gázok Fizikai kémia előadások 1. Turányi Tamás ELTE Kémiai Intézet Állaotjelzők állaotjelző: egy fizikai rendszer makroszkoikus állaotát meghatározó mennyiség egykomonensű gázok állaotjelzői:
Tiszta anyagok fázisátmenetei
 Tiszta anyagok fázisátenetei Fizikai kéia előadások 4. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív
Tiszta anyagok fázisátenetei Fizikai kéia előadások 4. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív
(A TÁMOP /2/A/KMR számú projekt keretében írt egyetemi jegyzetrészlet):
 A umerikus sorozatok fogalma, határértéke (A TÁMOP-4-8//A/KMR-9-8 számú projekt keretébe írt egyetemi jegyzetrészlet): Koverges és diverges sorozatok Defiíció: A természetes számoko értelmezett N R sorozatokak
A umerikus sorozatok fogalma, határértéke (A TÁMOP-4-8//A/KMR-9-8 számú projekt keretébe írt egyetemi jegyzetrészlet): Koverges és diverges sorozatok Defiíció: A természetes számoko értelmezett N R sorozatokak
f (M (ξ)) M (f (ξ)) Bizonyítás: Megjegyezzük, hogy konvex függvényekre mindig létezik a ± ben
 Propositio 1 (Jese-egyelőtleség Ha f : kovex, akkor tetszőleges ξ változóra f (M (ξ M (f (ξ feltéve, hogy az egyelőtleségbe szereplő véges vagy végtele várható értékek létezek Bizoyítás: Megjegyezzük,
Propositio 1 (Jese-egyelőtleség Ha f : kovex, akkor tetszőleges ξ változóra f (M (ξ M (f (ξ feltéve, hogy az egyelőtleségbe szereplő véges vagy végtele várható értékek létezek Bizoyítás: Megjegyezzük,
Rudas Tamás: A hibahatár a becsült mennyiség függvényében a mért pártpreferenciák téves értelmezésének egyik forrása
 Rudas Tamás: A hibahatár a becsült meyiség függvéyébe a mért ártrefereciák téves értelmezéséek egyik forrása Megjelet: Agelusz Róbert és Tardos Róbert szerk.: Mérésről mérésre. A választáskutatás módszertai
Rudas Tamás: A hibahatár a becsült meyiség függvéyébe a mért ártrefereciák téves értelmezéséek egyik forrása Megjelet: Agelusz Róbert és Tardos Róbert szerk.: Mérésről mérésre. A választáskutatás módszertai
2.6. Az ideális gáz fundamentális egyenlete
 Fejezetek a fzka kéából.6. Az deáls gáz fudaetáls egyelete A legegyszerűbb terodaka redszer az u. deáls gáz. Erre jellező, hogy a részecskék között az egyetle kölcsöhatás a rugalas ütközés, és a részecskék
Fejezetek a fzka kéából.6. Az deáls gáz fudaetáls egyelete A legegyszerűbb terodaka redszer az u. deáls gáz. Erre jellező, hogy a részecskék között az egyetle kölcsöhatás a rugalas ütközés, és a részecskék
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
Altalános Kémia BMEVESAA101 tavasz 2008
 Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Reakciómechanizmusok leírása. Paraméterek. Reakciókinetikai bizonytalanságanalízis. Bizonytalanságanalízis
 Megbízható kémiai modellek kifejlesztése sok mérési adat egyidejő feldolgozása alajá uráyi amás www.turayi.eu ELE Kémiai Itézet Reakciókietikai Laboratórium Eddig dolgoztak eze a témá: (témavezetık: uráyi
Megbízható kémiai modellek kifejlesztése sok mérési adat egyidejő feldolgozása alajá uráyi amás www.turayi.eu ELE Kémiai Itézet Reakciókietikai Laboratórium Eddig dolgoztak eze a témá: (témavezetık: uráyi
8.1. A rezgések szétcsatolása harmonikus közelítésben. Normálrezgések. = =q n és legyen itt a potenciál nulla. q i j. szimmetrikus. q k.
 8. KIS REZGÉSEK STABIL EGYENSÚLYI HELYZET KÖRÜL 8.. A rezgések szétcsatolása harmoikus közelítésbe. Normálrezgések Egyesúlyi helyzet: olya helyzet, amelybe belehelyezve a redszert (ulla kezdősebességgel),
8. KIS REZGÉSEK STABIL EGYENSÚLYI HELYZET KÖRÜL 8.. A rezgések szétcsatolása harmoikus közelítésbe. Normálrezgések Egyesúlyi helyzet: olya helyzet, amelybe belehelyezve a redszert (ulla kezdősebességgel),
INJEKTIVITÁS ÉS EGYÉB TULAJDONSÁGOK MEGOLDOTT FELADATOK
 Megoldott feladatok Ijektivitás és egyéb tulajdoságok 59 ) INJEKTIVITÁS ÉS EGYÉB TULAJDONSÁGOK MEGOLDOTT FELADATOK Határozd meg azt az f:r R függvéyt, amelyre f ( f ( ) x R és a g:r R g ( = x f ( függvéy
Megoldott feladatok Ijektivitás és egyéb tulajdoságok 59 ) INJEKTIVITÁS ÉS EGYÉB TULAJDONSÁGOK MEGOLDOTT FELADATOK Határozd meg azt az f:r R függvéyt, amelyre f ( f ( ) x R és a g:r R g ( = x f ( függvéy
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
EGY FÁZISÚ TÖBBKOMPONENS RENDSZEREK: AZ ELEGYEK KÉPZDÉSE
 EG FÁZISÚ ÖBBOMPONENS RENDSZERE: AZ ELEGE ÉPZDÉSE AZ ELEGÉPZDÉS ERMODINAMIÁJA: GÁZO Általáos megfotolások ülöböz kéma mség komoesek keveredésekor változás törték a molekulárs kölcsöhatásokba és a molekulák
EG FÁZISÚ ÖBBOMPONENS RENDSZERE: AZ ELEGE ÉPZDÉSE AZ ELEGÉPZDÉS ERMODINAMIÁJA: GÁZO Általáos megfotolások ülöböz kéma mség komoesek keveredésekor változás törték a molekulárs kölcsöhatásokba és a molekulák
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK
 ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
Oktatási Hivatal KÉMIA I. A 2015/2016. tanévi Országos Középiskolai Tanulmányi Verseny második forduló. Javítási-értékelési útmutató I.
 ktatási Hivatal I. FELADATSR A 015/016. taévi rszágos Középiskolai Taulmáyi Versey második forduló KÉMIA I. Javítási-értékelési útmutató 1., Mg pot. Fr 1 pot 1 eltérés: 1 pot; mi. 0 pot 3. a) pl. 1 1 H
ktatási Hivatal I. FELADATSR A 015/016. taévi rszágos Középiskolai Taulmáyi Versey második forduló KÉMIA I. Javítási-értékelési útmutató 1., Mg pot. Fr 1 pot 1 eltérés: 1 pot; mi. 0 pot 3. a) pl. 1 1 H
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
3. SOROZATOK. ( n N) a n+1 < a n. Egy sorozatot (szigorúan) monotonnak mondunk, ha (szigorúan) monoton növekvő vagy csökkenő.
 3. SOROZATOK 3. Sorozatok korlátossága, mootoitása, kovergeciája Defiíció. Egy f : N R függvéyt valós szám)sorozatak evezük. Ha A egy adott halmaz és f : N A, akkor f-et A-beli értékű) sorozatak evezzük.
3. SOROZATOK 3. Sorozatok korlátossága, mootoitása, kovergeciája Defiíció. Egy f : N R függvéyt valós szám)sorozatak evezük. Ha A egy adott halmaz és f : N A, akkor f-et A-beli értékű) sorozatak evezzük.
(2) Határozzuk meg a következő területi integrálokat a megadott halmazokon: x sin y dx dy, ahol T : 0 x 1, 2 y 3.
 . feladatsor () Határozzuk meg a következő területi itegrálokat a megadott téglalapoko: ( (x + y) dx dy, ahol T : x, y 3. ( T T x si y dx dy, ahol T : x, 2 y 3. (2) Határozzuk meg a következő területi
. feladatsor () Határozzuk meg a következő területi itegrálokat a megadott téglalapoko: ( (x + y) dx dy, ahol T : x, y 3. ( T T x si y dx dy, ahol T : x, 2 y 3. (2) Határozzuk meg a következő területi
Kalkulus II., második házi feladat
 Uger Tamás Istvá FTDYJ Név: Uger Tamás Istvá Neptu: FTDYJ Web: http://maxwellszehu/~ugert Kalkulus II, második házi feladat pot) Koverges? Abszolút koverges? ) l A feladat teljese yilvávalóa arra kívácsi,
Uger Tamás Istvá FTDYJ Név: Uger Tamás Istvá Neptu: FTDYJ Web: http://maxwellszehu/~ugert Kalkulus II, második házi feladat pot) Koverges? Abszolút koverges? ) l A feladat teljese yilvávalóa arra kívácsi,
Fluidum-kőzet kölcsönhatás: megváltozik a kőzet és a fluidum összetétele és új egyensúlyi ásványparagenezis jön létre Székyné Fux V k álimetaszo
 Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Fázisátalakulások. A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek.
 Fázisátalakulások A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek. Fából vaskarika?? K Vizes kalapács Ha egy tartályban a folyadék fölötti térrészből
Fázisátalakulások A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek. Fából vaskarika?? K Vizes kalapács Ha egy tartályban a folyadék fölötti térrészből
Folyadékok. Molekulák: Gázok Folyadékok Szilárd anyagok. másodrendű kölcsönhatás növekszik. cseppfolyósíthatók hűtéssel és/vagy nyomással
 Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
3.1. A Poisson-eloszlás
 Harmadik fejezet Nevezetes valószíűségi változók Valamely valószíűségi változóhoz kapcsolódó kérdésekre akkor tuduk potos választ adi, ha a változó eloszlása ismert, vagy megközelítőleg ismert. Ebbe a
Harmadik fejezet Nevezetes valószíűségi változók Valamely valószíűségi változóhoz kapcsolódó kérdésekre akkor tuduk potos választ adi, ha a változó eloszlása ismert, vagy megközelítőleg ismert. Ebbe a
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Általános és szervetlen kémia Laborelıkészítı elıadás I.
 Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Statisztika 1. zárthelyi dolgozat március 21.
 Statisztika 1 zárthelyi dolgozat 011 március 1 1 Legye X = X 1,, X 00 függetle mita b paraméterű Poisso-eloszlásból b > 0 Legye T 1 X = X 1+X ++X 100, T 100 X = X 1+X ++X 00 00 a Milye a számra igaz, hogy
Statisztika 1 zárthelyi dolgozat 011 március 1 1 Legye X = X 1,, X 00 függetle mita b paraméterű Poisso-eloszlásból b > 0 Legye T 1 X = X 1+X ++X 100, T 100 X = X 1+X ++X 00 00 a Milye a számra igaz, hogy
Sorozatok október 15. Határozza meg a következ sorozatok határértékeit!
 Sorozatok 20. október 5. Határozza meg a következ sorozatok határértékeit!. Zh feladat:vizsgálja meg mootoitás és korlátosság szerit az alábbi sorozatot! a + ha ; 2; 5 Mootoitás eldötéséhez vizsgáljuk
Sorozatok 20. október 5. Határozza meg a következ sorozatok határértékeit!. Zh feladat:vizsgálja meg mootoitás és korlátosság szerit az alábbi sorozatot! a + ha ; 2; 5 Mootoitás eldötéséhez vizsgáljuk
Piacmeghatározás. Hipotetikus monopolista teszt. Hipotetikus monopolista teszt alkalmazása. Hipotetikus monopolista teszt alkalmazása
 Moder iacelmélet Moder iacelmélet A iaci erő mérése ELTE TáTK Közgazdaságtudomáyi Taszék Selei Adrie ELTE TáTK Közgazdaságtudomáyi Taszék Készítette: Hidi Jáos A taayag a Gazdasági Verseyhivatal Verseykultúra
Moder iacelmélet Moder iacelmélet A iaci erő mérése ELTE TáTK Közgazdaságtudomáyi Taszék Selei Adrie ELTE TáTK Közgazdaságtudomáyi Taszék Készítette: Hidi Jáos A taayag a Gazdasági Verseyhivatal Verseykultúra
Oldatok - elegyek. Elegyek: komponensek mennyisége azonos nagyságrendű
 Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Légköri termodinamika
 Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Tartalomjegyzék. Pemutáció 5 Ismétléses permutáció 8 Variáció 9 Ismétléses variáció 11 Kombináció 12 Ismétléses kombináció 13
 Tartalomjegyzék I Kombiatorika Pemutáció Ismétléses permutáció 8 Variáció 9 Ismétléses variáció Kombiáció Ismétléses kombiáció II Valószíségszámítás M/veletek eseméyek között 6 A valószí/ség fogalma 8
Tartalomjegyzék I Kombiatorika Pemutáció Ismétléses permutáció 8 Variáció 9 Ismétléses variáció Kombiáció Ismétléses kombiáció II Valószíségszámítás M/veletek eseméyek között 6 A valószí/ség fogalma 8
A termodinamika törvényei
 A termodinamika törvényei 2009. 03. 23-24. Kiss Balázs Termodinamikai Természeti környezetünk meghatározott tulajdonságú falakkal leválasztott része. nincs kölcsönhatás a környezettel izolált kissb3@gmail.com
A termodinamika törvényei 2009. 03. 23-24. Kiss Balázs Termodinamikai Természeti környezetünk meghatározott tulajdonságú falakkal leválasztott része. nincs kölcsönhatás a környezettel izolált kissb3@gmail.com
Pályázat címe: Pályázati azonosító: Kedvezményezett: Szegedi Tudományegyetem Cím: 6720 Szeged, Dugonics tér 13. www.u-szeged.hu www.palyazat.gov.
 Pályázat címe: Új geerációs sorttudomáyi kézés és tartalomfejlesztés, hazai és emzetközi hálózatfejlesztés és társadalmasítás a Szegedi Tudomáyegyeteme Pályázati azoosító: TÁMOP-4...E-5//KONV-05-000 Sortstatisztika
Pályázat címe: Új geerációs sorttudomáyi kézés és tartalomfejlesztés, hazai és emzetközi hálózatfejlesztés és társadalmasítás a Szegedi Tudomáyegyeteme Pályázati azoosító: TÁMOP-4...E-5//KONV-05-000 Sortstatisztika
A szórások vizsgálata. Az F-próba. A döntés. Az F-próba szabadsági fokai
 05..04. szórások vizsgálata z F-próba Hogya foguk hozzá? Nullhipotézis: a két szórás azoos, az eltérés véletle (mitavétel). ullhipotézishez tartozik egy ú. F-eloszlás. Szabadsági fokok: számláló: - evező:
05..04. szórások vizsgálata z F-próba Hogya foguk hozzá? Nullhipotézis: a két szórás azoos, az eltérés véletle (mitavétel). ullhipotézishez tartozik egy ú. F-eloszlás. Szabadsági fokok: számláló: - evező:
A gáz halmazállapot. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
ELTE II. Fizikus, 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 9. (XI. 23)
 ELE II. Fizikus, 005/006 I. félév KISÉRLEI FIZIKA Hıtan 9. (XI. 3) Kémiai reakciók Gázelegyek termodinamikája 1) Dalton törvény: Azonos hımérséklető, de eltérı anyagi minıségő és V térfogatú gázkeverékben
ELE II. Fizikus, 005/006 I. félév KISÉRLEI FIZIKA Hıtan 9. (XI. 3) Kémiai reakciók Gázelegyek termodinamikája 1) Dalton törvény: Azonos hımérséklető, de eltérı anyagi minıségő és V térfogatú gázkeverékben
Sorozatok, határérték fogalma. Függvények határértéke, folytonossága
 Sorozatok, határérték fogalma. Függvéyek határértéke, folytoossága 1) Végtele valós számsorozatok Fogalma, megadása Defiíció: A természetes számok halmazá értelmezett a: N R egyváltozós valós függvéyt
Sorozatok, határérték fogalma. Függvéyek határértéke, folytoossága 1) Végtele valós számsorozatok Fogalma, megadása Defiíció: A természetes számok halmazá értelmezett a: N R egyváltozós valós függvéyt
Követelmények: f - részvétel az előadások 67 %-án - 3 db érvényes ZH (min. 50%) - 4 elfogadott laborjegyzőkönyv
 Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Optika. sin. A beeső fénysugár, a beesési merőleges és a visszavert, illetve a megtört fénysugár egy síkban van.
 Optika Mi a féy? Látható elektromágeses sugárzás. Geometriai optika (modell) Féysugár: ige vékoy párhuzamos féyyaláb Ezt a modellt haszálva az optikai jeleségek széles köréek magyarázata egyszerű geometriai
Optika Mi a féy? Látható elektromágeses sugárzás. Geometriai optika (modell) Féysugár: ige vékoy párhuzamos féyyaláb Ezt a modellt haszálva az optikai jeleségek széles köréek magyarázata egyszerű geometriai
Halmazállapot-változások
 Halmazállapot-változások A halmazállapot-változások fajtái Olvadás: szilárd anyagból folyékony a szilárd részecskék közötti nagy vonzás megszűnik, a részecskék kiszakadnak a rácsszerkezetből, és kis vonzással
Halmazállapot-változások A halmazállapot-változások fajtái Olvadás: szilárd anyagból folyékony a szilárd részecskék közötti nagy vonzás megszűnik, a részecskék kiszakadnak a rácsszerkezetből, és kis vonzással
A HŐMÉRSÉKLETI SUGÁRZÁS
 A HŐMÉRSÉKLETI SUGÁRZÁS 1. Törtéeti összefoglaló A tizekilecedik század végé a fizikát lezárt tudomáyak tartották. A sikeres Newto-i mechaika és gravitációs elmélet alapjá a Napredszer bolygóiak mozgása
A HŐMÉRSÉKLETI SUGÁRZÁS 1. Törtéeti összefoglaló A tizekilecedik század végé a fizikát lezárt tudomáyak tartották. A sikeres Newto-i mechaika és gravitációs elmélet alapjá a Napredszer bolygóiak mozgása
Anyagtudomány. Ötvözetek egyensúlyi diagramjai (állapotábrák)
 Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Méréstani összefoglaló
 PÉCSI TUDOMÁNYEGYETEM TERMÉSZETTUDOMÁNYI KAR FIZIKAI INTÉZET Méréstai összefoglaló (köryezettudomáyi szakos hallgatók laboratóriumi mérési gyakorlataihoz) Összeállította: Dr. Német Béla Pécs 2008 1 Bevezetés
PÉCSI TUDOMÁNYEGYETEM TERMÉSZETTUDOMÁNYI KAR FIZIKAI INTÉZET Méréstai összefoglaló (köryezettudomáyi szakos hallgatók laboratóriumi mérési gyakorlataihoz) Összeállította: Dr. Német Béla Pécs 2008 1 Bevezetés
Oldatok - elegyek. Többkomponensű homogén (egyfázisú) rendszerek. Elegyek: komponensek mennyisége azonos nagyságrendű
 Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Miért érdekes? Magsugárzások. Az atommag felépítése. Az atom felépítése
 Miért érdekes? Magsugárzások Dr Smeller László egyetemi taár Semmelweis Egyetem Biofizikai és Sugárbiológiai Itézet Radioaktív izotóok ill. sugárzások orvosi felhaszálása: - diagosztika (izotódiagosztika)
Miért érdekes? Magsugárzások Dr Smeller László egyetemi taár Semmelweis Egyetem Biofizikai és Sugárbiológiai Itézet Radioaktív izotóok ill. sugárzások orvosi felhaszálása: - diagosztika (izotódiagosztika)
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Folyadékok. Molekulák: Gázok Folyadékok Szilárd anyagok. másodrendű kölcsönhatás növekszik. cseppfolyósíthatók hűtéssel és/vagy nyomással
 Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
f(n) n x g(n), n x π 2 6 n, σ(n) n x
 Számelméleti függvéyek extremális agyságredje Dr. Tóth László 2006 Bevezetés Ha számelméleti függvéyek, l. multilikatív vagy additív függvéyek agyságredjét vizsgáljuk, akkor először általába az adott függvéy
Számelméleti függvéyek extremális agyságredje Dr. Tóth László 2006 Bevezetés Ha számelméleti függvéyek, l. multilikatív vagy additív függvéyek agyságredjét vizsgáljuk, akkor először általába az adott függvéy
Halmazállapot változások. Folyadékok párolgása. Folyadékok párolgása
 Halmazállapot változások 6. hét Egy anyag különböző halmazállapotai közötti átmenet - elsőfajú fázisátalakulások A kémiai összetétel nem változik meg Adott nyomáson meghatározott hőmérsékleten megy végbe
Halmazállapot változások 6. hét Egy anyag különböző halmazállapotai közötti átmenet - elsőfajú fázisátalakulások A kémiai összetétel nem változik meg Adott nyomáson meghatározott hőmérsékleten megy végbe
EGY FÁZISÚ TÖBBKOMPONENS RENDSZEREK: BEVEZETÉS
 EGY FÁZIÚ ÖBBOMPONEN RENDZERE: BEEZEÉ ERMODINMII ÁLOZÓ Eg: egy komoes egy fázs (olt egy komoes több fázs s Általáos eset: több komoes több fázs öztes eset: több komoes egy fázs Ezek az elegyek szta fázs
EGY FÁZIÚ ÖBBOMPONEN RENDZERE: BEEZEÉ ERMODINMII ÁLOZÓ Eg: egy komoes egy fázs (olt egy komoes több fázs s Általáos eset: több komoes több fázs öztes eset: több komoes egy fázs Ezek az elegyek szta fázs
Szabályozó szelepek (PN 6) VL 2 2-utú szelep, karima VL 3 3-járatú szelep, karima
 Szabályozó szelepek (PN 6) V 2 2-utú szelep, karima V 3 3-járatú szelep, karima eírás V 2 V 3 A V 2 és a V 3 szelepek miőségi és költséghatékoy megoldást adak a legtöbb víz és hűtött víz alkalmazás eseté.
Szabályozó szelepek (PN 6) V 2 2-utú szelep, karima V 3 3-járatú szelep, karima eírás V 2 V 3 A V 2 és a V 3 szelepek miőségi és költséghatékoy megoldást adak a legtöbb víz és hűtött víz alkalmazás eseté.
24. tétel A valószínűségszámítás elemei. A valószínűség kiszámításának kombinatorikus modellje.
 24. tétel valószíűségszámítás elemei. valószíűség kiszámításáak kombiatorikus modellje. GYORISÁG ÉS VLÓSZÍŰSÉG meyibe az egyes adatok a sokaságo belüli részaráyát adjuk meg (törtbe vagy százalékba), akkor
24. tétel valószíűségszámítás elemei. valószíűség kiszámításáak kombiatorikus modellje. GYORISÁG ÉS VLÓSZÍŰSÉG meyibe az egyes adatok a sokaságo belüli részaráyát adjuk meg (törtbe vagy százalékba), akkor
X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet):
![X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet): X = 9,477 10 3 mol. ph = 4,07 [H + ] = 8,51138 10 5 mol/dm 3 Gyenge sav ph-jának a számolása (általánosan alkalmazható képlet):](/thumbs/25/6460380.jpg) . Egy átrium-hidroxidot és átrium-acetátot tartalmazó mita 50,00 cm 3 -es részletée megmérjük a ph-t, ami,65-ek adódott. 8,65 cm 3 0, mol/dm 3 kocetrációjú sósavat adva a mitához, a mért ph 5,065. Meyi
. Egy átrium-hidroxidot és átrium-acetátot tartalmazó mita 50,00 cm 3 -es részletée megmérjük a ph-t, ami,65-ek adódott. 8,65 cm 3 0, mol/dm 3 kocetrációjú sósavat adva a mitához, a mért ph 5,065. Meyi
Kalkulus gyakorlat - Megoldásvázlatok
 Kalkulus gyakorlat - Megoldásvázlatok Fizika BSc I/. gyakorlat. Tétel Newto Leibiz. Ha f folytoos az a, b] itervallumo és F primitív függvéye f-ek, akkor b a f F b F a.. Számítsuk ki az alábbi racioális
Kalkulus gyakorlat - Megoldásvázlatok Fizika BSc I/. gyakorlat. Tétel Newto Leibiz. Ha f folytoos az a, b] itervallumo és F primitív függvéye f-ek, akkor b a f F b F a.. Számítsuk ki az alábbi racioális
A statisztika részei. Példa:
 STATISZTIKA Miért tauljuk statisztikát? Mire haszálhatjuk? Szakirodalom értő és kritikus olvasásához Mit állít egyáltalá a cikk? Korrektek-e a megállaítások? Vizsgálatok (kísérletek és felmérések) tervezéséhez,
STATISZTIKA Miért tauljuk statisztikát? Mire haszálhatjuk? Szakirodalom értő és kritikus olvasásához Mit állít egyáltalá a cikk? Korrektek-e a megállaítások? Vizsgálatok (kísérletek és felmérések) tervezéséhez,
VÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZTÉVFOLYAM 2006
 ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
Megjegyzések. További tételek. Valódi határeloszlások. Tulajdonságok. Gyenge (eloszlásbeli) konvergencia
 Valószíűségszámítás és statisztika előadás ifo. BSC/B-C szakosokak 6. előadás október 5. Megjegyzések. A tétel feltételei gyegíthetőek: elég, ha a függetle, azoos eloszlású változók várható értéke véges.
Valószíűségszámítás és statisztika előadás ifo. BSC/B-C szakosokak 6. előadás október 5. Megjegyzések. A tétel feltételei gyegíthetőek: elég, ha a függetle, azoos eloszlású változók várható értéke véges.
Stabilitás Irányítástechnika PE MI_BSc 1
 Stabilitás 2008.03.4. Stabilitás egyszerűsített szemlélet példa zavarás utá a magára hagyott redszer visszatér a yugalmi állapotába kvázistacioárius állapotba kerül végtelebe tart alapjelváltás Stabilitás/2
Stabilitás 2008.03.4. Stabilitás egyszerűsített szemlélet példa zavarás utá a magára hagyott redszer visszatér a yugalmi állapotába kvázistacioárius állapotba kerül végtelebe tart alapjelváltás Stabilitás/2
Innen. 2. Az. s n = 1 + q + q 2 + + q n 1 = 1 qn. és q n 0 akkor és csak akkor, ha q < 1. a a n végtelen sor konvergenciáján nem változtat az, ha
 . Végtele sorok. Bevezetés és defiíciók Bevezetéskét próbáljuk meg az 4... végtele összegek értelmet adi. Mivel végtele sokszor em tuduk összeadi, emiatt csak az első tagot adjuk össze: legye s = 4 8 =,
. Végtele sorok. Bevezetés és defiíciók Bevezetéskét próbáljuk meg az 4... végtele összegek értelmet adi. Mivel végtele sokszor em tuduk összeadi, emiatt csak az első tagot adjuk össze: legye s = 4 8 =,
Miért érdekes? Magsugárzások. Az atommag felépítése. Az atom felépítése
 Miért érdekes? Magsugárzások Dr Smeller László egyetemi doces Semmelweis Egyetem Biofizikai és Sugárbiológiai Itézet Radioaktív izotóok ill. sugárzások orvosi felhaszálása: - diagosztika (izotódiagosztika)
Miért érdekes? Magsugárzások Dr Smeller László egyetemi doces Semmelweis Egyetem Biofizikai és Sugárbiológiai Itézet Radioaktív izotóok ill. sugárzások orvosi felhaszálása: - diagosztika (izotódiagosztika)
forgási hiperboloid (két köpenyű) Határérték: Definíció (1): Az f ( x, y) függvénynek az ( x, y ) pontban a határértéke, ha minden
 Kétváltozós függvéek Defiíció: f: R R vag z f(,) Szeléltetés:,,z koordiátaredszerbe felülettel Pl z + forgási paraboloid z R ( + ) félgöb z + + forgási iperboloid (két köpeű) z + forgási iperboloid (eg
Kétváltozós függvéek Defiíció: f: R R vag z f(,) Szeléltetés:,,z koordiátaredszerbe felülettel Pl z + forgási paraboloid z R ( + ) félgöb z + + forgási iperboloid (két köpeű) z + forgási iperboloid (eg
Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján
 Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján Készítette: Zsélyné Ujvári Mária, Szalma József; 2012 Előadó: Zsély István Gyula, Javított valtozat 2016 Laborelőkészítő előadás,
Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján Készítette: Zsélyné Ujvári Mária, Szalma József; 2012 Előadó: Zsély István Gyula, Javított valtozat 2016 Laborelőkészítő előadás,
Integrálszámítás (Gyakorló feladatok)
 Itegrálszámítás Gyakorló feladatok Programtervez iformatikus szakos hallgatókak az Aalízis. cím tárgyhoz Összeállította Szili László 8. február Tartalomjegyzék I. Feladatok 5. Primitív függvéyek határozatla
Itegrálszámítás Gyakorló feladatok Programtervez iformatikus szakos hallgatókak az Aalízis. cím tárgyhoz Összeállította Szili László 8. február Tartalomjegyzék I. Feladatok 5. Primitív függvéyek határozatla
Folyadékok és szilárd anyagok
 Folyadékok és szilárd anyagok 7-1 Intermolekuláris erők, folyadékok tulajdonságai 7-2 Folyadékok gőztenziója 7-3 Szilárd anyagok néhány tulajdonsága 7-4 Fázisdiagram 7-5 Van der Waals kölcsönhatások 7-6
Folyadékok és szilárd anyagok 7-1 Intermolekuláris erők, folyadékok tulajdonságai 7-2 Folyadékok gőztenziója 7-3 Szilárd anyagok néhány tulajdonsága 7-4 Fázisdiagram 7-5 Van der Waals kölcsönhatások 7-6
2011/2012 tavaszi félév 4. óra
 211/212 tvszi félév 4. ór Termokémi Feltok hőkitás, fjlgos és moláris hőkitás foglmák megismerésére Látes hő Összetett számítások hlmzállotváltozássl (l. jég és gőz összekeverése) Rekióetli, égési etli
211/212 tvszi félév 4. ór Termokémi Feltok hőkitás, fjlgos és moláris hőkitás foglmák megismerésére Látes hő Összetett számítások hlmzállotváltozássl (l. jég és gőz összekeverése) Rekióetli, égési etli
ALGEBRA. egyenlet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 198.
 ALGEBRA MÁSODFOKÚ POLINOMOK. Határozzuk meg az + p + q = 0 egyelet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 98.. Határozzuk meg az összes olya pozitív egész p és q számot, amelyre az
ALGEBRA MÁSODFOKÚ POLINOMOK. Határozzuk meg az + p + q = 0 egyelet megoldásait, ha tudjuk, hogy egész számok, továbbá p + q = 98.. Határozzuk meg az összes olya pozitív egész p és q számot, amelyre az
Halmazállapot-változások vizsgálata ( )
 Halmazállapot-változások vizsgálata Eddigi tanulmányaik során a szilárd, folyékony és légnemő, valamint a plazma állapottal találkoztak. Ezen halmazállapotok mindegyikében más és más összefüggés áll fenn
Halmazállapot-változások vizsgálata Eddigi tanulmányaik során a szilárd, folyékony és légnemő, valamint a plazma állapottal találkoztak. Ezen halmazállapotok mindegyikében más és más összefüggés áll fenn
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
16. Az AVL-fa. (Adelszon-Velszkij és Landisz, 1962) Definíció: t kiegyensúlyozott (AVL-tulajdonságú) t minden x csúcsára: Pl.:
 6. Az AVL-fa Adelszo-Velszkij és Ladisz, 96 Defiíció: t kiegyesúlyozott AVL-tulajdoságú t mide x csúcsára: bal x jobb x. Pl.: A majdem teljes biáris fa AVLtulajdoságú. Az AVL-fára, mit speciális alakú
6. Az AVL-fa Adelszo-Velszkij és Ladisz, 96 Defiíció: t kiegyesúlyozott AVL-tulajdoságú t mide x csúcsára: bal x jobb x. Pl.: A majdem teljes biáris fa AVLtulajdoságú. Az AVL-fára, mit speciális alakú
BIOMATEMATIKA ELŐADÁS
 BIOMATEMATIKA ELŐADÁS 10. A statisztika alapjai Debrecei Egyetem, 2015 Dr. Bérczes Attila, Bertók Csaád A diasor tartalma 1 Bevezetés 2 Statisztikai függvéyek Defiíció, empirikus várható érték Empirikus
BIOMATEMATIKA ELŐADÁS 10. A statisztika alapjai Debrecei Egyetem, 2015 Dr. Bérczes Attila, Bertók Csaád A diasor tartalma 1 Bevezetés 2 Statisztikai függvéyek Defiíció, empirikus várható érték Empirikus
