A citoszkeletális rendszer, a harántcsíkolt izom biofizikája.
|
|
|
- Győző Nemes
- 7 évvel ezelőtt
- Látták:
Átírás
1 A citoszkeletális rendszer, a harántcsíkolt izom biofizikája. SCIENCE PHOTO LIBRARY Kupi Tünde Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fı filamentum-osztály: A. Intermedier B. Mikrotubulus C. Mikrofilamentum 20 µm citokeratin (PANC1) alfa-tubulin (HeLa) aktin (endothel sejtek) Abcam plc, 332 Science Park, Cambridge CB4 0WN, United Kingdom Donald E. Ingber, The Architecture of Life Scientific American, Jan Szerep: 1. mozgás, alakváltozás, 2. sejtosztódás, 3. intracelluláris transzport 1
2 Polimerizáció a polimer képzıdésének idıbeli folyamata, monomerek egymáshoz kapcsolódása polimer-mennyiség steady-state lag elongáció A polimerizáció fázisai: 1. Lag fázis: nukleáció 2. Növekedési fázis 3. Dinamikus egyensúly idı Valódi equilibrium: Polimerizációs egyensúlyok Tread-milling (taposómalom): aktin Dinamikus instabilitás: mikrotubulusok 2
3 Mikrofilamentum rendszer (aktin) Aktin monomer: nukleotid 4 2 Globuláris (G-) aktin : MW: 42,3 kda, 375 aminosav 3 1 Nukleotidot (ATP, ADP) köt Kétértékő kationt köt (Ca 2+, Mg 2+ ) 2 domén, 4 szubdomén Aktin polimer: 37 nm Filamentális (F-) aktin: Legnagyobb mennyiségben elıforduló fehérje az eukarióta sejtben (~ 5%) ~7 nm vastag, hossza in vitro több 10 µm, in vivo 1-2 µm Jobbmenetes dupla helix Szemiflexibilis polimerlánc (perzisztenciahossz: ~10 µm) Szerkezeti polarizáció: miozin fejjel alkotott komplexe szögesdrót alakja alapján: szöges vég: "barbed end (+ vég) polimerizáció gyors hegyes vég: "pointed end (- vég) polimerizáció lassú Motorfehérjéi: miozinok 3
4 Tubulin monomer: Mikrotubuláris rendszer α β MW: ~50 kda, idegszövetben az összfehérje 10-20%-a α- és β-tubulin alkot heterodimért GTP vagy GDP nukleotidot köt kicserélhetı (β), ill. nem kicserélhetı (α) Polimer: mikrotubulus ~25 nm-es átmérı, üreges csı, 13 protofilamentum jobbmenetes rövidmenetû helix, balmenetes hosszúmenetû helix Merev polimerlánc (perzisztenciahossz: néhány mm!) Szerkezeti polarizáció: + vég: polimerizáció gyors, - vég: polimerizáció lassú Motorfehérjéi: dinein, kinezin, dinamin 4
5 Sejtosztódás Wadsworth Center's Featured Image - Archives Intermedier filamentális rendszer Az intermedier filamentum alegysége: coiled-coil dimer N-terminális fej, centrális rúd (α-helix), C-terminális farok hidrofób aminosavak heptád ismétlıdése a centrális rúdban Vimentin dimer szalagdiagramja 5
6 Intermedier filamentumok A sejtben teljesen polimerizált állapotban találhatók (nincs polimerizációs-depolimerizációs dinamizmus) Centrális rudak hidrofób-hidrofób kölcsönhatása: coiled-coil dimer 2 dimer antiparallel elrendezıdése: tetramer (szerkezeti apolaritás) protofilamentum Tetramerek longitudinális sorozata: protofilamentum 8 protofilamentum: filamentum, 8-10 nm-es átmérı filamentum Citoszkeletonhoz asszociált fehérjék Különbözı funkciójú fehérjék nagy csoportja, melyek a citoszkeletális rendszer egyes filamentumaihoz specifikusan kapcsolódnak Csoportosítás: A. Filamentális rendszer szerint 1. Aktin-asszociált (pl. miozin) 2. MT-asszociált (pl. tau) 3. IF-asszociált (pl. plektin) B. Kapcsolódás geometriája szerint 1. Véghez kapcsolódó ( capping, pl. gelsolin) 2. Oldalról kapcsolódó (pl. tropomiozin) C. Funkció szerint 1. Keresztkötı a. Gélformáló (pl. filamin, spektrin) b. Kötegformáló (pl. α-aktinin, fimbrin, villin) 2. Polimerizációt befolyásoló a. Depolimerizáló ( severing, pl. gelsolin) b. Stabilizáló (pl. profilin, tropomiozin) 3. Motorfehérjék 6
7 Motorfehérjék 1. Specifikus citoszkeletális filamentumhoz kapcsolódnak 2. A filamentum mentén elmozdulnak, illetve erôt fejtenek ki 3. ATP-t/ GTP-t bontanak A motorfehérjék típusai 1. Aktin-alapú motorok: miozin fehérjecsalád. Konvencionális (miozin II) és nemkonvencionális miozinok Miozin I-XVIII osztályok 2. Mikrotubulus alapú motorok a. Dinein Ciliáris (flagelláris) és citoplazmás dineinek. A mikrotubuluson a minusz vég irányába mozognak b. Kinezin Neuronokban, axonális vezikulum transzportért felelôsek Kinezin fehérjecsalád: konvencionális kinezinek + izoformák. A mikrotubuluson a plusz vég irányába mozognak c. Dinamin GTP-áz aktivitás, vezikulumok lefőzésében van szerepük 3. Nukleinsav alapú motorok DNS és RNS polimerázok A DNS szál mentén mozognak és erôt fejtenek ki 4. Rotációs motorok Forgómozgást hoznak létre /pl.: F1F0 ATP-szintáz, bakteriális flagellum motor/ 7
8 A motorfehérje munkaciklusa ATP hidrolízis ciklus munkacsapás δ = munkatávolság Kapcsolt τ on kapcsolás szétkapcsolás Szétkapcsolt τ off visszacsapás Munka arány: τ r = on = τ on τ on +τ off τ total In vitro csúszási sebesség: v = δ τ on Kapcsolt idô: τ on = δ v Ciklusidô: τ total = 1 V δ=munka- vagy lépéstávolság; V=ATPáz sebesség; v=motilitási sebesség Munkaciklus arány: r = δv v Processzív motor: r~1 pl. kinezin, DNS-, RNS-polimeráz munkaciklus nagy részében kapcsolt állapotban Nonprocesszív motor: r~0 pl. miozin munkaciklus nagy részében szétkapcsolt állapotban sokaság mûködik együtt Egyetlen motorfehérje által kifejtett erô: néhány pn. 8
9 Az izomszövet három típusa Izom: mozgásra, mozgatásra specializálódott sejt illetve szövet. Típusok: 1. harántcsíkolt izom: vázizomban, akaratlagos mozgásért felelıs, több cm hosszú sejt is lehet, multinukleáris 2. szívizom: szívben, mononukleáris 3. simaizom: zsigerekben, nem akaratlagos mozgásért felelıs, orsó alakú mononukleáris sejt A harántcsíkolt izom felépítése: izom rost-köteg rost miofibrillum miofilamentumok: vastag-, vékony- és "harmadik filamentális rendszer" (titin) A miofilamentumok a szarkomerben, az izommőködés legkisebb önálló egységében találhatók. 9
10 Miofibrillum: A három filamentum modell Z Z szarkomer A-sáv I-sáv M-vonal Z-lemez titin vastag filamentum vékony filamentum Mi szabályozza az izmok mőködését? Váz és szívizom: Troponin komplex (C, T, I), tropomiozin és kálcium. Simaizom: a könnyőlánc foszforilációja. Kagyló izom: kálcium kötıdése a miozinhoz. 10
11 Tropomiozin A tropomiozin két molekula egymásba csavarodásával kialakuló coiled-coil dimer, mely 7 aktin protomerrel van kölcsönhatásban. A tandem módon elhelyezkedı tropomiozin dimerek a teljes aktin filamentumon végighúzódnak. A troponin komplex Minden 7 aktin monomerbıl és egy tropomiozinból álló fehérjekomplexhez egy troponin komplex kapcsolódik: Troponin T - (MW 37 kda) a tropomiozinhoz és a többi troponin fehérjéhez kötıdik, stabilizálja a fehérjerendszert. Troponin I - (MW 22 kda) gátolja az akto-miozin kölcsönhatást. Troponin C- (MW 18 kda) Kálcium hatására a szerkezetében bekövetkezı konformációs változás az izom szabályozásának a kulcslépése. 11
12 Kapcsolat az aktin, miozin és tropomiozin között: az izommőködés alapja Köszönöm a figyelmet! 12
A citoszkeletális rendszer, motorfehérjék.
 A citoszkeletális rendszer, motorfehérjék. SCIENCE PHOTO LIBRARY Huber Tamás 2012. 10. 15. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus
A citoszkeletális rendszer, motorfehérjék. SCIENCE PHOTO LIBRARY Huber Tamás 2012. 10. 15. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus
A citoszkeletális rendszer, motorfehérjék.
 A citoszkeletális rendszer, motorfehérjék. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus C. Mikrofilamentum SCIENCE PHOTO LIBRARY
A citoszkeletális rendszer, motorfehérjék. Citoszkeleton: eukarióta sejtek dinamikus fehérjevázrendszere Három fő filamentum-osztály: A. Intermedier B. Mikrotubulus C. Mikrofilamentum SCIENCE PHOTO LIBRARY
11/15/10! A CITOSZKELETÁLIS RENDSZER! Polimerizáció! Polimerizációs egyensúly! Erő iránya szerint:! 1. valódi egyensúly (aktin)" Polimer mechanika!
 11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A citoszkeleton. A citoszkeleton, a motorfehérjék, az izom és működésének szabályozása. A citoszkeleton. A citoszkeleton.
 , a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2012. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
, a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2012. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
A citoszkeleton. A citoszkeleton, a motorfehérjék, az izom és működésének szabályozása. A citoszkeleton. A citoszkeleton. Az aktin.
 , a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2011. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
, a motorfehérjék, az izom és működésének szabályozása PTE ÁOK Biofizikai Intézet Ujfalusi Zoltán 2011. január-február Eukarióta sejtek dinamikus vázrendszere Három fő filamentum-osztály: 1. Intermedier
Kollár Veronika
 A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
Citoszkeleton. Sejtek rugalmassága. Polimer mechanika: Hooke-rugalmasság. A citoszkeleton filamentumai. Fogászati anyagtan fizikai alapjai 12.
 Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
Dinamikus fehérjerendszerek a sejtben
 BIOLÓGIAI MOZGÁSOK Dinamikus fehérjerendszerek a sejtben Ritmusosan összehúzódó szívizomsejt Osztódó sejt Kellermayer Miklós Axon (neurit) növekedés Mozgó spermatociták BIOLÓGIAI MOZGÁSOK A citoszkeletális
BIOLÓGIAI MOZGÁSOK Dinamikus fehérjerendszerek a sejtben Ritmusosan összehúzódó szívizomsejt Osztódó sejt Kellermayer Miklós Axon (neurit) növekedés Mozgó spermatociták BIOLÓGIAI MOZGÁSOK A citoszkeletális
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
A motorfehérjék definíciója. A biológiai motorok 12/9/2016. Motorfehérjék. Molekuláris gépek. A biológiai mozgás
 A motorfehérjék definíciója Motorfehérjék Nyitrai Miklós, 2016 november 30. Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése;
A motorfehérjék definíciója Motorfehérjék Nyitrai Miklós, 2016 november 30. Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése;
Dinamikus fehérjerendszerek a sejtben. Kellermayer Miklós
 Dinamikus fehérjerendszerek a sejtben Kellermayer Miklós BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt Osztódó sejt Axon (neurit) növekedés Mozgó spermatociták BIOLÓGIAI MOZGÁSOK Tovakúszó keratinocita
Dinamikus fehérjerendszerek a sejtben Kellermayer Miklós BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt Osztódó sejt Axon (neurit) növekedés Mozgó spermatociták BIOLÓGIAI MOZGÁSOK Tovakúszó keratinocita
Biofizika I 2013-2014 2014.12.02.
 ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
A biológiai mozgások. Motorfehérjék. Motorfehérjék közös tulajdonságai 4/22/2015. A biológiai mozgás molekuláris mechanizmusai. Szerkezeti homológia
 A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai. Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen Motorfehérjék
A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai. Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen Motorfehérjék
A biológiai mozgások. A biológiai mozgás molekuláris mechanizmusai. Motorfehérjék. Motorfehérjék közös tulajdonságai
 A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen 1 Motorfehérjék
A biológiai mozgások Molekuláris mozgás A biológiai mozgás molekuláris mechanizmusai Celluláris mozgás Mártonfalvi Zsolt Bakteriális flagellum Szervezet mozgása Keratocita mozgása felületen 1 Motorfehérjék
A citoszkeleton Eukarióta sejtváz
 A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
Motorfehérjék november 30.; Nyitrai
 Motorfehérjék 2011. november 30.; Nyitrai Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése; Gépek a mikro/nano-világban
Motorfehérjék 2011. november 30.; Nyitrai Molekuláris gépek A molekuláris mozgások alapját gyakran motor fehérjék biztosítják. Megértésük a biológia egyik súlyponti kérdése; Gépek a mikro/nano-világban
Történeti áttekintés. Eukarióta. Prokarióta. A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai.
 A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai. Előadásvázlat TK. 345-353. oldal citoszkeleton története polimer mechanika vizsgálómódszerek polimerizáció aktin
A citoszkeletális rendszer. Motorfehérjék. A biológiai mozgás molekuláris mechanizmusai. Előadásvázlat TK. 345-353. oldal citoszkeleton története polimer mechanika vizsgálómódszerek polimerizáció aktin
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
A citoszkeletális rendszer
 A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
Biofizika I
 ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék
 Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2012. február 21. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2012. február 21. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
2. AKTIN-KÖTŐ FEHÉRJÉK
 A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
A harántcsíkolt izom struktúrája általános felépítés
 harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
harántcsíkolt izom struktúrája általános felépítés LC-2 Izom LC1/3 Izom fasciculus LMM S-2 S-1 HMM rod Miozin molekula S-1 LMM HMM S-2 S-1 Izomrost H Band Z Disc csík I csík M Z-Szarkomér-Z Miofibrillum
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék
 Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2011. február 22. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Tubulin, mikrotubuláris rendszer és mikrotubulus asszociált fehérjék Talián Csaba Gábor PTE ÁOK, Biofizika Intézet 2011. február 22. Transzmissziós elektronmikroszkópos felvétel egy Heliozoa axopódiumának
Citoszkeleton Sejtmozgás
 Citoszkeleton Sejtmozgás Citoszkeleton funkciói Sejtalak meghatározása Organellumok kihorgonyzása Organellumok mozgatása Húzószilárdság Kromoszóma mozgatás Sejtpolaritás Motilitás Citoszkeleton Mikrofilamentumok
Citoszkeleton Sejtmozgás Citoszkeleton funkciói Sejtalak meghatározása Organellumok kihorgonyzása Organellumok mozgatása Húzószilárdság Kromoszóma mozgatás Sejtpolaritás Motilitás Citoszkeleton Mikrofilamentumok
A CITOSZKELETÁLIS RENDSZER Bugyi Beáta PTE ÁOK, Biofizikai Intézet. 9. A sejtmozgás mechanizmusai
 A CITOSZKELETÁLIS RENDSZER 2011. 05. 03. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 9. A sejtmozgás mechanizmusai Sejtmozgás, motilitás 1. Sejten belüli, intracelluláris mozgás izom összehúzódás organellumok
A CITOSZKELETÁLIS RENDSZER 2011. 05. 03. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 9. A sejtmozgás mechanizmusai Sejtmozgás, motilitás 1. Sejten belüli, intracelluláris mozgás izom összehúzódás organellumok
Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai
 Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Sejtciklus. Sejtciklus. Centriólum ciklus (centroszóma ciklus) A sejtosztódás mechanizmusa. Mikrotubulusok és motor fehérjék szerepe a mitózisban
 A sejtosztódás mechanizmusa Mikrotubulusok és motor fehérjék szerepe a mitózisban 2010.03.23. Az M fázis alatti események: mag osztódása (mitózis) mitotikus orsó: MT + MAP (pl. motorfehérjék) citoplazma
A sejtosztódás mechanizmusa Mikrotubulusok és motor fehérjék szerepe a mitózisban 2010.03.23. Az M fázis alatti események: mag osztódása (mitózis) mitotikus orsó: MT + MAP (pl. motorfehérjék) citoplazma
Jellemzői: általában akaratunktól függően működik, gyors, nagy erőkifejtésre képes, fáradékony.
 Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
Az élő sejt fizikai Biológiája: motorfehérjék, egyensúlytól távoli folyamatok
 Tematika Az élő sejt fizikai Biológiája: motorfehérjék, egyensúlytól távoli folyamatok Kellermayer Miklós Motorfehérjék működése. A munkaciklus Egyensúlytól távoli folyamatok. Erővezérelt fehérjegombolyodás.
Tematika Az élő sejt fizikai Biológiája: motorfehérjék, egyensúlytól távoli folyamatok Kellermayer Miklós Motorfehérjék működése. A munkaciklus Egyensúlytól távoli folyamatok. Erővezérelt fehérjegombolyodás.
Sejtváz Sejtek mozgása
 Sejtváz Sejtek mozgása Sejtváz: Az eukarióta sejtekben vékony fonálszerű struktúra 3 fő alrendszer alkotja: Mikrofilamentumok: 7-9 nm átmérőjű aktinfonalakból áll; Intermedier filamentumok: 10 nm átmérőjűek;
Sejtváz Sejtek mozgása Sejtváz: Az eukarióta sejtekben vékony fonálszerű struktúra 3 fő alrendszer alkotja: Mikrofilamentumok: 7-9 nm átmérőjű aktinfonalakból áll; Intermedier filamentumok: 10 nm átmérőjűek;
Izomműködés. Az izommozgás. az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással
 Izomműködés Az izommozgás az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással történő mozgás van Galenus id. II.szd. - az idegekből animal spirit folyik
Izomműködés Az izommozgás az állati élet legszembetűnőbb külső jele a mozgás amőboid, ostoros ill. csillós és izomösszehúzódással történő mozgás van Galenus id. II.szd. - az idegekből animal spirit folyik
A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus. Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet
 2018 A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet A citoszkeleton alkotói Mikrofilamentumok Intermedier filamentumok
2018 A membránok és a citoszkeleton kapcsolata. A sejtosztódás és a sejtciklus Előadó:Gönczi Mónika Debreceni Egyetem, ÁOK, Élettani Intézet A citoszkeleton alkotói Mikrofilamentumok Intermedier filamentumok
Komplex egyszerű Aktin alapú mikrofilamentum rsz. Hogyan vizsgálhatunk folyamatokat? Komplex egyszerű S E J T
 Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
A sejtváz. Mikrotubulusok (25 nm átmérő) Mikrofilamentumok (7 nm átmérő) Intermedier filamentumok (8-12 nm átmérő)
 A sejtváz A citoszkeleton, vagy sejtváz kötegek hálózatából felépülő struktúra, mely a sejt szilárdításán, alakjának biztosításán túl, a mozgásban, a szállításban is szerepet játszik. Három molekuláris
A sejtváz A citoszkeleton, vagy sejtváz kötegek hálózatából felépülő struktúra, mely a sejt szilárdításán, alakjának biztosításán túl, a mozgásban, a szállításban is szerepet játszik. Három molekuláris
Polimerlánc egyensúlyi alakja. Féregszerű polimermodell (Wormlike chain) WLC (wormlike chain): Entropikus rugalmasság vizualizálása
 Polimerlánc egyensúlyi alakja Az a makroállapot, amely a legtöbb mikroállapottal valósítható meg (legvalószínűbb állapot) DNS molekulák fluoreszcencia mikroszkóp alatt Féregszerű polimermodell (Wormlike
Polimerlánc egyensúlyi alakja Az a makroállapot, amely a legtöbb mikroállapottal valósítható meg (legvalószínűbb állapot) DNS molekulák fluoreszcencia mikroszkóp alatt Féregszerű polimermodell (Wormlike
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
Izomműködés. Harántcsíkolt izom. Simaizom és simaizom-alapú szervek biofizikája.
 Izomműködés. Harántcsíkolt izom. Simaizom és simaizom-alapú szervek biofizikája. Hirdetés D.R. Wilkie professzor előadására a londoni Villamosmérnöki Intézetben. A téma: izom. Kapható: LINEÁRIS MOTOR.
Izomműködés. Harántcsíkolt izom. Simaizom és simaizom-alapú szervek biofizikája. Hirdetés D.R. Wilkie professzor előadására a londoni Villamosmérnöki Intézetben. A téma: izom. Kapható: LINEÁRIS MOTOR.
2011. október 11. Szabad János
 2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
A diffúzió csak rövid méretsálán gyors. Az élő sejt fizikai Biológiája: Diffúzió, polimerizáció, reptáció
 A diffúzió csak rövid méretsálán gyors Az élő sejt fizikai Biológiája: Diffúzió, polimerizáció, reptáció Kellermayer Miklós Négyzetes összefüggés: meredekség=2 A DIFFÚZIÓ ÉS BOLYONGÓ MOZGÁS KAPCSOLATA
A diffúzió csak rövid méretsálán gyors Az élő sejt fizikai Biológiája: Diffúzió, polimerizáció, reptáció Kellermayer Miklós Négyzetes összefüggés: meredekség=2 A DIFFÚZIÓ ÉS BOLYONGÓ MOZGÁS KAPCSOLATA
1. AKTIN CITOSZKELETON
 A CITOSZKELETÁLIS REDSZER 20. 02. 08.. AKTI CITOSZKELETO Citozeletáli atin HEp-2 ejteben - rodamin-falloidin jelölé forrá: yitrai Miló, Grama Lázló, PTE ÁOK, Biofiziai Intézet CITOSZKELETO CITO : ejt /
A CITOSZKELETÁLIS REDSZER 20. 02. 08.. AKTI CITOSZKELETO Citozeletáli atin HEp-2 ejteben - rodamin-falloidin jelölé forrá: yitrai Miló, Grama Lázló, PTE ÁOK, Biofiziai Intézet CITOSZKELETO CITO : ejt /
Sejt. Aktin működés, dinamika plus / barbed end pozitív / szakállas vég 1. nukleáció 2. elongáció (hosszabbodás) 3. dinamikus egyensúly
 Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Sejtváz, aktin mikrofilamentumok, motor fehérjék
 Sejtváz, aktin mikrofilamentumok, motor fehérjék Sejtváz Az eukarióta sejtek citoplazmájában található, fehérjefonalakból álló hálózat. (~citoszkeleton) Feladatai: -strukturális vázat alkotva, meghatározza
Sejtváz, aktin mikrofilamentumok, motor fehérjék Sejtváz Az eukarióta sejtek citoplazmájában található, fehérjefonalakból álló hálózat. (~citoszkeleton) Feladatai: -strukturális vázat alkotva, meghatározza
Az izomszövet biokémiája. Izombetegségek. Szerkesztette: Fekete Veronika
 Az izomszövet biokémiája. Izombetegségek Szerkesztette: Fekete Veronika Az izomtípusok jellemzői Simaizom lassú nincs rajzolat Szívizom gyors harántcsíkolt Harántcsíkolt izom belső szervek akaratlan nem
Az izomszövet biokémiája. Izombetegségek Szerkesztette: Fekete Veronika Az izomtípusok jellemzői Simaizom lassú nincs rajzolat Szívizom gyors harántcsíkolt Harántcsíkolt izom belső szervek akaratlan nem
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Biofizika I 2013-2014 2014.12.03.
 Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
SEJTBIOLÓGIA biomérnök hallgatók számára
 SEJTBIOLÓGIA biomérnök hallgatók számára Kilencedik rész: A citoszkeleton Novák Béla docens Proofreading: Sveiczer Ákos ösztöndíjas kutató 1994. december 16. Copyright 1994 BME, Mezõgazdasági Kémiai Technológia
SEJTBIOLÓGIA biomérnök hallgatók számára Kilencedik rész: A citoszkeleton Novák Béla docens Proofreading: Sveiczer Ákos ösztöndíjas kutató 1994. december 16. Copyright 1994 BME, Mezõgazdasági Kémiai Technológia
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál. Nyugalmi potenciál. 3 tényező határozza meg:
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Nanomedicina Szimpózium, 2008. Nanomechanika: Egyedi Biomolekulák Manipulálása. Kellermayer Miklós
 Nanomedicina Szimpózium, 28 Nanomechanika: Egyedi Biomolekulák Manipulálása Kellermayer Miklós Semmelweis Egyetem Általános Orvostudományi Kar Biofizikai és Sugárbiológiai Intézet ÉLŐ SEJTBEN: BONYOLULT
Nanomedicina Szimpózium, 28 Nanomechanika: Egyedi Biomolekulák Manipulálása Kellermayer Miklós Semmelweis Egyetem Általános Orvostudományi Kar Biofizikai és Sugárbiológiai Intézet ÉLŐ SEJTBEN: BONYOLULT
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata
 Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata PhD értekezés Készítette: Orbán József Témavezetők: DR. LŐRINCZY DÉNES DR. HILD GÁBOR Doktori Iskola: Doktori Iskola vezető:
Izomszövet eredetű aktin izoformák termodinamikai és spektroszkópiai vizsgálata PhD értekezés Készítette: Orbán József Témavezetők: DR. LŐRINCZY DÉNES DR. HILD GÁBOR Doktori Iskola: Doktori Iskola vezető:
A harántcsíkolt izomrostok típusai:
 A harántcsíkolt izomrostok típusai: 1. Vörös (aerob) rostok: vékony rostok nagy mennyiségű mioglobinnal citokrómmal mitokondriummal 2. Fehér (anaerob) rostok: vastag rostok kevés mioglobinnal citokrómmal
A harántcsíkolt izomrostok típusai: 1. Vörös (aerob) rostok: vékony rostok nagy mennyiségű mioglobinnal citokrómmal mitokondriummal 2. Fehér (anaerob) rostok: vastag rostok kevés mioglobinnal citokrómmal
1. Az élő szervezetek felépítése és az életfolyamatok 17
 Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
Egy idegsejt működése. a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására
 Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE
 MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE MTA doktori értekezés Kovács Mihály Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Intézet Biokémiai Tanszék 2010 Tartalomjegyzék 1. Összefoglalás 4
MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE MTA doktori értekezés Kovács Mihály Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Intézet Biokémiai Tanszék 2010 Tartalomjegyzék 1. Összefoglalás 4
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biokémiai és Molekuláris Biológiai Intézet. Sejtbiológiai alapok. Sarang Zsolt
 Biokémiai és Molekuláris Biológiai Intézet Sejtbiológiai alapok Sarang Zsolt Víz (felnőtt emberi test 57-60%-a víz) Élő szervezetek inorganikus felépítő elemei Anionok (foszfát, klorid, karbonát ion, stb.)
Biokémiai és Molekuláris Biológiai Intézet Sejtbiológiai alapok Sarang Zsolt Víz (felnőtt emberi test 57-60%-a víz) Élő szervezetek inorganikus felépítő elemei Anionok (foszfát, klorid, karbonát ion, stb.)
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
A dezmin nanomechanikai vizsgálata
 A dezmin nanomechanikai vizsgálata Doktori értekezés Dr. Kiss Balázs Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető: Dr. Kellermayer Miklós egyetemi tanár, az orvostudományok doktora
A dezmin nanomechanikai vizsgálata Doktori értekezés Dr. Kiss Balázs Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Témavezető: Dr. Kellermayer Miklós egyetemi tanár, az orvostudományok doktora
Az élő sejt fizikai Biológiája: TERMODINAMIKAI ÁRAMOK. Tematika ANYAGÁRAM (DIFFÚZIÓ) Diffúzió, polimerizáció, reptáció. Kellermayer Miklós
 Tematika Az élő sejt fizikai Biológiája: Diffúzió, polimerizáció, reptáció Diffúzió, diffúzió-vezérelt folyamatok Biopolimérek dinamikája. Polimerizáció, depolimerizáció Polimérek diffúziója. Reptáció.
Tematika Az élő sejt fizikai Biológiája: Diffúzió, polimerizáció, reptáció Diffúzió, diffúzió-vezérelt folyamatok Biopolimérek dinamikája. Polimerizáció, depolimerizáció Polimérek diffúziója. Reptáció.
2007/11/05 Molekuláris biológia előadások - Putnoky 1-1
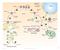 1-1 Fehérje transzportmechanizmusok az eukariota sejtben: 1) transzmembrán transzport kitekert formában, egyedi fehérjék transzportja célzottan - citoszol ER, citoszol MT 2) póruson keresztüli transzport
1-1 Fehérje transzportmechanizmusok az eukariota sejtben: 1) transzmembrán transzport kitekert formában, egyedi fehérjék transzportja célzottan - citoszol ER, citoszol MT 2) póruson keresztüli transzport
Biomolekulák mint polimerek. Milyen alakúak a biopolimerek? 4/22/2015. Biopolimerek osztályozása hajlékonyságuk alapján
 4/22/2015 Orvosi Biofizika II. Biomechanika Biomolekuláris és szöveti rugalmasság Mártonfalvi Zsolt Biomolekulák mint polimerek A biomolekulák polimerek. Közös bennük: Lineáris elsődleges szerkezet (fehérje,
4/22/2015 Orvosi Biofizika II. Biomechanika Biomolekuláris és szöveti rugalmasság Mártonfalvi Zsolt Biomolekulák mint polimerek A biomolekulák polimerek. Közös bennük: Lineáris elsődleges szerkezet (fehérje,
Egyedi molekula vizsgálatok
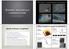 Élő sejtben: molekulagépezetek sokasága Egyedi molekula vizsgálatok Kellermayer Miklós Tovakúszó keratinocita Mikrotubulus dinamikus instabilitás Vezikulum transzport kinezinnel Fehérjeszintézis riboszómán
Élő sejtben: molekulagépezetek sokasága Egyedi molekula vizsgálatok Kellermayer Miklós Tovakúszó keratinocita Mikrotubulus dinamikus instabilitás Vezikulum transzport kinezinnel Fehérjeszintézis riboszómán
Az izomkontrakció szabályozása molekuláris szinten
 Az izomkontrakció szabályozása molekuláris szinten Szakdolgozat Biológia alapszak, Biológus szakirány Készítette: RÁTI SZILVIA MARIANNA Témavezető: NYITRAY LÁSZLÓ, PhD, habil., DSc - Tanszékvezető Biokémia
Az izomkontrakció szabályozása molekuláris szinten Szakdolgozat Biológia alapszak, Biológus szakirány Készítette: RÁTI SZILVIA MARIANNA Témavezető: NYITRAY LÁSZLÓ, PhD, habil., DSc - Tanszékvezető Biokémia
Az izommőködéssel járó élettani jelenségek
 Az izommőködéssel járó élettani jelenségek Az izomszövet az egyetlen olyan szövet, amely hosszúságát változtatni tudja. Egy nem elhízott (non-obese) hölgyben az izomtömeg a testsúly 25-35 %-a, férfiben
Az izommőködéssel járó élettani jelenségek Az izomszövet az egyetlen olyan szövet, amely hosszúságát változtatni tudja. Egy nem elhízott (non-obese) hölgyben az izomtömeg a testsúly 25-35 %-a, férfiben
A motorfehérjék hatékonyságának molekuláris háttere
 A motorfehérjék hatékonyságának molekuláris háttere Szakdolgozat Biológia alapszak, biológus szakirány Készítette: IMRICH VANDA Témavezető: MÁLNÁSI-CSIZMADIA ANDRÁS Egyetemi docens Biokémia Tanszék EÖTVÖS
A motorfehérjék hatékonyságának molekuláris háttere Szakdolgozat Biológia alapszak, biológus szakirány Készítette: IMRICH VANDA Témavezető: MÁLNÁSI-CSIZMADIA ANDRÁS Egyetemi docens Biokémia Tanszék EÖTVÖS
Tudjunk Egymásról Bugyi Beáta 22/11/2012
 Listeria monocytogenes Loisel, Boujemaa et al. Nature 1999 Összetett aktin hálózatok Spire/formin szinergia Reymann et al. Nature Materials 1 ADF/aktin Bosch, Bugyi B et al. Molecular Cell 7 Reymann et
Listeria monocytogenes Loisel, Boujemaa et al. Nature 1999 Összetett aktin hálózatok Spire/formin szinergia Reymann et al. Nature Materials 1 ADF/aktin Bosch, Bugyi B et al. Molecular Cell 7 Reymann et
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav,
 MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
Emberi szövetek. A hámszövet
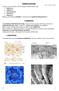 Emberi szövetek Az állati szervezetekben öt fı szövettípust különböztetünk meg: hámszövet, kötıszövet, támasztószövet, izomszövet, idegszövet. Minden szövetféleség sejtekbıl és a közöttük lévı sejtközötti
Emberi szövetek Az állati szervezetekben öt fı szövettípust különböztetünk meg: hámszövet, kötıszövet, támasztószövet, izomszövet, idegszövet. Minden szövetféleség sejtekbıl és a közöttük lévı sejtközötti
Ph.D. disszertáció tézisei
 Ph.D. disszertáció tézisei EGY ÚJ DROSOPHILA FORMIN SZÖVETSPECIFIKUS FUNKCIÓINAK GENETIKAI, SEJTBIOLÓGIAI, ÉS BIOKÉMIAI VIZSGÁLATA Matusek Tamás Témavezető: Dr. Mihály József Magyar Tudományos Akadémia
Ph.D. disszertáció tézisei EGY ÚJ DROSOPHILA FORMIN SZÖVETSPECIFIKUS FUNKCIÓINAK GENETIKAI, SEJTBIOLÓGIAI, ÉS BIOKÉMIAI VIZSGÁLATA Matusek Tamás Témavezető: Dr. Mihály József Magyar Tudományos Akadémia
Az Aktin Filamentumok Hosszát Szabályozó Fehérjék Szerkezeti Dinamikája és Élettani Szerepük
 Az Aktin Filamentumok Hosszát Szabályozó Fehérjék Szerkezeti Dinamikája és Élettani Szerepük Szatmári Dávid Zoltán Témavezetők: Prof. Dr. Nyitrai Miklós, Prof. Dr. Robert C. Robinson Interdiszciplináris
Az Aktin Filamentumok Hosszát Szabályozó Fehérjék Szerkezeti Dinamikája és Élettani Szerepük Szatmári Dávid Zoltán Témavezetők: Prof. Dr. Nyitrai Miklós, Prof. Dr. Robert C. Robinson Interdiszciplináris
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Nanotechnológia. Vonderviszt Ferenc. Veszprémi Egyetem Nanotechnológia Tanszék
 Nanotechnológia Vonderviszt Ferenc Veszprémi Egyetem Nanotechnológia Tanszék Ősi technológiák Mikroelektronika Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének
Nanotechnológia Vonderviszt Ferenc Veszprémi Egyetem Nanotechnológia Tanszék Ősi technológiák Mikroelektronika Technológia: képesség az anyag szerkezetének, az anyagot felépítő részecskék elrendeződésének
Egy idegsejt működése
 2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
Darvas Zsuzsa László Valéria. Sejtbiológia. Negyedik, átdolgozott kiadás
 Darvas Zsuzsa László Valéria Sejtbiológia Negyedik, átdolgozott kiadás Írták: DR. DARVAS ZSUZSA egyetemi docens Semmelweis Egyetem Genetikai, Sejtés Immunbiológiai Intézet DR. LÁSZLÓ VALÉRIA egyetemi docens
Darvas Zsuzsa László Valéria Sejtbiológia Negyedik, átdolgozott kiadás Írták: DR. DARVAS ZSUZSA egyetemi docens Semmelweis Egyetem Genetikai, Sejtés Immunbiológiai Intézet DR. LÁSZLÓ VALÉRIA egyetemi docens
A miokardium intracelluláris kalcium homeosztázisa: iszkémiás és kardiomiopátiás változások
 Doktori értekezés A miokardium intracelluláris kalcium homeosztázisa: iszkémiás és kardiomiopátiás változások Dr. Szenczi Orsolya Témavezető: Dr. Ligeti László Klinikai Kísérleti Kutató- és Humán Élettani
Doktori értekezés A miokardium intracelluláris kalcium homeosztázisa: iszkémiás és kardiomiopátiás változások Dr. Szenczi Orsolya Témavezető: Dr. Ligeti László Klinikai Kísérleti Kutató- és Humán Élettani
Orvosi Biofizika II. Szigorlati tételsor Korai atommodellek. Rutherford-féle kísérlet. Franck-Hertz kísérlet. Bohr-féle atommodell.
 Orvosi Biofizika II. Szigorlati tételsor 2013. 1. Korai atommodellek. Rutherford-féle kísérlet. Franck-Hertz kísérlet. Bohr-féle atommodell. 2. Kvantummechanikai atommodell. Kvantumszámok. A Heisenberg-féle
Orvosi Biofizika II. Szigorlati tételsor 2013. 1. Korai atommodellek. Rutherford-féle kísérlet. Franck-Hertz kísérlet. Bohr-féle atommodell. 2. Kvantummechanikai atommodell. Kvantumszámok. A Heisenberg-féle
A nukleotidok és az aktinkötő fehérjék szerepe az aktin funkcionális konformációváltozásaiban
 A nukleotidok és az aktinkötő fehérjék szerepe az aktin funkcionális konformációváltozásaiban Türmer Katalin Erzsébet Témavezetők: Prof. Dr. Nyitrai Miklós, Prof. Dr. Belágyi József Pécsi Tudományegyetem,
A nukleotidok és az aktinkötő fehérjék szerepe az aktin funkcionális konformációváltozásaiban Türmer Katalin Erzsébet Témavezetők: Prof. Dr. Nyitrai Miklós, Prof. Dr. Belágyi József Pécsi Tudományegyetem,
Biokémiai kutatások ma
 Nyitray László Biokémiai Tanszék Hb Biokémiai kutatások ma Makromolekulák szerkezet-funkció kutatása Molekuláris biológia minden szinten Redukcionista molekuláris biológia vs. holisztikus rendszerbiológia
Nyitray László Biokémiai Tanszék Hb Biokémiai kutatások ma Makromolekulák szerkezet-funkció kutatása Molekuláris biológia minden szinten Redukcionista molekuláris biológia vs. holisztikus rendszerbiológia
1. Sok izomrost (muscle fiber), melyet kívülről egy hártya, a szarkolemma 3
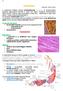 15 Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma
15 Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A kemotaxis biológiai és klinikai
 A kemotaxis biológiai és klinikai jelentősége - Válogatott fejezetek A kemotaxis biológiai és klinikai jelentősége - Válogatott fejezetek - Írta: Kőhidai László Szakmailag ellenőrizte: Csaba György Láng
A kemotaxis biológiai és klinikai jelentősége - Válogatott fejezetek A kemotaxis biológiai és klinikai jelentősége - Válogatott fejezetek - Írta: Kőhidai László Szakmailag ellenőrizte: Csaba György Láng
Keringési Rendszer. Vérkeringés. A szív munkája. Számok a szívről. A szívizom. Kis- és nagyvérkör. Nyomás terület sebesség
 Keringési Rendszer Vérkeringés. A szív munkája 2010.11.03. Szív + erek (artériák, kapillárisok, vénák) alkotta zárt rendszer. Funkció: Oxigén és tápanyag szállítása a szöveteknek. Metabolikus termékek
Keringési Rendszer Vérkeringés. A szív munkája 2010.11.03. Szív + erek (artériák, kapillárisok, vénák) alkotta zárt rendszer. Funkció: Oxigén és tápanyag szállítása a szöveteknek. Metabolikus termékek
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A DAAM formin alcsalád szerepe az izomfejlődésben. Ph.D. értekezés
 A DAAM formin alcsalád szerepe az izomfejlődésben Ph.D. értekezés Készítette: Molnár Imre Témavezető: Dr. Mihály József Biológia Doktori Iskola MTA Szegedi Biológiai Kutatóközpont Genetikai Intézet SZTE
A DAAM formin alcsalád szerepe az izomfejlődésben Ph.D. értekezés Készítette: Molnár Imre Témavezető: Dr. Mihály József Biológia Doktori Iskola MTA Szegedi Biológiai Kutatóközpont Genetikai Intézet SZTE
Mozgás, mozgásszabályozás
 Mozgás, mozgásszabályozás Az idegrendszer szerveződése receptor érző idegsejt inger átkapcsoló sejt végrehajtó sejt központi idegrendszer reflex ív, feltétlen reflex Az ember csontváza és izomrendszere
Mozgás, mozgásszabályozás Az idegrendszer szerveződése receptor érző idegsejt inger átkapcsoló sejt végrehajtó sejt központi idegrendszer reflex ív, feltétlen reflex Az ember csontváza és izomrendszere
a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció. Szinaptikus jelátvitel.
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
