1.1. A Humán Genom Projekt A Humán Genom Projekt célja A humán genom elsõ munkapéldányából levonható következtetések
|
|
|
- Erika Barna
- 8 évvel ezelőtt
- Látták:
Átírás
1 VIII. 1. A GENETIKAI POLIMORFIZMUSOK PSZICHOLÓGIAI ÉS PSZICHIÁTRIAI VONATKOZÁSAI Sasvári-Székely Mária 1, Székely Anna 2, Nemoda Zsófia 1 és Rónai Zsolt 1 1 Semmelweis Egyetem, Orvosi Vegytani, Molekuláris Biológiai és Pathobiokémiai Intézete 2 ELTE Pszichológiai Intézet, Budapest TARTALOMJEGYZÉK 1.1. A Humán Genom Projekt A Humán Genom Projekt célja A humán genom elsõ munkapéldányából levonható következtetések 1.2. A humán genom polimorf jellege Mennyire különbözik két (nem rokon) ember genomja? A polimorfizmusok fõ formái: SNP és VNTR 1.3. A polimorfizmusok felhasználása az öröklött tulajdonságokért felelõs gének meghatározásában Monogénes öröklõdésû betegségek Komplex öröklésmenetû betegségek 1.4. A genetikai polimorfizmusok pszichológiai vonatkozásai A dopamin D4-es receptor polimorfizmusa: a hosszú és a rövid allél A DRD4 hosszú allél asszociációs vizsgálatai A DRD4 gén szabályozó régióinak polimorfizmusa 1.5. A genetikai polimorfizmusok pszichiátriai vonatkozásai Alzheimer-kór Szkizofrénia Figyelemhiányos hiperaktivitási szindróma (ADHD)
2 1.1. A Humán Genom Projekt A Humán Genom Projekt 2001 elején bejelentett eredménye, a humán genetikai információ megfejtése mérföldkõ az emberi életmûködések molekuláris alapjainak megismerésében. E korszakhatárnak nevet is adtak: pre-genomikus éra alatt értik az eddig eltelt idõszakot, melyben a kutatások a humán genom információtartalmának ismerete nélkül zajlottak, míg a poszt-genomikus éra a teljes genetikai információtartalom ismeretében végzendõ vizsgálatokra vonatkozik. A poszt-genomikus éra vizsgálataiban felhasználhatók lesznek azok az adatbázisok, melyek tartalmazzák az összes emberi gén, és fehérje információját. Ez az orvos-biológiai periódusos rendszer a számítások szerint alapvetõ változásokat idéz majd elõ a kutatási módszerekben: elõtérbe kerülnek a sokfaktoros modelleket könnyen kezelõ eljárások. Ugyanakkor nemcsak a humán genom megismerése a cél, számos élõlény genetikai információjának megfejtése is folyamatban van. Elindult például az emberszabású majmok genom analízise, mely elõzetes becslések szerint kb. 99%-ban egyezik a humán genommal. A humán és pl. a csimpánz összehasonlító vizsgálatától sokat várnak az emberi kognitív funkciók genetikai alapjainak megértésében. Molekuláris biológiai alapfogalmak: Kromoszóma DNS A kromoszómákat, az öröklõdés sejttani alapjait a század elsõ negyedében fedezték fel, ezt követte a genetikai információt hordozó molekula, a DNS felfedezése. Minden emberi sejt 22 különbözõ, homológ párokban megtalálható (2 x 22) testi kromoszómát, és két, a nemnek megfelelõ ivari kromoszómát (fiú: XY, lány: XX) tartalmaz, ezen kívül a mitokondriumban is található DNS (1. ábra). A kromoszómák DNS-bõl, és a DNS-t burkoló fehérjékbõl állnak. A sejt osztódása során a kromoszómák, illetve a bennük lévõ DNS megkettõzõdik, majd eloszlik a két új sejt között. Így minden emberi sejt genetikai információtartalma (genomja) azonos, és az élet során nem változik.
3 Molekuláris biológiai alapfogalmak: Nukleotid (bázis, bázispár) - genom A DNS kettõs spirál információ rögzítési módja egy négybetûs kódrendszeren alapul. A négy betû kémiai szempontból a négyféle nukleotid bázisnak felel meg (A:adenin, G:guanin, C:citozin és T:timin), a kettõs szálban a bázispárok kialakulása szigorúan meghatározott (A-T vagy C-G): az egyik szál hordozza az információt ( értelmes szál), a másik ennek csupán tükörképe ( értelmetlen szál). A bázisokat a cukor-foszfát váz tartja (bázis+cukor+foszfát = nukleotid, 1. A. ábra). A bázis/bázispár/nukleotid kifejezések informatikai jelentése ugyanaz: a négyféle DNS betût jelenti. A Nukleotid egységek 1. ábra. A: A DNS és a bázispárok. B: Információátadás: DNS fehérje Foszfát-cukor váz T C Bázis párok G A A G T C A DNS két szálát összetartó erõk B DNS RNS C G G C T A G C G C A T T A A T C G A T C G T A T A T A T A G C C G C G C G U G G A U A C A C U U U U G C C fehérje Arg Gly Tyr Thr Phe Ala Ha a DNS-ben tárolt információ kifejezõdik, a DNS értelmes szálával azonos információjú RNS képzõdik (1. B. ábra, azonban T helyett az RNS-ben U(uracil) van). Ezt követõen az RNS irányítja a fehérje szintézisét oly módon, hogy három DNS/RNS-betû kódol egy fehérje-betût (aminosavat), összesen 20 féle aminosav van (pl. Arg, Gly, Tyr, stb.). A fehérjék valamennyi tulajdonságát az aminosavak sorrendje szabja meg hasonlóképp egy mondathoz, melynek értelmét a betûk sorrendje adja.
4 A humán genom (genetikai információnk összessége, a teljes humán DNS) 3 milliárd (3x10 9 ) db DNS-betûbõl (bázispárból/nukleotidból) áll, melynek nyomtatott formája az A, G,C, T betûk variációinak hosszú-hosszú sorozata lenne (a kettõs szálból csak az egyiket szokás felírni), ezt nevezzük DNS szekvenciának. Az információ mennyiség szemléltetésére azt a példát szokták használni, hogy ha a teljes genomiális szekvenciát olyan könyvben nyomtatnánk ki, melynek egy oldalán ezer betû van, és egy könyvben 1000 oldal volna, akkor 3000 ilyen könyvre lenne szükség. Molekuláris biológiai alapfogalmak: gén exon/intron összevágás (splicing) fehérje A DNS-ben tárolt genetikai információ egysége a gén. A genetikai információ minden sejtünkben azonos, az egyes sejtek mûködése mégsem egyforma. Bonyolult szabályozási folyamatok eredményeképpen például más gének fejezõdnek ki (expresszálódnak) az idegsejtben, megint mások a bõrben. A gén-expresszió szabályozásában fontos szerepet játszik a gén környezete, azaz a gént megelõzõ (5 UTR: 5 untranslated region) és a gént követõ (3 UTR) szakasz (2. ábra). DNS 5 UTR (promoter) (génexpresszió szabályozása) GÉN kódoló régiók (fehérje információ) intron1 intron2 exon 1 exon 2 exon 3 3 UTR (génexpresszió szabályozás) GÉNEXPRESSZIÓ Elsõdleges RNS másolat exon 1 exon 2 exon 3 ÖSSZEVÁGÁS (SPLICING) mrns (1) Exon 1 Exon 2 Exon 3 mrns (2) Exon 1 Exon 3 fehérje 1 fehérje 2 2. ábra. A hasznos információ (kódoló régiók) összevágása (splicing)
5 A génekben tárolt hasznos információ meglepõ módon szét van szabdalva. Az informatív szakaszok (exon vagy kódoló régió) közé feleslegesnek tûnõ, értelmetlen szakaszok (intron) ékelõdnek. A génexpresszió során elõször egy úgynevezett elsõdleges RNS másolat képzõdik (2. ábra). Az átírás során az értelmes szakaszokat a rendszer összevágja (splicing). Az exonok esetenként többféleképpen is összevághatók (alternatív splicing), így egyetlen génrõl nemcsak egy, de esetenként több (hasonló) fehérje is szintetizálódhat. Valamennyi, ma ismert élõ szervezet fehérje alapú, és mûködésének titka a szintetizált fehérjék összességében rejlik. A fehérjék szintézisére vonatkozó információ a génekben található. Míg a DNS az információ tárháza, avagy a tervrajz, a fehérjék a kivitelezõk: az élet minden funkciója a fehérjék mûködéséhez van kötve. Ha a genetikai információ hibás, egyes fehérjék mûködése zavart lesz, és ez patológiai elváltozásokhoz vezethet. A Humán Genom Projekt célja A Humán Genom Projekt (HGP) 1989-ben kezdõdött, célja a teljes humán DNS szekvencia (a 3 milliárd DNS-betû) megismerése. Ez a feladat eleinte reménytelennek tûnt: 1992-ben a DNS szekvenálási költségek átlaga 1 dollár/nukleotid volt, és átlagosan százezer nukleotidból álló szekvenciát határoztak meg évente. Ezek az adatok arra utaltak, hogy a 3 milliárd betû megismerése 3 milliárd dollárt és harmincezer évet igényelne. A szekvenálási technikák fejlõdése azonban lehetõvé tette, hogy az USA, Anglia, Németország, Franciaország, Japán és Kína állami támogatásával dolgozó, 20 csoportból álló konzorcium 2001-ben bejelentse, hogy a humán DNS szekvencia 94%-át megfejtették. Az utóbbi években azonos céllal megalakult egy privát szektor (fõleg gyógyszergyárak) által támogatott csoport is, a Celera. Így 2001 februárjára a humán genomnak két munkapéldányát készítették el: az egyik egy mindenki számára hozzáférhetõ adatbázis ( a másik a Celera saját adatbázisa ( Mit jelent a munkapéldány? Lényegében azt, hogy az információ megfejtése még nem fejezõdött be, de a jelenlegi adatok már sokoldalúan felhasználhatók. A hiányosságok kétfélék: egyrészt vannak olyan kisebb-nagyobb szakaszok, melyek szekvenciája (betûsorozata) még hiányzik (a hiány 2001 februárjában 6% volt, de ez az idõ elõrehaladtával drasztikusan csökken). Másrészt maga a DNS szekvencia még ellenõrzésre, pontosításra, javításra szorul. Úgy tûnik azonban, hogy ez a munka is igen jól halad végére már
6 három kromoszóma (20, 21 és 22) végleges DNS szekvenciája ismeretes, és a többi is gyors ütemben készül. A humán genom projekt elsõ célja tehát, hogy genetikai információnk mind a 3 milliárd betûjét megismerjük. Ezt követi az összes gén helyének azonosítása és annotációja (nevesítése, azaz funkciójának megismerése). A humán genom elsõ munkapéldányából levonható következtetések Mit tudunk kiolvasni a humán DNS szekvencia munkapéldányából? A legmeglepõbb eredmény talán az, hogy úgy tûnik, a humán genom információ tartalmának kevesebb, mint 5%-át alkotják az emberi fehérjék génjei, melyek számát ezerre becsülik (International Human Genome Sequencing Consortium, 2001). Ebbõl 2001 februárjában kb gén funkciója volt ismert, de ez a szám rohamosan nõ. A gének száma tehát meglepõen alacsony, hiszen mindössze kb. kétszerese annak, mint amit a gerinctelen állatokban találtak. Igen valószínû azonban, hogy az emberi fehérjék változatossága mégis sokkal nagyobb, mint a gerincteleneké. Ennek az ellentmondásnak az egyik lehetséges magyarázata az, hogy a humán fehérjékre különösen jellemzõ az exonok alternatív összerakási módjai (alternatív splicing, lásd 2. ábra), melynek során egy gén többféle fehérjét is meghatározhat. Másik eredmény, hogy az emberi fehérjék domain szerkezete igen gazdag. A domain a fehérje egy funkcionális egysége, amely gyakran de nem mindig megfelel egy exonnak. Nyelvtani hasonlattal élve a fehérje megfeleltethetõ egy mondatnak, melyben vannak olyan szavak, melyek más fehérjékben, vagyis más mondatokban is elõfordulnak. Egyes szavak/domainek rendkívül jellemzõek egy bizonyos fajta fehérjecsoportra, melyek feltehetõen közös eredetûek, és funkciójukban is hasonlók. Úgy tûnik, hogy a humán genetikai információ tárolásának elve valamelyest hasonlít a nyelv szerkezetére: az információ legfontosabb része a fehérje-domain (szó) készlet, amelybõl igen változatos formában rakhatók össze a fehérjék (mondatok). A viszonylag kisszámú humán gén megkönnyíti a további munkát. Feltehetõen hamarosan elkészülnek azok a gén- és fehérje-leltárak, melyek orvos-biológiai periódusos rendszerként funkcionálnak majd. Tudjuk, hogy ezekbõl a szerkezeti egységekbõl, illetve ezek kombinációjából áll a testünk, ezek a gyógyszerek támadáspontjai, és ezek mûködési rendellenessége okozza a betegségek jelentõs részét. A humán genom szekvencia mellett ezek a leltárak adják majd az in silico (internetes adatbázisok segítségével történõ) biológiai kutatások alapját. Egy példa az in silico kutatásokra: ismerünk egy fehérjét, és azt kérdezzük az adatbázistól, létezik-e genomunkban egy hasonló fehérje információja? Így
7 fedezték fel az Alzheimer kór kialakulásában szerepet játszó presenilin 2 fehérjét, vagy a teljes szerotonin receptor (5-HT 3A ) egyik eddig ismeretlen részét (5-HT 3B ). Felmerül ugyanakkor a kérdés, hogy milyen információt hordoz a humán genom maradék 95%-a? Természetesen vannak olyan informatív szekvenciák, amelyek nem fehérjéket kódolnak. Ide tartoznak az RNS-ek génjei, továbbá a gén kifejezõdésének (expressziójának) szabályozásáért felelõs DNS szakaszok (promoter, enhancer régiók). Mindezek mellett azonban ténylegesen van egy olyan része a genomnak, melynek biztosan semmi köze a humán funkciókhoz. Ez a meglehetõsen sok szemét DNS a humán genom mintegy 45%-át kitevõ, parazita szekvenciák (transzpozonok) sorozatai. Ezek ismétlõdõ szekvenciák (azonos betûsorozatok ismétlõdései), melyek önmagukat szaporították a törzsfejlõdés során. Ilyen például a LINE (long interspread elements, 6000 bp hosszú, kb példány van belõle egy humán genomban, genomunk 20 25%-át foglalja el), vagy a SINE (short interspread repeats, bp, szaporodásához a LINE szükséges, 1 2 millió példány van belõle, a genom 10 15%-át teszi ki). Érdekes megjegyezni, hogy a SINE szekvenciák legnagyobb része emberben az úgynevezett Alu szekvencia, mely jellemzõen a gének környezetében fordul elõ, ennek szerepe azonban nem ismeretes. Ezeken kívül sok, úgynevezett egyszerû ismétlés található a genomban (például A betûk hosszú sorozata), és jellemzõen sok a két vagy több példányban elõforduló gén, melyek közül a másodpéldány gyakran nem mûködik (pszeudogén). Vagyis a humán genom mai felfogásunk szerint tengernyi, számunkra nem informatív, sokszorosan ismétlõdõ szekvenciák (betûsorozatok) halmaza, melyben elszórva találhatók az életmûködések szempontjából lényeges génszigetek A humán genom polimorf jellege Mennyire különbözik két (nem rokon) ember genomja? A humán genom projekt valójában egyetlen ember haploid kromoszóma készletének (a homológ kromoszómák egyikének, összesen 23-nak) információját derítette fel. Hogy ki ez az ember, az természetesen nem ismert. Nyilvánvaló azonban a következõ lépés: annak feltérképezése, hogy mi a különbség az egyes emberek genomja között. Ez a munka is folyamatban van, és a jelenlegi becslések szerint két nem rokon ember között a különbség kb. 0,1%. A különbség szemléltetésére felhasználhatjuk az elõzõekben bemutatott könyvpéldát: ha az egyik ember genomja megfelel az A, G, C, T betûkbõl álló 3000 db 1000 oldalas könyvnek, akkor a másiké körülbelül ugyanilyen, kivéve, hogy minden oldalon
8 található kb. egy betûnyi eltérés. Hogy melyik az igazi információ, és melyik a sajtóhiba, azt nagyon sok esetben nem lehet megmondani, ezért manapság nemigen beszélünk hibákról/mutációkról, hanem inkább változatosságról, vagy más szóval polimorfizmusról. A genetikai polimorfizmus vizsgálat az egyes emberek genomjai közt fellelhetõ különbségek feltárásával foglalkozik, ez a különbség 2001-es becslések szerint az összes információnak kb. ezredrésze. Hogy ez az egy ezreléknyi különbség vajon sok vagy kevés, arra vonatkozóan a következõ példákat érdemes átgondolni. A hemoglobin génjének elsõ exonjában egy bizonyos DNS-betû megváltozása a hemoglobin teljes funkciókiesését okozza. A mutáció következménye egy súlyos betegség, a sarlósejtes anémia, amelyben a vörösvértestek oxigén szállító fehérjéi hosszú fonalakká csapódnak össze, és ez adja a sarló formájú sejtet, mely oxigén szállításra képtelen. Azokat a genetikai polimorfizmusokat, amelyek ritkák (kevesebb, mint 1% gyakoriság) és betegséget okoznak, mutációnak is szokás nevezni. Ugyanakkor a DNS ujjlenyomat készítésekor amit a kriminológiában használnak fel olyan, a géneken kívül esõ polimorfizmusokat vizsgálnak, melyek a populációban rendkívül változatos (polimorf) megjelenésûek, de az egyed egészségére semmilyen hatással nincsenek, azaz semleges hatású polimorfizmusok vagy markerek. Természetesen a genetikai variációk két, végletes hatása között nagyon sokféle átmenet létezik. Azokat a polimorfizmusokat, amelyeknek egyes változatai kismértékben hozzájárulnak egy komplex betegségek kialakulásához, rizikófaktoroknak szokás nevezni. A rizikófaktorok kutatása a mai molekuláris genetika legizgalmasabb területe. A polimorfizmusok tehát az egyes emberek DNS szekvenciájában (genetikai információtartalmában) fellelhetõ különbségek. Hatásukat tekintve lehetnek teljesen semlegesek, hozzájárulhatnak az emberek közti öröklött különbségek kialakulásához, de funkciókiesést és betegséget okozhatnak (rizikófaktorok, mutációk). A polimorfizmusok fõ formái: SNP és VNTR A polimorfizmusok egyik formája az egypontos nukleotid variáció (single nucleotide polymorphism, SNP) (3. A. ábra). Ebben az esetben a különbözõ emberek genomját összehasonlítva egy bizonyos helyen az egyik emberben nem ugyanazt a betû-párt találjuk, mint a másikban. Az ilyen eltérés maximum négyféle lehet (mert a genetikai információ négy betûbõl áll), de az a gyakori, hogy egy populációban két változat terjed el (az ábra például egy
9 AT GC cserét mutat, amit szokás csupán az egyik szál változásával jellemezni: A G). A Humán Genom Projekt SNP konszorciuma 2001 februárjában 1,4 millió SNP-t közölt, ez a szám az év végére megháromszorozódott ( Az SNP adatbázisoknak feltehetõen óriási jelentõsége lesz a komplex öröklõdésû betegségek (ide tartoznak a pszichiátriai betegségek is) feltérképezésében, és az emberi személyiség és kognitív funkciók öröklött eltéréseinek megértésében. A Genom 1 G A C A G T C T G T C A B Genom 1 4 ismétlõdés Genom 2 G A C G G T C T G C C A Genom 2 7 ismétlõdés SNP: 1 bázispár különbség Ismétlõdõ szekvencia ismétlési szám-polimorfizmusa (VNTR) 3. ábra. A genetikai polimorfizmusok fõ típusai: SNP(A) és VNTR (B) Genomunk egyik sajátos vonása, hogy sok benne az ismétlõdõ szekvencia részlet. Ez nem csak a parazita információra vonatkozik, a humán génekben is elõfordulnak ismétlõdések. Genetikai információt tartalmazó könyvünkben tehát egyes szavak (exonok) ismétlõdõ szótagokból (szekvenciákból) állnak. A genetikai információ változatossága abban nyilvánul meg, hogy az ismétlõdés száma eltérõ az egyes emberekben, ezt nevezzük hosszúságpolimorfizmusnak (variable number of tandem repeats, VNTR) (3. B. ábra) A polimorfizmusok felhasználása az öröklött tulajdonságokért felelõs gének meghatározásában A genetikai polimorfizmusok vizsgálata felvilágosítással szolgálhat arra nézve, hogy mely gének felelõsek az emberi tulajdonságok sokféleségéért. Ezen vizsgálati kör szûkebb területe az öröklõdõ betegségekért felelõs génváltozatok vizsgálata. Genetikai alapfogalmak: allél genotípus homozigóta heterozigóta A bevezetõben említettük, hogy a Humán Genom Projekt elsõ lépésként csak a haploid genom megfejtésével foglalkozik, azaz a 22 homológ kromoszómapárból csak az egyik információtartalmát határozza meg. Mit tudunk a homológ kromoszóma párokról? Ezek
10 információtartalma alapvetõen azonos, a különbség csupán a genetikai polimorfizmusból fakad. Vegyük példaként a dopamin D4-es receptor (DRD4) gén VNTR polimorfizmusát (4. ábra). A: DRD4 allélok DRD4 (2x) DRD4 (3x) DRD4 (4x) DRD4 (5x) DRD4 (6x) DRD4 (7x) DRD4 (8x) DRD4 (9x) DRD4 (10x) B: DRD4 genotípusok Homozigóta egyed (4x,4x) Heterozigóta egyed (4x,7x) 4. ábra. A dopamin D4-es receptor gén alléljai (A) és példa lehetséges genotípusokra (B) A DRD4 gén a 11-es kromoszómán található. A gén harmadik exonjában van egy ismétlõdõ szekvencia, az ismétlõdések száma 2 10 lehet. Ennek megfelelõen a DRD4 génnek kilenc féle (2, 3, 4, 5, 6, 7, 8, 9 és 10 ismétlõdést tartalmazó) változata, vagy más szóval allélja van. Az allél egy genetikai információrészlet, mely a populációban több, különbözõ formában fordul elõ (polimorfizmus). Minden személynek két homológ kromoszómája, ennek megfelelõen két allélja van. Ha a két allél azonos, homozigóta genotípusról, ha különbözõ, heterozigóta genotípusról beszélünk. Lehetséges például, hogy az egyik emberben mindkét (homológ) 11-es kromoszómájában a DRD4 gén négy ismétlõdést tartalmaz (DRD4 genotípus 4,4: homozigóta), de az is lehet, hogy az egyik 11-es kromoszómáján a négyszeres ismétlõdésû változat, a másikon viszont a hétszeres ismétlõdésû változat található meg (DRD4 genotípus 4,7: heterozigóta).
11 Genetikai alapfogalmak: Monogénes (mendeli) öröklésmenet A mendeli öröklésmenetben a genotípus (például egyetlen gén jelenléte vagy hiánya) közvetlenül hat a fenotípusra (az egyén megbetegszik-e, avagy nem). Domináns (mendeli) öröklésmenetrõl akkor beszélünk, ha az allél (például egy betegségokozó gén) hatása a fenotípusra nemcsak homozigóta, de heterozigóta formában is érvényesül (például betegséget okoz). Viszonylag kevés domináns öröklésmenetû betegséget ismerünk, azonban ide tartoznak a neurodegenerációs betegségek egyes formái (Huntington kór, mendeli öröklésmenetû Alzheimer kór). Ezzel kapcsolatban máris felmerül egy komoly etikai probléma: az ilyen mutációt homozigóta formában hordozó szülõ (aki idõsebb korában maga is megbetegszik) valamennyi gyereke örökölni fogja a betegséget, heterozigóta esetében pedig 50%-os eséllyel lesz a gyermek beteg (lásd 5. A. ábra). Ugyanakkor a neurodegenerációs betegségek csak felnõttkorban, általában az utódok létrehozása után manifesztálódnak. Kérdés, hogy szabad-e a genetikai diagnózis felállítása a gyermeknemzés elõtt, és ha igen, hogyan kezeljük ezt az információt? A B egészséges beteg egészséges beteg 5. ábra. Monogénes domináns (A) és recesszív (B) öröklésmenet A monogénes öröklésmenetû betegségek legnagyobb része azonban a recesszív (mendeli) öröklésmenetet követi. Ha mindkét szülõ heterozigóta, akik teljesen egészségesek, de hordozzák a betegségokozó gént (5. B. ábra), 25% eséllyel születik beteg gyermekük. Ilyen esetekben a szülõk genotípusának meghatározása segít abban, hogy a betegség megjelenésére
12 felkészüljünk. Újabban a magzat genetikai vizsgálata azt is lehetõvé teszi, hogy a terhesség igen korai fázisában megállapítsuk, beteg lesz-e a születendõ gyermek. A prenatális genetikai diagnózis eredménye segíthet a betegség kezelésében, mivel vannak olyan betegségek, melyek a terhesség alatt elkezdett terápiával gyógyíthatók (például a congenitális adrenális hyperplasia esetében, amelyben a leánygyermekek részben vagy teljesen fiú külsõ nemi szervekkel születhetnek; ez megakadályozható a terhesség korai szakaszában elkezdett hormonterápiával). Ha a betegség jelenleg gyógyíthatatlan és végzetes, a genetikus javasolhatja a mûvi vetélést, mivel az anyának 75% esélye van arra, hogy a következõ terhességébõl születendõ gyermeke egészséges lesz. A prenatális diagnózis eredményeinek értékelése orvosi-etikai szempontból azonban nem teljesen megoldott. Genetikai alapfogalmak: Kapcsoltsági csoportok linkage analysis Ha a két kiválasztott jellegért felelõs DNS szekvencia ugyanazon a kromoszómán található, nagy valószínûséggel együtt kerülnek át az utódba, míg ha különbözõ kromoszómákon vannak, szabadon kombinálódhatnak. Azonos kromoszómán található allélok (tulajdonságok, polimorfizmusok) az öröklõdés során kapcsoltsági csoportot alkotnak. A kapcsoltság annál erõsebb, minél közelebb van a két polimorfizmus, ezen alapul a kapcsoltsági csoportok vizsgálata (linkage analysis). Monogénes öröklõdésû betegségek A humán genom projekt eredményeit felhasználva óriási tempóban folyik a monogénes öröklõdésû betegségekért felelõs gének azonosítása ben több, mint harminc betegségben találták meg a betegségért felelõs génmutációt, ezeket az adatokat az OMIM (Online Mendelien Inheritance of Men) adatbázisban gyûjtik ( A vizsgálat elsõ lépése általában a betegséget okozó gén kromoszómális lokalizációjának meghatározása. Ez az érintett családokban több száz marker (polimorfizmus) vizsgálatával történhet. A család genetikai vizsgálata során megállapítható, hogy melyik marker jár szorosan együtt a betegség megjelenésével, így meghatározható a betegséget okozó mutáció kromoszómális lokalizációja (linkage analysis). Ezután a humán genom projekt eredményei alapján kiszámítható, hogy mely gén(ek) esnek erre a területre. A mutáció pontos meghatározása a betegbõl származó DNS
13 darab szekvenálásával ( DNS-betûinek meghatározásával), és az eredménynek a normális szekvenciával való összevetésével történik (6. ábra). A: lokalizáció a kromoszómán Linkage analysis kromoszómák * polimorf markerek * * * * * * * * * * * * * * * * * * * * # * * * * * * * LOD (log (rizikó)) B: gén-azonosítás gén1 gén2 * * * * * # * * * * * * markerek informatív marker C: DNS szekvenálás Normál DNS: AATTGCTTGCGTAGG Beteg DNS: AATTGCTGGCGTAGG 6. ábra. A monogénes öröklõdésû betegségek azonosításának elvi vázlata A monogénes (mendeli öröklõdésû) betegségeket okozó gének (génhibák) pontos megismerése nemcsak elméleti jelentõségû. Fontos gyakorlati következmény, hogy a továbbiakban a betegségre való genetikai esendõség szûrhetõ akár prenatálisan is. Továbbmenve, a betegség molekuláris okának megismerése hozzásegíthet a hatékony gyógyításhoz. Végül, de nem utolsósorban génjeink normális mûködését elsõsorban a mûködés kiesésébõl lehet igazán megismerni. Komplex öröklésmenetû betegségek A monogénes (mendeli) öröklésmenetû betegségek ritkák. A nagy populációt érintõ népbetegségek (szív és érrendszeri, mozgásszervi, neurológiai és pszichiátriai betegségek) genetikai hátterében poligénes rendszerek állnak. A poligénes rendszerek egyes genetikai elemeinek felkutatása nem egyszerû feladat (Baron, 2001). Különösen igaz ez a neurológiai és pszichiátriai betegségek esetében, ahol az idegrendszer rendkívüli plaszticitásával és komplexitásával is számolnunk kell. Megnehezíti a kutatásokat, hogy nemigen fordul elõ olyan pszichátriai betegség, mely egy adott fehérje funkció-kiesésének következménye, mert
14 a többi fehérje általában átveszi a kiesett komponens mûködését (például a dopamin D4-es receptor mûködésének teljes hiánya sem okoz jól definiálható problémákat, mivel funkcióját feltehetõleg átveszi a többi receptor). A komplex öröklõdésû (poligénes) betegségek vizsgálatára többféle stratégiát használnak. Egyrészt itt is próbálkoznak a fõ komponensek kromoszómális lokalizációjával (linkage analysis), de ez csak akkor járhat sikerrel, ha van néhány nagy hatású, ún. fõgénhatás. Egy alternatív módszer a kandidáns gének vizsgálata asszociációs analízissel. Ebben az esetben hipotetikusan kiválasztunk egy gént (kandidáns gén), amelyrõl feltételezzük, hogy szerepet játszhat egy adott betegség kialakulásában. Ezután a kandidáns gén polimorf alléljainak gyakoriságát megmérjük az egészséges és a beteg populációban (7. ábra). Ha statisztikai módszerekkel különbséget mutatható ki egy polimorf gén egyes allélváltozatainak gyakoriságában, például valamelyik allél gyakrabban fordul elõ a betegek közt, mint az egészségesek populációjában, akkor azt mondhatjuk, hogy szignifikáns asszociációt találtunk a kandidáns gén egy adott változata, és a betegség elõfordulása között. Ezt a polimorf változatot a továbbiakban az adott betegség rizikó faktorának nevezhetjük. A rizikó faktor jelenléte nem feltétlenül okoz betegséget, csupán megnöveli a betegség kialakulásának valószínûségét. A végsõ cél a genetikai és környezeti rizikófaktorok feltérképezése, amelyek alapján egy betegség kialakulása valószínûsíthetõ, vagy esetleg éppen elvethetõ (protektív faktorok). Családvizsgálat LINKAGE ANALYSIS Populációk vizsgálata ASSZOCIÁCIÓ VIZSGÁLAT A keresett gén(ek) kromoszómális lokalizációja teljes genomra kiterjedõ kandidáns gének Rizikó/protektív faktorok Családi hármas vizsgálata (TDT) 7. ábra. A komplex betegségek genetikájának kutatási irányai
15 Meg kell azonban jegyezni, hogy a multifaktoros (komplex) betegségek genetikai vizsgálata ma még nem teljesen megoldott. Sokféle probléma merül fel a jelenleg használt módszerekkel (linkage analysis vagy kandidáns gén asszociációs vizsgálat). A kapcsoltsági csoportok (linkage analysis) módszerének fõ problémája, hogy kiterjedt (sok tagú) családok vizsgálata szükséges hozzá, akiknél halmozottan fordul elõ a betegség, és a család minden tagjának diagnózisa rendelkezésre áll. Ugyanakkor csak abban az esetben kaphatunk eredményt, ha van néhány fõ-gén hatás, mert az analízis nagyon kis hatásokat nem tud kimutatni. A módszer egyáltalán nem használható sporadikus (elszórt) esetek genetikai rizikófaktorainak vizsgálatára. Az asszociációs vizsgálatokkal gyenge génhatások is kimutathatók. Elvben bármilyen komplex a betegség genetikája, elõbb-utóbb mód lehet arra, hogy minden komponenst feltérképezzünk. Ezen vizsgálatoknál a probléma inkább a hamis-pozitív eredményekkel van (a gyenge hatások miatt nehéz megkülönböztetni a valódi génhatásokat a véletlen asszociációtól). A megoldást ma egyelõre abban látják, hogy egy adott kandidáns gén betegség asszociációt többféle populációt vizsgálva, sokszorosan reprodukálni kell ahhoz, hogy az asszociáció elfogadható legyen. A másik érdekes probléma a vizsgált populáció genetikai rétegzõdése (populáció stratifikáció), mely szintén hamis-pozitív eredményekhez vezethet. Ennek elkerülésére ma egyre inkább összekapcsolják az asszociációs vizsgálatokat a családanalízissel. Ilyen például a TDT (transmission disequilibrium test), amely azt vizsgálja, hogy heterozigóta szülõk esetében a vizsgált kandidáns gén egyes polimorf változatai preferenciálisan kerülnek-e át a beteg utódokba (7. ábra). A komplex öröklõdésû betegségek és pszichológiai vonások vizsgálati módszerei kialakulóban vannak. Problémák nem csupán a genetikai módszerekkel vannak. A legnagyobb gond legtöbbször a fenotípus, azaz a pszichológiai jelleg, vagy a pszichiátriai betegség pontos azonosítása. A pszichiátriai genetikai vizsgálatokat valószínûleg megkönnyítené, ha a diagnózist jól definiált altípusokra lehetne szûkíteni. Ugyanakkor a pszichiátriai betegségek komorbiditása a diagnózis kiszélesítésének irányába hat, ezért jelenleg mindkét irányban történnek próbálkozások. Érdemes megjegyezni, hogy arra is van esély, hogy éppen a kandidáns gének polimorf változatainak azonosítása segít majd a pontos diagnózis felállításában. Erre például szolgál az Alzheimer kór génjeinek és rizikó faktorainak megismerése (lásd alább). Mindenesetre a pszichogenetikai vizsgálatok a pszichológus/pszichiáter és a molekuláris genetikus szoros együttmûködését kívánják meg.
16 1.4. A genetikai polimorfizmusok pszichológiai vonatkozásai A genetikai polimorfizmusok frappáns alkalmazása a személyiség pszichológiában Benjamin és mtsai., illetve Ebstein és mtsai ban megjelent asszociációs vizsgálata. A vizsgálat összekapcsolta a személyiség cloningeri pszichobiológiai modelljét, és a dopamin D4-es receptor gén ismert polimorfizmusát, és statisztikailag szignifikáns asszociációt mutatott ki a dopamin D4-es receptor hosszú alléljának jelenléte és a TPQ személyiség kérdõív újdonságkeresési dimenziójának pontszáma között. Ez a vizsgálat az elsõ asszociációs genetikai vizsgálat volt a személyiségpszichológia (és általában a pszichológia) területén, és számos, hasonló jellegû vizsgálatot indított el. A hagyományos viselkedés-genetikai kutatások eredményei alapján a személyiségdimenziók jelentõs (25% és 45% közötti) genetikai meghatározottságot mutatnak (Rose, 1995). Az asszociációs vizsgálatok azt kutatják, hogy mely géneken okozzák a genetikai hatást. Nyilvánvaló, hogy a személyiségjegyek genetikai meghatározottsága poligénes jellegû, ezért számos génhatást mutattak ki idáig, és még többet fognak kimutatni a jövõben. Mint minden poligénes rendszerben, itt is kicsi az egyes gének hatása, és emiatt a jelenlegi módszerek könnyen vezetnek hamis pozitív eredményekre. Mi tehát a megoldás? Hogyan fogjuk megismerni pl. a személyiség különbözõsége mögött álló genetikai faktorokat? A válasz ugyanaz, mint ami a komplex genetikájú betegségek esetében: a feladat újabb és újabb kandidáns gének vizsgálata, az eredmények reprodukciója különbözõ populációk esetében, és nem utolsósorban a fenotípus pontosítása. Az alábbiakban a cloningeri személyiség kérdõívvel mért újdonságkeresés és a D4-es dopamin receptor hosszú formájának asszociációját mutatjuk be, mint a személyiségjegyeket meghatározó kandidáns gének kutatásának ma már klasszikusnak nevezhetõ példáját. Cloninger pszicho-biológiai modellje Cloninger a személyiség pszicho-biológiai modelljének elsõ változatát 1987-ben dolgozta ki (Cloninger, 1987). Ebben három, egymástól biológiailag független személyiség-összetevõt különített el: az újdonság-keresést (novelty seeking), a fájdalom-elkerülést (harm avoidance) és a jutalom-függõséget (reward-dependence). A faktorok mérésére kidolgozta a 100 itemes, önbeszámolón alapuló TPQ (Tridimensional Personality Questionnaire) kérdõívet (Cloninger, 1991). Cloninger hipotézise szerint a temperamentum faktorok az öröklött
17 komponensek által determinált, automatikus, pre-konceptuális válaszok kialakításában játszanak szerepet. Az újdonságkeresés alapvetõ fontossággal bír az automatikus válaszok kialakításában, míg a jutalomfüggõség és fájdalomelkerülés dimenziói a válasz fenntartásában, illetve a viselkedés megszüntetésében játszanak kiemelkedõ szerepet. A modell az újdonságkeresés dimenzióját a dopamin, a fájdalomelkerülést a szerotonin, a jutalomfüggõség kialakulását pedig az adrenalin neurotranszmitter rendszer mûködésével hozta összefüggésbe. A modell továbbfejlesztett formájában a TCI (Temperament and Character Inventory) kérdõívet használja (Cloninger és mti. 1993). A genetikai komponensû temperamentum és a környezeti hatások által szabályozott karakter skálák (önirányultság, együttmûködés és transzcendencia) egyértelmû elkülönítése lehetõvé teszi a személyiség, illetve az egyéni viselkedés kapcsolatának árnyaltabb magyarázatát: egy extrém temperamentummal rendelkezõ egyén is jól beilleszkedhet, hasznos tagja a társadalomnak, amennyiben ezt a környezet, és karakterének kedvezõ összjátéka lehetõvé teszi. A dopamin D4-es receptor polimorfizmusa: a hosszú és a rövid allél Az öt dopamin receptor gén (DRD1 DRD5) közül a DRD4 kiemelkedõen variábilis. A DRD4 gén polimorf helyei közül a legizgalmasabb egy hosszúság polimorfizmus, melynél egy kicsi géndarab (48 bázispár hosszú) többször ismétlõdik, egymás után (lásd 4. ábra). Az ismétlési szám kettõtõl tízig terjedhet (Van Tol és mtsai, 1992), tehát van olyan személy, akinek a DRD4 génjében csak 5 vagy annál kevesebbszer ismétlõdik ez a szakasz, ebben az esetben a genetikai információ rövidebb fehérjét fog meghatározni ( rövid allél ). Másoknál elõfordul ennél több (6 10) ismétlõdés, így a dopamin D4-es receptor fehérje igen hosszú lesz ( hosszú allél, 8. ábra). A receptor szerkezetének variációi természetesen befolyásolják a funkciót. Valószínûleg a hosszú forma kevésbé hatékony a jelpálya közvetítésében (Van Tol, 1998). Ez azonban nem jelenti azt, hogy a hosszabb receptor rosszabbul mûködne, csupán egy kicsit másképp hat, mint a rövid forma. Többek közt ezért sem nevezik ezt mutációnak, csupán polimorfizmusnak, azaz az emberek közt fellelhetõ variációk egyik fajtájának.
18 kívül belül kívül belül DRD4 rövid DRD4 hosszú 8. A dopamin D4-es receptor fehérje rövid és hosszú formája A DRD4 hosszú allél asszociációs vizsgálatai Az újdonságkeresés és a DRD4 hosszú allél asszociációját Benjamin és Ebstein munkacsoportjának fent említett munkái írták le elõször 1996-ban. Azóta számos publikácó jelent meg, ezek megerõsítették vagy elvetették Benjamin és Ebstein eredményeit. Ebstein már egy 1997-es összefogalójában (Ebstein és Belmaker, 1995) megpróbálta rendszerezni az elsõ eredmény mellett és az ellene szóló adatokat. Ekkor úgy tûnt, hogy finn és svéd vizsgálatokban nem találták meg a szignifikáns összefüggést, de további amerikai, izraeli és japán vizsgálatok igazolták az elsõ asszociációt. Az is felmerült, hogy nõkben jobban kimutatható a hosszú allél és az újdonságkeresés összefüggése, mint férfiakban. Ebstein rámutatott arra is, hogy a vizsgált populáció kiválasztásánál bizonyos szabályokat be kellene tartani, pl. szûk életkoreloszlás (18 32), nem túl alacsony iskolázottsági szint (legalább középiskola), pszichiátriai betegségek, drog és alkoholizmus kizárása, stb. Egy újabb próbálkozás az eredmények rendszerezésére és értékelésére már a címében is szkeptikus: Novelty or nonsense? (Paterson és mtsai., 1999). A vizsgálatok ennek ellenére folytatódnak, mivel olyan pszichátriai betegcsoportokban is felmerült a hosszú allél nagyobb gyakorisága, mint például a figyelemhiányos hiperaktivitási szindróma (lásd késõbb), a beteges játékszenvedély (Perez és mtsai, 1997), vagy a drogfüggõség (Li és mtsai., 1997). A DRD4 gén szabályozó régióinak polimorfizmusa Mint említettük, a DRD4 rendkívül polimorf gén, és a fent említett hosszúság polimorfizmus mellet még más génvariációk is megfigyelhetõk a humán populációban. A legújabb kutatások a génexpresszió szabályozására vonatkoznak, melynek hatására egyes emberekben egy kicsit kevesebb, míg másokban valamivel több dopamin D4-es receptor
19 szintetizálódhat. Ezek a kutatások a gén elõtt lokalizálható (5 UTR promoter, lásd 2. ábra), úgynevezett promoter szakasz egyedi változatosságait vizsgálják (Mitsuyasu és mtsai., 1999). A promoter egy bizonyos pontján, melyet a 521-es pozícióval jelölnek (azért használnak negatív számot, mert ez a szekvencia a génen kívül van) a négy DNS betûbõl egyes emberekben C, míg másokban T van. Ezt nevezik 521 C/T polimorfizmusnak. Feltételezhetõ, hogy a C allél hatására több, a T allél hatására kevesebb receptor szintetizálódik. Pszichogenetikai vizsgálatok azt mutatták, hogy a 521 C/T polimorfizmus is hatással lehet a TCI kérdõívvel mérhetõ újdonságkeresés mértékére. Japán (Okuyama és mtsai., 2000) és magyar (Rónai és mtsai, 2001) kutatók szignifikáns asszociációt mutattak ki a 521 C/T polimorfizmus és a TCI kérdõívvel mért újdonságkeresés mértéke között. Eredményeik szerint azok a személyek, akik nem rendelkeztek T változattal, átlagosan magasabb pontszámot érnek el ebben a személyiség dimenzióban, mint T allélal rendelkezõ társaik. Meg kell jegyezni, hogy ezek a vizsgálatok csak nemrég kezdõdtek, és a szabályozó szekvenciák polimorfizmusának részletesebb megismerése feltehetõen újabb asszociációs vizsgálatokra fog inspirálni A genetikai polimorfizmusok pszichiátriai vonatkozásai A pszichiátriai genetikai vizsgálatok óriási száma és az eredmények ma még legtöbbször bizonytalan jellege miatt általános áttekintés helyett három példát ragadtunk ki. Az Alzheimer kór fõ génhatásainak megismerése a kapcsoltsági elemzés (linkage analysis) módszerének sikertörténete. A szkizofrénia genetikai hátterének kutatása ma még a jóformán teljes sikertelenség példája. A figyelemhiányos hiperaktivitási szindróma (ADHD) kandidáns génvizsgálatai pedig a jelenlegi asszociációs vizsgálatok legeredményesebb példája. Alzheimer-kór Az Alzheimer-kór biokémiája: a neurodegeneratív betegség két fõ jellemzõ patológiás képlete az extracelluláris neuritikus plakk és az intracelluláris neurofibrilláris szövevény (intracellular neuritic plaques). Az extracelluláris plakkok magja b-amiloidot (Ab) tartalmaz, amely az úgynevezett amyloid prekurzor fehérjébõl (amyloid precursor protein, APP) keletkezik (Price és Sisodia, 1998). A neurofibrilláris szövevényben pedig egy sejtváz-fehérje (tau protein) polimerizált terméke halmozódik fel.
20 Az Alzheimer kór genetikája: A betegség patomechanizmusának megértésében nagy áttörés volt azoknak a géneknek azonosítása, melyek mutációja Alzheimer-kórt okoz (Price és Sisodia, 1998). Eddig három gént azonosítottak, melyek mutációja a betegség kialakulásához vezet: az APP (amyloid precursor protein), a presenilin 1 és a presenilin 2. A gének kromoszómális térképezése és azonosítása az elõzõekben tárgyalt kapcsoltsági elemzéssel (linkage analysis) történt, kivéve a Presenilin 2 esetét, ezt már a humán genom in silico kutatásával fedezték fel. A családi halmozódásban elõforduló Alzheimer kór monogénes (mendeli), domináns öröklésmenetû, a betegség megjelenése korai (60 év alatt), azonban ez a forma szerencsére ritka (kevesebb, mint az összes megbetegedés 5%-a, lásd 9. ábra). apoe (65%) Monogénes öröklõdésû (<5%) PS 2 (0,1%) APP (0,4%)? Sporadikus (95%) PS 1 (3%)? (31,5%) 9. ábra. Az Alzheimer kór genetikája (Richard és Amouyel, 2001 nyomán) Az Alzheimer-kór leggyakrabban sporadikusan (elszórtan) fordul elõ, azaz öröklõdése nem követhetõ nyomon a családfában. Ez azonban nem jelenti azt, hogy ne lennének genetikai tényezõi a kialakuló betegségnek, csupán a genetikai rizikó faktor jelenléte nem egyértelmûen, hanem csupán bizonyos valószínûséggel, azaz más genetikai és környezeti rizikófaktorokkal együtt fejti ki hatását. Ezekben az esetekben lehetséges olyan rizikófaktorok keresése (asszociáció analízis), melyek elsõsorban a késõn manifesztálódó (60 év felett) betegség kialakulásának valószínûségét növelik meg. A rizikófaktorok közül jelenleg a legelfogadottabb az apoe e4 allél jelenléte (Chapman és mtsai., 2001). Az apoe (apolipoprotein E) a lipid (koleszterin) transzportban játszik szerepet, ennek óriási jelentõsége van az asztrociták által termelt koleszterin neuronokhoz való szállításában (a koleszterin a sejtmembrán fontos alkotórésze). Az apoe polimorf gén ε4 alléljának közvetlen szerepe a betegség kialakulásában jelenleg még nem ismert.
A HOSSZÚ ALLÉL TÖRTÉNETE
 A HOSSZÚ ALLÉL TÖRTÉNETE DOPAMIN D4-ES RECEPTOR GENETIKAI POLIMORFIZMUSÁNAK PSZICHOLÓGIAI VONATKOZÁSAI Székely Anna 1, Sasvári-Székely Mária 2 és Pléh Csaba 3 1 Ph.D hallgató, ELTE-BTK Kognitív Pszichológia
A HOSSZÚ ALLÉL TÖRTÉNETE DOPAMIN D4-ES RECEPTOR GENETIKAI POLIMORFIZMUSÁNAK PSZICHOLÓGIAI VONATKOZÁSAI Székely Anna 1, Sasvári-Székely Mária 2 és Pléh Csaba 3 1 Ph.D hallgató, ELTE-BTK Kognitív Pszichológia
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Többgénes jellegek. 1. Klasszikus (poligénes) mennyiségi jellegek. 2.Szinte minden jelleg több gén irányítása alatt áll
 Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai
 Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai Habilitációs dolgozat Veres-Székely Anna, Ph.D. 2010 TARTALOMJEGYZÉK BEVEZETÉS... 4 Ábrajegyzék... 6 Táblázatok
Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai Habilitációs dolgozat Veres-Székely Anna, Ph.D. 2010 TARTALOMJEGYZÉK BEVEZETÉS... 4 Ábrajegyzék... 6 Táblázatok
Molekuláris genetikai vizsgáló. módszerek az immundefektusok. diagnosztikájában
 Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Hátterükben egyetlen gén áll, melynek általában számottevő a viselkedésre gyakorolt hatása, öröklési mintázata jellegzetes.
 Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
A DNS szerkezete. Genom kromoszóma gén DNS genotípus - allél. Pontos méretek Watson genomja. J. D. Watson F. H. C. Crick. 2 nm C G.
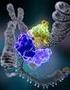 1955: 46 emberi kromoszóma van 1961: mrns 1975: DNS szekvenálás 1982: gén-bank adatbázisok 1983: R (polymerase chain reaction) Mérföldkövek 1 J. D. Watson F. H.. rick 2008 1953 2003 Watson genomja DNS
1955: 46 emberi kromoszóma van 1961: mrns 1975: DNS szekvenálás 1982: gén-bank adatbázisok 1983: R (polymerase chain reaction) Mérföldkövek 1 J. D. Watson F. H.. rick 2008 1953 2003 Watson genomja DNS
A HUMÁN GENOM PROJEKT Sasvári-Székely Mária* Semmelweis Egyetem, Orvosi Vegytani, Molekuláris Biológiai és Pathobiokémiai Intézet
 A HUMÁN GENOM PROJEKT Sasvári-Székely Mária* Semmelweis Egyetem, Orvosi Vegytani, Molekuláris Biológiai és Pathobiokémiai Intézet *Levelezési cím: Dr. Sasvári-Székely Mária, Semmelweis Egyetem, Orvosi
A HUMÁN GENOM PROJEKT Sasvári-Székely Mária* Semmelweis Egyetem, Orvosi Vegytani, Molekuláris Biológiai és Pathobiokémiai Intézet *Levelezési cím: Dr. Sasvári-Székely Mária, Semmelweis Egyetem, Orvosi
A kötődési mintázat és a
 Fakultatív program: Tudományos diákköri műhelyek: TDK háziverseny (dec 16. du) A kötődés mérése és genetikai háttere A gyermekkori temperamentum Személyiségvonások, mint endofenotípusok További érdekes
Fakultatív program: Tudományos diákköri műhelyek: TDK háziverseny (dec 16. du) A kötődés mérése és genetikai háttere A gyermekkori temperamentum Személyiségvonások, mint endofenotípusok További érdekes
T 038407 1. Zárójelentés
 T 038407 1 Zárójelentés OTKA támogatással 1996-ban indítottuk az MTA Pszichológiai Intézetében a Budapesti Családvizsgálatot (BCsV), amelynek fő célja a szülő-gyermek kapcsolat és a gyermekek érzelmi-szociális
T 038407 1 Zárójelentés OTKA támogatással 1996-ban indítottuk az MTA Pszichológiai Intézetében a Budapesti Családvizsgálatot (BCsV), amelynek fő célja a szülő-gyermek kapcsolat és a gyermekek érzelmi-szociális
Tudománytörténeti visszatekintés
 GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
A Hardy-Weinberg egyensúly. 2. gyakorlat
 A Hardy-Weinberg egyensúly 2. gyakorlat A Hardy-Weinberg egyensúly feltételei: nincs szelekció nincs migráció nagy populációméret (nincs sodródás) nincs mutáció pánmixis van allélgyakoriság azonos hímekben
A Hardy-Weinberg egyensúly 2. gyakorlat A Hardy-Weinberg egyensúly feltételei: nincs szelekció nincs migráció nagy populációméret (nincs sodródás) nincs mutáció pánmixis van allélgyakoriság azonos hímekben
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
HAPMAP -2010 Nemzetközi HapMap Projekt. SNP GWA Haplotípus: egy kromoszóma szegmensen lévő SNP mintázat
 HAPMAP -2010 Nemzetközi HapMap Projekt A Nemzetközi HapMap Project célja az emberi genom haplotípus* térképének(hapmap; haplotype map) megszerkesztése, melynek segítségével katalogizálni tudjuk az ember
HAPMAP -2010 Nemzetközi HapMap Projekt A Nemzetközi HapMap Project célja az emberi genom haplotípus* térképének(hapmap; haplotype map) megszerkesztése, melynek segítségével katalogizálni tudjuk az ember
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán
 A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
A PKU azért nem hal ki, mert gyógyítják, és ezzel növelik a mutáns allél gyakoriságát a Huntington kór pedig azért marad fenn, mert csak későn derül
 1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
A kromoszómák kialakulása előtt a DNS állomány megkettőződik. A két azonos információ tartalmú DNS egymás mellé rendeződik és egy kromoszómát alkot.
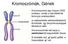 Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének centromer
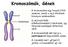 Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
A Humán Fenom Projekt
 A személyiség genetikája Endofenotípusok Endofenotípusok Temperamentum Személyiségdimenziók pszichogenetikai elemzése A Humán Fenom Projekt Intelligencia Személyiségvonások Hangulatzavarok ADHD Genom Drogfüggőség
A személyiség genetikája Endofenotípusok Endofenotípusok Temperamentum Személyiségdimenziók pszichogenetikai elemzése A Humán Fenom Projekt Intelligencia Személyiségvonások Hangulatzavarok ADHD Genom Drogfüggőség
Populációgenetikai. alapok
 Populációgenetikai alapok Populáció = egyedek egy adott csoportja Az egyedek eltérnek egymástól morfológiailag, de viselkedésüket tekintve is = genetikai különbségek Fenotípus = külső jellegek morfológia,
Populációgenetikai alapok Populáció = egyedek egy adott csoportja Az egyedek eltérnek egymástól morfológiailag, de viselkedésüket tekintve is = genetikai különbségek Fenotípus = külső jellegek morfológia,
Johann Gregor Mendel Az olmüci (Olomouc) és bécsi egyetem diákja Brünni ágostonrendi apát (nem szovjet tudós) Tudatos és nagyon alapos kutat
 10.2.2010 genmisk1 1 Áttekintés Mendel és a mendeli törvények Mendel előtt és körül A genetika törvényeinek újbóli felfedezése és a kromoszómák Watson és Crick a molekuláris biológoa központi dogmája 10.2.2010
10.2.2010 genmisk1 1 Áttekintés Mendel és a mendeli törvények Mendel előtt és körül A genetika törvényeinek újbóli felfedezése és a kromoszómák Watson és Crick a molekuláris biológoa központi dogmája 10.2.2010
Figyelemhiány/Hiperaktivitás Zavar - ADHD TÁJÉKOZTATÓ FÜZET. ADHD-s gyermekek családjai részére
 Figyelemhiány/Hiperaktivitás Zavar - ADHD TÁJÉKOZTATÓ FÜZET ADHD-s gyermekek családjai részére KEZELÉSI TÁJÉKOZTATÓ FÜZET Ezt a tájékoztató füzetet azért készítettük, hogy segítsünk a FIGYELEMHIÁNY/HIPERAKTIVITÁS
Figyelemhiány/Hiperaktivitás Zavar - ADHD TÁJÉKOZTATÓ FÜZET ADHD-s gyermekek családjai részére KEZELÉSI TÁJÉKOZTATÓ FÜZET Ezt a tájékoztató füzetet azért készítettük, hogy segítsünk a FIGYELEMHIÁNY/HIPERAKTIVITÁS
BIOLÓGIA HÁZIVERSENY 1. FORDULÓ BIOKÉMIA, GENETIKA BIOKÉMIA, GENETIKA
 BIOKÉMIA, GENETIKA 1. Nukleinsavak keresztrejtvény (12+1 p) 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 1. A nukleinsavak a.-ok összekapcsolódásával kialakuló polimerek. 2. Purinvázas szerves bázis, amely az
BIOKÉMIA, GENETIKA 1. Nukleinsavak keresztrejtvény (12+1 p) 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 1. A nukleinsavak a.-ok összekapcsolódásával kialakuló polimerek. 2. Purinvázas szerves bázis, amely az
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Human Genome Project, 1990-2005 5 évvel a tervezett befezés előtt The race is over, victory for Craig Venter. The genome is mapped* - now what?
 2000 június 26 Új út kezdete, vagy egy út vége? Human Genome Project, 1990-2005 5 évvel a tervezett befezés előtt The race is over, victory for Craig Venter. The genome is mapped* - now what? 2000 június
2000 június 26 Új út kezdete, vagy egy út vége? Human Genome Project, 1990-2005 5 évvel a tervezett befezés előtt The race is over, victory for Craig Venter. The genome is mapped* - now what? 2000 június
Példák a független öröklődésre
 GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
10. CSI. A molekuláris biológiai technikák alkalmazásai
 10. CSI. A molekuláris biológiai technikák alkalmazásai A DNS mint azonosító 3 milliárd bázispár az emberi DNS-ben (99.9%-ban azonos) 0.1%-nyi különbség elegendő az egyedek megkülönböztetéséhez Genetikai
10. CSI. A molekuláris biológiai technikák alkalmazásai A DNS mint azonosító 3 milliárd bázispár az emberi DNS-ben (99.9%-ban azonos) 0.1%-nyi különbség elegendő az egyedek megkülönböztetéséhez Genetikai
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós
 A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós Összefoglalás A humángenetika korunk egyik legdinamikusabban fejlődő tudományága. Ennek a fejlődésnek legfőbb mozgatórugója az, hogy a humángenetika,
A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós Összefoglalás A humángenetika korunk egyik legdinamikusabban fejlődő tudományága. Ennek a fejlődésnek legfőbb mozgatórugója az, hogy a humángenetika,
Recesszív öröklődés. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 Recesszív öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
12 Recesszív öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
Genetika 3 ea. Bevezetés
 Genetika 3 ea. Mendel törvényeinek a kiegészítése: Egygénes öröklődés Többtényezős öröklődés Bevezetés Mendel által vizsgált tulajdonságok: diszkrétek, két különböző fenotípus Humán tulajdonságok nagy
Genetika 3 ea. Mendel törvényeinek a kiegészítése: Egygénes öröklődés Többtényezős öröklődés Bevezetés Mendel által vizsgált tulajdonságok: diszkrétek, két különböző fenotípus Humán tulajdonságok nagy
Domináns-recesszív öröklődésmenet
 Domináns-recesszív öröklődésmenet Domináns recesszív öröklődés esetén tehát a homozigóta domináns és a heterozigóta egyedek fenotípusa megegyezik, így a három lehetséges genotípushoz (példánkban AA, Aa,
Domináns-recesszív öröklődésmenet Domináns recesszív öröklődés esetén tehát a homozigóta domináns és a heterozigóta egyedek fenotípusa megegyezik, így a három lehetséges genotípushoz (példánkban AA, Aa,
A függőség pszichogenetikája 2013.11.26
 A függőség pszichogenetikája 2013.11.26 A függőség pszichogenetikája Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció
A függőség pszichogenetikája 2013.11.26 A függőség pszichogenetikája Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció
Az agy betegségeinek molekuláris biológiája. 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5.
 Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
A DOPAMIN D4-ES RECEPTOR GÉNVARIÁNSOK VIZSGÁLATA FIGYELEMHIÁNYOS HIPERAKTIVITÁSI ZAVARBAN
 A DOPAMIN D4-ES RECEPTOR GÉNVARIÁNSOK VIZSGÁLATA FIGYELEMHIÁNYOS HIPERAKTIVITÁSI ZAVARBAN Kereszturi Éva 1, Király Orsolya 1, Csapó Zsolt 1, Tárnok Zsanett 2, Gádoros Júlia 2, Sasvári-Székely Mária 1 és
A DOPAMIN D4-ES RECEPTOR GÉNVARIÁNSOK VIZSGÁLATA FIGYELEMHIÁNYOS HIPERAKTIVITÁSI ZAVARBAN Kereszturi Éva 1, Király Orsolya 1, Csapó Zsolt 1, Tárnok Zsanett 2, Gádoros Júlia 2, Sasvári-Székely Mária 1 és
HABILITÁCIÓS PÁLYÁZAT. Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai" című habilitációs dolgozat
 HABILITÁCIÓS PÁLYÁZAT Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai" című habilitációs dolgozat T É Z I S E I Veres-Székely Anna, Ph.D. 2010 BEVEZETÉS Napjainkban
HABILITÁCIÓS PÁLYÁZAT Temperamentum, kognitív teljesítmény és hipnábilitás pszichogenetikai asszociációvizsgálatai" című habilitációs dolgozat T É Z I S E I Veres-Székely Anna, Ph.D. 2010 BEVEZETÉS Napjainkban
A függőség pszichogenetikája
 A függőség pszichogenetikája A függőség pszichogenetikája Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció Hétköznapi
A függőség pszichogenetikája A függőség pszichogenetikája Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció Hétköznapi
Genetikai vizsgálatok
 Genetikai vizsgálatok Családvizsgálatok Bottom-up Top-down Ikertanulmányok Adoptációs vizsgálatok Molekuláris genetikai vizsgálatok 1 Depresszió-Családvizsgálatok Bottom-up tanulmányok (MDD-s gyermek proband
Genetikai vizsgálatok Családvizsgálatok Bottom-up Top-down Ikertanulmányok Adoptációs vizsgálatok Molekuláris genetikai vizsgálatok 1 Depresszió-Családvizsgálatok Bottom-up tanulmányok (MDD-s gyermek proband
Diagnosztikai célú molekuláris biológiai vizsgálatok
 Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
A függőség fajtái 1. A függőség fajtái 2.
 A függőség pszichogenetikája A függőség pszichogenetikája 2013.11.26 Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció
A függőség pszichogenetikája A függőség pszichogenetikája 2013.11.26 Addikciók fenotípusos vonatkozásai Addikciók genetikai vonatkozásai E kettő közötti asszociációk Függőség, szenvedélybetegség, addikció
Az addikció molekuláris neurobiológiája. Barta Csaba
 Az addikció molekuláris neurobiológiája Barta Csaba Komplex jelleg: A szerfüggés etiológiája genetikai faktorok + környezeti tényezők és interakcióik családi halmozódás (Rounsaville, 1991; Luthar, 1992;
Az addikció molekuláris neurobiológiája Barta Csaba Komplex jelleg: A szerfüggés etiológiája genetikai faktorok + környezeti tényezők és interakcióik családi halmozódás (Rounsaville, 1991; Luthar, 1992;
Animal welfare, etológia és tartástechnológia
 Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 660 AZ AKTIVITÁS GENETIKAI HÁTTERÉNEK VIZSGÁLATA KANDIDÁNS GÉNMÓDSZERREL
Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 660 AZ AKTIVITÁS GENETIKAI HÁTTERÉNEK VIZSGÁLATA KANDIDÁNS GÉNMÓDSZERREL
Orvosi Genomtudomány 2014 Medical Genomics 2014. Április 8 Május 22 8th April 22nd May
 Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Orvosi Genomtudomány 2014 Medical Genomics 2014 Április 8 Május 22 8th April 22nd May Hét / 1st week (9. kalendariumi het) Takács László / Fehér Zsigmond Magyar kurzus Datum/ido Ápr. 8 Apr. 9 10:00 10:45
Tartalomjegyzék TARTALOMJEGYZÉK
 Tartalomjegyzék TARTALOMJEGYZÉK Tartalomjegyzék... 1 Rövidítések jegyzéke... 3 Ábrák és táblázatok jegyzéke... 5 Ábrák... 5 Táblázatok... 5 Bevezetés... 6 Irodalmi háttér... 8 Komplex öröklõdésû jellegek
Tartalomjegyzék TARTALOMJEGYZÉK Tartalomjegyzék... 1 Rövidítések jegyzéke... 3 Ábrák és táblázatok jegyzéke... 5 Ábrák... 5 Táblázatok... 5 Bevezetés... 6 Irodalmi háttér... 8 Komplex öröklõdésû jellegek
A PET szerepe a gyógyszerfejlesztésben. Berecz Roland DE KK Pszichiátriai Tanszék
 A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
A PET szerepe a gyógyszerfejlesztésben Berecz Roland DE KK Pszichiátriai Tanszék Gyógyszerfejlesztés Felfedezés gyógyszertár : 10-15 év Kb. 1 millárd USD/gyógyszer (beleszámolva a sikertelen fejlesztéseket)
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
OTKA K 81466, témavezető: Dr. Sasvári Mária.
 PROJEKT ZÁRÓ BESZÁMOLÓ A pályázati munkatervben a 4 éves futamidőre összesen 10 részfeladatot terveztünk, ezeket a feladatokat teljesítettük, és a kapott eredményeket nemzetközi folyóiratokban publikáltuk,
PROJEKT ZÁRÓ BESZÁMOLÓ A pályázati munkatervben a 4 éves futamidőre összesen 10 részfeladatot terveztünk, ezeket a feladatokat teljesítettük, és a kapott eredményeket nemzetközi folyóiratokban publikáltuk,
Szakmai zárójelentés A kutyaszemélyiség mint az emberi személyiségvizsgálatok modellje: etológiai, pszichológiai és genetikai megközelítés
 Szakmai zárójelentés A kutyaszemélyiség mint az emberi személyiségvizsgálatok modellje: etológiai, pszichológiai és genetikai megközelítés Bevezetés Korábbi támogatott pályázatok etológiai kutatatásai
Szakmai zárójelentés A kutyaszemélyiség mint az emberi személyiségvizsgálatok modellje: etológiai, pszichológiai és genetikai megközelítés Bevezetés Korábbi támogatott pályázatok etológiai kutatatásai
Human genome project
 Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
PrenaTest Újgenerációs szekvenálást és z-score
 PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
++ mm. +m +m +m +m. Hh,fF Hh,fF hh,ff hh,ff. ff Ff. Hh hh. ff ff ff ff. Hh Hh hh hh
 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
Kognitív teljesítménymutatók pszichogenetikai vizsgálata
 Kognitív teljesítménymutatók pszichogenetikai vizsgálata Absztrakt A kognitív képességek örökletessége ikervizsgálatok és genom-analízissel végzett kutatások tanúsága szerint jelentős (Butcher és mtsai,
Kognitív teljesítménymutatók pszichogenetikai vizsgálata Absztrakt A kognitív képességek örökletessége ikervizsgálatok és genom-analízissel végzett kutatások tanúsága szerint jelentős (Butcher és mtsai,
A Hardy Weinberg-modell gyakorlati alkalmazása
 1 of 6 5/16/2009 2:59 PM A Hardy Weinberg-modell gyakorlati alkalmazása A genotípus-gyakoriság megoszlásának vizsgálata 1. ábra. A Hardy Weinberg-egyensúlyi genotípus-gyakoriságok az allélgyakoriság Számos
1 of 6 5/16/2009 2:59 PM A Hardy Weinberg-modell gyakorlati alkalmazása A genotípus-gyakoriság megoszlásának vizsgálata 1. ábra. A Hardy Weinberg-egyensúlyi genotípus-gyakoriságok az allélgyakoriság Számos
A replikáció mechanizmusa
 Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
Téma 2: Genetikai alapelvek, a monogénes öröklődés -hez szakirodalom: (Plomin: Viselekedésgenetika 2. fejezet) *
 Téma 2: Genetikai alapelvek, a monogénes öröklődés -hez szakirodalom: (Plomin: Viselekedésgenetika 2. fejezet) * A mendeli öröklődés törvényei A Huntington-kór (HD) kezdetét személyiségbeli változások,
Téma 2: Genetikai alapelvek, a monogénes öröklődés -hez szakirodalom: (Plomin: Viselekedésgenetika 2. fejezet) * A mendeli öröklődés törvényei A Huntington-kór (HD) kezdetét személyiségbeli változások,
A (human)genetika alapja
 A (human)genetika alapja Genom diagnosztika - születés elött - tünetek megjelenése elött - hordozó diagnosztika Prenatalis genetikai diagnosztika indikációi emelkedett valószinüség egy gén betegségre egyik
A (human)genetika alapja Genom diagnosztika - születés elött - tünetek megjelenése elött - hordozó diagnosztika Prenatalis genetikai diagnosztika indikációi emelkedett valószinüség egy gén betegségre egyik
A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor,
 1 A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor, (Debreceni Egyetem Állattenyésztéstani Tanszék) A bármilyen
1 A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor, (Debreceni Egyetem Állattenyésztéstani Tanszék) A bármilyen
ISMÉTLDÉSI POLIMORFIZMUSOK A KUTYA DOPAMINERG GÉNJEIBEN
 ISMÉTLDÉSI POLIMORFIZMUSOK A KUTYA DOPAMINERG GÉNJEIBEN Biológia Doktori Iskola Vezet: Prof. Erdei Anna Doktori tézisek Héjjas Krisztina Eötvös Loránd Tudományegyetem Szerkezeti Biokémia Doktori Program
ISMÉTLDÉSI POLIMORFIZMUSOK A KUTYA DOPAMINERG GÉNJEIBEN Biológia Doktori Iskola Vezet: Prof. Erdei Anna Doktori tézisek Héjjas Krisztina Eötvös Loránd Tudományegyetem Szerkezeti Biokémia Doktori Program
A domináns öröklődés. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 A domináns öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
12 A domináns öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban
 BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
BEVEZETÉS ÉS A KUTATÁS CÉLJA A zsírszövet mellett az agyvelő lipidekben leggazdagabb szervünk. Pontosabban az agy igen gazdag hosszú szénláncú politelítetlen zsírsavakban (LCPUFA), mint az arachidonsav
Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak.
 Evolúció Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak. Latin eredetű szó, jelentése: kibontakozás Időben egymást
Evolúció Az evolúció folyamatos változások olyan sorozata, melynek során bizonyos populációk öröklődő jellegei nemzedékről nemzedékre változnak. Latin eredetű szó, jelentése: kibontakozás Időben egymást
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM
 INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
Szakmai beszámoló (időközi beszámoló: )
 Szakmai beszámoló (időközi beszámoló: 2012.02.01 2013.01.31) OTKA K-100845 Zsűri: PSP, futamidő: 48 hónap (2012.02.01 2016.01.31) Kutatásban résztvevők azonosak-e a szerződésben szereplő kutatókkal? NEM
Szakmai beszámoló (időközi beszámoló: 2012.02.01 2013.01.31) OTKA K-100845 Zsűri: PSP, futamidő: 48 hónap (2012.02.01 2016.01.31) Kutatásban résztvevők azonosak-e a szerződésben szereplő kutatókkal? NEM
I. A sejttől a génekig
 Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Gén kópiaszám és mikrorns kötőhely polimorfizmusok vizsgálata
 Gén kópiaszám és mikrorns kötőhely polimorfizmusok vizsgálata Doktori tézisek Dr. Kovács-Nagy Réka Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető: Dr. Rónai Zsolt egyetemi adjunktus,
Gén kópiaszám és mikrorns kötőhely polimorfizmusok vizsgálata Doktori tézisek Dr. Kovács-Nagy Réka Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető: Dr. Rónai Zsolt egyetemi adjunktus,
A metabolikus szindróma genetikai háttere. Kappelmayer János, Balogh István (www.kbmpi.hu)
 A metabolikus szindróma genetikai háttere Kappelmayer János, Balogh István (www.kbmpi.hu) Definíció WHO, 1999 EGIR, 1999 ATP III, 2001 Ha három vagy több komponens jelen van a betegben: Vérnyomás: > 135/85
A metabolikus szindróma genetikai háttere Kappelmayer János, Balogh István (www.kbmpi.hu) Definíció WHO, 1999 EGIR, 1999 ATP III, 2001 Ha három vagy több komponens jelen van a betegben: Vérnyomás: > 135/85
ELŐADÁS VÁZLAT. Balázs Judit
 ELŐADÁS VÁZLAT GYERMEKKORBAN KEZDŐDŐ FELNŐTT PSZICHIÁTRIAI KÓRKÉPEK: AUTIZMUS, ADHD, TIC-ZAVAR Balázs Judit 2012. november 15-17. SEMMELWEIS EGYETEM, KÖTELEZŐ SZINTEN TARTÓ TANFOLYAM AUTIZMUS FOGALMI SOKASÁG
ELŐADÁS VÁZLAT GYERMEKKORBAN KEZDŐDŐ FELNŐTT PSZICHIÁTRIAI KÓRKÉPEK: AUTIZMUS, ADHD, TIC-ZAVAR Balázs Judit 2012. november 15-17. SEMMELWEIS EGYETEM, KÖTELEZŐ SZINTEN TARTÓ TANFOLYAM AUTIZMUS FOGALMI SOKASÁG
Szakmai beszámoló (időközi beszámoló: 2014-02-01-2015-01-31)
 Szakmai beszámoló (időközi beszámoló: 2014-02-01-2015-01-31) OTKA K-100845 Zsűri: PSP, futamidő: 48 hónap (2012.02.01 2016.01.31) Kutatásban résztvevők azonosak-e a szerződésben szereplő kutatókkal? NEM
Szakmai beszámoló (időközi beszámoló: 2014-02-01-2015-01-31) OTKA K-100845 Zsűri: PSP, futamidő: 48 hónap (2012.02.01 2016.01.31) Kutatásban résztvevők azonosak-e a szerződésben szereplő kutatókkal? NEM
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Zárójelentés. A D4-es dopamin receptor gén 5 régiójának haplotípus szerkezete: molekuláris és pszichiátriai vonatkozások (2003 2006) F042730
 Zárójelentés A D4-es dopamin receptor gén 5 régiójának haplotípus szerkezete: molekuláris és pszichiátriai vonatkozások (2003 2006) F042730 Betegségeink kialakításában két f etiológiai faktor, a környezeti
Zárójelentés A D4-es dopamin receptor gén 5 régiójának haplotípus szerkezete: molekuláris és pszichiátriai vonatkozások (2003 2006) F042730 Betegségeink kialakításában két f etiológiai faktor, a környezeti
10. Genomika 2. Microarrayek és típusaik
 10. Genomika 2. 1. Microarray technikák és bioinformatikai vonatkozásaik Microarrayek és típusaik Korrelált génexpresszió mint a funkcionális genomika eszköze 2. Kombinált megközelítés a funkcionális genomikában
10. Genomika 2. 1. Microarray technikák és bioinformatikai vonatkozásaik Microarrayek és típusaik Korrelált génexpresszió mint a funkcionális genomika eszköze 2. Kombinált megközelítés a funkcionális genomikában
Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems)
 Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems) Christina Schwenck, Angelika Gensthaler Marcel Romanos Christine M. Freitag, Wolfgang Schneider, Regina
Az érzelmi felismerés viselkedészavaros lányokban (Emotion recognition in girls with conduct problems) Christina Schwenck, Angelika Gensthaler Marcel Romanos Christine M. Freitag, Wolfgang Schneider, Regina
Biológiai feladatbank 12. évfolyam
 Biológiai feladatbank 12. évfolyam A pedagógus neve: A pedagógus szakja: Az iskola neve: Műveltségi terület: Tantárgy: A tantárgy cél és feladatrendszere: Tantárgyi kapcsolatok: Osztály: 12. Felhasznált
Biológiai feladatbank 12. évfolyam A pedagógus neve: A pedagógus szakja: Az iskola neve: Műveltségi terület: Tantárgy: A tantárgy cél és feladatrendszere: Tantárgyi kapcsolatok: Osztály: 12. Felhasznált
szekely.anna@ppk.elte.hu kotyuk.eszter@ppk.elte.hu
 PSZB09-109 Veres-Székely Anna, Kótyuk Eszter és Sasvári Mária Prof. (2015 őszi félév:) szekely.anna@ppk.elte.hu kotyuk.eszter@ppk.elte.hu Fogadó óra: kedd 11-12 (Izu112) sasvari.maria@med.semmelweis-univ.hu
PSZB09-109 Veres-Székely Anna, Kótyuk Eszter és Sasvári Mária Prof. (2015 őszi félév:) szekely.anna@ppk.elte.hu kotyuk.eszter@ppk.elte.hu Fogadó óra: kedd 11-12 (Izu112) sasvari.maria@med.semmelweis-univ.hu
Genetikai vizsgálat. Intergenomialis kommunikációs zavarok (mtdns depléció/deléció jelenléte esetén javasolt) Alpers syndroma (POLG1 gén analízis)
 Genetikai vizsgálat Intergenomialis kommunikációs zavarok (mtdns depléció/deléció jelenléte esetén javasolt) Alpers syndroma (POLG1 gén analízis) SANDO (POLG1 gén analízis) TWINKLE ANT1 OPA1 SCO2 RRM2B
Genetikai vizsgálat Intergenomialis kommunikációs zavarok (mtdns depléció/deléció jelenléte esetén javasolt) Alpers syndroma (POLG1 gén analízis) SANDO (POLG1 gén analízis) TWINKLE ANT1 OPA1 SCO2 RRM2B
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
Embriószelekció PGD-vel genetikai terheltség esetén. Kónya Márton Istenhegyi Géndiagnosztika
 Embriószelekció PGD-vel genetikai terheltség esetén Kónya Márton Istenhegyi Géndiagnosztika A praeimplantatiós genetikai diagnosztika (PGD) a praenatalis diagnosztika legkorábbi formája, a beágyazódás
Embriószelekció PGD-vel genetikai terheltség esetén Kónya Márton Istenhegyi Géndiagnosztika A praeimplantatiós genetikai diagnosztika (PGD) a praenatalis diagnosztika legkorábbi formája, a beágyazódás
A DOPAMIN D4-ES RECEPTOR GÉN PROMOTER RÉGIÓJÁNAK FUNKCIONÁLIS VIZSGÁLATA
 A DOPAMIN D4-ES RECEPTOR GÉN PROMOTER RÉGIÓJÁNAK FUNKCIONÁLIS VIZSGÁLATA Doktori értekezés Kereszturi Éva Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Pathobiokémia Doktori Program Témavezető:
A DOPAMIN D4-ES RECEPTOR GÉN PROMOTER RÉGIÓJÁNAK FUNKCIONÁLIS VIZSGÁLATA Doktori értekezés Kereszturi Éva Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Pathobiokémia Doktori Program Témavezető:
CzB 2010. Élettan: a sejt
 CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
Intelligens Rendszerek Elmélete. Párhuzamos keresés genetikus algoritmusokkal
 Intelligens Rendszerek Elmélete Dr. Kutor László Párhuzamos keresés genetikus algoritmusokkal http://mobil.nik.bmf.hu/tantargyak/ire.html login: ire jelszó: IRE0 IRE / A természet általános kereső algoritmusa:
Intelligens Rendszerek Elmélete Dr. Kutor László Párhuzamos keresés genetikus algoritmusokkal http://mobil.nik.bmf.hu/tantargyak/ire.html login: ire jelszó: IRE0 IRE / A természet általános kereső algoritmusa:
Az etológia módszere és fogalmai. A Humánetológia
 Humánetológia Darwin evolúcióelmélete A fajok eredete (1859) az egyedek különböznek, és ezek a különbségek öröklődnek az egyedek versengenek A természetes kiválasztódás az a folyamat melynek során bizonyos
Humánetológia Darwin evolúcióelmélete A fajok eredete (1859) az egyedek különböznek, és ezek a különbségek öröklődnek az egyedek versengenek A természetes kiválasztódás az a folyamat melynek során bizonyos
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA NOVEMBER
 Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program
 Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program A D4 dopamin receptor és a katekol-o-metiltranszferáz gének polimorfizmusának hatása a figyelmi rendszerek működésére
Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program A D4 dopamin receptor és a katekol-o-metiltranszferáz gének polimorfizmusának hatása a figyelmi rendszerek működésére
Szelekció. Szelekció. A szelekció típusai. Az allélgyakoriságok változása 3/4/2013
 Szelekció Ok: több egyed születik, mint amennyi túlél és szaporodni képes a sikeresség mérése: fitnesz Szelekció Ok: több egyed születik, mint amennyi túlél és szaporodni képes a sikeresség mérése: fitnesz
Szelekció Ok: több egyed születik, mint amennyi túlél és szaporodni képes a sikeresség mérése: fitnesz Szelekció Ok: több egyed születik, mint amennyi túlél és szaporodni képes a sikeresség mérése: fitnesz
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
X-hez kötött öröklődés
 12 Pécsi Tudományegyetem Orvosi Genetikai Intézet H-7623 Pécs, József A.u.7. Tel.. (36)-72-535-976 Fax.: (36)-72-536-427 Honlap: www.genetics.aok.pte.hu/ Pécsi Tudományegyetem Szülészeti és Nőgyógyászati
12 Pécsi Tudományegyetem Orvosi Genetikai Intézet H-7623 Pécs, József A.u.7. Tel.. (36)-72-535-976 Fax.: (36)-72-536-427 Honlap: www.genetics.aok.pte.hu/ Pécsi Tudományegyetem Szülészeti és Nőgyógyászati
Terhesség és emlőrák genetikai szempontok. Kosztolányi György PTE Orvosi Genetikai Intézet
 erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
Populációgenetikai vizsgálatok eredményei hangulatzavarokban. Képalkotó vizsgálatok alkalmazása a neuropszichofarmakológiában
 Populációgenetikai vizsgálatok eredményei hangulatzavarokban Képalkotó vizsgálatok alkalmazása a neuropszichofarmakológiában Juhász Gabriella Semmelweis Egyetem, GYTK, Gyógyszerhatástani Intézet Neuroscience
Populációgenetikai vizsgálatok eredményei hangulatzavarokban Képalkotó vizsgálatok alkalmazása a neuropszichofarmakológiában Juhász Gabriella Semmelweis Egyetem, GYTK, Gyógyszerhatástani Intézet Neuroscience
Zárójelentés. Állati rotavírusok összehasonlító genomvizsgálata. c. OTKA kutatási programról. Bányai Krisztián (MTA ATK ÁOTI)
 Zárójelentés Állati rotavírusok összehasonlító genomvizsgálata c. OTKA kutatási programról Bányai Krisztián (MTA ATK ÁOTI) 2012 1 Az Állati rotavírusok összehasonlító genomvizsgálata c. programban azt
Zárójelentés Állati rotavírusok összehasonlító genomvizsgálata c. OTKA kutatási programról Bányai Krisztián (MTA ATK ÁOTI) 2012 1 Az Állati rotavírusok összehasonlító genomvizsgálata c. programban azt
3. Általános egészségügyi ismeretek az egyes témákhoz kapcsolódóan
 11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Kurrens, többnyire vitatott kutatási eredmények!!!
 A magatartáspszichológia kurrens vitái: aktuális kérdések a pszichogenetikában Komplex öröklődésű jellegek rizikófaktorai A személyiség Az gyermekkori kötődés, az ADHD és drogfüggőség A hipnózis iránti
A magatartáspszichológia kurrens vitái: aktuális kérdések a pszichogenetikában Komplex öröklődésű jellegek rizikófaktorai A személyiség Az gyermekkori kötődés, az ADHD és drogfüggőség A hipnózis iránti
Fogyatékossággal élő emberek életminősége és ellátási költségei különböző lakhatási formákban
 Fogyatékossággal élő emberek életminősége és ellátási költségei különböző lakhatási formákban Zárótanulmány a VP/2013/013/0057 azonosítószámú New dimension in social protection towards community based
Fogyatékossággal élő emberek életminősége és ellátási költségei különböző lakhatási formákban Zárótanulmány a VP/2013/013/0057 azonosítószámú New dimension in social protection towards community based
2006 1. Nemszinaptikus receptorok és szubmikronos Ca2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra.
 2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
Intelligencia és kognitív képességek
 Intelligencia és kognitív képességek Az intelligencia amit tudunk róla és amit nem (Neisser, 1996) A szellemi fogyatékosság genetikai alapjai Az intelligencia elméletei NEISSER, U. et al (1996) Intelligencia:
Intelligencia és kognitív képességek Az intelligencia amit tudunk róla és amit nem (Neisser, 1996) A szellemi fogyatékosság genetikai alapjai Az intelligencia elméletei NEISSER, U. et al (1996) Intelligencia:
Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK
 Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK HISTORY Antitestet találtak egy koraszülött gyermek anyjának szérumában; ez lenne felelős a gyermek haláláért?
Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK HISTORY Antitestet találtak egy koraszülött gyermek anyjának szérumában; ez lenne felelős a gyermek haláláért?
Magisztrális gyógyszerkészítés a Wilson kór terápiájában. Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4.
 Magisztrális gyógyszerkészítés a Wilson kór terápiájában Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4. A Wilson kór mérföldkövei 1912. Wilson: Progressive lenticular degeneration:
Magisztrális gyógyszerkészítés a Wilson kór terápiájában Dr. Birinyi Péter Mikszáth Gyógyszertár 1088 Budapest, Mikszáth Kálmán tér 4. A Wilson kór mérföldkövei 1912. Wilson: Progressive lenticular degeneration:
Hazai méhészeti genomikai és genetikai vizsgálatok
 AKÁCKÖRÚTON Hazai méhészeti genomikai és genetikai vizsgálatok Előző cikkünkben arról írtunk, milyen új eszköztárral rendelkezünk a XXI. században a genetikai vizsgálatok területén, és mit adhat a molekuláris
AKÁCKÖRÚTON Hazai méhészeti genomikai és genetikai vizsgálatok Előző cikkünkben arról írtunk, milyen új eszköztárral rendelkezünk a XXI. században a genetikai vizsgálatok területén, és mit adhat a molekuláris
Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program
 Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program A D4 dopamin receptor és a katekol-o-metiltranszferáz gének polimorfizmusának hatása a figyelmi rendszerek működésére
Semmelweis Egyetem, Mentális Egészségtudományok Doktori Iskola, Magatartástudományi Program A D4 dopamin receptor és a katekol-o-metiltranszferáz gének polimorfizmusának hatása a figyelmi rendszerek működésére
