Elmélet : P.W. Atkins: Fizikai kémia I.10, III, 30 fejezet ( , , ) oldal.
|
|
|
- Ábel Szabó
- 8 évvel ezelőtt
- Látták:
Átírás
1 Korróziós inhibitorok htékonyságánk vizsgált Elmélet : P.W. Atkins: iziki kémi I.10, III, 30 feezet ( , , ) oldl. Amiót z ember fémeszközöket hsznál, állndó hrcbn áll természettel. A ngy mennyiségű nyg, energi és munk ráfordításávl előállított fémeszközök ngy része megfelelő kezelés nélkül természet hívó szvánk engedelmeskedve vissztér természetes állpotáb, vgyis odálódik. A NACE (Ntionl Assocition of Corrosion Engineers) megfoglmzás szerint ózió "egy tárgy, rendszerint egy fém tönkremenetele környezettel vló kölcsönhtás mitt". Az ISO (Interntionl Orgniztion for Stndrdiztion) vslt szerint " ózió fiziki-kémii kölcsönhtás fémtárgy és környezete között, melynek révén fémtárgy tuldonsági megváltoznk. Ez kölcsönhtás fémtárgy részleges vgy teles tönkremeneteléhez vezethet". Tágbb értelemben ózió nemcsk fémből, hnem más nygból betonból, műnygból készült tárgyk környezeti htások mitt bekövetkező károsodását is elenti. Láthtó, hogy definíciók ózió negtív htását emelik ki, mi nem meglepő, figyelembe véve, hogy egyes becslések szerint évente világ fémtermelésének körülbelül 1/4-e megy veszendőbe. A közvetlen károk ( fémtárgyk időszkos vgy végleges hsználhttlnná válás illetve z ennek következtében felmerülő nyg-, energi- és munkigény) mellett közvetett károk ngyság szinte felmérhetetlen. Néhány kilyukdt vegyszeres trtály vítás csk egy úbb tétel egy válllt kidási között, míg trtályokból kiszbdult vegyi nygok áltl környezetben okozott kár pénzben sokszor ki sem feezhető. Közismert, hogy svs elektrolitok leggresszívebb óziós közegek közé trtoznk. A legtöbb fém ózióánk sebessége svs közegben igen ngy, különösen kkor, h fém felületén nem lkul ki vlmilyen védőréteg fém és óziós közeg közötti kölcsönhtás folytán keletkező óziós termékekből. A technikilg legelteredtebb széncélok ezen fémek közé trtoznk. A legtöbb iprágbn hsználnk svkt vlmilyen technológii folymtbn, például fémek mrtásár, hőcserélők tisztításár, kőoltermelő kutk ktiválásár stb. Sok esetben technológii folymt során képződik sv, például hidrolízis révén. Miközben kihsználuk svs közeg előnyeit, gondoskodni kell ozív htás megszüntetéséről vgy csökkentéséről. A fémek ózióát többféle módon is megszüntethetük. Vlmilyen védőbevont lklmzásávl fizikilg lehetetlenné tehetük fém és ozív közeg érintkezését, ez zonbn védőbevont megsérülésekor fém vgy bevont hsználhttlnná válásához vezethet. Elektrokémii módszerekkel nódos vgy któdos védelemmel termodinmikilg vgy kinetikilg gátolhtuk ózió végbemenetelét. Ezen módszerek hátrány z energiigény. Amennyiben nem törekszünk ózió teles megszüntetésére, megfelelő módszerek lklmzás esetén minimális ráfordítássl kiváló eredményeket érhetünk el. Ilyen módszer óziós inhibitorok lklmzás. A óziós inhibitorok ozív közegbe keverve már ngyon kis koncentráció esetén is elentősen lecsökkenthetik óziós folymtok sebességét nélkül, hogy közeg gresszivitását elentősen megváltozttnák. A óziós inhibitorok többsége szerves vegyület, de kdnk közöttük szervetlen nygok is. A óziós inhibitorok lklmzásánk, felesztésének lpvető követelménye z inhibitor htásmechnizmusánk ismerete. Mivel z inhibitorok ózió lpát képező 1
2 elektrokémii folymtok kinetikáát változtták meg, htásmechnizmusukt kkor tárhtuk fel, h megismerük z elektrokémi törvényszerűségeit inhibitorok elenlétében és molekuláris szintű htásukt óziós folymtokr. E két lpvető feldt megoldásávl fogllkozik lényegében z inhibitoros ózióvédelem tudományág. A fémek ózió elektrolitoldtokbn z esetek többségében lényegét tekintve elektrokémii folymt. Bármely elektrokémii ózió sebessége lpábn véve két, fém felületén végbemenő kpcsolt rekció sebességétől függ. Az egyik z nódos rekció, melyben fémtomok ionos formábn kilépnek fémrácsból és elektronok hátrhgyásávl átlépnek z oldtb, másik któdos rekció, melyben egy redukálhtó komponens (pl. oxigénmentes, svs közegben H + -ion) felveszi z nódos rekcióbn keletkezett elektronokt: M M n+ + n e - n e - +n H + n/2 H 2 Az inhibitorok záltl képesek megváltozttni ózió sebességét, hogy módosíták ózió nódos, któdos vgy mindkét részfolymtánk sebességét. Ezt körülményt figyelembe véve Evns z inhibitorok három csoportát különböztette meg: nódos, któdos és vegyes inhibitorokt. Svs elektrolitokbn elsősorbn szerves inhibitorokt lklmzzák. A szerves inhibitorok htásmechnizmusábn ngy elentősége vn z dszorpciónk és nnk, hogy ez milyen htássl vn któdos rekciór. Svs elektrolitokbn ugynis elentősen csökkenthető z oldódás sebessége, h lecsökkentük hidrogénionok vgy más depolrizátorok redukcióánk sebességét. Gykrn megfigyelhető zonbn, hogy egyes inhibitorok htnk z nódos rekciór is. A vs oxigénmentes svs közegben végbemenő ózió során leátszódó két félrekció Anód (B) e 2+ (q) + 2e e(s) E Ο 0,44 V Któd (J) 2 H + (q) + 2e H 2 (g) E Ο 0 V Bruttó (J B) e (s) + 2 H + (q) e 2+ + H 2(g) egy egy cellrekcióként foghtó fel. Az ezekre felírhtó Butler Volmer (Erdey Gruz Volmer) egyenletek, például oxigénmentes, svs közegben hidrogén redukcióár : 0 ' 0 e ' e (1 α ) η (1 α ') η e α η e α ' η (1). A óziós folymtbn egyensúlyi állpotról nem beszélhetünk, mivel mrdndó változás - nevezetesen fém oldódás és pl. hidrogénionok 2 1. ábr. Egyensúlyi folymt polrizációs görbée
3 redukció átszódik le és ez megfelelő körülmények között z időben állndó, stcionárius potenciál kilkulását eredményezi. Ezt nevezzük óziós potenciálnk ( Φk ), mi h elég távol vn mindkét elektród egyensúlyi potenciálától ( Φ e ), kkor fém redukció és H 2 oxidáció elhnygolhtóvá válik, ezért : k e 0 ' 0 e (1 α ) ( Φ Φ e ) ' z α ( Φ ' Φ e ) (2) H rekciók zonos felületeken átszódnk le, kkor óziós potenciálon kilkuló ármsűrűségekre igz: k,.(3) H z elektródokt polrizáluk (E Φ Φ potenciálr), kkor z 1. egyenlethez hsonló összefüggés vezethető le mért ármr: e ( 1 α ) E α ' E e Ngy nódos polrizáció esetén któdos árm ngyon kicsi, így második exponenciális tg elhnygolhtóvá válik. Tízes lpú logritmusr áttérve z állndókt összevonv Tfel áltl hidrogén túlfeszültség vizsgáltkor megállpított összefüggéshez utunk : E ln (1 α ) 4 + ln (1 ) 2. ábr. Korróziós folymt polrizációs görbée 3. ábr. Mért polrizációs görbe. + b lg Az előbbiekhez hsonlón któdos Tfel meredekséget (b k, ) pedig z nódos tg elhnygolásávl htározhtuk meg: Az E lg görbéklineáris szkszink meredekségei (Tfel egyenesek) b t, illetve b k t szolgáltták. E ln α H Tfel egyeneseket extrpoláluk óziós potenciálr, kkor óziós árm kiszámíthtó z előző két összefüggés lpán. H: E0; kkor (7) Deriváluk polrizációs ármr vontkozó egyenletet E szerint: + ln ' 3 ' + b ' lg
4 E (1 α ) e ( 1 α ) E ' z + α ' e α ' E Ennek z értéke z E 0 helyen z ún. polrizációs ellenállás: E E 0 (1 α ) + α ' 1 Rp Amit Tfel meredekségekkel is felírhtunk és kkor következő, Stern Gery áltl vsolt egyenletet kpuk: Rp 1 b b 2.303( b k + b k Amiből óziós ármsűrűség szintén 4. ábr. Polrizációs ellenállás görbe. kiszámíthtó polrizációs görbék felvétele után. Mivel ugynzon z elektród felületen átszódnk le z oxidációs és redukciós folymtok, ezért α', α, de, z feltétel nem biztos, hogy telesül. Ahhoz, hogy z elektródon egy folymt vlmilyen iránybn mérhető sebességgel menen végbe, z elektródpotenciálnk el kell térnie nyuglmi értéktől, polrizálni kell. A polrizációs görbék felvételéhez külső ármforrást hsználunk és ennek segítségével polrizáluk z elektródot, miközben mérük potenciálát egy másik, összehsonlító elektródhoz viszonyítv, mi áltlábn egy nehezen polrizálhtó, másodfú elektród. Ahhoz, hogy z elektrolitoldtbn z ohmikus potenciálesést minimálisr csökkentsük, referenselektródot Luggin kpillárisb helyezzük, minek vége munkelektród közvetlen közelében vn. A polrizáció megvlósításához egy segédelektródr (ellenelektródr) is szükség vn, ez áltlábn egy indifferens (pl. pltin) elektród. A polrizációs görbéket szttikus körülmények között szokás felvenni, ez zt elenti, hogy megváruk míg polrizáció htásár stcionárius állpot lkul ki rendszerben. H potenciált trtuk állndó értéken, kkor potencioszttikus mérésről, h z ármot, kkor glvnoszttikus mérésről beszélünk. A megfelelő vezérlést potenciosztáttl illetve glvnosztáttl végezzük. A potenciosztát állndó értékű polrizációt biztosít referens elektródhoz viszonyítv. A műszer legtöbbször úgy vn kilkítv, hogy glvnosztátként is hsználhtó, ekkor állndó erősségű ármot kényszerít át munk és segédelektród között. 4
5 Korróziós inhibitorok Azon nygokt, melyeket kis mennyiségben ozív közegbe dgolv csökkentik fém ózióánk sebességét, óziós inhibítoroknk nevezzük. Az inhibítorok htásosságát százlékos védőképességgel (I%) szokás kifeezni, melyet z lábbi összefüggéssel definiálunk:, I I% 100 hol és,i z dott közegben mért óziós ármsűrüség inhibítor nélkül és inhibítor elenlétében. Inhibítorhtást egymástól lényegesen eltérő típúsú és sátságú nygok is kifethetnek, és ennek megfelelően z inhibítorhtás mechnizmus is igen változtos lehet. Az inhibítorok legelentősebb csoportát z ún. dszorpciós inhibítorok képezik. Ezek áltlábn nitrogén, kén, oxigén trtlmú szerves vegyületek, melyek záltl fetik ki htásukt, hogy dszorpcióuk következtében blokkolák fémfelület ktív helyeit és így gátolák z nódos vgy któdos, esetleg mindkét folymt leátszódását. A óziós inhibítorok egy másik elentős csoportánál védőhtás zzl értelmezhető, hogy zok felületen védőfilmet (pl. polimerfilm) képeznek, mely csökkenti, vgy meggátol z gresszív közegnek fémfelülethez vló utását. A semlegeshez közeli ph ú vizes oldtokbn gykrn lklmznk olyn inhibitorokt, melyek védendő fém pssziválódását eredményezik (pl. kromátok, nitritek, stb.). Az inhibítorok ózió részfolymtir gykorolt htásuk folytán megváltoztták polrizációs görbék menetét. Ezt tényt felhsználhtuk z inhibitor htékonyságánk elektrokémii polrizációs módszerrel történő gyors meghtározásár. Az egyes inhibitorok típusuktól, htásmechnizmusuktól függően eltérő módon befolyásolák z árm feszültség (polrizációs) görbék lefutását. A vizsgáltok, ill. z értékelés szempontából zok z esetek kedvezőbbek, mikor inhibitor elenlétében is érvényes Tfel egyenlet, vgyis leglább z egyik részfolymtbn z átlépési rekció sebességmeghtározó. A gykorlt kivitelezése Az inhibítorok tnulmányozásához polrizációs görbéket glvnoszttikus körülmények között vesszük fel svs közegben. A polrizációt potenciosztát glvnoszttikus üzemmódábn vlósítuk meg, mely vizsgálndó (W) és segédelektród (A) között átfolyó ármot utomtikusn állndó értéken trt. A potenciosztát vezérlését (z ármerősség kívánt értékre történő beállítását, ill. változttását), mért (nlóg digitál átlkítóvl digitlizált) potenciál- árm értékpárok gyütését és z dtok feldolgozását személyi számítógépre írt progrm segítségével végezzük. 5
6 A mérőműszer 5. ábr. Az E 419 potenciosztát előlp Az ábr elölései: 1 Cstlkozóhelyek z elektródák bekötéséhez. 2 Cstlkozás külső mérőműszerekhez, pl. AD DA átlkítóhoz. 3 Kielző műszer z méréshtárváltó, b előelváltó c árm feszültségváltó kpcsolóvl. 4 Műszer üzemmód kpcsoló. 5 Ármmérő méréshtárváltó. 6 Kézi progrmfeszültség beállító potenciométer htárérték kpcsolóvl 7 A cell bekötésének ellenőrzésére szolgáló nyomógomb. 8 Potenciosztát glvnosztát átkpcsoló. 9 Hálózti kpcsoló. A műszeren tlálhtó egy nyomógomb (7: U R CONTROL), ennek segítségével zt ellenőrizhetük, hogy munk és referencielktród ármkörében vn e szkdás. A potenciosztátnk három üzemmód vn, z egyik DUMMY CELL, mikor műszerbe épített elektronikus műcell helyettesíti vizsgált elektrokémii mérőcellát. Ebben z üzemmódbn lehetőség vn pontos vezérlőfeszültség beállításár cell túlterhelése nélkül. Az O állásbn segédelektród ki vn kpcsolv z ármkörből, ilyenkor cell gykorltilg ármmentes állpotbn vn, ebben z állásbn mérhető meg nyuglmi potenciál. A cell polrizációát ON állásbn kell végezni, ekkor mindhárom elektród rá vn kötve műszer vezérlőármkörére. A referencielektród nódként vn bekötve, így mért elektromotoros erő negtív előelű lesz mérések többségében. 6
7 Mérés A mérőcell előkészítése Az inhibítor htékonyságánk megállpításához két mérést kell végezni; z elsőt z inhibítor trtlmú oldtbn, másodikt lpoldtbn végezzük el. A mérésekhez először 250 cm 3, dott összetételű oldtot készítünk. Alpoldtként HCl-oldtot hsználunk (3-10%; 1-2M), melyből megfelelő koncentrációú 100 cm 3 térfogtú (1-30 mmol dm 3 ) inhibítort trtlmzó oldtot is elkészítük. Az inhibitor bemérését célszerű tömegméréssel végezni. A gykorltvezető áltl megdott fémmintát előkészítük; felületét nedves, vízálló csiszolóppírrl fényesre csiszoluk, tolómérővel megmérük geometrii méreteit, miből felületét kiszámoluk. Acetonnl zsírtlnítuk és ktiválás célából 6. ábr. Mérőcell 30 másodpercre kb. 18% os (1:1 rányú) sósvoldtb mártuk, desztillált vízzel leöblitük és z elektródot celláb helyezzük. A celláb és Luggin-kpillárisb beletöltük z elektrolitoldtot. Az összehsonlító elektródot, mi célszerűen telített, vgy 1M klomelelektród ól zárón Lugginkpillárisb illesztük, ügyelve rr, hogy z oldt ne folyon ki és kpillárisbn ne legyen légbuborék. A pltin ellenelektród behelyezése után z elektródokt potenciosztát megfelelő kivezetéseihez cstlkozttuk: W munkelektród, vizsgálndó fémmint, R referenselektród, A (C) segédelektród. A készülék bekpcsolás: - eszültség lá helyezzük hálózti elosztót és bekpcsoluk. - A potenciosztátot bekpcsolás előtt ellenőrizzük DUMMY állásb állítuk; főkpcsolóát "ON" állásb kpcsolv mérőberendezést üzembe helyezzük. A készülékek bekpcsolás után z üzemmódkpcsoló O állásábn U R CONTROL gomb lenyomásávl ellenőrizzük, hogy cell szkdásmentes-e. A nyuglmi potenciálnk számottevően nem szbd változni gomb benyomáskor! H 30 mv nál ngyobb eltérést tpsztlunk mérőműszeren gomb nyomv trtáskor nyuglmi állpothoz képest, kkor z elektródák nincsenek rendesen bekötve, munkelektród és referencielektród között szkdt z ármkör, úr át kell vizsgálni cstlkozásokt és Luggin kpilláris feltöltését. 1. Nyuglmi potenciál mérés. A potenciosztátot O állásb kpcsoluk nyuglmi (óziós) potenciál méréséhez. H nyuglmi potenciál változás már elhnygolhtó (z elektródnk celláb történt behelyezését követően kb perc után), leolvssuk mért potenciál értékét és felegyezzük 7
8 egyzőkönyvbe. Után potenciosztátot kpcsoluk GALV. glvnosztát, z üzemmódkpcsolót pedig ON állásb. 2. Któdos polrizáció A méréshez állítsuk be következő polrizációs ármokt, ttól függően, hogy dekádonként (ngyságrendenként) hány mérést kér z okttó: Mérés Mivel mérést több ngyságrendben kell elvégezni dekádonként értelemszerűen következő ngyságrendben megdott érték 10-szerese (100-szoros, stb.) lesz beállítndó ármérték Ngyságrend váltáskor (ármmérő méréshtár) glvnosztátot váltsuk át DUMMY állásb, vgy váltás előtt állítsuk be körülbelüli következő ármértéket! Ne feletsük el visszváltni SZTÁT-ot ON állásb, pontos ármérték beállításához. A polrizációt ddig folytssuk, míg potenciál nyuglmi értéktől kb. 300 mv-l különbözik. Mindig váruk meg stcioner állpot kilkulását, zz leglább 3 perc várkozás után olvssuk le potenciál értékeket mérőműszerről. 3. Nyuglmi potenciál mérés. A któdos polrizáció után úbb, mx. fél órás nyuglmi potenciál mérés következik, ehhez ugyncsk O állásb kell kpcsolnunk potenciosztátot. 4. Anódos polrizáció percnyi nyuglmi potenciál mérés után z nódos polrizációt ismét ON állásbn végezzük el, hsonlón któdos polrizációhoz. A méréseket z inhibitor nélküli oldtbn is hsonló módon végezzük el Kiértékelés A gykorlt elvégzése közben, vgy után meg kell htározni: z oldtok összetételét bemérések/titrálás lpán, óziós (nyuglmi) potenciált és polrizációs ellenállást, któdos és nódos Tfel meredekségeket, óziós ármsűrűségeket és z inhibitor htékonyságát 1. A óziós potenciál (E ) meghtározásához któdos illetve nódos polrizációs görbe kezdeti szkszát rzoluk fel (E i grfikon) lineáris léptékekben (mx. "50 mv polrizáció). A kpott egyenes meredeksége polrizációs ellenállás R p, tengelymetszet óziós potenciál, mit át kell számítni stndrd hidrogénelektród potenciálár! 8
9 2. A Tfel meredekség (b c, b ) számításához z E-lg(i) vgy E ln(i) görbe meredekségét htározzuk meg. 3.. A óziós árm (i ) értékeit először Tfel egyenesek és óziós potenciálok metszéspontából számoluk ki, md felület ismeretében meghtározzuk óziós ármsűrűségeket ( ) is. 3.b. A óziós ármsűrűséget ( ), meghtározzuk polrizációs ellenállásokból is. 4. A óziósebességet megduk mm/év, illetve g/m 2 /év mértékegységben is! (Mr55,85; ρ7,85g/cm 3 ) 5. Az inhibitor htékonyságát óziós ármsűrűségek felhsználásávl számítuk ki. Tábláztosn duk meg z eredményeket sósvs lpoldtr és z inhibítort trtlmzó oldtr is: 9
Elektrokémia 05. Elektródreakciók kinetikája. Láng Győző. Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem Budapest
 Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W G v,,, G v,,, z ϕ αzf G G, ( ) ϕ zf α G G 1, ϕ αzf G
Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W G v,,, G v,,, z ϕ αzf G G, ( ) ϕ zf α G G 1, ϕ αzf G
Elektrokémia 05. Elektródreakciók kinetikája. Láng Győző. Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
 Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W ,, G G v,, v, z, G G, αzf F ϕ, G G 1 ( α ) zf ϕ zf,,
Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W ,, G G v,, v, z, G G, αzf F ϕ, G G 1 ( α ) zf ϕ zf,,
Ellenállás mérés hídmódszerrel
 1. Lbortóriumi gykorlt Ellenállás mérés hídmódszerrel 1. A gykorlt célkitűzései A Whestone-híd felépítésének tnulmányozás, ellenállások mérése 10-10 5 trtománybn, híd érzékenységének meghtározás, vlmint
1. Lbortóriumi gykorlt Ellenállás mérés hídmódszerrel 1. A gykorlt célkitűzései A Whestone-híd felépítésének tnulmányozás, ellenállások mérése 10-10 5 trtománybn, híd érzékenységének meghtározás, vlmint
REÁLIS GÁZOK ÁLLAPOTEGYENLETEI FENOMENOLOGIKUS KÖZELÍTÉS
 REÁLIS GÁZOK ÁLLAPOEGYENLEEI FENOMENOLOGIKUS KÖZELÍÉS Száos odell gondoljunk potenciálo! F eltérés z ideális gáz odelljétl: éret és kölcsönhtás Moszkópikus következény: száos állpotegyenlet (ld. RM-jegyzet
REÁLIS GÁZOK ÁLLAPOEGYENLEEI FENOMENOLOGIKUS KÖZELÍÉS Száos odell gondoljunk potenciálo! F eltérés z ideális gáz odelljétl: éret és kölcsönhtás Moszkópikus következény: száos állpotegyenlet (ld. RM-jegyzet
Törésmechanika. Statikus törésmechanikai vizsgálatok
 Törésmechnik (Gykorlti segédlet) A C törési szívósság meghtározás Sttikus törésmechniki vizsgáltok A vizsgáltokt áltlábn z 1. és. ábrán láthtó úgynevezett háromontos hjlító (TPB) illetve CT róbtesteken
Törésmechnik (Gykorlti segédlet) A C törési szívósság meghtározás Sttikus törésmechniki vizsgáltok A vizsgáltokt áltlábn z 1. és. ábrán láthtó úgynevezett háromontos hjlító (TPB) illetve CT róbtesteken
KORRÓZIÓS ÁRAM MÉRÉSE FÉM KORRÓZIÓSEBESSÉGÉNEK MEGHATÁROZÁSA KORRÓZIÓS ÁRAM MÉRÉSE ALAPJÁN
 7. Laboratóriumi gyakorlat KORRÓZIÓS ÁRAM MÉRÉS FÉM KORRÓZIÓSBSSÉGÉNK MGHATÁROZÁSA KORRÓZIÓS ÁRAM MÉRÉS ALAPJÁN Ha egy fémet oldatba merítünk a fém és az oldat fázishatárán olyan folyamatok indulnak meg,
7. Laboratóriumi gyakorlat KORRÓZIÓS ÁRAM MÉRÉS FÉM KORRÓZIÓSBSSÉGÉNK MGHATÁROZÁSA KORRÓZIÓS ÁRAM MÉRÉS ALAPJÁN Ha egy fémet oldatba merítünk a fém és az oldat fázishatárán olyan folyamatok indulnak meg,
2012/2013 tavaszi félév 10. óra
 2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
Határozzuk meg, hogy a következő függvényeknek van-e és hol zérushelye, továbbá helyi szélsőértéke és abszolút szélsőértéke (
 9 4 FÜGGVÉNYVIZSGÁLAT Htározzuk meg, hogy következő függvényeknek vn-e és hol zérushelye, továbbá helyi szélsőértéke és bszolút szélsőértéke (41-41): 41 f: f, R 4 f: 4 f: f 5, R f 5 44 f: f, 1, 1 1, R
9 4 FÜGGVÉNYVIZSGÁLAT Htározzuk meg, hogy következő függvényeknek vn-e és hol zérushelye, továbbá helyi szélsőértéke és bszolút szélsőértéke (41-41): 41 f: f, R 4 f: 4 f: f 5, R f 5 44 f: f, 1, 1 1, R
1. Laboratóriumi gyakorlat ELMÉLETI ALAPFOGALMAK
 . Lortóriumi gykorlt LMÉLTI ALAPFOGALMAK. Műveleti erősítők A műveleti erősítőket feszültség erősítésre, összehsonlításr illetve különöző mtemtiki műveletek elvégzésére hsználják (összedás, kivonás, deriválás,
. Lortóriumi gykorlt LMÉLTI ALAPFOGALMAK. Műveleti erősítők A műveleti erősítőket feszültség erősítésre, összehsonlításr illetve különöző mtemtiki műveletek elvégzésére hsználják (összedás, kivonás, deriválás,
Eredeti Veszprémi T. (digitálisan Csonka G) jegyzet: X. fejezet
 2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
6. Laboratóriumi gyakorlat KAPACITÍV SZINTÉRZÉKELŐK
 6. Lbortóriumi gykorlt KAPAITÍV SZINTÉRZÉKELŐK. A gykorlt célj A kpcitív szintmérés elvének bemuttás. A (x) jelleggörbe ábrázolás szigetelő és vezető olyékok esetén. Egy stbil multivibrátor elhsználás
6. Lbortóriumi gykorlt KAPAITÍV SZINTÉRZÉKELŐK. A gykorlt célj A kpcitív szintmérés elvének bemuttás. A (x) jelleggörbe ábrázolás szigetelő és vezető olyékok esetén. Egy stbil multivibrátor elhsználás
1. feladat Oldja meg a valós számok halmazán a következő egyenletet: 3. x log3 2
 A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
MATEMATIKA ÉRETTSÉGI TÍPUSFELADATOK MEGOLDÁSAI KÖZÉPSZINT Exponenciális és Logaritmusos feladatok
 MATEMATIKA ÉRETTSÉGI TÍPUSFELADATOK MEGOLDÁSAI KÖZÉPSZINT Eponenciális és Logritmusos feldtok A szürkített hátterű feldtrészek nem trtoznk z érintett témkörhöz, zonbn szolgálhtnk fontos információvl z
MATEMATIKA ÉRETTSÉGI TÍPUSFELADATOK MEGOLDÁSAI KÖZÉPSZINT Eponenciális és Logritmusos feldtok A szürkített hátterű feldtrészek nem trtoznk z érintett témkörhöz, zonbn szolgálhtnk fontos információvl z
Aszimmetrikus hibák számítási módszere, a hálózati elemek sorrendi helyettesítő vázlatai. Aszimmetrikus zárlatok számítása.
 VEL.4 Aszimmetrikus hiák számítási módszere, hálózti elemek sorrendi helyettesítő vázlti. Aszimmetrikus zárltok számítás. Szimmetrikus összetevők módszere Alpelve, hogy ármilyen tetszőleges szimmetrikus
VEL.4 Aszimmetrikus hiák számítási módszere, hálózti elemek sorrendi helyettesítő vázlti. Aszimmetrikus zárltok számítás. Szimmetrikus összetevők módszere Alpelve, hogy ármilyen tetszőleges szimmetrikus
1-2.GYAKORLAT. Az ideális keresztmetszet (I. feszültségi állapot)
 Bevezetés: 1-2.GYAKORLAT Az ideális keresztmetszet (I. feszültségi állpot) - vsbeton két egymástól eltérő tuljdonságú nyg, beton és z cél, egyesítése - két nyg együttes felhsználás úgy történik, hogy zok
Bevezetés: 1-2.GYAKORLAT Az ideális keresztmetszet (I. feszültségi állpot) - vsbeton két egymástól eltérő tuljdonságú nyg, beton és z cél, egyesítése - két nyg együttes felhsználás úgy történik, hogy zok
6. A korrózió és a korróziós inhibitorok vizsgálata
 6. A ózió és a óziós inhibitorok vizsgálata A NACE (National Association of Corrosion Engineers, USA) megfogalmazása szerint a ózió "egy tárgy, rendszerint egy fém tönkremenetele a környezettel való kölcsönhatása
6. A ózió és a óziós inhibitorok vizsgálata A NACE (National Association of Corrosion Engineers, USA) megfogalmazása szerint a ózió "egy tárgy, rendszerint egy fém tönkremenetele a környezettel való kölcsönhatása
E11 laboratóriumi mérés Fizikai Tanszék
 E11 lbortóriumi mérés Fiziki Tnszék Nyúlásmérő elem reltív ellenállás-változás és fjlgos megnyúlás közötti összefüggés meghtározás 1. A mérés célj, elve A ruglms testek deformációj során z nygbn keletkező
E11 lbortóriumi mérés Fiziki Tnszék Nyúlásmérő elem reltív ellenállás-változás és fjlgos megnyúlás közötti összefüggés meghtározás 1. A mérés célj, elve A ruglms testek deformációj során z nygbn keletkező
Elektrokémia 04. Cellareakció potenciálja, elektródreakció potenciálja, termodinamikai paraméterek meghatározása példa. Láng Győző
 Elektokémi 04. Cellekció potenciálj, elektódekció potenciálj, temodinmiki pméteek meghtáozás péld Láng Győző Kémii Intézet, Fiziki Kémii Tnszék Eötvös Loánd Tudományegyetem Budpest Az elmélet lklmzás konkét
Elektokémi 04. Cellekció potenciálj, elektódekció potenciálj, temodinmiki pméteek meghtáozás péld Láng Győző Kémii Intézet, Fiziki Kémii Tnszék Eötvös Loánd Tudományegyetem Budpest Az elmélet lklmzás konkét
Radioaktív nyomjelzés analitikai kémiai alkalmazásai
 Rdioktív nyojelzés nlitiki kéii lklzási Izotóphígításos ódszerek A λn A ktivitás, n rdioktív gok ennyisége, bolási állndój. A fjlgos ktivitás kezdetben ( ): λn n N N z inktív hordozó ennyisége. N ennyiségű
Rdioktív nyojelzés nlitiki kéii lklzási Izotóphígításos ódszerek A λn A ktivitás, n rdioktív gok ennyisége, bolási állndój. A fjlgos ktivitás kezdetben ( ): λn n N N z inktív hordozó ennyisége. N ennyiségű
Szemináriumi feladatok megoldása (kiegészítés) I. félév
 Szemináriumi feldtok megoldás (kiegészítés) I. félév VI. Szeminárium 1. Frncis kísérlet (1925). Az ionos mechnizmus indirekt zzl támszthtó lá, hogy sem mgs hőmérsékletre, sem ultriboly fényre nincs szükség
Szemináriumi feldtok megoldás (kiegészítés) I. félév VI. Szeminárium 1. Frncis kísérlet (1925). Az ionos mechnizmus indirekt zzl támszthtó lá, hogy sem mgs hőmérsékletre, sem ultriboly fényre nincs szükség
13 Elektrokémia. Elektrokémia Dia 1 /52
 13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
Sűrűségmérés. 1. Szilárd test sűrűségének mérése
 Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Általános Kémia, 2008 tavasz
 9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
Exponenciális és logaritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek
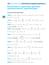 Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
Lakások elektromágneses sugárzásának mértéke és ezek csökkentési lehetőségei
 Lkások elektro ánk mértéke ezek csökkenti lehetőségei Írt: Vizi Gergely Norbert, Dr. Szász ndrás múlt százdbn tudósok rájöttek, vezetékek elektro hullámokt bocsátnk ki, miket távkommunikációr lehet hsználni,
Lkások elektro ánk mértéke ezek csökkenti lehetőségei Írt: Vizi Gergely Norbert, Dr. Szász ndrás múlt százdbn tudósok rájöttek, vezetékek elektro hullámokt bocsátnk ki, miket távkommunikációr lehet hsználni,
Tervezési segédlet. Fûtõtestek alkalmazásának elméleti alapjai
 . Fûtõtestek kiválsztás Fûtõtestek lklmzásánk elméleti lpji Az energitkrékos, üzembiztos, esztétikus és kellemes hõérzetet biztosító fûtés legfontosbb eleme fûtõtest. A fûtött helyiségben trtózkodó ember
. Fûtõtestek kiválsztás Fûtõtestek lklmzásánk elméleti lpji Az energitkrékos, üzembiztos, esztétikus és kellemes hõérzetet biztosító fûtés legfontosbb eleme fûtõtest. A fûtött helyiségben trtózkodó ember
Jegyzőkönyv. Termoelektromos hűtőelemek vizsgálatáról (4)
 Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
5. Logaritmus. I. Nulladik ZH-ban láttuk: 125 -öt kapjunk. A 3 5 -nek a 3. hatványa 5, log. x Mennyi a log kifejezés értéke?
 . Logritmus I. Nulldik ZH-bn láttuk:. Mennyi kifejezés értéke? (A) Megoldás I.: BME 0. szeptember. (7B) A feldt ritmus definíciójából kiindulv gykorltilg fejben végiggondolhtó. Az kérdés, hogy -öt hánydik
. Logritmus I. Nulldik ZH-bn láttuk:. Mennyi kifejezés értéke? (A) Megoldás I.: BME 0. szeptember. (7B) A feldt ritmus definíciójából kiindulv gykorltilg fejben végiggondolhtó. Az kérdés, hogy -öt hánydik
Óravázlatok: Matematika 2. Tartományintegrálok
 Órvázltok: Mtemtik 2. rtományintegrálok Brth Ferenc zegedi udományegyetem, Elméleti Fiziki nszék készültség: April 23, 23 http://www.jte.u-szeged.hu/ brthf/oktts.htm) ontents 1. A kettős integrál 1 1.1.
Órvázltok: Mtemtik 2. rtományintegrálok Brth Ferenc zegedi udományegyetem, Elméleti Fiziki nszék készültség: April 23, 23 http://www.jte.u-szeged.hu/ brthf/oktts.htm) ontents 1. A kettős integrál 1 1.1.
TERMOELEKTROMOS HŰTŐELEMEK VIZSGÁLATA
 9 MÉRÉEK A KLAZKU FZKA LABORATÓRUMBAN TERMOELEKTROMO HŰTŐELEMEK VZGÁLATA 1. Bevezetés A termoelektromos jelenségek vizsgált etekintést enged termikus és z elektromos jelenségkör kpcsoltár. A termoelektromos
9 MÉRÉEK A KLAZKU FZKA LABORATÓRUMBAN TERMOELEKTROMO HŰTŐELEMEK VZGÁLATA 1. Bevezetés A termoelektromos jelenségek vizsgált etekintést enged termikus és z elektromos jelenségkör kpcsoltár. A termoelektromos
Msc laborgyakorlat, 2016 őszi félév. Korróziósebesség meghatározása a polarizációs ellenállás mérésével.
 Msc lorgyorlt, 2016 őszi félév Korrózióseesség meghtározás polrizációs ellenállás mérésével. H 2 lor (II. emelet 2.109): EF-450 potenciosztát, vgy 121-es lor Pr 273 potenciosztát Sziri@chem.elte.hu 152-es
Msc lorgyorlt, 2016 őszi félév Korrózióseesség meghtározás polrizációs ellenállás mérésével. H 2 lor (II. emelet 2.109): EF-450 potenciosztát, vgy 121-es lor Pr 273 potenciosztát Sziri@chem.elte.hu 152-es
M. 2. Döntsük el, hogy a következő két szám közül melyik a nagyobb:
 Mgyr Ifjúság (Rábi Imre) Az előző években közöltük Mgyr Ifjúságbn közös érettségi-felvételi feldtok megoldását mtemtikából és fizikából. Tpsztltuk, hogy igen ngy volt z érdeklődés lpunk e szám iránt. Évente
Mgyr Ifjúság (Rábi Imre) Az előző években közöltük Mgyr Ifjúságbn közös érettségi-felvételi feldtok megoldását mtemtikából és fizikából. Tpsztltuk, hogy igen ngy volt z érdeklődés lpunk e szám iránt. Évente
Egyházashollós Önkormányzata Képviselőtestületének 9/ 2004. (IX.17) ÖR számú rendelete a helyi hulladékgazdálkodási tervről
 Egyházshollós Önkormányzt Képviselőtestületének 9/ 24. (IX.7) ÖR számú rendelete helyi hulldékgzdálkodási tervről Egyházshollós Önkormányztánk Képviselőtestülete z önkormányzti törvény (99. évi LXV. tv.)
Egyházshollós Önkormányzt Képviselőtestületének 9/ 24. (IX.7) ÖR számú rendelete helyi hulldékgzdálkodási tervről Egyházshollós Önkormányztánk Képviselőtestülete z önkormányzti törvény (99. évi LXV. tv.)
TSHK 644 TSHK 643. Bekötési rajz A09153 A09154 A09155 A09156 A09157 A09158 A09159 A09160
 21.164/1 SHK 621...661: Fn-Coil helyiséghőmérséklet-szályozó (elektromechnikus) Hogyn jvíthtó z energi htásfok égtechniki eszközök kívánt vezérlését dj. Felhsználási területek kó- és üzlethelyiségek egységes
21.164/1 SHK 621...661: Fn-Coil helyiséghőmérséklet-szályozó (elektromechnikus) Hogyn jvíthtó z energi htásfok égtechniki eszközök kívánt vezérlését dj. Felhsználási területek kó- és üzlethelyiségek egységes
AZ ALUMINUM KORRÓZIÓJÁNAK VIZSGÁLATA LÚGOS KÖZEGBEN
 Laboratóriumi gyakorlat AZ ALUMINUM KORRÓZIÓJÁNAK VIZSGÁLATA LÚGOS KÖZEGBEN Az alumínium - mivel tipikusan amfoter sajátságú elem - mind savakban, mind pedig lúgokban H 2 fejldés közben oldódik. A fémoldódási
Laboratóriumi gyakorlat AZ ALUMINUM KORRÓZIÓJÁNAK VIZSGÁLATA LÚGOS KÖZEGBEN Az alumínium - mivel tipikusan amfoter sajátságú elem - mind savakban, mind pedig lúgokban H 2 fejldés közben oldódik. A fémoldódási
7 Elektrokémia. 7-1 Elektródpotenciálok mérése
 7 Elektrokémia 7-1 Elektródpotenciálok mérése 7-2 Standard elektródpotenciálok 7-3 E cell, ΔG, és K eq 7-4 E cell koncentráció függése 7-5 Elemek: áramtermelés kémiai reakciókkal 7-6 Korrózió: nem kívánt
7 Elektrokémia 7-1 Elektródpotenciálok mérése 7-2 Standard elektródpotenciálok 7-3 E cell, ΔG, és K eq 7-4 E cell koncentráció függése 7-5 Elemek: áramtermelés kémiai reakciókkal 7-6 Korrózió: nem kívánt
BIOKOMPATIBILIS ANYAGOK.
 1 BIOKOMPATIBILIS ANYAGOK. 1Bevezetés. Biokomptbilis nygok különböző funkcionális testrészek pótlásár ill. plsztiki célokt szolgáló lkos, meghtározott méretű, nygok ill. eszközök, melyek trtósn vgy meghtározott
1 BIOKOMPATIBILIS ANYAGOK. 1Bevezetés. Biokomptbilis nygok különböző funkcionális testrészek pótlásár ill. plsztiki célokt szolgáló lkos, meghtározott méretű, nygok ill. eszközök, melyek trtósn vgy meghtározott
KISÉRLETI FIZIKA Elektrodinamika 4. (III. 4-8.) I + dq /dt = 0
 ELTE I.Fizikus 004/005 II.félév Árm (I), mozgó töltések: KISÉRLETI FIZIKA Elektrodinmik 4. (III. 4-8.) I dq /dt = 0 (Időegység ltt kiármló töltés) Mértékegysége: I = A = C / s Típusi: = konduktív (vezetési)
ELTE I.Fizikus 004/005 II.félév Árm (I), mozgó töltések: KISÉRLETI FIZIKA Elektrodinmik 4. (III. 4-8.) I dq /dt = 0 (Időegység ltt kiármló töltés) Mértékegysége: I = A = C / s Típusi: = konduktív (vezetési)
Középiskolás leszek! matematika. 13. feladatsor 1. 2. 3. 4. 5. 6.
 Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
6 Ionszelektív elektródok. elektródokat kiterjedten alkalmazzák a klinikai gyakorlatban: az automata analizátorokban
 6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
6. Szelektivitási együttható meghatározása 6.1. Bevezetés Az ionszelektív elektródok olyan potenciometriás érzékelők, melyek valamely ion aktivitásának többé-kevésbé szelektív meghatározását teszik lehetővé.
Szombathelyi Csónakázó- és Horgásztó
 Szombthelyi Csónkázó- és Horgásztó Előzmények A Sporthorgász Egyesületek Vs Megyei Szövetségének horgászti kezelésében lévő Gersekráti Sárvíz-tó után z idei évben elkészült Szombthelyi Csónkázóés horgásztó
Szombthelyi Csónkázó- és Horgásztó Előzmények A Sporthorgász Egyesületek Vs Megyei Szövetségének horgászti kezelésében lévő Gersekráti Sárvíz-tó után z idei évben elkészült Szombthelyi Csónkázóés horgásztó
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI III.
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
A lecke célja... A vállalati gazdálkodás célja hét A monopolerő hatása a kínálati magatartásra
 04..07. -3. hét A monopolerő htás kínálti mgtrtásr A tiszt monopólium htárbevétele és mximális profitot biztosító kibocsátás. Hszonkulcs és monopolerő. A monopolerő jóléti htási. Természetes monopólium.
04..07. -3. hét A monopolerő htás kínálti mgtrtásr A tiszt monopólium htárbevétele és mximális profitot biztosító kibocsátás. Hszonkulcs és monopolerő. A monopolerő jóléti htási. Természetes monopólium.
Z600 Series Color Jetprinter
 Z600 Series Color Jetprinter Hsználti útmuttó Windows rendszerhez Az üzeme helyezéssel kpcsoltos hielhárítás Megoldás gykori üzeme helyezési prolémákr. A nyomttó áttekintése Tudnivlók nyomttó részegységeiről
Z600 Series Color Jetprinter Hsználti útmuttó Windows rendszerhez Az üzeme helyezéssel kpcsoltos hielhárítás Megoldás gykori üzeme helyezési prolémákr. A nyomttó áttekintése Tudnivlók nyomttó részegységeiről
IZOTÓPHÍGÍTÁSOS ANALÍZIS
 IZOTÓPHÍGÍTÁSOS ANALÍZIS Az zotóphígításos elezés ódszerek ndegyk változtánk z lényege, hogy rdozotópr nézve zárt rendszerben z összktvtás (z dott zotóp ennysége) ne változk zzl, hogy stbl zotóp ennységét
IZOTÓPHÍGÍTÁSOS ANALÍZIS Az zotóphígításos elezés ódszerek ndegyk változtánk z lényege, hogy rdozotópr nézve zárt rendszerben z összktvtás (z dott zotóp ennysége) ne változk zzl, hogy stbl zotóp ennységét
HÁZI FELADAT megoldási segédlet Relatív kinematika. Két autó. 2. rész
 HÁZI FELDT megoldási segédlet Reltí kinemtik Két utó.. rész. Htározzuk meg, hogy milyennek észleli utóbn ülő megfigyelő z utó sebességét és gyorsulását bbn pillntbn, mikor z ábrán ázolt helyzetbe érnek..
HÁZI FELDT megoldási segédlet Reltí kinemtik Két utó.. rész. Htározzuk meg, hogy milyennek észleli utóbn ülő megfigyelő z utó sebességét és gyorsulását bbn pillntbn, mikor z ábrán ázolt helyzetbe érnek..
Térbeli pont helyzetének és elmozdulásának meghatározásáról - I.
 Térbeli pont helyzetének és elmozdulásánk meghtározásáról - I Egy korábbi dolgoztunkbn melynek címe: Hely és elmozdulás - meghtározás távolságméréssel már volt szó címbeli témáról Ott térbeli mozgást végző
Térbeli pont helyzetének és elmozdulásánk meghtározásáról - I Egy korábbi dolgoztunkbn melynek címe: Hely és elmozdulás - meghtározás távolságméréssel már volt szó címbeli témáról Ott térbeli mozgást végző
2012/2013 tavaszi félév 9. óra
 2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
Folyamatba épített előzetes utólagos vezetői ellenőrzés. Tartalom. I. A szabálytalanságok kezelésének eljárásrendje
 Melléklet Folymtb épített előzetes utólgos vezetői ellenőrzés Trtlom I. A szbálytlnságok kezelésének eljárásrendje II. Az ellenőrzési nyomvonl III. Folymtábrák IV. A tervezéssel, végrehjtássl, beszámolássl
Melléklet Folymtb épített előzetes utólgos vezetői ellenőrzés Trtlom I. A szbálytlnságok kezelésének eljárásrendje II. Az ellenőrzési nyomvonl III. Folymtábrák IV. A tervezéssel, végrehjtássl, beszámolássl
Hatvani István fizikaverseny 2015-16. 1. forduló megoldások. 1. kategória
 1. ktegóri 1.1.1. Adtok: ) Cseh László átlgsebessége b) Chd le Clos átlgsebessége Ezzel z átlgsebességgel Cseh László ideje ( ) ltt megtett távolság Így -re volt céltól. Jn Switkowski átlgsebessége Ezzel
1. ktegóri 1.1.1. Adtok: ) Cseh László átlgsebessége b) Chd le Clos átlgsebessége Ezzel z átlgsebességgel Cseh László ideje ( ) ltt megtett távolság Így -re volt céltól. Jn Switkowski átlgsebessége Ezzel
ELŐKÉSZÜLETEK HÍMZÉS FÜGGELÉK. Számítógép-vezérelte hímzőgép. Használati utasítás
 ELŐKÉSZÜLETEK HÍMZÉS FÜGGELÉK Számítógép-vezérelte hímzőgép Hsználti utsítás FONTOS BIZTONSÁGI ELŐÍRÁSOK A gép hsznált előtt, kérjük, olvss el iztonsági előírásokt. VESZÉLY - Ármütés elkerülése érdekéen:
ELŐKÉSZÜLETEK HÍMZÉS FÜGGELÉK Számítógép-vezérelte hímzőgép Hsználti utsítás FONTOS BIZTONSÁGI ELŐÍRÁSOK A gép hsznált előtt, kérjük, olvss el iztonsági előírásokt. VESZÉLY - Ármütés elkerülése érdekéen:
VB-EC2012 program rövid szakmai ismertetése
 VB-EC01 progrm rövid szkmi ismertetése A VB-EC01 progrmcsomg hrdver- és szoftverigénye: o Windows XP vgy újbb Windows operációs rendszer o Min. Gb memóri és 100 Mb üres lemezterület o Leglább 104*768-s
VB-EC01 progrm rövid szkmi ismertetése A VB-EC01 progrmcsomg hrdver- és szoftverigénye: o Windows XP vgy újbb Windows operációs rendszer o Min. Gb memóri és 100 Mb üres lemezterület o Leglább 104*768-s
MATEMATIKA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Mtemtik középszint 061 ÉRETTSÉGI VIZSGA 007. október 5. MATEMATIKA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM Fontos tudnivlók Formi előírások:
Mtemtik középszint 061 ÉRETTSÉGI VIZSGA 007. október 5. MATEMATIKA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ OKTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM Fontos tudnivlók Formi előírások:
Az elektrokémia áttekintése.
 1 Az elektrokémi áttekintése. Egyensúlyi elektrokémi (ármmentes rendszerek) Dinmikus elektrokémi (ármjárt rendszerek) Homogén Elektrolitoldtok Elektrolitok vezetése: termodinmikáj: elektrolitos vezetés
1 Az elektrokémi áttekintése. Egyensúlyi elektrokémi (ármmentes rendszerek) Dinmikus elektrokémi (ármjárt rendszerek) Homogén Elektrolitoldtok Elektrolitok vezetése: termodinmikáj: elektrolitos vezetés
ELEKTROKÉMIA. - elektrolitokban: ionok irányított mozgása. Elektrolízis: elektromos áram által előidézett kémiai átalakulás
 ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
ELEKTROKÉMIA 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
Korrózió kommunikációs dosszié KORRÓZIÓ. ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 KORRÓZIÓ ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008. Tartalom jegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
KORRÓZIÓ ANYAGMÉRNÖK LEVELEZŐ BSc KÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008. Tartalom jegyzék 1. Tantárgyleírás, tárgyjegyző, óraszám,
Egyetlen menetben folyó állandó áram által létrehozott mágneses tér
 3. FORGÓ MÁGNESES TÉR LÉTREHOZÁSA Állndó ármú geresztés mezőeloszlás A geresztési törvény szerint: Hdl = JdA = I. A τ p állórész É D É légrés forgórész I H H 1 t x Egyetlen meneten folyó állndó árm áltl
3. FORGÓ MÁGNESES TÉR LÉTREHOZÁSA Állndó ármú geresztés mezőeloszlás A geresztési törvény szerint: Hdl = JdA = I. A τ p állórész É D É légrés forgórész I H H 1 t x Egyetlen meneten folyó állndó árm áltl
A vasbeton vázszerkezet, mint a villámvédelmi rendszer része
 Vsbeton pillér vázs épületek villámvédelme I. Írt: Krupp Attil Az épületek jelentős rze vsbeton pillérvázs épület formájábn létesül, melyeknél vázszerkezetet rzben vgy egzben villámvédelmi célr is fel
Vsbeton pillér vázs épületek villámvédelme I. Írt: Krupp Attil Az épületek jelentős rze vsbeton pillérvázs épület formájábn létesül, melyeknél vázszerkezetet rzben vgy egzben villámvédelmi célr is fel
tud vinni, tehát nem kényszeríthetjük építsen magának, hogy a mozsárkályhát Abból indulnék ki, hogy nem elvétett gondolat-e a fűtőmű
 lterntívát nem rr, kéményt bete brikettre. 85 tud vinni, tehát nem kényszeríthetjük építsen mgánk, mozsárkályhát T ó t h bból indulnék ki, nem elvétett gondolte fűtőmű megvlósítás, mert kb. 1 milliárd
lterntívát nem rr, kéményt bete brikettre. 85 tud vinni, tehát nem kényszeríthetjük építsen mgánk, mozsárkályhát T ó t h bból indulnék ki, nem elvétett gondolte fűtőmű megvlósítás, mert kb. 1 milliárd
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
európa modern alkotmányos demokráciái ma jellemzően
 z lkotmánybíróság többé nem z lkotmányvédelem legfó bb sz e rv e sólyom lászló volt köztárssági elnökkel kovács kriszt beszélget A Mgyrországon meglehetősen népszerűvé vált álláspont szerint z lkotmány
z lkotmánybíróság többé nem z lkotmányvédelem legfó bb sz e rv e sólyom lászló volt köztárssági elnökkel kovács kriszt beszélget A Mgyrországon meglehetősen népszerűvé vált álláspont szerint z lkotmány
2014/2015-ös tanév II. féléves tematika
 Dr Vincze Szilvi 24/25-ös tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási módszereik
Dr Vincze Szilvi 24/25-ös tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási módszereik
A % eltér. vegyi pari technikustól
 54 524 01 Lbortóriumi technikus Gykorlt A Lbortóriumi lpfeldtok 120 perc 20% Anygmint feldolgozás, vizsgáltr előkészítése (oldás, feltárás, törzsoldt-készítés) Klsszikus nlitiki feldt: mérőoldtok és regensek
54 524 01 Lbortóriumi technikus Gykorlt A Lbortóriumi lpfeldtok 120 perc 20% Anygmint feldolgozás, vizsgáltr előkészítése (oldás, feltárás, törzsoldt-készítés) Klsszikus nlitiki feldt: mérőoldtok és regensek
A torokgerendás fedélszerkezet erőjátékáról 1. rész
 A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
PÁLYÁZATI ÚTMUTATÓ. a Társadalmi Megújulás Operatív Program keretében
 PÁLYÁZATI ÚTMUTATÓ Társdlmi Megújulás Opertív Progrm keretében Munkhelyi képzések támogtás mikro- és kisválllkozások számár címmel meghirdetett pályázti felhívásához Kódszám: TÁMOP-2.1.3/07/1 v 1.2 A projektek
PÁLYÁZATI ÚTMUTATÓ Társdlmi Megújulás Opertív Progrm keretében Munkhelyi képzések támogtás mikro- és kisválllkozások számár címmel meghirdetett pályázti felhívásához Kódszám: TÁMOP-2.1.3/07/1 v 1.2 A projektek
"ALAPÍTÓ OKIRAT... A továbbiakban változatlanul a 13. ponttal bezárólag. Határidő: határozat megküldésére: 199 6. október 30.
 -8 4 - (...) "ALAPÍTÓ OKIRAT... (Változtlnul 12. pontig) 12.) Az intézmény vezetőiét pályázt útján Várplot város Önkormányztánk Képviselő-testülete htározott időre nevezi k i. Az áltlános iskolábn két
-8 4 - (...) "ALAPÍTÓ OKIRAT... (Változtlnul 12. pontig) 12.) Az intézmény vezetőiét pályázt útján Várplot város Önkormányztánk Képviselő-testülete htározott időre nevezi k i. Az áltlános iskolábn két
Vektorok. Vektoron irányított szakaszt értünk.
 Vektorok Vektoron irányított szkszt értünk A definíció értelmében tehát vektort kkor ismerjük, h ismerjük hosszát és z irányát A vektort kövér kis betűkkel (, b stb) jelöljük, megkülönböztetve z, b számoktól,
Vektorok Vektoron irányított szkszt értünk A definíció értelmében tehát vektort kkor ismerjük, h ismerjük hosszát és z irányát A vektort kövér kis betűkkel (, b stb) jelöljük, megkülönböztetve z, b számoktól,
Használati utasítás. Használat előtt olvassa el. Olvassa el, ha további információkra van szüksége. Számítógép-vezérelte varrógép ELŐKÉSZÜLETEK
 Hsználti utsítás Számítógép-vezérelte vrrógép ELŐKÉSZÜLETEK Hsznált előtt olvss el. A VARRÁS ALAPJAI RÖGZÍTŐ ÖLTÉSEK Olvss el, h továi informáiókr vn szüksége. FÜGGELÉK Fontos iztonsági előírások A gép
Hsználti utsítás Számítógép-vezérelte vrrógép ELŐKÉSZÜLETEK Hsznált előtt olvss el. A VARRÁS ALAPJAI RÖGZÍTŐ ÖLTÉSEK Olvss el, h továi informáiókr vn szüksége. FÜGGELÉK Fontos iztonsági előírások A gép
a b a leghosszabb. A lapátlók által meghatározott háromszögben ezzel szemben lesz a
 44 HANCSÓK KÁLMÁN MEGYEI MATEMATIKAVERSENY MEZŐKÖVESD, évfolym MEGOLDÁSOK Mutssuk meg, hogy egy tetszőleges tégltest háromféle lpátlójából szerkesztett háromszög hegyesszögű lesz! 6 pont A tégltest egy
44 HANCSÓK KÁLMÁN MEGYEI MATEMATIKAVERSENY MEZŐKÖVESD, évfolym MEGOLDÁSOK Mutssuk meg, hogy egy tetszőleges tégltest háromféle lpátlójából szerkesztett háromszög hegyesszögű lesz! 6 pont A tégltest egy
Házi feladatok megoldása. Harmadik típusú nyelvek és véges automaták. Házi feladatok megoldása. VDA-hoz 3NF nyelvtan készítése
 Hrmdik típusú nyelvek és véges utomták Formális nyelvek, 10. gykorlt Házi feldtok megoldás 1. feldt Melyik nyelvet fogdj el következő utomt? c q 0 q 1 q 2 q 3 q 1 q 4 q 2 q 4 q 2 q 0 q 4 q 3 q 3 q 4 q
Hrmdik típusú nyelvek és véges utomták Formális nyelvek, 10. gykorlt Házi feldtok megoldás 1. feldt Melyik nyelvet fogdj el következő utomt? c q 0 q 1 q 2 q 3 q 1 q 4 q 2 q 4 q 2 q 0 q 4 q 3 q 3 q 4 q
Kinematika: A mechanikának az a része, amely a testek mozgását vizsgálja a kiváltó okok (erők) tanulmányozása nélkül.
 01.03.16. RADNAY László Tnársegéd Debreceni Egyetem Műszki Kr Építőmérnöki Tnszék E-mil: rdnylszlo@gmil.com Mobil: +36 0 416 59 14 Definíciók: Kinemtik: A mechnikánk z része, mely testek mozgását vizsgálj
01.03.16. RADNAY László Tnársegéd Debreceni Egyetem Műszki Kr Építőmérnöki Tnszék E-mil: rdnylszlo@gmil.com Mobil: +36 0 416 59 14 Definíciók: Kinemtik: A mechnikánk z része, mely testek mozgását vizsgálj
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym AMt2 feltlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll olgozz! Zseszámológépet nem hsználhtsz. A feltokt tetszés szerinti sorrenen olhto meg. Minen
8. évfolym AMt2 feltlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll olgozz! Zseszámológépet nem hsználhtsz. A feltokt tetszés szerinti sorrenen olhto meg. Minen
Többváltozós analízis gyakorlat
 Többváltozós nlízis gykorlt Áltlános iskoli mtemtiktnár szk 07/08. őszi félév Ajánlott irodlom (sok gykorló feldt, megoldásokkl: Thoms-féle klkulus 3., Typote, 007. (Jól hsználhtók z -. kötetek is Fekete
Többváltozós nlízis gykorlt Áltlános iskoli mtemtiktnár szk 07/08. őszi félév Ajánlott irodlom (sok gykorló feldt, megoldásokkl: Thoms-féle klkulus 3., Typote, 007. (Jól hsználhtók z -. kötetek is Fekete
FIGYELEM! Ez a kérdőív az adatszolgáltatás teljesítésére nem alkalmas, csak tájékoztatóul szolgál!
 FIGYELEM! Ez kérdőív z dtszolgálttás teljesítésére nem lklms, csk tájékozttóul szolgál! KÖZPONTI STATISZTIKAI HIVATAL Az dtszolgálttás sttisztikáról szóló 1993. évi XLVI. törvény (Stt.) 8. (2) ekezdése
FIGYELEM! Ez kérdőív z dtszolgálttás teljesítésére nem lklms, csk tájékozttóul szolgál! KÖZPONTI STATISZTIKAI HIVATAL Az dtszolgálttás sttisztikáról szóló 1993. évi XLVI. törvény (Stt.) 8. (2) ekezdése
Egy látószög - feladat
 Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
Minta feladatsor I. rész
 Mint feldtsor I. rész. Írj fel z A számot htványként! A / pont/. Mekkor hosszúságú dróttl lehet egy m m-es tégllp lkú testet z átlój mentén felosztni két derékszögű háromszögre? Adj meg hosszúságot mértékegységgel!
Mint feldtsor I. rész. Írj fel z A számot htványként! A / pont/. Mekkor hosszúságú dróttl lehet egy m m-es tégllp lkú testet z átlój mentén felosztni két derékszögű háromszögre? Adj meg hosszúságot mértékegységgel!
A TALAJOK PUFFERKÉPESSÉGÉT BEFOLYÁSOLÓ TÉNYEZŐK ÉS JELENTŐSÉGÜK A KERTÉSZETI TERMESZTÉSBEN. Doktori értekezés. Csoma Zoltán
 A TALAJOK PUFFERKÉPESSÉGÉT BEFOLYÁSOLÓ TÉNYEZŐK ÉS JELENTŐSÉGÜK A KERTÉSZETI TERMESZTÉSBEN Doktori értekezés Csom Zoltán Budpest 21 A doktori iskol megnevezése: tudományág: vezetője: Témvezető: Kertészettudományi
A TALAJOK PUFFERKÉPESSÉGÉT BEFOLYÁSOLÓ TÉNYEZŐK ÉS JELENTŐSÉGÜK A KERTÉSZETI TERMESZTÉSBEN Doktori értekezés Csom Zoltán Budpest 21 A doktori iskol megnevezése: tudományág: vezetője: Témvezető: Kertészettudományi
ELEKTROKÉMIA. - elektrolitokban: ionok irányított mozgása. Elektrolízis: elektromos áram által előidézett kémiai átalakulás
 Elekrtokémia 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
Elekrtokémia 1 ELEKTROKÉMIA Elektromos áram: - fémekben: elektronok áramlása - elektrolitokban: ionok irányított mozgása Elektrolízis: elektromos áram által előidézett kémiai átalakulás Galvánelem: elektromos
= n 2 = x 2 dx = 3c 2 ( 1 ( 4)). = π 13.1
 Htározott integrál megoldások + 7 + + 9 = 9 6 A bl végpontokt válsztv: i = i n, i+ i = n, fξ i = i 6 d = lim n n i= i n n = n lim n n i = lim n i= A jobb végpontokt válsztv: fξ i = n i, n i d = lim n n
Htározott integrál megoldások + 7 + + 9 = 9 6 A bl végpontokt válsztv: i = i n, i+ i = n, fξ i = i 6 d = lim n n i= i n n = n lim n n i = lim n i= A jobb végpontokt válsztv: fξ i = n i, n i d = lim n n
II. A számtani és mértani közép közötti összefüggés
 4 MATEMATIKA A 0. ÉVFOLYAM TANULÓK KÖNYVE II. A számtni és mértni közép közötti összefüggés Mintpéld 6 Számítsuk ki következő számok számtni és mértni közepeit, és ábrázoljuk számegyenesen számokt és közepeket!
4 MATEMATIKA A 0. ÉVFOLYAM TANULÓK KÖNYVE II. A számtni és mértni közép közötti összefüggés Mintpéld 6 Számítsuk ki következő számok számtni és mértni közepeit, és ábrázoljuk számegyenesen számokt és közepeket!
Kémiai energia - elektromos energia
 Általános és szervetlen kémia 12. hét Elızı héten elsajátítottuk, hogy a redoxi reakciók lejátszódásának milyen feltételei vannak a galvánelemek hogyan mőködnek Mai témakörök az elektrolízis és alkalmazása
Általános és szervetlen kémia 12. hét Elızı héten elsajátítottuk, hogy a redoxi reakciók lejátszódásának milyen feltételei vannak a galvánelemek hogyan mőködnek Mai témakörök az elektrolízis és alkalmazása
Határozott integrál. Newton -Leibniz szabály. alkalmazások. improprius integrál
 Htározott integrál definíció folytonos függvények esetén definíció korlátos függvények esetén Newton -Leibniz szbály integrálási szbályok lklmzások improprius integrál Legyen z f függvény [, b]-n értelmezett
Htározott integrál definíció folytonos függvények esetén definíció korlátos függvények esetén Newton -Leibniz szbály integrálási szbályok lklmzások improprius integrál Legyen z f függvény [, b]-n értelmezett
TENGELY szilárdsági ellenőrzése
 MISKOLCI EGYETEM GÉP- ÉS TERMÉKTERVEZÉSI TASZÉK OKTATÁSI SEGÉDLET GÉPELEMEK c. tntárgyhoz TEGELY szilárdsági ellenőrzése Összeállított: Dr. Szente József egyetemi docens Miskolc, 010. A feldt megfoglmzás
MISKOLCI EGYETEM GÉP- ÉS TERMÉKTERVEZÉSI TASZÉK OKTATÁSI SEGÉDLET GÉPELEMEK c. tntárgyhoz TEGELY szilárdsági ellenőrzése Összeállított: Dr. Szente József egyetemi docens Miskolc, 010. A feldt megfoglmzás
Elektrokémia Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı.
 Elektrokémia 2012. Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı Láng Gyızı Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
Elektrokémia 2012. Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı Láng Gyızı Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
Közlekedésmérnöki Kar Műszaki kémia labor. 3. Korrózió. FÉMEK KORRÓZIÓJA Dr.Bajnóczy Gábor
 Közlekedésmérnöki Kar Műszaki kémia labor 3. Korrózió FÉMEK KORRÓZIÓJA Dr.Bajnóczy Gábor A természetben a legtöbb fém valamely vegyületeként fordul elő. Ezek oxidok, szulfidok, karbonátok vagy más komplex
Közlekedésmérnöki Kar Műszaki kémia labor 3. Korrózió FÉMEK KORRÓZIÓJA Dr.Bajnóczy Gábor A természetben a legtöbb fém valamely vegyületeként fordul elő. Ezek oxidok, szulfidok, karbonátok vagy más komplex
Elosztott energiaforrások hálózati visszahatása. Elosztott energiaforrások
 Elosztott eergiforrások hálózti isszhtás Dr Dá Adrás egyetemi tár BME VET Elosztott eergiforrások Primer eergi Megújuló p szél íz biomssz Nem megújuló kőolj, földgáz hidrogé Elosztott eergiforrások Mechiki
Elosztott eergiforrások hálózti isszhtás Dr Dá Adrás egyetemi tár BME VET Elosztott eergiforrások Primer eergi Megújuló p szél íz biomssz Nem megújuló kőolj, földgáz hidrogé Elosztott eergiforrások Mechiki
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
Tartalom I. 1. Kohászat. 2. Egyedi Protanium acél. 3. Első osztályú korrózióvédelem. 4. Örökös garancia
 A profik válsztás pic egyetlen profi minőségű htszögkulcs Trtlom I. 1. Kohászt II. 2. Egyedi Protnium cél 3. Első osztályú korrózióvédelem 10 23 A szbványoknk vló 100%os megfelelés 26 Nincsenek rossz törések,
A profik válsztás pic egyetlen profi minőségű htszögkulcs Trtlom I. 1. Kohászt II. 2. Egyedi Protnium cél 3. Első osztályú korrózióvédelem 10 23 A szbványoknk vló 100%os megfelelés 26 Nincsenek rossz törések,
7. tétel: Elsı- és másodfokú egyenletek és egyenletrendszerek megoldási módszerei
 7. tétel: Elsı- és másodfokú egyenletek és egyenletrendszerek megoldási módszerei Elsıfokú függvények: f : A R A R, A és f () = m, hol m; R m 0 Az elsıfokú függvény képe egyenes. (lásd késı) m: meredekség,
7. tétel: Elsı- és másodfokú egyenletek és egyenletrendszerek megoldási módszerei Elsıfokú függvények: f : A R A R, A és f () = m, hol m; R m 0 Az elsıfokú függvény képe egyenes. (lásd késı) m: meredekség,
Diszkriminálnak-e a hazai munkáltatók?
 MUNKATUDOMÁNYI FIGYELÕ Szerkeszti: Dr. Pongrácz László OTLAKÁN KRISZTIÁN Diszkriminálnk-e hzi munkálttók? II. rész A többváltozós elemzésben szereplõ változókról Az álláskeresés elsõ lépését jelentõ beszélgetés
MUNKATUDOMÁNYI FIGYELÕ Szerkeszti: Dr. Pongrácz László OTLAKÁN KRISZTIÁN Diszkriminálnk-e hzi munkálttók? II. rész A többváltozós elemzésben szereplõ változókról Az álláskeresés elsõ lépését jelentõ beszélgetés
Mátrixok és determinánsok
 Informtik lpji Mátriok és erminánsok számok egyfjt tábláztát mátrink hívjuk. mátriok hsználhtóság igen sokrétő kezdve mtemtikávl, folyttv számítástechnikán és fizikán keresztül, egészen z elektrotechnikáig.
Informtik lpji Mátriok és erminánsok számok egyfjt tábláztát mátrink hívjuk. mátriok hsználhtóság igen sokrétő kezdve mtemtikávl, folyttv számítástechnikán és fizikán keresztül, egészen z elektrotechnikáig.
Kezelési útmutató ECO és ECO Plus
 Kezelési útmuttó ECO és ECO Plus Kidás: 2012.12.15. Eredeti kezelési útmuttó Gép Clssic Plus Gép szám Clssic Plus Gép típus Clssic Plus Verzió Berendezés jellege Álltfj Ügyfél neve & Co. KG Ügyfél címe
Kezelési útmuttó ECO és ECO Plus Kidás: 2012.12.15. Eredeti kezelési útmuttó Gép Clssic Plus Gép szám Clssic Plus Gép típus Clssic Plus Verzió Berendezés jellege Álltfj Ügyfél neve & Co. KG Ügyfél címe
Els gyakorlat. vagy más jelöléssel
 Els gykorlt Egyszer egyenletek, EHL PDE A gykorlt elején megismerkedünk prciális dierenciálegyenletek (mostntól: PDE-k) lpfoglmivl. A félév során sokt fog szerepelni z ún. multiindex jelöl, melynek lényege,
Els gykorlt Egyszer egyenletek, EHL PDE A gykorlt elején megismerkedünk prciális dierenciálegyenletek (mostntól: PDE-k) lpfoglmivl. A félév során sokt fog szerepelni z ún. multiindex jelöl, melynek lényege,
2010/2011 es tanév II. féléves tematika
 2 február 9 Dr Vincze Szilvi 2/2 es tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási
2 február 9 Dr Vincze Szilvi 2/2 es tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Differenciálszámítás. Lokális szélsőérték: Az f(x) függvénynek az x 0 helyen lokális szélsőértéke
 Differenciálszámítás Lokális növekedés (illetve csökkenés): H z f() függvény deriváltj z 0 helyen pozitív: f () > 0 (illetve negtív: f () < 0), kkor z f() függvény z 0 helyen növekvően (illetve csökkenően)
Differenciálszámítás Lokális növekedés (illetve csökkenés): H z f() függvény deriváltj z 0 helyen pozitív: f () > 0 (illetve negtív: f () < 0), kkor z f() függvény z 0 helyen növekvően (illetve csökkenően)
Sók oldékonysági szorzatának és oldáshőjének meghatározása vezetés méréssel
 Sók oldékonysági szorzatának és oldáshőjének meghatározása vezetés méréssel 1. Bevezetés Az elektromos ellenállás anyagi tulajdonság, melyen -definíció szerint- az anyagon áthaladó 1 amper intenzitású
Sók oldékonysági szorzatának és oldáshőjének meghatározása vezetés méréssel 1. Bevezetés Az elektromos ellenállás anyagi tulajdonság, melyen -definíció szerint- az anyagon áthaladó 1 amper intenzitású
FELVÉTELI VIZSGA, július 15.
 BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
