számot a Z felosztáshoz tartozó integrálközelít összegnek nevezzük. Jelöljük Z-vel a s i -számok leghosszabbikát.
|
|
|
- Klaudia Vörös
- 8 évvel ezelőtt
- Látták:
Átírás
1 MEMIKI KÖZBEEÉ: INERÁLÁ I. Bronstejn-zemengyajev: Matematikai Zsebkönyv Elsfajú görbementi integrálok Legyen K szakaszonként sima görbedarab, kezdontja, végontja B és uf(x,y) a K görbét tartalmazó tartományban értelmezett korlátos függvény. együk fel a K görbén az 0, 1,, n B ontokat. Jelöljük ezt a felosztást Z-vel. Jelöljük s i -vel az i-1 és i ontok közötti görbedarab ívhosszát. z elemi görbeszakaszok mindegyikében vegyünk fel egy tetszleges i, i koordinátákkal megadott M i ontot. n σ ( Z ) f ( ξ, η ) s számot a Z felosztáshoz tartozó integrálközelít összegnek nevezzük. Jelöljük Z-vel a s i -számok leghosszabbikát. i 1 i i i határozott integrál értelmezéséhez hasonlóan elsfajú görbementi integrálnak nevezzük az I számot, ha tetszleges >0 számhoz megadható ()>0 úgy, hogy minden olyan Z felosztásra, amelyre (Z)<, a M i ontok választásától függetlenül σ ( Z) I < ε teljesül. Jelölése: I ( K ) f ( x, y) ds XI/1
2 Másodfajú görbementi integrálok Legyen K szakaszonként sima görbedarab, kezdontja, végontja B és uf(x,y) a K görbét tartalmazó tartományban értelmezett korlátos függvény. együk fel a K görbén az 0, 1,, n B ontokat. Jelöljük ezt a felosztást Z-vel. felosztás elemi görbeszakaszainak mindegyikében vegyünk fel egy tetszleges i, i koordinátákkal megadott M i ontot. megfelel koordináták: i (x i, y i ), M i ( i, i ) n σ ( Z ) f ( ξ, η ) x számot a Z felosztáshoz tartozó integrálközelít összegnek nevezzük. Jelöljük Z-vel az i-1 és i ontok távolságának legnagyobbikát. i 1 i i i határozott integrál értelmezéséhez hasonlóan másodfajú görbementi integrálnak nevezzük az I számot, ha tetszleges >0 számhoz megadható ()>0 úgy, hogy minden olyan Z felosztásra, amelyre (Z)<, a M i ontok választásától függetlenül σ ( Z) I < ε teljesül. Jelölése: I ( K ) f ( x, y) dx Ha a görbe kezd- és végontja egybeesik, akkor zártgörbementi integrálról beszélünk. Jelölése: I ( K ) f ( x, y) dx XI/
3 KÉ ÚJ ÁLLPOFÜÉNY: ZBDENERI É ZBDENLPI FUNDMENÁLI EYENLEEK, PONÁN FOLYMOK KRIÉRIUMI É Z ÁLLPOFÜÉNYEK ERMÉZEE ÁLOZÓI Bels energia: UU(, ) (Fundamentális egyenlet energia rerezentációban.) Entalia: HH(, ) Entróia: (U, ) (Fundamentális egyenlet entróia rerezentációban.) De hát szeretnénk olyan függvénnyel dolgozni, amelyek természetes változói a és, vagy és. Ezen változók alkalmazása nehézkes, nem elég informatív a bels energia vagy az entalia esetén! Emlékezzünk, láttuk már ezeket az eseteket! Ez a sejtés adja a motivációt arra, hogy új állaotfüggvények után nézzünk! XI/3
4 (HELMHOLZ-FÉLE) ZBDENERI ezessük be az U- állaotfüggvényt! Neve: szabadenergia (Helmholtz szabadenergia). szabadenergia kis megváltozására: d du d d Clausius egyenltlenség állandó térfogaton, és ha nincs egyéb munkavégzés, (dqdu): Átrendezve: du/ d du d Állandó hmérsékleten az egyenlet bal oldala éen a szabadenergia kis megváltozásával egyenl: d, Állandó és mellett tehát biztosítja az önként lejátszódó folyamatok kritériumát (ha nincs egyéb munkavégzés). ejthetjük mik lesznek természetes változói XI/4
5 ZBDENLPI (IBB ZBDENERI, IBB- ENERI) ezessük be a H-U+- állaotfüggvényt! Neve: szabadentalia (ibbs szabadenergia, ibbsenergia). szabadentalia kis megváltozására: d dh d d Clausius egyenltlenség állandó nyomáson, és ha nincs egyéb munkavégzés, (dqdh): Átrendezve: dh/ d dh d Állandó hmérsékleten az egyenlet bal oldala éen a szabadentalia kis megváltozásával egyenl: d, Állandó és mellett tehát biztosítja az önként lejátszódó folyamatok kritériumát (ha nincs egyéb munkavégzés). ejthetjük mik lesznek természetes változói XI/5
6 ZBDENERI É MXIMÁLI MUNK Ismét vizsgáljunk meg egy D-i rendszert, a rendszer változását két állaot között. szabadenergia megváltozása: Használva az I. ftételt: 1 U U1 1 ( ) q + w ( ) 1 Most egy olyan folyamatot (l. kémiai reakció, stb.) vizsgálunk meg, amikor a folyamat mellett hfelvétel történhet egy állandó hmérséklet htartálytól, és közben a rendszer hmérséklete állandó, a htartály hmérsékletével egyezik meg. Clausius egyenltlenséget újra alkalmazhatjuk a rendszer által felvett hre: dq/ d Integrálva, állandóságát feltételezve q ( 1) Behelyettesítve a szabadenergia változásának egyenletébe (ahol 1 ): w ( ) 1 z egyenletben w a rendszer által végzett munka. z egyenlség a reverzibilis változásnak, az egyenltlenség az irreverzibilis folyamatnak felel meg. Mivel a jobb oldal állaotfüggvény, értéke adott, akár reverzibilis, akár irreverzibilis folyamatról van szó. XI/6
7 rendszer által elvégezhet maximális munka tehát egyenl a szabadenergia változásának negatívjával. Ezt csak reverzibilis esetben lehet kinyerni. ( w) ( ) max szabadenergia tehát úgy fogható fel, mint a bels energia izoterm folyamatokban történt megváltozásának azon része ami munkavégzésre maximálisan felhasználható! lternatív módon: w ( ) 1 Ez a felírás nem annyira informatív! z azonban mégis látszik, hogy ha nincs egyéb munka és a térfogat állandó (azaz nincs térfogati munka sem), akkor az egyenltlenség a sontán lejátszódó folyamatok kritériumát adja (állandó és mellett)! 0 1 XI/7
8 ZBDENLPI É MXIMÁLI MUNK Ismét vizsgáljunk meg egy D-i rendszert, a rendszer változását két állaot között. szabadentalia megváltozása: Használva az I. ftételt: + ( 1 1) ( 1 1) 1 U U1 1 q + w + ( 1 1) ( 1 1) Most egy olyan folyamatot vizsgálunk meg, amikor a folyamat mellett a) hfelvétel történhet egy állandó hmérséklet htartálytól, és b) közben a rendszer hmérséklete állandó, a htartály hmérsékletével egyezik meg. ovábbá c) a rendszeren kívüli egyetlen testnek, ami térfogatváltozáson mehet keresztül, állandó a nyomása,, és d) a rendszer nyomása állandó a folyamat során, ( 1 ), (bár térfogata változhat). Clausius egyenltlenséget újra alkalmazhatjuk a rendszer által felvett hre: dq/ d Integrálva, állandóságát feltételezve q ( 1) Behelyettesítve a szabadenergia változásának egyenletébe (ahol 1 ): w 1 ) ( ) ( 1 z egyenletben w a rendszer által végzett munka, míg ( 1 ) rendszeren végzett térfogati munka, azaz a rendszer által végzett térfogati munka negatívja. Ha van a térfogati munkán kívül más munka is, akkor a XI/8
9 w ) ( 1 w egyéb. ehát w egyéb ( ) 1 z egyenlség a reverzibilis változásnak, az egyenltlenség az irreverzibilis folyamatnak felel meg. Mivel a jobb oldal állaotfüggvény, értéke adott, akár reverzibilis, akár irreverzibilis folyamatról van szó. rendszer által elvégezhet maximális egyéb (azaz nem-térfogati) munka tehát egyenl a szabadentalia változásának negatívjával. Ezt csak reverzibilis esetben lehet kinyerni. lternatív módon: ( w) ( ) egyéb,max 1 w egyéb ( ) 1 Ez a felírás nem annyira informatív! z azonban mégis látszik, hogy ha nincs egyéb munka, akkor az egyenltlenség a sontán lejátszódó folyamatok kritériumát adja (állandó és mellett)! 0 XI/9
10 XI/10 FUNDMENÁLI EYENLE: ZBDENERI É ZBDENLPI szabadenergia szabadenergia megváltozása a definiáló egyenletbl: ddu-d()du-d-d bels energia fundamentális egyenletét beírva kajuk az szabadenergiára vonatkozó fundamentális egyenletet: d -d-d z egyenlet sugallja a szabadenergia hmérséklet, illetve nyomásfüggését, (, ). megfelel teljes differenciálból d d d + kifejezhet újabb két arciális differenciálhányados: és megfelel Maxwell-egyenlet:
11 XI/11 szabadentalia szabadentalia megváltozása a definiáló egyenletbl: ddu+d()-d()du+d+d-d-d bels energia fundamentális egyenletét beírva kajuk az szabadentaliára vonatkozó fundamentális egyenletet: d -d+d z egyenlet sugallja a szabadentalia hmérséklet, illetve nyomásfüggését, (, ). megfelel teljes differenciálból d d d + kifejezhet újabb két arciális differenciálhányados: és megfelel Maxwell-egyenlet:
12 ÁLLPOFÜÉNYEK (POENCIÁLFÜÉNYEK) EYZER ERMODINMIKI RENDZEREK Jele, származtatása, mértékegysége Bels energia U (I. ftétel) extenzív J Entalia HU+ extenzív J zabadenergia U- extenzív J zabadentalia U+- extenzív J Entróia (II. ftétel) extenzív JK -1 Moláris mennyiségek Moláris bels energia U m intenzív Jmol -1 Moláris entalia H m intenzív Jmol -1 Moláris szabadenergia m intenzív Jmol -1 Moláris szabadentalia m intenzív Jmol -1 Moláris entróia m intenzív Jmol -1 K -1 ermészetes változók, fundamentális egyenletek, sontán lejátszódó folyamatok kritériuma Bels energia U(, ) dud-d d U, Entalia H(, ) dh d+d d H, zabadenergia (, ) d -d-d d, zabadentalia (, ) d -d+d d, Entróia (U, ) 1 d du + d 0 d U, Fontos megjegyzés: vegyük észre a táblázat utolsó két oszloa közötti látszólagos ellentmondást! XI/1
A BELS ENERGIÁRA VONATKOZÓ ALAPVET EGYENLET. du=w+q
 AZ I. É II. FÉEL EGYEÍÉE A BEL ENERGIÁRA ONAKOZÓ ALAPE EGYENLE ekintsük a D. I. ftételét: Mi a jelentése? wq a egy egyszer zárt (nincs anyagcsere) D-i renszert vizsgálunk és a renszer változásai (h és
AZ I. É II. FÉEL EGYEÍÉE A BEL ENERGIÁRA ONAKOZÓ ALAPE EGYENLE ekintsük a D. I. ftételét: Mi a jelentése? wq a egy egyszer zárt (nincs anyagcsere) D-i renszert vizsgálunk és a renszer változásai (h és
6. Termodinamikai egyensúlyok és a folyamatok iránya
 6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához
 Dr. Pósa Mihály Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához 1. Bevezetés Shillady Don professzor az Amerikai Kémiai Szövetség egyik tanácskozásán felhívta a figyelmet a
Dr. Pósa Mihály Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához 1. Bevezetés Shillady Don professzor az Amerikai Kémiai Szövetség egyik tanácskozásán felhívta a figyelmet a
A termodinamika II. és III. főtétele
 A termodinamika II. és III. főtétele Fizikai kémia előadások 3. urányi amás ELE Kémiai Intézet A termodinamika II. főtétele Néhány dolgot természetesnek tartunk, de (a termodinamika tanulása előtt) nem
A termodinamika II. és III. főtétele Fizikai kémia előadások 3. urányi amás ELE Kémiai Intézet A termodinamika II. főtétele Néhány dolgot természetesnek tartunk, de (a termodinamika tanulása előtt) nem
EGYKOMPONENS RENDSZEREK: A FOLYADÉKFELÜLET HATÁSA
 EGYKOMPONEN RENDZEREK: A FOLYADÉKFELÜLE HAÁA A FOLYADÉKOK FELÜLEE Határfelületek hatását eddig elhanyagoltuk! De ha egy folyadék halmazállaotú termodinamikai rendszer határfelületének mérete összehasonlítható
EGYKOMPONEN RENDZEREK: A FOLYADÉKFELÜLE HAÁA A FOLYADÉKOK FELÜLEE Határfelületek hatását eddig elhanyagoltuk! De ha egy folyadék halmazállaotú termodinamikai rendszer határfelületének mérete összehasonlítható
Követelmények: f - részvétel az előadások 67 %-án - 3 db érvényes ZH (min. 50%) - 4 elfogadott laborjegyzőkönyv
 Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont)
 Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
5 = nr. nrt V. p = p p T T. R p TISZTA FÁZISOK TERMODINAMIKAI FÜGGVÉNYEI IDEÁLIS GÁZOK. Állapotegyenletbl levezethet mennyiségek. Az állapotegyenlet:
 IZA FÁZIOK ERMODINAMIKAI FÜGGÉNYEI IDEÁLI GÁZOK Állaotegyenletbl levezethet ennyiségek Az állaotegyenlet: Moláris térfogat egváltozása: R R R R eroinaikai függvények Bels energia onoatoos ieális gázra
IZA FÁZIOK ERMODINAMIKAI FÜGGÉNYEI IDEÁLI GÁZOK Állaotegyenletbl levezethet ennyiségek Az állaotegyenlet: Moláris térfogat egváltozása: R R R R eroinaikai függvények Bels energia onoatoos ieális gázra
Izolált rendszer falai: sem munkavégzés, sem a rendszer állapotának munkavégzés nélküli megváltoztatása nem lehetséges.
 ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
ERMODINMIK I. FÉELE els eergia: megmaraó meyiség egy izolált reszerbe (eergiamegmaraás törvéye) mikroszkóikus kifejezését láttuk Izolált reszer falai: sem mukavégzés sem a reszer állaotáak mukavégzés élküli
Termodinamika (Hőtan)
 Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Lagrange és Hamilton mechanika
 Lagrange és 2010. október 17. Lagrange és Tartalom 1 Variáció Lagrange egyenlet Legendre transzformáció Hamilton egyenletek 2 3 Szimplektikus sokaság Hamilton mez Hamilton és Lagrange egyenletek ekvivalenciája
Lagrange és 2010. október 17. Lagrange és Tartalom 1 Variáció Lagrange egyenlet Legendre transzformáció Hamilton egyenletek 2 3 Szimplektikus sokaság Hamilton mez Hamilton és Lagrange egyenletek ekvivalenciája
Hármas integrál Szabó Krisztina menedzser hallgató. A hármas és háromszoros integrál
 Hármas integrál Szabó Krisztina menedzser hallgató A hármas és háromszoros integrál Definició A fizikai meggondolások előzményeként jutunk el a hármas integrál következő értelmezéséhez. Legyen értelmezve
Hármas integrál Szabó Krisztina menedzser hallgató A hármas és háromszoros integrál Definició A fizikai meggondolások előzményeként jutunk el a hármas integrál következő értelmezéséhez. Legyen értelmezve
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1. Feladatok a termodinamika tárgyköréből
 . Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
valós számot tartalmaz, mert az ilyen részhalmazon nem azonosság.
 2. Közönséges differenciálegyenlet megoldása, megoldhatósága Definíció: Az y függvényt a valós számok H halmazán a közönséges differenciálegyenlet megoldásának nevezzük, ha az y = y(x) helyettesítést elvégezve
2. Közönséges differenciálegyenlet megoldása, megoldhatósága Definíció: Az y függvényt a valós számok H halmazán a közönséges differenciálegyenlet megoldásának nevezzük, ha az y = y(x) helyettesítést elvégezve
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA. A termodinamika alapproblémája
 A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA A termodinamika alapproblémája Első észrevétel: U, V és n meghatározza a rendszer egyensúlyi állapotát. Mi történik, ha változás történik a rendszerben? Mi lesz
A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA A termodinamika alapproblémája Első észrevétel: U, V és n meghatározza a rendszer egyensúlyi állapotát. Mi történik, ha változás történik a rendszerben? Mi lesz
BME Energetika Tanszék
 BME Energetika anszék A vastagon keretezett részt vizsgázó tölti ki!... név (a személyi igazolványban szerelő módon) HELYSZÁM: Hallgatói azonosító (NEPUN): KÉPZÉS: N-00 N-0E NK00 LK00 isztelt Vizsgázó!
BME Energetika anszék A vastagon keretezett részt vizsgázó tölti ki!... név (a személyi igazolványban szerelő módon) HELYSZÁM: Hallgatói azonosító (NEPUN): KÉPZÉS: N-00 N-0E NK00 LK00 isztelt Vizsgázó!
Axiomatikus felépítés az axiómák megalapozottságát a felépített elmélet teljesítképessége igazolja majd!
 Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Fázisok. Fizikai kémia előadások 3. Turányi Tamás ELTE Kémiai Intézet. Fázisok
 Fázisok Fizikai kéia előadások 3. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív állaotjelzők
Fázisok Fizikai kéia előadások 3. Turányi Taás ELTE Kéiai Intézet Fázisok DEF egy rendszer hoogén, ha () nincsenek benne akroszkoikus határfelülettel elválasztott részek és () az intenzív állaotjelzők
A termodinamika törvényei
 A termodinamika törvényei 2009. 03. 23-24. Kiss Balázs Termodinamikai Természeti környezetünk meghatározott tulajdonságú falakkal leválasztott része. nincs kölcsönhatás a környezettel izolált kissb3@gmail.com
A termodinamika törvényei 2009. 03. 23-24. Kiss Balázs Termodinamikai Természeti környezetünk meghatározott tulajdonságú falakkal leválasztott része. nincs kölcsönhatás a környezettel izolált kissb3@gmail.com
Integr alsz am ıt as. 1. r esz aprilis 12.
 Integrálszámítás. 1. rész. 2018. április 12. Területszámítás f : [a, b] IR + korlátos függvény. Mennyi a függvény grafikonja és az x tengely közti terület? Riemann integrál, ismétlés F: Az összes lehetséges
Integrálszámítás. 1. rész. 2018. április 12. Területszámítás f : [a, b] IR + korlátos függvény. Mennyi a függvény grafikonja és az x tengely közti terület? Riemann integrál, ismétlés F: Az összes lehetséges
T obbv altoz os f uggv enyek integr alja. 3. r esz aprilis 19.
 Többváltozós függvények integrálja. 3. rész. 2018. április 19. Kettős integrál Kettős integrál téglalap alakú tartományon. Ismétlés Ha = [a, b] [c, d] téglalap-tartomány, f : I integrálható függvény, akkor
Többváltozós függvények integrálja. 3. rész. 2018. április 19. Kettős integrál Kettős integrál téglalap alakú tartományon. Ismétlés Ha = [a, b] [c, d] téglalap-tartomány, f : I integrálható függvény, akkor
3. előadás Stabilitás
 Stabilitás 3. előadás 2011. 09. 19. Alapfogalmak Tekintsük dx dt = f (t, x), x(t 0) = x 0 t (, ), (1) Jelölje t x(t; t 0, x 0 ) vagy x(.; t 0, x 0 ) a KÉF megoldását. Kívánalom: kezdeti állapot kis megváltozása
Stabilitás 3. előadás 2011. 09. 19. Alapfogalmak Tekintsük dx dt = f (t, x), x(t 0) = x 0 t (, ), (1) Jelölje t x(t; t 0, x 0 ) vagy x(.; t 0, x 0 ) a KÉF megoldását. Kívánalom: kezdeti állapot kis megváltozása
A TERMODINAMIKA I. AXIÓMÁJA. Egyszerű rendszerek egyensúlya. Első észrevétel: egyszerű rendszerekről beszélünk.
 A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
VÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZTÉVFOLYAM 2006
 ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
ÁLASZOK A FIZKÉM I ALAPKÉRDÉSEKRE, KERESZÉFOLYAM 6. Az elszgetelt rendszer határfelületén át nem áramlk sem energa, sem anyag. A zárt rendszer határfelületén energa léhet át, anyag nem. A nytott rendszer
A van der Waals-gáz állapotegyenlete és a Joule Thompson-kísérlet Kiegészítés fizikus hallgatók számára
 van der Waals-gáz állaotegyenlete és a Joule homson-kísérlet Kiegészítés fizikus hallgatók számára Cserti József Eötvös Loránd udományegyetem, Komlex Rendszerek Fizikája anszék 006. december. van der Waals-állaotegyenlet:
van der Waals-gáz állaotegyenlete és a Joule homson-kísérlet Kiegészítés fizikus hallgatók számára Cserti József Eötvös Loránd udományegyetem, Komlex Rendszerek Fizikája anszék 006. december. van der Waals-állaotegyenlet:
1. Példa. A gamma függvény és a Fubini-tétel.
 . Példa. A gamma függvény és a Fubini-tétel.. Az x exp x + t )) függvény az x, t tartományon folytonos, és nem negatív, ezért alkalmazható rá a Fubini-tétel. I x exp x + t )) dxdt + t dt π 4. [ exp x +
. Példa. A gamma függvény és a Fubini-tétel.. Az x exp x + t )) függvény az x, t tartományon folytonos, és nem negatív, ezért alkalmazható rá a Fubini-tétel. I x exp x + t )) dxdt + t dt π 4. [ exp x +
2. Energodinamika értelmezése, főtételei, leírási módok
 Energetika 7 2. Energodinamika értelmezése, főtételei, leírási módok Az energia fogalmának kialakulása történetileg a munkavégzés definícióához kapcsolódik. Kezdetben az energiát a munkavégző képességgel
Energetika 7 2. Energodinamika értelmezése, főtételei, leírási módok Az energia fogalmának kialakulása történetileg a munkavégzés definícióához kapcsolódik. Kezdetben az energiát a munkavégző képességgel
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével
 5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
5. Az adszorpciós folyamat mennyiségi leírása a Langmuir-izoterma segítségével 5.1. Átismétlendő anyag 1. Adszorpció (előadás) 2. Langmuir-izoterma (előadás) 3. Spektrofotometria és Lambert Beer-törvény
1. Komplex függvények dierenciálhatósága, Cauchy-Riemann egyenletek. Hatványsorok, elemi függvények
 1. Komplex függvények dierenciálhatósága, Cauchy-Riemann egyenletek. Hatványsorok, elemi függvények 1.1. Dierenciálhatóság 1.1. deníció. Legyen a z 0 pont az f(z) függvény értelmezési tartományának torlódási
1. Komplex függvények dierenciálhatósága, Cauchy-Riemann egyenletek. Hatványsorok, elemi függvények 1.1. Dierenciálhatóság 1.1. deníció. Legyen a z 0 pont az f(z) függvény értelmezési tartományának torlódási
BME Energetika Tanszék
 BME Energetika anszék A vastagon bekeretezett részt vizsgázó tölti ki!... név (a személyi igazolványban szerelő módon) HELYSZÁM: Hallgatói azonosító (NEPUN): AGOZA: N NK LK Műszaki Hőtan I. (ermodinamika)
BME Energetika anszék A vastagon bekeretezett részt vizsgázó tölti ki!... név (a személyi igazolványban szerelő módon) HELYSZÁM: Hallgatói azonosító (NEPUN): AGOZA: N NK LK Műszaki Hőtan I. (ermodinamika)
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly
 Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
A talajok összenyomódásának vizsgálata
 A talajok összenyomódásának vizsgálata Amit már tudni kellene Összenyomódás Konszolidáció Normálisan konszolidált talaj Túlkonszolidált talaj Túlkonszolidáltsági arányszám,ocr Konszolidáció az az időben
A talajok összenyomódásának vizsgálata Amit már tudni kellene Összenyomódás Konszolidáció Normálisan konszolidált talaj Túlkonszolidált talaj Túlkonszolidáltsági arányszám,ocr Konszolidáció az az időben
Energiatételek - Példák
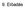 9. Előadás Húzott rúd potenciális energiája: Hooke-modell: σ = Eε Geom. hetséges Geometriai egyenlet: + geom. peremfeltételek: u εx = ε = x u(0) = 0 ul () = 0 du dx Energiatételek Példák = k l 0 pudx l
9. Előadás Húzott rúd potenciális energiája: Hooke-modell: σ = Eε Geom. hetséges Geometriai egyenlet: + geom. peremfeltételek: u εx = ε = x u(0) = 0 ul () = 0 du dx Energiatételek Példák = k l 0 pudx l
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok
 Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Zrínyi Miklós. Történeti visszatekintés. Történeti visszatekintés. Biofizikai termodinamika (Bio-termodinamika) Az energiamegmaradás tétele
 SEMMELWEIS EGYEEM Bofzka és Sugárbológa Intézet, Nanokéma utatócsoort Bofzka termodnamka (Bo-termodnamka) Zríny Mklós egyetem tanár, az MA levelező tagja mkloszrny@gmal.com örténet vsszatekntés -A hőmérséklet
SEMMELWEIS EGYEEM Bofzka és Sugárbológa Intézet, Nanokéma utatócsoort Bofzka termodnamka (Bo-termodnamka) Zríny Mklós egyetem tanár, az MA levelező tagja mkloszrny@gmal.com örténet vsszatekntés -A hőmérséklet
A munkavégzés a rendszer és a környezete közötti energiacserének a D hőátadástól eltérő valamennyi más formája.
 11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
Jármőtervezés és vizsgálat I. VALÓSZÍNŐSÉGSZÁMÍTÁSI ALAPFOGALMAK Dr. Márialigeti János
 BUDAPESTI MŐSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR JÁRMŐELEMEK ÉS HAJTÁSOK TANSZÉK Jármőtervezés és vizsgálat I. VALÓSZÍNŐSÉGSZÁMÍTÁSI ALAPFOGALMAK Dr. Márialigeti János Budapest 2008
BUDAPESTI MŐSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR JÁRMŐELEMEK ÉS HAJTÁSOK TANSZÉK Jármőtervezés és vizsgálat I. VALÓSZÍNŐSÉGSZÁMÍTÁSI ALAPFOGALMAK Dr. Márialigeti János Budapest 2008
Orvosi Fizika 11. Transzportfolyamatok termodinamikai vonatkozásai. Dr. Nagy László
 Orvosi Fizika 11. Transzportfolyamatok termodinamikai vonatkozásai Dr. Nagy László Egyensúlyi termodinamika A termodinamika a klasszikus értelezés szerint a hőserével együtt járó kölsönhatások tudománya.
Orvosi Fizika 11. Transzportfolyamatok termodinamikai vonatkozásai Dr. Nagy László Egyensúlyi termodinamika A termodinamika a klasszikus értelezés szerint a hőserével együtt járó kölsönhatások tudománya.
Maple: Deriváltak és a függvény nevezetes pontjai
 Maple: Deriváltak és a függvény nevezetes pontjai Bevezető Tudjuk, hogy a Maple könnyűszerrel képes végrehajtani a szimbólikus matematikai számításokat, ezért a Maple egy ideális program differenciál-
Maple: Deriváltak és a függvény nevezetes pontjai Bevezető Tudjuk, hogy a Maple könnyűszerrel képes végrehajtani a szimbólikus matematikai számításokat, ezért a Maple egy ideális program differenciál-
Rugalmas láncgörbe alapvető összefüggések és tudnivalók I. rész
 Rugalmas láncgörbe alapvető összefüggések és tudnivalók I rész evezetés rugalmas láncgörbe magyar nyelvű szakirodalma nem túl gazdag Egy viszonylag rövid ismertetés található [ 1 ] - ben közönséges ( azaz
Rugalmas láncgörbe alapvető összefüggések és tudnivalók I rész evezetés rugalmas láncgörbe magyar nyelvű szakirodalma nem túl gazdag Egy viszonylag rövid ismertetés található [ 1 ] - ben közönséges ( azaz
A kémiai és az elektrokémiai potenciál
 Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Meghatározás: Olyan egyenlet, amely a független változók mellett tartalmaz egy vagy több függvényt és azok deriváltjait.
 Közönséges differenciálegyenletek Meghatározás: Olyan egyenlet, amely a független változók mellett tartalmaz egy vagy több függvényt és azok deriváltjait. Célunk a függvény meghatározása Egyetlen független
Közönséges differenciálegyenletek Meghatározás: Olyan egyenlet, amely a független változók mellett tartalmaz egy vagy több függvényt és azok deriváltjait. Célunk a függvény meghatározása Egyetlen független
Megoldások. ξ jelölje az első meghibásodásig eltelt időt. Akkor ξ N(6, 4; 2, 3) normális eloszlású P (ξ
 Megoldások Harmadik fejezet gyakorlatai 3.. gyakorlat megoldása ξ jelölje az első meghibásodásig eltelt időt. Akkor ξ N(6, 4;, 3 normális eloszlású P (ξ 8 ξ 5 feltételes valószínűségét (.3. alapján számoljuk.
Megoldások Harmadik fejezet gyakorlatai 3.. gyakorlat megoldása ξ jelölje az első meghibásodásig eltelt időt. Akkor ξ N(6, 4;, 3 normális eloszlású P (ξ 8 ξ 5 feltételes valószínűségét (.3. alapján számoljuk.
A lineáris programozás alapfeladata Standard alak Az LP feladat megoldása Az LP megoldása: a szimplex algoritmus 2017/
 Operációkutatás I. 2017/2018-2. Szegedi Tudományegyetem Informatika Intézet Számítógépes Optimalizálás Tanszék 2. Előadás LP alapfeladat A lineáris programozás (LP) alapfeladata standard formában Max c
Operációkutatás I. 2017/2018-2. Szegedi Tudományegyetem Informatika Intézet Számítógépes Optimalizálás Tanszék 2. Előadás LP alapfeladat A lineáris programozás (LP) alapfeladata standard formában Max c
A lineáris programozás alapfeladata Standard alak Az LP feladat megoldása Az LP megoldása: a szimplex algoritmus 2018/
 Operációkutatás I. 2018/2019-2. Szegedi Tudományegyetem Informatika Intézet Számítógépes Optimalizálás Tanszék 2. Előadás LP alapfeladat A lineáris programozás (LP) alapfeladata standard formában Max c
Operációkutatás I. 2018/2019-2. Szegedi Tudományegyetem Informatika Intézet Számítógépes Optimalizálás Tanszék 2. Előadás LP alapfeladat A lineáris programozás (LP) alapfeladata standard formában Max c
Műszaki hőtan I. ellenőrző kérdések
 Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Dinamikus modellek felállítása mérnöki alapelvek segítségével
 IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
Termokémia. Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
FIZIKAI KÉMIA IV. Lente Gábor
 FIZIKAI KÉMIA I. Lente Gábor Ajánlott iroalom: P. W. Atkins: Fizikai kémia I-III. (ankönyvkiaó, Buaest, 2002) Keszei Ernő: Bevezetés a kémiai termoinamikába (htt://keszei.chem.elte.hu/fizkem1/ankonyv.f)
FIZIKAI KÉMIA I. Lente Gábor Ajánlott iroalom: P. W. Atkins: Fizikai kémia I-III. (ankönyvkiaó, Buaest, 2002) Keszei Ernő: Bevezetés a kémiai termoinamikába (htt://keszei.chem.elte.hu/fizkem1/ankonyv.f)
8. Belső energia, entalpia és entrópia ideális és nem ideális gázoknál
 8. első energia, entalpia és entrópia ideális és nem ideális gázoknál első energia első energia (U): a vizsgált rendszer energiája, DE nem tartozik hozzá - a teljes rendszer együttes mozgásából adódó mozgási
8. első energia, entalpia és entrópia ideális és nem ideális gázoknál első energia első energia (U): a vizsgált rendszer energiája, DE nem tartozik hozzá - a teljes rendszer együttes mozgásából adódó mozgási
Feladatok megoldásokkal a 9. gyakorlathoz (Newton-Leibniz formula, közelítő integrálás, az integrálszámítás alkalmazásai 1.
 Feladatok megoldásokkal a 9. gyakorlathoz (Newton-Leibniz formula, közelítő integrálás, az integrálszámítás alkalmazásai.). Feladat. Határozzuk meg az alábbi integrálokat: a) x x + dx d) xe x dx b) c)
Feladatok megoldásokkal a 9. gyakorlathoz (Newton-Leibniz formula, közelítő integrálás, az integrálszámítás alkalmazásai.). Feladat. Határozzuk meg az alábbi integrálokat: a) x x + dx d) xe x dx b) c)
{ } x x x y 1. MATEMATIKAI ÖSSZEFOGLALÓ. ( ) ( ) ( ) (a szorzás eredménye:vektor) 1.1. Vektorok közötti műveletek
 1. MAEMAIKAI ÖSSZEFOGLALÓ 1.1. Vektorok közötti műveletek Azok a fizikai mennyiségek, melyeknek nagyságukon kívül irányuk is van, vektoroknak nevezzük. A vektort egyértelműen megadhatjuk a hosszával és
1. MAEMAIKAI ÖSSZEFOGLALÓ 1.1. Vektorok közötti műveletek Azok a fizikai mennyiségek, melyeknek nagyságukon kívül irányuk is van, vektoroknak nevezzük. A vektort egyértelműen megadhatjuk a hosszával és
I. feladatsor i i i i 5i i i 0 6 6i. 3 5i i
 I. feladatsor () Töltse ki az alábbi táblázatot: Komplex szám Valós rész Képzetes rész Konjugált Abszolútérték + i i 0 + i i 5 5i 5 5i 6 6i 0 6 6i 6 5i 5 + 5i + i i 7i 0 7 7i 7 () Adottak az alábbi komplex
I. feladatsor () Töltse ki az alábbi táblázatot: Komplex szám Valós rész Képzetes rész Konjugált Abszolútérték + i i 0 + i i 5 5i 5 5i 6 6i 0 6 6i 6 5i 5 + 5i + i i 7i 0 7 7i 7 () Adottak az alábbi komplex
Lengyelné Dr. Szilágyi Szilvia április 7.
 ME, Anaĺızis Tanszék 2010. április 7. , alapfogalmak 2.1. Definíció A H 1, H 2,..., H n R (ahol n 2 egész szám) nemüres valós számhalmazok H 1 H 2... H n Descartes-szorzatán a következő halmazt értjük:
ME, Anaĺızis Tanszék 2010. április 7. , alapfogalmak 2.1. Definíció A H 1, H 2,..., H n R (ahol n 2 egész szám) nemüres valós számhalmazok H 1 H 2... H n Descartes-szorzatán a következő halmazt értjük:
KOVÁCS BÉLA, MATEMATIKA I.
 KOVÁCS BÉLA, MATEmATIkA I 19 XIX A HATÁROZOTT INTEGRÁL ALkALmAZÁSAI 1 TERÜLET ÉS ÍVHOSSZ SZÁmÍTÁSA Területszámítás Ha f az [a,b] intervallumon nemnegatív, folytonos függvény, akkor az görbe, az x tengely,
KOVÁCS BÉLA, MATEmATIkA I 19 XIX A HATÁROZOTT INTEGRÁL ALkALmAZÁSAI 1 TERÜLET ÉS ÍVHOSSZ SZÁmÍTÁSA Területszámítás Ha f az [a,b] intervallumon nemnegatív, folytonos függvény, akkor az görbe, az x tengely,
Fermi Dirac statisztika elemei
 Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Egy forgáskúp metszéséről. Egy forgáskúpot az 1. ábra szerint helyeztünk el egy ( OXYZ ) derékszögű koordináta - rendszerben.
 Egy forgáskúp metszéséről Egy forgáskúpot az 1. ábra szerint helyeztünk el egy ( OXYZ ) derékszögű koordináta - rendszerben. Az O csúcsú, O tengelyű, γ félnyílásszögű kúpot az ( XY ) sík itt két alkotóban
Egy forgáskúp metszéséről Egy forgáskúpot az 1. ábra szerint helyeztünk el egy ( OXYZ ) derékszögű koordináta - rendszerben. Az O csúcsú, O tengelyű, γ félnyílásszögű kúpot az ( XY ) sík itt két alkotóban
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Munka- és energiatermelés. Bányai István
 Munka- és energiatermelés Bányai István Joule tétele: adiabatikus munka A XIX. Sz. legnagyobb kihívása a munka Emberi erőforrás (rabszolga, szolga, bérmunkás, erkölcs?, ár!) Állati erőforrás (kevésbé erkölcssértő?,
Munka- és energiatermelés Bányai István Joule tétele: adiabatikus munka A XIX. Sz. legnagyobb kihívása a munka Emberi erőforrás (rabszolga, szolga, bérmunkás, erkölcs?, ár!) Állati erőforrás (kevésbé erkölcssértő?,
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Matematika III előadás
 Matematika III. - 3. előadás Vinczéné Varga Adrienn Debreceni Egyetem Műszaki Kar, Műszaki Alaptárgyi Tanszék Előadáskövető fóliák Vinczéné Varga Adrienn (DE-MK) Matematika III. 2016/2017/I 1 / 19 Skalármezők
Matematika III. - 3. előadás Vinczéné Varga Adrienn Debreceni Egyetem Műszaki Kar, Műszaki Alaptárgyi Tanszék Előadáskövető fóliák Vinczéné Varga Adrienn (DE-MK) Matematika III. 2016/2017/I 1 / 19 Skalármezők
Laplace-transzformáció. Vajda István február 26.
 Anlízis elődások Vjd István 9. február 6. Az improprius integrálok fjtái Tegyük fel, hogy egy vlós-vlós függvényt szeretnénk z I intervllumon integrálni, de függvény nincs értelmezve I minden pontjábn,
Anlízis elődások Vjd István 9. február 6. Az improprius integrálok fjtái Tegyük fel, hogy egy vlós-vlós függvényt szeretnénk z I intervllumon integrálni, de függvény nincs értelmezve I minden pontjábn,
Lagrange egyenletek. Úgy a virtuális munka mint a D Alembert-elv gyakorlati alkalmazását
 Lagrange egyenletek Úgy a virtuális munka mint a D Alembert-elv gyakorlati alkalmazását megnehezíti a δr i virtuális elmozdulások egymástól való függősége. (F i ṗ i )δx i = 0, i = 1, 3N. (1) i 3N infinitezimális
Lagrange egyenletek Úgy a virtuális munka mint a D Alembert-elv gyakorlati alkalmazását megnehezíti a δr i virtuális elmozdulások egymástól való függősége. (F i ṗ i )δx i = 0, i = 1, 3N. (1) i 3N infinitezimális
1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai
 3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
Differenciálegyenletek. Vajda István március 4.
 Analízis előadások Vajda István 2009. március 4. Függvényegyenletek Definíció: Az olyan egyenleteket, amelyekben a meghatározandó ismeretlen függvény, függvényegyenletnek nevezzük. Függvényegyenletek Definíció:
Analízis előadások Vajda István 2009. március 4. Függvényegyenletek Definíció: Az olyan egyenleteket, amelyekben a meghatározandó ismeretlen függvény, függvényegyenletnek nevezzük. Függvényegyenletek Definíció:
Függvények vizsgálata
 Függvények vizsgálata ) Végezzük el az f ) = + polinomfüggvény vizsgálatát! Értelmezési tartomány: D f = R. Zérushelyek: Próbálgatással könnyen adódik, hogy f ) = 0. Ezután polinomosztással: + ) / ) =
Függvények vizsgálata ) Végezzük el az f ) = + polinomfüggvény vizsgálatát! Értelmezési tartomány: D f = R. Zérushelyek: Próbálgatással könnyen adódik, hogy f ) = 0. Ezután polinomosztással: + ) / ) =
Visy Csaba Kredit 4 Heti óraszám 3 típus AJÁNLOTT IRODALOM. P. W. Atkins: Fizikai kémia I.
 A tárgy neve FIZIKAI KÉMIA 1. Meghirdető tanszék(csoport) SZTE TTK FIZIKAI KÉMIAI TANSZÉK Felelős oktató: Visy Csaba Kredit 4 Heti óraszám 3 típus Előadás Számonkérés Kollokvium Teljesíthetőség feltétele
A tárgy neve FIZIKAI KÉMIA 1. Meghirdető tanszék(csoport) SZTE TTK FIZIKAI KÉMIAI TANSZÉK Felelős oktató: Visy Csaba Kredit 4 Heti óraszám 3 típus Előadás Számonkérés Kollokvium Teljesíthetőség feltétele
1. Parciális függvény, parciális derivált (ismétlés)
 Operációkutatás NYME Gazdaságinformatikus mesterképzés El adó: Kalmár János (kalmar[kukac]inf.nyme.hu) Többváltozós széls érték számítás Parciális függvény, parciális derivált Széls érték korlátos zárt
Operációkutatás NYME Gazdaságinformatikus mesterképzés El adó: Kalmár János (kalmar[kukac]inf.nyme.hu) Többváltozós széls érték számítás Parciális függvény, parciális derivált Széls érték korlátos zárt
2. SZÉLSŽÉRTÉKSZÁMÍTÁS. 2.1 A széls érték fogalma, létezése
 2 SZÉLSŽÉRTÉKSZÁMÍTÁS DEFINÍCIÓ 21 A széls érték fogalma, létezése Azt mondjuk, hogy az f : D R k R függvénynek lokális (helyi) maximuma (minimuma) van az x 0 D pontban, ha van olyan ε > 0 hogy f(x 0 )
2 SZÉLSŽÉRTÉKSZÁMÍTÁS DEFINÍCIÓ 21 A széls érték fogalma, létezése Azt mondjuk, hogy az f : D R k R függvénynek lokális (helyi) maximuma (minimuma) van az x 0 D pontban, ha van olyan ε > 0 hogy f(x 0 )
Matematika II. 1 sin xdx =, 1 cos xdx =, 1 + x 2 dx =
 Matematika előadás elméleti kérdéseinél kérdezhető képletek Matematika II Határozatlan Integrálszámítás d) Adja meg az alábbi alapintegrálokat! x n 1 dx =, sin 2 x dx = d) Adja meg az alábbi alapintegrálokat!
Matematika előadás elméleti kérdéseinél kérdezhető képletek Matematika II Határozatlan Integrálszámítás d) Adja meg az alábbi alapintegrálokat! x n 1 dx =, sin 2 x dx = d) Adja meg az alábbi alapintegrálokat!
Kémiai egyensúly. Fizikai kémia előadások 6. Turányi Tamás ELTE Kémiai Intézet. ν j sztöchiometriai együttható
 émiai egyensúly Fizikai kémia előadások 6. Tuányi Tamás ELTE émiai Intézet Sztöchiometiai együttható ν sztöchiometiai együttható általános kémiai eakció: (a temokémiában használtuk előszö) ν A 0 ν A eaktánsa
émiai egyensúly Fizikai kémia előadások 6. Tuányi Tamás ELTE émiai Intézet Sztöchiometiai együttható ν sztöchiometiai együttható általános kémiai eakció: (a temokémiában használtuk előszö) ν A 0 ν A eaktánsa
sin x = cos x =? sin x = dx =? dx = cos x =? g) Adja meg a helyettesítéses integrálás szabályát határozott integrálokra vonatkozóan!
 Matematika előadás elméleti kérdéseinél kérdezhető képletek Analízis II Határozatlan integrálszámítás g) t = tg x 2 helyettesítés esetén mivel egyenlő sin x = cos x =? g) t = tg x 2 helyettesítés esetén
Matematika előadás elméleti kérdéseinél kérdezhető képletek Analízis II Határozatlan integrálszámítás g) t = tg x 2 helyettesítés esetén mivel egyenlő sin x = cos x =? g) t = tg x 2 helyettesítés esetén
 ö ü ö Ö ü ü ü ü Í Í Í Í ű ö ö ű ú ö ö ö ü ú ü ü ü ü ü ü ü ü ö ü ú ü ü ú ü ö ü ü ü ü ú ú ö ö ü ú Ö Ő Ü É Ó Ö Ó Ó ö ö ö ö É ü ö Í ö Ó Ó ű Ó Ó ű ü Ó Ó Í ü Ó Ü ü ü Ö ü ü Í ö ü ü ú ú ü ü ü ö ö ö ö ü ü ö ü ü
ö ü ö Ö ü ü ü ü Í Í Í Í ű ö ö ű ú ö ö ö ü ú ü ü ü ü ü ü ü ü ö ü ú ü ü ú ü ö ü ü ü ü ú ú ö ö ü ú Ö Ő Ü É Ó Ö Ó Ó ö ö ö ö É ü ö Í ö Ó Ó ű Ó Ó ű ü Ó Ó Í ü Ó Ü ü ü Ö ü ü Í ö ü ü ú ú ü ü ü ö ö ö ö ü ü ö ü ü
 ü Í Í Í Í Í Í Ö Í Í ú ő ü Ú ő Í Í Í ü ü ő ő ő ú Í ú ő Ó Í ő ü ű ű Í ő Í ű ű Í ú Í ú ü ú ő ő ü Ü Í Í ú Ó ű ő Í ő ő ü ő ő ő Í Í ü ü ú Ú ü ü ü ő ű ü ő ő ú ő ü ő ú ő ő ő ű ő ő ü ü ű ü ő ü ő ú ő ő ü ő ő ő ü
ü Í Í Í Í Í Í Ö Í Í ú ő ü Ú ő Í Í Í ü ü ő ő ő ú Í ú ő Ó Í ő ü ű ű Í ő Í ű ű Í ú Í ú ü ú ő ő ü Ü Í Í ú Ó ű ő Í ő ő ü ő ő ő Í Í ü ü ú Ú ü ü ü ő ű ü ő ő ú ő ü ő ú ő ő ő ű ő ő ü ü ű ü ő ü ő ú ő ő ü ő ő ő ü
 Ü É É ü ü ú ú Á ü ú ü ú ú ú ü ű É ü ü Ü É Á Á Á ú ü Ö Á ű ű ú ű É ú Ű ű ü ü ú ű ü ú ü ű ü ú ú ü Ú ú Ó ú ü ű ü Í ü ú ü ü ü ü ú ü ú ú ü ú ü ú ű ű ü Ü Ű ú ü ű ú ű ú ú ü Ü ü ü Ü ü Ü ü ü Ó Ö ü Ú ú ü ú ű ü ú
Ü É É ü ü ú ú Á ü ú ü ú ú ú ü ű É ü ü Ü É Á Á Á ú ü Ö Á ű ű ú ű É ú Ű ű ü ü ú ű ü ú ü ű ü ú ú ü Ú ú Ó ú ü ű ü Í ü ú ü ü ü ü ú ü ú ú ü ú ü ú ű ű ü Ü Ű ú ü ű ú ű ú ú ü Ü ü ü Ü ü Ü ü ü Ó Ö ü Ú ú ü ú ű ü ú
 Í Ú ü Á Á ü ű ü ü Ö É Ő ű ű ú ú ű É ű Í Ü É ü ü Ü úü ü ü Í ú ü Ő ű Í ű Í Ú Í Ú ü ú ű ű Ú ű É ú ú Í ü ü Ú Ú Ú Ú Á ű ü ü Í Ú Á Á ű ü ü Ú Á ű ü ú Ú ü ü Ú Ö É Ö ü ú ú ú ü ü ú Ö Ü ü Ü ú üü Á ú É Í É Í Í ű Á
Í Ú ü Á Á ü ű ü ü Ö É Ő ű ű ú ú ű É ű Í Ü É ü ü Ü úü ü ü Í ú ü Ő ű Í ű Í Ú Í Ú ü ú ű ű Ú ű É ú ú Í ü ü Ú Ú Ú Ú Á ű ü ü Í Ú Á Á ű ü ü Ú Á ű ü ú Ú ü ü Ú Ö É Ö ü ú ú ú ü ü ú Ö Ü ü Ü ú üü Á ú É Í É Í Í ű Á
 Ü Í ú Í É Ú É É Ú Ó ú ü ü ü ú ú Ő ú ú Í ú ú ú ú ű ú ú Á ú ú ú ú ú ú ü ú ü ű É ú ú ű ü ü ú ú ú ú ü ú ü Ú ü ú ú ü ű ú ü ü ü Í ü ú ú ü ú ü ü Ú ü ü ú Ú Á ü ű ü ű ú ú ü ü Ú ü ü ü ü ü ű ű ü ú ú Í ü ú ű ú Ú ü
Ü Í ú Í É Ú É É Ú Ó ú ü ü ü ú ú Ő ú ú Í ú ú ú ú ű ú ú Á ú ú ú ú ú ú ü ú ü ű É ú ú ű ü ü ú ú ú ú ü ú ü Ú ü ú ú ü ű ú ü ü ü Í ü ú ú ü ú ü ü Ú ü ü ú Ú Á ü ű ü ű ú ú ü ü Ú ü ü ü ü ü ű ű ü ú ú Í ü ú ű ú Ú ü
 É Ü ú ü Ü Ü ú Ü Ü ü ü Ü ú ú ú ű ü É Ü É Í Ó É ü ű Ü É ü ü É Ü Í Ó Ó Ó Ü Ó Í Ó Ó Ó Í Ü ü Ó Ö Ü ü ü Ü Ü ű Ü Ö Ü É Ü É Ü É É É É É ű Ó É Ö Ö ü ü ú ú ú Ü Ü Ü ú ú Ü ú ú ú ú ú ú Ü ú ú É Ú ü Ú Ú Í Í Ú É Ü Ü Í
É Ü ú ü Ü Ü ú Ü Ü ü ü Ü ú ú ú ű ü É Ü É Í Ó É ü ű Ü É ü ü É Ü Í Ó Ó Ó Ü Ó Í Ó Ó Ó Í Ü ü Ó Ö Ü ü ü Ü Ü ű Ü Ö Ü É Ü É Ü É É É É É ű Ó É Ö Ö ü ü ú ú ú Ü Ü Ü ú ú Ü ú ú ú ú ú ú Ü ú ú É Ú ü Ú Ú Í Í Ú É Ü Ü Í
 É É Ő ö ő ő ő ö ő ö É ő ő ő Ü ö Ó Ü ő ő ő Ü ö ö Ó ü ö ő ö ű ö ű ö ő ö Ö ö ö Ö ú ö Ü ü ő ő ő ö ő ü ő Ú ú Ü ő ö ő É ő ő ű Í ő ő ö É ö ő Ö ő É Í ő ö ő Ü ő Í ú Ó ü Ő ú ö ú ű ú ú Í Í Í Í Í ő ö ö ö ő ő Ö ö ü
É É Ő ö ő ő ő ö ő ö É ő ő ő Ü ö Ó Ü ő ő ő Ü ö ö Ó ü ö ő ö ű ö ű ö ő ö Ö ö ö Ö ú ö Ü ü ő ő ő ö ő ü ő Ú ú Ü ő ö ő É ő ő ű Í ő ő ö É ö ő Ö ő É Í ő ö ő Ü ő Í ú Ó ü Ő ú ö ú ű ú ú Í Í Í Í Í ő ö ö ö ő ő Ö ö ü
 Í Ö Ű ő í Ú Ó Á ú ó É ű ú ő ó ó ő ó ü Á ó ű Ű ő í Ó Á ű í Ó ó Ó Á ó ó í ó í ó Ö í ú Á É Í Í Ú í í űü í ő í É Ó í í Ú Ü ű Ú ő ő Ű ő ű ő Ú ő ő ő Ü ő ő ű ő í É í í Í Ő ő ó í í ő ő ú ő ő ó ó ő ő ú ő ő Ö ő
Í Ö Ű ő í Ú Ó Á ú ó É ű ú ő ó ó ő ó ü Á ó ű Ű ő í Ó Á ű í Ó ó Ó Á ó ó í ó í ó Ö í ú Á É Í Í Ú í í űü í ő í É Ó í í Ú Ü ű Ú ő ő Ű ő ű ő Ú ő ő ő Ü ő ő ű ő í É í í Í Ő ő ó í í ő ő ú ő ő ó ó ő ő ú ő ő Ö ő
 Í í ú ú ű í í í í í í Í í í í í í í í í í í í í Á í í í í í Ó ÜÜ Ü ü ü í Á Á Á Ö í Á Á í í ü í í í í í í Í í í í í í ü í í ü í í í í í í í í í í í í ü í í í í í í í í í í í í í í í í í í í í í ű ü í í
Í í ú ú ű í í í í í í Í í í í í í í í í í í í í Á í í í í í Ó ÜÜ Ü ü ü í Á Á Á Ö í Á Á í í ü í í í í í í Í í í í í í ü í í ü í í í í í í í í í í í í ü í í í í í í í í í í í í í í í í í í í í í ű ü í í
 Á Á ő É ö ö ő É ő ö ö ő ö É É Á ő É ő ö ö ö ő ő ő ő ő ő Ó É ő ő ő ő ü ő ő ü ü ö ö ő ő ú ű ű ö ő ö ú ő ü ő Ü ö ö ő ö ü ő ö ö ö ö ö ő ő ö ö ő ő ö ú ü ű ü ú ő É Á ő ő ö ő ő Ü ö ő ö ö ü ő ő ú ű ü ő Í ö ü ú
Á Á ő É ö ö ő É ő ö ö ő ö É É Á ő É ő ö ö ö ő ő ő ő ő ő Ó É ő ő ő ő ü ő ő ü ü ö ö ő ő ú ű ű ö ő ö ú ő ü ő Ü ö ö ő ö ü ő ö ö ö ö ö ő ő ö ö ő ő ö ú ü ű ü ú ő É Á ő ő ö ő ő Ü ö ő ö ö ü ő ő ú ű ü ő Í ö ü ú
 É É Í ü ü ü ű ü ü ü ü ü ü ú Í ű ú ü ű Á ú Ú ű űü Ú Ú É É ű Ú ü ú ű ú ű ü ű Í Í Ú É Ú Ú Ú Í ú ú Ú Ú É ü űü ü ü ü Ú ű ú ü ú ü ú ű ű ü ú ü ú ü Ú ü ú ü ü ú úü ú ú ü ú ü ú Ú ű ú ü ú Ú ű ü Ú ú ü ú ú ü ü ú ú
É É Í ü ü ü ű ü ü ü ü ü ü ú Í ű ú ü ű Á ú Ú ű űü Ú Ú É É ű Ú ü ú ű ú ű ü ű Í Í Ú É Ú Ú Ú Í ú ú Ú Ú É ü űü ü ü ü Ú ű ú ü ú ü ú ű ű ü ú ü ú ü Ú ü ú ü ü ú úü ú ú ü ú ü ú Ú ű ú ü ú Ú ű ü Ú ú ü ú ú ü ü ú ú
 ő ő Á ő ő ő ü ő ü ő ő ő ű ő ő ő ü ő ő ő ő ő ő ő ő ü ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ű ő ő ü ü ű ő ő ő Á ő ü Ó ő ő ő ő ő ü ő ü ő ő ő ő ü ő ő ü ő ő ü ő ü ő ü ő ő ő ő ő ü ő ü ü ő ő ő ű ő ű ü ü ő ő
ő ő Á ő ő ő ü ő ü ő ő ő ű ő ő ő ü ő ő ő ő ő ő ő ő ü ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ő ű ő ő ü ü ű ő ő ő Á ő ü Ó ő ő ő ő ő ü ő ü ő ő ő ő ü ő ő ü ő ő ü ő ü ő ü ő ő ő ő ő ü ő ü ü ő ő ő ű ő ű ü ü ő ő
 Í ü ú ü ü ü ü ú ű ű Á ü ü ű ü ű ű ü ü ü ü ü ü ü ű ű ű ű ű ü ű ü ű ü ü ű Ö ű ű ű ü Ö Í ü ű ü ű ű ű ű Í ü ű ű ü ű ű ü ű ü ű ü ű ű ü ű ű ű ű ű ü ü ü ű ü ű ü Í ű ü ű ű ű ü ű ü ü ű ü ű ü ű ü ű ű ű ű ü ü ü ü
Í ü ú ü ü ü ü ú ű ű Á ü ü ű ü ű ű ü ü ü ü ü ü ü ű ű ű ű ű ü ű ü ű ü ü ű Ö ű ű ű ü Ö Í ü ű ü ű ű ű ű Í ü ű ű ü ű ű ü ű ü ű ü ű ű ü ű ű ű ű ű ü ü ü ű ü ű ü Í ű ü ű ű ű ü ű ü ü ű ü ű ü ű ü ű ű ű ű ü ü ü ü
 Ü Ö Á Á Á Á É É Ü ű ű ű ű Á Ú Ü Ü ű Á Ú Ü Á Ü Ü Ü ű É Ü É Á ÜÜ Ü Á Ü Ü Ü Ü Ü Ü ű Ú ű ű ű Ü Ú Ü Ü ű Ü ű ű ű ű ű ű ű ű ű Ü Ü ű ű ű ű ű Ü Ü Ü Ú Ü Ü ű Ü Ü ű Ú Ú Ü ű ű Ü Ü Ü ű ű Ú ű Ő Ü Ü Ü Ü Ü Ö Ú ű Ú ű ű
Ü Ö Á Á Á Á É É Ü ű ű ű ű Á Ú Ü Ü ű Á Ú Ü Á Ü Ü Ü ű É Ü É Á ÜÜ Ü Á Ü Ü Ü Ü Ü Ü ű Ú ű ű ű Ü Ú Ü Ü ű Ü ű ű ű ű ű ű ű ű ű Ü Ü ű ű ű ű ű Ü Ü Ü Ú Ü Ü ű Ü Ü ű Ú Ú Ü ű ű Ü Ü Ü ű ű Ú ű Ő Ü Ü Ü Ü Ü Ö Ú ű Ú ű ű
 ö Ö ü ö ü ö Ö í ü ö ü ű ö ö í ö ö ö ö í ü í ö í ö ö ü ú ö í ö ö ö í ö ú ü ö ö ö ű ö ü í í ö í í ö ö ö ü Í í Ú ú ü ű ö í ű ö ö ö ü ú ö ö í ö í ú ö ö ö ö Ö ü Ö ű ö Ö ü ö ö ö ö ü ű ö í ú í Á ü í í ö ü ö Ö
ö Ö ü ö ü ö Ö í ü ö ü ű ö ö í ö ö ö ö í ü í ö í ö ö ü ú ö í ö ö ö í ö ú ü ö ö ö ű ö ü í í ö í í ö ö ö ü Í í Ú ú ü ű ö í ű ö ö ö ü ú ö ö í ö í ú ö ö ö ö Ö ü Ö ű ö Ö ü ö ö ö ö ü ű ö í ú í Á ü í í ö ü ö Ö
 ő ú É É ő ő ő ő ő ű ő ő ő ő ő ő ő ú ű ő ú ü ü ő ő ü ő ú ú ü ő ő ő Ó É ő ő ő ő ő ő ő ő ő ü ő ő ő Í ü ű ő ő Í ü ő úú ú ű ü É Ő Í ü ő ő ő ő ü ő ű ő ü ő ü Ű ü ü ú ü ü ü ü ú ő ő ő ő ű ő ő ú ü ő ü ő ő ű ü ő
ő ú É É ő ő ő ő ő ű ő ő ő ő ő ő ő ú ű ő ú ü ü ő ő ü ő ú ú ü ő ő ő Ó É ő ő ő ő ő ő ő ő ő ü ő ő ő Í ü ű ő ő Í ü ő úú ú ű ü É Ő Í ü ő ő ő ő ü ő ű ő ü ő ü Ű ü ü ú ü ü ü ü ú ő ő ő ő ű ő ő ú ü ő ü ő ő ű ü ő
 É É ő ő ő ő Ü ú ú ő ú ú ú ú Ú ő ű ú ű ú ő ú ú ú É É ú Ú ő ő ú ú Ó Ó ú ú ú ő É É Ü Ó É ő ű ú ő ő É ú ú ú ő ő ő ő ő ú ő ő ú ú ú ű ő ő ő ű ő ő ú ő ú ú Ó ő ú ú ú ú ú ő ú ő Ó ő ő ő ú ú ő ő ő ú ű ú ű ű ű ú ő
É É ő ő ő ő Ü ú ú ő ú ú ú ú Ú ő ű ú ű ú ő ú ú ú É É ú Ú ő ő ú ú Ó Ó ú ú ú ő É É Ü Ó É ő ű ú ő ő É ú ú ú ő ő ő ő ő ú ő ő ú ú ú ű ő ő ő ű ő ő ú ő ú ú Ó ő ú ú ú ú ú ő ú ő Ó ő ő ő ú ú ő ő ő ú ű ú ű ű ű ú ő
 Í ú Í Ú É Á É Á Ü Ü Ü É Ü Á É Á Á Í Á Á Á Á É É Á Á Ú É ú Í Ú Í Í ú ú ú Í ú ú ú ú Í ú Ú ú ú ú ú ú ú ú Í Í Í Í Ú Í ú Ú Ú Ö Í ú ú Ú É Ú É ú ű ú ú ú ú ú ú ű ű ú Í ú ú Ú É ú ú ű ú ú ú ú Ú ű Ú ú Ú ú Ú É ű ű
Í ú Í Ú É Á É Á Ü Ü Ü É Ü Á É Á Á Í Á Á Á Á É É Á Á Ú É ú Í Ú Í Í ú ú ú Í ú ú ú ú Í ú Ú ú ú ú ú ú ú ú Í Í Í Í Ú Í ú Ú Ú Ö Í ú ú Ú É Ú É ú ű ú ú ú ú ú ú ű ű ú Í ú ú Ú É ú ú ű ú ú ú ú Ú ű Ú ú Ú ú Ú É ű ű
 Ö Ú É ő ú Ü Ú É É ö ú ő ú ú ú ú ö ö ú ő ú ú ö ú Ő ö ő Ö Ú Ó ö ü ú Ü ö ú ü ü ú Ü Ú Ö Ú É ü Ú Ó ú Ú É É ő ú ő ő Ö ö Ö ü Ó Ú ú É ú ú ö úú ú ö Ü Ú É ö ő ő Ó É Ú Ú Ú Ó É É Ü É Ú Ú É ú ö ú ö ő Ú É ö ü ö ő ü
Ö Ú É ő ú Ü Ú É É ö ú ő ú ú ú ú ö ö ú ő ú ú ö ú Ő ö ő Ö Ú Ó ö ü ú Ü ö ú ü ü ú Ü Ú Ö Ú É ü Ú Ó ú Ú É É ő ú ő ő Ö ö Ö ü Ó Ú ú É ú ú ö úú ú ö Ü Ú É ö ő ő Ó É Ú Ú Ú Ó É É Ü É Ú Ú É ú ö ú ö ő Ú É ö ü ö ő ü
 ű ő Ü ő Ü ő ő ő ő ő ő ő Ó Ú Ú Ü Ú ű Ú Ö ő ő Ó ő Ú ő ő Ú Ú ű ő ő ő ő ő Ú ő ő ő ű ő Ú Ú ő ő ő ő ő Ü ő Ú ő ő ő ű ő Ú Ú ő Ú ő Ú ő Ü ő ő Ö ő ő Ú ő Ú Ú Ü ű Ö ű Ö Ó ő Ó Ú ő ő ő ű ő Ó Ú ő Ü Ú Ü ő ű ő ő ű ő ő ő
ű ő Ü ő Ü ő ő ő ő ő ő ő Ó Ú Ú Ü Ú ű Ú Ö ő ő Ó ő Ú ő ő Ú Ú ű ő ő ő ő ő Ú ő ő ő ű ő Ú Ú ő ő ő ő ő Ü ő Ú ő ő ő ű ő Ú Ú ő Ú ő Ú ő Ü ő ő Ö ő ő Ú ő Ú Ú Ü ű Ö ű Ö Ó ő Ó Ú ő ő ő ű ő Ó Ú ő Ü Ú Ü ő ű ő ő ű ő ő ő

