A tüdő neuroendokrin daganatainak patológiai diagnosztikája
|
|
|
- Zsigmond Kelemen
- 6 évvel ezelőtt
- Látták:
Átírás
1 ÖSSZEFOGLALÓ KÖZLEMÉNY 83 A tüdő neuroendokrin daganatainak patológiai diagnosztikája FILLINGER JÁNOS Országos Onkológiai Intézet, Daganatpatológiai Központ, Citopatológiai Osztály, Budapest Levelezési cím: Dr. Fillinger János, Országos Onkológiai Intézet, 1122 Budapest, Ráth György u fillinger@oncol.hu, tel.: /3741 Közlésre érkezett: március 5. Elfogadva: április 10. A tüdő neuroendokrin tumorainak heterogén csoportja megegyezés szerint négy fő típusba sorolható: típusos karcinoid (TC), atípusos karcinoid (AC), nagysejtes neuroendokrin karcinóma (LCNEC), valamint kissejtes karcinóma (SCLC). A besorolás alapja a sebészi reszekciós minták elemzése, mely az alapvető morfológiai jegyeken túl figyelembe veszi a 2 mm²-nyi területen számolt osztódásokat, a nekrózis jelenlétét vagy hiányát. Prognózis szerint a típusos karcinoid alacsony, az atípusos karcinoid intermedier, a kissejtes karcinóma és a nagysejtes neuroendokrin karcinóma magas grádusú, kifejezetten rossz prognózisú daganatok. A morfológiai diagnózist pontosítja a neuroendokrin immunhisztokémiai markerek használata. A szövettani diagnózis alapján a klinikai prognózis nem minden esetben egyértelmű. A Ki-67 meghatározása közelebb vihet a valós biológiai viselkedéshez. A diagnózis felállításához ma is az esetek több mint 2/3-ában kis minta (core-biopszia, bronhoszkópos biopszia, citológiai kenet) áll rendelkezésre. A reszekciós preparátumokra kidolgozott diagnosztikus algoritmusok csak korlátozottan alkalmazhatók ezekre a mintákra. Nem egy esetben a szövettani technikák széles tárházát kell alkalmazni a minta feldolgozása során, és még így is csak közelítő eredmény születik. A klinikus számára a mintákból nyerhető lehetséges információ ismerete segíthet a diagnosztikus és terápiás terv felállításában. Magy Onkol 62:83 89, 2018 Kulcsszavak: neuroendokrin tumorok, tüdő, core-biopszia, bronhoszkópia, citológia The heterogeneous group of lung neuroendocrine tumors are divided into four main types: typical carcinoid (TC), atypical carcinoid (AC), large cell neuroendocrine carcinoma (LCNEC), and small cell carcinoma (SCLC). Classification is based on the analysis of surgical resection specimens, which, in addition to basic morphological features, takes into account the mitotic count in 2 mm², the presence or absence of necrosis. According to prognosis, TC is low grade, AC is intermediate grade, while SCLC and LCNEC are high grade carcinomas with very poor prognosis. The morphological diagnosis can be refined by the use of neuroendocrine immunohistochemical markers. Based on the histological diagnosis, clinical prognosis is not always clear. Application of Ki-67 labeling can get closer to real biological behavior. Recently, more than 2/3 of the cases are small samples (core biopsy, bronchoscopic biopsy, cytological smears). Diagnostic algorithms developed for resection specimens has limited usage for these samples. In a single case, a wide range of histological techniques should be used in the processing of the sample, and still only an unsatisfactory result is obtained. Knowing the potential information content of the samples can help the clinician to set up a diagnostic and therapeutic plan. Filllinger J. Pathology of lung neuroendocrine tumors. Magy Onkol 62:83 89, 2018 Keywords: neuroendocrine tumors, lung, core biopsy, bronchoscopy, cytology
2 84 FILLINGER Rövidítések: TBNA: transzbronhiális vékonytű-aspiráció, TTP: transztorakális tűpunkció, EBUS: ultrahangvezérelt endoszkópos bronhoszkópos vizsgálat, DIPNECH: diffúz idiopátiás neuroendokrin sejtes hiperplázia, TC: típusos karcinoid, AC: atípusos karcinoid, LCNEC: nagysejtes neuroendokrin karcinóma, SCLC: kissejtes tüdőkarcinóma, NSCLC-NE: nem kissejtes karcinóma neuroendokrin immunhisztokémiai jelleggel, ROSE: on site (ágy melletti) citológiai vizsgálat, NGS: újgenerációs szekvenálás BEVEZETÉS A tüdődaganatok mintegy negyedét képező neuroendokrin tumorok között megtalálhatók a viszonylag jó életkilátásokkal bíró daganatok és az életet közvetlenül fenyegető rosszul differenciált karcinómák. A WHO évi beosztása szerint a neuroendokrin tumoroknak négy szubtípusa különböztethető meg. A típusos (TC) és atípusos karcinoid tumorok (AC) morfológiailag nagyon közel állnak a tüdő bronhiális hámjának neuroendokrin sejtjeihez. Szerkezetileg organoid struktúrák, trabekula-, rozettaképződés jellemzi őket. A mitózisok száma maximálisan 10/2 mm² lehet. Nekrózis teljes hiánya mellett fokális nekrózisok megengedettek. Bennük a neuroendokrin immunhisztokémiai markerek változó intenzitással egyértelműen pozitívak. A nagysejtes neuroendokrin karcinómát (LCNEC) a sejtmorfológia és a szerkezet közötti kettősség jellemzi. Sejtjei nem kissejtes karcinómára hasonlítanak, szerkezetében kiterjedt, térképszerű nekrózisokat mutató fészkek, rozettaképződés látható. A kissejtes karcinóma (SCLC) sejtjei neuroendokrin karakterűek, fészkeket, mezőket képeznek. A nekrózisok jelenléte változó. Utóbbi tumoroknál a mitózisszám igen magas, 70 90/2 mm² (1. táblázat). Immunhisztokémiai vizsgálatokkal a daganatok neuroendokrin eredete meghatározható, a reakciók az egyes karcinómákban változó erősségűek. A Ki-67-meghatározás a WHO 2015-ben kiadott kritériumai szerint nem befolyásolja 1. TÁBLÁZAT. A tüdő neuroendokrin tumorainak szövettani diagnosztikai kritériumai (WHO 2015) Típusos karcinoid (TC) Atípusos karcinoid (AC) Nagysejtes neuroendokrin karcinóma (LCNEC) Kissejtes karcinóma (SCLC) karcinoid morfológia <2 mitózis/2 mm² nincs nekrózis tumorméret >0,5 cm karcinoid morfológia 2 10 mitózis/mm² vagy nekrózis (akár pontszerű is) neuroendokrin szerkezeti morfológia, NSCLC sejtmorfológia >10 mitózis/2 mm² nagy zónaszerű nekrózis kis sejtek (3 limfocita) >10 mitózis/2 mm² nekrózisok a szövettani diagnózist. Értékelése ellentmondásos, számos szerző tör pálcát amellett, hogy a diagnosztikus algoritmusba való beillesztése információt nyújthat a prognózis megítéléséhez, klinikai használhatósága azonban nem egyértelmű (1 3). A fenti, sebészeti mintákra meghatározott hisztológiai definíciók alkalmazása biopsziás mintákra, citológiai kenetekre csak korlátozott, hiszen a mintában a tumor mennyisége kicsi, szerkezete nem ítélhető meg pontosan. A tüdő neuroendokrin tumorainak döntő többségét azonban ma is kis mintákból (biopszia, citológiai kenet) diagnosztizálják (4). A jelen dolgozat célja, hogy irodalmi adatokra, illetve saját tapasztalatra támaszkodva áttekintse a tüdő neuroendokrin daganatainak jellemzőit és az ezekből a kis mintákra alkalmazható diagnosztikus algoritmusokat, valamint megmutassa a diagnózisból a klinikum számára kinyerhető, a terápiás döntést segítő információt. MINTAVÉTELI TECHNIKÁK ÉS FELDOLGOZÁSI LEHETŐSÉGEK A tüdő invazív vizsgálómódszerei közül leggyakrabban a bronhoszkópos eljárás használatos. Segítségével szövettani biopszia, kefecitológiai minta, illetve transzbronhiális vékonytű-aspiráció (TBNA) végezhető. Utóbbi mintavételi eljárás segítségével citológiai kenet, valamint párhuzamosan sejtblokk készíthető (1. ábra). A Magyarországon még csak korlátozottan elérhető kriobiopsziás módszerrel 0,5 1 cm kiterjedésű szövetdarabok is nyerhetők, melyek segítségével a patológus részletesebb képet kaphat a vizsgált daganatról. A diagnosztikus pontosság növelésére, valamint a minta tumormennyiségének meghatározására használható az ágy melletti (ROSE) citológiai vizsgálat, melyet elsősorban ultrahangvezérelt (EBUS) mintavétel mellett alkalmaznak leginkább (5). A transztorakális módszerek közül a képalkotó kontroll mellett végzett, kevéssé elterjedt vékonytű-aspirációt, valamint a Nordenström-tűvel végzett punkciót (TTP) kell megemlíteni. Előbbivel kenet és sejtblokk, utóbbival kizárólag korlátozott számú kenet készíthető. Egyre elterjedtebb a CT-vezérelt core-biopsziás mintavétel. Előnye, hogy a nyert szövethenger találati pontossága magas, illetve lényegesen több tumorsejtet tartalmazhat, mint a bronhoszkópos biopszia. Hátránya, hogy a kivitelezése gyakorlott szakembert igényel, valamint a lehetséges szövődmények elkerülésére a mintavételt követően kórházi megfigyelés szükséges. A TBNA, TTP, hörgőkefekeneteken kívül bronhoszkópos biopsziás mintákról is készíthető úgynevezett lenyomati kenet. Egy-egy mintavételi módszerrel általában két-három kenet készíthető. A keneteket a vizsgáló patológus igényei szerint nedvesen vagy szárazon lehet fixálni. A fixálási mód meghatározza a későbbi festési metodikát. A nedvesen fixált keneten hematoxilin-eozin vagy Papanicolaou szerinti festés történik leginkább, a szárazon fixált kenetek Giemsa szerint festhetők. A feldolgozott keneteken a későbbiekben immuncitokémiai/immunhisztokémiai vizsgálatok, valamint in situ hibridizációs (FISH) eljárások alkalmazhatók. Ezen eljárások pontossága nagyban függ PROFESSIONAL PUBLISHING HUNGARY
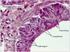
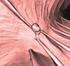
3 A BIOPSZIÁS MINTÁK DIAGNOSZTIKAI KORLÁTAI 85 a b c 1. ÁBRA. (a) TBNA-, FNA-aspirátum gyűjtése formalinba, (b) az elkészült sejtblokk, (c) a sejtblokkból készült metszet átnézeti képe sejtcsoportokkal, valamint a tűbe került vér öntvényeivel a kenetek minőségétől, melyet a megfelelő fixálás, valamint a sejtréteg vastagsága mellett a hordozó tárgylemez minősége is befolyásol. Ezért több laboratórium a kenetek elkészítését immunhisztokémiai vizsgálatokra alkalmas tárgylemezekre kéri. Mind a klinikum, mind a patológus számára fontos, hogy a nyert mintákból a tumorra vonatkozóan maximális mennyiségű információhoz jusson. Tapasztalataink szerint bármelyik vizsgálómódszert alkalmazzuk, maximum 3 darab, diagnózishoz elegendő mennyiségű tumorsejtet tartalmazó kenet nyerhető. Ezt a három kenetet kell úgy felhasználni, hogy azokon az alapfestésen túl a diagnózishoz szükséges számban az immuncitokémiai/immunhisztokémiai vizsgálatok is elvégezhetők legyenek. Az aspirációs technika (EBUS, TBNA) alkalmazásával sejtblokk készítésére alkalmas mennyiségű sejthez lehet jutni, amelyben nagyobb valószínűséggel lesz elegendő tumorsejt. A sejtblokk átmenetet képez a citológiai és szövettani minták között. Mikroszkópos képét tekintve hordozza a citológiai minták jellegzetességeit, vizsgálhatósága (immunhisztokémia, molekuláris patológia) a szövettani mintákéhoz áll közelebb (5). A bronhoszkópos és core-biopsziás minták szövettani minták, melyek általában megfelelő mennyiségű tumorsejtet tartalmaznak. A mintavétel sikerét azonban jelentősen befolyásolják a körülmények: a vizsgálandó beteg fizikai állapota, társbetegségei, a vizsgáló orvos gyakorlottsága, a vizsgálat során alkalmazott aneszteziológia. Optimális körülmények között bronhoszkópiával 3-4, egy-másfél mm nagyságú szövetminta kerül kicsípésre, core-biopsziás technikával egy-két, kb. 1 cm hosszúságú, 1 mm vastagságú szövethenger nyerhető (6). A minták feldolgozásakor figyelmet kell fordítani a fixálási időre, mely optimális esetben nem haladhatja meg a 48 órát. A minta későbbi értékelhetőségét a fixáló folyadék (pufferelt 8%-os formaldehid) minősége is befolyásolja. A nem megfelelő, illetve túl hosszú ideig alkalmazott fixálószerrel a mintában lévő daganatsejtek DNS-, RNS-tartalma károsodik, gátolva ezzel a további molekuláris patológiai vizsgálatokat. IMMUNHISZTOKÉMIAI/IMMUNCITOKÉMIAI VIZSGÁLATOK A morfológiai szerkezet elemzésére készített alapfestésen túl immunhisztokémiai/immuncitokémiai vizsgálatokkal a neuroendokrin karakter kerül megállapításra. A leggyakrabban használt markerek a szinaptofizin, a kromogranin A és a CD56. A szinaptofizin és a kromogranin A esetében a daganatok növekvő dedifferenciálódását az expresszió csökkenése, illetve eltűnése követi. Az újabban próbált, magreakciókat adó hash1 általában nem, vagy gyengén festődik karcinoid tumorokban és erős expressziót mutat high grade neuroendokrin karcinómákban. Egy másik, magfestést adó marker, az inzulinómaasszociált protein 1 (INSM1) konzisztensen festi az összes neuroendokrin daganatot (7). Az utóbbi marker előnye, hogy a rosszul differenciált neuroendokrin karcinómákban is észlelhető biztos expresszió akkor is, amikor a daganat más neuroendokrin markerekkel nem, vagy kétes értékű reakciót mutat. Immunhisztokémiai vizsgála-
4 86 FILLINGER tokkal a tüdő neuroendokrin tumorainak esetében a primer vagy szekunder jelleg biztonsággal nem határozható meg. A rendelkezésre álló reagensekkel (TTF1, CDX2, PAX8, CD5) a tumorok bizonytalanul vagy ellentmondásosan festődnek. A kérdés eldöntésében leggyakrabban a radiológiai kép, illetve a klinikai kórlefolyás ismerete segíthet. Az SSTR2, SSTR5 szomatosztatinreceptorok expressziójának mértéke fordított arányban van a NET differenciáltsági fokával. Ugyanakkor a specifikus terápia indikációját Magyarországon jelenleg a karcinoid szindróma jelenti, ami a neuroendokrin tüdődaganatok esetében nem gyakori (8 10). PROGNOSZTIKA A WHO által 2015-ben meghatározott diagnosztikai kritériumok alapján megállapított daganat szöveti típusai nem egy esetben másképp viselkednek, mint az klinikailag elvárható lenne. Ennek megfelelően a klinikumban már régóta nagy igény mutatkozik arra, hogy a patológus a szövettani leletben valamilyen módon jelezze a daganat várható viselkedését. Prognózis szempontjából a tumorok aktivitását a mitózisok száma viszonylag jól jellemzi. Ezen alapul a szövettani jellegzetességeken kívül a neuroendokrin tüdődaganatok szövettani beosztása is. A Ki-67 a sejtciklusban lévő daganatsejteket tudja immunhisztokémiai módszerrel kimutatni, ezért alkalmas lehet a daganat proliferációs potenciáljának meghatározására. Az immunhisztokémiai reakcióval a tumor proliferációs, aktív gócpontjai, az úgynevezett hot spotok pontosabban meghatározhatók. A Ki-67-index alkalmazásával értelemszerűen eltérés mutatkozik az osztódó alakok számolásán alapuló prognosztikai meghatározáshoz képest. Mindkét módszer alkalmazásának gyenge pontja a reprodukálhatóság. Hasznos volna az emlőrákok esetében elvégzett technológiai és értékelési eljárások összevetése és standardizálása (11). Használhatósága jelenleg is vizsgálatok tárgyát képezi, azonban egyes guideline-okban (ENETS 2015) már megjelenik (12 15). A Ki-67 százalékos értéke alapján a mitózisindex meghatározása (osztódás/mm 2 ), a nekrózis jelenlétének megítélése mellett, amik a szöveti típus megállapítását szolgálják, a tüdő neuroendokrin daganatait 4 fő prognosztikai csoportba lehet sorolni (2. táblázat). A Ki-67- index finomabb érzékenységének megfelelően az egyes szöveti típusokba besorolt tumorok klinikai viselkedése jobban korrelál a klinikai tapasztalattal. A csoportok alkalmazásával magyarázható például a néhány esetben észlelt szokatlanul hosszú túlélést mutató kissejtes karcinóma jelenléte (16). GENETIKAI ELTÉRÉSEK A tüdőben lévő neuroendokrin daganatok genetikai vizsgálata egyértelműen két csoportra osztotta a tumorokat. A karcinoidcsoportban a dohányzással összefüggő 3p-deléció ritka, szemben a karcinómacsoportéval, ahol is a kissejtes karcinómákban kifejezetten magas. A sporadikus karcinoid tumorokban a 11q karon (11q13), a MEN1 gén lókuszában a heterozigótaság elvesztése (LOH) mutatható ki gyakrabban, ami az ún. tumorletekben hiányzik. Tekintettel arra, hogy 2. TÁBLÁZAT. A WHO 2015 kritériumai szerint megállapított szövettani típusok (TC, AC, LCNEC, SCLC) Ki-67-index alapján kialakított csoportjai és lehetséges terápiás vonatkozásai Tumortípus Ki-67-index Terápiás lehetőségek I. TC, AC <5% sebészi kezelés szomatosztatinanalógok mtor-gátlók II. ritkán TC, AC, LCNEC (karcinoid típus) III. AC, LCNEC (NSCLC típus), ritkán SCLC IV. LCNEC (SCLC típus), SCLC 5 25% sebészi kezelés szomatosztatinanalógok egyértelmű javaslat nincs 25 60% sebészi kezelés kissejtes cc. protokoll nem kissejtes cc. protokoll célzott terápia (EGFR) % sebészi kissejtes cc. protokoll a tumorlet bizonyos lokalizációjú karcinoidok prekurzorának tekinthető, feltételezhető, hogy az eltérés a tumorgenezis késői fázisában jelenik meg (17). A nagysejtes neuroendokrin karcinóma (LCNEC) molekuláris szempontból is kettősséget mutat. Genetikai eltérések szerint két nagyobb csoportra különül. Az egyikben olyan gének mutációi gyakoriak, melyek kissejtes karcinómára (SCLC) jellemzőek, a másikban nem kissejtes karcinómákra (NSCLC) jellemző génmutációk gyakoribbak. Ez a prognózisban is megfigyelhető, és felveti annak lehetőségét, hogy a nem kissejtes csoportba sorolható LCNEC esetén nem kissejtes karcinóma szerinti terápiát válasszanak (18 20). A neuroendokrin tüdőtumorok genetikai vizsgálata kezdi feltárni a daganatok eredetét, prekurzorait. Nyilvánvalóvá vált, hogy a karcinoidok és a neuroendokrin karcinómák eltérő fejlődési útvonalon alakulnak ki, és előbbiek nem prekurzorai az utóbbiaknak. Úgy tűnik, tumorgenezis szempontjából fontos a lokalizáció. A DIPNECH és a tumorletek a perifériás karcinoidok prekurzorainak tekinthetők, a centrálisan elhelyezkedőknek azonban nem. Hasonló módon a neuroendokrin sejtekből csak centrálisan megjelenő SCLC származhat. Ugyanakkor egyes genetikai vizsgálati eredmények felvetik annak lehetőségét, hogy a tüdői SCLC-k a II-es típusú pneumocitákból is kiindulhatnak mind perifériás, mind centrális elhelyezkedésben. Ezek a teóriák azonban a neurendokrin daganatok genetikai tartalmának újgenerációs szekvenálás (NGS) módszerével való feltárása eredményeképpen jelentősen módosulhatnak (21, 22). DIAGNOSZTIKA A tüdő neuroendokrin tumorainak diagnosztikájában kulcsfontosságú a morfológiai megjelenés, a tumorban észlelhető mitózisok száma, valamint a nekrózisok jelenléte, illetve a neuroendokrin jelleg immunhisztokémiai igazolása. A citológiai és biopsziás minták esetében ezek a kritériumok nem érvényesülhetnek teljes egészében (23). PROFESSIONAL PUBLISHING HUNGARY
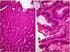
5 A BIOPSZIÁS MINTÁK DIAGNOSZTIKAI KORLÁTAI 87 a a neuroendokrin karakter igazolása mellett a kizárandó egyéb tumor szöveti típusát, a keneteken biztonsággal elvégezhető reakciókat (membrán/plazma vagy magreakció). Biopsziás minták (bronhoszkópos biopszia, core-biopszia) A biopsziás minták diagnosztikus tumorsejttartalma sejttől több száz sejtig terjedhet. A daganatsejtek általában normális szöveti környezetben helyezkednek el, viszonyítási alapot adva a tumorszerkezet elemzéséhez. Ennek megfelelően a neuroendokrin szerkezet és sejtmorfológia felismerhető. A minták zöme a mitózisszám megállapításához nem tartalmaz 2 mm²-nyi tumoros területet. Nekrózisok sem jelennek meg minden esetben. b Sejtblokk Az aspiráció (TBNA, EBUS) után 2 5 millió sejt marad a tűben és a fecskendő kónuszában (25). Ennek átmosásával nyert sejtszuszpenzió képezi a sejtblokk alapját (2. ábra). A sejtek mellett a tűvastagságtól függően kisebb szövetdarabok is bekerülhetnek a fixáló folyadékba. A metszetekben látható sejtek a citológiai mintákhoz hasonlóan mutatják a neuroendokrin sejtmorfológiát, ugyanakkor megfelelő mennyiségű sejt esetén további immunhisztokémiai reakcióval igazolható a neuroendokrin karakter, illetve proliferációs markerrel (Ki-67) pontosítható a differenciáltsági fok (low grade/high grade) (3. ábra). a 2. ÁBRA. (a) Karcinoid tumor citológiai képe: szétszóródott, monoton megjelenésű sejtek (Giemsa-festés, 200 ); (b) kissejtes karcinóma citológiai képe: szorosan illeszkedő polimorf tumorsejtek (Giemsa-festés, 400 ) Citológiai minták (hörgőkefe, TBNA, lenyomati kenetek, mellkasfolyadékok) Korlátozott számú, általában két-három tárgylemezen elhelyezkedő tumorsejtek kisebb csoportokat képeznek, zömében azonban elszóródott sejtalakokat mutatnak. A morfológiai megjelenés elsősorban a magok szerkezeti és alakbeli megítélésére szorítkozik, osztódó alakok ritkán azonosíthatók. Fokális nekrózisok felismerése bizonytalan (24). A kenetkészítés következtében létrejövő sejtkárosodások sok esetben korlátozzák a magmorfológia biztonságos megítélését. A magok szerkezete és morfológiája azonban nem teljes mértékben specifikus a neuroendokrin tumorokra. Számos, tüdőben gyakori daganat (nem kissejtes karcinóma) mutathat hasonló sejtmag-morfológiát. Ez főleg a nagysejtes neuroendokrin karcinóma esetében zavaró. A felhasználni kívánt immunhisztokémiai reakciók kiválasztásakor figyelembe kell venni b 3. ÁBRA. a) Karcinoid tumor sejtblokkban (H&E festés, 200 ); (b) kromogranin A-pozitív karcinoid tumorsejtek (immunhisztokémia, 400 )
6 88 FILLINGER Folyékony biopszia A keringő SSTR5 meghatározása mellett új lehetőséget jelent a daganatokra jellemző mrns vérből történő meghatározása. Vizsgálatok igazolták, hogy neuroendokrin tumorokban (elsősorban karcinoid tumor) gyakori gének transzkripciós termékei korrelálnak a vérben észlelhető transzkripciós termékekkel. Így lehetőség van tumorazonosításra, a tumorprogresszió követésére (26, 27). MEGBESZÉLÉS A tüdő neuroendokrin daganatainak diagnosztikájához rendelkezésre áll a sebészi mintákra kidolgozott kritériumrendszer (28). Az e kritériumok alapján felállított diagnózisok azonban nem minden esetben reprodukálhatók egyértelműen. Ez különösen problematikus a határterületi daganatoknál, mint a TC vs. AC, illetve az AC vs. SCLC, amikor a patológiai diagnózisra nem egy esetben a klinikai kórlefolyás rácáfol. Ilyenkor szokás agresszíven viselkedő típusos karcinoidról (TC) vagy hosszú túlélést mutató kissejtes karcinómáról beszélni (29). Nyilvánvaló, hogy e diagnosztikus bizonytalanság a kis biopsziák és citológiai minták esetében a leggyakoribb. A protokollokban megadott, viszonylag kicsi számítási terület (2 mm²) azt feltételezi, hogy a daganat egységes, minden részletében azonos módon viselkedik. A vizsgáló orvos szubjektivitásának, egyéni tapasztalatának függvénye, hogy mely daganatterületet választja a mitózisszám megállapítására és a nekrózisok megítélésére. Arra vonatkozóan megoszlanak a vélemények, hogy hány területet kell átvizsgálni, és mi a teendő akkor, ha a vizsgált területek között pl. mitózisszámban nagyobb eltérés mutatkozik. Immunhisztokémiai vizsgálatokkal a neuroendokrin karaktert szükséges igazolni, kiegészítő vizsgálatokkal egyéb, főleg nem kissejtes karcinómákat kell kizárni. A reakciókat panelban végzik, mely tartalmazza a neuroendokrin és az egyéb tumorokra vonatkozó markereket. Mindezek mellett egyre gyakrabban kerül alkalmazásra a Ki-67 proliferációs marker, melynek értékelésétől a prognózis pontosabb megítélését várják annak ellenére, hogy az eredmények értékelése még mindig bizonytalan. A neuroendokrin tüdődaganatok diagnosztikájához vett kis minták szövettani és/vagy citológiai feldolgozást tesznek lehetővé. E minták méretüknél és sebészi mintához képest mérsékelt tumorsejttartalmuknál fogva csak korlátozottan felelnek meg a sebészi mintákra kidolgozott diagnosztikai algoritmusoknak. Ugyanezen okból az immunhisztokémiai vizsgálatok kivitelezése és értékelése sem mindig egyértelmű e mintákban. A tumorok nem egyenletes immunreaktivitása álnegatív eredményeket hozhat. A morfológiai kép alapján a típusos karcinoid elkülönítése az atípusos karcinoidtól alig lehetséges. A biopsziás mintákon a Ki-67 meghatározása sem képes pontos különbséget tenni a két tumortípus között, mivel nem áll rendelkezésre elegendő tumorsejt az értékeléshez. A mintába esetlegesen bekerülő aktív tumorterület (hot spot) nem biztos, hogy reprezentálja a daganat egészét, és az így meghatározott magasabb Ki-67-index rosszabb prognózisú tumor (AC) szöveti diagnózisát adhatja. Kissejtes karcinóma esetében tovább rontja az immunhisztokémiai reaktivitást a sejtek nagyfokú sérülékenysége. A nagysejtes neuroendokrin karcinóma citológiai és szerkezeti kettőssége egyáltalán nem tud érvényesülni. A nem kissejtes karcinómákra jellemző sejtmorfológia miatt e tumortípus a pozitív NE markerek miatt megkülönböztethetetlen a neuroendokrin immunhisztokémiai jelleggel bíró nem kissejtes karcinómától (NSCLC-NE). Citológiai mintákban a low grade és high grade neuroendokrin tumorok általában elkülöníthetők (karcinoid vs. karcinóma). Immunhisztokémiai vizsgálatokkal a daganatok neuroendokrin eredete igazolható. A spektrum szélein levő daganatok (AC/ TC és SCLC/ LCNEC) azonban egymástól már nehezen különíthetők el. Különösen citológiai kenetek esetében színesíti a képet, hogy a mintát értékelő patológus gyakorlottsága mellett a kenetek minősége alapvetően befolyásolja a diagnózist. ÖSSZEFOGLALÁS A tüdő neuroendokrin daganatainak diagnosztizálása, más típusú tüdőrákokhoz hasonlóan, ma is döntően citológiai vagy biopsziás mintákból történik. A szokásos citológiai és szövettani feldolgozás mellett szerepet kaphat a diagnosztikában az aspirációs minták sejtblokkban való feldolgozása. Az egyes minták viszonylag korlátozott tumorsejttartalma miatt a sebészi mintákra kidolgozott algoritmusok közvetlenül nem használhatók. A biopsziák és kenetek értékelése gyakorlottságot igényel, különös tekintettel a citológiai mintákra (29). A minta minőségétől függően immunhisztokémiai reakciókkal, Ki-67 proliferációs marker segítségével pontosítható a morfológiai képnek megfelelően felállított diagnózis. A szöveti kép alapján biztonsággal elkülöníthető a karcinoidcsoport a karcinómacsoporttól. Nem állnak azonban rendelkezésre olyan vizsgálómódszerek, amelyekkel szubtípusokra szétválasztható a két csoport. A karcinoidcsoporton belüli szétválasztásnak (TC/AC) klinikai relevanciája kétséges, mivel az esetek túlnyomó többsége műtétre kerül (30, 31). A karcinómacsoportban (LCNEC/SCLC) a nagysejtes neuroendokrin karcinóma sejtmorfológiai és szerkezeti kettőssége kis mintában nem érvényesül, míg biopsziás mintákban immunhisztokémiai vizsgálatokkal és a Ki-67-index meghatározásával pontosítható a diagnózis, de a definitív diagnózis felállítása nem lehetséges. Citológiai mintákban az NE karakter igazolása mellett a magas Ki-67-index utalhat rákra, de a pontos szöveti diagnózis ebben az esetben is lehetetlen. A kissejtes karcinóma sejtjeinek nagyfokú sérülékenysége miatt a neuroendokrin sejtmorfológia nem mindig nyilvánvaló. A sejtek hisztogenezisének megállapításához immunhisztokémiai panel ajánlott, mely tartalmazza a differenciáldiagnosztika szempontjából szóba jövő daganatokra (limfóma, laphámkarcinóma, rosszul differenciált adenokarcinóma) specifikus reagenseket. A molekuláris vizsgálatok fejlődésével lassan ismertté válnak a karcinoid- és karcinómacsoportokat szétválasztó génhibák. Emellett megfelelő markerek segítségével folyékony biopsziából is azonosíthatók lesznek ezek a tumorok, illetve klinikai viselkedésük is követhető lesz. PROFESSIONAL PUBLISHING HUNGARY
7 A BIOPSZIÁS MINTÁK DIAGNOSZTIKAI KORLÁTAI 89 IRODALOM 1. Travis W, Brambilla, Burke A, et al. WHO Classification of Tumours of the Lung, Pleura, Thymus and Heart, Forth Ed. World Health Organization Classification of Tumours. IARC Press, Lyon Caplin ME, Baudin E, Ferolla P, et al. Pulmonary neuroendocrine (carcinoid) tumors: European Neuroendocrine Tumor Society expert consensus and recommendations for best practice for typical and atypical pulmonary carcinoids. ENETS consensus conference participants. Ann Oncol 26: , Pelosi G, Sonzogni A, Harari S, et al. Classification of pulmonary neuroendocrine tumors: new insights. Transl Lung Cancer Res 6: , Travis WD, Brambilla E, Noguchi M, et al. Diagnosis of lung cancer in small biopsies and cytology: implications of the 2011 International Association for the Study of Lung Cancer/American Thoracic Society/European Respiratory Society classification. Arch Pathol Lab Med 137: , Jain D, Allen TC, Aisner DL, et al. Rapid on-site evaluation of endobronchial ultrasound-guided transbronchial needle aspirations for the diagnosis of lung cancer: a perspective from members of the Pulmonary Pathology Society. Arch Pathol Lab Med 142: , Marchianò AV, Cosentino M, Di Tolla G, et al. FNA and CNB in the diagnosis of pulmonary lesions: a single-center experience on 665 patients, comparison between two periods. Tumori 103: , Fujino K, Motooka Y, Hassan WA, et al. Insulinoma-associated protein 1 is a crucial regulator of neuroendocrine differentiation in lung cancer. Am J Pathol 185: , Thunnissen E, Borczuk AC, Flieder DB, et al. the use of immunohistochemistry improves the diagnosis of small cell lung cancer and its differential diagnosis. An international reproducibility study in a demanding set of cases. J Thorac Oncol 12: , Travis WD, Brambilla E, Nicholson AG. Testing for neuroendocrine immunohistochemical markers should not be performed in poorly differentiated NSCCs in the absence of neuroendocrine morphologic features according to the 2015 WHO classification. J Thorac Oncol 11:e26 27, Marchevsky AM, Wick MR. Diagnostic difficulties with the diagnosis of small cell carcinoma of the lung. Semin Diagn Pathol 32: , Ács B, Kulka J, Kovács KA, et al. Comparison of 5 Ki-67 antibodies regarding reproducibility and capacity to predict prognosis in breast cancer. Human Pathol 65:31 40, Fabbri A, Cossa M, Sonzogni A, et al. Ki-67 labeling index of neuroendocrine tumors of the lung has a high level of correspondence between biopsy samples and surgical specimens when strict counting guidelines are applied. Virchows Arch 470: , Pelosi G, Rindi G, Travis WD, Papotti M. Ki-67 antigen in lung neuroendocrine tumors: unraveling a role in clinical practice. J Thorac Oncol 9: , Pelosi G, Pattini L, Morana G, et al. Grading lung neuroendocrine tumors: Controversies in search of a solution. Histol Histopathol 32: , Swarts DR, Rudelius M, Claessen SM, et al. Limited additive value of the Ki-67 proliferative index on patient survival in World Health Organization-classified pulmonary carcinoids. Histopathology 70: , Rindi G, Klersy C, Inzani F, et al. Grading the neuroendocrine tumors of the lung: an evidence-based proposal. Endocr Relat Cancer 21:1 16, Swarts DR, Van Neste L, Henfling ME, et al. An exploration of pathways involved in lung carcinoid progression using gene expression profiling. Carcinogenesis 34: , George J, Walter V, Peifer M, et al. Integrative genomic profiling of largecell neuroendocrine carcinomas reveals distinct subtypes of high-grade neuroendocrine lung tumors. Nat Commun 9:1048, Rekhtman N, Pietanza CM, Sabari J, et al. Pulmonary large cell neuroendocrine carcinoma with adenocarcinoma-like features: napsin A expression and genomic alterations. Mod Pathol 31: , Rekhtman N, Pietanza MC, Hellmann MD, et al. Next-generation sequencing of pulmonary large cell neuroendocrine carcinoma reveals small cell carcinoma-like and non-small cell carcinoma-like subsets. Clin Cancer Res 22: , Swarts DR, Ramaekers FC, Speel EJ. Molecular and cellular biology of neuroendocrine lung tumors: evidence for separate biological entities. Biochim Biophys Acta 1826: , Pelosi G, Bianchi F, Dama E, et al. Most high-grade neuroendocrine tumours of the lung are likely to secondarily develop from pre-existing carcinoids: innovative findings skipping the current pathogenesis paradigm. Virchows Arch 462: , Wick MR, Marchevsky AM. Neuroendocrine neoplasms of the lung: Concepts and terminology. Semin Diagn Pathol 32: , Layfield LJ, Baloch Z, Elsheikh T, et al. Standardized terminology and nomenclature for respiratory cytology: The Papanicolaou Society of Cytopathology guidelines. Diagn Cytopathol 44: , Rajer M, Kmet M. Quantitative analysis of fine needle aspiration biopsy samples. Radiol Oncol 39: , Childs A, Vesely C, Ensell L, et al. Expression of somatostatin receptors 2 and 5 in circulating tumour cells from patients with neuroendocrine tumours. Br J Cancer 115: , Kidd M, Modlin IM, Drozdov I, et al. A liquid biopsy for bronchopulmonary/ lung carcinoid diagnosis. Oncotarget 9: , den Bakker MA, Thunnissen FB. Neuroendocrine tumours: challenges in the diagnosis and classification of pulmonary neuroendocrine tumours. J Clin Pathol 66: , Pelosi G, Fabbri A, Cossa M, et al. What clinicians are asking pathologists when dealing with lung neuroendocrine neoplasms? Semin Diagn Pathol 32: , Swarts DR, van Suylen RJ, den Bakker MA, et al. Interobserver variability for the WHO classification of pulmonary carcinoids. Am J Surg Pathol 38: , Filosso PL, Ferolla P, Guerrera F, et al. Multidisciplinary management of advanced lung neuroendocrine tumors. European Society of Thoracic Surgeons Lung Neuroendocrine Tumors Working-Group Steering Committee. J Thorac Dis 7(Suppl 2):S , 2015
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek?
 Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében
 A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában
 Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
A hólyagrák aktuális kérdései a pathologus szemszögéből. Iványi Béla SZTE Pathologia
 A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A patológiai vizsgálatok metodikája. 1. Biopsziástechnikák 2. Speciális vizsgálatok
 A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
GRADING. Az emlő invazív és in situ carcinomái. Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet
 GRADING Az emlő invazív és in situ carcinomái Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet Invazív carcinoma Scarff-Bloom-Richardson grade Elston és Ellis által módosított Scarff- Bloom-Richardson
GRADING Az emlő invazív és in situ carcinomái Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet Invazív carcinoma Scarff-Bloom-Richardson grade Elston és Ellis által módosított Scarff- Bloom-Richardson
Mit is csinál pontosan a patológus?
 Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
Emlőbetegségek komplex diagnosztikája
 Emlőbetegségek komplex diagnosztikája Preoperatív citológiai-patológiai diagnosztika Dr. Hamar Sándor SZTE ÁOK Patológiai Intézet Emlőbetegségek diagnosztikája Az emlőbetegségek diagnosztikájában a nem
Emlőbetegségek komplex diagnosztikája Preoperatív citológiai-patológiai diagnosztika Dr. Hamar Sándor SZTE ÁOK Patológiai Intézet Emlőbetegségek diagnosztikája Az emlőbetegségek diagnosztikájában a nem
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi Tudományegyetemen
 SZEGEDI TUDOMÁNYEGYETEM Szent-Györgyi Albert Klinikai Központ Patológiai Intézet Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi
SZEGEDI TUDOMÁNYEGYETEM Szent-Györgyi Albert Klinikai Központ Patológiai Intézet Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi
20 éves a Mamma Klinika
 20 éves a Mamma Klinika A sejtdiagnosztika modern eszközei a diagnosztikában és terápiában dr Járay Balázs, dr Székely Eszter Medserv Kft, Semmelweis Egyetem II. Patológiai Intézet Budapest 1 22196 betegből
20 éves a Mamma Klinika A sejtdiagnosztika modern eszközei a diagnosztikában és terápiában dr Járay Balázs, dr Székely Eszter Medserv Kft, Semmelweis Egyetem II. Patológiai Intézet Budapest 1 22196 betegből
Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban
 Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban Zombori Tamás, Furák József, Urbán Dániel, Némedi Réka, Nyári Tibor, Cserni Gábor, TiszlaviczLászló Pathologiai Intézet, ÁOK Szegedi Tudományegyetem
Grádus rendszerek vizsgálata IAés IB stádiumú adenocarcinomákban Zombori Tamás, Furák József, Urbán Dániel, Némedi Réka, Nyári Tibor, Cserni Gábor, TiszlaviczLászló Pathologiai Intézet, ÁOK Szegedi Tudományegyetem
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján)
 pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet. Frank Diagnosztika Szimpózium, DAKO workshop 2012.
 Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
Diffúz idiopatiás pulmonális neuroendokrinsejtes hiperplázia (DIPNECH)
 Diffúz idiopatiás pulmonális neuroendokrinsejtes hiperplázia (DIPNECH) Fillinger János¹,Kerényi Anna Mária¹, Soltész Ibolya¹,Kosztics Szilárd² 1 OKTPI Budapest Pathológiai Osztály 2 OKTPI Budapest Mellkassebészeti
Diffúz idiopatiás pulmonális neuroendokrinsejtes hiperplázia (DIPNECH) Fillinger János¹,Kerényi Anna Mária¹, Soltész Ibolya¹,Kosztics Szilárd² 1 OKTPI Budapest Pathológiai Osztály 2 OKTPI Budapest Mellkassebészeti
2354-06 Nőgyógyászati citodiagnosztika követelménymodul szóbeli vizsgafeladatai
 1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában. Cifra János. Tolna Megyei Balassa János Kórház, Pathologia Osztály
 A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
A.) Biopsziás mintavétel lehetőségei és a biopsziás anyagok kezelésével kapcsolatos tudnivalók.
 II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI
 DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
Fejezetek a klinikai onkológiából
 Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK
 SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
A vesedaganatok sebészi kezelése
 A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA. Péter Ilona. ziuma Budapest 2008.
 ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA Péter Ilona Az Országos Onkológiai Intézet és s a Dako közös s szimpóziuma ziuma Budapest 2008. Oncocyta a pajzsmirigyben Definíci
ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA Péter Ilona Az Országos Onkológiai Intézet és s a Dako közös s szimpóziuma ziuma Budapest 2008. Oncocyta a pajzsmirigyben Definíci
NEM-VILÁGOSSEJTES VESERÁKOK
 NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
67. Pathologus Kongresszus
 A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
70. Patológus Kongresszus: Metszetszeminárium 3
 70. Patológus Kongresszus: Metszetszeminárium 3 Dr. Khoór András Associate Professor and Chair Department of Laboratory Medicine and Pathology Mayo Clinic, Jacksonville, Florida Kórtörténet Egy 67 éves
70. Patológus Kongresszus: Metszetszeminárium 3 Dr. Khoór András Associate Professor and Chair Department of Laboratory Medicine and Pathology Mayo Clinic, Jacksonville, Florida Kórtörténet Egy 67 éves
A tüdő adenocarcinomák szubklasszifikációja. Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5.
 A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
2355-06 Egyéb citológiai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata
 Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
ALK+ tüdőrák a klinikai gyakorlatban. Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest
 ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A tüdő neuroendokrin daganatainak tünetei és diagnosztikája
 ÖSSZEFOGLALÓ REFERÁTUMOK A tüdő neuroendokrin daganatainak tünetei és diagnosztikája Tamási Lilla dr. Müller Veronika dr. Semmelweis Egyetem, Általános Orvostudományi Kar, Pulmonológiai Klinika, Budapest
ÖSSZEFOGLALÓ REFERÁTUMOK A tüdő neuroendokrin daganatainak tünetei és diagnosztikája Tamási Lilla dr. Müller Veronika dr. Semmelweis Egyetem, Általános Orvostudományi Kar, Pulmonológiai Klinika, Budapest
Lezárás dátuma: HU/GIO/1017/00033
 Az előadás megjelenését a Boehringer Ingelheim támogatta. Az előadás tartalma az előadó (eredményeit és) önálló szakmai álláspontját tükrözi és nem tekinthető a Boehringer Ingelheim részéről közzétett
Az előadás megjelenését a Boehringer Ingelheim támogatta. Az előadás tartalma az előadó (eredményeit és) önálló szakmai álláspontját tükrözi és nem tekinthető a Boehringer Ingelheim részéről közzétett
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban. Doktori tézisek. Dr. Bogos Krisztina
 A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Doktori tézisek Dr. Bogos Krisztina Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Pulmonológia program
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Doktori tézisek Dr. Bogos Krisztina Semmelweis Egyetem Klinikai Orvostudományok Doktori Iskola Pulmonológia program
A tüdő neuroendokrin daganatainak diagnózisa és kezelése
 ÖSSZEFOGLALÓ KÖZLEMÉNY 113 A tüdő neuroendokrin daganatainak diagnózisa és kezelése GÁLFFY GABRIELLA Tüdőgyógyintézet, Törökbálint Levelezési cím: Dr. Gálffy Gabriella, Kutatási és Oktatási Igazgató, Onko-Pulmonológiai
ÖSSZEFOGLALÓ KÖZLEMÉNY 113 A tüdő neuroendokrin daganatainak diagnózisa és kezelése GÁLFFY GABRIELLA Tüdőgyógyintézet, Törökbálint Levelezési cím: Dr. Gálffy Gabriella, Kutatási és Oktatási Igazgató, Onko-Pulmonológiai
Diagnózis és prognózis
 Diagnózis, prognózis Általános vizsgálat Diagnózis és prognózis Fizikális vizsgálat Endoszkópia Képalkotás Sebészi feltárás A kezelés megválasztása Specifikus elemzés Kórszövettan/citológia Klinikai kémia
Diagnózis, prognózis Általános vizsgálat Diagnózis és prognózis Fizikális vizsgálat Endoszkópia Képalkotás Sebészi feltárás A kezelés megválasztása Specifikus elemzés Kórszövettan/citológia Klinikai kémia
IPF és tüdőrák együttes előfordulása. Dr Bohács Anikó Ph.D. egyetemi docens Semmelweis Egyetem, Pulmonológiai Klinika
 IPF és tüdőrák együttes előfordulása Dr Bohács Anikó Ph.D. egyetemi docens Semmelweis Egyetem, Pulmonológiai Klinika Kivizsgálás Endobronchialis eltérés nem volt. Mikrobiológia tenyésztés negatív. BAL:
IPF és tüdőrák együttes előfordulása Dr Bohács Anikó Ph.D. egyetemi docens Semmelweis Egyetem, Pulmonológiai Klinika Kivizsgálás Endobronchialis eltérés nem volt. Mikrobiológia tenyésztés negatív. BAL:
A patológiai vizsgálatok metodikája. 1. Biopsziás technikák 2. Speciális vizsgálatok
 A patológiai vizsgálatok metodikája 1. Biopsziás technikák 2. Speciális vizsgálatok Biopszia indikációk Disszeminált/diffúz eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges
A patológiai vizsgálatok metodikája 1. Biopsziás technikák 2. Speciális vizsgálatok Biopszia indikációk Disszeminált/diffúz eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges
A klinikai citológia alapjai
 A klinikai citológia alapjai Vajdovich Péter Szent István Egyetem Állatorvos-tudományi Kar Belgyógyászati Tanszék és Klinika Budapest A citológiai vizsgálatok célja elváltozások: normál, hiperplasztikus
A klinikai citológia alapjai Vajdovich Péter Szent István Egyetem Állatorvos-tudományi Kar Belgyógyászati Tanszék és Klinika Budapest A citológiai vizsgálatok célja elváltozások: normál, hiperplasztikus
M E G B Í Z Á S I S Z E R Z Ő D É S
 M E G B Í Z Á S I S Z E R Z Ő D É S EGÉSZSÉGÜGYI TEVÉKENYSÉG VÉGZÉSÉRŐL (a továbbiakban: Szerződés) amely létrejött egyrészről....(cégjegyzékszáma:..; székhelye:...; adószáma:, képviseli: ) mint egészségügyi
M E G B Í Z Á S I S Z E R Z Ő D É S EGÉSZSÉGÜGYI TEVÉKENYSÉG VÉGZÉSÉRŐL (a továbbiakban: Szerződés) amely létrejött egyrészről....(cégjegyzékszáma:..; székhelye:...; adószáma:, képviseli: ) mint egészségügyi
Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán
 Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán 1.Számú Patológiai és Kísérleti Rákkutató Intézet Diagnózis (definitív): benignus, malignus, intermedier malignitás, borderline
Szövettan kérdései Ami a terápiát meghatározza és ami segíti Dr. Sápi Zoltán 1.Számú Patológiai és Kísérleti Rákkutató Intézet Diagnózis (definitív): benignus, malignus, intermedier malignitás, borderline
meghatározásának jelentősége
 A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
M E G B Í Z Á S I S Z E R Z Ő D É S
 M E G B Í Z Á S I S Z E R Z Ő D É S EGÉSZSÉGÜGYI TEVÉKENYSÉG VÉGZÉSÉRŐL (a továbbiakban: Szerződés) amely létrejött egyrészről (cégjegyzékszáma.; székhelye:.; adószáma:..; képviseli: ), mint egészségügyi
M E G B Í Z Á S I S Z E R Z Ő D É S EGÉSZSÉGÜGYI TEVÉKENYSÉG VÉGZÉSÉRŐL (a továbbiakban: Szerződés) amely létrejött egyrészről (cégjegyzékszáma.; székhelye:.; adószáma:..; képviseli: ), mint egészségügyi
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában
 Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010.
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010.
Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás
 Kovács Ilona Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás (Hamberger et al. 1982) FNA használata mellett
Kovács Ilona Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás (Hamberger et al. 1982) FNA használata mellett
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén
 Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
A fasciitis nodularis ritka formája
 Az Országos Traumatológiai Intézet közleménye A fasciitis nodularis ritka formája DR. RÉKÓ GYULA, DR. LACZKÓ TIBOR Érkezett: 1999. február 22. ÖSSZEFOGLALÁS A szerzõk az agresszív fibromatosisok csoportjába
Az Országos Traumatológiai Intézet közleménye A fasciitis nodularis ritka formája DR. RÉKÓ GYULA, DR. LACZKÓ TIBOR Érkezett: 1999. február 22. ÖSSZEFOGLALÁS A szerzõk az agresszív fibromatosisok csoportjába
OncotypeDX és más genetikai tesztek emlőrákban és azon túl. Dr. Nagy Zoltán Med Gen-Sol Kft.
 OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
Dr Csőszi Tibor Hetenyi G. Kórház, Onkológiai Központ
 Dr Csőszi Tibor Hetenyi G. Kórház, Onkológiai Központ Azért, mert a kemoterápia bizonyított módon fokozza a gyógyulás esélyét! A kemoterápiának az a célja, hogy az esetleg, vagy biztosan visszamaradt daganatsejtek
Dr Csőszi Tibor Hetenyi G. Kórház, Onkológiai Központ Azért, mert a kemoterápia bizonyított módon fokozza a gyógyulás esélyét! A kemoterápiának az a célja, hogy az esetleg, vagy biztosan visszamaradt daganatsejtek
A göbös pajzsmirigy kivizsgálása, ellátása. Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika
 A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
A rosszindulatú daganatos halálozás változása 1975 és 2001 között Magyarországon
 A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
A rosszindulatú daganatos halálozás változása és között Eredeti közlemény Gaudi István 1,2, Kásler Miklós 2 1 MTA Számítástechnikai és Automatizálási Kutató Intézete, Budapest 2 Országos Onkológiai Intézet,
A pajzsmirigy benignus és malignus daganatai
 A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
1. eset. Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály
 1. eset Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Anamnézis 42 éves férfi véres széklet hátterében más intézetben az anustól3 cm-re kezdődően 11-12 cm hosszan
1. eset Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Anamnézis 42 éves férfi véres széklet hátterében más intézetben az anustól3 cm-re kezdődően 11-12 cm hosszan
Genomikai Medicina és Ritka Betegségek Intézete Semmelweis Egyetem
 Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
2353-06 Citotechnológia követelménymodul szóbeli vizsgafeladatai
 1. feladat Vendég érkezik a munkahelyére. Az Ön feladata, hogy megismertesse az osztályon használt mikroszkópokkal (fénymikroszkóp, polarizációs, fáziskontraszt és fluorescensz mikroszkóp) alkalmazási
1. feladat Vendég érkezik a munkahelyére. Az Ön feladata, hogy megismertesse az osztályon használt mikroszkópokkal (fénymikroszkóp, polarizációs, fáziskontraszt és fluorescensz mikroszkóp) alkalmazási
A lézer-szkenning citometria lehetőségei. Laser-scanning cytometer (LSC) Pásztázó citométer. Az áramlási citometria fő korlátai
 Az áramlási citométer bevezetésének fontosabb állomásai A lézer-szkenning citometria lehetőségei Bacsó Zsolt Coulter, 1949 Coulter számláló szabadalmaztatása Crosland-Taylor, 1953 sejtek hidrodinamikai
Az áramlási citométer bevezetésének fontosabb állomásai A lézer-szkenning citometria lehetőségei Bacsó Zsolt Coulter, 1949 Coulter számláló szabadalmaztatása Crosland-Taylor, 1953 sejtek hidrodinamikai
Diagnosztikai problémák onkoplasztikai műtétek után a radiológus szemszögéből
 Diagnosztikai problémák onkoplasztikai műtétek után a radiológus szemszögéből Bidlek M., Kovács E. Országos Onkológiai Intézet 2013. május 17-18 Szenológiai Kongresszus Kecskemét Műtéti típusok Kozmetikai
Diagnosztikai problémák onkoplasztikai műtétek után a radiológus szemszögéből Bidlek M., Kovács E. Országos Onkológiai Intézet 2013. május 17-18 Szenológiai Kongresszus Kecskemét Műtéti típusok Kozmetikai
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
 Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
A világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009.
A világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009.
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Neuroendokrin tüdőtumorok laboratóriumi kivizsgálása
 108 ÖSSZEFOGLALÓ KÖZLEMÉNY Neuroendokrin tüdőtumorok laboratóriumi kivizsgálása KAPPELMAYER JÁNOS, BHATTOA HARJIT PAL Debreceni Egyetem, Általános Orvostudományi Kar, Laboratóriumi Medicina Intézet, Debrecen
108 ÖSSZEFOGLALÓ KÖZLEMÉNY Neuroendokrin tüdőtumorok laboratóriumi kivizsgálása KAPPELMAYER JÁNOS, BHATTOA HARJIT PAL Debreceni Egyetem, Általános Orvostudományi Kar, Laboratóriumi Medicina Intézet, Debrecen
Hivatalos Bírálat Dr. Gődény Mária
 Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
Semmelweis Egyetem Urológiai Klinika Budapest. European Board of Urology Certified Department
 Nem-izominvazív hólyagrák terápiája Dr. Riesz Péter Semmelweis Egyetem Urológiai Klinika Budapest European Board of Urology Certified Department A hólyagrák halálozása Magyarországon Halálesetek száma
Nem-izominvazív hólyagrák terápiája Dr. Riesz Péter Semmelweis Egyetem Urológiai Klinika Budapest European Board of Urology Certified Department A hólyagrák halálozása Magyarországon Halálesetek száma
OncotypeDX az emlőrák kezelésében
 OncotypeDX az emlőrák kezelésében Dr. Nagy Zoltán Med Gen-Sol Kft. Szenológiai Kongresszus Kecskemét 2018. 04. 13-14. Slide 1 Az Oncotype DX korai emlőrák teszt 16 tumorral kapcsolatos gén Ösztrogén csoprt
OncotypeDX az emlőrák kezelésében Dr. Nagy Zoltán Med Gen-Sol Kft. Szenológiai Kongresszus Kecskemét 2018. 04. 13-14. Slide 1 Az Oncotype DX korai emlőrák teszt 16 tumorral kapcsolatos gén Ösztrogén csoprt
Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekbe
 Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekben a korcsoportokban ez a leggyakoribb daganatos halálozási
Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekben a korcsoportokban ez a leggyakoribb daganatos halálozási
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend)
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
A gasztroenteropankreatikus neuroendokrin daganatok klinikopatológiája
 90 ÖSSZEFOGLALÓ KÖZLEMÉNY A gasztroenteropankreatikus neuroendokrin daganatok klinikopatológiája BORKA KATALIN Semmelweis Egyetem, II. Sz. Patológiai Intézet, Budapest Levelezési cím: Dr. Borka Katalin,
90 ÖSSZEFOGLALÓ KÖZLEMÉNY A gasztroenteropankreatikus neuroendokrin daganatok klinikopatológiája BORKA KATALIN Semmelweis Egyetem, II. Sz. Patológiai Intézet, Budapest Levelezési cím: Dr. Borka Katalin,
Többes malignus tumoros eseteink elemzése. Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya
 Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei
 Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Diagnosztikai irányelvek Paget-kórban
 Diagnosztikai irányelvek Paget-kórban Dr. Donáth Judit Országos Reumatológiai és Fizioterápiás Intézet, Budapest HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012-2014 2015. ÁPRILIS 17.
Diagnosztikai irányelvek Paget-kórban Dr. Donáth Judit Országos Reumatológiai és Fizioterápiás Intézet, Budapest HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012-2014 2015. ÁPRILIS 17.
Kovács Ilona Hargitai Zoltán Chalupa Istvánné
 Kovács Ilona Hargitai Zoltán Chalupa Istvánné Acta Cytologica Volume 51March April 2007Number 2 How Technology Is Reshaping the Practice of Nongynecologic Cytology Frontiers of Cytology Symposium Moderator
Kovács Ilona Hargitai Zoltán Chalupa Istvánné Acta Cytologica Volume 51March April 2007Number 2 How Technology Is Reshaping the Practice of Nongynecologic Cytology Frontiers of Cytology Symposium Moderator
Terhességi papilláris pajzsmirigycarcinoma Citodiagnózis, kiegészítő vizsgálatok
 Terhességi papilláris pajzsmirigycarcinoma Citodiagnózis, kiegészítő vizsgálatok Esetbemutatás dr. Székely Tamás, dr. Székely Eszter, dr. Istók Roland, dr. Kovács István, dr. Járay Balázs dr. Tóbiás Bálint*,
Terhességi papilláris pajzsmirigycarcinoma Citodiagnózis, kiegészítő vizsgálatok Esetbemutatás dr. Székely Tamás, dr. Székely Eszter, dr. Istók Roland, dr. Kovács István, dr. Járay Balázs dr. Tóbiás Bálint*,
Engedélyszám: /2011-EAHUF Analitika követelménymodul szóbeli vizsgafeladatai
 1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás
 Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
Ilona Kovács. Debrecen
 Ilona Kovács Debrecen 3-6% -ban fordul elő kóros Pap kenet terhességben Cervix carcinoma incidenciája terhesség alatt 1 eset jut 2000-2200 terhességre A méhnyakrákos nők 1-3%-a terhes a diagnózis idején
Ilona Kovács Debrecen 3-6% -ban fordul elő kóros Pap kenet terhességben Cervix carcinoma incidenciája terhesség alatt 1 eset jut 2000-2200 terhességre A méhnyakrákos nők 1-3%-a terhes a diagnózis idején
A/a. Cervix citológia
 II./2.6. fejezet: Daganatok citológiai kórisméje Sápi Zoltán A fejezet célja, hogy megismerje a hallgató a citológiai diagnosztika lehetőségeit. A fejezet teljesítését követően képes lesz arra, hogy megfelelő
II./2.6. fejezet: Daganatok citológiai kórisméje Sápi Zoltán A fejezet célja, hogy megismerje a hallgató a citológiai diagnosztika lehetőségeit. A fejezet teljesítését követően képes lesz arra, hogy megfelelő
Az Egészségügyi Minisztérium módszertani levele. Az aspirációs citológiai vizsgálatok gyakorlatáról. Bevezetés. 3450 EGÉSZSÉGÜGYI KÖZLÖNY 21.
 3450 EGÉSZSÉGÜGYI KÖZLÖNY 21. szám 1.3. A centrumok ellátási területe: A centrumok elsõsorban a területébe tartozó klinikák és osztályok diagnosztikus tevékenységét látják el, azonban ez nem zárja ki annak
3450 EGÉSZSÉGÜGYI KÖZLÖNY 21. szám 1.3. A centrumok ellátási területe: A centrumok elsõsorban a területébe tartozó klinikák és osztályok diagnosztikus tevékenységét látják el, azonban ez nem zárja ki annak
Kettős férfi emlőrák és a beteg utógondozása
 Bevezetés A férfi emlőrák ritka betegség, általában 100 női emlőrákra jut egy férfi emlőrákos beteg. Egyes populációkban ez az arány más lehet, így például az afrikai fekete lakosság körében 2,4% (1).
Bevezetés A férfi emlőrák ritka betegség, általában 100 női emlőrákra jut egy férfi emlőrákos beteg. Egyes populációkban ez az arány más lehet, így például az afrikai fekete lakosság körében 2,4% (1).
A STRATÉGIAALKOTÁS FOLYAMATA
 BUDAPESTI CORVINUS EGYETEM VÁLLALATGAZDASÁGTAN INTÉZET VERSENYKÉPESSÉG KUTATÓ KÖZPONT Szabó Zsolt Roland: A STRATÉGIAALKOTÁS FOLYAMATA VERSENYBEN A VILÁGGAL 2004 2006 GAZDASÁGI VERSENYKÉPESSÉGÜNK VÁLLALATI
BUDAPESTI CORVINUS EGYETEM VÁLLALATGAZDASÁGTAN INTÉZET VERSENYKÉPESSÉG KUTATÓ KÖZPONT Szabó Zsolt Roland: A STRATÉGIAALKOTÁS FOLYAMATA VERSENYBEN A VILÁGGAL 2004 2006 GAZDASÁGI VERSENYKÉPESSÉGÜNK VÁLLALATI
TÜDİRÁKOK ONKOLÓGIÁJA
 TÜDİRÁKOK ONKOLÓGIÁJA Dr. Maráz Anikó Szegedi Tudományegyetem Onkoterápiás Klinika 2012. november 14. Daganatos halálozás Európában, 1955-2015 Daganatos betegségek incidenciája /WHO, 2006/ Tüdı 1 200 000
TÜDİRÁKOK ONKOLÓGIÁJA Dr. Maráz Anikó Szegedi Tudományegyetem Onkoterápiás Klinika 2012. november 14. Daganatos halálozás Európában, 1955-2015 Daganatos betegségek incidenciája /WHO, 2006/ Tüdı 1 200 000
Percutan diagnosztika és kezelés
 Percutan diagnosztika és kezelés MRT 2016 Diagnoszták és terápeuták Klinikum, labor és képalkotók Non-invazív és invazív diagnosztika Sebészi, onkológiai és minimálisan invazív terápia És ezek kombinációi
Percutan diagnosztika és kezelés MRT 2016 Diagnoszták és terápeuták Klinikum, labor és képalkotók Non-invazív és invazív diagnosztika Sebészi, onkológiai és minimálisan invazív terápia És ezek kombinációi
Döntéshozatal a klinikai gyakorlatban. Fülep Zoltán Bács-Kiskun Megyei Kórház, Szegedi Egyetem Általános Orvostudományi Kar Oktató Kórháza Kecskemét
 Döntéshozatal a klinikai gyakorlatban Fülep Zoltán Bács-Kiskun Megyei Kórház, Szegedi Egyetem Általános Orvostudományi Kar Oktató Kórháza Kecskemét Cogito ergo sum René Descartes Immanuel Kant A klinikai
Döntéshozatal a klinikai gyakorlatban Fülep Zoltán Bács-Kiskun Megyei Kórház, Szegedi Egyetem Általános Orvostudományi Kar Oktató Kórháza Kecskemét Cogito ergo sum René Descartes Immanuel Kant A klinikai
Új guideline-ok - szűrés és management Dr. Francz Monika Ph.D. Nőgyógyászati citológia tanfolyam március 30. Siófok
 Új guideline-ok - szűrés és management Dr. Francz Monika Ph.D. Nőgyógyászati citológia tanfolyam 2017. március 30. Siófok 2 A méhnyakrák szűrés, mint folyamat Behívás Minta vétele Minta feldolgozása A
Új guideline-ok - szűrés és management Dr. Francz Monika Ph.D. Nőgyógyászati citológia tanfolyam 2017. március 30. Siófok 2 A méhnyakrák szűrés, mint folyamat Behívás Minta vétele Minta feldolgozása A
Kvantitatív immunhisztokémia a patológiában
 Kvantitatív immunhisztokémia a patológiában Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet, Budapest MPT Kongresszus Siófok, 2013. szeptember 26-28. Kvantitatív Patológia
Kvantitatív immunhisztokémia a patológiában Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet, Budapest MPT Kongresszus Siófok, 2013. szeptember 26-28. Kvantitatív Patológia
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI
 KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
A 22C3 PD-L1 tesztek értékelése intézetünkben. Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs
 A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A VIZELET CYTOLÓGIAI (TPS) NOMENKLATÚRA A PÁRIZSI RENDSZER TÜKRÉBEN. Horváth Ilona dr.
 A VIZELET CYTOLÓGIAI NOMENKLATÚRA A PÁRIZSI RENDSZER TÜKRÉBEN (TPS) Horváth Ilona dr. 2017 A HÚGYHÓLYAGRÁK TÚLÉLŐI RENDSZERES KÖVETÉST IGÉNYELNEK A KÖVETÉSBEN AZ INVAZÍV DIAGNOSZTIKUS ESZKÖZÖK RENDKÍVÜL
A VIZELET CYTOLÓGIAI NOMENKLATÚRA A PÁRIZSI RENDSZER TÜKRÉBEN (TPS) Horváth Ilona dr. 2017 A HÚGYHÓLYAGRÁK TÚLÉLŐI RENDSZERES KÖVETÉST IGÉNYELNEK A KÖVETÉSBEN AZ INVAZÍV DIAGNOSZTIKUS ESZKÖZÖK RENDKÍVÜL
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3,
 Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában. Nagy Tünde Országos Onkológiai Intézet B belosztály
 Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában Nagy Tünde Országos Onkológiai Intézet B belosztály A tüdőrák a vezető daganatos halálok USA-ban: férfiak daganatos mortalitása 1930-2000*
Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában Nagy Tünde Országos Onkológiai Intézet B belosztály A tüdőrák a vezető daganatos halálok USA-ban: férfiak daganatos mortalitása 1930-2000*
A méhnyak daganat megelőző állapotainak komplex szűrése
 A méhnyak daganat megelőző állapotainak komplex szűrése rizikóbecslés, citológia, HPV tipizálás,biomarkerek használata a másodlagos megelőzésben Járay Balázs Semmelweis Egyetem, II. Patologiai Intézet
A méhnyak daganat megelőző állapotainak komplex szűrése rizikóbecslés, citológia, HPV tipizálás,biomarkerek használata a másodlagos megelőzésben Járay Balázs Semmelweis Egyetem, II. Patologiai Intézet
VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN
 VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN Ostoros Gyula 1, Döme Balázs 1, Strausz János 1, Tímár József 2 1 Országos Korányi Tbc és Pulmonológiai Intézet, 2 Semmelweis
VÁLTOZÁSOK A NEM-KISSEJTES TÜDŐRÁK DIAGNOSZTIKUS ÉS TERÁPIÁS STRATÉGIÁJÁBAN Ostoros Gyula 1, Döme Balázs 1, Strausz János 1, Tímár József 2 1 Országos Korányi Tbc és Pulmonológiai Intézet, 2 Semmelweis
SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ
 SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ Írta: Rajtár Mária 1. Háttér információk és definíciók Az emlőrák sebészi kezelése során az axillaris blockdissectióval eltávolított
SENTINEL NYIROKCSOMÓ SZCINTIGRÁFIA EMLŐRÁKBAN- MÓDSZERTANI ÚTMUTATÓ Írta: Rajtár Mária 1. Háttér információk és definíciók Az emlőrák sebészi kezelése során az axillaris blockdissectióval eltávolított
