A HGF/C-MET RENDSZER SZEREPE A DAGANAT PROGRESSZIÓBAN
|
|
|
- Zsuzsanna Vörösné
- 9 évvel ezelőtt
- Látták:
Átírás
1 A HGF/C-MET RENDSZER SZEREPE A DAGANAT PROGRESSZIÓBAN Fazekas Károly Semmelweis Egyetem Doktori Iskola Témavezeto: Dr. Tímár József Országos Onkológiai Intézet Tumor Progressziós Osztály Budapest 2003
2 Tartalomjegyzék Összefoglalás 4 Summary 5 I. Bevezetés 6 A daganatos progresszió 6 Az áttétképzés folyamata, a metasztatikus kaszkád 6 A lokális invázió mechanizmusa 6 Adhézió 7 Mátrixbontás 8 Migráció 9 A szóródás mechanizmusa 9 Tumorsejt ECM kölcsönhatások a keringésben 9 Tumorsejt normál sejt kölcsönhatások az érpályában 9 A/ Tumorsejt endotél kölcsönhatás 9 B/ Tumorsejt trombocita kölcsönhatás 10 Az extravazáció mechanizmusa 10 A daganatok szervi áttétei 11 Tüdo metasztázis 11 Májáttét 12 Csontáttét 12 Agyi áttét 13 A metasztázis képzés szerv-specifitása 13 A hepatocita növekedési faktor és receptora, a c-met onkoprotein 15 Tumor-indukált angiogenezis, az angiogenezis formái 17 A vaszkulogenezis 17 Az angiogenezis 18 Tumor-indukálta angiogenezis 19 Vaszkuláris mimikri 20 Ér inkorporáció 20 Az antiangiogenetikus terápia jelenlegi lehetoségei 21 Hagyományos terápiás szerek 21 Endotél növekedési faktor ligandok 22 Endoteliális mitogén receptorok 23 Angiogén jelátvitel 23 Endotélsejt-ECM kölcsönhatásra ható terapeutikumok 24 II. Cékituzések 25 III. Anyag és módszer In vitro módszerek 27 Bázikus peptidek szintézise 27 Sejtek 27 Beteganyag 28 Statisztika 28 Sejtproliferáció vizsgálata in vitro 28 Migrációs teszt In vivo módszerek 29 2
3 In vivo lép-máj kolonizációs modell 29 Szubkután tumornövekedés vizsgálata 29 Peptid kezelés máj kolonizációs modellben 30 Tumor-indukált angiogenezis meghatározása 30 Angiogenezis vizsgálata in vivo Molekuláris biológiai módszerek 31 C-met expresszió meghatározása RT-PCR-ral 31 C-met protein kimutatása western blot módszerrel 32 Sejtvonalakon 32 Tumorszöveten 32 A c-met expresszió meghatározása áramlásos citometriával 33 Heparánszulfát proteoglikán expresszió meghatározása áramlásos citometriával Morfológiai módszerek 34 C-met protein kimutatása patológiai anyagon 34 Antigén expresszió vizsgálata adherens sejteken lézer-scanning mikroszkóppal 34 IV. Eredmények 36 Bázikus peptidek heparinköto képességének vizsgálata 36 I. fejezet: C-met expresszió vizsgálata humán kolorektális karcinómákon, és a HGF in vitro biológiai hatása 37 Humán koloektális sektvonalak áttétképzése 37 Humán kolorektális sejtvonalak c-met expressziója 37 HSPG expresszió vizsgálata áramlásos citometriával 42 HGF hatása humán kolorektális karcinóma sejtvonalak motilitására in vitro 43 A c-met fehérje expressziója primer kolón daganatokban 45 II. fejezet: HGF mimetikus peptidek biológiai hatásai 49 HGP peptidek hatása in vitro sejtproliferációra 49 HGP kezelés hatása különbözo típusú tumorsejtek in vitro növekedésére és májáttét képzésére 50 Bázikus HGP-szeru hexapeptidek in vitro hatásai 53 III. fejezet: HGP peptidek hatása az angiogenezisre 55 Bázikus, és HGF eredetu bázikus peptidek hatása angiogenezisre csirke chorioallantois membrán rendszerben 55 Bázikus peptidek hatása Kaposi szarkóma sejtek proliferációjára 57 Bázikus peptidek in vitro hatása humán agyi mikroér endotél sejtekre 57 Tumor-indukált angiogenezis vizsgálata 58 V. Diszkusszió A HGF és c-met rendszer szerepe kolorektális daganatok áttétképzésben HGF eredetu és kisméretu peptidek biológiai hatásai I.: Antitumorális hatás HGF eredetu és kisméretu peptidek biológiai hatásai II.:Antiangiogén hatás Új eredmények és megállapítások 66 VI. Irodalomjegyzék 69 VII. Az értekezés alapját képezo saját közlemények 79 VIII. Függelék 81 A táblázatok listája 81 Az ábrák listája 81 Rövidítések 82 3
4 Összefoglalás Az irodalomból ismert, hogy a c-met onkoprotein többféle tumorban, köztük a kolorektális daganatokban overexpresszált. Az azonban nem tisztázott, hogy ennek van-e szerepe a kolorektális tumorok áttétképzésében, s ha igen, az milyen mechanizmuson alapszik. Mivel a HGF a máj egyik növekedési faktora és ez a szerv a kolorektális daganatok áttétképzésének fo célpontja, felmerült annak a lehetosége, a HGF c-met kapcsolat szerepet játszik ebben a folyamatban. Arra, hogy ez milyen mechanizmus szerint történik, többféle lehetoség kínálkozott. Munkánk célja néhány potenciális hatásmechanizmus vizsgálata és az eredmények gyakorlati (terápiás) hasznosítási lehetoségeinek tisztázása volt. Az elso, legkézenfekvobb lehetoség, hogy a HGF c-met kapcsolat a tumorsejt számára mitogén, motogén, vagy mindkét úton segíti elo az áttétképzést. Mivel ismert, hogy a plazmából tisztított HGF angiogenezist indukál, másodikként megvizsgáltuk a c-met, illetve rekombináns humán HGF szerepét a daganatok angiogenezisében. Reális lehetoségként merült fel, hogy a HGF?-láncának kisméretu bázikus, feltehetoen heparinköto peptidjei, valamint a HGFszekvenciák alapján tervezett szintetikus bázikus hexapeptidek befolyásolják a tumorok viselkedését, mivel irodalmi adatok azt igazolták, hogy a HGF heparinköto növekedési faktor, és a megfelelo szekvenciával rendelkezo bázikus, heparinköto peptidek különbözo biológiai aktivitással bírnak. Megvizsgáltuk e peptidek hatását sejtproliferációra, áttétképzésre, valamint angiogenezisre egyaránt. Azon eredményeinkbol, amelyek azt igazolták, hogy a vad típusú c-met protein expressziója csak metasztatikus sejtvonalainkon volt kimutatható, hogy a rhhgf csak az áttétképzo sejtvonalak motilitását növelte és hogy a Duke s C stádiumú humán kolorektális adenokarcinómákban a c-met expressziója magasabb volt mint a Duke s B stádiumúaké, arra következtetünk, hogy HGF c-met rendszer a kolorektális daganatok áttétképzésében inkább a motogén, mintsem a mitogén hatásával vesz részt. Abból, hogy a HGP1 és HGP2 HGF?-lánc peptidek képesek voltak gátolni a HT25 humán kolorektális adenokarcinóma és az M1/9 humán melanóma sejtvonal in vitro proliferációját, hogy a HGP1 HGF?-lánc peptid gátolta a HT25 humán kolorektális adenokarcinóma szubkután növekedését és a HGP1 HGF?-lánc peptid gátolta HT25 humán kolorektális adenokarcinóma, M1/9 humán melanóma, valamint 3LL-HH egér tüdokarcinóma állatokban történo áttétképzését, arra következtetünk, hogy a kisméretu HGF?-lánc peptidek antitumorális hatással bírhatnak. Abból, hogy a HGP1, HGP2 HGF?-lánc peptid és a BP4 bázikus hexapeptid gátolta az angiogenezist in vivo choriallantois membrán modellben, a HGP1, HGP2 HGF?-lánc peptid és a BP4 bázikus hexapeptid gátolta humán kisagyi endotélsejtek proliferációját in vitro és hogy a HGP1 HGF?-lánc peptid befolyásolta szubkután növo HT25 humán kolorektális adenokarcinóma által indukált angiogenezist, arra következtettünk, hogy a kisméretu HGF?- lánc peptidek, valamint kisméretu bázikus peptidek antiangiogenikus hatással bírhatnak. Mindez azt jelentheti, hogy kisméretu bázikus, növekedési faktor eredetu, vagy tervezett peptidek a tumorellenes szerek egy csoportjának kiindulópontjai lehetnek. 4
5 Summary It is known that c-met protein is overexpressed in several types of tumors including colorectal carcinomas. But it is not clear what is the role of this in the metastasis of colorectal cancers. Since HGF is one of the growth factors of the liver and main target of metastatsis of colorectal cancers it has been arose that relation between HGF and c-met play role in this process. There are several kinds of possible mechanism. The aim of our work was to study of some possible mechanism and to clarify the possible therapeutic value of our results. The most obviuos possibility is that the HGF - c-met relation helps the metastasis by mitogenic or motogeginic or both way. Since it is known HGF purufied from blodd plasma induces angiogenesis secondly the role of HGF and c-met in angiogenesis of tumors was studied. It seemed to be a real possibility that small basic presumably heparin binding peptides of HGF? chain and bsaic hexapeptides designed on the basis of HGF sequence could influence the behaviour of tumors because earlier studies has proven HGF is a heparin binding growth factor and basic heparin binding peptides have several biological activity. The effect of these peptides on cell proliferation, metastasis and angiogenesis was studied, too. We demonstrated that the expression of wild type c-met was detectable on metastatic cell lines, moreover the motility of metastatic human colorectal adenocarcinomas was increased by rhhgf treatment. On the other hand the expression of c-met was higher in Duke's C human colorectal cancer than in Duke s B tumors. These data suggest that the HGF c-met system plays role in metastasis of colorectal cancers by its motogenic effects. We found that proliferation of HT25 human colorectal adenocarcinoma and M1/9 human melanoma was inhibited by HGP1 and HG2 HGF? chain peptides. Furthermore the subcutaneous growth of HT25 human colorectal adenocarcinoma was inhibited by HGP1 HGF? chain peptide. Moreover the liver metastasis of HT25 human colorectal adenocarcinoma, M1/9 human melanoma and 3LL-HH rident lung carcinoma was inhibited by HGP1 HGF? chain peptide. These results suggest that small HGF? chain peptides could have antitumoral effect. We showed that angiogenesis was inhibited in chicken choriallantois membrane model by HGP1 and HG2 HGF? chain peptides and the artificial BP4 basic hexapeptide. Moreover the proliferation of human cerebellar endothelial cells was inhibited by HGP1 and HG2 HGF? chain peptides and the artificial BP4 basic hexapeptide. Furthermore the angiogenesis induced by subcutaneous HT25 human colorectal adenocarcinoma was influenced by HGP1 HGF? chain peptide. These findings suggest that small basic peptides of HGF? chain and small basic hexapeptides could have antiangiogenic effect All of these data could mean that small basic peptides derived from growth factors could be developed as of a new group of anticancer agents. 5
6 I. Bevezetés A daganatos progresszió Az áttétképzés folyamata, a metasztatikus kaszkád (1) Az invázió folyamata a daganat típusától függetlenül hasonló lépésekben játszódik le. A folyamat több lépésbol áll, és ezek mindig feltételezik az elozo bekövetkeztét. Ez azt is jelenti, hogy a tumorsejteknek egyre összetettebb biológiai tulajdonságokkal kell rendelkezniük. Az inváziós és metasztatikus kaszkád magába foglalja tehát a folyamat egyes lépéseit, a primer tumorból történo leszakadástól, a távoli szervekben történo letelepedésig. A folyamat a primer tumorból történo sejtleválással kezdodik, ami aktív folyamat, és a környezo mátrixhoz történo kitapadást (adhézió), annak legalább részleges lebontását (degradáció) és az azon való átjutást (migráció) jelenti. A tumorsejtek ekkor addig vándorolnak, amíg újabb mátrixhatárhoz nem érnek, ami lehet a nyirokerek, vagy vérerek (általában venulák) fala, ahol a bazális membránhoz kitapadva azt lebontják, és az endotél sejtek között átnyomakodva az erek lumenébe kerülnek (intravazáció). A tumorsejtek a nyirokerekbe az érfal bontása nélkül is bejuthatnak, hiszen ezen erek fal nélküli szövetrésként kezdodnek. Az ereken belül sajátos sejt sejt, illetve sejt mátrix kölcsönhatások lépnek fel. A tumorsejt mátrix kölcsönhatás az érpályában keringo szolúbilis mátrix fehérjékkel való kapcsolatot jelenti, míg a tumorsejt normál sejt kölcsönhatás alatt a vérlemezkékkel és az immunrendszer specifikus és nem specifikus effektor sejtjeivel való kapcsolatokat értjük. A mindezeket túlélo tumorsejtek a távoli szervek terminális érszakaszaiba jutva, ott megakadnak, és a keringésbol kiléphetnek. Az extravazáció során a keringésben lévo tumorsejtek eloször az endotélsejtekhez kapcsolódnak, összehúzódásukat váltják ki, majd kapcsolatba lépnek az endotél alatti mátrixszal, és itt ugyanaz történik, mint az intravazáció során: kitapadás, lebontás. 6
7 A folyamat végén, az új helyen megtelepedett tumorsejtek proliferálni kezdenek, és a primer tumorhoz hasonlóan bizonyos nagyság elérése után stromát és érújdonképzodést indukálnak. (I. táblázat) I. táblázat.a metasztatikus kaszkád Primer tumor Lokális invázió Szóródás Áttét Lokális invázió Proliferáció Tumor-indukált angiogenezis Kitapadás a környezo mátrixhoz Mátrix enzimatikus bontása Migráció a lebontott mátrixon át Intravazáció Kitapadás a szubendoteliális bazális membránhoz Bazális membrán enzimatikus bontása Bevándorlás az ér lumenébe Keringés Fibrinogén és más szérumfehérjék megkötése Aggregálódás trombocitákkal Heterotípiás kölcsönhatás keringo mononukleáris sejtekkel Extravazáció Kitapadás az endotél luminális felszínéhez; endotélretrakció Kitapadás a szubendoteliális bazális membránhoz Bazális membrán enzimatikus bontása Migráció a környezo intersticiumba Proliferáció Tumor-indukált angiogenezis A lokális invázió mechanizmusa Adhézió A tumorsejtek ECM-fehérjékkel kialakuló kölcsönhatása a fentiek alapján kulcsfontosságú eleme az inváziónak. A kölcsönhatást úgynevezett adhéziós receptorok közvetítik, melyek integrinek, nem-integrin típusúak és proteoglikánok. Az integrinek normál és daganatos sejtek legfontosabb adhéziós receptorai és különleges szignálreceptorként funkcionálnak. Az integrinek expressziójában jelentos változások mennek végbe a malignus transzformáció során, az eredeti receptor mintázathoz képest. A leggyakoribb jelenség a legáltalánosabb fibronektinreceptor az? 5? 1 integrin expressziójának csökkenése vagy eltunése. Az inváziós képesség 7
8 kialakulásakor nemcsak a kiinduló (normál) sejtekre jellemzo integrin expresszió vész el, hanem új, sokszor ektópiás integrin expressziója jelenik meg. Jó példa erre a limfoid daganatokban fokozódó? 2 integrin expressziója (2, 3), a rhabdomyosarcomákban megjeleno? 2? 1 (4), vagy a melanómákban észlelheto fokozott? v? 3 (5, 6)és a megjeleno? II? 3 (7) expresszió. Az integrinek mellett a lamininreceptorok is fontos szerepet játszanak; a fokozódó lamininreceptor-expresszió és funkció általában emloés vastagbélrákok jellemzoje (8, 9, 10, 11). A mátrixfehérjék nem specifikus, de annál fontosabb sejtfelszíni receptorai, normál és tumorsejtekben egyaránt a proteoglikánok, ezek közül is a heparánszulfát (HS) proteoglikánok. Ennek oka az, hogy a mátrixfehérjék többségén (fibronektin, laminin, vitronektin, intersticiális kollagén) specifikus HS-köto helyek vannak, míg a proteoglikánok jelentos része, mint transzmembrán fehérje, képes mátrixintegráló funkciót betölteni. Az inváziós/metasztatikus képességu tumorsejteken bizonyos típusú HS proteoglikánok mennyisége megno (12, 13, 53). Mátrixbontás Normális sejtek esetében a kitapadás általában a sejtek lehorgonyzását eredményezi, differenciálódási lehetoséget jelent. Malignus tumorsejtek esetében pedig lizoszómális enzimek szekretálódnak a mátrix kötés helyén. A fokozott mátrixbontás másik oka az, hogy az invazív tumorsejtekben számos mátrixbontó enzim expressziója fokozódik: a mátrix metalloproteinázoké (MMP), a katepszineké, és a plazminogénaktivátoroké. Az MMP család tagjai közül az MMP9 normál sejtekben is expresszálódik, mikor azok bazális membránon jutnak keresztül (pl. limfociták, makrofágok). Ugyanakkor az MMP2, gyakran expresszálódik invazív tumorsejtekben és indukálódik a daganatos strómában is. A katepszin D, illetve G expressziója mellrákokban, a katepszin B expressziója egyéb tumorféleségekben is megemelkedik (14, 25). Legáltalánosabb jelenség, hogy a tpa, illetve upa expressziója jelenik meg, illetve fokozódik (16). Ez az enzim nemcsak a környezo mátrixot bontja, de aktivál más mátrixbontó enzimeket is. Természetesen a bontó enzimek aktivitása szabályozás alatt áll, ezt két mechanizmus látja el. Az egyik a génszintu szabályozás, azaz amikor az enzim génje aktiválódik a tumorsejtben, adott esetben pl. autokrin vagy parakrin növekedési faktor vagy citokin 8
9 hatására. A másik szabályozási ág a gátlórendszerek. Mind a három mátrixbontó enzimrendszernek van inhibitora. Az MMP-k gátlói a TIMP fehérjék, a katepszinek gátlói a stefinek, a plazminogénaktivátoroké a PAI-k (PA inhibitor). Invazív fenotípus esetén nemcsak a bontóenzimek expressziója fokozódhat, hanem a gátlórendszer is sérülhet (17, 18, 19). Migráció (20, 21, 22) A migráció, az aktív mozgás képessége elengedhetetlen feltétele a lokális inváziónak, s így az áttétképzésnek. A tumorsejtek vándorlásuk során folyton kapcsolatban vannak a környezo mátrixfehérjékkel, ezért ebben a folyamatban a mátrixreceptorok, s ezeken belül különösen az integrinek alapveto szerepet töltenek be. Ezek részben olyan jeleket indítanak el a sejtekben, melyek hatására a sejtek mobilizálódnak, másrészt a degradáló enzimek hatására felszabaduló kis peptidek kemotaktikus jeleit ismerik fel. Emellett számos auto- és parakrin növekedési faktor és citokin is képes a migrációt szabályozni, mint például az AMF (autokrin motilitási faktor) és a HGF (hepatocita növekedési faktor). Szóródás mechanizmusa Tumorsejt-ECM kölcsönhatások a keringésben Az intravazáció során a keringésbe jutott tumorsejtek az érpályában oldott állapotban levo mátrixfehérjékkel, foleg a vitronektinnel, a fibronektinnel, és a fibrinogénnel léphetnek kapcsolatba. Ezek a kapcsolatok az integrin receptorokon keresztül valósulnak meg. Azok a tumorsejtek képesek a szérum ECM-fehérjéivel kapcsolatba lépni, melyeknek fibrinogén/vitronektin receptoruk van, mint a? 3 integrin család (vitronektinreceptor:? v? 3, fibrinogénreceptor:? II? 3). Tumorsejt normál sejt kölcsönhatás az érpályában A/ Tumorsejt endotél kölcsönhatás (23, 24) Az intravazáció során a szubendoteliális bazális membrán felol érkezo tumorsejt betör az endotél rétegbe és ott mechanikus károsítás révén jut az ér lumenébe. Ez a károsodás 9
10 bekövetkezhet attól is, hogy az endotél sejtek, ha idolegesen is, de elvesztik kapcsolatukat a bazális membránjukkal. B/ Tumorsejt trombocita kölcsönhatás (25) A hematogén áttétet adó tumorsejtek jó trombocita aggregáló képességgel bírnak. A kialakuló vérlemezke buroknak két szerepe lehetséges. Egyfelol a véráramban a tumorsejtek nagy mechanikai traumának vannak kitéve, és ezt fogják fel a trombociták. Másrészrol a burokban a tumorsejtek rejtetté válnak az immunrendszer elol. Olyan tumorsejtek képesek vérlemezke aggregációra, melyek felszínén az? II? 3 integrin vagy más fibrinogén-receptor expresszálódik, mivel a vérlemezke aggregáció elsosorban a vérlemezke? II? 3 integrinje és a szérum fibrinogénje által mediált folyamat. A trombocita-tumorsejt aggregátumok létrejöttéhez a tumorsejteken trombocitákra jellemzo sejtadhéziós molekuláknak kell megjelenniük. Ilyenek a P-szelektinek, melyek gyenge adhéziós molekulák és a kezdeti véletlenszeru sejt sejt találkozások hatására jelennek meg. Kapcsolódásuk hatására újabb kálcium- függo adhéziós molekula, a PE- CAM jelenik meg a sejten. Ezek olyan jeleket indítanak el a sejtekben, melyek hatására integrinek megjelenését váltják ki; ez utóbbiak már tartós sejt mátrix vagy sejt-sejt kapcsolatot biztosíthat. Az extravazáció mechanizmusa (26, 27, 28) Ebben a folyamatban a tumorsejt endotél kapcsolat és a tumorsejt szubendoteliális membrán kölcsönhatások játszanak szerepet. A tumorsejt és az endotél közötti kölcsönhatás a lassuló keringésben az úgynevezett gö rdülési fázisban jön létre. Ekkor E- szelektinekkel közvetített gyenge cukor cukor kölcsönhatások alakulnak ki. A szelektinek aktiválódása révén elindított jelek az E-CAM (I-CAM) adhéziós molekula endotél- és tumorsejt felszínén fokozódó megjelenését eredményezik. Az I-CAM molekulák ligandjai az ellenoldali sejten lévo? 4? 1 integrinek. Ez a kapcsolat olyan aktiválást eredményez a két sejttípusban, melynek eredményeként a gördülés leáll és fix tumorsejt endotél kapcsolat alakulhat ki, amit a felszínre kerülo integrinek, a tumorsejt felol az? v? 3 vagy? II? 3, az endotél felol pedig az? v? 3 közvetít. A folyamat eredményeként az érintett endotél sejtek összehúzódnak, hozzáférhetové téve a szubendoteliális membránt. A mátrix a fokozott? 3 integrin expresszióval rendelkezo tumorsejteket kitapadásra készteti. A folyamat révén gerjesztett izgalmi állapot 10
11 eredményeként a tumorsejtek citoplazmájában rendelkezésre álló lizoszómális enzimek egy része (katepszin B, upa, kollagenáz IV) szekretálódik, és az adhéziós pontoknál degradálja az ECM fehérjét. A szolubilizálódó ECM fehérjék kemotaktikus ingerként elindítják a tumorsejtek vándorlását. A szubendoteliális mátrixban levo növekedési és motilitási faktorok szintén segíthetik az extravazáció folyamatát. A daganatok szervi áttétei Tüdo metasztázis Az emberi daganatok áttétképzésében az egyik leggyakrabban érintett szerv a tüdo.(1. táblázat) Ezt azzal a ténnyel lehet magyarázni, hogy a rosszindulatú daganatok többsége olyan anatómiai elhelyezkedésu, ahonnan az elfolyó vénák a tüdobe vezetnek, valamint a nyirokrendszeren keresztül szóródó tumorok is végül szintén a vena cava superior-ba jutnak. Az intratumorális véredényekbe kerülo tumorsejtek gyakran a vénákon keresztül jutnak a keringésbe, majd a tüdo artériába kerülnek, és mint kis embolusok elérik prekapilláris venulákat. Említésre érdemes, hogy a tüdo metasztázisok gyakran a pleura közelében helyezkednek el, aminek az oka nagyrészt ismeretlen. A nyirokrendszeri áttét a primer tumor felszínérol indul, minthogy a tumorokon belül nincsenek nyirokerek. A tumorsejtek a tüdoparenchimát retrográd módon, a mediastinális-hiláris nyirokcsomókból is elérhetik. 1. táblázat. A különbözo primer tumorok szervi áttéteinek gyakorisága Primer hely Metasztázis helye Csont (%) Agy (%) Tüdo (%) Máj (%) Tüdo Emlo Prosztata Vastag- és végbél Másrészrol, nagyon fontos és még megmagyarázatlan az, miképp képesek a tüdo artériában levo tumorsejtek átjutni a tüdo mikrocirkulációs rendszerén és az artériás keringésen át esetleg más szervekbe jutni. Ez a jelenség, melyet "ugráló 11
12 metasztázisnak neveznek, tovább erosíti az áttéti folyamat szerv szelektivitásának elméletét (30). Májáttét A máj, hasonlóan a tüdohöz, gyakran érintett a tumor szóródásban. A gasztrointesztinális rendszer daganatainak állandó jellemzoje, de a tüdo, emlo, vese, húgyhólyag, here tumorai, valamint a melanóma is gyakran ad áttétet a májba. Ez utóbbiak esetében ez inkább e tumorok szóródásának szervspecifitásával magyarázhatók, mint az anatómiai elhelyezkedésükkel, miképp a gasztrointesztinális rendszer daganatai esetében. A tumorsejtek a vena porta-ból a perilobuláris ágaknál lépnek be a májba. Többségük azonban eléri a szinuszoidokat, ezért a máj mikrometasztázisainak többsége intralobulárisan kezd el fejlodni (31). Másrészrol a mikrometasztázisok májbeli eloszlása véletlenszeru, ami a lobus preferencia hiányára utal. Jelentos, újabb keletu megfigyelés, ami ellentmond a régi dogmának, hogy a májáttétek többsége vagy szimpla portális vérellátású, vagy dupla, portális és artériás vérellátású (32). Ezt a tényt a máj metasztázisának lokoregionális kezelése tervezésénél megfontolás tárgyává kell tenni (33). Csontáttét A harmadik leggyakoribb áttéti szerv a csont. A csontáttét az emlo- és a prosztatarák jellemzoje, de a tüdo, vastagbél, vese, pajzsmirigy, here, és a húgyhólyag, vese daganatai is az esetek %-ban képeznek csontáttétet, amit szintén nem lehet megmagyarázni anatómiai okokkal. Korábban dogmatikusan úgy tartották, hogy a prosztata tumor a Batson vénákon keresztül szóródik a gerincbe (34). Manapság ezt megkérdojelezik, rámutatva a regionális artériás rendszer ezen folyamatban, hasonlóan más tumor típusokban (35, 38), betöltött szerepére. A csontvelobe bejutva a tumorsejtek vagy évekig alvó állapotban maradnak, mint ahogy az emlotumorok esetében ez általános (36), vagy proliferálni kezdenek és átalakítják a csontszövetet, ami két módon történhet. Az emlo- és vese karcinómák sejtjei, valamint a plazmocitóma sejtek osteoclast aktivációt indukálnak, ami helyi csont rezorpcióhoz, azaz oszteolitikus csont metasztázishoz vezet (37). Vannak olyan tumorok is, pl prosztata rák, amelyek gyakrabban oszteoplasztikus áttéteket képeznek, aminek az oszteoblaszt aktiváció a kulcslépése (38). 12
13 Agyi áttét Az áttétek negyedik leggyakoribb helye az agy. Elsosorban a tüdo és az emlo tumorok jellemzoje, más szervek malignitásainál ez sokkal ritkább. A leggyakrabban primer vagy szekunder tüdo tumorokból származó sejtek az artériás keringés által szóródnak. A tumorsejt embolusok a szürke- és fehérállomány határán elszukülo erekben elakadnak. Az agy különbözo területeinek artériás vérellátása nem egyforma. A kifejlodo metasztázisok gyakorisága követi ezt a mintázatot (80 % féltekei, 15 % kisagyi, 5 % agytörzsi). Érdekes, hogy más tumoroktól eltéroen, a melanóma és a tüdorák hajlamos többszörös agyi áttétek képzésére. A metasztázis képzés szerv-specificitása Az áttétkéozés szervspecificitásának problémáját Paget 1889-ben ismerte fel. Elmélete ellentétes Ewing (1928) (39) mechanikus kiszurodés elméletével. Paget felvetése a mag és talaj elmélet, mely szerint mind a tumorsejt, mind a gazdaszerv egyedi fenotípusa felelos az adott szervi metasztázis kialakulásáért. Az eltelt bo száz évben még mindig nem sikerült eleget megtudni a szervspecifikus áttétképzés részleteirol. Tudjuk, hogy az MHC molekulák és a sejtadhéziós molekulák alapján a szervek mikroerei, a tumorsejtek elsodleges szuroi, szerv-specifikus fenotípussal rendelkeznek. Így ez a fenotípus szolgálhat elsodleges felismerési mechanizmusként (40). A szubendoteliális mátrix, amely szerkezetileg eltéro szervenként, és különbözo szervspecifikus citokineket tartalmaz, ami egy másik felismerési mechanizmust jelenthet (40). Fontos felidézni azokat a kísérletes tanulmányokat, melyek azt mutatják, hogy a bazális membránok különbözo módon érintettek erosen metasztatikus tumorok szerv kolonizációjában: A máj metasztázisok a szinuszoidális szubendoteliális mátrix heparán - szulfát komponensétol, a tüdo metasztázisok pedig a mátrix laminin és fibronektin komponenseitol függtek (41). Végül a tumorsejteknek képesnek kell lenni arra, hogy reagáljanak a helyi mitogénekre, s ez korlátozó tényezo lehet a szervi metasztázis kialakulásában. Kísérletes adatok arra utalnak, hogy a különbözo tumortípusok fokozott agyi és tüdo áttét-képzo képessége tüdo- vagy agyi- eredetu transzferrinre való válaszképességtol függhet (42). Ugyanakkor a receptor, melyhez ez a transzferrin 13
14 kötodhet a tumorsejten, még nincs azonosítva: ez lehet maga a transzferrin receptor, vagy más transzferrin köto sejtfelszíni fehérjék. Sajnos, ezeket a megfigyeléseket nem követték humán tüdo vagy agyi metasztatikus tumorokon végzett tanulmányok. Az olyan, májeredetu, a humán kolón karcinóma sejtek májmetasztázis kialakulását elosegíto mitogének, mint a TGF?, EGF, és a HGF, bizonyultak a helyi növekedési faktoroknak. Másrészrol, a kolón karcinóma sejtek EGFR expresszióját próbálták összefüggésbe hozni májmetasztatikus potenciáljukkal, hogy legalább egy munkamodellt hozzanak létre a gasztrointesztinális rendszer tumorainak májszelektivitására (43). A metasztatikus folyamat csont specifitásban csont mátrix-fehérjék tumorsejtekben történo ektópiás expressziója játszhat szerepet. Azok a tumorok, amelyekben oszteonektin, oszteokalcin, és/vagy csont-szialoprotein expresszió fordul elo, (emlo-, prosztata-, és pajzsmirigydaganatok), jellemzoje a csontáttétképzés. Ezeket a daganatokat csontmetasztázis preferencia jellemzi (44, 45, 46). Szintén vannak arra utaló adatok, hogy a prosztata tumorsejtek által termelt endothelin-1, upa és PSA a csont stróma sejtek csont növekedési- (bfgf, TGF?, HGF, IGF) és csont morfogén fehérjék (BMP) termeléséhez és így az áttéti fókusz körüli új csont képzodéshez vezet (46). Oszteolítikus metasztázis akkor alakul ki, mikor a tumorsejtek oszteoklasztaktváló citokineket, PTH-szeru peptideket, TGF? -t, TNF? -t, TNF?-t, M-CSF-t, IL-16- t, vagy prostanoidokat termelnek. Jelen dolgozat szempontjából a daganatos progresszió elemei közül a HGF-fel, mint lokális növekedési faktorral, az angiogenezissel, mint a folyamat egyik limitáló lépésével, valamint a proteoglikánok ezen folyamatokban betöltött szerepével óhajtunk részletesebben foglalkozni. 14
15 A hepatocita növekedési faktor és receptora, a c-met onkoprotein Irodalmi adatok szerint kísérletes körülmények között a megnövekedett májáttét képzo képesség a tumorsejtek megnövekedett sejtfelszíni heparánszulfát proteoglikán expressziójával volt kapcsolatos (53). A hepatocita növekedési faktort (HGF) eloször patkány vérlemezkékbol (55), fulmináns májkárosodott betegek szérumából (56), valamint nyúlszérumból (57) izolálták. A HGF egy heterodimér protein, mely egy 69 kda? láncból és egy 34 kda? láncból áll (55, 56, 57). A humán HGF teljes aminósav szekvenciája ismert. (1. ábra) 1. ábra. A humán HGF szekvenciája és domén szerkezete. K1-K4=Kringle1-4 domén. Dolt betu=bázikus szekvenciák. Félkövér dolt betuk=megszintetizált bázikus szekvenciák. (54, 55, 56,57, 58, 59) signal peptide 32-alpha chain 1 MWVTKLLPAL LLQHVLLHLL LLPIAIPYAE G QRKRRNTIH EFKKSAKTTL IKIDPALKIK hairpin loop 61 TKKVNTADQC ANRCTRNKGL PFTCKAFVFD KARK QCLWFP FNSMSSGVKK EFGHEFDLYE 128 K1 121 NKDYIRNCII GKGRSYKGTV SITKSGIKCQ PWSSMIPHEH SFLPSSYRGK DLQENYCRNP K2 181 RGEEGGPWCF TSNPEVRYEV CDIPQCSEVE CMTCNGESYR GLMDHTESGK ICQRWDHQTP HRHKFLPERY PDKGFDDNYC RNPDGQPRPW CYTLDPHTRW EYCAIKTCAD NTMNDTDVPL 305 K3 301 ETTECIQGQG EGYRGTVNTI WNGIPCQRWD SQYPHEHDMT PENFKCKDLR ENYCRNPDGS K4 361 ESPWCFTTDP NIRVGYCSQI PNCDMSHGQD CYRGNGKNYM GNLSQTRSGL TCSMWDKNME DLHRHIFWEP DASKLNENYC RNPDDDAHGP WCYTGNPLIP WDYCPISRCE GDTTPTIVNL 495-beta chain HGP2 481 DHPVISCAKT KQLRVVNGIP TRTNIGWMVS LRYRNKHICG GSLIKESWVL TARQCFPSRD 541 LKDYEAWLGI HDVHGRGDEK CKQVLNVSQL VYGPEGSDLV LMKLARPAVL DDFVSTIDLP HGP1 601 NYGCTIPEKT SCSVYGWGYT GLINYDGLLR VAHLYIMGNE KCSQHHRGKV TLNESEICAG 661 AEKIGSGPCE GDYGGPLVCE QHKMRMVLGV IVPGRGCAIP NRPGIFVRVA YYAKWIHKII 721 LTYKVPQS 15
16 A HGF egyláncú 728 aminosavból álló prepropeptidként szintetizálódik, amibol 29 aminosav a szignálszekvencia és 25 aminosav a pro-szekvencia. A láncot a 494. arginin és a 495. valin között széthasítja egy proteáz, majd a keletkezett láncok diszulfid híddal kapcsolódnak. Mindkét alegységen 2 potenciális N-glikolizációs hely van, és O-kötött szénhidrátot is megfigyeltek a? láncon (57). Az? alegységen 4 db u.n. kringle domén van, és az? lánc szerepel a c-met receptor, valamint a heparin-kötésben is. A HGF-nek létezik 2 rövidebb alternatív formája is, az NK1 és az NK2. Az NK1 az? lánc N terminusától az elso kringle domén végéig tart és tartalmaz egy intron szekvenciát is (58, 59). Az NK2 lánc az? lánc N terminusától a második kringle domén végéig tart (60). A HGF génje egy másolatban van jelen a genomban, egérben az 5. kromoszómára, emberben a 7. kromoszóma q21.1 helyére lokalizálódik (61, 62). A HGF receptora a c-met onkoprotein (63), melynek génje emberben a 7. kromoszóma q21-31 helyére lokalizálódik. A c-met szintén hetrodimér protein, ami az 50 kda? láncból, valamint a hozzá diszulfid hidakkal kötött, 145 kda molekula tömegu, extracelluláris, transzmembrán, és intracelluláris katalitikus doménekbol felépülo? alegységbol áll (64, 65, 66, 67). Humán hámsejteken a c-met többféle formában expresszálódhat, melynek oka az alternatív splicing, s ennek eredményeként 200, 170, 65 kda formák jelenhetnek meg. Ez utóbbinak, melynek nincs extracelluláris doménje, src-szeru tirozin-kináz aktivitása van, s elsosorban tumorsejteken jelenik meg (68). Irodalmi adatok szerint a HGF sejtfelszíni heparánszulfát-proteoglikánokhoz történo kötodése segíti a c-met jelátviteli aktiválódását (69). Korábbi cikkek rámutattak arra, hogy a sejtfelszíni proteoglikánok fontos szerepet játszanak egyes rágcsáló és humán tumorok májáttét képzésében (30). Ezek az adatok a sejtfelszíni HSPG-k metasztázisban betöltött szerepére utalnak, ugyanakkor a HGF c-met rendszerrel fennálló esetleges kapcsolatról nincs még adatunk. A HGF és heparin közötti kölcsönhatást a citokin pozitívan töltött aminosav csoportjai (Lys, Arg, His) és a proteoglikánok glikózaminóglikánjainak negatívan töltött cukor tagjai (szulfát vagy karboxil láncok) közvetítik (70, 71, 72). A protein GAG 16
17 kölcsönhatás minimum feltétele az 5-6 egységbol álló oligoszachharid, valamint az 5-6 aminosavból álló bázikus peptid szakasz (73, 74). A HGF-et a májban az Ito-sejtek termelik (82), fiziológiás szerepe a májkárosodás utáni májregenerációban van (83). A májban a HGF jelentos része a periportális területekre lokalizálódik, s a májkárosodás utáni mitogén jel eloször a periportális területekrol indul (84). A HGF plazmaszintje emberben kisebb, mint 0.5 ng/ml (85), patkányban 20 ng/ml (86). Tumor-idukált angiogenezis, az angiogenezis formái (III) A véredények az embrióban az u.n. vaszkulogenezis során alakulnak ki. E folyamat során a differenciálatlan angioblastok in situ endotél sejtekké érnek, amelyek érhálózattá állnak össze (87). Az angoigenezis kifejezés újabban azt a folyamatot jelenti, melynek során az egyszeru érhálózat átalakul komplex hálózattá (88). Felnottben új erek foleg angiogenezissel alakulnak ki, de vaszkulogenezis is elofordulhat. A vaszkuláris miogenezis során a periciták stabilizálják az újonnan képzodött véredényeket, úgy, hogy gátolják az endotél sejtek proliferációját és migrációját, valamint serkentik az extracelluláris mátrix képzését. Az új erek gyorsabban degradálódnak, ha nem fedik oket simaizom-sejtek (89). A vaszkulogenezis A vaszkulogenezis folyamata a következo: Az endotél sejteknek és a hemopoietikus sejteknek közös osük van, a hemangioblast. A szikzacskóban a hemangioblastok csoportokat képeznek, a belso sejtek hematopoietikus progenitorokká, a külso sejtek pedig endotél sejtekké fejlodnek. Az angioblasztok migrálni képesek az in situ differenciáció elott. A VEGF, a VEGFR2, és a bfgf és receptora a FGFR (FGF receptor) befolyásolja az angioblast differenciációt (90, 91, 92, 93). A FN és receptorai az? 5? 1 és? 5? 3, valamint? v? 3 integrinek, amelyek kölcsönhatásokat közvetítenek az endotél sejtek és a mátrix makromolekulák között, szintén befolyásolják a 17
18 vaszkulogenezist. Madarakban az? v? 3 integrin részt vesz a vaszkulogenezisben, de rágcsáló embriókban nem (95). Korábban úgy gondolták, hogy endotél prekurzor sejtek csak az embrionális élet során vannak jelen, azonban felnott csontveloben és perifériás vérben kimutattak ilyen sejteket. VEGF, GM-CSF, bfgf és IGF-1 stimulálja differenciációjukat és mobilizációjukat (96, 97). Az angiogenezis Az angiogenezis újabb értelmezés szerinti folyamata az (88) a 2. táblázatban látható. Az angiogenezis vazodilatációval kezdodik, mely folyamat résztvevoje a nitrogén monoxid. VEGF hatására megno az éral permeabilitás, így plazma fehérjék jutnak ki, amelyek kijelölik a lehetséges útvonalat a migráló endotél sejteknek. Ez a permeabilitás növekedés fenesztrációk, vezikulo-vakouláris organellumok, valamint a PECAM-1 és VE-cadherin molekulák átrendezodése által jön létre (98). Az angiopoietin-1, endotél sejtek Tie2 receptorának liganduma, a vaszkuláris permeabilitás természetes gátlója. Ha kifejlett erekhez adják, védelmet ad a plazmaszivárgás ellen anélkül, hogy alapvetoen befolyásolná az ér morfológiáját (99). Az endotél sejteknek ahhoz, hogy migráljanak el kell veszíteniük interendoteliális kapcsolataikat, tehát az érett ereknek destabilizálódniuk kell. Az angiopoietin2, a Tie2 receptor szignál gátlója, feltehetoen a simaizom-sejtek endotélrol történo leválásában vesz részt (100). 2. táblázat. Az angiogenezis lépései Vazodilatáció, endotél permeabilitás növekedés és periendoteliális támogatás Endotél sejt proliferáció és migráció Endotél túlélés Endotél differenciáció A vaszkularizáció alapveto fontosságú a növekvo szövetek, de különösképpen a malignus tumorok számára, melyek e nélkül 1-2 mm-nél nagyobbra nem képesek noni (101). Az érképzodés egyik, és a legjobban tanulmányozott formája a tumor-indukálta 18
19 érújdonképzodés. Azonban más lehetoségek is vannak a tumor beerezodésre: 1. az ér inkorporáció és 2. az embrionális genotípus visszaszerzése, a vaszkuláris mimikri. Az, hogy melyik következik be a tumor típusától és a karcinogenezis során érvényesülo genetikai változásoktól függ. Tumor-indukálta neoangiogenezis Tulajdonképpen a tumor-indukálta érújdonképzodés az angiogén folyamatok túlsúlyát jelenti az anti-angiogén folyamatok felett. Napjainkra elfogadottá vált, hogy a tumorsejtek fiziológiás útvonalakat használva tudják bekapcsolni az angiogén geno- és fenotípust. (102, 103, 104). Ebben az esetben a növekvo tumorszövet hipoxiás sejtjei, melyek vad típusú HIF1a gént expresszálnak, aktiválják a HRE-t tartalmazó angiogén faktorok, köztük a fo angiogén mitogén, a VEGF génjeinek expresszióját. Daganatokban különbözo onkogének amplifikációja az angiogén faktorok túlzott kifejezodéséhez vezet. Ez jellemzo genetikai változás azon humán daganatok jelentos részében, melyekben a vad p53 expresszió elvész. Ennek az angiogenezisre ható következménye az, hogy az ilyen sejtek nem képesek expresszálni az egyik fiziológiásan legjelentosebb angiogenezis inhibitort, a thrombospondint. Ezen változások eredményeként felborul az egyensúly az angiogén és antiangiogén faktorok expressziója közt, ami elosegíti az angiogén konverzió kialakulását (105). A tumorindukált angiogenezis elso lépése az, hogy a tumorszövet körüli venulák teljes kerületén megváltozik a bazális membrán. Ez a folyamat valószínuleg a tumorsejtek által termelt mátrix metalloproteinázok, vagy plazminogén aktivátorok közremuködésével történik. Ez a változás lehet részben felelos az endotélsejtek osztódásának és migrációjának megindulásáért. Másrészt, a folyamat során olyan, a tumorsejtek, vagy a gazda sejtek által termelt angiogenetikus faktorok szabadulhatnak fel, mint a bfgf vagy VEGF. A migráló endotélsejteknek csak egyik pólusukon nincs bazális membrán. A migráció során az endotélsejtek egymással párhuzamosan helyezkednek el és megtartják bazálisluminális polaritásukat (106), következésképpen, az endotélsejtek egy hasadék-szeru lument alkotnak. Ez a lumen az eredeti ér- lumenének folytatása és intakt interendoteliális kapcsolat zárja le. Ezen modell szerint nem kell külön stimulus a lumen kialakításához, és az endotélsejtek megtartott polaritása lehetové teszi a bazális membrán folyamatos kialakítását.(106) Számos adat arra utal, hogy az új érsarjadékok 19
20 nem irányulnak a tumor felé, inkább a folyamat a tumorsejt szigetek perifériáján dús kapilláris hálózatot eredményez (107). Ez vezet ahhoz a megfigyelt tulajdonsághoz, miszerint az érdenzitás a tumor körül sokkalta nagyobb, mint magában a tumor belsejében. Az egyik lehetséges magyarázat az, hogy a folyamatosan növekvo tumorszigetek benövik az ereket a tumorfészkek perifériáján így vékonyítva ezt az érhálózatot, míg az érháló folyamatosan fejlodik az elorehaladó tumor kötoszövet határfelületen. Az erek intuszuszceptív típusú növekedése az aktív kapilláris növekedési zónán kívüli, nagyszámú nagy átméroju ereket eredményez, melyek feltehetoen a tumor táplálásában jelentosen nem vesznek részt, inkább az új érhajtásoknak biztosít helyet (106). Vaszkuláris mimikri Azok a megfigyelések, hogy a tumorsejtek maguk is képesek csatornákat formálni in vitro, a tumor erezodés egy új formáját jelenthetik. A tumorsejtek ektópiásan expresszálhatnak olyan endotél-specifikus géneket, mint pl. a TIE1, upa, HGF/c-met, amivel embrionális geno- és fenotípusra térnek vissza. A tumorsejtek csatornákat képezhetnek, melyek véletlenszeruen összekapcsolódhatnak a tumor mikrokapillárisaival. Ilyen típusú tumor szinuszok létezését humán tumorokban többen is megfigyelték (108, 109). Egyébiránt más, elméleti lehetoségek is vannak az ilyen szinuszok kialakulására, pl. a már tumor által benott normál erek programozott sejthalála (110) vagy az intratumorális erek tumorsejtek általi infiltrációja révén, ami úgynevezett mozaik erek kialakulásához vezet, amelyekben mind az endotél sejtek, mind a tumorsejtek résztvesznek a lumen megformálásában (111). Ér inkorporáció Ez a folyamat a malignus tumorok vérellátásának egyik alternatív mechanizmusa lehet. Ebben az esetben a növekvo tumorszövet benövi a már korábban létezo gazda ereket (112). Kimutatták, hogy az ilyen tumorok angiogenetikus és antiangiogenetikus faktorokat termelnek, melyek egyensúlya alapvetoen befolyásolja mind az érképzodés folyamatát, mind a bekebelezett erezet átépülését. Megfigyelték, hogy az 20
21 antiangiogenetikus faktorok túlsúlya az inkorporált erek endotél sejtjei degenerációjához és apoptózisához vezet (113). Ez a folyamat tumorsejtek által szegélyezett szinuszok kialakulásához vezethet. Ezek a csatornák elméletileg fenntarthatják kapcsolatukat a túlélo intratumorális kiserekkel, az átalakulást túlélo szubendoteliális mátrix hálózat segítségével. Ha ilyen kapcsolat létezik, akkor az ilyen szinuszokat szegélyezo tumorsejtek igen egyszeruen beléphetnek a keringésbe (ami az elso lépése a hematogén szóródásnak!) a komplex intravazációs folyamat nehézségei nélkül (114). Az antiangiogenetikus terápia jelenlegi lehetoségei Napjainkra elegendo adat gyult össze az angiogenezist szabályzó molekuláris mechanizmusokról. Világossá vált, a patológiás neoangiogenezis befolyásolása több úton érheto el, és ehhez különbözo molekulák és antiangiogenikus faktorok kombinációja szükségeltetik. Hagyományos terápiás szerek 3. táblázat. Antiangiogenikus potenciálú hagyamányos szerek Primer indikáció Molekuláris célpont Angiogenikus célpont Vinblasztin daganat Mikrotubulus Endotél permeabilitás Taxol daganat Mikrotubulus Endotél proliferáció Dolestatin daganat Mikrotubulus Endotél proliferáció Combrestatin A daganat Mikrotubulus Endotél proliferáció flavon ecetsav daganat Citokin expresszió Angiogenezis alacsony dózisú 5- daganat Timidilát szintáz Endotél proliferáció FU alacsony dózisú daganat Antifólsav Endotél proliferáció metotrexát Irsogladine gyomor fekély? Angiogenezis Radicicol bakteriális Hsp90 Angiogenezis fertozés Cyclosporin immunszupresszió Jelátvitel Angiogenezis Captopril ACE gátló ACE Ér fejlodés Celecoxib gyulladás COX-2 Endotél proliferáció Ez az érdekes csoport olyan hagyományos szereket foglal magába, amelyeket nem feltétlenül angiogenezissel kapcsolatos betegségekre terveztek eredetileg, azonban olyan mellékhatással rendelkeznek, mint pl. antiangiogenetikus képesség. Foleg daganatellenes szerek tartoznak ebbe a csoportba, de más szerek is csatlakozhatnak a 21
22 csoporthoz (3. táblázat). Ez a folyamatosan növekvo csoport új szereket biztosított már klinikai próbákra elorehaladott daganatos betegségek és szembetegségek esetében (179). Endotél növekedési faktor ligandok Mivel az elmúlt évek kutatásai azonosították a fo endotél mitogén növekedési faktorokat (VEGF, FGF, PDGF, HGF), ezek a ligandumok és a receptoraikkal történo kölcsönhatásaik lettek a fo farmakológiai célpontok. A csoport közös tulajdonsága, a heparin kötés, aminek felismerése egyszeru, de nem antiangiogén specifikus terápiás célpontot biztosít. Az elso gátlószerek szulfatált poliszacharidok (D54152), kationos peptidek (protamin) vagy molekulák (suramin) voltak. A fo angiogén mitogének peptid szekvenciáinak megismerése megkönnyítette a VEGF vagy a HGF heparinköto peptidjeinek azonosítását. Ezek az általában kis molekulájú gátlószerek kompetitív antagonistaként hatnak megakadályozva a receptor aktivációt. Bár a koncentrációjuknak in vivo sokkalta magasabbnak kell lennie a liganduménál, mégis biztonsággal adhatók, mert aránylag nem toxikusak. A legspecifikusabb megközelítés a legspecifikusabb endoteliális mitogén, a VEGF165 célpontként alkalmazása. A VEGF165 másodlagos és harmadlagos szerkezetének megismerése új információkat nyújt olyan ligandumok, monoklonális antitestek, vagy peptidomimetikumok tervezéséhez, amelyek képesek eliminálni a VEGF hatását. Különbözo sikeres kísérleti angiogenezis modellek, köztük tumor progressziós modellek után klinikai fázisba lépett a humanizált anti-vegf165 monoklonális antitest. Egy klinikumba már régen bevezetett citokint, az interferont (? /? ) újabban arra használják, hogy mind az endotél sejtekben, mind a stróma- és tumorsejtekben gátolják a FGF expressziót.(101, 105, 180, 179, 181, 182). (4. táblázat) 4. táblázat. Angiogén mitogéneken ható inhibitorok. Célpont Klinikai vizsgálat D54152-szulfatált poliszacharid FGF kationos protein (Protamin) Heparin köto ágensek kationos peptid VEGF-bol VEGF suramin (poliszulfonált naftil-urea) FGF, VEGF, HGF + anti-vegf antitest VEGF165 DistamycinA BFGF, PDGF-B Interferon? és? Citokin expresszió + Angiozyme (ribozim) VEGF + 22
23 Endoteliális mitogén receptorok A fo endoteliális növekedési faktorok megismerése lehetové tette receptoraik (flt1, KDR) azonosítását is. A VEGF165 receptor (KDR) majdnem kizárólag az endotél sejteken expresszálódik, ami egy nagyon specifikus endoteliális célpontot jelent. Már hozzáférhetoek olyan monoklonális antitestek, melyek felismerik a KDR extracelluláris doménjének különbözo epitopjait. Némely antitest, mint pl. a DC101 képes a KDR jelátvitelét befolyásolni, hasonlóan néhány anti-c-erb2 monoklonális antitesthez. Önmagában nem túl ígéretes a tumorok antiangiogén terápiája, alacsony dózisú hagyományos citosztatikus szerekkel (pl. vinblasztin) kombinálva lehetové teszi a nem kívánt mellékhatások csökkentését úgy, hogy a tumorellenes hatás megmaradjék. A PF- 4 egy természetes, endotél sejteken ható angiogenezis gátló, és rekombináns variánsát az FGF receptor kötés gátlására használják. (105) Angiogén jelátvitel Mivel az angiogén mitogének többsége tirozin kináz receptorhoz kötodik, a proliferáló endotél sejtek tirozin kináz aktivitása terápiás célpont lehet. Az angiogén jelátvitel további lépései, úgy, mint a PKC aktiváció vagy a kalcium jeltovábbítás, eroteljes de kevésbé specifikus célpontot jelenthetnek. Minthogy a mitogén jelátviteli utak révén mind a tumorsejtek, mind az endotél sejtek érintettek a terápiában, a széles spektrumú tirozin kináz gátlók használata hasznos lehet. (105, 180, 181, 183). Az ilyen hatásmechanizmusú vegyületek az 5. táblázatban láthatók. 5. táblázat. Jelátvitelre ható angiogenezis inhibitorok. Célpont Klinikai vizsgálat Izoflavonoidok Nem specifikus PTK gátlók + Staurosporin származékok Nem specifikus PTK gátlók Genistein Nem specifikus PTK gátló + SU5416(adenin mimetikus) VEGFR2 - PTK gátló + Tyrphostinek VEGFR2 - PTK gátló Izoquinolinok PDGFR - PTK gátló + Retinsav PKC gátló + Karboxiamidotriazol Ca 2+ csatorna blokkoló + TNP-470 Sejtciklus kontroll + Ocreotide Jelátvitel + PTK=protein tirozin kináz PKC=protein kináz C 23
24 Endotél sejt - ECM kölcsönhatásra ható terapeutikumok A neoangiogenezist az endotélsejt - ECM kapcsolatok megváltozása jellemzi. Az angiogén faktorok hatására olyan új adhéziós molekulák jelennek meg, mint az? v? 3 vagy? v? 5 integrinek (98). A permeábilis véredényfal átenged olyan oldékony mátrix ligandumokat, mint a vitronektin, fibrinogén, tenascin, amelyek alapveto összetevoi az újjáalakuló véredény mátrixának (184). A mitotikusan aktivált endotél sejteknek legalább részben degradálniuk kell a saját szubendoteliális membránjukat. Ezért a mitogének proteáz szekréciót is indukálnak (upa, MMP-2, MMP-9). Mivel ezek az események mind alapvetok az angiogenezis megindulásához, gyógyszerek támadási pontjai lehetnek. (6. táblázat) 6. táblázat. Endotél sejt - ECM kölcsönhatásra ható terápiás lehetoségek. Célpont Klinikai próba Mátrix ligandum Rh-angiostatin UPAR, ATP-szintáz + Rh-endostatin Kollagén receptorok + Ciklikus RGD peptid? v? 3 Accutin-disintegrin? v? 3,? v? 5 Benzodiazepinek? v? 3 Mátrix receptor Humanizált anti-? v? 3 Ab? v? 3 + Proteáz Rh-PAI-2 UPA Amilorid UPA p-amidobenzamidin UPA Anti-uPA Ab UPA Anti-uPAR Ab UPAR L-fenilalanin-N-metilamidok MMP-2, MMP-9 + (Batimastat, Marimastat) AG3340 MMP-k + Minocycline MMP-k 24
25 Az? v? 3 integrinért folyó ligand kompetíció elegendo ahhoz, hogy az endotél sejtek leváljanak mátrixukról, és mozgásképtelenné váljanak, ami apoptózishoz vezet (98). Ezt különbözo módon lehet elérni: ciklikus RGD peptidek (185), kémiai RGD mimetikumok (186), vagy kígyóméreg ligandumok (? v? 3 specifitású disintegrinek [187]). A neoangiogenezist és az endotélsejtek proliferációját és migrációját legerosebben gátló mátrix ligandumok a perivaszkuláris mátrix degradációjának termékei, a plazmin, a kollagén XVIII, angiostatin (188), valamint az endostatin (189). Ezek a proteinek igen hatékonyak mind in vitro, mind in vivo. Széles terápiás ablakkal rendelkeznek, továbbá hosszú ideig adagolható anélkül, hogy az endotél sejtekben rezisztencia alakulna ki. Az? v?3 integrin expresszió egyértelmu markere a proliferáló endotél sejtnek. Némely anti-? v? 3 monoklonális antitest antiangiogenetikus hatásúnak bizonyult, részben azért, mert apoptózist indukál. A humanizált? v? 3 antitest kifejlesztése (Vitaxin - MedImmune, RheoPro - Centocor) lehetové tette ilyen típusú ágensek klinikai alkalmazását. Az endotél sejtek migrációjához elengedhetetlen az olyan mátrix degradáló enzimek, mint a MMP-2 és upa muködése. Érdekes, hogy bár számos terápiás értéku upa inhibitor (kémiai gátlók, anti upa antitestek, anti-upar antitestek), 2001 elso feléig egy sem került klinikai vizsgálatra (180). A MMP gátlók azonban klinikai vizsgálatra kerültek (179). Mind széles spektrumú, mind MMP-2 és MMP-9 specifikus gátlók léteznek. 25
26 II. Célkituzések Humán kolorektális daganatokban kimutatták a c-met protein overexpresszióját, illetve ezen esetek 10 %-ban a gén amplifikációját. Bár a stádiummal az overexpresszió nem mutatott korrelációt, a c-met proteint overexpresszáló daganatok szignifikánsan nagyobb méretunek bizonyultak társaiknál, továbbá a vastagbél daganatok májáttéteteinek 90 %-a fokozottan expresszálta a c-met onkoproteint, az azonban nem tisztázott, hogy a HGF c-met rendszer mitogén vagy motogén hatásain keresztül játszik szerepet a kolorektális daganatok áttétképzésében (140, 141, 142, 143). A különbözo méretu bázikus peptidek különbözo biológiai aktivitással rendelkeznek a sejtproliferációban, a véralvadásban, a sejtadhézióban, stb (75, 76, 77, 78, 79, 80, 81). A HGF trunkált változatainak kísérletes rendszerekben antitumorális hatása van (192, 193). A HGF és a sejtfelszíni HSPG-k májáttétképzésben betöltött általános fontos szerepének figyelembevételével felmerült a kérdés, vajon a HGF kisméretu bázikus peptidjeinek van-e biológiai hatása a tumorsejtekre. Hogy megválaszoljuk ezt a kérdést, megszintetizáltattuk a HGF béta-láncának bázikus hexapeptid részeit és hasonló u.n. kevert bázikus hexapeptideket, azon célból, hogy megvizsgáljuk antitumorális hatásukat (7. táblázat). Jelen munka során a következo kérdések megválaszolását tuztük ki: 1. A HGF, mint a máj egyik lokális növekedési faktora szerepet játszik-e a kolorektális daganatok májáttét képzésében, azaz a HGF befolyásolja-e humán kolorektális daganatok biológiai viselkedését (proliferáció, migráció)? 2. A HGF, mint angiogén faktor befolyásolja-e a humán kolorektális daganatok esetében a neoangiogenezist? 3. A HGF heparin köto peptid szekvenciáinak van-e tumorbiológiailag értékelheto aktivitása. 4. A HGF heparin köto peptid szekvenciáinak van-e antiangiogén hatása. 26
METASZTÁZISKÉPZÉS. Láng Orsolya. Kemotaxis speciálkollégium 2005.
 METASZTÁZISKÉPZÉS Láng Orsolya Kemotaxis speciálkollégium 2005. TUMOROK ÉS MIGRÁCIÓ PRIMER TUMOR METASZTÁZIS Angiogenezis Adhézió SEJT - SEJTCIKLUS Apoptózis Kemokinek Növekedési faktorok Szabályozó fehérjék
METASZTÁZISKÉPZÉS Láng Orsolya Kemotaxis speciálkollégium 2005. TUMOROK ÉS MIGRÁCIÓ PRIMER TUMOR METASZTÁZIS Angiogenezis Adhézió SEJT - SEJTCIKLUS Apoptózis Kemokinek Növekedési faktorok Szabályozó fehérjék
I./5. fejezet: Daganatok növekedése és terjedése
 I./5. fejezet: Daganatok növekedése és terjedése Tímár József A fejezet célja, hogy a hallgató megismerje a daganatok növekedésének és biológiai viselkedésének alapjait. A fejezet teljesítését követően
I./5. fejezet: Daganatok növekedése és terjedése Tímár József A fejezet célja, hogy a hallgató megismerje a daganatok növekedésének és biológiai viselkedésének alapjait. A fejezet teljesítését követően
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
http://www.rimm.dote.hu Tumor immunológia
 http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Az Oxidatív stressz hatása a PIBF receptor alegységek összeszerelődésére.
 Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai előadás. Sej-sejt kommunikációk az immunválaszban.
 Immunológia alapjai 7-8. előadás Sej-sejt kommunikációk az immunválaszban. Koreceptorok és adhéziós molekulák. Cytokinek, chemokinek és receptoraik. A sejt-sejt kapcsolatok mediátorai: cross-talk - Szolubilis
Immunológia alapjai 7-8. előadás Sej-sejt kommunikációk az immunválaszban. Koreceptorok és adhéziós molekulák. Cytokinek, chemokinek és receptoraik. A sejt-sejt kapcsolatok mediátorai: cross-talk - Szolubilis
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi
Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése
 Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése Dr. Kerpel-Fronius Sándor Egyetemi tanár Farmakológiai és Farmakoterápiás Tanszék Semmelweis Egyetem Budapest Email: kerfro@pharma.sote.hu
Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése Dr. Kerpel-Fronius Sándor Egyetemi tanár Farmakológiai és Farmakoterápiás Tanszék Semmelweis Egyetem Budapest Email: kerfro@pharma.sote.hu
Az immunológia alapjai
 Az immunológia alapjai 8. előadás A gyulladásos reakció kialakulása: lokális és szisztémás gyulladás, leukocita migráció Berki Timea Lokális akut gyulladás kialakulása A veleszületeh és szerzeh immunitás
Az immunológia alapjai 8. előadás A gyulladásos reakció kialakulása: lokális és szisztémás gyulladás, leukocita migráció Berki Timea Lokális akut gyulladás kialakulása A veleszületeh és szerzeh immunitás
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
Immunológia alapjai. Az immunválasz szupressziója Előadás. A szupresszióban részt vevő sejtes és molekuláris elemek
 Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 3. Részjelentés: 2003. November
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 3. Részjelentés: 2003. November
Immunológia alapjai 7-8. előadás Adhéziós molekulák és ko-receptorok.
 Immunológia alapjai 7-8. előadás Adhéziós molekulák és ko-receptorok. Az immunválasz kezdeti lépései: fehérvérsejt migráció, gyulladás, korai T sejt aktiváció, citokinek. T sejt receptor komplex ITAMs
Immunológia alapjai 7-8. előadás Adhéziós molekulák és ko-receptorok. Az immunválasz kezdeti lépései: fehérvérsejt migráció, gyulladás, korai T sejt aktiváció, citokinek. T sejt receptor komplex ITAMs
A HGF/C-MET RENDSZER SZEREPE A DAGANATOK PROGRESSZIÓJÁBAN
 A HGF/C-MET RENDSZER SZEREPE A DAGANATOK PROGRESSZIÓJÁBAN Fazekas Károly Témavezeto: Dr. Tímár József Országos Onkológiai Intézet Tumorprogressziós Osztály Semmelweis Egyetem Doktori Iskola Budapest, 2003
A HGF/C-MET RENDSZER SZEREPE A DAGANATOK PROGRESSZIÓJÁBAN Fazekas Károly Témavezeto: Dr. Tímár József Országos Onkológiai Intézet Tumorprogressziós Osztály Semmelweis Egyetem Doktori Iskola Budapest, 2003
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
A CSONTPÓTLÓ MŰTÉTEK BIOLÓGIAI ALAPJAI, A JÖVŐ LEHETŐSÉGEI
 Semmelweis Egyetem Arc- Állcsont- Szájsebészeti- és Fogászati Klinika Igazgató: Prof. Németh Zsolt A CSONTPÓTLÓ MŰTÉTEK BIOLÓGIAI ALAPJAI, A JÖVŐ LEHETŐSÉGEI Dr. Barabás Péter, Dr. Huszár Tamás SE Szak-
Semmelweis Egyetem Arc- Állcsont- Szájsebészeti- és Fogászati Klinika Igazgató: Prof. Németh Zsolt A CSONTPÓTLÓ MŰTÉTEK BIOLÓGIAI ALAPJAI, A JÖVŐ LEHETŐSÉGEI Dr. Barabás Péter, Dr. Huszár Tamás SE Szak-
Immunológia Alapjai. 13. előadás. Elsődleges T sejt érés és differenciálódás
 Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Allergia immunológiája 2012.
 Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav,
 MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
A kemotaxis kiváltására specializálódott molekula-család: Cytokinek
 A kemotaxis kiváltására specializálódott molekula-család: Cytokinek Cytokinek - definíció Cytokin (Cohen 1974): Sejtek közötti kémi miai kommunikációra alkalmas anyagok; legtöbbjük növekedési vagy differenciációs
A kemotaxis kiváltására specializálódott molekula-család: Cytokinek Cytokinek - definíció Cytokin (Cohen 1974): Sejtek közötti kémi miai kommunikációra alkalmas anyagok; legtöbbjük növekedési vagy differenciációs
A 22C3 PD-L1 tesztek értékelése intézetünkben. Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs
 A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE
 Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
A sejtfelszíni receptorok három fő kategóriája
 A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
Tumor Immunológia. Tímár József Semmelweis Egyetem (SE) 2.sz. Patológiai Intézet SE Molekuláris Onkológiai Kutatócsoport
 Tumor Immunológia Tímár József Semmelweis Egyetem (SE) 2.sz. Patológiai Intézet SE Molekuláris Onkológiai Kutatócsoport Figure?3 Emerging Hallmarks and Enabling Characteristics An increasing body of research
Tumor Immunológia Tímár József Semmelweis Egyetem (SE) 2.sz. Patológiai Intézet SE Molekuláris Onkológiai Kutatócsoport Figure?3 Emerging Hallmarks and Enabling Characteristics An increasing body of research
FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére FEHÉRJE VAKCINÁK BIOTECHNOLÓGIAI ELŐÁLLÍTÁSA III.
Apoptózis. 1. Bevezetés 2. Külső jelút 3. Belső jelút
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM. Jelutak. 1. a sejtkommunikáció alapjai
 Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
A fiziológiás terhesség hátterében álló immunológiai történések
 A fiziológiás terhesség hátterében álló immunológiai történések APAI Ag ANYAI Ag FERTŐZÉS AUTOIMMUNITÁS MAGZATI ANTIGEN ALACSONY P SZINT INFERTILITAS BEÁGYAZÓDÁS ANYAI IMMUNREGULÁCIÓ TROPHOBLAST INVÁZIÓ
A fiziológiás terhesség hátterében álló immunológiai történések APAI Ag ANYAI Ag FERTŐZÉS AUTOIMMUNITÁS MAGZATI ANTIGEN ALACSONY P SZINT INFERTILITAS BEÁGYAZÓDÁS ANYAI IMMUNREGULÁCIÓ TROPHOBLAST INVÁZIÓ
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Az immunrendszer felépítése Veleszületett immunitás (komplement, antibakteriális
Kutatási beszámoló ( )
 Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
Kutatási beszámoló (2008-2012) A thrombocyták aktivációja alapvető jelentőségű a thrombotikus betegségek kialakulása szempontjából. A pályázat során ezen aktivációs folyamatok mechanizmusait vizsgáltuk.
Immunológia alapjai előadás. A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és
 Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Dr. Nemes Nagy Zsuzsa Szakképzés Karl Landsteiner Karl Landsteiner:
 Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
Doktori értekezés tézisei
 Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Immunológia 4. A BCR diverzitás kialakulása
 Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Általános daganattan II.
 Általános daganattan II. Benignus és malignus hámtumorok Semmelweis Egyetem II. Sz. Patológiai Intézet Neoplasia fogalma Kóros szövetszaporulat Genetikai és epigenetikai változásokon alapuló klonális proliferáció
Általános daganattan II. Benignus és malignus hámtumorok Semmelweis Egyetem II. Sz. Patológiai Intézet Neoplasia fogalma Kóros szövetszaporulat Genetikai és epigenetikai változásokon alapuló klonális proliferáció
A GI daganatok onkológiai kezelésének alapelvei. dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika
 A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
Immunológia Világnapja
 a Magyar Tudományos Akadémia Biológiai Osztály, Immunológiai Bizottsága és a Magyar Immunológiai Társaság Immunológia Világnapja - 2016 Tumorbiológia Dr. Tóvári József, Országos Onkológiai Intézet Mágikus
a Magyar Tudományos Akadémia Biológiai Osztály, Immunológiai Bizottsága és a Magyar Immunológiai Társaság Immunológia Világnapja - 2016 Tumorbiológia Dr. Tóvári József, Országos Onkológiai Intézet Mágikus
Az ellenanyagok szerkezete és funkciója. Erdei Anna Immunológiai Tanszék ELTE
 Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Az ellenanyagok szerkezete és funkciója Erdei Anna Immunológiai Tanszék ELTE Bev. 1. ábra Immunhomeosztázis A veleszületett és az adaptív immunrendszer szorosan együttműködik az immunhomeosztázis fenntartásáért
Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025)
 Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025) A pályázat megvalósítása során célunk volt egyrészt a molekulák asszociációjának tanulmányozására
Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025) A pályázat megvalósítása során célunk volt egyrészt a molekulák asszociációjának tanulmányozására
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterkézés megfeleltetése az Euróai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi biotechnológiai
Az orvosi biotechnológiai mesterkézés megfeleltetése az Euróai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi biotechnológiai
ÖSSZ-TARTALOM. 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3.
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
A trombocitózis, mint prediktív faktor értékelése kolorektális tumorokban
 A trombocitózis, mint prediktív faktor értékelése kolorektális tumorokban Doktori értekezés Dr. Baranyai Zsolt Semmelweis Egyetem Klinikai orvostudományok Doktori Iskola Konzulens: Hivatalos bírálók: Dr.
A trombocitózis, mint prediktív faktor értékelése kolorektális tumorokban Doktori értekezés Dr. Baranyai Zsolt Semmelweis Egyetem Klinikai orvostudományok Doktori Iskola Konzulens: Hivatalos bírálók: Dr.
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Spondylitis ankylopoeticahoz társuló osteoporosis
 Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Spondylitis ankylopoeticahoz társuló osteoporosis Szántó Sándor DE OEC, Reumatológiai Tanszék 2013.11.05. Szeminárium Csontfelszivódás és csontképzés SPA-ban egészséges előrehaladott SPA Spondylitis ankylopoetica
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia alapjai előadás MHC. szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás.
 Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
Immunológia alapjai 5-6. előadás MHC szerkezete és genetikája, és az immunológiai felismerésben játszott szerepe. Antigén bemutatás. Antigén felismerés Az ellenanyagok és a B sejt receptorok natív formában
INTRACELLULÁRIS PATOGÉNEK
 INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
INTRACELLULÁRIS PATOGÉNEK Bácsi Attila, PhD, DSc etele@med.unideb.hu Debreceni Egyetem, ÁOK Immunológiai Intézet INTRACELLULÁRIS BAKTÉRIUMOK ELLENI IMMUNVÁLASZ Példák intracelluláris baktériumokra Intracelluláris
A Caskin1 állványfehérje vizsgálata
 A Caskin1 állványfehérje vizsgálata Doktori tézisek Balázs Annamária Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezeto: Dr. Buday László egyetemi tanár, az orvostudományok doktora
A Caskin1 állványfehérje vizsgálata Doktori tézisek Balázs Annamária Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezeto: Dr. Buday László egyetemi tanár, az orvostudományok doktora
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet november 19., ÁOK, III.
 ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
A kemotaxis jelentősége a. betegségek kialakulásában
 A kemotaxis jelentősége a betegségek kialakulásában A kemotaxis jelentősége fertőzések esetén (1) Akut bőrsérülések citokin (IL-8)) felszabadulás TNF ill. IL-6 6 NEM szabadul fel Pseudomonas aeruginosa
A kemotaxis jelentősége a betegségek kialakulásában A kemotaxis jelentősége fertőzések esetén (1) Akut bőrsérülések citokin (IL-8)) felszabadulás TNF ill. IL-6 6 NEM szabadul fel Pseudomonas aeruginosa
Antigén, Antigén prezentáció
 Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői.
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Sejt - kölcsönhatások az idegrendszerben
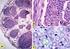 Sejt - kölcsönhatások az idegrendszerben dendrit Sejttest Axon sejtmag Axon domb Schwann sejt Ranvier mielinhüvely csomó (befűződés) terminális Sejt - kölcsönhatások az idegrendszerben Szinapszis típusok
Sejt - kölcsönhatások az idegrendszerben dendrit Sejttest Axon sejtmag Axon domb Schwann sejt Ranvier mielinhüvely csomó (befűződés) terminális Sejt - kölcsönhatások az idegrendszerben Szinapszis típusok
A jel-molekulák útja változó hosszúságú lehet. A jelátvitel. hírvivő molekula (messenger) elektromos formában kódolt információ
 A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
9. előadás Sejtek közötti kommunikáció
 9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
10. Tumorok kialakulása, tumor ellenes immunmechanizusok
 10. Tumorok kialakulása, tumor ellenes immunmechanizusok Kacskovics Imre Biológiai Intézet Immunológiai Tanszék 2016. április 27. TUMOR Tumor (neoplázia): növekedési kontroll (immunosurveillance) alól
10. Tumorok kialakulása, tumor ellenes immunmechanizusok Kacskovics Imre Biológiai Intézet Immunológiai Tanszék 2016. április 27. TUMOR Tumor (neoplázia): növekedési kontroll (immunosurveillance) alól
B-sejtek szerepe az RA patológiás folyamataiban
 B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán
 Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán Dr. Gelencsér Viktória, Dr. Boér Katalin Szent Margit Kórház, Onkológiai
Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán Dr. Gelencsér Viktória, Dr. Boér Katalin Szent Margit Kórház, Onkológiai
A véralvadás zavarai I
 A véralvadás zavarai I Rácz Olivér Miskolci Egyetem Egészségügyi kar 27.9.2009 koagmisks1.ppt Oliver Rácz 1 A haemostasis (véralvadás) rendszere Biztosítja a vérrög (véralvadék, trombus) helyi keletkezését
A véralvadás zavarai I Rácz Olivér Miskolci Egyetem Egészségügyi kar 27.9.2009 koagmisks1.ppt Oliver Rácz 1 A haemostasis (véralvadás) rendszere Biztosítja a vérrög (véralvadék, trombus) helyi keletkezését
HORMONKEZELÉSEK. A hormonkezelés típusai
 HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA NOVEMBER
 Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
15. * A sejtbiológia gyakorlata. 15.1. Sejt- és szövettenyésztés: módszertani alapismeretek MADARÁSZ EMÍLIA
 15. * A sejtbiológia gyakorlata 15.1. Sejt- és szövettenyésztés: módszertani alapismeretek MADARÁSZ EMÍLIA 15.1.1. A sejt- és szövettenyészetek típusai 15.1.2. Sejttenyészetek készítése 15.1.2.1. Primer
15. * A sejtbiológia gyakorlata 15.1. Sejt- és szövettenyésztés: módszertani alapismeretek MADARÁSZ EMÍLIA 15.1.1. A sejt- és szövettenyészetek típusai 15.1.2. Sejttenyészetek készítése 15.1.2.1. Primer
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban
 A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Írta: Dr. Bogos Krisztina Országos Korányi Tbc és Pulmonológiai Intézet Semmelweis Egyetem, Klinikai Orvostudományi
A csontvelői eredetű haem-és lymphangiogén endothel progenitor sejtek szerepe tüdőrákokban Írta: Dr. Bogos Krisztina Országos Korányi Tbc és Pulmonológiai Intézet Semmelweis Egyetem, Klinikai Orvostudományi
Receptorok, szignáltranszdukció jelátviteli mechanizmusok
 Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont
 Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Az adaptív immunválasz kialakulása. Erdei Anna Immunológiai Tanszék ELTE
 Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
Az adaptív immunválasz kialakulása Erdei Anna Immunológiai Tanszék ELTE NK sejt T Bev. 1. ábra Immunhomeosztázis A veleszületett immunrendszer elemei nélkül nem alakulhat ki az adaptív immunválasz A veleszületett
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 6. előadás Humorális és celluláris immunválasz A humorális (B sejtes) immunválasz lépései Antigén felismerés B sejt aktiváció: proliferáció, differenciálódás
Immunológiai módszerek a klinikai kutatásban 6. előadás Humorális és celluláris immunválasz A humorális (B sejtes) immunválasz lépései Antigén felismerés B sejt aktiváció: proliferáció, differenciálódás
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
4. A humorális immunválasz október 12.
 4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
A rosszindulatú daganatok metasztatizálásában kitüntetett szerepe van a sejtek mozgási képességének. A tumorok beereződése után egyes sejtek leválnak
 A rosszindulatú daganatok metasztatizálásában kitüntetett szerepe van a sejtek mozgási képességének. A tumorok beereződése után egyes sejtek leválnak a tumorszövetről, és lokális invázió után a keringésbe
A rosszindulatú daganatok metasztatizálásában kitüntetett szerepe van a sejtek mozgási képességének. A tumorok beereződése után egyes sejtek leválnak a tumorszövetről, és lokális invázió után a keringésbe
