TRANSZPORTFOLYAMATOK 1b. Fehérjék. 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS
|
|
|
- Marika Hegedűs
- 9 évvel ezelőtt
- Látták:
Átírás
1 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen 100,000 félét). A különféle fehérjék kb. fele a sejtmembránba épül be vagy kiválasztódik (szekretálódik). Sok hormon receptor és transzporter protein a plazma membránhoz szállítódik, más fehérjék, pl. az RNS polimeráz és DNS polimeráz a sejtmagba transzportálódnak, míg az extracelluláris mátrix komponensei a sejtfelszínre kerülnek, a hormonok és az emésztő enzimek pedig kiválasztódnak. A fehérjetranszport 3 fő típusát különböztetjük meg: (1) membránokba vagy a membránokon keresztül (mitokondrium, kloroplasztisz, peroxiszóma) történő transzport (2) transzport hólyagok (vezikulumok) általi szállítás (ER, Golgi, lizoszóma, sejtfelszín, endoszóma) (3) a magpóruson keresztül történő fehérje transzport (sejtmagba, vagy sejtmagból) Az 1A DIÁ-n a (2)-es típusú útvonala szekretoros, a másik kettőt pedig nem-szekretotos útvonalaknak nevezzük. Az újonnan szintetizált fehérjék szállítását a rendeltetési hely felé a fehérjék célbajuttatásának (angolul: protein targeting vagy protein sorting) nevezzük, mely két alapvetően különböző mechanizmust foglal magában. A nem szekretoros útvonal során a fehérjék egyedileg szállítódnak, míg a szekretoros útvonal a fehérjék nagy tömegben való szállítását teszi lehetővé. Mindkét esetben szignál szekvenciák határozzák meg a szállítás célpontját. Az egyedileg szállított fehérjék maguk tartalmazzák ezt a szignált, míg a szekretoros útvonal esetén ez a szignál vezikulumok felszínén található. Mindkét esetben a transzport infrastruktúráját a mikrotubulusok alkotják, a szállítás pedig a motorfehérjék segítségével megy végbe (ezek felismerik a szállítandó fehérjéket). 1 DIA 1C (A) A nem-szekretoros útvonal során egy fehérje egy sejtszervecske (organellum) membránjába vagy a belső üregébe kerül (lumen) kerül. A membrán proteinek esetén a célbajuttatás a lipid kettős rétegbe való beépüléshez vezet, míg a vízoldékony fehérjék esetében, a fehérje a sejtszervecske belsejébe kerül. Ebben a folyamatban a riboszómákon keletkezett fehérjék (1) vagy a citoplazmában maradnak ha nincs szignál szekvenciájuk; (2), vagy mitokondriumba (3), a kloroplasztiszba (4), a peroxiszómába (5) ill. a sejtmagba (6) szállítódnak. DIA 1C (B) A szekretoros útvonal azokra a fehérjékre jellemző, amelyek az durva-felszínű ER membránba integrálódnak, vagy azért mert az ER membránja vagy lumene a végcéljuk, vagy csak átmenetileg tartózkodnak ebben a sejtszervecskében. Ebben az útvonalban a fehérjék mozgásának iránya a következő lehet: az újonnan képződött fehérje (1) a durva-felszínű ER felé irányítódik (2), majd innen a Golgiba (3), innen pedig a plazma membránba (4a), vagy a lizoszómákba (4b) kerülnek, vagy kiválasztódnak a sejtből (nincs ábrázolva). Az ER-ba való irányítás során a fehérjék szintézise még folyamatban van. A Golgi, a lizoszómák ill. a citoplazma membrán felé való szállítás a transzport vezikulumokban (szállító hólyagocskákban) történik. A vezikulumok membrán lefűződéssel válnak le a donor (küldő) sejtszervecskékről, majd membránfúzió révén ürítik a tartalmukat a cél-organellumokba. A szekretoros útvonal során képződött fehérjéket szekretoros proteineknek nevezzük. Megjegyzés: az ER-ba való transzport célja kettős lehet: az ER lehet a fehérje transzport végcélja, vagy csak átmeneti állomása. Azok a fehérjék, amelyek végleges helye az ER, szintén a szekretoros útvonalra
2 kerülnek, mivel, rendszerint a Golgi készülékbe transzportálódnak, ahol poszt-transzlációs módosításokon (pl. glükoziláció) mennek keresztül, majd visszakerülnek az ER-ba. Minden mrns a citoplazmás riboszómákon kezd el szintetizálódni, de a szekretoros útvonal fehérjéit leolvasó riboszómák az ER-hoz vándorolnak, s ott folytatják a transzlációt. Az ER-hez való transzportot a fehérjéken lévő ER szignál szekvenciák határozzák meg. Azt az információt, amely meghatározza, hogy hová kerüljön egy protein, egy az N-terminálison elhelyezkedő aminosavat tartalmazó aminosav szekvencia hordozza, melyet szignál szekvenciának nevezünk (a szignál szekvenciát nem tartalmazó fehérjék a citoplazmában maradnak). Minden sejtszervecske tartalmaz olyan receptorokat, amelyek felismerik a szignál szekvenciákat pontosabban a szignál szekvenciákhoz kapcsolódó szignál felismerő részecskéket (SRP; signal recognition particle), így biztosítván, hogy a fehérje megfelelő helyre kerüljön. Amint egy szignál szekvenciát tartalmazó fehérje kapcsolatba lép (az SRP-n keresztül) a megfelelő receptorral, a fehérje egy ún. transzlokációs csatornába kerül, amely lehetővé teszi a membránon való áthaladást. Ezt követően, bizonyos típusú fehérjék a membránban maradnak, mások pedig tovább szállítódnak a sejtszervecske valamilyen szub-kompartmenjébe, mely folyamathoz más szignál szekvenciák és receptorok is szükségesek. A szignál szekvenciákat - a feladatuk elvégzését követően - egy specifikus proteáz (szignál peptidáz) eltávolítja a fehérjéből. 2 TRANSZPORT AZ ENDOPLAZMÁS RETIKULUMBA A szekretoros proteinek transzlokációja az ER membránon át A szekretoros proteinek a citoszólban lévő riboszómákon kezdenek el szintetizálódni. Ezt követően, a fehérje N-terminálisán elhelyezkedő aminosavból álló szignál peptid (= szignál szekvencia) egy specifikus SRP-hez kapcsolódik, ami az ER membránja felé irányítja a riboszómákat, ahol megkezdődik a még szintetizálódó fehérjék ER membránon keresztüli transzlokációja (áthelyeződése). A különböző szekretoros proteinek szignál szekvenciája egy vagy több pozitív töltésű aminosavat tartalmaz, mely 6-12 hidrofób aminosavval határos, de egyébként más hasonlósággal nem rendelkeznek. A legtöbb szekretoros protein szignál szekvenciája levágódik még azelőtt, hogy a fehérje transzlációja befejeződött volna, ezért az érett fehérjék zöme nem tartalmaz az ER felismeréséhez szükséges szignál szekvenciát. A célba juttatás (targeting) két kulcskomponense a (1) szignál-felismerő részecske (SRP) és az SRP-t felismerő (2) SRP receptor, mely az ER membránban helyezkedik el. Az SRP egy citoplazmás ribonukleoprotein (egy 300 nukleotidból álló RNS-ből és 6 fehérje alegységből álló komplex), amely átmenetileg kapcsolódik a képződő fehérje ER szignál szekvenciájához, a riboszóma nagy alegységéhez, és az SRP receptorhoz (= szignál szekvencia receptor). Az SRP és az SRP receptor nem csupán a fehérje és az ER membrán kölcsönhatását segítik, hanem engedélyezik a fehérjeszintézis elongációját is, de csak az ER membrán jelenlétében (tehát, az SRP szabályozza a transzlációt). Végső soron, az SRP és az SRP receptor funkciója a fehérjéket szintetizálódó riboszómák ER membránhoz való szállítása. A riboszóma és a képződő fehérjelánc átkerül az ún. transzlokonra (másnéven transzlokációs csatorna), ami egy 3 fehérje által bélelt csatorna a membránban. A transzláció előrehaladtával a növekvő fehérjelánc a riboszóma nagy alegységéről közvetlenül a transzlokon központi pórusába kerül. A 60S riboszómális alegység úgy helyezkedik el, hogy a növekvő peptidlánc nem kerül érintkezésbe a citoplazmával, és nem kezd kialakulni a 3D-s szerkezete. A transzlokon egy szabályozott csatorna, csak akkor nyílik ki, ha hozzákötődik a riboszóma-fehérje komplex. Az ER lumenében a szignál peptidáz enzim levágja a növekvő polipeptid szignál szekvenciáját. Ez a proteáz egy transzmembrán ER protein, amely a transzlokonhoz kapcsolódik. A szignál szekvencia eltávolítását követően a szintetizálódó fehérjelánc áthalad a transzlokonon keresztül, s az ER lumenébe kerül. A transzlokon addig van nyitott állapotban, amíg a transzláció be nem fejeződik, s a teljes polipeptid lánc át nem kerül az ER lumenébe.
3 DIA 2 ER szignál szekvencia A fehérjeszintézis során a riboszómákon készülő szignál szekvenciát tartalmazó polipeptidek, még a szintézis befejezése előtt elkezdik transzportjukat az ER-ba. 1. A fehérjeszintézis a citoplazmában kezdődik, majd a durva-felszínű ER-on folytatódik. 2. A polipeptid szignál szekvenciája a szignál felismerő részecskéhez (SRP) kötődik, majd az SRP-t felismeri az ER membrán receptor proteinje (SRP receptor). 3. A SRP leválik, a szignál szekvencia pedig a receptor csatornáján áthalad. 4. Az ER-ban a szignál szekvenciát a szignál peptidáz enzim eltávolítja. 5. A polipeptid lánchosszabbodása (elongáció) folytatódik. 6. A transzláció befejeződik. 7. A riboszóma leválik, a fehérje pedig feltekeredik (kialakul a normál térszerkezete chaperonok segítségével) az ER-ban. Megjegyzés: ez az ábra nem tartalmazza az SR-t és annak receptorát. 3 Az ER-ben képződő fehérjék többsége elhagyja az ER-t (az ER-ben maradást egy 4 aminosavból álló peptid szignál határozza meg: lys-asp-glu-leu). Az ER-ről lefűződő transzport vezikulumok a Golgi felé veszik az útjukat, ahol a szállított fehérjék glükozilálódnak, majd a sejten belüli transzportjukat (sejtmembrán vagy a lizoszómák) további szignál szekvenciák és a glükozilációval kapcsolódott oligoszacharidok határozzák meg. Azok az ER-ba került fehérjék, amelyeknek nincsenek egyéb szignáljai, kiválasztásra kerülnek. Néhány szignál szekvencia-féleség elnevezése: a sejtmagba irányító szignál szekvencia neve NLS (nuclear localization signal); a mitokondriumba irányító szignál: MTS (mitochondrial targeting signal), a sejtmagvacskába az NoLS (nucleolar localization signal) irányít, a CTS (chloroplast transit signal) a kloroplasztiszba, a PTS (peroxisomal targeting signal) pedig a peroxiszómákba irányít. A szignál szekvenciák rendszerint a fehérjék N-terminálisán helyezkednek el, kivéve a PTS2-t, ami a C-terminálison található (de a PTS1 az N-terminálison). A szignál szekvencia egyéb elnevezései: szignál peptid, lokalizációs szignál, targeting szignál és tranzit peptid. Szignál szekvenciának nevezik a szignál peptidet kódoló DNS régiót is. A szignál szekvenciák felfedezéséért Günter Blobel Nobel díjban részesült (1999). Megjegyzés: azoknak a fehérjéknek, melyek NoLS szekvenciákat tartalmaznak, rendelkezniük kell NLSel is a sejtmagba való bejutáshoz. DIA 3 Protein transzport az ER-ba röviden: csak az előző ábrán nem említetteket tárgyaljuk. A riboszómákat, az mrns-t és a képződő fehérjét szállító SRP és az SRP receptor kapcsolódását erősíti a GTP kötődése mind az SRP-hez és az SRP receptorhoz. Ezt követően az SRP receptor közelében lévő zárt transzlokon közelébe kerül a riboszóma a növekvő fehérje lánccal, ami a transzlokon kinyílását eredményezi. Az SRP és az SRP receptor GTP-jének a hidrolízise (GDP-vé alakulása) biztosítja az energiát a polipetid áthaladáshoz a transzlokon központi pórusán, s közben az inaktívvá vált SRP leválik a szignál szekvenciáról. A folyamat további részleteit illetően ld. DIA3. DIA 4 A szignál felismerő részecske szerkezete és alegységeinek funkcióit illetően ld. az ábrát. Egy SRP 6 fehérje alegységből és egy 300 bp hosszúságú kis nem-kódoló RNS-ből (7 SL RNS) áll. Általánosan az ilyen fehérje-rns komplexeket ribonukleo-proteineknek (RNP)-knek nevezzük. A P68/P72 és a P9/P14 alegységek dimereket alkotnak. A fehérje alegységeket gyakran P (pl. P54, P19) helyett SRP -nek nevezik (SRP54, SRP19).
4 Proteinmódosítás, folding és minőségkontroll az ER-ben A durva felszínű ER felszínén képződő membrán fehérjék és az oldható szekretoros fehérjék 4 fő módosuláson esnek át mielőtt elérik a rendeltetési helyüket: (1) glükoziláció (szénhidrátok hozzáadása és módosítása az ER-ben és a Golgi-ban) (2) diszulfid híd képzése az ER-ben (3) a polipeptid lánc helyes térszerkezetének kialakítása (folding = hajtogatás, tekeredés) és a több alegységből álló proteinek összeszerelődése (4) specifikus proteolitikus vágások az ER-ban, a Golgi-ban és a szekretoros vezikulumokban A durva felszínű ER-ok felszínén képződő fehérjék túlnyomó többségéhez szénhidrátok kapcsolódnak, s így a glükoziláció a legfontosabb poszt-transzlációs módosítás. A glükoproteinek szénhidrát lánca kapcsolódhat a szerin és a treonin hidroxil csoportjához (O-kapcsolt oligoszacharid), vagy az aszparagin amid nitrogénjéhez (N-kapcsolt oligoszacharid). Az O-kapcsolt oligoszacharidok, mint pl. a kollagénhez kapcsolt típusok, csak 1-4 cukor alegységet tartalmaznak, míg a gyakoribb N- kapcsolt oligoszacharidok komplexebbek, több elágazást tartalmaznak az emlős sejtekben. Az N-kapcsolt oligoszacharidok az ER-ben szintetizálódnak, majd kémiailag módosulnak az ER-ban, s főként a Golgi-ban. A diszulfid híd képződés a folding és a multimer fehérjék összeszerelődése a durva felszínű ER-ben történik, csupán helyesen összeszerelt fehérjék transzportálódnak az ER-ből a Golgi komplexbe, majd onnan a végső célállomásra, a nem megfelelően összeszerelt fehérjék szelektíven visszatartódnak az ER-ben. 4 DIA 5 (1) Glükoziláció Az N-kapcsolt oligoszacharidok bioszintézise a durva felszínű ER-ban történik egy előre elkészített oligoszacharid prekurzor (14 alegységből áll) fehérjéhez való hozzáadásával. Ez a prekurzor ugyanaz az állatokban, a növényekben és az egysejtűekben: egy elágazó oligoszacharid, amely 3 glükózt, 9 mannózt, és 2 N-acetilglükózamin molekulát tartalmaz. Ez az elágazó szénhidrát szerkezet módosul az ER-ben és a Golgi-ban. A glükoproteinek oligoszacharidjai különféle funkciót töltenek be: (1) ER-ben való összeszerelődésben (néhány protein esetében); (2) stabilitásban (sok szekretált protein esetében); (3) a sejt adhézióban; (4) más sejtfelszíni molekulák szénhidrát oldalláncai immunválaszt képesek kiváltani. (2) Diszulfid híd (nincs DIA) Mind az intra- és intermolekuláris diszulfid hidak ( S S ; két cisztein által létesített) a fehérjék harmadlagos- és negyedleges szerkezetét stabilizálják. A diszulfid kötések a durva felszínű ER lumenében képződnek, tehát, csak a szekretoros proteinekben és a membrán fehérjék exoplazmás doménjeiben fordulnak elő. A citoszólikus és organellum fehérjék nem tartalmaznak diszulfid hidakat. A diszulfid híd kialakulását a protein diszulfid izomeráz (PDI) enzim végzi, mely különösen nagy mennyiségben fordul elő a máj és a hasnyálmirigy szekretoros sejtjeiben. A diszulfid híd kialakulása szekvenciálisan történik, tehát, a ciszteinek a képződésük sorrendjében kapcsolódnak össze egymással. Néha, a szekvenciális összekapcsolódás nem megfelelő. Például, a proinzulin 3 diszulfid hídja szekvenciálisan képződik (1 2, 3 4, 5 6 a ciszteinek kötési sorrendje), de az érett fehérje már 1-4, 2-6, és 3 5 sorrendben tartalmazza a ciszteineket. Az újrarendeződést szintén a PDI enzim végzi. DIA 6 (3) Chaperonok és egyéb ER proteinek segítik a fehérjék foldingját és összeszerelését Habár sok denaturált fehérje képes in vitro körülmények között spontán újra kialakítani a natív 3D-s szerkezetét, ez a folyamat több órát vesz igénybe. Az ER-ben képződő membrán fehérjék azonban a keletkezésüket követően néhány perc alatt kialakítják a normális térszerkezetüket. Ezt a folyamatot specifikus ER lumenben előforduló proteinek végzik. A trimer szerkezetű hemagglutinin (HA 0 ) molekula feltekeredését mutatjuk be az ábrán. A BiP (binding immunoglobulin protein), mely egy chaperon, átmenetileg kapcsolódik a képződő fehérjékhez, s ezáltal megakadályozza hibás foldingot és az aggregátumok képződését. A PDI is részt vesz a fehérje stabilitás kialakításában (diszulfid híd kialakítása). Két másik ER protein, a kalnexin és a kalretikulin (ezek ún. lektinek; szénhidrát-kötő fehérjék) szelektíven kötnek bizonyos N-kapcsolt oligoszacharidokat a még nem összeállt vagy rosszul összeállt proteineken, s ezáltal megakadályozza az aggregációjukat. Egy másik fontos proteinfolding katalizátor a peptidil-prolil izomeráz, amely felgyorsítja a peptidil-prolil kötések körüli rotációt. A fenti kölcsönhatások révén kialakult HA 0 monomer egyetlen -hélix segítségével beépül a membránba. A transzmembrán szegmensek kölcsönhatása következtében kialakul a stabil trimer szerkezet. Megjegyzések: (1) Az oligoszacharil transzferáz a glükozilációért felelős enzim. (2) A prolin a fehérjelánc görbületeinek kialakulásában kulcsszerepet játszik: a prolin cisz transz konformáció váltását (izomerek) a peptidil-prolil izomeráz enzim katalizálja.
5 A MEMBRÁN FEHÉRJÉK OSZTÁLYAI DIA 7 Az integráns fehérjék 4 topológiai osztálya A membránfehérjék jellemzője, hogy hány membránba épülő szegmenst tartalmaznak. Egy szegmens hidrofób aminosavból áll, s -hélix szerkezetű. Az integráns membrán proteineket 4 topológiai (térszerkezeti) csoportba lehet sorolni. Az I., II. és III. topológiai osztályú fehérjék egyetlen transzmembrán szegmenst tartalmaznak. Az I. típusú proteinek N-terminális vége a lumen belsejében helyezkedik el (a szignál szekvenciája levágódott), a C- terminális része pedig a citoszólba lóg. A II. típusú proteinek esetében fordított a helyzet: az N- terminális a citoszól felé, a C-terminális pedig a lumen belseje felé néz. A III. típusú proteinek az I. típusú fehérjékhez hasonló szerkezetűek, de nincs levágható szignál szekvenciájuk. A IV. típusú fehérjék többszörös membrán-átszelő szegmenst tartalmaz (az ábra egy G protein-kapcsolt receptort mutat be: e receptor család jellemzője a 7 transzmembrán szegmensből álló szerkezet). 5 Az I. típusú membrán proteinek esetében 2-, a II. és III. típusú proteineknél 1-, a IV. típusú fehérjéknél pedig változó számú szekvencia határozza meg a membránba való integrációt és a membránban való elhelyezkedés irányultságát (orientációt); ezeket a szekvenciákat topogén szekvenciáknak nevezzük. DIA 8 I. típusú membrán proteinek Minden I. típusú transz-membrán protein tartalmaz egy N- terminális szignál szekvenciát (ER-szignál peptid: az ER-be irányítja a fehérjét) és hidrofób aminosavakból álló -hélixet, ami az ER membránba ágyazódik. Amint a növekvő polipeptid lánc N- terminálisa belép a lumenbe, a szignál szekvencia levágódik. A szekretoros proteinekkel szemben, a polipeptid nem halad tovább a lumen felé, mert egy a fehérje közepén elhelyezkedő, 22 hidrofób aminosavból álló szekvencia megállítja a transzfer folyamatát. Ez a belső topogén szekvencia, lévén hidrofób, képes laterális (oldali) irányban mozogni a transzlokonon át, s így a foszfolipid kettősrétegbe kerül, ahol lehorgonyoz. E kettős funkciója miatt, ezt a 22 aminosavból álló szakaszt stop-transzfer horgony szekvenciának nevezzük. A transzlokáció megszakítását követően a transzláció folytatódik a riboszómákon. A fehérje C-terminálisa a citoszólba kerül. Ezek a fehérjék tehát két topogén szekvenciát tartalmaznak: (1) a szignál szekvencia és (2) a stop-transzfer horgony szekvencia. Megjegyzés: a durva-felszínű ER membránjába beépülő fehérjék ezen típusa tehát nem kerül a Golgiba, hanem ottmarad az eredeti helyén. Más ER fehérjék azonban a szekretoros útvonalon eljutnak a Golgiba, majd visszaszállítódnak az ER-be. DIA 9 II. és III. típusú membrán proteinek, eltérően az I. típusú fehérjéktől, nem rendelkeznek N- terminális ER szignál szekvenciával. Ehelyett, mindkettő tartalmaz egy egyedi belső hidrofób szignálhorgony szekvenciát, amely kettős funkcióval rendelkezik: 1. ER szignál szekvencia (ezt ismeri fel egy SRP) és 2. membrán-kihorgonyzó szekvencia. A II. és III. típusú proteinek ellentétes orientációban helyezkednek el a membránban; ez a különbség a szignál-horgony szekvenciájuk orientációjától függ. (a) A II. típusú fehérjék esetében a szignál-horgony szekvencia úgy irányítja a fehérjeláncot a membránba, hogy az N-terminus a citoszól felé néz. Ez a szekvencia nem vágódik le, és a transzlokonban marad, mialatt a C-terminális régió benyomul az ER lumenébe. A szintézis alatt a szignál-horgony szekvencia laterálisan mozog, s bekerül a foszfolipid rétegbe, ahol membrán horgonyként funkcionál. (b) A III. típusú proteinek esetében, a szignál-horgony szekvencia, mely az N- terminushoz közel helyezkedik el, a növekvő láncot fejjel az ER lumen felé irányítja. A szignál-horgony szekvencia szintén megakadályozza a polipeptid lánc ER lumenben való haladását, s stop-transzfer szekvenciaként funkcionál. A beépülés orientációját meghatározó szignál-horgony szekvenciák egyik sajátossága, hogy a hidrofób szegmens közelében nagy sűrűségben fordulnak elő pozitív töltésű aminosavak, melyek, valamilyen ok miatt, a citoszólban való elhelyezkedést preferálják, s ezáltal meghatározzák a fehérje transzlokonban való orientációját. A II. típusú proteinek szignál-horgony
6 szekvenciákhoz képest az N-terminális oldalon tartalmazzák a pozitív töltésű aminosavakat, míg a III. típusúak a C-terminálisuk felé. Megjegyzés: az ábrán csak a II. típusú fehérjéket mutatjuk be. DIA 10 IV. típusú membrán proteinek: többszörös belső topogén szekvenciák A IV. típusú proteinek 2 altípusba sorolhatóak, attól függően, hogy az N-terminálisuk a citoszólba vagy az exoplazmás térbe (ER: lumenbe; plazma membrán: extracelluláris térbe) nyúlik. Ezt az N-terminálishoz legközelebb elhelyezkedő hidrofób szegmens és az ezt határoló szekvenciák töltése határozza meg. Ha egy IV. típusú protein páros számú transzmembrán -hélixet tartalmaz, akkor mind az N- és a C-terminus a membrán ugyanazon oldalán fog elhelyezkedni. Ellenben, ha a protein páratlan számú transzmembrán szegmenst tartalmaz, a két vég a membrán ellenkező oldalán fog elhelyezkedni. Mindkét típus tartalmaz belső stop transzfer horgony (STA) és szignál horgony (SA) szekvenciákat. IV-A típusú proteinek: N-terminus a citoszólban Ebbe a típusba tartoznak pl. a különféle glükóz transzporterek és a legtöbb ioncsatorna. Ezeknél a proteineknél az N-terminálishoz legközelebbi hidrofób szegmens a citoszól felé orientálja az N- terminálist (mint a belső szignál-horgony szekvencia a II. típusú fehérjéknél). A transzláció során a láncnövekedés folytatódik egészen a 2. hidrofób -hélix képződéséig, ami megakadályozza a transzlokonon keresztül való további haladást (hasonlóan az I. típusú fehérjék stop-transzfer szekvenciáihoz). Az első két transzmembrán szegmens szintézisét követően a fehérje mindkét vége a citoszólban helyezkedik el, míg a köztük lévő hurok az ER lumenében. A C-terminus tovább növekszik a citoszólban (mint az I. és III. típusú fehérjéknél). A 3. -hélix egy másik szignál-horgony szekvenciaként funkcionál, míg a 4. -hélix egy stop-transzfer szekvencia szerepét tölti be. 6 IV-B típusú proteinek: N-terminus az exoplazmás térben A G-protein-kapcsolt receptorok családja alkotja a IV-B típusú proteinek legnépesebb csoportját. Ezek a proteinek 7 transzmembrán -hélixet tartalmaznak, az N-terminálisuk az exoplazmás térbe (lumen vagy extracelluláris tér) irányul, s az N-terminusokhoz legközelebb eső -hélixet egy pozitív töltésű aminosavakból álló szekvencia követi (hasonlóan a III. típusú fehérjékhez). Ez azt eredményezi, hogy az első -hélix a növekvő polipetid lánc N-terminálisa az ER lumenbe kerül. A lánc növekedésével, a váltakozó szignál-horgony és stoptranszfer szekvenciák segítségével, a fehérje beépül a membránba. DIA 11 Egy foszfolipid horgony bizonyos sejtfelszíni proteineket kipányváz a membránban Néhány sejt-felszíni molekula nem hidrofób aminosavak által horgonyzódik a sejtmembránba, hanem kovalensen kötött amfipatikus molekulák által; ilyen pl. a glükozil-foszfatidil-inozitol (GPI). Ezek a fehérjék - hasonlóan az I. típusú fehérjékhez - az ER membránba épülnek be. A folyamatot az N-terminális szignál szekvencia és belső stop-transzfer horgony szekvencia irányítják. A transzamináz enzim (ER membránban helyezkedik el) azonban eltávolítja az eredeti stop-transzfer horgony szekvenciát (ezzel együtt a C- terminális szekvenciákat is) és a maradék fehérjét elszállítja egy GPI horgonyhoz. A citoszólba nyúló domén eltávolítása pl. azzal a következménnyel jár, hogy a GPI-hez kötött fehérjék könnyen mozoghatnak a membránban. Ezzel szemben sok olyan protein, amely transzmembrán -hélixekkel rögzül a membránban, immobilizálódik (mozgásképtelenné válik), mert a citoszólba nyúló C-terminális szekvenciák kölcsönhatásba lépnek a citoszkeletonnal. PROTEIN TRANSZPORT A MITOKONDRIUMBA A citoszól riboszómáin képződő fehérjék a mitokondriumba, a kloroplasztiszba és a peroxiszómákba transzportálódnak. A mitokondrium és a kloroplasztisz kettős membránnal határolt, míg a peroxiszómákat egyrétegű membrán veszi körül (csak a mitokondriumokat tárgyaljuk). Azok a fehérjék, melyeket a mitokondrium (és a kloroplasztisz) saját DNS-e kódol a sejtszervecskék riboszómáin képződnek, és közvetlenül a képződés után a megfelelő al-kompartmentekbe vándorolnak. A mitokondrium (és kloroplasztisz) fehérjéinek többsége azonban a sejtmagban kódolt, ezért azokat transzportálni kell a sejtszervecskékhez. Megjegyzés: a mitokondrium (és kloroplasztisz) DNS-e bakteriális eredetű. Az idők során a DNS szekvenciák zöme eliminálódott (eltűnt), egy jelentős része a magi DNS-be került (ennek mechanizmusát nem ismerjük), s csupán egy kis része maradt a sejtszervecskékben. Azok a prekurzor fehérjék, amelyek a mitokondrium mátrixába (ill. a kloroplasztisz sztrómájába) kerülnek specifikus mátrix targeting szekvenciákat tartalmaznak, amelyek a sejtszervecske felszínén elhelyezkedő receptorokhoz való kapcsolódásért felelősek. Ezek a szekvenciák
7 rendszerint levágódnak a mátrixba kerülést közben. A mitokondriumba és a kloroplasztiszba irányuló transzport energiaigényes, az energianyerés a külső és belső membrán érintkezésénél történik. A kettős membrán miatt, az ezekbe a sejtszervecskékbe történő transzport két targeting szekvenciát és két membránhoz kötött transzlokációs rendszert kíván: az egyik a szervecskéhez való transzporthoz, a másik pedig a sejtszervecske belsejébe, vagy annak membránjába való bejutáshoz szükséges. Amfipatikus N-terminális szignál szekvenciák irányítják a fehérjéket a mitokondriális mátrixba Az összes fehérje, amelyik a citoszólból a mitokondriumba szállítódik, a targeting szignáljukban szekvenciálisan hasonló motívumokkal rendelkezik. Ezek közül a legismertebbek a mátrix-targeting szekvenciák, aminosavat tartalmaznak, a fehérje N-terminálisán helyezkednek el, -helikális szerkezűek: a spirál egyik oldalán pozitív töltésű aminosavak, a másikon pedig hidrofób aminosavak dominálnak ezt nevezzük amfipatikus sajátságnak. DIA 12 (1) Transzport a mitokondrium mátrixba (mátrix proteinek szállítása) A mitokondriális protein importhoz szükségesek külső-membrán receptorok és transzlokonok mindkét membránban. A citoszólban való szintézist követően a fehérjék a mitokondrium felszínéhez kerülnek, s a prekurzor fehérjék közvetlenül kerülnek kapcsolatba a mitokondrium import receptorával (nincs SRP). A 3D-s konformációjú fehérjék membránon való áthaladása nem lehetséges, ezért nem teljesen kész fehérjék szállítódnak a mitokondriumba. (1) A chaperonok, mint pl. a citoszólikus Hsc70 a fehérjéket össze nem tekeredett (unfolded) vagy részlegesen összetekeredett állapotban tartják. (2) E fehérjék mitokondriális (mátrix) targeting szekvenciái a külső mitokondriális membrán import receptorához kapcsolódnak. Az N-terminális mátrix targeting szekvenciákat a Tom20 és Tom22 (translocon of the outer membrane; a külső membrán transzlokonja) import receptor fehérjék ismerik fel, amik, ezt követően (3) a prekurzor proteineket egy import csatornához szállítják. Ezt a csatorna a Tom40 protein. (4, 5) A mátrixba kerülő prekurzor fehérjék transzportja egyidejűleg történik a külső és a belső membránon egy belső membrán csatornán át, amely Tim23 és Tim17 proteinekből áll (translocon of the inner membrane; a belső membrán transzlokonja). A mátrixba történő transzlokáció a két membrán egymáshoz közeli, kontakt helyein történik. A transzfer folyamatot a mátrix Hsc70 chaperon segíti (a chaperont a Tim44-hez való kötődés hozza közel a transzlokonhoz), melyhez az energiát az ATP-ből szerzi. (6) A mátrix-targeting szekvenciát egy proteáz enzim levágja a mitkondriális mátrixban, s ezzel egyidejűleg a Hsc70 leválik a fehérjéről. (7) Néhány importált fehérje esetében spontán kialakul az aktív térszerkezet, sok mátrix fehérjének azonban chaperoninek segítenek ebben. 7 DIA 13 Többszörös szignálok és útvonalak irányítják a proteineket a szubmitokondriális kompartmentekbe Eltérően a mátrixba való transzporttól, fehérjék szállítása a mitokondrium külső- és belső membránjába, vagy a membránok közötti térbe, általában több targeting szekvencia és több útvonal részvételét követeli meg (ld. lentebb). A dia teljes anyaga csak illusztrációként szolgál, nem kell megtanulni. DIA 14 (2) Transzport a belső mitokondrium membránba (belső membrán proteinek szállítása) Három különböző útvonal irányítja a fehérjéket a belső mitokondrium membránba. (A) Az A útvonal ugyanazt a molekuláris mechanizmust használja, amely a mátrixba szállítja a proteineket (ld. DIA 12). Például, a citokróm oxidáz CoxVa alegysége szállítódik ezen az útvonalon. A prekurzor CoxVa N-terminális mátrix-targeting szekvenciáját a dimer szerkezetű Tom20/22 import receptor ismeri fel. Ezt követően a fehérje átjut a külső membrán általános import pórusán (Tom40) és a belső membrán Tim23/17 transzlokációs komplexén. A mátrix-targeting szekvencián (amely levágódik az import közben) kívül a CoxVa tartalmaz még egy hidrofób stop-transzfer szekvenciát is. A transzfer folyamatot a mátrix Hsc70 chaperon segíti (a chaperont a Tim44-hez való kötődés hozza közel a transzlokonhoz), melyhez az energiát az ATP-ből szerzi. Ahogy a fehérje áthalad a Tim23/17 csatornán, a stop-transzfer szekvencia blokkolja a C-terminus belső membránon keresztüli transzlokációját, majd ezt követően laterálisan (oldal irányban) szállítódik a lipid kettős rétegben. (B) A belső membránba történő szállítás B útvonalát az ATP szintetáz 9-es alegységének transzportja révén mutatjuk be. Ez a fehérje tartalmaz egy mátrix-targeting szekvenciát és egy belső hidrofób domént, melyet egy belső membrán protein, az Oxa1 ismer fel. Ez az útvonal magában foglalja a prekurzor protein egy részének a mátrixba való transzportját a Tom20/22 és Tim23/17 csatornák segítségével. A mátrix-targeting szekvencia levágását követően, a fehérje a belső membránba épül be egy olyan folyamat révén, amelyhez az Oxa1 protein szükséges. A Hsc70 chaperon ebben a folyamatban is részt vesz. (C) A C útvonal a 6 membrán domént tartalmazó fehérjék szállítását végzi. Ezek a fehérjék nem rendelkeznek N-terminális mátrix-targeting szekvenciával, de többszörös belső mitokondriális targeting szekvenciákat tartalmaznak. A belső szekvenciákat a Tom70 ismeri fel, majd ezután az importált fehérjék áthaladnak a külső membrán általános import pórusán. Ezt követően, a protein egy a belső membránban elhelyezkedő 2. transzlokációs komplexhez szállítódik (Tim22/54 komplex). Ezt a folyamatot két kis protein, a dimert alkotó Tim9 és Tim10 (intermembrán térben helyezkednek el) chaperonként segíti. A Tim22/54 komplex felelős a többszörös hidrofób szegmensek belső membránba való beépüléséért.
8 DIA 15 (3) Transzport a mitokondriális inter-membrán térbe (Inter-membrán-tér proteinek szállítása; inter-membrán = membránok közötti) Két útvonalon kerülhet egy citoszólikus fehérje a külső vagy a belső mitokondriális membrán közé. (A) A fő útvonalat a citokróm b2 fehérje transzportjával illusztráljuk. E fehérje prekurzora két különböző N-terminális targeting szekvenciát tartalmaz, melyek a folyamat végén levágódnak. Az N-terminálishoz közelebb eső szekvencia, egy mátrixtargeting szekvencia, melyet a mátrix proteázok vágnak le. A második targeting szekvencia egy hidrofób szegmens, amely blokkolja az import fehérje teljes transzlokációját a belső membránon keresztül. Ezt követően a membránba ágyazott fehérje laterálisan diffundál a Tim23/17 transzlokációs csatornától elfelé, közben egy proteáz levágja a hidrofób transzmembrán szegmenst, s így a maradék fehérje az intermembrán térbe kerül. (B) A citokróm c hem liáz (a hem citokróm c-hez való kovalens kötődésért felelős enzim) transzportján keresztül illusztráljuk ezt a mechanizmust. Ebben az útvonalban a protein közvetlenül szállítódik az intermembrán térbe, az általános import póruson (Tom40) keresztül, transzlokációs faktorok részvétele nélkül. Nincs DIA (4) Transzport a külső mitokondrium membránba (külső membrán proteinek szállítása) A mitokondriális porin (P70) szolgáltat példát erre a transzport folyamatra. A fehérjén egy rövid mátrix-targeting szekvencia (N-terminálison) követően egy hosszú hidrofób szekvencia található; az utóbbi hiányában a fehérje a mátrixban halmozódik fel. Ebből az következik, hogy a hidrofób szekvenciák stop-transzfer szekvenciákként funkcionálnak, melyek megakadályozzák a protein mátrixba való transzportját és kikötik azt a külső membránhoz. Normálisan, sem a mátrix-targeting-, sem a stop-transzfer szekvencia nem vágódik le a fehérjéről. 8
1b. Fehérje transzport
 1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
Kevéssé fejlett, sejthártya betüremkedésekből. Citoplazmában, cirkuláris DNS, hisztonok nincsenek
 1 A sejtek felépítése Szerkesztette: Vizkievicz András A sejt az élővilág legkisebb, önálló életre képes, minden életjelenséget mutató szerveződési egysége. Minden élőlény sejtes szerveződésű, amelyek
1 A sejtek felépítése Szerkesztette: Vizkievicz András A sejt az élővilág legkisebb, önálló életre képes, minden életjelenséget mutató szerveződési egysége. Minden élőlény sejtes szerveződésű, amelyek
7. A SEJT A SEJT 1. ÁLTALÁNOS TUDNIVALÓK
 A SEJT 1. ÁLTALÁNOS TUDNIVALÓK DIA 1 DIA 2 DIA 3 DIA 4 A sejtbiológia a biológiának az a tudományterülete, amely a sejt szerkezeti felépítésével, a különféle sejtfolyamatokkal (sejtlégzés, anyagtranszport,
A SEJT 1. ÁLTALÁNOS TUDNIVALÓK DIA 1 DIA 2 DIA 3 DIA 4 A sejtbiológia a biológiának az a tudományterülete, amely a sejt szerkezeti felépítésével, a különféle sejtfolyamatokkal (sejtlégzés, anyagtranszport,
Egy idegsejt működése
 2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
Riboszóma. Golgi. Molekuláris sejtbiológia
 Molekuláris sejtbiológia d-er Riboszóma Golgi Dr. habil KŐHIDAI László egyetemi docens Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. október 27. Endoplamatikus = sejten belüli; retikulum
Molekuláris sejtbiológia d-er Riboszóma Golgi Dr. habil KŐHIDAI László egyetemi docens Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. október 27. Endoplamatikus = sejten belüli; retikulum
Élettan. előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45
 Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
2011. október 11. Szabad János
 2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
2011. október 11 Szabad János szabad@mdbio.szote.u-szeged.hu Egy állatsejt szervez dése - Export a sejtmagból a citoplazmába - Import a citoplazmából a sejtmagba - Import a sejtszervecskékbe - A szekréciós
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
CzB 2010. Élettan: a sejt
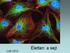 CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
9. előadás Sejtek közötti kommunikáció
 9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
Fehérjebiotechnológia Emri, Tamás Csősz, Éva Tőzsér, József Szerkesztette Tőzsér, József, Debreceni Egyetem
 Fehérjebiotechnológia Emri, Tamás Csősz, Éva Tőzsér, József Szerkesztette Tőzsér, József, Debreceni Egyetem Fehérjebiotechnológia írta Emri, Tamás, Csősz, Éva, Tőzsér, József, Tőzsér, József, és Szerzői
Fehérjebiotechnológia Emri, Tamás Csősz, Éva Tőzsér, József Szerkesztette Tőzsér, József, Debreceni Egyetem Fehérjebiotechnológia írta Emri, Tamás, Csősz, Éva, Tőzsér, József, Tőzsér, József, és Szerzői
OZMÓZIS, MEMBRÁNTRANSZPORT
 OZMÓZIS, MEMBRÁNTRANSZPORT Vig Andrea PTE ÁOK Biofizikai Intézet 2014.10.28. ÁTTEKINTÉS DIFFÚZIÓ BROWN-MOZGÁS a részecskék rendezetlen hőmozgása DIFFÚZIÓ a részecskék egyenletlen (inhomogén) eloszlásának
OZMÓZIS, MEMBRÁNTRANSZPORT Vig Andrea PTE ÁOK Biofizikai Intézet 2014.10.28. ÁTTEKINTÉS DIFFÚZIÓ BROWN-MOZGÁS a részecskék rendezetlen hőmozgása DIFFÚZIÓ a részecskék egyenletlen (inhomogén) eloszlásának
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A géntechnológia genetikai alapjai (I./3.)
 Az I./2. rész (Gének és funkciójuk) rövid összefoglalója A gének a DNS információt hordozó szakaszai, melyekben a 4 betű (ATCG) néhány ezerszer, vagy százezerszer ismétlődik. A gének önálló programcsomagként
Az I./2. rész (Gének és funkciójuk) rövid összefoglalója A gének a DNS információt hordozó szakaszai, melyekben a 4 betű (ATCG) néhány ezerszer, vagy százezerszer ismétlődik. A gének önálló programcsomagként
Az endomembránrendszer részei.
 Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
A replikáció mechanizmusa
 Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK A membránok minden sejtnek lényeges alkotórészei. Egyrészt magát a sejtet határolják - ez a sejtmembrán vagy
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK A membránok minden sejtnek lényeges alkotórészei. Egyrészt magát a sejtet határolják - ez a sejtmembrán vagy
6. Zárványtestek feldolgozása
 6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül.
 7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
Transzláció. Leolvasás - fehérjeszintézis
 Transzláció Leolvasás - fehérjeszintézis Fehérjeszintézis DNS mrns Transzkripció Transzláció Polipeptid A trns - aminosav kapcsolódás 1 A KEZDETEK ELŐTT Az enzim aktiválja az aminosavat azáltal, hogy egy
Transzláció Leolvasás - fehérjeszintézis Fehérjeszintézis DNS mrns Transzkripció Transzláció Polipeptid A trns - aminosav kapcsolódás 1 A KEZDETEK ELŐTT Az enzim aktiválja az aminosavat azáltal, hogy egy
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN. Somogyi János -- Vér Ágota Első rész
 A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont
 Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori értekezés Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori értekezés Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
1. SEJT-, ÉS SZÖVETTAN. I. A sejt
 1. SEJT-, ÉS SZÖVETTAN SZAKMAI INFORMÁCIÓTARTALOM I. A sejt A sejt cellula az élő szervezet alapvető szerkezeti és működési egysége, amely képes az önálló anyag cserefolyamatokra és a szaporodásra. Alapvetően
1. SEJT-, ÉS SZÖVETTAN SZAKMAI INFORMÁCIÓTARTALOM I. A sejt A sejt cellula az élő szervezet alapvető szerkezeti és működési egysége, amely képes az önálló anyag cserefolyamatokra és a szaporodásra. Alapvetően
1. Bevezetés. Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei
 1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
Vírusok I: általános
 1 Mi egy vírus? VÍRUSOK-I Vírusok I: általános I. Bevezetés A vírusok sejtparaziták, ami azt jelenti, hogy (1) a sejten kívül nem képesek élettevékenységet folytatni. (2) Továbbá, a vírusok a fertőzött
1 Mi egy vírus? VÍRUSOK-I Vírusok I: általános I. Bevezetés A vírusok sejtparaziták, ami azt jelenti, hogy (1) a sejten kívül nem képesek élettevékenységet folytatni. (2) Továbbá, a vírusok a fertőzött
ANATÓMIA FITNESS AKADÉMIA
 ANATÓMIA FITNESS AKADÉMIA sejt szövet szerv szervrendszer sejtek általános jellemzése: az élet legkisebb alaki és működési egysége minden élőlény sejtes felépítésű minden sejtre jellemző: határoló rendszer
ANATÓMIA FITNESS AKADÉMIA sejt szövet szerv szervrendszer sejtek általános jellemzése: az élet legkisebb alaki és működési egysége minden élőlény sejtes felépítésű minden sejtre jellemző: határoló rendszer
A kémiai energia átalakítása a sejtekben
 A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
Fehérje szintézis 2. TRANSZLÁCIÓ Molekuláris biológia kurzus 7. hét. Kun Lídia Genetikai, Sejt- és immunbiológiai Intézet
 Fehérje szintézis 2. TRANSZLÁCIÓ Molekuláris biológia kurzus 7. hét Kun Lídia Genetikai, Sejt- és immunbiológiai Intézet Gén mrns Fehérje Transzkripció Transzláció A transzkriptum : mrns Hogyan mutatható
Fehérje szintézis 2. TRANSZLÁCIÓ Molekuláris biológia kurzus 7. hét Kun Lídia Genetikai, Sejt- és immunbiológiai Intézet Gén mrns Fehérje Transzkripció Transzláció A transzkriptum : mrns Hogyan mutatható
A sejtes szervezıdés elemei (sejtalkotók / sejtorganellumok)
 A sejtes szervezıdés elemei (sejtalkotók / sejtorganellumok) 1 Sejtorganellumok vizsgálata: fénymikroszkóp elektronmikroszkóp pl. scanning EMS A szupramolekuláris struktúrák további szervezıdése sejtorganellumok
A sejtes szervezıdés elemei (sejtalkotók / sejtorganellumok) 1 Sejtorganellumok vizsgálata: fénymikroszkóp elektronmikroszkóp pl. scanning EMS A szupramolekuláris struktúrák további szervezıdése sejtorganellumok
BIOLÓGIA VERSENY 10. osztály 2016. február 20.
 BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK
 POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont
 Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Fehérjeglikoziláció az endoplazmás retikulumban mint lehetséges daganatellenes támadáspont Doktori tézisek Dr. Konta Laura Éva Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
A jel-molekulák útja változó hosszúságú lehet. A jelátvitel. hírvivő molekula (messenger) elektromos formában kódolt információ
 A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
A koleszterin-anyagcsere szabályozása (Csala Miklós)
 A koleszterin-anyagcsere szabályozása (Csala Miklós) A koleszterin fontos építőeleme az emberi sejteknek, fontos szerepe van a biológiai membránok fluiditásának szabályozásában. E mellett hormonok és epesavak
A koleszterin-anyagcsere szabályozása (Csala Miklós) A koleszterin fontos építőeleme az emberi sejteknek, fontos szerepe van a biológiai membránok fluiditásának szabályozásában. E mellett hormonok és epesavak
Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira
 Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira Doktori értekezés Magyar Éva Judit Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
Teaflavanolok hatása az endoplazmás retikulum fehérjeérési és minőségellenőrzési folyamataira Doktori értekezés Magyar Éva Judit Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
AZ ÖNEMÉSZTÉS, SEJTPUSZTULÁS ÉS MEGÚJULÁS MOLEKULÁRIS SEJTBIOLÓGIÁJA
 TÁMOP 4.1.2.B.2-13/1-2013-0007 ORSZÁGOS KOORDINÁCIÓVAL A PEDAGÓGUSKÉPZÉS MEGÚJÍTÁSÁÉRT MEGHÍVÓ AZ ÖNEMÉSZTÉS, SEJTPUSZTULÁS ÉS MEGÚJULÁS MOLEKULÁRIS SEJTBIOLÓGIÁJA 15 ÓRÁS INGYENES SZAKMAI TOVÁBBKÉPZÉS
TÁMOP 4.1.2.B.2-13/1-2013-0007 ORSZÁGOS KOORDINÁCIÓVAL A PEDAGÓGUSKÉPZÉS MEGÚJÍTÁSÁÉRT MEGHÍVÓ AZ ÖNEMÉSZTÉS, SEJTPUSZTULÁS ÉS MEGÚJULÁS MOLEKULÁRIS SEJTBIOLÓGIÁJA 15 ÓRÁS INGYENES SZAKMAI TOVÁBBKÉPZÉS
Glukuronidtranszport az endoplazmás retikulumban
 Glukuronidtranszport az endoplazmás retikulumban Doktori értekezés Dr. Révész Katalin Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető: Dr. Csala Miklós egyetemi docens, Ph.D. Hivatalos
Glukuronidtranszport az endoplazmás retikulumban Doktori értekezés Dr. Révész Katalin Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető: Dr. Csala Miklós egyetemi docens, Ph.D. Hivatalos
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
TRANSZPORTFOLYAMATOK A SEJTEKBEN
 16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
 A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
Diabéteszes redox változások hatása a stresszfehérjékre
 Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
Semmelweis Egyetem Molekuláris Orvostudományok Tudományági Doktori Iskola Pathobiokémia Program Doktori (Ph.D.) értekezés Diabéteszes redox változások hatása a stresszfehérjékre dr. Nardai Gábor Témavezeto:
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban
 A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
Eszközszükséglet: Szükséges anyagok: tojás, NaCl, ammónium-szulfát, réz-szulfát, ólom-acetát, ecetsav, sósav, nátrium-hidroxid, desztillált víz
 A kísérlet, megnevezés, célkitűzései: Fehérjék tulajdonságainak, szerkezetének vizsgálata. Környezeti változások hatásának megfigyelése a fehérjék felépítésében. Eszközszükséglet: Szükséges anyagok: tojás,
A kísérlet, megnevezés, célkitűzései: Fehérjék tulajdonságainak, szerkezetének vizsgálata. Környezeti változások hatásának megfigyelése a fehérjék felépítésében. Eszközszükséglet: Szükséges anyagok: tojás,
Belső elválasztású mirigyek
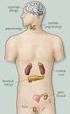 Belső elválasztású mirigyek Szekréciós szervek szövettana A különböző sejtszervecskék fejlettsége utal a szekretált anyag jellemzőire és a szekréciós aktivitás mértékére: Golgi komplex: jelenléte szekrétum
Belső elválasztású mirigyek Szekréciós szervek szövettana A különböző sejtszervecskék fejlettsége utal a szekretált anyag jellemzőire és a szekréciós aktivitás mértékére: Golgi komplex: jelenléte szekrétum
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
1. ábra: A hasnyálmirigy Langerhans-szigete
 génmanipulált mikroorganizmusokkal Az elsődleges és másodlagos anyagcseretermékek előállítása után a rekombináns fehérjék gyártásáról lesz szó. Ezek olyan fehérjék, melyeket a sejt eredeti genomja nem
génmanipulált mikroorganizmusokkal Az elsődleges és másodlagos anyagcseretermékek előállítása után a rekombináns fehérjék gyártásáról lesz szó. Ezek olyan fehérjék, melyeket a sejt eredeti genomja nem
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
A proteomika új tudománya és alkalmazása a rákdiagnosztikában
 BIOTECHNOLÓGIAI FEJLESZTÉSI POLITIKA, KUTATÁSI IRÁNYOK A proteomika új tudománya és alkalmazása a rákdiagnosztikában Tárgyszavak: proteom; proteomika; rák; diagnosztika; molekuláris gyógyászat; biomarker;
BIOTECHNOLÓGIAI FEJLESZTÉSI POLITIKA, KUTATÁSI IRÁNYOK A proteomika új tudománya és alkalmazása a rákdiagnosztikában Tárgyszavak: proteom; proteomika; rák; diagnosztika; molekuláris gyógyászat; biomarker;
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése
 Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
SEJTBIOLÓGIA biomérnök hallgatók számára
 SEJTBIOLÓGIA biomérnök hallgatók számára Hetedik rész: Intracelluláris kompartmentek: a fehérjék elosztása Novák Béla docens Proofreading: Sveiczer Ákos ösztöndíjas kutató 1994. november 30. Copyright
SEJTBIOLÓGIA biomérnök hallgatók számára Hetedik rész: Intracelluláris kompartmentek: a fehérjék elosztása Novák Béla docens Proofreading: Sveiczer Ákos ösztöndíjas kutató 1994. november 30. Copyright
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Génszerkezet és génfunkció
 Általános és Orvosi Genetika jegyzet 4. fejezetének bővítése a bakteriális genetikával 4. fejezet Génszerkezet és génfunkció 1/ Bakteriális genetika Nem szükséges külön hangsúlyoznunk a baktériumok és
Általános és Orvosi Genetika jegyzet 4. fejezetének bővítése a bakteriális genetikával 4. fejezet Génszerkezet és génfunkció 1/ Bakteriális genetika Nem szükséges külön hangsúlyoznunk a baktériumok és
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE
 Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
sejt működés jovo.notebook March 13, 2018
 1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
Az Agrármérnöki MSc szak tananyagfejlesztése. TÁMOP-4.1.2-08/1/A-2009-0010 projekt
 Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 projekt NÖVÉNYÉLETTAN c. TANTÁRGY JEGYZET Debreceni Egyetem Nyugat-magyarországi Egyetem Pannon Egyetem SZERZŐK: Ördög Vince Molnár
Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 projekt NÖVÉNYÉLETTAN c. TANTÁRGY JEGYZET Debreceni Egyetem Nyugat-magyarországi Egyetem Pannon Egyetem SZERZŐK: Ördög Vince Molnár
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
EMELT SZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2016. május 11. BIOLÓGIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 11. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA
ÉRETTSÉGI VIZSGA 2016. május 11. BIOLÓGIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 11. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA
Bioaktív peptidek technológiáinak fejlesztése
 Bioaktív peptidek technológiáinak fejlesztése BIOAKTÍV PEPTIDEK A kolosztrum kitűnő fehérjeforrás, melyben az esszenciális aminosavak és más organikus nitrogén-forrásként szolgáló vegyületek rendkívül
Bioaktív peptidek technológiáinak fejlesztése BIOAKTÍV PEPTIDEK A kolosztrum kitűnő fehérjeforrás, melyben az esszenciális aminosavak és más organikus nitrogén-forrásként szolgáló vegyületek rendkívül
A fehérjék térszerkezetének jóslása (Szilágyi András, MTA Enzimológiai Intézete)
 A fehérjék térszerkezetének jóslása (Szilágyi András, MTA Enzimológiai Intézete) A probléma bonyolultsága Általánosságban: találjuk meg egy tetszőleges szekvencia azon konformációját, amely a szabadentalpia
A fehérjék térszerkezetének jóslása (Szilágyi András, MTA Enzimológiai Intézete) A probléma bonyolultsága Általánosságban: találjuk meg egy tetszőleges szekvencia azon konformációját, amely a szabadentalpia
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék
 A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
Élettan-anatómia. 1. félév
 Élettan-anatómia 1. félév Dr. Világi Ildikó docens ELTE TTK Élettani és Neurobiológiai Tanszék tematika, előadások anyaga, fogalomjegyzék, esszé témakörök: http://physiology.elte.hu/elettan_pszicho.html
Élettan-anatómia 1. félév Dr. Világi Ildikó docens ELTE TTK Élettani és Neurobiológiai Tanszék tematika, előadások anyaga, fogalomjegyzék, esszé témakörök: http://physiology.elte.hu/elettan_pszicho.html
,:/ " \ OH OH OH - 6 - / \ O / H / H HO-CH, O, CH CH - OH ,\ / "CH - ~(H CH,-OH \OH. ,-\ ce/luló z 5zer.~ezere
 - 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
- 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
Az önemésztés, sejtpusztulás és megújulás molekuláris sejtbiológiája
 TÁMOP 4.1.2.B.2-13/1-2013-0007 ORSZÁGOS KOORDINÁCIÓVAL A PEDGÓGUSKÉPZÉS MEGÚJÍTÁSÁÉRT Az önemésztés, sejtpusztulás és megújulás molekuláris sejtbiológiája Szerzők: Kovács Attila Lajos, Lőw Péter, László
TÁMOP 4.1.2.B.2-13/1-2013-0007 ORSZÁGOS KOORDINÁCIÓVAL A PEDGÓGUSKÉPZÉS MEGÚJÍTÁSÁÉRT Az önemésztés, sejtpusztulás és megújulás molekuláris sejtbiológiája Szerzők: Kovács Attila Lajos, Lőw Péter, László
A sejtek lehetséges sorsa. A sejtek differenciálódása. Sejthalál. A differenciált sejtek tulajdonságai
 A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
TRANSZPORTEREK Szakács Gergely
 TRANSZPORTEREK Szakács Gergely Összefoglalás A biológiai membránokon keresztüli anyagáramlást számos membránfehérje szabályozza. E fehérjék változatos funkciója és megjelenésük mintázata biztosítja a sejtek
TRANSZPORTEREK Szakács Gergely Összefoglalás A biológiai membránokon keresztüli anyagáramlást számos membránfehérje szabályozza. E fehérjék változatos funkciója és megjelenésük mintázata biztosítja a sejtek
M E G O L D Ó L A P. Egészségügyi Minisztérium
 Egészségügyi Minisztérium Szolgálati titok! Titkos! Érvényességi idő: az írásbeli vizsga befejezésének időpontjáig A minősítő neve: Vízvári László A minősítő beosztása: főigazgató M E G O L D Ó L A P szakmai
Egészségügyi Minisztérium Szolgálati titok! Titkos! Érvényességi idő: az írásbeli vizsga befejezésének időpontjáig A minősítő neve: Vízvári László A minősítő beosztása: főigazgató M E G O L D Ó L A P szakmai
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
AZ EMBERI TEST FELÉPÍTÉSE
 AZ EMBERI TEST FELÉPÍTÉSE Szalai Annamária ESZSZK GYITO Általános megfontolások anatómia-élettan: az egészséges emberi szervezet felépítésével és működésével foglalkozik emberi test fő jellemzői: kétoldali
AZ EMBERI TEST FELÉPÍTÉSE Szalai Annamária ESZSZK GYITO Általános megfontolások anatómia-élettan: az egészséges emberi szervezet felépítésével és működésével foglalkozik emberi test fő jellemzői: kétoldali
Jellemzői: általában akaratunktól függően működik, gyors, nagy erőkifejtésre képes, fáradékony.
 Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
Izomszövetek Szerkesztette: Vizkievicz András A citoplazmára általában jellemző összehúzékonyság (kontraktilitás) az izomszövetekben különösen nagymértékben fejlődött ki. Ennek oka, hogy a citoplazma összehúzódásáért
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Biokémiai és Molekuláris Biológiai Intézet. Sejtbiológiai alapok. Sarang Zsolt
 Biokémiai és Molekuláris Biológiai Intézet Sejtbiológiai alapok Sarang Zsolt Víz (felnőtt emberi test 57-60%-a víz) Élő szervezetek inorganikus felépítő elemei Anionok (foszfát, klorid, karbonát ion, stb.)
Biokémiai és Molekuláris Biológiai Intézet Sejtbiológiai alapok Sarang Zsolt Víz (felnőtt emberi test 57-60%-a víz) Élő szervezetek inorganikus felépítő elemei Anionok (foszfát, klorid, karbonát ion, stb.)
Lipidek. Lipidek. Viaszok. Lipidek csoportosítása. Csak apoláros oldószerben oldódó anyagok.
 Lipidek sak apoláros oldószerben oldódó anyagok. Lipidek (ak és származékaik, valamint olyan vegyületek, amelyek bioszintézisükben vagy biológiai szerepükben összefüggenek velük + szteroidok, zsíroldható
Lipidek sak apoláros oldószerben oldódó anyagok. Lipidek (ak és származékaik, valamint olyan vegyületek, amelyek bioszintézisükben vagy biológiai szerepükben összefüggenek velük + szteroidok, zsíroldható
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Az idegsejtek kommunikációja. a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
A programozott sejthalál mint életfolyamat
 APOPTOSIS Réz Gábor A programozott sejthalál mint életfolyamat A sejteknek, legyenek bár prokarióták vagy eukarióták, öröklött képességük van arra, hogy belső vagy külső jelek hatására beindítsák a programozott
APOPTOSIS Réz Gábor A programozott sejthalál mint életfolyamat A sejteknek, legyenek bár prokarióták vagy eukarióták, öröklött képességük van arra, hogy belső vagy külső jelek hatására beindítsák a programozott
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Biológia 3. zh. A gyenge sav típusú molekulák mozgása a szervezetben. Gyengesav transzport. A glükuronsavval konjugált molekulákat a vese kiválasztja.
 Biológia 3. zh Az izomösszehúzódás szakaszai, molekuláris mechanizmusa, az izomösszehúzódás során milyen molekula deformálódik és hogyan? Minden izomrosthoz kapcsolódik kegy szinapszis, ez az úgynevezett
Biológia 3. zh Az izomösszehúzódás szakaszai, molekuláris mechanizmusa, az izomösszehúzódás során milyen molekula deformálódik és hogyan? Minden izomrosthoz kapcsolódik kegy szinapszis, ez az úgynevezett
3. Kombinált, amelynek van helikális és kubikális szakasza, pl. a bakteriofágok és egyes rákkeltő RNS vírusok.
 Vírusok Szerkesztette: Vizkievicz András A XIX. sz. végén Dmitrij Ivanovszkij orosz biológus a dohány mozaikosodásának kórokozóját próbálta kimutatni. A mozaikosodás a levél foltokban jelentkező sárgulása.
Vírusok Szerkesztette: Vizkievicz András A XIX. sz. végén Dmitrij Ivanovszkij orosz biológus a dohány mozaikosodásának kórokozóját próbálta kimutatni. A mozaikosodás a levél foltokban jelentkező sárgulása.
A plazmamembrán felépítése
 A plazmamembrán felépítése Folyékony mozaik membrán Singer-Nicholson (1972) Lipid kettősréteg Elektronmikroszkópia Membrán kettősréteg Intracelluláris Extracelluláris 1 Lipid kettősréteg foszfolipidek
A plazmamembrán felépítése Folyékony mozaik membrán Singer-Nicholson (1972) Lipid kettősréteg Elektronmikroszkópia Membrán kettősréteg Intracelluláris Extracelluláris 1 Lipid kettősréteg foszfolipidek
Transzgénikus növények előállítása
 Transzgénikus növények előállítása Növényi biotechnológia Területei: A növények szaporításának új módszerei Növényi sejt és szövettenyészetek alkalmazása Mikroszaporítás Vírusmentes szaporítóanyag előállítása
Transzgénikus növények előállítása Növényi biotechnológia Területei: A növények szaporításának új módszerei Növényi sejt és szövettenyészetek alkalmazása Mikroszaporítás Vírusmentes szaporítóanyag előállítása
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
Fehérjék rövid bevezetés
 Receptorfehérj rjék szerkezetének felderítése Homológia modellezés Fehérjék rövid bevezetés makromolekulák számos biológiai funkció hordozói: enzimatikus katalízis, molekula transzport, immunválaszok,
Receptorfehérj rjék szerkezetének felderítése Homológia modellezés Fehérjék rövid bevezetés makromolekulák számos biológiai funkció hordozói: enzimatikus katalízis, molekula transzport, immunválaszok,
Az örökítőanyag. Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase
 SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
