(11) Lajstromszám: E (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
|
|
|
- Ágnes Lukács
- 9 évvel ezelőtt
- Látták:
Átírás
1 !HU T2! (19) HU (11) Lajstromszám: E (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E (22) A bejelentés napja: (96) Az európai bejelentés bejelentési száma: EP (97) Az európai bejelentés közzétételi adatai: EP A (97) Az európai szabadalom megadásának meghirdetési adatai: EP B (1) Int. Cl.: C07D 1/12 (06.01) A61K 31/06 (06.01) A61P 2/16 (06.01) C07D 417/12 (06.01) (87) A nemzetközi közzétételi adatok: WO PCT/US 04/01717 () Elsõbbségi adatok: P US (72) Feltalálók: LIVERTON, Nigel, J., Rahway, NJ (US); CLAIBORNE, Christopher, F., Rahway, NJ (US); CLAREMON, David, A., Rahway, NJ (US); MCCAULEY, John, A., Rahway, NJ (US) (73) Jogosult: Merck & Co., Inc., Rahway, New Jersey (US) (74) Képviselõ: dr. Svingor Ádám, DANUBIA Szabadalmi és Jogi Iroda KFt., Budapest (4) N-szubsztituált nonaril-heterociklusos vegyületek, eljárás elõállításukra és alkalmazásuk (7) Kivonat HU T2 A találmány (I) képletû vegyületekre, azok gyógyászatilag elfogadható sóira, azok elõállítására és alkalmazására vonatkozik, ahol a képletben A leírás terjedelme 16 oldal HetAr jelentése 1 vagy 2 nitrogén gyûrûatomot tartalmazó, vagy 6 tagú heteroaromás gyûrû, tiazolil vagy tiadiazolil; R 1 és R 2 jelentése egymástól függetlenül H, C 1 4 alkil, fluor, klór, bróm vagy jód; A jelentése egy kötés vagy C 1 2 alkilén¹; és B jelentése aril-(ch 2 ) 0 3 O (O), indanil- (CH 2 ) 0 3 O C(O), aril-(ch 2 ) 1 3 C(O), aril-ciklopropil-c(o), aril-(ch 2 ) 1 3 NH C(O), ahol bármelyik aril adott esetben szubsztituálva van 1 szubsztituenssel, ahol a szubsztituensek jelentése egymástól függetlenül C 1 4 alkil, fluor vagy klór. Az európai szabadalom ellen, megadásának az Európai Szabadalmi Közlönyben való meghirdetésétõl számított kilenc hónapon belül, felszólalást lehet benyújtani az Európai Szabadalmi Hivatalnál. (Európai Szabadalmi Egyezmény 99. cikk (1)) A fordítást a szabadalmas az 199. évi XXXIII. törvény 84/H. -a szerint nyújtotta be. A fordítás tartalmi helyességét a Magyar Szabadalmi Hivatal nem vizsgálta.
2 1 HU T2 2 A találmány N¹szubsztituált nonaril-heterociklusos vegyületekre vonatkozik. Közelebbrõl a találmány olyan N¹szubsztituált nonaril-heterociklusos vegyületekre vonatkozik, amelyek NMDA NR2B-antagonisták, és felhasználhatók Parkinson-betegség és fájdalom kezelésére. Az NMDA NR2B-antagonisták ismertek a WO 02/689 számú nemzetközi közrebocsátási iratból. Az ionok, így a glutamát kulcsszerepet játszanak a krónikus fájdalomra és fájdalommal társuló neurotoxicitásra vonatkozó eljárásokban elsõdlegesen az N¹metil-D-aszpartát ( NMDA )-receptorokon keresztül hatva. Így az ilyen hatás gátlása ioncsatorna antagonistákat, különösen NMDA-antagonistákat használva kedvezõ lehet Parkinson-betegség és fájdalom kezelésében és szabályozásában. Az NMDA-receptorok alegységek heteromer társulásai, amelyek közül az NR1 és NR2 jelû két fõ alegységcsaládot klónozták. Az elmélethez való ragaszkodás nélkül általában azt hiszik, hogy az emlõsök központi idegrendszerében ( CNS ) csupán az NR1 és az NR2 alegységek kombinációja által képzõdnek különbözõ funkcionális NMDA-receptorok, amelyek glicin¹, illetve glutamátfelismerõ helyeket fejeznek ki. Az NR2 alegységcsalád viszont négy egyéni alegységtípusra oszlik: ezek az NR2A, az NR2B, az NR2C és az NR2D típusok. T. Ishii és munkatársai, [J. Biol. Chem., 268, (1993)] és D. J. Laurie és munkatársai [Mol. Brain. Res., 1, (1997)] leírják, hogy az így keletkezõ különbözõ kombinációk hogyan hoznak létre NMDA-receptor-változatokat, amelyek fiziológiai és farmakológiai tulajdonságokban különböznek, így iongátló tulajdonságokban, magnéziumérzékenységben, farmakológiai profilban, valamint anatómiai eloszlásban. Például míg az NR1 megtalálható az egész agyban, az NR2 alegységek differenciálisan vannak eloszolva. Nevezetesen úgy vélik, hogy az NR2B eloszlási térképe csökkenti a mellékhatások valószínûségét Parkinson-betegség vagy fájdalom kezelésekor. Így kívánatos lenne olyan új NMDA-antagonisták szolgáltatása, amelyek az NR2B receptorra hatnak. A találmány összefoglalása A jelen találmány az (I) képletû, N¹szubsztituált nonaril-heterociklusos vegyületekre, (I) vagy azok gyógyászatilag elfogadható sóira vonatkozik. A jelen találmány az említett vegyületeket tartalmazó gyógyászati kompozíciókat is szolgáltat. Ez a találmány továbbá módszereket ismertet bizonyos állapotok, így Parkinson-betegség, fájdalom, Alzheimer-kór és epilepszia kezelésére és megelõzésére, a jelen vegyületek és kompozíciók felhasználásával. A találmány részletes leírása A találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, (I) ahol HetAr 1 vagy 2 hidrogén gyûrûatomot tartalmazó, vagy 6 tagú heteroaromás gyûrût vagy tiazolilt vagy tiadiazolilt jelent; R 1 és R 2 jelentése egymástól függetlenül H, C 1 4 alkil, fluor, klór, bróm vagy jód; A jelentése egy kötés vagy C 1 2 alkilén¹; és B jelentése aril-(ch 2 ) 0 3 O C(O), indanil- (CH 2 ) 0 3 O C(O), aril-(ch 2 ) 1 3 C(O), aril-ciklopropil-c(o), aril-(ch 2 ) 1 3 )-NH C(O), ahol bármelyik arilcsoport adott esetben szubsztituálva lehet 1 szubsztituenssel, ahol mindegyik szubsztituens egymástól függetlenül C 1 4 alkil, fluor vagy klór lehet. Egy szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 1 vagy 2 nitrogén gyûrûatomot tartalmazó 6 tagú heteroaromás gyûrû. Ennek az elsõ szempontnak egy kiviteli alakja esetén a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 1 nitrogén gyûrûatomot tartalmazó, 6 tagú heteroaromás gyûrû. Ennek az elsõ szempontnak egy másik kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 2 nitrogén gyûrûatomot tartalmazó, 6 tagú heteroaromás gyûrû. Egy második szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése tiazolil vagy tiadiazolil. Ennek a második szempontnak egy kiviteli alakja esetén a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 1,2,4-tiadiazolil. Ennek a második szempontnak egy másik kiviteli alakja esetén a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése tiazolil. Egy harmadik szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol A jelentése egy kötés vagy C 1 2 alkilén¹. 2
3 1 HU T2 2 Ennek a harmadik szempontnak egy kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol A jelentése egy kötés. Ennek a harmadik szempontnak egy másik kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol A jelentése metilén. Ennek a harmadik szempontnak egy további kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol A jelentése C 2 alkilén¹. Egy negyedik szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-ciklopropil-c(o) vagy aril- (CH 2 ) 0 3 O C(O), ahol az aril adott esetben szubsztituálva van C 1 4 alkillal. Ennek a negyedik szempontnak egy kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-ciklopropil-c(o), ahol aril jelentése fenil, adott esetben C 1 4 alkillal szubsztituálva. Ennek a negyedik szempontnak egy további kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-(ch 2 ) 0 3 O C(O), ahol aril jelentése fenil, adott esetben C 1 4 alkillal szubsztituálva. Ennek a negyedik szempontnak egy még további kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-o C(O), ahol aril jelentése fenil, adott esetben C 1 4 alkillal szubsztituálva. Ennek a negyedik szempontnak egy még további kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-(ch 2 ) O C(O), ahol aril jelentése fenil, adott esetben C 1 4 alkillal szubsztituálva. Ennek a negyedik szempontnak egy még további kiviteli alakja szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol B jelentése aril-(ch 2 ) O C(O), ahol aril jelentése 4¹tolil. Egy ötödik szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 2 nitrogén gyûrûatomot tartalmazó, 6 tagú heteroaromás gyûrû; A jelentése metilén; és B jelentése aril-(ch 2 ) O C(O), ahol aril jelentése 4¹tolil. Egy hatodik szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 1,2,4-tiadiazolil; A jelentése metilén; és B jelentése aril-(ch 2 ) O C(O), ahol aril jelentése 4¹tolil Egy hetedik szempont szerint a találmány szerinti vegyületek vagy azok gyógyászatilag elfogadható sói (I) képletûek, ahol HetAr jelentése 2 nitrogén gyûrûatomot tartalmazó, 6 tagú heteroaromás gyûrû; A jelentése metilén; B jelentése aril-ciklopropil-c(o), ahol aril jelentése fenil, adott esetben C 1 4 alkillal szubsztituálva. Az itt használt alkil kifejezés, valamint minden olyan egyéb kifejezés, amely alk elõtaggal kezdõdik, amilyenek például az alkoxi, alkanoil, alkenil, alkinil és hasonlók, szénláncokat jelent, amely lehet egyenes vagy elágazó vagy azok kombinációja. Az alkilcsoportok példáiként megemlítjük a metil¹, etil¹, propil¹, izopropil¹, butil¹, szek- ésterc-butil¹, pentil¹, heptilcsoportokat és hasonlókat. Az aril kifejezés, ha külön nem említjük másként, adott esetben szubsztituált többszörös és egyszeres gyûrûrendszereket jelöl, így például fenil¹, naftil- és tolilcsoportot. A HetAr kifejezés például heteroaromás gyûrûket, így például pirimidint és piridint jelent. A (CH 2 ) 0 kifejezés azt jelenti, hogy a metilcsoport nincs jelen. Így a (CH 2 ) 0 3 kifejezés azt jelenti, hogy nullától háromig terjedõ számú metilcsoport van jelen, vagyis 3, 2 vagy 1 metilcsoport van jelen vagy egy sincs jelen. Amikor egy kötõ alkilcsoportban nincs jelen metilcsoport, a kötés egy közvetlen kötés. Az adott esetben szubsztituált kifejezéssel mind szubsztituált, mind szubsztituálatlan csoportokat szándékszunk jelölni. Így például az adott esetben szubsztituált aril jelenthet egy pentafluor-fenil- vagy egy fenilgyûrût. Továbbá a szubsztitúció a csoportok bármelyikén lehet. Például a szubsztituált aril-(c 1 6 ) alkil jelenthet szubsztitúciót az arilcsoporton, valamint szubsztitúciót az alkilcsoporton. Az itt leírt vegyületek egy vagy több aszimmetriacentrumot tartalmazhatnak, és így diasztereomerek és optikai izomerek jelenlétét jelenthetik. A jelen találmány felöleli az összes lehetséges diasztereomert, valamint azok racém elegyeit, azok lényegileg tiszta rezolvált enantiomerjeit, összes lehetséges geometriai izomerjeit, és azok gyógyászatilag elfogadható sóit. A fentebbi (I) képletet úgy mutatjuk, hogy azon nem tüntetünk fel egy meghatározott sztereokémiát bizonyos helyzetekben. A jelen találmány az (I) képlet összes sztereoizomerjét és azok gyógyászatilag elfogadható sóját is felöleli. Továbbá a találmány oltalmi köre kiterjed a sztereoizomerek elegyeire, valamint elkülönített sajátos sztereoizomerekre is. Az ilyen vegyületek elõállítására használt szintetikus eljárások során vagy a szakemberek számára ismert racemizálási vagy epimerizálási eljárások alkalmazásakor az ilyen eljárások termékei sztereoizomerek elegyei lehetnek. A gyógyászatilag elfogadható sók kifejezés gyógyászatilag elfogadható nem toxikus savakkal, ideértve szervetlen és szerves savakat, készített sókra vonatkozik. Az ilyen savak közül megemlítjük például az ecetsavat, a benzolszulfonsavat, a benzoesavat, a kámforszulfonsavat, a citromsavat, az etánszulfonsavat, a fu- 3
4 1 HU T2 2 mársavat, a glukonsavat, a glutaminsavat, a brómhidrogénsavat, a sósavat, az izetionsavat, a tejsavat, a maleinsavat, az almasavat, a mandulasavat, a metánszulfonsavat, a nyálkasavat, a salétromsavat, a pamoesavat, a pantoténsavat, a foszforsavat, a borostyánkõsavat, a kénsavat, a borkõsavat, a p¹toluolszulfonsavat és hasonlókat. Különösen elõnyös a citromsav, a hidrogén-bromid, a sósav, a maleinsav, a foszforsav, a kénsav és a borkõsav. A találmány szerinti gyógyászati készítmények hatóanyagként egy (I) képletû vegyületet (és/vagy annak gyógyászati sóját/sóit) tartalmazzák, továbbá egy gyógyászatilag elfogadható hordozót és adott esetben egyéb gyógyászati alkotóelemeket vagy adjuvánsokat. Ezek a kompozíciók orális, rektális, topikális és parenterális (ideértve a szubkután, intramuszkuláris és intravénás) adagolásra alkalmas komponenseket tartalmaznak, habár adott esetben a legalkalmasabb adagolási út a betegtõl, valamint állapotának jellegétõl és súlyosságától függ, amelyre a hatóanyagot adagoljuk. A gyógyászati kompozíciókat célszerûen egységdózis alakban adhatjuk és a gyógyszerészetben jól ismert módszerekkel állíthatjuk elõ. A gyakorlatban a találmány szerinti, (I) képletû vegyületeket vagy azok gyógyászatilag elfogadható sóit hatóanyagként bensõ keverékben egyesíthetjük egy gyógyászati hordozóval a szokásos gyógyászati technikákkal. A hordozó sokféle formájú lehet az adagoláshoz megkívánt elõállítási formában, például orális vagy parenterális (ideértve az intravénás alakot is) formában. Így a találmány szerinti gyógyászati kompozíciókat adagolhatjuk orális adagolásra alkalmas különálló egységekként, így kapszulákként, pasztillákként vagy tablettánként, amelyek mindegyike a hatóanyag elõre meghatározott mennyiségét tartalmazza. Továbbá a kompozíciók adagolhatók porként, szemcsékként, oldatként, vizes folyadékban szuszpenzióként, nemvizes folyadékként, olaj a vízben emulzióként vagy víz az olajban folyékony emulzióként. A fentebb ismertetett szokásos adagolási formák mellett az (I) képletû vegyület és/vagy annak gyógyászatilag elfogadható sója/sói adagolhatók szabályzott felszabadulást biztosító eszközökként és/vagy átadó készülékekként. A kompozíciókat a gyógyszerészet bármelyik módszerével elõ lehet állítani. Általában az ilyen módszerek abból állnak, hogy egy lépésben a hatóanyagot összehozzuk a hordozóval, amely egy vagy több szükséges komponenst képez. Általában a kompozíciókat úgy állítjuk elõ, hogy a hatóanyagot egyenletesen és bensõségesen elegyítjük a folyékony hordozókkal vagy finoman elosztott szilárd hordozókkal vagy mindkettõvel. A terméket azután megfelelõen formázhatjuk a kívánt alakra. Így a találmány szerinti gyógyszer-kompozíciók tartalmazhatnak egy gyógyászatilag elfogadható hordozót és egy (I) képletû vegyületet vagy gyógyászatilag elfogadható sót. Az (I) képletû vegyületek vagy azok gyógyászatilag elfogadható sói a gyógyszer-kompozíciókban egy vagy több egyéb, gyógyászatilag hatékony vegyülettel kombinálva is elõfordulhatnak A felhasznált gyógyászati hordozó lehet például szilárd, folyadék vagy gáz. A szilárd hordozók példáiként megemlítjük a laktózt, a fehérföldet, a szacharózt, a talkumot, a zselatint, az agart, a pektint, az akáciát, a magnézium-sztearátot és a sztearinsavat. A folyékony hordozók példáiként megemlítjük a cukorszirupot, a mogyoróolajat, az olívaolajat és a vizet. A gáz alakú hordozók példáiként megemlítjük a szén-dioxidot és a nitrogént. Az orális adagolási formájú kompozíciók elõállításához felhasználhatunk bármilyen megfelelõ gyógyszerészeti közeget. Például vizet, glikolokat, olajokat, alkoholokat, ízesítõanyagokat, tartósítószereket, színezõanyagokat és hasonlókat felhasználhatunk orális folyékony készítmények, így szuszpenziók, elixírek és oldatok elõállításához; míg hordozókat, így keményítõket, cukrokat, mikrokristályos cellulózt, hígítószereket, szemcsézõszereket, csúsztatóanyagokat, kötõanyagokat, szétesést elõsegítõ anyagokat és hasonlókat használhatunk fel orális szilárd készítmények, így porok, kapszulák és tabletták elõállításához. Könnyû adagolhatásuk miatt a tabletták és a kapszulák az elõnyös orális adagolási egységek, amelyeknél szilárd gyógyszerészeti hordozókat alkalmazunk. A tablettákat adott esetben bevonhatjuk szokásos vizes vagy nemvizes eljárásokkal. A találmány szerinti kompozíciót tartalmazó tablettákat sajtolással vagy ömlesztéssel lehet elõállítani, adott esetben egy vagy több kiegészítõ alkatrésszel vagy adjuvánssal. A sajtolt tablettákat sajtolással állíthatjuk elõ megfelelõ gépben, ahol a hatóanyag szabadon folyó alakban, így porként vagy szemcsékként van jelen, adott esetben egy kötõanyaggal, csúsztatóanyaggal, egy közömbös hígítószerrel, felületaktív anyaggal vagy diszpergálószerrel elegyítve. A formázott tablettákat megfelelõ gépben lehet elõállítani ömlesztéssel, ahol a porított vegyületet egy semleges folyékony hígítószerrel nedvesítjük. Minden egyes tabletta elõnyösen körülbelül 0, mg¹tól körülbelül g¹ig terjedõ mennyiségû hatóanyagot tartalmaz, és mindegyik kapszula elõnyösen körülbelül 0, mg¹tól körülbelül g¹ig terjedõ mennyiségû hatóanyagot tartalmaz. A találmány szerinti kompozíciók hatóanyagként (I) képletû vegyületet (vagy annak gyógyászatilag elfogadható sóit), egy gyógyszerészetileg elfogadható hordozót és adott esetben egy vagy több további gyógyászati hatóanyagot vagy adjuvánst tartalmaznak. Ezek a kompozíciók orális, rektális, topikális és parenterális (ideértve a szubkután, intramuszkuláris és intravénás) adagolásra alkalmas kompozíciókat tartalmaznak, habár egy adott esetben a legmegfelelõbb adagolási út függeni fog a betegtõl, valamint azoknak az állapotoknak a természetétõl és súlyosságától, amelyekre a hatóanyagot adagoljuk. A gyógyászati kompozíciókat elõnyösen adagolhatjuk egységdózis alakban, és a gyógyszerészetben jól ismert bármelyik módszerrel állíthatjuk elõ õket. A jelen találmány szerinti, parenterális adagolásra alkalmas gyógyászati kompozíciókat a hatóanyag vízben készített oldataiként vagy szuszpenzióiként állíthat- 4
5 1 HU T juk elõ. Megfelelõ felületaktív anyagot is beiktathatunk, így például hidroxi-propil-cellulózt. Diszperziókat is elõállíthatunk glicerinben, folyékony polietilénglikolokban és azok olajokban készített elegyeiben. Továbbá tartósítóanyagot is beiktathatunk annak érdekében, hogy meggátoljuk mikroorganizmusok káros növekedését. A befecskendezésre alkalmas, találmány szerinti gyógyászati kompozíciók steril vizes oldatokat vagy diszperziókat tartalmaznak. A kompozíciók készülhetnek továbbá az ilyen steril injektálható oldatok vagy diszperziók azonnali felhasználásához steril porok alakjában. Mindegyik esetben a végsõ injektálható alaknak sterilnek kell lennie, és kellõen folyékonynak is kell lennie ahhoz, hogy könnyen felszívható legyen a fecskendõbe. A gyógyászati kompozícióknak stabilnak kell lenniük a gyártás és a tárolás körülményei között. Így elõnyösen meg kell õket védeni mikroorganizmusok, így baktériumok és gombák szennyezõ hatásával szemben. A hordozóanyag oldószer vagy diszpergáló közeg lehet, amely például vizet, etanolt, poliolt (például glicerint, propilénglikolt és folyékony polietilénglikolt), növényi olajokat és azok megfelelõ elegyeit tartalmazza. A találmány szerinti gyógyászati kompozíciók topikális felhasználásra alkalmas alakban lehetnek, így például aeroszolok, krémek, kenõcsök, testápolók, porozószerek vagy hasonlók. A kompozíciók továbbá lehetnek transzdermális készülékekben való felhasználásra alkalmas alakban. Ezek a készítmények a szokásos módszerekkel állíthatók elõ, ahol a találmány szerinti, (I) képletû vegyületet vagy annak gyógyászatilag elfogadható sóit használjuk fel. Példaként említjük, hogy egy krémet vagy kenõcsöt úgy állítunk elõ, hogy egy hidrofil anyagot és vizet elegyítünk a vegyület körülbelül súly%-tól körülbelül súly%¹ig terjedõ mennyiségével, a kívánt konzisztenciájú krém vagy kenõcs elõállítása céljából. A találmány szerinti gyógyászati kompozíciók rektális adagolásra alkalmas alakban is lehetnek, ahol a hordozó egy szilárd anyag. Elõnyös, ha az elegy egységdózisú kúpokat képez. Megfelelõ hordozók a kakaóvaj és a szakmában általánosan alkalmazott egyéb anyagok. A kúpokat célszerûen úgy alakítjuk ki, hogy elõször a kompozíciót meglágyított vagy megömlesztett hordozóval/hordozókkal elegyítjük, majd öntõformákban lehûtjük és alakra visszük. A fentebb említett hordozóanyagok mellett a fentebb leírt gyógyászati készítmények tartalmazhatnak célszerûen egy vagy több további hordozókomponenst, így hígítószereket, puffereket, ízesítõanyagokat, kötõanyagokat, felületaktív anyagokat, sûrítõanyagokat, kenõanyagokat, tartósítószereket (ideértve az antioxidánsokat) és hasonlókat. Továbbá egyéb adjuvánsokat is beiktathatunk annak érdekében, hogy a készítményt izotóniássá tegyük a megcélzott befogadó vérével. Az (I) képletû vegyületet és/vagy annak gyógyászatilag elfogadható sóit tartalmazó kompozíciókat elõállíthatjuk por vagy folyékony koncentrátum alakjában is. Vizsgálati eljárások Sejtalapú funkcionális próba NR2B-antagonisták IC 0 -értékének meghatározására Kiválasztott vegyületek NR1a/NR2B NMDA receptor-gátló képességét NR1a/NR2B receptor által közvetített Ca 2+ -beáramlással mérve a következõ kalciumáramlásos próba eljárással határoztuk meg: Transzfektált NR1a/NR2B receptor L(tk¹) sejteket 3 4 sejt per lyuk koncentrációban felvittünk egy 96 lyukú lemezre, és két napon át tenyésztettük õket normál növekedési közegben (Dulbecco-féle MEM nátrium-piruváttal, 0 mg glukóz, pen/strep, glutamin, % FCS és 0, mg/ml geneticin). Ezekben a sejtekben az NR1a/NR2B expressziót azzal idéztük elõ, hogy 4 nm dexametazont adtunk hozzájuk órán át 00 M ketamin jelenlétében. NR2B-antagonista-oldatokat DMSO-ban készítettünk és sorozatban hígítottunk DMSO-val, és így tíz háromszoros koncentrációkülönbségû oldatot kaptunk. Egy 96 lyukú gyógyszerlemezt úgy állítottunk elõ, hogy a DMSO-oldatot -szeresre hígítottuk próbapufferbe [Hanks Balanced Salt Solution (HBSS) Mg 2+ -mentes (Gibco # , amely oldat mm HEPES¹t, 2 mm CaCl 2 ¹t, 1% BSA¹t és M Probenecid¹et (Sigma # P¹8761) tartalmaz]. Indukció után a sejteket kétszer mostuk (Labsystem sejtmosó, háromszoros hígítás, 0 L¹t hagyva) próbapufferrel, és 4 M fluo3 AM (Molecules Probes # P¹1241) kalciumfluoreszcens indikátorral töltöttük fel Pluronic F¹127¹et (Molecular Probes # P¹00) és M ketamint tartalmazó próbapufferben 37 C¹on egy órán át. A sejteket ezután nyolcszor mostuk próbapufferrel, minden egyes lyukban 0 L puffert hagyva. A fluoreszcenciaintenzitást közvetlenül mértük egy FLIPRben (Fluorometric Imaging Plate Reader, Molecular Devices), 488 nm¹es gerjesztést és nm¹en emissziót használva. A fluoreszcenciaintenzitás feljegyzésének megkezdése után másodperccel 0 L agonistaoldatot ( M glutamát/glicin, a végsõ koncentráció M) adtunk hozzá, és egy perc után, amikor a fluoreszcenciajel stabil volt, 0 L NR2B-antagonistát és a gyógyszerlemezrõl kontrolloldatokat adtunk hozzá, majd a fluoreszcenciaintenzitást további percen át feljegyeztük. Az IC 0 -értékeket úgy határoztuk meg, hogy a végpontfluoreszcencia-értékeket nem lineáris legkisebb négyezetek módszerével illesztettük az alábbi #1 egyenlet értékeihez. #1 egyenlet: (Ymax. Ymin.) Végpont-fluoreszcencia= 1+([gyógyszer]/IC 0 ) nh +Ymin. ahol Ymin. az 1 M AMD-2¹t tartalmazó kontroll-lyukak átlagos végpont-fluoreszcenciája és Ymax. a 0,1% DMSO¹t próbapufferben tartalmazó lyukak átlagos végpont-fluoreszcenciája.
6 1 HU T2 2 Kötési próba a K I NR2B-antagonisták meghatározására A radioligandumos kötési próbát szobahõmérsékleten 90 lyukú mikrotiterlemezeken végeztük 1,0 ml végsõ próbatérfogattal mm NaCl¹t tartalmazó mm Hepes-pufferben (ph=7,4). NR2B-antagonista-oldatokat DMSO-ban készítettünk és sorozatban hígítottunk DMSO-val, ilyen módon háromszoros koncentrációkülönbséget mutató oldatot kaptunk, ahol mindegyik oldat térfogata L volt. A nem specifikus kötést (NSB) úgy határoztuk meg, hogy AMD-1¹et használtunk ( M végkoncentrációval), és a teljes kötést (TB) DMSO (2%¹os végkoncentráció) hozzáadásával mértük. A mikrotiterlemez minden egyes lyukához NR1a/NR2B receptorokat expresszáló membránokat 1 ( pm végkoncentráció) és tríciumozott AMD-2¹t (1 nm végkoncentráció) adtunk. Szobahõmérsékleten 3 órán át végzett inkubálás után a mintákat Packard GF/B szûrõkön átszûrtük (amelyeket elõzetesen 0,0%¹os PEI-ben, polietileninin Sigma P¹3143) és tízszer mostuk 1 ml hideg mm Hepes-pufferral mosásonként. A szûrõlemezek vákuumszárítása után L Packard Microscint-¹at adtunk hozzá, és a kötött radioaktivitást Packard TopCount készülékben meghatároztuk. A látszólagos disszociációs állandót (K I ),amaximális százalékos gátlást (%I max. ), a minimális százalékos gátlást (%I min. ) és az iránytangenst (nh) úgy határoztuk meg, hogy a megkötött radioaktivitást (megkötött CPM) nem lineáris legkisebb négyzetes módszerrel hozzáigazítottuk az alábbi # 2 egyenlethez. # 2 egyenlet: (SB)(%I max. -%I min. )/0 Megkötött CPM= +NSB+(SB)(0 %I max. )/0 (1+([gyógyszer]/(K I (1+[AMD¹2]/K D )) nh ) ahol K D a receptor radioligandumának látszólagos disszociációs állandója forró telítési kísérlettel meghatározva, és SB a specifikus megkötött radioaktivitás a TB és NSB kontroll-lyukak különbségébõl meghatározva. AMD-1 2 AMD-2 Az AMD-1¹et a C. F. Claiborne et al. által leírt általános eljárás szerint lehet szintetizálni [Bioorganic & Medchem Letters 13, (03)]. A radiojelzett AMD¹1 szintézisének 3¹as prekurzorát a következõ eljárás szerint lehet szintetizálni: 1a) reakcióvázlat 4 1 Az 1a) reakcióvázlat szerint szobahõmérsékleten hidrogén-kloridot buborékoltatunk át az 1 cinnamonitril metanolos oldatán. Az illékony anyagokat csökkentett nyomás alatt eltávolítjuk, és a kapott maradékot éterrel kezeljük, majd leszûrjük; így a 2 imidált közbensõ terméket kapjuk. A 2 imidátot környezõ hõmérsékleten feloldjuk metanolban, környezõ hõmérsékleten a aminnal (kereskedelmileg kapható az Acros Chemicalstõl) kezeljük, és argonatmoszférában keverjük. Az illékony anyagokat csökkentett nyomáson eltávolítjuk, és a maradékot preparatív nagynyomású folyadékkromatográfiával vagy éterrel végzett kezeléssel tisztítjuk; így a 3 amidint kapjuk. 3 Tríciumozott AMD¹2 szintézise 2. reakcióvázlat 3 tríciumozott AMD-2 6
7 1 HU T2 2 A tríciumozott AMD-2¹t a 2. reakcióvázlaton szemléltetett alábbi eljárással állítottuk elõ: a 3 prekurzort (2 mg, 0,008 mmol) egy órán át oldottuk 1,2 mg káliumkarbonátot tartalmazó 0,6 ml dimetil-formamidban. Ezután nagy aktivitású tríciumozott metil-jodidot (0 mci, 0,0006 mmol, 1 ml toluolban; kereskedelmileg kapható az American Radiolabeled Chemicalstõl) adtunk hozzá szobahõmérsékleten, majd 2 órán át kevertük. A reakcióelegyet leszûrtük Whatman PTFE 0,4 m¹os, fecskendõmentes szûrõkészüléken, hogy eltávolítsuk az oldhatatlan kálium-karbonátot, abszolút etanollal (2 ml, kereskedelmileg kapható a Pharmcotól) mostuk, és az egyesített szûrleteket szobahõmérsékleten forgóbepárlón szárazra pároltuk; ezzel eltávolítottuk a reagálatlan tríciumozott metil-jodidot is. A maradékot nagynyomású kromatográfiával tisztítottuk egy Phenomenx Luna C8 félpreparatív oszlopon [Luna micro C8(2),,0 mm], percen át az alábbi gradiensrendszert használva: /80 acetonitril/víz 0,1% trifluor-ecetsavval 0% acetonitrilhez 0,1% trifluor-ecetsavval. A termék teljes aktivitása 8 mci volt. További tisztítást végeztünk egy Waters C¹18 Sep-Pak oszlopon (Waters Sep-Pak PLUS C18) végzett abszorpcióval és vízzel, majd abszolút etanollal végzett eluálással. A terméket abszolút etanollal ( ml) hígítottuk a végsõ elemzés elõtt. Jelzetlen AMD¹2 szintézise 1b) reakcióvázlat Az 1b) reakcióvázlat szerint hidrogén-kloridot buborékoltatunk át az 1 cinnamonitril metanolos oldatán szobahõmérsékleten. Az illékony anyagokat csökkentett nyomáson eltávolítjuk, és a kapott maradékot éterrel kezeljük, majd leszûrjük; így a 2 közbensõ imidátot kapjuk. A 2 imidátot környezõ hõmérsékleten feloldjuk metanolban, környezõ hõmérsékleten a 6 aminnal kezeljük, és argonatmoszférában keverjük. Az illékony anyagokat csökkentett nyomáson eltávolítjuk, és a maradékot preparatív nagynyomású folyadékkromatografálással vagy éterrel végzett kezeléssel tisztítjuk; így az amidint kapjuk. A találmány szerinti vegyületek a funkcionális, illetve kötési próbákban 0 M-nál kisebb IC 0 ¹, illetve K I - értékeket mutatnak. Elõnyös, ha az IC 0 ¹ésaK I -értékek a funkcionális, illetve a kötési próbában kisebbek M-nál. Elõnyösebb, ha az IC 0 ¹, illetve a K I -értékek a funkcionális, illetve a kötési próbában kisebbek 1 Mnál. Még elõnyösebb, ha az IC 0 ¹, illetve a K I -értékek a funkcionális, illetve a kötési próbában kisebbek 0,1 Mnál. A jelen vegyületek NMDA NR2B receptor antagonisták, és mint ilyenek hasznosak az NR2B receptor által elõidézett betegségek és rendellenességek kezelésében és megelõzésében. Az ilyen betegségek és rendellenességek közül korlátozási szándék nélkül megemlítjük a Parkinson-betegséget, a neuropátiás fájdalmat, így a posztherpetikus neuroalgiát, az idegsérülést, a diniákat, például a vulvodiniát, a lábcsonkok fantomfájdalmát, a foggyökér-avulziókat, a fájdalmas diabetikus neuropátiát, a fájdalmas traumás mononeuropátiát, a fájdalmas polineuropátiát, a központi fájdalomszindrómákat (amelyeket potenciálisan a központi idegrendszer bármelyik szintjének sérülése okozhat) és a sebészi beavatkozás utáni fájdalomszindrómákat (például a mell eltávolítása utáni szindrómát, a mûtét utáni mellkasszindrómát, a csonkfájdalmat), a csont- és kapcsolt fájdalmat (osteoartritisz), az ismétlõdõ mozgás által okozott fájdalmat, a fogfájdalmat, a rák által okozott fájdalmat, az izomhüvelyfájdalmat (izomsérülés, fibromialgia), a mûtét által okozott fájdalmat (általános sebészet, nõgyógyászat), a krónikus fájdalmat, a fájdalmas menstruációt, valamint az angina által okozott fájdalmat és a különbözõ eredetû gyulladásos fájdalmakat (például az oszteoartritiszt, a reumaszerû ízületi gyulladást, a reumás megbetegedéseket, a teno-szinovitiszt és a köszvényt), a fejfájást, a migrént és a csomós fejfájást, a depressziót, a szorongást, a skizofréniát, a szélütést, a traumás agykárosodást, az Alzheimer-kórt, az agyi ischaemiát, az amiotrófiás laterális sclerosist, a Huntington-betegséget, a szenzorineurális hallásvesztést, a fülcsengést, a zöld hályogot, az epilepsziás rohamok vagy neurotoxiás mérgezés vagy az agy glükóz- és/vagy oxigénszintjének károsodása által okozott idegkárosodást, a látási utak neurodegenerációja által okozott látásvesztés, a nyugtalanláb-szindrómát, a multiszisztémás sorvadást, a nem vaszkuláris fejfájást, az elsõdleges hiperalgéziát, a másodlagos hiperalgéziát, az elsõdleges allodiniát, a másodlagos allodiniát vagy egyéb fájdalmakat, amelyeket a központi idegrendszer érzékenyítése okoz. Az (I) képletû vegyületeket fel lehet használni diszkinéziák, különösen az L¹Dopa szokásos dózisait kísérõ mellékhatások megelõzésére. Továbbá az (I) képletû vegyületek felhasználhatók a fájdalom opioid kezelésétõl való függés csökkentésére és a megvonási tünetek, például az alkohol, opioidok és kokain megvonási tüneteinek a kezelésére. Úgy gondoljuk, hogy a találmány szerinti vegyületek profilaktikusan hatékony dózisszinteken adagolhatók a fentebb felsorolt állapotok megelõzésére, valamint az NMDA NR2B receptor által okozott állapotok megelõzésére. 7
8 1 HU T2 2 Az (I) képletû vegyületeket fel lehet használni egyéb olyan gyógyszerekkel való kombinációban, amelyeket olyan betegségek vagy állapotok kezelésére /megelõzésére/elnyomására vagy javítására használnak, amelyekre nézve hasznosak az (I) képletû vegyületek. Az ilyen egyéb gyógyszereket a szokásos úton és mennyiségben lehet adagolni egy (I) képletû vegyülettel egyidejûleg vagy egymást követõen. Amikor egy (I) képletû vegyületet egy vagy több más gyógyszerrel egyidejûleg használunk, elõnyös az olyan gyógyászati kompozíció, amely az ilyen egyéb gyógyszereket az (I) képletû vegyülettel együtt tartalmazza. Ennek megfelelõen a jelen találmány szerinti gyógyászati kompozíciók az (I) képletû vegyület mellett egy vagy több egyéb hatóanyagot is tartalmaznak. Az olyan hatóanyag példáiként, amelyeket kombinálni lehet egy (I) képletû vegyülettel, külön adagolva vagy ugyanabban a gyógyászati kompozícióban, az alábbiakat soroljuk fel anélkül, hogy a találmány oltalmi körét ezekre korlátoznánk: (1) nem szteroid gyulladásgátló anyagok; (2) COX¹2 inhibitorok; (3) bradikinin B1 receptor antagonisták; (4) nátriumcsatorna-blokkolók és antagonisták; () nitrogén-oxid-szintáz (NOS) inhibitorok; (6) helyi glicinantagonisták; (7) káliumcsatorna-nyitók; (8) AMPA/kainát receptor antagonisták; (9) kalciumcsatorna-antagonisták; () GABA A receptor modulátorok (például egy GABA A receptor agonista); (11) mátrixmetalloproteáz (MMP) inhibitorok; (12) vérrögoldó anyagok; (13) opioidok, mint a morfin; (14) neutrofil gátló faktor (NIF); (1) L¹Dopa; (16) karbidopa; (17) levodopa/karbidopa; (18) dopaminagonisták, mint a bromokriptin, a pergolid, a pramipexol, a ropinirol; (19) antikolinergikumok; () amantadin; (21) karbidopa; (22) katechol-o-metil-transzferáz ( COMT ) inhibitorok, mint az entakapon és a tolkapon; (23) monoamin-oxidáz B ( MAO¹B ) inhibitorok; (24) opiátagonisták vagy antagonisták; (2) HT receptor agonisták vagy antagonisták; (26) NMDA receptor agonisták vagy antagonisták; (27) NK1 antagonisták; (28) szelektív szerotoninújrafelvétel-inhibitorok ( SSRI ) és/vagy szelektív szerotonin- és norepinefrinújrafelvétel-inhibitorok ( SSNR1 ); (29) triciklusos antidepresszáns gyógyszerek; () norepinefrinmodulátorok; (31) lítium; (32) valproát; és (33) neurontin (gabapentin). A találmány szerinti vegyületeket tartalmazó krémek, kenõcsök, zselék, oldatok vagy szuszpenziók alkalmazhatók topikális felhasználásra. Szájöblítõk és toroköblítõk is a találmány szerinti célokra történõ topikális felhasználás területére tartoznak. A humán célra történõ orális adagolásra szánt készítmény célszerûen körülbelül 0, mg¹tól körülbelül mg¹ig terjedõ mennyiségû hatóanyagot tartalmazhat megfelelõ és alkalmas mennyiségû hordozóanyaggal társítva, amely a teljes kompozíció körülbelül %¹tól körülbelül 9%¹ig terjedõ mennyiségét képezheti. Az egységdózis alakok általában körülbelül 1 mg¹tól körülbelül 00 mg¹ig terjedõ mennyiségû hatóanyagot tartalmazhatnak. Az itt említett állapotokat kezelni vagy megelõzni lehet körülbelül 0,01 mg¹tól körülbelül 1 mg¹ig terjedõ mennyiségû találmány szerinti vegyület napi adagolásával egy kg testsúlyra vonatkoztatva. Megemlítjük azonban, hogy egy különleges páciens sajátos dózisszintje számos tényezõtõl függ. Az ilyen tényezõk közül megemlítjük a páciens korát, testsúlyát, általános egészségi állapotát, nemét és diétáját. Egyéb tényezõk közül megemlítjük az adagolás idejét és útját, a kiválasztás mértékét, a gyógyszer-kombinációt és a kezelendõ sajátos betegség típusát és súlyosságát. Például a gyulladásos fájdalom hatásosan kezelhetõ körülbelül 0,01 mg¹tól körülbelül 7 mg¹ig terjedõ mennyiségû jelen vegyülettel naponta testsúly-kilogrammonként, vagy másként körülbelül 0, mg¹tól körülbelül 3, mg¹ig terjedõ mennyiséggel páciensenként naponta. A neuropátiás fájdalom hatásosan kezelhetõ körülbelül 0,01 mg¹tól körülbelül 12 mg¹ig terjedõ mennyiségû találmány szerinti vegyülettel testsúly-kilogrammonként naponta, vagy másként körülbelül 0, mg¹tól körülbelül, g¹ig terjedõ mennyiségû vegyülettel páciensenként és naponként. Az itt használt rövidítések a következõk, kivéve, ha másként adjuk meg: 4-MeBnOH 4-Metil-benzil-alkohol CDI 1,1 -Karbonil-diimidazol TEA Trietil-amin TBSC1 t-butil-dimetil-szilil-klorid DMF Dimetil-formamid (+)-BINAP (+)-2,2 -Bisz(difenil-foszfino)-1,1 -binaftil NaOtBu Nátrium-t-butoxid DIPEA Diizopropil-etil-amin EtOAc Etil-acetát TBSOTf t-butil-dimetil-szilil-triflát TBS t-butil-dimetil-szilil THF Tetrahidrofurán DMAP 4-Dimetil-amino-piridin RT Szobahõmérséklet h Órák min Percek DCM Diklór-metán MeCN Acetonitril iproh 2-Propanol n-buoh 1-Butanol EDC 1-(3¹Dimetil-amino-propil)-3-etilkarbodiimid-hidroklorid HOAt 1-Hidroxi-7-aza-benzotriazol Szintézismódszerek 3. reakcióvázlat 8
9 1 HU T reakcióvázlat. reakcióvázlat A találmány szerinti vegyületeket az alább található reakcióvázlatok szerint, valamint a példákban ismertetett eljárásokkal lehet elõállítani. Az alábbi reakcióvázlatok és példák tovább leírják, de nem korlátozzák a találmány oltalmi körét. 1. és 2. példa 1. példa (3S,4R)-4-Metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát példa (3R,4S)-4-Metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát 1. lépés 4-Metil-benzil-4-oxo-piperidin-1-karboxilát elõállítása 9
10 1 HU T2 2 4-Metil-benzil-alkoholt (37,6 g, 8 mmol) adtunk szobahõmérsékleten 1,1 -karbonil-diimidazol (0,0 g, 8 mmol) dimetil-formamidos oldatához, és egy órán át kevertük szobahõmérsékleten. Hozzáadtunk 4¹piperidon-hidrát hidrokloridot (47,0 g, 8 mmol, kereskedelmileg kapható a Sigma-Aldrich cégtõl), és az így kapott reakcióelegyet azután 0 C¹ra melegítettük és 1 órán át kevertük. A reakcióelegyet etil-acetáttal hígítottuk és 0,1 M sósavval, vízzel (négyszer) és konyhasóoldattal mostuk, Na 2 SO 4 fölött szárítottuk, leszûrtük és betöményítettük. Szilikagélen végzett kromatografálással (gradienseluciós lépés: %, 2%, 0% EtOAc hexánokban) a cím szerinti vegyületet kaptuk (42,4 g, 8%¹os hozam) tiszta olajként. 1 H NMR (0 MHz, CDCl 3 ) 7,24 (d, 2H), 7,1 (d, 2H),,08 (s, 2H), 3,79 (t, 4H), 2,4 (br s, 4H) 2,31 (s, 3H) ppm; HRMS (ES) m/z 248,1281 [(M+H) + ;C 14 H 18 NO 3 ¹ra számítva: 248,1287]. Elemzési eredmény C 14 H 17 NO 3 ¹ra számítva: C, 68,03; H, 7,0; N,,9. Talált: C, 68,00; H, 6,93; N,, lépés (±)-4-Metil-benzil-3-fluor-4-oxo-piperidin-1- karboxilát elõállítása 1 2 4,23 (d, 1H), 3,90 (m, 1H), 3, (m, 1H), 3,3 (t, 1H), 2,8 (m, 2H), 2,3 (s, 3H) ppm; HRMS (ES) m/z 284,1292 [(M+H) + ; C 14 H 18 FNO 4 ¹re számítva: 284,1293]. Elemzési eredmény C 14 H 18 FNO 4.1,2 H 2 O¹ra számítva: C, 8,61; H, 6,46; N, 4,88. Talált: C, 8,28; H, 6,06; N, 4, lépés (±)-4-Metil-benzil¹(E)-4-(2¹etoxi-2-oxo-etilidén)-3- fluor-piperidin-1-karboxilát elõállítása és és (±)-4-metil-benzil¹(Z)-4-(2¹etoxi-2-oxo-etilidén)- 3-fluor-piperidin-1-karboxilát elõállítása 4-Metil-benzil-4-oxo-piperidin-1-karboxilát (21,2 g, 8,7 mmol) és diizopropil-etil-amin (71,3 ml, 428 mmol) diklór-metános (42 ml) oldatát 0 C¹ra hûtöttük és kevertük. Lassan TBSOTf¹et (29, ml, 129 mmol) adtunk hozzá, a belsõ hõmérsékletet C alatt tartva. Vizes NaHCO 3 ¹at ( ml) adtunk hozzá, és a rétegeket szétválasztottuk. A szerves réteget vizes NaHCO 3 -oldattal (kétszer) és vizes konyhasóoldattal mostuk, Na 2 SO 4 fölött szárítottuk, leszûrtük és betöményítettük; így a nyers TBS-enol-étert kaptuk. A nyers TBS-enol-étert szobahõmérsékleten feloldottuk DMF-ben (12 ml). Selectfluor reagenst (kereskedelmileg beszerezhetõ az Air Products and Chemicals, Inc.¹tól,,4 g, 8,7 mmol) adtunk hozzá, és a reakcióelegyet percen át kevertük. A reakcióelegyet megosztottuk EtOAc és H 2 O között, és a szerves réteget vízzel (háromszor) mostuk. Az egyesített vizes rétegeket EtOAc-vel extraháltuk (kétszer), és az egyesített szerves rétegeket Na 2 SO 4 fölött szárítottuk, leszûrtük és betöményítettük. Az egész fenti reakciót megismételtük, és a kapott reakciótermékeket egyesítettük; így a cím szerinti terméket ( g) kaptuk, amit tisztítás nélkül használtunk fel a következõ lépésben. Az NMRés tömegspektrum-adatok arra engednek következtetni, hogy a keton-funkció hidrátként van jelen a termékben. 1 H NMR (0 MHz, CDCl 3 ) 7,24 (m, 2H), 7,19 (m, 2H),,18 (s, 2H), 4,81 (br d, 1H), 4,0 (br d, 1H), (±)-4-Metil-benzil-3-fluor-oxo-piperidin-1-karboxilát ( g, mmol) toluolos (0 ml) oldatához szobahõmérsékleten (karbetoxi-metilén)-trifenil-foszforánt (63,0 g, 181 mmol) adtunk, és a reakcióelegyet egy órán át kevertük. A reakcióelegyet betöményítettük és szilikagélen végzett kromatografálással (gradienseluálás: % % EtOAc hexánokban) tisztítottuk; így az alábbi két olefint kaptuk: (±)-4-metil-benzil¹(E)-4-(2¹etoxi-2-oxo-etilidén)-3-fluor-piperidin-1-karboxilát és (±)-4- metil-benzil¹(z)-4-(2¹etoxi-2-oxo-etilidén)-3-fluor-piperidin-1-karboxilát (41,0 g, 78%¹os hozam, 3 lépés) 3:1 E:Z elegyként. Ezt az elegyet közvetlenül felhasználtuk a következõ lépésben. Az elegy egy kis mintáját szilikagél-kromatografálással elkülönítettük azonosítási célokból. (±)-4-Metil-benzil¹(E)-4-(2¹etoxi-2-oxo-etilidén)-3- fluor-piperidin-1-karboxilát: fehér szilárd anyag; 1 H NMR (0 MHz, CDCl 3 ) 7,26 (d, 2H), 7,17 (d, 2H),,98 (s, 1H),,11 (s, 2H), 4,8 (m, 1H), 4,18 (q, 2H), 4,08 (br d, 1H), 3,70 (m, 1H), 3, (m, 1H) 3,41 (m, 1H), 3,33, (m, 1H), 2,63 (br d, 1H), 2,3 (s, 3H), 1,29 (t, 3H) ppm; HRMS (ES) m/z 38,14 [(M+Na) + ; C 18 H 22 FNO 4 - Na¹ra számítva: 38,142]. Elemzési eredmény C 18 H 22 FNO 4 ¹re számítva: C, 64,21; H, 6,8; N, 4,27. Talált: C, 64,46; H, 6,61; N, 4,18. (±)-4-Metil-benzil¹(Z)-4-(2¹etoxi-2-oxo-etilidén)-3- fluor-piperidin-1-karboxilát: fehér szilárd anyag; 1 H NMR (0 MHz, CDCl 3 ) 7,24 (d, 2H), 7,1 (d, 2H), 6,41 (m, 1H),,82 (s, 1H),,11 (d, 2H), 4,61 (m, 1H), 4,38 (brd, 1H), 4,16 (q, 2H), 3,0 2,9 (m, 1H),
11 1 HU T2 2 2,9 2,7 (m, 2H), 2,33 (s, 3H), 2,13 (m, 1H), 1,27 (t, 3H) ppm; HRMS (ES) m/z 38,1422 [(M+Na) + ;C 18 H 22 FNO 4 Na¹ ra számítva: 38,142]. 4. lépés (±)-cisz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3-fluorpiperidin-1-karboxilát és (±)-transz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3- fluor-piperidin-1-karboxilát elõállítása A 3. lépés olefinkeverékének (,0 g, 29,8 mmol) toluolos (1 ml) és CH 2 Cl 2 ¹s (1 ml) oldatához difenil-szilánt (,3 ml, 29,8 mmol) és (R)-BINAP¹ot (1,86 g, 2,98 mmol) adtunk. Ezután nátrium-t-butoxidot (0,29 g, 2,98 mmol) és CuCl¹t (0, g, 2,98 mmol) adtunk a reakcióelegyhez, amelyet fénytõl védtünk és 1 órán át kevertünk. További difenil-szilán (2,76 ml), NaOtBu (0,29 g) és CuCl (0, g) részleteket adtunk a reakcióelegyhez, amelyet szobahõmérsékleten 24 órán át kevertünk. Az elegyet ezután celiten át szûrtük és betöményítettük. Szilikagélen végzett tisztítással (lépcsõs gradienseluálás: %, %, 1%, 2%, % EtOAc hexánokban) visszanyert kiindulási anyagokat (3, g, 3%¹os hozam), (±)-cisz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3-fluor-piperidin-1-karboxilátot (,0 g, 0%¹os hozam) és (±)-transz-4-metil-benzil-4-(2¹etoxi- 2-oxo-etil)-3-fluor-piperidin-1-karboxilátot (1,2 g, 12%¹os hozam) kaptunk. (±)-cisz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3-fluorpiperidin-1-karboxilát: tiszta olaj; 1 H NMR (0 MHz, CDCl 3 ) 7,2 (d, 2H), 7,1 (d, 2H),, (s, 2H), 4,80 4, (m, 3H), 4,1 (q, 2H), 3, 2,73 (m, 2H), 2,2 (dd, 1H), 2,3 (s, 3H), 2, (dd, 1H), 2, (m, 1H), 1,72 1,48 (m, 2H), 1,29 (t, 3H) ppm; HRMS (ES) m/z 338,1689 [(M+H) + ; C 18 H 2 FNO 4 ¹re számítva: 338,1762]. (±)-transz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3- fluor-piperidin-1-karboxilát: tiszta olaj; 1 H NMR (0 MHz, CDCl 3 ) 7,24 (d, 2H), 7,1 (d, 2H),,08 (s, 2H), 4,0 3,9 (m, 3H), 4,1 (q, 2H), 2,81 (br t, 2H), 2,70 (br d, 1H), 2,3 (s, 3H), 2,17 (m, 2H), 1,89 (br d, 1H), 1,2 (m, 1H), 1,22 (t, 3H) ppm; HRMS (ES) m/z 338,1699 [(M+H) + ; C 18 H 2 FNO 4 ¹re számítva: 338,1762] lépés (±)-((cisz)-3-fluor-1-{[(4¹metil-benzil)-oxi]-karbonil}- piperidin-4¹il)-ecetsav elõállítása (±)-cisz-4-metil-benzil-4-(2¹etoxi-2-oxo-etil)-3-fluorpiperidin-1-karboxilát (,0 g, 29,6 mmol) tetrahidrofurános (0 ml) oldatához vizes NaOH¹t (1 M, 0 ml) adtunk. A reakcióelegyet szobahõmérsékleten órán át kevertük, majd EtOAc-vel és 1 M HCl-lel hígítottuk. A rétegeket elválasztottuk egymástól, és a vizes réteget kétszer extraháltuk EtOAc-vel. Az egyesített szerves rétegeket vizes konyhasóoldattal mostuk, Na 2 SO 4 fölött szárítottuk, szûrtük és betöményítettük; így a cím szerinti vegyületet (9,1 g) fehér szilárd anyagként kaptuk, amelyet a következõ lépésben további tisztítás nélkül használtunk fel. 1 H NMR (0 MHz, CDCl 3 ) 7,24 (d, 2H), 7,1 (d, 2H),,08 (s, 2H), 4,79 4,16 (m, 3H), 3,0 2,7 (m, 2H), 2,9 (dd, 1H), 2,36 (dd, 1H), 2,31 (s, 3H), 2, 2,02 (m, 1H), 1, (m, 2H) ppm; HRMS (ES) m/z 3,147 [(M+H) + ; C 16 H 21 FNO 4 ¹re számítva: 3,1449]. Elemzési eredmény C 16 H FNO 4.0,1 H 2 O¹ra számítva: C, 62,13; H, 6,2; N, 4,3. Talált: C, 61,; H, 6,37; N, 4, lépés (±)-cisz-4-metil-benzil-4-(amino-metil)-3-fluorpiperidin-1-karboxilát elõállítása Nyers (±)-((cisz)-3-fluor-1-{[(4¹metil-benzil)-oxi]-karbonil}-piperidin-4¹il)-ecetsav (9,1 g, 29,4 mmol) toluolos (80 ml) szuszpenziójához trietil-amint (,2 ml, 73, mmol) és difenil-foszforil-azidot (9,2 ml, 44,1 mmol) adtunk. A reakcióelegyet felmelegítettük 70 C¹ra és percen át kevertük. Dioxán (80 ml) és 1 M NaOH (80 ml) elegyét adtuk a reakcióelegyhez, amelyet ezután lehûtöttünk szobahõmérsékletre. A reakcióelegyet betöményítettük a dioxán eltávolítása céljából, majd EtOAc-vel háromszor extraháltuk, Na 2 - SO 4 fölött szárítottuk, leszûrtük és betöményítettük. A maradékot szuszpendáltuk CH 2 Cl 2 -ben, percen át kevertük, és a fehér csapadékot leszûrtük. A szûrletet betöményítettük; így a nyersterméket (7, g) sárga olajként kaptuk, amelyet a következõ lépésben közvetlenül felhasználtunk. Egy analitikai mintát szilikagélen végzett kromatografálással (gradienseluálás: CH 2 Cl 2 és CH 2 Cl 2 :MeOH: NH 4 OH=80::2) tisztítottunk jellemzés céljából: 11
12 1 HU T2 2 1 H NMR (0 MHz, CDCl 3 ) 7,24 (d, 2H), 7,1 (d, 2H),,08 (s, 2H), 4,90 4,18 (m, 3H), 2,9 2,7 (m, 2H), 2,79 (dd, 1H), 2,70 (dd, 1H), 2,3 (s, 3H), 1,9 (m, 3H) ppm; HRMS (ES) m/z 281,168 [(M+H) + ;C 1 H 22 FN 2 O 2 ¹re számítva: 281,16]. 7. lépés (3S,4R)-4-Metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát és (3R,4S)-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát elõállítása Két lezárt csövet megtöltöttünk nyers (±)-cisz-4-metil-benzil-4-(amino-metil)-3-fluor-piperidin-1-karboxilát (6. lépés, 3,7 g, 13,2 mmol) és 2¹klór-pirimidin (1,1 g, 13,2 mmol) n¹butanol/diizopropil-etil-aminban (1:1, 13 ml) készített elegyével. A csöveket lezártuk, és az elegyeket 1 C¹ra hevítettük és 2 órán át kevertük. Szobahõmérsékletre való lehûlés után a reakcióelegyeket egyesítettük és EtOAc-val és telített NaHCO 3 -mal hígítottuk. A rétegeket elválasztottuk egymástól, és a szerves réteget vízzel és vizes konyhasóoldattal mostuk, Na 2 SO 4 fölött szárítottuk, leszûrtük és betöményítettük. Szilikagélen végzett kromatografálással (gradienseluálás: 1:1 hexánok:etoac EtOAc) végzett tisztítás után racém cisz-4-metil-benzil-3-fluor-4-[(pirimidin- 2-il-amino)-metil]-piperidin-1-karboxilátot (6,9 g, 6%¹os hozam, 3 lépés) kaptunk fehér szilárd anyagként. Az enantiomereket preparatív nagynyomású folyadékkromatografálással ChiralPak AD oszlopokon ( cm 0 cm, M) MeOH:MeCN (1:8, ml/perc) eluálószert alkalmazva elválasztottuk. Az 1. példa sósavas sóját úgy állítottuk elõ, hogy (3S,4R)- cisz-4-metil-benzil-3-fluor-4-[(pirimidin-2-il-amino)-metil]-piperidin-1-karboxilátot (6,9 g, 19,3 mmol) iprohban (0 ml) feloldottunk 6 C¹on. HCl iproh-val készített oldatát (1,8 M, 12,6 ml,,2 mmol) adtuk hozzá, és az oldatot lassan hûtöttük szobahõmérsékletre 1 órán át. Et 2 O¹t (2 ml) adtunk hozzá, és az elegyet 3 órán át kevertük, lehûtöttük 0 C¹ra, egy órán át kevertük és leszûrtük. Így (3S,4R)-4-metil-benzil-3- fluor-4-[(pirimidin-2-il-amino)-metil]-piperidin-1-karboxilát-hidrokloridot kaptunk fehér szilárd anyagként (7,0 g, 92%¹os kitermelés) A (3R,4S)-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát hidrokloridsóját hasonló eljárást alkalmazva állítottuk elõ. (3S,4R)-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát.HCl: [ ] D 36,4 (c 0,17, MeOH); olvadáspont: 149 C; 1 H NMR (0 MHz, CD 3 OD) 8,8 (br s, 2H), 7,21 (d, 2H), 7,17 (d, 2H), 6,99 (t, 1H),,06 (s, 2H), 4,79 (m, 1H), 4,42 (t, 1H), 4,21 (d, 1H), 3, (dd, 1H), 3,0 (dd, 1H), 3,1 2,80 (m, 2H), 2, (s, 3H), 2, (m, 1H), 1,61 (m, 2H) ppm; HRMS (ES) m/z 39,1879 [(M+H) + ;C 19 H 24 FN 4 O 2 ¹ra számítva: 39,1878]. Elemzési eredmény C 19 H 23 FN 4 O 2.HCl.0,2 H 2 O¹ra számítva: C, 7,27; H, 6,17; N, 14,06. Talált: C, 7,22; H, 6,37; N, 14,16. (3R,4S)-4-Metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát.HCl: [ ] D +34,9 (c 0,18, MeOH); olvadáspont: 149 C; 1 H NMR (0 MHz, CD 3 OD) 8,8 (br s, 2H), 7,21 (d, 2H), 7,17 (d, 2H), 6,99 (t, 1H),,06 (s, 2H), 4,79 (m, 1H), 4,42 (t, 1H), 4,21 (d, 1H), 3, (dd, 1H), 3,0 (dd, 1H), 3,1 2,80 (m, 2H), 2, (s, 3H), 2, (m, 1H), 1,61 (m, 2H) ppm; HRMS (ES) m/z 39,1870 [(M+H) + ;C 19 H 24 FN 4 O 2 ¹re számítva: ]. Elemzési eredmény C 19 H 23 FN 4 O 2.HCl.0, H 2 O¹ra számítva: C, 6,0; H, 6,24; N, 13,87. Talált: C, 6,68; H, 6,27; N, 13, és 4. példa ( )-transz-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát (3. példa) és (+)-transz-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát (4. példa) A cím szerinti vegyületeket (±)-transz-4-metilbenzil-4-(2¹etoxi-2-oxo-etil)-3-fluor-piperidin-1-karboxilátból (1. és 2. példa, 4. lépés) állítottuk elõ, az 1. és 2. példa., 6. és 7. lépésében leírt eljárásokat használva. ( )-transz-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát.hcl: [ ] D 11, (c 0,22, MeOH); olvadáspont: C; 1 H NMR (0 MHz, CD 3 OD) 8,80 8,39 (m, 2H), 7,24 (d, 2H), 7,1 (d, 2H), 7,00 (t, 1H),,08 (s, 2H), 4,49 4,21 (m, 2H), 4,00 (d, 1H), 3,81 (dd, 1H), 3,8 (dd, 1H), 2,9 (m, 1H), 2,31 (s, 3H), 2,12 (m, 1H), 1,90 (m, 1H), 1,34 (m, 1H) ppm; HRMS (ES) m/z 39,1867 [(M+H) + ; C 19 F 24 FN 4 O 2 ¹re számítva: 39,1878]. 12
13 1 HU T2 2 Elemzési eredmény C 19 H 23 FN 4 O 2.HCl.H 2 O¹ra számítva: C,,27; H, 6,3; N, 13,7. Talált C,,08; H, 6,11; N, 13,36. (+)-transz-4-metil-benzil-3-fluor-4-[(pirimidin-2-ilamino)-metil]-piperidin-1-karboxilát.hcl: [ ] D +16,3 (c 0,17, MeOH); olvadáspont: C 1 H NMR (0 MHz, CD 3 OD) 8,80 8,39 (m, 2H), 7,24 (d, 2H), 7,1 (d, 2H), 7,00 (t, 1H),,08 (s, 2H), 4,49 4,21 (m, 2H), 4,00 (d, 1H), 3,81 (dd, 1H), 3,8 (dd, 1H), 2,9 (m, 1H), 2,31 (s, 3H), 2,12 (m, 1H), 1,90 (m, 1H), 1,34 (m, 1H) ppm; HRMS (ES) m/z 39,1873 [(M+H) + ;C 19 H 24 FN 4 O 2 ¹re számítva: 39,1878]. Elemzési eredmény C 19 H 23 FN 4 O 2.HCl.H 2 O¹ra számítva: C,,27; H, 6,3; N, 13,7. Talált: C,,18; H, 6,11; N, 13,38.. példa (3S,4R)-N-[(3¹cisz-Fluor-1-{[(1R,2R)-2-fenil- ciklopropil]-karbonil}-piperidin-4¹il)-metil]-pirimidin- 2-amin elõállítása (3S,4R)-4-Metil-benzil-3-fluor-4-[(pirimidin-2-il-amino)-metil]-piperidin-1-karboxilátot (1. példa) (0 mg, 1,16 mmol) feloldottunk 3 N HCl-ben (4 ml), felmelegítettük 90 C¹ra és egy órán át kevertük. A reakcióelegyet betöményítettük, és a nyers amin-hidrokloridot szobahõmérsékleten feloldottuk DMF-ben (3 ml), majd hozzáadtunk (1R,2R)-2-fenil-ciklopropán-karbonsavat (188 mg, 1,16 mmol) [elõállítva a T. N. Riley és C. G. Brier által leírt módon, J. Org. Chem. 1, (1972)], EDC¹t (222 mg, 1,16 mmol), HOAt¹t (18 mg, 1,16 mmol) és trietil-amint (323 L, 2,32 mmol). A reakcióelegyet 70 C¹ra melegítettük és percen át kevertük. Szobahõmérsékletre való lehûlés után a reakcióelegyet EtOAc-vel és H 2 O-val hígítottuk. A rétegeket elkülönítettük, és a szerves réteget H 2 O-val és vizes konyhasóoldattal mostuk, Na 2 SO 4 fölött szárítottuk, leszûrtük és betöményítettük. Szilikagélen végzett kromatografálással (gradienseluálás: 1:1 hexánok:etoac 90::1 EtOAc:MeOH:NH 4 OH) végzett tisztítás után a cím szerinti vegyületet (3 mg, 78%¹os hozam) fehér szilárd anyagként kaptuk. A vegyületet hidrokloridsóként jellemeztük, amelyet hasonló módon állítottunk elõ, mint ahogyan az 1. példa 7. lépésében le van írva. [ ] D 164 (c 0,22, MeOH); olvadáspont: C; 1 H NMR (0 MHz, CD 3 OD) 8,9 (br s, 2H), 7,2 (m, 2H), 7,17 (m, 3H), 7,01 (t, 1H), 4,8 (m, 2H), 4,6 4, (m, 2H), 3, (m, 2H), 3, (m, 1H), 2,80 m, 1H), 2,39 (m, 1H), 2, 2, (m, 2H), 1,7 (m, 1H), 1, (m, 2H), 1,33 (m, 1H) ppm; HRMS (ES) m/z 3,192 [(M+H) + ; C H 24 FN 4 O¹ra számítva: 3,1929] Elemzési eredmény C H 23 FN 4 O.HCl.H 2 O¹ra számítva: C, 8,7; H, 6,41; N, 13,70. Talált: C, 8,7; H, 6,44; N, példa ( )-cisz-4-metil-benzil-3-fluor-4-[(1,3,4-tiadiazol-2- il-amino)-metil]-piperidin-1-karboxilát 1. lépés (±)-cisz-4-metil-benzil-4-{[(hidrazino-karbonotioil)- amino]-metil}-3-fluor-piperidin-1-karboxilát elõállítása (±)-cisz-4-metil-benzil-4-(amino-metil)-3-fluor-piperidin-1-karboxilát (1. példa, 6. lépés) (0 mg, 0,71 mmol) DMF¹es (2 ml) oldatát adtuk cseppenként tiokarbonil-dimidazol (127 mg, 0,71 mmol) DMF¹es (4 ml) kevert és lehûtött (0 C) oldatához. A reakcióelegyet percen át kevertük, a hûtõfürdõt eltávolítottuk, és a reakcióelegyet szobahõmérsékleten egy órán 13
14 1 HU T2 2 át kevertük. Ezután hidrazint (0,066 ml, 2,14 mmol) adtunk a reakcióelegyhez, amelyet további percen át kevertünk. A reakcióelegyet vízbe öntöttük és etilacetáttal extraháltuk. A szerves réteget telített nátriumhidrogén-karbonát-oldattal, vízzel és vizes konyhasóoldattal mostuk, nátrium-szulfát fölött szárítottuk, és az oldószert vákuumban bepároltuk; így a nyersterméket szilárd anyagként kaptuk. A nyers szilárd anyagot metanollal ( ml) kezeltük és leszûrtük; így 180 mg cím szerinti terméket kaptunk. 1 H NMR (0 MHz, CDCl 3 ) 7,67 (br s, 2H), 7,2 (d, 2H), 7,19 (d, 2H),, (s, 2H), 4,80 4, (br m, 3H), 3,7 (s, 2H), 3,80 3, (m, 2H), 3,0 2,70 (m, 2H), 2,38 (s, 3H), 2, (m, 1H), 1, (m, 2H) ppm. 2. lépés ( )-cisz-4-metil-benzil-3-fluor-4¹[1,3,4-tiadiazol-2-ilamino)-metil]-piperidin-1-karboxilát (±)-cisz-4-metil-benzil-4-{[(hidrazino-karbonotioil)- amino]-metil}-3-fluor-piperidin-1-karboxilát (180 mg, 0,1 mmol) etanollal ( ml) készített szuszpenzióját trietil-ortoformáttal (11 mg, 1,02 mmol) és tömény sósavval (0,01 ml) kezeltük, és szobahõmérsékleten kevertük 18 órán át nitrogénatmoszférában. Az összes szilárd anyag feloldódása után a reakcióelegyet 1, órán át visszafolyató hûtõ alatt forraltuk, majd lehûtöttük szobahõmérsékletre, és az illékony anyagokat lehajtottuk. A maradékot megosztottuk etil-acetát és híg nátrium-hidrogén-karbonát-oldat között, a szerves réteget vizes konyhasóoldattal mostuk, nátrium-szulfát fölött szárítottuk, és az oldószert lehajtottuk. A nyersterméket szilikagélen végzett gradienselúcióval (0% etil-acetáthexán % metanol:etil-acetát) tisztítottuk; így a cím szerinti terméket fehér szilárd termékként kaptuk. A ( )-enantiomert elkülönítettük, és a hidrokloridsót az 1. és 2. példa 7. lépésében leírt módon állítottuk elõ. [ ] D 47,4 (c 0,17, MeOH); olvadáspont: C; 1 H NMR (0 MHz, CDCl 3 ) 8,37 (s, 1H), 7,2 (d, 2H), 7,16 (d, 2H), 6,7 (br s, 1H),, (d, 2H), 4,79 (dd, 1H), 4,6 (m, 1H), 4,29 (m, 1H), 3,44 (d, 2H), 3, 2,77 (m, 2H), 2,3 (s, 3H), 2,2 (m, 1H), 1,63 (m, 2H); HRMS (ES) m/z 36,1437 [(M+H) + ;C 17 H 22 FN 4 O 2 S¹re számítva: 36,1442]. Elemzési eredmény C 17 H 21 FN 4 O 2 S¹re számítva: C, 6,03; H,,81; N, 1,37. Talált: C,,82; H,,74; N, 1, példa (+)-transz-4-metil-benzil-3-fluor-4-[(1,3,4-tiadiazol- 2-il-amino)-metil]-piperidin-1-karboxilát: A cím szerinti vegyületet (±)-transz-4-metil-benzil- 4-(2¹etoxi-2-oxo-etil)-3-fluor-piperidin-1-karboxilátból (1. és 2. példa, 4. lépés) állítottuk elõ, az 1. és 2. példa. és 6. lépésében leírt eljárást használva, amit a 6. példában leírt tiadiazolképzés követett. A (+)-enantiomert királis nagynyomású folyadékkromatografálással különítettük el az 1. és 2. példa 7. lépésében leírt módon. [ ] D +37,1 (c 0,6, MeOH); olvadáspont: 93 9 C; 1 H NMR (0 MHz, CDCl 3 ) 8,36 (s, 1H), 7,28 (d, 2H), 7,19 (d, 2H), 6,6 (br s, 1H),,04 (s, 2H), 4,4 (m, 2H), 4,17 (m, 1H), 3,6 (m, 2H), 2,80 (m, 2H), 2,3 (s, 3H), 2, (m, 1H), 1,96 (m, 1H), 1,39 (m, 1H) ppm; HRMS (ES) m/z 36,1432 [(M+H) + ;C 17 H 22 FN 4 O 2 S¹re számítva: 36,1442]. Elemzési eredmény C 17 H 21 FN 4 O 2 S 0,2 H 2 O¹ra számítva: C,,34; H,,87; N, 1,19. Talált: C,,0; H,,61; N, 14,81. SZABADALMI IGÉNYPONTOK 1. Egy(I) képletû vegyület (I) vagy annak egy gyógyászatilag elfogadható sója, ahol HetAr jelentése 1 vagy 2 nitrogén gyûrûatomot tartalmazó, vagy 6 tagú heteroaromás gyûrû, tiazolil vagy tiadiazolil; R 1 és R 2 jelentése egymástól függetlenül H, C 1 4 alkil, fluor, klór, bróm vagy jód; A jelentése kötés vagy C 1 2 alkilén¹; és B jelentése aril-(ch 2 ) 0 3 O (O), indanil- (CH 2 ) 0 3 O C(O), aril-(ch 2 ) 1 3 C(O), aril-ciklopropil-c(o), aril-(ch 2 ) 1 3 ¹NH C(O), ahol bármelyik aril adott esetben szubsztituálva van 1 szubsztituenssel, ahol a szubsztituensek jelentése egymástól függetlenül C 1 4 alkil, fluor vagy klór. 2. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sója, ahol HetAr jelentése 2 nitrogén gyûrûatomot tartalmazó, 6 tagú heteroaromás gyûrû. 3. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sója, ahol HetAr jelentése tiadiazolil. 4. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sója, ahol A jelentése metilén.. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sója, ahol 14
15 1 HU T2 2 B jelentése aril-ciklopropil-c(o), ahol az említett aril adott esetben az 1. igénypont szerinti módon van szubsztituálva. 6. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sója, ahol B jelentése aril-(ch 2 ) 0 3 O C(O), ahol az említett aril adott esetben az 1. igénypontban meghatározott módon van szubsztituálva. 7. Az 1. igénypont szerinti vegyület, ahol az említett vegyület ( ) (+) ( ) (+) vagy azok gyógyászatilag elfogadható sója. 8. Az 1. igénypont szerinti vegyület, ahol az említett vegyület. Az 1. igénypont szerinti vegyület, ahol az említett vegyület 4 vagy annak egy gyógyászatilag elfogadható sója. 9. Az 1. igénypont szerinti vegyület, ahol az említett vegyület 0 vagy annak egy gyógyászatilag elfogadható sója. 11. Az 1. igénypont szerinti vegyület, ahol az említett vegyület ( ) vagy annak egy gyógyászatilag elfogadható sója. vagy annak egy gyógyászatilag elfogadható sója. (+) 1
16 1 HU T Gyógyászati kompozíció, amely közömbös hordozót és 1. igénypont szerinti vegyület gyógyászatilag hatásos mennyiségét tartalmazza. 13. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sójának alkalmazása páciensben fájdalom kezelésére vagy megelõzésére szolgáló gyógyszer elõállítására. 14. Az 1. igénypont szerinti vegyület vagy annak egy gyógyászatilag elfogadható sójának alkalmazása páciensben Parkinson-kór kezelésére vagy megelõzésére szolgáló gyógyszer elõállítására. Kiadja a Magyar Szabadalmi Hivatal, Budapest Felelõs vezetõ: Törõcsik Zsuzsanna Windor Bt., Budapest
(11) Lajstromszám: E 004 888 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (I)
 !HU000004888T2! (19) HU (11) Lajstromszám: E 004 888 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 770962 (22) A bejelentés napja:
!HU000004888T2! (19) HU (11) Lajstromszám: E 004 888 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 770962 (22) A bejelentés napja:
(11) Lajstromszám: E 008 536 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008536T2! (19) HU (11) Lajstromszám: E 008 536 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 05 717379 (22) A bejelentés
!HU000008536T2! (19) HU (11) Lajstromszám: E 008 536 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 05 717379 (22) A bejelentés
(11) Lajstromszám: E 008 147 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA. (54) Gaboxadol depresszió és más emocionális rendellenességek kezelésére
 !HU000008147T2! (19) HU (11) Lajstromszám: E 008 147 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73896 (22) A bejelentés napja:
!HU000008147T2! (19) HU (11) Lajstromszám: E 008 147 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73896 (22) A bejelentés napja:
(11) Lajstromszám: E 007 003 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007003T2! (19) HU (11) Lajstromszám: E 007 003 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 7882 (22) A bejelentés napja:
!HU000007003T2! (19) HU (11) Lajstromszám: E 007 003 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 7882 (22) A bejelentés napja:
(11) Lajstromszám: E 008 303 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000083T2! (19) HU (11) Lajstromszám: E 008 3 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 774778 (22) A bejelentés
!HU0000083T2! (19) HU (11) Lajstromszám: E 008 3 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 774778 (22) A bejelentés
(11) Lajstromszám: E 005 564 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000064T2! (19) HU (11) Lajstromszám: E 00 64 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 704342 (22) A bejelentés napja: 0.
!HU0000064T2! (19) HU (11) Lajstromszám: E 00 64 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 704342 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 006 966 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006966T2! (19) HU (11) Lajstromszám: E 006 966 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 717644 (22) A bejelentés napja:
!HU000006966T2! (19) HU (11) Lajstromszám: E 006 966 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 717644 (22) A bejelentés napja:
(11) Lajstromszám: E 008 464 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008464T2! (19) HU (11) Lajstromszám: E 008 464 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 05 787786 (22) A bejelentés
!HU000008464T2! (19) HU (11) Lajstromszám: E 008 464 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 05 787786 (22) A bejelentés
(11) Lajstromszám: E 004 263 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004263T2! (19) HU (11) Lajstromszám: E 004 263 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 70014 (22) A bejelentés napja:
!HU000004263T2! (19) HU (11) Lajstromszám: E 004 263 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 70014 (22) A bejelentés napja:
(11) Lajstromszám: E 007 404 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000074T2! (19) HU (11) Lajstromszám: E 007 4 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7796 (22) A bejelentés napja: 03.
!HU0000074T2! (19) HU (11) Lajstromszám: E 007 4 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7796 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 004 705 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000470T2! (19) HU (11) Lajstromszám: E 004 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81479 (22) A bejelentés napja: 0.
!HU00000470T2! (19) HU (11) Lajstromszám: E 004 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81479 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 005 787 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000787T2! (19) HU (11) Lajstromszám: E 00 787 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7421 (22) A bejelentés napja: 03.
!HU00000787T2! (19) HU (11) Lajstromszám: E 00 787 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7421 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 008 672 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008672T2! (19) HU (11) Lajstromszám: E 008 672 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 79006 (22) A bejelentés
!HU000008672T2! (19) HU (11) Lajstromszám: E 008 672 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 79006 (22) A bejelentés
(11) Lajstromszám: E 003 764 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003764T2! (19) HU (11) Lajstromszám: E 003 764 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 76838 (22) A bejelentés napja:
!HU000003764T2! (19) HU (11) Lajstromszám: E 003 764 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 76838 (22) A bejelentés napja:
(11) Lajstromszám: E 007 802 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007802T2! (19) HU (11) Lajstromszám: E 007 802 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 79176 (22) A bejelentés napja:
!HU000007802T2! (19) HU (11) Lajstromszám: E 007 802 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 79176 (22) A bejelentés napja:
(11) Lajstromszám: E 003 246 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA. (51) Int. Cl.: C07C 253/30 (2006.01) (VI)
 !HU000003246T2! (19) HU (11) Lajstromszám: E 003 246 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 290309 (22) A bejelentés napja:
!HU000003246T2! (19) HU (11) Lajstromszám: E 003 246 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 290309 (22) A bejelentés napja:
(11) Lajstromszám: E 003 889 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003889T2! (19) HU (11) Lajstromszám: E 003 889 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPA SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 78601 (22) A bejelentés napja:
!HU000003889T2! (19) HU (11) Lajstromszám: E 003 889 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPA SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 78601 (22) A bejelentés napja:
(11) Lajstromszám: E 004 708 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004708T2! (19) HU (11) Lajstromszám: E 004 708 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 797 (22) A bejelentés napja: 0.
!HU000004708T2! (19) HU (11) Lajstromszám: E 004 708 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 797 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 006 148 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006148T2! (19) HU (11) Lajstromszám: E 006 148 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 839331 (22) A bejelentés napja:
!HU000006148T2! (19) HU (11) Lajstromszám: E 006 148 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 839331 (22) A bejelentés napja:
(11) Lajstromszám: E 007 583 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007583T2! (19) HU (11) Lajstromszám: E 007 583 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 743056 (22) A bejelentés napja:
!HU000007583T2! (19) HU (11) Lajstromszám: E 007 583 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 743056 (22) A bejelentés napja:
(11) Lajstromszám: E 005 217 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
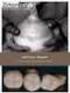 !HU00000217T2! (19) HU (11) Lajstromszám: E 00 217 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 777132 (22) A bejelentés napja:
!HU00000217T2! (19) HU (11) Lajstromszám: E 00 217 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 777132 (22) A bejelentés napja:
(11) Lajstromszám: E 004 313 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004313T2! (19) HU (11) Lajstromszám: E 004 313 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 771807 (22) A bejelentés napja:
!HU000004313T2! (19) HU (11) Lajstromszám: E 004 313 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 771807 (22) A bejelentés napja:
(11) Lajstromszám: E 007 328 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007328T2! (19) HU (11) Lajstromszám: E 007 328 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 797669 (22) A bejelentés napja:
!HU000007328T2! (19) HU (11) Lajstromszám: E 007 328 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 797669 (22) A bejelentés napja:
(11) Lajstromszám: E 003 697 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003697T2! (19) HU (11) Lajstromszám: E 003 697 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7987 (22) A bejelentés napja:
!HU000003697T2! (19) HU (11) Lajstromszám: E 003 697 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7987 (22) A bejelentés napja:
(11) Lajstromszám: E 007 474 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007474T2! (19) HU (11) Lajstromszám: E 007 474 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 722932 (22) A bejelentés napja:
!HU000007474T2! (19) HU (11) Lajstromszám: E 007 474 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 722932 (22) A bejelentés napja:
(11) Lajstromszám: E 005 510 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000010T2! (19) HU (11) Lajstromszám: E 00 10 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 769233 (22) A bejelentés napja: 2004.
!HU0000010T2! (19) HU (11) Lajstromszám: E 00 10 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 769233 (22) A bejelentés napja: 2004.
(11) Lajstromszám: E 005 012 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000012T2! (19) HU (11) Lajstromszám: E 00 012 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 0124 (22) A bejelentés napja: 03.
!HU00000012T2! (19) HU (11) Lajstromszám: E 00 012 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 0124 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 008 330 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000083T2! (19) HU (11) Lajstromszám: E 008 3 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 731998 (22) A bejelentés
!HU0000083T2! (19) HU (11) Lajstromszám: E 008 3 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 731998 (22) A bejelentés
(11) Lajstromszám: E 005 397 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000397T2! (19) HU (11) Lajstromszám: E 00 397 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 81106 (22) A bejelentés napja:
!HU00000397T2! (19) HU (11) Lajstromszám: E 00 397 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 81106 (22) A bejelentés napja:
(11) Lajstromszám: E 006 819 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006819T2! (19) HU (11) Lajstromszám: E 006 819 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7669 (22) A bejelentés napja:
!HU000006819T2! (19) HU (11) Lajstromszám: E 006 819 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7669 (22) A bejelentés napja:
(11) Lajstromszám: E 003 189 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003189T2! (19) HU (11) Lajstromszám: E 003 189 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7082 (22) A bejelentés napja:
!HU000003189T2! (19) HU (11) Lajstromszám: E 003 189 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7082 (22) A bejelentés napja:
(11) Lajstromszám: E 008 195 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000819T2! (19) HU (11) Lajstromszám: E 008 19 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 727742 (22) A bejelentés napja:
!HU00000819T2! (19) HU (11) Lajstromszám: E 008 19 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 727742 (22) A bejelentés napja:
(11) Lajstromszám: E 006 710 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000067T2! (19) HU (11) Lajstromszám: E 006 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 731277 (22) A bejelentés napja: 04.
!HU0000067T2! (19) HU (11) Lajstromszám: E 006 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 731277 (22) A bejelentés napja: 04.
(11) Lajstromszám: E 008 254 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000824T2! (19) HU (11) Lajstromszám: E 008 24 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 791108 (22) A bejelentés napja:
!HU00000824T2! (19) HU (11) Lajstromszám: E 008 24 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 791108 (22) A bejelentés napja:
(11) Lajstromszám: E 006 017 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006017T2! (19) HU (11) Lajstromszám: E 006 017 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 760778 (22) A bejelentés napja:
!HU000006017T2! (19) HU (11) Lajstromszám: E 006 017 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 760778 (22) A bejelentés napja:
(11) Lajstromszám: E 004 130 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000041T2! (19) HU (11) Lajstromszám: E 004 1 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 71 (22) A bejelentés napja: 0. 02.
!HU0000041T2! (19) HU (11) Lajstromszám: E 004 1 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 71 (22) A bejelentés napja: 0. 02.
(11) Lajstromszám: E 006 522 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA. (54) S-omeprazol magnéziumsó szilárd alakjai és eljárás elõállításukra
 !HU00000622T2! (19) HU (11) Lajstromszám: E 006 22 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 760736 (22) A bejelentés napja:
!HU00000622T2! (19) HU (11) Lajstromszám: E 006 22 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 760736 (22) A bejelentés napja:
(11) Lajstromszám: E 008 154 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000814T2! (19) HU (11) Lajstromszám: E 008 14 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 81727 (22) A bejelentés napja:
!HU00000814T2! (19) HU (11) Lajstromszám: E 008 14 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 81727 (22) A bejelentés napja:
(11) Lajstromszám: E 004 517 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000417T2! (19) HU (11) Lajstromszám: E 004 17 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 813663 (22) A bejelentés napja:
!HU00000417T2! (19) HU (11) Lajstromszám: E 004 17 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 813663 (22) A bejelentés napja:
(11) Lajstromszám: E 006 385 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000638T2! (19) HU (11) Lajstromszám: E 006 38 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 7498 (22) A bejelentés napja: 06.
!HU00000638T2! (19) HU (11) Lajstromszám: E 006 38 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 7498 (22) A bejelentés napja: 06.
(11) Lajstromszám: E 005 557 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007T2! (19) HU (11) Lajstromszám: E 00 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 026690 (22) A bejelentés napja: 03.
!HU000007T2! (19) HU (11) Lajstromszám: E 00 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 026690 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 003 868 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003868T2! (19) HU (11) Lajstromszám: E 003 868 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73619 (22) A bejelentés napja:
!HU000003868T2! (19) HU (11) Lajstromszám: E 003 868 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73619 (22) A bejelentés napja:
(11) Lajstromszám: E 008 447 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008447T2! (19) HU (11) Lajstromszám: E 008 447 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 749 (22) A bejelentés
!HU000008447T2! (19) HU (11) Lajstromszám: E 008 447 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 749 (22) A bejelentés
(11) Lajstromszám: E 005 036 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000036T2! (19) HU (11) Lajstromszám: E 00 036 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7113 (22) A bejelentés napja: 04.
!HU00000036T2! (19) HU (11) Lajstromszám: E 00 036 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7113 (22) A bejelentés napja: 04.
(11) Lajstromszám: E 006 271 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006271T2! (19) HU (11) Lajstromszám: E 006 271 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 112327 (22) A bejelentés napja:
!HU000006271T2! (19) HU (11) Lajstromszám: E 006 271 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 112327 (22) A bejelentés napja:
(11) Lajstromszám: E 007 800 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007800T2! (19) HU (11) Lajstromszám: E 007 800 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 787403 (22) A bejelentés napja:
!HU000007800T2! (19) HU (11) Lajstromszám: E 007 800 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 787403 (22) A bejelentés napja:
(11) Lajstromszám: E 003 780 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003780T2! (19) HU (11) Lajstromszám: E 003 780 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 701 (22) A bejelentés napja:
!HU000003780T2! (19) HU (11) Lajstromszám: E 003 780 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 701 (22) A bejelentés napja:
(11) Lajstromszám: E 005 758 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000078T2! (19) HU (11) Lajstromszám: E 00 78 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 766 (22) A bejelentés napja: 03.
!HU0000078T2! (19) HU (11) Lajstromszám: E 00 78 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 766 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 006 028 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000028T2! (19) HU (11) Lajstromszám: E 006 028 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 700 (22) A bejelentés napja: 03.
!HU0000028T2! (19) HU (11) Lajstromszám: E 006 028 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 700 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 005 409 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000009T2! (19) HU (11) Lajstromszám: E 00 9 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 791698 (22) A bejelentés napja: 03.
!HU000009T2! (19) HU (11) Lajstromszám: E 00 9 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 791698 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 007 747 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007747T2! (19) HU (11) Lajstromszám: E 007 747 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 803296 (22) A bejelentés napja:
!HU000007747T2! (19) HU (11) Lajstromszám: E 007 747 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 803296 (22) A bejelentés napja:
(11) Lajstromszám: E 007 688 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007688T2! (19) HU (11) Lajstromszám: E 007 688 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 81138 (22) A bejelentés napja:
!HU000007688T2! (19) HU (11) Lajstromszám: E 007 688 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 81138 (22) A bejelentés napja:
(11) Lajstromszám: E 004 779 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004779T2! (19) HU (11) Lajstromszám: E 004 779 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 299 (22) A bejelentés napja: 0.
!HU000004779T2! (19) HU (11) Lajstromszám: E 004 779 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 299 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 005 976 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000976T2! (19) HU (11) Lajstromszám: E 00 976 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 728268 (22) A bejelentés napja:
!HU00000976T2! (19) HU (11) Lajstromszám: E 00 976 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 728268 (22) A bejelentés napja:
(11) Lajstromszám: E 003 879 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003879T2! (19) HU (11) Lajstromszám: E 003 879 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 290990 (22) A bejelentés napja:
!HU000003879T2! (19) HU (11) Lajstromszám: E 003 879 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 290990 (22) A bejelentés napja:
(11) Lajstromszám: E 007 298 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007298T2! (19) HU (11) Lajstromszám: E 007 298 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7196 (22) A bejelentés napja:
!HU000007298T2! (19) HU (11) Lajstromszám: E 007 298 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 7196 (22) A bejelentés napja:
(11) Lajstromszám: E 007 869 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007869T2! (19) HU (11) Lajstromszám: E 007 869 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 7464 (22) A bejelentés napja:
!HU000007869T2! (19) HU (11) Lajstromszám: E 007 869 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 7464 (22) A bejelentés napja:
(11) Lajstromszám: E 003 925 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000392T2! (19) HU (11) Lajstromszám: E 003 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 014936 (22) A bejelentés napja:
!HU00000392T2! (19) HU (11) Lajstromszám: E 003 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 014936 (22) A bejelentés napja:
(11) Lajstromszám: E 004 311 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004311T2! (19) HU (11) Lajstromszám: E 004 311 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 729 (22) A bejelentés napja:
!HU000004311T2! (19) HU (11) Lajstromszám: E 004 311 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 729 (22) A bejelentés napja:
(11) Lajstromszám: E 005 421 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000421T2! (19) HU (11) Lajstromszám: E 00 421 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 742911 (22) A bejelentés napja:
!HU00000421T2! (19) HU (11) Lajstromszám: E 00 421 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 742911 (22) A bejelentés napja:
(11) Lajstromszám: E 006 740 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000067T2! (19) HU (11) Lajstromszám: E 006 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 293297 (22) A bejelentés napja: 03.
!HU0000067T2! (19) HU (11) Lajstromszám: E 006 7 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 293297 (22) A bejelentés napja: 03.
(11) Lajstromszám: E 007 815 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000781T2! (19) HU (11) Lajstromszám: E 007 81 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 024638 (22) A bejelentés napja:
!HU00000781T2! (19) HU (11) Lajstromszám: E 007 81 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 024638 (22) A bejelentés napja:
(11) Lajstromszám: E 005 784 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000784T2! (19) HU (11) Lajstromszám: E 00 784 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 71341 (22) A bejelentés napja:
!HU00000784T2! (19) HU (11) Lajstromszám: E 00 784 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 71341 (22) A bejelentés napja:
(11) Lajstromszám: E 008 241 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008241T2! (19) HU (11) Lajstromszám: E 008 241 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 771268 (22) A bejelentés napja:
!HU000008241T2! (19) HU (11) Lajstromszám: E 008 241 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 771268 (22) A bejelentés napja:
(11) Lajstromszám: E 004 871 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004871T2! (19) HU (11) Lajstromszám: E 004 871 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 76231 (22) A bejelentés napja:
!HU000004871T2! (19) HU (11) Lajstromszám: E 004 871 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 76231 (22) A bejelentés napja:
01/2008:40202 4.2.2. MÉRŐOLDATOK
 Ph.Hg.VIII. Ph.Eur.5.6-6.0-1 4.2.2. MÉRŐOLDATOK 01/2008:40202 A mérőoldatokat a szokásos kémiai analitikai eljárások szabályai szerint készítjük. A mérőoldatok előállításához használt eszközök megfelelő
Ph.Hg.VIII. Ph.Eur.5.6-6.0-1 4.2.2. MÉRŐOLDATOK 01/2008:40202 A mérőoldatokat a szokásos kémiai analitikai eljárások szabályai szerint készítjük. A mérőoldatok előállításához használt eszközök megfelelő
(11) Lajstromszám: E 005 087 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000087T2! (19) HU (11) Lajstromszám: E 00 087 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 76909 (22) A bejelentés napja: 0.
!HU00000087T2! (19) HU (11) Lajstromszám: E 00 087 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 76909 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 006 749 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006749T2! (19) HU (11) Lajstromszám: E 006 749 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 818248 (22) A bejelentés napja:
!HU000006749T2! (19) HU (11) Lajstromszám: E 006 749 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 818248 (22) A bejelentés napja:
(11) Lajstromszám: E 007 570 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000770T2! (19) HU (11) Lajstromszám: E 007 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 78798 (22) A bejelentés napja:
!HU00000770T2! (19) HU (11) Lajstromszám: E 007 70 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 78798 (22) A bejelentés napja:
(11) Lajstromszám: E 006 436 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006436T2! (19) HU (11) Lajstromszám: E 006 436 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 79470 (22) A bejelentés napja:
!HU000006436T2! (19) HU (11) Lajstromszám: E 006 436 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 79470 (22) A bejelentés napja:
(11) Lajstromszám: E 007 867 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007867T2! (19) HU (11) Lajstromszám: E 007 867 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 84214 (22) A bejelentés napja:
!HU000007867T2! (19) HU (11) Lajstromszám: E 007 867 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 84214 (22) A bejelentés napja:
(11) Lajstromszám: E 006 488 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006488T2! (19) HU (11) Lajstromszám: E 006 488 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 7123 (22) A bejelentés napja:
!HU000006488T2! (19) HU (11) Lajstromszám: E 006 488 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 7123 (22) A bejelentés napja:
(11) Lajstromszám: E 005 981 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000981T2! (19) HU (11) Lajstromszám: E 00 981 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 764090 (22) A bejelentés napja:
!HU00000981T2! (19) HU (11) Lajstromszám: E 00 981 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 764090 (22) A bejelentés napja:
(11) Lajstromszám: E 005 647 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000647T2! (19) HU (11) Lajstromszám: E 00 647 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 721199 (22) A bejelentés napja:
!HU00000647T2! (19) HU (11) Lajstromszám: E 00 647 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 721199 (22) A bejelentés napja:
PHENOXYMETHYLPENICILLINUM KALICUM. Fenoximetilpenicillin-kálium
 Phenoxymethylpenicillinum kalicum Ph.Hg.VIII. Ph.Eur.6.1-1 01/2008:0149 javított 6.1 PHENOXYMETHYLPENICILLINUM KALICUM Fenoximetilpenicillin-kálium C 16 H 17 KN 2 O 5 S M r 388,5 [132-98-9] DEFINÍCIÓ A
Phenoxymethylpenicillinum kalicum Ph.Hg.VIII. Ph.Eur.6.1-1 01/2008:0149 javított 6.1 PHENOXYMETHYLPENICILLINUM KALICUM Fenoximetilpenicillin-kálium C 16 H 17 KN 2 O 5 S M r 388,5 [132-98-9] DEFINÍCIÓ A
(11) Lajstromszám: E 004 563 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000463T2! (19) HU (11) Lajstromszám: E 004 63 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 749820 (22) A bejelentés napja:
!HU00000463T2! (19) HU (11) Lajstromszám: E 004 63 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 749820 (22) A bejelentés napja:
(11) Lajstromszám: E 008 405 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008T2! (19) HU (11) Lajstromszám: E 008 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 77970 (22) A bejelentés napja:
!HU000008T2! (19) HU (11) Lajstromszám: E 008 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 77970 (22) A bejelentés napja:
Gyógyszerhatóanyagok azonosítása és kioldódási vizsgálata tablettából
 Gyógyszerhatóanyagok azonosítása és kioldódási vizsgálata tablettából ELTE TTK Szerves Kémiai Tanszék 2015 1 I. Elméleti bevezető 1.1. Gyógyszerkönyv A Magyar gyógyszerkönyv (Pharmacopoea Hungarica) első
Gyógyszerhatóanyagok azonosítása és kioldódási vizsgálata tablettából ELTE TTK Szerves Kémiai Tanszék 2015 1 I. Elméleti bevezető 1.1. Gyógyszerkönyv A Magyar gyógyszerkönyv (Pharmacopoea Hungarica) első
(11) Lajstromszám: E 004 471 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000004471T2! (19) HU (11) Lajstromszám: E 004 471 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7662 (22) A bejelentés napja:
!HU000004471T2! (19) HU (11) Lajstromszám: E 004 471 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7662 (22) A bejelentés napja:
MAGYAR ÉLELMISZERKÖNYV (Codex Alimentarius Hungaricus)
 Az 56/2004. (IV. 24.) FVM rendelet mellékletének 68. sorszámú előírása MAGYAR ÉLELMISZERKÖNYV (Codex Alimentarius Hungaricus) 1-2-2006/129 számú előírás A színezékeken és édesítőszereken kívüli egyéb élelmiszer-adalékanyagokra
Az 56/2004. (IV. 24.) FVM rendelet mellékletének 68. sorszámú előírása MAGYAR ÉLELMISZERKÖNYV (Codex Alimentarius Hungaricus) 1-2-2006/129 számú előírás A színezékeken és édesítőszereken kívüli egyéb élelmiszer-adalékanyagokra
CALCII STEARAS. Kalcium-sztearát
 Calcii stearas Ph.Hg.VIII. Ph.Eur.6.3-1 CALCII STEARAS Kalcium-sztearát 01/2009:0882 DEFINÍCIÓ Különböző zsírsavak kalciumsóinak keveréke; a savkomponenst főként sztearinsav (oktadekánsav) [(C 17 H 35
Calcii stearas Ph.Hg.VIII. Ph.Eur.6.3-1 CALCII STEARAS Kalcium-sztearát 01/2009:0882 DEFINÍCIÓ Különböző zsírsavak kalciumsóinak keveréke; a savkomponenst főként sztearinsav (oktadekánsav) [(C 17 H 35
XANTHANI GUMMI. Xantán gumi
 Xanthani gummi Ph.Hg.VIII. Ph.Eur.6.4-1 [11138-66-2] DEFINÍCIÓ XANTHANI GUMMI Xantán gumi 04/2009:1277 A xantán gumi nagy molekulatömegű anionos poliszacharid, melyet szénhidrátok Xanthomonas campestris-szel
Xanthani gummi Ph.Hg.VIII. Ph.Eur.6.4-1 [11138-66-2] DEFINÍCIÓ XANTHANI GUMMI Xantán gumi 04/2009:1277 A xantán gumi nagy molekulatömegű anionos poliszacharid, melyet szénhidrátok Xanthomonas campestris-szel
(11) Lajstromszám: E 006 537 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000637T2! (19) HU (11) Lajstromszám: E 006 37 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 708911 (22) A bejelentés napja:
!HU00000637T2! (19) HU (11) Lajstromszám: E 006 37 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 708911 (22) A bejelentés napja:
(11) Lajstromszám: E 003 967 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003967T2! (19) HU (11) Lajstromszám: E 003 967 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 006681 (22) A bejelentés napja:
!HU000003967T2! (19) HU (11) Lajstromszám: E 003 967 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 006681 (22) A bejelentés napja:
(11) Lajstromszám: E 005 115 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000011T2! (19) HU (11) Lajstromszám: E 00 11 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 21 (22) A bejelentés napja: 0. 06.
!HU0000011T2! (19) HU (11) Lajstromszám: E 00 11 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 21 (22) A bejelentés napja: 0. 06.
(11) Lajstromszám: E 005 846 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000846T2! (19) HU (11) Lajstromszám: E 00 846 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 787448 (22) A bejelentés napja:
!HU00000846T2! (19) HU (11) Lajstromszám: E 00 846 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 787448 (22) A bejelentés napja:
(11) Lajstromszám: E 005 509 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000009T2! (19) HU (11) Lajstromszám: E 00 09 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 774961 (22) A bejelentés napja: 2004.
!HU0000009T2! (19) HU (11) Lajstromszám: E 00 09 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 774961 (22) A bejelentés napja: 2004.
(11) Lajstromszám: E 007 276 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA. 1. ábra
 !HU000007276T2! (19) HU (11) Lajstromszám: E 007 276 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 023139 (22) A bejelentés napja:
!HU000007276T2! (19) HU (11) Lajstromszám: E 007 276 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 023139 (22) A bejelentés napja:
(11) Lajstromszám: E 006 900 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000006900T2! (19) HU (11) Lajstromszám: E 006 900 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 737113 (22) A bejelentés napja:
!HU000006900T2! (19) HU (11) Lajstromszám: E 006 900 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 06 737113 (22) A bejelentés napja:
(11) Lajstromszám: E 003 815 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000381T2! (19) HU (11) Lajstromszám: E 003 81 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7948 (22) A bejelentés napja: 04.
!HU00000381T2! (19) HU (11) Lajstromszám: E 003 81 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 7948 (22) A bejelentés napja: 04.
(11) Lajstromszám: E 003 977 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000003977T2! (19) HU (11) Lajstromszám: E 003 977 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal (21) Magyar ügyszám: E 06 008081 (22) A bejelentés napja: 06. 04. 19. (96) Az európai bejelentés
!HU000003977T2! (19) HU (11) Lajstromszám: E 003 977 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal (21) Magyar ügyszám: E 06 008081 (22) A bejelentés napja: 06. 04. 19. (96) Az európai bejelentés
AMOXICILLINUM TRIHYDRICUM. Amoxicillin-trihidrát
 Amoxicillinum trihydricum Ph.Hg.VIII. Ph.Eur.7.6-1 01/2013:0260 AMOXICILLINUM TRIHYDRICUM Amoxicillin-trihidrát C 16 H 19 N 3 O 5 S.3H 2 O M r 419,4 [61336-70-7] DEFINÍCIÓ (2S,5R,6R)-6-[[(2R)-2-Amino-2-(4-hidroxifenil)acetil]amino]-3,3-dimetil-7-oxo-4-tia-1-azabiciklo[3.2.0]heptán-2-
Amoxicillinum trihydricum Ph.Hg.VIII. Ph.Eur.7.6-1 01/2013:0260 AMOXICILLINUM TRIHYDRICUM Amoxicillin-trihidrát C 16 H 19 N 3 O 5 S.3H 2 O M r 419,4 [61336-70-7] DEFINÍCIÓ (2S,5R,6R)-6-[[(2R)-2-Amino-2-(4-hidroxifenil)acetil]amino]-3,3-dimetil-7-oxo-4-tia-1-azabiciklo[3.2.0]heptán-2-
(11) Lajstromszám: E 007 888 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007888T2! (19) HU (11) Lajstromszám: E 007 888 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 763701 (22) A bejelentés napja:
!HU000007888T2! (19) HU (11) Lajstromszám: E 007 888 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 763701 (22) A bejelentés napja:
(11) Lajstromszám: E 008 114 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000008114T2! (19) HU (11) Lajstromszám: E 008 114 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 764249 (22) A bejelentés napja:
!HU000008114T2! (19) HU (11) Lajstromszám: E 008 114 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 764249 (22) A bejelentés napja:
(11) Lajstromszám: E 004 765 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000476T2! (19) HU (11) Lajstromszám: E 004 76 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 744629 (22) A bejelentés napja:
!HU00000476T2! (19) HU (11) Lajstromszám: E 004 76 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 744629 (22) A bejelentés napja:
(11) Lajstromszám: E 005 864 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000864T2! (19) HU (11) Lajstromszám: E 00 864 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81166 (22) A bejelentés napja: 0.
!HU00000864T2! (19) HU (11) Lajstromszám: E 00 864 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 0 81166 (22) A bejelentés napja: 0.
(11) Lajstromszám: E 003 959 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000399T2! (19) HU (11) Lajstromszám: E 003 99 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 71434 (22) A bejelentés napja:
!HU00000399T2! (19) HU (11) Lajstromszám: E 003 99 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 71434 (22) A bejelentés napja:
(11) Lajstromszám: E 003 099 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU0000099T2! (19) HU (11) Lajstromszám: E 003 099 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 76424 (22) A bejelentés napja:
!HU0000099T2! (19) HU (11) Lajstromszám: E 003 099 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 76424 (22) A bejelentés napja:
(11) Lajstromszám: E 007 855 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007855T2! (19) HU (11) Lajstromszám: E 007 855 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 792252 (22) A bejelentés napja:
!HU000007855T2! (19) HU (11) Lajstromszám: E 007 855 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 792252 (22) A bejelentés napja:
ACIDUM ASCORBICUM. Aszkorbinsav
 01/2009:0253 javított 7.0 ACIDUM ASCORBICUM Aszkorbinsav C 6 H 8 O 6 M r 176,1 [50-81-7] DEFINÍCIÓ (5R)-5-[(1S)-1,2-Dihidroxietil]-3,4-dihidroxifurán-2(5H)-on. Tartalom: 99,0 100,5%. SAJÁTSÁGOK Küllem:
01/2009:0253 javított 7.0 ACIDUM ASCORBICUM Aszkorbinsav C 6 H 8 O 6 M r 176,1 [50-81-7] DEFINÍCIÓ (5R)-5-[(1S)-1,2-Dihidroxietil]-3,4-dihidroxifurán-2(5H)-on. Tartalom: 99,0 100,5%. SAJÁTSÁGOK Küllem:
