Alap szerves kémiai reakciók szisztematikus tárgyalása
|
|
|
- Benedek Juhász
- 6 évvel ezelőtt
- Látták:
Átírás
1 Alap szerves kémiai reakciók szisztematikus tárgyalása
2 A biokémia is a szerves molekulák kémiája Egy példa arra, hogy a szerves kémiai reakciók és az enzimkatalizált biokémiai reakciók hasonló alapelvek mentén szerveződnek, ám eltérő módon kiviteleződnek. a reakció célja: (mindkét esetben ugyanaz): redukáljuk a dihidrofolsavat tetrahidrofolsavvá. dihidrofolsav ( 2 F) 2 redukció tetrahidrofolsav ( 4 F) 2 C 2 C 2 C C C C C 2 C 2 C 2 C 2 C C C C gondok: - legyen szelektív a redukció: csak a pirazin gyűrűt érintse (dihidropirazin piperazin), (a pirimidin és a benzol gyűrűket ne telítsük) - legyen sztereoszelektív a redukció: cél csak az egyik diaszteromer előállítása, mert csak az hordoz biológia aktivitást. a termék (4F) jelentősége: - purin- és pirimidinvázas vegyületek, - egyes aminosavak bioszintéziséhez szükséges. (S) (S)
3 A klasszikus szerves kémiai megoldás: megjegyzés: a reakció során csak a dihidropirazin gyűrű redukálódott, de a hidrogénezéshez Pt katalizátor kell, és ez a redukció nem sztereoszelektív.
4 Az enzimatikus megoldás: A dihidrofolát-reduktáz (DFR, EC ) végzi a reakciót, amely enzim mind prokarióta, mind eukarióta sejtben életfontosságú és nélkülözhetetlen a normális anyagcseréhez. memo: ez az enzim a rákellenes és antibakteriális szerek célpontja. Számos hatóanyag, például a metotrexát és a trimetoprim ezt az enzimet gátolja (kiemelt gyógyászati jelentőségű). megoldás: az enzim és szubsztrát mellett kell még egy koenzim is: ez a ADP. nikotinsavamid-adenin-dinukleotidfoszfát (ADP röviden )
5 Az enzimatikus reakció, - amely során a dihidrofolsav redukálódik és - a koenzim (ADP) pedig oxidálódik dihidrofolsav ( 2 F) ADP () megjegyzés: a ADP itt hasonló szerepet tölt be, mint a klasszikus reakcióban a 2 /Pt heterogén fázisú katalizátor. A Pt szerepe hasonló a ADP-hez, hiszen hordozza és aktiválja a hidrogént. tetrahidrofolsav ( 4 F) ADP + ( + ) megjegyzés: A ADP nem-aromás (sp3-as C-atom), de a ADP(+) már aromás, s ezért stabilabb : ez a reakció hajtóereje!
6 Mind a sztereoszelektivitást, mind a reakció nagy sebességét a komponensek optimális térbeli pozicionálása biztosítja: ez megvalósul a fehérjében A s p 2 7 1) Asp- - és 3 + egyensúlyi rendszer kiegészül a dihidrofolsavval és a ADP-val. 2) xo-enol tautomerizációval aromássá válik az Agyűrű (extra stabilitás, mint a folyamat hajtóereje). Ezt hívják átprotonálódási lépésnek. 3) A víz protonvesztése (kék ) visszafordítja a tautomerizéciót és az aromatizálódást. A s p 2 7 A B á t p r o t o n á l ó d á s R 4) A kék hidrogének átmennek a B-gyűrűre, de eközben a ADP+ kialakul, amely során a nikotinamid gyűrűje aromássá válik, valamint a Asp27 ismét deprotonálódik. p r o - R - 2 R ' s z t e r e o s p e c i f i k u s á t a d á s
7 Mind a sztereoszelektivitást, mind a reakció nagy sebességét a komponensek optimális térbeli pozicionálása biztosítja: ez megvalósul a fehérjében A s p 2 7 A s p 2 7 A á t p r o t o n á l ó d á s A s z t e r e o s p e c i f i k u s á t a d á s B B R R p r o - R - p r o - R R ' R ' 1) Asp- - és 3 + egyensúlyi rendszer kiegészül a dihidrofolsavval és a ADP-val. 2) xo-enol tautomerizációval aromássá válik az A-gyűrű (extra stabilitás, mint a folyamat hajtóereje). Ezt hívják átprotonálódási lépésnek. 3) A víz protonvesztése (kék ) visszafordítja a tautomerizéciót és az aromatizálódást. 4) A kék -atomok átmennek a B-gyűrűre, de eközben a ADP+ kialakul, amely során a nikotinamid gyűrűje aromássá válik, valamint a Asp27 ismét deprotonálódik.
8 Mind a sztereoszelektivitást, mind a reakció nagy sebességét a komponensek optimális térbeli pozicionálása biztosítja: ez megvalósul a fehérjében A s p 2 7 A.. B R p r o - R R ' 1) Asp- - és 3 + egyensúlyi rendszer kiegészül a dihidrofolsavval és a ADP-val. 2) xo-enol tautomerizációval aromássá válik az A-gyűrű (extra stabilitás, mint a folyamat hajtóereje). Ezt hívják átprotonálódási lépésnek. A s p 2 7 A.. B R 2 p r o - R - R ' 3) A víz protonvesztése (kék ) visszafordítja a tautomerizéciót és az aromatizálódást. 4) A kék -atomok átmennek a B-gyűrűre, de eközben a ADP+ kialakul, amely során a nikotinamid gyűrűje aromássá válik, valamint a Asp27 ismét deprotonálódik.
9 1) Mind a sztereoszelektivitást, mind a reakció nagy sebességét a komponensek optimális térbeli pozicionálása biztosítja. 2) Mindez egy evolúciósan finomhangolt fehérjében optimálisan tud meg valósulni. Sawaya, M.R., Kraut, J. Biochemistry 36: (1997) dihidrofolsav ADP koenzim és szubsztrát optimális elhelyezkedése
10 A teljes folyamat kinetikája elemi lépésenként feltérképezett: E M -1 s s -1 E. 2 F 5 M -1 s s -1 E F Rövidítések: dihidrofolát-reduktáz (E) dihidrofolsav ( 2 F) tetrahidrofolsav ( 4 F) nikotinsavamid-adenin-dinukleotidfoszfát () nikotinsavamid-adenin-dinukleotidfoszfát oxidált formája ( + ) konklúzió: az enzimkatalizált reakció kémiája igen hasonló ahhoz mint amit a lombikban végzünk de, finomabban hangolt, gyorsabb és jobban kontrolált folyamat, viszont mindennek az az ára hogy komplexebb rendszert igényel. 3.5 s s -1 E. E.. 4 F E. 4 F M -1 s s -1 M -1 s -1 M -1 s -1 M -1 s s s -1 M -1 s s -1 5 M -1 s -1 E.. 2 F 0.6 s s -1 E F M -1 s s s -1 M -1 s -1 M -1 s -1 M -1 s -1 E E. + E F 300 s -1 6 s -1
11 memo: dihidrofolát reduktáz metotrexáttal együtt kristályosítva metotrexát ADP Bolin, J.T., Filman, D.J., Matthews, D.A., amlin, R.C., Kraut, J. J.Biol.Chem. 257: (1982)
12 Szerves kémiai alapreakciók I. Bevezető gondolatok 1. Funkciós csoportok Azonos funkciós csoportot tartalmazó molekulák rendelkeznek hasonló kémiai tulajdonságokkal. 2. Reakciótípusok 2 C hidroxil amino karbonil karboxil ciano Az elemi reakciók típusa kevés: - Szubsztitúció: a brómatomot helyettesítjük a hidroxilcsoporttal. - Addíció: brómatomokat adunk telítetlen kötésű szénatompárra. - Elimináció: egy hidrogénatomot és egy hidroxilcsoportot elvonunk a molekulából.
13 3. Kötések kialakítása és felbontása 3 C Br + 3 C + Br 4. A görbe nyíl jelentése 3 C Br 3 C A két atom (C és Br) között lévő kötés egy elektronpárt jelent. A görbe vonal azt mutatja, hogy a kötéshez az elektronpár honnan jön és hova tart. Br C 3 Br C3 + Br A kötéshez az elektronpár a hidroxidiontól jön, illetve a C- kötés heterolitikus bomlását követően a Br atomtörzséhez kapcsolódik. 5. Kötéspolaritás Az atomok Pauling-féle elektronegativitás értéke: K-héj e L-héj Li Be B C F e Így mivel a C 2.5 és a Br pedig 2.8, ezért a kötés a két atom között poláros jellegű lesz. jelölésmódok: C Br C Br C Br
14 6. Reagens típusok A) ukleofil (lat, nucleus `mag`) (gör, filosz `valamit kedvelő`) esettanulmány 1. Vegyünk egy viszonylagos elektronhiányos szénatomot pl.: 2. Ezt a C-atomot egy elektronban gazdag reagens fogja leginkább megtámadni pl.: Et EtS 2 3 Ezek a csoportok jellegzetesen bázisok és esetenként redukáló hatásukat egy elektronpár közösbeadásán keresztül fejtik ki: B) Elektrofil esettanulmány 1. Vegyünk egy elektronban viszonylag gazdag szénatomot pl.: 2 C C 2 2. továbbá egy elektronban szegény reagenst pl.: 2 Br Br 3 AlCl 3 Az utóbbi csoportok, jellegzetesen Lewis-savak és oxidáló hatásúak, tevékenységüket egy elektronpár elszívásán keresztül fejtik ki. C 2 C 2 + Br Br Br C 2 C 2 Br C Br C 3 Br C 3 + Br Megjegyzés : míg a Br 2 molekula külső héján összesen 14 közös elektron van, addig az 1,2- dibrometánban (2*8=) már 16 elektron van a 2 Br körül.
15 C) Gyök esettanulmány 1. vegyünk egy elektronszerkezetében kiegyensúlyozott molekulát (pl.: C 4 ), amellyel se egy nukleofil, se egy elektrofil nem tud eredményesen reagálni, 2. továbbá egy gyököt (pl.: Cl.) a végbemenő reakció során a párosítatlan elektronnal rendelkező klóratom reagál: 3 C + Cl Cl 3 C Cl + Cl fény Cl Cl Cl + Cl Megjegyzés : ha nincs foton, akkor nincs gyökképződés és akkor nincs reakció (avagy sötétben nincs semmi, de UV. fény hatására robban a gázkeverék.) UV. + C 4 + Cl 2 =
16 Egy gyökös reakció általában kevéssé szelektív: Pl.: lehet gyökösen, de lehet alkalmas katalizátorral is klórozni a toluolt: : 1) más és más lesz a termék, mert eltérő a klórozás 2 útja (más mechanizmusok): 2) A gyökös klórozás esetében jellegzetesen több terméket (keveréket) kapunk, a reakció nem szelektív, s ez általában nem szerencsés:. A molekulaszerkezet befolyásoló hatások: A) elektronos hatás B) sztérikus hatás (térhatás) esettanulmány : 3 C Br + 3 C + Br C 3 C 2 Br + C 3 C 2 + Br Megfigyelés : a második reakció 12 szer lassúbban megy végbe mint az első, de miért?
17 elektronos hatás: az etilcsoportban a metilcsoport elektronküldő hatása miatt a metiléncsoport szenének pozitív polarizáltsága csökken: kevésbé pozitív Me C 2 Br 3 C Br kék, zöld, sárga, piros pozitívabb sztérikus hatás: az etilcsoport nagyobb térigényű mint a metilcsoport
18 8. Az egyenletírás alapkövetelményei: A) tömeg megmaradás (mass balance) B) töltésmegmaradás (charge balance) C) spinállapot megmaradás (spin balance) A) 2 C C 2 + Br Br Br C 2 C 2 Br MW=28.05 MW= MW= C 3 Br + C 3 + Br MW=94.94 MW=17.01 MW=32.04 MW=79.90 a protonok hiánya nem zavaró C 3 C 2 2 C C 2 + B) MW=46.07 a proton csak katalizátor MW=28.05 MW=18.02 C) C 3 + Cl Cl Cl + doublett singlett doublett párosítatlen a zárt héj párosítatlen elektron elektron 3 C singlett zárt héj Cl
19 II. ukleofil szubsztitúció II/A. ukleofil szubsztitúció telített szénatomon Ruff-Csizmadia kérdés: egyformán befolyásolja-e a reagens és a szubsztrátum koncentrációja az eredményes reakciót? módszer: megfigyeljük a résztvevő molekulák koncentrációinak alakulását t-függvényében. tapasztalat: igen, mind a reagens ( - ), mind a szubsztrátum (C 3 Br) moláris koncentrációja befolyásolja a reakciósebességet. A keletkezett anyag C 3 knoc. változása az időben: d[c 3 ]/dt = k[c 3 Br ][ - ] azaz d[x]/dt = k[a][b] = k[a] 2 ez egy másodrendű reakció sebességi egyenlete, ahol k a reakció sebességi együtthatója Általánosítás: S 2 bimolekuláris szubsztitúció nukleofil memo: a kémiai reakció előrehaladását annak sebességével (v) mérjük, ahol a jelen esetben v = d[a]/dt = d[b]/dt = + d[x]/dt, azaz v a koncentrációk időegység alatti megváltozása. (Azért van a előjel az A és a B esetében, mert azok koncentrációja (mind A-nak, mind B-nek) csökken az időben (elfogynak), ám a sebesség definíciószerűen pozitív szám kell hogy legyen.) Ruff-Csizmadia 75- memo: kinematikában a haladás ds/dt, reakciókinetikában ugyanez d[konc.]/dt. A sebesség dimenziója [konc.] * idő 1 azaz, [mol/dm 3 ] * s 1. (a k dimenziója a sebességi egyenlettől függ!)
20 Az S 2 reakciómechanizmus részleteinek leírása kérdés: hogyan rendeződnek át kötések a reakció során? A hidroxidion egy elektronpárt küld a pozitívan polározott szénatom felé (az elektron ha lehet akkor kiterjed ), amely kiterjedés az elektorsztatikának megfelelő orientációjú Az átmeneti állapotban az -C kötés részlegesen kialakult, míg a C-Br kötés részlegesen elhasadt. (A C- atom konfigurációja az inverzió felé tart.) Az -C kötés kialakult, a C-Br kötés megszűnt. memo: A C-atom invertálódott. Solomons 237 memo: ha a kiindulási anyag királis és optikailag tiszta, akkor az S 2 reakció során inverzió történik nem azonos a 2 sztereokémia ( tükörképi párok) 3
21 kérdés: hogyan csökken az A és B kiindulási anyagok koncentrációja az időben? válasz: 1/[A]= kt +1/[A] 0 illetve 1/[B]= kt +1/[B] 0 függvények szerint! De miért is? levezetés: Me konc. képződési sebessége azonos a Me-Br konc. fogyási sebességével s ezért d[x]/dt = d[a]/dt Továbbá korábban leszögeztük hogy d[x]/dt = k[a] 2. E 2 egyenlet összevonásával kapjuk a d[a]/dt = k[a] 2 (ez a másodrendű reakció integrált sebességi egyenlete) d[a]/[a] 2 = kdt amelynek integrálalakja [A]0 [A] d[a]/[a] 2 = k [0] [t] dt a kiindulási koncentráció: [A] 0 =[ - ] 0 [A] [t] 1/[A] [A]0 = k [t] [0] amely azonos az 1/[A] 1/[A] 0 = kt egyenlettel Tehát : 1/[A]= kt +1/[A] 0 f(t)=mt+b egyenes egyenlete azaz ha [A] 0 =1 (tehát egységnyi volt a kiindulási Me koncentráció), akkor a 0 t idő intervallumra a fenti ábrát kapjuk, ahonnan a meredekség alapján meghatározhatjuk a reakció sebességi együtthatóját. kérdés: hogyan nő a keletkezett anyag (pl. metanol) koncentrációja az időben? levezetés: mivel a Me-Br [B] és a Me [X] koncentrációjának összege a reakció minden pillanatában a Me-Br kiindulási koncentrációjával azonos, azaz a [B] 0 al, ezért [B] + [X] = [B] 0 ahonnan kifejezve [B] = [B] 0 [X]. Mivel a korábbiak értelmében [B] = [A], ezért az 1/[B]= kt +1/[B] 0 egyenletet kapjuk ahová behelyettesítve a [B] = [B] 0 [X] az alábbi kifejezéshez jutunk: 1/([B] 0 [X]) = kt +1/[B] 0 ahonnan [X]-et kifejezve kapjuk: [X]= [B] 0 1/(kt +1/[B] 0 ), ha [B] 0 = 1 akkor [X]= 1 1/(kt) /[A] ,8 0,6 0,4 0,2 0 1/[A] t [A] [X] t
22 A felezési időben (τ) az az idő amely alatt a kiindulási anyag koncentrációja a kezdeti érték felére csökken, tehát [A]= [A] 0 /2 behelyettesítve a 1/[A]= kt +1/[A] 0 kapjuk : 2/[A] 0 = kt +1/[A] 0 ahol t = t azaz 2/[A] 0 = kt +1/[A] 0 Összevonás után: t =1/k[A] 0 tehát a felezési idő mind a sebességi együttható, mind a kezdeti koncentráció reciprokával arányos. [A 1 ] 0 [A 2 ] 0 t 1 t 2 Ebből következik hogy: 1) Minél nagyobb a kezdeti koncentráció (azaz [A] 0 ), annál gyorsabb a reakció (v = d[a]/dt ), s ezért annál hamarabb érünk a reakció félidejéhez. A vas oxidációja (Fe +2 Fe()2 majd 2 hatására Fe23) (rozsdásodás) kis reakciósebességű, míg a cellulóz égése nagy reakciósebességű oxidáció. 2) Ugyanolyan kezdeti koncentráció [A] 0 esetén ha k értéke nagyobb, akkor t kisebb. Mondjuk pl. ha ugyanazt a reakciót két eltérő oldószerben valósítjuk meg.
23 memo: a S 2 reakciómechanizmus részleteinek leírása: C Cl C Cl C + Cl A szabadentalpia diagram: DG Solomons 237 kérdés: végbe megy-e a reakció, avagy mekkora a K eq értéke az Arrhenius egyenlet alapján? DG o = 100 kj/mol (szabadentalpia) átmeneti állapot DG # (aktiválási szabadentalpia) reakciókoordináta [X] [Y] K eq = = [A] [B] k 1 k -1 DG 0 = -100 kj.mol -1, ha T=333 K (60 C) DG o = RT logk eq logk eq = DG o /2.303 RT = ( 100 kj/mol) kj/molk 333K = 15.7 konklúzió: mivel DG kellően nagy negatív szám ( 100 kj/mol) és ezért az egyensúlyi állandó logaritmusa nagy pozitív szám (15.7), s ezért a reakció teljesen végbemegy.
24
25
26
27 kérdés: ugyanaz marad-e a mechanizmus, ha a metilcsoport egyik hidrogénjét egy metilcsoportra cseréljük? C 3 2 C Br + C Br módszer: megfigyeljük a résztvevő molekulák koncentrációinak alakulását az idő függvényében. tapasztalat: bár lassul a reakció, de mind a reagens ( - ) mind a szubsztrát (C 2 5 Br) moláris koncentrációja befolyásolja a reakciósebességet. Azaz továbbra is d[c 2 5 ]/dt = k[c 2 5 Br][ - ] (másodrendű reakció sebességi egyenlete egy másik k sebességi együtthatóval) válasz: igen, ez is S 2 reakció. további megfigyelés: k relatív C Br MeC 2 Br Me 2 C Br
28 DG = D TDS D ha a reakció során stabilabb kötések jönnek létre, akkor D negatív és a folyamat exoterm. DS ha a molekuláris rendszer rendezettsége nő, akkor a rendszer entrópiája csökken. memo: DG az entalpia (azaz D) szabadon felhasználható része. kérdés: milyen hőmérsékleten megy végbe eredményesen a reakció? Ruff-Csiz. 59 DG DG o = 100 kj/mol (szabadentalpia) memo: ha DG # < 84 kj/mol akkor már szobahőmérsékleten is megy a reakció DG # =103 kj/mol (aktiválási szabadentalpia) memo: Vegyük észre, hogy a reakció sebességi együtthatója az aktiválási szabentalpiától exponenciálisan függvénye (k 0 az abszolút reakció sebességi együttható = s -1 [25 o C-on]). Tehát egy elsőrendű reakcióra (lásd később pl. S 1 reakció) a k = exp(-37.22) s -1 azaz k = s 1. A reakció felezési ideje: τ = ln2/k τ =1603s ~27perc Tehát a reakció 27 perc alatt már félig végbement. reakciókoordináta + C 3 Cl C 3 + Cl DG # = 103 kjmol -1 ha T=333 K Tehát a metilklorid + hidroxidion reakció (DG # = 103 kj/mol) szobahőmérsékleten nem megy végbe, mert kevés az eredményes ütközések száma, de 60 o C-on (333 K) már kellően magas az eredményes ütközések száma és a reakció végbemegy: k k = k 0 exp( DG # /RT)
29 kérdés: ugyanez marad-e a mechanizmus, ha akár az összes hidrogént lecseréljük metilcsoportokra? megfigyelés: k relatív ! 3 C Br MeC 2 Br Me 2 C Br Me 3 C Br válasz: nem lehet ugyanaz a mechanizmus a t Bu Br esetében mint a korábban leírt S 2, noha marad a szubsztitúció és a nukleofil támadás. kérdés: egyformán befolyásolja-e mind a reagens mind a szubsztrát koncentrációja az eredményes reakciót? C 3 3 C C Br C Br tapasztalat: C 3 míg a reaktáns (C 4 9 Br) moláris koncentrációja befolyásolja a reakciósebességet, az nem függ a reagens ( - ) moláris koncentrációjától. Azaz : d[c 4 9 ]/dt = k[c 4 9 Br ] elsőrendű reakció sebességi egyenlete, ahol k a sebességi együttható válasz: nem a reakciósebesség csak a reaktáns (C 4 9 Br) koncentrációjától függ. Általánosítás: S 1 monomolekuláris szubsztitúció nukleofil
30 S 1 reakció mechanizmusa: C 3 C 3 C 3 - C Cl C 3 C3 C C 3 átmeneti termék C 3 C 3 + Cl C C 3 C 3 3 C 3 C C A poláris oldószer által segített klóratom eltávolodik a központi szénatomtól, a kovalens kötést heterlitikusan elhasítva. Az átmeneti termék létrejötte, mely során a karbokation kialakul (sp 2 -es C-atom), ez a reakció lassú lépése. A hidroxidion egy elektronpárt küld a karbokation felé. Az -C kötés kialakult. (a a C-atom királis volt, akkor a termék racemát.) Solomons 245 memo: a tisztán S 2 mechanizmusú reakció ha királis szénen történik, akkor az inverzióhoz vezet. a tisztán S 1 mechanizmusú reakció ha királis szénen történik, akkor az racemátot eredményez.
31 S 1 reakció mechanizmusa: DG DG # (1) (aktiválási szabadentalpia) DG # (2) (aktiválási szabadentalpia) DG o (szabadentalpia) reakciókoordináta C 3 C 3 C Br 3 C C 3 C C 3 Br lassú lépés C 3 C 3 C C(C 3 ) 3 nagyon gyors lépés 3 C C 3 megjegyzés: a nukleofil szubsztitúcióra bemutatott két mechanizmus (S 1 és S 2) a két szélsőség. Tipikusan S 1 a t Bu Br és S 2 a Me Br hidrolízise, ám számos (pl. szekunder) alkil-halogenid esetében vegyes mechanizmust észlelhetünk.
32 S 1 beceneve: reakció a csináld magad mozgalom keretében kérdés: hogyan képes a t Bu Br heterolitikusan bomlani és hogyan stabilizálódnak a visszamaradó ionok? Me 3 C Br Me 3 C Br Me 3 C Br Me Me C Br a megnövekedett kötéshossz növeli a részleges töltéseket, a kialakuló karbokationt stabilizálja a metilcsoportok elektronküldő (+I) effektusa Me 109 o Me C Me Me Br 120 o Me Me C Me Br a síkalkatú karbokationban a metilcsoportok jobban elférnek mint a tetraéderes tbu Br - ban, ahol a nagy térigényű -Br torzító hatása jelentős. kérdés: hogyan hat az alkilhalogenid szerkezete az S reakció mechanizmusára? tapasztalat: bonyolultabb (esetleg elágazó) alkilcsoport esetén az S 1 valószínűbb, különösen ha a karbokationt valamilyen hatás stabilizálja: Me 3 C Br Me 3 C Br k = 1 (C 6 5 ) 3 C Br (C 6 5 ) 3 C Br k 10 8 kérdés: miért gyorsabb ~100 milliószor a trifenilmetil-bromid, mint a terc.-butil-bromid S reakciója?
33 válasz: mert a 3 fenilcsoport eredményesebben stabilizálja a karbokationt: A pozitív töltés delokalizációját leíró komboszerkezet atár- vagy kanonikus-szerkezetek: < EPS < vörös, sárga, zöld, kék, mélykék C C C C C C C
34 memo.: legyen a molekula kiindulási koncentrációja: [C 4 9 Br] 0 d[x]/dt = k[a] mivel A X ezért d[x]/dt = d[a]/dt d[a]/dt = k[a] (ez az elsőrendű reakció integrált sebességi egyenlete) d[a]/[a] = kdt amelynek integrálalakja [A]0 [A] d[a]/[a] = k [0] [t] dt [A] [t] ln[a] [A]0 = k [t] [0] amely azonos az t ln(a) ln[a] ln[a 0 ] = kt avagy az ln([a]/[a 0 ]) = kt egyenlettel, amely exponenciális alakja : [A]=[A 0 ]exp( kt) Azaz az ha A 0 =1 és 0 t akkor: ,8 0,6 ln[a] [A] [X] A felezési időben (τ) [A]=[A] 0 /2 azaz ln{([a 0 ]/2)/[A 0 ]} = kt az alapegyenletünk: t =ln2/k. memo: ln(1/2)=ln(2 1 )= ln(2) tehát a felezési idő csak a sebességi együttható reciprokával arányos. 0,4 0, t
35 Poláris protikus oldószerek: ldószerhatás 0,39 0,01 0,01-0,49 0,11 0,11-0,28-0,60 0,18 0,39 0,11 0,01-0,34 0,37-0,61 0,07 0,04 0,30 0,35-0,24 0,07-0,72-0,04-0,04 0,07 0,36 0,36
36 1. kérdés: hogyan hat az alkil-halogenidek S 2 reakcióinak sebességére az oldószer milyensége? Cl ldószerhatás k C 3 I Cl C 3 + I megfigyelés: a nukleofil szolvatációjának csökkenése gyorsítja a reakciót: k relatív * C C C 3 C C 3 C 3 C 3 nincs Cl - szolvatáció és Me Me Cl Me Me Me C C Me Cl Me C C Me magyarázat: a nukleofil (Cl ) szolvatáltsága egyre csökken: (Me>CMe>CMe 2 ) a gyengülő -hidak miatt, s ezért reaktivitása egyre nő. A CMe 2 (DMF) csak -híd akceptor; nincs proton donor tulajdonsága.
37 2. kérdés: ldószerhatás hogyan hat az alkil-halogenidek S 1 reakcióinak sebességére az oldószer milyensége? lassú Me 3 C Br Me 3 C Br megfigyelés: az oldószer polaritásának növekedése (hatékonyabb szolvatáció) gyorsítja a reakciót k relatív Et Et/ 2 [1:1] lassú Me 3 C Br Me R 3 C Br Br magyarázat: az S 1 reakció eredményességét meghatározó csináld magad elkülönülési lépést két módon is segíti a poláris oldószer (pl. víz): 1) a bromidaniont a + polaritású hidrogénjével a víz, 2) az alkilkationt a polaritású oxigénjével stabilizálja a víz.
38 3. kérdés: ogyan hat a belépőcsoport (a nukleofil) bázicitása az S reakció sebességére? memo.: bázicitás: proton irányába kifejtett elektronpár-donálási képesség nukleofilitás: szén vagy más atom irányába kifejtett elektronpár donálási képesség tapasztalat: bázicitás és nukleofilitás gyakran párhuzamosan változik. Tekintsük az alábbi oxigén kulcsatomot tartalmazó vegyületsorozatot (etoxid, fenoxid, acetát, nitrát): Et > C 6 5 ~ > MeC 2 > 3 legerősebb bázis legerősebb nukleofil leggyengébb bázis leggyengébb nukleofil 0,04 válasz: ha a vegyületsorozatban azonos atomtípus az elektronpár-donor (jelen esetben az - ), akkor minél jobb bázis annál jobb nukleofil is a molekula ~ atomi töltéssel korreláltatható. -0,04-0,04-0,15 0,63-0,25-0,88-0,25 0,08 0,05-0,05-0,34-0,05 0,05 0,58 0,09-0,40-0,40 0,09-0,71 0,01 0,01-0,24 0,01-0,75-0,63-0,63 0,73-0,75-0,63 0,89
39 4. kérdés: ogyan hat a belépőcsoport (a nukleofil) bázicitása az S reakció sebességére változó elektrondonor esetén? memo: a nukleofil erősség az S 2 reakció sebessége miatt fontos, ám az S 1 mechanizmus esetén annak sebességére nem hat. tapasztalat: a bázicitás és a nukleofilitás nem párhuzamosan változik. Tekintsük az alábbi vegyületsorozatot: bázis erősség: nukleofilitási képesség: magyarázat: minél nagyobb az elektronpárt donáló atom rádiusza, annál lazábban kötött az elektronpár. Ezért az jobban polarizálható, s így könnyebben alakítanak ki kötést. szolvatációs effektus memo: lehetnek : vannak semleges vegyületek, amelyekben van elektronpárt donáló atom, így ezek is jó nukleofilok 3 R Br 3 R + Br
40 5. kérdés: hogyan hat az Y távozó csoport bázicitása az S reakció sebességére? + R Y R + Y tapasztalat: mind S 2 mind S 1 mechanizmus esetén a távozó csoport bázicitása erősen befolyásolja a reakciósebességet. bázicitás erõssége távozási képesség R I R Br R Cl R F magyarázat: minél erősebb a bázis (pl. F > Cl >Br >J ), annál rosszabb távozócsoport az Y-csoport, s így annál lassabb a reakció. memo: Ezért is nem megy a következő reakció: memo: Br + R Br R + C kötés nagyon erős. o meg azért sem megy ez a reakció, mert a hidrid anion nagyon reaktív. A távozó csoport célszerű módosítása megoldhatja ezt a problémát: R- rossz távozó csoport mert erős bázis R- 2 2 jó távozó csoport mert gyenge bázis
41 II/B. ukleofil subsztitúció telítetlen szénatomon kérdés: nem gátolja-e a nukleofil szubsztitúciót ha azt egy telítetlen pl. sp 2 szénen kíséreljük meg? memo.: - egy telítetlen szénatom jellegzetesen elektrondús molekularészlet, - a C Y (ahol Y a feltételezett távozó csoport) kötéshossz lerövidül Pl.: Cl Cl C C 2 0,04 < EPS < + 0,04 1. várt tapasztalat: a klórbenzol vagy a vinil-klorid S reakciója - nukleofillal csak 200 o C feletti hőmérsékleten megy végbe, míg egyszerű alkil-halogenidek esetében ugyanez a reakció már szobahőmérsékleten is lezajlik. következtetés: tehát a szubsztrátum kulcsatomjának fokozott -elektron-gazdagsága rossz.
42 kérdés: hogyan csökkenthető egy telítetlen szén körül az elektronsűrűség? memo: az - 2 -csoport elektronvonzó tulajdonságú tapasztalat: nitroklórbenzolok esetén a reaktivitás így fokozódik: Cl Cl Cl Cl Cl Mulliken töltések: a kiszemelt C atomon csökken az elektronsűrűség: Mind a reagens ( - ) mind a reaktáns (Ar Cl) moláris koncentrációja befolyásolja a reakciósebességet. Azaz d[ar ]/dt = k[ar Cl][ - ] másodrendű reakció sebességi egyenlete ahol k a sebességi együttható memo.: -ellentétben az analóg alifás reakcióval, aromás S reakció esetén a távozó csoport milyenségének más szerepe van: pl. R I gyorsabban reagál mint R F, de Ar I lassabb mint Ar F
43 kérdés: Lehet-e ennek ismeretében az aromás esetben is csupán egyetlen lépés az S 2 reakció? S 2 alifás S 2 aromás R al R al R + al memo.: Alifás esetben (R X) az S 2 reakció egyetlen átmeneti állapoton átvezető lépés. válasz: em egyetlen lépés az aromás S 2 reakció. A negatív töltésű szigmakomplex (intermedier vagy köztitermék) kialakulása a reakció sebességmeghatározó lépése. A nitrocsoport szerepe kettős: 1. elszívja a -elektronokat a C X szénről, növelve annak részleges pozitív jellegét, segítve a nukleofil támadását, 2. delokalizáció révén stabilizálja a szigma-komplex negatív töltését. S 2 aromás σ-komplexek + Cl Cl Cl Cl Cl lassú gyors 2 2
44 A szigma-komplex egyes esetekben izolálható, pl.: Me Et Me Et 2 2 Et K 2 Me K 2 2 K
45 2. em várt tapasztalat: ha a klórbenzol S reakciójában a nukleofilt lecseréljük ( ), akkor a reakció már 33 o C -on is végbemegy. (A reakciót folyékony ammóniában kivitelezzük, innen a 33 o C.) memo.: Emlékezzünk arra hogy klórbenzol S reakciója - nukleofillal csak 200 o C feletti őmérsékleten következett be. Cl 2 megfigyelés: o C folyékony 3 + Cl magyarázathoz vezető út: Cl folyékony 3 +? -33 o C Me Me Me várt p-aminotoluol 38% nem várt m-aminotoluol 62%
46 memo.: ez a szubsztitúciós reakció valójában Meegy elimináció és egy addíció Me elemi lépés együttese Me (E + Ad). Cl Cl köztitermék Me Me Me Me 38% 62% Me vagy: Me 38% 62% Me 2. memo: az -nál nem sokkal jobb nukleofil az 2, ám az utóbbi sokkal erősebb bázis mint a hidroxid anion!
47 A hármas kötés sp 2 hibridállapotú C atomok közt jön létre nem igazi a 2. kötés memo.: az orto-klórtoluol esetében is megy a reakció és szintén két terméket kapunk: 2 Me Cl 2 / 3 Me 45% Cl Me Me 2 / 3 2 / 3 Me 2 de: 55% memo: ha a távozó csoporthoz viszonyítva mindkét orto helyzet már szubsztituált, azaz nincs atom amit le tud szakítani a bázis, akkor nem megy a reakció.
48 Összegzés és kitekintés eddig volt: ukleofil szubsztitúció (telített és telítetlen szénatomokon alifás illetve aromás/kettős kötéses rendszerek) nukleofil távozó-csoport nukleofil távozó-csoport + távozó-csoport nukleofil távozó-csoport nukleofil szolvatációs effektus: mechanizmusfüggő nukleofil: általában negatív töltésű (kivétel: pl. 3 ) nukleofil erősség: töltés, polarizálhatóság, szolvatáltság mértékének függvénye távozási hajlandóság: bázicitás növekedésével csökken most jön: Elektrofil szubsztitúció elektrofil: pozitív töltésű vagy semleges távozó csoport: általában a + E + R E R +
49 Az elektrofil reagensek elektronhiányos vegyületek, melyek gyakran pozitív töltést hordoznak 2 Br Br 3 AlCl 3
50 II. Elektrofil szubsztitúció Ruff-Csizmadia II/A Elektrofil szubsztitúció telített szénatomon kérdés: az S reakciók analógiájára lehet-e S E reakciót kivitelezni? válasz: - a sikeres reakció esetén az Y R -kötés heterolitikusan bomlik, a C-atomon visszahagyva az elektronpárt. Ez a reakció csak akkor kivitelezhető, ha Y elektronegativitása kisebb mint a szénatomé! - a tehát Y=, vagy halogén (F, Cl, Br, I) atom, akkor ez a feltétel nem teljesül, s az S E reakció nem mehet végbe. - Fémorganikus molekula esetén viszont kivitelezhető az S E reakció a szén-centrumon, mivel itt a Y elektronegativitása tényleg kisebb mint a szénatomé. Fémorganikus vegyületek: fém-c kötés (M-C) tartalmaznak, míg a fém pozitív, addig a C-atom negatív polározottságú
51 Fémorganikus vegyületek:
52 Fémorganikus vegyületek: 1760: Louis Claude Cadet de Gassicourt kakodil-oxid előállítása 4 KC 3 C + As 2 3 As 2 (C 3 ) K 2 C 3 + C : Kémiai obel díj: François Auguste Victor Grignard "for the discovery of the so-called Grignard reagent, which in recent years has greatly advanced the progress of organic chemistry" R 1 -Br + Mg 2005: Kémiai obel díj: Yves Chauvin, Robert. Grubbs and Richard R. Schrock "for the development of the metathesis method in organic synthesis"
53 II. Elektrofil szubsztitúció II/A Elektrofil szubsztitúció telített szénatomon S E 2 B r g R B r B r R B r + g B r 2 s - B u S n R 3 B r B r s - B u B r + S n R 3 B r elektronegativitás C 2,55 g 2,00 Sn 1,96 távozó csoport (gbr +, SnR ) 3+, + ) elektrofil reagens (Br 2 (valójában Br + )) S E 1 3 C C C 3 3 C C C B r b á z i s k a t a l. B r 3 C C C C C C 2 B r + B r 3 C C C 3 3 C C C 2 jó erős bázis: bázis pl. LDA (lítium-diizopropil-amid) 3 C C C C C C 2 Li + (C 3 ) 2 C--C(C 3 ) 2
54 II/B Elektrofil subsztitúció telítetlen szénatomon kérdés: megoldható-e egy S E reakció telítetlen szénen? pl: tapasztalat: ( + -t cserélünk 2+ -ra (nitrónium kation): S E ) magyarázat: c s a k c c. 3 n e m m e g y s z á m o t t e v Ő m ó d o n a r e a k c i ó n i n c s t e r m é k S 4 pk a 2 S c s a k c c. 2 S S 4 c c S 4 c c. 2 S S 4 megjegyzés: a nitrónium kation ( 2+ ) kiváló elektrofil amely pl BF 4 só formájában is felhasználható. b r u t t ó r e a k c i ó e g y e n l e t : S S S 4
55 kérdés: mi lehet ennek az S E reakciónak mechanizmusa ( 2+ BF4 -et használva + 2 forrásként)? módszer: megfigyeljük a résztvevő molekulák koncentrációinak alakulását az idő függvényében. tapasztalat: mind a reagens ( + 2 ), mind a szubsztrát (Ar ) moláris koncentrációja befolyásolja a reakciósebességet, azaz a reakciósebesség (a termék koncentrációjának időbeli változása): d[ar 2 ]/dt = k[ 2+ ][Ar - ]. másodrendű reakció sebességi egyenlet, ahol k a sebességi együttható válasz: bimolekulás azaz S E 2. kérdés: melyik az alábbi reakciómechanizmusok közül (1, 2 vagy 3) a legvalószínűbb? + 2 1: 2 + 1) Egy lépés 2) Két lépés, ahol az első a seb. meghatározó 3) Két lépés, ahol a második a seb. meghatározó + 2 2: lassú 2 gyors 2 + -komplex 3: 2 2 memo: a lassú a sebességmeghatározó lépés. + 2 gyors lassú +
56 módszer: kémiai alap: megfigyelés: kinetikus izotóp effektus azonos molekuláris környezetben a C D kötés erősebb mint a C kötés, ezért az előbbi nehezebben hasad. mind a benzol mind a perdeuterobenzol esetében ugyanolyan gyors a reakció.
57 módszer: kémiai alap: megfigyelés: kinetikus izotóp effektus azonos molekuláris környezetben a C D kötés erősebb mint a C kötés, ezért az előbbi nehezebben hasad. mind a benzol mind a perdeuterobenzol esetében ugyanolyan gyors a reakció. 1: : lassú gyors + 3: gyors lassú + következtetés: válasz: memo.: tehát nem a C kötés elhasadása a sebességmeghatározó lépés, ezért a mind a 3-as mind az 1-es reakció utakat ki lehet zárni. (Mivel mindkét kizárt esetben a sebesség meghatározó lépés tartalmazza a C kötés hasadását.) a 2-es mechanizmus a valószínűsíthető út, itt az első lépés során ugyanis nincs C- kötéshasadás. Az elektrofil támadása és a szigma-komplex kialakulása a sebességmeghatározó lépés. mindez nem bizonyítja hogy maximum két lépésben játszódik le a reakció.
58 memo: vegyük észre, hogy a -komplex kialakulása megbontotta a -szextettet! Az arénium kation továbbalakulása elvileg lehetne egy addíciós lépés: - nem a proton távozik (ahogy azt már bemutattuk), - hanem a hidrogénszulfát anion lép be a pozitívan töltött szénre. de: ez nem így van: nincs addíció! (S 4 - túl jó távozócsoport). (memo: akkor van S 4 a reakciótérben ha a nitrálást nitrálósavval végezzük) szubsztitúció -komplex 2 + S 4 S 3 addíció
59 kérdés: hasonló S E 2 reakció mechanizmussal lehet-e más szubsztituenst is bevinni az aromás gyűrűre? igen, pl. halogénezés válasz: A halogénezés: Br Br FeBr 3 Br Br FeBr 3 δ- Br Br FeBr3 Br Br memo: memo: FeBr 4 FeBr 3 Br a megfelelő Lewis-savval (FeBr 3 ) polarizált brómmolekula pozitív fele ugyanazt a szerepet tölti be mint a nitrónium kation a nitrálás során. (Más Lewis-sav is alkalmazható pl. AlCl 3.) 1) A benzol esetében a Br 2 önmagában (Lewis-sav nélkül) nem elég elektrofil, de fenol esetében már igen: Br 2 Br Br 2 2) F 2 -el (Lewis-sav jelenlétében) túlságosan hevesen, míg I 2 val nem megy a reakció. Br
60 kérdés: lehet-e S E 2 reakcióval alkilcsoportot bevinni? válasz: R Cl igen: Friedel Crafts-alkilezési reakció a már önmagában is polarizált alkilhalogenid Lewis-sav hatására elegendően erős elektrofil az S E 2 reakcióhoz. δ- R Cl AlCl3 R R Charles Friedel James Mason Crafts problémák: túl-alkileződés alkil-csoport átrendeződés AlCl 4 Cl + AlCl 3 Memo: ilyen Friedel Crafts-alkilezés során állították elő izolálható -komplexet (láh és Kuhn, 1958). narancssárga stabil -komplex
61 kérdés: lehet-e S E 2 reakcióval acilcsoportot bevinni? válasz: igen: Friedel Crafts-acilezési reakció a már önmagában is polarizált acil-halogenid karbonilcsoportjának szénatomja Lewis-sav hatására tovább polarizálódik és így elegendően erős elektrofil lesz egy S E 2 reakcióhoz. p o l a r i z á l t k o m p l e x i o n p á r R C δ- C l A l C l 3 R C A l C l 4 R C R C C l A l C l 3 + C l oleum 2 2 S 4 S S S 4 igen: a kéntrioxid S elegendően 3 + erős 3 elektrofil + Segy 4 S E 2 reakcióhoz. 2 2 S 4 S S + S 4 S S S 3 S 3 S S 3 S 3 - S S 3 S 3 S 3 - kérdés: lehet-e S E 2 reakcióval szulfonálni? válasz: S 3 -
62 kérdés: hová megy az új szubsztituens ha már van egy szubsztituens (vagy több) az aromás gyűrűn? orto Y orto? meta meta para Válasz: az Y szubsztituenstől függ, és a -komplex töltéseloszlásától: elektronküldő szubsztituens (-C 3 ): para orto meta C ová kerül a pozitív töltés? relatív energia: 0.0 kj/mol 5.0 kj/mol 20.4 kj/mol
63 kérdés: hová megy egy szubsztituens ha már van egy (vagy több) az aromás gyűrűn? orto Y orto? meta meta para Válasz: az Y szubsztituenstől függ, és a -komplex töltéseloszlásától: 0.14 kérdés: ol lokalizálódik a +1 pozitív töltés? elektronvonzó szubsztituens (- 2 ): para orto meta C relatív energia: 9.3 kj/mol 5.2 kj/mol 0.0 kj/mol
64 tapasztalat: Y: irányításának helye elektronküldő orto/para C 3, R 2, R 2 Y elektronvonzó meta R C, RC C 2, C 2 R, S 3 magyarázat: -komplex határszerkezeteit kell megvizsgálni: CF 3, CCl 3 o-támadás p-támadás m-támadás Y Y Y 2 2 Y Y Y Y Y Y 2 megoldás: mely határszerkezet esetében képes az elektronküldő szubsztituens stabilizálni a - komplexet? A két kiemelt határszerkezet esetében erre lehetőség nyílik. memo: Az irányítás általában nem kizárólagos, csak a szelektivitást fokozza
65 kérdés: hogyan képes pl. a metil ( Y= C 3 ) vagy a metoxi ( Y= C 3 ) szubsztituens a két kiemelt határszerkezeten keresztül stabilizálni a -komplexet, s így aktiválni valamint orto-, illetve para- helyzetbe irányítani az új szubsztituenst? válasz: - az Y elektronküldő hatása révén, - további delokalizációs lehetőség biztosításával: Y= C 3 C 3 C 3 C 3 C C 3 o-támadás p -támadás C 3 C itt csak elektronküldő hatás itt elektronküldő és delokalizációs hatások együttese magyarázat: Az S E 2 aromás reakció sebességmeghatározó lépése a -komplex kialakulása, mely folyamatot gyorsítják és szelektívebbé teszik a stabilizált -komplexek.
66 kérdés: hogyan magyarázzuk hogy az elektronvonzó szubsztituensek (Y= R 3+, 2 ) dezaktiválnak és meta- helyzetbe irányítják az új szubsztituenst? megoldás: ugyanazon két határszerkezet megvizsgálásával mint az előbb: Y= R R 3 o-támadás tényleges pozitív töltés R formális pozitív töltés p-támadás 2 2 magyarázat: a -komplex pozitív töltése és az Y-szubsztituens pozitív töltése (formális vagy valós) destabilizálják mindkét határszerkezetet, s ezért nem kapunk se orto-, se para-terméket. memo: Jobb híján a meta termék dúsul fel. Ez az okfejtés minden elektronvonzó Y esetén igaz, akár pozitívan töltött akár nem.
67 kérdés: megfigyelés: igen Y: % orto- % para- C C 2 C C(C 3 ) C(C 3 ) befolyásolja-e az Y-mérete az orto:para termékarányt? magyarázat: sztérikus gátlás (Az Y növekvő mérete miatt az új szubsztituens nem fér az orto-helyzetez.) kérdés: megfigyelés: igen E+: % orto- % para- Cl Br S befolyásolja-e az E + -mérete az orto:para termékarányt? magyarázat: sztérikus gátlás (Az E + növekvő mérete miatt nem fér az orto-pozícióhoz.) kérdés: egy korábban bevitt szubsztituens el tud-e távozni az aromás gyűrűről? Y Y E E árnyékolás mértéke megfigyelés: igen ipso-szubsztitúció.ha Y jó távozó csoport, pl: Y + C(C 3 ) 2 + S 3 E - Y S 3 - S S 4
68 kérdés: mitől függ a sebességmeghatározó lépés gyorsasága, a -komplex kialakulása? megfigyelés: egyes Y-csoportok aktiválják, mások dezaktiválják az S E 2-t. memo: Már láttuk az irányításnál hogy miért aktivál a Me vagy Me és miért dezaktivál az R 3 + vagy 2. C(C 3 ) 2 C(C 3 ) 2 C(C 3 ) C(C 3 ) 2 + C(C 3 ) 2 C(C 3 ) : 5
69 Összefoglaló S S E A reakció- centrum szenének típusa telített : sp 3 (R) telítetlen, aromás: sp 2 (Φ) telített: sp 3 (R) telítetlen, aromás: sp 2 (Φ) Cl reaktáns, mechanizmus - C Cl S 2 C 3 - C 3 C Cl C Brg C 2 C 3 S E 2 S 2 aromás C S E 2 aromás C 3 S 1 reagens Br 2 2 nukleofil nukleofil elektrofil elektrofil - - C Cl Cl 2 közti-termék Me Me C Me Q Q potencirozás Q= 2 e-szívó Q=alil e-küldő
70 R alkohol Alkil-halogenidek átalakítása S 2 reakciókkal R' R R' éter S R S tiol R'S R SR' tioéter R X - X C R C nitril R = Me, primer vagy szekunder alkil X = Cl, Br vagy I R C C R'C R R C C C R' R' alkin észter R' 3 R R' 3 X kvaterner ammónium halogenid 3 - R 3 alkil-azid
71 ldószerhatás Apoláris oldószerek: realtív permittivitás pentán hexán * dipólus momentum ciklohexán benzol * toluol kloroform dietil-éter
72 ldószerhatás Poláris aprotikus oldószerek: diklórmetán realtív permittivitás dipólus momentum tetrahidrofurán etil-acetát aceton acetonitril dimetilformamid dimetilszulfoxid
73 ldószerhatás Poláris protikus oldószerek: realtív permittivitás dipólus momentum metilformamid ammónia D t-butanol propanol etanol metanol ecetsav víz
74 ldószerhatás Dimetilszulfoxid (DMS): miracle solvent erősen polarizált oxigénatom atomi töltések: -0,41 nemkötő elektronpár 0,26 0,15-0,37 enyhén savanyú hidrogének vegyületek széles körének oldószere vízzel korlátlanul elegyedik forráspont: 189 C, fagyáspont: 19 C sejtek (pl. hámsejtek) permeabilitását megnöveli toxikus (?)
Alap szerves kémiai reakciók szisztematikus tárgyalása
 Alap szerves kémiai reakciók szisztematikus tárgyalása A biokémia is a szerves molekulák kémiája Egy példa arra, hogy a szerves kémiai reakciók és az enzimkatalizált biokémiai reakciók hasonló alapelvek
Alap szerves kémiai reakciók szisztematikus tárgyalása A biokémia is a szerves molekulák kémiája Egy példa arra, hogy a szerves kémiai reakciók és az enzimkatalizált biokémiai reakciók hasonló alapelvek
Alap szerves kémiai reakciók szisztematikus tárgyalása
 Alap szerves kémiai reakciók szisztematikus tárgyalása A biokémia is a szerves molekulák kémiája Egy példa arra, hogy a szerves kémiai reakciók és az enzimkatalizált biokémiai reakciók hasonló alapelvek
Alap szerves kémiai reakciók szisztematikus tárgyalása A biokémia is a szerves molekulák kémiája Egy példa arra, hogy a szerves kémiai reakciók és az enzimkatalizált biokémiai reakciók hasonló alapelvek
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
HALOGÉNEZETT SZÉNHIDROGÉNEK
 ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
AROMÁS SZÉNHIDROGÉNEK
 AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Aromás vegyületek II. 4. előadás
 Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
H 3 C H + H 3 C C CH 3 -HX X 2
 1 Gyökös szubsztitúciók (láncreakciók gázfázisban) - 3 2 2 3 2 3-3 3 Szekunder gyök 3 2 2 2 3 2 2 3 3 2 3 3 Szekunder gyök A propánban az azonos strukturális helyzetű hidrogének és a szekunder hidrogének
1 Gyökös szubsztitúciók (láncreakciók gázfázisban) - 3 2 2 3 2 3-3 3 Szekunder gyök 3 2 2 2 3 2 2 3 3 2 3 3 Szekunder gyök A propánban az azonos strukturális helyzetű hidrogének és a szekunder hidrogének
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
Összefoglaló előadás. Sav-bázis elmélet
 Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
Beszélgetés a szerves kémia elméleti alapjairól III.
 Beszélgetés a szerves kémia elméleti alapjairól III. Csökkentett vagy fokozott reakciókészségű halogénszármazékok? A középiskolai szerves kémiai tananyag alapján, a telített alkil-halogenidek reakcióképes
Beszélgetés a szerves kémia elméleti alapjairól III. Csökkentett vagy fokozott reakciókészségű halogénszármazékok? A középiskolai szerves kémiai tananyag alapján, a telített alkil-halogenidek reakcióképes
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Reakciókinetika. aktiválási energia. felszabaduló energia. kiindulási állapot. energia nyereség. végállapot
 Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
Reakció kinetika és katalízis
 Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének alogénezett szénhidrogének Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br 1,91 66
elyettesített Szénhidrogének alogénezett szénhidrogének Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br 1,91 66
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
H H 2. ábra: A diazometán kötésszerkezete σ-kötések: fekete; π z -kötés: kék, π y -kötés: piros sp-hibrid magányos elektronpár: rózsaszín
 3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Halogénezett szénhidrogének
 Halogénezett szénhidrogének - Jellemző kötés (funkciós csoport): X X = halogén, F, l, Br, I - soportosítás: - halogénatom(ok) minősége szerint (X = F, l, Br, I) - halogénatom(ok) száma szerint (egy-, két-
Halogénezett szénhidrogének - Jellemző kötés (funkciós csoport): X X = halogén, F, l, Br, I - soportosítás: - halogénatom(ok) minősége szerint (X = F, l, Br, I) - halogénatom(ok) száma szerint (egy-, két-
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
10. Kémiai reakcióképesség
 4. Előadás Kémiai reakciók leírása. Kémiai reakciók feltételei. Termokémia. A szerves kémiai reakciómechanizmusok felosztása és terminológiája. Sav-bázis reakció. Szubsztitució. Addició és elimináció.
4. Előadás Kémiai reakciók leírása. Kémiai reakciók feltételei. Termokémia. A szerves kémiai reakciómechanizmusok felosztása és terminológiája. Sav-bázis reakció. Szubsztitució. Addició és elimináció.
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Beszélgetés a szerves kémia elméleti
 Beszélgetés a szerves kémia elméleti alapjairól V. Az alkének eiektrofil addiciójának irányítottsága: Markovnikov szabály vagy anti-markovnyikov "szabály"? 1. kérdés Mint elméleti, mint gyakorlati szempontból
Beszélgetés a szerves kémia elméleti alapjairól V. Az alkének eiektrofil addiciójának irányítottsága: Markovnikov szabály vagy anti-markovnyikov "szabály"? 1. kérdés Mint elméleti, mint gyakorlati szempontból
Beszélgetés a szerves kémia eméleti alapjairól IV.
 Beszélgetés a szerves kémia eméleti alapjairól IV. Az alkének elektrofil addiciós reakciói Az alkénekben levő kettős kötés pi-elekronrendszerének jellegzetes térbeli orientáltsága kifejezetten nukleofil
Beszélgetés a szerves kémia eméleti alapjairól IV. Az alkének elektrofil addiciós reakciói Az alkénekben levő kettős kötés pi-elekronrendszerének jellegzetes térbeli orientáltsága kifejezetten nukleofil
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. 1; PAP
 Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. H 1; PAP H FeCl 2 és PAP reakciója metanolban oxigén atmoszférában Fe 2 (PAP)( -OMe)
Új oxo-hidas vas(iii)komplexeket állítottunk elő az 1,4-di-(2 -piridil)aminoftalazin (1, PAP) ligandum felhasználásával. H 1; PAP H FeCl 2 és PAP reakciója metanolban oxigén atmoszférában Fe 2 (PAP)( -OMe)
Zárójelentés a. című pályázatról ( , )
 Zárójelentés a Reakciósorozatokban érvényesülő szubsztituens és oldószerhatás elemzése aktiválási paraméterekből leszármaztatott reakciókonstansok alkalmazásával című pályázatról (2006-2009, 060889) A
Zárójelentés a Reakciósorozatokban érvényesülő szubsztituens és oldószerhatás elemzése aktiválási paraméterekből leszármaztatott reakciókonstansok alkalmazásával című pályázatról (2006-2009, 060889) A
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
10. Előadás. Heterociklusos vegyületek.
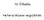 0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
Részletes tematika: I. Félév: 1. Hét (4 óra): 2. hét (4 óra): 3. hét (4 óra): 4. hét (4 óra):
 Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
leírás: típusai: memo:
 VI. Bázissal (nukleofillal) -kiváltott elimináció (E) definíció: A molekula két vagy több szubsztituensét úgy távolítjuk el, hogy azok helyére új szubsztituens nem kerül. Két szubsztituens eltávolítása
VI. Bázissal (nukleofillal) -kiváltott elimináció (E) definíció: A molekula két vagy több szubsztituensét úgy távolítjuk el, hogy azok helyére új szubsztituens nem kerül. Két szubsztituens eltávolítása
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
KARBONSAV-SZÁRMAZÉKOK
 KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
AMINOK. Aminok rendűsége és típusai. Levezetés. Elnevezés. Alkaloidok (fiziológiailag aktív vegyületek) A. k a. primer RNH 2. szekunder R 2 NH NH 3
 Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Oldószerek csoportosítása
 ldószerek csoportosítása Vegyülettípus szerint 1. Telített alifás szénhidrogének petroléter (alacsony forráspontú szénhidrogének keveréke), pentán, hexán, heptán 2. Aromás szénhidrogének benzol, toluol,
ldószerek csoportosítása Vegyülettípus szerint 1. Telített alifás szénhidrogének petroléter (alacsony forráspontú szénhidrogének keveréke), pentán, hexán, heptán 2. Aromás szénhidrogének benzol, toluol,
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Tantárgycím: Szerves kémia
 Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
A KÉMIA ÚJABB EREDMÉNYEI
 A KÉMIA ÚJABB EREDMÉNYEI A KÉMIA ÚJABB EREDMÉNYEI 98. kötet Szerkeszti CSÁKVÁRI BÉLA A szerkeszt bizottság tagjai DÉKÁNY IMRE, FARKAS JÓZSEF, FONYÓ ZSOLT, FÜLÖP FERENC, GÖRÖG SÁNDOR, PUKÁNSZKY BÉLA, TÓTH
A KÉMIA ÚJABB EREDMÉNYEI A KÉMIA ÚJABB EREDMÉNYEI 98. kötet Szerkeszti CSÁKVÁRI BÉLA A szerkeszt bizottság tagjai DÉKÁNY IMRE, FARKAS JÓZSEF, FONYÓ ZSOLT, FÜLÖP FERENC, GÖRÖG SÁNDOR, PUKÁNSZKY BÉLA, TÓTH
A kémiai kötés. Kémiai kölcsönhatás
 A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Laboratóriumi technikus laboratóriumi technikus Drog és toxikológiai
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Budapest, szeptember 5. Dr. Tóth Tünde egyetemi docens
 SZERVES KÉMIA I. levelező B.Sc. képzés, kód: BMEVESZAL17 Tantárgy követelményei 2016/2017. tanév I. félév Az alaptárgy heti 2,5 óra (páratlan héten 2 óra, páros héten 3 óra) előadásból és ezzel integrált
SZERVES KÉMIA I. levelező B.Sc. képzés, kód: BMEVESZAL17 Tantárgy követelményei 2016/2017. tanév I. félév Az alaptárgy heti 2,5 óra (páratlan héten 2 óra, páros héten 3 óra) előadásból és ezzel integrált
Cikloalkánok és származékaik konformációja
 1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
Név: Pontszám: 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 7. Átrendez dések. Szén-nitrogén kötések kialakítása. Kovács Lajos 1 Átrendez dések elektronhiányos szénre 1. A Wagner-erwein-átrendez ı dés 3 C 3 C 3 C 1 3 C 3 C 3 C
Szerves kémiai szintézismódszerek 7. Átrendez dések. Szén-nitrogén kötések kialakítása. Kovács Lajos 1 Átrendez dések elektronhiányos szénre 1. A Wagner-erwein-átrendez ı dés 3 C 3 C 3 C 1 3 C 3 C 3 C
Szerves Kémia. Farmakológus szakasszisztens képzés 2012/2013 ősz
 Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Toluol (Bruckner II/1 476) µ= 0.33 Debye
 E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötés Lewis elmélet
 Kémiai kötés 10-1 Lewis elmélet 10-2 Kovalens kötés: bevezetés 10-3 Poláros kovalens kötés 10-4 Lewis szerkezetek 10-5 A molekulák alakja 10-6 Kötésrend, kötéstávolság 10-7 Kötésenergiák Általános Kémia,
Kémiai kötés 10-1 Lewis elmélet 10-2 Kovalens kötés: bevezetés 10-3 Poláros kovalens kötés 10-4 Lewis szerkezetek 10-5 A molekulák alakja 10-6 Kötésrend, kötéstávolság 10-7 Kötésenergiák Általános Kémia,
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Szabadalmi igénypontok
 l Szabadalmi igénypontok l. A dihidroxi-nyitott sav szimvasztatin amorf szimvasztatin kalcium sója. 5 2. Az l. igénypont szerinti amorf szimvasztatin kalcium, amelyre jellemző, hogy röntgensugár por diffrakciós
l Szabadalmi igénypontok l. A dihidroxi-nyitott sav szimvasztatin amorf szimvasztatin kalcium sója. 5 2. Az l. igénypont szerinti amorf szimvasztatin kalcium, amelyre jellemző, hogy röntgensugár por diffrakciós
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása
 Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
