10. Előadás. Szerves vegyületek kénatommal. Heterociklusos (porfinvázas) vegyületek.
|
|
|
- Tivadar Pataki
- 5 évvel ezelőtt
- Látták:
Átírás
1 10. Előadás zerves vegyületek kénatommal. eterociklusos (porfinvázas) vegyületek.
2 ZEVE VEGYÜLETEK KÉATMMAL Példák: C 2 =C-C 2 ---C 2 -C=C 2 diallil-diszulfid (fokhagyma olaj) szacharin merkapto-purin tiofén C 2 C3 szén-diszulfid szulfonamid (Ultraseptyl) C 3 C C2 2 cisztein (Cys) 2 metionin (Met) tio-glikolsav (merkaptoecetsav, szulfhidril-ecetsav) ciszteamin 3C C3 P... adenozin-3,5 -difoszfát pantoténsav pantotein KEZIM A
3 Áttekintés A kénatomhoz kapcsolódó ligandumok száma [1] [2] [3] [4] ' tiovegyület (pl. tioketon) tiol ' + ' " X- szulfóniumsó ' ' " ''' szulfurán ' szulfid szulfoxid szulfon ' ' diszulfid szulfilimin szulfénsav szulfinsav szulfonsav Csoportok: - Cl 2 tiokarbonil merkapto- (szulfhidril) szulfonil-klorid szulfon(sav)amid
4 omenklatúra, példákkal 3 C C Cl etán-tiol (etil-hidrogénszulfid, etil-merkaptán) 3-klór-2-metil-1- propántiol 2-merkapto-etanol Cl C 3 C 3 etil-metil-szulfid dimetil-szulfoxid 3 3 C 3 5 C 2 C 3 1 C metánszulfonsav metánszulfonsavetilészter 1-klór-2,3-epitiopropán 3-szulfo-1- ciklohexánkarbonsav 2 2 C 3 metánszulfonamid tetrametilén-szulfid
5 zerkezet Elektronok I. sor C F II. sor i P Cl E (2,5) < E (3,5) Jellegzetességek A. analógia oxigénnel B. nagyobb sugarú vegyértékhéj kisebb E kisebb bázicitás polározhatóság C. különleges sztereokémia : 3s 2 3p x2 3p y1 3p z1 3d ligandumos kénvegyületek (tiovegyületek) C.... s kötés: C(2sp 2 ) (3sp 2 ) p kötés: C(2p) (3p) nem stabil C3 Példa: 3 C 3 -C= tioaldehid C 3 C3 de: C C - + stabil tioészter: konjugált rendszer
6 2 ligandumos kénvegyületek (tiol, tioéter) nem lineáris C 3 C 3 C 3 ) ) ) < 92,5 C < 96,5 CC < 98,5 104,5 C 105 CC 112 s: (s) (p); C(2sp 3 ) (3p) - : 335 kj/mol C - : 267 kj/mol : 452 kj/mol C : 347 kj/mol 3 ligandumos kénvegyületek (szulfoxid, szulfóniumsó) s: (3sp 3 ) (2sp 3 ) C 3 C 3 C 3 C 3 C 3 C - 3 C 3 C : 1,83Å CC kötésszög: 103 piramisos, királis C : 1,81 Å C : 1,47 Å CC kötésszög: 96,4 C: 106,7 piramisos, királis s: C(2sp 3 ) (3sp 3 ) (3sp 3 ) (2sp 2 ) p: (3d) (2p) Összevetés
7 Összegzés C 3 C 3 C 3 C 3 C 3 C 3 szulfid szulfoxid szulfon Kötéshosszak: C 1,82Å C 1,81Å = 1,47Å C 1,78Å = 1,44Å Kötésszögek: CC 98,5 DE: CC 96,4 C 106,7 CC 103 C 108,7 118
8 Fizikai tulajdonságok A. Tiolok Forráspont ( C) X= X= 2 X* /10 millió C 3 X* 6 65 C 3 C 2 X* C 3 XC nincs -híd kötés* illékonyság: C 3 C 2 C 2 hagyma C 3 (C 2 ) 3 görény B. zulfoxidok, szulfonok d+ d- -híd: akceptor 3C 3C op: 18 C dipoláros, aprotikus oldószer C. zulfonsavak (- sav) oldékonyság detergensek: C n 2n+1 - a + nátrium-alkilszulfát
9 1. av-bázis sajátság Kémiai reakciók Tiol, szulfid savas jelleg, pk a =11 (vö. pk a =17) bázikus jelleg (gyengébb, mint :: ) zulfoxid, szulfon savas jelleg ' a C 2 ' a C 2 bázikus jelleg Példa: --C Et - ' C - ' C - konjugáció: delokalizált, nincs tautomerizáció!
10 2. xidáció, redukció Tiol - 2 vagy I diszulfid 3 vagy szulfonsav cisztein cisztin red. ox. liponsav dihidroliponsav királis karbonsav, kofaktor, piruvát-dehidrogenáz komplex része, antioxidáns
11 zulfid szulfid szulfoxid szulfon Példa: C3 2 C3 2 3C 2 metionin metionin szulfoxid metionin szulfon
12 3. ukleofil szubsztitúció 3.1. Alkilezés (tiol, tioéter) Et - -Et - -: - -: - + -X -- + X X X éter - ofmann-analóg elimináció szulfóniumsó C 1, 2, 3 C (C 3 ) 2 - Me 2-2 tiol szulfónium só alkén 1: Et -, MeI; 2: MeI, éter; 3: Ag 2, Acilezés + 3C Cl C3 + Cl acetil-klorid alkil-tioacetát acil transzferáz C3 koenzim A acetil-koenzim A
13 - vs - reaktivitása - összevetés (tiol, merkaptán = mercurium captans ) 1. ukleofil sajátság 3C C2 - C 3 C2-2. avi jelleg - > - 3. xidáció Tiolok előállítása Et 1. C 3 C 2 -Br (I) + K + 2 C 3 C KBr + 2 felesleg ha nincs felesleg: C 3 C K C 3 C K + C 3 C K + + C 3 C 2 -Br C 3 C 2 --C 2 C 3 + KBr tioéter.. Et + 2. C 3 C 2 -Br + ( 2 ) 2.. C= ( 2.. ) 2 C=-C 2 C 3 Br - tiourea -etil-izotiourónium-bromid ( 2 ) 2 C= + C 3 C / urea (karbamid) etántiol
14 Kimutatás: Aminok reakciója szulfonil-kloriddal (insberg-reakció) 1. Primer amin.. K - Cl 2 + Cl -alkil-szulfonsavamid (tiszta oldat + csapadék) 2. zekunder-amin ' '.. ' K + Cl - Cl ',-dialkil-szulfonsavamid (csapadék) 3. Tercier-amin.. Cl K - Cl +,,-trialkil-szulfonsavamid (csapadék tiszta oldat) - hidrolízis
15 Antibiotikumok: szulfonamidok Gerhard Domagk (1932), patológus, bakteriológus Münsteri Egyetem, I.G. Farben d , az első kereskedelmi forgalomba is kerülő antibiotikumok, a szulfonamidok felfedezéséért ( ) 2 2 in vivo Prontosil (narancsvörös) in vitro : üvegben in vivo: életben para-amino-benzolszulfonamid (PAB, fehér) (folsavszintézishez) -- C3 C3 C C3 2 Ultraseptyl uperseptyl ulfaguanidin
16 A fodrásznál -C 2 -C tiogliokolsav 2 2 Mérgezés (tiol, merkaptán* jelentése = mercurium captans, capturing mercury ) g 2+ -g- As 3 3- enzim (protein) arzenit - -As *1832, William Christopher Zeise, dán szerves kémikus, fémorganikus vegyületek
17 eterociklusos vegyületek
18 ETECIKLU VEGYÜLETEK Felosztás: 1. telített telítetlen 2. heteroatomok száma 3. gyűrűk száma 4. heteroatomok milyensége (,,, P, As, i) oxa- tia- aza- I. Monociklusos, egy heteroatomos vegyületek 4 C 3 C C C C 5 1 C 2 C C 1 2 furán* tiofén* pirrol* piridin* oxol tiol azol azin 2 C C 2 2 C C 2 C 2 2 C C 2 2 C C 2 2 C C 2 2 C C 2 2 C C 2 2 C C 2 tetrahidrofurán* oxolán tetrahidrotiofén* tiolán pirrolidin* azolidin piperidin* perhidroazin
19 II. Monociklusos, két heteroatomos vegyületek Azolok: 5-tagú gyűrű + legalább 1 más heteroatom oxazol tiazol imidazol (hisztidinben) Azinok: 6-tagú gyűrű + legalább 1 más heteroatom () pirimidin (1,3-diazin) (D, -ben) pirazin (1,4-diazin) piridazin (1,2-diazin) triazinok (3), tetrazinok (4) III. Biciklusos, kondenzált heteroatomos vegyületek 8 1 pirimidin imidazol pirazin pirimidin indol (triptofánban) purin (D, -ben) pteridin (folsavban) kinolin (benzopiridin) izokinolin Festék alapanyag, tartósítószer, fertőtlenítő, oldószer, izokinolinvázas alkaloidok
20 IV. Tri-,...-ciklusos, heteroatomos vegyületek 2 C 3 Akridin (váz) 9-aminoakridin: erős fertőtlenítő szer fluoreszcens tulajdonságú 5 C 2 C 2 5 lizergsav-dietilamid (LD) op C (anyarozs alkaloid) indol Folsav analógok 2 pteridin gyűrű 1 C C 2 - C (C 2 ) 2 Glu C 2 C 1 =, 2 = folsav; B9-vitamin, M-vitamin. 1 = 2, 2 = aminopterin 1 = 2, 2 = C 3 amethopterin, methotrexat Folsav: terhesség korai szakaszában embrió gerinc, velőcsövet, fehérvérsejtek, vörösvértestek, vérlemezkék képzésében, az aminosavak és nukleinsavak anyagcseréjében Metotrexát: tumorellenes szer, reumatoid artritisz
21 Elektronszerkezet Aromás jelleg (pirrol, furán, tiofén) (ückel szabály: 4n+2 elektron) Q - I effektus (hetero atom E-nak megfelelő mértékben vonzza az elektronokat) Q = ::, :, :: E = 2,6 3,0 3,5 < < Tiofén hasonlít legjobban a benzolra,de az elektrofil szubsztitúciós reakció gyorsabbak. K-effektus - 0,2-0,2 + 0, ,2-0,2 d- d- + egyenletes valóságos elektroneloszlás csak határszerkezetekből d+ + határszerkezetek! - 0,04-0,15 d+ 0,2 d+ 0,3 d+ 0,38 + nem bázis, nem proton kedvelő piridin + 0,18 + 0,05 + 0,15-0,58 + 0,15 bázis, proton kedvelő
22 Téralkat Konjugált kettős kötés esetén az egyes és kettős kötés hossza pm: m Å: m izolált egyes kötés izolált kettős kötés aromás rendszer Kötéshossz : -C > -C > -C
23 Fizikai tulajdonságok a a molekulában van -donor (pl. -) és -akceptor (pl. ), akkor tud -kötést kialakítani pirazol imidazol
24 Kémiai reakciók 1A. av-bázis sajátság (egy heteroatom) (sav: protont tud leadni; bázis: protont tud felvenni) tiofén nem bázis, nem sav (C- nem proton donor, a kén atom E nem elég nagy, hogy vonzza a -t) pirrol: + 2 megszűnik az aromás jelleg + + K K + ½ 2 aromás marad (tehát gyenge - sav) + (pk = 15) furán: piridin: pk b = 8,8 gyenge bázis
25 1B. av-bázis sajátság (két heteroatom) pirazol imidazol Piridin jellegű Piridin jellegű Pirrol jellegű amfoter pirimidin bázikus bázikus Piridin jellegű
26 2. Elektrofil szubsztitúciók Feltétel: elektronban gazdag gyűrűk A. pirrol, furán, tiofén, indol Irányítás pozitív töltés vagy parciális pozitív töltésű rész támad elektronban gazdag helyre d- - 0,04 d- d+ - 0,15 Q eaktivitás σ-komplexek lehetséges határszerkezete 2-es és 3-as helyzetű szubsztitúció esetén: jobb elektron eloszlás, stabilabb σ-komplex Példák 2-nitropirrol 5 o C 2-acetilpirrol 250 o C
27 B. piridin + 0,18 Irányítás eaktivitás + 0,15-0,58 + 0,05 + 0,15 legkevésbé + helyre igyekszik kötődni stabilabb σ-komplex
28 Példák (kénsav protonálódás) 3-brómpiridin 3-nitropiridin piridin-3 szulfonsav Áttekintés benzol pirrol furán tiofén piridin nitrálás * + szulfonálás * diazo kapcsolás Friedel- Crafts acilezés Ar- + + C 3 -C-Q brómozás Br * protonálás után
29 Példa: triptofán (Trp) szintézise (indol E reakció) 1. lépés Aminometilezés + + C 2 C 3 C 3 E C 2 C 3 C 3 2. lépés Alkilezés C 2 C 3 C 3 + C 3 I (jó távozó csoport, ld. offman elimináció) C 2 + C 3 C 3 C 3 I - C 2 + C 3 C 3 C 3 + Ac C - CEt CEt 2 CEt C 2 EtC Ac 3. lépés idrolizis, dekarboxilezés CEt C 2 EtC Ac 1. észter hidrolízis 2. dekarboxilezés C C 2 2 Triptofán (Trp) nátrium-etilát (igen erős bázis) CEt Ac C C - CEt Et - Ac - + CEt CEt acetamidomalonészter (C- sav)
30 3. ukleofil szubsztitúciók Feltétel: elektronban szegény gyűrűk C 6 5- Li + C65 Összehasonlítás
31 Kétheteroatomos vegyületek reaktivitása d- - 0,04 d + piridin szerű d + d- - 0,15 d+ + 0,18 d - d - pirrol szerű (tautoméria) + 0,05 + 0,15-0,58 + 0,15 b a piridin szerű Pozíció a b 2 d+ d+ 4 d+ d+ 5 d- d- 6 d+ d+ elatív elektronhiány: 4 = 6 > 2 > 5 Magyarázat: a parciális töltések szuperponálódnak E E E E pirazol imidazol pirimidin
32 Tautoméria egy kettős kötés és egy proton helyzetének megváltozása Imidazol Piridin származékok keto-enol amino-imino Pirimidin (citozin)) keto-enol Purin (adenin) 2 amino-imino
33 Furán, tiofén, pirrol vázas vegyületek szintézise (Paal-Knorr) cc. 2 4 ' ' 3 nyomás ' 1,4-dioxo-vegyület (1,4-dienol is jó) P 4 10 Foszfor-pentaszulfid ' Példák a amidin-származék imidazol-származék a bróm - keton karbonsavamid-származék oxazol-származék tioamid-származék tiazol-származék
34 Piridin szintézis (antzsch) EtC a b ' aldehid 3 CEt EtC ' CEt b - oxo karbonsav észter EtC ' CEt ox. EtC ' CEt - 2 piridin-származék
35 Purin szintézis 2,4,6-trihidroxi-pirimidin (barbitursav) dilaktám-enol dilaktám-keto 2 /Cl 2 2 /red Cl 1 2 2,4,6-trihidroxi-5-aminopirimidin 1. KC 2. Wöhlerizomerizáció pszeudohúgysav Cl ,6,8-triklór-purin 9 8 Cl - 2 Cl (20%) PCl o C 2,6,8-trihidroxi-purin (húgysav) keto enol tautoméria
36 Purin szintézis (folytatás) eaktivitási sorrend 6 > 2 > 8 Cl 1 2 Cl ,6,8-triklór-purin Cl eduktív dehalogénezés purin a + Et K 2. 3 Et 2 Cl Cl Cl Et Cl 2 1. Elfőzés (cc. Cl) 2. red.dehalogénezés red. dehal. red. dehal. 2 2 xantin 6-aminopurin (adenin) guanin
37 Porfinvázas vegyületek
38 Makrociklus: ciklusba zárt molekula (nincs végcsoport) vagy molekularészlet, amely > 12 atomot tartalmaz Porfinvázas vegyületek: négy pirrol vagy részlegesen telitett pirrolgyűrűt 2 a A B d b 8 D C g porfin váz Egyszerűsített jelölésmód porfin izoporfin Jellemzés: 1. síkalkat, 4n+2 elektron (26) aromás makrociklus 2. amfoter jelleg a) protonleadás b) : proton felvétel
39 Porfinvázak 2 a 3 1 A B 4 d b 8 D C 5 7 g 6 porfin váz klorin (7,8-dihidro-porfin) váz (hem-proteinek) (klorofill) Fe 2+ / Fe 3+ Mg 2+ 2 a 3 1 A B 4 b 8 D C 5 7 g 6 korrin (B 12 vitamin) Co 3+
40 Funkció: 1. C 2 asszimiláció (pl. klorofill) 2. Biológiai oxidáció (pl. hemoglobin) Csoportosítás 1. Kromoproteidek (protein + prosztetikus csoport) 1.1 emoglobin (gerincesek) 1.2 Mioglobin (izomsejtek, gerincesek/gerinctelenek) 1.3 Eritrokruorin (gerinctelenek, 150 hem) 1.4 Kataláz, peroxidáz (protoporfirin, Fe 3+ ) 1.5 Citokrómok (terminális oxidáció, Fe 2+ Fe 3+ ) 2. Klorofill (zöld növények) 3. Cianokobalamin (B12 vitamin)
41 1.1. emoglobin (1862, kristályos) Prosztetikus csoport (vörös) + globin (4 polipeptid lánc, Mt: ) Max F. Perutz, 1960 obel díj, (J. Kendrew) phm.utoronto.ca
42 em: Fe(III) só oxidáció emin: Fe(II) só 2C C3 C2 2C C3 C2 3C 3C Fe (III) C3 Ac Br 3C 3C C3 C C C C Jellemzés: Protoporfirin (vas mentes) 1. porfin származékok 2. sötétvörös, kristályos 3. síkalkat, 4n+2 elektron aromás makrociklus 4. amfoter jelleg a) protonleadás b) : proton felvétel 5. hem totálszintézise:. Fischer, 1929
43 globin is 87 is Paál. G. A fehérjeműködés paradigmája: mioglobin és hemoglobin
44 1.2. Mioglobin Prosztetikus csoport (vörös) + globin (1 polipeptidlánc) 153 aminosav 2C C3 C2 2C C3 C2 3C 3C Fe (II) ox. Fe (III) red. 3C C3 3C C3 C C C C hemokromogén hemin Jellemzés: 1. izomban fordul elő 2. 2 megkötés (nagyobb, mint hemoglobin) 3. térszerkezet (J. Kendrew, obel díj) első fehérje, hem protein zseb (is szerepe)
45 A mioglobin és 2 kötőhelye guweb2.gonzaga.edu Disztális hisztidin E7 (távoli) hem Proximális (közeli) hisztidin F8
46 Mioglobin, hemoglobin összegzés váz fémion prosztetikus csoport Protoporfirin protein Fe 2+ hem ferrohemoglobin (hemoglobin) Fe 3+ hemin ferrihemoglobin (hemiglobin) funkció 2 kötés 2 Fe 2+ hem oximioglobin 2 kötés Fe 3+ hemin ferrimioglobin 2 Fe 2+ hem dezoximioglobin 2 kötés humán hemoglobin F1 F2 F3 F4 F5 F6 F7 F8 F9 a lánc Leu er Ala Leu er Asp Leu is Ala b lánc Phe Ala Thr Leu er Glu Leu is Cys ámbráscet mioglobin Leu Lys Pro Leu Ala Gln er is Ala
47 1.3. Eritrokruorin és klorokruorin xigén szállító, hem-tartalmú fehérjék (Mt > 3,5 millió Da) Gyűrűsférgek, soksertéjűek (Polychaeta) Eritrokruorin (4 x 36 globin) Prosztetikus csoport klorokruorin
48 %-os 2 telítettség Légzési színezékek (kiegészítés) 2 diffúzió: 2 mm mélység szállítófolyadék molekula szín fémion tömeg példa hemoglobin világospiros sötétvörös Fe 3+ Fe gerinces körszájúak rákok, férgek mioglobin világospiros Fe gerinces gyűrűs férgek sötétpiros Fe 2+ klorokruorin zöld zöld Fe 3+ Fe soksertéjű férgek hemocianin kék színtelen Cu 2+ Cu rákok (languszták) tőrfarkúak 100 xigénaffinitás 50 mioglobin hemoglobin hemocianin nyomás [Torr]
49 emocianin (metalloprotein) Megathura crenulata (keyhole limpet) Cu = narancs, = vörös emocianin from Pandinus imperator E. Jaenicke et al. PLo ne 2012, 7(3) e
50 Epefestékek hemoglobin hem részének bomlástermékei A. biliverdin, zöld (máj) B. bilirubin, sárga (máj). Legrégebben ismert; biliverdin oxidációja. vér c = 0,5 mg/100 ml sárgaság, máj epe bélrendszer 250 mg/nap 2C C3 C2 2C C3 C2 3C 3C oxidáció 3C C3 3C C3 C C protoporfirin C C biliverdin C 2 5, lúg / redukció 3C 3C C3 C3 3C 2C C3 C2 3C C3 3C C3 C C C C hematoporfirin bilirubin
51 2. Klorofill zöld szemcsék (kloroplasztok) pigmentje izolálás: Willstätter ( ) szerkezet: Fischer (1940) szintézis: Woodward (1960) Összetétel: klorofill A + klorofill B = 3:1 + Mg 2C C = -C 3 A 3C C2 C3 = -C B Mg 3C * * C2 C2 C * C3 CC3 C Cianokobalamin (B 12 ) Co 3+, 4,3% kobalt C Co (C ) fitol észter Cisz-7()-11 ()-3,7,11,15-tetrametil-2-hexadecén-1-ol
52 A D B C 2 -C 2 (C 3 )- (2-hidroxil-propilamin) + 3 P D-ribóz + F E hidrolízis + C3 a-glikozid kötés G C3 C3 korrin-váz (nem aromás!) C2 C3 Variációk: - C B 12 - B 12a - 2 B 12c 1-(a-D-ribofuranozil)-5,6- -dimetil-benzimidazol 1926: májkivonat vészes vérszegénység (Minot, Murphy) 1947: mikrobák növekedési faktora (horiz) 1948: izolálás tengeri algákból (Folkers, mith) : térszerkezet (odgkin)
10. Előadás. Heterociklusos vegyületek.
 0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
11. Előadás. Heterociklusos vegyületek
 11. Előadás eterociklusos vegyületek ETECIKLUSS VEGYÜLETEK Felosztás: 1. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
11. Előadás eterociklusos vegyületek ETECIKLUSS VEGYÜLETEK Felosztás: 1. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
HETEROCIKLUSOS VEGYÜLETEK
 ETERCIKLU VEGYÜLETEK ETERCIKLU VEGYÜLETEK Csoportosítás eteroatom minősége:,, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Telítettség mértéke szerint: - heteroaromás - heteroalkén - heteroalkán - Elnevezés: elsősorban
ETERCIKLU VEGYÜLETEK ETERCIKLU VEGYÜLETEK Csoportosítás eteroatom minősége:,, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Telítettség mértéke szerint: - heteroaromás - heteroalkén - heteroalkán - Elnevezés: elsősorban
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
10. Előadás Porfinvázas vegyületek
 10. Előadás Porfinvázas vegyületek Makrociklus: ciklusba zárt molekula (nincs végcsoport) vagy molekularészlet, amely > 12 atomot tartalmaz Porfinvázas vegyületek: négy pirrol vagy részlegesen telitett
10. Előadás Porfinvázas vegyületek Makrociklus: ciklusba zárt molekula (nincs végcsoport) vagy molekularészlet, amely > 12 atomot tartalmaz Porfinvázas vegyületek: négy pirrol vagy részlegesen telitett
Porfin vázas vegyületek (PORFIRINEK)
 Porfin vázas vegyületek (PRFIRIEK) Az élő szervezetekre jellemző kémiai átalakulások két kiemelkedő fontosságú folyamata a porfinvázas vegyületekhez kapcsolódik. Az egyik a zöld növények széndioxid-asszimilációja,
Porfin vázas vegyületek (PRFIRIEK) Az élő szervezetekre jellemző kémiai átalakulások két kiemelkedő fontosságú folyamata a porfinvázas vegyületekhez kapcsolódik. Az egyik a zöld növények széndioxid-asszimilációja,
COOCH 3. Ca + O - NH 2 OCH 2 CH 2 CH 3 NO 2 N H H 3 CO N OCH 3 COOH
 9. Előadás itrogéntartalmú vegyületek 26. ITGÉTATALMÚ VEGYÜLETEK épszerű származékok 3 2 metil-antranilát (szőlő) 300 S szacharin (1977) S - kalcium-ciklamát (1970: rák) a + 2 2 3 2 2 3 2 2 3 2 2 2 glükóz:
9. Előadás itrogéntartalmú vegyületek 26. ITGÉTATALMÚ VEGYÜLETEK épszerű származékok 3 2 metil-antranilát (szőlő) 300 S szacharin (1977) S - kalcium-ciklamát (1970: rák) a + 2 2 3 2 2 3 2 2 3 2 2 2 glükóz:
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Heterociklusos vegyületek
 eterociklusos vegyületek ETERCIKLUSS VEGYÜLETEK eteroatom minősége:, S, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Elnevezés: elsősorban triviális nevek piridin furán izokinolin 2 evezéktan szabályai 5 4 3 R β'
eterociklusos vegyületek ETERCIKLUSS VEGYÜLETEK eteroatom minősége:, S, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Elnevezés: elsősorban triviális nevek piridin furán izokinolin 2 evezéktan szabályai 5 4 3 R β'
Szerves kémiai nevezéktan IV.
 zerves kémiai nevezéktan IV. A magyar kémiai elnevezés és helyesírás szabályai, az IUPAC (International Union of Pure and Applied Chemistry) zerves Kémiai ómenklatúrabizottságának 99-as ajánlása alapján.
zerves kémiai nevezéktan IV. A magyar kémiai elnevezés és helyesírás szabályai, az IUPAC (International Union of Pure and Applied Chemistry) zerves Kémiai ómenklatúrabizottságának 99-as ajánlása alapján.
AMINOK. Aminok rendűsége és típusai. Levezetés. Elnevezés. Alkaloidok (fiziológiailag aktív vegyületek) A. k a. primer RNH 2. szekunder R 2 NH NH 3
 Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
AROMÁS SZÉNHIDROGÉNEK
 AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2000
 Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Nitrogé ntartalmú hétérociklúsos végyú léték
 itrogé ntartalmú hétérociklúsos végyú léték A nitrogéntartalmú heterociklusos vegyületek a természetben előforduló jelentős vegyületek közé tartoznak. Piridin C55 Szerkezete o A benzolhoz hasonló a felépítése,
itrogé ntartalmú hétérociklúsos végyú léték A nitrogéntartalmú heterociklusos vegyületek a természetben előforduló jelentős vegyületek közé tartoznak. Piridin C55 Szerkezete o A benzolhoz hasonló a felépítése,
Bevezetés. Szénvegyületek kémiája Organogén elemek (C, H, O, N) Életerő (vis vitalis)
 Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Tantárgycím: Szerves kémia
 Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
HALOGÉNEZETT SZÉNHIDROGÉNEK
 ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Részletes tematika: 1 hét (3 óra)
 Részletes tematika: 1 hét (3 óra) Telített Heterociklusos Vegyületek Előállítás. Konformációs Viszonyok. Reaktivitás Fontosabb N-, O- és S-Telített Heterociklusok. Penicillinek Nevezéktan, triviális név,
Részletes tematika: 1 hét (3 óra) Telített Heterociklusos Vegyületek Előállítás. Konformációs Viszonyok. Reaktivitás Fontosabb N-, O- és S-Telített Heterociklusok. Penicillinek Nevezéktan, triviális név,
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Budapest, augusztus 22. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
Szerves Kémia. Farmakológus szakasszisztens képzés 2012/2013 ősz
 Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Természetes színezékek
 Természetes színezékek Karotinoid színezékek: Magasabb rendű növények lipidjeiben oldva: sárga, narancssárga, vörös, ibolyaszínű. Kémiai szerkezet: 40 szénatom, konjugált kettős kötések, transz konfiguráció;
Természetes színezékek Karotinoid színezékek: Magasabb rendű növények lipidjeiben oldva: sárga, narancssárga, vörös, ibolyaszínű. Kémiai szerkezet: 40 szénatom, konjugált kettős kötések, transz konfiguráció;
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
β-dikarbonil-vegyületek szintetikus alkalmazásai
 β-dikarbonil-vegyületek szintetikus alkalmazásai A β-dikarbonil vegyületek tipikus szerkezeti egysége a két karbonilcsoport, melyeket egy metilén híd köt össze. Ezek a származékok két fontos tulajdonsággal
β-dikarbonil-vegyületek szintetikus alkalmazásai A β-dikarbonil vegyületek tipikus szerkezeti egysége a két karbonilcsoport, melyeket egy metilén híd köt össze. Ezek a származékok két fontos tulajdonsággal
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
O S O. a konfiguráció nem változik O C CH 3 O
 () ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
() ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
7. évfolyam kémia osztályozó- és pótvizsga követelményei Témakörök: 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2.
 7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
Szerves kémia Fontosabb vegyülettípusok
 Fontosabb vegyülettípusok Szénhidrogének: alifás telített (metán, etán, propán, bután, ) alifás telítetlen (etén, etin, ) aromás (benzol, toluol, naftalin) Oxigéntartalmú vegyületek: hidroxivegyületek
Fontosabb vegyülettípusok Szénhidrogének: alifás telített (metán, etán, propán, bután, ) alifás telítetlen (etén, etin, ) aromás (benzol, toluol, naftalin) Oxigéntartalmú vegyületek: hidroxivegyületek
Toluol (Bruckner II/1 476) µ= 0.33 Debye
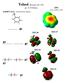 E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
OXOVEGYÜLETEK. Levezetés. Elnevezés O CH 2. O R C R' keton. O R C H aldehid. funkciós csoportok O. O CH oxocsoport karbonilcsoport formilcsoport
 XVEGYÜLETEK Levezetés 2 aldehid ' keton funkciós csoportok oxocsoport karbonilcsoport formilcsoport Elnevezés Aldehidek nyíltláncú (racionális név: alkánal) 3 2 2 butánal butiraldehid gyűrűs (cikloalkánkarbaldehid)
XVEGYÜLETEK Levezetés 2 aldehid ' keton funkciós csoportok oxocsoport karbonilcsoport formilcsoport Elnevezés Aldehidek nyíltláncú (racionális név: alkánal) 3 2 2 butánal butiraldehid gyűrűs (cikloalkánkarbaldehid)
Aromás vegyületek II. 4. előadás
 Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
1,3,5-trimetil-benzol. 2 3 m-metil-etil-benzol vagy m-etil-toluol CH3. izopropil-benzol(kumol) 1,8-dimetil-naftalin
 X.-XII. osztály, III. forduló, megoldás 011 / 01 es tanév, XVII. évfolyam 1. a) 1,,-trimetil-benzol o-metil-etil-benzol vagy o-etil-toluol 1,,4-trimetil-benzol 1,,5-trimetil-benzol m-metil-etil-benzol
X.-XII. osztály, III. forduló, megoldás 011 / 01 es tanév, XVII. évfolyam 1. a) 1,,-trimetil-benzol o-metil-etil-benzol vagy o-etil-toluol 1,,4-trimetil-benzol 1,,5-trimetil-benzol m-metil-etil-benzol
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
Részletes tematika: I. Félév: 1. Hét (4 óra): 2. hét (4 óra): 3. hét (4 óra): 4. hét (4 óra):
 Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Budapest, augusztus 26. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
Összefoglaló előadás. Sav-bázis elmélet
 Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
CHO H H H OH H OH OH H CH2OH HC OH HC OH HC OH CH 2
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
A tételek: Elméleti témakörök. Általános kémia
 A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Tartalomjegyzék. Szénhidrogének... 1
 Tartalomjegyzék Szénhidrogének... 1 Alkánok (Parafinok)... 1 A gyökök megnevezése... 2 Az elágazó szénláncú alkánok megnevezése... 3 Az alkánok izomériája... 4 Előállítás... 4 1) Szerves magnéziumvegyületekből...
Tartalomjegyzék Szénhidrogének... 1 Alkánok (Parafinok)... 1 A gyökök megnevezése... 2 Az elágazó szénláncú alkánok megnevezése... 3 Az alkánok izomériája... 4 Előállítás... 4 1) Szerves magnéziumvegyületekből...
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Budapest, február 1. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2017 tanév II. félév Az alaptárgy heti 3 óra ( hetente
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2017 tanév II. félév Az alaptárgy heti 3 óra ( hetente
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor)
 2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
Budapest, február 1. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2018 tanév II. félév Az alaptárgy heti 3 óra ( hetente
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2018 tanév II. félév Az alaptárgy heti 3 óra ( hetente
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
Kémia OKTV I. kategória II. forduló A feladatok megoldása
 ktatási ivatal Kémia KTV I. kategória 2008-2009. II. forduló A feladatok megoldása I. FELADATSR 1. A 6. E 11. A 16. C 2. A 7. C 12. D 17. B 3. E 8. D 13. A 18. C 4. D 9. C 14. B 19. C 5. B 10. E 15. E
ktatási ivatal Kémia KTV I. kategória 2008-2009. II. forduló A feladatok megoldása I. FELADATSR 1. A 6. E 11. A 16. C 2. A 7. C 12. D 17. B 3. E 8. D 13. A 18. C 4. D 9. C 14. B 19. C 5. B 10. E 15. E
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
8. Előadás Karbonsavak. Karbonsav származékok.
 8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
4) 0,1 M koncentrációjú brómos oldat térfogata, amely elszínteleníthető 0,01 mól alkénnel: a) 0,05 L; b) 2 L; c) 0,2 L; d) 500 ml; e) 100 ml
 1) A (CH 3 ) 2 C=C(CH 3 ) 2 (I) és CH 3 -C C-CH 3 (II) szénhidrogének esetében helyesek a következő kijelentések: a) A vegyületek racionális (IUPAC) nevei: 2-butén (I) és 2-butin (II) b) Az I-es telített
1) A (CH 3 ) 2 C=C(CH 3 ) 2 (I) és CH 3 -C C-CH 3 (II) szénhidrogének esetében helyesek a következő kijelentések: a) A vegyületek racionális (IUPAC) nevei: 2-butén (I) és 2-butin (II) b) Az I-es telített
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Kémia fogorvostan hallgatóknak Munkafüzet 13. hét
 Kémia fogorvostan hallgatóknak Munkafüzet 13. hét Szerves anyagok vizsgálata II. (174-176. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
Kémia fogorvostan hallgatóknak Munkafüzet 13. hét Szerves anyagok vizsgálata II. (174-176. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás, Nagy Veronika, Radó-Turcsi
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
8. Előadás. Karbonsavak. Karbonsav származékok.
 8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
Aminosavak általános képlete NH 2. Csoportosítás: R oldallánc szerkezete alapján: Semleges. Esszenciális aminosavak
 Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
A gázcsere alapjai, a légzési gázok szállítása
 A gázcsere alapjai, a légzési gázok szállítása Alapfogalmak szárazföldi gerincesek: a hatékony gázcseréhez a környezet és a sejtek közötti egyszerű diffúzió nem elég - légutak kialakítása (melegítés, párásítás,
A gázcsere alapjai, a légzési gázok szállítása Alapfogalmak szárazföldi gerincesek: a hatékony gázcseréhez a környezet és a sejtek közötti egyszerű diffúzió nem elég - légutak kialakítása (melegítés, párásítás,
