Preambulum. Komplexitásinformációtartalom. egy példa. biológia. kémia. sokaság-sokszínűség (kda) Szövet, organizmus. Sejt
|
|
|
- Anna Barta
- 7 évvel ezelőtt
- Látták:
Átírás
1 Preambulum Komplexitásinformációtartalom egy példa Szövet, organizmus biológia Sejt Szupramolekuláris komplexek és nanorendszerek Biomolekulák Biológiai kémia; a természetes vegyületek kémiája kémia sokaság-sokszínűség (kda) P Q= adenozin-5'-monofoszfát Q= dezoxiadenozin-5'-monofoszfát N Q N N N N 2
2 A biopolimerek három legfontosabb képviselője: -a peptidek és fehérjék - az oligo- és poliszacharidok - a nukleinsavak
3 Aminosav-, peptid- és fehérjekémiai kisszótár: Aminosavak: Elsődleges szerkezet: Esszenciális aminosavak: glicin, glikokoll <gör. glüküsz édes és kolla enyv szavakból>, Gly, G, 2 NC 2 C: az ecetsav α- aminoszármazéka, a húszféle fehérjealkotó aminosav között a legegyszerûbb és az egyetlen akirális. Színtelen, édes ízû, kristályos anyag, 233 C-on bomlik. Vízben jól, alkoholban, éterben nem oldódik. Szinte minden fehérjében megtalálható, legnagyobb mennyiségben a selyemfibroin és a zselatin tartalmazza. Az enyv savas hidrolizátumából különítette el elôször. Braconnot (1820). A ~ volt az elsô mesterségesen elôállított aminosav, a bróm-ecetsav és ammónia reakciójával nyerte W.. Perkin (1858). A formaldehid (C 2 ), hidrogén-cianid (CN) és ammónia (N 3 ) reakciójával elôállított amino-acetonitril ( 2 NC 2 CN) hidrolízise útján gyártják. Az élô szervezetben a glikolsav-ciklus tagjaként játszik fontos szerepet. Bár nem esszenciális aminosav, emberi és állati táplálékok kiegészítôje lehet, a nitrogénszükségletet fedezi. Az intravénás infúziós folyadékok egyik fô komponense. armadlagos szerkezet: Moduláris fehérje domének: Másodlagos szerkezet: Negyedleges szerkezet: Természetes aminosavak: Térszerkezet: Savasság (pka): Dipoláris ion: Iker (Zwitter) ion: Izoelektromos pont (pi): enderson-asselbalch equation: DL-aminosavak: Rezolválás: Enantiomer szelektív szintézis: Kaotróp:
4 Amid- v. peptidkötés: ligo- és polipeptidek: Parciális hidrolízis: ely specifikus hasítás (site-specific cleavage): Peptidszekvenálás: xitocin: Vazopresszin: Inzulin: Proteáz: idroláz: Kináz: Foszfatáz: emoglobin: Tripszin: Kimotripszin: Z-csoport: Boc-csoport: Fmoc-csoport: kinetikus rezolválás: mikor egy reakció sebessége az egyik enantiomer esetében lényegesen eltérő a másik enantiomerétől, és ezért az egyik sztereoizomer túlsúlyát kapjuk
5 Kapcsolás vegyesanhidriddel: Kapcsolás aktívészterrel: Automata peptidszintézis: ldatfázisú peptidszintézis: rtogonális védőcsoportok: Proteomics Genomics: α-hélix: β-redőzött réteg: PoliProlinII téralkat: Kollagén: Kanyar térszerkezetek: urok térszerkezetek: A coiled-coil téralkat: Diszulfidhíd: idrofób mag: Aktív centrum: Enzimspecificitás: Szubsztrát: Inhibitor: Sztereospecificitás: Kofaktor: Koenzim: Prosztetikus csoport: Lizozim:
6 Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai Nobel-díjak: James Batcheller Sumner 1946 Nobel-díj Az enzimek kristályosíthatóak John oward Northrop Wendell Meredith Stanley 1946 Nobel-díj Enzim és vírusfehérjék izolálása tisztítása Linus Pauling 1954 Nobel-díj fehérje szerkezet alapjai Vincent du Vigneaud 1955 Nobel-díj Biológiailag aktív kénvegyületek és polipeptid hormonok szintéziséért
7 Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai Nobel-díjak: Frederick Sanger 1958 Nobel-díj Az inzulin szekvenálása Sir John Cowdery Kendrew Ferdinand Max Perutz 1962 Nobel-díj xigén-transzport fehérjék szerkezetmeghatározása Christian B. Anfinsen 1972 Nobel-díj Ribonukleáz feltekeredése Bruce R. Merrifield 1984 Nobel-díj A szilárdfázisú peptidszintézis felfedezése Robert Brainard Corey ( ) Az α-hélix és a β-redő felfedezője
8 John B. Fenn Kurt Wüthrich Koichi Tanaka Nobel-díj 2002 makromolekulák szerkezetvizsgálati módszerek: NMR, MS Peter Agre Roderick MacKinnon Nobel-díj 2003 membrán csatornák mélyebb megértése Aaron Ciechanover Avram ershko Nobel-díj 2004 Az ubiquitin megjelöli azokat a fehérjéket, amelyeket a proteoszóma meg fog emészteni. Irwin Rose samu Shimomura Martin Chalfie Roger Y. Tsien Nobel-díj 2008 GFP-fehérjék
9 Az aminosavak peptidek és fehérjék koronázatlan királyai, orvosi Nobel-díjak: Frederick Grant Banting John James Richard Macleod 1923 Nobel-díj az inzulin felfedezéséért memo: Banting sértőnek és igazságtalannak találta, hogy asszisztensét Charles Best-et mellőzték, s ezért a díjat és az elismerést megosztotta vele. Ennek hatására Macleod is megosztotta az elismerést James Collip-pal. Az inzulinra vonatkozó szabadalmukat pedig - 1 dollár ellenében - átadták a Torontói Egyetemnek. A monomer formában aktív inzulint szervezetünk hexamerként tárolja. (6 is imidazol gyűrűje koordinálódik a Zn-ion köré, három-fogású szimmetriával. Charles Best James Collip
10 Az aminosavak peptidek és fehérjék koronázatlan királyai, orvosi Nobel-díjak: tto einrich Warburg 1931 Nobel-díj for his discovery of the nature and mode of action of the respiratory enzyme Axel ugo Theodor Theorell 1955 Nobel-díj for his discoveries concerning the nature and mode of action of oxidation enzymes Robert W. olley ar Gobind Khorana Marshall W. Nirenberg 1968 Nobel-díj for their interpretation of the genetic code and its function in protein synthesis
11 Az aminosavak peptidek és fehérjék koronázatlan királyai, orvosi Nobel-díjak: Gerald M. Edelman Rodney R. Porter 1972 Nobel-díj for their discoveries concerning the chemical structure of antibodies Roger Guillemin Andrew V. Schally 1977 Nobel-díj agyi peptid hormonok Rosalyn Yalow 1986 Nobel-díj for their discoveries of growth factors Stanley Cohen Rita Levi-Montalcini
12 Az aminosavak peptidek és fehérjék koronázatlan királyai, orvosi Nobel-díjak: Alfred G. Gilman Martin Rodbell 1994 Nobel-díj for their discovery of G-proteins and the role of these proteins in signal transduction in cells Günter Blobel 1999 Nobel-díj for the discovery that proteins have intrinsic signals that govern their transport and localization in the cell Stanley B. Prusiner 1997 Nobel-díj for his discovery of Prions - a new biological principle of infection
13 A legsokrétűbb biopolimer a fehérje; - katalizáló és szabályzó funkció (enzimek és hormonok) - jelző és jelátviteli funkció - szerkezeti funkciók (aktin, tubulin, kollagén, elasztin, keratin, stb.) - szállító fehérjék (pl. hemoglobin [oxigén], kazein [Ca 2+ ], ioncsatornák, stb.) - motorfehérjék (miozin, kinezin, dinein, stb.) - Minden sokrétűségük ellenére a fehérjék kémiailag igen konzervatív molekulák; csupán lineáris polimerek! elágazásmentes poliamidok tipikus építőelem
14 Az amid vagy peptidkötés kötésrendje és polaritása: határszerkezetek (rezonancia szerkezetek): C C N C C C N C tautomerek tautomerek C C N C C C N C határszerkezetek (rezonancia szerkezetek): Az amidkötésnek jelentős: - polaritása van (jelentős dipól ~3.5 Debye ) - kettőskötés jellege van a C-N kötés mentén.
15 A peptidkötés körüli geometriai izoméria: C C N C C C N transz és cisz izomerek C C C C N C C C N C C
16 Az aminosavak - szerkezet - előfordulása α-aminosav (β, γ, δ ) konstitúció L aminosav (D) konfiguráció fehérjealkotó (proteinogenic) α-l-aminosav természetes (natural) α-l-aminosav >200 fehérjealkotó (proteinogenic) α-l-aminosav összesen 22, ebből 20 az amelyik genetikailag kódolt, (spec. a yp és cisztin), memo: szelenocisztein) nélkülözhetetlen (essential) aminosav olyanok, amelyeket nem tud az organizmus de novo előállítani (humán pl. Ile, Arg, Lys, Met,..) Betegség: Kwashiorkór nem-szokványos (uncommon, non-standard) aminosavak: - fehérjékben (pl. yp) - fehérjéken kívül (pl. lantionin, 2-amino-izubutánsav, dehidroalanin)
17 Konfiguráció A fehérjealkotó (proteinogenic) α-aminosavak, a glicin kivételével mind királisak és a Cys kivételével mindegyik S-abszolút konfigurációjú. R C 2 Az alanin két enantiomerje 2 N 2 N C C 3 C N N C 2 N R R C C 2 C 2 C C 3 2 D- -alanin (R) 3 C 2 L- -alanin (S) az L- -aminosavak többnyire (S)-konf igurációjuak L-glicerinaldehid (S)
18 omokiralitás L-aminosav "S" 1 N 2 2 C 2 C 4 Q 3 1 N 2 4 Q 3 De: 2 N C 2 C glicin akirális 1 N 2 3 C 4 C 2 S 2 L-cisztein "R"
19 Két kiralitáscentrummal rendelkező aminosavak: C R N 2 2 N S C C R N 2 2 N S C S R R C 3 C 3 S C 3 C 3 C 2 5 C 2 5 D-treonin (2R,3S) L-treonin (2S,3R) D-izoleucin (2R,3R) L-izoleucin (2S,3S) C R N 2 2 N S C C R N 2 2 N S C R S C 3 S R C 3 C 3 C 3 C 2 5 C 2 5 allo-d-treonin (2R,3R) allo-l-treonin (2S,3S) allo-d-izoleucin (2R,3S) allo-l-izoleucin (2S,3R) (2X,3Y)-2-amino-3-hidroxibutánsav (2X,3Y)-2-amino-3-metilpentánsav
20 A konfiguráció jelentősége: L-aminosavak - L-Phe (phenylketonuria, PKU) genetikailag öröklődő anyagcserezavar (fenilalanin-hidroxiláz enzim hiánya, Phe nem bontódik le, idegrendszeri károsodás) - L-Glu (Monosodium glutamate, MSG [E621]) ízfokozó, (1-2 milló tonna/év) - Pht-glutárimid (Contergan, thalidomide) Racém aminosavak: - szintézis - rezolválás - kormeghatározás (sztereo szelektivitás szignifikánsan csökken az idővel, múmia) D-aminosavak a természetben: - D-Glu (baktériumsejtfal, pl. lépfene) - D-Ser (földigiliszta) - D-Pro (anyarozs) - D-Phe (antibiotikumok, pl. gramicidin) - D-Cys (antibiotikumok, pl. penicillin) N f talimido rész glutárimid rész thalidomid (contergan) egyik enantiomer teratogén kísérleteznek ma is vele, mint AIDS, agydaganat stb. elleni szer (S) vagy D-Cys N
21 Fehérjealkotó aminosavak: 2 N glicin Gly G esszenciális aminosavak Semleges oldallánccal rendelkező apoláris, alifás aminosavak: etimológia: glikokoll <gör. glüküsz édes és kolla enyv szavakból> az ecetsav α-aminoszármazéka, fehérjében csak kis mennyiségben (kivéve a kollagént, a selyemfibroint és a zselatint) előállítás először (. Braconnot 1820): enyv savas hidrolízise Az első mesterségesen szint. aminosav (W.. Perkin 1858): bróm-ecetsav + ammónia Gyártás ma: formaldehid (C 2 ) + hidrogén-cianid (CN) + ammónia (N 3 ) -> amino-acetonitril ( 2 NC 2 CN), amit hidrolízálunk Ala 2-aminopropánsav N 2 alanin Ala A N 2 valin Val V N 2 izoleucin Ile I N 2 leucin Leu L
22 Fehérjealkotó aminosavak: esszenciális aminosavak Semleges oldallánccal rendelkező apoláris, aromás aminosavak: fenilalanin Phe F N 2 tirozin Tyr Y 2 N N N 2 triptofán Trp W
23 Semleges oldallánccal rendelkező aminosavak: N 2 szerin Ser S N 2 treonin Thr T N N prolin Pro P hidroxiprolin yp S N 2 cisztein Cys C
24 Diszulfidkötés: R S [] tiol [] R S S R diszulfid BPTI
25 Semleges oldallánccal rendelkező aminosavak: S N 2 metionin Met M 2 N N 2 aszparagin Asn N 2 N glutamin Gln Q N 2
26 Savas oldallánccal rendelkező aminosavak: 2 N glutaminsav Glu E Bázikus oldallánccal rendelkező aminosavak: 2 N N 2 N lizin Lys K 2 N N N 2 arginin Arg R
27 Szisztematikus nevezéktan: IUPAC-IUB (Recommendations 1983) Ala 2-aminopropánsav Arg 2-amino-5-guanidinopentánsav Asn 2-amino-3-karbamoilpropánsav Glu 2-aminopentándisav is 2-amino-3(1-imidazol-4-il)propánsav Lys 2,5-diaminohexánsav Met 2-amino-4-(metilszulfanil)butánsav Trp 2-amino-3(1-indol-3-il)propánsav Tyr 2-amino-3-(4-hidroxifenil)propánsav Val 2-amino-3-metilbutánsav Kémiai tulajdonságok és következményei: savas és bázisos jelleg (acidity, basicity) polaritás (polarity) aromacitás (aromaticity) térkitöltés (bulkiness) konformációs flexibilitás (conformational flexibility) keresztkötés-hajlam (ability to Xlink) -kötés akceptor/donor (ability to -bond) kémiai reaktivitás (chemical reactivity)
28 Az aminosavak ikerionos szerkezete (avagy önmaga sója): Egy aminosavnak van mind bázikus (-N 2 ), mind savas (-C) csoportja, tehát amfoter. - gázfázisban neutrális, - szilárd vízmentes közegben dipoláris (iker- vagy zwitter-ionos), - vizes oldatban a p függvényében az egyensúlyi formák a jellemzőek: a kationos, az ikerionos vagy az anionos formák. Kajtár ha erősen savanyú a közeg főleg kation, - ha erősen bázikus a közeg főleg anion formában van jelen. A két p állapot között van az izoelektromos pont, IEP vagy pi, amikor az ikerionos forma koncentrációja a maximális, és a kationos és anionos formák egyensúlyban vannak egymással. 1) Az IEP-ban a molekula össztöltése zéró! 2) A pi minden aminosavra más és más (a konstitúció függvénye), ami kihasználható a jellemzésükre is. pi = ½ (pk a1 +pk a2 ) így az alanin izoelektromos pontja ½ (2,3+9,7) = 6,0
29 Tények, amelyek alátámasztják az aminosavak dipoláris jellegét: 1) igen magas (op.> 200 C) olvadáspont (amit bomlás pl. C 2 vesztés kísér) Ala 297 C, Ala.Cl 204 C Glu 248 C, Ala.Cl 214 C Gly 233 C, Ala.Cl 182 C Lys 224 C, Ala.Cl 263 C 2) Vízben jobban oldódnak (hidratáció), mint Et 2, C 2 Cl 2 és más szerves oldószerekben (szolvatáció) 3) Akár egy nagyságrenddel nagyobb a dipólus momentumuk, mint az egyszerű karbonsavaké vagy alifás aminoké: (D=Debye) 4) az ikerionos forma kevésbé savanyú, mint egy alifás karbonsav és kevésbé bázikus, mint egy alkilamin: memo: az ikerion nem -, hanem N-sav és nem N-, hanem -bázis!
30 rekollekció: savak és bázisok erőssége: K a és pk a A Cl vagy 2 S 4 tól eltérően a szerves karbonsavak gyenge savak T= 25 o C csak ~1% az Ac az egyensúlyi reakció jellemzése: K a egyensúlyi együttható K eq = C 3 C 3 C 3 C 2 K a = K eq 2 = C 3 C 3 C C Mivel a víz koncentrációja közel állandó (55,5M), ezért célszerű bevezetni K a -t a savi egyensúlyi együtthatót. Pl: hangyasavra; K a C = 1, , ecetsavra; K a Ac = 1, (memo: Praktikusabb a pk a = lgk a = log 10 (K a ) értéket megadni Néhány pk a érték: 1,4 (N 3 ), 0,18(TFA), 3,7( 2 C 3 ), 4,75(Ac), 9,9(fenol), 38(N 3 ) és 50(etán) 3 ha K a értéke nagy, akkor erős, ha kicsi, akkor gyenge a sav) pka analóg a p definíciójával növekvő savi erősség memo: C 3 C 2 C 3 C CF 3 C Cl pk a= 16 < 4,75 < 0,2 < esetén csak minden százezredik molekula deprotonált -7 esetén csak minden tízmilliomodik molekula protonált.
31 Emlékeztető kérdések: kérdés: mekkora a hidroxóniumion és mekkora a C 2 koncentráció a hangyasav 0,1M-os vizes oldatában (K a = 1, )? A hangyasav hány százaléka ionizált ekkor? Legyen x mind a [ 3 + ] mind a [C 2 ] és így (0,1 x) a [C]. Mivel K a kicsi ezért x értéke is kicsi és így (0,1 x)~ 0,1 tehát x 2 /0,1 = azaz x = 0,0042M (4,2mM), Az ionizáció mértéke (%) = 0,0042/0,1 *100 = 4,2% kérdés: mekkora a víz K a -ja, ha abba 25 o C-on az [ ]=10 7? válasz: K a =(10 7 )*(10 7 )/55,5 = 1, tehát a pka = 15.7 kérdés: az egyik sav K a ja 10-7 a másiké pedig +5. Melyik az erősebb sav? válasz: pk a = (log 10 7 ) = 7 valamint pk a = (log 5) = 0,699, tehát a második az erősebb sav.
32 Iker- vagy Zwitterion C C memo: az ecetsav disszociációja: + pk = 4,8 C C: 2 N C C Q + 3 N C C: 2 N C C: + Q Q pk 1 = 2,4 pk 2 = 9,6 pk a1 = első savi disszociációs állandó pk a2 = második savi disszociációs állandó memo: a metilamin disszociációja: 3 N C + 2 N C pk = 10,6
33 Aminosav pk a1 pk a2 pk a3 pi α-c α-n + 3 R-csoport semlegesek G Gly 2,3 9,6 6,0 A Ala 2,3 9,7 6,0 V Val 2,3 9,6 6,0 L Leu 2,4 9,6 6,0 I Ile 2,4 9,7 6,1 F Phe 1,8 9,1 5,5 Y Tyr 2,2 9,1 10,1 5,7 W Trp 2,4 9,4 5,9 S Ser 2,2 9,2 5,7 T Thr 2,6 10,4 6,5 P Pro 2,0 10,6 6,3 yp 1,9 9,7 6,3 C Cys 1,7 10,8 8,3 5,0 Cys-Cys 1,6; 2,3 7,9; 9,9 5,1 M Met 2,3 9,2 5,8 N Asn 2,0 8,8 5,4 Q Gln 2,2 9,1 5,7
34 Aminosav pk a1 pk a2 pk a3 pi α-c α-n + 3 R-csoport savasak D Asp 2,1 9,8 3,9 3,0 E Glu 2,2 9,7 4,3 3,2 bázikusak protonált R-csoport K Lys 2,2 9,0 10,5 9,8 R Arg 2,2 9,0 12,5 10,8 is 1,8 9,2 6,0 7,6 memo: egy α-aminosav (de nem az ikerion) a konjugáció miatt erősebb sav, mint a megfelelő alifás karbonsav: 3 N alanin kation (pk a1 =2,3) 3 N alanin ikerion pk a2 =9.7
35 Sav és konjugált bázisának egyensúlya: A A + Η + enderson-asselbalch-egyenlet: pk a = p + lg([a]/[a ]) A levezetés: K a = [+ ] [A ] [A] [ + ] = K a [A] [A ] [A] pk a = p + log [A ] [A] log [ + ] = log K a log [A ] p = pk a [A] log [A ] a savi disszociációs állandó, pk a tehát az a p érték, - ahol a sav félig semlegesített, azaz [A]=[A ]. indoklás (bizonyítás): mivel pk a = p ezért 0 = log([a]/[a ]), azaz 1= [A]/[A ] s ez pont az amit állítottunk!
36 kérdés: mire jó a enderson asselbalch egyenlet? válasz: ha tudjuk egy ionizálható csoport pk a értékét, akkor a &- egyenlet segítségével meg tudjuk határozni annak töltését, pontosabban a [A]/[A ] értéket a p függvényében gyakorlat: a például a p=(pk a 2), akkor a & szerint +2 = lg[a]/[a ] azaz 100[A ]=[A], vagyis a funkciós csoport ~99%-ban protonált, s így annak kémiai jellege függvényében töltése vagy 0, vagy +1. a a p=(pk a +2), akkor a & szerint -2 = lg[a]/[a ] azaz 0,01[A ]=[A], vagyis a funkciós csoport ~99%-ban deprotonált, s így a kémiai jellegének függvényében töltése vagy -1, vagy 0. a a p=pk a, akkor a & szerint 0 = lg[a]/[a ] azaz [A ]= [A], vagyis a funkcióscsoport 50%-ban deprotonált Ez a ±2 szabály (K a =±2), a protonáltsági fokra ad jó kvalitatív becslést.
37 A glicin titrálása, avagy p kontrolált töltésállapotok: 100% 3 N C 2 C: Izoelektromos pont Isoelectric point, pi 2,4 + 9,6 2 = 6,0 2 N C 2 C pk 1 pk p=2,3 p= 6,0 50% 50% p=9,6 p>11.5, akkor lényegében csak anion van jelen az oldatban. p=9.6, akkor az ikerionos forma fele már az anionos formává alakult át. 2 N C 2 C: p=6, akkor az összes kationos forma már ikerion formává alakult át. p=2.3, akkor a kationos forma fele már ikerion formává alakult át. p<1 akkor lényegében csak kation van jelen az oldatban.
38 Savas oldallánccal rendelkező aminosavak pi = ½ (pk a1 +pk a2 ) így az aszparaginsav izoelektromos pontja ½ (2,1+3,9) = 3,0 aszparaginsav
39 Az aszparaginsav titrálása aszparaginsav 1,9 + 3,6 2 = 2,75 pi = 3,0 3 N C C: C 2 C pk 1 pk 2 pk p 2,1 p 3,9 p 9,8 3 N C C C 2 C 2 N C C: C 2 C: 2 N C C: C 2 C:
40 Bázikus oldallánccal rendelkező aminosavak pi = ½ (pk a2 +pk a3 ), így a lizin izoelektromos pontja ½ (9,0+10,5) = 9,8
41 9,0 + 10,5 = 9,75 2 pi = 9,75 3 N C C: C 2 N 2 pk 1 pk 2 pk p 2,2 p 9,0 p 10,5 3 N C C (C 2 ) n N 3 2 N C C: (C 2 ) n N 2 2 N C C: (C 2 ) n N 2
42 A hisztidin titrálása 3 N C C: C 2 6,0 + 9,2 2 = 7,6 : N : N pi = 7,6 pk 1 pk 2 p K 3 pk p 1,8 p 6,0 p 9,2 p 15 3 N C C C 2 N : N 3 N C C: C 2 : N N 3 N C C: 2 N C C: C 2 C 2 : N : N : : : N : N
43 Az elektroforézis: The distribution of charged species in a sample can be shown experimentally by observing the movement of solute molecules in an electric field, using the technique of electrophoresis. Kísérleti körülmények: For such experiments an ionic buffer solution is incorporated in a solid matrix layer, composed of paper or a crosslinked gelatin-like substance. A kísérlet kivitelezésének módja: A small amount of the amino acid, peptide or protein sample is placed near the center of the matrix strip and an electric potential is applied at the ends of the strip. The solid structure of the matrix retards the diffusion of the solute molecules, which will remain where they are inserted, unless acted upon by the electrostatic potential. Példa: In the example shown here, four different amino acids are examined simultaneously in a p= 6.00 buffered medium.
44 Note that the colors in the display are only a convenient reference, since these amino acids are colorless.
45 Megfigyelés: 1) At p 6.00 Ala (alanine) and Ile (isoleucine) exist on average as neutral zwitterionic molecules and are not influenced by the electric field. 2) Arg (arginine) is a basic amino acid. Both base functions exist as "onium" conjugate acids in the p 6.00 matrix. The solute molecules of arginine therefore carry an excess positive charge, and they move toward the cathode. 3) The two carboxyl functions in Asp (aspartic acid) are both ionized at p 6.00, and the negatively charged solute molecules move toward the anode in the electric field. Megfigyelés és következtetések: It should be clear that the result of this experiment is critically dependent on the p of the matrix buffer. 1) If we were to repeat the electrophoresis of these compounds at a p of 3.00, the aspartic acid would remain at its point of origin, and the other amino acids would move toward the cathode. 2) Ignoring differences in molecular size and shape, the arginine would move twice as fast as the alanine and isoleucine because its solute molecules on average would carry a double positive charge.
46 fford-féle szabály: µ A = k z A M A 2/3 µ = mozgékonyság z = töltés M = molekulatömeg k = koefficiens fford-féle szabály alkalmazása: µ rel = µ A µ B = z A z B M B M A 2/3
47 Peptidek/fehérjék töltésviszonyai, fehérjék: komplex titrálási görbe N C C N C C N C C N C C N C C C C 2 3 C C 3 C C 2 S :N :N (C 2 ) 4 N 2 p p
48 α-aminosavak előállítása (pl.: Met) 1) módosított Gabriel-szintézissel kálium-ftálimidből
49 memo: aminok előállítása R-X + 2N 3 R-N 2 + N 4 X ahol X=F, Cl, Br alkil-halogenid alkil-amin Bruckner I/ o. gond: keveréket kapunk (R-N 2, R 2 N, R 3 N és R 4 NX) túlalkileződés primer szek. terc. kvat. 1. Primer aminok előállítása: (Gabriel-féle szint. 1887) N K -KBr Br R N-R ftálsav 2. Szekunder aminok előállítása: f tálimid-kálium N-alkilf tálimid 3 C C 3 C C + R'Br N R N R R' primer savamid szekunder savamid 3. Tercier aminok előállítása: szekunder aminok reakciója alkil-halogenidekkel. cc. Cl fõzés + R-N 2 C 3 -C R'R-N szekunder amin
50 α-aminosavak előállítása (pl.: Met) 2) Strecker-szintézis R CN N 3 CN R N ,hõ C R N 3 -amino-nitril DL- -aminosav A Strecker-szintézis mechanizmusa:
51 DL-aminosavak rezolválása C + R N 3 C R + N 3 racém elegy R R + C N 3 C N 3 (C 3 C) 2 R C N N-acil-aminosav egy (R)-konfigurációjúak L-α-aminosav egy (S)-konfigurációjúak L-α-aminosav deaciláz enzim R L- -aminosav C N D-N-acil-aminosav memo: a legtöbb enzim zsebe enantiospecifikus felismerő képességgel rendelkezik.
52 aszimmetrikus szintézis: C 3 C 3 C C NCC 3 2 [(Rh(R,R)-DiPAMP)cod] + BF 4 katalizátor C 3 C + 3 C C 3 C 100% kitermelás 95% enantioszelektivitás NCC 3 N 2 L-DPA (S)-3,4-dihidroxifenilalanin C 3 P P C 3 (R,R)-DiPAMP (R,R)-1,2-bisz[(2-metoxi-fenil)-fenil-foszfino]etán ródium királis liganduma cod 1,5-ciklooktadién
53 C NCC 3 katalitikus aszimmetrikus hidrogénezés 83% enantioszelektivitás (1) 2 / (R,R)-PNNP-Rh(I) (2) C 3, A 97% enantioszelektivitás átkristályosítás után C CC 3 CC 3 N 2 2 N S-fenilalanin-metilészter L-aszparaginsav N 2 N CC 3 C aszpartám 3 C N N C 3 P P (R,R)-PNNP N,N'-bisz(difenil-foszfino)-bisz[(R)-1-fenil-etil]etiléndiamin ródium királis liganduma
54 [Rh(nbd) 2 ]Cl 4 (R)-profosz [Rh((R)-profosz)(nbd)]Cl 4 + nbd királis ródium-komplex 7 3 C (C 6 5 ) 2 P P(C 6 5 ) 2 (R)-profosz (R)-1,2-bisz(difenil-foszfino)-propán 5 4 nbd 2,5-norbornadién 3 C 2 C (1), 2, hõ C NCC 3 [Rh((R)-profosz)() 2 (C 2 5 ) 2 ] + N 2 (2) N3 2-acetilamino-propénsav N-acetil-L-alanin 90% enanetioszelektivitás L-alanin R C NCC 3 (Z)-3-szubsztituált 2-acetilamino-propénsav (1) 2 / [Rh((R)-profosz)() 2 (oldószer) 2 ] + (2), 2, hõ (3) N3 C L-aminosav 87-93% enanetioszelektivitás
aminosav!-aminosav természetes (natural)!-aminosav >200 fehérjealkotó (proteinogenic)!-aminosav genetikailag kódolt
 aminosav!-aminosav természetes (natural)!-aminosav >00 fehérjealkotó (proteinogenic)!-aminosav genetikailag kódolt 0 + 1 nélkülözhetetlen (essential) aminosav nemszokványos (uncommon) aminosav glicin alanin
aminosav!-aminosav természetes (natural)!-aminosav >00 fehérjealkotó (proteinogenic)!-aminosav genetikailag kódolt 0 + 1 nélkülözhetetlen (essential) aminosav nemszokványos (uncommon) aminosav glicin alanin
Aminosavak általános képlete NH 2. Csoportosítás: R oldallánc szerkezete alapján: Semleges. Esszenciális aminosavak
 Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Preambulum: az élet hajnala és a víz
 Preambulum: az élet hajnala és a víz Szilárd kéreg és Ősatmoszféra (>4,5 milliárd éve ): forróság, C 2, vízgőz - Vizek áramlása ás körforgása: gradiens (vízpára, eső, patak, folyó, tó, óceán,..) - földön
Preambulum: az élet hajnala és a víz Szilárd kéreg és Ősatmoszféra (>4,5 milliárd éve ): forróság, C 2, vízgőz - Vizek áramlása ás körforgása: gradiens (vízpára, eső, patak, folyó, tó, óceán,..) - földön
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Hullámok és harmonikus felhangjaik feltérjék a forrást
 Hullámok és harmonikus felhangjaik feltérjék a forrást következtetés: a hangok (frekvenciák) visszatükrözik a hang forrását: a hegedűt vagy a zongorát. A Wilkinson mikrohullámú anizotrópia szonda (Wilkinson
Hullámok és harmonikus felhangjaik feltérjék a forrást következtetés: a hangok (frekvenciák) visszatükrözik a hang forrását: a hegedűt vagy a zongorát. A Wilkinson mikrohullámú anizotrópia szonda (Wilkinson
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai Nobel-díjak:
 Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai obel-díjak: Linus Pauling 1954 obel-díj fehérje szerkezet alapjai Frederick Sanger 1958 obel-díj Az inzulin szekvenálása Sir. John owdery
Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai obel-díjak: Linus Pauling 1954 obel-díj fehérje szerkezet alapjai Frederick Sanger 1958 obel-díj Az inzulin szekvenálása Sir. John owdery
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
4. FEHÉRJÉK. 2. Vázanyagok. Az izmok alkotórésze (pl.: a miozin). Inak, izületek, csontok szerves komponensei, az ún. vázfehérjék (szkleroproteinek).
 4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
INFORMATIKA EMELT SZINT%
 Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
A fehérjék hierarchikus szerkezete
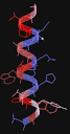 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Bioinformatika 2 5.. előad
 5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
Aminosavak, peptidek, fehérjék. Béres Csilla
 Aminosavak, peptidek, fehérjék Béres Csilla Aminosavak Az aminosavak (más néven aminokarbonsavak) olyan szerves vegyületek, amelyek molekulájában aminocsoport (- NH 2 ) és karboxilcsoport (-COOH) egyaránt
Aminosavak, peptidek, fehérjék Béres Csilla Aminosavak Az aminosavak (más néven aminokarbonsavak) olyan szerves vegyületek, amelyek molekulájában aminocsoport (- NH 2 ) és karboxilcsoport (-COOH) egyaránt
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Toluol (Bruckner II/1 476) µ= 0.33 Debye
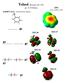 E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
(11) Lajstromszám: E 007 952 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
!HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
KARBONSAV-SZÁRMAZÉKOK
 KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
A tejfehérje és a fehérjeellátás
 A tejfehérje A tejfehérje és a fehérjeellátás Fejlődő országok: a lakosság 20 30%-a hiányosan ellátott fehérjével. Fejlett ipari országok: fehérje túlfogyasztás. Az emberiség éves fehérjeszükséglete: 60
A tejfehérje A tejfehérje és a fehérjeellátás Fejlődő országok: a lakosság 20 30%-a hiányosan ellátott fehérjével. Fejlett ipari országok: fehérje túlfogyasztás. Az emberiség éves fehérjeszükséglete: 60
Szabó Dénes Molekulák és reakciók három dimenzióban
 Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Peptidek (savamidok) szintézise. feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik.
 Peptidek (savamidok) szintézise feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik. 1 avamidok (peptidek) szintézise és hidrolízise megfigyelés:
Peptidek (savamidok) szintézise feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik. 1 avamidok (peptidek) szintézise és hidrolízise megfigyelés:
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
,:/ " \ OH OH OH - 6 - / \ O / H / H HO-CH, O, CH CH - OH ,\ / "CH - ~(H CH,-OH \OH. ,-\ ce/luló z 5zer.~ezere
 - 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
- 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
Aminosavak, peptidek, fehérjék. Szerkezet, előállítás, kémiai tulajdonság
 Aminosavak, peptidek, fehérjék Szerkezet, előállítás, kémiai tulajdonság Aminosavak Aminosavaknak nevezzük azokat a karbonsavakat, amelyekben a szénlánc egy vagy több hidrogénjét amino (NH 2 ) csoportra
Aminosavak, peptidek, fehérjék Szerkezet, előállítás, kémiai tulajdonság Aminosavak Aminosavaknak nevezzük azokat a karbonsavakat, amelyekben a szénlánc egy vagy több hidrogénjét amino (NH 2 ) csoportra
A fehérjék hierarchikus szerkezete. Szerkezeti hierarchia. A fehérjék építőkövei az aminosavak. Fehérjék felosztása
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
A kémiatanári zárószigorlat tételsora
 1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
Aminosavak, peptidek, fehérjék
 Aminosavak, peptidek, fehérjék Jelentőség Protein (Berzelius: protos, proteios) ligo- és polipepitdek (hormonok) Önmagában hormon és neurotranszmitter Aminosav bifunkciós vegyület Aminocsoport Karboxilcsoport
Aminosavak, peptidek, fehérjék Jelentőség Protein (Berzelius: protos, proteios) ligo- és polipepitdek (hormonok) Önmagában hormon és neurotranszmitter Aminosav bifunkciós vegyület Aminocsoport Karboxilcsoport
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
3. Aminosavak gyártása
 3. Aminosavak gyártása Előállításuk Fehérje-hidrolizátumokból: cisztein, leucin, aszparaginsav, tirozin, glutaminsav Kémiai szintézissel: metionin, glicin, alanin, triptofán (reszolválás szükséges) Biotechnológiai
3. Aminosavak gyártása Előállításuk Fehérje-hidrolizátumokból: cisztein, leucin, aszparaginsav, tirozin, glutaminsav Kémiai szintézissel: metionin, glicin, alanin, triptofán (reszolválás szükséges) Biotechnológiai
A gyógyszerek és a kiralitás
 Szent László TÖK A gyógyszerek és a kiralitás Dr. Zsigmond Ágnes SZTE Szerves Kémiai Tanszék Budapest, 2012.04.26. Vázlat Mi az a kiralitás? A kiralitás és a gyógyszerek. A királis katalizátorok alkalmazása.
Szent László TÖK A gyógyszerek és a kiralitás Dr. Zsigmond Ágnes SZTE Szerves Kémiai Tanszék Budapest, 2012.04.26. Vázlat Mi az a kiralitás? A kiralitás és a gyógyszerek. A királis katalizátorok alkalmazása.
HALOGÉNEZETT SZÉNHIDROGÉNEK
 ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
AquaWorld Resort, Budapest 2017 április
 AquaWorld Resort, Budapest 2017 április 27-28. História Hungalimentaria 2015. április 22-23. AquaWorld AquaWorld Resort, Budapest 2017 április 27-28. 20 év Hungalimentaria 2017. április 26-27. Budapest
AquaWorld Resort, Budapest 2017 április 27-28. História Hungalimentaria 2015. április 22-23. AquaWorld AquaWorld Resort, Budapest 2017 április 27-28. 20 év Hungalimentaria 2017. április 26-27. Budapest
TAKARMÁNYOZÁSTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Takarmányok fehérjetartalma Az állati szervezet létfontosságú vegyületei fehérje természetűek Az állati termékek
TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Takarmányok fehérjetartalma Az állati szervezet létfontosságú vegyületei fehérje természetűek Az állati termékek
2. Aminosavak - Treonin
 Az aminosavak felhasználása nátrium-glutamát ízfokozó (Delikát, Vegeta) lizin, metionin, treonin, triptofán takarmány- és élelmiszerkiegészítő aszparaginsav és fenilalanin aszpartám édesítőszer gyártásához
Az aminosavak felhasználása nátrium-glutamát ízfokozó (Delikát, Vegeta) lizin, metionin, treonin, triptofán takarmány- és élelmiszerkiegészítő aszparaginsav és fenilalanin aszpartám édesítőszer gyártásához
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
1. Tömegszámváltozás nélkül milyen részecskéket bocsáthatnak ki magukból a bomlékony atommagok?
 A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának feladatlapja KÉMIÁBÓL I-II. kategória I. FELADATSOR Az I. feladatsorban húsz kérdés szerepel. Minden kérdés után
A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának feladatlapja KÉMIÁBÓL I-II. kategória I. FELADATSOR Az I. feladatsorban húsz kérdés szerepel. Minden kérdés után
Kolloidstabilitás. Berka Márta 2010/2011/II
 Kolloidstabilitás Berka Márta 2010/2011/II Kolloid stabilitáshoz taszítás kell. Sztérikus stabilizálás V R V S sztérikus stabilizálás: liofil kolloidok alkalmazása védőhatás adszorpció révén (természetes
Kolloidstabilitás Berka Márta 2010/2011/II Kolloid stabilitáshoz taszítás kell. Sztérikus stabilizálás V R V S sztérikus stabilizálás: liofil kolloidok alkalmazása védőhatás adszorpció révén (természetes
Oligo- és polipeptidek:
 ligo- és polipeptidek: 1) Amid kötés hidrolízise és szintézise 2) Amid kötés kialakítása: preparatív lehetőségek 2.1) savkloridok 2.2) savanhidridek 2.3) aktívészterek 3) Aminosavak összekapcsolása 4)
ligo- és polipeptidek: 1) Amid kötés hidrolízise és szintézise 2) Amid kötés kialakítása: preparatív lehetőségek 2.1) savkloridok 2.2) savanhidridek 2.3) aktívészterek 3) Aminosavak összekapcsolása 4)
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
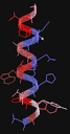 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel
 Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció. Szinaptikus jelátvitel.
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
Az aminosav anyagcsere orvosi vonatkozásai Csősz Éva
 Az aminosav anyagcsere orvosi vonatkozásai Csősz Éva E-mail: cseva@med.unideb.hu Általános reakciók az aminosav anyagcserében 1. Nitrogén eltávolítás: transzaminálás dezaminálás: oxidatív nem oxidatív
Az aminosav anyagcsere orvosi vonatkozásai Csősz Éva E-mail: cseva@med.unideb.hu Általános reakciók az aminosav anyagcserében 1. Nitrogén eltávolítás: transzaminálás dezaminálás: oxidatív nem oxidatív
Enzimek. Enzimek! IUBMB: szisztematikus nevek. Enzimek jellemzése! acetilkolin-észteráz! legalább 10 nagyságrend gyorsulás. szubsztrát-specificitás
 Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
AMINOSAVAK, PEPTIDEK, FEHÉRJÉK
 AMISAVAK, PEPTIDEK, FEÉJÉK Aminosavak szerkezete, fizikai, kémiai tulajdonságai, biokémiai szerepük. Konvenció szerinti rövidítések. Aminosavak szintézise. A kötés szerkezete. Peptidszintézisek, védőcsoportok,
AMISAVAK, PEPTIDEK, FEÉJÉK Aminosavak szerkezete, fizikai, kémiai tulajdonságai, biokémiai szerepük. Konvenció szerinti rövidítések. Aminosavak szintézise. A kötés szerkezete. Peptidszintézisek, védőcsoportok,
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
HŐ (q) és MUNKA (w): energia átmenet közben a rendszer és környezete között. A különböző energiafajták átalakulásukkor végső soron termikus energiává
 TERMODINAMIKA 1 HŐ (q) és MUNKA (w): energia átmenet közben a rendszer és környezete között. A különböző energiafajták átalakulásukkor végső soron termikus energiává degradálódnak (disszipáció). BELSŐ
TERMODINAMIKA 1 HŐ (q) és MUNKA (w): energia átmenet közben a rendszer és környezete között. A különböző energiafajták átalakulásukkor végső soron termikus energiává degradálódnak (disszipáció). BELSŐ
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
Sav bázis egyensúlyok vizes oldatban
 Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
Sav bázis egyensúlyok vizes oldatban Disszociációs egyensúlyi állandó HAc H + + Ac - ecetsav disszociációja [H + ] [Ac - ] K sav = [HAc] NH 4 OH NH 4 + + OH - [NH + 4 ] [OH - ] K bázis = [ NH 4 OH] Ammóniumhidroxid
hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) olajsav (cisz-9 oktadecénsav) néhány, állatokban előforduló zsírsav
 Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
1. feladat (3 pont) Az 1,2-dibrómetán főként az anti-periplanáris konformációban létezik, így A C-Br dipólok kioltják egymást, a molekula apoláris.
 1. feladat (3 pont) Az 1,2-dibrómetán apoláris molekula. Az etilénglikol (etán-1,2-diol) molekulának azonban mérhető dipólusmomentuma van. Mi ennek a magyarázata? Az 1,2-dibrómetán főként az anti-periplanáris
1. feladat (3 pont) Az 1,2-dibrómetán apoláris molekula. Az etilénglikol (etán-1,2-diol) molekulának azonban mérhető dipólusmomentuma van. Mi ennek a magyarázata? Az 1,2-dibrómetán főként az anti-periplanáris
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Aminosavak, peptidek
 Aminosavak, peptidek Aminosavak Neutrális aminosavak + H 3 N C O O - C H + H 3 N + H 3 N COO- COO- C H CH H CH 3 CH 3 CH 3 H 3 N glicin (Gly) alanin (Ala) valin (Val) C O O - + + C C H 2 H H 3 N H COO-
Aminosavak, peptidek Aminosavak Neutrális aminosavak + H 3 N C O O - C H + H 3 N + H 3 N COO- COO- C H CH H CH 3 CH 3 CH 3 H 3 N glicin (Gly) alanin (Ala) valin (Val) C O O - + + C C H 2 H H 3 N H COO-
Az idegsejtek kommunikációja. a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Indikátorok. brómtimolkék
 Indikátorok brómtimolkék A vöröskáposzta kivonat, mint indikátor Antociánok 12 40 mg/100 g ph Bodzában, ribizliben is! A szupersavak Szupersav: a kénsavnál erősebb sav Hammett savassági függvény: a savak
Indikátorok brómtimolkék A vöröskáposzta kivonat, mint indikátor Antociánok 12 40 mg/100 g ph Bodzában, ribizliben is! A szupersavak Szupersav: a kénsavnál erősebb sav Hammett savassági függvény: a savak
Táplálkozási ismeretek. Fehérjék. fehérjéinek és egyéb. amelyeket
 Táplálkozási ismeretek haladóknak I. Az előző három fejezetben megismerkedtünk az alapokkal (táplálék-piramis, alapanyag-csere, napi energiaszükséglet, tápanyagok energiatartalma, naponta szükséges fehérje,
Táplálkozási ismeretek haladóknak I. Az előző három fejezetben megismerkedtünk az alapokkal (táplálék-piramis, alapanyag-csere, napi energiaszükséglet, tápanyagok energiatartalma, naponta szükséges fehérje,
A bórsavtól a lipofil karboránt tartalmazó peptidomimetikumokig
 A bórsavtól a lipofil karboránt tartalmazó peptidomimetikumokig Egy "új" elem" " a növényvédelmi kémiában? Ujváry István MTA Növényvédelmi Kutatóintézete Bruckner-termi előadások,, 1999. október 29. ELTE,
A bórsavtól a lipofil karboránt tartalmazó peptidomimetikumokig Egy "új" elem" " a növényvédelmi kémiában? Ujváry István MTA Növényvédelmi Kutatóintézete Bruckner-termi előadások,, 1999. október 29. ELTE,
Nagyhatékonyságú folyadékkromatográfia (HPLC)
 Nagyhatékonyságú folyadékkromatográfia (HPLC) Kromatográfiás módszerek osztályba sorolása 2 Elúciós technika A mintabevitel ún. dugószerűen történik A mozgófázis a kromatogram kifejlesztése alatt folyamatosan
Nagyhatékonyságú folyadékkromatográfia (HPLC) Kromatográfiás módszerek osztályba sorolása 2 Elúciós technika A mintabevitel ún. dugószerűen történik A mozgófázis a kromatogram kifejlesztése alatt folyamatosan
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Szerves Kémiai Problémamegoldó Verseny 2014. április 25. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Név: Pontszám: / 3 pont. 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét!
 Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Név: Pontszám: / 3 pont 1. feladat Adja meg a hiányzó vegyületek szerkezeti képletét! Név: Pontszám: / 4 pont 2. feladat Az ábrán látható vegyületnek a) hány sztereoizomerje, b) hány enantiomerje van?
Enzim-katalizált (biokatalitikus) reakcióutak tervezése. Schönstein László Enzimtechnológiai Fejlesztő Csoport Debrecen, November 11.
 Enzim-katalizált (biokatalitikus) reakcióutak tervezése Schönstein László Enzimtechnológiai Fejlesztő Csoport Debrecen, 2016. November 11. ENANTIOMEREK JELENTŐSÉGE A GYÓGYSZERKUTATÁSBAN Mik az enantiomerek?
Enzim-katalizált (biokatalitikus) reakcióutak tervezése Schönstein László Enzimtechnológiai Fejlesztő Csoport Debrecen, 2016. November 11. ENANTIOMEREK JELENTŐSÉGE A GYÓGYSZERKUTATÁSBAN Mik az enantiomerek?
ZÁRÓJELENTÉS. OAc. COOMe. N Br
 ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
AMINOSAVAK, FEHÉRJÉK
 AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
Kémiai alapismeretek 6. hét
 Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
