Bár az elő szervezetek 70 95%-a víz, a többi elsősorban szénalapú vegyületekből áll
|
|
|
- Brigitta Fehérné
- 8 évvel ezelőtt
- Látták:
Átírás
1 Szén a szerves molekulák alapja Bár az elő szervezetek 70 95%-a víz, a többi elsősorban szénalapú vegyületekből áll A szén példátlan képessége, hogy nagyméretű, komplex, különböző molekulákat képes kialakítani 1828 Wöhler karbamid szintézise (Kohlbe, ecetsav) cáfolja az életerőt
2 Urea
3 Miller kísérlete (1953) Vízgőz CH 4 Atmoszféra Elektróda Kondenzáló Szerves molekulákat tartalmazó hűtött víz hideg víz Számos szerves molekula képződött, köztük formaldehid, hidrogén cianid, valamint aminosavak, szénhidrogének H 2 O tenger Mintavétel a kémiai analízishez
4 A szénlánc többféle formát is felvehet: Etán Propán 1-Butén 2-Butén (a) Változó hossz (c) Kettős kötés Bután (b) Elágazás 2-Metil propán (izobután) Ciklohexán (d) Gyűrűk Benzén
5 Izomerek Az Izomerek azonos molekuláris formulával leírható, de különböző szerkezettel és tulajdonságokkal rendelkező vegyületek: Szerkezeti izomerek: az atomok kovalens elrendezése különböző Térizomerek: hasonlókovalens, de különböző térbeli elrendezés Enantiomerek a térbeli elrendezés tükörképe a másiknak, egymásba át nem forgatható
6 Pentán 2-methyl bután (a) Szerkezeti izomer cisz izomer: a két X azonos oldalon van transz izomer: A két X átellenes oldalon van (b) Térizomer (c) Enantiomer L izomer D izomer
7 Az enantiomerek a gyógyszeriparban kiemelt fontosságúak
8 A biológiai molekulák funkcióiban kis számú funkciós csoport játszik fontos szerepet A szerves molekulák különböző funkciói nemcsak a szénváztól, hanem az ahhoz kapcsolódó csoportoktól is függenek A funkciós csoportok száma és elrendeződése a molekulának egyedi tulajdonságokat
9 Ösztradiol Testosteron
10 Hét funkciós csoport a legfontosabb az elő szervezetekben előforduló molekulákban: Hidroxil csoport Karbonil csoport Karboxil csoport Amino csoport Sulfhidril csoport Foszfát csoport Methil csoport
11 KÉMIAI CSOPORT HIdroxIl KarbonIl KarboxIl SZERKEZET (néha HO ) VEGYÜLET NEVE Alkoholok Ketonok, ha láncközben van Karbonsavak / szerves savak Aldehidek, ha lánc végén van PÉLDA etanol Acetone Ecetsav Propanal FUNKCIONÁLIS TULAJDONSÁGOK Az oxigén elektronnegativitása miatt poláros csoport A ketonok és aldehidek strukturális izomerek lehetnek eltérő tulajdonságokkal. Savas karaktere van a poláros O-H kötés miatt Hidrogén kötések kialakítására képes. Ez a két csoport cukrokban is megtalálható (aldózok és ketózok) Ecetsav Acetát ion A sejtben ionizált formában van jelen (karboxilát ion).
12 Amino SZERKEZET Aminok VEGYÜLET NEVE PÉLDA Bázisként viselkedik, protont vesz fel FUNKCIONÁLIS TULAJDONSÁGOK Glicin Mivel a glicin amino csoporttal is rendelkezik, ezért aminosav (nonionized) (ionized) Sejtekben ionizált formában fordul elő.
13 Szulfhidril SZERKEZET Tiolok VEGYÜLET NEVE (néha HS ) PÉLDA Két szulfhidril csoport kovalensen képes összekapcsolódni (pl fehérjék). FUNKCIONÁLIS TULAJDONSÁGOK Cisztein A cisztein fontos kén tartalmú aminosav A ciszteinek közötti keresztkötések képesek stabilizálni a hajban található fehérjéket, megadva ezzel a haj formáját.
14 Foszfát SZERKEZET Szerves foszfátok VEGYÜLET NEVE PÉLDA Negatív töltést kölcsönöz a molekulának. FUNKCIONÁLIS TULAJDONSÁGOK Glycerol foszfát Számos kémiai reakció mellet a glicerol foszfát a foszfolipidek kémiai alapját is képezi. Vízzel képes reakcióba lépni, energiát szabadít fel.
15 Metil SZERKEZET Metilált vegyületek VEGYÜLET NEVE PÉLDA DNS metilálása. FUNKCIONÁLIS TULAJDONSÁGOK 5-Methyl citidin A metil csoportok különzöző elhelyezkedése a női és férfi nemi hormonon különböző hatást eredményez. Az 5-Methyl citidine a DNS egy metilálódott alkotója.
16 Az élőt felépítő molekulák Az élőt felépítő nagyméretű molekulák négy fő csoportba tartoznak: szénhidrátok, lipidek, nukleinsavak és fehérjék A sejten belül a kisméretű szerves molekulák makromolekulákat hozhatnak létre A molekulák szerkezete és funkciója szorosan összefügg
17 A makromolekulák polimerek, melyek monomerekből épülnek fel Polimernek nevezzük az ismétlődő egységekből, monomerekből felépülő nagyméretű molekulákat, melyekben az egységeket (monomer) kémiai kötések kapcsolják össze. Polimereket találunk a: szénhidrátok fehérjék nukleinsavak között
18 A polimerek szintézise és lebomlása Kondenzációs reakció vagy dehidrációs reakció akkor fordul elő, ha két monomer víz kilépésével kapcsolódik össze A polimerek monomerekké való szétbontása a hidrolízis, a hidratációs reakció megfordítása
19 HO H HO H Rövid polimer Dehidráció, a vízmolekula kilép Nemkapcsolt monomer H 2 O HO Hosszú polimer H (a) A polimer szintézise során dehidráció megy végbe HO H Hidrolízis, vízmolekula belépésével a kötés felszakad H 2 O HO H HO H (b) A polimer hidrolízise
20 A szénhidrátok energia termelőként és szilárdító elemként szolgálnak A szénhidrátok cukrokat és cukor polimereket jelentenek A legegyszerűbb szénhidrátok a monoszaharidok vagy egyszerű cukrok A szénhidrát makromolekulák, a poliszaharidok, egyszerű cukrok polimerizációjával keletkeznek
21 Cukrok A Monoszaharidok molekuláris képletében (összegképlet) általában a CH 2 O többszöröse szerepel A monoszaharidokat osztályozhatjuk A karbonil csoport pozíciója szerint (aldózok vagy ketózok) A szénlánc szénatomszáma szerint (pentóz, hexóz stb.)
22 Triózok (C 3 H 6 O 3 ) Pentózok (C 5 H 10 O 5 ) Hexózok (C 6 H 12 O 6 ) Ketózok Aldózok Gliceraldehid Dihidroxiaceton Ribóz Glükóz Galaktóz Ribulóz Fruktóz
23 Bár lineáris formában ábrázoltuk a legtöbb monoszaharid vizes közegben gyűrűt hoz létre (a) Nyíltláncú és gyűrű forma (b) Egyszerűsített gyűrű
24 Diszaharidok A diszaharidok a monoszaharidok dehidrációjával alakulnak ki (glikozidos kötés)
25 Poliszaharidok A poliszaharidok cukor polimerek A poliszaharidok szerkezetét és funkcióját a cukor monomeker és a glikozidos kötés helyzete határozza meg
26 Raktározó poliszaharidok A keményítő, egy növényekben előforduló raktározó poliszaharid. A glikogén az állatok raktározó poliszaharidja.
27 Fig. 5-6 Színtest Keményítő zárvány Mitokondriumok Glikogén granulumok 1 µm 0.5 µm Amilóz Amilopektin Glycogen (a) Keményítő (plasztiszokban) (b) Glikogén (izomban, májban)
28 Szerkezeti poliszaharidok A cellulóz a növényi sejtfal fő komponense (a) α ésβ glükóz gyűrűs szerkezete α Glükóz β Glükóz (b) Keményítő: 1 4 α glikozidos kötés (b) Cellulóz: 1 4 β glikozidos kötés
29 Az α glükóz polimerjei helikálisak A β glükóz polimerjei egyenesek A szálak között hidrogén kötések alakulnak ki A párhuzamos cellulóz molekulák mikroszálakká állnak össze Copyright 2008 Pearson Education, Inc., publishing as Pearson Benjamin Cummings
30 Sejtfalak Cellulóz mikroszálak a növényi sejtfalban Mikroszál 10 µm 0.5 µm Cellulóz molekulák b Glükóz monomer
31 Az α kötéseket hidrolizáló enzimek nem tudják bontani a cellulóz β kötéseit A cellulóz ezért az emberi emésztőrendszeren mint oldhatatlan rost halad át A cellulóz bontása csak mikroorganizmusok segítségével lehetséges
32 Kitin, a gombák sejtfalában és a rovarok külső vázában található N-tartalmú poliszaharid (a) The structure (b) Chitin forms the (c) of the chitin exoskeleton of monomer. arthropods. Chitin is used to make a strong and flexible surgical thread.
33 Az élő rendszerek konzervatív struktúrái: A fehérjék
34 A fehérjék számos szerkezetet alakíthatnak ki, mely széleskörű biológiai funkciókat eredményez A sejt szárazanyag tartalmának 50-70%-t fehérjék alkotják A fehérjék számos funkcióval rendelkeznek: kémiai reakciók gyorsítása, raktározás, szilárdítás, szállítás, kommunikáció, mozgás.
35 A fehérjék számos szerkezetet alakíthatnak ki, mely széleskörű biológiai funkciókat eredményez! Figure 5.15 An overview of protein functions. Enzymatic proteins Defensive proteins Function: Selective acceleration of chemical reactions Example: Digestive enzymes catalyze the hydrolysis of bonds in food molecules. Function: Protection against disease Example: Antibodies inactivate and help destroy viruses and bacteria. Enzyme Antibodies Bacterium Virus Storage proteins Transport proteins Function: Storage of amino acids Examples: Casein, the protein of milk, is the major source of amino acids for baby mammals. Plants have storage proteins in their seeds. Ovalbumin is the protein of egg white, used as an amino acid source for the developing embryo. Function: Transport of substances Examples: Hemoglobin, the iron-containing protein of vertebrate blood, transports oxygen from the lungs to other parts of the body. Other proteins transport molecules across cell membranes. Ovalbumin Transport protein Amino acids for embryo Cell membrane Hormonal proteins Receptor proteins Function: Coordination of an organism s activities Example: Insulin, a hormone secreted by the pancreas, causes other tissues to take up glucose, thus regulating blood sugar concentration. Function: Response of cell to chemical stimuli Example: Receptors built into the membrane of a nerve cell detect signaling molecules released by other nerve cells. Receptor protein Insulin secreted High blood sugar Normal blood sugar Signaling molecules Contractile and motor proteins Structural proteins Function: Movement Examples: Motor proteins are responsible for the undulations of cilia and flagella. Actin and myosin proteins are responsible for the contraction of muscles. Function: Support Examples: Keratin is the protein of hair, horns, feathers, and other skin appendages. Insects and spiders use silk fibers to make their cocoons and webs, respectively. Collagen and elastin proteins provide a fibrous framework in animal connective tissues. Actin Myosin Collagen Muscle tissue Connective tissue 100 µm Amino Acid Monomers All amino acids share a common structure. An amino acid is an organic molecule possessing both an Side chain (R group) R! carbon H O 60 µm boxyl group, a hydrogen atom, and a variable group symbolized by R. The R group, also called the side chain, differs with each amino acid. Figure 5.16 shows the 20 amino acids that cells use to
36 Az enzimek biokatalizátorok Az enzimek biokatalizátorok, melyek a kémiai reakciók aktiválási energiáját csökkentik, így anélkül gyorsítják a kémiai reakciókat, hogy ők megváltoznának.
37 1 A szubsztrátok belépnek az aktív centrumba; Az enzim alakja megváltozik, hogy az aktív hely beburkolja a szubsztrátokat. 2 A szubsztrátok gyenge kötésekkel (hidrogén kötés, ionos interakció) kötődnek az aktív centrumhoz Szubsztrátok Enzim-szubsztrát komplex 3 Az aktív hely csökkenti az E A -t és így felgyorsítja a reakciót. 6 Aktiv hely újra elérhető a szubsztrát molekulák számára. Enzim 5 A termékek leválnak. 4 A szubsztrátok termékekké alakulnak. Termékek
38 Polipeptidek és monomerjeik, az aminosavak A funkcionális fehérjék egy vagy több polipeptid láncból állnak, melyek az aminosavak el nem ágazó polimerjei Az aminosavak karboxil és amino csoporttal is rendelkező, amfoter molekulák A fehérjéket felépítő α-amonosavak eltérő tulajdonságai az α-szénatomhoz kapcsolódó oldallánctól (R csoport) függenek.
39 α szénatom Amino csoport Karboxil csoport
40 Aminosavak csoportosítása az oldalláncok kémiai tulajdonságai alapján Glicin (Gly or G) Alanin (Ala or A) Apoláros Valin (Val or V) Leucin (Leu or L) Izoleucin (Ile or I) Metionin (Met or M) Fenilalanin (Phe or F) Triptofán (Trp or W) Proline (Pro or P) Poláros Szerin (Ser or S) Treonin (Thr or T) Cisztein (Cys or C) Tirozin (Tyr or Y) Aszparagin (Asn or N) Glutamin (Gln or Q) Elektromos töltéssel rendelkező Acidic Basic Aszpartát (Asp or D) Glutamát (Glu or E) Lizin (Lys or K) Arginin (Arg or R) Hisztidin (His or H)
41 Az aminosavak polimerizációja Az aminosavakat peptid kötések kapcsolják össze. Minden polipeptid egyedi, lineáris aminosav szekvenciával rendelkezik. A polipeptidek állhatnak néhány vagy akár több ezer aminosav maradékból is.
42 Peptid kötés Peptide bond Oldallánc A molekula gerince Amino terminális (N-terminális) Karboxil terminális (C-terminális)
43 A proteinek szerkezete és funkciója összefügg A funkcionális fehérjék egy vagy több polipeptid lánc egyedi alakba csavarodott, hajtogatott, feltekeredett származékai. árok árok (a) A lizozim szalagmodellje (b) A lizozim hely-kitöltő modellje
44 A fehérjék négy szintű szerkezete A fehérjék elsődleges szerkezetét az egyedi aminosavszekvencia jelenti. A másodlagos szerkezet, mely a legtöbb fehérjében megtalálható, a fehérje lánc tekeredése és hajtogatódása következtében alakul ki. A harmadlagos szerkezet a különböző oldalláncok (R csoportok) közötti kölcsönhatás eredménye Negyedleges szerkezet akkor áll fent, ha a fehérje több polipeptid láncból épül fel.
45 Az elsődleges szekezet, vagyis az aminosavak kapcsolódási sorrendje a genetikai információból származik
46 A másodlagos szerkezet a polipeptid lánc gerincében az egyes szakaszok között kialakuló hidrogén kötések eredménye. Tipikus másodlagos szerkezetek a felcsavarodott α hélix és hajtogatott β redő/ lemez.
47 Másodlagos szerkezet β-lemez Aminosav maradékok α-hélix
48 A pókok potroh mirigye által termelt pókselyem β redőt tartalmazó vázfehérje.
49 A harmadlagos szerkezet elsősorban az oldalláncok közötti interakció eredményeként jön létre. Az R csopotok közötti kölcsönhatások lehetnek hidrogén kötések, ionos kötések, hidrofób kölcsönhatások, és van der Waals interakciók Erős kovalens kötések, vagyis diszulfid hidak cisztein aminosav maradékok között alakulnak ki, és szilárdítják a fehérjék szerkezetét.
50 Hidrofób és van der Waals kölcsönhatások Hidrogén kötés Polipeptid gerinc Diszulfid híd Ionos kötés
51 Harmadlagos Negyedleges szerlezet
52 Negyedleges szerkezet akkor alakul ki, ha egy fehérjét több polipeptidlánc épít fel Például a kollagén egy szálas szerkezetű fehérje, melyet három egymás köré csavarodó polipeptid lánc épít fel. A Hemoglobin egy globuláris fehérje, mely négy polipeptidből ál: két alfa és két béta láncból. Az egyes polipeptid láncokat ilyen esetekben alegységeknek is nevezik.
53 Polipeptid lánc β láncok Vas Hem csoport Kollagén α láncok Hemoglobin
54 Elsődleges szerkezet Másodlagos szerkezet Harmadlagos szerkezet Negyedleges szerkezet β redő + H 3 N Amino terminális Aminosav maradékok α hélix
55 Sarló-sejtes vérszegénység oka: Változás a fehérje elsődleges szerkezetében Az elsődleges szerkezet kismértékű megváltozása a fehérje struktúrájának és funkciójának megváltozását okozhatja A sarló-sejtes vérszegénység egy öröklődő betegség, mely a hemoglobin fehérje egy aminosavának kicserélődése miatt alakul ki.
56 Elsődleges szerkezet Normál hemoglobin Val His Leu Thr Pro Glu Glu elsődleges szerkezet Sarló sejtes hemoglobin Val His Leu Thr Pro Val Glu Másodlagos és harmadlagos szerkezet β alegység Másodlagos és harmadlagos szerkezet Hidrofób terület β alegység Negyedleges szerkezet Normál hemoglobin (felülnézet) α β α β Negyedleges szerkezet Sarló-sejtes hemoglobin β α β α Funkció A molekulák nem assziciálódnak; mindegyik szállít oxigént. Funkció A molekulák kölcsönhatásba lépnek egymással, és szálakat alakítanak ki; így az oxigén kötő képesség nagymértékben csökken. 10 µm 10 µm Vörösvérsejtek alakja Normál alakú vörösvérsejt Vörösvérsejtek alakja Az abnormális hemoglobin szálak deformálják a vérsejt alakját.
57 Mi határozza meg a fehérjék szerkezetét? Az elsődleges zserkezet mellett fizikai és kémiai körülmények is befolyásolhatják a szerkezetet. Változások a ph-ban, a só koncentrációkban, a hőmérsékletben mind okozhatják a fehérje kigombolyodását. Ha a fehérje elveszti natív szerkezetét akkor denaturációról beszélünk. A denaturált fehérje biológiailag inaktív.
58 Denaturáció Normál protein Denaturált protein Renaturáció (de nem mindig!!)
59 A fehérjék hajtogatása a sejtben Az egyes szerkezeti szintek következnek egymásból. A harmadlagos állapot hátterében termodinamikai megfontolás áll. Ch. Anfinsen kísérlete (1961): Ribonukleáz feltekeredése
60 A fehérjék hajtogatása a sejtben Nagyon nehéz megjósolni a fehérjék szerkezetét az aminosav szekvenciából A legtöbb fehérje számos állapoton keresztül jut el a stabil struktúráig Dajka/Chaperon fehérjék segítenek a proteinek helyes felgombolyodásában.
61 Sapka Polipeptid Helyesen gombolyodott fehérje Üreges henger Dajkafehérje (teljesen összeszerelt) A dajkafehérje működésének lépései: 1 A polipeptid belép a hengerbe. 2 A sapka záródása a henger 3 alakváltozását okozza, mely hidrofil környezetet teremt segítve a fehérje helyes felgombolyodását. A sapka leválik és a helyesen felgombolyodott fehérje kijut.
62 5.27. ábra: A folding tölcsér. A folding tölcsért a feltekeredés termodinamikai hátterének illusztrálására vezették be, ennek részleteit lásd a főszövegben.
63 Hogyan ismerhetjük meg a fehérjék térszerkezetét? A fehérje szerkezet tanulmányozásának egyik módja a Röntgen (X-ray) krisztallográfia. Lehetőség van mágneses rezonancia spektroszkópia (NMR) alkalmazására is, ez nem igényli a fehérje kristályosítását A bioinformatikai módszer segítségével, számítógépes modellezést felhasználva, az aminosav sorendből próbálják jósolni a térszerkezetet.
64 KÍSÉRLET Röntgen forrás Diffraktált Röntgen sugár Röntgen sugár Fehérje kristály Detektor Röntgen diffrakciós mintázat EREDMÉNY RNS polimeráz II DNS RNS
3. előadás: A víz szerepe az élő szervezetekben
 3. előadás: A víz szerepe az élő szervezetekben A víz a földi élet alapja A víz az élet biológiai közege a Földön Az egyetlen gyakori molekula, mely midhárom halmazállapotban jelen van Minden élő szervezetnek
3. előadás: A víz szerepe az élő szervezetekben A víz a földi élet alapja A víz az élet biológiai közege a Földön Az egyetlen gyakori molekula, mely midhárom halmazállapotban jelen van Minden élő szervezetnek
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
A fehérjék hierarchikus szerkezete
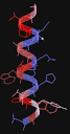 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
SZÉNHIDRÁTOK. Biológiai szempontból legjelentősebb a hat szénatomos szőlőcukor (glükóz) és gyümölcscukor(fruktóz),
 SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE
 AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Tel: ;
 BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
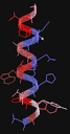 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Szénhidrátok. Szénhidrátok. Szénhidrátok. Csoportosítás
 Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
4. FEHÉRJÉK. 2. Vázanyagok. Az izmok alkotórésze (pl.: a miozin). Inak, izületek, csontok szerves komponensei, az ún. vázfehérjék (szkleroproteinek).
 4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
Táptalaj E. coli számára (1000 ml vízben) H 2 O 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen ion 1%
 Az E. coli kémiai összetétele Táptalaj E. coli számára (1000 ml vízben) Na 2 P 4 6,0 g K 2 P 4 3,0 g Glükóz 4,0 g N 4 l 1,0 g MgS 4 0,13g 2 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen
Az E. coli kémiai összetétele Táptalaj E. coli számára (1000 ml vízben) Na 2 P 4 6,0 g K 2 P 4 3,0 g Glükóz 4,0 g N 4 l 1,0 g MgS 4 0,13g 2 70% Fehérje 15% Nukleinsav 7% (1+6) Szénhidrát 3% Lipid 2% Szervetlen
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT)
 BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
SZÉNHIDRÁTOK. 3. Válogasd szét a képleteket aszerint, hogy aldóz, vagy ketózmolekulát ábrázolnak! Írd a fenti táblázat utolsó sorába a betűjeleket!
 funkciós kimutatása molekulák csoport betűjele neve képlete helye 1. Írd a táblázatba a szénhidrátok összegképletét! általános képlet trióz tetróz 2. Mi a különbség az aldózok és a ketózok között? ALDÓZ
funkciós kimutatása molekulák csoport betűjele neve képlete helye 1. Írd a táblázatba a szénhidrátok összegképletét! általános képlet trióz tetróz 2. Mi a különbség az aldózok és a ketózok között? ALDÓZ
Aminosavak általános képlete NH 2. Csoportosítás: R oldallánc szerkezete alapján: Semleges. Esszenciális aminosavak
 Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
Aminosavak 1 Aminosavak általános képlete N 2 soportosítás: oldallánc szerkezete alapján: Apoláris Poláris Bázikus Savas Semleges Esszenciális aminosavak 2 (apoláris) Glicin Név Gly 3 Alanin Ala 3 3 Valin
INFORMATIKA EMELT SZINT%
 Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
A fehérjék hierarchikus szerkezete. Szerkezeti hierarchia. A fehérjék építőkövei az aminosavak. Fehérjék felosztása
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Aminosavak, peptidek, fehérjék. Béres Csilla
 Aminosavak, peptidek, fehérjék Béres Csilla Aminosavak Az aminosavak (más néven aminokarbonsavak) olyan szerves vegyületek, amelyek molekulájában aminocsoport (- NH 2 ) és karboxilcsoport (-COOH) egyaránt
Aminosavak, peptidek, fehérjék Béres Csilla Aminosavak Az aminosavak (más néven aminokarbonsavak) olyan szerves vegyületek, amelyek molekulájában aminocsoport (- NH 2 ) és karboxilcsoport (-COOH) egyaránt
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék. elrendeződés, rend, rendszer, periodikus ismétlődés
 Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Bioinformatika 2 5.. előad
 5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
Élettan. előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45
 Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel
 Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
3.6. Szénidrátok szacharidok
 3.6. Szénidrátok szacharidok általános összegképlet: C n (H 2 O) m > a szén hidrátjai elsődleges szerves anyagok mert az élő sejt minden más szerves anyagot a szénhidrátok további átalakításával állít
3.6. Szénidrátok szacharidok általános összegképlet: C n (H 2 O) m > a szén hidrátjai elsődleges szerves anyagok mert az élő sejt minden más szerves anyagot a szénhidrátok további átalakításával állít
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
1. jelentésük. Nevüket az alkotó szén, hidrogén, oxigén 1 : 2 : 1 arányából hajdan elképzelt képletről [C n (H 2 O) m ] kapták.
![1. jelentésük. Nevüket az alkotó szén, hidrogén, oxigén 1 : 2 : 1 arányából hajdan elképzelt képletről [C n (H 2 O) m ] kapták. 1. jelentésük. Nevüket az alkotó szén, hidrogén, oxigén 1 : 2 : 1 arányából hajdan elképzelt képletről [C n (H 2 O) m ] kapták.](/thumbs/55/37234755.jpg) Összefoglalás II. Szénhidrátok 1. jelentésük Nevüket az alkotó szén, hidrogén, oxigén 1 : 2 : 1 arányából hajdan elképzelt képletről [C n (H 2 O) m ] kapták. Ha ezeket az anyagokat hevítjük vizet vesztenek
Összefoglalás II. Szénhidrátok 1. jelentésük Nevüket az alkotó szén, hidrogén, oxigén 1 : 2 : 1 arányából hajdan elképzelt képletről [C n (H 2 O) m ] kapták. Ha ezeket az anyagokat hevítjük vizet vesztenek
1. Bevezetés. Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei
 1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) olajsav (cisz-9 oktadecénsav) néhány, állatokban előforduló zsírsav
 Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
Lipidek: zsírsavak hosszú szénláncú, telített vagy telítetlen karbonsavak palmitinsav (hexadekánsav) sztearinsav (oktadekánsav) olajsav (cisz-9 oktadecénsav) Szénatomszám Kettős kötések száma néhány, állatokban
Az élethez szükséges elemek
 Az élethez szükséges elemek 92 elemből kb. 25 szükséges az élethez Szén (C), hidrogén (H), oxigén (O) és nitrogén (N) alkotja az élő szervezetekben előforduló anyag 96%-t A fennmaradó 4% legnagyobb része
Az élethez szükséges elemek 92 elemből kb. 25 szükséges az élethez Szén (C), hidrogén (H), oxigén (O) és nitrogén (N) alkotja az élő szervezetekben előforduló anyag 96%-t A fennmaradó 4% legnagyobb része
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A biokémia alapjai. Typotex Kiadó. Wunderlich Lívius Szarka András
 A biokémia alapjai Wunderlich Lívius Szarka András Összefoglaló: A jegyzet elsősorban egészségügyi mérnök MSc. hallgatók részére íródott, de hasznos segítség lehet biomérnök és vegyészmérnök hallgatók
A biokémia alapjai Wunderlich Lívius Szarka András Összefoglaló: A jegyzet elsősorban egészségügyi mérnök MSc. hallgatók részére íródott, de hasznos segítség lehet biomérnök és vegyészmérnök hallgatók
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
(11) Lajstromszám: E 007 952 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
!HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
TAKARMÁNYOZÁSTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Takarmányok fehérjetartalma Az állati szervezet létfontosságú vegyületei fehérje természetűek Az állati termékek
TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Takarmányok fehérjetartalma Az állati szervezet létfontosságú vegyületei fehérje természetűek Az állati termékek
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE
 Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok)
 SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
7. évfolyam kémia osztályozó- és pótvizsga követelményei Témakörök: 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2.
 7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
,:/ " \ OH OH OH - 6 - / \ O / H / H HO-CH, O, CH CH - OH ,\ / "CH - ~(H CH,-OH \OH. ,-\ ce/luló z 5zer.~ezere
 - 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
- 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Az anyag- és energiaforgalom alapjai
 Az anyag- és energiaforgalom alapjai Anyagcsere Tápanyagbevitel a szükségletnek megfelelően - test felépítése - energiaszükséglet fedezete Szénhidrátok, Zsirok, Fehérjék, Nukleinsavak, Munka+hő+raktározás
Az anyag- és energiaforgalom alapjai Anyagcsere Tápanyagbevitel a szükségletnek megfelelően - test felépítése - energiaszükséglet fedezete Szénhidrátok, Zsirok, Fehérjék, Nukleinsavak, Munka+hő+raktározás
Röntgen sugárzás. Wilhelm Röntgen. Röntgen feleségének keze
 Röntgendiffrakció Kardos Roland 2010.03.08. Előadás vázlata Röntgen sugárzás Interferencia Huygens teória Diffrakció Diffrakciós eljárások Alkalmazás Röntgen sugárzás 1895 röntgen sugárzás felfedezés (1901
Röntgendiffrakció Kardos Roland 2010.03.08. Előadás vázlata Röntgen sugárzás Interferencia Huygens teória Diffrakció Diffrakciós eljárások Alkalmazás Röntgen sugárzás 1895 röntgen sugárzás felfedezés (1901
AMINOSAVAK, FEHÉRJÉK
 AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Szerves kémiai és biokémiai alapok:
 Szerves kémiai és biokémiai alapok: Másodlagos kémiai kötések: A másodlagos kötések energiája nagyságrenddel kisebb, mint az elsődlegeseké. Energiaközlés hatására a másodlagos kötések bomlanak fel először,
Szerves kémiai és biokémiai alapok: Másodlagos kémiai kötések: A másodlagos kötések energiája nagyságrenddel kisebb, mint az elsődlegeseké. Energiaközlés hatására a másodlagos kötések bomlanak fel először,
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások
 ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások
 Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Zsírsav szintézis. Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P. 2 i
 Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Valin H 3 C. Treonin. Aszpartát S OH
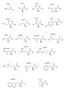 2 Glicin C 3 Alanin C 3 Valin 3 C Leucin 2 2 2 C 3 Izoleucin 2 zerin 2 Treonin 2 Tirozin 2 Cisztein Metionin Aszpartát 2 C 3 2 Glutamát 2 2 Aszparagin 2 Glutamin 2 Arginin 2 2 2 2 2 Lizin isztidin Fenilalanin
2 Glicin C 3 Alanin C 3 Valin 3 C Leucin 2 2 2 C 3 Izoleucin 2 zerin 2 Treonin 2 Tirozin 2 Cisztein Metionin Aszpartát 2 C 3 2 Glutamát 2 2 Aszparagin 2 Glutamin 2 Arginin 2 2 2 2 2 Lizin isztidin Fenilalanin
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során
 Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során Az aminosavak átalakulása a feldolgozás és tárolás során A fehérjék hőkezelése aminosavak deszulfurálódása, dezaminálódása, izomerizációja,
Élelmiszer-fehérjék átalakulása a feldolgozás és tárolás során Az aminosavak átalakulása a feldolgozás és tárolás során A fehérjék hőkezelése aminosavak deszulfurálódása, dezaminálódása, izomerizációja,
Laboratóriumi technikus laboratóriumi technikus Drog és toxikológiai
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
SZÉNHIDRÁTOK (H 2. Elemi összetétel: C, H, O. O) n. - Csoportosítás: Poliszacharidok. Oligoszacharidok. Monoszacharidok
 Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
A tejfehérje és a fehérjeellátás
 A tejfehérje A tejfehérje és a fehérjeellátás Fejlődő országok: a lakosság 20 30%-a hiányosan ellátott fehérjével. Fejlett ipari országok: fehérje túlfogyasztás. Az emberiség éves fehérjeszükséglete: 60
A tejfehérje A tejfehérje és a fehérjeellátás Fejlődő országok: a lakosság 20 30%-a hiányosan ellátott fehérjével. Fejlett ipari országok: fehérje túlfogyasztás. Az emberiség éves fehérjeszükséglete: 60
TestLine - Biogén elemek, molekulák Minta feladatsor
 TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
