HIV combo REF A Felhasználás. Összefoglaló és magyarázatok
|
|
|
- Barnabás Imre Magyar
- 8 évvel ezelőtt
- Látták:
Átírás
1 HIV combo REF A59428 Felhasználás Az Access HIV combo próba egy paramágneses részecskéket tartalmazó kemilumineszcens immunpróba, amelynek célja a HIV-1 p24 antigén, HIV-1 (M és O csoportok) és HIV-2 antitestek minőségi kimutatása humán szérumban vagy plazmában (lítium-heparin) Access Immunoassay Rendszerek használatával. Az Access HIV combo próba felhasználható a HIV-1 vagy HIV-2 fertőzés diagnosztizálásában, valamint szűrővizsgálatként vér és plazmadonorok esetén. A próba nem használható fel vizsgálatként vagy szűrővizsgálatként gyűjtött/poolozott mintákhoz. Az Access HIV combo próba nyomán elért eredmény nem tesz különbséget a HIV-1 p24 antigén, a HIV-1 vagy HIV-1-O és HIV-2 antitestek között. In Vitro diagnosztikai célra használható Az előállított és forgalomba hozott reagensek minőségügyi rendszerünk előírásainak vannak alávetve a nyersanyagok bevételezésétől kezdve a termék forgalomba kerüléséig. Minden egyes tétel minőségellenőrzésen esik át, és csak a jóváhagyási feltételeknek való megfelelőséget követően kerül forgalomba. Az egyes tételek előállítása és ellenőrzése során készült jegyzőkönyveket vállalatunk őrzi. Összefoglaló és magyarázatok A szerzett immunhiányos tünetegyüttes (AIDS) egy vírus okozta fertőző betegség, amely egy mély, sejten belüli immunhiányban nyilvánul meg. Az AIDS kórban vagy ennek a korai szindrómáiban szenvedő páciensek limfocitáiból két, a Lentivírus alcsaládhoz tartozó vírustípus izolálása történt meg (1,2,3). Az első vírust, amelynek megnevezése HIV-1 (humán immundeficiencia vírus), először Franciaországban, majd az Amerikai Egyesült Államokban izolálták. A második vírust, amelynek megnevezése HIV-2, két afrikai eredetű páciensben azonosították, és mint kiderült, ez szolgált alapul egy új AIDS gócpont kialakulásához Nyugat-Afrikában (3,4,5,6). A HIV törzsek genetikai variabilitására vonatkozó ismeretek az adott altípusra vonatkozó reprezentatív törzsek GAG, POL és ENV génjeinek szekvenálásából származik (7). Egy filogenetikai elemzés lehetővé tette a HIV-1 különböző csoportjainak megkülönböztetését: M csoport (major), N csoport (nem M, nem O), O csoport (Outlier) és P csoport (8,9,10,11,12,13). Access HIV combo 1/22 A97222B
2 A HIV-1 M csoport 9 altípust (A, B, C, D, F, G, H, J és K) (11) és keringő rekombináns formákat (CRF altípusok) tartalmaz (11,14). A különböző altípusok földrajzi eloszlása mára viszonylag jól meghatározott (15,16). Néhány HIV-1 variáns csupán 70%-os homológiát mutat a GAG és POL génekre vonatkozóan a fő izolátumokkal, az ENV gén esetén ez pedig csupán 50%-os. Ezek a különbségek felelősek a betegség számos páciensben való fel nem ismeréséért (17). A különböző HIV-2 törzsek közös antigén-tulajdonságokat mutatnak a majom-immundeficiens vírussal (SIV), függetlenül a vizsgált vírusproteintől (envelop fehérje és magfehérje; heterológ jelleg: 30%). Ezek kisebb, mint 40%-os homológiát mutatnak a HIV-1 envelop fehérjéjével (3,18,19,20). Ugyanakkor a HIV-2 kevésbé patogén a HIV-1 változatnál, valamint lassabb a megbetegedés lefolyása, alacsonyabbak a titerek, valamint alacsonyabb mértékű a függőleges és merőleges irányú fertőzés (21,22,23,24). A HIV antigének és antitestek a fertőzés különböző szakaszaiban jelennek meg és válnak érzékelhetővé (25,26,27). A HIV fertőzés jelenlegi diagnosztizálásához az anti-hiv antitestek szérumbeli jelenlétének kimutatása szükséges, amely az ELISA módszerrel történik (28,29,30). Ugyanakkor a kitettség és az első antitestek megjelenése között átlagosan három hetes időszak telik el. Ebben az időszakban a p24 antigén kimutatható a HIV-1 vírussal fertőzött egyének nagy részénél, földrajzi származásuktól függetlenül (31,32). Az Access HIV combo próba lehetővé teszi a HIV-1 és HIV-2 antitestek egyidejű azonosítását. Ez a próba is, többek között monoklonális antitesteket használ a HIV p24 antigén szerokonverzió előtti azonosításához, ez által csökkentve a szerokonverziós ablakperiódust, és javítva a HIV fertőzés korai azonosításának esélyét (33,34,35,36). Az eljárás leírása Az Access HIV combo próba egy szekvenciális, két lépéses, immunoenzimatikus ( szendvics ) próba. A teszt első lépésében összekeverésre kerül a minta, a bevont paramágneses részecskék, a biotinilált monokolánis p24 antitestek és a részecske adalékanyagok. A paramágneses részecskék rekombináns HIV-1 fehérjével, HIV-1-O / HIV-2 polipeptidekkel és a HIV-1 p24 antigénnel reakcióba lépő monoklonális antitestekkel vannak bevonva. A reakciós edényben való inkubálást követően a szilárd fázison megkötött anyagok mágneses mezőbe kerülnek, a kötetlenül maradt anyagok pedig lemosásra kerülnek. A második lépésben 3 polipeptid és alkalikus-foszfatázzal jelölt streptavidin kerül hozzáadásra és a konjugát adalékanyag. Az inkubálást követően a kötetlenül maradt reagensek eltávolításra kerülnek mágneses mezőben történő elválasztás és mosás segítségével. Az edénybe hozzáadjuk a kemilumineszcens Lumi-Phos* 530 szubsztrátot és a reakció által kibocsátott fényt egy luminométer leméri. A kibocsátott fény a reakció végén fennmaradó enzim-konjugátum mennyiségétől függ. A minta esetében mért fénymennyiség lehetővé teszi az anti-hiv-1 vagy HIV-2 antitestek és/vagy p24 antigének jelenlétének kimutatását, mivel ez a mennyiség összehasonlításra kerül egy olyan határértékkel/cut-off értékkel, amelynek meghatározása műszeren végzett kalibrálásakor történt. Amennyiben a fénytermelés nagyobb vagy egyenlő a határértékkel, a minta reaktívnak minősül az Access HIVcombo assay során. A97222B Access HIV combo 2/22
3 Termékinformáció Access HIV combo Reagens csomagok Katalógusszám: A59428: 100 meghatározás, 2 csomag, 50 teszt/csomag Azonnal felhasználhatók. Tárolja függőleges helyzetben, 2-10 C hőmérsékleten. A műszeren való használatot megelőzően legalább két órán keresztül tárolja lehűtve 2-10 C közötti hőmérsékleten C közötti tárolás esetén minőségét megőrzi a címkén jelzett szavatossági időig (ha a reagens csomagolása nem lett kinyitva) C hőmérséklet között tárolva minőségét megőrzi az első használat dátumától számított 56 napig. Az esetleges károsodás jelei lehetnek a csomagolás megszakadt elasztomeres rétege vagy a megfelelő tartományon kívüli kontrollértékek. Sérült reagens csomag esetén (például megszakadt elasztomer) selejtezze le a csomagot. R1a: Rekombináns HIV-1 fehérjével (gp 160), HIV-1-O (gp 41) és HIV-2 (gp 36) polipeptidekkel, valamint p24 HIV-1 antigénre specifikus monoklonális antitestekkel bevont paramágneses részecskék TRIS pufferes sóoldatban feloldva, 0,1 %-os nátrium-azid és ProClin**300-al (0,25%). R1b: R1c: R1d: Konjugátum adalékanyag: TRIS pufferes sóoldat 0,1%-os nátrium-aziddal és ProClin**300-al (0,25%). Részecske adalékanyag: TRIS pufferes sóoldat biotinilált monoklonális HIV-1 p24 antitestekkel, 0,1%-os nátrium-aziddal és ProClin**300-al (0,25%). Konjugátumok: HIV-1, HIV-1-O, HIV-2 polipeptidek és alkalikus-foszfatázzal konjugált streptavidin 0,1%-os nátrium-aziddal és ProClin**300-al (0,25%). Figyelmeztetések és óvintézkedések In vitro diagnosztikai célra használható. A betegminták és a véralapú termékek rutinszerűen feldolgozhatók minimális kockázattal a leírt eljárás betartásával. Ugyanakkor ezeket a termékeket kezelje potenciálisan fertőző anyagként, és tartsa be az általános óvintézkedéseket, valamint a klinikai laboratóriumokban bevált gyakorlatokat, függetlenül a termékek eredetétől, kezelésétől vagy előző megjelölésüktől. A dekontaminációhoz használjon megfelelő fertőtlenítőszert. Ezeket az anyagokat és tartályaikat a helyi szabályozásoknak és útmutatásoknak megfelelően tárolja és selejtezze le (37). A nátrium-azid reakcióba léphet az ólmot és rezet tartalmazó vezetékekkel, és így rendkívül robbanékony fém-azid alakulhat ki. Leselejtezéskor öblítse le nagy mennyiségű vízzel, így elkerülve az azid kialakulását (38). A ProClin**300 potenciálisan bőrizgató hatású. Kerülje ennek a reagensnek a bőrre vagy ruházatra való ömlését vagy fröccsenését. A reagenssel való kapcsolat esetén az érintett felületet alaposan mossa le vízzel és szappannal. Xn. Ártalmas: 0,1% nátrium-azid és 0,25% ProClin**300. R 22: Lenyelve ártalmas. R 43: Bőrrel érintkezve túlérzékenységet okozhat. S 23: A keletkező gázt/füstöt/gőzt/permetet nem szabad belélegezni. S 24: A bőrrel való érintkezés kerülendő. S 37: Megfelelő védőkesztyűt kell viselni. S 60: Az anyagot és/vagy edényzetét veszélyes hulladékként kell ártalmatlanítani. Az anyagbiztonsági adatlap (MSDS) kérésre rendelkezésre bocsátható. Access HIV combo A97222B 3/22
4 A minta begyűjtése és előkészítése Készletben található anyagok Szükséges, de a készletben nem megtalálható anyagok 1. A javasolt minták a szérum (beleértve a szérum szeparáló csöveket) és a plazma (lítium-heparin, beleértve a plazma szeparáló csöveket). 2. A mintákat nem szabad melegíteni. 3. A vérminták kezelése, feldolgozása és tárolása során tartsa be az alábbi ajánlásokat (39) : Mindig a vénaszúrással kapcsolatos rutin óvintézkedések betartásával vegye le a vérmintákat. Centrifugálás előtt hagyja, hogy a minták teljesen megalvadjanak. A csöveket mindig tartsa lezárva. A mintákat szorosan lezárva tárolja szobahőmérsékleten (15-23 C), maximum huszonnégy órán keresztül. Amennyiben a vizsgálat elvégzése nem huszonnégy órán belül történik, hűtse le a mintákat 2-8 C hőmérsékletre. Amennyiben a vizsgálat elvégzése nem történik meg nyolc napon belül 2-8 C hőmérsékleten, vagy a minták szállítása esetén fagyassza le ezeket legalább -20 C hőmérsékleten 4. A minták előkészítésekor kövesse az alábbi útmutatásokat: Bizonyosodjon meg arról, hogy a visszamaradt fibrin és a sejtes összetevők eltávolításra kerültek a mintából az elemzés megkezdése előtt. A centrifugálásra vonatkozóan kövesse a vérgyűjtő cső gyártójának előírásait. 5. Minden laboratóriumnak önállóan kell meghatároznia, hogy milyen vérgyűjtő csöveket és szérum szeparáló termékeket alkalmaz. Ezen termékek esetén különbségek merülhetnek fel gyártónként és néha tételenként is. 6. Ne olvassza fel a mintákat háromnál több alkalommal. Egy tanulmányban megvizsgálásra került 25 friss nem reaktív szérum és 25 friss reaktív szérum, és ezek nem mutattak semmilyen jelentős klinikai dózisváltozást három fagyasztás-felolvasztás ciklust követően. 7. A felolvasztást követően a mintát újra le kell centrifugálni, 3000 g sebességen 15 percig, majd át kell helyezeni egy csőbe/reakció edénybe a szuszpendált fibrin részecskék és az álpozitív eredményt okozó aggregátumok eltávolítása érdekében. 8. A legfeljebb 200 mg/l és 300 mg/l konjugált, illetve konjugálatlan bilirubint tartalmazó, illetve legfeljebb 90 g/l albumint, valamint a 30 g/l triolein (triglicerid) ekvivalenst tartalmazó lipémiás, illetve a max. 2 g/l hemoglobintartalmú hemolizált minták az eredményeket nem befolyásolják. R1 reagens csomagok Access HIV combo assay-hez 1. Access HIV combo Kalibrátorok Egy HIV antitest negatív szérum és egy HIV antitest pozitív szérum formájában található meg a készletben. Katalógusszám: A Minőségellenőrzési anyagok: Minőségellenőrzés Access HIV combo assay egy HIV antitest negatív szérum és egy anti-hiv-1 pozitív szérum, valamint egy HIV-1 antigén pozitív Tris puffer oldatban Katalógusszám: A Access Szubsztrát Katalógusszám: Access 2: mosópuffer: Access Wash Buffer II, Katalógusszám: A UniCel DxI : mosópuffer: UniCel DxI Wash Buffer II, Katalógusszám: Készülékek: Access 2, UniCel DxI 800 és 600 immunpróba rendszerek, UniCel DxC 880i, 860i, 680i és 660i Synchron Access Klinikai Rendszerek. A97222B Access HIV combo 4/22
5 Eljárással kapcsolatos megjegyzések Eljárás Kalibrálási részletek Minőségellenőrzés 1. A beszerelési, beindítási, működési alapelvek, a rendszer teljesítményjellemzői, kezelési utasításai, a kalibrálási eljárások, az eljárási korlátozások és az óvintézkedések, veszélyek, karbantartás és hibaelhárítás pontos leírása ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. 2. Keverje össze az új (ki nem lyukasztott) reagens csomagokat óvatosan felfordítva ezeket párszor a műszerbe történő betöltést megelőzően. Ne fordítson fel nyitott (kilyukasztott) csomagokat. 3. A mintatartály és a rendszer holttérfogatán túlmenően használjon 110 μl mintát minden egyes meghatározáshoz. A minimálisan szükséges mintamennyiség ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. 4. Az első eredmény körülbelül 60 perc alatt készül el. 5. A rendszer alapértelmezett mértékegysége mintaeredmények méréséhez a Jel/Cut-off (S/CO) arány. A minták kezelésével, a tesztek konfigurálásával, ezek lekérésével és a teszteredmények áttekintésével kapcsolatos információk ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. Egy aktív kalibrálási pont szükséges az összes teszthez. Az Access HIV combo assay esetén kalibrálásra 56 naponta van szükség. A kalibrációs elméletre, a kalibrátorok konfigurációjára, a kalibrátor teszt lekérésének bevitelére és a kalibrációs adatok áttekintésére vonatkozó információ ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. A minőségellenőrzéshez használt anyagok a betegminták jellemzőit szimulálják, és nélkülözhetetlenek a rendszer immunkémiai próbák elemzésekor biztosított teljesítményének a monitorozásához. Mivel a minták inkább véletlenszerű hozzáférés formátumban dolgozhatók fel bármikor, mint tömbösített formátumban, a minőségellenőrzési anyagok minden 24 órás időszakban a minták részét kell képezzék (40). A vizsgálatba vonja be az Access HIV combo assay minőségellenőrző terméket vagy egyéb kereskedelmi forgalomban kapható, legalább két analit szinttel rendelkező minőségellenőrző anyagot. A kontrollok gyakoribb használata vagy további kontrollok használata a felhasználó belátására van bízva, mely alapulhat a laboratóriumokban bevált gyakorlaton vagy a laboratóriumi akkreditáció előírásain, avagy a hatályos törvényeken. A feloldás és tárolás ügyében kövesse a gyártó utasításait. Mindegyik laboratóriumnak kötelessége átlagértékek és elfogadható tartományok meghatározására a megfelelő teljesítmény biztosítása érdekében. Az elfogadható tartományon kívül eső minőségellenőrzési eredmények érvénytelen teszteredményekre utalhatnak. Ennek az analitnak a vonatkozásában vizsgálja meg az utolsó elfogadható minőségellenőrzési tesztpont óta készült összes teszteredményt. A minőségellenőrzési eredmények áttekintése ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. Az Access HIV combo assay kiértékelése C hőmérséklettartományban történt. Optimális eredmények elérése érdekében javasolt, hogy a próba kalibrálása és a páciensminta tesztelése hasonló hőmérsékleti körülmények között történjen. Amennyiben a laboratóriumi hőmérséklet több, mint ± 5 C eltérést mutat a kalibrálás során mért hőmérséklettől, tekintse át a minőségellenőrzési eredményeket, és szükség esetén végezzen ismételt kalibrálást. Access HIV combo A97222B 5/22
6 Eredmények A betegminta eredményeinek kiszámítását a rendszerszoftver automatikusan végzi az aktív kalibrálás során meghatározott Cut-off érték felhasználásával. Az eredmények (jel/cut-off érték= S/CO) reaktív vagy nem reaktív jelzést kapnak a Cut-off értékhez való viszonyuk alapján (a jel a Cut-off értéknél nagyobb, illetve annál kisebb vagy azzal egyenlő). Ugyanakkor a Cut-off értéknél 10 %-kal alacsonyabb eredmények óvatosan kezelendők, és párhuzamosan ismét tesztelendők. Ez a javasolt szürke zóna (0,9 értéktől 1,0 értékig) a felhasználó által tárolandó a rendszerszoftverben (a kvalitatív assay során észlelhető szürke zónákra vonatkozó összes utasítás ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és / vagy a Súgó rendszerből). Így egy jellegzetes jelölés kerül automatikus megjelenítésre, aminek köszönhetően gyorsan azonosíthat egy szürke zónában található eredményt. A betegminta eredményei áttekinthetők a Mintaeredmények (Sample Results) ablakban. Az eredmények áttekintésére vonatkozó összes utasítás ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. Első eredmény elemzése: Bármely, 0,9 aránynál/ratio (S/CO) kisebb értékkel rendelkező minta nem-reaktívnak minősül az Access HIV combo teszt vonatkozásában. Ha mintáknak az S/CO aránya nagyobb vagy egyenlő, mint 0,9 és 1-nél kisebb értékük van, akkor a szürke zónában találhatók, és a végső értelmezést megelőzően ismételten vizsgálandóak. Ha a minták S/CO aránya 1, vagy 1 nagyobb, akkor elsőre reaktívnak tekintendők az Access HIV combo teszt vonatkozásában, és ezeket a mintákat ismét le kell tesztelni a végső értelmezést megelőzően. Második eredmény elemzése: Az összes elsőre reaktív vagy szürke zónában található minta ismételten vizsgálandó az Access HIV combo assay segítségével: Amennyiben a párhuzamos minták eredményei < 1,0 S/CO, akkor a minta nem reaktívnak tekintendő (negatív) a HIV combo teszt vonatkozásában. Amennyiben a két eredmény egyike 1,0 S/CO, az első eredmények megismételhetők, és a minta reaktívnak tekintendő az Access HIV combo teszt vonatkozásában. Ugyanakkor a helyi szabályozásoknak megfelelően minden reaktív minta esetén kiegészítő tesztek végrehajtása szükséges, ezeken belül legalább egy megerősítő teszt, a pozitív eredmény egyértelmű meghatározása érdekében. A97222B Access HIV combo 6/22
7 1. táblázat: az Access HIV combo assay eredményének értelmezése Eredmény Arány: Jel/Határérték Értelmezés Kiegészítő tesztek Első eredmény elemzése S/CO < 0,9 Nem reaktív HIV-1 p24 és/vagy HIV-1/HIV-1-O/HIV-2 antitest nincs kimutatva Nem alkalmazandó S/CO 1 Reaktív Elsőre reaktív Ismételt tesztelés párhuzamosan 0,9 S/CO < 1,0 Szürke zóna Elsőre reaktív Ismételt tesztelés párhuzamosan Második eredmény elemzése Ismételt tesztelés párhuzamosan: Amennyiben a 2 eredmény < 1 Nem reaktív HIV-1 p24 és/vagy HIV-1/HIV-1-O/HIV-2 antitest nincs kimutatva Nem alkalmazandó Ismételt tesztelés párhuzamosan: Amennyiben a 2 eredmény egyike 1 Reaktív Kimutatott HIV-1 p24 és/vagy HIV-1/ HIV-1-O/HIV-2 antitest Ismételten reaktív Megerősítő teszt Az eljárás korlátai 1. Az Access HIV combo assay kizárólag humán szérumból vagy plazmából (Lítium-heparin) nyert mintával történő felhasználásra készült. Az egyéb típusú mintákkal elért teljesítményjellemzők nem kerültek meghatározásra vagy korlátozottak. 2. Az Access HIV combo assay kizárólag a HIV-1 antigén és a HIV-1/HIV-1-O/HIV-2 antitestek humán szérumból vagy plazmából (Lítium-heparin) történő kimutatására korlátozott. 3. Az Access HIV combo assay-vel elért eredményeknek meg kell felelniük az esetlegesen létező tünetekkel és a klinikai jelentésekben található előzményekkel. 4. Az antitesteken alapuló assay esetén fennáll a betegmintában szereplő heterofil antitestekkel való interferenciának az esélye. Az állatokkal rendszeresen érintkező betegek vagy olyan személyek, akik immunterápiában, diagnosztikai eljárások felhasználásával előállított immunoglobulinokat, vagy immunoglobulin fragmenteket kaptak, antitesteket termelhetnek, ilyen például a HAMA, amelyek interferálhatnak az immunassay-kel. Ezen túlmenően egyéb heterofil antitestek is jelen lehetnek a betegmintákban, mint például a humán anti-kecske antitestek (41,42). Ilyen interferáló antitestek hibás eredményekhez vezethetnek. Figyelmesen értékelje ki a gyanú szerint ilyen antitestekkel rendelkező betegek eredményeit. 5. A transzplantációban érintett betegek mintái fagyasztás előtt tesztelendők. 6. A teljesítmény meghatározása során a humán szérum és plazma kivételével más, holttestekből származó minták és testnedvek nem kerültek felhasználásra. 7. A mért eredmény határérték feletti szintje nem jelzésértékű a jelenlévő antitestek és/vagy antigének összmennyiségét illetően. 8. Az Access HIV combo assay eredmények értékelése a beteg összes klinikai jellemzőinek fényében kell történjen. Ilyen jellemzők: klinikai előzmény, további tesztekből származó adatok és egyéb megfelelő információ. 9. Egy nem reaktív eredmény azt jelzi, hogy a tesztelt minta nem tartalmaz az Access HIV combo assay-vel kimutatható antigéneket és antitesteket. Ez azonban nem zárja ki a HIV-1 vagy HIV-2 fertőzés lehetőségét. Access HIV combo A97222B 7/22
8 10.A fertőzés határozott kijelentése érdekében az Access HIV combo assay-vel elért reaktív eredmény megerősítendő egy megfelelő módszer alkalmazásával. 11.A legyengült immunrendszerű egyének, valamint olyan kórképek megléte esetén, mint például a súlyos fertőzés vagy immunszuppresszív gyógyszerterápia alkalmazása esetén olyan alacsony antitest szint lehetséges a szervezetben, amely a próba által érzékelhető szint alatt található. Az ilyen mintákból leszűrt eredmények óvatossággal értelmezendők. Specifikus teljesítmény-jel lemzők Érzékenység Az Access HIV combo assay-vel végzett érzékenységi tanulmányok megerősített HIV antitest mintákon, akut fertőzött betegektől származó mintákon, kereskedelmi forgalomban kapható szerokonverziós paneleken és HIV antigén mintákon (hígítatlan és hígított) történtek. 1. Analitikai érzékenység Az Access HIV combo assay HIV-1 p24 antigénnel szembeni analitikai érzékenysége < 2 NE/ml. A WHO (Egészségügyi Világszervezet) 90/636 NIBSC kódú paneljének és a Bio-Rad belső HIV antigén szabványának regressziós analízise lehetővé tette a próba érzékenységi határértékének meghatározását. 2. Klinikai érzékenység Megerősített HIV antitest pozitív minták AHIV-1 érzékenység vizsgálata 674 megerősített pozitív mintán történt, és a vizsgálat eredménye 100%-os lett (95% CI: 99,41-100%). A minták között a következő genotípusos altípusok és variánsok szerepeltek: M csoport: A, B, C, D, F, G, H, J, K, CRF O csoport N csoport A kérelmeknek megfelelően altípusonként minimum 3 minta tesztelésére került sor. A HIV-2 érzékenység 126 jól dokumentált minta vizsgálatával történt, és 100%-osnak lett nyilvánítva (95% CI: 97,11 100%). Akut fertőzésben szenvedő betegek és kereskedelmi forgalomban elérhető szerokonverziós panelek mintái A HIV-1 M csoporttal szembeni érzékenység szerokonverzió előtt és alatt 86 mintán került megvizsgálásra. Az Access HIV combo assay szerokonverziós érzékenységének vizsgálata 61 jól dokumentált, kereskedelmi forgalomban elérhető szerokonverziós panelekből származó szekvenciális mintákon történt (131 korai szerokonverziós mintával). A 2. táblázatban 6 szerokonverziós panelből származó eredmény látható. A97222B Access HIV combo 8/22
9 2. táblázat: Szerokonverziós panelek Panel Mintaazonosító Napok száma az 1. vérvételt követően Access kombinált HIV próba (S/CO) PCR* Western Blot* BBI ,53 Pozitív Negatív ,21 Pozitív Negatív ,36 Pozitív Negatív ,32 Pozitív Pozitív BBI ,19 Pozitív Pozitív ,48 Pozitív Pozitív ,15 Pozitív Pozitív ,44 Pozitív Pozitív ,67 Pozitív Pozitív ,27 Pozitív Pozitív BBI ,77 Pozitív Negatív ,81 Pozitív Negatív ,31 Pozitív Negatív PRB 950 PRB ,29 Pozitív Negatív PRB ,12 Pozitív Negatív PRB ,03 Pozitív Negatív PRB ,15 Pozitív Pozitív BBI ,28 Pozitív Negatív ,75 Pozitív Negatív ,47 Pozitív Meghatározatlan Zeptometrix ,37 Pozitív Meghatározatlan ,37 Pozitív Meghatározatlan ,89 Pozitív Meghatározatlan * Beszállítóktól származó adatok ,68 Pozitív Meghatározatlan ,06 Pozitív Meghatározatlan Access HIV combo A97222B 9/22
10 HIV-1 antigén minták Érzékenység = 100% (104/104) (95% CI: 96,52 100%) A próba érzékenységének felmérése 104 jól dokumentált minta tesztelésével történt, amelyek közt megtalálható volt: 44 HIV antigén felülúszó sejtkultúrát tartalmazó M csoportba tartozó HIV-1 minta a következő genotípusokból: 10A, 5B, 8C, 5D, 10E, 1F, 2G, 1H, 2J 21 HIV-antigén kereskedelemben kapható pozitív minta 39 HIV-antigén pozitív minta a szerokonverzió különböző szakaszaiban lévő 86 szérum-mintából Friss minták 103 HIV-pozitív minta tesztelésére került sor a vérvételt követő 1 napon belül. Specificitás Az Access HIV combo assay specificitása 99,5%. A specificitás vizsgálata az alábbi minták tesztelésével történt: IR specificitás RR specificitás Minta típusa szám % 95%-os konfidenciaintervallum szám % 95%-os konfidenciaintervallum Véradók 7656 / ,90 [99,79-99,95%] 7664 / ,00 [94,95-100%] Kiválasztott kórházi betegek 1961 / ,59 [99,20-99,82%] 1966 / ,85 [99,56-99,97%] Ki nem választott kórházi betegek 1121 / ,91 [99,50-100%] 1121 / ,91 [99,50-100%] Terhes nők 200 / ,00 [98,17-100%] 200 / ,00 [98,17-100%] Összesített átlag / ,84 [99,75-99,91%] / ,96 [99,91-99,99%] 477 minta tesztelésére került sor, amelyek olyan betegektől származtak, akik különböző kórtant mutattak vagy állapotuk a HIV vírussal nincs kapcsolatban: terhes nők, reumatoid faktor, cirózis, krónikus veseelégtelenség, dialízis, transzplantáció, Lenograstim kezelés, humán anti-egér Ig, antinukleáris antitestek, mycoplasma pneumoniae, erythrovírus B19, myeloma, egyéb vírusos vagy bakteriális fertőzések (HAV, HBV, HCV, rubeola, toxoplazmózis, szifilisz, mumpsz, himlő, CMV, HSV, EBV, VZV, HTLVI, malária, influenza elleni beoltott betegek). A97222B Access HIV combo 10/22
11 A specificitás értéke 98,10% (414/422) (95% CI: 96,30-99,18%) volt, a fagyasztott transzplantált populáció nélkül (az eljárás korlátait illetően lásd az 5. pontot). Öt nem specifikus reakció került dokumentálásra: VZV pozitív minták (7,7 %) EBV pozitív minták (6,7 %) HCV pozitív minták (2,9 %) Reumatoid faktor (7,1 %) Szifilisz pozitív minták (2,3 %) Pontosság Az Access HIV combo assay pontossága 13 minta elemzésével került meghatározásra: egy negatív minta, egy alacsony pozitív minta (Low 1), egy Cut-off érték közeli minta (Low 2), egy közepes pozitív minta HIV-1, HIV-2, HIV-1-O és HIV antigénekre. A mérésen belüli pontosság meghatározása ezen 13 minta egyszeri 30 párhuzamosának 1 rendszeren történő megvizsgálásával történt. Meghatározásra kerültek a variációs koefficiensek (CV). A mérések közötti pontosság meghatározása ezen 13 minta 1 tételen belüli, párhuzamosított, 2 különböző napszakban (délelőtt és délután) 2 különböző kezelővel történő megvizsgálásával történt 20 napos időszak alatt. A tételek közti pontosság meghatározása ezen 13 minta 5 párhuzamosított mintán, 4 különböző tételben 4 különböző kalibrátor tételben történő megvizsgálásával történt. Az eredmények az alábbi táblázatokban láthatók: Mérésen belüli pontosság: N = 30 Átlag (jel / Cut off arány) % C.V. Negatív minták HIV Low 1 minták HIV HIV-1-O HIV-1 Antigén HIV Low 2 minták HIV HIV-1-O HIV-1 Antigén HIV Medium 1 minták HIV HIV-1-O HIV-1 Antigén Access HIV combo A97222B 11/22
12 Mérések közti pontosság: N = 80 Átlag (jel / Cut off arány) % C.V. Negatív minták HIV Low 1 minták HIV HIV-1-O HIV-1 Antigén HIV Low 2 minták HIV HIV-1-O HIV-1 Antigén HIV Medium 1 minták HIV HIV-1-O HIV-1 Antigén A97222B Access HIV combo 12/22
13 Lotok közötti pontosság: N = 20 Inter Cal % C.V Inter RP % C.V. Całkowity % C.V. Negatív minták HIV Low 1 minták HIV HIV-1-O HIV-1 Antigén HIV Low 2 minták HIV HIV-1-O HIV-1 Antigén HIV Medium 1 minták HIV HIV-1-O HIV-1 Antigén Az Access, SYNCHRON LX, UniCel, DxI és a Beckman Coulter logó a Beckman Coulter, Inc. védjegyei. * A Lumi- Phos a Lumigen, Inc., a Beckman Coulter, Inc. leányvállalatának a védjegye. ** A ProClin a Rohm and Haas Company vagy a leányvállalatainak vagy társvállalatainak a védjegye. Access HIV combo A97222B 13/22
14 A97222B Access HIV combo 14/22
15 HIV combo Calibrators REF A59429 Felhasználás Az Access HIV combo Kalibrátorok célja az Access HIV combo assay kalibrálása HIV-1 antigén és HIV-1/HIV-1-O/HIV-2 antitestek humán szérumban vagy plazmában (Lítium-heparin) való minőségi kimutatásának céljából Access Immunoassay Rendszerekkel történő alkalmazásakor. In Vitro diagnosztikai célra használható Az előállított és forgalomba hozott reagensek minőségügyi rendszerünk előírásainak vannak alávetve a nyersanyagok bevételezésétől kezdve a termék forgalomba kerüléséig. Minden egyes tétel minőségellenőrzésen esik át, és csak a jóváhagyási feltételeknek való megfelelőséget követően kerül forgalomba. Az egyes tételek előállítása és ellenőrzése során készült jegyzőkönyveket vállalatunk őrzi. Összefoglaló és magyarázat Nyomonkövethetőség Termékinformáció Az Access HIV combo Kalibrátorok célja a kalibrálás végrehajtása (Cut-off érték meghatározása) az Access HIV combo assay-hez. A minta által kibocsátott fény mennyiségének a Cut-off értékkel való összehasonlításával meghatározható a HIV-1 antigén és/vagy HIV-1/HIV-1-O/HIV-2 antitestek mintabeli jelenléte vagy hiánya. Az Access HIV combo Kalibrátorokban mérendő analit visszavezethető a gyártó munkakalibrátorához. A visszavezethetőségi eljárás az EN ISO szabványon alapul. Access HIV combo Kalibrátorok Katalógusszám A59429: C0-C1, 1,7 ml/ampulla Azonnal felhasználhatók. Tárolja függőleges helyzetben, 2-10 C hőmérsékleten. Az ampulla tartalmát óvatos felfordítással keverje össze használat előtt. Kerülje a buborékok kialakulását C közötti tárolás esetén minőségét megőrzi a címkén jelzett szavatossági időig C hőmérséklet között tárolva az ampulla minőségét megőrzi az első használattól számított 120 napig. Az esetleges károsodást a megfelelő tartományon kívüli határérték jelzi. r C0: Negatív (nem reaktív) humán szérum HIV-1 antigénre és HIV-1/HIV-1-O/ HIV-2 antitestekre 0,1 %-os nátrium-aziddal és 0,25 %-os ProClin*300-al. C1: Pozitív (reaktív) humán szérum anti-hiv-1 antitestekre 0,1 %-os nátrium-aziddal és 0,25 %-os ProClin*300-al. Kalibrációs kártya: 1 Access HIV combo 15/22 A97222B
16 Figyelmeztetések és óvintézkedések Eljárás Kalibrálási részletek Az eljárás korlátozásai In vitro diagnosztikai célra használható. A betegminták és a véralapú termékek rutinszerűen feldolgozhatók minimális kockázattal a leírt eljárás betartásával. Ugyanakkor ezeket a termékeket kezelje potenciálisan fertőző anyagként, és tartsa be az általános óvintézkedéseket, valamint a klinikai laboratóriumokban bevált gyakorlatokat, függetlenül a termékek eredetétől, kezelésétől vagy előző jelzésüktől. A dekontaminációhoz használjon megfelelő fertőtlenítőszert. Ezeket az anyagokat és tartályaikat a helyi szabályozásoknak és útmutatásoknak megfelelően tárolja és selejtezze le. A kalibrátorok elkészítéséhez használt emberi forrásanyagok vizsgálatokon estek át, amelynek eredményeképpen bebizonyosodott, hogy ezek nem reaktívak a hepatitisz B felületi antigénre (HBsAg), a hepatitisz C vírus antitestekre (HCV), a humán immundeficiencia vírus (HIV-1 és HIV-2) antitestekre és a HIV-1 antigénre, kivéve a C1 kalibrátort, amely pozitív eredményt ad HIV-1 antitestekre. Mivel semmilyen ismert tesztmódszer nem adhat teljes biztonságot a fertőző ágensek jelenlétének kizárására, a reagenseket és a betegmintákat fertőző betegségek továbbítására képes anyagként kezelje (37). A nátrium-azid reakcióba léphet az ólmot és rezet tartalmazó vezetékekkel, és így rendkívül robbanékony fém-azid alakulhat ki. Leselejtezéskor öblítse le nagy mennyiségű vízzel, így elkerülve az azid kialakulását (38). A ProClin*300 potenciálisan bőrizgató hatású. Kerülje ennek a reagensnek a bőrre vagy ruházatra való ömlését vagy fröccsenését. A reagenssel való kapcsolat esetén az érintett felületet alaposan mossa le vízzel és szappannal. Xn. Ártalmas: 0,1% nátrium-azid és 0,25% ProClin*300. R 22: Lenyelve ártalmas. R 43: Bőrrel érintkezve túlérzékenységet okozhat. S 23: A keletkező gázt/füstöt/gőzt/permetet nem szabad belélegezni. S 24: A bőrrel való érintkezés kerülendő. S 37: Megfelelő védőkesztyűt kell viselni. S 60: Az anyagot és/vagy edényzetét veszélyes hulladékként kell ártalmatlanítani. Az anyagbiztonsági adatlap (MSDS) kérésre rendelkezésre bocsátható. A kalibrációs elméletre, a kalibrátorok konfigurációjára, a kalibrátor teszt lekérésének bevitelére és a kalibrációs adatok áttekintésére vonatkozó információ ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. Az Access HIV combo kalibrátorok negatív (C0) és pozitív (C1) formában érhetők el. Az Access HIV combo assay kalibrálást igényel (a Cut-off érték meghatározása) annak érdekében, hogy aktív kalibrálással rendelkezzen. A kalibrálási adatok 56 napig érvényesek. Mindegyik kalibráláshoz 220 μl folyadék szükséges a C0 kalibrátorból (párhuzamos duplikát meghatározások) és 330 μl folyadék a C1 kalibrátorból (párhuzamos triplokát meghatározások) a mintatartály és a rendszer holttérfogatán túlmenően. Egy csepp körülbelül 40 μl folyadéknak felel meg. Amennyiben a reagens mikrobiológiai szennyeződésére utaló bizonyíték van, vagy az ampulla tartalma túlzottan zavaros, selejtezze le az ampullát. Az Access, SYNCHRON LX, UniCel, DxI és a Beckman Coulter logó a Beckman Coulter, Inc. védjegyei. * A ProClin a Rohm and Haas Company vagy a leányvállalatainak vagy társvállalatainak a védjegye. A97222B Access HIV combo 16/22
17 HIVcombo QC REF A59430 Felhasználás Az Access HIV combo QC célja az Access HIV combo assay rendszerteljesítményének a monitorozása. In Vitro diagnosztikai célra használható Az előállított és forgalomba hozott reagensek minőségügyi rendszerünk előírásainak vannak alávetve a nyersanyagok bevételezésétől kezdve a termék forgalomba kerüléséig. Minden egyes tétel minőségellenőrzésen esik át, és csak a jóváhagyási feltételeknek való megfelelőséget követően kerül forgalomba. Az egyes tételek előállítása és ellenőrzése során készült jegyzőkönyveket vállalatunk őrzi. Összefoglaló és magyarázat Nyomonkövethetőség Termékinformáció A minőségellenőrző anyagok a betegminták jellemzőit szimulálják, és nélkülözhetetlenek az Access HIV combo assay rendszerteljesítményének monitorozásához. Ezen túlmenően szerves részét képezik a bevált laboratóriumi gyakorlatnak (40, 43-49). A HIV-1 antigének és anti-hiv-1/hiv-1-o/hiv-2 antitestek kimutatását célzó, az Access reagensekkel végzett próbák elvégzésekor vonja bele a vizsgálatba a minőségellenőrző anyagokat a próba helyességének érvényesítése érdekében. A próba során nyert értékek az elfogadható tartományba kell essenek a tesztrendszer megfelelő működése esetén. Az Access HIV combo QC-ben mérendő érték (analit) visszavezethető a gyártó munkakalibrátorához. A visszavezethetőségi eljárás az EN ISO szabványon alapul. Access HIV combo QC Katalógusszám: A59430: 4,4 ml/ampulla, 2 ampulla szintenként Azonnal felhasználhatók. Tárolja függőleges helyzetben, 2-10 C hőmérsékleten. Az ampulla tartalmát óvatos felfordítással keverje össze használat előtt. Kerülje a buborékok kialakulását C közötti tárolás esetén minőségét megőrzi a címkén jelzett szavatossági időig C hőmérséklet között tárolva az ampulla minőségét megőrzi az első használattól számított 120 napig. Az esetleges károsodást a megfelelő tartományon kívüli határérték jelzi. A szórások (SD) és az átlagértékek ügyében tájékozódjon a minőségellenőrző kártyán szereplő értékből. Access HIV combo 17/22 A97222B
18 QC 1: Negatív (nem reaktív) humán szérum HIV-1 antigénre és anti HIV-1/HIV-1-O/ HIV-2 antitestekre, 0,1 %-os nátrium-aziddal és 0,25 %-os ProClin*300-al. QC 2: Pozitív (reaktív) humán szérum anti-hiv-1 antitestekre, 0,1 %-os nátrium-aziddal és 0,25 %-os ProClin*300-al. QC 3: QC kártya: 1 Hővel inaktivált, tisztított HIV-1 antigén chaotropikus hatóanyaggal, 0,1%-os ProClin*300-zal. Figyelmeztetések és óvintézkedések In vitro diagnosztikai célra használható. A betegminták és a véralapú termékek rutinszerűen feldolgozhatók minimális kockázattal a leírt eljárás betartásával. Ugyanakkor ezeket a termékeket kezelje potenciálisan fertőző anyagként, és tartsa be az általános óvintézkedéseket, valamint a klinikai laboratóriumokban bevált gyakorlatokat, függetlenül a termékek eredetétől, kezelésétől vagy előző jelzésüktől. A dekontaminációhoz használjon megfelelő fertőtlenítőszert. Ezeket az anyagokat és tartályaikat a helyi szabályozásoknak és útmutatásoknak megfelelően tárolja és selejtezze le. A minőségellenőrző anyag elkészítéséhez használt emberi forrásanyagok vizsgálatokon estek át, amelynek eredményeképpen bebizonyosodott, hogy ezek nem reaktívak a hepatitisz B felületi antigénre (HBsAg) és a hepatitisz C vírus (HCV) antitestekre. Mivel semmilyen ismert tesztmódszer nem adhat teljes biztonságot a fertőző ágensek jelenlétének kizárására, a reagenseket és a betegmintákat fertőző betegségek továbbítására képes anyagként kezelje (37). A nátrium-azid reakcióba léphet az ólmot és rezet tartalmazó vezetékekkel, és így rendkívül robbanékony fém-azid alakulhat ki. Kiselejtezéskor öblítse le nagy mennyiségű vízzel, így elkerülve az azid kialakulását (38). A ProClin*300 potenciálisan bőrizgató hatású. Kerülje ennek a reagensnek a bőrre vagy ruházatra való ömlését vagy fröccsenését. A reagenssel való kapcsolat esetén az érintett felületet alaposan mossa le vízzel és szappannal. Xn. Ártalmas: 0,1% nátrium-azid és 0,25% ProClin*300. R 22: Lenyelve ártalmas. R 43: Bőrrel érintkezve túlérzékenységet okozhat. S 23: A keletkező gázt/füstöt/gőzt/permetet nem szabad belélegezni. S 24: A bőrrel való érintkezés kerülendő. S 37: Megfelelő védőkesztyűt kell viselni. S 60: Az anyagot és/vagy edényzetét veszélyes hulladékként kell ártalmatlanítani. Az anyagbiztonsági adatlap (MSDS) kérésre rendelkezésre bocsátható. A97222B Access HIV combo 18/22
19 Eljárás Az eljárás korlátozásai Várható értékek Az Access HIV combo QC ugyanúgy kezelendő, mint a betegminták, használatának pedig az alkalmazott műszerre és / vagy módszerre vonatkozó utasításnak megfelelően kell történnie. Az Access HIV combo QC feldolgozásához 110 μl mennyiségű minta szükséges mindhárom szinten a mintatartály és a rendszer holttérfogatán túlmenően (egyszeri meghatározás). Egy csepp körülbelül 40 μl folyadéknak felel meg. Mivel a minták inkább véletlenszerű hozzáférés formátumban dolgozhatók fel bármikor, mint tömbösített formátumban, a minőségellenőrzési anyagok minden 24 órás időszakban a minták részét kell képezzék (40). A kontrollok gyakoribb használata vagy további kontrollok használat a felhasználó belátására van bízva, mely alapulhat a laboratóriumokban bevált gyakorlatokon vagy a laboratóriumi akkreditáció előírásain, avagy a hatályos törvényeken. A minőségellenőrzési elméletre, a minőségellenőrzés konfigurációjára, a minőségellenőrző tesztminta lekérésének bevitelére és a minőségellenőrzési adatok áttekintésére vonatkozó információ ügyében tájékozódjon a megfelelő rendszerkezelési kézikönyvből és/vagy a Súgó rendszerből. 1. Az Access HIV combo QC kizárólag az Access HIV combo assay-vel lett a gyártó által kipróbálva. 2. Mivel a minták inkább véletlenszerű hozzáférés formátumban dolgozhatók fel bármikor, mint tömbösített formátumban, a minőségellenőrzési anyagok minden 24 órás időszakban a minták részét kell képezzék (40). A laboratórium minőségellenőrző rendszerének képezze a részét bármely, kereskedelmi forgalomban kapható minőségellenőrző termék és / vagy egyéb forrásokból származó kiegészítő minőségellenőrző termék 3. Az elfogadható tartományon kívül eső minőségellenőrzési eredmények érvénytelen teszteredményekre utalhatnak. Ennek az analitnak a vonatkozásában vizsgálja meg az utolsó elfogadható minőségellenőrzési tesztpont óta készült összes teszteredményt. 4. Amennyiben a reagens mikrobiológiai szennyeződésére utaló bizonyíték van, vagy az ampulla tartalma túlzottan zavaros, selejtezze ki az ampullát. A várható Access HIV combo QC1, QC2 és QC3 átlagok ( ) és SD értékek (σ) a minőségellenőrző kártyán találhatók, amely az előzetes minőségellenőrzési rendszerkonfigurációhoz szükséges készlet részét képezik. Mindegyik laboratóriumnak kötelessége meghatározni a saját megfelelőségi kritériumait a minőségellenőrzési eredmények vonatkozásában alkalmazott minőségellenőrzési szabályok kiválasztásával. Az egyéni ellenőrzési eredmények az előzetesen meghatározott megfelelőségi tartományba kell essenek, ugyanakkor mindegyik laboratóriumnak kötelessége frissíteni az átlagértékeket és SD értékeket megfelelő mennyiségű adat összegyűjtését követően. Figyelembe véve azt, hogy az adott reaktivitási szintek váltakozhatnak a különböző gyártók próbái, a különböző eljárások, a különböző tételszámok és a különböző laboratóriumok függvényében, mindegyik laboratóriumnak kötelessége meghatározni az adott reaktivitási szintet és az elfogadható értékeket felölelő tartományt. A megfelelőségi tartomány az akár 30 napos időszakon belül elvégzett 20 meghatározás 20 adatpontjának átlagának ± 2 SD tartalmazhatja. A BIO-RAD JÓTÁLLÁST VÁLLAL AZÉRT, HOGY EZEK A TERMÉKEK A CÍMKÉKEN ÉS A BIZTOSÍTOTT IRODALOMBAN FOGLALTAKNAK MEGFELELŐEN TELJESÍTENEK. A BIO-RAD ELÁLL MINDEN VÉLELMEZETT JÓTÁLLÁSTÓL, AMI AZ ÉRTÉKESÍTHETŐSÉGRE VAGY A BÁRMILYEN EGYÉB CÉLRA TÖRTÉNŐ FELHASZNÁLHATÓSÁGRA VONATKOZIK. A BIO-RAD SEMMILYEN KÖRÜLMÉNYEK KÖZÖTT NEM VONHATÓ FELELŐSSÉGRE SEMMILYEN, A FENT EMLÍTETT KIFEJEZETT SZAVATOSSÁGBÓL ADÓDÓ BÁRMILYEN KÖVETKEZMÉNYES KÁROKÉRT. Az Access, SYNCHRON LX, UniCel, DxI és a Beckman Coulter logó a Beckman Coulter, Inc. védjegyei. * A ProClin a Rohm and Haas Company vagy a leányvállalatainak vagy társvállalatainak a védjegye. Access HIV combo A97222B 19/22
20 Referenciák 1 Barre-Sinoussi F., Chermann JC., Rey F. et al.: - Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immunodeficiency syndrome (AIDS). Science, 1983, 200, Popovic M., Sarngadhar M.G., Read E., Gallo R.C.: - Detection, isolation and continuous production of cytopathic retroviruses (HTLV III) from patients with AIDS AND pre-aids. Science, 1984, 224, Clavel F., Guetard D., Brun-Vézinet F. et al.: Isolation of a new human retrovirus from West African patients with AIDS. Science, 1986, 233: Barin F., M Boup S., Denis F. et al.: Serological evidence for virus related to simian T-lymphotropic retrovirus III in residents of West Africa. Lancet, 1985, 2: Clavel F., Brun-Vézinet F., Guetard D. et al.: - LAV II a second rétrovirus associé au SIDA en Afrique de l'ouest. C.R. Acad. Sc. Paris, 1986, 13, Clavel F.: HIV-2, the West African AIDS virus. AIDS, 1987, 1: Clavel F., Guyader M., Guetard D. et al.: Molecular cloning and polymorphism of the human immune deficiency virus type 2. Nature, 1986, 324: Gürtler L.G., Hauser P.H., Eberle J. et al.: A new subtype of human immunodeficiency virus type 1 (MVP-5180) from Cameroon. J. Virol., 1994, 68 (3): Leitner T.: Genetic subtypes of HIV-1. In Myers G, Korber BT, Foley BT et al., editors. Human Retroviruses and AIDS. Los Alamos National Laboratory, 1996, III-28-III-40. (Available on-line at 10 Peeters M., Gueye A., M Boup S., et al.: Geographical distribution of HIV-1 group 0 viruses in Africa. AIDS, 1997, 11, Robertson D.L., Anderson J.P., Bradac J.A, et al.: HIV-1 nomenclature proposal: a reference guide to HIV-1 classification. In: Kuiken CL, Foley B, Hahn B, et al., editors. Human Retroviruses and AIDS. Los Alamos National Laboratory, 1999, (Available on-line at 12 Simon F., Mauclere P., Roques P. et al.: Identification of a new human immunodeficiency virus type 1 distinct from group M and group O. Nature Medicine, 1998, 4 (9): Plantier J.C., Leoz M., Dickerson J.E. et al. : A new human immunodeficiency virus derived from gorillas. Nature Medicine, 2009, 15: Peeters M.: Recombinant HIV sequences: their role in the global epidemic. In: Kuiken C, Foley B, Hahn B, et al., editors. HIV sequence compendium. Los Alamos National Laboratory, 2000, (Available on-line at 15 Couroucé A.M. Et al.: A prospective study of HIV II prevalence in France. AIDS, 1988, 2: Janssens W., Buve A., Nkengason J.N: The puzzle of HIV-A subtypes in Africa. AIDS, 1997, 11: Apetrei C., Loussert-Ajaka I., Descamps D., et al.: Lack of screening test sensitivity during HIV-1 non subtype B seroconversion. AIDS, 1996, 10: F57-F Kanki P.J., Barin G., M Boup S. et al.: New human T-Lymphotropic retrovirus related to Simian T-lymphotropic virus type III (STLV III Agm). Science, : Gao F., Yue L. Robertson D.L. et al.: Genetic diversity of human immunodeficiency virus type 2: evidence for distinct sequence subtypes with differences in virus biology. J. Virol. 1994, 68: Norrby E., Biberfeld G., Johnson P.R., et al.: The chemistry of Site-Directed Serology for HIV infections. AIDS Res and Human Retroviruses, 1989, 5(5): DeCock K.M., Adjorlolo G., Ekpini E., et al.: Epidemiology and transmission of HIV-2: why there is no HIV-2 pandemic. JAMA, 1993, 270: Kanki P.J., Travers K.U., M Boup S., et al.: Slower heterosexual spread of HIV-2 than HIV-1. Lancet, 1994, 343: Marlink R.G., Ricard D., M Boup S., et al.: Clinical, hematologic, and immunologic cross-sectional evaluation of individuals exposed to human immunodeficiency virus type-2 (HIV-2). AIDS, Res Hum Retroviruses 1988, 4: Simon F., Matheron S., Tamalet C., et al.: Cellular and plasma viral load in patients infected with HIV-2. AIDS, 1993, 7: Gürtler L.: Difficulties and strategies of HIV diagnosis. The Lancet, 1996, 348 (9021): ; 26 Petersen L.R., Satten G.A., Dodd R., et al.: Duration of time from onset of human immunodeficiency virus type 1 infectiousness to development of detectable antibody. 1994, 34 (4): Constantine N.T.: Serologic tests for retroviruses: approaching a decade of evolution. AIDS, 1993, 7: Zaaijer H.L., Exel-Oehlers P.V., Kraaijeveld T., et al.: Early detection of antibodies to HIV1 by third-generation assays. The Lancet, 1992, 340: Nair B.C., Ford G., Kalyanaraman V.S., et al.: Enzyme immunoassay using native envelope glycoprotein (gp 160) for detection of human immunodeficiency virus type 1 antibodies. J. Clin. Microbio., 1994, 32: Courcoué A.M., Barin F., Boudelot J., Botté C et al. : - Réévaluation de la sensibilité de 19 trousses de dépistage des anticorps anti-vih. Revue Française des Laboratoires, 1995, 279 : Busch M.P., Satten G.A.: Time course of viremia and antibody seroconversion following human immunodefiency virus exposure. American Journal of Medicine, 1997, 102: Busch M.P., Lee L.L.L., Satten G.A., et al.: Time course of detection of viral and serologic markers preceding human immunodeficiency virus type 1 seroconversion: implications for screening of blood and tissue donors. Transfusion, 1995, 35 (2): Gürtler, L., Muhlbacher A., Michl U., et al.: Reduction of the diagnostic window with a new combined p24 antigen and human immunodeficiency virus antibody screening assay. Journal Virological Methods, 1998, 75: A97222B Access HIV combo 20/22
ACCESS Immunoassay System. HIV combo QC4 & QC5. Az Access HIV combo próba rendszer-teljesítményének monitorozásához. B71111A - [HU] /01
![ACCESS Immunoassay System. HIV combo QC4 & QC5. Az Access HIV combo próba rendszer-teljesítményének monitorozásához. B71111A - [HU] /01 ACCESS Immunoassay System. HIV combo QC4 & QC5. Az Access HIV combo próba rendszer-teljesítményének monitorozásához. B71111A - [HU] /01](/thumbs/53/32115786.jpg) ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Az Access HIV combo próba rendszer-teljesítményének monitorozásához. - [HU] - 2015/01 Tartalomjegyzék Access HIV combo QC4 & QC5 1 Rendeltetés... 3
ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Az Access HIV combo próba rendszer-teljesítményének monitorozásához. - [HU] - 2015/01 Tartalomjegyzék Access HIV combo QC4 & QC5 1 Rendeltetés... 3
HIV combo Calibrators
 ACCESS Immunoassay System HIV combo 2 x 50 A59428 A HIV p24 antigén és a HIV-1/O/2 elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS
ACCESS Immunoassay System HIV combo 2 x 50 A59428 A HIV p24 antigén és a HIV-1/O/2 elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS
HCV Ab PLUS 34330 2 x 50. HCV Ab PLUS CALIBRATORS 34335. HCV Ab PLUS QC 34339
 ACCESS Immunoassay System HCV Ab PLUS 34330 2 x 50 A HCV elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS Immunoassay System HCV Ab
ACCESS Immunoassay System HCV Ab PLUS 34330 2 x 50 A HCV elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS Immunoassay System HCV Ab
In vitro diagnosztikai alkalmazásra
 HCV Ab PLUS 34330 Alkalmazás Az Access HCV Ab PLUS teszt az Access immunvizsgálati rendszerek (Access, Access 2, UniCel DxI ) segítségével működő enzimimmunoassay módszer a hepatitis C vírussal szemben
HCV Ab PLUS 34330 Alkalmazás Az Access HCV Ab PLUS teszt az Access immunvizsgálati rendszerek (Access, Access 2, UniCel DxI ) segítségével működő enzimimmunoassay módszer a hepatitis C vírussal szemben
CMV-IgM-ELA Test PKS medac. Magyar 110-PKS-VPU/010512
 CMVIgMELA Test PKS medac Magyar 0123 110PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
CMVIgMELA Test PKS medac Magyar 0123 110PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
Hantavírus (Puumala) IgG/IgM-ELISA. 4. Szükséges anyagok és reagensek, amelyeket a teszt nem tartalmaz. Használati Utasítás /Instruction Sheet/
 Hantavírus (Puumala) IgG/IgM- Enzimes immunvizsgálat az IgG és az IgM Puumala szerotipusú antitestek meghatározására. Kódszám: Tartalom: Tárolás: PR59156 96 teszt +2-8ºC Használati Utasítás /Instruction
Hantavírus (Puumala) IgG/IgM- Enzimes immunvizsgálat az IgG és az IgM Puumala szerotipusú antitestek meghatározására. Kódszám: Tartalom: Tárolás: PR59156 96 teszt +2-8ºC Használati Utasítás /Instruction
Magyarország-Budapest: Vérvizsgálati reagensek 2013/S Tájékoztató az eljárás eredményéről. Árubeszerzés
 1/5 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:341991-2013:text:hu:html Magyarország-Budapest: Vérvizsgálati reagensek 2013/S 198-341991 Tájékoztató az eljárás eredményéről
1/5 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:341991-2013:text:hu:html Magyarország-Budapest: Vérvizsgálati reagensek 2013/S 198-341991 Tájékoztató az eljárás eredményéről
HCV Ab V3 Calibrators
 ACCESS Immunoassay System HCV Ab V3 2 x 50 B33458 A HCV elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS Immunoassay System HCV Ab V3
ACCESS Immunoassay System HCV Ab V3 2 x 50 B33458 A HCV elleni antitestek minőségi kimutatása humán szérumban és plazmában az Access Immunoassay Systems segítségével. ACCESS Immunoassay System HCV Ab V3
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban
 11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
Quality Control a napi gyakorlatban
 Quality Control a napi gyakorlatban Fizil Attila Bio-Rad Magyarország Kft. A laboratóriumi vizsgálatok kontrollrendszerei Belsı kontroll (IQC) kalibrátorok valódiság kontrollok gyártói kontrollok független
Quality Control a napi gyakorlatban Fizil Attila Bio-Rad Magyarország Kft. A laboratóriumi vizsgálatok kontrollrendszerei Belsı kontroll (IQC) kalibrátorok valódiság kontrollok gyártói kontrollok független
QUANTA Flash Jo-1 701163 In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORT CÉLJÁRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ.
 QUANTA Flash Jo-1 701163 In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORT CÉLJÁRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ. Javasolt alkalmazás The QUANTA Flash Jo-1 kemilumineszcens immunoassay (CIA)
QUANTA Flash Jo-1 701163 In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORT CÉLJÁRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ. Javasolt alkalmazás The QUANTA Flash Jo-1 kemilumineszcens immunoassay (CIA)
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén
 Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
QUANTA Lite TM OMP Plus ELISA 704530 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas
 QUANTA Lite TM OMP Plus ELISA 704530 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas Alkalmazási terület A QUANTA Lite TM OMP Plus készlet enzimhez kapcsolt immunszorbens assay (ELISA), amely
QUANTA Lite TM OMP Plus ELISA 704530 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas Alkalmazási terület A QUANTA Lite TM OMP Plus készlet enzimhez kapcsolt immunszorbens assay (ELISA), amely
HASZNÁLATI UTASÍTÁS PARASITE SUSPENSIONS. n Parasite Suspensions formalinban FELHASZNÁLÁSI JAVALLAT ÖSSZEFOGLALÁS ÉS MAGYARÁZAT ALAPELVEK ÖSSZETÉTEL
 HASZNÁLATI UTASÍTÁS n Parasite Suspensions formalinban FELHASZNÁLÁSI JAVALLAT A Microbiologics Parasite Suspensions minőségbiztosítási programokat támogatnak, mivel olyan minőség-ellenőrzési provokációs
HASZNÁLATI UTASÍTÁS n Parasite Suspensions formalinban FELHASZNÁLÁSI JAVALLAT A Microbiologics Parasite Suspensions minőségbiztosítási programokat támogatnak, mivel olyan minőség-ellenőrzési provokációs
HIV-1/2 Ag/Ab Combo. Jelmagyarázat. Tárolás 2 30ºC-on. CHASE BUFFER Chase puffer. EDTA CAPILLARY TUBES EDTA kapilláris csövek REF 7D2646, 7D2647
 REF 7D2646, 7D2647 Determine HIV-1/2 Ag/Ab Combo Jelmagyarázat Tárolás 2 30ºC-on. CHASE BUFFER Chase puffer EDTA CAPILLARY TUBES EDTA kapilláris csövek november 2013 241052HU Determine HIV-1/2 Ag/Ab Combo
REF 7D2646, 7D2647 Determine HIV-1/2 Ag/Ab Combo Jelmagyarázat Tárolás 2 30ºC-on. CHASE BUFFER Chase puffer EDTA CAPILLARY TUBES EDTA kapilláris csövek november 2013 241052HU Determine HIV-1/2 Ag/Ab Combo
BACTEC Mycosis-IC/F Culture Vials Szeletkív tápközeg élesztõkhöz és gombákhoz
 BACTEC Mycosis-IC/F Culture Vials Szeletkív tápközeg élesztõkhöz és gombákhoz Magyar HASZNÁLATI JAVASLAT BACTEC Mycosis-IC/F tenyésztõ palackok aerob vérkultúrákhoz használandók. Elsõsorban élesztõk és
BACTEC Mycosis-IC/F Culture Vials Szeletkív tápközeg élesztõkhöz és gombákhoz Magyar HASZNÁLATI JAVASLAT BACTEC Mycosis-IC/F tenyésztõ palackok aerob vérkultúrákhoz használandók. Elsõsorban élesztõk és
Genscreen HIV-1/2 Version 2 1 lemez lemez
 Genscreen HIV-1/2 Version 2 1 lemez 96 72278 5 lemez 480 72279 SZŰRŐVIZSGÁLATI TESZTKÉSZLET HIV-1 ÉS HIV-2 ELLENANYAGOK KIMUTATÁSÁRA SZÉRUMBÓL VAGY PLAZMÁBÓL ENZIM-IMMUNASSAY MÓDSZERREL 883666-2014/01
Genscreen HIV-1/2 Version 2 1 lemez 96 72278 5 lemez 480 72279 SZŰRŐVIZSGÁLATI TESZTKÉSZLET HIV-1 ÉS HIV-2 ELLENANYAGOK KIMUTATÁSÁRA SZÉRUMBÓL VAGY PLAZMÁBÓL ENZIM-IMMUNASSAY MÓDSZERREL 883666-2014/01
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 8. előadás Immunszerológia, immunkémia Az immunoassay-k érzékenysége A fő szérumfehérje frakciók és az ahhoz tartozó fehérjék Az Ig valencia és aviditás viszonya
Immunológiai módszerek a klinikai kutatásban 8. előadás Immunszerológia, immunkémia Az immunoassay-k érzékenysége A fő szérumfehérje frakciók és az ahhoz tartozó fehérjék Az Ig valencia és aviditás viszonya
2. Fotometriás mérések II.
 2. Fotometriás mérések II. 2008 október 31. 1. Ammónia-nitrogén mérése alacsony mérési tartományban és szabad ammónia becslése 1.1. Háttér A módszer alkalmas kis ammónia-nitrogén koncentrációk meghatározására;
2. Fotometriás mérések II. 2008 október 31. 1. Ammónia-nitrogén mérése alacsony mérési tartományban és szabad ammónia becslése 1.1. Háttér A módszer alkalmas kis ammónia-nitrogén koncentrációk meghatározására;
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban
 11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása - (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása - (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011.
 BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011. 1 Mérési adatok feldolgozása A mérési eredmény megadása A mérés dokumentálása A vállalati mérőeszközök nyilvántartása 2 A mérés célja: egy
BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011. 1 Mérési adatok feldolgozása A mérési eredmény megadása A mérés dokumentálása A vállalati mérőeszközök nyilvántartása 2 A mérés célja: egy
Használati útmutató IVD Matrix HCCA-portioned
 Használati útmutató IVD Matrix HCCA-portioned Tisztított mátrixanyag mátrixtámogatott lézer deszorpciós és ionizációs repülési idő tömegspektrometriához (MALDI-TOF-MS). A CARE termékek ügyfeleink kiváló
Használati útmutató IVD Matrix HCCA-portioned Tisztított mátrixanyag mátrixtámogatott lézer deszorpciós és ionizációs repülési idő tömegspektrometriához (MALDI-TOF-MS). A CARE termékek ügyfeleink kiváló
Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában
 Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában Minőségi indikátorok az analitikai szakaszban Dr. Kocsis Ibolya Semmelweis Egyetem Laboratóriumi Medicina Intézet Központi Laboratórium
Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában Minőségi indikátorok az analitikai szakaszban Dr. Kocsis Ibolya Semmelweis Egyetem Laboratóriumi Medicina Intézet Központi Laboratórium
EZ-FPC mikroorganizmusok
 EZ-FPC mikroorganizmusok Az EZ-FPC mikroorganizmus preparátumok segítségével kihívás elé állíthatóak az ételbiztonsági és ételminőségi minőségi és mennyiségi tesztmódszerek. RENDELTETÉS Az EZ-FPC (Food
EZ-FPC mikroorganizmusok Az EZ-FPC mikroorganizmus preparátumok segítségével kihívás elé állíthatóak az ételbiztonsági és ételminőségi minőségi és mennyiségi tesztmódszerek. RENDELTETÉS Az EZ-FPC (Food
1. SZAKASZ- - - - - - - - - - - - - - - - - A TERMÉK MEGHATÁROZÁSA - - - - - - - - - - - - - - - - - - - - - - - - - -
 B I Z T O N S Á G I A D A T L A P ECN: 435936 Módosítás dátuma: 04/10/13 Mód. 0 KIZÁRÓLAG EXPORTCÉLÚ FELHASZNÁLÁSRA - AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ 1. SZAKASZ- - - - - - - - - - - - - - - -
B I Z T O N S Á G I A D A T L A P ECN: 435936 Módosítás dátuma: 04/10/13 Mód. 0 KIZÁRÓLAG EXPORTCÉLÚ FELHASZNÁLÁSRA - AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ 1. SZAKASZ- - - - - - - - - - - - - - - -
Újrahasznosítás előkészítése útmutatás VITROS 5600 integrált rendszer VITROS XT 7600 integrált rendszer
 Újrahasznosítás előkészítése útmutatás VITROS 5600 integrált rendszer VITROS XT 7600 integrált rendszer Kiadvány száma: J39845 HU Kiadás dátuma: 2018-05-07 Cél A VITROS 5600, illetve XT 7600 integrált
Újrahasznosítás előkészítése útmutatás VITROS 5600 integrált rendszer VITROS XT 7600 integrált rendszer Kiadvány száma: J39845 HU Kiadás dátuma: 2018-05-07 Cél A VITROS 5600, illetve XT 7600 integrált
Kémiai jellemzők: felületaktív anyagok és ártalmatlan összetevők keveréke Ártalmas összetevők:
 Biztonsági adatlap a 1907/2006/EK szerint 1. Az anyag/készítmény/vállalat azonosítása Termék: Regisztrációs szám: Felhasználás: Azonosított felhasználás: CLFBUBBLE5L besorolás szappanbuborék készítés Gyártó/szállító:
Biztonsági adatlap a 1907/2006/EK szerint 1. Az anyag/készítmény/vállalat azonosítása Termék: Regisztrációs szám: Felhasználás: Azonosított felhasználás: CLFBUBBLE5L besorolás szappanbuborék készítés Gyártó/szállító:
COOPEX-B TETŰIRTÓ POROZÓSZER
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/6 BIZTONSÁGI ADATLAP COOPEX-B TETŰIRTÓ POROZÓSZER 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: használatra kész, ember
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/6 BIZTONSÁGI ADATLAP COOPEX-B TETŰIRTÓ POROZÓSZER 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: használatra kész, ember
Ax-DL100 - Lézeres Távolságmérő
 Ax-DL100 - Lézeres Távolságmérő 1. Áttekintés Köszönjük, hogy a mi termékünket választotta! A biztosnágos és megfelelő működés érdekében, kérjük alaposan olvassa át a Qick Start kézikönyvet. A globálisan
Ax-DL100 - Lézeres Távolságmérő 1. Áttekintés Köszönjük, hogy a mi termékünket választotta! A biztosnágos és megfelelő működés érdekében, kérjük alaposan olvassa át a Qick Start kézikönyvet. A globálisan
akkreditálása Dr. Dán D n Anikó Központi Laboratórium rium
 Point of care vizsgálatok akkreditálása Dr. Dán D n Anikó Kenézy Gyula KórhK rház-ri. Központi Laboratórium rium Ki törődik t a minőséggel? Technikai fejlődés Gyártók szerepe Laboratóriumok szerepe - személyi
Point of care vizsgálatok akkreditálása Dr. Dán D n Anikó Kenézy Gyula KórhK rház-ri. Központi Laboratórium rium Ki törődik t a minőséggel? Technikai fejlődés Gyártók szerepe Laboratóriumok szerepe - személyi
PLATELIA Mumps IgM TESZT
 PLATELIA Mumps IgM 72689 48 TESZT MUMPS VÍRUS ELLENI IgM ANTITESTEK MINŐSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL Ref. 91076/BRD 1/9 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2. A TESZT ÁTTEKINTÉSE
PLATELIA Mumps IgM 72689 48 TESZT MUMPS VÍRUS ELLENI IgM ANTITESTEK MINŐSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL Ref. 91076/BRD 1/9 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2. A TESZT ÁTTEKINTÉSE
GYORSTESZTEK ALKALMAZÁSA A
 GYORSTESZTEK ALKALMAZÁSA A GYÓGYSZERTÁRAKBAN DR. MISETA ILDIKÓ GÖLLE, SZENT ISTVÁN GYÓGYSZERTÁR Rozsnyay Mátyás emlékverseny Debrecen, 2012. május 10-12. BEVEZETÉS - CÉLKITŰZÉS Miért kell a gyorstesztekkel
GYORSTESZTEK ALKALMAZÁSA A GYÓGYSZERTÁRAKBAN DR. MISETA ILDIKÓ GÖLLE, SZENT ISTVÁN GYÓGYSZERTÁR Rozsnyay Mátyás emlékverseny Debrecen, 2012. május 10-12. BEVEZETÉS - CÉLKITŰZÉS Miért kell a gyorstesztekkel
In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORTCÉLÚ FELHASZNÁLÁSRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ.
 QUANTA Flash Reagensek Scl-70 701158 In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORTCÉLÚ FELHASZNÁLÁSRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ. Javasolt alkalmazás The QUANTA Flash Scl-70 kemilumineszcens
QUANTA Flash Reagensek Scl-70 701158 In Vitro diagnosztikai alkalmazásra KIZÁRÓLAG EXPORTCÉLÚ FELHASZNÁLÁSRA. AZ EGYESÜLT ÁLLAMOKBAN NEM FORGALMAZHATÓ. Javasolt alkalmazás The QUANTA Flash Scl-70 kemilumineszcens
Kontrol kártyák használata a laboratóriumi gyakorlatban
 Kontrol kártyák használata a laboratóriumi gyakorlatban Rikker Tamás tudományos igazgató WESSLING Közhasznú Nonprofit Kft. 2013. január 17. Kis történelem 1920-as években, a Bell Laboratórium telefonjainak
Kontrol kártyák használata a laboratóriumi gyakorlatban Rikker Tamás tudományos igazgató WESSLING Közhasznú Nonprofit Kft. 2013. január 17. Kis történelem 1920-as években, a Bell Laboratórium telefonjainak
hungarian Item# 3001-2177-70 rev. 05/12 HUN 1001-0284 - 25 Teszt 1001-0285 - 100 Teszt
 1001-0284 - 25 Teszt 1001-0285 - 100 Teszt hungarian Ezt a használati útmutatót teljesen olvassa el a termék használata előtt. A teszt elvégzésekor pontosan kövesse az utasításokat, figyelmen kívül hagyásuk
1001-0284 - 25 Teszt 1001-0285 - 100 Teszt hungarian Ezt a használati útmutatót teljesen olvassa el a termék használata előtt. A teszt elvégzésekor pontosan kövesse az utasításokat, figyelmen kívül hagyásuk
CytoFuge 2 Sejtkoncentrátor. Felhasználói kézikönyv
 CytoFuge 2 Sejtkoncentrátor Felhasználói kézikönyv VIGYÁZAT A minták kezelésekor az általános laboratóriumi biztonsági szabályokat tartsuk be, függetlenül attól, hogy ismerten fertz mintát kezelünk-e vagy
CytoFuge 2 Sejtkoncentrátor Felhasználói kézikönyv VIGYÁZAT A minták kezelésekor az általános laboratóriumi biztonsági szabályokat tartsuk be, függetlenül attól, hogy ismerten fertz mintát kezelünk-e vagy
Synovasure PJI immunkromatográfiás tesztkontroll-készlet
 Synovasure PJI immunkromatográfiás tesztkontroll-készlet Alfa-defenzin teszt periprosztetikus ízületi gyulladáshoz Forgalmazza: További információért látogasson el a www.cddiagnostics.com oldalra A termék
Synovasure PJI immunkromatográfiás tesztkontroll-készlet Alfa-defenzin teszt periprosztetikus ízületi gyulladáshoz Forgalmazza: További információért látogasson el a www.cddiagnostics.com oldalra A termék
REFERENCIA MÉRÉSI RENDSZEREK A GENETIKAI DIAGNOSZTIKÁBAN: DNS-ALAPÚ REFERENCIA ANYAGOK FEJLESZTÉSE. PhD tézis rövid összefoglaló.
 REFERENCIA MÉRÉSI RENDSZEREK A GENETIKAI DIAGNOSZTIKÁBAN: DNS-ALAPÚ REFERENCIA ANYAGOK FEJLESZTÉSE PhD tézis rövid összefoglaló Márki-Zay János Reference Materials Unit, Institute for Reference Materials
REFERENCIA MÉRÉSI RENDSZEREK A GENETIKAI DIAGNOSZTIKÁBAN: DNS-ALAPÚ REFERENCIA ANYAGOK FEJLESZTÉSE PhD tézis rövid összefoglaló Márki-Zay János Reference Materials Unit, Institute for Reference Materials
Platelia Mumps IgG. 1 lemez /12 MUMPS VÍRUS ELLENI IGG ANTITESTEK MINŐSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL
 Platelia Mumps IgG 1 lemez - 48 72688 MUMPS VÍRUS ELLENI IGG ANTITESTEK MINŐSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL 2014/12 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2. A TESZT ÁTTEKINTÉSE
Platelia Mumps IgG 1 lemez - 48 72688 MUMPS VÍRUS ELLENI IGG ANTITESTEK MINŐSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL 2014/12 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2. A TESZT ÁTTEKINTÉSE
A Virológiai főosztály szolgáltatásainak jegyzéke
 Virológiai főosztály szolgáltatásainak jegyzéke Virológiai főosztály osztályai (VF) laboratóriumi diagnosztikai vizsgálatokat végeznek, a megrendelő(k) által beküldött, és az Intézet Vérvételi helyén vett
Virológiai főosztály szolgáltatásainak jegyzéke Virológiai főosztály osztályai (VF) laboratóriumi diagnosztikai vizsgálatokat végeznek, a megrendelő(k) által beküldött, és az Intézet Vérvételi helyén vett
Nova Vet vércukor és β-keton szint meghatározó készülék HASZNÁLATI UTASÍTÁS
 Nova Biomedical Taiwan Corporation New Taipei City Taiwan 235 (R.O.C.) vevőszolgálat: www.novacares.com Made in Taiwan Nova Vet vércukor és β-keton szint meghatározó készülék HASZNÁLATI UTASÍTÁS U.S. Patent
Nova Biomedical Taiwan Corporation New Taipei City Taiwan 235 (R.O.C.) vevőszolgálat: www.novacares.com Made in Taiwan Nova Vet vércukor és β-keton szint meghatározó készülék HASZNÁLATI UTASÍTÁS U.S. Patent
5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK
 1 5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK 07/2009:50205 javított 6.5 1. ALKALMAZÁSI TERÜLET Az állatgyógyászati célra szánt immunológiai gyógyszerek
1 5.2.5. ÁLLATGYÓGYÁSZATI IMMUNOLÓGIAI GYÓGYSZEREK ELŐÁLLÍTÁSÁRA SZÁNT ÁLLATI EREDETŰ ANYAGOK 07/2009:50205 javított 6.5 1. ALKALMAZÁSI TERÜLET Az állatgyógyászati célra szánt immunológiai gyógyszerek
2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN
 2.6.16. Vizsgálatok idegen kórokozókra Ph.Hg.VIII. - Ph.Eur.7.0 1 2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN 01/2011:20616 Azokhoz a vizsgálatokhoz, amelyekhez a vírust előzőleg
2.6.16. Vizsgálatok idegen kórokozókra Ph.Hg.VIII. - Ph.Eur.7.0 1 2.6.16. VIZSGÁLATOK IDEGEN KÓROKOZÓKRA HUMÁN ÉLŐVÍRUS-VAKCINÁKBAN 01/2011:20616 Azokhoz a vizsgálatokhoz, amelyekhez a vírust előzőleg
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST BIZTONSÁGI ADATLAP PESTSTOP B 5 CS
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: mikrokapszulázott rovarirtó koncentrátum A készítmény
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: mikrokapszulázott rovarirtó koncentrátum A készítmény
Transzfúzióval átvihető fertőzések Véradó donorok fertőző ágens szűrővizsgálatai. Terenyei Eszter OVSzK Donorkivizsgáló Laboratórium
 Transzfúzióval átvihető fertőzések Véradó donorok fertőző ágens szűrővizsgálatai Terenyei Eszter OVSzK Donorkivizsgáló Laboratórium Transzfúzióval átvihető fertőző ágensek Vírusok Legkomolyabb kockázat:
Transzfúzióval átvihető fertőzések Véradó donorok fertőző ágens szűrővizsgálatai Terenyei Eszter OVSzK Donorkivizsgáló Laboratórium Transzfúzióval átvihető fertőző ágensek Vírusok Legkomolyabb kockázat:
December 1. az AIDS világnapja. 1th December is the World AIDS Day. Dr. Forrai Judit
 December 1. az AIDS világnapja 1th December is the World AIDS Day forrai.judit@med.semmelweis-univ.hu Semmelweis Egyetem Népegészségtani Intézet Initially submitted November 15, 2013; accepted for publication
December 1. az AIDS világnapja 1th December is the World AIDS Day forrai.judit@med.semmelweis-univ.hu Semmelweis Egyetem Népegészségtani Intézet Initially submitted November 15, 2013; accepted for publication
PROTECT-B PUMPÁS KULLANCS- ÉS SZÚNYOGRIASZTÓ AEROSZOL
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT-B PUMPÁS KULLANCS- ÉS SZÚNYOGRIASZTÓ AEROSZOL 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa:
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT-B PUMPÁS KULLANCS- ÉS SZÚNYOGRIASZTÓ AEROSZOL 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa:
Kalibráló oldatok a ph-érték méréséhez
 Kalibráló oldatok a méréséhez A ph oldatokkal a ph-mérők kalibrálása végezhető el a teljes ph-tartományban. A puffer oldatok többféle mennyiséget tartalmazó kiszerelésben vásárolhatók meg, ilyenek például
Kalibráló oldatok a méréséhez A ph oldatokkal a ph-mérők kalibrálása végezhető el a teljes ph-tartományban. A puffer oldatok többféle mennyiséget tartalmazó kiszerelésben vásárolhatók meg, ilyenek például
TECHNIKAI ADATLAP 1. SZAKASZ AZ ANYAG/KEVERÉK ÉS A VÁLLALAT/VÁLLALKOZÁS AZONOSÍTÁSA:
 lakk Elkészítés időpontja: 2012.02.05. 1 / 4. oldal TECHNIKAI ADATLAP 1. SZAKASZ AZ ANYAG/KEVERÉK ÉS A VÁLLALAT/VÁLLALKOZÁS AZONOSÍTÁSA: 1.1. Termék azonosító: Termékszám: JK 246 221 00 PN 112 474 06 Korrózió
lakk Elkészítés időpontja: 2012.02.05. 1 / 4. oldal TECHNIKAI ADATLAP 1. SZAKASZ AZ ANYAG/KEVERÉK ÉS A VÁLLALAT/VÁLLALKOZÁS AZONOSÍTÁSA: 1.1. Termék azonosító: Termékszám: JK 246 221 00 PN 112 474 06 Korrózió
Posztanalitikai folyamatok az orvosi laboratóriumban, az eredményközlés felelőssége
 Posztanalitikai folyamatok az orvosi laboratóriumban, az eredményközlés felelőssége Autovalidálási folyamatok Lókiné Farkas Katalin Az autovalidálás elméleti alapjai Az előző eredménnyel való összehasonlítás
Posztanalitikai folyamatok az orvosi laboratóriumban, az eredményközlés felelőssége Autovalidálási folyamatok Lókiné Farkas Katalin Az autovalidálás elméleti alapjai Az előző eredménnyel való összehasonlítás
PROTECT -B HÁZTARTÁSI POROZÓSZER
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT -B HÁZTARTÁSI POROZÓSZER 1. A KÉSZÍTMÉNY NEVE Az anyag és készítmény azonosítása: A készítmény típusa: inszekticid tartalmú
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT -B HÁZTARTÁSI POROZÓSZER 1. A KÉSZÍTMÉNY NEVE Az anyag és készítmény azonosítása: A készítmény típusa: inszekticid tartalmú
Debreczeni Lóránd, Kovácsay Anna,Szakony Szilvia Fővárosi Önkormányzat Szent Imre Kórház, Központi Laboratórium
 Verifikált módszerek m belső minőségellen gellenőrzése (IQC) Debreczeni Lóránd, Kovácsay Anna,Szakony Szilvia Fővárosi Önkormányzat Szent Imre Kórház, Központi Laboratórium BioRad Továbbképzés, Budapest
Verifikált módszerek m belső minőségellen gellenőrzése (IQC) Debreczeni Lóránd, Kovácsay Anna,Szakony Szilvia Fővárosi Önkormányzat Szent Imre Kórház, Központi Laboratórium BioRad Továbbképzés, Budapest
PROTECT SZÚNYOG ÉS KULLANCS RIASZTÓ AEROSZOL (PUMPÁS)
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT SZÚNYOG ÉS KULLANCS RIASZTÓ AEROSZOL (PUMPÁS) 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa:
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT SZÚNYOG ÉS KULLANCS RIASZTÓ AEROSZOL (PUMPÁS) 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa:
Syphilis Total Ab 1 lemezes 96 72530 5 lemezes 480 72531
 Syphilis Total Ab 1 lemezes 96 72530 5 lemezes 480 72531 A TREPONEMA PALLIDUM ELLENI ANTITEST HUMÁN SZÉRUMBAN VAGY PLAZMÁBAN ENZIM IMMUNPRÓBA TECHNIKÁVAL TÖRTÉNŐ KVALITATÍV KIMUTATÁSÁRA SZOLGÁLÓ KÉSZLETEK
Syphilis Total Ab 1 lemezes 96 72530 5 lemezes 480 72531 A TREPONEMA PALLIDUM ELLENI ANTITEST HUMÁN SZÉRUMBAN VAGY PLAZMÁBAN ENZIM IMMUNPRÓBA TECHNIKÁVAL TÖRTÉNŐ KVALITATÍV KIMUTATÁSÁRA SZOLGÁLÓ KÉSZLETEK
Racionális kontrollfelhasználás, sokparaméteres kontrollok. (Fizil Attila, Bio-Rad Magyarország Kft.)
 Racionális kontrollfelhasználás, sokparaméteres kontrollok (Fizil Attila, Bio-Rad Magyarország Kft.) KALIBRÁTOR KONTROLL Navigare necesse est... Ha már muszáj, csináljuk értelmesen! 1. Határozzuk meg a
Racionális kontrollfelhasználás, sokparaméteres kontrollok (Fizil Attila, Bio-Rad Magyarország Kft.) KALIBRÁTOR KONTROLL Navigare necesse est... Ha már muszáj, csináljuk értelmesen! 1. Határozzuk meg a
AMS Hereimplantátum Használati útmutató
 AMS Hereimplantátum Használati útmutató Magyar Leírás Az AMS hereimplantátum szilikon elasztomerből készült, a férfi herezacskóban levő here alakját utánzó formában. Az implantátum steril állapotban kerül
AMS Hereimplantátum Használati útmutató Magyar Leírás Az AMS hereimplantátum szilikon elasztomerből készült, a férfi herezacskóban levő here alakját utánzó formában. Az implantátum steril állapotban kerül
BIZTONSÁGI ADATLAP 2. ÖSSZETÉTEL/ÖSSZETEVŐKKEL KAPCSOLATOS INFORMÁCIÓ. Tömegszázalék % CAS (TSCA) szám
 X200, EX3001A-0101, 1/5 1. A TERMÉK ÉS A VÁLLALAT AZONOSÍTÁSA Termék neve: Xstamper Refill Ink CS-10N, CS-20N, CS-60N (fekete)(kék)(piros)(zöld)(barna)(narancssárga)(lila)(sárga)(rózsaszín) Általános
X200, EX3001A-0101, 1/5 1. A TERMÉK ÉS A VÁLLALAT AZONOSÍTÁSA Termék neve: Xstamper Refill Ink CS-10N, CS-20N, CS-60N (fekete)(kék)(piros)(zöld)(barna)(narancssárga)(lila)(sárga)(rózsaszín) Általános
: ERDAL SHOE CREAM BLACK 75ML SK1
 1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Azonosító szám : 60901 Az anyag/készítmény felhasználása : Ápoló szer Társaság : Erdal Ges.m.b.H. Neualmerstrasse
1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Azonosító szám : 60901 Az anyag/készítmény felhasználása : Ápoló szer Társaság : Erdal Ges.m.b.H. Neualmerstrasse
Tisztított limfociták preparálásához és izolálásához közvetlenül teljes vérből TERMÉKISMERTETŐ. In vitro diagnosztikai alkalmazásra PI-TT.
 Tisztított limfociták preparálásához és izolálásához közvetlenül teljes vérből TERMÉKISMERTETŐ In vitro diagnosztikai alkalmazásra PI-TT.610-HU-V6 Útmutató tájékoztatás Rendeltetés A T-Cell Xtend reagens
Tisztított limfociták preparálásához és izolálásához közvetlenül teljes vérből TERMÉKISMERTETŐ In vitro diagnosztikai alkalmazásra PI-TT.610-HU-V6 Útmutató tájékoztatás Rendeltetés A T-Cell Xtend reagens
Nemzeti Akkreditáló Testület. BŐVÍTETT RÉSZLETEZŐ OKIRAT (1) a NAT-1-1668/2012 nyilvántartási számú akkreditált státuszhoz
 Nemzeti Akkreditáló Testület BŐVÍTETT RÉSZLETEZŐ OKIRAT (1) a NAT-1-1668/2012 nyilvántartási számú akkreditált státuszhoz Az Országos Epidemiológiai Központ Virológiai főosztály (1097 Budapest, Albert
Nemzeti Akkreditáló Testület BŐVÍTETT RÉSZLETEZŐ OKIRAT (1) a NAT-1-1668/2012 nyilvántartási számú akkreditált státuszhoz Az Országos Epidemiológiai Központ Virológiai főosztály (1097 Budapest, Albert
Mátrix effektus a 25(OH)D-vitamint és a parathormont mérő módszerekben valamint. a 2013-as QuliCont eredményekből levonható tanulságok
 Mátrix effektus a 25(OH)D-vitamint és a parathormont mérő módszerekben valamint a 2013-as QuliCont eredményekből levonható tanulságok Toldy Erzsébet, Kányási Mária, Walentin Szilvia QuliCont Fórum 2015.
Mátrix effektus a 25(OH)D-vitamint és a parathormont mérő módszerekben valamint a 2013-as QuliCont eredményekből levonható tanulságok Toldy Erzsébet, Kányási Mária, Walentin Szilvia QuliCont Fórum 2015.
a NAT /2010 nyilvántartási számú akkreditált státuszhoz
 Nemzeti Akkreditáló Testület RÉSZLETEZÕ OKIRAT a NAT-1-1628/2010 nyilvántartási számú akkreditált státuszhoz A Mezõgazdasági Szakigazgatási Hivatal Központ Állategészségügyi Diagnosztikai Igazgatóság Kaposvári
Nemzeti Akkreditáló Testület RÉSZLETEZÕ OKIRAT a NAT-1-1628/2010 nyilvántartási számú akkreditált státuszhoz A Mezõgazdasági Szakigazgatási Hivatal Központ Állategészségügyi Diagnosztikai Igazgatóság Kaposvári
A Virológiai főosztály szolgáltatásainak jegyzéke
 Virológiai főosztály akkreditálási okiratának (NT-1-1473/2008) érvényessége: 2010. július 5. z újraakkreditálás NT-1-1668 eljárás nyilvántartási számon folyamatban van. Virológiai főosztály szolgáltatásainak
Virológiai főosztály akkreditálási okiratának (NT-1-1473/2008) érvényessége: 2010. július 5. z újraakkreditálás NT-1-1668 eljárás nyilvántartási számon folyamatban van. Virológiai főosztály szolgáltatásainak
17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására
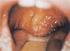 11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
11. 2016. nov 30. 17.2. ábra Az immunválasz kialakulása és lezajlása patogén hatására 17.3. ábra A sejtközötti térben és a sejten belül élő és szaporodó kórokozók ellen kialakuló védekezési mechanizmusok
BIZTONSÁGI ADATLAP. FRESSH CITROM ILLATÚ WC-gél 1. A KÉSZÍTMÉNY NEVE
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/4 BIZTONSÁGI ADATLAP FRESSH CITROM ILLATÚ WC-gél 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: WC-gél A készítmény megnevezése:
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/4 BIZTONSÁGI ADATLAP FRESSH CITROM ILLATÚ WC-gél 1. A KÉSZÍTMÉNY NEVE Az anyag vagy készítmény azonosítása: A készítmény típusa: WC-gél A készítmény megnevezése:
8806361JAA 2004/06 Magyar BBL Preparált, kémcsőben és palackban kiszerelt, gombák szelektív tenyésztésére szolgáló táptalaj
 8806361JAA 2004/06 Magyar BBL Preparált, kémcsőben és palackban kiszerelt, gombák szelektív tenyésztésére szolgáló táptalaj Sabouraud Dextrose Agar, Emmons, with Gentamicin A jelmagyarázat a használati
8806361JAA 2004/06 Magyar BBL Preparált, kémcsőben és palackban kiszerelt, gombák szelektív tenyésztésére szolgáló táptalaj Sabouraud Dextrose Agar, Emmons, with Gentamicin A jelmagyarázat a használati
A vizsgálat kivitelezése. A kit összetevői
 SeroMP IgG Enzimmel kapcsolt immunoszorbens assay (ELISA) a Mycoplasma pneumoniae ellenes specifikus IgG antitestek szemi-kvantitatív meghatározására humán szérumban. Használati utasítás Teszt kit 96 meghatározáshoz
SeroMP IgG Enzimmel kapcsolt immunoszorbens assay (ELISA) a Mycoplasma pneumoniae ellenes specifikus IgG antitestek szemi-kvantitatív meghatározására humán szérumban. Használati utasítás Teszt kit 96 meghatározáshoz
ACC# Biztonsági Adatlap Nyomtatva: DharmaFECT Transfection Reagent Átnézve: verzió
 1.SZAKASZ: A TERMÉK ÉS A VÁLLALAT AZONOSÍTÁSA A biztonsági adatlap neve: DharmaFECT Transfection Reagent Katalógus szám: T-2001-01, T-2001-02, T-2001-03, T-2001-04, T-2002-01, T-2002-02, T-2002-03, T-2002-04,
1.SZAKASZ: A TERMÉK ÉS A VÁLLALAT AZONOSÍTÁSA A biztonsági adatlap neve: DharmaFECT Transfection Reagent Katalógus szám: T-2001-01, T-2001-02, T-2001-03, T-2001-04, T-2002-01, T-2002-02, T-2002-03, T-2002-04,
Rubella-IgG-ELISA PKS medac. Magyar 136-PKS-VPU/010512
 RubellaIgGELISA PKS medac Magyar 0123 136PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
RubellaIgGELISA PKS medac Magyar 0123 136PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
QUANTA Lite TM ssdna 708525 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas
 QUANTA Lite TM ssdna 708525 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas Javasolt alkalmazás QUANTA Lite TM ssdna egy szemi-kvantitatív enzimmel kapcsolt immunoszorbens assay (ELISA) az
QUANTA Lite TM ssdna 708525 In Vitro diagnosztikai alkalmazásra CLIA Bonyolultság: magas Javasolt alkalmazás QUANTA Lite TM ssdna egy szemi-kvantitatív enzimmel kapcsolt immunoszorbens assay (ELISA) az
A minőségirányítási rendszer auditálása laboratóriumunkban. Nagy Erzsébet Budai Irgalmasrendi Kórház Központi Laboratórium
 A minőségirányítási rendszer auditálása laboratóriumunkban Nagy Erzsébet Budai Irgalmasrendi Kórház Központi Laboratórium Alkalmazott standardok MSZ EN ISO 9000:2001 (EN ISO 9000: 2000) Minőségirányítási
A minőségirányítási rendszer auditálása laboratóriumunkban Nagy Erzsébet Budai Irgalmasrendi Kórház Központi Laboratórium Alkalmazott standardok MSZ EN ISO 9000:2001 (EN ISO 9000: 2000) Minőségirányítási
Pulyka légzőszervi betegségek
 Pulyka A kórokozók Légzőszervi Gyakorlati helyzet Betegségek Alacsony patogenitású madárinfluenza XXIII. DERZSY NAPOK 2015. június 4-5. Zalakaros A jelenlegi megoldások Merial Avian Technical Services
Pulyka A kórokozók Légzőszervi Gyakorlati helyzet Betegségek Alacsony patogenitású madárinfluenza XXIII. DERZSY NAPOK 2015. június 4-5. Zalakaros A jelenlegi megoldások Merial Avian Technical Services
MYCOBACTERIUM GORDONAE CULTURE IDENTIFICATION TEST KIZÁRÓLAG EXPORTRA (biomérieux ref. 39005 / Gen-Probe Cat. No. 2850)
 FELHASZNÁLÁSI TERÜLET MYCOBACTERIUM GORDONAE CULTURE IDENTIFICATION TEST KIZÁRÓLAG EXPORTRA (biomérieux ref. 39005 / Gen-Probe Cat. No. 2850) Az ACCUPROBE MYCOBACTERIUM GORDONAE CULTURE IDENTIFICATION
FELHASZNÁLÁSI TERÜLET MYCOBACTERIUM GORDONAE CULTURE IDENTIFICATION TEST KIZÁRÓLAG EXPORTRA (biomérieux ref. 39005 / Gen-Probe Cat. No. 2850) Az ACCUPROBE MYCOBACTERIUM GORDONAE CULTURE IDENTIFICATION
QUANTA Lite dsdna SC ELISA 704650 In vitro diagnosztikai alkalmazásra CLIA komplexitás: Magas
 QUANTA Lite dsdna SC ELISA 704650 In vitro diagnosztikai alkalmazásra CLIA komplexitás: Magas Javasolt alkalmazás Ez az assay a dupla láncú dezoxiribonukleinsav (dsdna) ellen a humán szérumban megjelenő
QUANTA Lite dsdna SC ELISA 704650 In vitro diagnosztikai alkalmazásra CLIA komplexitás: Magas Javasolt alkalmazás Ez az assay a dupla láncú dezoxiribonukleinsav (dsdna) ellen a humán szérumban megjelenő
PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM. Humán plazma, kevert, vírus-inaktiválás céljából kezelt
 conditumque ad exstinguendum virum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1646 PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM Humán plazma, kevert, vírus-inaktiválás céljából kezelt DEFINÍCIÓ
conditumque ad exstinguendum virum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1646 PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM Humán plazma, kevert, vírus-inaktiválás céljából kezelt DEFINÍCIÓ
KEDVEZMÉNYES VIZSGÁLATI CSOMAGOK
 ár Élni jó csomag Páros csomag D-vitamin csomag Manager csomag Egészség 50+ csomag hölgyeknek Egészség 50+ csomag férfiaknak Vérkép automatával (kvalitatív vérképpel) (GGT), Alkalikus foszfatáz (ALP),
ár Élni jó csomag Páros csomag D-vitamin csomag Manager csomag Egészség 50+ csomag hölgyeknek Egészség 50+ csomag férfiaknak Vérkép automatával (kvalitatív vérképpel) (GGT), Alkalikus foszfatáz (ALP),
Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára. Nagy Melinda. MART VII. kongresszusa Sümeg,
 Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára Nagy Melinda MART VII. kongresszusa Sümeg, 215.5.8-9 Bevezetés Intézetünk egyik feladata a férfi infertilitás alapos kivizsgálása,
Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára Nagy Melinda MART VII. kongresszusa Sümeg, 215.5.8-9 Bevezetés Intézetünk egyik feladata a férfi infertilitás alapos kivizsgálása,
BÁBOLNA BIOENVIRONMENTAL CENTRE LTD. BUDAPEST BIZTONSÁGI ADATLAP BIOPREN 50 LML. szúnyoglárvairtó koncentrátum. Kiadás dátuma: 2013.05.22.
 ENVIRONMENTAL CENTRE LTD. BUDAPEST 1/6 BIZTONSÁGI ADATLAP BIOPREN 50 LML szúnyoglárvairtó koncentrátum Kiadás dátuma: 2013.05.22. Verzió: 1 1. SZAKASZ A keverék és a vállalkozás azonosítása 1.1 A keverék
ENVIRONMENTAL CENTRE LTD. BUDAPEST 1/6 BIZTONSÁGI ADATLAP BIOPREN 50 LML szúnyoglárvairtó koncentrátum Kiadás dátuma: 2013.05.22. Verzió: 1 1. SZAKASZ A keverék és a vállalkozás azonosítása 1.1 A keverék
H Hódmezővásárhely Garzó I. u. 3.
 H- 6800 Hódmezővásárhely Garzó I u 3 Dátum: 20080716 Oldal:1/5 Verzió: 2 1 Termék neve Kereskedelmi elnevezés: Gyártó és forgalmazó cég: Cím: Telefon: Fax: Veszély esetén hívható: WONDERCLEAN ZSÍRTALANÍTÓ
H- 6800 Hódmezővásárhely Garzó I u 3 Dátum: 20080716 Oldal:1/5 Verzió: 2 1 Termék neve Kereskedelmi elnevezés: Gyártó és forgalmazó cég: Cím: Telefon: Fax: Veszély esetén hívható: WONDERCLEAN ZSÍRTALANÍTÓ
PROTECT -B ROVARIRTÓ POROZÓ
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT -B ROVARIRTÓ POROZÓ 1. A KÉSZÍTMÉNY NEVE Az anyag és készítmény azonosítása: A készítmény típusa: inszekticid tartalmú háztartási
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/5 BIZTONSÁGI ADATLAP PROTECT -B ROVARIRTÓ POROZÓ 1. A KÉSZÍTMÉNY NEVE Az anyag és készítmény azonosítása: A készítmény típusa: inszekticid tartalmú háztartási
BIZTONSÁGI ADATLAP 1. SZAKASZ: A TERMÉKRE ÉS A VÁLLALATRA VONATKOZÓ INFORMÁCIÓK
 BIZTONSÁGI ADATLAP A Zymo Research minden vásárló vagy ügyfél számára javasolja a biztonsági adatlap alapos/körültekintő áttanulmányozását a termékkel kapcsolatos veszélyek megismerése érdekében. Az olvasó
BIZTONSÁGI ADATLAP A Zymo Research minden vásárló vagy ügyfél számára javasolja a biztonsági adatlap alapos/körültekintő áttanulmányozását a termékkel kapcsolatos veszélyek megismerése érdekében. Az olvasó
PLATELIA VZV IgG 72684 48 TESZT
 PLATELIA VZV IgG 72684 48 TESZT VARICELLA ZOSTER ELLENI IgG ANTITESTEK MINİSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL Ref. 91078/BRD Hungarian 1/9 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2.
PLATELIA VZV IgG 72684 48 TESZT VARICELLA ZOSTER ELLENI IgG ANTITESTEK MINİSÉGI MEGHATÁROZÁSA HUMÁN SZÉRUMBÓL IMMUNOENZIMATIKUS MÓDSZERREL Ref. 91078/BRD Hungarian 1/9 TARTALOMJEGYZÉK 1. FELHASZNÁLÁS 2.
(EGT-vonatkozású szöveg) Első közzététel a HL-ben Ez az első közzététel. Ez az első közzététel
 2009.12.2. Az Unió Hivatalos Lapja C 293/69 A Bizottság közleménye az in vitro diagnosztikai orvostechnikai eszközökről szóló, 1998. október 27-i 98/79/EK európai parlamenti és tanácsi irányelv végrehajtása
2009.12.2. Az Unió Hivatalos Lapja C 293/69 A Bizottság közleménye az in vitro diagnosztikai orvostechnikai eszközökről szóló, 1998. október 27-i 98/79/EK európai parlamenti és tanácsi irányelv végrehajtása
Kiállítás dátuma: 10/11/2005 Nyomtatás dátuma: 2009.02.18.
 BIZTONSÁGI ADATLAP Oldal 1 / 5 1. Az anyag / készítmény megjelölése és a cégjelzés 1.1 A termék kereskedelmi megnevezése: Adhesor carbofine 1.2 Termék alkalmazhatósága Alábélelő amalgam és kompozittömésekhez,
BIZTONSÁGI ADATLAP Oldal 1 / 5 1. Az anyag / készítmény megjelölése és a cégjelzés 1.1 A termék kereskedelmi megnevezése: Adhesor carbofine 1.2 Termék alkalmazhatósága Alábélelő amalgam és kompozittömésekhez,
BIZTONSÁGI ADATLAP CIF POWER CREAM KONYHAI TISZTITÓSZER
 Készítés dátuma: 2013.09.06. BIZTONSÁGI ADATLAP Cif Power Cream Konyhai 1.VEGYI ANYAG NEVE BIZTONSÁGI ADATLAP CIF POWER CREAM KONYHAI TISZTITÓSZER A Készitmény Neve A Készitmény Felhasználása Gyártó Forgalmazó
Készítés dátuma: 2013.09.06. BIZTONSÁGI ADATLAP Cif Power Cream Konyhai 1.VEGYI ANYAG NEVE BIZTONSÁGI ADATLAP CIF POWER CREAM KONYHAI TISZTITÓSZER A Készitmény Neve A Készitmény Felhasználása Gyártó Forgalmazó
: FROSCH SODA KITCHEN CLEANER 500ML SO1
 1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Azonosító szám : 64286 Az anyag/készítmény felhasználása : Tisztítószer Társaság : Erdal Ges.m.b.H. Neualmerstrasse
1. AZ ANYAG/KÉSZÍTMÉNY ÉS A TÁRSASÁG/VÁLLALKOZÁS AZONOSÍTÁSA Termék tájékoztató Márkanév : Azonosító szám : 64286 Az anyag/készítmény felhasználása : Tisztítószer Társaság : Erdal Ges.m.b.H. Neualmerstrasse
SZENNYVÍZKEZELÉS NAGYHATÉKONYSÁGÚ OXIDÁCIÓS ELJÁRÁSSAL
 SZENNYVÍZKEZELÉS NAGYHATÉKONYSÁGÚ OXIDÁCIÓS ELJÁRÁSSAL Kander Dávid Környezettudomány MSc Témavezető: Dr. Barkács Katalin Konzulens: Gombos Erzsébet Tartalom Ferrát tulajdonságainak bemutatása Ferrát optimális
SZENNYVÍZKEZELÉS NAGYHATÉKONYSÁGÚ OXIDÁCIÓS ELJÁRÁSSAL Kander Dávid Környezettudomány MSc Témavezető: Dr. Barkács Katalin Konzulens: Gombos Erzsébet Tartalom Ferrát tulajdonságainak bemutatása Ferrát optimális
Olvassa el a címkét! Amit feltétlenül tudnia kell a mosó- és tisztítószerek biztonságos otthoni használatáról
 Olvassa el a címkét! Amit feltétlenül tudnia kell a mosó- és tisztítószerek biztonságos otthoni használatáról Hamarosan új figyelmeztető címkék jelennek meg a háztartási tisztítószereken. Az eddig megszokott
Olvassa el a címkét! Amit feltétlenül tudnia kell a mosó- és tisztítószerek biztonságos otthoni használatáról Hamarosan új figyelmeztető címkék jelennek meg a háztartási tisztítószereken. Az eddig megszokott
Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban
 GLP Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban 31/1999. (VIII.6.) EÜM-FVM együttes rendelet az emberi felhasználásra kerülő gyógyszerekre és a növényvédő szerekre vonatkozó
GLP Minőségbiztosítás gyógyszer és növényvédő szer vizsgáló laboratóriumokban 31/1999. (VIII.6.) EÜM-FVM együttes rendelet az emberi felhasználásra kerülő gyógyszerekre és a növényvédő szerekre vonatkozó
HU-Budapest: Vérvizsgálati reagensek 2012/S 114-188857. Ajánlati/részvételi felhívás. Árubeszerzés
 1/16 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:188857-2012:text:hu:html HU-Budapest: Vérvizsgálati reagensek 2012/S 114-188857 Ajánlati/részvételi felhívás Árubeszerzés
1/16 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:188857-2012:text:hu:html HU-Budapest: Vérvizsgálati reagensek 2012/S 114-188857 Ajánlati/részvételi felhívás Árubeszerzés
Akkreditáció. Avagy nem minden arany, ami fénylik Tallósy Judit
 Akkreditáció Avagy nem minden arany, ami fénylik Tallósy Judit 2018.01.18. A nagy pecsét és ami mögötte van PCDA ciklus PDCA-ciklus egy ismétlődő, négylépéses menedzsment módszer, amelyet a termékek és
Akkreditáció Avagy nem minden arany, ami fénylik Tallósy Judit 2018.01.18. A nagy pecsét és ami mögötte van PCDA ciklus PDCA-ciklus egy ismétlődő, négylépéses menedzsment módszer, amelyet a termékek és
CMV-IgA-ELA Test PKS medac. Magyar 112-PKS-VPU/010708
 CMVIgAELA Test PKS medac Magyar 0123 112PKSVPU/010708 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
CMVIgAELA Test PKS medac Magyar 0123 112PKSVPU/010708 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
2 HASZNÁLATI ÚTMUTATÓ
 PLATELIA ASPERGILLUS Ag 1 микроплака 96 62794 A Platelia Aspergillus Ag immuno-enzimatikus szendvics mikrolemez vizsgálat az aspergillus galaktomannan antigén kimutatására szérumban és bal folyadékban
PLATELIA ASPERGILLUS Ag 1 микроплака 96 62794 A Platelia Aspergillus Ag immuno-enzimatikus szendvics mikrolemez vizsgálat az aspergillus galaktomannan antigén kimutatására szérumban és bal folyadékban
MIÉRT MÉRJÜK MEG AZ ELŐKELTETŐGÉP HŐMÉRSÉKLET-EGYENLŐTLENSÉGÉT?
 Az előkeltetőgépek hőmérséklet-egyenlőtlenségének Az előkeltetőgépek hőmérsékletegyenlőtlenségének MIÉRT MÉRJÜK MEG AZ HŐMÉRSÉKLET-EGYENLŐTLENSÉGÉT? Az előkeltetőgépeken belüli és azok közötti hőmérséklet-egyenlőtlenségek
Az előkeltetőgépek hőmérséklet-egyenlőtlenségének Az előkeltetőgépek hőmérsékletegyenlőtlenségének MIÉRT MÉRJÜK MEG AZ HŐMÉRSÉKLET-EGYENLŐTLENSÉGÉT? Az előkeltetőgépeken belüli és azok közötti hőmérséklet-egyenlőtlenségek
A FOREST LABORATORIES, INC. ÉS A RICHTER GEDEON NYRT
 A FOREST LABORATORIES, INC. ÉS A RICHTER GEDEON NYRT. KÖZLEMÉNYE A CARIPRAZINE SKIZOFRÉNIÁBAN SZENVEDŐ BETEGEK KÖRÉBEN VÉGZETT FÁZIS IIB KLINIKAI VIZSGÁLATÁNAK POZITÍV EREDMÉNYEIRŐL NEW YORK, 2009. október
A FOREST LABORATORIES, INC. ÉS A RICHTER GEDEON NYRT. KÖZLEMÉNYE A CARIPRAZINE SKIZOFRÉNIÁBAN SZENVEDŐ BETEGEK KÖRÉBEN VÉGZETT FÁZIS IIB KLINIKAI VIZSGÁLATÁNAK POZITÍV EREDMÉNYEIRŐL NEW YORK, 2009. október
szerepe a gasztrointesztinális
 A calprotectin és egyéb biomarkerek szerepe a gasztrointesztinális gyulladásos betegségek differenciál diagnosztikájában 1 Halmainé Kiss Ilona, 2 Rutka Mariann, 1 Földesi Imre Szegedi Tudományegyetem 1
A calprotectin és egyéb biomarkerek szerepe a gasztrointesztinális gyulladásos betegségek differenciál diagnosztikájában 1 Halmainé Kiss Ilona, 2 Rutka Mariann, 1 Földesi Imre Szegedi Tudományegyetem 1
REACH: R- és S-mondatok. A veszélyes anyagok veszélyeire/kockázataira utaló R-mondatok:
 REACH: R- és S-mondatok A veszélyes anyagok veszélyeire/kockázataira utaló R-mondatok: R 1 Száraz állapotban robbanásveszélyes R 2 Ütés, súrlódás, tűz vagy más gyújtóforrás robbanást R 3 Ütés, súrlódás,
REACH: R- és S-mondatok A veszélyes anyagok veszélyeire/kockázataira utaló R-mondatok: R 1 Száraz állapotban robbanásveszélyes R 2 Ütés, súrlódás, tűz vagy más gyújtóforrás robbanást R 3 Ütés, súrlódás,
Dr. Nemes Nagy Zsuzsa Szakképzés Karl Landsteiner Karl Landsteiner:
 Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
Az AB0 vércsoport rendszer Dr. Nemes Nagy Zsuzsa Szakképzés 2011 Az AB0 rendszer felfedezése 1901. Karl Landsteiner Landsteiner szabály 1901 Karl Landsteiner: Munkatársai vérmintáit vizsgálva fedezte fel
Brodifakum 0.005% 56073-10-0 259-980-5 T +, N 27/28-48/24/25-50/53 Bitrex 0.001 % 3734-33-6 223-095-2 Xn 22
 BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/4 BIZTONSÁGI ADATLAP KILRAT PLUS RÁGCSÁLÓIRTÓ PÉP Az anyag vagy készítmény azonosítása: A készítmény típusa: felhasználásra kész rágcsálóirtó csalétek
BÁBOLNA KÖRNYEZETBIOLÓGIAI KÖZPONT KFT. BUDAPEST 1/4 BIZTONSÁGI ADATLAP KILRAT PLUS RÁGCSÁLÓIRTÓ PÉP Az anyag vagy készítmény azonosítása: A készítmény típusa: felhasználásra kész rágcsálóirtó csalétek
A 453/2010 EK, a 1907/2006 EK (REACH) és a 1272/2008 EK rendeletek (CLP- GHS) szerint. 1. Anyagmegnevezés, gyártó és forgalmazó megnevezése
 Biztonsági adatlap A 453/2010 EK, a 1907/2006 EK (REACH) és a 1272/2008 EK rendeletek (CLP- GHS) szerint. A készítés dátuma: 2017. június 23. 1. Anyagmegnevezés, gyártó és forgalmazó megnevezése Termék
Biztonsági adatlap A 453/2010 EK, a 1907/2006 EK (REACH) és a 1272/2008 EK rendeletek (CLP- GHS) szerint. A készítés dátuma: 2017. június 23. 1. Anyagmegnevezés, gyártó és forgalmazó megnevezése Termék
