Transzdifferenciáció és regeneratív medicina
|
|
|
- Hanna Deák
- 10 évvel ezelőtt
- Látták:
Átírás
1 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Transzdifferenciáció és regeneratív medicina Dr. Balogh Péter Dr. Engelmann Péter
2
3 Transzdifferenciáció és regeneratív medicina Dr. Balogh Péter Dr. Engelmann Péter Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosítószám:TÁMOP /1/A Pécsi Tudományegyetem Pécs, 2011 Dr. Balogh Péter, Dr. Engelmann Péter, 2011 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
4 Kézirat lezárva: november 11. A kiadásért felel a: Pécsi Tudományegyetem Felelős szerkesztő: Dr. Balogh Péter, Dr. Engelmann Péter, Bognár Rita Műszaki szerkesztő: Bencze Zsolt, Csöngei Veronika és Czulák Szilvia Lektorálta: Dr. Miskei György Terjedelem: 90 oldal
5 Tartalom Ábrajegyzék... 5 I Az őssejtek és csoportjaik meghatározása, fennmaradásuk és homeosztázisuk... 7 II Regeneráció állatmodellekben III Epigenetikus faktorok a transzdifferenciációban IV Genomiális és más sejt nyomonkövetéses eljárások, újra-programozás V Őssejtek és transzdifferenciálódás a vérképzésben VI Izom regeneráció VII Máj regeneráció VIII Hasnyálmirigy differenciáció és regeneráció IX Transzdifferenciáció a központi idegrendszeri regenerációban X Kardiovaszkuláris regeneráció XI Vese regeneráció XII Daganat őssejtek XIII Az őssejt-kutatás és terápia etikai háttere Ajánlott irodalom Azonosítószám: TÁMOP /1/A
6
7 Ábrajegyzék I-1. ábra: ES sejtek forrásai... 8 I-2. ábra: ES sejtek membrán markerei... 9 I-3. ábra: Reprogramozás: Pluripotenciál-indukció ips sejtekben I-4. ábra: Érési sorrend és pluripotenciál II-1. ábra: Regenerációs hasonlóságok II-2. ábra: Regenerációs bevésődés II-3. ábra: Idegi őssejtek és differenciálódási kapacítás III-1. ábra: Az őssejt genom epigenetikus szabályozása III-2. ábra: DNS metiláció az őssejtekben III-3. ábra: mirns és őssejt differenciálódás IV-1. ábra: Őssejt eredet és újraprogramozás IV-2. ábra: Sejt nyomonkövetés az őssejtbiológiában IV-3. ábra: A sejtmegújhodás molekuláris mechanizmusai V-1. ábra: Az embrionális vérképzés kialakulása V-2. ábra: A korai hemopoetikus elköteleződés transzkripcionális szabályozása V-3. ábra: A mieloid differenciálódás transzkripcionális szabályozása V-4. ábra: Transcriptional regulation of lymphoid differentiation V-5. ábra: Állandó és aktivált vérképzés VI-1. ábra: A vázizom szerkezete és regenerációja VI-2. ábra: Az izom-regenerációban alkalmazható nem-sc sejtek VI-3. ábra: Az izom-gyógyulás kinetikája VII-1. ábra: A máj és hasnyálmirigy differenciálódásának fejlődéstani kapcsolatai VII-2. ábra: A hepatoblasztok fejlődésének transzkripcionális szabályozása Azonosítószám: TÁMOP /1/A
8 Transzdifferenciáció és regeneratív medicina VII-3. ábra: A májlebeny szerkezete VII-4. ábra: A máj regeneráció főbb szakaszai VIII-1. ábra: A pankreász embrionális fejlődése VIII-2. ábra: β sejt és az autoimmun diabétesz folyamata VIII-3. ábra: Embrionális őssejtekből történő inzulin-termelő β sejt differenciálódás IX-1. ábra: Transzkripciós faktorok és neurális őssejtek IX-2. ábra: A gerincvelői sérülés folyamata és az őssejtek direk manipulációja a sérülés után IX-3. ábra: Retinális progenitor sejtek és plaszticitásuk X-1. ábra: Szívizom-regenerációra alkalmazott sejt-források X-2. ábra: ips közvetítette újraprogramozás szívizom-regenerációban XI-1. ábra: A vese felépítése és progenitor sejtjei XI-2. ábra: Őssejtek által medial folyamatok a vese regenerációjában XII-1. ábra: Daganat és daganat-őssejt teória XII-2. ábra: CSC fejlődés XII-3. ábra: CSC és az őssejt-niche megváltozása XII-4. ábra: AML fészek jellegzetességek XII-5. ábra: Kombinált tumor-terápia CSC és a niche kezelése A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
9 I Az őssejtek és csoportjaik meghatározása, fennmaradásuk és homeosztázisuk Az őssejteket (SC) egyrészt eredetük (embrionális/esc vagy felnőtt SC) vagy differenciálódási képességük és spektrumuk (spontán pluripotens, indukált pluripotens vagy elkötelezett, pl. hemopoetikus, mezenhimális SC, stb). A petesejt megtermékenyülését követően a zigóta morula formációvá hasad, mely az implantáció előtti (pre-implantációs) embrióban a korai blasztociszta stádiumó ébrénnyé fejlődik, amely külső sejt-réteget (a Cdx2 transzkripciós faktor által irányított trofoektoderma) és belső sejt-csoportot tartalmaz, az utóbbi differenciálódását az Oct3/4 transzkripciós faktorok irányítják. A belső sejtcsoportot (ICM, inner cell mass) alkotó sejtek a Nanog transzkripciós faktor hatására (az Oct4 és Sox2 hatásával egyidejűleg) elősegítik a késői blasztociszta stádium kialakulását, melyben két sejtréteg különül el. Az egyik sejtréteget alkotó epiblaszt sejtekből fejlődik ki mindhárom csíralemez (ektoderma, mezoderma és endoderma) a beágyazódás után (posz-implantációs) ébrényben zajló gasztruláció során, míg a másik lemezt alkotó hipoblaszt sejtekből az extraembrionális membránok alalkulnak ki. Ezen embrionális összetevők közül az ICM és epiblaszt sejteket használják ESC forrásként. Azonosítószám: TÁMOP /1/A
10 Transzdifferenciáció és regeneratív medicina Morula Korai blasztociszta Késői blasztociszta Korai cilinder stádium Oct3/4 Inner cell mass (ICM) Nanog Epiblaszt Primitív ektoderma Csírasejt-vonal Testi sejt irányok Ektoderma Mezoderma Endoderma Blasztocisztaüreg Gata6 Primitív endoderma Zsigeri endoderma Fali endoderma Proamnion üreg Cdx2 Trofektoderma Extraembrionális ektoderma I-1. ábra: ES sejtek forrásai Megfelelő körülmények között az ES sejtek hosszú időn keresztül fenntartják differenciálatlan állapotukat, ennek megfelelően azokból mindhárom csíralemez és az ivarsejtek is kialakulhatnak. Ennek megfelelően az ES sejtekben történt manipulálás az ivarsejtek közvetítésével transzgenikus egerekben átörökíthető. Ugyanakkor egyéb, hasonló differenciálódási spektrummal rendelkező sejtek nagyfokban rosszindulatú daganatokat (teratokarcinoma) képezhetnek, melyben mindhárom csíralemez származékai megtalálhatók. Az ES sejtek azonosítására és fejlődéstani vizsgálatára számos sejtfelszíni marker meghatározása fontos adatot szolgáltathat. Ezek közé tartozik az oligoszacharid szerkezetű stádium-specifikus embrionális antigének több tagja (SSEA3-6), valalmint a komplex proteoglikán szerkezetű tumor rejekciós antigének (TRA). További őssejtantigén a CD34 glikoprotein, mint a hemopoetikus őssejtek és endotél-sejtek által is kifejezett marker, valamint az intracelluláris alkalikus foszfatáz-pozitivitás. 8 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
11 Az őssejtek és csoportjaik meghatározása, fennmaradásuk és homeosztázisuk Lewis X PSA-NCAM Glc Gal CD34 Man Tra 1-60 (KSPG) NG2 és473hd (CSPG) GlcNAc GalNAc SSEA-3 SSEA-4 GlcA IdoA Xyl Fuc Sia I-2. ábra: ES sejtek membrán markerei Az őssejtek számát, funkcionális aktivitását és differenciálódási állapotát külső és belső stimulusok és szignálok határozzák meg. Ezeknek a jelzéseknek együttese dönti el a sejtek ön-megújítását (ezáltal a pluripotenciál fenntartását) és az elköteleződést (ezáltal a differenciálódási jellemzők kialakulását). Ebben a folyamatban az elkötelezetlen utódsejtben a differenciációs szignálokkal szembeni ellenállás küszöbnek kell némiképp emelkednie, másrészről az elkötelezett utódsejtben az induktív szignálokkal szembeni érzékenységnek kell fokozódnia. A külső környezetet az őssejtfészek (niche) alkotja, amely az egyes szervek között jelentékeny különbségeket mutat. Általában az őssejt-fészket az extracelluláris matrix komponensek, immobilizált növekedési/differenciálódási faktorok és fészek-képző sejtek alkotják, melyek az érett sejtekkel együtt hozzák létre a szövet jellegzetességeinek megfelelő fészek részleteket (csontvelő, agy, bőr, petefészek, stb). A belső szabályozás alapját az egymással meglehetősen komplex kapcsolatrendszerben álló transzkripciós faktor-hálózatok alakítják ki, melyek hatásai Azonosítószám: TÁMOP /1/A
12 Transzdifferenciáció és regeneratív medicina egymás befolyásolása (antagonizálás vagy szinergia) révén érvényesülnek. A legfontosabb SC-szabályzó transzkripciós faktorok közé tartoznak az Oct4, Sox2, Nanog és Stat3 factorok, melyekkel szemben hat a Cdx2 transzkripciós faktor. Hatásaik számos metabolikus és szabályzó útvonalon kertesztül érvényesülnek, egyebek között a Wnt szignalizáció, epigenetikus módosítás, telomer-szabályozás, mrns lebomlás és interferencia valamint sejt-ciklus kontrol részvételével. Az ips sejtek felhasználásán alapuló kísérletes modellekben lehetőség nyílik az egyes transzkripciós faktorok közötti kölcsönhatások részletesebb vizsgálatára, melyek további génexpressziós hatásokon vagy epigenetikus változtatásokon keresztül fejtik ki hatásukat, melyek maguknak a transzkripciós faktoroknak a közvetlen hatásait is modulálhatják. Oct3/4 Klf4 Sox2 Transzkripciós faktorok Célgének c-myc Epigenetikai módosítók I-3. ábra: Reprogramozás: Pluripotenciál-indukció ips sejtekben Az őssejt-szerű differenciálódási potenciálnak már kiérett sejtekben való kialakíthatósága az érett sejtek pluripotenciájáról és transzdifferenciálódásáról való korábbi elképzeléseink gyökeres átértékeléséhez vezetett. Eszerint a pluripotenciál fenntartásához a differenciációt kiváltó szignálokkal szembeni ellenállás-növekedésre 10 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
13 Az őssejtek és csoportjaik meghatározása, fennmaradásuk és homeosztázisuk van szükség, míg ezen differenciációs stimulusok iránti érzékenység fokozatosan alakul ki, mely a pluripotenciával szembeni ellenállást fokozza. Ugyanakkor ez a fokozott ellenállás viszonylagos, pluripotenciál-indukáló transzkripciós faktorok kifejeződésének felerősödése egy megemelt szinten állíthatja helyre a differenciációs szignálokkal szembeni rezisztenciát és a pluripotenciál-indukcióval szembeni érzékenységet. I-4. ábra: Érési sorrend és pluripotenciál Azonosítószám: TÁMOP /1/A
14
15 II Regeneráció állatmodellekben Számos élőlény képes arra, hogy a sérült vagy autotomia által elvesztett testrészeit pótolja. A fiziológiás regeneráció magában foglal olyan szezonális és hormonális ciklusokat amilyen például a szarvasok agancsváltása illetve az epitél sejtek és vérsejtek cserélődése. A szöveti regenerálódás definiálható tulajdonképpen úgy, hogy a sérült szövetek helyreállítása a regenerációs blasztéma létrehozása nélkül történik illetve az epimorfikus regeneráció alatt egy őssejtekből kialakuló blasztéma állitja helyre a sérült vagy hiányzó szöveteket. Hipertrofiának vagy szöveti túltengésnek nevezik azt a fajta regenerációt, ami akkor alakulhat ki, amikor egy páros szerv (vese vagy tüdő) egyik tagjának elvesztése során a megmaradt tag kompenzálja (szöveti növekedés során) a sérült szerv mükődését. A morfallaxis folyamat során a súlyosan sérült szövet újraszerveződése, kicserélődése zajlik le a tulajdonképpeni sérült szövettől távolabb. Jól ismert tény, hogy a gerinctelen állatok igen nagy mértékű regenerációra képesek. A hidrák, laposférgek egy súlyos sérülés után képesek lehetnek akár egész testüket regenerálni. Amíg a gyűrűsférgek komoly regenerációra képesek, addig bizonyos rovarok (pl. legyek) ezt a képességüket csak a lárvakorban tudják kifejteni. Ezzel szemben más rovarok kifejlett korukban is megőrízték ezt a tulajdonságukat. A szervek regenerációs képessége igen változatos a gerinces fajok között. A végtagok regenerációja például az emlősökben csak az ujjhegyek helyreállítására szorítkozik, míg a kétéltűek képesek a teljes végtag regenerációjára a proximális és a distális tengely irányában. Ez a végtag regenerációs folyamat számos lépésre osztható. A rovarokkal és a kétéltűekkel folytatott végtag regenerációs kísérletek bizonyitékokat szolgáltattak a végtag tengelyi pozició információjának fontosságára. A tipikus epimorfikus végtag regeneráció során mind a kétéltűekben és a rovarokban a Azonosítószám: TÁMOP /1/A
16 Transzdifferenciáció és regeneratív medicina végtagfüggelék csonki régiója hozza létre a regenerációs blasztémát és megnyúlik a PD tengely írányában. Egy ilyen regenerációs folyamat során lehetőség van arra, hogy meghatározzuk a szekvenciális értékeket a PD tengely hosszában. A PD tengely menti normál nem-szomszédos pozíciók értékeit demonstrálni lehet transzplantációs kísérletekkel. Amikor a proximális és disztális értékek szembekerülnek egymással, akkor a PD tengely közbülső régiójában egy deléció történik. Ez a regenerációs válasz mind a rovarok mind pedig a gerincesek végtag regenerációjában megfigyelhető. A beiktató válaszban a poziciónális értékekbe egy minimális sorrend ékelődik be (legrövidebb beékelődési szabály) és a szomszédos poziciós értékek folytonossága megmarad. Ha a PD tengely mentén a szembesülés a közbülső régió duplikációjával jön létre, akkor a beékelődő válasz nem játszódik le a gerincesek végtagjain. Ez a folyamat azonban lezajlik a rovarlábak regenerációja során, így egy hosszabb végtag képződik. PD deléció PD duplikáció Kétéltűek Transzplantáció Beékelődés Transzplantáció Nincs beékelődés Rovarok Transzplantáció 5 Beékelődés Transzplantáció Beékelődés II-1. ábra: Regenerációs hasonlóságok 14 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
17 Regeneráció állatmodellekben Bizonyos gének újboli expressziója feltétlenül szükséges a mintázatformáláshoz a végtag regenerációban. A körülmények azonban nem mindig azonosak, mivel az újrarendeződésre csak a végtag sérült részéban van szükség. A farkos kétéltűek (szalamandrák) képesek arra, hogy a végtag amputáció után a hiányzó disztális részt a PD tengely bármelyik poziciójában újonnan létrehozzák. Feltehetően, ez csak úgy lehetséges, hogy a csonk területén maradt sejtek emlékeznek a pozicionális információra a végtag mindhárom tengelye mentén. Ez a memorizált pozicionális információ lehetővé teszi a blasztéma sejtek számára, hogy csak az elvesztett részt regenerálják. Disztálisabb poziciójú régiók regenerálódása egy újonnan képződő folyamat révén jön létre. Amputáció Génexpresszió Memorizált Újonnan képződött On On On Aktiváció Off Inaktiváció Nincs expresszió M On Off Off M Off Off M Off A11 On Off A11 On Off A11 Off A13 On A13 On A13 On II-2. ábra: Regenerációs bevésődés A regenerációban résztvevő sejtek eredete kérdéses. Lehetséges, hogy a regeneráció a meglévő, helyi sejtek transzdifferenciójával, átalakulásával történik (pl. fibroblasztok segítségével). Az is elképzelhető, hogy a még nem differenciálódott Azonosítószám: TÁMOP /1/A
18 Transzdifferenciáció és regeneratív medicina sejtek, vagy más kifejezéssel élve, felnőtt őssejtek már jelen vannak, melyek a megfelelő jelet megkapva aktiválodnak és képesek számos különböző szöveti sejttipussá átalakulni. Jó példa lehet erre a folyamatra a központi idegrendszer őssejtjei. A pluripotens őssejtekből történő in vitro neurális differenciálódás tulajdonképpen utánozza a neurális őssejtek differenciálódási kapacitásának időszakos változásait. A pluripotens őssejtek (mind az embrionális és indukált pluripotens őssejtek) képesek átvenni a neurális sejtsorsot ugyanolyan körülmények között (neurális differenciálódásra elkötelezett embrionális testecskéből kiindulva). Számos, egymást követő passzázs után elsődleges és másodlagos neurális gömböcskék jönnek létre. Az elsődleges neurális gömböcskék túlnyomórészt korai neuronokká alakulnak át, míg a másodlagosak neuronokká, asztrocitákká és oligodendrocitákká alakulnak, követve a neurális őssejtek differenciálódási kapacitásának időbeni lefutását. Blasztociszta invitro Neurogenezis Gliogenezis Noggin Low-RA FGF-2 FGF-2 ips sejtek ES sejtek Embrioid testecske Passzázs (6 nap) Primér Másodlagos neuroszféra neuroszféra Differenciáció Differenciáció Testi sejtek Neuron Neuron Asztrocita Oligodendrocita invivo Neurogenezis Gliogenezis Blasztociszta Embrió Újszülött Felnőtt Korai neurogenezis Projektáló neuron Cholinerg neuron Dopaminerg neuron Motor neuron Késői neurogenezis Interneuron GABAerg neuron II-3. ábra: Idegi őssejtek és differenciálódási kapacítás 16 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
19 III Epigenetikus faktorok a transzdifferenciációban Az epigenetika a kromoszóma régiók nem szekvencia alapú strukturális változásait jelenti, mely alatt a külső behatásokra adott génexpressziós válaszok módosulását értjük. Az epigenetikai módosítás főbb típusai közé tartozik a DNS metiláció, a hiszton módosítás, kromatin újrarendeződés és a nem-kódoló RNS-szekvenciák. A genomi DNS szekvenciával az un. genetikai kóddal manapság már egyenértékűek a szabályzó információkat hordozó hiszton módosítások, az un. hiszton kódok. A hisztonok több mint nyolc különböző módositási mechanizmusnak lehetnek célpontjai. Ezek a kovalens módosítások kitüntetett szerepet játszanak a kromatin kondenzáció, replikáció, DNSjavítás és a transzkripció szabályozásának folyamatában. Ezek közül a metiláció és az acetiláció a leggyakrabban tanulmányozott hisztonmodifikációs mechanizmus. A hiszton acetiláció igen gyakran az aktívan átírodó genomi régióval asszociált, továbbá a modifikáció mértéke korrelál az átíródás mértékével. A hiszton metiláció különböző kihatással lehet a génátírodásra, attól függően, hogy melyik régió változik meg a folyamat során. A különböző hisztonmódosítások közül fontosságban kitűnik a hiszton 3-as fehérje 4. és 27. lizinjének a metilációja. Ezeket a módosításokat a trithorax (TrxG) és polycomb (PcG) transzkripciós molekula komplexek végzik. A módosítások kulcsszerepet játszanak a fejlődési mintázatképzésben és a leszármazási vonalakra specifikus gének bekapcsolásában. A 4. lizin metilációja pozitívan szabályozza a génexpressziót azzal, hogy a nukleoszóma átalakító enzimkomplex számára egy kapcsolódási pontot képez. A lizin 27 metilációja negatívan szabályozza a génexpressziót, mivel a kompakt kromatin állomány léttrejöttét segíti elő. Az előbbiekhez hasonlóan a H3K36me3 módosítás jellemző az átíródó génrégiókra, míg a Azonosítószám: TÁMOP /1/A
20 Transzdifferenciáció és regeneratív medicina H3K9me3 módosítás az inaktiv genomi szakaszokat jellemzi. Különösen fontos a H3K4me3 módosítás az átírodó gének promotere szempontjából, és a H3K36me3 módositás, mely egy indikátora a transzkripciós elongációnak. Ezek a hiszton módositások különböző referenciául szolgálhatnak a genom-szintű transzkripciós egységek meghatározásában. A kromatin szerveződésre és a transzkripció szabályozására ható hiszton modifikációs mechanizmusok még részleteiben nem teljesen tisztázottak. Igen vonzó elképzelés az, hogy az epigenetikus faktorok (módosító enzimek és átalakító faktorok) tulajdonképpen kipányvázzák a kromatint, hogy létrejöhessenek további cis és trans kapcsolódások. Ezen interakciók feltehetőleg a DNS, és egészében véve, a kromatin szerkezeti változását okozzák. A módosítások újabb fehérje komplexekkel való kapcsolatot indítanak be, melyek a konformációs változást okoznak a kromatin szerkezetében. A kapcsolodások megváltoztatják a kromatin fizikai tulajdonságait és befolyásolják a kromatin magasabbrendű szerveződését. 18 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
21 Epigenetikus faktorok a transzdifferenciációban DNS replikáció DNS javítás DNS metiláció Kromatin újraprogramozás Nem-kódoló RNS-ek Hiszton modifikáció Kromatin csomag H3 H2A H4 H2B Transzkripciós szabályozás H3 H4 H2B Metiláció Acetiláció Foszforiláció Ubiquitináció III-1. ábra: Az őssejt genom epigenetikus szabályozása Emlős sejtekben mind a DNS metiláció, mind a hiszton módosítás szerepet játszik a kromatin csendesítésben. A DNS metilációt és a hiszton módosítást egymástól független folyamatnak képzelték el. Jelenlegi tanulmányok arra utalnak, hogy a hiszton acetiláció és a DNS demetiláció kombinált hatása indukálja a neuronális őssejtek (NSC) transzdifferenciációját hematopoetikus sejtekké. Embrionális őssejtekben a teljes nukleáris struktúra dekondenzált állapotban van jelen, kondenzáció csak a differenciáció során jelentkezik. A hiszton módosítás jellegzetes változásait mutatták ki az őssejtek differenciálódása és az emlősök embrionális fejlődése során. A szimmetrikus DNS metilációs mintázat kialakulását, passzív módon meg lehet akadályozni a kettőződés során a Dnmt1 enzim sztérikus gátlásával. Ez úgy történhet, hogy az újraprogramozási faktorok kapcsolodnak be sztérikusan a kőtőhelyekre, vagy indirekt úton gátoljuk a Dnmt1 aktivitását. Folyamatos sejtosztódás során a DNS Azonosítószám: TÁMOP /1/A
22 Transzdifferenciáció és regeneratív medicina hemimetiláltsága is kialakulhat, mivel fokozatosan elveszti a metilációt. Másik lehetőség, hogy egy demetiláló enzim segítségével aktív úton távolítjuk el a cél DNS-ről a metilált szakaszokat. Passzív demetiláció Transzkripcionális aktiváció Transzkripcionális gátlás Klf4 Oct4 Sox2 Transzkripcionális aktiváció DNMT1 Aktív demetiláció Transzkripcionális gátlás Transzkripcionális aktiváció Klf4 Sox2 Oct4 Klf4 Sox2 Oct4 Demetiláz Szimmetrikusan metilált DNS Hemimetilált DNS III-2. ábra: DNS metiláció az őssejtekben Jelenleg egy új, integrált hálózati elképzelés ismert a kromatin újraszerveződésében szerepet játszó komponensek, transzkripciós faktorok, és a kis nem kódoló RNS-k közötti kölcsönhatások modellezesére. E három mechanizmus összehangolt koreográfiája alapján történik az őssejtek önmegújítása és differenciálódása más sejttípusokká. Az emlős sejtek számos kis, nem-kódoló RNS-t tartalmaznak. Ezek a következők: kis nukleoláris RNS-k (snorna), mikrorns-k (mirna), kis interferáló RNS-k (sirnas) és a kis kettős-láncú RNS-k. Ezek a molekulák szabályozzák a génátíródást számos szerveződési szinten, beleértve a kromatin szerveződést is. A molekulák jellegzetes időbeni- és sejt-specifikus 20 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
23 Epigenetikus faktorok a transzdifferenciációban expressziós mintázatot mutatnak a különböző szövetekben. Számos mirns például igen jellegzetesen expresszálódik az embrionális őssejtek differenciálódása során, illetve az embriogenezis, a neuronális differenciálódás és a hemopoetikus sejtvonal elköteleződések során. Néhány mirns-ről (ESC mirns, Myc-indukálta mirns-k, a mir-92b, és a mir- 520 csoport) kimutatták, hogy pozitívan szabályozzák az embrionális őssejtek önmegújító képességét és pluripotenciálját. Ezek közül egyelőre csak az ESC mirns-k szerepét vizsgálták a sejtek újraprogramozásában. Emellett, jónéhány szövet specifikus mirns-ről, mint például a let-7, mir-134, mir-470, mir-296, és mir-145 ismert, hogy befolyásolják az embrionális őssejtek önmegújítását és pluripotenciálját. Nem ismert még azonban részleteiben, hogy ezek a molekulák hogyan befolyásolják a sejtek újraprogramozását. A let-7 molekuláról már kimutatták, hogy gátlása elősegíti a sejtek újraprogramozását. Egy másik mirns, a mir-125 gátolja a Lin28 expresszióját, így pozitívan befolyásolja az újraprogramozás folyamatát. További érdekes információ, hogy a mirns számos, igen fontos jelátviteli útvonalat (pl. TGF-beta szignalizáció) és epigenetikus folyamatot (pl. DNS metiláció) befolyásolhat, ezzel is elősegítve az újraprogramozást. A Dlk1 Dio3 géncsoport által kódolt mirns-k szintén fontos szerepet játszhatnak ebben a folyamatban, mivel ezen gének aktivációja alapvető az indukált pluripotens őssejtek (ips) kialakításában. Azonosítószám: TÁMOP /1/A
24 Transzdifferenciáció és regeneratív medicina ES/iPS sejtek Myc indukált mirns-ek mir-520 klaszter mir-92b ESCC mirns-ek + + TGF-béta jelátvitel mir-470 Önmegújhodás és pluripotencia Aktív Dlk1-Dio3 gén klaszter CpG Oct4 mir-296 mir-134 mir-145 inhibitor? mir p21 + Újraprogramozás Sox2, Oct4, Klf4, és c-myc vagy Sox2, Oct4, Nanog, és Lin28 által + let-7 inhibitor? mir-24-1, mir-23b, mir-21 gátlók mir-125 inhibitor Inaktív Dlk1-Dio3 génklaszter +? HDAC inhibitor Dlk1-Dio3 génklaszter által kódolt mirns +? Géncsendesített Dnmt/Dnmt inhibitorok Dnmt 3a és 3b mir-29b p53 mir-470 inhibitor mir-296 inhibitor? mir-134 inhibitor? ESCC mirns? + mir-92b?? mir-125 mir-520 klaszter? let-7 Testi sejtek Myc indukált mirns mir-24-1 mir-23b mir-21 mcpg mir-200 mir-141 mir-429 mir klaszter? Oct4 III-3. ábra: mirns és őssejt differenciálódás 22 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
25 IV Genomiális és más sejt nyomonkövetéses eljárások, újra-programozás Az embrionális őssejtek a korai embrió belső sejttömegéből (ICM) származnak. A belső sejttömeg sejtjeihez hasonlóan az embrionális őssejtek is nagy fejlődési potenciállal un. pluripotenciállal rendelkeznek és képesek egy szervezet minden sejttípusává átalakulni, kivéve az extraembrionális szöveteket. Emellett az embrionális őssejtek képesek önmegújításra és korlátlanul osztódnak, in vitro körülmények között. Az embrionális őssejtek igéretes lehetőségeket nyújthatnak a klinikai regeneratív terápiában, ha megértjük a molekuláris mechanizmusokat melyek szabályozzák a szaporodásukat és pluripotenciáljukat. Az embrionális őssejtek pluripotenciálját három fő transzkripciós faktor, az Oct4, Sox2 és Nanog által kialakitott szabályozási hálózat biztosítja. Ezek a központi transzkripciós faktorok egymással összehangolva szabályozzák más gének müködését, így fenntartva az önmegújhodást és a pluripotenciált. Másrészről az epigenetikus módosítások, mint a DNS metiláció és hiszton acetiláció, a transzkripciós faktorok mellett szinergista módon befolyásolhatják az őssejt gének expresszióját. Együttesen a két szabályozó mechanizmus kontrollálja az őssejtek tulajdonságait (önmegújítás és pluripotencia). Ezzel szemben a pluripotencia elvesztése feltételezi a transzkripcionális program átváltását a differenciálódás irányába. Azonosítószám: TÁMOP /1/A
26 Transzdifferenciáció és regeneratív medicina Zigóta Blasztociszta Epiblaszt (beágyazódás után) Késői embrió/ korai foetus Felnőtt Elköteleződés Elköteleződés Bőr Belső sejttömeg Epiblaszt Primordiális ivarsejtek Központi idegrendszer Csontvelő Totipotens Embrionális őssejtek Pluripotens Epiblaszt őssejtek Pluripotens Embrionális őssejtek Pluripotens Felnőtt őssejtek Multipotens vagy unipotens Egyéb Indukált pluripotens őssejtek Pluripotens + Oct4, Sox2, Klf4, Myc IV-1. ábra: Őssejt eredet és újraprogramozás Jelenleg már számos olyan kísérleti megközelítés áll a rendelkezésünkre, ami alkalmas az őssejtek jelölésére és követésére, mint pl. a BrdU inkorporáció, fluoreszcens festés, GFP, mágneses, és izotóp jelölési technikák. Továbbá számos követési eljárás alkalmazható akár transzplantátumokban a sejtek azonosítására. Az őssejtek követésére legelöször a BrdU inkorporációt és a különböző fluoreszcens vitális festékeket (CFSE, DiI, PKH26) használták könnyű kezelhetőségük miatt. Bár a fluoreszcens festékek intenzitása az idő előrehaladtával egyre csökken, ezért nem alkalmasak hosszab idejű követési alkalmazásokban. Jelenleg az egyik leggyakrabban használt eljárás sejtkövetésre a GFP riporter fehérje detektálása, stabil expressziója, magas specifitása és az in vivo azonosítás lehetősége miatt is. Habár azt is tudni kell, hogy a túlzottan erős GFP mennyiség toxikus lehet a sejtekre. Emellett egy másik rekombináns marker, a LacZ riporter gén is használatos. További lehetőség az Y kromoszómát markerként használni FISH detektálással. 24 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
27 Genomiális és más sejt nyomonkövetéses eljárások, újra-programozás Az MRI és az izotóp követési technikák mostanában kerültek alkalmazásra a beültetett őssejtek in vivo nem-invaziv nyomon követésére. Bár az MRI jelölési technika okozhat ál-pozítiv eredményt is és az izotóp technika használata igen limitált az elérhető kis számú őssejtmarker miatt. Az idő-kinetikai- és két-foton mikroszkópok kifejlesztésével újabb lehetőségek nyiltak az őssejtekkel kapcsolatos in vivo képalkotás területén. Az idő-kinetikai mikroszkópia igen hasznos eszköz lehet az élő őssejtek viselkedésének vizsgálatában. A különböző időpontokban és szöveti környezetben fotózva az őssejteket, majd az eredményt statisztikailag feldolgozva meg lehet határozni a sejtek dinamikus viselkedési, vándorlási mintázatát. A különböző őssejttípusok funckiójához tartozó eredmények, értékelések is feldolgozhatóak ezzel a módszerrel. A sejtmigráció, alakváltozás, proliferációs ráta mellett további pontok lényegesek az őssejtsorsok szempontjából: a sejthalál (1); az öregedés (2); szimmetrikus sejtosztódás (valamilyen stresszre adott válaszként) (3); aszimmetrikus sejtosztódás ahol egy őssejt és egy már részben differenciált sejt jön létre (megfelelő körülmények között ez a domináns forma) (4); és a szimmetrikus depletáló osztódás (mindkét leánysejt elveszti az őssejt tulajdonságot, amely a felnőtt őssejtek növekedésére jellemző in vitro); (5). Azonosítószám: TÁMOP /1/A
28 Transzdifferenciáció és regeneratív medicina z x t 1 y t 2 Automatizált kép és statisztikai analízis t n Migráció Proliferáció Sejt-forma változás Sejtsors analízis IV-2. ábra: Sejt nyomonkövetés az őssejtbiológiában A sejtek akkor írhatóak le pluripotensként, ha képesek létrehozni egy szervezet minden egyes sejttípusát. Ha emellett képesek extraembrionális szöveteket is létrehozni akkor totipotensként definiálhatóak. A multipotens őssejtek képesek egy adott szövet összes differenciált sejttípusát létrehozni. Egyes esetekben a szövetek egy differenciált sejtvonalból eredeztethetőek és a fenntartó őssejtek un. unipotensek. A posztnatális spermatogoniumok unipotensek in vivo, de pluripotensnek tekinthetőek mesterséges körülmények között. 26 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
29 Genomiális és más sejt nyomonkövetéses eljárások, újra-programozás Lif PI3K Grb2 Jak Akt MAPK STAT3 Tbx3 Klf4 Sejt-ciklus szabályozás Nanog Sox2 b-myb S G2 Oct3/4 c-myc G1 M Cdx2 Gata4 A differenciálódás megelőzése IV-3. ábra: A sejtmegújhodás molekuláris mechanizmusai A már differenciálódott sejteket 4 különböző stratégiával lehet újraprogramozni embrionális állapotba. Ezek a következő módszerek: szomatikus sejtmag transzfer (SCNT), sejtfúzió, a sejtkultúra indukálta újraprogramozás, és az indukált pluripotens őssejtek (ipsc) létrehozása. Az embrionális ivarsejtek, spermatógoniumok sejtkultúra indukálta újraprogramozása bár fontos eredmény, de nem a megfelelő példa a radikális újraprogramozásra. A sejtfúziós megközelítés nem eredményezett pluripotens diploid sejteket, bár ez a jővőben lehetséges lehet. Ezzel ellentétben mind a szomatikus sejtmag transzfer és az indukált pluripotens őssejtek létrehozása teljesítette az elvárásokat. Az SCNT, sejtfúzió és ipsc módszerek segítségével meg lehetett figyelni az újraprogramozás kinetikáját és mechanizmusát. Mind a SCNT és az ipsc létrehozása az utóbbi kémiai ágensek hiányában nem hatékony módszer. Egér fibroblasztokat felhasználva 3.4% volt az SCNT esetében a legjobb hatékonyság, míg ez 1 3% volt ipsc létrehozással. Az ipsc sejtvonalak létrehozása igen hosszú időt vesz igénybe, így Azonosítószám: TÁMOP /1/A
30 Transzdifferenciáció és regeneratív medicina az idő előrehaladtával nem kivánatos változások is előfordulhatnak a sejtekkel. Más módon megfogalmazva az SCNT, sejtfúzió, és ipsc általi újraprogramozás egymástól igen eltérő folyamatokat jelent. Az SCNT esetében az újraprogramozás viszonylag rövid időt vesz igénybe. Egér SCNT blasztocisztákban az Oct4 faktor expressziója már órán belül detektálható volt, habár számos embrionális gén aktiválása kiszámithatatlan, továbbá a gének expressziója embriónként nagyon különbözhet. Gyors Oct4 és SSEA4 expresszió az egér ESC szomatikus sejtek 13 16%-ban megfigyelhető volt. Mindkét folyamat során egy szignifikáns, gyors sejtmagduzzadás jelentkezik, ez valószinüleg a kromatin dekondenzációnak tudható be, ami jelzi az újraprogramozás beinditását. Ezen folyamattal ellentétben az ipsc létrehozás során, igen kevés sejtben, csak mintegy 2 hét után detektálható az Oct4 expresszió. Ezek az adatok is jelzik azt, hogy a folyamatok természetére jellemző valamennyire a rendszertelenség. Az újraprogramozás a sejtfúzióban és SCNT-ben jóval gyorsabban beindul. Egyik esetben sem ismert az, hogy a sejtek újraprogramozása feltételezi-e a DNS replikációt és a sejtosztódást. Kétéltűekben az embrionális vagy pluripotencia asszociált gének aktivációja nem igényli a gazdasejt DNS kettőzödését és osztódását. Hasonlóan ehhez a megfigyeléshez, a pluripotencia-asszociált gének expressziója már detektálható a heterokaryon szomatikus részében még mielőtt a tényleges magfúzió megtörténne. Ezzel szemben az ipsc sejtek mindig osztódó testi sejtekből hozhatóak létre, bár az nem ismert, hogy a DNS replikáció és sejtosztódás szükséges része-e ennek a folyamatnak. Összegezve, a sejtfúzió és SCNT folyamata a pluripotencia gének gyors aktivációját okozza sejtosztódás hiányában is. Ez annak tudható be, hogy az oocita vagy az ESC citoplazmája és/vagy nukleoplazmája hatékonyabb faktorokat nyújt egy gyors újraprogramozáshoz, mint a meghatározott transzkripciós faktorok. Ugyanakkor az ipsc újraprogramozási kísérletekhez feltétlenül szükséges a DNS replikáció és a 28 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
31 Genomiális és más sejt nyomonkövetéses eljárások, újra-programozás sejtosztódás. A kísérleti körülmények különbözőségéből adodóan, nehéz meghatározni, hogy ezek az újraprogramozás hatékonyságbeli eltérések nem az ipsc sejtek változatos eredetéből adódnak-e. Azonosítószám: TÁMOP /1/A
32
33 V Őssejtek és transzdifferenciálódás a vérképzésben Az őssejtekből történő vérképződés három szempont miatt jelentős a regeneratív medicina tudományterületén belül. Az egyik a vérképzésnek önmagának mint biológiai folyamatnak a létrejötte, mely a képzett sejt-termékek spektrumának a változékonyságát mutatja attól függően, hogy milyen eltérő helyeken és időpontokban képződtek (szikzacskó, embrionális máj vagy felnőtt csontvelő). A második szempont fontossága, hogy jelenleg a vérképzés helyreállítása leukémiás vagy egyéb vérképzőszervi megbetegedés esetén a viszonylag kevés, ugyanakkor széles körben elterjedten alkalmazott regeneratív klinikai terápiás eljárások egyike. A hemopoetikus regeneráció harmadik jelentőségét az adja, hogy hemopoetikus őssejtek alkalmazása felmerült nemhemopoetikus szövetek degeneratív, traumás vagy nekrotikus károsodás utáni helyreállítására, így például szívizom-infarktus vagy idegszöveti károsodások esetében. Az egyedfejlődés során elsőként fellépő hemopoetikus sejt-képző aktivitás a szikzacskó falában elhelyezkedő vér-szigeteknél figyelhető meg, melyek extraembrionális szövetek. Ezekben a területekben párhuzamosan zajlik a hemopoetikus (vörösvértest-képzés) és az endotél-irányú differenciálódás, mely a közös hemangioblaszt előalak jelenlétére utal. A két sejt-vonal közötti kapcsolódást támasztja alá a későbbi időszakban az embrión belül az aorta hasi szegmentumában, az aortogonád-mezonefrosz (AGM) területében megfigyelhető közös fizikai kapcsolat az érendotél és a fejlődő vérsejtek között. Ezt követően a vérkeringés kialakulásával párhuzamosan a vérképzés áthelyeződik az embrionális májba és kisebb mértékben az embionális lépbe. Vérsejtek a hemogén endotél sejtekből is képződhetnek, és az időszaktól függően, amikor a vérsejt-képzés kialakul, megkülönböztetünk pro-definitív, Azonosítószám: 31 TÁMOP /1/A
34 Transzdifferenciáció és regeneratív medicina mezo-definitív, meta-definitív és végül felnőtt definitív vérképzést. A szikzacskó típusú vérképzést primitív vérképzésnek nevezzük, mely így megelőzi a definitív vérképzés bármely formáját. A terhesség vége felé a fejlődő csontvelőt oszteoklaszt-szerű sejtek kolonizálják, melyek az oszteoblasztokkal, stromális fibroblasztokkal és extracelluláris matrix komponensekkel együtt létrehozzák a hemopoetikus őssejtek (HSC) számára a megfelelő befogadó-képességgel rendelkező csontvelői őssejt-fészket. Allantois Chorion Szikzacskó Szikzacskó vérszigetek Placenta Köldök artéria Placenta Vitellin artéria Köldök artéria Vitellin artéria Máj AGM Embrió Allantois psp AGM Szikzacskó Máj E7.5 E8.25 E9.0 E10.5 Hemangioblaszt Hemogén Endotélium Primitív Pro-definitív Mezo-definitív Meta-definitív Mieloid Limfoid-Mieloid CFU-k Újszülött HSC Felnőtt-definitív HSC V-1. ábra: Az embrionális vérképzés kialakulása Ezeken a területeken a HSC sejtek sejtfelszíni markereik alapján azonosíthatók, melyek egérben a Sca-1, c-kit, CD45, valamint számos egyéb, hemopoetikusendotheliális marker, pl. CD31, CD34 és VE-kadherin glikoproteinek. A vérképzés elindulásához a HSC sejtek Runx, Scl és GATA-2 transzkripciós faktorokat expresszálnak. Emellett a belső programozás mellett az embrión belüli topográfiai viszonyoknak is nagy jelentősége van a vérképzés aktiválódásában. Az aortán belüli has-irányú szegmentális preferenciát (ventralizáció) elősegítő 32 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
35 Őssejtek és transzdifferenciálódás a vérképzésben morfogenetikai faktorok (VEGF, bfgf, TGFβ és BMP4) szintén elősegítik a vérképzést, míg az ezzel ellentétes, ektodermális/dorzalizációs irányt fokozó faktorok (EGF és TGFα) gátolják a vérsejt-képzést. A vérképzés elindulását követően számos döntési lépés szükséges a HSC sejtek sejtvonal-elköteleződéséhez. Az egyik korai ellenőrzési/döntési pont a pluripotenciál megőrzése, amit valószínúleg több transzkripciós faktor egyidejű hatása szabályoz, elsősorban a Notch-1, GATA-2, HoxB4 és Ikaros transzkripciós faktorok. Emellett a sejt-ciklus gátló p21 is fontos szerepet tölt be a HSC sejtek nagy részének nyugalmi állapotban való fennmaradásában. A következő szakaszban a főbb sejtvonal-irányok kialakításában a PU1 és GATA- 1 aránya alapján az erithroid/megakariocita irányt a GATA-1 dominancia, a mieloid irányt a PU1 túlsúly irányítja, míg a köztes GATA-1/PU1 expresszió az Ikaros transzkripciós faktor kifejeződésével együtt a HSC sejtek limfoid irányú stabilizálódását segíti elő. Azonosítószám: TÁMOP /1/A
36 Transzdifferenciáció és regeneratív medicina Hemangioblaszt Hemogén endotél SCL AML-1 GATA-2 Lmo p21 HSC Notch1 Ikaros HoxB4 GATA-2 PU.1/GATA-1 PU.1/GATA-3/Ikaros Bcl-2 CMP CLP Apoptózis V-2. ábra: A korai hemopoetikus elköteleződés transzkripcionális szabályozása A mieloid irány preferenciáját követően a PU1 és GATA-1 expresszió aránya és kifejeződésének stabilitása segíti elő az eritroid/megakariocita (GATA-1/s) vagy mielomonocita (PU1) irányú elköteleződést. A PU1 mellett a C/EBPα vagy C/EBPβ transzkripciós faktorok expressziója tovább irányítja a közös mieloid prekurzorokat a granulocita irányok felé. 34 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
37 Őssejtek és transzdifferenciálódás a vérképzésben ICSBP, PU.1 Monocita PU.1 GMP C/EBPα Neutrofil HSC PU.1 & GATA-1 CMP C/EBPβ, GATA-1 Eozinofil GATA-1/FOG EMP GATA-1 Vörösvértest GATA-1, 2 Megakaryocita V-3. ábra: A mieloid differenciálódás transzkripcionális szabályozása A köztes PU1/GATA-1 kifejeződés és az Ikaros transzkripciós faktor expressziója a közös limfoid-mieloid prekurzor (CMLP) limfoid irányú fejlődését támogatja. A folyamatban jelentős változást eredményez az interleukin 7 (IL-7) receptorának sejtfelszíni megjelenése, amihez a mieloid preferenciájó citokin-receptorok (GM-CSF és G-CSF) valamint az őssejt-faktort felismerő c-kit receptor kifejeződésének csökkenése társul. A közös limfoid progenitor (CLP) a Notch1 receptor-közvetítette módon T-sejt irányban, vagy az E2A transzkripciós faktor expresszió-fokozódásán keresztül B-sejt irányban kötelezheti el magát. Ezen a ponton az Id2 transzkripciós faktor eltérítheti a differenciálódást NK-irányba a limfoid csoporton belül. A CLP-stádiumban még flexibilis limfoid előalakok a timuszba lépve az ott nagy mennyiségben jelen lévő Notch1 ligandumok (Jagged, stb.) hatására T-sejtvonal irányban köteleződhetnek el. Érdekes módon az E2A expresszió-fokozódás ellenére bizonyos korai B-sejt előalakok továbbra is flexibilisek maradhatnak, akár a makrofág-irányú reverzió mértékéig. Azonosítószám: TÁMOP /1/A
38 Transzdifferenciáció és regeneratív medicina Pro-T HSC PU.1 IL-7R GM-CSFR Notch1 CLP PU.1 Monocita Pu.1, E2A Prepro-B Pax5? EBF D-JH Pax5 V-D-JH Korai pro-b Késői pro-b B-sejt V-4. ábra: Transcriptional regulation of lymphoid differentiation A folyamatos és meghatározott sejt-arány fenntartása mellett zajló vérképzést külső stimulusok (pl. hipoxia, gyulladás), melyekhez a szervezetben mediátorok (eritropoietin, TNFα, stb.) felszabadulása társulhat, jelentékeny mértékben megváltoztathatják a limfoid/mieloid sejt-képződés arányát, elsősorban a csontvelőn belüli nagyobb mértékű G-CSF and GM-CSF termelődésen keresztül. Anemia Hypoxia EPO HSC Endotél Fibroblaszt SCF, FLT-3I, TPO G-CSF, GM-CSF HSC Oszteoblaszt HSC HSC Érszakasz Makrofág EPO IL-1α TNFα HSC Fibroblaszt G-CSF, GM-CSF HSC Oszteoblaszt TGF-β Endotél TPO HSC HSC Bakteriális fertőzés Gyulladás V-5. ábra: Állandó és aktivált vérképzés 36 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
39 Őssejtek és transzdifferenciálódás a vérképzésben A vérképzés fenntartása és helyreállítása mellett a HSC sejtek nem-hemopoetikus szövet-rekonstrukciós képességét is intenzíven vizsgálták. Így pl. károsodott izom, máj és neurális sejtek regenerációját remélték a HSC bejuttatásától. A regenerációt elősegítő hatások viszonylag szerények voltak, és a hatás mechanizmusa is meglehetősen vitatott. A lehetséges összetevők közé tartozik a HSC sejtek közvetlen transz-differenciálódása szöveti őssejtté, vagy olyan sejtté, mely elősegíti a degeneratív szövetek eltávolítását, esetleg a fokozott ér-képződést helyi angiogenetikus folyamatokon keresztül, mely a vérellátás révén javítja a szöveti oxigenizációt és tápanyag-ellátást. Azonosítószám: TÁMOP /1/A
40
41 VI Izom regeneráció A vázizom alkotja a szervezet legnagyobb tömegű mezodermális/kötőszöveti összetevőit, rendkívül változatos eredettel és fejlődési jellegzetességekkel. Így pl. a külső szemizmok a nem szegmentált koponya-mezodermából, a nyelv-izmok a koponyaalapi szomitákból származnak, a hipaxiális végtag-izmok és az epaxiális törzsizmok a szomiták dermatomiotom részletéből differenciálódnak. A mezoderma miogén programozása során a Pax3 jelentős expresszió-fokozódása a MyoD transzkripciós faktor direkt vagy Myf5 és Myf6 faktorokon keresztüli indirekt expresszióerősödése figyelhető meg. A mikrokörnyezeti szabályzók közül a velőcső és az oldallemez mezoderma által termelt BMP4 gátolja, míg a notochord általi Sonic hedgehog faktor (Shh) és a testfelszíni ektodermális eredetű Wnt faktorok elősegítik a miogén differenciálódást. A vázizom regenerációja vagy a vázizom alkalmazása renegerációs beavatkozásra három fő felhasználási csoportba osztható: (1) Vázizom-regeneráció traumát követően vagy a vázizmot érintő örökletes megbetegedés esetén (leggyakrabban Duchenne izomdisztrófia során). A Duchenneizomdisztrófia (DMD) a legnagyobb ismert emlős gén, a disztrofin gén X- kromoszómához kapcsoltan öröklődő mutációja, ennek prevalenciája 1:3 500 fiú újszülöttek között. A betegség korai gyermekkorban manifesztálódik, jellemző a végtag-, rekesz- és szívizomzat progresszív sorvadása, mely légzési-keringési elégtelenséghez vezet, mely következtében a halál általában a fiatal felnőttkorban, a 20- as évek legelején jelentkezik. (2) Szívizom-infarktust követően a szívizomzat regenerációja (3) Záróizom-regeneráció hólyag-inkontinencia esetén a vázizom őssejtek (szatellita sejtek CS) felhasználásával. Azonosítószám: TÁMOP /1/A
42 Transzdifferenciáció és regeneratív medicina A vázizom szerkezeti egysége az izomrost, mely az endomizum vagy alaphártya által közrefogott izomsejt-hálózat. Az izomrostok sejtmaggal és mitokondriumokkal rendelkező fúzionált sejtekből és kontraktilis miofilamentumot tartalmazó miofibrillumokból állnak. Az alaphártya és a miofibrillumok sejtmembránja között találhatók a mononukleáris SC sejtek, melyeket először Alexander Mauro észlelt ben elektronmikroszkópos vizsgálatai során. Aktiváció Nyugvó SC Pax7 + Izomszál Hemopoietikus sejtek Visszatérés nyugalmi állapotba Asszimmetrikus osztódás Aktivált SC Pax7 + Myf5 + MyoD + Lamina basalis Pericita Szimmetrikus osztódás Mioblaszt Pax7 - Myf5 + MyoD + Szatellita sejt (SC) Izomsejt-mag Endotélsejt Intersticiálissejt Miocita MyoD + Fúzió és differenciáció Izomrost Arteriola és kapillárisok VI-1. ábra: A vázizom szerkezete és regenerációja A szöveti elhelyezkedésüktől és fejlődéstani jellegzetességeitől függően különböző izom-területek SC sejtjei különböző sejtfelszíni jellegzetességeket és mrns expressziós profilt mutatnak, így régió-függő eltérések lehetnek a CD34. Sca-1, M- cadherin, CD56, a HGF/Scatter factort felismerő c-met receptor mint sejtfelszíni molekulák, vagy a Pax3 és Pax7 miogén transzkripciós faktorok kifejeződésében. Az SC sejtek mellett más sejt-csoportok izom-regenerációra való felhasználásának lehetősége is felmerült. Így pl. hemopoetikus őssejtek, endotél alcsoportok, 40 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
43 Izom regeneráció mezenhimális őssejtek illetve az izomszövetben előforduló egyéb, nem-sc-típusú pluripotens sejtek alkalmazhatóságát vizsgálták. Regenerációs eljárásokra vagy allogén prekurzor/őssejtek, vagy génmódosított autológ őssejtek felhasználásával próbálkoztak. Érés Differenciálódás Proliferáció Aktiváció Sérülés utáni napok VI-2. ábra: Az izom-regenerációban alkalmazható nem-sc sejtek Az SC sejtek változatos módokon vehetnek részt az izom-regenerációban, így transzdifferenciálódással, más sejtek differenciálódásának elősegítésével, vagy a maradék izomrostokkal való sejtfúzió révén. Modellkísérletekben kardiotoxinnal létrehozott miogén károsodást követően elsőként szolubilis faktorok (IGF, FGF, HGF/scatter factor) aktiválják a SC sejteket, melyek a károsodás utáni 2 3 nap körül osztódnak. Ezt követően centrális elhelyezkedésű magot tartalmazó, viszonylag kis átmérőjű izomrostok jönnek létre a sérülést követő nap alatt, melyek a miociták fúziója révén érett és regenerálódott izomrosttá alakulnak. Ezek nagyobb átmérővel rendelkeznek, a sejtmag a sejtmembrán közelébe a rost perifériás részébe kerül. Azonosítószám: TÁMOP /1/A
44 Transzdifferenciáció és regeneratív medicina Erek Periciták Mioendotelsejtek EPCs MSCs Bőr vagy egyéb szövet Újraprogramozás Vér Hemopoetikus őssejtek Side population CD133+ őssejtek ips sejtek Vázizom Jellemzők SCsés alcsoportjaik MDSCs CD133 + őssejtek Mezenhimális differenciáció Csontvelő Hemopoetikus őssejtek Side population Mezenhimálisőssejtek Egyéb források Zsírszövet eredetű őssejtek MyoD-konvertált sejtek Autológ transzplantáció (genetikai korrekció után) Tenyésztés Elköteleződés (ha szükséges) Allogén transzplantáció VI-3. ábra: Az izom-gyógyulás kinetikája Az allogén sejtek felhasználása immunszuppressziós kezelést tesz szükségessé, melyek mellékhatásaként mioblaszt apoptózis léphet fel. A DMD kezelésére korrigált disztrofin-gént kifejező miogén őssejtek szintén immunválaszt válthatnak ki mutált génnel született egyedekben. A speciális elhelyezkedés és a szövet kiterjedtsége miatt a lehetséges őssejtek bejuttatása is nehézségeket okozhat, elsősorban a miogén sejtek rövid vándorlási képessége miatt, ami mintegy 100 injekció elvégzését igényelné 1 cm 2 felületen. A vázizom SC sejtek mint szívizomzat regenerációjára alkalmas őssejt-jelöltek felhasználása mérsékelt balkamra funkció-javulást és teljesítmény-fokozódást eredményezett, ugyanakkor megnövekedett a ritmuszavarok gyakorisága, mely antiarritmiás szerekkel kezelhető volt. A vázizom SC sejtek fibroblasztokkal vagy más támasz-sejtekkel való együttes alkalmazása záróizom-elégtelenség korrekciójára ugyan eredményezett némi javulást, de ez csak jelentős késedelemmel volt észlelhető. 42 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
45 VII Máj regeneráció Végstádiumú (gyulladás, veleszületett vagy szerzett metabolikus rendellenességek miatt kialakuló) krónikus májelégtelenségben illetve súlyos akut májelégtelenségben szenvedő betegek számára a jelenleg egyedül alkalmazható terápiás eljárást a májtranszplantáció jelenti. A korlátozott donorszám miatt sejt-transzplantáción alapuló regeneratív eljárásokra van szükség, melyek helyreállíthatják a máj-sejttömeget és funkciókat. Bár a túlélő hepatociták jelentékeny mértékben regenerációképesek és helyreállíthatják a májat, az arra alkalmas őssejtek felhasználásával további, hatékonyabb eljárások kialakítása lehetséges. A máj-regeneráció elősegítésére többféle őssejt-típust vizsgáltak, így mezodermális progenitorokat, különböző differenciáltságú máj-progenitorokat valamint hemopoetiikus progenitorokat. Számottevő előrelépés történt az embrionális, újszülöttkori valamint felnőtt májban kimutatható őssejt-funkciójú sejtek tanulmányozása során. Különböző olyan sejtvonalakat sikerült előállítani (pl. embrionális őssejtekből [ES], embrionális máj és őssejt-tulajdonságokat mutató ovális sejtekből [OS]), melyek hepatocitákká és/vagy epekapilláris sejtekké differenciálódhatnak in vitro és in vivo. Ugyanakkor mindezen sejtek a jelenleg alkalmazott eljárásokban túlnyomórészt csak igen korlátozott repopulációra voltak képesek, a patkány embrionális máj ős/progenitorsejtek kivételépvel, melyek jelentékeny mértékű és tartós májszöveti korrekcióra voltak képesek. A máj a ventrális endodermális epitéliumból származik, melyből hetapociták, érkapilláris sejtek és a hasnyálmirigy bizonyos részletei származnak, míg a hasnyálmirigy további részei a dorzális endodermából fejlődnek. Azonosítószám: TÁMOP /1/A
46 Transzdifferenciáció és regeneratív medicina Ovális sejt progenitor? Hasnyálmirigy progenitor(ok) Máj ovális sejt Hasnyálmirigy ovális sejt Epevezeték Májsejt Endokrin sejt Hasnyálmirigysejt Hasnyálmirigykivezető sejt VII-1. ábra: A máj és hasnyálmirigy differenciálódásának fejlődéstani kapcsolatai A FoxA és GATA transzkripciós faktor család különböző tagjai a FGF és BMP szolúbilis faktorokkal együtt elősegítik az endoderma hepatoblaszt irányú elköteleződését, amely a máj-sejtek és az epekapilláris sejtek közös előalakja. A hatások következtében fokozottan kifejeződő transzkripciós faktorok valamint Notch és Wnt mediátorok irányítják a későbbi hepatocita vagy epekapilláris-sejtek differenciálódását, amelyekből további érési folyamatok során alakulnak ki a máj-kötegek és az epevezetékek. 44 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
47 Máj regeneráció Hepatoblaszt HGF C/EBPα HNF-6 Tbx3 HNF-1β HNF-1α LRH-1 Májsejt Központi TF hálózat HNF-4α HNF-1β HNF-6 Foxa2 ECM HNF-4α Albumin Notch2? Jagged Wnt BMP+FGF FoxM1B ECM Epevezeték-sejt Hex HNF-6/OC-2 HNF-1β C/EBPα Parenchyma Sox9 TGFβ Periportális Májköteg-érés Epevezeték-sejt érés VII-2. ábra: A hepatoblasztok fejlődésének transzkripcionális szabályozása Ez az érési folyamat összekapcsolódik a hepatoblasztok sejt-vándorlási és az érpálya megfelelő kialakulásának eseményeivel, melyeket a Prox1, Tbx3 és WT1 transzkripciós faktorok irányítanak. További specializáció során alalkul ki a májlebeny komplex struktúrája, amelyben az egyes régiók, így a periportális (6 8 sejt) centrolobuláris (8 10 sejt) és a centrálisan elhelyezkedő GS (glutamin szintetáz, 1 3 sejt) hepatociták a génexpressziós mintázatuk alapján elkülöníthetők. Azonosítószám: TÁMOP /1/A
48 Transzdifferenciáció és regeneratív medicina Centrális véna Bile canaliculi Centrális véna Májkapu (triádok) Szinuszoidok Májkapu Epe kivezető cső Portális véna elágazása Májartéria elágazása Limiting plate Periportális (6-8 sejt) Centrilobuláris (8-10 sejt) Glutamin szintetáz+ (1-3 sejt) VII-3. ábra: A májlebeny szerkezete Sérülést vagy károsodást követően a periszinuszális, nyugvó állapotú A-vitamintároló (Ito-féle) sejtek és az apototikus sejtek kapcsolódása az előbbi Toll-like receptorain keresztüli stimulációját váltja ki. Ezen Ito-sejtek alapvető szerepet töltenek be a máj kötőszövetes/fibrotikus regenerációjában. A májon kívüli szövetekből bevándorló fibrocitákkal valamint a hepatocitáknak az aktivált T-sejtek részvételével elősegített epitél-mezenhimális átalakulásával és extracelluláris mátrix-remodellálással együtt az Ito-sejtek szövet-specifikus pericitákká való átalakulása jelentékenyen fokozza a máj miofibroblaszt mennyiségét. A létrejött miofibroblasztok fokozott PDGFválaszkészsége a megnövekedett vándorlásukkal és kontraktilitásukkal együtt megváltoztatja a szöveti mikrocirkulációt, elősegítve a fibrózis és hegszövet-képződést. A máj parenhimális regenerációja a máj-sejtvesztés utáni májsejt-transzformáció eredménye, amely során a nyugvó hepatociták osztódó sejtekké alalkulnak. Tömeges májsejt-vesztés (pl. mérgezés után) illetve hepatocita-regeneráció (pl. krónikus májgyulladás) során a regeneráció elsődlegesen az ovális sejtekből, mint szövet- 46 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
49 Máj regeneráció specifikus őssejtekből indul. Az ovális sejtek aktiválásának kiváltása valószínűleg TNF család tagjai és receptoraik részvételével történik, melyben a közös gp130 alegységet tartalmazó citokin-receptorok is szerepet játszanak (IL-6, onkostatin M [OSM] és leukémia inhibitor faktor [LIF]). Az ovális sejtek heterogének, éretlen és érett fenotípusú epekapilláris sejtekként és köztes differenciáltságú hepatocitákként egyaránt előfordulhatnak. Számos ovális sejt-marker érett epekapilláris-sejteken és hepatocitákon valamint embrionális bipotenciális hepatoblasztokon is előfordulhat. A korai hepatocita progenitor (HPC) markerek közé tartozik a C-kit, Sca-1, NCAM és multidrog transporter, melyek segítségével áramlási citometriás eljárásokban azonosítható az ún. mellék- vagy oldalsó populáció (side population). Ezen SP sejteket először a hemopoetikus sejtekben azonosították, ahol a Hoechst fluoreszcens festék hatékony kipumpálásával és a csökkent fluoreszcencia-felvétellel váltak kimutathatóvá. Ez az eljárás a máj esetében is alkalmas az éretlen sejtek kimutatására, akár a máj embrionális organogenezise, akár daganatos átalakulás során. Az ovális sejtekben nem fejeződik ki a 7. típusú citokeratin, mely az érett hepatocitákra jellemző, ugyanakkor az alfa-fötoporotein (αfp) jellemző az ovális sejtekre és májrákokra egyaránt. Kísérletes vagy terápiás célzatú hepatikus őssejt-átültetés során számos mechanizmus segíti elő a máj-regenerációt. Elsőként a hepatikus őssejtek a lépen kertesztüli bejuttatásukat követően a portális keringésen keresztül a máj-parenchimába vándorolnak. Károsodott májban a kemoattraktív faktorok (SDF-1, HGF és SCF stem cell factor) termelődése fokozódik, ami az őssejtek megfelelő CXCR4, c-met és c-kit receptorain keresztül az őssejtek helyi felhalmozódását segíti elő. A megtelepedési folyamatot a MMP9 matrix proteináz is fokozza, mely az extracelluláris matrix szerkezetét alakítja át. A fenti folyamatok ugyanakkor a bejuttatott sejteknek csak Azonosítószám: TÁMOP /1/A
50 Transzdifferenciáció és regeneratív medicina kisebb részét érintik, a sejtek túlnyomó többsége a portális területekben zajló fokozott fagocitózis során megsemmisül. Az őssejt-közvetítette regeneráció egyik fontos eseménye a bejuttatott sejtek kilépése az érpályából. Normál körülmények között s helyben képzett VEGF a különböző MMP enzimek hatásával együtt fokozza az ér-permeabilitást, melyet különböző citosztatikus szerek felerősíthetnek. Ezt követően a helyi mikrokörnyezet az osztódás-serkentő citokinek (HGF, FGF, TGFα) termelésén keresztül megfelelővé válik a hepatocita-proliferáció számára. Sejt-bejuttatást követő szerkezeti vizsgálatok kimutatták a gap junction típusú összekapcsolódás kialakulását a transzplantáció utáni 3 7 nap körül. A bejuttatott sejtek a hepatocita irányú differenciálódás spektrumának megfelelően meglehetősen változékony sejtes-fenotípusos jellemzőkkel rendelkeznek. 1. Migráció Mozgósítás SDF-1 HGF (SCF) Fizikai/kémiai/genetikai hatás MMP-9 Szervkárosodás Centrális véna Gadolinium klorid / monocrotaline Kupffer sejtek (fagocitózis) 3. Elhalt sejtek eltávolítása Elpusztult sejt Centrális véna Őssejtek (c-kit, c-met, CXCR4) 2. Integráció Szervkárosodás VEGF HGF TGFα FGF MMP-9 MMP-2 MT1-MMP 70-80%-os sejtpusztulás Monocrotaline Doxorubicin Májkárosodás VEGF Szinusz endotél permeábilitása Effektor sejtek Centrális véna Véráramlás megváltozása Gap junction-ok Változékony in vivo sejt fenotípus Immunszuppresszió Enkapszuláció Ko-transzplantáció Értágítók VII-4. ábra: A máj regeneráció főbb szakaszai 48 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
51 Máj regeneráció Azokat a sejteket, melyek nem a megfelelő regeneratív mikrokörnyezetbe kerültek, a Kupffer-sejtek távolítják el. A regeneráció befejező szakaszában a májlebenyek alalkulnak ki ismét, a megfelelő véráramlás és az epeürítés helyreállításával. Azonosítószám: TÁMOP /1/A
52
53 VIII Hasnyálmirigy differenciáció és regeneráció A cukorbetegek száma járványszerűen emelkedik világszerte, mindez komoly egészségügyi, társadalmi és gazdasági hatást fejt ki. Az Amerikai Diabétesz Szövetség jelenlegi felmérése szerint a 2000-ben született amerikaiak egyharmada cukorbetegségre veszélyeztetett. A cukorbetegség akkor alakulhat ki, ha a Langerhans szigetek β sejtjei nem képesek olyan mennyiségű inzulint termelni, ami megfelelne a perifériás szövetek (máj, zsír és izom) metabolikus igényeinek. A β-sejtek számának csökkenése és funkciójának zavara hiperglikémiát (megemelkedett vércukorszint) idéz elő 1-es és 2-es típusú diabéteszben. Így a β-sejtek számának és funkciójának csökkenése az alapja a teljes spektrumú diabétesz kialakulásának. Ez a folyamat természetesen ösztönző erővel hat olyan kutatásokra, ami új inzulint termelő β-sejtek forrását jelentené, melyek potenciálisan felhasználhatóak lehetnek a regenerációs terápiákban. A klinikai célú alapkutatások fontos információkat szolgáltattak a transzkripciós faktorok és extracelluláris szignálok szerepéről a hasnyármirigy embrionális fejlődésében. A hasnyálmirigy embrionális fejlődése során az elsődleges anterior-poszterior mintázatképzés és a gasztruláció az e7.5 stádiumú embrióban történik meg, a végleges endoderma elkezd felcsavarodni és kialakítja a bélcsövet. A belet formáló endodermára egy helyi génexpressziós mintázat (BMP, Gata4, Furin, matrix metalloproteináz 2) jellemző. Az e.8-s stádiumú embrióban az előbél/középbél csatlakozási régióban az endodermális sejtek hasnyálmirigy irányban köteleződnek el, a Pdx1, Ptf1a, Hnf1b, Azonosítószám: TÁMOP /1/A
54 Transzdifferenciáció és regeneratív medicina Hhex, Foxa2, Mnx1 (Hlxb9), és Onecut1 (Hnf6a) transzkripciós faktorok expressziója emelkedik meg. A retinsav általi jelátvitelnek kitüntetett szerepe van az előbél és a pankreász mintázatképzésében és befolyásolja más, a pankreász fejlődésében kulcsfontosságú transzkripciós faktorok (pl. Pdx1) müködését. Amií ezek a transzkripciós faktorok kritikusak a pankreász fejlődése és funkciója szempontjából, addig egyik sem kizárólagos a pankreász vagy endoderma eredetű sejtsorsok meghatározásában. A 9.5 napos embrionális stádiumban jelentkezik az első morfológiai bizonyiték a pankreász megjelenésére: a bél dorzális oldalán egy megvastagodás jön létre. Ez a megvastagodás átalakul dorzális pankreász kezdeménnyé, amelyet 1 napra rá követ 2 ventrális/laterális kezdemény, ezek közül az egyik dominál és egyesül a dorzális kezdeménnyel. Különböző jelátviteli mechanizmusok irányítják a dorzális és ventrális kezdemény fejlődését, habár a hedgehog jelátviteli út gátlása mindkettő régió kialakításában fontos. Kezdetben az Shh expresszió kiterjed a fejlődő endodermális bélcső anterior poszterior tengelyére is, de ezt a régiót későbbiekben specifkusan gátolja a gerinchúr által termelt FGF2 és aktivin. Ellentétben ezzel, a kardiális mezodermából származó FGF2 szignál indukálja a májszövet irányú elköteleződést a ventrális régióban, amely FGF2 hiányában hasnyálmiriggyé alakul. Ahogy a szervkezdemények megjelennek, a növekvő pankreász epitélium aktiválja számos transzkripciós faktor expresszióját (Sox9, Nkx2.2, és Nkx6.1), emellett a fentebb említett bél endoderma mintázat formáló gének is expresszálódnak (Pdx1, Ptf1a, Hnf1b, Hhex, Foxa2, Mnx1, és Onecut1). Érdekességképpen az Mnx1 a dorsális kezdemény, a Hhex a ventrális kezdemény kialakulásában fontos faktor, míg a mezenhimális epitéliumból származó FGF10 mindkét oldali pankreász epitélium fejlődését biztosítja. A 12.5 stádiumú embrióban a béltraktus elfordulása miatt a dorzális és ventrális pankreász kezdemény közelebb kerül egymáshoz. A duodenumba vezető dorzális 52 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
55 Hasnyálmirigy differenciáció és regeneráció pankreász vezeték elhal, míg a ventrális vezeték kialakítja a fő pankreász kapcsolatot a duodenummal. Az endokrin sejtek differenciációja valamivel korábban indul be a dorzális régióban (glukagon pozítiv sejtek először a 9.5 stádiumban jelennek meg) mint a ventrálisban. Az endokrin sejtek differenciációja feltételezi az Ngn3 transzkripciós faktor tranziens expresszióját, amely indukálja az epitél sejtek elköteleződését endokrin irányba. A pankreász epitéliumban nagymértékben expresszált Sox9, Hnf1b, Foxa2, és Onecut1 transzkripciós faktorok közreműködnek a Ngn3 faktor aktiválásában. A Notch- Delta jelátviteli molekulák aktiválják a Hes1 gátló transzkripciós faktort, ami gátolja az Ngn3 expressziót és ezáltal megakadályozza az pankreász epitél sejtek nagyobb részének az endokrin irányba történő differenciálódását. Az e10.5 stádiumban a primitiv előtelepekben már lehet inzulin pozitív sejteket találni azonban ezek a sejtek és a fentebb említett korai glukagon expresszáló sejtek sem rendelkeznek a felnőtt β- és α-sejtek jellemzőivel. Az e13 stádiumban egy másodlagos átalakulás indul be, melynek a csúcsa az e14.5 stádium körül van, ezalatt az Ngn3 expresszió második hulláma jelentkezik. Az Ngn3 számos endokrin transzkripciós faktort aktivál beleértve a Neurod1, Pax4, és Nkx2.2 molekulákat. Az utolsó kettő molekula kulcsfontosságú a β-sejt irányú átalakulásban. Számos faktor együttes hatásaként alakul ki a specifikus endokrin sejtek identitása a szigetsejtekben. Alapvetően az α- sejteket a Pax6, Nkx2.2, Irx1 és 2, Brn4, és Arx faktorok jellemzik; a β-sejtek Pax4, Pax6, Nkx2.2, Nkx6.1, Mnx1, MafA, és Pdx1 molekulákat expresszálnak; a δ-sejtek Pax4 és Pax6; míg a PP-sejtek az Nkx2.2 által jellemezhetőek. Az ɛ-sejtek számára fontos faktorok egyelőre nem ismertek. Azonosítószám: TÁMOP /1/A
56 Transzdifferenciáció és regeneratív medicina e4.5 e5.5 e6.5 e7.5 e8.5 e9.5 e10.5 e11.5 e12.5 e13.5 e14.5 1WD 2WD 3WD 4WD 5WD 6WD Egér Ember Oct4 Sox2 Nanog Brachyury T Gsc Gata5 Sox17 Pdx1 Foxa2 Hnf4a Hhex Mnx1 Ptf1a Sox9 Hnf1b Onescut1 Ngn3 Nkx6.1 Nkx2.2 Pax6 Neurod1 Pax4 Insm1 MafA Exokrin Vezeték Vezeték Vezeték VIII-1. ábra: A pankreász embrionális fejlődése Az 1. típusú diabéteszben megfigyelt β-sejtek ellen kialakuló autoimmun folyamat drasztikusan lecsökkenti a β-sejtek tömegét, hypoinsulinemiát és ketoacidózist okoz. Ezzel szemben a 2. típusú diabéteszben egy inzulin rezisztencia (károsodik az inzulin hatásmechanizmus) alakul ki mely végülis egy részleges, de szignifikáns β- sejtszám csökkenéshez vezet. Utóbbi időben vált ismertté egy olyan autoimmun folyamat, ami a 2. típusú diabéteszes betegek egy részét is érintheti. Ezt a típust LADAnak, vagy felnőttkorú látens autoimmun diabétesznek nevezték el. Ennek alapján érdemes a diabétesz betegség felosztását újragondolni. Ezek az adatok megerősíthetik az esetleges kapcsolatot az 1. típusú és a 2. típusú betegség között és felerősítik az immunitás és a gyulladás szerepét a 2. típusú betegségben megfigyelhető β-sejt zavarban. Ezzel ellentétben viszont ismert az, hogy a csökkent β-sejt funkcióból adódó ketózis elősegíti a diabétesz kialakulását autoimmun folyamat nélkül is. 54 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
57 Hasnyálmirigy differenciáció és regeneráció Vírusok, endogén ligandok? β sejt Citokinek TNF IL-1β Makrofág INF-γ INF-α és INF-β TLR3/4, RIG-I, MDA5, egyéb receptorok Cytokin receptor jelátvitel T-sejt STAT-1, NFκB, IRF3, egyéb(?) - - JunB INF-α és INF-β + MHC I ER stressz Apoptózis jelátvitel Kemokinesk Citokinek Kemokinek Citokinek + Módosult antigének bemutatása Sejthalál + + Dendritikus sejt MHC I T-sejt Apoptótikus β sejt VIII-2. ábra: β sejt és az autoimmun diabétesz folyamata Számos mostani tanulmány igéretes eredményeket mutatott be az embrionális őssejtek területén, ahol in vivo és in vitro inzulin expresszáló sejteket hoztak létre endodermális embrionális őssejtekből feltárva ezzel az új terápiás lehetőségeket. A blasztociszta stádiumú embriók belső sejttömegéből izolált embrionális őssejtek korlátlanul képesek önmegújításra, ha szérumtartalmú tápoldatban és mitotikusan inaktív feeder sejteken növesztjük a sejteket. Továbbá megőrzik azt a képességüket, hogy bármilyen sejttípust képesek létrehozni. Jelenleg a módszerek eléggé fejlettek ahhoz, hogy humán embrionális őssejteket lehessen fenntartani humán feeder sejteken vagy feeder -mentes környezetben megfelelő növekedési faktorokkal kiegészítve az alap tápoldatot. Ezenkivül lehetséges, hogy a humán embrionális őssejteket feeder sejtekről feeder -mentes közegbe vigyük át, avagy fordítva anélkül, hogy a sejtek elvesztenék pluripotenciáljukat, habár ezek a manipulációk befolyásolhatják a termelt fehérjék expressziós mintázatát. Függetlenül ettől, a fentebb részletezett előrelépések lehetővé teszik azt, hogy olyan klinikai szintű sejtvonalakat állíthassanak elő, ahol Azonosítószám: TÁMOP /1/A
58 Transzdifferenciáció és regeneratív medicina elkerülhetőek a nem-humán eredetű komponensek hozzáadása. Az embriónális őssejtek spontán differenciálódását indukálhatjuk oldatban, hogy aggregátumokat (embrioid testecskék) képezzenek az önmegújitást elősegítő faktorok adása nélkül. Számos kutatócsoport beszámolt arról, hogy spontán differenciálodó sejtkulturákból endokrin, hormon termelő sejteket tudtak létrehozni. A legkorábbi tanulmányokban egér embriónális őssejtekből differenciáltattak inzulin szekretáló sejteket. Ezen módszerek alapja valamilyen antibiotikum rezistencia gént és inzulin promotert hordozó expressziós vektor felhasználása a transzfekcióban illetve embrioid testecske létrehozása volt. Humán embrionális őssejtekből is sikerült inzulin-termelő sejteket létrehozni, utalva elöször arra, hogy a humán embrionális őssejtek is képesek β-sejt tulajdonságú sejtekké átalakulni. Ha in vitro differenciációs kísérleti protokoll során a humán ES sejteket aktivin A és Wnt faktorokkal kezelik, majd ismét aktivint adnak utána egy definitív endoderma alakul ki, melyet a Sox17, FoxA2, az egér Cerberus homologja a CER, és a CXCR4 kemokin receptor jelenléte jellemez. Ezután, az Fgf10 és egy hedgehog gátló a cyclopamin adása ill. ismételt retinsav kezelés után kezdetleges bélcső-szerű sejtek jöttek létre, melyek a HNF1 és HNF4 faktorokat expresszálják. Ezeket követve poszterior előbél-szerű sejtek keletkeztek, melyek Pdx1, HNF6, és Hb9 markerekkel lehetett azonosítani. Végül Nkx6.1, Ngn3, Pax4, Nkx2.2 molekulákat expresszáló pankreász/endokrin prekurzokat és inzulin hormont termelő sejteket hoztak létre egy Notch jelátvitel gátló (DAPT) és egy glukagon-szerű peptid (GLP-1) receptor agonista (Exendin-4) együttes adásával, melyet még kiegészítettek különböző növekedési faktorokkal (inzulin-szerű novekedési faktor - IGF 1; hepatocita növekedési faktor HGF). A GLP-1 elősegíti a fetális β sejt érést kulturában, a HGF mitogén hatású anyag, amíg az IGF-1 posztnatálisan hat a β sejt differenciációra és túlélésre. Ily módon összefoglaltuk a jelátviteli útvonalakat melyek irányítják a β sejtek embriónális 56 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
59 Hasnyálmirigy differenciáció és regeneráció fejlődését és differenciálodását, és azon sejtekét melyek a speciális transzkripciós mintázatot expresszálva jelképezik az ES eredetű β-sejteket. További kísérletekben sikerült specifikus többlépéses módszerrel az egér embrionális őssejteket olyan idegszövetté differenciáltatni, ami szigetsejt hormonokat is tartalmazott. Habár ezekben a kísérletekben a C-peptid és az inzulin mrns hiánya arra utalt, hogy az intracelluláris inzulin nem a sejtek közvetlen terméke, hanem az a tenyésztő médiumból származik. Ezenkivül a legtöbb szigetsejt marker ami manapság használatos, például a fentebb említett transzkripciós faktorok, nem kizárólagosak a hasnyálmirigy sejtjeire, hanem számos egyéb sejtet is jellemeznek, különösen igaz ez idegi ektoderma eredetű sejtekre. Jelenleg az eredetileg egér embrionális őssejtek differenciálására kialakított módszert módosították és alkalmazták emberi embrionális őssejtekre is, bár a létrehozott sejtek karakterizálása igen limitált. Aktivin A Aktivin A Wnt Fgf10 Cyclopamine Fgf11 Cyclopamine Retinsav DAPT Exendin-4 Exendin-4 IGF-1 HGF Humán ES sejt Oct4 Nanog Sox2 E-cad Mezendoderma Bra Fgf4 Wnt3 N-cad Aktivin A Wnt Aktivin A Definitív endoderma Sox17 Cer FoxA2 Cxcr4 Primitív bélcső Hnf1b Hnf4a Noggin Keratinocita Cyclopamine növekedési faktor Retinsav Poszterior előbél Hnf6 Pdx1 Hlxb9 Endokrin progenitor Ngn3 Nkx2.2 Pax4 Nkx6.1 Éretlen endokrin Ins Glu Ghr Som PP In vivo környezet Humán ES sejt Oct4 Nanog Sox2 E-cad Mezendoderma Bra Fgf4 Wnt3 N-cad Definitív endoderma Sox17 Cer FoxA2 Cxcr4 Primitív bélcső Hnf1b Hnf4a Poszterior előbél Hnf6 Pdx1 Prox1 Sox9 Pankreász endoderma/ Endokrin prekurzorok Nkx6.1 Ptf1a Nkx2.2 Ngn3 Endokrin MafA Ins Glu Ghr Som PP VIII-3. ábra: Embrionális őssejtekből történő inzulin-termelő β sejt differenciálódás Azonosítószám: TÁMOP /1/A
60
61 IX Transzdifferenciáció a központi idegrendszeri regenerációban A központi idegrendszer számos olyan különleges tulajdonsággal rendelkezik, ami egyedülállóvá teszi a többi szövet-féleséghez képest. Végtére is ezek a tulajdonságok a központi idegrendszer heterogén sejtösszetételéből adódnak, ami alapja a hatalmas mennyiségű információ komplex feldolgozásának. Történetileg, ez a komplexitás kapcsolódott ahhoz az elképzeléshez, hogy a felnőtt agyban nincs sejtmegújhodás. Az idegszövet mint örökké változatlan, ez a dogmatikus felfogás mára kicserélődőtt azzal, hogy a felnőtt agy speciális területein történhet sejtkicserélődés. Ezt a neurogenetikus folyamatot, az agy bizonyos területein előforduló, hosszú életű neurális őssejtek tartják fenn. Következetes adatok mutatnak arra, hogy új neuronok folyamatos létrehozása történik a felnőtt emlős agyi hippocampus dentat gyrus subgranuláris régiójában és az oldalsó agyüreg (lateral ventriculus) subventriculáris zónájában (SVZ). Az újonnan létrehozzott neuronok elhagyják a subventriculáris zónát és egy hosszabb vándorlási útvonalat, a már jól ismert un. rosztrális migrációs vonalat, követve jutnak el a szagló gumóba. A felnőtt agyi SVZ-nak van a legmagasabb neurogenetikus aránya, és ebből a régióból izoláltak először olyan neuráls őssejteket amelyek képesek voltak nem-neurális sejtek létrehozására. Számos megfigyelés jelzi, hogy az SVZ eredetű asztroglia sejtek egyik specifikus altípusa alkotja aktuálisan a neurális őssejteket. Azonosítószám: TÁMOP /1/A
62 Transzdifferenciáció és regeneratív medicina Önmegújítás Sox2 HMGA2 BMI-1 Hes1,5 SoxB1 Rest Id4 HesR1,2 CBF1 GLI-2/3 HES1/5 HESR1/2 Gátlás A differenciálódás gátlása Korai differenciálódás Mash1 Phox2A Ngn1 Pax6 Sox1 Osztódás SoxB OLIG2 ID4 ID2 GLI-1 Neuron Stemness Multipotencia Asztrocita Oligodendrocita Önmegújítás Osztódás Hes1,5 Sox2 HmgA2 BMI-1 Gli2,3 CBF-1 Hes1,5 SoxB1 Gli1,2,3 Id2,4 Olig2 Terminális differenciálódás Pax2 Pax6 Ngn3 IX-1. ábra: Transzkripciós faktorok és neurális őssejtek Az emlős, felnőtt neurális őssejtek/progenitor sejtek (SPC) karakterizálása jelenleg intenzív kutatás tárgya. Ennek ismeretében új sejtes-alapú regeneratív kezeléseket lehetne alkalmazni a központi idegrendszer patológiájában, mint pl. a gerincvelői sérülésekben (spinal cord injury, SPI). A gerincvelői sérülésekben károsodnak a leszálló és felszálló axonális útvonalak és sejtpusztulás, gyulladás, demielináció történik. Ez a mozgás, érzékelés és a vegetatív idegrendszeri kontroll sérülését jelenti, a lézió szintjén és alatta. A sérülésnek két fő patológiás stádiuma van: az elsődleges sérülés során a sejtek és szövetek mechanikai károsodása történik, míg a másodlagos sérülés során a biokémiai események sorozata a gerincvelői szövetek progresszív pusztulását okozza. A gerincvelői sérülések terápiájában jelenleg nagy dózisú methylprednisolon kezelést alkalmaznak, amely elősegíti a másodlagos sérülések csökkentését, továbbá sebészeti beavatkozásokkal stabilizálják és nyomástalanítják a gerincvelőt. Ezt kiegészítve alkalmaznak még intenzív orvosi ellátást és rehabilitációs terápiát. Habár ezek a kezelési lehetőségek 60 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
63 Transzdifferenciáció a központi idegrendszeri regenerációban számos előnnyel járnak, a gerincvelői sérülések komplex patogenezise és az optimális gyógyulás érdekében igen nagy igény van új terápiás megközelítésekre. Számos preklinikai felfedezés arra irányul, hogy csökkentsék a másodlagos sérüléseket és emeljék a megmaradt ép neuronális hálózat müködőképességét illetve regenerációját. Egy ilyen igéretes lehetőség lehet a neurális őssejteken alapuló regeneratív terápia. A gerincvelői sérülés során megfigyelhető a gerincvelői progenitor sejtek (SPC) osztódása, vándorlása és érése. A felnőtt gerincvelőből eredeztetett gerincvelői progenitor sejtek képesek arra, hogy neuronokat és oligodendrocitákat hozzanak létre, például ha a hippocampus neurális régiójába transzplantálták őket. Nyilvánvaló tehát, hogy a környezet kitüntetett szerepet játszik az előalakok sorsának meghatározásában. Az utolsó néhány évben különböző módszertani megközelítéssel sikerült a gerincvelő környezetét úgy manipulálni, hogy a progenitor sejtek neuronális vagy glia irányba differenciálódtak. Az újszülött és felnőtt hippocampus illetve újszülött gerincvelő neurális régióiból származó primér asztrociták elősegítették a felnőtt hippocampális progenitor sejtek neuronális differenciálódását, míg azok az asztrociták, amelyek nem neurális régióból származtak, nem fejtettek ki ilyen hatást. Az asztrociták által indukált neurogenezis során az interleukin 1 (IL-1) és interleukin-6 (IL-6) elősegítette a progenitor sejtek neuronális differenciálódását, míg az inzulin-szerű növekedési faktor kőtő protein 6 (IGFBP6) és a proteoglycan decorin gátolta a folyamatot. Érdekességképpen, ezek a faktorok szintén szerepet játszanak gerincvelői sérülést követő gyulladásban. SGZ asztrociták beültetése vagy sonic hedgehog beinjektálása sikeresen indukálta a neurogenezist a felnőtt egér nem-neurogén kérgi régiójában. Azonosítószám: TÁMOP /1/A
64 Transzdifferenciáció és regeneratív medicina Különböző növekedési faktorok használatosak, hogy indukálják az endogén progenitor sejtek osztodását és befolyásolják a differenciálódást. Az FGF-2 és EGF bejuttatása a laterális ventriculusba az SVZ progenitor sejtek osztódását okozta. Egy másik lehetséges molekula, amelyik a neurális progenitor sejtek manipulációjában szerepet játszik az IGF-1 Az IGF1-ről kimutatták, hogy stimulálja a multipotens hippokampális progenitor sejtekből kiinduló oligodendrocita differenciációt, olyan módon, hogy megemeli a csont morfogén fehérje (BMP) antagonista Smad6, Smad7 és a Noggin molekulák expresszióját, ezáltal gátolja a BMP utat. Az asztrociták nagy mennyiségben termelik együttesen a Noggin és az agyi neurotrofikus faktort (BDNF) ezáltal a sztriátumbeli (ami általában nem neurogén) asztrociták elindulnak a neuronális differenciálódás útján. A BDNF képes arra, hogy stimulálja in vitro a spinális progenitor sejtekből kiindulva új neuronok képződését és túlélését. 62 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
65 Transzdifferenciáció a központi idegrendszeri regenerációban Gyulladás Limfociták és makrofágok bevándorlása Mikroglia aktiváció Mielin hüvely Axon T-sejtek Makrofágok/ mikroglia B-sejtek Ciszta Asztrociták Demielináció Wallerián degeneráció A neuronális hálózat elvesztése A neuronok és oligodendrociták károsodása Gliális forradás (gliosis) Remielináció Mash1 Ngn2 IL-6 LIF FGF2 EGF Oligodendrocita Ciszta IL-6 Asztrociták Neuronok IX-2. ábra: A gerincvelői sérülés folyamata és az őssejtek direk manipulációja a sérülés után Az idegrendszer más területein is lehetne hasznosítani a őssejtek manipulációján alapuló lehetséges regenerációs terápiai megközelítéseket. A progenitor sejtek retina regenerációban betöltött szerepének tisztázása lehet például egy ilyen terület. Az itt szerzett információ nagy segítséget nyújthat a látás elvesztését eredményező retina degeneráció megakadályozásában. A retinális progenitor sejtek jellegzetes génexpressziós mintázattal (Rax, Pax6, és Chx10) rendelkeznek. Részben, a Notch aktivitás hatására ezek a sejtek differenciálatlanok és osztodóképességük is megmarad. Azonosítószám: TÁMOP /1/A
66 Transzdifferenciáció és regeneratív medicina A korai fejlődés során az egyik progenitor alpopuláció csökkenti a Notch expressziót, kilép a sejtciklusból és korai neuronokká, retinális ganglion sejtekké, csapokká, amakrin és horizontális sejtekké fejlődik. A Notch, Rax, Chx10 és egyéb progenitor gének hatására a retinális progenitor sejtek egy része differenciálatlan marad és egy későbbi fejlődési stádiumot ér el, ahol a neurogenezis és gliagenezis is lehetséges. A késői retinális, progenitor sejtek lecsökkentik Notch aktivitásukat majd kilépnek a sejtciklusból, így köteleződnek el a neuronális vagy gliális sorsok irányába. A nagy mennyiségű pozítiv bhlh molekula kedvezően befolyásolja a neuronális sejtsorsokat. A Notch jelátvitel újrainditása és az ezzel járó negativ blhl emelkedés a gliális sejtsorsot helyezi előnybe. Valószinüleg más pro-gliogén faktorok, amilyen a p27, Sox9, és az EGF szignalizáció, is szerepet játszhatnak. A neuronális sérülések, betegségek vagy a hypoxia különböző elváltozásokhoz vezetnek, melyek során a vér-retina gát permeabilitása megemelkedik és ezt követően gyulladásos mediátorok szabadulhatnak fel. Ezek a faktorok indukálják a gliális aktivitást, amely a Kir csatorna müködésének a csökkenésében jelentkezik. Ezalatt a folyamat alatt nincs sejtosztódás. A csökkent Kir csatorna aktivítás a BK csatorna aktivitásának emelkedésével jellemzi a proliferációs gliózist. A p27 csökkenése egy olyan iniciális molekuláris változás, amely belépést jelent a sejtciklusba. Az intermedier filamentumok, mint a vimentin és a GFAP expressziója megemelkedik. Ezt kővetően a cyclin D3 csökkenése határozza meg a sejtciklusok számát, melyen a Müller glia sejt keresztülmegy. A neuronok képződése csak a Müller-féle gliasejtek egy részéből történik meg. A sejtek olyan jeleket használnak, melyek különböznek a gliagenezisben megfigyelhető szignáloktól. 64 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
67 Transzdifferenciáció a központi idegrendszeri regenerációban Notch Notch Notch Pozitív bhlh Retina előalak (RPC) Éretlen Müller glia (MG) sejt/ Neurogén gliasejt Kir csatorna RPC Notch (rax, chx10) p27, EGF Negatív bhlh Notch aktivitás? Neuron Sérülés Kir csatorna BK csatorna p27 cyclin D3 Érett MG sejt Nem-proliferálódó MG sejt Nem-proliferálódó MG sejt Proliferálódó MG sejt IX-3. ábra: Retinális progenitor sejtek és plaszticitásuk Azonosítószám: TÁMOP /1/A
68
69 X Kardiovaszkuláris regeneráció A szívizom regenerálására leggyakrabban az isémiás szívbetegségek (így miokardiális infarktus) és pangásos szívelégtelenség esetén van szükség. Az eljárás során több körülményt is figyelembe kell venni, így (1) három különböző sejtpopuláció (pacemaker és pitvari/kamrai szívizomsejtek, endotél és ér-simaizomsejtek) helyreállítását, (2) az immunológiai reaktivitás megelőzését valamint (3) a komplex három-dimenziós szerkezet kialakítását a folyamatos szívműködés és a környezetifizikai igénybevételhez való alkalmazkodás fenntartásával. A humán szívizomregenerációra irányuló vizsgálatokat nagymértékben nehezítette a szív-őssejt (CSC) azonosításának és ezek kialakulását szabályzó transzkripcionális elemek meghatározásának hiányosságai. Emellett a releváns in vivo tanulmányok elsősorban egér szív-modellkísérleteken alapulnak, mely számos élettani jellemzőiben eltér a humán szívtől (szív-frekvencia, a működés időtartama). Blasztociszta Bőr fibroblaszt Szív Zsír, köldökzsinór Csontvelő Vér ES ips CPC MSC EPC Szívizom kijavítás SMC EC Differenciáció Szívizomsejt X-1. ábra: Szívizom-regenerációra alkalmazott sejt-források Azonosítószám: TÁMOP /1/A
70 Transzdifferenciáció és regeneratív medicina A szívizom sejt-közvetítette regenerációjához számos szöveti forrást vizsgáltak. Ezek közül a felnőtt/autológ lehetőségként felvetődött csoportba tartoznak a szívizom önmaga (szív-progenitorok/cpc illetve szív-őssejtek/csc), a csontvelő vagy véreredetű endotél-progenitorok (EPC), vázizomsejtek/mioblasztok illetve a szatellita sejtként (SC) ismert nyugvó előalakjaik, mezenhímális őssejtek (MSC), valamint indukált őssejtekké (ips) dedifferenciált bőr fibroblasztok. Embrionális jelölt-sejtekként a blasztocisztából izolált ICM sejtek lehetséges hatását elemezték. A vizsgált sejtek által kiváltott regeneráció részben egyedi sejt-differenciálódáson, illetve parakrin folyamat részeként a túlélő sejt vagy egyéb progenitor szívizom-sejtté történő érésén keresztül történhet. A pontos mechanizmus azonosítását tovább nehezíti, hogy genetikus markerekkel jelölt sejtek felhasználásával végzett kísérletekben nem lehet megkülönböztetni a sejtes transzdifferenciálódást a sejtfúzió-közvetítette regenerációtól. A csontvelő-eredetű mononukleáris sejtek felhasználásával a szívizom regenerálódására irányuló vizsgálatok által nyújtott eredmények meglehetősen ellentmondásosak és vitatottak. Bár az eljárás javította a szívizom-károsodás utáni korai időszakban vizsgált bal kamra funkciókat, a hatékonyságot nagymértékben befolyásolta a sejt-bejuttatás módja (szívizomba vagy a koszorús erekbe történő injektálás). Ezen sejtek felhasználása során vagy endotél-előalakok vagy akár azok G-CSF általi mobilizációjával felszabaduló csontvelői prekurzorai bejuthattak a sérült szívizomba, és ott neoangiogenezis indukciója révén az infarktus körüli hipertrófiás mioblasztok/miociták hatékonyabb oxigenizációját és tápanyag-ellátását segíthetik elő, valamint fokozhatják az endogén regenerációt is. Az endogén mezenhímális őssejtekből (MSC) történő regenerációt elsőként azon férfibetegek szívében kimutatható Y-kromoszóma jelenléte vetette fel, akiket korábban női szívvel transzplantáltak. Az allogén MSC használatát elősegíti, hogy ezek nem 68 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
71 Kardiovaszkuláris regeneráció fejezik ki a B-7 és MHC II antigéneket mint allogén stimulátor molekulákat, valamint a részleteiben kidolgozott eljárás a csontvelői előalakokból való izolálásukra. Sejtfelszíni jellemzőik alapján ezek a sejtek egérben CXCR4 + /Sca-1 + /lin /CD45, emberben CXCR4 + /CD34 + /AC133 + /CD45 fenotípusú monoukleáris sejtek. A sejtek károsodott szívizmon belüli mozgását a SDF-1-CXCR4, HGF-c-Met, és LIF-LIF-R kölcsönatások irányítják. Emellett fontos körülmény, hogy az MSC differenciálódási spektruma felöleli a kardiomiocita mellett az endotél és simaizom-irányú fejlődési irányokat is. A MSC sejtek kardiomiocita irányú differenciálódása a szív-specifikus transzkripciós faktorok kifejeződésétől függ, amelyek közül legfontosabbak az Nkx2-5/Csx, GATA-4 és MEF2C. Ezt alátámasztja, hogy ezen transzkripciós faktorok felnőtt bőrfibroblasztokban való fokozott expressziója ips-közvetítette reprogramozás részeként kontraktilis miokardiális sejtek kialakulásához vezetett. Azonosítószám: TÁMOP /1/A
72 Transzdifferenciáció és regeneratív medicina Fibroblasztok Gata4/Mef2c/Tbx5 Transzplantáció Szív-progenitorok Indukált szívizomsejtek X-2. ábra: ips közvetítette újraprogramozás szívizom-regenerációban Amint a bevezetőben említettük, a szívizom-szövet rekonstrukciója jóval komplexebb folyamat, mnint egyféle sejtszövet helyreállítása a kardiomiocita differenciálódási útvonal mentén. Szintén fontos szerep jut a szívizom-matrix kialakításának, a megfelelő elektromechanikus összekapcsolódásnak, tömeges és stabil, de ugyanakkor változtatható összehúzódási aktivitásnak és funkcióképes ér-hálózatot eredményező neovaszkularizációnak. A szívizom regenerálása mellett hasonló sejt-források alkalmazhatóságát vizsgálták elsősorban perifériás érbetegségek (PVD) kezelésében is. Ezen kórképek 70 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
73 Kardiovaszkuláris regeneráció előfordulási gyakorisága életkortól függően 3 10% körül van, és leggyakrabban ateroszklerózis vagy valamely vaszkulitisz kialakulásához kapcsolódik. Korai mérsékelt klinikai tünetei közé tartozik az átmeneti bicegés-sántikálás, míg a súlyos végtagérellátási hiány esetében súlyos izom-sorvadás és lábszárfekélyhez kapcsolódó izomszövet-vesztés is létrejön, mely a végtag amputációjához vezethet. PVD kezelése során az alkalmazott kezelés hatékonyságának megítélésében annak az egyéb szövetekre (idegszövet, vázizomzat, bőr) kifejtett hatását is figyelembe kell venni. Azonosítószám: TÁMOP /1/A
74
75 XI Vese regeneráció A vese a testünk leginkább differenciált szervének tekinthető. Ezt támasztja alá az is, hogy a terhesség 36. hete után már nem képződnek új nefronok a mezenhima kimerülése miatt. Ezzel ellentmondásban ismert az, hogy bizonyos mértékű regenerációra a vese is képes. A vese progenitor sejtjeit a vizeleti pólusnál találjuk és ezek a sejtek szoros kapcsolatban állnak a tubuloglomeruláris régióban található tubuláris vese sejtekkel. Ez a tranzicionális sejtcsoport a renális progenitorok és a proximális tubulus sejtjeinek a tulajdonságaival rendelkezik. Ha a tubuláris sejtek megsérülnek, akkor a szomszédos tubuláris sejtek osztódni kezdenek, hogy pótolják az elveszett sejteket. Ismételt sejtosztódási ciklusok képesek kimeríteni a vese tubulus epitél sejtjeinek regenerációs kapacítását. Bár a renális progenitor sejtek képesek fenntartani az osztódó sejtek tömegét, így új tubuláris progenitorsejtek jönnek létre a tubuloglomeruláris régióban. Leváló podocita Vaszkuláris kocsány Podocita progenitorok Leváló podocita Híd Érett podociták Renális előalakok Vizeleti pólus XI-1. ábra: A vese felépítése és progenitor sejtjei Azonosítószám: TÁMOP /1/A
76 Transzdifferenciáció és regeneratív medicina A CD24+, CD133+, Oct4+, Bml1+, Pdx-, nestin- markerekkel fémjelzett renális progenitor sejtek a vizeleti pólus mellett lokalizálódnak és kapcsolatban állnak az érkocsányon lévő podocitákkal is. A glomerulus vaszkuláris kocsányán olyan tranzicionális sejtek találhatóak, melyek expresszálnak progenitor markereket (CD24+, CD133+), de megjelennek a podocita markerek (Pdx+, nestin+) és a fenotipusos jellemzőik is a differenciálodott podocitákra emlékeztetnek. A vese progenitor sejtek képesek arra, hogy az érkocsány irányába történő vándorlással, osztódással és differenciálódással új podocitákat (CD133-, CD24-, Pdx+, nestin+) hozzanak létre. Ez a folyamat normálisan is megtörténik, amint a vese növekszik gyerek és kamaszkorban, és feltehetőleg jelentkezik sérülés (pl. veseeltávolítás uninefrectomia) után, amikor a vese lassan regenerálódik. Glomeruláris betegségekben, amit súlyos vagy akut podocita pusztulás/leválás jellemez, a renális progenitor sejtek képesek hídat képezni a Bowmann tok és glomerulus bojt között, ami így lehetőséget ad egy szomszédos progenitor sejt vándorlására és differenciálódására, így az elvesztett podociták gyorsan pótlodhatnak. Habár azt is tudni kell, hogy egy rosszul szabályozott folyamat könnyen indukálhat hiperplasztikus glomeruláris léziókat is. Bizonyos elképzelések szerint az őssejtek képesek genetikai anyagot átadni más sejteknek membrán-határolt extracelluláris komponensekkel. A genetikai anyag kicserélése feltehetőleg kétirányú a sérült sejtek és csontvelői vagy helyi őssejtek között. A mikrovezikulák által a károsodott sejt-őssejt irányú kommunikáció során feltehetőleg az őssejtbe bejutatott mrns vagy mirns elősegíti az őssejt újraprogramozását, hogy szövetspecifikussá váljon. Az őssejt-károsodott sejt irányú kommunikáció során az őssejtek a keringésből érkeznek a sérülés helyére és talán olyan 74 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
77 Vese regeneráció faktorokat juttatnak vezikuláik segítségével a rezidens sejtekbe, melyek a szöveti sejtek dedifferenciációját, újraprogramozását és végsősoron a regenerációt segítik elő. Sérült sejt-őssejt kommunikáció Tubuláris epitél sérülés Parakrin mediátorok EGF, IGF-1, VEGF, MSP, HGF mrns vagy mirns tartalmú mikrovezikulák Keringés Szövet regeneráció Differenciáció Contvelői eredetű vagy helyi szöveti őssejtek Őssejt-sérült sejt kommunikáció mrns vagy mirns tartalmú mikrozeikulák Tubuláris epitél sérülés De-differenciáció Proliferáció Parakrin mediátorok EGF, IGF-1, VEGF, MSP, HGF Re-differenciáció Keringés Csontvelői eredetű őssejtek Tubuláris epitél regeneráció Helyi szöveti őssejtek XI-2. ábra: Őssejtek által medial folyamatok a vese regenerációjában Azonosítószám: TÁMOP /1/A
78
79 XII Daganat őssejtek A múlt század első felében végzett megfigyelések kimutatták, hogy tumortranszplantációs kísérletekben viszonylag alacsony gyakorisággal fordulnak elő azok a daganat-sejtek, melyek hatékonyan tudnak transzplantálható tumort indukálni. Beültetésüket követően viszont gyakran figyeltek meg nagyfokú fenotípus- illetve sejtciklusbéli heterogenitást a daganat összetételében, mely erőteljesen emlékeztetett a klasszikus hematológiai klísérletekben tanulmányozott kolónia-képző sejtek (CFU) jellegzetességeire. Ezen hasonlóság kihangsúlyozására a transzplantált tumor-kolóniákat CFU-T rövidítéssel jelölték, a lépben képződő hemopoetikus sejtcsoportok analógiájára (CFU-S). Ezt követően az akut mieloid leukémia egysejt-szintű vizsgálata és klonális analízise igazolta, hogy egyetlen sejt képes a meglehetősen heterogén sejt-összetétel teljes spektrumának kialakítására. Ezt követően a daganat/rák-őssejt (CSC) koncepció fokozatosan általánosan elfogadottá vált, és jelentékeny mértékben hozzájárult különböző rosszindulatú betegségek hatékonyabb kezelésének kialakításához. Az őssejt-alapú regeneratív medicina tipikus megközelítésével és céljával ellentétben ugyanakkor a leglényegesebb különbség, hogy tumor-terápia során nem a regenerálódást, hanem pontosan a daganat újdonképzését kívánjuk megakadályozni, melyet akár a daganatok citotoxikus kezelés utáni spontán regenerációjának is tekinthetünk. Az őssejtek alapvető jellegzetességeiből (önmegújítás és differenciálódási potenciál) kiindulva a fejlődés és regenerációs során a daganat őssejtek a normál őssejtekhez képest eltérő megjelenési sorrendet mutatnak. Daganatok esetében az eredeti onkogén transzformáció egy korlátozott mértékű klonális expanzióhoz vezet, amely a diagnózis felállításának időszakára magába foglal egy olyan kisebb alcsoportot, Azonosítószám: TÁMOP /1/A
80 Transzdifferenciáció és regeneratív medicina mely addigra újraébresztette az őssejt-szerű programozódását. Ez a programozás egyidejűleg jeleníti meg az onkogén mutáció megtartását és egy nagyobb proliferációs aktivitású sejtszármazék folyamatos képzésére való képességet. Onkogén átalakulás Terápia Kiinduló sejt Idő Daganat előtt Daganat-diagnózis Javulás Visszaesés XII-1. ábra: Daganat és daganat-őssejt teória A citotoxikus terápia eredményeképpen a proliferatív összetevő elpusztul vagy nagymértékben csökken, ugyanakkor az őssejt-szerű komponens kikerüli a kezelést, és idővel regenerálhatja az elpusztult tumor-sejteket. Ebből következően a tumorok heterogenitását két fő tényező határozza meg (a) a biológiailag különböző variánsok kialakulása a tumoros transzformáció és a citotoxikus kezelés megkezdése között eltelt időszakban, valamint (b) azon természetes szelekciós variánsok létrejötte mindkét alcsoporton belül, melyek a citortoxikus kezelésekre (gyógyszeres, irradiációs, stb) rezisztensek voltak a kelezés befejeződése után. 78 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
81 Daganat őssejtek Szelekciós nyomás Daganat őssejtek XII-2. ábra: CSC fejlődés Az eltérő jellegzetességű programozással rendelkező (őssejt-jellegű vagy proliferatív) összetevők kialakulását két különböző modell írja le. A sztochasztikus mechanizmus révén az eltérő őssejt- illetve proliferatív-frakciók az őket körülvevő mikrokörnyezeti, vagy egyéb, az onkogén transzformációtól független aktuális belső állapota (sejt-ciklus, transzkripciós faktor-mintázat, stb) alapján jöhetnek létre. A hierarchikus modell szerint először az önmegújító összetevő alakul ki és a domináns, mely mennyiségét a belőlük később kialakuló proliferatív összetevő elnyomja, ameddig a daganatra jellemző önmegújító-proliferatív steady state sejt-arány/mennyiség létrejön. A CSC sejtek jelenlétét sorozat-transzplantációs kísérletekkel igazolhatjuk, amiben az eredeti tumorból megfelelő sejtfelszíni markerek felhasználásával izolált CSC sejteket egy elsődleges recipiensbe, majd abból ismételt CSC-tisztítással a másodlagos recipiensbe oltjuk. Ha a másodlagos recipiensben megtapadt daganat heterogén, akkor azt CSC-eredetűnek, míg ha nem indul növekedésnek, illetve a gyors növekedést követően túlnyomórészt homogén összetételű, akkor proliferatív eredetűnek Azonosítószám: TÁMOP /1/A
82 Transzdifferenciáció és regeneratív medicina tekintjük. Ilyen eljárásokkal sikerült emlőrák, agydaganat, hasnyálmirigy-rák, tüdőrák, retinoblasztoma, vastagbélrák és melanoma CSC kimutatása. Azonosításuk és tisztításuk általában CD34, CD44 és sejtvonal-marker negativitás melletti CD133 antigén expresszió alapján történt. A fiziológiás őssejtekhez hasonlóan a CSC sejtek szintén szoros kapcsolatban állnak az őket körülvevő fészekkel (niche). Ugyanakkor a niche összetétele és szerkezete a partnersejtekel való kontaktus során változhat, így a CSC számára megfelelőbb környezet jöhet létre, és ennek során a CSC-niche kölcsönhatás elsősorban a CSC, és nem a fiziológiás őssejt-igényekkel mutathat nagyobb harmóniát. Normál körülmények között Niche Niche Átmeneti szignál Domináns szignál Őssejt Nyugvó Önmegújítás Őssejt Lassú sejtosztódás Szabályozott osztódás Megfelelő differenciálódás Daganatokban Niche Őssejt Nyugvó Niche Domináns szignál Átmeneti szignál Őssejt Lassú sejtosztódás Szabályozatlan osztódás és károsodott differenciálódás, további genetikai mutációkkal szembeni érzékenység XII-3. ábra: CSC és az őssejt-niche megváltozása Akut mieloid leukémia esetén a leukémiás sejtek infiltrálhatják az egészséges hemopoetikus fészkeket, és a tumoros sejtek számára protektív irányban modulálhatják ezeket, ezáltal az AML sejtek rezisztensebbé válhatnak a citotoxikus kezeléssel szemben. Ezen a módon a hemopoetikus niche oszteoblaszt komponense fokozott 80 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
83 Daganat őssejtek támogatja az AML CSC proliferációt (Wnt, Notch-szignalizáció), míg a vaszkuláris elemek a CSC sejtek számára mutattak nagyobb homing aktivitást a megfelelő kemokinek termelődésének megváltozásán keresztül. Károsodott normál HSC fészek funkció A fészek inváziója Citokin (SCF) szekréció Fokozott ön-megújítás Fokozott leukémia őssejt nyugalom Kemoterápia-rezisztencia Normál HSC (LKS +, CD34, CD150 +, CD48 - ) A hagyományos fészek-függés megszűnése és alternatív fészekbe való áthelyeződés Szabályozatlan megtelepedés CXCR4/CXCR12 interakciók VLA-4 fokozott expressziója Szimpatikus idegrendszeri szabályozás Leukemia őssejt (humán CD34 + /CD38 - ; egér lin -, c-kit +, Sca-1 - ) Érett hemopoetikus sejtek (parakrin citokinek) Fokozott citokin válaszkészség Immunfenotípus kialakulása Endoszteális szabályzó elemek (oszteoblaszt, oszteoklaszt, csont matrix, oszteopontin, Ca) Perivaszkuláris regulátor elemek (endotél, CAR, MSC) XII-4. ábra: AML fészek jellegzetességek A CSC eliminálás céljára a lehetséges terápiás eljárások kiszélesítését igénylik. Hagyományosan elsősorban a proliferatív tumor-komponens citotoxikus terápiával történő elpusztítása volt az elsődleges cél, ugyanakkor újabb, specifikus kinázblokkolók, adhéziós molekulapárok gátlása illetve szignál-útvonalak modulálása (BMP, Wnt) a jövőben jelentékeny kiegészítő hatást nyújthat a CSC niche funkciók befolyásolásával a tumor-ellenes gyógykezelésekben. Azonosítószám: TÁMOP /1/A
84 Transzdifferenciáció és regeneratív medicina Daganat őssejtek célzott kezelése DNS ellenőrző kinázok Notch szignálút NFkB szignálút ROS állapot Daganat-őssejt depléciója Tumor visszafejlődése Anti-angiogén BMP-k Vérerek képződésének gátlása Daganat őssejt fennmaradás-gátlás Többi sejt proliferációjaleáll Daganat-őssejtek differenciálódása Tumortömeg csökkenése XII-5. ábra: Kombinált tumor-terápia CSC és a niche kezelése 82 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
85 XIII Az őssejt-kutatás és terápia etikai háttere Kevés téma és kutatási terület váltott ki az utóbbi időben akkora és olyan jellegű vitát, mint az őssejt-izolálás és felhasználása szöveti regeneráció céljára. Figyelembe véve számtalan társadalmi elemét (orvosi kutatástól és terápiától üzleti lehetőségig, vallási meggyőződésig és politikai stb. álláspontig), a téma számos részletének szerteágazó etikai konzekvenciáit érdemes megkülönböztetni. Különösképpen élénk vita alalkult ki azon témákról, amelyek az őssejtek eredetére (embrionális vagy felnőtt) illetve felhasználási céljára (reproduktív vagy terápiás) vonatkoznak, melyek érintik a páciensek kiválasztását, valamint a nem felhasznált embrionális szövet további sorsát. Egyéb őssejtek (beleértve a köldökzsinór őssejteket) valamelyest kevésbé intenzív vitát váltottak ki, ugyanakkor ezek raktározásának és felhasználásának egyre szélesedő körben való elterjedése és bővülő alkalmazási lehetőségei feltehetőleg további etikai kérdéseket vethetnek fel. Az etikai vélemények alakulása és ütköztetése szorosan követte a fő kutatási irányok alalkulását, ami a humán embrionális őssejt (hesc) vizsgálatával vált először élessé. Általánosságban az embrionális őssejtek kutatási vagy terápiás vizsgálatának megkérdőjelezését a pro-life politikai meggyőződés azon összetevője motiválta, melyben a hangsúly az implantáció előtti embrió jogi-erkölcsi státuszára és sorsára helyeződik. Azon személyek és csoportok véleménye szerint, akik ellenzik az embrionális őssejt-kutatást, az embrió jogi-morális státusza megegyezik bármely élő személyével, beleértve az egyed életének értékét és védendő jellegét. Ugyanakkor egy személy élő vagy halott állapotának eldöntésére alkalmazott orvosi meghatározások egyike sem alkalmazható ebben a stádiumban. Emellett az ilyen korai, differenciálatlan állapotú Azonosítószám: TÁMOP /1/A
86 Transzdifferenciáció és regeneratív medicina organizmusokból származó sejtek komplex szövetek helyreállítására szolgálnak, nem lehet definiálni ezen sejtek és más, így differenciálódott limfoid sejtek státusza közötti különbséget, melyből szintén sikerült teljes klónozott állatot előállítani. Ezen vélemény szerint a kutatási során felhasznált embriók elpusztítása egyenértékű a gyilkossággal, és semmiféle nemes kutatási cél sem igazolhatja ezek megtörténtét. A témára vonatkozó vallási vélemények meglehetősen eltérőek, amennyiben a legfontosabb vallási tanítások nem fogadják el a korai embriók önálló teljes jogú mibenlétét. Nyugati keresztény, zsidó, iszlám, politeista hindu vagy buddhista tanítások szerint az önálló személyiség megjelenése a terhesség során későbbre tehető, míg más vallások szerint az önállóság és teljes jogállás az anyaméhen kívüli önálló életképességhez kötött. A hesc kutatás más ellenzőinek elképzelése szerint a preimplantációs embriók rendelkeznek a teljes szervezetté válás képességével, ezért erkölcsileg mindenképpen hibás egy ilyen képesség elpusztítása. Ez az elképzelés ugyanakkor nem veszi figyelembe a gyakorlati életben kimutatott nyilvánvaló minőségi különbséget az in vitro megtermékenyítés (IVF) során képzett embriók és a természetes megtermékenyülés során képződött embriók között, ahol az utóbbi esetében is megfigyelhető 70 80%-os embrió-elhalás. Mivel ezek a viták általában szélesebb filozófiai, vallási vagy politikai ügyek kapcsán merülnek fel, a résztvevők véleménye csak ritkán alapoz tisztán tudományos érvekre. A differenciált sejtek újraprogramozása révén indukált pluripotens őssejt (ips) kialakításának lehetősége az őssejt-kutatás körüli vita jelentős mérséklődését eredményezte. Ugyanakkor ezen sejtek differenciálódási potenciálja nem helyettesítheti az embrionális őssejt-kutatást, elsősorban eltérő differenciálódási jellemzőik, másrészről az esetleges daganatos transzformáció veszélye miatt. A többi alapkutatáshoz hasonlóan az össejtkutatás is nagymértékben nemzetközi együttműködéseken alapul, ezért az 84 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
87 Az őssejt-kutatás és terápia etikai háttere egyes nemzeti törvénykezési különbségek az őssejt-kutatás területén érzékenyen befolyásolhatják, gyakran akadályozzák a gyorsabb fejlődést. Az alapkutatáshoz kapcsolódó bioetikai viták mellett ugyanolyan fontosak azok az etikai kérdések, melyek a kutatás gyakorlati alkalmazásakor jelentkeznek. Terápiás célú alkalmazásuk kétségtelenül teljes jogosultsággal bíró személyeket érint, akik jogai és érdekei sérülhetnek az eljárás során. Egészen a legutóbbi időkig nem voltak olyan, kutatókra vonatkozó foglalkozási szabályok, melyek irányt mutathattak volna azon kutatók számára, akik kutatási eredményeiket klinikai terápiában kívánták volna alkalmazni ben az International Society for Stem Cell Research (ISSCR) olyan irányelveket javasolt, amelyek ezt a hiányt pótolták. A kutatás és beteg kezelése (bench-to-bedside) számos bonyolult eljárást érint, jószerivel mindegyik valamilyen bioetikai területtel összekapcsolódva, elsősorban a kockázat/haszon megítélése kapcsán. Így például a sejtek kezelésére vonatkozó személyeknek és intézményeknek egy közös minőségi eljárásban kell megállapodniuk az őssejt izolálás, jellemzés és tárolás tekintetében, beleértve az egyéni kutatókat és profit-érdekelt sejtbankokat és a szabályzó hatóságokat. A preklinikai kipróbálás során alkalmazandó állatmodellekben szintén hasonló referenciákra van szükség, valalmint a humán kipróbálásra regisztrált jelöltek kiválasztásában is. Az ISSCR klinikai alkalmazási irányelvei különösképpen kihangsúlyozzák az őssejtkutatásban résztvevők személyes részvételének fontosságát a humán alkalmazásra való engedélyezési eljárás minden szakaszában. Az őssejt-kutatásban jártas személyek a legalkalmasabbak kutatóknak és kutatási bizopttságoknak való segítségnyújtásra a javasolt vizsgálatok tudományos megalapozottságának elbírálásában, lehetséges kockázat-felmérésben. Az ISSCR irányelvei szintén kiemelik, hogy a betegek kiválasztásakor a lehetséges veszélyek ismertetésére különösképpen részletesen Azonosítószám: TÁMOP /1/A
88 Transzdifferenciáció és regeneratív medicina terjedjen ki a projekt bemutatása. Ezek a lehetséges veszélyek magukba foglalják a daganat-képződés lehetőségét, immunológiai reakciókat, a bejuttatott sejtek előre nem megjósolható viselkedését és egyéb, nem előre meghatározható egészségi kockázatokat. A jövőbeli kutatási résztvevőket érintő veszélyek esélye tovább csökkenthető a résztvevő személyek alapos és folyamatos ellenőrzésével és vizsgálatával, valamint az észlelt eltérések és komplikációk lelkiismeretes és időben megtett bejelentésével. Az egyik legjobb példa ezen utóbbi előírás fontosságára az alapos és átlátható szabályzás keretében az őssejtek nem hagyományos felhasználása. Jelenleg az őssejtalapú terápiák közül csak a hemopoetikus őssejtek hematológiai kórképekben történő alkalmazása, valamint szaruhártya-regenerációban és súlyos égésekben epiteliális őssejt-terápia a klinikai standard eljárás. Ugyanakkor a közvélemény gyakran nincs tisztában egy-egy új eljárás kifejlesztéséhez szükséges, megfelelő tudományos hátterű munka idő- és energiaigényével Ezt az információhiánnyal párosult megalapozatlan reménykedést több esetben is kihasználják gátlástalan személyek, akik megfelelő anyagi térítés ellenében hatékony őssejt-terápia lehetőségével kecsegtetik a tájékozatlan betegeket. Ezek az úgynevezett őssejt-klinikák hiteles tudományos bizonyítékok és magyarázatok nélkül hirdetik szolgáltatásaikat, mellyel akár a jelenleg is meglévő hatályos törvényeket szegik meg. 86 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
89 Az őssejt-kutatás és terápia etikai háttere Kutatási szakasz Etikai kérdések A biológiai anyagok gyűjtése Informált és önkéntes beleegyezés hesc kutatás Az embriók megsemmisítése Csak kutatás céljára létrehozott embriók 1. Petesejt donorok megfizetése 2. Petesejt izolálás orvosi kockázata 3. A meddőségi kezelésben résztvevő nők termékenységi érdekeinek elsődlegessége Más helyen előállított őssejtek Esetleg ellentétes jogi és etikai szabályozás használata Őssejt klinikai eljárások A kísérletes eljárás veszélyei és haszna Megfelelő felvilágosításon alapuló beleegyezés Azonosítószám: TÁMOP /1/A
90
91 Ajánlott irodalom Christophersen NS, Helin K. Epigenetic control of embryonic stem cell fate. J Exp Med 2010; 207: Comyn O, Lee E, MacLaren RE. Induced pluripotent stem cell therpaies for retinal disease. Curr Opin Neurol 2010; 23:4 9. Crane JF, Trainor PA. Neural crest stem and progenitor cells. Annu Rev Cell Dev Biol 2006; 22: Gilbert SF. Developmental Biology Sinauer Associates. Lagasse E, Shizuru JA, Uchida N, Tsukamoto A, Weismann IL. Toward regenerative medicine. Immunity 2001; 14: Lazzeri E, Mazzinghi B, Romagnani P. Regeneration and the kidney. Curr Opin Nephrology Hypertension 2010; 19: Lobo NA, Shimono Y, Qian D, Clarke M. The biology of cancer stem cells. Annu. Rev Cell Dev Biol 2007; 23: Azonosítószám: TÁMOP /1/A
92 Transzdifferenciáció és regeneratív medicina Meivar-Levi I, Ferber S. New organs from our own tissues: liver to pancreas transdifferentiation. Trends Endocrin Metabol 2003; 14: Ralston A, Rossant J. The genetics of induced pluripotency. Reproduction 2010; 139: Suaudeau J From embryonic stem cells to ips an ethical perspecive. Cell Prolif 2011; 44: Tiscornia G, Belmonte JCI. MicroRNAs in embryonic stem cell function and fate. Genes and Development 2010; 24: Watt FM, Driskell RR. The therapeutic potential of stem cells. Phyl. Trans. R. Soc. B. 2010; 365: Weissmann IL, Anderson DJ, Cage F. Stem and progenitor cells: origins, phenotpyes, lineage commitments and transdifferentiations. Annu Rev Cell Dev Biol 2001; 17: Yakushiji N, Yokoyama H, Tamura K. Repatterning in amphibian limb regeneration: A model for study of genetic and epigenetic control of organ regeneration. Semin Cell Dev Biol. 2009; 20: Zhou Q, Melton DA. Extreme makeover: converting one cell into another. Cell Stem Cells 2008; 3: A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
93
94
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
TÁMOP-4.1.2-08/1/A-2009-0011 Tantárgy címe: Transzdifferenciáció és regeneratív medicina Dr. Balogh Péter és Dr. Engelmann Péter
 Előadás Előadás címe Dia Dia címe száma 1. Őssejtek és transzdifferenciáció: bevezetés, alapok 2. Őssejt-típusok, fenntartásuk és homeosztázisuk 3. Regeneráció állatmodellekben 2. Alapfogalmak 3. Őssejt-kutatás
Előadás Előadás címe Dia Dia címe száma 1. Őssejtek és transzdifferenciáció: bevezetés, alapok 2. Őssejt-típusok, fenntartásuk és homeosztázisuk 3. Regeneráció állatmodellekben 2. Alapfogalmak 3. Őssejt-kutatás
Transzdifferenciáció és regeneratív medicina
 Balogh, Péter, PTE Általános Orvostudományi Kar Engelmann, Péter, PTE Általános Orvostudományi Kar műszaki szerkesztő: Bencze, Zsolt, Csöngei, Veronika, Czulák, Szilvia felelős szerkesztő: Péter, Balogh,
Balogh, Péter, PTE Általános Orvostudományi Kar Engelmann, Péter, PTE Általános Orvostudományi Kar műszaki szerkesztő: Bencze, Zsolt, Csöngei, Veronika, Czulák, Szilvia felelős szerkesztő: Péter, Balogh,
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Őssejtek és hemopoiézis 1/23
 Őssejtek és hemopoiézis 1/23 Sejtsorsok Sejtosztódás Sejt differenciáció sejtvonulatok szövetek (több sejtvonulat) Sejt pusztulás Sejtvonulat az őssejtek és azok utódai egy adott szöveti sejt differenciációja
Őssejtek és hemopoiézis 1/23 Sejtsorsok Sejtosztódás Sejt differenciáció sejtvonulatok szövetek (több sejtvonulat) Sejt pusztulás Sejtvonulat az őssejtek és azok utódai egy adott szöveti sejt differenciációja
Őssejtek és hemopoiézis 1/23
 Őssejtek és hemopoiézis 1/23 Sejtsorsok Sejtosztódás Sejt differenciáció sejtvonulatok szövetek (több sejtvonulat) Sejt pusztulás Sejtvonulat az őssejtek és azok utódai egy adott szöveti sejt differenciációja
Őssejtek és hemopoiézis 1/23 Sejtsorsok Sejtosztódás Sejt differenciáció sejtvonulatok szövetek (több sejtvonulat) Sejt pusztulás Sejtvonulat az őssejtek és azok utódai egy adott szöveti sejt differenciációja
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Sejtek - őssejtek dióhéjban. 2014. február. Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest
 Sejtek - őssejtek dióhéjban 2014. február Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest A legtöbb sejtünk osztódik, differenciálódik, elpusztul... vérsejtek Vannak
Sejtek - őssejtek dióhéjban 2014. február Sarkadi Balázs, MTA-TTK Molekuláris Farmakológiai Intézet - SE Kutatócsoport, Budapest A legtöbb sejtünk osztódik, differenciálódik, elpusztul... vérsejtek Vannak
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Molekuláris Medicina
 Molekuláris Medicina Molekuláris Medicina Őssejt terápia Génterápia Tumor terápia Immunterápia Egyéb terápiák Vakcinák Genetikai diagnosztika Orvosi genomika Terápiák Diagnosztikák Orvostudomány: régi
Molekuláris Medicina Molekuláris Medicina Őssejt terápia Génterápia Tumor terápia Immunterápia Egyéb terápiák Vakcinák Genetikai diagnosztika Orvosi genomika Terápiák Diagnosztikák Orvostudomány: régi
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Immunológia alapjai előadás. Az antigén-receptor gének szerveződése és átrendeződése. Primer B-sejt fejlődés
 Immunológia alapjai 11-12. előadás Az antigén-receptor gének szerveződése és átrendeződése. Primer B-sejt fejlődés Az antigén-receptor gének kifejeződésének főbb kérdései Minden testi sejt tartalmaz TcR/BcR
Immunológia alapjai 11-12. előadás Az antigén-receptor gének szerveződése és átrendeződése. Primer B-sejt fejlődés Az antigén-receptor gének kifejeződésének főbb kérdései Minden testi sejt tartalmaz TcR/BcR
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Őssejtkezelés kardiovaszkuláris kórképekben
 Őssejtkezelés kardiovaszkuláris kórképekben Papp Zoltán Debreceni Egyetem Kardiológiai Intézet Klinikai Fiziológiai Tanszék Megmenthető a károsodott szív őssejtekkel? Funkcionális változások az öregedő
Őssejtkezelés kardiovaszkuláris kórképekben Papp Zoltán Debreceni Egyetem Kardiológiai Intézet Klinikai Fiziológiai Tanszék Megmenthető a károsodott szív őssejtekkel? Funkcionális változások az öregedő
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Mikrogliák eredete és differenciációja
 Mikrogliák eredete és differenciációja 2017. 10. 24. Jordán Viktória F. Ginhoux et al. Origin and differentiation of microglia, 2013 F. Ginhoux et al. Fate mapping anaylsis reveals that adult microglia
Mikrogliák eredete és differenciációja 2017. 10. 24. Jordán Viktória F. Ginhoux et al. Origin and differentiation of microglia, 2013 F. Ginhoux et al. Fate mapping anaylsis reveals that adult microglia
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE
 Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Az immunrendszer működésében résztvevő sejtek Erdei Anna Immunológiai Tanszék ELTE Tanárszakosok, 2017. Bev. 2. ábra Az immunválasz kialakulása 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán
Immunológia Alapjai. 13. előadás. Elsődleges T sejt érés és differenciálódás
 Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Molekuláris biológiai összefoglaló kurzus 11. Hét. Kun Lídia, Semmelweis Egyetem, genetikai Sejt- és Immunbiológiai Intézet
 Molekuláris biológiai összefoglaló kurzus 11. Hét Kun Lídia, Semmelweis Egyetem, genetikai Sejt- és Immunbiológiai Intézet Megtermékenyítés I. Folliculus sejtek Zona pellucida(zp-1, ZP- 2,3) Membrán Citoplazma
Molekuláris biológiai összefoglaló kurzus 11. Hét Kun Lídia, Semmelweis Egyetem, genetikai Sejt- és Immunbiológiai Intézet Megtermékenyítés I. Folliculus sejtek Zona pellucida(zp-1, ZP- 2,3) Membrán Citoplazma
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje
 1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
http://www.geneticliteracyproject.org Nagy Krisztina Semmelweis Egyetem, Orálbiológiai Tanszék
 ŐSSEJTEK http://www.geneticliteracyproject.org 2015. május 6. Nagy Krisztina Semmelweis Egyetem, Orálbiológiai Tanszék Az őssejt definíciója korlátlan önmegújító képesség differenciált utódsejtek létrehozása
ŐSSEJTEK http://www.geneticliteracyproject.org 2015. május 6. Nagy Krisztina Semmelweis Egyetem, Orálbiológiai Tanszék Az őssejt definíciója korlátlan önmegújító képesség differenciált utódsejtek létrehozása
Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig
 Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig induced Pluripotens Stem sejt (ipss) első közlemény 2006-ban egér / humán, embrionális / felnőtt fibroblasztok
Indukált pluripotens sejtek (IPs) 6 év alatt a Nobel-díjig...... és 8 év alatt az öngyilkosságig induced Pluripotens Stem sejt (ipss) első közlemény 2006-ban egér / humán, embrionális / felnőtt fibroblasztok
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre ([email protected]) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre ([email protected]) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
In vivo szövetanalízis. Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra
 In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
In vivo szövetanalízis Különös tekintettel a biolumineszcens és fluoreszcens képalkotási eljárásokra In vivo képalkotó rendszerek Célja Noninvazív módon Biológiai folyamatokat képes rögzíteni Élő egyedekben
SEJT,SZÖVET,SZERV BIOLÓGIAI ÖSSZEFOGLALÓ KURZUS 6. HÉT. Kun Lídia Semmelweis Egyetem, Genetika, Sejt és Immunbiológiai Intézet
 SEJT,SZÖVET,SZERV BIOLÓGIAI ÖSSZEFOGLALÓ KURZUS 6. HÉT Kun Lídia Semmelweis Egyetem, Genetika, Sejt és Immunbiológiai Intézet Egy eukarióta sejt általában Kompartmentalizáció = különböző sejtfolyamatok
SEJT,SZÖVET,SZERV BIOLÓGIAI ÖSSZEFOGLALÓ KURZUS 6. HÉT Kun Lídia Semmelweis Egyetem, Genetika, Sejt és Immunbiológiai Intézet Egy eukarióta sejt általában Kompartmentalizáció = különböző sejtfolyamatok
A polikomb fehérje, Rybp kulcsfontosságú az egér embrionális őssejtek neurális differenciációjához
 A polikomb fehérje, Rybp kulcsfontosságú az egér embrionális őssejtek neurális differenciációjához Ph.D. értekezés tézisei Kovács Gergő Témavezető: Dr. Pirity Melinda MTA-Szegedi Biológiai Kutatóközpont,
A polikomb fehérje, Rybp kulcsfontosságú az egér embrionális őssejtek neurális differenciációjához Ph.D. értekezés tézisei Kovács Gergő Témavezető: Dr. Pirity Melinda MTA-Szegedi Biológiai Kutatóközpont,
Immunológia I. 2. előadás. Kacskovics Imre ([email protected])
 Immunológia I. 2. előadás Kacskovics Imre ([email protected]) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre ([email protected]) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A kemotaxis kiváltására specializálódott molekula-család: Cytokinek
 A kemotaxis kiváltására specializálódott molekula-család: Cytokinek Cytokinek - definíció Cytokin (Cohen 1974): Sejtek közötti kémi miai kommunikációra alkalmas anyagok; legtöbbjük növekedési vagy differenciációs
A kemotaxis kiváltására specializálódott molekula-család: Cytokinek Cytokinek - definíció Cytokin (Cohen 1974): Sejtek közötti kémi miai kommunikációra alkalmas anyagok; legtöbbjük növekedési vagy differenciációs
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai. Az immunválasz szupressziója Előadás. A szupresszióban részt vevő sejtes és molekuláris elemek
 Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai előadás. A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és
 Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Immunológia alapjai 15-16. előadás A humorális immunválasz formái és lefolyása: extrafollikuláris reakció és csíracentrum reakció, affinitás-érés és izotípusváltás. A B-sejt fejlődés szakaszai HSC Primer
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Degeneráció és regeneráció az idegrendszerben
 Degeneráció és regeneráció az idegrendszerben Axonális sérülés és regeneráció August Waller, 1850: Waller-féle degeneráció (Wallerian degeneration) disztális axonális csonk: degeneráció 24-36 órán belül
Degeneráció és regeneráció az idegrendszerben Axonális sérülés és regeneráció August Waller, 1850: Waller-féle degeneráció (Wallerian degeneration) disztális axonális csonk: degeneráció 24-36 órán belül
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
OTKA ZÁRÓJELENTÉS
 NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
NF-κB aktiváció % Annexin pozitív sejtek, 24h kezelés OTKA 613 ZÁRÓJELENTÉS A nitrogén monoxid (NO) egy rövid féléletidejű, számos szabályozó szabályozó funkciót betöltő molekula, immunmoduláns hatása
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Új terápiás lehetőségek (receptorok) a kardiológiában
 Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
Új terápiás lehetőségek (receptorok) a kardiológiában Édes István Kardiológiai Intézet, Debreceni Egyetem Kardiomiociták Ca 2+ anyagcseréje és új terápiás receptorok 2. 1. 3. 6. 6. 7. 4. 5. 8. 9. Ca
http://www.rimm.dote.hu Tumor immunológia
 http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Problémák és lehetőségek a helyreállító gyógyítás területén
 Problémák és lehetőségek a helyreállító gyógyítás területén Sarkadi Balázs MTA-TTK Enzimológiai Intézet, Semmelweis Egyetem 2017. december 13. Fejlett terápiás orvosi készítmények (ATMP): az EMA-CAT szerepe
Problémák és lehetőségek a helyreállító gyógyítás területén Sarkadi Balázs MTA-TTK Enzimológiai Intézet, Semmelweis Egyetem 2017. december 13. Fejlett terápiás orvosi készítmények (ATMP): az EMA-CAT szerepe
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Sejtfeldolgozás Felhasználás
 Sejtterápia Sejtfeldolgozás Felhasználás Fagyasztva tárolás Sejtmosás Alap sejtszelekció Komplex sejtszelekció Ex vivo sejtszaporítás Sejtaktiválás Immunizálás Génmodifikálás Köldökzsinórvér bank Limfocita
Sejtterápia Sejtfeldolgozás Felhasználás Fagyasztva tárolás Sejtmosás Alap sejtszelekció Komplex sejtszelekció Ex vivo sejtszaporítás Sejtaktiválás Immunizálás Génmodifikálás Köldökzsinórvér bank Limfocita
1. Az immunrendszer működése. Sejtfelszíni markerek, antigén receptorok. 2. Az immunrendszer szervei és a leukociták
 Sejtfelszíni markerek, antigén receptorok A test őrei 1. Az immunrendszer működése Az individualitás legjobban az immunitásban mutatkozik meg. Feladatai: - a saját és idegen elkülönítése, felismerése -
Sejtfelszíni markerek, antigén receptorok A test őrei 1. Az immunrendszer működése Az individualitás legjobban az immunitásban mutatkozik meg. Feladatai: - a saját és idegen elkülönítése, felismerése -
Immunológia alapjai. T-sejt differenciálódás és szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe
 Immunológia alapjai T-sejt differenciálódás és szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe A limfocita fejlődés lépései Recirkuláció a periférián Korai érés és növekedési
Immunológia alapjai T-sejt differenciálódás és szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe A limfocita fejlődés lépései Recirkuláció a periférián Korai érés és növekedési
A harántcsíkolt vázizom differenciációja, regenerációja
 A harántcsíkolt vázizom differenciációja, regenerációja Shahragim Tajbakhsh Current Opinion in Genetics & Development 2003, 13:413 422 közti mezoderma vese ivarszervek Paraxiáls mezoderma Fej szomiták
A harántcsíkolt vázizom differenciációja, regenerációja Shahragim Tajbakhsh Current Opinion in Genetics & Development 2003, 13:413 422 közti mezoderma vese ivarszervek Paraxiáls mezoderma Fej szomiták
Doktori értekezés tézisei
 Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Doktori értekezés tézisei A komplement- és a Toll-szerű receptorok kifejeződése és szerepe emberi B-sejteken fiziológiás és autoimmun körülmények között - az adaptív és a természetes immunválasz kapcsolata
Apoptózis. 1. Bevezetés 2. Külső jelút 3. Belső jelút
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
BIOLÓGIAI HATÓANYAGOK TESZTELÉSE BIOTECHNOLÓGIAI MÓDSZEREKKEL
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 BIOLÓGIAI HATÓANYAGOK
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 BIOLÓGIAI HATÓANYAGOK
B-sejtek szerepe az RA patológiás folyamataiban
 B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
B-sejtek szerepe az RA patológiás folyamataiban Erdei Anna Biológiai Intézet Immunológiai Tanszék Eötvös Loránd Tudományegyetem Immunológiai Tanszék ORFI, Helia, 2015 április 17. RA kialakulása Gary S.
A Notch jeltovábbító rendszer és a galektin-1 molekula szerepe a vérképző őssejt niche működésének szabályozásában. Vas Virág
 A Notch jeltovábbító rendszer és a galektin-1 molekula szerepe a vérképző őssejt niche működésének szabályozásában Vas Virág Témavezető: Professzor Dr. Pálóczi Katalin Országos Gyógyintézeti Központ 2005
A Notch jeltovábbító rendszer és a galektin-1 molekula szerepe a vérképző őssejt niche működésének szabályozásában Vas Virág Témavezető: Professzor Dr. Pálóczi Katalin Országos Gyógyintézeti Központ 2005
Immunológia. Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun
 Immunológia Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun Hogyan működik az immunrendszer? Milyen stratégiája van? Milyen szervek / sejtek alkotják?
Immunológia Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun Hogyan működik az immunrendszer? Milyen stratégiája van? Milyen szervek / sejtek alkotják?
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában
 Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
NÖVÉNYÉLETTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
Vásárhelyi Barna. Semmelweis Egyetem, Laboratóriumi Medicina Intézet. Az ösztrogénekimmunmoduláns hatásai
 Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
Vásárhelyi Barna Semmelweis Egyetem, Laboratóriumi Medicina Intézet Az ösztrogénekimmunmoduláns hatásai Ösztrogénhatások Ösztrogénhatások Morbiditás és mortalitási profil eltérő nők és férfiak között Autoimmun
Immunológia Világnapja
 a Magyar Tudományos Akadémia Biológiai Osztály, Immunológiai Bizottsága és a Magyar Immunológiai Társaság Immunológia Világnapja - 2016 Tumorbiológia Dr. Tóvári József, Országos Onkológiai Intézet Mágikus
a Magyar Tudományos Akadémia Biológiai Osztály, Immunológiai Bizottsága és a Magyar Immunológiai Társaság Immunológia Világnapja - 2016 Tumorbiológia Dr. Tóvári József, Országos Onkológiai Intézet Mágikus
A sejtek lehetséges sorsa. A sejtek differenciálódása. Sejthalál. A differenciált sejtek tulajdonságai
 A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
10. előadás: A sejtciklus szabályozása és a rák
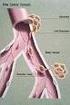 10. előadás: A sejtciklus szabályozása és a rák sejtciklus = Azon egymást követő fázisok vagy szakaszok sorrendje, amelyen egy sejt áthaladaz egyik osztódástól a következőig.) A sejtciklus változatai szabálytalan
10. előadás: A sejtciklus szabályozása és a rák sejtciklus = Azon egymást követő fázisok vagy szakaszok sorrendje, amelyen egy sejt áthaladaz egyik osztódástól a következőig.) A sejtciklus változatai szabálytalan
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnolóiai mesterképzés mefeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományeyetemen és a Debreceni Eyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi biotechnolóiai
Az orvosi biotechnolóiai mesterképzés mefeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományeyetemen és a Debreceni Eyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi biotechnolóiai
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Vérképző és egyéb szöveti őssejtek
 Vérképző és egyéb szöveti őssejtek Uher Ferenc Országos Vérellátó Szolgálat, Őssejt-biológia, Budapest Őssejtek Totipotens őssejtek Pluripotens (embrionális) őssejtek Multipotens (szöveti) őssejtek Elkötelezett
Vérképző és egyéb szöveti őssejtek Uher Ferenc Országos Vérellátó Szolgálat, Őssejt-biológia, Budapest Őssejtek Totipotens őssejtek Pluripotens (embrionális) őssejtek Multipotens (szöveti) őssejtek Elkötelezett
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Transzgénikus állatok előállítása
 Transzgénikus állatok előállítása A biotechnológia alapjai Pomázi Andrea Mezőgazdasági biotechnológia A gazdasági állatok és növények nemesítése új biotechnológiai eljárások felhasználásával. Cél: jobb
Transzgénikus állatok előállítása A biotechnológia alapjai Pomázi Andrea Mezőgazdasági biotechnológia A gazdasági állatok és növények nemesítése új biotechnológiai eljárások felhasználásával. Cél: jobb
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Immunológia alapjai 11-12. előadás T-sejt differenciálódás T sejt szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe
 Immunológia alapjai 11-12. előadás T-sejt differenciálódás T sejt szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe A limfocita fejlődés lépései Recirkuláció a periférián
Immunológia alapjai 11-12. előadás T-sejt differenciálódás T sejt szelekció a tímuszban: a mikrokörnyezet és szolubilis faktorok szabályozó szerepe A limfocita fejlődés lépései Recirkuláció a periférián
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Epigenetikai szabályozás
 Epigenetikai szabályozás 1. A Transzkripció epigenetikai szabályozása Dia 1 A kromatin szerkezete A sejtciklus S fázisában egyetlen sejtben kb 4x1 méter hosszúságú DNS található 4x23 darabra vágva (4N
Epigenetikai szabályozás 1. A Transzkripció epigenetikai szabályozása Dia 1 A kromatin szerkezete A sejtciklus S fázisában egyetlen sejtben kb 4x1 méter hosszúságú DNS található 4x23 darabra vágva (4N
Sejtmag, magvacska magmembrán
 Sejtmag, magvacska magmembrán Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Kompartmentalizáció Prokaryóta Cytoplazma Eukaryóta Endomembrán Kromatin Plazma membrán Eredménye
Sejtmag, magvacska magmembrán Láng Orsolya Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet Kompartmentalizáció Prokaryóta Cytoplazma Eukaryóta Endomembrán Kromatin Plazma membrán Eredménye
Jelutak ÖSSZ TARTALOM. Jelutak. 1. a sejtkommunikáció alapjai
 Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
A preventív vakcináció lényege :
 Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Szövettípusok a növény és állatvilágban
 Szövettípusok a növény és állatvilágban Hogyan növekednek és fejlődnek a növények, állatok? Milyen állandósult szövetek alkotják? Többsejtűség Óriás gomba: Armillaria ostoyae, Oregon, 8.9 km 2 Óriás vízi
Szövettípusok a növény és állatvilágban Hogyan növekednek és fejlődnek a növények, állatok? Milyen állandósult szövetek alkotják? Többsejtűség Óriás gomba: Armillaria ostoyae, Oregon, 8.9 km 2 Óriás vízi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Hamar Péter. RNS világ. Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. www.meetthescientist.hu 1 26
 Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Hamar Péter RNS világ Lánczos Kornél Gimnázium, Székesfehérvár, 2014. október 21. 1 26 Főszereplők: DNS -> RNS -> fehérje A kód lefordítása Dezoxy-ribo-Nuklein-Sav: DNS az élet kódja megkettőződés (replikáció)
Anyai eredet kromoszómák. Zigóta
 2012. február 28. Anyai eredet kromoszómák Apai eredet kromoszómák Zigóta Muslica embrió Fej Nem képz dik fej, az embrió elpusztul A muslica blasztoderma sorstérképe Genetikai boncolás + + STERIL FEJ
2012. február 28. Anyai eredet kromoszómák Apai eredet kromoszómák Zigóta Muslica embrió Fej Nem képz dik fej, az embrió elpusztul A muslica blasztoderma sorstérképe Genetikai boncolás + + STERIL FEJ
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
A B sejtek érése, aktivációja, az immunglobulin osztályok kialakulása. Uher Ferenc, PhD, DSc
 A B sejtek érése, aktivációja, az immunglobulin osztályok kialakulása Uher Ferenc, PhD, DSc Az immunglobulinok szerkezete Fab V L V H C L C H 1 C H 1 Az egér immunglobulin géncsaládok szerveződése Hlánc
A B sejtek érése, aktivációja, az immunglobulin osztályok kialakulása Uher Ferenc, PhD, DSc Az immunglobulinok szerkezete Fab V L V H C L C H 1 C H 1 Az egér immunglobulin géncsaládok szerveződése Hlánc
Allergia immunológiája 2012.
 Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
Allergia immunológiája 2012. AZ IMMUNVÁLASZ SZEREPLŐI BIOLÓGIAI MEGKÖZELÍTÉS Az immunrendszer A fő ellenfelek /ellenségek/ Limfociták, makrofágok antitestek, stb külső és belső élősködők (fertőzés, daganat)
PLASZTICITÁS. Merisztémák merisztemoidok őssejtek (stem cells) stem cell niche
 PLASZTICITÁS Definíció: A növényi sejtek átalakulhatnak egymásba. A differenciált sejtek dedifferenciálódhatnak, totipotens ősmerisztéma sejtté. Ebből új differenciálódás indulhat el (redifferenciáció).
PLASZTICITÁS Definíció: A növényi sejtek átalakulhatnak egymásba. A differenciált sejtek dedifferenciálódhatnak, totipotens ősmerisztéma sejtté. Ebből új differenciálódás indulhat el (redifferenciáció).
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 2. előadás A veleszületett és specifikus immunrendszer sejtjei Vérképzés = Haematopeiesis, differenciálódás Kék: ősssejt Sötétkék: éretlen sejtek Barna: érett
Immunológiai módszerek a klinikai kutatásban 2. előadás A veleszületett és specifikus immunrendszer sejtjei Vérképzés = Haematopeiesis, differenciálódás Kék: ősssejt Sötétkék: éretlen sejtek Barna: érett
ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS
 ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS Mi az öregedés? Egyrészről az idő múlásával definiálható, a születéstől eltelt idővel mérhető, kronológiai sajátosságú, Másrészről az idő múlásához köthető biológiai,
ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS Mi az öregedés? Egyrészről az idő múlásával definiálható, a születéstől eltelt idővel mérhető, kronológiai sajátosságú, Másrészről az idő múlásához köthető biológiai,
3. Főbb Jelutak. 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3.
 Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
