Ph.D. ÉRTEKEZÉS TÉZISEI
|
|
|
- Alexandra Somogyi
- 6 évvel ezelőtt
- Látták:
Átírás
1 Ph.D. ÉRTEKEZÉS TÉZISEI Funkcionális fehérjedinamikai vizsgálatok fluoreszcencia és femtoszekundumos időfelbontású tranziens abszorpciós spektroszkópiai módszerekkel Lukács András Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet 2007
2 Ph.D. ÉRTEKEZÉS TÉZISEI Funkcionális fehérjedinamikai vizsgálatok fluoreszcencia és femtoszekundumos időfelbontású tranziens abszorpciós spektroszkópiai módszerekkel Lukács András Program: Biokémia és molekuláris biológia Programvezető: Dr. Sümegi Balázs Alprogram B-130: Funkcionális fehérjedinamika vizsgálata biofizikai módszerekkel Alprogramvezető: Dr. Somogyi Béla Témavezetők: Dr. Somogyi Béla Dr. Nyitrai Miklós Dr. Marten H. Vos Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet
3 1. Az aktomiozin komplex dinamikájának vizsgálata fluoreszcencia spektroszkópiai módszerekkel Bevezetés Az izomösszehúzódás során az aktin és a miozin ciklikus kölcsönhatása biztosítja a két filamentális rendszer egymáshoz képest történő elmozdulását. A két fehérje komplexén belül a kontrakció során bekövetkező konformációs módosulások meghatározó szerepet játszanak az erőkifejtés létrejöttében. A miozin Szerkezeti szempontból a miozin egy hosszú, aszimmetrikus molekula, amelyen egy feji és egy farki rész különböztethető meg. Erős denaturáló ágensek (5 M HCl vagy 8 M urea ) jelenlétében a miozin hat polipeptid láncra esik szét: két nehéz láncra, amelyek tömege egyenként Da körüli, illetve négy könnyűláncra, amelyek közül kettőnek a tömege Da, kettőnek pedig Da. A két nehéz lánc egy kettős hélixet alkot, amelynek egyik végén mindkét lánc globuláris alakot vesz fel. Ezek a miozin fejei, amelyekhez hozzákapcsolódnak a könnyűláncok, fejenként kettő-kettő. Proteolitikus emésztéssel a miozin több fragmentumra bontható. Kimotripszines emésztést követően kapjuk a 350 kda körüli nehéz (HMM, heavy meromyosin ) és a 150 kda körüli könnyű meromiozint (LMM, light meromyosin ). A HMM papainnal történő emésztéssel tovább bontható az S1 (szubfragmentum 1) és S2 (szubfragmentum 2) fragmensekre. Az emésztés során kapott alkotók közül a HMM-nek és az S1-nek jut kitüntetett szerep, mindkét komponens kötődik ugyanis az aktinhoz, rendelkezik ATPáz aktivitással, valamint képes az aktin filamentum mozgatására. Az S1 további emésztése megmutatta, hogy ez a fragmens a miozin legkisebb olyan aktív egysége, amely az aktint mozgatni tudja 1. A fej két ellentétes oldalán helyezkednek el az aktin-kötő és a nukleotid-kötő regiók, amelyek két hélixen keresztül kommunikálnak egymással. A nyaki régióban a C terminálishoz közel található egy 85 Ǻ hosszú α-hélix, amelyhez kötődik a regulációs könnyűlánc, illetve az esszenciális könnyűlánc. Ezek együttesen úgy hatnak, mint egy 3
4 emelőkar, amely a nukleotid-kötő régió kis konformációs változásait nagy szögű elmozdulásokká erősíti. Az aktin Az aktin monomer egy 43 kda molekulatömegű globuláris fehérje, amely két fő doménből áll. Mindkét domén tovább osztható két-két szubdoménre. A két fő domén között található az úgynevezett kation- és nukleotid-kötő hasadék, amelyben kétvegyértékű kationok (fiziológiás esetben Mg 2+, in vitro körülmények között az aktinpreparálás oldatai és a kationokhoz való affinitás miatt Ca 2+ ) illetve ATP, ADP.P i, valamint ADP helyezkedhet el. Nukleotidmentes környezetben az aktin denaturálódik. Fiziológiás sókoncentrációk mellett az aktin gyorsan polimerizálódik, egy kettős hélixet alkotva. Az aktin filamentumok mellett mindig található egy olyan aktin populáció, amely monomer formában van jelen. Egyensúly esetében a monomerek koncentrációja a kritikus koncentráció, amely alatt az aktin már nem képes polimerizálódásra. A kritikus koncentráció értéke több paramétertől (például a nukleotidok és a kationok koncentrációjától) függ. Az aktomiozin kölcsönhatás. A kontrakciós ciklus Az aktomiozin kölcsönhatás leírására a legelfogadottabb a lengő emelőkar ( swinging lever arm ) modell, amely szerint az S1 farki része az ATP hidrolízis következtében létrejövő orientációs változások során egyfajta emelőként húz egyet az aktin filamentumon. Nukleotidmentes állapotban az S1 az aktinhoz erősen kötött (rigor) állapotban található, miközben hosszanti tengelye 45 o -os szöget zár be az aktin filamentummal. Az S1 nukleotid-kötő zsebe ilyenkor nyitott állapotban található. A miozin fejek aktinkötésének affinitása nukleotidfüggő; a rigor állapottal összevetve az ATP állapot affinitása erősen lecsökken, aminek következtében a miozin fej disszociál az aktin filamentumról, és a nukleotid-kötő zseb zárt állapotba kerül. Az ATP hidrolízist követően a nukleotid-kötő zsebben ADP és inorganikus foszfát (P i ) lesz jelen, a fej 4
5 pedig elfordul és gyengén kötődik az aktin filamentumhoz; a nukleotid-kötő zseb újra nyitott állapotba kerül, ami lehetővé teszi a foszfát disszociációját. Ezt követően a nukleotid-kötő zsebben csak ADP található, aminek következtében az aktin-miozin kötés erősebb lesz, mivel az ADP állapotban a miozin aktinhoz való affinitása meghaladja az ATP és az ADP.Pi állapot affinitását. A következő lépésben (ez a húzási szakasz) disszociál az ADP, ami az S1 konverter doménjának közel 70 o -os elfordulásával jár, amely pedig az emelőkar elfordulásához vezet. Ez vezethet terheletlen esetben - az aktin filamentum mintegy 10 nm-es elmozdulásához. Célkitűzések Tekintettel arra, hogy az izomösszehúzódás során kiemelt szerep jut az aktomiozin komplexben bekövetkező konformációváltozásoknak, lényeges ismernünk az aktomiozin komplex különböző régióinak dinamikai parmatéreit az egyes fázisokban. Munkám célja az aktomiozin komplex katalitikus doménjének, illetve a könnyűlánckötő domén flexibilitásának a vizsgálata volt, rigor állapotban. A dinamikai vizsgálatok elvégzéséhez első lépésként találni kell olyan módszereket, amelyek alkalmasak a fehérjedinamikai paraméterek jellemzésére. Tekintettel arra, hogy az aktin monomeren Cys-374, az S1 katalitikus doménen a Cys- 707, az esszenciális könnyűláncon pedig a Cys-177 nagy reaktivitású cisztein, fluorofórokkal szelektíven jelölhető, fluoreszcencia spektroszkópiai módszereket lehet alkalmazni. A kérdéses fehérjerégiók egymáshoz viszonyított helyzetét fluoreszcencia rezonancia energiatranszfer (FRET) mérések segítségével lehet jellemezni. Első lépésként tehát olyan FRET módszerek alkalmazása illetve kidolgozása a cél, amelyek segítségével jól jellemezhetőek a kölcsönható fehérjék dinamikai tulajdonságai. A megfelelő módszerek kiválasztását követően annak a feltérképezése a feladat, hogy a nukleotidmentes állapotban (amelynek esetében a miozin fej erős kötésben van az aktin filamentummal) a miozin-s1 katalitikus doménje, illetve könnyűlánc-kötő doménje milyen dinamikai tulajdonságokkal rendelkeznek. 5
6 Alkalmazott módszerek Az aktomiozin komplex dinamikai tulajdonságainak jellemzésére két saját fejlesztésű fluoreszcencia spektroszkópiai módszert alkalmaztunk. Mindkét módszer a fluoreszcencia rezonancia energiatranszfer (FRET) elnevezésű jelenségre épül. Röviden összefoglalva, a fluoreszcencia rezonancia energiatranszfer egy dipól-dipól csatoláson keresztül megvalósuló szinglet-szinglet energiatranszfer, amelynek során a donor molekula foton emissziója nélkül ad át energiát az akceptor molekulának. A gyakorlatban az energiatranszfer hatásfoka a steady-state spektrumokból illetve a fluoreszcencia élettartamokból határozható meg: τ DA FDA E = 1 = 1 (I.1) τ D FD ahol τ DA és F DA az akceptor jelenlétében, a τ D és F D pedig az akceptor hiányában mért fluoreszcencia élettartam, illetve fluoreszcencia intenzitás. A FRET alkalmazása helikális szimmetriával rendelkező fehérjék esetén Az általunk kidolgozott módszer a fehérjékben fellelhető helikális szimmetriákat használja ki, segítségével távolságokat tudunk meghatározni, illetve következtetéseket tudunk levonni a fehérje konformációs állapotára vonatkozóan. A módszert, amelyet eredetileg aktin filamentumra dolgoztak ki 2, mi az aktomiozin komplexalkalmazásokhoz fejlesztettük tovább 3. Valójában bármilyen helikális struktúra esetén alkalmazható. A módszert az aktomiozin komplex esetében fogom ismertetni. Egy donor egy akceptor esetében a FRET hatásfok az alábbiak szerint számítható: E ( R / R) 6 = ( R0 / R), (I.2) ahol R a donor-akceptor távolság, R 0 pedig az a donor-akceptor távolság (Förster távolság), amelynek esetében az energiatranszfer hatásfoka 0,5 (50%). Az általunk vizsgált esetekben a donor egy aktin-kötő fehérjén helyezkedett el, az akceptorok pedig az aktin protomereken. Ennek megfelelően egy donor több akceptorral állt kölcsönhatásban. Ebben az esetben a megfigyelt FRET hatásfok az individuális FRET hatásfokok összege 4, és az alábbi módon számítható: 6
7 E N i= 1 = N 1+ 6 ( R / R ) i= ( R / R ) 0 i i, (I.3) ahol R i az egyedi donor-akceptor távolságokat jelenti, N pedig az akceptorok számát. Tekintve, hogy a távolabbi monomerek járuléka igen kicsi, az egyszerűség kedvéért a transzferhatásfok kiszámítása során csak a donorhoz legközelebb fekvő öt monomeren levő akceptor járulékát vettük figyelembe. Az egyedi R i távolságok kiszámításakor figyelembe vettük az aktin helikális szerkezetét: az F-aktint egy 13/6 geometriájú hélixként lehet jellemezni (6 fordulatban 13 monomer követi egymást), amelyben két egymást követő aktin monomer egymáshoz képest 166 o -kal fordul el, köztük levő távolság (a z tengely mentén) pedig 27,5 Ǻ. Ennek megfelelően az akceptorok térbeli elhelyezkedése felírható; az aktin filamentum képzeletbeli tengelyéhez rögzített Descartes koordinátarendszerben az akceptorok x,y,z koordinátája a következőképpen számítható: x i =r cos((3-i)166 o ) (I.4a) y i =r sin((3-i)166 o ) (I.4b) z i =(3-i)27.5 Å, (I.4c) ahol r az akceptor radiális koordinátája, vagyis a filamentum hosszanti, z tengelyétől mért távolsága. Esetünkben r értéke a röntgenkrisztallográfiás adatokból ismert volt (~ 25 Ǻ), az akceptorok ugyanis az aktin monomer 374-es ciszteinjéhez kötődtek specifikusan. Az energiatranszfer hatásfokának számításakor figyelembe kell venni a monomerek betöltöttségét, vagyis azt, hogy az adott monomeren található-e akceptor. A lehetőségek száma egy kis módosítással binomiális eloszlást követ; az energiatranszfer hatásfokának kiszámításához ugyanis nem kell figyelembe vennünk azt az esetet, amikor egyetlen monomeren sem helyezkedik el akceptor. Ennek megfelelően összesen 31 esetet különböztethetünk meg. Az akceptor moláris arány (g) ismeretében annak a valószínűsége, hogy k számú monomer van megjelölve, a következő módon számítható: k 5 k pk g (1 g) =, (I.5) ahol k a betöltött monomerek száma, g pedig a jelölési arány. 7
8 Az energiatranszfer hatásfoka g akceptor jelölési arány esetében ennek megfelelően: E 5 = pe, (I.6) g k k k = 1 ahol E k a k számú jelölt monomer esetében számított energiatranszfer hatásfok, p k pedig az elrendezés valószínűsége. Azzal a feltételezéssel, hogy a donor és az akceptor molekulák közötti távolság nem rögzített, hanem egy eloszlást követ, a módszer a fehérjék heterogenitásának jellemzésére is alkalmassá tehető 3. A donor-akceptor távolságot az ω(r) Gauss-eloszlás segítségével közelítettük a következő módon: 1 ( R R ) ω ( R) = exp c 2 σ 2π 2σ 2, (I.7) ahol R c a tengelytől való távolság középértéke, σ pedig a félértékszélessége. Ennek megfelelően az energiatranszfer hatásfokának számítása a következőképpen módosul: E = pω( R ) E. (I.8) g k j jk jk A módszer alkalmazása a gyakorlatban úgy történt, hogy az akceptor moláris arány függvényében mért fluoreszcencia rezonancia energiatranszfer hatásfok értékekre illesztve egy MatLab programnyelvben írt algoritmus segítségével kerestük azokat az R c és σ értékeket, amelyek esetén a mért értékektől való eltérés a legkisebb volt. Fehérje flexibilitásának karakterizálása FRET segítségével Az előző fejezetben említett módszer mellett egy másik FRET módszert is alkalmaztunk a vizsgálataink tárgyát képező fehérjék dinamikai tulajdonságainak feltérképezésére. A módszer lényege, hogy az energiatranszfer mechanizmusának köszönhetően bevezethető egy olyan f paraméter, amelynek hőmérsékletfüggő változása a fehérjemátrix flexibilitására jellemző mennyiség 5. Minél meredekebben változik f a hőmérséklet függvényében, annál flexibilisebb a donor-akceptor pár között elhelyezkedő fehérjemátrix. f = E F DA (I.9) 8
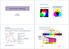
9 Eredmények és következtetések Konformációs eloszlások és távolságok a rigor aktomiozin komplexben A jelenleg leginkább elfogadott, ún. emelőkar ( lever arm ) modell szerint a miozin fej könnyű-lánc-kötő doménjének az aktin filamentum tengelyéhez képest történő, a kötött nukleotidok által szabályozott elfordulása biztosítja a két filamentális rendszer relatív elmozdulásához szükséges molekuláris hátteret. Az itt ismertetett kísérletek során a miozin S1 úgynevezett katalitikus doménjének, illetve a lever arm részét képező könnyűlánc-kötő doménnek aktintól mért távolságát határoztuk meg rigor állapotban, vagyis abban az esetben, amikor a miozin fej nukleotidmentes állapotban van 6. A távolságok meghatározására a helikális fehérjékre kidolgozott FRET módszerünket alkalmaztuk. A katalitikus domén és az aktin filamentum közötti távolság meghatározása érdekében a miozin S1 707-es ciszteinjét jelöltük specifikusan az IAEDANS nevű fluoreszcens festékkel, amely jelen esetben a donor szerepét töltötte be. A könnyűlánc-kötő domén aktin filamentum távolság meghatározásának érdekében a donort az S1 177-es ciszteinjéhez kötöttük. I.1. ábra Az aktomiozin szerkezeti modellje. A szerkezeten feltüntettük azokat az aminosavakat, amelyekhez a donor (Cys-707, Cys-177) valamint az akceptor (Cys-374) molekulákat kötöttük. Mindkét esetben az akceptorok (IAF) az aktin filamentumot alkotó monomerekhez (Cys-374) voltak kötve. A távolabbi akceptorok elhanyagolható járuléka 9
10 miatt a FRET mérések során a donorhoz legközelebb eső öt akceptor (vagyis öt monomer) járulékát vettünk figyelembe. Abban az esetben, amikor a donort az S1 Cys-707 aminosavhoz kötöttük, a fluoreszcencia energiatranszfer hatásfoka lineárisan változott az akceptor moláris arány függvényében, ami tipikusan az egy donor-egy akceptor rendszerekre jellemző (I.2a. ábra). Ha a donort a Cys-177 aminosavhoz illesztettük, a mért értékeknek az akceptor moláris aránytól való függése már nem volt lineáris, és jelentős eltérést mutattak az egy donor egy akceptor esetet feltételező tendenciától (I.2b. ábra) Energia transzfer hatásfok (%) Energia transzfer hatásfok (%) ,0 0,2 0,4 0,6 0,8 Akceptor moláris arány 0,0 0,2 0,4 0,6 0,8 Akceptor moláris arány I.2. ábra. Az ábrán a mért fluoreszcencia energia transzfer hatásfok látható a Cys-707 (a) esetében (fekete körök) illetve a Cys-177 esetében (b). Folytonos vonallal van feltüntetve a legjobb lineáris illesztés, szaggatott vonallal pedig a röntgenkrisztallográfiás adatokból számolt, mozdulatlanságot feltételező értékek. A mért fluoreszcencia energiatranszfer hatásfok értékeket a módszerekről szóló fejezetben ismertetett eljárás segítségével értékeltük ki, két esetet különböztetve meg: homogén, illetve heterogén eloszlású S1 populációt feltételezve. A homogén esetben minden S1 molekula ugyanabban a konformációban található, ennek megfelelően a donor ugyanolyan távolságra helyezkedik el a filamentumhoz képest, a heterogén esetben az S1 molekulák egy konformációeloszlással rendelkeznek (I.3. ábra). Ez utóbbi esetben a FRET hatásfokának számításánál azt feltételeztük, hogy az aktin tengelytől mért távolságok egy Gauss-eloszlást követnek. Abban az esetben, ha a donor a katalitikus doménen (Cys-707) helyezkedett el, homogén konformációeloszlást feltételezve az illesztés szemmel láthatóan jó minőségű. 10
11 0,4 40 Energia transzfer hatásfok (%) 0,3 0,2 0,1 0,0 Energia transzfer hatásfok (%) ,0 0,2 0,4 0,6 0,8 Akceptor moláris arány 0,0 0,2 0,4 0,6 0,8 Akceptor moláris arány I.3. ábra. Az energia transzfer hatásfokának függése a Cys-707 (a) és Cys-177 (b) esetében. Folytonos vonallal ábrázoltuk a heterogén eloszlást, szaggatottal pedig a homogén eloszlást feltételező illesztéseket. Fekete körökkel ábrázoltuk a mért értékeket. A számított FRET hatásfokok eltérése a mért értékektől akkor a legkisebb, amikor a donor aktin filamentumtól mért távolságát az x=77 ± 3 Å, y=5±5 Å, z=3±4 Å koordinátákkal adtuk meg. Figyelembe véve, hogy a radiális távolság (az akceptor távolsága az aktin tengelyétől) 25 Å, a donornak a legközelebbi aktin monomertől mért távolsága 52 ± 3 Å. Ez az érték jó egyezést mutat más szerzők egy donor egy akceptor esetet feltételező számításaival Mint azt a későbbiekben majd láthatjuk a katalitikus domén esetében a homogén és a heterogén eset feltételezése hasonló eredményre vezet. A könnyűlánc-kötő doménen elhelyezkedő donor (Cys-177) esetében, homogén eloszlást feltételezve, a számított energiatranszfer értékek látványosan eltérnek a mért értékektől, heterogén konformációeloszlást feltételezve azonban sikerült jó illesztést kapni a mért értékekre. A tapasztalt heterogenitás hátterében feltételezésünk szerint az áll, hogy az S1 molekula és ezen belül is a könnyűlánc-kötő domén számos konformációban létezik, amelyben a donor-akceptor távolság tág intervallumon belül változhat. A donor-akceptor távolság karakterizálása érdekében az energiatranszfer számításánál azt feltételeztük, hogy a donor-akceptor távolság Gauss-eloszlást követ. Az eloszlás átlagértékét és a félértékszélességét az illesztésből határoztuk meg. Ahogy az a I.20. ábrán látszik, a donor-akceptor távolságeloszlás feltételezése jó illesztéshez vezet. A legjobb illesztés esetén a Cys-177 távolsága az aktin tengelytől 98 ± 3 Å, ennek megfelelően 73 ± 3 Å a legközelebbi aktin monomertől. Az eloszlás félértékszélessége 102 ± 4 Å volt. Annak a magyarázata, hogy a donor-akceptor távolság, és valószínűleg ennek megfelelően a könnyűlánc ilyen nagy intervallumon 11
12 belül mozoghat, egyik lehetséges oka a protein mátrix nagyfokú flexibilitása. Elképzelhető azonban az is, hogy ez a nagy távolságeloszlás nem a fehérjemátrix flexibilitásával, hanem nagyszámú, de merev konformáció jelenlétével magyarázható. A távolságeloszlást feltételező illesztést elvégeztük abban az esetben is, amikor a donor a katalitikus doménen helyezkedett el. Az előzetes várakozásoknak megfelelően a távolságeloszlás feltételezése nem javította az illesztés minőségét. Az illesztés eredményeképpen az átlagos távolság 52 ± 2 Å-nak adódott, ami megegyezett a homogén esetben kapott értékkel. A távolságeloszlás félértékszélessége 5 ± 3 Å volt. A Cys-177 aktin filamentumtól való távolságára kapott érték (73 Å) eltér a mások által korábban megfigyelt értékektől (50-60 Å), de viszonylag közel van a röntgenkrisztallográfiás adatokból számolt 89 Å höz. Az, hogy a mi általunk kapott távolság közelebb van a röntgenkrisztallográfiás eredményekhez, mint a korábbi FRET mérések eredményei, valószínűleg a több akceptor figyelembe vétele, illetve a távolságeloszlás feltételezése miatt adódott. Méréseink megerősítik azt az EPR spektroszkópiával kapott megfigyelést 11, mely szerint a katalitikus domén és a könnyűlánc-kötő domén el tud fordulni egymáshoz képest. Méréseink egyeznek annak a szaturációs transzfer-epr kísérletnek a megfigyelésével is, amely arra a következtetésre jutott, hogy a katalitikus domént és a könnyűlánc-kötő domént egy flexibilis csukló köti össze 12. Az aktomiozin komplex flexibilitásának vizsgálata Az S1 dinamikai tulajdonságainak további feltérképezése érdekében az alkalmazott módszerek fejezetben ismertetett FRET eljárással vizsgáltuk az aktomiozin komplex flexibilitását. A fehérjemátrix flexibilitásának vizsgálatához az energiatranszfer hatásfokának és a donor akceptor jelenlétében mért fluoreszcencia intenzitásának arányát mértük a hőmérséklet függvényében. Az f paraméter hőmérsékletfüggése információt szolgáltat a fehérjemátrix flexibilitásában bekövetkezett változásokról, illetve esetleg a hőmérsékletváltozás által indukált konformációváltozásokról 5. Tekintettel arra, hogy az átfedési integrál hőmérsékletfüggése torzíthatja az f paramétert, az f értékét minden hőmérsékleten normáltuk a hozzá tartozó átfedési integrál értékével. 12
13 4 4 3 relatív f ' (%) Hõmérséklet ( o C) I.4. ábra. Az f paraméter hőmérsékletfüggése abban az esetben, ha a donor a katalitikus doménhez (piros körök), illetve ha az esszenciális könnyűlánc doménhez (kék körök) volt kötve. Az f paraméter hőmérsékletfüggését (I.4. ábra) vizsgálva feltűnő, hogy abban az esetben, ha a donor a katalitikus doménen helyezkedett el, az f értéke alig változik a hőmérséklet növekedésével. Ezzel szemben, ha a donor az esszenciális könnyűláncon helyezkedett el, akkor az f értéke monoton módon, és meredeken nőtt. A módszer értelmében: ha f hőmérsékletfüggése meredekebb a fehérjemátrix flexibilisebb (ha nem következik be lényeges konformációváltozás.) Ennek alapján azt a következtetést vonhatjuk le, hogy a donor és az akceptorok között elhelyezkedő fehérjemátrix flexibilisebb az esszenciális könnyűlánc és az aktin között, mint a katalitikus domén és az aktin között. Felidézve azt, hogy a katalitikus domén esetében a távolságeloszlás félértékszélessége nagyon keskeny, f értéke pedig a teljes hőmérséklettartományon közel állandó és nincs konformációváltozás, arra következtethetünk, hogy nukleotidmentes állapotban a katalitikus domén és az aktin kötése erős, a két jelölő közötti fehérjemátrix merev. Az esszenciális könnyűlánc esetében megfigyeltek alapján ugyanakkor kijelenthető: az f paraméter meredek hőmérsékletfüggése arra utal, hogy a donor és az akceptorok közötti fehérjemátrix flexibilis. Az f paraméter mérésével sikerült kizárni 13
14 annak a lehetőségét, hogy a könnyűlánc-kötő domén esetében megfigyelt széles távolságeloszlás oka egy nagyszámú, de egyenként merev fehérjemátrix. Összefoglalás Sikerült kidolgoznunk egy olyan fluoreszcencia rezonancia energiatranszfer mérésen alapuló módszert, amely helikális szimmetriával rendelkező rendszerek esetén távolságeloszlások meghatározására lehet használni. A módszert a gyakorlatba ültettük, és azt az aktomiozin komplex esetében használtuk. Az eljárás segítségével kvantitatív képet kaptunk a miozin-s1 katalitikus, illetve könnyűlánc-kötő doménjének az aktin filamentumhoz viszonyított elhelyezkedéséről. A távolságeloszlások feltételezésével kvantitatív képet kaptunk a katalitikus domén és a könnyűlánc-kötő domén flexibilitásáról is. Az f paraméter hőmérsékletfüggésének mérésén alapuló módszer alkalmazásával pontosítottuk a fent említett módszer által kapott távolságeloszlások jelentését. Ennek megfelelően a katalitikus domén erős kötésben van az aktin filamentummal, a könnyűlánc-kötő domén viszont erősen fluktuál az aktin filamentumhoz képest. Méréseink megerősítik azokat a korábbi megfigyeléseket 11, amelyek szerint a katalitikus domén és a könnyűlánc-kötő domén el tud fordulni egymáshoz képest. 14
15 2. A fotoliáz fotoaktivációjának vizsgálata femtoszekundumos tranziens abszorpciós mérések segítségével Bevezetés A fotoliáz UV fény hatására a DNS-ben a szerkezet kémiai megváltozásához vezető fotoreakciók zajlanak le. Ezek közül a két legismertebb a ciklobután pirimidin dimer (Pyr<>Pyr) illetve a pirimidin-pirimidon(6-4) (Pyr[6-4]Pyr) kialakulása, amelynek során két egymást követő timin primidin gyűrűi kapcsolódnak egybe. Vizsgálatunk középpontjában a fotoliáz nevű enzim működése állt, amely képes arra, hogy fotokémiailag katalizálja a DNS hibákat javító reakciót 13. A fotoliáz a flavoproteinek családjába tartozik, amelyek esetében a flavin kofaktor számos biokémiai reakcióban játszik intermedier szerepet; a flavoproteinekben található flavin kromofór jellegzetes abszorpciós spektrummal rendelkezik UV és látható hullámhosszokon egyaránt; legtöbbjük esetében a fiziológiai funkciót nem befolyásolja a fényabszorpció. A fotoliáz ebből a szempontból kivételt képez, az enzim működését ugyanis és ennek következtében a DNS-szál javítását egy UV/látható foton abszorpciója katalizálja. A javítási ciklus során a hibás DNS-hez specifikusan kapcsolódott fotoliáz kétszeresen redukált állapotban levő flavin kofaktora (FADH ) egy elektront injektál a pirimidin dimerre, aminek következtében a kötés felhasad. A fotoliázokat a javított terméktől függően ciklobután pirimidin dimer fotoliázok, a II-es típusú fotoliázok pedig a (6-4) fototermékek javítását végzik el. A fotoliázok olyan aminosavból álló globuláris, monomer fehérjék, amelyek két nemkovalensen kötött kofaktort tartalmaznak. Ezek közül az egyik az eddig ismert típusok mindegyikében a flavin adenin dinukleotid (FAD), a második pedig vagy egy pterin (MTHF), vagy egy deazaflavin (8-HDF) kromofór. A flavin az egyik leggyakrabban előforduló kofaktor (legkevesebb 151 enzim tartalmazza FAD és/vagy FMN formában), a fotoliázban a FAD formája található meg, három redox állapotban: oxidált, egy elektronnal redukált illetve két elektronnal redukált állapotban. A fotoliáz esszenciális kofaktora, a flavin 14-16, a katalízis során 15
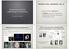
16 specifikusan kötődik a sérült DNS szakaszhoz. DNS javítására a flavin csak a kétszeresen redukált FADH állapotában alkalmas. Vizsgálataink tárgya az a folyamat fotoaktiváció volt, amelynek során a flavin a kétszeresen redukált FADH állapotba kerül. II.1. ábra. Az E. coli fotoliáz szerkezete. MTHF fotoantenna (kék), FAD kofaktor (piros), a fotoaktivációban fontos szerepet betöltő három triptofán (lila). A fotoliáz másik kofaktora az általunk vizsgált esetben az MTHF kromofór, amit fotoantennának is neveznek (az A. Nidulans, illetve T. Thermophilus fotoliázok esetében 8-HDF). A katalízis az enzim-szubsztrát kötésre hatást nem gyakorló MTHF illetve 8- HDF kofaktorok nélkül is végbemegy 17, 18, jelenlétük azonban jelentősen ( szoros mértékben) megnöveli a javítás sebességét 13. Ez annak köszönhető, hogy az MTHF vagy 8-HDF kofaktorok extinkciós maximuma (400 nm körül) jelentősen nagyobb, mint az FADH kofaktoré, az így abszorbeált energia pedig szintén eljut fluoreszcencia rezonancia energiatranszferrel a flavin kofaktorhoz 17,
17 Fotoreaktiváció illetve fotoaktiváció az E. coli fotoliázban A fotoliázban két fotoindukált elektrontranszfer folyamat megy végbe: a DNS javítást végző fotoreaktiváció illetve a flavin kofaktort redukáló fotoaktiváció. A fotoreaktiváció során egy közeli UV/látható foton által indukált folyamat zajlik le, amelynek során a ciklobután-pirimidin kötés felhasad. A reakció mechanizmusa a következő: a pirimidin dimerhez kötődött fotoliáz antennája (MTHF) elnyel egy UV/kék fotont, majd fluoreszcencia rezonancia energiatranszferrel gerjeszti a kétszeresen redukált állapotban található FADH -t (a flavin gerjesztése közvetlenül is megtörténhet). A gerjesztett állapotban levő FADH -ról ~170 ps alatt egy elektron ugrik a Pyr <> Pyr gyűrűre 22. Mivel a ciklobután 5-5 és 6-6 kötései ezt követően már sértik a Hückel-szabályt, ennek megfelelően a Pyr <> Pyr felbomlik két pirimidinre. Ezt követően az elektron ~560 ps alatt visszatranszferálódik a félig redukálódott flavinra, amely ennek következtében újra a teljesen redukálódott FADH állapotba kerül. Egy kivétellel az összes eddig izolált fotoliázban igaz az, hogy a flavin kofaktor alapesetben az FADH állapotban található meg. Ahhoz azonban, hogy a fotoreaktiváció végbemenjen, a flavin kofaktornak a kétszeresen redukált FADH állapotban kell lennie. A fotoliázban végbemegy egy második fotoreakció is, amelynek során külső redukálószer jelenlétében az FADH redukálódik, és a katalitikusan aktív FADH állapotba kerül. A folyamat neve ennek megfelelően fotoaktiváció. Az E. coli -ból származó fotoliáz esetében mint azt a továbbiakban részletesen tárgyalni fogom az FADH redukálása egy három tagból álló triptofán láncon (W382- W359-W306) keresztül haladó elektrontranszfer segítségével valósul meg 23 (II.2. ábra), amelynek során a terminális elektron-donor a flavin kofaktortól 15 Ǻ távolságban elhelyezkedő, oldószerrel kölcsönhatásban álló W306-os triptofán 24. A W306 redukálása egy külső elektron donorral stabilizálja a flavin kofaktor FADH állapotát, külső elektron donor hiányában a töltés rekombináció következtében a kofaktor visszakerül az FADH állapotba 23,
18 2. Célkitűzések Vizsgálataim során a W382-W359-W306 triptofánlánc mentén végbemenő elektrontranszfer folyamat részletesebb megértését tűztem ki célul. Kollégáim korábbi munkája, amelynek során mutagenezissel egy a triptofánhoz hasonló geometriájú, de redoxsemleges fenilanalinnel cserélték ki a W382-es triptofánt igazolta az a feltételezést, hogy a fotoaktiváció első lépéseként a W382-es triptofánról egy elektron ugrik a flavin kofaktorra. A mérések elkezdésekor tehát a következő kérdések megválaszolását tűztem ki célul: 1) Megfigyelhető-e a flavin kofaktor redukálódása abban az esetben, ha a W359-es triptofánt a hasonló geometriájú, de redox inert fenilanalinre cseréljük? 2) Létrejön-e a W359 W382 elektrontranszfer lépés a fotoaktiváció során? 3) Milyen gyors a W359 W382 elektrontranszfer folyamat? 18
19 Alkalmazott módszerek Vizsgálataimat a pumpa-próba módszerrel megvalósított tranziens abszorpciós mérésekkel végeztem. A tranziens abszorpciós pumpa-próba rendszer alapelve könnyen megérthető a következő ábrából: a gerjesztő pumpa impulzust követően, a mintát meghatározott időpontokban, úgynevezett próbaimpulzusokkal világítjuk meg, és detektáljuk a minta transzmisszióját. A vázolt tranziens abszorpciós berendezés (II.2. ábra) tehát néhány femtoszekundumos időközönként méri az abszorpcióváltozást, ennek megfelelően a femtoszekundumos időskálán lezajló abszorpciós változások mérésére alkalmas. II.2. ábra. A tranziens abszorpciós elrendezés illetve a mért görbe. (Forrás:Vos M H, ) A detektált abszorpcióváltozás mögött a következő jelenségek húzódhatnak meg: 1. Kifehéredés vagy bleaching. 2. Stimulált emisszió. 3. Fotoindukált abszorpció vagy gerjesztett állapoti abszorpció ( excited state absorption, ESA). 19
20 Eredmények és következtetések A három triptofán elektrontranszferben betöltött szerepének vizsgálata érdekében a triptofánokat mutagenezissel egyenként egy hasonló geometriájú, de az elektrontranszfer szempontjából inert fenilanalinre cseréltük (W382F, W359F). Kollégáimnak a W382F mutánson végzett kísérletei 25 tisztázták a kofaktorhoz legközelebb álló triptofán (W382) szerepét az elektron transzfer folyamatban, illetve az FADH * állapot saját relaxációs idejét. A vad típus esetében a sebességi állandó (24 ps) -1 körül, míg a mutáns esetében (80 ps) -1 körül adódott a teljes mért spektrális tartományon. A mutáns esetében megfigyelt hosszabb relaxációs idő arra utal, hogy nem jön létre elektrontranszfer, vagyis a W382-es triptofán az elsődleges elektron donor. A mutáns esetében megfigyelt (80 ps) -1 körüli lecsengés az FADH * saját relaxációs idejének felel meg. A vad típusnál megfigyelt 30 ps körüli relaxációs idő ennek megfelelően két kompetitív folyamat az FADH * állapot elektrontranszfer következtében megvalósuló, illetve saját relaxációjának eredménye. Ennek megfelelően az elsődleges elektron transzfer lépés mintegy ps alatt megy végbe. A kísérleteket ezúttal is két részletben végeztük: a nm közötti tranziens abszorpciós mérésekhez 620 nm-es pumpa impulzust alkalmaztunk, a nm közötti tartományban végzett mérésekhez pedig 550 nm-es pumpaimpulzust használtunk. A nm-en kapott eredményeket vizsgálva megfigyelhető, hogy a mutáns esetében az abszorpcióváltozás kinetikája egyezést mutat a vad típusban megfigyelttel. Mivel ezen a tartományon az abszorpcióváltozást csak az FADH * állapot befolyásolja, a sebességi állandók egyezéséből azt a következtetést lehet levonni, hogy a mutáns W359F fotoliázban a gerjesztett flavin kofaktor a vad típusnál megismert módon, vagyis elektron transzferrel relaxálódik. A másik tartományt ( nm) vizsgálva, ahol fotoindukált abszorpció lép fel az enzimben, mind a vad típus, mind a mutáns esetében hasonló kinetikát figyelhetünk meg: 434 nm-en a gerjesztett állapot relaxációjának sebességi állandója szintén ~30 ps. A nm tartományban a relaxáció élettartama az előzőekhez hasonlóan mind a vad típus, mind a mutáns esetében ~30 ps. Feltűnő különbség azonban, hogy amíg a vad típusban 150 ps után is marad abszorpciókülönbség, ez a mutáns esetében gyakorlatilag teljesen eltűnik (II.3. ábra). 20
21 0,5 0,0 ΔAbszorpció (10-3 ) -0,5-1,0-1,5-2,0-2,5 W359F (468 nm) W359F WT t (ps) II.3. ábra. Az abszorpcióváltozás kinetikája a vad típus (teli körök) és a mutáns esetében (négyzetek). Üres körökkel ábrázoltuk az izobesztikus pontban mért abszorpcióváltozást. A vad típus tranziens spektrumait elemezve látszik, hogy a 145 ps-os mérési ablakban a minta gyakorlatilag felveszi a t= időpillanathoz tartozó nyugalmi vagy végső spektrumot, amely az FADH W + állapotnak feleltethető meg. A mutáns esetében ez a karakterisztikus spektrum azonban eltűnik: a 145 pikoszekundumos késleltetés esetén mért abszorpcióváltozás (ennek megfelelően a végső aszimptotikus spektrum is) a vizsgált spektrális tartományon gyakorlatilag nulla (II.4 ábra). 4 A gerjesztett állapot abszorpciója WT 4 4 W359F W359F ΔAbsorpció (10-3 ) ps 15 ps 45 ps 145 ps Az FADH o abszorpciójának kifehéredése ΔAbszorpció (10-3 ) ΔAbsorpció (10-3 ) Hullámhossz (nm) initial final 2 ps 15 ps 45 ps 145 ps Hullámhossz (nm) Hullámhossz (nm) II.4. ábra Vad típusú (WT) és mutáns (W359F) fotoliáz tranziens abszorpciós spektruma különböző késleltetések esetén. 21
22 A kinetikai eredményeket és a tranziens spektrumok kapcsán megfigyelteket egybevetve a következő megállapításokat tehetjük: a ~30 ps relaxációs idő a töltésszétválasztás létrejöttére utal, ellenkező esetben a W382F mutáns fotoliáz esetében megfigyelt 80 ps körüli relaxációs időt kellett volna visszakapnunk. A t= időpillanathoz tartozó spektrum, a W382F esetében megfigyeltekhez hasonlóan az FADH W + állapot hiányára utal a W359F-ben. Összegezve tehát, a kapott eredmények arra utalnak, hogy bár az elsődleges transzfer lépés a W382-es triptofánról a flavin kofaktorra megtörténik, a flavin nem marad a kétszeresen redukált FADH állapotban, vagyis a kezdeti töltésszétválasztást követően egy gyors töltés-visszarendeződésnek kell bekövetkeznie. A reakciómechanizmust leíró differenciál-egyenletrendszer megoldásával, illetve a mérések során kapott sebességi állandók behelyettesítésével sikerült megbecsülnünk ennek a töltés rekombinációnak a felső határát, amely 4 ps körül adódott. 22
23 Összefoglalás Méréseim eredményeit tehát a következőkben lehet összegezni: 1) Sikerült igazolnom, hogy a W359 triptofánnak a redox semleges fenilanalinre cserélése megakadályozza azt az elektrontranszfer folyamatot, amelynek következtében a flavin kofaktor redukált állapotba kerül. A W359F esetében ugyanis a flavin kofaktor nem marad redukált állapotban, amiből arra következtettünk, hogy a triptofán-fenilanalin cserével blokkoltuk a flavin kofaktor redukáláshoz szükséges elektrontranszfert. 2) Sikerült fényt derítenem arra, hogy a W359F fotoliázban, több ismert flavoproteinhez hasonlóan, a flavin gerjesztett állapota egy rövid élettartamú oxidáció által relaxálódik. 3) Méréseim bizonyítékot szolgáltattak arra is, hogy a W382 FADH * elektrontranszfer lépés elengedhetetlen a W359-es (és valószínűleg a W306-os) triptofán oxidálásához. 4) Sikerült megbecsülnöm a másodlagos elektrontranszfer lépés kinetikáját: az FADH W382 + állapotot megvalósító töltésszétválasztást egy gyors elektrontranszfer lépés követi (W359 W382 + ) <4 ps alatt. 23
24 Irodalomjegyzék 1. Spudich, J. A. & Watt, S. The regulation of rabbit skeletal muscle contraction. J. Biol. Chem. 246, (1971). 2. Taylor, D. L., Reidler, J., Spudich, J. A. & Stryer, L. Detection of Actin Assembly by Fluorescence Energy-Transfer. Journal of Cell Biology 89, (1981). 3. Nyitrai, M., Hild, G., Bodis, E., Lukacs, A. & Somogyi, B. Flexibility of myosinsubfragment-1 in its complex with actin as revealed by fluorescence resonance energy transfer. European Journal of Biochemistry 267, (2000). 4. Gennis, R. B. & Cantor, C. R. Use of nonspecific dye labeling for singlet energytransfer measurements in complex systems. A simple model. Biochemistry 11, (1972). 5. Somogyi, B. et al. Förster-type energy transfer as a probe for changes in local fluctuations of the protein matrix. Biochemistry 23, (1984). 6. Nyitrai, M., Hild, G., Lukacs, A., Bodis, E. & Somogyi, B. Conformational distributions and proximity relationships in the rigor complex of actin and myosin subfragment-1. Journal of Biological Chemistry 275, (2000). 7. Takashi, R. Fluorescence energy transfer between subfragment-1 and actin points in the rigor complex of actsubfragment-1. Biochemistry 18, (1979). 8. Trayer, H. R. & Trayer, I. P. Fluorescence energy transfer between the myosin subfragment-1 isoenzymes and F-actin in the absence of nucleotides. Eur. J. Biochem. 135, (1983). 9. Xing, J. & Cheung, H. C. Internal movement in myosin subfragment-1 detected by fluorescence resonance energy transfer. Biochemistry 34, (1995). 10. Miki, M. & Wahl, P. Fluorescence energy transfer between points in actosubfragment-1 rigor complex. Bichim. Biophys. Acta 790, (1984). 11. Rooparine, O., Szent-Györgyi, A. G. & Thomas, D. D. Microsecond rotational dynamics of spin-labeled myosin regulatory light-chian induced by relaxation and contraction of scallop muscle. Biochemistry 37, (1998). 12. Adhikari, B., Hideg, K. & Fajer, P. G. Independent mobility of catalytic and regulatory domains of myosin heads. Proc. Natl. Acad. Sci. USA 94, (1997). 13. Sancar, A. Structure and Function of DNA Photolyase and Cryptochrome Blue-Light Photoreceptors. Chem. Rev. 103, (2003). 14. Sancar, G. B. et al. Action Mechanism of Escherichia-Coli DNA Photolyase.3. Photolysis of the Enzyme-Substrate Complex and the Absolute Action Spectrum. Journal of Biological Chemistry 262, (1987). 15. Heelis, P. F. & Sancar, A. Photochemical properties of Escherichia coli DNA photolyase: a flash photolysis study. Biochemistry 25, (1986). 16. Jorns, M. S., Baldwin, E. T., Sancar, G. B. & Sancar, A. Action Mechanism of Escherichia-Coli DNA Photolyase.2. Role of the Chromophores in Catalysis. Journal of Biological Chemistry 262, (1987). 17. Heelis, P. F., Payne, G. & Sancar, A. Photochemical Properties of Escherichia-Coli DNA Photolyase - Selective Photodecomposition of the 2Nd Chromophore. Biochemistry 26, (1987). 18. Jorns, M. S., Wang, B. & Jordan, S. P. DNA-Repair Catalyzed by Escherichia-Coli DNA Photolyase Containing Only Reduced Flavin - Elimination of the Enzymes 2Nd 24
25 Chromophore by Reduction with Sodium-Borohydride. Biochemistry 26, (1987). 19. Payne, G. & Sancar, A. Absolute Action Spectrum of E-Fadh2 and E-Fadh2-Mthf Forms of Escherichia-Coli DNA Photolyase. Biochemistry 29, (1990). 20. Jorns, M. S., Wang, B. Y., Jordan, S. P. & Chanderkar, L. P. Chromophore Function and Interaction in Escherichia-Coli DNA Photolyase - Reconstitution of the Apoenzyme with Pterin and or Flavin Derivatives. Biochemistry 29, (1990). 21. Lipman, R. S. A. & Jorns, M. S. Direct Evidence for Singlet Singlet Energy-Transfer in Escherichia-Coli DNA Photolyase. Biochemistry 31, (1992). 22. Kao, Y. T., Saxena, C., Wang, L. J., Sancar, A. & Zhong, D. P. Direct observation of thymine dimer repair in DNA by photolyase. Proceedings of the National Academy of Sciences of the United States of America 102, (2005). 23. Aubert, C., Vos, M. H., Mathis, P., Eker, A. P. M. & Brettel, K. Intra-protein radical transfer during photoactivation of DNA photolyase. Nature 405, (2000). 24. Li, Y. F., Heelis, P. F. & Sancar, A. Active site of DNA photolyase: tryptophan-306 is the intrinsic hydrogen atom donor essential for flavin radical photoreduction and DNA repair in vitro. Biochemistry 30, (1991). 25. Byrdin, M., Eker, A. P. M., Vos, M. H. & Brettel, K. Dissection of the triple tryptophan electron transfer chain in Escherichia coli DNA photolyase: Trp382 is the primary donor in photoactivation. Proc. Natl. Acad. Sci. U.S.A. 100, (2003). 26. Vos, M. H. & Martin, J.-L. Femtosecond processes in proteins. Biochim. Biophys. Acta 1411, 1-20 (1999). 25
26 Publikációk Az értekezés alapjául szolgáló saját közlemények 1. Nyitrai, M., G. Hild, B. Bódis, A. Lukács és B. Somogyi. Flexibility of Myosin- Subfragment-1 in its Complex with Actin as Revealed by Fluorescence Resonance Energy Transfer. Eur J Biochem 267(14): , IF: Nyitrai, M., G. Hild, A. Lukács, E. Bódis és B. Somogyi. Conformational distributions and proximity relationships in the rigor complex of actin and myosin subfragment-1. J Biol Chem 275(4): , IF: Lukacs, A., A.P.M. Eker, M. Byrdin, S. Villette, J. Pan, K. Brettel és M.H. Vos. Role of the Middle Residue in the Triple Tryptophan Electron Transfer Chain of DNA Photolyase: Ultrafast Spectroscopy of a Trp-->Phe Mutant. J Phys Chem B 110, , IF: 4,033 Összesített impakt faktor: 14,140 Az értekezés alapjául szolgáló saját poszterek, előadások 1. Lukács A., Nyitrai M., Hild G., Bódis E. és Somogyi B.. A miozin és az aktin relatív pozíciója az akto-miozin komplexen belül: fluoreszcencia rezonancia energiatranszfer folyamatok számítógépes szimulációja. XXIX. Membrántranszport Konferencia, Sümeg, Lukács A., Nyitrai M., Halasi S., Bódis E. és Somogyi B. Fluoreszcencia élettartam mérési eredmények kiértékelésének alternatív módszerei: a fluoreszcencia emisszió sebességi állandójának alkalmazása fázisfluorimetriás adatok kiértékelése során. XIX. Biofizikai Vándorgyűlés, Kecskemét, Nyitrai, M., G. Hild, A. Lukács, E. Bódis, S. Halasi és B. Somogyi. The dynamic and conformational properties of the catalytic and light-chain-binding domains of S1 in the acto-myosin complex. 5th Symposium on Instrumental Analysis, Graz, Austria, Nyitrai M., Hild G., Bódis E., Halasi S., Lukács A. és Somogyi B. Az akto-miozin komplex flexibilitása rigor és ADP állapotokban: fluoreszcencia rezonancia energiatranszfer vizsgálatok. XXII. Országos Lumineszcencia-Spektroszkópia Konferencia, Pécs,
27 5. Nyitrai M., Hild G., Lukács A., Bódis E., Halasi S. és Somogyi B. A miozin S1 katalitikus es könnyu-lánc-kötő doménjeinek dinamikai tulajdonságai akto-miozin komplexben. XIX. Biofizikai Vándorgyulés, Kecskemét, Nyitrai, M., G. Hild, A. Lukács, E. Bódis, S. Halasi és B. Somogyi. The dynamic and conformational properties of the catalytic and light-chain-binding domains of S1 in the acto-myosin complex. XXVIII. European Muscle Congress, York, UK, Somogyi, B., M. Nyitrai, G. Hild, A. Lukács és E. Bódis. The dynamic and conformational properties of the catalytic and light-chain-binding domains of S1 in the acto-myosin complex. 44th Annual Meeting of the American Biophysical Society, New Orleans, USA, Lukács, A., M. Nyitrai, E. Bódis, G. Hild és B. Somogyi. The effect of ADP on the flexibility and conformation of myosin-subfragment-1 in its complex with actin XXX. European Muscle Conference, Pavia, Italy, Lukács, A., M. Nyitrai, J. Gallay, M. Vincent, E. Bódis és B. Somogyi. Nucleotide induced flexibility of acto-s1 complex revealed by fluorescence spectroscopy 10th European Conference on the Spectroscopy of Biological Molecules, Szeged, Lukacs, A., M.H. Vos, A.P.M. Eker, M. Byrdin és K. Brettel. Mechanism of radical transfer during photoactivation of the flavoprotein DNA photolyase 15 th International Conference on Ultrafast Phenomena, Pacific Grove, California, USA, 2006 Egyéb saját közlemények 1. Nyitrai, M., G. Hild, A. Lukács, J. Belágyi és B. Somogyi. The flexibility of actin filaments as revealed by fluorescence resonance energy transfer: the influence of divalent cations, J. Muscle Res. Cell M., Vol 20, 1, 1999 IF: Somogyi, B., M. Nyitrai, G. Hild, A. Lukács és E. Bódis The dynamic and conformational properties of the catalyitic and light-chain-binding domains of S1 in the acto-myosin complex, Biophys. J. Vol 78, Number 1, 2000 IF: Lukács, A., M. Nyitrai, E. Bódis, G. Hild és B. Somogyi. The effect of ADP on the flexibility and conformation of myosin-subfragment-1 in its complex with actin J Muscle Res Cell Motil, 22(7):563, IF:
28 Könyvfejezetek 1. Lukacs, A., M.H. Vos, A.P. M. Eker, M. Byrdin és K. Brettel. Mechanism of radical transfer during photoactivation of the flavoprotein DNA photolyase Ultrafast Phenomena XV, Springer Series in Chemical Physics, Lukács, A., Z. Várallyay és R. Szipőcs. Cubic phase distortion of single attosecond pulses being reflected on narrowband Mo/Si filtering mirrors. Trends in Optics and Photonics Series, Vol 98, p , Rozsa, B., E.S. Vizi, G. Katona, A. Lukács, Z. Várallyay, A. Sághy, L. Valenta, P. Maák, J. Fekete, Á. Bányász és R. Szipőcs. Real time 3D nonlinear microscopy. Trends in Optics and Photonics Series, Vol 98, p ,
Ph.D. ÉRTEKEZÉS TÉZISEI
 Ph.D. ÉRTEKEZÉS TÉZISEI Funkcionális fehérjedinamikai vizsgálatok fluoreszcencia és femtoszekundumos időfelbontású tranziens abszorpciós spektroszkópiai módszerekkel Lukács András Pécsi Tudományegyetem
Ph.D. ÉRTEKEZÉS TÉZISEI Funkcionális fehérjedinamikai vizsgálatok fluoreszcencia és femtoszekundumos időfelbontású tranziens abszorpciós spektroszkópiai módszerekkel Lukács András Pécsi Tudományegyetem
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
Biofizika I 2013-2014 2014.12.02.
 ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
Komplex egyszerű Aktin alapú mikrofilamentum rsz. Hogyan vizsgálhatunk folyamatokat? Komplex egyszerű S E J T
 Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
Biofizikai módszerek a citoszkeleton vizsgálatára I. Kinetikai, steady-state módszerek, spektroszkópiai vizsgálatok Komplex egyszerű S E J T A citoszkeletális rendszer Orbán József, 213 Április Aktin citoszkeleton
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
Sejt. Aktin működés, dinamika plus / barbed end pozitív / szakállas vég 1. nukleáció 2. elongáció (hosszabbodás) 3. dinamikus egyensúly
 Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Biofizikai módszerek a citoszkeleton vizsgálatára I: Kinetikai és steady-state spektroszkópiai módszerek Sejt Citoszkeletális rendszerek Orbán József, 2014 április Institute of Biophysics Citoszkeleton:
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Tartalomjegyzék. Emlékeztetõ. Emlékeztetõ. Spektroszkópia. Fényelnyelés híg oldatokban A fény; Abszorpciós spektroszkópia
 Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2015 január 27.) Az abszorpció mérése;
Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2015 január 27.) Az abszorpció mérése;
Abszorpció, emlékeztetõ
 Hogyan készültek ezek a képek? PÉCI TUDMÁNYEGYETEM ÁLTALÁN RVTUDMÁNYI KAR Fluoreszcencia spektroszkópia (Nyitrai Miklós; február.) Lumineszcencia - elemi lépések Abszorpció, emlékeztetõ Energia elnyelése
Hogyan készültek ezek a képek? PÉCI TUDMÁNYEGYETEM ÁLTALÁN RVTUDMÁNYI KAR Fluoreszcencia spektroszkópia (Nyitrai Miklós; február.) Lumineszcencia - elemi lépések Abszorpció, emlékeztetõ Energia elnyelése
Tartalomjegyzék. Emlékeztetõ. Emlékeztetõ. Spektroszkópia. Fényelnyelés híg oldatokban 4/11/2016. A fény; Abszorpciós spektroszkópia
 Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2016 március 1.) Az abszorpció mérése;
Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2016 március 1.) Az abszorpció mérése;
Abszorpciós spektroszkópia
 Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Speciális fluoreszcencia spektroszkópiai alkalmazások. Emlékeztető: az abszorpció definíciója. OD = A = - log (I / I 0 ) = ε (λ) c x
 Speciális fluoreszcencia spektroszkópiai alkalmazások Nyitrai Miklós; 2011 február 21. FRET Emlékeztető: az abszorpció definíciója I 0 I anyag OD = A = - log (I / I 0 ) = ε (λ) c x Röv: optical density
Speciális fluoreszcencia spektroszkópiai alkalmazások Nyitrai Miklós; 2011 február 21. FRET Emlékeztető: az abszorpció definíciója I 0 I anyag OD = A = - log (I / I 0 ) = ε (λ) c x Röv: optical density
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
BIOMECHANIKA 2 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI MOLEKULÁRIS MOZGÁS MOTORFEHÉRJÉK DR. BUGYI BEÁTA - BIOFIZIKA ELŐADÁS PÉCSI TUDOMÁNYEGYETEM
A módszerek jelentősége. Gyors-kinetika módszerek. A módszerek közös tulajdonsága. Milyen módszerekről tanulunk?
 Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
Lumineszcencia spektrometria összefoglaló
 Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
Bevezetés a fluoreszcenciába
 Bevezetés a fluoreszcenciába Gerjesztett Excited Singlet szingulett Manifold állapot S1 Jablonski diagram Belső internal konverzió conversion S2 k isc k -isc Triplett állapot Excited Triplet Manifold T1
Bevezetés a fluoreszcenciába Gerjesztett Excited Singlet szingulett Manifold állapot S1 Jablonski diagram Belső internal konverzió conversion S2 k isc k -isc Triplett állapot Excited Triplet Manifold T1
Kémiai Intézet Kémiai Laboratórium. F o t o n o k k e r e s z tt ü z é b e n a D N S
 Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
Szerves oldott anyagok molekuláris spektroszkópiájának alapjai
 Szerves oldott anyagok molekuláris spektroszkópiájának alapjai 1. Oldott molekulában lejátszódó energetikai jelenségek a Jablonski féle energia diagram alapján 2. Példák oldatok abszorpciójára és fotolumineszcenciájára
Szerves oldott anyagok molekuláris spektroszkópiájának alapjai 1. Oldott molekulában lejátszódó energetikai jelenségek a Jablonski féle energia diagram alapján 2. Példák oldatok abszorpciójára és fotolumineszcenciájára
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Kollár Veronika
 A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
A harántcsíkolt izom szerkezete, az izommőködés és szabályozás molekuláris alapjai Kollár Veronika 2010. 11. 11. Az izom citoszkeletális filamentumok és motorfehérjék rendezett összeszervezıdésébıl álló
Abszorpciós fotometria
 abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
Lumineszcencia spektroszkópia
 Lumineszcencia spektroszkópia Elektron+vibrációs+rotációs-spektroszkópia alapjai 213. február Fizika-Biofizika II. szemeszter Orbán József PTE ÁOK Biofizikai Intézet Definíciók, törvények SPEKTROSZKÓPIAI
Lumineszcencia spektroszkópia Elektron+vibrációs+rotációs-spektroszkópia alapjai 213. február Fizika-Biofizika II. szemeszter Orbán József PTE ÁOK Biofizikai Intézet Definíciók, törvények SPEKTROSZKÓPIAI
 RÉSZLETES BESZÁMOLÓ Az OTKA által támogatott konzorcium működésében az Uzsoki utcai Kórház feladata a szövetminták gyűjtése, előzetes feldolgozása, ill. a betegek utánkövetése, valamint az utánkövétésre
RÉSZLETES BESZÁMOLÓ Az OTKA által támogatott konzorcium működésében az Uzsoki utcai Kórház feladata a szövetminták gyűjtése, előzetes feldolgozása, ill. a betegek utánkövetése, valamint az utánkövétésre
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
A MITOKONDRIÁLIS CITOKRÓM C POSZTTRANSZLÁCIÓS ÉRÉSE. Doktori (Ph.D.) értekezés tézisei. Tenger Katalin
 A MITOKONDRIÁLIS CITOKRÓM C POSZTTRANSZLÁCIÓS ÉRÉSE Doktori (Ph.D.) értekezés tézisei Tenger Katalin Témavezető: Dr. Zimányi László Konzulens: Dr. Rákhely Gábor Biológia Doktori Iskola Szegedi Tudományegyetem
A MITOKONDRIÁLIS CITOKRÓM C POSZTTRANSZLÁCIÓS ÉRÉSE Doktori (Ph.D.) értekezés tézisei Tenger Katalin Témavezető: Dr. Zimányi László Konzulens: Dr. Rákhely Gábor Biológia Doktori Iskola Szegedi Tudományegyetem
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Lumineszcencia Fényforrások
 Kiegészítés: színkeverés Lumineszcencia Fényforrások Alapszinek additív keverése Alapszinek kiegészítő szineinek keverése: Szubtraktív keverés Fidy udit Egyetemi tanár 2015, November 5 Emlékeztető.. Abszorpciós
Kiegészítés: színkeverés Lumineszcencia Fényforrások Alapszinek additív keverése Alapszinek kiegészítő szineinek keverése: Szubtraktív keverés Fidy udit Egyetemi tanár 2015, November 5 Emlékeztető.. Abszorpciós
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására
 Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
Tropomiozin és nehéz meromiozin hatása a formin által nukleált aktin filamentumok flexibilitására Ujfalusi Zoltán Témavezető: PROF. DR. N YITRAI MIKLÓS Doktori iskola: I n t e r d i s z c i p l i n á r
Modern Fizika Labor. A mérés száma és címe: A mérés dátuma: Értékelés: Infravörös spektroszkópia. A beadás dátuma: A mérést végezte:
 Modern Fizika Labor A mérés dátuma: 2005.10.26. A mérés száma és címe: 12. Infravörös spektroszkópia Értékelés: A beadás dátuma: 2005.11.09. A mérést végezte: Orosz Katalin Tóth Bence 1 A mérés során egy
Modern Fizika Labor A mérés dátuma: 2005.10.26. A mérés száma és címe: 12. Infravörös spektroszkópia Értékelés: A beadás dátuma: 2005.11.09. A mérést végezte: Orosz Katalin Tóth Bence 1 A mérés során egy
AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: Gyimesi Máté
 AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: AZ AKTIN KÖZVETLENÜL AZ ERŐGENERÁLÓ LÉPÉST GYORSÍTJA MIOZIN II-BEN Gyimesi Máté Témavezető: Dr. Málnási-Csizmadia András Biológia Doktori Iskola, iskolavezető: Prof.
AZ AKTIN AKTIVÁCIÓ ÚJ MECHANIZMUSA: AZ AKTIN KÖZVETLENÜL AZ ERŐGENERÁLÓ LÉPÉST GYORSÍTJA MIOZIN II-BEN Gyimesi Máté Témavezető: Dr. Málnási-Csizmadia András Biológia Doktori Iskola, iskolavezető: Prof.
Lumineszcencia spektrometria összefoglaló
 Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
Lumineszcencia spektrometria összefoglaló Ismétlés: fény (elektromágneses sugárzás) elnyelés: abszorpció elektron gerjesztés: excitáció alap és gerjesztett állapot atomi energiaszintek, energiaszintek
A fény. Abszorpciós fotometria Fluoreszcencia spektroszkópia. A fény. A spektrumok megjelenési formái. A fény kettıs természete: Huber Tamás
 A fény Abszorpciós fotometria Fluoreszcencia spektroszkópia. 2010. október 19. Huber Tamás PTE ÁOK Biofizikai Intézet E A fény elektromos térerısségvektor hullámhossz A fény kettıs természete: Hullám (terjedéskor)
A fény Abszorpciós fotometria Fluoreszcencia spektroszkópia. 2010. október 19. Huber Tamás PTE ÁOK Biofizikai Intézet E A fény elektromos térerısségvektor hullámhossz A fény kettıs természete: Hullám (terjedéskor)
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Név... intenzitás abszorbancia moláris extinkciós. A Wien-féle eltolódási törvény szerint az abszolút fekete test maximális emisszióképességéhez
 A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Biomolekuláris szerkezeti dinamika
 Kísérletek, mérések célja Biomolekuláris szerkezeti dinamika Kellermayer Miklós Biomolekuláris szerkezet és működés pontosabb megismerése (folyamatok, állapotok, átmenetek, kölcsönhatások, stb.) Rádióspektroszkópiák
Kísérletek, mérések célja Biomolekuláris szerkezeti dinamika Kellermayer Miklós Biomolekuláris szerkezet és működés pontosabb megismerése (folyamatok, állapotok, átmenetek, kölcsönhatások, stb.) Rádióspektroszkópiák
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia. 2008. május 6.
 Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia Értékelés: A beadás dátuma: 28. május 13. A mérést végezte: 1/5 A mérés célja A mérés célja az
Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia Értékelés: A beadás dátuma: 28. május 13. A mérést végezte: 1/5 A mérés célja A mérés célja az
Abszorpciós fotometria
 A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
PhD értekezés. Az aktin konformációs és dinamikai tulajdonságainak tanulmányozása fluoreszcencia spektroszkópiás módszerekkel. dr.
 PhD értekezés Az aktin konformációs és dinamikai tulajdonságainak tanulmányozása fluoreszcencia spektroszkópiás módszerekkel dr. Hild Gábor Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai
PhD értekezés Az aktin konformációs és dinamikai tulajdonságainak tanulmányozása fluoreszcencia spektroszkópiás módszerekkel dr. Hild Gábor Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai
Nemzetközi folyóiratban megjelent tudományos közlemények, könyvfejezet
 PUBLIKÁCIÓS LISTA Nemzetközi folyóiratban megjelent tudományos közlemények, könyvfejezet Papp, G., Bugyi, B., Ujfalusi, Z., Halasi, Sz. and Orbán, J.: The effect of ph on the thermal stability of α-actin
PUBLIKÁCIÓS LISTA Nemzetközi folyóiratban megjelent tudományos közlemények, könyvfejezet Papp, G., Bugyi, B., Ujfalusi, Z., Halasi, Sz. and Orbán, J.: The effect of ph on the thermal stability of α-actin
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Compton-effektus. Zsigmond Anna. jegyzıkönyv. Fizika BSc III.
 Compton-effektus jegyzıkönyv Zsigmond Anna Fizika BSc III. Mérés vezetıje: Csanád Máté Mérés dátuma: 010. április. Leadás dátuma: 010. május 5. Mérés célja A kvantumelmélet egyik bizonyítékának a Compton-effektusnak
Compton-effektus jegyzıkönyv Zsigmond Anna Fizika BSc III. Mérés vezetıje: Csanád Máté Mérés dátuma: 010. április. Leadás dátuma: 010. május 5. Mérés célja A kvantumelmélet egyik bizonyítékának a Compton-effektusnak
Abszorpciós fotometria
 abszorpció A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2013. január Elektromágneses hullám Transzverzális hullám elektromos térerősségvektor hullámhossz E B x mágneses térerősségvektor
abszorpció A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2013. január Elektromágneses hullám Transzverzális hullám elektromos térerősségvektor hullámhossz E B x mágneses térerősségvektor
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Koherens lézerspektroszkópia adalékolt optikai egykristályokban
 Koherens lézerspektroszkópia adalékolt optikai egykristályokban Kis Zsolt MTA Wigner Fizikai Kutatóközpont H-1121 Budapest, Konkoly-Thege Miklós út 29-33 2015. június 8. Hogyan nyerjünk információt egyes
Koherens lézerspektroszkópia adalékolt optikai egykristályokban Kis Zsolt MTA Wigner Fizikai Kutatóközpont H-1121 Budapest, Konkoly-Thege Miklós út 29-33 2015. június 8. Hogyan nyerjünk információt egyes
AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA
 Budapesti Műszaki és Gazdaságtudományi Egyetem, Fizikai Kémia Tanszék Ph.D. értekezés tézisei AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA Készítette
Budapesti Műszaki és Gazdaságtudományi Egyetem, Fizikai Kémia Tanszék Ph.D. értekezés tézisei AZ ACETON ÉS AZ ACETONILGYÖK NÉHÁNY LÉGKÖRKÉMIAILAG FONTOS ELEMI REAKCIÓJÁNAK KINETIKAI VIZSGÁLATA Készítette
PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL
![PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL PANNON EGYETEM. 2,3-DIHIDRO-2,2,2-TRIFENIL-FENANTRO-[9,10-d]-1,3,2λ 5 -OXAZAFOSZFOL KIALAKULÁSA ÉS REAKCIÓJA SZÉN-DIOXIDDAL ÉS DIOXIGÉNNEL](/thumbs/36/17536851.jpg) PA EGYETEM 2,3-DIHID-2,2,2-TIFEIL-FEAT-[9,10-d]-1,3,2λ 5 -XAZAFSZFL KIALAKULÁSA ÉS EAKCIÓJA SZÉ-DIXIDDAL ÉS DIXIGÉEL Doktori (Ph.D) értekezés tézisei Készítette: Bors István okleveles kémia-környezettan
PA EGYETEM 2,3-DIHID-2,2,2-TIFEIL-FEAT-[9,10-d]-1,3,2λ 5 -XAZAFSZFL KIALAKULÁSA ÉS EAKCIÓJA SZÉ-DIXIDDAL ÉS DIXIGÉEL Doktori (Ph.D) értekezés tézisei Készítette: Bors István okleveles kémia-környezettan
Orvosi Biofizika I. 12. vizsgatétel. IsmétlésI. -Fény
 Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Modern mikroszkópiai módszerek 2 2011 2012
 FLUORESZCENCIA MIKROSZKÓPIA A mintának a megvilágító fény által kiváltott fluoreszcencia emisszióját képezzük le. 1 Bugyi Beáta - PTE ÁOK Biofizikai Intézet 2 FLUOROFÓROK BELSŐ (INTRINSIC) FLUORESZCENCIA
FLUORESZCENCIA MIKROSZKÓPIA A mintának a megvilágító fény által kiváltott fluoreszcencia emisszióját képezzük le. 1 Bugyi Beáta - PTE ÁOK Biofizikai Intézet 2 FLUOROFÓROK BELSŐ (INTRINSIC) FLUORESZCENCIA
A fény tulajdonságai
 Spektrofotometria A fény tulajdonságai A fény, mint hullámjelenség (lambda) (nm) hullámhossz (nű) (f) (Hz, 1/s) frekvencia, = c/ c (m/s) fénysebesség (2,998 10 8 m/s) (σ) (cm -1 ) hullámszám, = 1/ A amplitúdó
Spektrofotometria A fény tulajdonságai A fény, mint hullámjelenség (lambda) (nm) hullámhossz (nű) (f) (Hz, 1/s) frekvencia, = c/ c (m/s) fénysebesség (2,998 10 8 m/s) (σ) (cm -1 ) hullámszám, = 1/ A amplitúdó
Lumineszcencia. Lumineszcencia. mindenütt. Lumineszcencia mindenütt. Lumineszcencia mindenütt. Alapjai, tulajdonságai, mérése. Kellermayer Miklós
 Alapjai, tulajdonságai, mérése Kellermayer Miklós Fotolumineszcencia Radiolumineszcencia Fotolumineszcencia Radiolumineszcencia Aurora borrealis (sarki fény) Biolumineszcencia GFP-egér Biolumineszcencia
Alapjai, tulajdonságai, mérése Kellermayer Miklós Fotolumineszcencia Radiolumineszcencia Fotolumineszcencia Radiolumineszcencia Aurora borrealis (sarki fény) Biolumineszcencia GFP-egér Biolumineszcencia
Dipoláris relaxáció vizsgálata idıbontott spektroszkópiai módszerekkel
 PhD értekezés Dipoláris relaxáció vizsgálata idıbontott spektroszkópiai módszerekkel Buzády Andrea Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet 2002 Program megnevezése: Funkcionális
PhD értekezés Dipoláris relaxáció vizsgálata idıbontott spektroszkópiai módszerekkel Buzády Andrea Pécsi Tudományegyetem Általános Orvostudományi Kar Biofizikai Intézet 2002 Program megnevezése: Funkcionális
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok december 6. 18:00 Posztoczky Károly Csillagvizsgáló, Tata Posztoczky Károly
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok december 6. 18:00 Posztoczky Károly Csillagvizsgáló, Tata Posztoczky Károly
PÉCSI TUDOMÁNYEGYETEM
 PÉCSI TUDOMÁNYEGYETEM Kémia Doktori Iskola Fehérje szerkezet és működés c. program Glicerinezett izomrostok vizsgálata ATP hidrolízis köztes állapotaiban EPR és DSC technikával PhD értekezés Degez Tímea
PÉCSI TUDOMÁNYEGYETEM Kémia Doktori Iskola Fehérje szerkezet és működés c. program Glicerinezett izomrostok vizsgálata ATP hidrolízis köztes állapotaiban EPR és DSC technikával PhD értekezés Degez Tímea
Fehérjékben lejátszódó fizikai folyamatok dinamikája kinetikus abszorpciós spektroszkópiával vizsgálva
 Fehérjékben lejátszódó fizikai folyamatok dinamikája kinetikus abszorpciós spektroszkópiával vizsgálva Ph.D. disszertáció tézisei Petro Khoroshyy Témavezető: Prof. Zimányi László Magyar Tudományos Akadémia
Fehérjékben lejátszódó fizikai folyamatok dinamikája kinetikus abszorpciós spektroszkópiával vizsgálva Ph.D. disszertáció tézisei Petro Khoroshyy Témavezető: Prof. Zimányi László Magyar Tudományos Akadémia
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai
 Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
PÉCSI TUDOMÁNYEGYETEM. Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise
 PÉCSI TUDOMÁNYEGYETEM Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise Forminok hatása az aktin filamentum konformációs és dinamikai tulajdonságaira PhD értekezés tézisei
PÉCSI TUDOMÁNYEGYETEM Biológia Doktori Iskola Mikroorganizmusok életfolyamatainak molekuláris analízise Forminok hatása az aktin filamentum konformációs és dinamikai tulajdonságaira PhD értekezés tézisei
Modern Fizika Labor. 12. Infravörös spektroszkópia. Fizika BSc. A mérés dátuma: okt. 04. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Biofizika I 2013-2014 2014.12.03.
 Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet A KERESZTHÍD CIKLUSHOZ KAPCSOLÓDÓ ERŐKIEJTÉS egy kereszthíd ciklus során a miozin II fej elmozdulása: í ~10 nm 10 10 egy kereszthíd
Hőmérsékleti sugárzás
 Ideális fekete test sugárzása Hőmérsékleti sugárzás Elméleti háttér Egy ideális fekete test leírható egy egyenletes hőmérsékletű falú üreggel. A fala nemcsak kibocsát, hanem el is nyel energiát, és spektrális
Ideális fekete test sugárzása Hőmérsékleti sugárzás Elméleti háttér Egy ideális fekete test leírható egy egyenletes hőmérsékletű falú üreggel. A fala nemcsak kibocsát, hanem el is nyel energiát, és spektrális
kutatás során legfőbb eredményeinket a szerin proteázok aktiválódásának mechanizmusával és az aktiválódás fiziológiai következményeinek
 Fehérjék konformációs flexibilitása mint a biomolekuláris felismerés és a jeltovábbítás alapvető eleme (OTKA NK 77978) Zárójelentés (2009. ápr. 1-től 2013. márc. 31-ig) A biológiai rendszerek önszerveződésének
Fehérjék konformációs flexibilitása mint a biomolekuláris felismerés és a jeltovábbítás alapvető eleme (OTKA NK 77978) Zárójelentés (2009. ápr. 1-től 2013. márc. 31-ig) A biológiai rendszerek önszerveződésének
E (total) = E (translational) + E (rotation) + E (vibration) + E (electronic) + E (electronic
 Abszorpciós spektroszkópia Abszorpciós spektrofotometria 29.2.2. Az abszorpciós spektroszkópia a fényabszorpció jelenségét használja fel híg oldatok minőségi és mennyiségi vizsgálatára. Abszorpció Az elektromágneses
Abszorpciós spektroszkópia Abszorpciós spektrofotometria 29.2.2. Az abszorpciós spektroszkópia a fényabszorpció jelenségét használja fel híg oldatok minőségi és mennyiségi vizsgálatára. Abszorpció Az elektromágneses
K68464 OTKA pályázat szakmai zárójelentés
 K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
Modern fizika laboratórium
 Modern fizika laboratórium Röntgen-fluoreszcencia analízis Készítette: Básti József és Hagymási Imre 1. Bevezetés A röntgen-fluoreszcencia analízis (RFA) egy roncsolásmentes anyagvizsgálati módszer. Rövid
Modern fizika laboratórium Röntgen-fluoreszcencia analízis Készítette: Básti József és Hagymási Imre 1. Bevezetés A röntgen-fluoreszcencia analízis (RFA) egy roncsolásmentes anyagvizsgálati módszer. Rövid
Lumineszcencia alapjelenségek
 Lumineszcencia alapjelenségek (Nyitrai Miklós; 211 február 7.) Lumineszcencia Definíció: Egyes anyagok spontán fénykibocsátása, a termikus fényemissziótól függetlenül, elektrongerjesztést követően. Lumineszcens
Lumineszcencia alapjelenségek (Nyitrai Miklós; 211 február 7.) Lumineszcencia Definíció: Egyes anyagok spontán fénykibocsátása, a termikus fényemissziótól függetlenül, elektrongerjesztést követően. Lumineszcens
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
2010. január 31-én zárult OTKA pályázat zárójelentése: K62441 Dr. Mihály György
 Hidrosztatikus nyomással kiváltott elektronszerkezeti változások szilárd testekben A kutatás célkitűzései: A szilárd testek elektromos és mágneses tulajdonságait az alkotó atomok elektronhullámfüggvényeinek
Hidrosztatikus nyomással kiváltott elektronszerkezeti változások szilárd testekben A kutatás célkitűzései: A szilárd testek elektromos és mágneses tulajdonságait az alkotó atomok elektronhullámfüggvényeinek
MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE
 MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE MTA doktori értekezés Kovács Mihály Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Intézet Biokémiai Tanszék 2010 Tartalomjegyzék 1. Összefoglalás 4
MOTORENZIMEK MŰKÖDÉSÉNEK SOKFÉLESÉGE MTA doktori értekezés Kovács Mihály Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Intézet Biokémiai Tanszék 2010 Tartalomjegyzék 1. Összefoglalás 4
11/15/10! A CITOSZKELETÁLIS RENDSZER! Polimerizáció! Polimerizációs egyensúly! Erő iránya szerint:! 1. valódi egyensúly (aktin)" Polimer mechanika!
 11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
Atomfizika. A hidrogén lámpa színképei. Elektronok H atom. Fényképlemez. emisszió H 2. gáz
 Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
KÖLCSÖNHATÁS ÉS DINAMIKA. az NMR spektroszkópia, mint a modern szem. Bodor Andrea
 KÖLCSÖNHATÁS ÉS DINAMIKA az NMR spektroszkópia, mint a modern szem Bodor Andrea ELTE Szerkezeti Kémiai és Biológiai Laboratórium A Magyar Tudomány Ünnepe, 2012.11.08. Edvard Munch: A Nap (1911-1916) AZ
KÖLCSÖNHATÁS ÉS DINAMIKA az NMR spektroszkópia, mint a modern szem Bodor Andrea ELTE Szerkezeti Kémiai és Biológiai Laboratórium A Magyar Tudomány Ünnepe, 2012.11.08. Edvard Munch: A Nap (1911-1916) AZ
Modern Fizika Labor Fizika BSC
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Mézerek és lézerek. Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19.
 és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
Folyadékszcintillációs spektroszkópia jegyz könyv
 Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés
 Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés A gyakorlatra vigyenek magukkal pendrive-ot, amire a mérési adatokat átvehetik. Ajánlott irodalom: P. W. Atkins: Fizikai
Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés A gyakorlatra vigyenek magukkal pendrive-ot, amire a mérési adatokat átvehetik. Ajánlott irodalom: P. W. Atkins: Fizikai
DR. MÁLNÁSI-CSIZMADIA ANDRÁS
 DR. MÁLNÁSI-CSIZMADIA ANDRÁS Eötvös Loránd Tudományegyetem, Természettudományi Kar Biokémiai Tanszék Utazás a motor domén körül: Konformációs átalakulások és intramolekuláris kommunikációs útvonalak a
DR. MÁLNÁSI-CSIZMADIA ANDRÁS Eötvös Loránd Tudományegyetem, Természettudományi Kar Biokémiai Tanszék Utazás a motor domén körül: Konformációs átalakulások és intramolekuláris kommunikációs útvonalak a
Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség
 Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség Osváth Szabolcs Evans-Searles fluktuációs tétel Denis J Evans, Ezechiel DG Cohen, Gary P Morriss (1993) Denis J Evans, Debra
Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség Osváth Szabolcs Evans-Searles fluktuációs tétel Denis J Evans, Ezechiel DG Cohen, Gary P Morriss (1993) Denis J Evans, Debra
A citoszkeletális rendszer
 A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 5. mérés: Elektronspin rezonancia. 2008. március 18.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
PhD értekezés tézisei. Buzády Andrea. Alprogram: Funkcionális fehérjedinamika vizsgálata biofizikai módszerekkel Alprogramvezetı: Dr.
 PhD értekezés tézisei Dipoláris relaxáció vizsgálata idıbontott spektroszkópiai módszerekkel Buzády Andrea Alprogram: Funkcionális fehérjedinamika vizsgálata biofizikai módszerekkel Alprogramvezetı: Dr.
PhD értekezés tézisei Dipoláris relaxáció vizsgálata idıbontott spektroszkópiai módszerekkel Buzády Andrea Alprogram: Funkcionális fehérjedinamika vizsgálata biofizikai módszerekkel Alprogramvezetı: Dr.
Modern fizika laboratórium
 Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Biomolekuláris szerkezeti dinamika
 Kísérletek, mérések célja Biomolekuláris szerkezeti dinamika Kellermayer Miklós Biomolekuláris szerkezet és működés pontosabb megismerése (folyamatok, állapotok, átmenetek, kölcsönhatások, mozgások, stb.)
Kísérletek, mérések célja Biomolekuláris szerkezeti dinamika Kellermayer Miklós Biomolekuláris szerkezet és működés pontosabb megismerése (folyamatok, állapotok, átmenetek, kölcsönhatások, mozgások, stb.)
Al-Mg-Si háromalkotós egyensúlyi fázisdiagram közelítő számítása
 l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
Biofizika I
 ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
ÁTTEKINTÉS AZ IZOM 9. A HARÁNTCSÍKOLT IZOM SZERKEZETE ÉS MECHANIKÁJA 10. AZ IZOMMŰKÖDÉS ÉS SZABÁLYOZÁS MOLEKULÁRIS ALAPJAI TÍPUSAI: SZERKEZET és FUNKCIÓ MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSAI MECHANIKAI
Műholdas és modell által szimulált globális ózon idősorok korrelációs tulajdonságai
 Műholdas és modell által szimulált globális ózon idősorok korrelációs tulajdonságai Homonnai Viktória II. éves PhD hallgató Témavezető: Dr. Jánosi Imre ELTE TTK, Komplex Rendszerek Fizikája Tanszék Bevezetés
Műholdas és modell által szimulált globális ózon idősorok korrelációs tulajdonságai Homonnai Viktória II. éves PhD hallgató Témavezető: Dr. Jánosi Imre ELTE TTK, Komplex Rendszerek Fizikája Tanszék Bevezetés
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Gyors-kinetikai módszerek
 Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Az elektromágneses hullámok
 203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
