Fehérjék: tartalomjegyzék
|
|
|
- Diána Kozma
- 5 évvel ezelőtt
- Látták:
Átírás
1 Fehérjék: tartalomjegyzék 1) Bevezető 2) A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosav sorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) 3) A fehérjék térszerkezet-viszgálati módszerei 4) A fehérjék belső mozgékonysága 5) Bevezetés az enzimek világába - oxidoreduktázok (az alkohol-dehidrogenáz) - transzferázok - hidrolázok (a szerinproteázok, a lizozim) - liázok - izomerázok - ligázok 6) Érdekes fehérjék
2 1) Bevezető - az élő rendszerekben a víz után a fehérje a legelterjedtebb molekulatípus, - a fehérjék lokális koncentrációja igen magas, - sokrétű feladatot látnak el: motorfehérjék, enzimek, antitestek, hormonok, szállítanak, etc. - a sejtben előforduló szinte összes kémiai átalakítást fehérjék végzik RNS vírus: DNS vírus: Baktérium: 1-25 gén gén gén ember (~ bp): gén ~ fehérjét kódol növény: > gén A fehérjék természetes lineáris polimerek: poliamidok
3 Poliamid polimerek: kémiai összetétel Egyetlen amino-karbonsavból is felépíthetünk lineáris poliamid rendszereket: 1 mol e-kaprolaktám poliaddíciós reakciója 1 mol vízzel elindítható, amely e-peptideket eredményez (~260 C /N 2 atmoszféra, 4-5 óra reakcióidő után az ismert műanyagot a poliamid 6-ot vagy más néven a Nylon 6-ot kapjuk).
4 Poliamid polimerek: az amidkötés téralkata A határszerkezetek szemléltetik hogy 2 nemkötő elektronpár 3 centrumra (, C és N) delokalizálódik, így a C-N kötésnek is van kettőskötés jellege, s ezért válik a peptidkötés síkalkatúvá: 6 atom (C a,c, és a C a, N NH,H NH ) egy síkban van. Az amidkötés adatai: Az amid síkalkatú, s ennek következménye, hogy a polipeptidlánc nem teljesen flexibilis. A főláncban az ismétlődő amidokat a C α atomok kötik össze. Az N NH -C α és a C α -C kovalens σ-kötések mentén az elfordulás viszonylagosan szabad, annak mértékét a φ és a ψ torziósszögek nagysága méri. (Az oldalláncok torziósszög értékeit a χ(i) változók rögzítik.)
5 2) A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosavsorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) Az elsődleges szerkezet a fehérjét felépítő aminosavak sorrendje: balról jobbra, az N-terminálistól a C-terminális felé írjuk és rajzoljuk a polipeptidláncot. A kémiai összetételt, azaz az aminosavakat és azok sorrendjét a megfelelő gén(ek) kódolják. H-Thr--His--Ile--Ser--Ser--Ile-Met-Pro-Leu-Glu-H
6 A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosavsorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) A szabályos (periodikus és aperiodikus) valamint szabálytalannak (fokozott belső mozgásúnak leírt, rendezetlennek) mondott fehérjerészek együttese. Elsőként Linus Pauling javasolta az a-hélix és a b-redőzött rétegek megjelölést. E két fajta, valamint a többi tipikus konformációs építőelem a Ramachandranfelület jellegzetes régióiban azonosítható. Meghatározásukhoz gyakran ismétlődő alapalkatok (foldamer) és mintázatok (pl. H-híd) felismerése vezet. a-hélix b-redő -kanyar tipikus peptidkonformerek elhelyezkedése a Ramachandran-felületen: 0 o j,y 360 o intervallum esetén a E=E(j, y) térképen
7 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. Polipeptidek térszerkezete szabályos,tipikus konformerek szabálytalan, atipikus konformerek periodikus, homo-konformerek aperiodikus, hetero-konformerek f(i) = f(i 1) és y(i) = y (i 1) , a-, π- hélix, - b-redőzött réteg, - kollagén-hélix (PPII szerkezet) f(i) f(i 1) és y(i) y (i 1) b-kanyar szerkezetek: - I (és I ) típusú - II (és II ) típusú - VIa (és VIb) típusú - VIII típusú
8 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. - alfa hélix (α-hélix): a természetes L-aminosavak esetében a jobb (csavar)menet téralkat a szokásos (rugó). Itt minden (i+4). amidcsoport H-donor az i. amid C= felé. alfa hélix: Pauling-Corey-Branson C-terminális jobbmenetes a-hélix balmenetes a-hélix N-terminális f(i) = f(i 1) ~ 54º és y(i) = y (i 1) ~ 45º memo: a 2 db a-hélixből feltekeredő coiled-coil szerkezet, balmenetes szupramolekuláris komplexet eredményez. => harmadlagos szerkezet
9 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. Helikális vagy spirális téralkat: lehet jobbmenetes vagy balmenetes 1) ha a spirális szerkezeti elemnek nincs kitüntetett vége (vagy eleje) (pl. rugó) akkor is lehet a tükörképi párja. 2) ha a spirális szerkezeti elemnek van kitüntetett vége (vagy eleje): pl. oszlop (töve és teteje), csavarhúzó (feje), peptid hélix (N- és C-term.) N-term. C-term. A jobbkéz szabály: tehát ez egy jobbmenetes csavar tehát ez egy jobbmenetes a-hélix memo: Jobbkezesek a fehérjékben található a-hélixek,a DNS A és B formái, stb. def.: Nézzük a hélixet a hossztengelye mentén. Ha a helikális elmozdulás, amely a nézőtől távolodik az óramutató járásával megegyező irányú, akkor az a hélix jobbmenetes. (Ezt a hélix típust szokás P-helixnek (plusznak) nevezni.)
10 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. Az a-hélix tipikus geometriai jellemzői: jobbmenetes 3,6 aminosav menetenként 0,54 nm menetmagasság 0,15 nm emelkedés/aminosav periodikus: 5 csavar/18 aminosavrész után d = 1,05 nm R-csoportok a palástra merőlegesen kifelé H-kötések hélix tengellyel párhuzamosak Robert Brainard Corey ( ) Az a-hélix és a b-redő felfedezője Animáció
11 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. A kollagén: (a görög kolla ( enyv ) és gennao ( nemz, létrehoz ) elemekből, tehát enyvképző. a kollagén téralkata: a természetes L-aminosavak esetében az egyes szálak balcsavarmenetűek. Ideális aminosav összetétel: - PG-. X Y Gly X Y Gly Y Gly X Y Gly X Gly X Y Gly X Y a tropokollagén: a három kollagén szál együttese, amely jobbmenetes hélixet eredményez! (1954) f(i) = f(i 1) ~ 60º és y(i) = y (i 1) ~ +135º memo: Testtömegünk közel negyedét ez a fehérje teszi ki; hialuronsavval és kondroitin szulfáttal kiegészülve a bőr, a porc, az ín, az ízület és csont meghatározó komponense. Animáció
12 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. b-redőzött réteg (vagy b-redő) téralkat esetén - antiparallel és - parallel redőket különböztetünk meg. Ezen másodlagos szerkezeti forma a gerincatomok H-hidas összekapcsolódásának következménye, melyben az oldalláncok csak közvetetten vesznek részt s ezért sokfajta aminosav azonosítható a a különböző b-redőkben. (Az oldalláncok a redő síkja alatt és felett helyezkednek el) - az antiparallel redőzött réteg térszerkezet: f(i) = f(i 1) ~ 150º y(i) = y (i 1) ~ +150º Animáció
13 A parallel redőzött réteg térszerkezet: N C a C N H N C a C N H H C a C N H C a C N C a C a C N H C N H Egy érdekes példa: a selyemszál: - aminosav összetétele konzervatív (Gly:Ala:Ser = 3:2:1) - szekvenciális összetétele: Gly Ala Gly Ala Gly Ser - térszerkezete jellegzetes b-szál jellemzői: feszes lánc nem nyújtható hajlékony rétegek elcsúszhatnak selyemfény rétegek fénytörése
14 A másodlagos szerkezeti elemek: a-hélix, b-redő, stb. -a b-kanyar térszerkezet: -a hurkok: i+1 i+2 i i+3
15 A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosavsorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) Egy fehérje harmadlagos szerkezete azonos az azt felépítő egyetlen polipeptidlánc 3D- vagy térszerkezetével. A másodlagos szerkezeti elemek feltekeredése következtében létrejövő téralkat egy időátlagban kvázi azonos konformer. Jellegzetes hidrofób- és ionos (só-híd) kölcsönhatások, illetve a diszulfid-hidak stabilizálják a kialakult 3D szerkezetet. A fehérjék téralkatát stabilizáló 5-fajta kötés: peptidkötés, hidrogén-híd (kötés), diszulfid kötés, ionos kötések, hidrofób erők (kötés)
16 A harmadlagos szerkezet (domének és modulok) Milyen erősek a fehérjéket összetartó kötések és erők? Kovalens kötés Hidrogén-híd Ionos-kötés Van der Waals Hidrofób erők ~100 kcal/mol ~3 kcal/mol ~ 5 kcal/mol ~1 kcal/mol ~3 kcal/mol megosztott elektronok víz-víz teljes töltésátadás fluktuál nem igazi kötés szerves-vizes H-híddal kompetícióban indukált dipól entrópia vezérelt szerves-szerves erős száraz kristályokban csak sztérikus közelség esetén csak vízben hatásos erős gyenge, orientáció érzékeny vízben gyenge gyenge gyenge A biomolekulák harmadlagos szerkezetének kialakítása során a gyenge kötések (kölcsönhatások) összessége igen jelentős.
17 túl közel ideális túl távol taszítás egyensúly vonzás Van der Waals- (hidrofób) potenciál 3 2,5 V/ek r 0 = 2.58 Å - túl távol aszimmetrikusan polarizált elektronfelhők vonzása - túl közel elektronfelhők egymásba hatolása taszítást okoz 2 1,5 1 0,5 0-0,5-1 -1,5 (r 0 /r) -12 (r 0 /r) (r 0 /r) ,5 3 3,5 4 4,5 5 ideális (van der Waals) távolság -(r 0 /r) -6 r Johannes Diderik van der Waals ( ) -2
18 A harmadlagos szerkezet (domének és modulok) a-domén szerkezetek: négyes hélixköteg (four-helix bundle) citokróm b 562 (a légzési elektrontranszportlánc része) Keratin fibrilláris szerkezeti fehérje a-keratin (haj, gyapjú, köröm) és b-keratin (köröm, kagylóhéj, teknőspáncél) coiled-coil GCN4 transzkripciós faktor Aktin: mikrofilament monomer egysége Miozin
19 A harmadlagos szerkezet (domének és modulok) b-redő topológiák N C aszpartát transzkarbamoiláz enzim C N bab-motívumok flavodoxin (redox fehérje) Greek key motívum C N C N tripszin (vágva) plasztocianin (elektrontranszporter)
20 A harmadlagos szerkezet (domének és modulok) A bab-motívum: C N részlet az alkohol dehidrogenáz enzim szerkezetéből (szalagmodell)
21 A harmadlagos szerkezet (domének és modulok) A globuláris fehérjék térszerkezete igen sokféle.
22 A fehérjék feltekeredése (vízben) A szerkezeti biokémia dogmája Általánosan elfogadott, hogy az aminosav-szekvencia határozza meg a fehérje térszerkezetét. Bizonyíték: denaturációs-renaturációs kísérletek (Anfinsen). A fehérje natív térszerkezete az esetek túlnyomó többségében a globális energiaminimumnak felel meg. Hogyan találja meg a fehérje a natív térszerkezetét? Levinthal-paradoxon: egy polipeptidlánc lehetséges konformációs állapotainak száma csillagászati: (pl. 100 aminosav, 9 gerinckonformer/aminosav: x ) Az ismert fehérjék néhány másodperc (vagy rövidebb idő) alatt feltekerednek: nincs idő a lehetséges téralkatok töredékének kipróbálására sem (világegyetem kora < s) A feltekeredés adott útvonalon (útvonalakon) zajlik, lényeges a lokális kölcsönhatások és az azok révén kialakuló szerkezeti magok szerepe Alapvető feltekeredési modellek: másodlagos szerkezeti elemek kialakulása hidrofób összeomlás feltekeredett (folded) fehérje kitekeredett (unfolded) fehérje feltekeredési mag (folding nucleus)
23 A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen 1972 Nobel-díj Ribonukleáz feltekeredése A ribonukleáz renaturálódása feltekeredés folding
24 A harmadlagos szerkezet (domének és modulok) Fehérjék denaturálásához használt reagensek: kaotróp molekulák Fehérjék denaturálásához használt reagensek: az SS- kötések redukciójához
25 A harmadlagos szerkezet (domének és modulok) definíció: 50%-os feltekeredés: amikor a molekulák fele feltekeredett, ám a másik fele kitekeredett marad. memo: nincs félig feltekeredés!!!
26 A harmadlagos szerkezet: a termostabilitás A hődenaturálás: Ubiquitin (76 as., 8,5kDa) DSC: Differential Scanning Calorimetry C p,exp / (mj o C -1 ) T m 50 o C Θ/ o C Az Ubiquitin DSC termogramja alapján a fehérje 40 o C alatt megtartja natív téralkatát, aztán endotermikus konformáció változáson megy át. T m, olvadáspont (~50 o C olvadási hőmérséklet, melting temperature) az a hőmérséklet, ahol egy adott nyomáson a folyadék és a szilárd fázis egyensúlyban van. Ribonukleáz T 1 T m = 47 o C (320K). ph=7 és T=298K a fehérje letekeredéshez szükséges DG mindössze 22.5 kj.mol -1, ami alig több, mint egy erősebb H-híd (DG 20 kjmol -1 ). Hogy lehet ez, amikor ugyanez a fehérje tele van a-hélixszel és b-redővel, amely egy sor H-hidat tartalmaz? Atkins de Paula 118
27 Példa: DG = DH-TDS = = 4 kcal.mol -1 Ribonukleáz T 1 Ha T=298K akkor a fehérje letekeredéshez szükséges DG mindössze 22.5 kj.mol -1, ami alig több, mint egy H-híd (DG 20 kjmol -1 ). Kérdés: Hogy lehet ez, amikor ugyanez a fehérje tele van a-hélixszel és b-redővel, amely egy sor H-hidat tartalmaz? Becsüljük meg a DH-t: ~ 4 menet hélix 3.6*4 ~ 15 a.s ~ 12 H-híd ~ 12*2= 24 kcal.mol -1 ~ 3 hosszabb b-redő 3*8 ~ 24 a.s ~ 22 H-híd ~ 22*2 = 44 kcal.mol -1 Σ DH > 68 kcal.mol -1 Atkins de Paula 118 Becsüljük meg a DS-t: 1) Legyen a fehérje letekeredett állapotában minden aminosavnak 3 lehetséges és egyforma valószínűséggel megjelenő gerinc konformere. Ekkor S = R ln (3 100 ). 2) Ha feltekeredik egy ötös peptid rész (pl. kanyar) és annak már csak 1 lehetséges konformere van, akkor S = R ln (3 95 ) már csak. (A változás Rln(3 5 ) ami szobahőn (T=25 o C) ~ 3.2 kcal.mol -1. 3) Ha az egész feltekeredik, mit 20 db. pentapeptid darab, akkor az S ~ 20* 3.2 = 64 kcal.mol- 1.
28 A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosavsorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) A fehérjék negyedleges szerkezetének kialakulása során több, akár eltérő, akár azonos polipeptidlánc vagy fehérje kapcsolódik össze, s alkot funkcionális egységet. A keletkező dimerek, trimerek, tetramerek stb. akkor nevezzük homo-dimernek, homo-trimernek stb. ha a felépítő egységek azonosak. Ha eltérőek, akkor a hetero- előtagot használjuk. Az IL-8 biológiai szerepe: a legfontosabb a célsejteken (fehérvérsejteken) a kemotaxis kiváltása.
29 A negyedleges szerkezet A hemoglobin térszerkezete és működése: kék: a-alegységek, sárga: b-alegységek, lila: vas centrumok eritrocita, thrombocita, leukocita vörösvérsejt, vérlemezke, fehérvérsejt A hemoglobin a vörösvértest szállító metalo-fehérje, amely az oxigén transzportban vesz részt. (A gerincesekben jellegzetes) Egyetlen Glu Val aminosav csere befolyásolja a hemoglobin tészerkezetét és működését, amely fiziológiás koncentrációban a sarlósejtes anémia betegségéhez vezet. (De a maláriával szemben ellenállóbb a szervezet.) sarló alakú vörösvérsejtek
30 A negyedleges szerkezet Több doménből felépülő fehérjék a működéshez elengedhetetlen a domének kooperativitása sejt-mátrix kapcsolatot kialakító fehérjék (integrinek) aktiválódása során jellegzetes makroszkopikus szerkezetváltozás következik be.
31 Fehérjék: tartalomjegyzék 1) Bevezető 2) A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosav sorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) 3) A fehérjék térszerkezet-viszgálati módszerei 4) A fehérjék belső mozgékonysága 5) Bevezetés az enzimek világába - oxidoreduktázok (az alkohol-dehidrogenáz) - transzferázok - hidrolázok (a szerinproteázok, a lizozim) - liázok - izomerázok - ligázok 6) Érdekes fehérjék
32 3) A fehérjék térszerkezet-viszgálati módszerei Fehérjék analitika és térszerkezet-vizsgálati módszerei: Az atomi szintű szerkezetkutatás legfontosabb eszközei: - NMR-spektroszkópia - röntgen-krisztallográfia - molekula-modellezés
33 A fehérjék térszerkezet-viszgálati módszerei Mit rejt a kristály? Fehérje röntgenkrisztallográfia: kémiai Nobel-díj, 1962 Max Perutz, John Kendrew kristályban az egyes atomok helye térben jól meghatározott részletgazdag térszerkezet
34 A negyedleges szerkezet Mit rejt az oldat: NMR-spektroszkópia Fehérje NMR: kémiai Nobel-díj, 2002 Kurt Wüthrich anyagszükséglet: 1 mm vizes oldatból μl szerkezeti sokaság
35 4) A fehérjék belső mozgékonysága A makroszkopikus mozgás mikroszkopikus háttere: a táncrend 10 cm 0,1 mm szervezet sejtek 1 nm 0,1 m fehérjemolekulák sejtalkotók
36 A fehérjék belső mozgékonysága Minden fehérje határozott, belsőleg kódolt mozgékonysággal rendelkezik: szinkronizáltabb mozgás, rendezettebb téralkat szinkronizálatlan mozgás, rendezetlenebb téralkat memo: egymásba ágyazott, eltérő időskálájú mozgások ~ 1s 10 5 s ~ 1h s ~ 1év
37 A fehérjék belső mozgási időskálája hurkok és kanyarok záródása 0.1ms 10ms másodlagos szerkezeti elemek 10ns 1ms feltekeredés 1ms 1h H/D R ex Rot. Dif. korrel. idő 1ns<t c < 10ns gerinc dinamika 1ps 10ns t lokális aggregáció 1 s 1 év t effektiv = t C +t lok. oldallánc forgás 0.1ps 10 ps
38 Fehérjék: tartalomjegyzék 1) Bevezető 2) A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosav sorrend) - másodlagos szerkezet (a-hélix, b-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges szerkezet (alegység-struktúrák) 3) A fehérjék térszerkezet-viszgálati módszerei 4) A fehérjék belső mozgékonysága 5) Bevezetés az enzimek világába - oxidoreduktázok (az alkohol-dehidrogenáz) - transzferázok - hidrolázok (a szerinproteázok, a lizozim) - liázok - izomerázok - ligázok 6) Érdekes fehérjék
39 5) Bevezetés az enzimek világába energia a sejtben előforduló szinte összes kémiai átalakítást biológiai katalizátorok, az enzimek végzik! - a legtöbb enzim fehérje - az átalakítás sebessége akár szeres lehet a biokatalízis hatására. - így lehetséges, hogy a reakciók végbemennek már 37 o C-on és neutrális ph-n. specificitás: az enzim nagy affinitással kötödik mind a saját szubsztrátjához, mind a termékhez. (E. Fischer kulcs-zár modell megalkotása.) memo: Arrhenius egyenlet (a sebességi egyenlet T függése): k= A exp ( E a /RT) E a k növekvő E a Tipikus enzimreakció: Keeler 138 reakció koordináta T(K) enzim + szubsztrát enzim-szubsztrát komplex enzim + termék A reakció helye: az aktív hely ( centrum ), ahová a szubsztrát tipikusan nem-kovalans kötésen keresztül kötődik. Az enzimreakciók leggyakrabban teljesen sztereospecifikusak.
40 Bevezetés az enzimek világába példa: egy lipáz enzimmel történő észterhidrolízis: alapreakció: a lipáz enzimek a zsírsavészterek szelektív hidrolízisében vesznek részt. A glicerin rész megfelelő pontján hidrolizálnak: sztereospecificitás: legyen az észter királis és használjunk egy racemátot megfigyelés: az egyik enantiomer észter elhidrolizál, a másik nem vagy csak nagyon lassan. (a jelenség neve: kinetikus rezolválás) F racemát észter kiindulási anyag C Et H lipáz H F C C Et (R)-(+)-2-fluorhexánsav-etil-észter >99% enantiomer túlsúly H magyarázat: (S)-(+)-2-fluorhexánsav >69% enantiomer túlsúly - a lipáz aktív zsebébe nem fér be az (R)-enantiomer, ezért az visszamarad és a hidrolízis során 99%-ig dúsul, - míg az (S)-(-)-sav éppen 69%-ban keletkezik. F H Et
41 Geometriai specificitás megadja, hogy mennyire szigorúan csak egyetlen szubsztrátot fogad el az enzim: pl: 1) Karboxipeptidáz A a polipeptidlánc C-terminálisáról lehasít egy aminosavat, ha az nem Arg, Lys, Pro és a megelőző aminosav nem Pro. 2) kimotripszin: észtert is, amidot is hidrolizál. R N H peptid R' + H 2 kimotripszin R + H 3 N + R' Inhibitor: molekula, amely az enzimműködésre negatívan hat, azt gátolja. Kompetitív inhibitor: amelyik a szubsztráttal versenyez az aktív helyért vagy annak bekötését oda gátolja. R N H R' + H 2 Kofaktor: nem-fehérje jellegű, de az enzimhez ideiglenesen kötött molekula/ion, olyan amelyik a katalízist segíti (apoenzim [fehérje] + kofaktor = holoenzim) Koenzim: (spec. kofaktor): olyan segédmolekula, mely nincs permanensen az enzimhez kötve pl. NAD Prosztetikus csoport: (spec. kofaktor): olyan molekula, amely permanensen az enzimhez van kötve pl. Fe-S centrum, hem, stb. memo: sok vízoldható vitamin koenzim prekurzor: nikotinsav NAD, pantoténsav CoA észter Fe 2+ kimotripszin R H + H R' H Koenzim A N niacin
42 Szerinproteázok (sok egymással nem - feltétlenül - rokon fehérje) A fehérjék lebontó enzimek (proteázok): pl. kimotripszin, tripszin és elasztáz (Azért szerinproteáz, mert van benne egy a katalízis szempontjából döntő fontosságú Ser.) A Kimotripszin: specificitása: főleg Trp, Tyr, Phe, de Leu, Met után is hasítja az amidkötést memo: észtereket is hidrolizál memo: a tripszin más specificitású: Arg vagy Lys után hasít. Az inaktív kimotripszinogénből (245 as.) két dipeptid kihasadása és egy refolding során képződik az enzim. A konformációs átrendeződés eredményeként sztérikusan közel kerül a katalitikus triád 3 eleme. A katalitikus triád: Asp His Ser
43 Szubsztrátkötő hely Aktív hely, benne a katalitikus triáddal oxianion üreg ez a peptidkötés fog elhasadni szubsztrátkötő zseb egy aromás (R1) csoporttal rendelkező szubsztrát N- terminális része
44 Proteolízis, biodegradáció: Amid-hidrolízis elemi (szereves kémiai) reakciólépései: - nukleofil addíció, - elimináció. A deprotonált aszpartát az imidazol protonját vonzva, növeli az imidazol másik nitrogénjének protonvonzó képességét, minek hatására a Ser oldalláncának H- kötése lazul, s így az oxigén jobb nukleofil lesz! memo: lombikban, vízben az amidkötés nem hidrolizál, felezési ideje években mérhető, pedig a H 2 kb. olyan nukleofil mint a H- CH 2 - Ser oldallánca. (lásd peptidek 5-6 oldal)
45 Asp 102 H 2 C C H H 2 Az aktív hely regenerálódása N His 57 CH 2 N H R H N C Ser 195 CH 2 R acilezett szerin memo: a hasítandó peptid időlegesen kovalensen kötődik az enzimhez: C-terminális acilezi a Ser oldalláncát (észter), míg az elhasított amidkötés N-terminális része távozik az aktív centrumból. Asp 102 H 2 C C H N His 57 CH 2 Ser 195 RNH 2 N H CH 2 H C R acilezett szerin memo: észter hidrolízise, Ad Nu
46 Asp 102 H 2 C C H N His 57 CH 2 N H Ser 195 CH 2 tetraéderes intermedier H C R Asp 102 H 2 C C H N His 57 CH 2 N H Ser 195 CH 2 regenerált aktív centrum memo: lehet készíteni olyan enzimet, amelyik a fordított folyamatot katalizálja. karbonsav termék H C R Feltehetőleg a riboszómán a fehérjeszintézis során (RNS-részek közreműködésével) ilyen fordított folyamat zajlik.
47 Összefoglalás: A kimotripszin irreverzibilis inhibitora: pl. DIPF
48 Lizozim: egy tipikus enzimműködés (Lysozyme:= lyse: felold + enzyme) A Lizozim feloldja (kilukasztja) a baktériumok sejtfalát: katalizálja a sejtfal poliszacharid egy adott részének hidrolízisét. Nag-Nam-Nag-Nam-Nag-Nam Alexander Fleming 1922-ben megfázott H H R 1 R 2 R 1 R 3 A B H C R 3 D H E R 3 F R 2 R 1 R 2 R 1 R 2 R 1 R 2 R 1 R 2 H HCH 2 H H H NHCCH 3 b-d-n-acetil-glükozamin (Nag) R 1 = CH 2 H R 2 = NHCCH 3 R 3 = CH(CH 3 )CH H HCH 2 R H R: CH 3 H CH NHCCH 3 b-d-n-acetil-muraminsav (Nam)
49 A Lizozim biokatalizált glikozidkötés hidrolízisének molekuláris háttere: 1) A D-E glükopiranóz gyűrűk elhidrolizálása: David Chilton Phillips memo: a D-gyűrű a bekötés következtében konformációsan eltorzul, a térszerkezet feszült lesz. 2) A molekuláris felismerés és a hexaszacharid (zöld) megkötésének atomi részletei:
50 3) A hidrolízis legvalószínűbb mechanizmusának kétfajta bemutatása: memo: a természetes védekezésünk fontos enzimje tehát a Lizozim, amely patogének (pl. Salmonella, E.coli vagy Pseudomonas) ellen nyújt védelmet.
51 Alkohollebontás (oxidoredukció, aromatizáció): A NADH egyensúlyi reakciója az acetaldehidet etil-alkohollá redukálja. A működés lépései és leírása: 1) A NADH és az aldehid megkötődik, utóbbit a Zn 2+ koordinálja, 2) a nikotinsavamid nitrogénjének nemkötő elektronpárja delokalizálódik, a dihidropiridin gyűrű aromássá válik az egyik C4-es hidrogénatomot anionként leadva. (oxidáció) alkoholdehidrogenáz enzim (NADH + inhibitor komplex) 3) A hidridion redukálja az acetaldehidet, majd a képződő alkoholát anion protonálódik. A cink mint Lewissav fokozza a karbonil-szén pozitív polározottságát, s így annak elektrofil jellegét. méregtelenítés: ha nagy az alkoholkoncentráció, akkor az egyensúlyi reakció megfordul és az etilalkohol acetaldehidé oxidálódik, amely mérgező és a vegyület a másnaposság legfőbb oka.
52 az alkohol-dehidrogenáz enzim apoenzim + koenzim + inhibitor (80 kda dimer, az emberben legalább 6 variánsa van, előfordulás, máj és gyomor) memo: Miért mérgezők az alkohol végzetes adalékai: metanol, etilénglikol? NH 2 H feladatuk: - egyensúlyt tartani az alkoholok aldehidek és ketonok között. N N N N H H H H P H P H 2 N H H N H H - méregtelenítés (emlősben): a toxikus alkoholból aldehidet csinál - fermentálás (baci és élesztő): aldehidből alkoholt készít (redukció) A NAD+ (Nikotinsavamid-adenin-dinukleotid) (az élő sejt egyik oxidáló vagy dehidrogénező szere)
53 A kulcs & zár modell (Emil Fischer) Hogyan tervezzünk hatóanyagot vagy gyógyszert? Minél többet meg kell tudnunk a fehérjék dinamikus téralkatáról, annál nagyobb a sikeres tervezés esélye!
54 6) Érdekes fehérjék Újrahasznosítás: mit őrizzünk meg és mit dobjunk ki? Az Ubiquitin Számos sejten belüli folyamat szabályzó és kontroláló fehérjéje a viszonylag kicsi, egy doménből felépülő Ubiquitin. Az evolúció során nem változott: az élesztőben vagy a humán sejtekben rendre ugyanúgy néz ki. Legfontosabb feladata, hogy megjelölje a valamilyen okból sérült fehérjéket, amelyeket később a sejt felismer, majd lebont. A lebontott fehérjék aminosavai újrahasznosításra kerülnek, új peptidek vagy fehérjék épülnek fel belőlük. (Nincs hulladék!)
55 Érdekes fehérjék Sejten belüli kommunikáció és információ-feldolgozás A TNF-a: tumor nekrózis faktor-a A sejtben sok molekula feladata a jelátadás vagy a jelfeldolgozás; melyre jó példa a TNF-a. lyan esetekben, amelyekben az organizmust külső támadás éri (pl. baktériumok) az immunsejtek TNF-a-t termelnek és bocsájtanak ki. A TNF-a túltermelődése a tumoros megbetegedés egy jele.
56 Érdekes fehérjék An army of emergency doctors cares for the health of the proteins in each cell Legend: The small heat shock protein a chaperone ne of the most severe dangers for a cell is the loss of the 3-dimensional structure and function of its proteins. This so-called denaturation can be caused by various influences, among them aging or heat. Denaturation is also the reason why egg white becomes turbid when cooked. Special proteins, the chaperones, rescue denatured proteins by re-folding them. Chaperones thus are the molecular emergency doctors of the cell.
57 Érdekes fehérjék Staples hold our body together Legend: Cadherin ur body consists of trillions of cells that all work together to keep us alive. Between the cells there is a complex network of molecular cables and connection proteins that keep the cells together. They prevent our body from falling apart. Cadherin is one of these connection proteins. It is a long protein that staples together the membranes of two adjacent cells.
58 Érdekes fehérjék A molecular drill P22 tailspike protein. The semi-transparent surface shows the global shape of the protein. Viruses can infect not only higher organisms, such as birds or humans, but also bacteria. Viruses of this type are called bacteriophages, or phages for short. The bacteriophage P22 infects salmonella that cause, e.g., typhus. In order to infect bacteria, phages have a special injection machine that drills through the membrane of the bacterium. These are the so-called tailspike proteins.
59 Érdekes fehérjék A bacterial defense against antibiotics (b-lactamase/inhibitor complex) In the past years, alarming news about antibiotics-resistant bacteria repeatedly appeared in the media. The enzyme beta-lactamase is one of the main defense mechanisms of bacteria against the class of beta-lactam antibiotics such as the well-known penicillin. These antibiotics have a chemical ring structure called beta-lactam. Beta-lactamase cleaves this ring and hence deactivates the anti-bacterial activity of antibiotics.
60 Érdekes fehérjék How is oxygen transported from the lungs to the cells and why is blood red? Legend: Hemoglobin and its pigment heme (in pink) In our blood, hemoglobin is responsible for transporting oxygen. It consists of four proteins and the red pigment heme. Hemoglobin thus is the reason for the red color of blood. In the lungs, the hemoglobins are loaded with oxygen, which they then transport to the cells of our body. The image shows an enlarged detail of hemoglobin with the oxygen-carrying pigment heme shown in pink.
61 Érdekes fehérjék Why are we hung over after a night of excessive drinking? Legend: Alcohol dehydrogenase Alcohol dehydrogenase is responsible for the degradation of alcohol in our liver. Each molecule of alcohol that we drink ends up in the liver, where it is broken down to acetaldehyde by this protein. The degradation product is, however, even more toxic than alcohol itself, and it causes headaches and digestion problems. Fortunately our liver also has a protein that degrades the toxic acetaldehyde. This protein, however, works slower than its colleague alcohol dehydrogenase, providing one of the limits to our drinking capabilities.
62 Érdekes fehérjék Where poisons attack us Legend: The star-like structure of the nicotine-acetylcholine receptor Nicotine-acetylcholine receptors (AChR) are, e.g., responsible for muscle contraction. In addition, they also play essential roles in the processes of thinking and learning in our brain. AChR are the target of many naturally occurring poisons such as, e.g., nicotine, which leads to the production of adrenaline, or snake and spider venoms that paralyze the muscles. Also synthetic poisons such as the lethal nerve gas Sarin, or clinically used painkillers and anesthetics act through AChR. szarin
63 Érdekes fehérjék Arteriosclerosis: touchy giant proteins transport fat Legend: Two units of apolipoprotein B100 interact In our blood, cholesterol is transported in so-called LDL particles. LDL particles contain several lipids (fats) as well as a lipid membrane. They are kept together by apolipoprotein B100, one of the largest proteins known. The lipids, as well as apob, are very sensitive to oxidation. When oxidized, LDL particles can stick together and deposit on the interior walls of the blood vessels. The result is one of the most frequent causes of death in the western world: arteriosclerosis.
64 Kinesin (a motor protein) pulling some kind of vesicle along some kind of cytoskeletal filament
65 A DNS-töl a fehérjéig: Fehérjék élete / funkciója: Fehérje lebontás: Sejtalkotók, működésük:
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Fehérjék Bevezető A fehérjék szerkezeti hierarchiája:
 Fehérjék Bevezető A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosav sorrend) - másodlagos szerkezet (α-hélix, β-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges
Fehérjék Bevezető A fehérjék szerkezeti hierarchiája: - elsődleges szerkezet (aminosav sorrend) - másodlagos szerkezet (α-hélix, β-redő, stb.) - harmadlagos szerkezet (domének és modulok) - negyedleges
Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai Nobel-díjak:
 Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai obel-díjak: Linus Pauling 1954 obel-díj fehérje szerkezet alapjai Frederick Sanger 1958 obel-díj Az inzulin szekvenálása Sir. John owdery
Az aminosavak peptidek és fehérjék koronázatlan királyai, kémiai obel-díjak: Linus Pauling 1954 obel-díj fehérje szerkezet alapjai Frederick Sanger 1958 obel-díj Az inzulin szekvenálása Sir. John owdery
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel
 Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
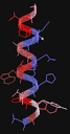 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Enzimek. Enzimek! IUBMB: szisztematikus nevek. Enzimek jellemzése! acetilkolin-észteráz! legalább 10 nagyságrend gyorsulás. szubsztrát-specificitás
 Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék. elrendeződés, rend, rendszer, periodikus ismétlődés
 Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
A fehérjék hierarchikus szerkezete. Szerkezeti hierarchia. A fehérjék építőkövei az aminosavak. Fehérjék felosztása
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Fehérjék felépítése és struktúrája. Aminosav oldalláncok. A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel
 Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
Fehérjék. SZTE ÁOK Biokémiai Intézet
 Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ENZIMSZINTŰ SZABÁLYOZÁS
 ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK. Rausch Péter kémia-környezettan
 AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK Rausch Péter kémia-környezettan Hogy viselkedik az ember egyedül? A kémiában ritkán tudunk egyetlen részecskét vizsgálni! - az anyagi részecske tudja hogy kell
AZ ANYAGI HALMAZOK ÉS A MÁSODLAGOS KÖTÉSEK Rausch Péter kémia-környezettan Hogy viselkedik az ember egyedül? A kémiában ritkán tudunk egyetlen részecskét vizsgálni! - az anyagi részecske tudja hogy kell
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Gáspári Zoltán. Élő molekulák az élet molekulái
 Gáspári Zoltán Élő molekulák az élet molekulái Invokáció Kajtár Márton 1929-1991 www.eotvoskiado.hu Élő és élettelen? Élő és élettelen: a kemoton Élő kémiai rendszer, de nem élőlény (Gánti, 1975) Autokatalitikus
Gáspári Zoltán Élő molekulák az élet molekulái Invokáció Kajtár Márton 1929-1991 www.eotvoskiado.hu Élő és élettelen? Élő és élettelen: a kemoton Élő kémiai rendszer, de nem élőlény (Gánti, 1975) Autokatalitikus
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Élettan. előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45
 Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Bioinformatika 2 5.. előad
 5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Bevezetés a bioinformatikába. Harangi János DE, TEK, TTK Biokémiai Tanszék
 Bevezetés a bioinformatikába Harangi János DE, TEK, TTK Biokémiai Tanszék Bioinformatika Interdiszciplináris tudomány, amely magába foglalja a biológiai adatok gyűjtésének,feldolgozásának, tárolásának,
Bevezetés a bioinformatikába Harangi János DE, TEK, TTK Biokémiai Tanszék Bioinformatika Interdiszciplináris tudomány, amely magába foglalja a biológiai adatok gyűjtésének,feldolgozásának, tárolásának,
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
1b. Fehérje transzport
 1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások
 Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
Nevezze meg a jelölt csontot latinul! Name the bone marked! Nevezze meg a jelölt csont típusát! What is the type of the bone marked?
 1 Nevezze meg a jelölt csontot latinul! Name the bone marked! 2 Nevezze meg a jelölt csont típusát! What is the type of the bone marked? 3 Milyen csontállomány található a jelölt csont belsejében? What
1 Nevezze meg a jelölt csontot latinul! Name the bone marked! 2 Nevezze meg a jelölt csont típusát! What is the type of the bone marked? 3 Milyen csontállomány található a jelölt csont belsejében? What
Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis
 Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
9. Előadás. Fehérjék
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E. Fischer : Gly-Gly 1932 Max Bergman és Leonidas Zervas : Benziloxi-karbonil csoport 1963 B. Merrifield : Szilárd fázisú
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E. Fischer : Gly-Gly 1932 Max Bergman és Leonidas Zervas : Benziloxi-karbonil csoport 1963 B. Merrifield : Szilárd fázisú
 A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Altalános Kémia BMEVESAA101 tavasz 2008
 Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK)
 BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK) 1. Keresse meg a baloldali oszlopban található fehérje szerkezeti szintekre jellemző a jobboldali oszlopban lévő
BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK) 1. Keresse meg a baloldali oszlopban található fehérje szerkezeti szintekre jellemző a jobboldali oszlopban lévő
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Kémia. Tantárgyi programjai és követelményei A/2. változat
 5. sz. melléklet Kémia Tantárgyi programjai és követelményei A/2. változat Az 51/2012. (XII. 21.) számú EMMI rendelethez a 6/2014. (I.29.) EMMI rendelet 3. mellékleteként kiadott és a 34/2014 (IV. 29)
5. sz. melléklet Kémia Tantárgyi programjai és követelményei A/2. változat Az 51/2012. (XII. 21.) számú EMMI rendelethez a 6/2014. (I.29.) EMMI rendelet 3. mellékleteként kiadott és a 34/2014 (IV. 29)
NMR a peptid- és fehérje-kutatásban
 NMR a peptid- és fehérje-kutatásban A PDB adatbázisban megtalálható NMR alapú fehérjeszerkezetek számának alakulása az elmúlt évek során 4000 3500 3000 2500 2000 1500 1000 500 0 1987 1988 1989 1990 1991
NMR a peptid- és fehérje-kutatásban A PDB adatbázisban megtalálható NMR alapú fehérjeszerkezetek számának alakulása az elmúlt évek során 4000 3500 3000 2500 2000 1500 1000 500 0 1987 1988 1989 1990 1991
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Prológus helyett polimorfizmus kapcsolodó-mutációk
 Prológus helyett polimorfizmus kapcsolodó-mutációk egy vesebetegség öröklésének vizsgálata során rámutattak, hogy hogyan okozhatnak gyakori genetikai variánsok ritka betegséget. Jó hír ez, mivel segíthet
Prológus helyett polimorfizmus kapcsolodó-mutációk egy vesebetegség öröklésének vizsgálata során rámutattak, hogy hogyan okozhatnak gyakori genetikai variánsok ritka betegséget. Jó hír ez, mivel segíthet
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
4. FEHÉRJÉK. 2. Vázanyagok. Az izmok alkotórésze (pl.: a miozin). Inak, izületek, csontok szerves komponensei, az ún. vázfehérjék (szkleroproteinek).
 4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
4. FEÉRJÉK 4.0. Bevezetés A fehérjék elsısorban α-l-aminosavakból felépülı biopolimerek. A csak α-laminosavakat tartalmazó fehérjék a proteinek. evüket a görög proteios szóból kapták, ami elsırangút jelent.
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
