Dr. Róka András. Az építészet rövid történetének kémiai háttere
|
|
|
- Regina Kisné
- 7 évvel ezelőtt
- Látták:
Átírás
1 Szki Szki Dr. Rók András Az építészet rövid történetének kéii háttere A házkt, középületeket, teplookt, plotákt, várkt (gyerekkori játékidhoz hsonlón) kisebb egységekbl, épít eleekbl illesztették össze. Az els próbálkozások után hr rájöhettek, hogy z összetrtáshoz kötnyg is szükséges. Egészen XVIII -XIX. százdig, vs, ceent ngyüzei elállításáig, beton és vsbeton lklzásáig, z eberiség terészetben tlálhtó nygokt hsznált fel z építészetben. Az eber elbontott és elhordt hegyeket, hogy áshol és ásképpen rkj össze. Úgy 4.5 illiárd éve, Föld kilkulás kezdetén z nygok olvdás- és forráspontjuk, vlint srségük lpján elkülönültek egyástól. A ngyon lcsony olvdás- és forráspontú, szerkezetüket tekintve olekulrácsos eleek és vegyületek gáz fázisbn rdtk. Ezek lkották z si légkört. (Feltételezések szerint szén-dioxid, etán, óni, kén-hidrogén, vízgz, nitrogén és neesgázok.) Az si Föld kkoribn egy izzó, kolvdék bolygó volt. Anyg leginkább vulkánkitörések lklávl felszínre kerül lávához hsonlított. A grekciók áltl terelt h folytosn elegen trtj Föld belsejét. Ennek köszönheten kéreg ltt elhelyezked gköpeny is olvdék. A hideg világr zonbn elnyelte felszín áltl kisugárzott ht. Ezért felszín hérséklete fokoztosn csökkent. A kis srségük itt felszínre szoruló, többnyire ionrácsos vegyületek z olvdáspontjuknk egfelel hérsékleten elkezdtek kikristályosodni, st összekristályosodni. Így lkult ki z z elsdleges ásványtársulás (vgy prier kzet), i kéreg legöregebb röghegységeit lkotj. Mire z eber építkezni kezdett, felszínt foráló folytok sok helyen átlkították z si kzetet. A kontinentális leezek vándorlás, vulknizus, hérsékletingdozás, szél és víz okozt erózió, vízben oldott nygok okozt állás, jd terjeszked élvilág szinte együtt és egyszerre fejtette ki roboló és épít htását. Ennek egfelelen kzeteket háro típusb soroljuk: vulkáni vgy g eredetek gás kzetek. Az erózió és állás során keletkez szecsék, továbbá z elpusztult éllények eszes vázánk kiülepedésével és elkövülésével képzdnek z üledékes kzetek. E két fjt kzettípus összetétele és szerkezete ngyértékben változht hérséklet és/vgy nyoás változásánk htásár. Az ilyen átlkulást szenved kzeteket nevezzük etorf kzeteknek. Az építnygot keres eber ezekkel kzetekkel tlálkozott, egunkálhtóságuk szerint ezekbl válogthtott. A földkéreg hierrchiáj I. Kéii foglk eleek szigorú vegyülési rányok vegyületek változó rányok keverékek Ásvány- és kzettni foglk kzetlkotó eleek ásványok kzetek ásványtársulások (ásványok keveréke) A Föld si kérge ngy vlószínséggel periódusos rendszer összes eleét trtlzt. Az építészet szepontjából terészetesen legngyobb ennyiségben tlálhtó ásványi nygok jöhettek száításb. A kéreg leggykoribb kzetlkotó eleei következk: oxigén, szilíciu, luíniu, klciu, gnéziu, nátriu, káliu, vs, titán, szén. A kéreg igen eltér tuljdonságú kzetlkotó eleei többnyire ionrácsos vegyületeket lkotnk. Ezek közül leggykoribbk z oxidok és sók. A sók közül csk vízoldhttln krbonátok és szilikátok jöhetnek száításb.
2 Szki Szki *A többnyire ionrácsos vegyületek képletei csk vegyülési rányokt fejezik ki. Az építészet fejldését érnöki tlálékonyság ellett fiziki és kéii iseretek fejldése tette lehetvé. Aíg z építény felállítás sttiki isereteket kívánt, z építés technológiáj ögött nygiseret, szerszákészítés és néhány egyszer kéii folyt iserete húzódik. Az építészet lpjit, kötnygit tuljdonképpen ár z ókorik jól iserték. A szerszáok tökéletesedése, egy-egy nyg újszer lklzás, vgy újbb építnygok egiserése inkább stílusjegyekben iserhet fel. Meglit építészetben ne volt szükség kötnygr. A több tonnás képítkockákt többnyire súlyukból ered tpdás trtj össze, de pontos illeszkedést olykor ( LEGO-ból isert) cspokkl biztosították. Stonehenge egyenetlen köveihez képest gizi pirisok szinte szbályosr vágott khsábji, vgy krnki Áon-teplo hengeresre csiszolt óriásoszlopi árulkodnk szerszáok és kegunkálás fejldésérl. A eglit építészetben viszonylg könnyen hsdó, vághtó, csiszolhtó köveket kerestek, int például z üledékes hookk, észk, vlint gás eredet gránit. Érdekes, hogy döngöléssel, tpsztássl készült sárkunyhók esetében z gygszecséket éppúgy tpdás trtj össze, int eglit építényeket. Ezek z erk zonbn ikroszkopikus éret szilikátkristályok felületi kölcsönhtásánk, felületén elhelyezked részecskék vonzásánk köszönhet. A kben szegény helyeken, int például Mezopotáiábn és Mexikóbn, ikrokristályok kölcsönhtásán lpult z építészet. Agygból kis éret építkockákt, téglákt készítettek, elyeket kezdetben npon szárítottk, késbb ki is égettek. A téglák kötéséhez ár i.e körül (oltott észbl és hookból álló) hbrcsot hsználtk. A fzeks esterség fejldésével z építészetben is egjelentek kiégetett, jd ázs gygcserepek, téglák, elyeket tetfedésre és flk díszítésére hsználtk. A díszíteleekkel egjelent burkolás. Kötnygként bituent, vgy hbrcsot hsználtk. A görögök és róik építészetében egjelent ngy teherbírású, égis könnyen egunkálhtó észk-ódosult, etorf típusú árvány. Így z oszlopok kecsesebbekké és díszesebbekké válhttk. (Prthenon, Athén, i.e , hbrcs nélkül illesztett árványtöbök) A rói építészetben z etruszkok nyoán igénnyé válik bels építészet. A csiszolt k és árványburkolt ellet egjelenik bels vkolás ( flzó hbrcshoz képest finobb szecseéret ész- vgy gipszhbrcs). A rói építészet ásik fontos jellezje vulkáni eredet építnygok lklzás. A képítészetben vulkáni gázok áltl hbosított, porózus szerkezet tuf. Egészen XIX. százdig egyedül álló újításnk száított betonozás eldje, terészetes ceent (puccolán) lklzás. A víz htásár fokoztosn egszilárduló ssz (k vgy tégltörelékkel kevert vulkáni hu) lehetvé tette például kupol építését. Ezzel elször született eg z oszttln, tágs bels tér (Ró, Pntheon). A középkori várkhoz hsonlón védeli jelleget suglló, robosztus roán (rói) stílushoz képest gsb tör gótik könnyszerkezetes képítészetnek tekinthet. A ngy teherbírású árvány lklzásávl kecsesebbé váltk trtó pillérek, necsk ngyobbr, hne gsbbr épültek teplook. A siár csiszolt, olykor színes árvány ne igényelt vkolást. A pillérek teherentesítették flkt, így zokr blkot vághttk. Így
3 Szki 345 onuentális gótikus ktedrálisokb ár beengedhették fényt. A kiséret, színezett üveglpokt ólokerettel vgy kcsipkével ngyéret ozikokká, rózsblkokká fogták össze. A reneszánsz inkább z építészeti technikák szintézise. Követ, téglát, árványt, üveget, kötnygot, vkolást és burkolást egyszerre lklzott. Mesteri szintre eelkedett bels vkolás. A több réteg, rétegenként különböz összetétel vkolton egjelentek z óriási flfestények, freskók vgy seccók. (Michelngelo: Szent-Péter székesegyház, Vtikán). A brokk építészet újdonság gipsz belsépítészeti lklzás. Az idigényes kszobrásztot felváltott gyors, foráb önt sokszorosítás, gipszstukkók készítése. Áltlánossá válik z üvegezés. A klsszicizus és rontik egyúttl ngyüzei vs-és üveggyártás kor. Ezért egyre ngyobb szerephez jut z öntött- és kovácsoltvs, és z üveg. Az összefügg sík üvegfelületen keresztül ég több fény árdt z építényekbe. A fény száár szinte teljesen átjárhtó építények sokáig egyedül álló változt londoni Kristályplot volt. A vsvázt síküveg fedte. (Joseph Pxton, ). Hsonló éret, kuttó üvegházt csk között építettek Arizonábn (Bioszfér II. USA Arizon, Tucson). Az építészek szbdság, fntáziájuk szárnylás ceent ngyüzei elállításávl, beton, jd vsbeton felfedezésével vlósulhtott eg. A vsbeton lklzás tette lehetvé gsság legyzését, felhkrcolók és TV tornyok verseng építését, továbbá z olyn egzotikus forák egjelenését, int Gudi befejezetlen szibolikus ktedrális, Sgrd Fili Brcelonábn, vgy Jorn Utzon vitorlás hjók ihlette, kgylóhéjkr elékeztet operház Sydneyben.
4 346 Gondolkodó GONDOLKODÓ MIÉRT? (WHY? WARUM?) Alkotó szerkeszt: Dr. Rók András Ebben rovtbn áltltok is jól isert jelenségek, vgy otthon is elvégezhet kísérletek gyráztát várjuk el tletek. A feldtok egoldásávl inden korosztály próbálkozht, hiszen jelenséget különböz tudásszinten is lehet értelezni. Éppen ezért részegoldásokt is be lehet küldeni! A lényeg z iseretek ozgósítás, z önálló elképzelés bizonyító erej kifejtése. A kérdéseket (olykor) szándékosn foglzzuk eg indennpok nyelvén, hogy reényünk szerint inél inkább lényegre irányítsuk figyelet. Jó szórkozást és sikeres unkát kívánunk! A fori követelényeknek egfelel dolgoztokt nevezési lppl együtt következ cíen várjuk jnuár 12-ig postár dv: KÖKÉL Miért ELTE Fiskoli Kéii Tnszék Budpest Pf A klórolekul ugynúgy poláris, int hidrogénolekul, égis oldódik vízben. Miért? Mi hsonlóság és i különbség két olekul szerkezetében? 2. A szén-dioxid éppúgy szén- és oxigéntookból áll, int szén-onoxid. A szietrikus töltéseloszlás itt ugynúgy Gondolkodó 347 polárisnk tekintjük, int szén-onoxidot. Mégis oldódik vízben. Miért? 3. Egy áztln gyghenger guidugón keresztül egy közleked edénnyel vn kpcsoltbn. Az gyghengerre egy hidrogénnel telt fzpohrt helyezünk. A közleked edény ekkor hengeren belüli tér nyoásnövekedését jelzi. Miért ébred nyoáskülönbség, ikor küls és bels tér, vgyis hidrogén és leveg hérséklete és nyoás ráhelyezés eltt zonos, hiszen fzpohár nyitott. 4. Kcs vgy reális z techniki körökben terjed hír, hogy benzin olekulái képesek kölcsönhtásb lépni ágneses térrel? Trtlznk-e olyn részecskéket szénhidrogénolekulák, elyek ágneses sjátsággl rendelkeznek? 5. Az égés feltételeinek egiserése során zvrb ejt tpsztlt volt, hogy lpor légritkított térben is égett. A lpor hevítés htásár szén-dioxidot trtlzó lobik lján is lángr lobbn. Miért? 6. Az utó - versenyutó tuning terjed változt nitro vgy nitróz lklzás, i dinitrogén-oxid fedneve. A könnyen cseppfolyósíthtó dinitrogén-oxidot z üzenyggl együtt fecskendezik otor hengereibe. Mi lehet z ok teljesítény növekedésének? 7. A versenyutók, repülgépek sebessége ögött éppúgy z égés sebessége rejlik, int gyerty esetében. A vdászgépek felszálláskor egy-egy hjtó ásodpercenként több int 1 liter kerozint fogyszt. Hogyn biztosítják z égés feltételét? Mi hsonlóság, és i különbség gyerty égése és hjtóvek ködése között? 8. Igz-e z, hogy benzinhez, illetve gázoljhoz kis ennyiségben kevert víz otorbn hidrogénre és oxigénre bolik, és otor z így keletkezett durrnógáz robbnó erejét is hsznosítj?
5 348 Gondolkodó Feldtok kezdknek Alkotó szerkeszt: Tóth Albertné A fori követelényeknek egfelel dolgoztokt következ cíen várjuk jnuár 12-ig postár dv: KÖKÉL Feldtok kezdknek Irinyi János Gináziu és Szkközépiskol 4024 Debrecen Irinyi utc 1. K96. A fénykép egy ikroszkóp lencséje ltt lév ngán-oxlát kristályról készült. A vegyület 38,43 /% Mn-t, 44,77 /% oxigént és 16,80 /% szenet trtlz..) Htározd eg kristályvíz entes ngán-oxlát képletét! b.) A ngán-oxlát sój sósksvként is isert kétérték oxálsvnk. Ez sv szilárd hlzállpotú és kristályvízzel kristályosodik. Az oxálsv : kristályvíz nygennyiség rány eghtározás céljából szárítószekrényben kiszárítottunk 1-1 vegyszeres knálnyi kristályos oxálsvt. Htározd eg kristályos sósksv összegképletét táblázt érési eredényei lpján! Id: Cselekvés /velet I. int II. int Méredények töegének leérése 35,40 g 35,88 g Méredény+kristályos oxálsv töege 39,41 g 38,89 g Szárítás szárítószekrényben 105 C-on A inták kihlése exszikkátorbn A vízentes oxálsv+edények töege 38,26 g 38,03 g Gondolkodó 349 K97. Vlely iseretlen vegyület lkálifé-, és hlogenid ionokból áll. Az lkotó took közül ngyobb elektronegtivitású tonk 4-szer ngyobb z elektronvonzó képessége, int ásik toénk. A két to elektronegtivitásánk különbsége: 3..) Mennyi vegyületet lkotó took elektronegtivitás? b.) Miért nevezetes két to EN értéke? c.) Mi kérdéses vegyület képlete és neve? d.) A feldtbn szerepl kétféle to (illetve ele) indegyike különkülön is lkot vegyületet H-nel. Mi z összetételük és i nevük ezeknek vegyületeknek? Milyen hlzállpotúk? e.)hogyn gyrázzuk zt tényt, hogy hidrogén-hlogenid srsége várkozássl szeben ne kisebb, hne ngyobb leveg srségétl? K98 A tudoány nyelve z ngol kcentussl vélekedik Oláh György Nobel-díjs kéikus, ki sját szkterületén is egtpsztlhtt ezt különböz nezetiség kuttókkl vló (sikeres) együttködésben.. A szénvegyületek pozitív töltés ionjink ( krboktionoknk) z elállításához hsznált rendkívül rekcióképes svk,z un.. szupersvk közül is kitnik egy, ely ágikus sv cíet viseli. Htározd eg ennek bizonyos ágikus svnk z összetételét! Az áltlánosn FSO 3 HMeF x - nek jelölt képletben z Me egy iseretlen féet,z x egy eghtározndó index száot jelöl.a ágikus sv fé-ion trtl 38,43 töegszázlék, illetve 8,33 ól%.. K99. A Lidocin érzéstelenítt elször 1946-bn állították el. A Lidocin szenet, hidrogént, nitrogént és oxigént trtlz.111 g Lidocin elégetésével 286 g CO 2 gáz keletkezik. Htározd eg vegyület összegképletét, iserve, hogy vegyület nitrogéntrtl 12,61 /%, oxigéntrtl 7,21 /%. Dr. Kéki Sándor, Debreceni Egyete K100. Zöld Kéii szepontból indokolt volt z nygok elállításár, keletkezésére vontkozón bevezetni környezeti fktor foglát. A környezeti fktorrl z 1kg végterékre es hulldék töegét djuk eg kg egységben. Az lábbi rekciókbn közös vonás, hogy indegyikben CCO 3 keletkezik Tekintsük ezt célteréknek, többit hulldéknk! A rekcióegyenletek tábláztb történ beírás után htározd eg folytok környezeti (f) fktorát!
6 350 Gondolkodó A folyt neve: Rekcióegyenlet: Fktor(f) Keényvíz(CCl 2 ) szódás vízlágyítás A cseppkképzdés folyt A eszelt fl szárdás Égetett ész és széndioxid rekciój Olvsány A Zöld Kéi 12 pontj 1. Megelzés (A hulldék keletkezésének egelzése késbbi egseisítése helyett) 2. Mxiális nygfelhsználás(törekvés ellékterékek képzdésének visszszorításár.) 3. A legkevésbé veszélyes rekció keresése:(a régi és z új nygok környezetre ne ártlsk.) 4. A legkevésbé érgez nygok tervezése:( A célterék érgez htás inél kisebb legyen.) 5. Környezetbrát oldószerek és segédnygok hsznált: (Segédnygok inilizálás) 6. Az energifelhsználás csökkentése:(közönséges hérsékleten és nyoáson enjenek végbe) 7. Megújuló nyersnygok hsznált:(lehetleg egújuló nyersnygokt hsználjunk fel). 8. A szárzékkészítés csökkentése: (A gyártásközi és ellékterékek elállításánk csökkentése.) 9. Ktlizátorok hsznált: (A szelektív ktlizátorok elnyösek ngy ennyiségben hsznált regensekkel szeben.) 10. Leboló nygok tervezése: (A terékek bolás során keletkez nygok környezetre ártltlnok legyenek.) 11. Állndó ellenrzés:(új nlitiki ódok lklzásávl veszélyes nygok képzdésének idben történ észlelése.) 12. A vegyipri blesetek vlószínségének csökkentése:(anygok, technológiák kiválsztás.) Gondolkodó 351 ROSSZUL OLDÓDÓ SÓK OLDHATÓSÁGI EGYENSÚLYAI Igz Srolt Bevezetés Száos péld uttj, hogy egy dott hérsékleten (és nyoáson) egy dott oldószer csk eghtározott ennyiség nygot képes oldtbn trtni (telített oldt), de ez ennyiség z oldndó nyg inségétl függ. A vízben jól oldódó vegyületek oldhtóságát áltlábn 100 g oldószerre vontkozttv dják eg. Ez z összefoglló vízben rosszul oldódó vegyületek, vgy közisert nevükön cspdékok oldódásánálkiválásánál kilkuló heterogén egyensúlyi rendszer törvényszerségeivel fogllkozik. Az oldhtósági szorzt (L) M A szilárd nyg -ely rosszul oldódó cspdék- és felette lev oldt között dinikus egyensúly áll be: M A (sz) M A (q) M + + A Mivel cspdékok áltlábn ers elektrolitok, z oldott olekulák (M A (q) ionpárok ) jól disszociálnk. Az egyszerbb jelölés érdekében továbbikbn M + ktiont M-el, A niont A-vl jelöljük. A teljes folytr felírv z egyensúlyi állndót: K = [ M] [ A] [ MA ] sz A telített oldt koncentrációj független fel ne oldódott vegyület ennyiségétl (indegy, hogy néhány sze kristály vgy 100 g fel ne oldódott nyg, ettl független z oldhtóság) így szilárd nyg koncentrációját (ktivitását) egységnyinek vehetjük. Az egyensúlyi állndó szorzttá lkul: L = [ M ] [ A] Ezt szorztot nevezzük oldhtósági szorztnk. Az oldhtósági szorztbn, cskúgy int vlennyi egyensúlyi állndóbn z egyensúlyi koncentrációk szerepelnek. Mértékegysége: (ol/d 3 ) +
7 352 Gondolkodó Az oldhtósági szorzt értéke (int inden egyensúlyi állndóé) terészetesen függ hérséklettl, de dott hérsékleten állndó. A levált cspdék gykrn átkristályosodik, ódosultváltozás történik, így egváltoznk z oldhtósági viszonyok, ezért ne inden esetben egyezik eg cspdék leválásánál és feloldódásánál érvényes oldhtósági szorzt. Például NiS α-ódosultánál L=1, β- ódosultánál L=1, A cspdék leválásánál α-ódosult keletkezik, így ersen svs oldtból ne lehet leválsztni cspdékot, de seleges közegben leválsztott cspdék ne oldhtó fel ersen svs közegben, ert β-ódosulttá lkul. Az oldhtóság (S) A cspdékok oldhtóságát telített oldt koncentrációjávl (ol/d 3 ) jelleezhetjük, jele: S Mivel z oldhtósági szorzt és z oldhtóság között ne egyenes z rányosság, z oldhtósági szorzt értéke csk zonos típusú cspdékok oldhtóságánk összehsonlításár lkls. pl: AgCl: L=1, S=1, AgBr: L=7, S=8, Ag 3 PO 4 : L=1, S=1, CSAPADÉKOK OLDÓDÁSA TISZTA VÍZBEN Az M A cspdék oldhtósági szorzt: [ M] [ A] L = H S ol/d 3 cspdék oldhtóság, kkor S ol/d 3 koncentrációbn keletkezik z M ktion S ol/d 3 koncentrációbn keletkezik z A nion. M A M + A S S S ol/d 3 ol/d 3 ol/d 3 Gondolkodó 353 Az ion koncentrációj: [M] = S [A] = S Ezt visszhelyettesítve z oldhtósági szorztb: L = + ( S ) ( S ) = S Az egyenletbl z oldhtóság könnyen száíthtó: = S + L Az oldhtóság egdj telített oldt koncentrációját ( szilárd fázis feloldódott részét). A késbbiek során tiszt vízben száított oldhtóság jelölésére z S víz forát hsználjuk, hogy összehsonlíthtó legyen z egyéb körülények között száított oldhtósággl. A CSAPADÉKOK OLDHATÓSÁGÁT BEFOLYÁSOLÓ TÉNYEZK A cspdékok oldhtóságát száos tényez befolyásolj, ezek közül legfontosbbk: sját ionok htás ph htás koplexképzés idegen ionok htás Most z els háro befolyásoló htássl fogllkozunk részletesebben. SAJÁT IONOK HATÁSA AZ OLDHATÓSÁGRA A cspdék felépítésében résztvev ionok feleslegének htását z oldhtóságr sját ion htásnk nevezzük. A töeghtás törvényének értelében cspdék oldódás visszszorul: M A (sz) M + A Ez z oldhtóság csökkenését vonj g után. Vizsgáljuk eg M A cspdék oldhtóságát C M koncentrációbn lév M ktiont trtlzó oldtbn (pl.mx-oldt):
8 354 Gondolkodó S ol cspdék 1 d 3 oldtbn történ oldódáskor S ol M ktion és S ol A nion keletkezik. Így cspdékot felépít ionok koncentrációj: [M] = S + C M [A] = S Ezt visszhelyettesítve z oldhtósági szorztb: L = [ M] [ A] = ( S + C ) ( S ) Az estek többségében S << C M, így z oldhtósági szorzt: L = (C M ) ( S) Az egyenletbl z oldhtóság kifejezhet: 1 L CM S =. Vigyázt, h C M értéke összeérhet koncentrációvl, kkor ne hsználhtó ez z egyszersített for! H z oldhtóságot C A koncentrációbn jelenlév A nion oldtábn vizsgáljuk és S <<C A, kkor 1 L CA S =. Áltlábn tehát sját ionnk oldhtóságot csökkent htás vn (kivétel koplexképzés)! M Gondolkodó 355 A ph HATÁSA A CSAPADÉK OLDHATÓSÁGÁRA A ph, vgyis z oxóniu-ion koncentráció, többféle ódon befolyásolhtj cspdék oldhtóságát: hidroxid cspdékok esetén, ivel z oxóniu-ion koncentráció egyértelen eghtározz hidroxid-ion koncentrációját, sját ion htásként vehetjük figyelebe ph htását. H n ph, cspdék oldhtóság csökken. (kivétel hidroxokoplex képzk esete) ph terészetesen htássl vn ktion hidrolízisére. Pl. egy ph=7,00 oldtbn BiI 3 cspdék oldódásából keletkez Bi 3+ -ionok hidrolizálnk, így lecsökken Bi 3+ -ion koncentráció, i BiI 3 oldhtóságánk növekedését eredényezi. ph htás érvényesül bbn z esetben is, ikor pl. cspdék nionj sv htásár inségi átlkulást szenved pl.: 2 PbCrO 4 +2 H + 2 Pb 2+ + Cr 2 O H 2 O A keletkez cspdék oldhtóság növekedhet zért is, ert keletkez nion koncentrációj protonálódás következtében lecsökken (CO 3 2 cspdék, HCO3 ne). Ez kkor következik be, h cspdék nion brønstedi érteleben bázis (gyenge sv svrdék). Az oldhtóság ph függése ltt elssorbn ez utóbbi típusb sorolhtó eseteket értik. A következkben beuttásr kerül száítások ilyen típusú cspdékok oldhtóságánk ph függését írják le. Egy MA típusú cspdék oldhtóság, hol z oldódás itt keletkez A nion egy gyenge sv svrdék (konjugált bázis), z oldt oxóniu-ion koncentrációjától függ. MA (sz) M + + A A + H 3 O + HA + H 2 O A cspdék oldódásávl oldtb került nionok részben protonálódnk, így z nion koncentráció lecsökken s z egyensúly eltolódás itt több
9 356 Gondolkodó cspdék oldódik, vgyis z oxóniu-ion koncentrációjánk növelésével n cspdék oldhtóság. Az oldhtósági szorzt: L = [M + ] [A ]. A cspdék oldódáskor keletkez féionok változtln forábn rdnk, de z nionok egy része protonálódik, így részben A, részben HA forábn lesz jelen. H S ol/d 3 cspdék oldhtóság, kkor S ol/d 3 koncentrációbn keletkezik M + ktion és S ol/d 3 koncentrációbn keletkezik A nion, de ez részben protonálódik. MA M + + A +HA Az oldhtóság tehát: hol S ol S ol S ol S = [M + ], illetve S = [A ], [A ] = [A ] + [HA] *, vgyis cspdékból szárzó nion teljes koncentrációj (különböz értékben protonált foráibn). HA koncentrációját kifejezhetjük svi disszociációs állndóból: K s H O A + 3 = [ HA] [ HA] Ezt behelyettesítve csillggl jelölt egyenletbe + H3O A =. K + + H [A 3O H3O ] = A A A 1 + K = +. s Ks A szorzt ásodik tgj z isert α H függvény, így ibl [A ] = [A ] α H, s Gondolkodó 357 A S A = =. α α Visszhelyettesítve z ionkoncentrációkt z oldhtósági szorztb: H L = [M + ] [A ] = S L = α 2, H H S S α Bevezethetünk egy úgynevezett látszólgos oldhtósági szorztot: L = L α H = S 2, S = L Így z oldhtóság ár jól isert törvényszerségek lpján könnyen száíthtó látszólgos oldhtósági szorztból (1:1 cspdék esetén). M A cspdékr, h A nion H n A gyenge sv svrdék, hsonló egfontolások lpján ( töltések ellzésével): M A M + (A+HA+H 2 A+ +H n A) S ol S ol S ol Az ionkoncentrációknk z oldhtósággl vló összefüggése: illetve hol [M] = S, [A ] = S, [A ] = [A] + [HA] + + [H n A]. A cspdék nionjából szárzó ionok és olekulák H n A sv disszociációs állndóiból kifejezhetk: H
10 358 Gondolkodó vgyis [A - ], [ ] [ H3O ] [ H3O ] [ H3O ] = A 1+ K sn + K z egyensúlyi nion koncentráció: sn K sn 1 [A] = [A] α H + + K [ A], [ A] = vgy [ A] α H sn K sn 1 = S α H n K Az ionkoncentrációkt visszhelyettesítve z oldhtósági szorztb: L = ( S ) = S S α H α H + Itt is bevezethetünk egy látszólgos oldhtósági szorztot:, L = L H + ( α ) = S Láthtó, hogy látszólgos oldhtósági szorztból pontosn ugynúgy száolhtjuk z dott ph-n z oldhtóságot, int z oldhtósági szorztból tiszt vízben vló oldhtóságot. ( α ), L L + S + H = = S L = + A szorzt els tgját ár egisertük tiszt vízben száolt oldhtóságnál, vgyis cspdék oldhtóság cspdék tiszt vízben száolt oldhtóságánk -szoros. αh α H s1, Gondolkodó 359 Mivel α H értéke z oxóniu-ion koncentrációtól függ, így z oldhtóság is. Minél ngyobb z oxóniu-ion koncentráció, nnál ngyobb z α H (α H 1!) és nnál ngyobb z oldhtóság. Az α H függvényt disszociációs állndókkl kifejezve (H n A svr): H O H O H O αh = K K K K K K sn sn sn 1 sn sn 1 s1 Terészetesen függvényt protonálódási állndókr is felírhtjuk pl. H 3 A sv esetén: A protonálódási állndók: K K K 2 HA 1 = = K p1 3 + A H3O s3 = = K H2A 1 p2 2 + HA H3O p3 [ ] s2 disszociációs állndók: 3 + A H3O K s 3 = 2 K s2 n HA 2 + HA H3O = H2A + H3A 1 H2A H3O K + s1 = H2A H3O K s1 [ H3A] = = Az utolsó disszociációs állndó reciprok tehát egegyezik z els protonálódási állndóvl. Az utolsó eltti disszociációs állndó reciprok tehát egegyezik ásodik protonálódási állndóvl. Így terészetesen z α H függvényt felírhtjuk protonálódási állndókkl is: α H = 1+K p1 [H 3 O + ] + K p1 K p2 [H 3 O + ] K p1 K p2 K pn [H 3 O + ] n
11 360 Gondolkodó KOMPLEXKÉPZDÉS HATÁSA A CSAPADÉK OLDHATÓSÁGÁRA H cspdék ktionj koplexképzési rekcióbn vesz részt, kkor z oldhtóság növekszik, st ne egyszer olyn értékben, ely cspdék oldódásához vezet. Az oldhtóság növekedését szbd féionok koncentrációjánk csökkenése idézi el, elyet lépcszetesen kilkuló koplexek okoznk. A koplexképzésnek két fjtáját célszerû egkülönböztetni: -koplexképzdés idegen ligndul: pl. AgCl + 2NH 3 [Ag(NH 3 ) 2 ] + + Cl -koplexképzdés sját ion felesleggel: pl. BiI 3 +I BiI 4., Koplexképzdés idegen ligndul Az oldtb vitt lignduot L-lel jelölve, cspdék (M A ) oldódásából keletkez féionok egy része különböz koordinációs száú koplexek forájábn vn jelen. H cspdék oldhtóság S ol/d 3, kkor S ol/d 3 koncentrációbn keletkezik féion, ely különböz koordinációs száú koplexeket lkot és S ol/d 3 koncentrációjú keletkezett nion. M A (M+ML+ML ML n ) + A S ol S ol S ol Az oldhtóság: [ M], S = illetve S = hol [M] jelenti cspdékból szárzó összes féion koncentrációját, beleértve különböz koordinációs száú koplexekben lévkét is. [ A] Gondolkodó 361 [M] = [M]+[ML]+[ML 2 ]+ +[ML n ] A teljes féion koncentrációt kifejezhetjük lépcszetes képzdési állndókból. A lépcszetesen kilkuló koplexek stbilitási állndói: M + L ML ML + L ML 2 ML n 1 + L ML n K = 1 K = K 2 n = [ ML] [ M] [ L] [ ML2 ] [ ML] [ L] [ MLn ] [ ML ] [ L] A teljes féion koncentráció lépcszetes képzdési állndókkl kifejezve: n 1 [M] = [M] (1 + K 1 [L] + K 1 K 2 [L] K 1 K 2 K n [L] n ) vgy z összesített (kuultív) képzdési állndókkl kifejezve: [M] = [M] (1 + β 1 [L] + β 2 [L] βn [L] n ) hol [L] ligndu egyensúlyi koncentrációját jelöli. A szorzt ásodik tgj z ún. α L függvény. A cspdék oldhtósági szorzt: [M] = [M] α L L = [M] [A] Behelyettesítve egfelel ionkoncentrációkt: S L = α L ( S)
12 362 Gondolkodó Bevezethetünk isét egy látszólgos oldhtósági szorztot: L = L α L L = S + vgyis látszólgos oldhtósági szorztból pontosn ugynúgy száolhtunk koplexképzés esetén, inth ne lenne koplexképzés. Az oldhtóság: Gondolkodó 363 Az oldhtóság sját ion felesleg esetén: L S = illetve S = [M] A [ ] hol [M] jelenti teljes féion koncentrációt, beleértve koplex forákbn lévkét is: [M] = [M] + [MA] (q) + [MA 2 ] + + [MA n ] A teljes féion koncentrációt kifejezhetjük koplex lépcszetes S = +, L képzdési állndóikból, vgy kár z összesített képzdési állndókból, így b., Koplexképzdés sját ion felesleggel: H cspdék féionj cspdék nionjávl képez koplexet, egy sjátos egyensúlyi rendszerrel tlálkozunk. A cspdék leválsztás során z nion koncentráció növelésével z oldhtóság egy iniuot fog uttni ( sját ion oldhtóság csökkent htás), jd növekedni fog ( koplexképzdés oldhtóság növel htás). Legyen MA cspdék, elynek M + ktionj A nionnl MA n xiális koordinációs száú koplexet képez. Vizsgáljuk eg cspdék oldódását A nion oldtábn: MA (sz) M + + A S ol/d 3 cspdék oldódás esetén S ol féion jut oldtb, ely részben szbd, részben különböz koordinációs száú koplexek forájábn lesz jelen, és S ol nion kerül z oldtb, de sját ion felesleg itt ár eleve vn z oldtbn cspdék nionjából, hiszen ez egyben koplexképz ligndu is. [M] = [M] (1 + K 1 [A] + K 1 K 2 [A] K 1 K 2 K n [A] n ) [M] = [M] (1 + β 1 [A] + β 2 [A] βn [A] n ) A szorztok ásodik tgj ár isert α L függvény, így A cspdék oldhtósági szorzt: [M] = [M] α L L = [M] [A] Behelyettesítve féion koncentrációt: S L = α L [ A] Bevezetve látszólgos oldhtósági szorztot: L = L α L L = S [A] Vgyis z nion egyensúlyi koncentrációjánk iseretében z oldhtóság száíthtó. A ktion teljes koncentrációj egegyezik z oldhtósággl, z nion teljes koncentrációj: [A] = [A] + [MA] (q) + 2 [MA 2] + + n [MA n ]
13 364 Gondolkodó Hsonló egfontolások lpján M A cspdék oldhtóságát is száíthtjuk sját ionnl történ koplexképzdés esetén. A cspdék oldódásából szárzó ktion különböz koordinációs száú koplexek forájábn vn jelen. [M] = [M] + [MA] + [MA 2 ] + + [MA n ] Az oldhtóság "A" sját nion feleslegében egegyezik ktion teljes koncentrációjánk -ed részével: Gondolkodó 365 S = L [ A] L S = α L, [ A] Vgyis ezen esetben z oldhtóság, koplexképzés nélküli sját ion felesleggel száolt oldhtóság α L -szerese. S = [ M], A teljes féion koncentráció z egyensúlyi koncentráció α L -szerese: Az oldhtósági szorzt: [M] = [M] α L L = [M] [A] Behelyettesítve egfelel ionkoncentrációkt: S L = αl [ A] Bevezetve látszólgos oldhtósági szorztot: L =L α L L = S [A] A látszólgos oldhtósági szorzt lklzás esetén pontosn úgy száolhtunk, inth csk sját ion felesleg lenne koplexképzés nélkül! Vgyis z oldhtóság: A vlóságbn ngyon ritkán tlálkozhtunk olyn esettel, ikor cspdék oldhtóság csk koplexképzktl függ. H cspdék nionj gyenge sv konjugált bázis (pl.: S 2, CO 3 2, PO 4 3 ), kkor z oldhtóság eleve ph függ. H koplexképz ligndu protonálódht, ely kevés kivételtl eltekintve (pl.: I, Br ) így is vn, z oldhtóság isét függ phtól. Így cspdék csupán koplexképzés közben vló oldódásánk száításár csk kevés esetben és egfelel egszorító feltételek ellett vn lehetség. Feldtok hldóknk Szerkeszt: Mgyrflvi Gábor és Vrg Szilárd (ggyrf@che.elte.hu, szilrd.vrg@bolyi.elte.hu) A fori követelényeknek egfelel dolgoztokt nevezési lppl együtt következ cíen várjuk jnuár 12-ig postár dv: KÖKÉL Feldtok hldóknk ELTE Kéii Intézet Budpest 112 Pf
14 366 Gondolkodó H96. Mérhengerrel kiértünk 100 c 3 15,0 töegszázlékos kénsvoldtot (srsége 1,102 g/c 3 ). Mennyi ugyncsk 15,0 töegszázlékos NOH oldtot (srsége 1,164 g/c 3 ) djunk hozzá, hogy seleges oldtot kpjunk? ( etilvörös és fenolftlein indikátor se vált benne színt, ph-j 5,5 és 8,5 között vn) Hogyn végezzük el kísérletet lbortóriubn? Ne feledkezzünk eg térfogtér eszközök érési pontosságáról! Mgyrflvi Gábor H97. 1,300 g BO 2 -ot szórunk 200,0 c 3 0,050 ol/d 3 -es kénsv oldtb. Hány g szilárd nyg rd vissz? Mennyi z egyes ionok koncentrációj z oldtbn? Mennyi z oldt ph-j? Az oldtot egsvnyítjuk és KI-ot dunk hozzá, jd kiváló jódot titráljuk 0,010 ol/d 3 -os tioszulfát oldttl. Mennyi fogyás? BSO 4 : L = 1, Vrg Szilárd H98. Két szilárd ele keverékébl veszünk háro 1,52 gros intát. Sósv-oldt feleslegével regálttv 0,896 d 3 norálállpotú gáz fejldik és 0,56 oldhttln nyg rd vissz. 10 töegszázlékos NOH-oldttl regálttv ugynnnyi gáz fejldik, de 0,56 g szilárd nyg rd vissz. Egy hrdik intát levegtl elzárv végzett gs hérséklet hevítés után sósvbn oldv keletkezett vegyület rdék nélkül feloldódik és 0,448 d 3 gáz fejldik. Ez utóbbi gázt egy 1 literes, légköri nyoású oxigénnel töltött edénybe vezetve egy rekció lejátszódás tpsztlhtó, i után z edényben nyoás hozzávetleg egytizedére csökken. Milyen rekciók játszódtk le? Száolásokkl igzoljuk! diákolipii feldt H99. Mekkor z oldhtóság ) tiszt vízben i. CSO 4 -nk; ii. CF 2 -nk; iii. Bi 2 S 3 -nk? b) 0,10 ol/d 3 -es KI-oldtbn Gondolkodó 367 i. z AgI-nk; ii. z PbI 2 -nk? CSO 4 : L = 2, CF 2 : L = 3, AgI: L = 8, PbI 2 : L = 1, lg 1 = 1,68 lg 2 = 3,00 lg 3 = 4,36 lg 4 = 4,76 Vrg Szilárd H100. ) Mekkor lehet xiálisn nnk NCl oldtnk koncentrációj, hogy zt 0,100 ol/d 3 koncentrációjú TlNO 3 - oldttl bárilyen térfogtránybn összeöntve ne váljon le TlCl cspdék? A térfogtokt tekintsük összedhtónk! Egy edénybe 1,00 c 3 0,100 ol/d 3 koncentrációjú TlNO 3 oldtot öntünk, jd belehelyezünk egy fé tlliu elektródot és egy Cl ionokr szelektív elektródot (ely lkls Cl ionok koncentrációjánk követésére), és két elektródot egy voltérvel összekötjük. Az így elkészített tlliu-nitrát oldthoz 0,030 ol/d 3 koncentrációjú NCl oldtot csepegtetünk. A térfogtokt tekintsük dditívnek! b) Ábrázoljuk levált TlCl cspdék nygennyiségét NCl oldt térfogtánk függvényében 0 4,00 c 3 térfogttrtoánybn, 0,10 c 3 -es lépésközzel! c) Ábrázoljuk z elektródokból létrejött glvánele elektrootoros erejét hozzádott NCl oldt térfogtánk függvényében, szintén 0,10 c 3 -es lépésközzel! A 0,00 c 3 -hez trtozó EME-t ne kell feltüntetni! Hogy lehet függvénygörbe egyes szkszink jellegét eggyrázni? TlCl: L = 6, A tlliu elektród potenciálját z lábbi képlettel htározhtjuk eg: ε (1) = 340 V + 59 V lg [Tl + ] A Cl ionszelektív elektród potenciálját pedig z lábbi képlet dj: ε (2) = V 59 V lg [Cl ] Benk Zoltán HO-40. ) 1 gr szilárd PbCl 2 -re 0,01 ol/d 3 N 2 SO 4 -oldtot öntünk és egvárjuk, hogy egyensúly álljon be. Hány c 3 lenne elvileg
15 368 Gondolkodó szükséges hhoz, hogy cspdék töegének pontosn fele PbCl 2 legyen? b) 1 gr szilárd PbSO 4 -r 0,01 ol/d 3 NCl-oldtot öntünk és egvárjuk, hogy egyensúly álljon be. Hány c 3 lenne elvileg szükséges hhoz, hogy cspdék töegének pontosn fele PbCl 2 legyen? PbSO 4 : L = 1, PbCl 2 : L = 2, Koároy Dávid HO-41. Mekkor BCrO 4 oldhtóság 9,0-es, illetve 5,0-ös ph-r pufferelt oldtbn? Mi z egyes krótrtlú részecskék koncentrációj különböz ph-kon? BCrO 4 : L =1, HCrO 4 = Cr 2 O H 2 O pk = 1,5 HCrO 4 = CrO H + pk 2 = 6,5 Vrg Szilárd HO-42. Összeöntünk 100,00 c 3 0,2 ol/d 3 NCl és 100,00 c 3 0,2 ol/d 3 AgNO 3 oldtot. ) Mi lesz kiváló cspdék töege és z oldt ezüstion koncentrációj! Ezt követen z oldtot kén-hidrogén gázzl telítjük és egvárjuk z egyensúly beálltát ([H 2 S] = 0,1 ol/d 3 ). b) Mi lesz z így kilkuló cspdék töege, /%-os összetétele, továbbá z oldt ezüst- és hlogenidion koncentrációj és phj! c) Mennyiben ódosulnk ezek z értékek, h z így kilkult rendszerhez 100,00 c 3 0,5 ol/d 3 NCl oldtot dunk? Egy ásik lobikbn összeöntünk 100,00 c 3 0,2 ol/d 3 NI és 100,00 c 3 0,2 ol/d 3 AgNO 3 oldtot, jd ezt is telítjük H 2 S-el. d) Végezzük el z és b pont száításit ezzel rendszerrel is! H 2 S: K 1 = 9, ; K 2 = 1, AgCl: L = 1, Ag 2 S: L = 1, AgI: L = 8, Klencsár Blázs
16 Kéi idegen nyelven 369 Kéi idegen 370 nyelven KÉMIA IDEGEN NYELVEN Kedves Diákok! Kéi ngolul Szerkesztı: McLen Ildikó Ngyon izgtottn váro ár, hogy egérkezzenek z elsı fordítások (lpzártkor Ti ég, gondolo buzgón fordítotok). Az elért eredényeiteket késıbbiekben feltétlenül figyelebe szeretné venni egfelelı szöveg kiválsztáskor. Hrosn ktuális lesz következı szöveg téáj: hópelyhek kéiáj. A szöveg elején könnyen tászkodhttok eglévı kéii és fiziki isereteitekre, de úgy érze néi újdonságot is sikerült becsepészni szövegbe. A fordítást következı círe küldjétek: kokelngol@gil.co esetleg hgyoányos levél forájábn: KÖKÉL Kéi idegen nyelven BME Két Tnítási Nyelvő Gináziu 1111 Budpest, Egry József utc Beküldési htáridı: jnuár 5. Íe, z izgls szöveg, elyhez jó unkát és egyben Áldott, békés Krácsonyt kívánok indnyájtoknk! Snowflke Cheistry Snowflkes re prticulr for of wter ice. Snowflkes for in clouds, which consist of wter vpor. When the teperture is 0 C or colder, wter chnges fro its liquid for into ice. Severl fctors ffect snowflke fortion. Teperture, ir currents, nd huidity ll influence shpe nd size. Dirt nd dust prticles cn get ixed up in the wter nd ffect crystl weight nd durbility. The dirt prticles ke the snowflke hevier, nd cn cuse crcks nd breks in the crystl nd ke it esier to elt. Snowflke fortion is dynic process. A snowflke y encounter ny different environentl conditions, soeties elting it, soeties cusing growth, lwys chnging its structure. Wht re coon snowflke shpes? Generlly, six-sided hexgonl crystls re shped in high clouds; needles or flt six-sided crystls re shped in iddle height clouds; nd wide vriety of six-sided shpes re fored in low clouds. Colder tepertures produce snowflkes with shrper tips on the sides of the crystls nd y led to brnching of the snowflke rs (dendrites). Snowflkes tht grow under wrer conditions grow ore slowly, resulting in soother, less intricte shpes. Why re snowflkes syetricl (se on ll sides)? First, not ll snowflkes re the se on ll sides. Uneven tepertures, presence of dirt, nd other fctors y cuse snowflke to be lop-sided. Yet it is true tht ny snowflkes re syetricl nd intricte. This is becuse snowflke's shpe reflects the internl order of the wter olecules. Wter olecules in the solid stte, such s in ice nd snow, for wek bonds (clled hydrogen bonds) with one nother. These ordered rrngeents result in the syetricl, hexgonl shpe of the snowflke. During crystlliztion, the wter olecules lign theselves to xiize ttrctive forces nd iniize repulsive forces. Consequently,
17 Kéi idegen nyelven 371 wter olecules rrnge theselves in predeterined spces nd in specific rrngeent. Wter olecules siply rrnge theselves to fit the spces nd intin syetry. Is it true tht no two snowflkes re identicl? Yes nd no. No two snowflkes re exctly identicl, down to the precise nuber of wter olecules, spin of electrons, isotope bundnce of hydrogen nd oxygen, etc. On the other hnd, it is possible for two snowflkes to look exctly like nd ny given snowflke probbly hs hd good tch t soe point in history. Since so ny fctors ffect the structure of snowflke nd since snowflke's structure is constntly chnging in response to environentl conditions, it is iprobble tht nyone would see two identicl snowflkes. If wter nd ice re cler, then why does snow look white? The short nswer is tht snowflkes hve so ny light-reflecting surfces they sctter the light into ll of its colors, so snow ppers white. The longer nswer hs to do with the wy the hun eye perceives color. Even though the light source ight not be truly 'white' light (e.g., sunlight, fluorescent, nd incndescent ll hve prticulr color), the hun brin copenstes for light source. Thus, even though sunlight is yellow nd scttered light fro snow is yellow, the brin sees snow s white becuse the whole picture received by the brin hs yellow tint tht is utoticlly subtrcted. Melting Snow nd Ice with Slt If you live in n re with cold nd icy winter, you hve probbly experienced slt on sidewlks nd rods, used to elt the ice nd snow nd keep it fro refreezing. Slt is lso used to ke hoede ice cre. In both cses, the slt works by lowering the elting or freezing point of wter. The effect is tered 'freezing point depression'. More Prticles Men More Melting Power Kéi idegen 372 nyelven Sodiu chloride isn't the only slt used for de-icing, nor is it necessrily the best choice. Sodiu chloride dissolves into two types of prticles: one sodiu ion nd one chloride ion per sodiu chloride 'olecule'. A copound tht yields ore ions into wter solution would lower the freezing point of wter ore thn slt. For exple, clciu chloride (CCl 2 ) dissolves into three ions (one of clciu nd two of chloride) nd lowers the freezing point of wter ore thn sodiu chloride. Here re soe other de-icing copounds: Cheicls Used to Melt Ice! # #! 2 ', $ ' #, $!!, #, 3 " " )1 " #!! -. #!! $ %%& ' ()* + /0' %.. 4!!'. 2 3
18 Kéi idegen nyelven 373!!! 0 $ " 5 3%!( 0!&.$! -.!.
19 374 Mhely Mhely 375 MHELY Kérjük, hogy MHELY cí ódszertni rovtb szánt írásikt közvetlenül szerkeszthöz küldjék lehetleg e-il ellékletként vgy postán következ círe: Dr. Tóth Zoltán, Debreceni Egyete Kéi Szkódszertn, 4010 Debrecen, Pf. 66. E-il: Telefon: / es ellék. Kiss Edin A tnulók tévképzeteinek és fogli fejldésének vizsgált kéi néhány lpfoglánk területén 1. Bevezetés és célkitzések A terészettudoányos nevelés npjinkbn gyökeres változáson egy keresztül. Az iskolától diszciplináris tudás helyett indennpi életben felhsználhtó iseretek közvetítését várják el. A terészettudoányos tntárgyknk többszörös kihívássl kell szebenézniük, kéi helyzete ezen belül z utóbbi idben tovább nehezedett. A tnulók nehezen tnulhtó, elvont tudoánynk trtják kéiát, és társdlo ellenszenve se könnyíti eg nevelk feldtát tntárgy népszersítésében. A tnulók ne képesek kell A Szerznek Debreceni Egyete Kéi Doktori Iskolájábn készített és október 8-án sikeresen egvédett doktori (PhD) értekezésének (tévezet: Dr. Tóth Zoltán) tézisei. értékben elsjátítni tudoányos foglkt. Joggl erül fel kérdés, hogy i ennek z ok, és hogyn lehet egoldni probléát. Az utóbbi négy évtizedben száos kuttás zjlott tnulók terészettudoányos isereteinek feltérképezésére vontkozón. Az egyik f kuttási irányzt célj tnulói iseretek feltárás (tévképzetkuttás), ásiké z iseretelsjátítás folytánk vizsgált (fogli fejldés és fogli váltás kuttás). Az eredények zt bizonyítják, hogy gyerekek igen speciális iseretrendszerrel rendelkeznek ár z iskoláb lépés eltt is. Ezeknek z isereteknek egy része ne egyeztethet össze tudoányosn elfogdottkkl és sjnos z okttás során ngyon nehezen lehet lecserélni ket. Azzl, hogy egiserjük ezeket z okttást egelz isereteket, vlint zt, hogy hogyn lkulnk ki és iként változnk z iskolábn eltöltött évek során, elsegítjük z okttás folytát, egfelel ódszerek kidolgozását hhoz, hogy tnulóink könnyebben elsjátíthssák terészettudoány és zon belül kéi isereteit. A terészettudoányos és zon belül kéii veltség elsjátításánk értéke ngybn függ z lpfoglk egértéstl. Kuttáso során ezért kéi néhány lpvet foglán (fiziki változás, kéii változás, nygennyiség, ele, vegyület, keverék) keresztül vizsgált, hogy 13 és 17 év közötti tnulók képesek-e egérteni ezeket foglkt. Arr kérdésre kereste válszt, hogy hogyn fejldik z ezzel kpcsoltos tudásuk z okttássl, zz vn-e fogli fejldés tnulók életkoránk elrehldásávl. Egy viszonylg új kuttási ódszer dt lehetséget hhoz, hogy egvizsgálj, hogyn szervezdik kéi lpfoglivl kpcsoltos tudás különböz korosztályokhoz trtozó tnulók kognitív rendszerében. Ne utolsósorbn célji között szerepelt tnulók tévképzeteinek feltárás is A éreszköz 2. A vizsgált ódszerei Kuttásohoz háro írásbeli felérlpot készítette következ kéii lpfoglkkl kpcsoltbn: (1) Fiziki változás, kéii változás; (2) Az nygennyiség és ól; (3) Ele, vegyület, keverék. A felérlpok kitöltése 2003 ájusábn és júniusábn történt, illetve bellük készült portugál felérlpokkl 2004 áprilisábn, ájusábn végezte vizsgáltokt.
20 376 Mhely Mhely A int A populációt 13 és 17 év közötti gyr ginzisták lkották. Kifejezetten ht-, illetve nyolcosztályos középiskolákt válsztott, hol kéiokttás folyt ne törik eg z iskolváltássl nyolcdik osztály után. A int felérlp szerinti és évfolyonkénti összetételét z 1. táblázt uttj. Portugáliábn hsonló korosztályból egy kisebb int összeállításávl került sor néhány feldt egoldásár, elyek gyr felérlp feldti közül kerültek ki. A 2. táblázt ennek portugál intánk z összetételét szelélteti évfolyonként. 1. táblázt: A int felérlp szerinti eloszlás 7. Évf. 8. Évf. 9. Évf. 10. Évf. 11. Évf. Összesen 1. felérlp felérlp felérlp N (f) táblázt: A portugál int egoszlás évfolyonként 7. Évf. 8. Évf. 9. Évf. 10. Évf. 11. Évf. Összesen N (f) Az értékelés ódszerei A tnulói definíciók trtli elezése A nyílt vég kérdésekre dott tnulói definíciók trtli elezését egy szkirodloból átvett htfokú skál felhsználásávl végezte. Ez ódszer inden egyes válszhoz egy 0-tól 5-ig terjed pontszáot rendel ttól függen, hogy z dott definíció ennyire áll közel z áltlunk elfogdotthoz, illetve ilyen értékben trtlz tévképzetet. A tnulói válszok értékelésének egy ásik szepont lpján vló vizsgáltát fenoenogrfikus elezés tette lehetvé, elynek kidolgozás Mrton nevéhez fzdik. A fenoenogrfikus elezés során tnulók válsziból képezünk ktegóriákt függetlenül ttól, hogy zok helyesek-e vgy se A tnulócsoportok jellez tudásszerkezetének vizsgált A tnulócsoportok jellez tudásszerkezetét didktiki kuttásbn ég ne ngy últr vissztekint tudástér-elélet lpján htározt eg. A tudástér zon iseretek összessége, elyek egy dott té egértéséhez elengedhetetlenek. A kéiábn gykrn kérünk száon egy tékört feldtok egy csoportjávl, elyek egoldásukhoz szükséges iseretek lpján egy hierrchikus rendszert lkotnk. Ezt rendszert egy ún. Hsse-digrl ábrázolhtjuk. A Hsse-digr egy olyn irányított gráf, elyben lul helyezkednek el legkevesebb tudást igényl feldtok, jd nyilk entén eljuthtunk z ezekre épül, bonyolultbb feldtokhoz is. A tudástér-elélet lpfeltevése szerint, h egy tnuló eg tud oldni egy feldtot hierrchiábn, kkor vlószínleg z ltt lévket is képes egoldni. Minden tnulóhoz hozzárendelhetünk egy tudásállpotot, ely tnuló áltl helyesen egoldott probléák összessége. A tudásállpotok rendszerét tudásszerkezetnek nevezzük, ely ár z dott tnulócsoport jellezje lehet. A tudásszerkezet csk olyn tudásállpotokt trtlzht, elyek hierrchikus hálóbn leglább egy ltt, illetve egy felette lév tudásállpottl kpcsoltbn vnnk. A ódszer lkls tnulócsoport jellez tudásszerkezetének z ún. szkérti tudásszerkezettel vló összehsonlításár, tudásszerkezet lpján egszerkesztett ún. jellez tnulási út segítségével eghtározhtjuk z iseretnyg tnításánk egfelel sorrendjét, tnulányozhtjuk különböz tényezk htását tudás szervezdésére, vlint fogli fejldést is vizsgálhtjuk jellez tudásszerkezet változásánk követésével Az dtok sttisztiki értékelése Az dtok leíró sttisztiki jellezit, vlint z egyes tnulócsoportok közötti különbségek szignifiknciáját (egy-, ill. kétintás t-prób, vrincinlízis) z SPSS progrcsoggl száolt, grfikonok, digrok szerkesztésére pedig fleg Microsoft Excel progrot hsznált
21 378 Mhely Mhely Új tudoányos eredények 3.1. A fiziki változás és kéii változás foglávl, egértésével kpcsoltos eredények A tnulók fiziki változás és kéii változás definícióját elssorbn kroszinten foglzzák eg, részecskeszint értelezéssel ne tudják zt összekpcsolni. A htfokú skál (0-5) lpján száolt egértési szint fiziki változás esetén 3,6, kéii változásr 4,0. A fenoenogrfikus elezés szerint két f ktegóriáb sorolhtók be tnulói definíciók (kroszint, részecskeszint). A tnulók indkét változás esetén kroszint eghtározásokt részesítették elnyben. A tudástér-elélet lpján szkérti úthoz hsonlón tnulók tudásszerkezetében indkét változás esetén kroszint értelezés egelzi részecskeszintt. Azzl ellentétben zonbn kéii változás elrébb helyezkedik el, int fiziki változás. A legszebetnbb eltérés pedig z, hogy fiziki változás részecskeszint értelezése kéii változás részecskeszint egközelítésére épül. Az okttás elrehldásávl ne változik tudásszerkezet. A kéii változás tnulói értelezéseit öt különböz odell segítségével írhtjuk le. A legjobbn illeszked odell ind kroszint, ind részecskeszint értelezést trtlzz, viszont zok között nincs kpcsolt, i zt jelenti, hogy legtöbb tnuló ne képes összefüggést tlálni kétféle értelezés között. H égis, kkor tudoányos odellel ellentétben, éppen kroszint értelezésre építi részecskeszint egközelítést A konkrét folytok zonosítás során tnulók kéii változások, illetve kroszinten értelezett folytok esetén legsikeresebbek. Az egyes évfolyok teljesíténye indössze 44-55% között vn, szignifikáns fejldés 7. évfoly után utthtó ki. Legsikeresebb kroszint folytok besorolás, de z életkor elrehldásávl nincs növekedés. Ezt követik részecskeszint folytok, hol kis érték fejldés tpsztlhtó z évfoly növekedésével. Legnehezebb szibóluszinten egdott folytok besorolás, viszont szebetn fejldés hldv z okttássl. A folytok típusát tekintve kéii változások feliserése legkönnyebb, ezután következnek fiziki változások. Mindkét esetben vn fejldés z életkor elrehldásávl. Ezzel szeben z oldási folytok besorolás ngyon kritikus és nincs változás z idvel. Két áltlános tévképzet figyelhet eg: A tnulók z oldódást kéii változásnk tekintik. Az indoklások lpján ennek z z ok, hogy folytok egítélésekor kéii változás kroszint jellezi eghtározók. (Ez tévképzet portugál int jelents részénél is elfordult.) A szibóluszinten egdott folytokt is kéii változásként értelezik, és 8.-bn vlint 9.-ben szignifikánsn n e tnulók szá. Ennek hátterében z tévképzet áll, hogy vegyjelekkel és képletekkel csk kéii rekciókt lehet leírni. A tudástér-elélet segítségével eghtározott jellez tnulási utkkl kpcsoltbn egállpíthtó, hogy z egyes tnulócsoportokr jellez tnulási utk lényegesen különböznek szkérti úttól. Attól eltéren, z oldási folytok indenütt z utolsó helyre kerülnek A portugál int fiziki illetve kéii változássl kpcsoltbn z esetek többségében ugynzokkl tévképzetekkel rendelkezett, int gyr. Ez bizonyítj zt ár nezetközileg isert tényt, hogy tévképzetek többnyire netl, kortól és kultúrától függetlenül jelennek eg A folytok jellezinek besoroláskor tnulók ktegorikusn rgszkodnk vgy fiziki, vgy kéii változáshoz ég kkor is, h z dott tuljdonság indkettre jellez lehet. Az összesen 25 jelleznél 12 helyen tlált olyn tévképzetet, ely csk fiziki változásr vontkozik, 19 tévképzet csk kéii változásr és 1 tévképzet indkettre érvényes, ez összesen 32 tévképzet. Itt ezek közül csk jelents értékben (több int 50%-bn) elfordulókt foglzo eg: Az nyg fiziki tuljdonság kizárólg fiziki változás lklávl változht eg. A hlzállpot egváltozás csk fiziki változás során következhet be.
22 380 Mhely Mhely 381 Új tuljdonságú nyg csk kéii változás során keletkezhet. Az nyg összetétele csk kéii folyt során változht eg. Elsrend kéii kötések csk kéii változás során boolhtnk fel. Elsrend kéii kötések csk kéii változás során lkulhtnk ki. Másodrend kötések csk kéii változás során boolhtnk fel, vgy lkulhtnk ki. A részecskék elektronszerkezetének egváltozás csk kéii folyt során vlósulht eg. Az tog összetételének egváltozás csk kéii folyt során vlósulht eg. Csk kéii folytokt lehet vegyjelekkel és képletekkel leírni. A tnulók z áltlábn indkét változásr jellez tuljdonságokt kizárólg z egyik változáshoz rendelik. Ennek ok bbn rejlik, hogy tnkönyvek külön tárgylják fiziki, illetve kéii változást, és végén ne fogllkoznk z zok közötti hsonlóságokkl és különbségekkel. Fogli fejldés összességében 9. és 10. évfolyokon következik be Az nygennyiséggel kpcsoltos fogli egértés vizsgáltánk eredényei Az nygennyiség tnulói definícióink elezése során kiderült, hogy legkritikusbb foglol állunk szeben, legkevésbé ezt foglt értik tnulók. Az ezzel kpcsoltos tévképzeteik nezetközi szinten ár isert tévképzetekkel egyeznek eg. A htfokú skál lpján értékelve válszokt, tnulók közel egyhrd ne tudott válszolni, ásik hrduk tévképzetekkel rendelkezik, és csk egyötödük tudott olyn eghtározást írni, ely elfogdhtó volt. A egértési szint ngyon lcsony inden évfolyon, z átlg 1,7. A két leggykoribb tévképzet: Az nygennyiség eguttj z nygbn lév took száát. Az nygennyiség zt uttj eg, hogy 1 ol részecskének ekkor töege Egy bináris vegyület összetételével kpcsoltos feldt egoldásánk elezése során kiderült, hogy korábbi nezetközi tpsztltokkl ellentétben gyr tnulók z iskolábn tnult lgoritusokt részesítik elnyben logiki ódszer helyett. A tnulók feldtegoldó ódszerei lpján háro strtégi különböztethet eg: ól ódszer hársszbály logiki ódszer A tnulók z iskolábn tnult strtégiákt részesítik elnyben, különösen ól ódszert. Minél képzettebbek tnulók kéiából, nnál inkább elnyben részesítik ezt ódszert. Az isert strtégiák sikeressége sokkl ngyobb érték, int z zonosíthttln ódszereké. A legsikeresebb logiki ódszer, de csk kevesen lklzták. Különbség figyelhet eg lányok és fiúk strtégiválsztás között. A lányok sokkl gykrbbn hsználták hársszbályt, int fiúk. A fiúk reltíve ngyobb ránybn lklzták ól ódszert, vgy dolgoztk zonosíthttln strtégiávl, int lányok. Érdekes tpsztlt volt, hogy tnulók egy része (13%) gnéziu-krbid széntrtlánk száításávl kpcsoltos probléát gnéziu és szén között végbeen kéii rekcióként értelezte. Ez vlószínleg nnk következénye, hogy kéii probléák egoldás során kéi tnárok és tnkönyvek kiindulási pontként kéii rekció felírását jvsolják. A ásik figyelereéltó észrevétel, hogy tnulók 14%- ( válszdók 23%-) hsznált C 2 jelölést MgC 2 -ben lév szén leírásár Az ele, vegyület és keverék foglávl, vlint egértésével kpcsoltos eredények Az ele, vegyület és keverék foglk tnulói egértése közepes szint, ely jelents értékben elforduló tévképzeteknek köszönhet. A htfokú skál lpján száított évfolyonkénti átlgok 2 és 2,5 között vnnk, i közepes eredénynek száít egértésre
23 382 Mhely Mhely 383 vontkozón. A teljes int átlg elere 2,3, vegyületre 2,2, keverékre 2,3. A legrosszbb eredények 9. és 11. évfolyokon születtek. A tnulói definíciók elezése során feltárt tipikus tévképzetek következk: Az ele seleges kéii részecske. Az ele zonos tookból álló olekul. A vegyület különböz tookból felépül olekul. A keverék két vgy nnál több nyg rekciób lépésének eredénye. A keverék esterségesen állíthtó el. A keverékben z lkotórészek rány állndó Az nyg felépítésével kpcsoltos ondtok kiegészítése során gykrn tlálkozt z to és olekul, z to és ele, vlint olekul és vegyület foglk sszociációjávl, keverésével. A külföldi tpsztltokhoz hsonlón gyr tnulók is gykrn keverik kroszint foglkt (ele, vegyület) részecskeszint foglkkl (to, olekul). A feltárt tévképzetek következk: A kovlens kötés eredényeként néhány eghtározott száú to összekpcsolódásávl vegyület keletkezik. H vizet elektroos árl bontjuk (elektrolizáljuk), kkor kétféle to keletkezik. A szilárd jód elegítésekor lilás szín gz keletkezik, elyben jód took vnnk. Az took z egyszer nygok közé trtoznk. A SiO 2 összegképlet olekul felépítésében szilíciu to és oxigén to/olekul vesznek részt. Az O 3 és O 2 olekulák egyzon ele, z oxigén to részecskéi. Az összetett nygok közé trtozik olekul. Az óni vegyület lkj hároszög lpú piris, és benne vlennyi hidrogén olekul egyvegyérték. A kénsv vegyület felépítésében hároféle ele vesz részt: hidrogén olekul, kén olekul, és oxigén olekul. Nátriu to és klór olekul/to rekciójábn NCl olekul keletkezik. Az took/eleek periódusos rendszerében áltlábn feltüntetik z to(ok) hlzállpotát és z ele(ek) éretét is. A periódusos rendszer ne trtlz olekulá(k) oldhtóságár vgy vegyület(ek) lkjár vontkozó dtokt A részecskeábrák zonosításkor hlzállpot eghtározás legkönnyebb, keverékek egkülönböztetése legnehezebb. Kisérték fejldés 8. és 10. évfolyokon tpsztlhtó. A tnulók hlzállpot egítélésében, különösen szilárd nyg egállpításábn voltk legsikeresebbek. Kooly gondjik voltk hoogén és heterogén keverék egkülönböztetésében. A legtöbb osztályozási strtégi z ábrák vizuális és forális vizsgáltán lpult. A feltárt tévképzetek: A víz indig folyékony hlzállpotú. A gázokt zonos részecskék lkotják. A szilárd intákbn részecskék ugynolyn sorrendben isétldnek. Az eleek és vegyületek indig tiszt nygként vnnk jelen. A heterogén keverékekben különböz típusú részecskék eloszlás rendezetlen. A tudástér-elélet lpján ne utthtó ki hosszú távú változás tnulók kognitív struktúrájábn. A sttisztiki, trtli és strukturális elezés egyönteten zt írj le, hogy 8. és 10. évfolyokon következik be kisérték fejldés. A 8. évfolyon szervetlen kéiát, 10. évfolyon pedig szerves kéiát tnulnk diákok. Ez lpján vlószínsíthet, hogy konkrét kéii rendszerek vizsgált és zok terészetének tnulányozás jobbn hozzájárulnk részecskeábrák zonosításánk sikerességéhez, illetve z nyg terészetének részecskeszint beuttásához, int egygábn z áltlános kéi tnulás.
24 384 Mhely Mhely Az eredények lklzási lehetségei Az eredények közvetlen lklzásár háro f területen látok lehetséget. Elsként tnárképzést kell egelíteni. Másodsorbn tnári segédletek létrehozását, íg hrdikként eredényei további kuttási irányok kijelölésére is lklsk. A felsokttás tnárképzésben betöltött egyik feldt, hogy egfelel esterségbeli kopetenciákkl vértezze fel leend tnárokt, kik z iskol flin belül képesek lesznek olyn isereteket átdni tnulóknk, elyeket zok z iskolpdból kikerülve is hsznukr fordíthtnk. Ehhez tnároknk fel kell venni versenyt indennpok igényeivel, illetve zok htásávl. A kéi okttás különösen nehéz feldtot ró tnárinkr. Miután kéi egy olyn világot tár tnulóink elé, ely szeel láthttln, ngyon fontos lenne, hogy z lpfoglkt kell értékben elsjátítsák. Ez zonbn ne indig történik eg, diákjink ngyon sok tévképzetet hordoznk. Két eset fordulht el. Vgy ár z iskoláb lépéskor rendelkeznek ezekkel z elzetes iseretekkel, vgy z okttás során lkulnk ki. Ahhoz, hogy tnárink felkészültek legyenek probléár, tisztábn kell lenniük tnuló iseretelsjátítási folytávl, vlint konkrétn iserniük kell egy-egy dott tékör tévképzeteit is. Tudniuk kell, hogy ilyen elzetes elképzeléseket hogyn, ilyen lépéseken keresztül lehet felváltni tudoányos iseretre, hogy késbb zokt trtósítni tudják. Azz ne elegend pusztán tévképzetekkel egisertetni ket, hne különböz ódszertni eszközöket kell rendelkezésükre bocsátni, illetve eg kell tnítni ket rr, hogy hogyn készíthetik el önállón zokt. Meg kell iserniük fogli fejldés, illetve fogli váltás dinikáját, hogy guk is el tudják idézni zt. Ez terészetesen zt is jelenti, hogy lpveten eg kell változttni hozzáállásukt z iseretelsjátítás folytához, illetve gához z okttáshoz is. A kéiokttás egyik probléáj, hogy didktiki kuttások eredényei ngyon nehezen, hosszú id elteltével kerülnek át gykorltb. Ezt probléát többek között zzl is egpróbálhtjuk leküzdeni, hogy - int zt ár elítette - olyn ódszertni eszközöket bocsátunk tnárok rendelkezésére, elyek ngy segítséget jelenthetnek indennpi gykorltbn, z okttás során. A legjobb z lenne, h gához tnkönyvekhez, unkfüzetekhez kpcsolódón készülnének el ezek segédletek, így rögtön bevethetk lennének. Ezzel jelents idt tkríthtnánk eg tnárinknk. Egyben példákt is szolgáltthtnánk további, önálló unkák elkészítéséhez. Ezek z eszközök tuljdonképpen tévképzetkuttás, illetve fogli fejldés, fogli váltás vizsgált során hsznált eszközök közül kerülhetnének ki elsdlegesen. Konkrétn lehetnek fogli térképek, dignosztizáló tesztek, utótesztek, illetve tnítási ódszerek is. E ódszerek között kell felsorolni fogli váltás technikáit is. Az dtok értelezését több feldtnál ngybn elsegítette tudástér-elélet hsznált, ely kéi területén ég új, idehz pedig egyedi vizsgálti ódszernek száít. Az egyes tnulócsoportok tnulási útjánk eghtározásávl olyn tnenetek készítését segíthetjük, elyekben tnnyg eleei z életkori sjátosságoknk egfelel sorrendben kerülnek egtnításr. Végül eg kell elíteni jövbeni kuttások fontosságát is. Célo gyr tnulók kéii tévképzeteinek feltárás volt z lpfoglk területén, de eredényei további kérdések egfoglzását vonták guk után. Hipotéziseket lkott z egyes tévképzetek kilkulásánk okáról, elyek cskis újbb kuttások segítségével igzolhtók. Idszervé vált z elz bekezdésben elített eszközök elkészítése, jd gykorltbn vló tesztelése, htásuk vizsgált tnulási folytbn. 5. Tudoányos publikációk Referált, nezetközi folyóirtbn egjelent tudoányos közleények dti: 1. Tóth Zoltán Kiss Edin Hungrin secondry school students strtegies in solving stoichioetric probles Journl of Science Eduction, Vol. 6. No. 1, (2005) p Tóth Zoltán Kiss Edin Using Prticulte Drwings to Study Yer Olds Understnding of Physicl nd Cheicl Coposition of Mtter s well s the Stte of Mtter Prctice nd Theory in Systes of Eduction, Vol. 1. No. 1, (2006) p ( 3. Tóth Zoltán Kiss Edin Modelling Students Thinking Ptterns in Describing Cheicl Chnge t Mcroscopic nd Subicroscopic Levels
25 386 Mhely Mhely 387 Journl of Science Eduction (egjelenés ltt) Referált, gyr nyelv folyóirtbn egjelent közleény: 1. Tóth Zoltán Kiss Edin A fiziki és kéii változások zonosításávl kpcsoltos tudásszerkezet Iskolkultúr, 17. évfoly, 1. szá, (2007) Ne-referált folyóirtokbn egjelent közleények: 1. Tóth Zoltán Kiss Edin Középiskoli tnulók feldtegoldó strtégiái egyszer sztöchioetrii probléákr A Kéi Tnítás, 12. évfoly, 1. szá, (2004) Kiss Edin Sebestyén Annári Dr. Tóth Zoltán A tnulók tévképzetei és fogli fejldése fiziki változás és kéii változás tékörében A Kéi Tnítás, 13. évfoly, 4. szá, (2005) Kiss Edin Dr. Tóth Zoltán A tnulók nygennyiséggel kpcsoltos fogli egértése és fejldése Középiskoli Kéii Lpok, XXXIII. évf. 1. szá, (2006) Konferenciákon trtott eldások: 1. Kiss Edin Tévképzet kuttás kéi néhány lpvet foglánk területén III. Országos Neveléstudoányi Konferenci, Budpest, (Progr és Trtli Összefogllók, 347. o.) 2. Kiss Edin Tóth Zoltán Tnulói tévképzetek vizsgált kéi lpfoglink területén IX. Nezetközi Vegyészkonferenci, Kolozsvár, Roáni, (Összefogllók, o.) 3. Kiss Edin Tóth Zoltán Tnulói tévképzetek kuttás kéi lpfoglink területén XXI. Kéitnári Konferenci, Pécs, (Összefogllók, o.) 4. Kiss Edin Tóth Zoltán A tnulók fogli fejldésének vizsgált z ele, vegyület és keverék tékörben XXI. Kéitnári Konferenci, Pécs, (Összefogllók, o.) 5. Kiss Edin Az nygennyiség foglávl kpcsoltos tévképzetek IV. Országos Neveléstudoányi Konferenci, Budpest, (Progr és Trtli Összefogllók, 310. o.) 6. Kiss Edin Dr. Tóth Zoltán Tévképzetek kéiábn Tvszi Szél 2005 VIII. Országos PhD Konferenci, Debrecen, (Konferenci kidvány o.) 7. Kiss Edin A tnulók részecskeábrák zonosításábn uttott teljesíténye és tudásszerkezete V. Országos Neveléstudoányi Konferenci, Budpest, (Progr és Trtli Összefogllók, 159. o.) 8. Tóth Zoltán Kiss Edin Áltlános és középiskolás tnulók fiziki és kéii változások egkülönböztetésével kpcsoltos tudásszerkezete VI. Országos Neveléstudoányi Konferenci, Budpest, (Progr és Trtli Összefogllók, 139. o.) Konferenciákon beuttott poszterek: 1. Kiss Edin Tóth Zoltán Hungrin students isconceptions in bsic cheistry ides 7 th Europen Conference on Reserch in Cheicl Eduction, Ljubljn, Sloveni, (Progre nd bstrcts, p ) 2. Kiss Edin Tóth Zoltán Students isconceptions regrding to the ole concept 8 th Europen Conference of Cheistry Techers, Eisenstdt, (Book of Abstrcts, p. 68.) 3. Tóth Zoltán Kiss Edin Using Prticulte Drwings to Study Yer Olds Understnding of Physicl nd Cheicl Coposition of Mtter s well s the Stte of Mtter 1 st Europen Cheistry Congress, Budpest, (Abstrct Book, p. 237.) 4. Teres M. Sntos Kiss Edin Fontes Ros Nilz Cost Tóth Zoltán Detecço de Concepçes Alterntivs, ou Errds, e Conceitos Básicos de Quíic, e Alunos Húngros e Portugueses: Estudo Coprtivo XII. Encontro Ncionl Educco e Ciencis, Vil Rel, Portugáli szepteber Teres M. Sntos Kiss Edin Nilz Cost Tóth Zoltán Ros Fontes Estudo Coprtivo e Alunos Húngros e Portugueses: Detecço de Concepçes Alterntivs, ou Errds, e Conceitos Básicos de Quíic V. Encontro ncionl d Diviso de Ensino e Divulgço d Quíic, (DEDQ) Brg, Portugáli, noveber A kuttást z OTKA (T és T ) között táogtt.
26 388 Htártln kéi Dr. Szly Luc Htártln kéi Angol vendégelıdók XXIII. Kéitnári Konferencián (II. rész) A XXIII. Kéitnári Konferenci idejét, helyét és progrját tekintve is több ponton kpcsolódott 40. Nezetközi Kéii Diákolipi eseényeihez. Az tény, hogy indkettı Budpesten, z Eötvös Loránd Tudoányegyeteen zjlott júliusábn, többféle ( résztvevı kollégáktól kpott rekciók lpján igen szerencsés válsztásnk bizonyult) progrpontr is lehetıséget dott. Így, z olipi gykorlti feldtink kipróbálásán túl, gyr kéitnárok háro olyn ngol vendégelıdó áltl trtott elıdást is eghllgthttk, kiknek unkáj szorosn kpcsolódik kéi okttásához, ill. népszerősítéséhez. Azok kedvéért, kik ne lehettek jelen konferencián, z ı ondnivlójuk lényegének gyrr fordított és szerkesztett változt olvshtó ebben tnévben KÖKÉL háro különbözı száánk Htártln kéi rovtábn. E Woodley: Hogyn segíti kéitnárok unkáját Royl Society of Cheistry? A Royl Society of Cheistry (RSC) kéi ügyének elıozdításár létrehozott szervezetek közül Európábn legngyobb. Az okttássl kpcsoltos tevékenységei kielégítik kéikusok inden korcsoportjánk igényeit. Az okttási segédnygok széles skáláját kínálj tnárok, egyetei elıdók és diákok száár, képzéseket és tnfolyokt szervez, Htártln kéi 389 szki dtbázisokt trt fenn, befolyásolj z okttáspolitikát és egy sor egyéb tevékenységet is folytt. Táogtjuk kéi okttását z áltlános és középiskolákbn, vlint szkképzésben. Ingyenes okttási segédnyginkt eljutttjuk z Egyesült Királyság és Írország iskoláib és szkképzı intézényeibe. Okttási segédnygokt készítünk ngyon változtos forákbn könyvekben, CD ROM-okon, DVD-ken és z interneten. Mindezekrıl további inforáció, vlint bizonyos esetekben ingyenesen letölthetı nygok is elérhetıek LernNet nevő weboldlunkon (1). Az Eduction in Cheistry cíő, kéthvont egjelenı folyóirtunkt tnárok és elıdók száár hoztuk létre, de ennek vn éves diákoknk szóló elléklete is. Ezt ingyenesen jutttjuk el z Egyesült Királyság és Írország középiskoláib, szkképzı intézényeibe és z egyeteekre. Igyekszünk odernizálni tnterveket, és terészettudoányos okttás átfogó és koherens egközelítése érdekében szoros együttőködésben dolgozunk z Egyesült Királyság korányávl, ennek szervezeteivel, szki testületekkel és tudoányos társságokkl. A tntervek változás idején irányuttást dunk tnároknk zzl kpcsoltbn, hogy ezek változások iként érintik ıket. Hozzájárulunk z okttáspolitik lkításához, regálunk különféle konzultációk eredényére, és elıkészítı jellegő unkát is folyttunk záltl, hogy olyn jelentéseket készíttetünk, elyek tényszerő bizonyítékokkl szolgálnk z ktuális kérdések és probléák egvittásához. Táogtjuk zokt kezdeényezéseket, elyek társdlo bárely rétegébıl szárzó diákok figyelét kéii tudoányok felé fordítják és tudtosítják z ilyen életpály válsztásánk lehetıségét. Tnácsdó szolgáltunk és pályválsztást segítı kidványink elérhetıek diákok, szülık és tnárok száár is. Az Egyesült Királyságbn z RSC nyújtj legtöbb, ne álli finnszírozású továbbképzési lehetıséget tnároknk, kéitudásuk és okttási ódszereik egújítását célzó tnfolyok és bentlkásos kurzusok forájábn. Internetes (on line) dtbázisok A CheistryTechers.org (2) dtbázis z RSC vgy ások áltl létrehozott okttási segédnygok gyors egtlálását teszi lehetıvé világon bárhol kéiát és terészettudoányt okttó tnárok száár. Az nyg kéi területeinek vlint z Egyesült Királyságbn hsználtos tnterv
27 390 Htártln kéi téköreinek egfelelıen vn csoportosítv, így z dtbázisbn indkét szepont szerint lehet keresni. Az itt elérhetı okttási segédnygok inden korosztályt (5-11, 11-14, és 16 év fölöttieket) lefednek. Forátuuk sokféle (pl. Word vgy pdf fájlok, Excel tábláztok, PowerPoint prezentációk, videóbejátszások, niációk stb.), de z dtbázis ás weboldlkr uttó linkeket is trtlz. Az oldl folytosn fejlıdik, tntervi változások esetén frissítik és z új forrásunkákkl is rendszeresen bıvítik. Az RSC nygi ingyenesen hsználhtók, beleértve hálóztb kpcsolt száítógépeket is. A színvonls és inden tekintetben egfelelı kéii kísérletek rendkívül fontos szerepet játsznk tnításbn és tnulásbn. Hsználhtók tnulás htékonyságánk növelésére, és z eléleti háttér bizonyos spektusink tisztázásár. A gykorlti tevékenység szórkozttóvá teszi kéiát, és lehetıséget d diákoknk rr is, hogy ár eglévı tudásukt lklzzák tpsztltok gyráztár. A PrcticlCheistry.org (3) weboldlon kísérletek széles skáláj tlálhtó. Ezek elveket vgy folytokt illusztrálnk, vizsgáltok kiindulópontjként szolgálhtnk, és olyn fogllkozások, eseények érdekesebbé tételére is hsználhtók, int diákkörök vgy nyílt npok. A weboldl lehetıvé teszi kísérletek osztályteri beuttásávl kpcsoltos tpsztltok egyás közötti egosztását is, sıt lboránsok száár is sok hsznos inforációt trtlz. Sok nglii iskol hsználj npság Virtul Lerning Environents (VLEs) -et, zz Virtuális Tnulási Környezet -et tnítás és tnulás segítésére. Ez z interneten keresztül őködtethetı kiterjedt eszköztár, például z értékeléshez és tnulási folyt követéséhez. A BestChoice VLE (4) egy interktív okttási weboldl, i z Egyesült Királyság érettségi vizsgkövetelényeiben, ill. felsıokttás elsı évében elıírt kéi tnnyg elsjátításához nyújt segítséget. 100 odul érhetı el, és rendszer 8000 válszdási lehetıséget kínál fel. A hngsúly z interktivitáson vn. A diákokt úgy vonj be tnulási folytb, hogy folytosn kell inforációkt betáplálniuk, jd ezt követıen zonnl visszcstolást és irányuttást kpnk. A BestChoice kiegészítheti tnárokr, tnkönyvekre és gykorlti tevékenységre lpozott tnulást. A BestChoice szbdon elérhetı. A diákok elıször hsználhtják deo ódbn is, hogy lássák, ire vló, és ztán regisztrálhtnk. H Htártln kéi 391 diák regisztrált, kkor BestChoice tárolj betáplált válszokt, elyek következı bejelentkezésekkor is visszkereshetık. Könyvek Cheistry for the Gifted nd Tlented (Kéi különleges tehetségeknek) Az ngol nyelv ás-ás kifejezést hsznál z eléleti tárgyk területén legjobb képességőnek bizonyuló, ill. sport és ővészetek terén kieelkedı teljesítényre képes tehetségek egjelölésére. Azok diákok, kik indkét területen jó dottságokkl rendelkeznek, tehetségek különleges csoportját lkotják. Minden diák egérdeli, hogy olyn okttást kpjon, i lehetıséget nyújt száár dottsági xiális kiknázásr. A diákoknk olyn feldtokt kell dni, elyeknek egoldás során kihsználhtják képességeiket és ár eglévı tudásukt. Az osztályteri fogllkozások egtervezésénél összhngb kell hozni tehetségesek igényeinek egfelelı sjátos ódszereket többi diák igényeivel. Htls hozdék lehet nnk, h tnítási ódszereinket lklssá tesszük rr, hogy legtehetségesebb diákok érdeklıdését is fenntrtsuk, és száukr is biztosítsuk fejlıdési lehetıséget. Az RSC elkötelezett z iránt, hogy legtehetségesebb diákok figyelét fölhívj kéi irányáb vló továbbtnulás lehetıségére. Az itt közölt gykorltokt és fogllkozásokt elyek tnári felügyelettel, és lklnként nélkül is hsználhtók rr tervezték, hogy fölkeltsék fitlok érdeklıdését tntárgyunk iránt, és hogy kooly kihívást és izgls feldtot jelentsenek tehetséges diákoknk is. Az RSC áltl z iskolák száár kidott könyvekrıl további részletek is olvshtók szervezet honlpján (5). Schools nd Colleges Publiction Service (Iskolák és Szkképzı Intézények Publikációs Szolgált) Bárely ország iskolái és szkképzı intézényei felirtkozhtnk z RSC Schools nd Colleges Publiction Service nevő szolgálttásánk igénybevételére. Ez lehetıvé teszi száukr, hogy évente ht lklol egkpják z ktuális kidványok olyn csogját, ely világon egjelent legérdekesebb és leginfortívbb publikációkt trtlzz, lefedve kéi tnításánk inden spektusát. Az ár évi 79 z Egyesült Királyság területén kívülrıl felirtkozók száár. Ezért z összegért következı nygok kphtók eg: Eduction in Cheistry (és InfoChe) z Egyesült Királyságból
28 392 Htártln kéi Che 13 News Kndából Che NZ Új-Zélndról Cheistry in Action Írországból Cheistry Reviews z Egyesült Királyságból CheMtters z Aeriki Egyesült Állokból csog trtlzz z RSC áltl egjelentetett legújbb publikációkt is, ide értve z okttási segédnygokt - könyveket, CD ROM-okt és DVD-ket pályválsztást segítı nygokt posztereket kuttásokról szóló jelentéseket. Az RSC Okttási Osztályánk tevékenységérıl további inforációk is olvshtók szervezet honlpján (6). A beuttott (és z lábbi irodlojegyzék lpján egkereshetı) okttási segédnygokkl, ill. z elıdás során elhngzott kijelentésekkel kpcsoltos kérdéseket e-il-ben lehet föltenni közvetlenül E Woodley-nek (Royl Society of Cheistry, Burlington House, Piccdilly, London, W1J 0BA, UK, e-il: woodleye@rsc.org) vgy Szly Lucánk luc@che.elte.hu cíen. Irodlojegyzék: (1) (2) (3) (4) (5) (6) (Az utolsó látogtás dátu inden fentebb felsorolt weboldl esetében: noveber 8.) Dr. Szly Luc ELTE Kéii Intézet luc@che.elte.hu
29 Nprkész Nprkész A díjzottk NAPRAKÉSZ Tíz éve gyr kéiokttásért Idén tizedik lklol osztották ki A Mgyr Kéi Okttásértdíjt. Az október 20-i ünnepélyes díjátdásnk ezúttl is Mgyr Tudoányos Akdéi dott otthont. Kieelkedı szki unkásságáért négy kéitnár részesült z eliserésben: Thúróczy Év középiskoli tnár (Budi Ciszterci Szent Ire Gináziu, Budpest), Kleeberg Zoltánné középiskoli tnár (Mechtroniki Szkközépiskol és Gináziu, Budpest), Ngy Ferencné nyuglzott áltlános iskoli tnár (Körzeti Áltlános Iskol és Óvod, Litke), Pp László nyuglzott középiskoli tnár (Ady Endre Eléleti Líceu, Ngyvárd). A díjt 1999-ben lpított Richter Gedeon gyógyszercég zzl szándékkl, hogy hzi kéiokttásbn és z zzl kpcsoltos iseretterjesztésben közvetlenül vállljon táogtó szerepet. A díjt Richter Gedeon Alpítvány Mgyr Kéi Okttásért hárotgú kurtóriu évente ítéli od olyn közép- és áltlános iskoli kéitnároknk, kik évtizedeken át trtó áldoztos unkájukkl jelentısen hozzájárulnk gs színvonlú szkképzéshez, tehetséges diákok felkrolásához, ezáltl z utánpótlás neveléshez.. A díjr htáron túli iskolák gyr nyelven tnító tnári is jelölhetık. Az elúlt években többször elıfordult, hogy guk diákok jelölték kéitnárukt, kit bíráló bizottság is érdeesnek tlált z eliserésre. A díjt eddig összesen 43 kéitnár vette át, elyhez összesen 9 és fél illió forint pénzjutlo társult. THÚRÓCZY ÉVA 1977-ben szerzett fizik-kéi szkos tnári oklevelet z Eötvös Loránd Tudoányegyeteen, jd z Egészségügyi Szkiskolábn, 1984-tıl pedig Móricz Zsigond Gináziubn fizikát és kéiát tnított. İ trtott kéi fkultációt, kéi szkkört vezetett, 1997-re gináziu eghtározó tnáregyéniségévé vált. Ekkor cstlkozott Budi Ciszterci Szent Ire Gináziu lkuló tnári krához, ost is ott dolgozik. Mindkét tárgyát tnítj évfolybn, ezen kívül trt kéi felvételi elıkészítıt, kísérletezı és feldtegoldó kéiszkkört. Szbdidejét feláldozv külön fogllkozik z egyénileg kieelkedıen tehetséges és versenyezni vágyó diákokkl, szerényebb képességő diákoknk korrepetációt trt. İ z iskol kéi unkcsoportjánk vezetıje, legtekintélyesebb kéitnár. Bár kéiát gyerekekkel nehéz egszerettetni, ert Szent Ire Gináziu huán beállítottságú és ilyen órákkl z átlgosnál jobbn egterheli z od járó diákokt, Thúróczy tnárnı növendékei z országos kéiversenyeken égis száos esetben érnek el kiváló helyezéseket, ne egyszer elsı helyet. KLEEBERG ZOLTÁNNÉ 1978-bn vegyészérnöki, 1987-ben vegyipri őszki tnári képesítést szerzett, de ár elsı diploáj egszerzése ót tnári pályán dolgozik, 26 éve középiskoli tnárként. A Mechtroniki Szkközépiskol és Gináziubn 1990-es eglkulás ót tnít. Kiváló szktnár, diákjivl szeben is igényes, kooly, de reális követelényeket tászt. Tnítványi szeretik, és sokn ez áltl kedvelik eg kéiát. Okttóunkájár jellezı, hogy ár z iskol őködésének elsı éveiben is volt z Irinyi János Kéiverseny országos döntıjébe kerülı tnítvány. Diákji sok lklol értek el hsonló sikereket. Az Irinyi János versenyen például két évben is z ı tnítvány kpt z országos elsı helyezést! A sikereket kitrtó óri és szkköri unkávl, vlint iskoli versenyek szervezésével lpozz eg. Ngy szerepe volt z újonnn eginduló iskol kéiszertáránk kilkításábn és felszerelésében is. Jelentıs részt válll z iskol nevelıtevékenységébıl, kiváló osztályfınök. Sokt tesz fitlok egészséges életódr neveléséért, fı szervezıje z iskol drog-, AIDS- és dohányzásegelızı progrjink.
30 Nprkész Nprkész NAGY FERENCNÉ 1968-bn szerzett tetik-kéi szkos tnári diploát z egri Tnárképzı Fıiskolán. Már 1965-tıl tnított litkei Körzeti Áltlános Iskol és Óvodábn, elynek 1975-tıl igzgtóhelyettese, 1997-tıl 2002-ig igzgtój volt, nyugdíjzásáig tıl Nógrád Megyei Pedgógii Intézet kéi szktnácsdój. Már pályáj elején szép eredényeket ért el tehetséggondozás területén. A vidéki körzeti iskol hlozottn hátrányos helyzető, több int felerészben ro szárzású növendékei közül inden évben volt olyn tnítvány, ki Hevesy György Országos Kéiverseny területi és egyei fordulóin elıkelı helyezést ért el. Volt, ki z országos döntı 2. helyezettje lett z ELTE-n tnít, ásik tnítvány 2006-os brzílii és 2007-es tjvni Nezetközi Junior Terészettudoányi Diákolipián nyert bronz fokoztot ót Nógrád egye kéii szktnácsdójként neve összenıtt szktárgyávl. Kollégái eliserik, értékelik unkáját, és i npig kérik segítségét. Blssgyrton és Slgótrjánbn inden évben tnév elıkészítı tnácskozást trtott, több lklol rendezett beuttó órákt, tnkönyvbeuttót, tnulányi kirándulásokt szervezett kéiát tnító nevelıknek. Közokttási szkértıként tnkönyvet lektorált, véleényezte egye öt iskolájánk és egy budpesti intézény pedgógii progrját. Diákji közül sokn válsztottk vlilyen kéiához kpcsolódó fogllkozást. 15 lett vegyész, illetve vegyészérnök, 8 tnár, 13 gyógyszerész, 49 orvos. Vlennyien egbecsült szkeberek. Vn közöttük egyetei, illetve fıiskoli tnár, doktori vgy PhD fokozttl rendelkezı. PAP LÁSZLÓ 1964-ben kolozsvári Bbes-Bolyi Tudoányegyeteen szerzett fizik-kéi szkos tnári diploát. Tnári pályáját Szilágysolyói Eléleti Líceubn kezdte, 1980-bn került Ngyvárdr, hol elıször egy könnyőipri líceubn, jd 1984-tıl z 5-ös száú Ipri Líceubn i Ady Endre Eléleti Líceubn tnított kinevezett-, között nyugdíjs órdó tnárként. Mindháro iskolábn ódszertni unkközösség vezetıje volt ig Bihr egyei Tnfelügyelıség kéi szkos tnfelügyelıje volt. Részt vett lterntív kéitnkönyvek és tntervek kidolgozásábn. Jelentısen hozzájárult kéitnítás nygi feltételeinek jvításához és kéitnítás kísérleti oldlánk kihngsúlyozásához. A száítógépet is lklzt z okttásbn. Sok diákj vett részt eredényesen tntárgyi versenyeken ind helyi, jd 1990 után gyrországi Irinyi versenyen és 2000 között tnítványi egyei versenyen 18 lklol szereztek I. díjt, z országos döntın két tnuló III. díjt, közülük z egyik legjobb lborgykorltért járó díjt is egszerezte.
ROSSZUL OLDÓDÓ SÓK OLDHATÓSÁGI EGYENSÚLYAI
 ROSSZUL OLDÓDÓ SÓ OLDHATÓSÁGI EGYENSÚLYAI Igz Srolt Bevezetés Száos péld uttj, hogy egy dott hőérsékleten (és nyoáson) egy dott oldószer csk eghtározott ennyiségű nygot képes oldtbn trtni (telített oldt),
ROSSZUL OLDÓDÓ SÓ OLDHATÓSÁGI EGYENSÚLYAI Igz Srolt Bevezetés Száos péld uttj, hogy egy dott hőérsékleten (és nyoáson) egy dott oldószer csk eghtározott ennyiségű nygot képes oldtbn trtni (telített oldt),
Radioaktív nyomjelzés analitikai kémiai alkalmazásai
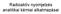 Rdioktív nyojelzés nlitiki kéii lklzási Izotóphígításos ódszerek A λn A ktivitás, n rdioktív gok ennyisége, bolási állndój. A fjlgos ktivitás kezdetben ( ): λn n N N z inktív hordozó ennyisége. N ennyiségű
Rdioktív nyojelzés nlitiki kéii lklzási Izotóphígításos ódszerek A λn A ktivitás, n rdioktív gok ennyisége, bolási állndój. A fjlgos ktivitás kezdetben ( ): λn n N N z inktív hordozó ennyisége. N ennyiségű
REÁLIS GÁZOK ÁLLAPOTEGYENLETEI FENOMENOLOGIKUS KÖZELÍTÉS
 REÁLIS GÁZOK ÁLLAPOEGYENLEEI FENOMENOLOGIKUS KÖZELÍÉS Száos odell gondoljunk potenciálo! F eltérés z ideális gáz odelljétl: éret és kölcsönhtás Moszkópikus következény: száos állpotegyenlet (ld. RM-jegyzet
REÁLIS GÁZOK ÁLLAPOEGYENLEEI FENOMENOLOGIKUS KÖZELÍÉS Száos odell gondoljunk potenciálo! F eltérés z ideális gáz odelljétl: éret és kölcsönhtás Moszkópikus következény: száos állpotegyenlet (ld. RM-jegyzet
Ez a kifejezés ekvivalens a termokémia részben már megismert standard reakció szabadentalpiával! A termodinamikai egyensúlyi állandó: egyensúlyi
 ÜLÖNÖZ REACIÓ EGYENSÚLYI ÁLLANDÓ Egyensúlybn: r G + RT ln Az egyenlet els tgj különböz ódokon írhtó el stndrd állotok egválsztásától üggen Ezek szerint ásodik tg s így z állndó értéke is változik h különböz
ÜLÖNÖZ REACIÓ EGYENSÚLYI ÁLLANDÓ Egyensúlybn: r G + RT ln Az egyenlet els tgj különböz ódokon írhtó el stndrd állotok egválsztásától üggen Ezek szerint ásodik tg s így z állndó értéke is változik h különböz
Sűrűségmérés. 1. Szilárd test sűrűségének mérése
 Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Radioaktív nyomjelzés analitikai kémiai alkalmazásai
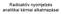 Rdioktív nyojelzés nlitiki kéii lklzási A rdioizotópos nyojelzős ódszerek csoportosítás gykorlti szepontok szerint Fiziki kéii ódszerek, pl.: oldékonyság eghtározás, diffúzió vizsgált, fázisok közötti
Rdioktív nyojelzés nlitiki kéii lklzási A rdioizotópos nyojelzős ódszerek csoportosítás gykorlti szepontok szerint Fiziki kéii ódszerek, pl.: oldékonyság eghtározás, diffúzió vizsgált, fázisok közötti
IZOTÓPHÍGÍTÁSOS ANALÍZIS
 IZOTÓPHÍGÍTÁSOS ANALÍZIS Az zotóphígításos elezés ódszerek ndegyk változtánk z lényege, hogy rdozotópr nézve zárt rendszerben z összktvtás (z dott zotóp ennysége) ne változk zzl, hogy stbl zotóp ennységét
IZOTÓPHÍGÍTÁSOS ANALÍZIS Az zotóphígításos elezés ódszerek ndegyk változtánk z lényege, hogy rdozotópr nézve zárt rendszerben z összktvtás (z dott zotóp ennysége) ne változk zzl, hogy stbl zotóp ennységét
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI III.
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
Általános Kémia Gyakorlat III. zárthelyi november 7.
 A1 Figyelem! Csak a követhetıen kidolgozott feladatokra adunk pontot. Kérjük, az összes eredményét ezeken a lapokon adja be, egyéb papírt nem fogadunk el. A megoldást minden esetben arra a lapra írja fel,
A1 Figyelem! Csak a követhetıen kidolgozott feladatokra adunk pontot. Kérjük, az összes eredményét ezeken a lapokon adja be, egyéb papírt nem fogadunk el. A megoldást minden esetben arra a lapra írja fel,
Radioaktív nyomjelzés a fizikai kémiában
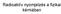 Rdioktív nyojelzés fiziki kéiábn Rdioktív nyojelzés fiziki kéiábn Oldékonyság eghtározás Hevesy: PbS oldékonyságánk eghtározás Pb ( NO 3 ) 0 PbS fjlgos ktivitás ugynnnyi szilárd ill. oldott állpotbn: /=áll.
Rdioktív nyojelzés fiziki kéiábn Rdioktív nyojelzés fiziki kéiábn Oldékonyság eghtározás Hevesy: PbS oldékonyságánk eghtározás Pb ( NO 3 ) 0 PbS fjlgos ktivitás ugynnnyi szilárd ill. oldott állpotbn: /=áll.
7. osztály 2 Hevesy verseny, országos döntő, 2004.
 7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
7. osztály 2 Hevesy verseny, országos döntő, 2004. Kedves Versenyző! Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő tíz feladat megoldására 90 perc áll rendelkezésedre.
Modern műszeres analitika szeminárium Mintavétel
 Modern űszeres nlitik szeináriu Mintvétel Glbács Gábor MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk és képletek áttekintése MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk
Modern űszeres nlitik szeináriu Mintvétel Glbács Gábor MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk és képletek áttekintése MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk
A vasbeton vázszerkezet, mint a villámvédelmi rendszer része
 Vsbeton pillér vázs épületek villámvédelme I. Írt: Krupp Attil Az épületek jelentős rze vsbeton pillérvázs épület formájábn létesül, melyeknél vázszerkezetet rzben vgy egzben villámvédelmi célr is fel
Vsbeton pillér vázs épületek villámvédelme I. Írt: Krupp Attil Az épületek jelentős rze vsbeton pillérvázs épület formájábn létesül, melyeknél vázszerkezetet rzben vgy egzben villámvédelmi célr is fel
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
Gyakorló feladatsor 9. osztály
 Gykorló feldtsor 9. osztály Hlmzok. Sorold fel z lábbi hlmzok elemeit! ) A={ legfeljebb kétjegyű 9-cel oszthtó páros pozitív számok} b) B={:prímszám, hol < 7} c) C={b=n+, hol nϵz és- n
Gykorló feldtsor 9. osztály Hlmzok. Sorold fel z lábbi hlmzok elemeit! ) A={ legfeljebb kétjegyű 9-cel oszthtó páros pozitív számok} b) B={:prímszám, hol < 7} c) C={b=n+, hol nϵz és- n
A torokgerendás fedélszerkezet erőjátékáról 1. rész
 A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
Szemináriumi feladatok megoldása (kiegészítés) I. félév
 Szemináriumi feldtok megoldás (kiegészítés) I. félév VI. Szeminárium 1. Frncis kísérlet (1925). Az ionos mechnizmus indirekt zzl támszthtó lá, hogy sem mgs hőmérsékletre, sem ultriboly fényre nincs szükség
Szemináriumi feldtok megoldás (kiegészítés) I. félév VI. Szeminárium 1. Frncis kísérlet (1925). Az ionos mechnizmus indirekt zzl támszthtó lá, hogy sem mgs hőmérsékletre, sem ultriboly fényre nincs szükség
Középiskolás leszek! matematika. 13. feladatsor 1. 2. 3. 4. 5. 6.
 Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
Az anyagi rendszerek csoportosítása
 Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Általános és szervetlen kémia 1. hét A kémia az anyagok tulajdonságainak leírásával, átalakulásaival, elıállításának lehetıségeivel és felhasználásával foglalkozik. Az általános kémia vizsgálja az anyagi
Összegezés az ajánlatok elbírálásáról
 Összegezés z jánltok elbírálásáról I. szksz: Ajánltkérő I.1) Név és cíek 1 (jelölje eg z eljárásért felelős összes jánltkérőt) Hivtlos név: Nyírtelek Város Önkorányzt Posti cí: Petőfi u. 28. Város: Nyírtelek
Összegezés z jánltok elbírálásáról I. szksz: Ajánltkérő I.1) Név és cíek 1 (jelölje eg z eljárásért felelős összes jánltkérőt) Hivtlos név: Nyírtelek Város Önkorányzt Posti cí: Petőfi u. 28. Város: Nyírtelek
2012/2013 tavaszi félév 9. óra
 2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
Magyar Mérnöki Kamara Beszámoló vizsga. Kérdésbank. Felkészülési segédlet. Mintakérdések. Geotechnika GT, SZÉS8. 2014. szeptember 08.
 Mgyr Mérnöki Kr Beszáoló vizsg Kérdésbnk Felkészülési segédlet Mintkérdések Geotechnik GT, SZÉS8 2014. szepteber 08. Trtlojegyzék I. Kérdésbnk....3 II. Mintkérdések..6 III. Felkészülési segédlet.7 1 I.
Mgyr Mérnöki Kr Beszáoló vizsg Kérdésbnk Felkészülési segédlet Mintkérdések Geotechnik GT, SZÉS8 2014. szepteber 08. Trtlojegyzék I. Kérdésbnk....3 II. Mintkérdések..6 III. Felkészülési segédlet.7 1 I.
Eredeti Veszprémi T. (digitálisan Csonka G) jegyzet: X. fejezet
 2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
VI. Deriválható függvények tulajdonságai
 1 Deriválhtó függvének tuljdonsági VI Deriválhtó függvének tuljdonsági Ebben fejezetben zt vizsgáljuk, hog deriválhtó függvének esetén derivált milen összefüggésben vn függvén más tuljdonságivl, és hogn
1 Deriválhtó függvének tuljdonsági VI Deriválhtó függvének tuljdonsági Ebben fejezetben zt vizsgáljuk, hog deriválhtó függvének esetén derivált milen összefüggésben vn függvén más tuljdonságivl, és hogn
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján.
 A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
A 27/2012. (VIII. 27.) NGM rendelet (29/2016. (VIII. 26.) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. Szakképesítés azonosítószáma és megnevezése 54 524 03 Vegyész technikus Tájékoztató
TENGELY szilárdsági ellenőrzése
 MISKOLCI EGYETEM GÉP- ÉS TERMÉKTERVEZÉSI TASZÉK OKTATÁSI SEGÉDLET GÉPELEMEK c. tntárgyhoz TEGELY szilárdsági ellenőrzése Összeállított: Dr. Szente József egyetemi docens Miskolc, 010. A feldt megfoglmzás
MISKOLCI EGYETEM GÉP- ÉS TERMÉKTERVEZÉSI TASZÉK OKTATÁSI SEGÉDLET GÉPELEMEK c. tntárgyhoz TEGELY szilárdsági ellenőrzése Összeállított: Dr. Szente József egyetemi docens Miskolc, 010. A feldt megfoglmzás
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
Kémia OKTV 2006/2007. II. forduló. A feladatok megoldása
 Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
1. feladat Oldja meg a valós számok halmazán a következő egyenletet: 3. x log3 2
 A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
Tartalom I. 1. Kohászat. 2. Egyedi Protanium acél. 3. Első osztályú korrózióvédelem. 4. Örökös garancia
 A profik válsztás pic egyetlen profi minőségű htszögkulcs Trtlom I. 1. Kohászt II. 2. Egyedi Protnium cél 3. Első osztályú korrózióvédelem 10 23 A szbványoknk vló 100%os megfelelés 26 Nincsenek rossz törések,
A profik válsztás pic egyetlen profi minőségű htszögkulcs Trtlom I. 1. Kohászt II. 2. Egyedi Protnium cél 3. Első osztályú korrózióvédelem 10 23 A szbványoknk vló 100%os megfelelés 26 Nincsenek rossz törések,
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
2012/2013 tavaszi félév 10. óra
 2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
Egy látószög - feladat
 Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Egyházashollós Önkormányzata Képviselőtestületének 9/ 2004. (IX.17) ÖR számú rendelete a helyi hulladékgazdálkodási tervről
 Egyházshollós Önkormányzt Képviselőtestületének 9/ 24. (IX.7) ÖR számú rendelete helyi hulldékgzdálkodási tervről Egyházshollós Önkormányztánk Képviselőtestülete z önkormányzti törvény (99. évi LXV. tv.)
Egyházshollós Önkormányzt Képviselőtestületének 9/ 24. (IX.7) ÖR számú rendelete helyi hulldékgzdálkodási tervről Egyházshollós Önkormányztánk Képviselőtestülete z önkormányzti törvény (99. évi LXV. tv.)
Mátrixok és determinánsok
 Informtik lpji Mátriok és erminánsok számok egyfjt tábláztát mátrink hívjuk. mátriok hsználhtóság igen sokrétő kezdve mtemtikávl, folyttv számítástechnikán és fizikán keresztül, egészen z elektrotechnikáig.
Informtik lpji Mátriok és erminánsok számok egyfjt tábláztát mátrink hívjuk. mátriok hsználhtóság igen sokrétő kezdve mtemtikávl, folyttv számítástechnikán és fizikán keresztül, egészen z elektrotechnikáig.
5 = nr. nrt V. p = p p T T. R p TISZTA FÁZISOK TERMODINAMIKAI FÜGGVÉNYEI IDEÁLIS GÁZOK. Állapotegyenletbl levezethet mennyiségek. Az állapotegyenlet:
 IZA FÁZIOK ERMODINAMIKAI FÜGGÉNYEI IDEÁLI GÁZOK Állaotegyenletbl levezethet ennyiségek Az állaotegyenlet: Moláris térfogat egváltozása: R R R R eroinaikai függvények Bels energia onoatoos ieális gázra
IZA FÁZIOK ERMODINAMIKAI FÜGGÉNYEI IDEÁLI GÁZOK Állaotegyenletbl levezethet ennyiségek Az állaotegyenlet: Moláris térfogat egváltozása: R R R R eroinaikai függvények Bels energia onoatoos ieális gázra
Modern m szeres analitika szeminárium Mintavétel
 Modern szeres nlitik szeináriu Mintvétel Glbács Gábor MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk és képletek áttekintése MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk
Modern szeres nlitik szeináriu Mintvétel Glbács Gábor MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk és képletek áttekintése MINTAVÉTELLEL KAPCSOLATOS SZÁMÍTÁSI FELADATOK A vontkozó foglk
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont. HCl (1 pont) HCO 3 - (1 pont) Ca 2+ (1 pont) Al 3+ (1 pont) Fe 3+ (1 pont) H 2 O (1 pont)
 KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
KÉMIAI ALAPISMERETEK (Teszt) Összesen: 150 pont 1. Adja meg a következő ionok nevét, illetve képletét! (12 pont) Az ion neve Kloridion Az ion képlete Cl - (1 pont) Hidroxidion (1 pont) OH - Nitrátion NO
FELVÉTELI VIZSGA, július 15.
 BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Exponenciális és logaritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek
 Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
T I T - M T T. Hevesy György Kémiaverseny. országos dönt. Az írásbeli forduló feladatlapja. 8. osztály. 2. feladat:... pont. 3. feladat:...
 T I T - M T T Hevesy György Kémiaverseny országos dönt Az írásbeli forduló feladatlapja 8. osztály A versenyz azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
T I T - M T T Hevesy György Kémiaverseny országos dönt Az írásbeli forduló feladatlapja 8. osztály A versenyz azonosítási száma:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:...
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. osztály 2 Hevesy verseny, megyei forduló, 2009.
 8. osztály 2 Hevesy verseny, megyei forduló, 2009. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthet legyen! A feladatok megoldásában a gondolatmeneted követhet
8. osztály 2 Hevesy verseny, megyei forduló, 2009. Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthet legyen! A feladatok megoldásában a gondolatmeneted követhet
Minőségi kémiai analízis
 Minőségi kémiai analízis Szalai István ELTE Kémiai Intézet 2016 Szalai István (ELTE Kémiai Intézet) Minőségi kémiai analízis 2016 1 / 32 Lewis-Pearson elmélet Bázisok Kemény Lágy Határestek H 2 O, OH,
Minőségi kémiai analízis Szalai István ELTE Kémiai Intézet 2016 Szalai István (ELTE Kémiai Intézet) Minőségi kémiai analízis 2016 1 / 32 Lewis-Pearson elmélet Bázisok Kemény Lágy Határestek H 2 O, OH,
Modul I Képzési szükségletek elemzése
 Modul I Képzési szükségletek elemzése A Képzési szükséglet-elemzési kézikönyv szerzoje: Instituto do Emprego e Formção Profissionl 1 Képzési szükségletek elemzése A következo oldlkon Önnek módj lesz föltenni
Modul I Képzési szükségletek elemzése A Képzési szükséglet-elemzési kézikönyv szerzoje: Instituto do Emprego e Formção Profissionl 1 Képzési szükségletek elemzése A következo oldlkon Önnek módj lesz föltenni
KÉMIA FELVÉTELI KÖVETELMÉNYEK
 KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
KÉMIA FELVÉTELI KÖVETELMÉNYEK Atomszerkezettel kapcsolatos feladatok megoldása a periódusos rendszer segítségével, illetve megadott elemi részecskék alapján. Az atomszerkezet és a periódusos rendszer kapcsolata.
Szent-Györgyi Albert kémiavetélkedő
 9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
9. osztály Kedves Versenyző! A jobb felső sarokban található mezőbe a verseny lebonyolításáért felelős személy írja be a kódot a feladatlap minden oldalára a verseny végén. A feladatokat lehetőleg a feladatlapon
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
V É R Z K A S A Y E N P
 Hevesy György Országos Kémiaverseny Kerületi forduló 2012. február 14. 7. évfolyam 1. feladat (1) Írd be a felsorolt anyagok sorszámát a táblázat megfelelő helyére! fémek anyagok kémiailag tiszta anyagok
Hevesy György Országos Kémiaverseny Kerületi forduló 2012. február 14. 7. évfolyam 1. feladat (1) Írd be a felsorolt anyagok sorszámát a táblázat megfelelő helyére! fémek anyagok kémiailag tiszta anyagok
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
Összesen: 20 pont. 1,120 mol gázelegy anyagmennyisége: 0,560 mol H 2 és 0,560 mol Cl 2 tömege: 1,120 g 39,76 g (2)
 I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
I. FELADATSOR (KÖZÖS) 1. B 6. C 11. D 16. A 2. B 7. E 12. C 17. E 3. A 8. A 13. D 18. C 4. E 9. A 14. B 19. B 5. B (E is) 10. C 15. C 20. D 20 pont II. FELADATSOR 1. feladat (közös) 1,120 mol gázelegy
Oldódás, mint egyensúly
 Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott K
2014/2015-ös tanév II. féléves tematika
 Dr Vincze Szilvi 24/25-ös tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási módszereik
Dr Vincze Szilvi 24/25-ös tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási módszereik
Megint a szíjhajtásról
 Megint szíjhjtásról Ezzel témávl már egy korábbi dolgoztunkbn is foglkoztunk ennek címe: Richrd - II. Most egy kicsit más lkú bár ugynrr vontkozó képleteket állítunk elő részben szkirodlom segítségével.
Megint szíjhjtásról Ezzel témávl már egy korábbi dolgoztunkbn is foglkoztunk ennek címe: Richrd - II. Most egy kicsit más lkú bár ugynrr vontkozó képleteket állítunk elő részben szkirodlom segítségével.
Juhász István Orosz Gyula Paróczay József Szászné Dr. Simon Judit MATEMATIKA 10. Az érthetõ matematika tankönyv feladatainak megoldásai
 Juhász István Orosz Gyul Próczy József Szászné Dr Simon Judit MATEMATIKA 0 Az érthetõ mtemtik tnkönyv feldtink megoldási A feldtokt nehézségük szerint szinteztük: K középszint, könnyebb; K középszint,
Juhász István Orosz Gyul Próczy József Szászné Dr Simon Judit MATEMATIKA 0 Az érthetõ mtemtik tnkönyv feldtink megoldási A feldtokt nehézségük szerint szinteztük: K középszint, könnyebb; K középszint,
Szombathelyi Csónakázó- és Horgásztó
 Szombthelyi Csónkázó- és Horgásztó Előzmények A Sporthorgász Egyesületek Vs Megyei Szövetségének horgászti kezelésében lévő Gersekráti Sárvíz-tó után z idei évben elkészült Szombthelyi Csónkázóés horgásztó
Szombthelyi Csónkázó- és Horgásztó Előzmények A Sporthorgász Egyesületek Vs Megyei Szövetségének horgászti kezelésében lévő Gersekráti Sárvíz-tó után z idei évben elkészült Szombthelyi Csónkázóés horgásztó
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
Indikátorok. brómtimolkék
 Indikátorok brómtimolkék A vöröskáposzta kivonat, mint indikátor Antociánok 12 40 mg/100 g ph Bodzában, ribizliben is! A szupersavak Szupersav: a kénsavnál erősebb sav Hammett savassági függvény: a savak
Indikátorok brómtimolkék A vöröskáposzta kivonat, mint indikátor Antociánok 12 40 mg/100 g ph Bodzában, ribizliben is! A szupersavak Szupersav: a kénsavnál erősebb sav Hammett savassági függvény: a savak
Oldhatósági számítások
 Oldhatósági számítások I. Az oldhatóság értelmezése A) A jód telített vizes oldatára vonatkozó adat nem megfelelő módon került megadásra. Nevezze meg a hibát, és számolja ki a helyes adatot! A hiba: Az
Oldhatósági számítások I. Az oldhatóság értelmezése A) A jód telített vizes oldatára vonatkozó adat nem megfelelő módon került megadásra. Nevezze meg a hibát, és számolja ki a helyes adatot! A hiba: Az
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
8. évfolym Mt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden oldhtod meg.
Interjú Dr. VÁRY Annamáriával
 18 Interjú Dr. VÁRY Annmáriávl MA MÁR NEM PÁLYÁRA, HANEM ÁTMENETEKRE ÉS MÓDOSÍTÁSOK SOROZATÁRA KELL FELKÉSZÜLNI. D r. Váry Annmári kliniki és pálytnácsdó szkpszichológus, pszichoterpeut, Wekerle Sándor
18 Interjú Dr. VÁRY Annmáriávl MA MÁR NEM PÁLYÁRA, HANEM ÁTMENETEKRE ÉS MÓDOSÍTÁSOK SOROZATÁRA KELL FELKÉSZÜLNI. D r. Váry Annmári kliniki és pálytnácsdó szkpszichológus, pszichoterpeut, Wekerle Sándor
Egészsége és jó közérzete
 Egészsége és jó közérzete Kidney Disese nd Qulity of Life (KDQOL-SF ) Ez kérdőív zt méri fel, hogy Ön hogyn vélekedik z egészségéről. Az így kpott információ segíteni fog nyomon követni, hogy Ön hogy érzi
Egészsége és jó közérzete Kidney Disese nd Qulity of Life (KDQOL-SF ) Ez kérdőív zt méri fel, hogy Ön hogyn vélekedik z egészségéről. Az így kpott információ segíteni fog nyomon követni, hogy Ön hogy érzi
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
1. Végezd el a kijelölt mûveleteket a betûk helyére írt számokkal! Húzd alá azokat a mûveleteket,
 Számok és mûveletek + b b + Összedásnál tgok felcserélhetõk. (kommuttív tuljdonság) ( + b) + c + (b + c) Összedásnál tgok csoportosíthtók. (sszocitív tuljdonság) b b ( b) c (b c) 1. Végezd el kijelölt
Számok és mûveletek + b b + Összedásnál tgok felcserélhetõk. (kommuttív tuljdonság) ( + b) + c + (b + c) Összedásnál tgok csoportosíthtók. (sszocitív tuljdonság) b b ( b) c (b c) 1. Végezd el kijelölt
2010/2011 es tanév II. féléves tematika
 2 február 9 Dr Vincze Szilvi 2/2 es tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási
2 február 9 Dr Vincze Szilvi 2/2 es tnév II féléves temtik Mátrix foglm, speciális mátrixok Műveletek mátrixokkl, mátrix inverze 2 A determináns foglm és tuljdonsági 3 Lineáris egyenletrendszerek és megoldási
A BUX-index alakulása a 4. héten ( )
 A BUX-index lkulás A BUX-index lkulás 2010 jnuár 30. Flg 0 Értékelés kiválsztás Még Givenincs A BUX-index értékelve lkulás Give A BUX-index lkulás Give A BUX-index lkulás Mérték Give A BUX-index lkulás
A BUX-index lkulás A BUX-index lkulás 2010 jnuár 30. Flg 0 Értékelés kiválsztás Még Givenincs A BUX-index értékelve lkulás Give A BUX-index lkulás Give A BUX-index lkulás Mérték Give A BUX-index lkulás
Az ABCD köré írható kör egyenlete: ( x- 3) + ( y- 5) = 85. ahol O az origó. OB(; 912). Legyen y = 0, egyenletrendszer gyökei adják.
 5 egyes feldtok Az dott körök k : x + ( y- ) = és k : ( x- ) + y = K (; 0), r, K (; 0), r K K = 0 > +, két körnek nincs közös pontj Legyen (; ) Az egyenlô hosszú érintôszkszokr felírhtjuk következô egyenletet:
5 egyes feldtok Az dott körök k : x + ( y- ) = és k : ( x- ) + y = K (; 0), r, K (; 0), r K K = 0 > +, két körnek nincs közös pontj Legyen (; ) Az egyenlô hosszú érintôszkszokr felírhtjuk következô egyenletet:
A Szolgáltatás minőségével kapcsolatos viták
 I. A Szolgálttó neve, címe DITEL 2000 Kereskedelmi és Szolgálttó Korlátolt Felelősségű Társság 1051. Budpest, Nádor u 26. Adószám:11905648-2- 41cégjegyzékszám: 01-09-682492 Ügyfélszolgált: Cím: 1163 Budpest,
I. A Szolgálttó neve, címe DITEL 2000 Kereskedelmi és Szolgálttó Korlátolt Felelősségű Társság 1051. Budpest, Nádor u 26. Adószám:11905648-2- 41cégjegyzékszám: 01-09-682492 Ügyfélszolgált: Cím: 1163 Budpest,
Bevezetés. Mi a koleszterin?
 Bevezet betegklub feldt tgji számár betegségükkel kpcsoltos szkszerű információkt megdni. Ebben füzetben koleszterin htásiról cukorbetegségről gyűjtöttünk össze hsznos információkt. Mi koleszterin? koleszterin
Bevezet betegklub feldt tgji számár betegségükkel kpcsoltos szkszerű információkt megdni. Ebben füzetben koleszterin htásiról cukorbetegségről gyűjtöttünk össze hsznos információkt. Mi koleszterin? koleszterin
MATEMATIKA FELADATLAP a 6. évfolyamosok számára
 6. évfolym AMt2 feldtlp MATEMATIKA FELADATLAP 6. évfolymosok számár 2011. jnuár 27. 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden
6. évfolym AMt2 feldtlp MATEMATIKA FELADATLAP 6. évfolymosok számár 2011. jnuár 27. 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrenden
1. feladat Összesen: 8 pont. 2. feladat Összesen: 11 pont. 3. feladat Összesen: 7 pont. 4. feladat Összesen: 14 pont
 1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
Elektrokémia 04. Cellareakció potenciálja, elektródreakció potenciálja, termodinamikai paraméterek meghatározása példa. Láng Győző
 Elektokémi 04. Cellekció potenciálj, elektódekció potenciálj, temodinmiki pméteek meghtáozás péld Láng Győző Kémii Intézet, Fiziki Kémii Tnszék Eötvös Loánd Tudományegyetem Budpest Az elmélet lklmzás konkét
Elektokémi 04. Cellekció potenciálj, elektódekció potenciálj, temodinmiki pméteek meghtáozás péld Láng Győző Kémii Intézet, Fiziki Kémii Tnszék Eötvös Loánd Tudományegyetem Budpest Az elmélet lklmzás konkét
6. Laboratóriumi gyakorlat KAPACITÍV SZINTÉRZÉKELŐK
 6. Lbortóriumi gykorlt KAPAITÍV SZINTÉRZÉKELŐK. A gykorlt célj A kpcitív szintmérés elvének bemuttás. A (x) jelleggörbe ábrázolás szigetelő és vezető olyékok esetén. Egy stbil multivibrátor elhsználás
6. Lbortóriumi gykorlt KAPAITÍV SZINTÉRZÉKELŐK. A gykorlt célj A kpcitív szintmérés elvének bemuttás. A (x) jelleggörbe ábrázolás szigetelő és vezető olyékok esetén. Egy stbil multivibrátor elhsználás
a. 35-ös tömegszámú izotópjában 18 neutron található. b. A 3. elektronhéján két vegyértékelektront tartalmaz. c. 2 mól atomjának tömege 32 g.
 MAGYAR TANNYELVŰ KÖZÉPISKOLÁK IX. ORSZÁGOS VETÉLKEDŐJE AL IX.-LEA CONCURS PE ŢARĂ AL LICEELOR CU LIMBĂ DE PREDARE MAGHIARĂ FABINYI RUDOLF KÉMIA VERSENY - SZERVETLEN KÉMIA Marosvásárhely, Bolyai Farkas
MAGYAR TANNYELVŰ KÖZÉPISKOLÁK IX. ORSZÁGOS VETÉLKEDŐJE AL IX.-LEA CONCURS PE ŢARĂ AL LICEELOR CU LIMBĂ DE PREDARE MAGHIARĂ FABINYI RUDOLF KÉMIA VERSENY - SZERVETLEN KÉMIA Marosvásárhely, Bolyai Farkas
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Mi a hasonlóság és mi a különbség a felsorolt kémiai részecskék között? Hasonlóság:... Különbség: atom a belőle származó (egyszerű) ion
 Kedves Versenyző! 2 Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási feladatok
Kedves Versenyző! 2 Köszöntünk a Hevesy György kémiaverseny országos döntőjének írásbeli fordulóján. A következő kilenc feladat megoldására 90 perc áll rendelkezésedre. A feladatokat a számítási feladatok
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyz jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym TMt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. évfolym TMt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
A bizonytalanság és az információ közgazdaságtana
 (C) hp://kg.be.h/ /4 A bizonylnság és z inforáció közgzdságn Mjor Iván A közgzdságn fıárlánk lpelvei A neoklssziks közgzdságn lpji: közgzdságn, in ársdli fizik (Jevons, Menger, Böh-Bwerk és z oszrák iskol)
(C) hp://kg.be.h/ /4 A bizonylnság és z inforáció közgzdságn Mjor Iván A közgzdságn fıárlánk lpelvei A neoklssziks közgzdságn lpji: közgzdságn, in ársdli fizik (Jevons, Menger, Böh-Bwerk és z oszrák iskol)
ÖSSZEHASONLÍTÓ ELEMZÉS
 ÖSSZEHASONLÍTÓ ELEMZÉS AZ X11-ARIMA/88 ÉS A TRAMO/SEATS eljárások lklzásáról unkügyi idősorokon (Előzetes változt) Készítette MultiRáció Kt. Budest, 2006. noveber 1 Bevezetés Társságunk "Az Eberi Erőorrások
ÖSSZEHASONLÍTÓ ELEMZÉS AZ X11-ARIMA/88 ÉS A TRAMO/SEATS eljárások lklzásáról unkügyi idősorokon (Előzetes változt) Készítette MultiRáció Kt. Budest, 2006. noveber 1 Bevezetés Társságunk "Az Eberi Erőorrások
II. A számtani és mértani közép közötti összefüggés
 4 MATEMATIKA A 0. ÉVFOLYAM TANULÓK KÖNYVE II. A számtni és mértni közép közötti összefüggés Mintpéld 6 Számítsuk ki következő számok számtni és mértni közepeit, és ábrázoljuk számegyenesen számokt és közepeket!
4 MATEMATIKA A 0. ÉVFOLYAM TANULÓK KÖNYVE II. A számtni és mértni közép közötti összefüggés Mintpéld 6 Számítsuk ki következő számok számtni és mértni közepeit, és ábrázoljuk számegyenesen számokt és közepeket!
Jegyzőkönyv. Termoelektromos hűtőelemek vizsgálatáról (4)
 Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
3-4.elıadás: Optimális választás; A fogyasztó kereslete
 (C) htt://kgt.e.hu/ / 3-4.elıdás: Otiális válsztás; A fogysztó kereslete A fogysztó válsztási roléáj A fogysztó száár elérhetı (egfizethetı) jószágkosrk közül neki legjot válsztj A fogysztó költségvetési
(C) htt://kgt.e.hu/ / 3-4.elıdás: Otiális válsztás; A fogysztó kereslete A fogysztó válsztási roléáj A fogysztó száár elérhetı (egfizethetı) jószágkosrk közül neki legjot válsztj A fogysztó költségvetési
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyz jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Javítókulcs (Kémia emelt szintű feladatsor)
 Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. C 2. B. fenolos hidroxilcsoport, éter, tercier amin db. ; 2 db. 4. észter 5. E 6. A tercier amino-nitrogén. 7. Pl. a trimetil-amin reakciója HCl-dal.
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
2018/2019-es iskolaév, júniusi vizsgaidőszak A VIZSGAKÉRDÉSEK LISTÁJA A VÁLASZTHATÓ TANTÁRGYBÓL
 MŰSZAKI ISKOLA ÉRETTSÉGI VIZSGA ADA, 09 árcius 08/09-es iskolév, júniusi vizsgidőszk A VIZSGAKÉRDÉSEK LISTÁJA A VÁLASZTHATÓ TANTÁRGYBÓL Munkterület: GÉPÉSZET, ELEKTROTECHNIKA, ÉPITÉSZET Tntárgy: MATEMATIKA
MŰSZAKI ISKOLA ÉRETTSÉGI VIZSGA ADA, 09 árcius 08/09-es iskolév, júniusi vizsgidőszk A VIZSGAKÉRDÉSEK LISTÁJA A VÁLASZTHATÓ TANTÁRGYBÓL Munkterület: GÉPÉSZET, ELEKTROTECHNIKA, ÉPITÉSZET Tntárgy: MATEMATIKA
Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása
 Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Vektortér fogalma vektortér lineáris tér x, y x, y x, y, z x, y x + y) y; 7.)
 Dr. Vincze Szilvi Trtlomjegyzék.) Vektortér foglm.) Lineáris kombináció, lineáris függetlenség és lineáris függőség foglm 3.) Generátorrendszer, dimenzió, bázis 4.) Altér, rng, komptibilitás Vektortér
Dr. Vincze Szilvi Trtlomjegyzék.) Vektortér foglm.) Lineáris kombináció, lineáris függetlenség és lineáris függőség foglm 3.) Generátorrendszer, dimenzió, bázis 4.) Altér, rng, komptibilitás Vektortér
Oldódás, mint egyensúly
 Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott =
Oldódás, mint egyensúly Szilárd (A) anyag oldódása: K = [A] oldott [A] szilárd állandó K [A] szilárd = [A] oldott S = telített oldat conc. Folyadék oldódása: analóg módon Gázok oldódása: [gáz] oldott =
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
8. évfolym Mt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zsebszámológépet nem hsználhtsz. A feldtokt tetszés szerinti sorrendben oldhtod meg.
JÁRÁSI SZINTŰ ESÉLYTEREMTŐ PÜSPÖKL ADÁNYI JÁRÁS
 Püspökldány Város Önkormányzt 4150 Püspökldány, Bocski u. 2. Telefon 54/451-510 www.pupokldny.hu JÁRÁSI SZINTŰ ESÉLYTEREMTŐ PROGRAMTERV PÜSPÖKL ADÁNYI JÁRÁS 2015-2020 Készült: Püspökldány Város Önkormányzt
Püspökldány Város Önkormányzt 4150 Püspökldány, Bocski u. 2. Telefon 54/451-510 www.pupokldny.hu JÁRÁSI SZINTŰ ESÉLYTEREMTŐ PROGRAMTERV PÜSPÖKL ADÁNYI JÁRÁS 2015-2020 Készült: Püspökldány Város Önkormányzt
7. osztály Hevesy verseny, megyei forduló, 2003.
 Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
A feladatok megoldásához csak a kiadott periódusos rendszer és számológép használható!
 1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
1 MŰVELTSÉGI VERSENY KÉMIA TERMÉSZETTUDOMÁNYI KATEGÓRIA Kedves Versenyző! A versenyen szereplő kérdések egy része általad már tanult tananyaghoz kapcsolódik, ugyanakkor a kérdések másik része olyan ismereteket
