Chaperonok. A felgombolyodás orvosi és biotechnológiai vonatkozásai.
|
|
|
- Mariska Kocsis
- 8 évvel ezelőtt
- Látták:
Átírás
1 Chaperonok. A felgombolyodás orvosi és biotechnológiai vonatkozásai. 1. Chaperonok 2. Amiloidózisok és prionbetegségek 3. Inklúziós testek renaturálása A chaperonok (dajkafehérjék, chaperon=gardedám) más fehérjék nemnatív állapotaihoz kötõdnek ezeket segítik a natív konformáció elérésében általában ATP felhasználásával Chaperonok Miért van szükség chaperonokra? In vitro is számos fehérjét nem tudunk renaturálni In vivo többféle szituáció teszi szükségessé a chaperonokat: a fehérjeszintézis során a naszcens polipeptidlánc inkorrekt kölcsönhatásokba léphet saját magával vagy a környezetében lévõ molekulákkal (pl. ha az N terminálisnak a C terminálissal kellene kölcsönhatásba kerülnie, de a C terminális még nincs készen) A membránokon transzlokálódó fehérjéknek részlegesen vagy teljesen legombolyodott állapotban kell átbújniuk a membránon. Szükséges egy mechanizmus, ami erre az idõre legombolyodott állapotban tartja, utána lehetõvé teszi a felgombolyodást. Számos fehérje funkciójához hozzátartozik, hogy alegységei disszociáljanak, s amikor kell, újra asszociálódjanak (pl. mikrotubulusok, klatrinburkos vezikulák, DNS replikáció egyes fehérjéi) Egyes organellumfehérjék alegységeinek egy része az organellumban, más része a citoplazmában szintetizálódik (pl. Rubisco). Meg kell akadályozni az inkorrekt kölcsönhatásokat, míg az összes alegység egy helyre nem kerül. Stressz hatására (pl. hõsokk) sok fehérje denaturálódik, aggregálódik. Ebbõl az állapotból regenerálódni kell. Példák chaperonokra Család Tagok Egyéb nevek Chaperoninok Hsp70 Hsp90 PapD GimC Chaperonin 60 Chaperonin 10 Hsp68, 72, 73; DnaK BiP, Grp75, 78, 80, Hsc70 KAR2, SSAI 4, stb. Hsp83, 87, HtpG PapD, FimC Gim1 6, Gim1, Gim5 Bakteriális: GroEL (E. coli) Kloroplasztisz: RBP (Rubisco subunit Binding Protein) Mitokondriális: Hsp60 Eukariota citoszol: TRiC Bakteriális: GroES Mitokondriális Ezeken kívül még számos család (Hsp100, Hsp90, Hsp40, kis Hsp k, stb.) 1
2 Az egyes chaperonféleségek mûködési módjukban is különböznek. A két legjobban jellemzett csoport (csak ezek létfontosságúak, a többi chaperon nem): Hsp70: nyújtott lánc egy pontjához kötõdik, lokálisan hat Hsp60 (chaperoninok): kompakt nemnatív állapotot köt, az egészet körülveszi A Hsp70 chaperoncsalád Stressz hatására is indukálódik, de normál körülmények között is jelen van segíti egyes, újonnan transzlálódott fehérjék felgombolyodását segíti fehérjék transzlokációját membránokon segíti oligomerek szétszerelõdését segíti az instabil fehérjék proteolitikus degradációját egyes fehérjék (pl. transzkripciós faktorok) aktivitását is szabályozza Legjobban jellemzett: bakteriális Hsp70: DnaK A Hsp70 hatása A nyújtott lánchoz egy ponton kötõdik, ezzel megóvja a láncot az aggregációtól vagy a felgombolyodástól. ATP hidrolízise szabályozza a disszociációt. Doménszerkezet 2
3 ATPáz domén: N terminális, 44 kda szubsztrátkötõ domén: 25 kda, két részdoménbõl áll: tulajdonképpeni szubsztrátkötõ domén: 15 kda C terminális domén: 10 kda, kevésbé konzerválódott DnaK fehérje szubsztrátkötõ doménje és NRLLLTG peptid komplexe Két négyszálú béta lemez egymás fölött, ezek fölött néhány hélix a felsõ béta lemez négy hurkot bocsát ki, kettõ képezi a szubsztrátkötõ zsebet, ami egy 5x7 angström keresztmetszetû csatorna A B hélix fedélszerûen ráborul a hurkokra, a csatorna tetejét képezve A hélix egy ponton fel tud nyílni, szabaddá téve a zsebet A peptid nyújtott, mintegy átszúrja a fehérjét, három középsõ hidrofób oldallánca és a végeken lévõ egyéb oldalláncok lépnek csak kölcsönhatásba a fehérjével A csatorna végei negatív töltésûek Mit köt a DnaK? Konszenzusmotívum: 2 4 hidrofób oldallánc, melyek végein egyéb, de nem savas oldallánc van. Ilyen motívum minden fehérjében átlag 36 aminosavanként elõfordul 3
4 A DnaK ATPáz doménje Két nagy, globuláris szubdomén, köztük mély hasadék, ez a nukleotidkötõ zseb A DnaK két állapota ATP kötött állapot: a fehérjeszubsztrát kötõ csatorna nyitva van, szubsztrát szabadon kötõdhet, ill. leválhat ATP nélküli (azaz nukleotid nélküli vagy ADP kötött) állapot: a fehérjeszubsztrát kötõ csatorna zárva van, szubsztrát be van zárva (ha van) A mechanikai munka keletkezésének mechanizmusa, az ATPáz doménrõl a szubsztrátkötõ doménre az információ átvitelének mikéntje nem tisztázott Kochaperonok A DnaK önmagában is mûködik, de nem elég hatékony. Két kochaperon segíti: DnaJ és GrpE. Együtt több százszorosára növelik a DnaK turnoverjét. DnaJ GrpE J domén: N terminális 80 aminosav Maga is képes a peptidszubsztrátot kötni, azt a DnaK nak át tudja adni A DnaK ATPáz aktivitását stimulálja A DnaK ATPáz doménjéhez köt, serkenti az ADP disszociációját. A DnaK rendszer mûködése 4
5 1. A DnaJ megköti a szubsztrátot [a DnaK ATP is megkötheti] 2. A DnaJ a J doménjével kötõdik a DnaK ATP ATPáz doménjéhez, átadja a szubsztrátkötõ doménnek a szubsztrátot, és elõsegíti az ATP hidrolizálását 3. Megtörténik az ATP hidrolízise. A szubsztrátkötõ zseb bezárul, a DnaJ leválik 4. Jön a GrpE és letaszítja az ADP t 5. Az ADP helyére bejön egy ATP. A zseb felnyílik, a szubsztrát kiszabadul. A GrpE leválik. Kezdõdhet a ciklus elölrõl. Általában többször ismétlõdik a szubsztrát kötése és disszociációja A disszociált szubsztrát lehetõségei: felgombolyodik aggregálódik visszaköt a Hsp70 hez más chaperonhoz köt A Hsp60 chaperoncsalád (chaperoninok) Chaperonin: kezdetben egy olyan csoportnak adták a nevet, amit prokariotákban, valamint mitokondriumokban és kloroplasztiszokban találtak. Késõbb eukariota citoplazmában is felfedezték. Stressz hatására indukálódik, de normálisan is sok van belõle segíti a fehérjék felgombolyodását, fõleg "misfolded" ("félregombolyodott") állapotból segíti az oligomerizációt (a monomerek helyes felgombolyodásának elõsegítésével) E. coliban GroEL, GroES: életfontosságú fehérjék GroEL: az E. coli összes fehérjéjének felét köti legombolyodott állapotban fehérjeszintézisnél és membrántranszportnál is kötõdik a polipeptidekhez Kloroplasztiszban: RBP Rubisco Binding Protein: hozzákötõdik a Rubisco nagy alegységeihez, amíg a kis alegységek meg nem érkeznek a citoplazmából Legjobban jellemzett: E. coli GroEL, GroES A GroEL/ES szerkezete 5
6 GroEL: 2x7 alegységbõl álló, gyûrû alakú komplex, közepén nagy üreggel GroES: 7 db, 10 kda alegységbõl álló gyûrû Két fõ állapot: peptidfogadó állapot (ábra bal oldal): az üreg nyitott a külvilág felé, belsõ hidrofób felszíne köti a szubsztrátfehérjét felgombolyodás aktív állapot (ábra jobb oldal): ATP kötés és a GroES sapka bekötõdése révén jön létre. Az üreg megnõ, a GroES kupolája lezárja. Az üreg falának jellege megváltozik (inkább hidrofil lesz). Az üregben lévõ fehérje felgombolyodik. Átkapcsolás a két állapot között 6
7 A GroEL alegység 3 doménbõl áll: apikális (a csúcsnál), ekvatoriális (a komplex középvonala felé esõ), köztes (a kettõ között) Az átkapcsolásnál nagyszabású doménmozgások történnek: A köztes domén 25 fokkal lehajlik, bezárva az alatta az ekvatoriális doménben lévõ ATP t Az apikális domén 65 fokkal felhajlik, azaz nagyban megemelõdik, s eközben hossztengelye körül is 90 fokkal elfordul Az üreg térfogata kétszeresére nõ Teljesen megváltozik az üreg falának a jellege, a szubsztrátfehérje leválik a falról A két gyûrû együttmûködése Az egyik gyûrûben az ATP k bekötõdése (7 db!) kiváltja a másik gyûrûben az ES sapka és az ADP k disszociációját Az ES kötése az egyik gyûrûhöz erõsen gátolja egy másik ES kötését a másik gyûrûhöz Egy gyûrûn belül az ATP k kötése kooperatív, a másik gyûrû ATP kötését viszont hátráltatja Az ATP kötés és az ATP hidrolízis szerepe ATP kötés: a GroES kötéssel együtt ez idézi elõ az átkapcsolást a felgombolyodás aktív állapotba, azaz a nagyléptékû doménmozgásokat a másik gyûrûnél kiváltja a GroES és az ADP k lelökõdését ATP hidrolízis: meggyengíti a GroES kötõdését, hogy az késõbb leválhasson ezáltal továbblépteti a "gépet" a következõ állapotba Idõtartamok (23 Celsius fokon) Az üregbe bekötõdik a felgombolyítandó fehérje Kötõdik az ATP és a GroES 1 másodperc múlva megtörténik az átkapcsolás, a szubsztrátfehérje leválik az üreg faláról és elkezd felgombolyodni 5 10 másodperc múlva megtörténik az ATP hidrolízise A szubsztrátfehérje még további másodpercet tölt a zárt üregben, próbál gombolyodni (összesen kb. 20 másodperce van) ezután megtörténik a GroES lelökõdése, a szubsztrátfehérje távozik Hatékonyság: több mint 90% ban sikeres felgombolyítás A mûködés sémája 7
8 Valószínûleg kétütemû mûködés (hol az egyik, hol a másik üreg dolgozik) Nyitott kérdések Milyen konformációban kötõdik a szubsztrátfehérje? (Valószínûleg részlegesen felgombolyodott, félregombolyodott, olvadt gombóc jellegû) A kötõdés növeli e a szubsztrát legombolyodottságát? Az átkapcsoláskor a doménmozgás tovább gombolyítja e le a szubsztrátot? (Vsz. igen) Miután a szubsztrát levált a csatorna faláról, kölcsönhatásba lép e még vele, vagy úgy érzékeli, hogy semmi sincs körülötte (végtelen higítás)? Ha többször átmegy a szubsztrát a chaperonon, közben fejlõdik e az állapota, vagy mindig ugyanabból az állapotból indul? Egyáltalán: mi történik a szubsztrát konformációjával az egész folyamatban? Felgombolyodási betegségek: amiloidózisok Amiloid: rostos fehérjelerakódások (extra vagy intracellulárisak), melyek betegségekkel járnak együtt Amiloidózisok: Lassan kialakuló, degeneratív betegségek Sok esetben azonosították a rostos lerakódások fõ fehérjekomponensét: Betegségek Fehérje Betegség ABri alpha Synuclein A beta (amiloid béta peptid) Gelsolin Huntingtin IAPP (islet amyloid polypeptide) Immunoglobulin V L domain Lysozyme Medin SAA (serum amyloid A) Tau Familial British dementia Parkinson kór Alzheimer kór Finnish type familial amyloidosis Huntington kór Type II diabetes Light chain amyloidosis Hereditary systemic amyloidosis Aortic medial amyloid Secondary systemic amyloidosis Alzheimer kór, frontotemporal dementia TTR (transthyretin) Senile systemic amyloidosis, familial amyloid polyneuropathy A rostok jellemzõen "kereszt béta" szerkezetûek: a hossztengelyre merõleges béta szálakat tartalmaznak 8
9 A betegségek okai valószínûleg a lerakódások (a betegségre való hajlamot fokozó mutációkról több esetben kimutatták, hogy növelik az adott fehérje rostképzõ hajlamát) A résztvevõ fehérjék sokfélék, natív szerkezetük között nincs hasonlóság A rostképzõdés részlegesen fel, ill. legombolyodott állapotból indul Több globuláris fehérjérõl (lizozim, TTR, V L ) kimutatták: részlegesen le kell gombolyodniuk a rostképzéshez A fokozott rostképzõdést okozó mutációk ált. destabilizálják a natív konformációt, növelve a részlegesen felgombolyodott állapot populációját Több fehérjébõl sikerült részlegesen denaturáló körülmények között rostképzõdést kiváltani Legombolyodott állapotban a legstabilabbak a következõ peptidekn: amiloid béta peptid (A béta), IAPP, alfa synuclein, tau. Az A béta és a IAPP esetében kimutatták: a rostképzõdést megelõzi egy olvadt gombóc jellegû, a natívnál jóval több másodlagos szerkezetet tartalmazó állapot átmeneti jelentkezése Proteolízis és rostképzõdés Számos amiloidogén fehérje egy nagyobb lánc proteolitikus fragmentuma (pl. A béta, ABri, medin, gelsolin). A proteolízisre való érzékenységet megnövelõ mutációk növelik a peptid mennyiségét > nõ a rostképzõdés valószínûsége A rostképzõdés mechanizmusa: nukleációfüggõ oligomerizáció Globuláris fehérjébõl vagy legombolyodott fehérjébõl részleges szerkezetû amiloidogén intermedier keletkezik A némi béta szerkezetet is tartalmazó intermedier rendezetlen, amorf aggregátumokat képezhet, vagy ha a koncentráció meghalad egy kritikus értéket, akkor rendezett önasszociáció révén béta lemezes nukleuszt képez a béta lemez növekedésével a szerkezet növekszik, oligomer, majd fibrillum jön létre Protofibrillumok A fibrillum ált. nem monomerek hozzáadásával növekszik, hanem hosszabb rövidebb protofibrillumok jönnek létre, s ezek állnak össze Elektronmikroszkópos kép: azt mutatja, hogy a protofibrillumok gyöngysorszerûek, gömböcskékbõl állnak Több protofibrillum összecsavarodhat, így állnak össze fibrillummá 9
10 bal: gyöngysorszerû protofibrillumok; jobb: kész fibrillumok is A rostok 3D szerkezete Egy vastag rost több szálból (protofilamentumból) állhat Sokféle morfológia lehet (egyenes, görbült, csavart, nem csavart, stb.) Fehérje Morfológia Méretek (nm) Acylphosphatase Egyenes d = 3 5 alpha Synuclein (wild type, A53T, A30P) Egyenes, csavart d=10, h=8 10, d=10 19, d=12 IAPP Egyenes vagy kissé görbe, csavart h=5.2, p=49, h=6.8, p=25 Abeta42 Egyenes d = 7 10 CspB (residues 1 22) Egyenes d = 10 10
11 Gelsolin (residues ) Egyenes vagy kissé görbe d = Immunoglobulin V L domain Egyenes d = 5 Lithostathine (residues ) Egyenes, sima d = Medin (residues ) Egyenes d = 7 P22 tailspike beta helix domain Görbe, csavart d = 50 SAA (residues 1 11) Pálcika vagy szalagszerû, csavart d = 4 7 (h: magasság, d: átmérõ, p: tengely menti periodicitás) További kutatási irányok A rostképzõdés in vivo mechanizmusa A környezet hatása (hõmérséklet, ionerõsség, ph, redoxpotenciál) A felületek hatása (membránok közelsége) A betegség kialakulása (milyen káros hatása van a rostoknak, a protofibrillumoknak, stb.) Felgombolyodási betegségek: Prionbetegségek Prionbetegség: ez is amiloidózis, de fertõzõ Transmissible spongiform encephalopathies (átvihetõ szivacsos agyvelõelváltozások), TSE marha: BSE, ember: Creutzfeldt Jakob (CJD), Gerstmann Straussler Scheinker (GSS), fatal familial insomnia (FFI) A prionok tulajdonságai Normális, celluláris forma: PrP C központi idegrendszerben (nyirokszövetben, ideg izom kapcsolatnál) funkciója nem ismert glikozilált sejtfelszíni fehérje, glikolipid horgony tartja (NMR szerk. alapján, aminosavak, a többi rendezetlen) 11
12 Kóros ("scrapie") forma: PrP Sc csak konformációban tér el a PrP C tõl önasszociáció révén stabil aggregátumokat képez senki sem tisztította még meg konformációja nem ismert ellenáll a proteináz K kezelésnek Mi a fertõzõ ágens? Hipotézis: maga a PrP Sc fertõzhet nukleinsav mentes fertõzõ kivonatokat lehet készíteni > "protein only" hipotézis Különvélemények: nem a PrP Sc (egyes kísérleti eredmények) A terjedés modellje (a) egyensúly a PrP C és a PrP Sc között (utóbbi ritka) (b) a PrP Sc monomerek gyengén és reverzibilisen asszociálódnak, míg ki nem alakul egy stabil, fertõzõképes mag (c) a kritikus méret elérése után a monomerek már irreverzibilisen asszociálódnak hozzá a lánchoz, ami tovább növekszik (d) a fertõzõ részecske kisebb, stabil darabokra törve "szaporodik" Másik modell: a PrP C átalakul egy köztes, PrP * állapotba, ehhez hozzáköt a PrP Sc és öntõformaként szolgálva átalakítja PrP Sc vé. Mindkét modell megmagyarázza, hogy a prionbetegség a következõ módokon alakul ki: a priongén öröklött mutációja miatt a PrP C kevésbé stabil, könnyebben átalakul PrP Sc vé Kívülrõl bevitt PrP Sc (táplálékkal vagy orvosi bevatkozásnál) Szomatikus mutáció Ritkán: spontán átalakulás Felgombolyodási kísérletek Élettani körülmények között gyors, kétállapotú átmenet Savas ph n (ph=4) jelentõs egyensúlyi intermedier, túlnyomórészt béta szerkezetû, rostokká aggregálódik, ellenáll a proteináz K nak. Ez lehet a PrP Sc felé vezetõ állapot. Nyitott kérdések Valóban a prion a fertõzõ ágens? Mi pusztítja el a sejteket? 12
13 Egyéb felgombolyodási betegségek Hibás felgombolyodás miatt az aktív fehérje hiánya által okozott betegségek: Sarlósejtes vérszegénység: A hemoglobin béta alegységében Glu6 Val pontmutáció miatt a deoxigenált hemoglobin oldhatósága csökkent, rostos precipitátumokat képez. Sarló alakú vörösvérsejtek. Juharszirup vizelet: az elágazó láncú aminosavak lebontását végzõ mitokondriális alfa ketoacid dehidrogenáz enzimkomplex egyes részeiben fellépõ pontmutáció miatt az enzimkomplex nem szerelõdik össze, ezért lebomlik. Anyagcserezavar alakul ki. Fenilketonuria: fenilalanin hidroxiláz enzim pontmutációi miatt az enzim könnyen aggregálódik, a fenilalanin felhalmozódik. Kollagénnel kapcsolatos betegségek: mutációk miatt csontfejlõdési, ízületi, bõrproblémák, stb. Cisztikus fibrózis: az esetek 70% ában a CFTR fehérjében (cystic fibrosis transmembrane conductance regulator) a Phe 508 deléciója okozza. A mutáció miatt a CFTR nem gombolyodik fel jól, ezért nem hagyja el az endoplazmás retikulumot és nem épül be a helyére, a hámsejtek membránjába, ahol kloridionokat kellene transzportálnia. Ez többek között tüdõfertõzésekhez vezet. A p53 tumorszupresszor fehérje mutációi: a p53 DNS kötõ fehérje, a károsodott sejtek programozott sejthalálának kivitelezésében vesz részt. Egyes mutációk miatt nem gombolyodik fel jól, ekkor a rák keletkezésének valószínûsége megnövekszik, az emberi rákfajták felénél ez megfigyelhetõ. Szerpinekkel kapcsolatos betegségek: a szerpinek bizonyos típusú szerin proteáz inhibitorok. Aktív formájuk metastabil, mutációk miatt rögtön a stabilabb inaktív állapot alakulhat ki. Pl. véralvadási betegségek, bizonyos tüdõbetegségek hátterében ez áll. Hályogok: károsodott krisztallin (szemlencsefehérje) aggregációja miatt Inklúziós testek renaturálása Rekombináns fehérjék sokszor inaktív, inszolubilis formában termelõdnek (idegen környezet miatt) Renaturáció: Sok milliárd dolláros biznisz Inklúziós testek 0,2 1,5 mikron átmérõjûek igen tömörek, enyhén porózusak Inklúziós testek E. coliban 13
14 nem hasonlítanak az amorf fehérjeprecipitátumokra, inkább már már kristályszerûek ritkán kristály is létrejön Szerkezetük Félregombolyodott fehérjék aggregátumai Sokszor nagymértékben natívszerû a szerkezet (doménaggregátumok?): enzimaktivitás is részben megmaradhat Képzõdésüket befolyásoló tényezõk nincs egyszerû összefüggés semmilyen tényezõvel fizikai tulajdonságok: fehérje töltésével pozitív korreláció gazdasejt élettani sajátosságai, fermentációs körülmények Kulcs: a tenyésztés hõmérséklete (alacsonyabb hõmérsékleten ált. kisebb az inklúzióstest képzõdés) ph, ozmolaritás, cukrok: direkt vagy indirekt módon befolyásolnak termelés intenzitása növeli sokkhatások: hõsokkfehérjék termelése révén befolyásolnak Az inklúziós testek kinyerése 14
15 Stratégiák inklúziós testek renaturálására A sejtek feltárása A fermentációs oldatot lehûtjük, a sejteket lecentrifugáljuk vagy leszûrjük meghatározott pufferben bármilyen módszer használható a feltárásra: az inklúziós testek igen ellenállóak nagynyomású homogenizátor: 400 bar nyomással egy kis nyíláson át lapos felületre spriccel, stb. a sejtek kijuthatnak a légtérbe, ez veszélyes lehet, ezért gyakran elõzõleg megölik õket (benzil alkohol, oktánsav, kloroform, toluén, stb.) Az inklúziós testek elválasztása Centrifugálás folyamatos üzemû, átfolyós, ipari centrifugában az átfolyási sebesség ügyes beállításával vagy ismételt reszuszpenzióval és újracentrifugálással >90% tisztaság érhetõ el Szûrés rossz hatékonyságú, a szûrõmembrán hamar tönkremegy Szelektív kémiai extrakció Ha sejttörmelék maradt a frakcióban, akkor abban membránfehérjék is vannak, ettõl meg kell szabadulni kezelés: kelátképzõ (EDTA), detergens (Triton X), 2M urea, stb. A biológiailag aktív fehérje kinyerése Az inklúziós testben a fehérjéket erõs nemkovalens erõk tartják össze Elsõ lépés ált. a szolubilizáció, ami teljes denaturálást jelent ezután visszagombolyítás Mellékreakciók: aggregáció + degradáció (proteázszennyezéstõl): empirikus receptek vannak, amelyek a felgombolyodás mechanizmusa szempontjából semmit nem mondanak Szolubilizáció Detergensek (Pl.: SDS, n lauryl sarcosine) Elõnyök: 15
16 aggregáció kevésbé fordul elõ harmadlagos szerk és aktivitás megmaradhat Hátrányok: hozzákötõdik a fehérjéhez és nehéz eltávolítani megzavarja a késõbbi ioncserélõ és hidrofób tisztítási lépéseket Kaotrop oldószerek (guanidin hidroklorid, urea) koncentráció: kb. amennyinél a fehérje legombolyodik GdmCl: drága urea: olcsó, de cianátot képezhet, ami módosítja a fehérje aminocsoportjait (az ureaoldat ioncserélésével és aminopuffer használatával kivédhetõ) Extrém ph k olcsó sok fehérjét irreverzibilisen módosíthat Szolubilizáló keverékek Renaturáció Urea + kaotrop sók/ecetsav/dimetilszulfon/lúg/2 amino 2 metil 1 propanol, stb. : sikerrel alkalmazták pár esetben Tisztítás: ált. nem érdemes refolding (visszagombolyítás) elõtt tisztítani Legfontosabb: aggregáció megakadályozása: Alacsony fehérjekoncentráció mellett egy lépésben higítás. Egyes fehérjéknél nagy higítás kell > nagy költség Higítás két szakaszban: elõbb közepes denaturálószer koncentrációra, majd teljesen. Nagyon függ a fehérje és denaturálószer koncentrációktól: sok játszadozás Aggregációcsökkentõ pufferadalékok: pl. arginin, glicin, polietilén glikol Kémiai módosítás: pl. citrakonilálás az aminocsoportokat negatív töltésûre változtatja, a fehérje polianionná válik, ez megakadályozza az aggregációt, a módosítás reverzibilis Kovalens, reverzibilis immobilizálás pl. Sepharose oszlopra puffertartalmú micellákba zárjuk a fehérjemolekulákat (egyenként), majd a micellákat szerves oldószerben diszpergáljuk A diszulfidhidak képzõdésének elõsegítése Levegõ olcsó, ezért gyakran használt ha a fehérje nem közel natív konformációjú, akkor félregombolyodott állapotok keverékét kapjuk lassú diszulfidhídban nem résztvevõ ciszteinek zavarnak Diszulfidcsere Redoxpuffer rendszer, 5:1 vagy 10:1 arányban redukált és oxidált tiollal 1mM GSH és 0,2mM GSSG nagyon jó, de drága ciszteint, DTT t, merkaptoetanolt, ciszteamint tartalmazó keverékek A tiolcsoportok védelme diszulfidhidas aggregátumok elkerülésére nagy koncentrációban oxidálószert adunk az oldathoz, minden tiolcsoport vegyes diszulfidot képez így tisztítjuk, majd a végsõ fázisban tesszük redoxpufferbe Ipari méretekben történõ renaturáció A laboratóriumi eljárásból indulunk ki Elsõsorban költségcsökkentés a cél: pufferek, reagensek, stb. lecserélése olcsóbbra Eljárás egyszerûsítése, lépések sorrendjének megváltoztatása (kevesebb puffercsere, stb.) 16
17 Fehérje nagyüzemi kinyerése E. coli inklúziós testbõl Az inklúziós test tulajdonságai igen kedvezõek a tisztítás szempontjából (ellenálló, homogén, nagy sûrûségû, stb.) De: Problémát okoz (az inklúziós testeket használó eljárás nem mûködik): Szekrécióval együtt poszttranszlációs módosítást igénylõ fehérjék (pl. eritropoetin glikozilálása) Nagy molekulatömegû (>30 kda), többdoménes, 4 diszulfidhídnál többet tartalmazó fehérjék Nagy molekulatömegû, heterooligomer fehérjék, pl. antitestek 17
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjék szerkezetének kialakulása II. Semmelweis Egyetem. Osváth Szabolcs
 Fehérjék szerkezetének kialakulása II Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Egy kis fehérje gombolyodása több párhuzamos úton hélix kialakulás és kollapszus több párhuzamos úton
Fehérjék szerkezetének kialakulása II Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Egy kis fehérje gombolyodása több párhuzamos úton hélix kialakulás és kollapszus több párhuzamos úton
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjék szerkezetének kialakulása II
 Egy kis fehérje gombolyodása több párhuzamos úton Fehérjék szerkezetének kialakulása II Osváth Szabolcs Semmelweis Egyetem hélix kialakulás és kollapszus több párhuzamos úton további kollapszus és hélix
Egy kis fehérje gombolyodása több párhuzamos úton Fehérjék szerkezetének kialakulása II Osváth Szabolcs Semmelweis Egyetem hélix kialakulás és kollapszus több párhuzamos úton további kollapszus és hélix
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék
 A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
A citoszol szolubilis fehérjéi. A citoplazma matrix (citoszol) Caspase /Kaszpáz/ 1. Enzimek. - Organellumok nélküli citoplazma
 A citoplazma matrix (citoszol) A citoszol szolubilis fehérjéi 1. Enzimek - Organellumok nélküli citoplazma -A sejt fejlődéstani szempontból legősibb része (a sejthártyával együtt) Glikolízis teljes enzimrendszere
A citoplazma matrix (citoszol) A citoszol szolubilis fehérjéi 1. Enzimek - Organellumok nélküli citoplazma -A sejt fejlődéstani szempontból legősibb része (a sejthártyával együtt) Glikolízis teljes enzimrendszere
6. Zárványtestek feldolgozása
 6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
1b. Fehérje transzport
 1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
1b. Fehérje transzport Fehérje transzport CITOSZÓL Nem-szekretoros útvonal sejtmag mitokondrium plasztid peroxiszóma endoplazmás retikulum Szekretoros útvonal lizoszóma endoszóma Golgi sejtfelszín szekretoros
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Biofizika I 2013-2014 2014.12.02.
 ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
ÁTTEKINTÉS AZ IZOM TÍPUSAI: SZERKEZET és FUNKCIÓ A HARÁNTCSÍKOLT IZOM SZERKEZETE MŰKÖDÉSÉNEK MOLEKULÁRIS MECHANIZMUSA IZOM MECHANIKA Biofizika I. -2014. 12. 02. 03. Dr. Bugyi Beáta PTE ÁOK Biofizikai Intézet
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Citoszkeleton. Sejtek rugalmassága. Polimer mechanika: Hooke-rugalmasság. A citoszkeleton filamentumai. Fogászati anyagtan fizikai alapjai 12.
 Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
Fogászati anyagtan fizikai alapjai 12. Sejtek rugalmassága Citoszkeleton Eukariota sejtek dinamikus vázrendszere Három fő filamentum-osztály: A. Vékony (aktin) B. Intermedier C. Mikrotubulus Polimerizáció:
6. szeminárium - Fehérjeszerkezethez kötött patológiás állapotok kémiája
 6. szeminárium Fehérjeszerkezethez kötött patológiás állapotok kémiája A fehérjék háromdimenziós, specifikus funkcióra alkalmas szerkezetét natív konformációnak nevezzük, melyet egy dinamikus feltekeredési
6. szeminárium Fehérjeszerkezethez kötött patológiás állapotok kémiája A fehérjék háromdimenziós, specifikus funkcióra alkalmas szerkezetét natív konformációnak nevezzük, melyet egy dinamikus feltekeredési
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK
 POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
TRANSZPORTFOLYAMATOK 1b. Fehérjék. 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS
 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
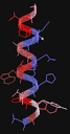 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
"Olvadt gombócok" és más kompakt denaturált állapotok
 "Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
"Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Prolinizomerizáció. A diszulfidhidak képzõdése.
 1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása
 A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu reakció t 1/2 25 ºC-on t 1/2 100 ºC-on DNS hidrolízis Biopolimerek
A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu reakció t 1/2 25 ºC-on t 1/2 100 ºC-on DNS hidrolízis Biopolimerek
A fehérjéket felépítő húsz standard aminosav
 Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Biopolimerek reakció t 1/2 25 ºC-on t 1/2 100 ºC-on egy polimerben lévő kötések tipikus száma hányfajta
Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Biopolimerek reakció t 1/2 25 ºC-on t 1/2 100 ºC-on egy polimerben lévő kötések tipikus száma hányfajta
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Fehérjék felépítése és struktúrája. Aminosav oldalláncok. A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel
 Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Folyadékkristályok; biológiai és mesterséges membránok
 Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
Felgombolyodási kinetikák, mechanizmusok
 Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
K68464 OTKA pályázat szakmai zárójelentés
 K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
VEBI BIOMÉRÖKI MŰVELETEK KÖVETELMÉNYEK. Pécs Miklós: Vebi Biomérnöki műveletek. 1. előadás: Bevezetés és enzimkinetika
 VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
VEBI BIOMÉRÖKI MŰVELETEK
 VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése
 1. 2. Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése A több doménbõl álló fehérjék felgombolyodása 1. Domének 2. Izolált domének felgombolyodása 3. A doménpárosodás mint sebességmeghatározó
1. 2. Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése A több doménbõl álló fehérjék felgombolyodása 1. Domének 2. Izolált domének felgombolyodása 3. A doménpárosodás mint sebességmeghatározó
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben
 BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
BIOMECHANIKA 3 Erőhatások eredete és következményei biológiai rendszerekben A MOZGÁS MOLEKULÁRIS MECHANIZMUSAI SZERVEZET SZINTŰ MOZGÁS AZ IZOMMŰKÖDÉS MOLEKULÁRIS MECHANIZMUSAI DR. BUGYI BEÁTA- BIOFIZIKA
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
Telomerek a lineáris kromoszómák végei
 Telomer Telomeráz Telomerek a lineáris kromoszómák végei Repetitív DNS szekvencia, TTAGGG gerincesekben Speciális telomerkötő fehérjék Telomer méret Telomer-3D lineáris? A telomerek szerkezete: t &D hurok
Telomer Telomeráz Telomerek a lineáris kromoszómák végei Repetitív DNS szekvencia, TTAGGG gerincesekben Speciális telomerkötő fehérjék Telomer méret Telomer-3D lineáris? A telomerek szerkezete: t &D hurok
A citoszkeletális rendszer
 A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
A citoszkeleton Eukarióta sejtváz
 A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
Egy idegsejt működése. a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
2. AKTIN-KÖTŐ FEHÉRJÉK
 A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
A CITOSZKELETÁLIS RENDSZER 2011. 02. 15. Bugyi Beáta PTE ÁOK, Biofizikai Intézet 2. AKTIN-KÖTŐ FEHÉRJÉK Citoszkeletális aktin HEp-2 sejtekben - rodamin-falloidin jelölés forrás: Nyitrai Miklós, Grama László,
11/15/10! A CITOSZKELETÁLIS RENDSZER! Polimerizáció! Polimerizációs egyensúly! Erő iránya szerint:! 1. valódi egyensúly (aktin)" Polimer mechanika!
 11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál. Nyugalmi potenciál. 3 tényező határozza meg:
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
15. Fehérjeszintézis: transzláció. Fehérje lebontás (proteolízis)
 15. Fehérjeszintézis: transzláció Fehérje lebontás (proteolízis) 1 Transzláció fordítás A C G T/U A C D E F G H I K L M N P Q R S T V W Y 4 betűs írás (nukleinsavak) 20 betűs írás (fehérjék) 2 Amit már
15. Fehérjeszintézis: transzláció Fehérje lebontás (proteolízis) 1 Transzláció fordítás A C G T/U A C D E F G H I K L M N P Q R S T V W Y 4 betűs írás (nukleinsavak) 20 betűs írás (fehérjék) 2 Amit már
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Az agy betegségeinek molekuláris biológiája. 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5.
 Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
Az agy betegségeinek molekuláris biológiája 1. Prion betegség 2. Trinukleotid ripít betegségek 3. ALS 4. Parkinson kór 5. Alzheimer kór 28 Prion betegség A prion betegség fertőző formáját nem egy genetikai
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
IPARI ENZIMEK 2. Proteázok. Alkalikus proteázok. Pécs Miklós: Biotermék technológia 1. 6. fejezet: Ipari enzimek 2.
 IPARI ENZIMEK 2 Proteázok A proteázok az ipari enzimek egyik legfontosabb csoportja (6200 t tiszta E/év) Peptid kötéseket bont (létrehoz) (hidrolízis, szintézis) Fehérje lebontás: élelmiszer, tejalvadás,
IPARI ENZIMEK 2 Proteázok A proteázok az ipari enzimek egyik legfontosabb csoportja (6200 t tiszta E/év) Peptid kötéseket bont (létrehoz) (hidrolízis, szintézis) Fehérje lebontás: élelmiszer, tejalvadás,
AMINOSAVAK, FEHÉRJÉK
 AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
Biotechnológiai gyógyszergyártás
 Biotechnológiai gyógyszergyártás Dr. Greiner István 2013. november 6. Biotechnológiai gyógyszergyártás Biotechnológiai gyógyszerek Előállításuk és analitikájuk Richter és a biotechnológia Debrecen A jövő
Biotechnológiai gyógyszergyártás Dr. Greiner István 2013. november 6. Biotechnológiai gyógyszergyártás Biotechnológiai gyógyszerek Előállításuk és analitikájuk Richter és a biotechnológia Debrecen A jövő
1. Az élő szervezetek felépítése és az életfolyamatok 17
 Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
A felgombolyodás problémája
 1. A probléma 2. A fehérjék stabil konformációs állapotai 3. A felgombolyodás általános tulajdonságai 4. A felgombolyodás modelljei 5. A felgombolyodás nyomon követésének technikái 6. A felgombolyodás
1. A probléma 2. A fehérjék stabil konformációs állapotai 3. A felgombolyodás általános tulajdonságai 4. A felgombolyodás modelljei 5. A felgombolyodás nyomon követésének technikái 6. A felgombolyodás
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
(11) Lajstromszám: E 007 017 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000007017T2! (19) HU (11) Lajstromszám: E 007 017 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 7232 (22) A bejelentés napja:
!HU000007017T2! (19) HU (11) Lajstromszám: E 007 017 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 07 7232 (22) A bejelentés napja:
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Dér András MTA SZBK Biofizikai Intézet
 Hogyan befolyásolja a határfelületi vízréteg szerkezete a fehérjeműködést? Dér András MTA SZBK Biofizikai Intézet Felületi feszültség Geometriai optimalizáció Biológiai érhálózat γ dw da Eötvös mérései
Hogyan befolyásolja a határfelületi vízréteg szerkezete a fehérjeműködést? Dér András MTA SZBK Biofizikai Intézet Felületi feszültség Geometriai optimalizáció Biológiai érhálózat γ dw da Eötvös mérései
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel
 Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Jedlovszky Pál Eszterházy Károly Egyetem, Kémiai és Élelmiszerkémiai Tanszék Tanszék, 3300 Eger, Leányka utca 6
 Jedlovszky Pál Eszterházy Károly Egyetem, Kémiai és Élelmiszerkémiai Tanszék Tanszék, 33 Eger, Leányka utca 6 - Fluid határfelületek modellezésének alapkérdései -Ízelítő a csoportunkban több évtizede folyó
Jedlovszky Pál Eszterházy Károly Egyetem, Kémiai és Élelmiszerkémiai Tanszék Tanszék, 33 Eger, Leányka utca 6 - Fluid határfelületek modellezésének alapkérdései -Ízelítő a csoportunkban több évtizede folyó
A rácsmodell. Szabadenergia felületek.
 1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
