Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése
|
|
|
- Karola Csonkané
- 8 évvel ezelőtt
- Látták:
Átírás
1 1. 2. Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése A több doménbõl álló fehérjék felgombolyodása 1. Domének 2. Izolált domének felgombolyodása 3. A doménpárosodás mint sebességmeghatározó lépés 4. Versengés a felgombolyodás és az aggregáció között A több alegységbõl álló fehérjék összeszerelõdése 1. Többalegységes fehérjék 2. A több alegység szerepe a funkció szempontjából 3. Az alegységek közötti kölcsönhatások 4. Az alegység asszociáció tanulmányozásának módszerei 5. Példák többalegységes fehérjék összeszerelõdésére 6. Versengõ mellékreakciók Domének A több doménbõl álló fehérjék felgombolyodása Többféle definíció: Stabil egység (limitált proteolízissel vagy génsebészettel elkülöníthetõ) Termodinamikai egység (kooperatívan gombolyodik le és fel) Felgombolyodási egység (függetlenül gombolyodik) Szerkezeti egység (látszik a röntgenszerkezetben) Genetikai egység (szekvenciaösszehasonlítások alapján jósolható) Evolúciós egység (exonoknak felel meg) Funkcionális egység (meghatározott részfunkciója van, pl. NAD kötés) Izolált domének felgombolyodása A polipeptidláncot a doménhatároknál szétvágva a domének izolálhatóak, ill. az egyes domének génsebészeti úton külön külön elõállíthatóak. Számos izolált doménrõl mutatták ki, hogy önállóan, reverzibilisen fel /legombolyodik (triptofán szintetáz, béta laktamáz, aszpartokináz homoszerin dehidrogenáz, plazminogén, PGK, stb.) 1
2 A domének termodinamikai stabilitása Speciális esetekben igazolták, hogy a domének a fehérje többi részével együtt és anélkül is nagyjából azonos stabilitásúak (ez nem feltétlenül általánosítható) Plazminogén és különféle fragmentumainak kalorimetriás görbéi A doménpárosodás mint sebességmeghatározó lépés Számos jel szerint a többdoménes, egyláncú fehérjék felgombolyodásában a leglassúbb lépés a már felgombolyodott domének párosodása (asszociációja). Ennek 3 bizonyítéka: 1. Az enzimaktivitás csak a felgombolyodás legkésõbbi szakaszában jelenik meg. Az aktív hely általában a domének érintkezésénél van, az egyes domének hordozzák az egyes szubsztrátokat. 2. A felgombolyodás sebessége fordítottan arányos az oldat viszkozitásával 2
3 (A: Oktopin dehidrogenáz, B: AK HDH felgombolyodási sebességének reciproka a viszkozitás függvényében. Viszkozitásnövelõk: glicerin, glükóz, szukróz A viszkozitástól való függés nagyméretû egység elmozdulását feltételezi 3. Az egyik doménben létrehozott, felgombolyodást lassító mutáció hatása kompenzálható a másik doménben létrehozott, önmagában szintén lassító mutációval Létezik tehát egy állapot, melyben a domének már fel vannak gombolyodva, de még nem asszociálódtak. Ennek neve: FUD (Folded but Unpaired Domains): felgombolyodott, de még nem párosodott domének Általános reakcióséma: Legombolyodott áll. (domének gyors felgombolyodása) > FUD (domének lassú párosodása) > natív 3
4 Doménasszociációval járó folyamatok: 1': izolált domének felgombolyodása; 2': izolált domének asszociációja; 1: domének önálló felgombolyodása, FUD kialakulása; 2: a domének asszociációja, létrejön a natív szerkezet; 3: párosodás másik molekula doménjével > aggregáció Versengés a felgombolyodás és az aggregáció között A FUD intermedierben a domének kontaktfelszíne szabad > más láncok komplementer felszíneihez is kapcsolódhatnak > aggregáció! Erõsen koncentrációfüggõ: Laktát dehidrogenáz aggregációja (háromszög) és felgombolyodása (kör) a fehérjekoncentráció függvényében Az aggregációban valóban a FUD intermedier vesz részt. Ennek bizonyítékai: 1. Az aggregáció akkor a legerõteljesebb, ha részlegesen felgombolyodott molekulák nagy számban vannak jelen 2. Az aggregáció specifikus. Más fehérjék jelenléte nem befolyásolja (még hasonló fehérjéké sem) 4
5 3. Az aggregáció sokkal kisebb, ha a domének között nincs kovalens kapcsolat (izolált domének) A több alegységbõl álló fehérjék összeszerelõdése Kérdések: Mennyiben befolyásolja az alegységek szerkezetét, stabilitását a többi alegység jelenléte? A felgombolyodási folyamat melyik fázisában történik az alegységek asszociációja? Teljesen kész, merev szerkezetû alegységek asszociálódnak, vagy inkább két olajcsepp egybeolvadásához hasonló az asszociáció? Utóbbi esetben mi biztosítja a specificitást? Egy "olvadt gombóc" jellegû intermedier mutathat e specificitást? Többalegységes fehérjék M r = molekulatömeg alatt többnyire monomer, M r = fölött többnyire oligomer fehérjék (Kivételek: pl. izoleucin trns szintetáz (M r = ) monomer; inzulin (M r =5700) és MetJ represszor (M r =12 000) dimerek) Néhány negyedleges szerkezet: Negyedleges szerkezet Példa Homooligomerek a 2 a 3 a 4 a 6 a 8 a 12 a 14 a 24 Kreatin kináz Kloramfenikol acetiltranszferáz Laktát dehidrogenáz Glutamát dehidrogenáz Izocitrát dehidrogenáz Glutamin szintetáz GroEL chaperonin Apoferritin Heterooligomerek ab ab 5 a 2 b 2 a 6 b 6 a 8 b 8 abc a 4 b 4 c 4 d 4 a 2 bb'c a 3 b 3 cde Laktóz szintáz Koleratoxin Triptofán szintáz Aszpartát karbamoiltranszferáz Rubisco Troponin Foszforiláz kináz RNS polimeráz F1 ATPáz Általában szimmetrikus szerkezetek: 5
6 izopropil malát dehidrogenáz (dimer) kloramfenikol acetiltranszferáz (trimer) szérum amiloid P komponens C reaktív protein (hexamer) LHC komplex (light harvesting complex) (nonamer) 6
7 TRAP (Trp attenuation protein) (undekamer, 11 mer) A negyedleges szerkezet és az élettani funkció összefüggése: glutamin szintetáz (dodekamer, 12 mer) Szekretált fehérjék (pl. tripszin, lizozim): ált. kicsi, egydoménes monomerek, diszulfidhidakkal > különféle környezetekben ellenálló Vérplazma fehérjéi: nagy monomerek (pl. szérumalbumin 65 kd) vagy ezek oligomerjei (alfa 2 makroglobulin, 4 alegység, 4x180 kd) > nem szûrõdnek át az erek falán vagy a vesében Intracelluláris fehérjék: Ált. több alegység A több alegység szerepe a funkció szempontjából 1. Az aktivitás szabályozása 2. Újfajta aktivitások létrehozása 3. Nagy szerkezetek képzõdése 4. A felgombolyodott láncok stabilizálása 5. Egyéb Az aktivitás szabályozása Az alegységek között pozitív vagy negatív kooperativitás lehet Hemoglobin (oxigénkötése) foszfofruktokináz aszpartát karbamoiltranszferáz szigmoid alakú függés a szubsztrátkoncentrációtól glutamát dehidrogenáz: negatív kooperáció a NAD kötõ helyek között Különbözõ ligandumok közötti kölcsönhatás > szabályozó funkciók (regulátor molekulák) A konformációváltozás ált. kimutatható Újfajta aktivitások létrehozása Számos enzim aktív helye több alegység oldalláncaiból tevõdik össze (pl. glutamin szintetáz, aszpartát aminotranszferáz, triózfoszfát izomeráz, citrát szintáz, gliceraldehid 3 foszfát dehidrogenáz) 7
8 Citrát szintáz aktív helye. A * gal jelölt oldallánc a másik alegységbõl van Az alegység asszociáció változtathat is a specificitáson: E. coli triptofán szintáz: triptofán bioszintézisének utolsó lépése: indol glicerin foszfát + szerin < > triptofán + gliceraldehid 3 foszfát + H 2 O Szerkezete: a 2 b 2. 1M KSCN jelenlétében disszociál: Az a és a b 2 egységek két félreakciót katalizálnak: a 2 b 2 > 2a + b 2 indol glicerin foszfát < > indol + gliceraldehid 3 foszfát indol + szerin < > triptofán + H 2 O Az a 2 b 2 teljes enzim hatékonyabban katalizál és elnyomja a káros mellékreakciókat. Az indol az a alegység aktív helyérõl "channeling" révén, egy "alagúton" jut el a b alegység aktív helyére Laktóz szintáz: A és B alegység (a B az alfa laktalbumin): B nélkül az A N acetil glükózaminból N acetil laktózamint készít B vel glükózból laktózt szabályozás: szülés után megnövekszik a B alegység szintje, így a tejcukor termelése Nagy szerkezetek képzõdése GroEL chaperonin: gyûrû 14 alegységbõl, közepén lyukkal, mely befogad egy rosszul felgombolyodott fehérjét aktin > aktinszál alfa és béta tubulin > mikrotubulus flagellin > bakteriális ostor A felgombolyodott láncok stabilizálása Az asszociáció növeli az alegységek stabilitását (hidrofób foltokat, laza hurkokat eltüntet) Nehéz mérni a stabilizáció mértékét (disszociáló körülmények az alegységet is destabilizálják) Mérés: Mátrixhoz kötött fehérjérõl a szabad alegységet ledisszociáltatjuk, a megmaradót visszagombolyítjuk, stabilitását mérjük Egyéb szerepek A sejt ozmotikus nyomásának csökkentése A hibás felgombolyodás esélye kisebb, ha több, önálló alegységbõl épül fel a fehérje, mint ha egyetlen nagy láncból 8
9 Az alegységek közötti kölcsönhatások Ugyanazok, mint az alegységen belüliek (hidrofób, H kötés, elektrosztatikus, Van der Waals) Asszociációs állandó (K): M 1 Standard szabadentalpia (deltag o ): kj/mol (mérésbõl) A mért deltag o ben benne van a transzlációs és rotációs szabadsági fokok elvesztésébõl származó járulék is. Ennek értéke vitatott. Kétféle becslés: Gázok statisztikus mechanikája alapján a "Sackur Tetrode" egyenletbõl > nagy entrópiaértékek (100 cal/m/k), nehéz magyarázni Keverési entrópia (a disszociálódó alegységek elkeverednek az oldatban): S mix =k B ln x ahol x a móltört, 1M referenciakoncentrációra (a víz koncentrációja 55M) számítva kb. 10 cal/m/k érték adódik. Mérés: nehéz, értékek inkább a 10 cal/m/k hoz közeliek. Mégis, elméleti alapon a Sackur Tetrode módszert tartják többen helyesnek. Becslés: az asszociációkor eltemetett hidrofób felszínbõl: 100 négyzetangströmönként 10,5 kj/mol szabadentalpia (konyhaszabály) Az alegység asszociáció tanulmányozásának módszerei Két megközelítés: Olyan körülményeket teremtünk, ahol felgombolyodott, de disszociált monomerek vannak. Ezután visszaállítva az eredeti paramétereket az asszociáció elkülönítve vizsgálható. (Ez sokszor nem járható út.) Disszociált és legombolyodott monomerekbõl indulunk ki, együttesen vizsgáljuk a monomerek felgombolyodását és asszociációját. Disszociált natív (vagy kvázinatív) alegységek nyerése Higítás Akkor használható, ha nem túl erõs az alegységek közötti kapcsolat (pl. piruvát karboxiláz, foszfofruktokináz) Hidegdisszociáció Hidrofób kölcsönhatás meggyengülése miatt. Pl. élesztõ gliceraldehid 3 foszfát dehidrogenáz (tetramer) 0 Celsius fokon kvázinatív monomerekre esik szét (NAD kötõ képesség megmarad) Kémiai módosítás Pl. lizinek töltésének megfordítása dibázikus sav anhidridjével való módosítással (reverzibilis!). Pl. élesztõ zsírsav szintetáznál (a 6 b 6 ) bevált. Ligandumindukált disszociáció Bizonyos speciális esetekben. Pl. glutamát dehidrogenáz (hexamer) GTP hatására szétesik; camp függõ protein kinázról camp hatására a katalitikus egység leválik Enyhén denaturáló körülmények (esetleg stabilizálószer egyidejû alkalmazásával) Triptofán szintáz (a 2 b 2 ) KSCN hatására Laktát dehidrogenáz (tetramer) 1M glicin/h 3 PO 4 +EDTA, ph 2,3, plusz 1M Na 2 SO 4 stabilizáló só hatására Laktát dehidrogenáz 2M ureában v. 0,8 1,2M GdmCl ben dimerekre esik szét Glutamát dehidrogenáz (hexamer): 1 1,5M GdmCl ben két natívszerû trimerre esik szét, 3M nél ezek is szétesnek és legombolyodnak 9
10 (kör: M r fényszórással mérve; háromszög, négyzet: másodlagos és harmadlagos szerkezet CD vel, ill. fluoreszcenciával mérve) Nagy nyomás >1 kbar nyomás hatására az oligomerek gyakran szétesnek (pl. laktát dehidrogenáz), mert ezzel csökkenhet a térfogat (oldószer hozzáfér az eddig eltemetett részekhez) Az asszociáció nyomonkövetése: Biofizikai módszerek fehérje fehérje kölcsönhatások mérésére Surface Plasmon Resonance (felületi plazmonrezonancia) A kötõ alegységeket egy optikai chip felületén immobilizáljuk. A fölötte lévõ pufferbe bevisszük a kötõdõ molekulát Kötéskor a tömegváltozás optikai változást okoz, ezt méri a mûszer BIAcore: áramló puffer, Affinity Sensors: kevert puffer Alkalmas: kötõdik/nem kötõdik eldöntésére, kötési affinitás mérésére Izotermikus titrációs kalorimetria A kötõ alegységek oldata van a mérõtérben Ehhez injektáljuk kis adagokban a másik alegység oldatát A mûszer a felszabaduló hõt méri, a hõmérsékletet állandó értéken tartva 10
11 Számítható: kötési entalpia, asszociációs állandó, entrópia Homooligomernél: üres pufferbe tömény fehérjeoldatot injektálgatunk, higítási hõket mérve Fluoreszcencia Ált. fluoreszcenciás rezonancia energiatranszfer (FRET) segítségével mérhetõ a két alegység távolsága: Ha egy fluorofor (donor) emissziós spektruma átfed egy közeli fluorofor (akceptor) abszorpciós spektrumával, köztük rezonanciás energiatranszfer lép fel, melynek hatékonysága: K a dipól dipól orientációs tényezõ Q a donor kvantumhatásfoka transzfer hiányában J a spektrumok átfedési integrálja n az oldószer törésmutatója E = R 0 6 /(R 6 + R 0 6 ), ahol R 0 = 979(K 2 QJn 4 ) 1/6, ahol Hátrány: ált. fluoroforokat kell bevinni, ezek nagyméretû csoportok, amelyek az asszociációt is befolyásolhatják! Tömegspektroszkópia Fényszórás Az átlagos részecskeméretet méri Disszociációnál jól használható, asszociációnál az aggregáció miatt kevésbé A turbiditás spektroszkópiával is mérhetõ (megfelelõ korrekciók alkalmazásával) Gélszûrés HPLC vel (A HPLC elég gyors, 1 órán belül elvégezhetõ) Az összeszerelõdés idõbeli nyomon követésének módszerei Keresztkötés és SDS PAGE (nagyágyú!) A visszagombolyítás folyamatában bizonyos idõpontokban mintát veszünk, azt gyorsan ható keresztkötõ reagenssel elkeverjük, ez az oligomereket rögzíti SDS PAGE (poliakrilamid gélelektroforézis SDS detergensben) elemzés szétválasztja a különbözõ tömegû molekulákat Legjobb keresztkötõ reagens: Lizineket köti össze glutáraldehid: OHC CH 2 CH 2 CH 2 CHO Mindig ki kell kísérletezni, mi a legjobb glutáraldehid koncentráció Hátrány: Néha nincs elég lizin megfelelõ helyen Eredmények élesztõ foszfoglicerát mutáznál: 11
12 Csak dimer intermedier figyelhetõ meg. Hibridizáció izoenzimmel vagy módosított alegységekkel (kör: monomer, háromszög: dimer, négyzet: tetramer) A visszagombolyítás folyamatában adott idõpontban nagy mennyiségben izoenzim alegységeket vagy kémiailag módosított alegységeket adunk az oldathoz Az idegen alegységek lekötik a még szabad molekulákat Natív gélelektroforézissel elemezzük az eloszlást Feltétel: az idegen alegység elektroforetikusan különbözzön a vizsgálttól Problémák: az idegen alegység lassú felgombolyodása, disszociáció, stb. alkalmazták pl. kreatin kináznál, aszpartát karbamoiltranszferáznál Reaktiváció mérése Gyors aktivitásmérések alapján Fehérjekoncentráció függvényében Malát dehidrogenáznál: 12
13 Az adatok elemzése (az egyes görbék más más fehérjekoncentráció mellett készültek, a fehérjekoncentráció alulról fölfelé növekszik; a grafikonon 2 óránál idõskála váltás) Elvégezzük: Keresztkötés és SDS PAGE, valamint reaktivációs mérések, sokféle fehérjekoncentráció mellett (kiegészítve spektroszkópiai mérésekkel) Az adatok alapján felállítható egy reakcióséma, a sebességi állandók kiszámíthatóak. A reakcióséma unimolekuláris (izomerizációs) és bimolekuláris (asszociációs) lépésekbõl áll. Pl. tetramernél: (M: monomer, D: dimer, T: tetramer) 4M u > 4M > 2D' > 2D > T' > T Rendszerint a reakcióegyenletek analitikus vagy numerikus megoldásával ellenõrizzük a modell és a paraméterek helyességét, ill. számítjuk ki a sebességi állandókat. Példák többalegységes fehérjék összeszerelõdésére UDP glükóz dehidrogenáz Hexamer. [Keresztkötésbõl hexamerek (hatszög), tetramerek (négyzet), trimerek (háromszög), dimerek (félkörök), monomerek (kör) mennyisége. Reaktiváció (teli hatszög).] Trimereket és pentamereket nem lehet megfigyelni Az aktivitás visszanyerése a hexamerképzõdéssel párhuzamos Reakcióséma: 6M u > 6M > 3D > Hexamer Az elsõ két lépés sebességi állandói: k 1 =4,5x10 4 s 1 (elsõrendû) és k 2 =1,6x10 4 M 1 s 1 (másodrendû) Aszpartokináz homoszerin dehidrogenáz (AK HBH) (E. coli) Tetramer Bifunkciós enzim, négy bifunkciós alegység Treonin bioszintézisének két korai lépését katalizálja Treonin allosztérikusan gátolja Mérések: 13
14 [háromszögek: CD, fluoreszcencia; teli kör: kináz aktivitás, X: dehidrogenáz aktivitás; üres kör: a kináz aktivitás allosztérikus gátlása treoninnal] Reakcióséma: 4M u >4M' >4M >2D' >2D >T 4M u 4M' 4M 2D' 2D T Kináz aktivitás gátolhatósága treoninnal + Dehidrogenáz aktivitás gátolhatósága treoninnal + + Natív fluoreszcencia Natív távoli UV CD Versengõ mellékreakciók Alacsony fehérjekoncentrációnál: az asszociációs lépések lelassulnak a nemasszociált alegységek hosszú ideig fennmaradnak csökkent stabilitásuk miatt veszélyeknek vannak kitéve: degradáció proteázszennyezés által, kémiai módosulás, edény falára tapadás, stb. Magas fehérjekoncentrációnál: Aggregáció következhet be: valamelyik korai intermedier hidrofób felszínei révén (általában nemspecifikus) asszociáció Tehát a közepes koncentrációk az ideálisak (alkalmazások: ld. következõ elõadás) Laktát dehidrogenáz reaktiválhatósága a fehérjekoncentráció függvényében 14
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Felgombolyodási kinetikák, mechanizmusok
 Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék
 A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Biofizika szeminárium PTE ÁOK Biofizikai Intézet Huber Tamás 2014. 02. 11-13. A gerjesztett állapotú elektron lecsengési lehetőségei Gerjesztés Fluoreszcencia
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek
 Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
Fluoreszcencia módszerek (Kioltás, Anizotrópia, FRET) Modern Biofizikai Kutatási Módszerek 2012. 11. 08. Fotonok és molekulák ütközése Fény (foton) ütközése a molekulákkal fényszóródás abszorpció E=hν
A fehérjék hierarchikus szerkezete
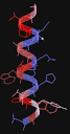 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
"Olvadt gombócok" és más kompakt denaturált állapotok
 "Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
"Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Enzimaktivitás szabályozása
 2017. 03. 12. Dr. Tretter László, Dr. olev rasziir Enziaktivitás szabályozása 2017. árcius 13/16. Mit kell tudni az előadás után: 1. Reverzibilis inhibitorok kinetikai jellezői és funkcionális orvosbiológiai
2017. 03. 12. Dr. Tretter László, Dr. olev rasziir Enziaktivitás szabályozása 2017. árcius 13/16. Mit kell tudni az előadás után: 1. Reverzibilis inhibitorok kinetikai jellezői és funkcionális orvosbiológiai
Biomolekuláris kölcsönhatások vizsgálata felületi plazmonrezonancia elvén működő Biacore keszülékkel
 Biomolekuláris kölcsönhatások vizsgálata felületi plazmonrezonancia elvén működő Biacore keszülékkel Biomolekuláris interakciók Fehérje-fehérje Fehérje-ligand Fehérje-DNS/RNS fehérje/ligand-lipid Alegység-kölcsönhatások,
Biomolekuláris kölcsönhatások vizsgálata felületi plazmonrezonancia elvén működő Biacore keszülékkel Biomolekuláris interakciók Fehérje-fehérje Fehérje-ligand Fehérje-DNS/RNS fehérje/ligand-lipid Alegység-kölcsönhatások,
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
Zsírsav szintézis. Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P. 2 i
 Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET)
 Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
Fluoreszcencia 2. (Kioltás, Anizotrópia, FRET) Gerjesztés A gerjesztett állapotú elektron lecsengési lehetőségei Fluoreszcencia 10-9 s k f Foszforeszcencia 10-3 s k ph 10-15 s Fizika-Biofizika 2. Huber
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA
 A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
A CITOSZKELETÁLIS RENDSZER FUTÓ KINGA 2013.10.09. CITOSZKELETON - DEFINÍCIÓ Fehérjékből felépülő, a sejt vázát alkotó intracelluláris rendszer. Eukarióta és prokarióta sejtekben egyaránt megtalálható.
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Általános kémia képletgyűjtemény. Atomszerkezet Tömegszám (A) A = Z + N Rendszám (Z) Neutronok száma (N) Mólok száma (n)
 Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
A módszerek jelentősége. Gyors-kinetika módszerek. A módszerek közös tulajdonsága. Milyen módszerekről tanulunk?
 Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
ALLOSZTÉRIKUSAN SZABÁLYOZÓ METABOLITOK HATÁSA A PIRUVÁT-KINÁZ L és M IZOENZIMRE
 ALLOSZTÉRIKUSAN SZABÁLYOZÓ METABOLITOK HATÁSA A PIRUVÁT-KINÁZ L és M IZOENZIMRE A glukóz piruváttá (illetve laktáttá) történő átalakulása során (glikolízis), illetve a glukóz reszintézisben (glukoneogenezis)
ALLOSZTÉRIKUSAN SZABÁLYOZÓ METABOLITOK HATÁSA A PIRUVÁT-KINÁZ L és M IZOENZIMRE A glukóz piruváttá (illetve laktáttá) történő átalakulása során (glikolízis), illetve a glukóz reszintézisben (glukoneogenezis)
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
A metabolizmus energetikája
 A metabolizmus energetikája Dr. Bódis Emőke 2015. október 7. JJ9 Miért tanulunk bonyolult termodinamikát? Miért tanulunk bonyolult termodinamikát? Mert a biokémiai rendszerek anyag- és energiaáramlásának
A metabolizmus energetikája Dr. Bódis Emőke 2015. október 7. JJ9 Miért tanulunk bonyolult termodinamikát? Miért tanulunk bonyolult termodinamikát? Mert a biokémiai rendszerek anyag- és energiaáramlásának
Abszorpciós fotometria
 abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK)
 BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK) 1. Keresse meg a baloldali oszlopban található fehérje szerkezeti szintekre jellemző a jobboldali oszlopban lévő
BIOKÉMIA GYAKORLÓ TESZT 1. DEMO (FEHÉRJÉK, ENZIMEK, TERMODINAMIKA, SZÉNHIDRÁTOK, LIPIDEK) 1. Keresse meg a baloldali oszlopban található fehérje szerkezeti szintekre jellemző a jobboldali oszlopban lévő
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
A felgombolyodás problémája
 1. A probléma 2. A fehérjék stabil konformációs állapotai 3. A felgombolyodás általános tulajdonságai 4. A felgombolyodás modelljei 5. A felgombolyodás nyomon követésének technikái 6. A felgombolyodás
1. A probléma 2. A fehérjék stabil konformációs állapotai 3. A felgombolyodás általános tulajdonságai 4. A felgombolyodás modelljei 5. A felgombolyodás nyomon követésének technikái 6. A felgombolyodás
Fehérjék. SZTE ÁOK Biokémiai Intézet
 Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
ENZIMSZINTŰ SZABÁLYOZÁS
 ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
A citoszkeletális rendszer
 A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A citoszkeletális rendszer Az eukarióta sejtek dinamikus fehérje-vázrendszere, amely specifikus fehérjepolimer filamentumokból épül fel. Mikrofilamentumok Mikrotubulusok Intermedier filamentumok Aktin
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Fotoszintézis. fotoszintetikus pigmentek Fényszakasz - gránum/sztrómalamella. Sötétszakasz - sztróma
 Fotoszintézis fotoszintetikus pigmentek Fényszakasz - gránum/sztrómalamella Sötétszakasz - sztróma A növényeket érı hatások a pigmentösszetétel változását okozhatják I. Mintavétel (inhomogén minta) II.
Fotoszintézis fotoszintetikus pigmentek Fényszakasz - gránum/sztrómalamella Sötétszakasz - sztróma A növényeket érı hatások a pigmentösszetétel változását okozhatják I. Mintavétel (inhomogén minta) II.
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
Gyors-kinetikai módszerek
 Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Kémiai alapismeretek 6. hét
 Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Kémiai alapismeretek 6. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék biner 2013. október 7-11. 1/15 2013/2014 I. félév, Horváth Attila c Egyensúly:
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
A fehérjék hierarchikus szerkezete. Szerkezeti hierarchia. A fehérjék építőkövei az aminosavak. Fehérjék felosztása
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérje-fehérje kölcsönhatások és kölcsönhatási hálózatok. Szilágyi András
 Fehérje-fehérje kölcsönhatások és kölcsönhatási hálózatok Szilágyi András Vázlat Fehérje-fehérje kölcsönhatások Kölcsönhatási hálózatok Kísérleti módszerek Bioinformatikai vonatkozások adatbázisok szerkezetfüggetlen
Fehérje-fehérje kölcsönhatások és kölcsönhatási hálózatok Szilágyi András Vázlat Fehérje-fehérje kölcsönhatások Kölcsönhatási hálózatok Kísérleti módszerek Bioinformatikai vonatkozások adatbázisok szerkezetfüggetlen
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Enzimek. Enzimek! IUBMB: szisztematikus nevek. Enzimek jellemzése! acetilkolin-észteráz! legalább 10 nagyságrend gyorsulás. szubsztrát-specificitás
 Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
, mitokondriumban (peroxiszóma) citoplazmában
 -helye: máj, zsírszövet, vese, agy, tüdő, stb. - nem a β-oxidáció megfordítása!!! β-oxidáció Zsírsav-szintézis -------------------------------------------------------------------------------------------
-helye: máj, zsírszövet, vese, agy, tüdő, stb. - nem a β-oxidáció megfordítása!!! β-oxidáció Zsírsav-szintézis -------------------------------------------------------------------------------------------
A LIZOFOSZFATIDSAV SZEREPE A β 2 -MIKROGLOBULIN AMILOIDKÉPZÉSÉBEN
 Pál-Gábor Henrietta A LIZOFOSZFATIDSAV SZEREPE A β 2 -MIKROGLOBULIN AMILOIDKÉPZÉSÉBEN című doktori értekezés tézisei Témavezetők: Dr. Kardos József Eötvös Loránd Tudományegyetem, Biokémiai Tanszék Dr.
Pál-Gábor Henrietta A LIZOFOSZFATIDSAV SZEREPE A β 2 -MIKROGLOBULIN AMILOIDKÉPZÉSÉBEN című doktori értekezés tézisei Témavezetők: Dr. Kardos József Eötvös Loránd Tudományegyetem, Biokémiai Tanszék Dr.
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Tartalom. A citoszkeleton meghatározása. Citoszkeleton. Mozgás a biológiában A CITOSZKELETÁLIS RENDSZER 12/9/2016
 Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Tartalom A CITOSZKELETÁLIS RENDSZER Nyitrai Miklós, 2016 november 29. 1. Mi a citoszkeleton? 2. Polimerizáció, polimerizációs egyensúly 3. Filamentumok osztályozása 4. Motorfehérjék A citoszkeleton meghatározása
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025)
 Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025) A pályázat megvalósítása során célunk volt egyrészt a molekulák asszociációjának tanulmányozására
Részletes szakmai beszámoló Az erbb proteinek asszociációjának kvantitatív jellemzése című OTKA pályázatról (F049025) A pályázat megvalósítása során célunk volt egyrészt a molekulák asszociációjának tanulmányozására
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Reakciókinetika. aktiválási energia. felszabaduló energia. kiindulási állapot. energia nyereség. végállapot
 Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
A kovalens kötés polaritása
 Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
[S] v' [I] [1] Kompetitív gátlás
![[S] v' [I] [1] Kompetitív gátlás [S] v' [I] [1] Kompetitív gátlás](/thumbs/93/114506146.jpg) 8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
A rácsmodell. Szabadenergia felületek.
 1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk.
 .5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
.5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
Dér András MTA SZBK Biofizikai Intézet
 Hogyan befolyásolja a határfelületi vízréteg szerkezete a fehérjeműködést? Dér András MTA SZBK Biofizikai Intézet Felületi feszültség Geometriai optimalizáció Biológiai érhálózat γ dw da Eötvös mérései
Hogyan befolyásolja a határfelületi vízréteg szerkezete a fehérjeműködést? Dér András MTA SZBK Biofizikai Intézet Felületi feszültség Geometriai optimalizáció Biológiai érhálózat γ dw da Eötvös mérései
3/11/2015 SZEDIMENTÁCIÓ ELEKTROFORÉZIS. Szedimentáció, elektroforézis. Alkalmazások hematológia - vér frakcionálása
 PÉCSI TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNYI KAR hematológia - vér frakcionálása Példa: teljes vérkép www.aok.pte.hu SZÉTVÁLASZTÁSI MÓDSZEREK: SZEDIMENTÁCIÓ ELEKTROFORÉZIS vérplazma (55 %) BIOFIZIKA
PÉCSI TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNYI KAR hematológia - vér frakcionálása Példa: teljes vérkép www.aok.pte.hu SZÉTVÁLASZTÁSI MÓDSZEREK: SZEDIMENTÁCIÓ ELEKTROFORÉZIS vérplazma (55 %) BIOFIZIKA
Kémiai reakciók. Közös elektronpár létrehozása. Általános és szervetlen kémia 10. hét. Elızı héten elsajátítottuk, hogy.
 Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Abszorpciós spektroszkópia
 Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Abszorpciós fotometria
 A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
K68464 OTKA pályázat szakmai zárójelentés
 K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
K68464 OTKA pályázat szakmai zárójelentés A fehérjeaggregáció és amiloidképződés szerkezeti alapjai; a különféle morfológiájú aggregátumok kialakulásának körülményei és in vivo hatásuk vizsgálata Vezető
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Prolinizomerizáció. A diszulfidhidak képzõdése.
 1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Szedimentáció, elektroforézis. Biofizika előadás Talián Csaba Gábor
 Szedimentáció, elektroforézis Biofizika előadás Talián Csaba Gábor 2012.03.20. szedimentáció = ülepedés Sedeo2, sedi, sessum ül Sedimento 1 - ülepít Cél: 1 - elválasztás 2 - a részecskék méretének vagy
Szedimentáció, elektroforézis Biofizika előadás Talián Csaba Gábor 2012.03.20. szedimentáció = ülepedés Sedeo2, sedi, sessum ül Sedimento 1 - ülepít Cél: 1 - elválasztás 2 - a részecskék méretének vagy
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai
 Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Kutatási programunk fő célkitűzése, az 2 -plazmin inhibitornak ( 2. PI) és az aktivált. XIII-as faktor (FXIIIa) közötti interakció felderítése az 2
 Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
AMINOSAVAK, FEHÉRJÉK
 AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
AMINOSAVAK, FEHÉRJÉK Az aminosavak olyan szerves vegyületek, amelyek molekulájában aminocsoport (-NH2) és karboxilcsoport (-COOH) egyaránt előfordul. Felosztás A fehérjéket feloszthatjuk aszerint, hogy
11/15/10! A CITOSZKELETÁLIS RENDSZER! Polimerizáció! Polimerizációs egyensúly! Erő iránya szerint:! 1. valódi egyensúly (aktin)" Polimer mechanika!
 11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
11/15/10! A CITOSZKELETÁLIS RENDSZER! 1. Mi a citoszkeleton?! 2. Polimerizáció, polimerizációs egyensúly! 3. Filamentumok osztályozása! Citoszkeleton : Eukariota sejtek dinamikus vázrendszere! Három fő
