A felgombolyodás problémája
|
|
|
- Margit Királyné
- 8 évvel ezelőtt
- Látták:
Átírás
1 1. A probléma 2. A fehérjék stabil konformációs állapotai 3. A felgombolyodás általános tulajdonságai 4. A felgombolyodás modelljei 5. A felgombolyodás nyomon követésének technikái 6. A felgombolyodás kinetikai jellemzõi 7. Az "új szemlélet" A felgombolyodás problémája A felgombolyodási probléma Centrális dogma: DNS > RNS > polipeptidlánc? >? mûködõképes konformáció (genetikai kód második fele) Anfinsen kísérlete (1961) Ribonukleáz enzim, benne 8 cisztein, 4 diszulfidhíd Diszulfidhidakat béta merkapto etanollal redukáljuk és a fehérjét 8M ureával denaturáljuk > rendezetlen szerkezet, hiányzó aktivitás Levegõn állni hagyjuk > lassú oxidáció > néhány óra alatt a szerkezet helyreáll, az enzim aktívvá válik Oxidálószerrel gyors oxidáció > diszulfidhidak rossz párosításban állnak helyre > sem a szerkezet, sem az aktivitás nem áll helyre Ez a hibás szerkezet kevés redukálószer hozzáadására kijavítódik Következtetés: az aminosavsorrend tartalmazza a háromdimenziós szerkezet kialakulásához szükséges összes információt. A felgombolyodás termodinamikai kontroll alatt áll: a natív szerkezet a termodinamikailag legstabilisabb állapot. 1
2 Tehát: az elsõdleges szerkezet meghatározza a 3D szerkezetet. De HOGYAN? Ez a felgombolyodási probléma. Alproblémák: Milyen kinetikus folyamat vagy útvonal révén veszi fel a fehérje a natív, biológiailag aktív konformációt? Mi a felgombolyodott konformációk stabilitásának fizikai alapja? Az aminosavsorrend miért éppen azt a 3D szerkezetet és felgombolyodási mechanizmust határozza meg, amit, és miért nem valami mást? Ha adott egy fehérje aminosavsorrendje, hogyan lehet abból a háromdimenziós szerkezetet megjósolni? Az elsõ kérdés részkérdései: A felgombolyodás termodinamikai vagy kinetikai kontroll alatt áll? Hogyan képes a polipeptidlánc rövid idõ alatt megtalálni a natív szerkezetet? Mi indítja el a felgombolyodást, és mi az ehhez szükséges legrövidebb idõ? Milyen útvonalon történik a felgombolyodás? Milyen a köztitermékek szerkezete? Az in vitro kísérletek alapján felismert szabályszerûségek érvényesek e in vivo is? A felgombolyodási probléma jelentõsége Elméleti jelentõség: A molekuláris biológia és a fehérjebiofizika egyik legizgalmasabb, legtöbb fejtörést okozó problémája. Számos sejtbiológiai folyamattal nagyon szorosan összefügg. A genetikai kód második fele A fehérjék bioszintézise és degradációja Hõsokk Biotechnológiai jelentõség: A baktériumban túlexpresszióval termeltetett idegen fehérjék legtöbbször ún. inklúziós testekké tapadnak össze. Ezekbõl kell a fehérjéket renaturálni. Orvosi jelentõség: "felgombolyodási betegségek": Mutáció hatására vagy nem megfelelõ körülmények között egyes fehérjék rosszul gombolyodnak fel, aggregálódnak. Prionbetegségek: Amiloid lerakódások keletkezése szivacsos agysorvadásban (kergemarhakór, Creutzfeld Jakob) Amiloid rostok Alzheimer kórban A Levinthal paradoxon: termodinamikai vagy kinetikai kontroll? Anfinsen kísérlete > a natív térszerkezet a polipeptidlánc szabadentalpia minimumának felel meg, azaz termodinamikailag az a legstabilabb állapot az adott körülmények között. Tehát a felgombolyodás termodinamikai kontroll alatt áll. Hogyan találja meg a lánc az energiaminimumot? Minden peptidegységnek kb. 10 különbözõ konformációja van Tehát egy 100 aminosavból álló láncnak különbözõ konformációja van. Egyik aminosavkonformáció a másikba legalább másodperc alatt alakul át, a teljes láncra vonatkoztatva mp alatt. Tehát a natív konformáció megtalálásához kb másodpercre, azaz kb évre van szükség. A valóságban 1 másodpercen belül felgombolyodik. A gyors felgombolyodás csak úgy lehetséges, ha a konformációs tér nem férhetõ hozzá teljes egészében a lánc számára, hanem a folyamat egy útvonalon halad, kinetikai kontroll alatt áll. Ez a Levinthal paradoxon (Levinthal 1968): az Anfinsen kísérlet szerint termodinamikai kontroll van, az állapotszámlálás szerint kinetikai kontroll. Most akkor melyik? A paradoxon feloldása: lásd késõbb. 2
3 A fehérjék stabil konformációs állapotai A legombolyodott (denaturált) állapot. Jele: U (unfolded) vagy D (denatured) A felgombolyodott (natív, általában biológiailag aktív) állapot. Jele: F (folded) vagy N (natív). A köztes állapotok (köztitermékek, intermedierek). Jelük: I (intermediate) A legombolyodott (denaturált) állapot Ideális esetben: véletlen elrendezõdésû lánc (random coil) minden torziós szög független a szekvenciában távolabbi torziós szögektõl minden konformációnak kb. azonos a szabadentalpiája kivéve, ahol a lánc átfedné önmagát (kizárttérfogat effektus) 100 aminosav > konformáció. Ha egy oldatban 10 mg fehérje van, ez kb db molekula. Tehát: várhatóan mindegyik molekula más más konformációban van. Erõs denaturálószerekben (6M GdmHCl, 8M urea) a fehérjék jó közelítéssel valóban véletlen elrendezõdésûek (hidrodinamikai tul. szerint) Enyhébb denaturálószerek, ill. ph vagy hõmérsékleti szélsõségek: a szerkezet kevésbé random, s valamivel kompaktabb. Lokális hidrofób oldallánc csoportosulások egy kevés hélixtartalom (fõleg alkoholos oldatban) Termodinamikailag a legombolyodott állapot egységes: nem tartalmazhat kooperatívan felgombolyodott részstruktúrákat. A teljesen felgombolyodott, natív állapot Alapegység a domén Számos esetben kimutatták, hogy az izolált domének önállóan képesek felgombolyodni. Azonban az izolált domének többnyire nem olyan stabilak, mint a teljes fehérje (pl. foszfoglicerát kináz) Az izolált doménekbõl általában nem rakódik össze a funkcióképes fehérje Szubdomének (doménnél kisebb töredékek): egyes esetekben szintén képesek önálló felgombolyodásra, más esetekben nem. Doménméret felsõ határa kb. 200 aminosav. Ennél nagyobb feltehetõen nem gombolyodna fel. A szerkezet állandósága: A különbözõ kristályformákból röntgendiffrakcióval és az oldatból NMR rel nyert 3D szerkezetek lényegében mindig azonosak A szerkezet kisebb nagyobb mértékben flexibilis (Brown mozgás, kis fehérjék néhány óránként vagy naponként teljesen le is gombolyodnak), de közel marad az átlagszerkezethez. A köztes állapotok Másképpen: kompakt denaturált állapotok. Csak akkor figyelhetõk meg, ha elég sok molekula veszi fel ezeket, tehát ha eléggé stabilak. Híg denaturálószerben vagy szerves oldószerben A leginkább vizsgált: "olvadt gombóc" (molten globule) állapot kompakt nagy konformációs fluktuációk, különösen az oldalláncoknál laza, nemspecifikus hidrofób kölcsönhatások rendezetlen, fluktuáló harmadlagos szerkezet ellenben a natívhoz hasonló másodlagos szerkezet számos fehérjében kimutatták (pl. alfa laktalbumin, mioglobin) "Pre olvadt gombóc" (pre molten globule): kevésbé kompakt, sokkal lazább van másodlagos szerkezet, de nem mindig hasonlít a natívhoz néhány fehérjénél kimutatták (citokróm c, triptofán szintáz) "Nagy rendezettségû" olvadt gombóc: a natív harmadlagos szerkezet egy része megvan kevésbé fluktuál 3
4 néhány fehérjénél találták (ubiquitin, antitest) Vitatott, hogy a köztes állapotok rajta vannak e a felgombolyodás útvonalán, vagy "útelágazások" eredményei. A felgombolyodás általános tulajdonságai A natív állapot többnyire reverzibilisen legombolyítható: denaturálószer hozzáadásával melegítéssel vagy hûtéssel ph változtatásával (savanyítás, lúgosítás) nagy nyomással a diszulfidkötések elhasításával Kicsi, egydoménes fehérjék esetében többnyire: kétállapotú átmenet (N natív, D denaturált áll.) A köztes állapotok ezeknél nem figyelhetõek meg. Kooperativitás érvényesül: egy molekula vagy az N, vagy a D állapotban marad csak meg tartósan, minden egyéb állapotból vagy az egyikbe, vagy a másikba ugrik. Más fehérjéknél köztes állapotok is fellépnek A populációk eloszlása a felgombolyodottság mértékének függvényében: Bal oldal: egy kétállapotú, kooperatív átmenetet mutató fehérje populációeloszlásai (kicsi, egydoménes fehérjékre jellemzõ) Jobb oldal: köztes állapottal rendelkezõ, nemkooperatív úton legombolyodó, hipotetikus fehérje populációeloszlásai A felgombolyodott állapot stabilitása Mennyiségek és értelmezésük Állandó nyomás és hõmérséklet: a rendszer egyensúlyi állapotát a szabadentalpia (G) minimuma adja. 4
5 Kedvezõ és ezért spontán módon végbemegy az a folyamat, melynek során G csökken. Kedvezõtlen, ezért spontán módon nem megy végbe az a folyamat, melynek során G növekedne. A folyamat jellege G változása H változása S változása Értelmezés Kedvezõ kicsi kicsi + Kölcsönhatások jönnek létre, melyek csökkentik a belsõ energiát, ezáltal a szabadentalpiát A rendszer mozgásszabadsága nõ, így növekszik az entrópia és ezzel a szabadentalpia Kedvezõtlen + + kicsi + kicsi Kölcsönhatások szakadnak fel, melyek növelik a belsõ energiát, ezáltal a szabadentalpiát A rendszer mozgásszabadsága csökken, így csökken az entrópia és ezzel a szabadentalpia Az entrópia és az entalpia általában egyirányba változik: Ha kölcsönhatások jönnek létre, az entalpia csökken, s a mozgásszabadság csökken, így az entrópia is csökken Ha kölcsönhatások szakadnak fel, az entalpia nõ, s a mozgásszabadság nõ, így az entrópia is nõ Mi dönti el, hogy az entalpiacsökkentõ vagy az entrópianövelõ folyamat valósul e meg? A hõmérséklet, amely a szabadentalpia kifejezésében az entrópiát súlyozza. Hõmérséklet Kedvezõ folyamat Hová törekszik a rendszer? Alacsony Magas Entalpiacsökkenés: kölcsönhatások kialakulása (emiatt valószínûleg a mozgásszabadság csökkenése: entrópiacsökkenés) Entrópianövekedés: a mozgásszabadság növekedése (emiatt valószínûleg kölcsönhatások felbomlása: entalpianövekedés) Az alacsony entalpiájú állapotok felé (melyekben a mozgásszabadság valószínûleg korlátozott, az entrópia alacsony) A magas entrópiájú állapotok felé (melyekben a kölcsönhatások valószínûleg felbomlanak, az entalpia magas) Példa: két állapottal rendelkezõ rendszer esetében: 1. állapot: alacsony entalpia, alacsony entrópia (pl. fehérje natív állapota: sok kölcsönhatás, kicsi mozgásszabadság) 2. állapot: magas entalpia, magas entrópia (pl. fehérje denaturált állapota: kevés kölcsönhatás, nagy mozgásszabadság [a lánc mozgásszabadságát a konformációs entrópia jellemzi) 5
6 A valóságban a helyzet bonyolultabb, mert denaturált állapotban az apoláros oldalláncok körül a víz rendezett, alacsony entrópiájú, a felgombolyodásnál ezek a vízmolekulák felszabadulnak, ami entrópianövekedéssel jár. A konformációs entrópia csökkenése azonban jelentõsebb ennél. A fehérjék termodinamikai paramétereinek hõmérsékletfüggése A lizozim termodinamikai paraméterei: A natív és a denaturált állapot közötti entalpia és entrópiakülönbség erõsen hõmérsékletfüggõ, mert a két állapot hõkapacitása erõsen eltér (a denaturálté sokkal nagyobb a nagyobb hidrofób felszín miatt) A natív állapot stabilitásának mértéke a natív és a denaturált állapot közötti szabadentalpia különbség (deltag). deltag egy parabolaszerû görbe, amely két helyen metszi a vízszintes tengelyt: 6
7 deltag nek közepes hõmérsékleten van egy szélsõértéke. Itt maximális a stabilitás Az egyik metszéspont a hõdenaturáció hõmérséklete (olvadáspont, T m ) A másik metszéspont a hidegdenaturáció hõmérséklete (gyakran 0 Celsius alá esik) deltag 5 15 kcal/mol (20 60 kj/mol) közé esik, tehát a fehérjék stabilitása kicsi. (Nagy számok kis különbsége) az N és U állapotok közötti egyensúlyi állandó körüli. A felgombolyodás kooperativitása Mi az oka a kétállapotú átmenet kooperativitásának? A részlegesen felgombolyodott állapotokban olyan kedvezõtlen kölcsönhatások lehetnek, amelyek sem a natív, sem a denaturált állapotban nincsenek meg Az egyes kölcsönhatások kooperativitása Két kölcsönhatás. Mindkettõ erõsíti a másikat egy lambda kooperativitási faktorral. Ok: közelebb hozza a kölcsönható partnereket, így kisebb lesz az entrópiaköltség. Több kölcsönhatás esetén: Példa: 7
8 10 kölcsönhatás van, a legombolyodott állapotban mindegyikre K=10 4 A kooperativitás lambda=10 együtthatóval érvényesül Emiatt ha n kölcsönhatás már megvan, akkor az n+1. K*lambda n egyensúlyi állandóval jön létre (felsõ grafikon) Alsó grafikon: A legombolyodott állapot és az n kölcsönhatást tartalmazó állapot közötti egyensúlyi állandó. Eleinte csökken, majd nõni kezd. 10 kölcsönhatásnál az állapot stabilizálódik. Tehát sok gyenge kölcsönhatás a kooperativitás miatt stabilizálja egymást. A felgombolyodás modelljei "Nukleáció és gyors növekedés" (Wetlaufer 1973) A sebességmeghatározó lépés egy "folding mag" keletkezése. Ha ez megvan, a felgombolyodás már erre építkezve gyorsan végbemegy. (Téves.) Kinetikai séma: "Puzzle játék" (jigsaw puzzle, Harrison és Durbin 1985) Mivel a denaturált állapotban minden molekula konformációja más, mindegyik más útvonalon gombolyodik fel. Ahogyan egy puzzle t is sokféle sorrendben lehet összerakni. Kinetikai séma: 8
9 "Diffúzió kollízió adhézió" (Karplus és Weaver 1976) A legombolyodott fehérjében idõnként natívszerû mikrodomének (pl. hélixrészlet) jelennek meg, miközben a lánc részei diffúziós mozgást végeznek. Ha a mikrodomének összetalálkoznak, összetapadnak és stabilizálják egymást. Hierarchikus modellek: Felgombolyodás a szerkezeti hierarchia szerint. Mag, másodlagos szerkezet, szupermásodlagos, domén, monomer, oligomer. Moduláris modellek Szubdomének mint modulok önállóan felgombolyodnak, majd asszociálódnak "Keretmodell" (framework model, Baldwin 1989) A másodlagos szerkezeti elemek korán létrejönnek (ez a felgombolyodás elsõ lépése) és meglehetõsen stabilak. Késõbb jön létre a harmadlagos szerkezet. (Ez egy hierarchikus modell.) "Hidrofób kollapszus" (Dill 1985) Az elsõ lépés a lánc összeesése a hidrofób kölcsönhatás miatt. A másodlagos szerkezet csak ezután vagy ezzel egyidõben jön létre. "Hidrofób cipzár" (Dill 1993) A hidrofób kölcsönhatás cipzárszerû viselkedése segíti a másodlagos szerkezeti elemek létrejöttét. 9
10 A felgombolyodás nyomon követésének technikái Általánosan: a fehérjét denaturáló közegbõl gyorsan olyan környezetbe visszük, amely a natív állapotnak kedvez. Pl. nemdenaturáló pufferrel kihigítjuk hidegdenaturált fehérjét hirtelen fölmelegítünk (T ugrás) fotokémiai reakcióval indítunk Ezután a felgombolyodás folyamatát követjük. A felgombolyodás beindításának módszerei Keveréses módszerek Stopped flow módszer (enzimkinetikából ismert) Itt a két hengerben nem szubsztrát és enzim, hanem fehérje és nemdenaturáló puffer van. A dugattyúkat benyomjuk gyors összekeveredés. A megállító dugattyú ütközése állítja meg az áramlást és indítja el a mérést. Holtidõ: kb. 1 ms. Turbulens keverõk Pl. Berger féle golyós keverõ. Holtidõ: >100 mikrosec vagy több Folyamatos áramlású rendszerek. Holtidõ: pár 10 mikrosec. "freejet" (szabad sugaras) módszer: lamináris áramlás kis nyíláson. Holtidõ: pár 10 mikrosec. Nem keveréses módszerek Flash fotolízis: fotoreakció lézervillanással Fényindukált elektrontranszfer (redoxfehérjénél oxidált denaturált állapotban elektrontranszfer felgombolyodást indít) Holtidõ: < 1 mikrosec T ugrás, gyors fûtéssel 10
11 elektromos kisüléssel: holtidõ 10 mikrosec lézerrel: 20 nanosec!!! A felgombolyodás követésének módszerei Tulajdonság Módszer Felbontás Mit mér? Belsõ fluoreszcencia <1 ms Fõleg a triptofánok orientációja és környezete A hidrofób mag szorossága Ultraibolya elnyelés ms Fõleg a tirozinok orientációja és környezete Külsõ (ANS) fluoreszcencia ms Hidrofób foltok és árkok képzõdése, felbomlása Fluoreszcencia quenching ms A triptofánok elszigeteltsége külsõ, hidrofil quencherektõl Ciszteinil quenching 10 s A ciszteinek védettsége hidrofil reagensektõl Fluoreszcencia anizotrópiája ms A triptofánok mozgékonysága és kb. molekulaméret A molekula mérete Fluoreszcenciás energiatranszfer ms Triptofán és egy kovalensen kapcsolt fluorofór távolsága Kisszögû röntgenszórás <100 ms Átlagos girációs sugár Kvázielasztikus fényszórás 1 s Átlagos girációs sugár Másodlagos szerkezet és tartós H kötések Cirkuláris dikroizmus távoli UV ben ms Szekvenciára és populációra átlagolt gerinckonformáció "Pulse labelling" NMR 5 10 ms Hol vannak stabil amid és triptofán H kötések "Pulse labelling" tömegspektroszkópia 5 10 ms Hidrogénkötések képzõdése diszkrét intermedierekben. Heterogén populációt felbontja! 11
12 Harmadlagos Biológiai aktivitás ms s Natív szerkezet az aktív helyen szerkezeti kontaktusok, natív szerkezet megléte Megszakított felgombolyodás CIrkuláris dikroizmus közeli UV ben 10 ms ms Diszkrét intermedierek legombolyodási sebessége (mint stabilitásuk mértéke) Stabil kontaktusok aromás csoportok között, diszulfidhidak Valós idejû NMR 1 s Specifikus kontaktusok oldalláncok között Mutációs vizsgálatok Az egyes oldalláncok energiajáruléka a diszkrét intermedierek stabilitásához Az átmeneti állapotok jellemzése Átmeneti állapot: nagy energiájú, igen rövid élettartamú (ne keverjük össze a köztes állapottal), állapot, két stabil állapot közötti energiagát teteje. Jellemzése csak közvetett módszerekkel lehetséges: Különféle tényezõk hatását vizsgáljuk a felgombolyodás sebességére, ebbõl az átmeneti állapot tulajdonságaira következtethetünk. Pl.: Hõmérséklet > termodinamika, aktiválási energia Nyomás > relatív moláris térfogat denaturálószerek > vízzel érintkezõ felszínek ionerõsség, ph > ionizálható csoportok járulékai Ezekbõl általános kép: az átmeneti állapot kompakt, de laza konformációk halmaza A felgombolyodás kinetikai jellemzõi Két állapot esetén a felgombolyodás "reakcióegyenlete": k f a felgombolyodás, k u a legombolyodás sebességi állandója. A sebességi állandók kapcsolata az aktiválási energiákkal: k f =A f e Ea,f/RT, k u =A u e Ea,u/RT. Az egyensúlyi állandó: K eq =k f /k u A sebességi és egyensúlyi állandók tipikus hõmérsékletfüggése (Arrhenius ábrázolás és Van't Hoff ábrázolás) 12
13 Az ln K ábrázolva 1/T függvényében: Van't Hoff ábrázolás. Meredekségébõl a reakció entalpiája (deltah) számítható ki. Az ln k ábrázolva 1/T függvényében: Arrhenius ábrázolás. Meredekségébõl a reakció aktiválási energiája számítható ki. A K eq Van't Hoff ábrázolása kismértékben görbült, ez deltah hõmérsékletfüggésébõl ered, ez pedig a natív és denaturált állapot közötti hõkapacitás különbségbõl. Utóbbi abból adódik, hogy a felgombolyodás során hidrofób felszínek temetõdnek el. (A hõkapacitás ugyanis arányos a szabadon lévõ hidrofób felszínek összfelületével.) k f és k u Arrhenius ábrázolásából az átmeneti állapot milyenségére lehet következtetni: k unfolding (=k u ) Arrhenius ábrázolása lineáris > a legombolyodás aktiválási energiája hõmérsékletfüggetlen, tehát az átmeneti állapot hõkapacitása megegyezik a natívéval. Ez azt jelenti, hogy az átmeneti állapotban ugyanakkora hidrofób felszín van szabadon, mint a natív állapotban. k refolding (=k f ) Arrhenius ábrázolása erõsen görbült > a felgombolyodás aktiválási energiája hõmérsékletfüggõ, tehát az átmeneti állapot hõkapacitása eltér a denaturáltétól. Ez azt jelenti, hogy a denaturált állapotból az átmeneti állapotba kerülés során hidrofób felszínek temetõdnek el. Konklúzió: az átmeneti állapot sokkal inkább a natív állapothoz hasonlít, mint a denaturálthoz. (Csak véletlen, hogy a három görbe egy pontban metszi egymást) Kinetikai modellek A legombolyodás kinetikája ált. egyszerû: két állapot, egy sima sebességi állandó A felgombolyodás kinetikája ált. bonyolult néhány kis fehérje esetében itt is jó a kétállapot modell de általában több kinetikai fázis: A nemnatív állapotok heterogén populációt alkotnak 13
14 A felgombolyodás realisztikusabb sémája (a) legombolyodott molekulák (b) hidrofób kollapszus, megjelenõ másodlagos szerkezeti elemek, nukleációs helyek (g) a végcél: a natív fehérje, jobbkezes hélixköteg (f) rossz konnektivitású konformáció (d) rossz topológia: balkezes elrendezõdés (hibás) (e) megfelelõ elrendezõdésû, de még laza állapot (c) a nem megfelelõ köztitermék újból legombolyodhat (c') vagy átrendezõdhet. Tölcsér: a folyamat során egyre csökken a hozzáférhetõ állapotok száma (entrópia) Az "új szemlélet" A kismolekuláknál megszokott reakciókinetika fogalmai nehézkesen alkalmazhatóak a felgombolyodásra. Heterogén populációk vannak Nincs egyértelmû reakciókoordináta Az új szemlélet kulcsfogalma: energiafelület Felgombolyodási tölcsér Szabadentalpia felület Függõleges tengely: a molekula ún. belsõ szabadentalpiája. (az adott konformációhoz tartozó szabadentalpia, figyelembe véve az összes lehetséges oldószer konfigurációt). Tehát a molekula konformációs entrópiája nincs benne. Vízszintes tengelyek: a fehérjéhez tartozó konformációs szabadsági fokok. (Pl. az összes lehetséges torziós szög a fehérjében). Tehát a felület minden egyes pontja a fehérje egy konformációjának felel meg. Sokdimenziós felület sokdimenziós hipertérben. A 3D ábrázolások csak szemléltetések 14
15 Az egyes molekulák a legmélyebb pontot keresik, minden molekula más más útvonalat bejárva, miközben a hõmozgás löködi õket. A felület globális minimuma a fehérje natív állapotának felel meg, ide szánkáznak le a molekulák a tölcsér oldalán. A fenti sima felület a legegyszerûbb, kétállapotú rendszernek felel meg. Általános eset: bonyolult domborzat, dombok, gödrök, árkok, sok lokális minimum > bonyolult felgombolyodási kinetika Két frakcióból álló sokaság a denaturált állapotban (lizozim ilyen): lassan (B) és gyorsan (A) gombolyodó frakció A Levinthal paradoxon feloldása Hibás kiindulópont: Levinthal javaslata: útvonalak: 15
16 Valóság: tölcsér! A felgombolyodás termodinamikai vagy kinetikai kontroll alatt áll? Válasz: A natív szerkezet termodinamikai kontroll alatt áll (a szabadentalpiafelület globális minimuma). Ezt az állapotot azonban a felgombolyodás során kinetikus kontroll alatt álló intermediereken keresztül éri el a fehérje. Mindig a globális minimum e a natív állapot? Nem. Ellenpélda: plazminogén aktivátor inhibitor 1 A biológiailag aktív forma instabil, pár óra alatt átalakul egy stabilabb állapotba Szerkezeti változás: a lánc egy része beépül a középsõ béta lemezbe Energiafelülete efféle: A régi és az új szemlélet összehasonlítása Régi szemlélet Új szemlélet Színpad Útvonal Energiafelület (tölcsér) Szereplõk Történés Kísérleti háttér Elméleti alap Jól elkülönülõ, határozott szerkezetû, megjelölhetõ állapotok (pl. N, D, I 1, I 2, stb.) Egymás után, meghatározott sorrendben történõ események sorozata Hagyományos, optikai jelek változásain alapuló mérések Klasszikus kémiai reakciókinetika A konformációk heterogén, dinamikus sokaságai Sok párhuzamos szálon futó, diffúziószerû mikroszkopikus események Modern módszerek (pulse labelling NMR és tömegspektroszkópia, mutációs vizsgálatok, gyors, lézerindítású mérések) Statisztikus fizika: spinüveg modellek és rácsmodellek 16
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Felgombolyodási kinetikák, mechanizmusok
 Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
Felgombolyodási kinetikák, mechanizmusok 1. Alapkísérletek 2. Többállapotú viselkedés 3. Hidrogénkicserélõdéses módszerek 4. Példák a felgombolyodás részletes jellemzésére Alapkísérletek Egyensúlyi felgombolyodásvizsgálatok
A rácsmodell. Szabadenergia felületek.
 1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
1. A spinüveg modell 2. A rácsmodellek típusai 3. A rácsmodellek elõnyei és hátrányai 4. A rácsmodellek elemzése 5. Egyszerû rácsmodellek 6. Rácsmodellek natív állapotai 7. Oldalláncok 8. Rácsmodellek
Szimulációk egyszerősített fehérjemodellekkel. Szilágyi András
 Szimulációk egyszerősített fehérjemodellekkel Szilágyi András Szimulációs módszerek alkalmazhatósági tartományai Egyszerősített modellek Három típusát mutatjuk be: Játék rácsmodellek Realisztikusabb rácsmodellek
Szimulációk egyszerősített fehérjemodellekkel Szilágyi András Szimulációs módszerek alkalmazhatósági tartományai Egyszerősített modellek Három típusát mutatjuk be: Játék rácsmodellek Realisztikusabb rácsmodellek
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
"Olvadt gombócok" és más kompakt denaturált állapotok
 "Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
"Olvadt gombócok" és más kompakt denaturált állapotok 1. Egy kis tudománytörténet 2. Az "olvadt gombóc" modell 3. Egyensúlyi köztitermékek 4. Kinetikus köztitermékek 5. Vitás kérdések 6. Az olvadt gombócok
A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása
 A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu reakció t 1/2 25 ºC-on t 1/2 100 ºC-on DNS hidrolízis Biopolimerek
A fehérjéket felépítő húsz standard aminosav Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu reakció t 1/2 25 ºC-on t 1/2 100 ºC-on DNS hidrolízis Biopolimerek
A fehérjéket felépítő húsz standard aminosav
 Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Biopolimerek reakció t 1/2 25 ºC-on t 1/2 100 ºC-on egy polimerben lévő kötések tipikus száma hányfajta
Fehérjék szerkezetének kialakulása Osváth Szabolcs Semmelweis Egyetem szabolcs.osvath@eok.sote.hu Biopolimerek reakció t 1/2 25 ºC-on t 1/2 100 ºC-on egy polimerben lévő kötések tipikus száma hányfajta
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Reakciókinetika. aktiválási energia. felszabaduló energia. kiindulási állapot. energia nyereség. végállapot
 Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
Reakiókinetika aktiválási energia kiindulási állapot energia nyereség felszabaduló energia végállapot Reakiókinetika kinetika: mozgástan reakiókinetika (kémiai kinetika): - reakiók időbeli leírása - reakiómehanizmusok
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Fehérjék felépítése és struktúrája. Aminosav oldalláncok. A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel
 Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
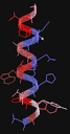 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Biopolimer 12/7/09. Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. DNS. Polimerek. Kardos Roland DNS elsődleges szerkezete
 Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Biopolimerek Makromolekulák szerkezete. Fehérje szerkezet, és tekeredés. Osztódó sejt magorsófonala Kardos Roland 2009.10.29. Dohány levél epidermális sejtjének aktin hálózat Bakteriofágból kiszabaduló
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
összetevője változatlan marad, a falra merőleges összetevő iránya ellenkezőjére változik, miközben nagysága ugyanakkora marad.
 A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
A módszerek jelentősége. Gyors-kinetika módszerek. A módszerek közös tulajdonsága. Milyen módszerekről tanulunk?
 Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
Gyors-kinetika módszerek módszerek jelentősége 2010. március 9. Nyitrai Miklós biológiai mechanizmusok megértése; iológiai folyamatok időskálája; Vándorló melanocita (Victor SMLL). ms skálán való mérések.
A metabolizmus energetikája
 A metabolizmus energetikája Dr. Bódis Emőke 2015. október 7. JJ9 Miért tanulunk bonyolult termodinamikát? Miért tanulunk bonyolult termodinamikát? Mert a biokémiai rendszerek anyag- és energiaáramlásának
A metabolizmus energetikája Dr. Bódis Emőke 2015. október 7. JJ9 Miért tanulunk bonyolult termodinamikát? Miért tanulunk bonyolult termodinamikát? Mert a biokémiai rendszerek anyag- és energiaáramlásának
Reakciókinetika és katalízis
 Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Határfelületi jelenségek. Fogorvosi anyagtan fizikai alapjai 3. Általános anyagszerkezeti ismeretek. N m J 2
 Határelületi jelenségek 1. Felületi eszültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagszerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eszültség adhézió nedvesítés ázis ázisdiagramm
Határelületi jelenségek 1. Felületi eszültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagszerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eszültség adhézió nedvesítés ázis ázisdiagramm
Mi mekkora? Fehérjék a Biológiába és a Nanotechnológiában. Plenty of Room at the Bottom. Hullám részecske kettősség 2/15/17
 Fehérjék a Biológiába és a Nanotechnológiában Mi mekkora? Osváth Szabolcs Semmelweis Egyetem osvath.szabolcs@med.semmelweis-univ.hu Plenty of Room at the Bottom " The principles of physics, as far as I
Fehérjék a Biológiába és a Nanotechnológiában Mi mekkora? Osváth Szabolcs Semmelweis Egyetem osvath.szabolcs@med.semmelweis-univ.hu Plenty of Room at the Bottom " The principles of physics, as far as I
Energia. Energiamegmaradás törvénye: Energia: munkavégző, vagy hőközlő képesség. Az energia nem keletkezik, nem is szűnik meg, csak átalakul.
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Energiamegmaradás törvénye: Az energia nem keletkezik, nem is szűnik meg, csak átalakul. A világegyetem energiája állandó. Energia
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Energiamegmaradás törvénye: Az energia nem keletkezik, nem is szűnik meg, csak átalakul. A világegyetem energiája állandó. Energia
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai
 Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
Fogorvosi Anyagtan Fizikai Alapjai Biomolekulák nanomechanikája A biomolekuláris rugalmasság alapjai Mártonfalvi Zsolt Biofizikai és Sugárbiológiai Intézet Semmelweis Egyetem Budapest Biomolekulák mint
6. Zárványtestek feldolgozása
 6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
6. Zárványtestek feldolgozása... 1 6.1. A zárványtestek... 1 6.1.1. A zárványtestek kialakulása... 2 6.1.2. A feldolgozási technológia... 3 6.1.2.1. Sejtfeltárás... 3 6.1.2.2. Centrifugálás, tisztítás...
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Speciális fluoreszcencia spektroszkópiai módszerek
 Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
Speciális fluoreszcencia spektroszkópiai módszerek Fluoreszcencia kioltás Fluoreszcencia Rezonancia Energia Transzfer (FRET), Lumineszcencia A molekuláknak azt a fényemisszióját, melyet a valamilyen módon
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Gyors-kinetikai módszerek
 Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Gyors-kinetikai módszerek Biofizika szemináriumok Futó Kinga Gyorskinetika - mozgástan Reakciókinetika: reakciók időbeli leírása reakciómechanizmusok reakciódinamika (molekuláris szintű történés) reakciósebesség:
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz
 Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz A házi feladatok beadhatóak vagy papír alapon (ez a preferált), vagy e-mail formájában is az rkinhazi@gmail.com címre. E-mail esetén ügyeljetek a
Fizikai kémia 2 Reakciókinetika házi feladatok 2016 ősz A házi feladatok beadhatóak vagy papír alapon (ez a preferált), vagy e-mail formájában is az rkinhazi@gmail.com címre. E-mail esetén ügyeljetek a
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Fehérjeszerkezet, fehérjetekeredés
 Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
Fehérjeszerkezet, fehérjetekeredés A fehérjeszerkezet szintjei A fehérjetekeredés elmélete: Anfinsen kísérlet Levinthal paradoxon A feltekeredés tölcsér elmélet 2014.11.05. Aminosavak és fehérjeszerkezet
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
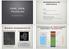 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Prolinizomerizáció. A diszulfidhidak képzõdése.
 1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
1. 2. Prolinizomerizáció. A diszulfidhidak képzõdése. Prolinizomerizáció A prolin cisz és transz állapota A prolinizomerizációs hipotézis A prolinizomerizáció próbái Mutációs kísérletek Nagyobb fehérjék
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Határfelületi jelenségek. Fogorvosi anyagtan fizikai alapjai 3. Általános anyagszerkezeti ismeretek E A J 2. N m
 Határelületi jelenségek 1. Felületi eültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eültség adhézió nedvesítés ázis ázisdiagramm
Határelületi jelenségek 1. Felületi eültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eültség adhézió nedvesítés ázis ázisdiagramm
Szabadentalpia nyomásfüggése
 Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség
 Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség Osváth Szabolcs Evans-Searles fluktuációs tétel Denis J Evans, Ezechiel DG Cohen, Gary P Morriss (1993) Denis J Evans, Debra
Evans-Searles fluktuációs tétel Crooks fluktuációs tétel Jarzynski egyenlőség Osváth Szabolcs Evans-Searles fluktuációs tétel Denis J Evans, Ezechiel DG Cohen, Gary P Morriss (1993) Denis J Evans, Debra
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
Univerzalitási osztályok nemegyensúlyi rendszerekben, Ódor Géza
 Univerzalitási osztályok nemegyensúlyi rendszerekben, Ódor Géza odor@mfa.kfki.hu 1. Bevezetõ, dinamikus skálázás, kritikus exponensek, térelmélet formalizmus, renormalizáció, topológius fázis diagrammok,
Univerzalitási osztályok nemegyensúlyi rendszerekben, Ódor Géza odor@mfa.kfki.hu 1. Bevezetõ, dinamikus skálázás, kritikus exponensek, térelmélet formalizmus, renormalizáció, topológius fázis diagrammok,
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
A TERMODINAMIKA I. AXIÓMÁJA. Egyszerű rendszerek egyensúlya. Első észrevétel: egyszerű rendszerekről beszélünk.
 A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
Egy részecske mozgási energiája: v 2 3 = k T, ahol T a gáz hőmérséklete Kelvinben 2 2 (k = 1, J/K Boltzmann-állandó) Tehát a gáz hőmérséklete
 Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék
 A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
A negyedleges szerkezet szerepe a kis hő-sokk fehérjék chaperon működésében Készítette: Böde Csaba Témavezető: Dr. Fidy Judit egyetemi tanár Semmelweis Egyetem Elméleti Orvostudományok Doktori Iskola Szigorlati
Az energia. Energia : munkavégző képesség (vagy hőközlő képesség)
 Az energia Energia : munkavégző képesség (vagy hőközlő képesség) Megjelenési formái: Munka: irányított energiaközlés (W=Fs) Sugárzás (fényrészecskék energiája) Termikus energia: atomok, molekulák véletlenszerű
Az energia Energia : munkavégző képesség (vagy hőközlő képesség) Megjelenési formái: Munka: irányított energiaközlés (W=Fs) Sugárzás (fényrészecskék energiája) Termikus energia: atomok, molekulák véletlenszerű
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Belső energia, hőmennyiség, munka Hőtan főtételei
 Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
Biofizika szeminárium. Diffúzió, ozmózis
 Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Bioinformatika 2 6. előadás
 6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése
 1. 2. Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése A több doménbõl álló fehérjék felgombolyodása 1. Domének 2. Izolált domének felgombolyodása 3. A doménpárosodás mint sebességmeghatározó
1. 2. Több doménbõl, ill. több alegységbõl álló fehérjék összeszerelõdése A több doménbõl álló fehérjék felgombolyodása 1. Domének 2. Izolált domének felgombolyodása 3. A doménpárosodás mint sebességmeghatározó
Molekuláris motorok működése
 Biológiai molekuláris motorok tulajdonságai Molekuláris motorok működése Osváth Szabolcs Semmelweis Egyetem - anyaguk lágy (biopolimerek) - nem kovalens kölcsönhatások vezérlik a működést - nincsenek sima
Biológiai molekuláris motorok tulajdonságai Molekuláris motorok működése Osváth Szabolcs Semmelweis Egyetem - anyaguk lágy (biopolimerek) - nem kovalens kölcsönhatások vezérlik a működést - nincsenek sima
Mivel foglalkozik a hőtan?
 Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
A diffúzió leírása az anyagmennyiség időbeli változásával A diffúzió leírása a koncentráció térbeli változásával
 Kapcsolódó irodalom: Kapcsolódó multimédiás anyag: Az előadás témakörei: 1.A diffúzió fogalma 2. A diffúzió biológiai jelentősége 3. A részecskék mozgása 3.1. A Brown mozgás 4. Mitől függ a diffúzió erőssége?
Kapcsolódó irodalom: Kapcsolódó multimédiás anyag: Az előadás témakörei: 1.A diffúzió fogalma 2. A diffúzió biológiai jelentősége 3. A részecskék mozgása 3.1. A Brown mozgás 4. Mitől függ a diffúzió erőssége?
Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis
 Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Termodinamika (Hőtan)
 Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
Reakció kinetika és katalízis
 Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet
 Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS 2013. Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet DIFFÚZIÓ 1. KÍSÉRLET Fizika-Biofizika I. - DIFFÚZIÓ 1. kísérlet: cseppentsünk tintát egy üveg vízbe 1. megfigyelés:
Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS 2013. Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet DIFFÚZIÓ 1. KÍSÉRLET Fizika-Biofizika I. - DIFFÚZIÓ 1. kísérlet: cseppentsünk tintát egy üveg vízbe 1. megfigyelés:
Peptidek és fehérjék 1. Fehérjék Fehérjetekeredés. Fehérje (protein) Fehérje (protein) Aminosavak. Aminosavak
 Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Fehérjék Fehérjetekeredés Peptidek és fehérjék 1 peptid: rövid, peptid kötéssel összekapcsolt aminosavakból álló polimer (< ~50 aminosav) fehérje: hosszú, peptid kötéssel összekapcsolt aminosavakból álló
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
Axiomatikus felépítés az axiómák megalapozottságát a felépített elmélet teljesítképessége igazolja majd!
 Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Diffúzió. Diffúzió sebessége: gáz > folyadék > szilárd (kötőerő)
 Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel
 Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Peptidek és fehérjék szerkezetvizsgálata spektroszkópia és in silico módszerekkel Mik a peptidek és fehérjék? L-konfigurációjú a-aminosavakból felépülő lineáris polimerek 3 betűs kód: -Thr-His-Ile-Ser-Ser-Ile-Met-Pro-Leu-Glu-
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Termokémia, termodinamika
 Termokémia, termodinamika Szalai István ELTE Kémiai Intézet 1/46 Termodinamika A termodinamika a természetben végbemenő folyamatok energetikai leírásával foglalkozik.,,van egy tény ha úgy tetszik törvény,
Termokémia, termodinamika Szalai István ELTE Kémiai Intézet 1/46 Termodinamika A termodinamika a természetben végbemenő folyamatok energetikai leírásával foglalkozik.,,van egy tény ha úgy tetszik törvény,
Hőtan I. főtétele tesztek
 Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek
 TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek A talajszennyezés csökkenése/csökkentése bekövetkezhet Természetes úton Mesterséges úton (kármentesítés,
TALAJVÉDELEM XI. A szennyezőanyagok terjedését, talaj/talajvízbeli viselkedését befolyásoló paraméterek A talajszennyezés csökkenése/csökkentése bekövetkezhet Természetes úton Mesterséges úton (kármentesítés,
N I. 02 B. Mágneses anyagvizsgálat G ép. 118 2011.11.30. A mérés dátuma: A mérés eszközei: A mérés menetének leírása:
 N I. 02 B A mérés eszközei: Számítógép Gerjesztésszabályzó toroid transzformátor Minták Mágneses anyagvizsgálat G ép. 118 A mérés menetének leírása: Beindítottuk a számtógépet, Behelyeztük a mintát a ferrotestbe.
N I. 02 B A mérés eszközei: Számítógép Gerjesztésszabályzó toroid transzformátor Minták Mágneses anyagvizsgálat G ép. 118 A mérés menetének leírása: Beindítottuk a számtógépet, Behelyeztük a mintát a ferrotestbe.
Anyagok az energetikában
 Anyagok az energetikában BMEGEMTBEA1, 6 krp (3+0+2) Környezeti tényezők hatása, időfüggő mechanikai tulajdonságok Dr. Tamás-Bényei Péter 2018. szeptember 19. Ütemterv 2 / 20 Dátum 2018.09.05 2018.09.19
Anyagok az energetikában BMEGEMTBEA1, 6 krp (3+0+2) Környezeti tényezők hatása, időfüggő mechanikai tulajdonságok Dr. Tamás-Bényei Péter 2018. szeptember 19. Ütemterv 2 / 20 Dátum 2018.09.05 2018.09.19
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék. elrendeződés, rend, rendszer, periodikus ismétlődés
 Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
Reakciókinetika és katalízis 2. előadás: 1/18 Kinetika: Kísérletekkel megállapított sebességi egyenlet(ek). A kémiai reakció makroszkópikus, fenomenológikus jellemzése. 1 Mechanizmus: Az elemi lépések
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
A fehérjék hierarchikus szerkezete
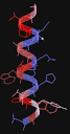 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Általános kémia képletgyűjtemény. Atomszerkezet Tömegszám (A) A = Z + N Rendszám (Z) Neutronok száma (N) Mólok száma (n)
 Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
VEBI BIOMÉRÖKI MŰVELETEK KÖVETELMÉNYEK. Pécs Miklós: Vebi Biomérnöki műveletek. 1. előadás: Bevezetés és enzimkinetika
 VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly
 Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
A fény tulajdonságai
 Spektrofotometria A fény tulajdonságai A fény, mint hullámjelenség (lambda) (nm) hullámhossz (nű) (f) (Hz, 1/s) frekvencia, = c/ c (m/s) fénysebesség (2,998 10 8 m/s) (σ) (cm -1 ) hullámszám, = 1/ A amplitúdó
Spektrofotometria A fény tulajdonságai A fény, mint hullámjelenség (lambda) (nm) hullámhossz (nű) (f) (Hz, 1/s) frekvencia, = c/ c (m/s) fénysebesség (2,998 10 8 m/s) (σ) (cm -1 ) hullámszám, = 1/ A amplitúdó
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
