Válasz prof.dr. Kopper László bírálatára
|
|
|
- Mihály Orosz
- 8 évvel ezelőtt
- Látták:
Átírás
1 Válasz prof.dr. Kopper László bírálatára Tisztelettel köszönöm Kopper László Professzor Úrnak az igen alapos, részletekbe menő bírálatát és a nyilvános vitára bocsátást támogató nyilatkozatot. Válaszok a bíráló kérdéseire: Nem említi a jelenleg a klinikumban alkalmazott tumormarkereket (pl.cea, PSA, CA125) és azt a markerekkel kapcsolatos gondot, hogy szenzitivitásuk és specificitásuk alacsony - gondolja a jelölt, hogy az általa talált markerek ettől mentesek? A dolgozat formai korlátai nem tették lehetővé, hogy a tumorok követésére és felderítésére is alkalmazott valamennyi tumormarkert részletesen bemutassuk. A bevezetőben ezért csak a vizsgálatok szempontjából releváns kettő biomarkert (a HER2 és az ösztrogén receptort) tárgyaltuk részletesen. Az általunk azonosított új markerekrek sem érik el a 100%-os szenzitivitást és specificitást. A tumorok heterogenitása miatt ezt csak több marker kombinációjával és egyidejű vizsgálatával lehet a jövőben javítani. A tamoxifen meghatározásával kapcsolatban említi az IHC-t és a microarrayt (utóbbi mellett foglal állást) - megbecsülné a költség/hatékonyságot a két módszer esetében? Amennyiben a gén chipeket csak az ösztrogén receptor meghatározására használnánk, akkor a költség/hatékonyság terén az IHC messze hatékonyabb lenne. Azonban a dolgozat alapfeltevése, hogy egy gén-chip alapú többgénes tesztet végzünk, amellyel egyidejűleg tudjuk az ösztrogén receptor státuszt is meghatározni. A gén chipek felépítése miatt a mért gének számának növelése a költségeket semennyivel sem növeli (kb. 20 ezer gén méréséig), ezért egy ilyen esetben már microarray-ok vezetnek a költség/hatékonyság terén. a klinikumban csak negatív biomarkerekkel találkozunk a jelölt szerint ezt gondolja pl. a tüdőrák esetében a mutáns EGFR1-ről vagy az ALK-ról? Ezek ugyanis pozitívan utalnak a kiválasztandó terápiás szerekre. Ha a HER2 pozitivitás mértéke egyenesen arányos a trastuzumab kezelésre várható válasz mértékével akkor a HER2 miért negatív biomarker? Az dolgozatban használt beosztás alapja, hogy egy biomarker két különböző csoportot tud azonosítani: vagy azokat a betegeket mutatja meg, akik reagálni fognak a terápiára ( pozitív biomarker ), vagy azokat a betegeket, mutatja meg, akik nem fognak reagálni ( negatív biomarker ). A bíráló által említett három gén (HER2, ALK, EGFR) esetén alapvetően igaz, hogy a negatív betegek nem reagálnak. Ez kiegészül azzal, hogy: 1
2 A HER2 ellenes trastuzumab kezelésre az objektív válasz a HER2 pozitív betegeken belül 50%-os (Ref: Brufsky, Am J Clin Oncol, 2010). Az ALK kinázra hat a crizotinib, amelyet az amerikai FDA ALK expresszáló NSCLC kezelésére hagyott jóvá. Az ennek alapjául szolgáló két vizsgálatban az ALK pozitív betegek 50% és 61%-a reagált a gyógyszerre (Ref: Malik, Clin Cancer Res, 2014). Az EGFR inhibitor erlotinibet NSCLC és hasnyálmirigyrák kezelésére hagyta jóvá az FDA, az EGFR pozitív tumorok 65%-a válaszolt a kezelésre (Ref: Rossell, Lancet, 2012). Ki kell emelni, hogy az onkológiában alkalmazott gyógyszerek között ezek kimagaslóan jó eredmények, azonban a pozitív betegek nagyon nagy aránya továbbra sem mutat a kezelésre választ. Tehát egyik szer esetén sem mondhatjuk, hogy a gén által kiválasztott betegcsoport benne van a kezelésre reagáló betegek egy egyébként tágabb csoportjában - ebben az esetben beszélhetnénk ugyanis egy valódi pozitív biomarkerről. Ugyanaz a molekuláris hiba különböző tumorokban támogathatja a célzott terápiát, vannak ez alól kivételek is (nem is kevés). Jelölt ezeket kivételként értékeli? Annak ellenére sem mondanám, hogy ezek feltétlenül kivételek, hogy a jelenlegi tudásunk alapján annak tűnnek. Egy példával illusztrálva: amikor eredetileg a KRAS-t független prognosztikai tényezőként azonosították (Ref: Andreyec, JNCI, 1998), akkor számtalan vizsgálat indult, amelyekben azonban ezt nem sikerült igazolni (Ref: Samowitz, Can Epidemiol Biomarkers Prev 2000; Ince, JNCI, 2005; Ogino, Gut, 2008). Később, amikor egyes terápiákhoz viszonyították, akkor igazolást nyert, hogy a KRAS mégis egy klinikailag is használható biomarker csak nem prognosztikai hanem prediktív előrejelzőként (Ref: Karapetis, NEJM, 2008; Bokemeyer, JCO, 2008; Tejpar, JCO, 2008; Van Cutsem, JCO, 2008; Van Cutsem, NEJM, 2009; Amado, JCO, 2008). Lényegében tehát a későbbi tudásunk alapján, egy másik kérdésben, vagy másik gyógyszerrel kombinációban lehet, hogy ezek a molekuláris hibák is segíteni fognak a helyes célzott terápia megválasztásában. A tamoxifen és a trastuzmab csak a részletes tárgyalás miatt maradtak ki a szisztémás terápiával szembeni rezisztencia tárgyalása során. Ha egyszer a minták heterogének, akkor hogy lehet a különböző sejtvonalakat összehasonlítani? Az általunk végzett vizsgálatok során szinte mindig több különböző sejtvonalat használtunk. Abból a feltevésből indultunk ki, hogy a sejtvonalak közötti különbségek mellett egy-egy hasonló tulajdonság (pld adott gyógyszerrel szemben létrehozott rezisztencia) alapján hasonlítani fognak 2
3 egymásra és így segíthetnek az adott tulajdonság molekuláris jellemzőinek felderítésében. Ezen túlmenően ki kell emelnem, hogy a rezisztencia párhuzamos modellezése során pontosan ez is volt a célunk. A klinikailag heterogén mintákban egy adott szerrel szembeni rezisztencia különböző molekuláris mechanizmusokkal jöhet létre. Amennyiben több nagyon hasonló, párhuzamosan kezelt sejtvonalat tanulmányozunk, akkor az ezek közötti eltérés már azt is lehetővé teheti, hogy a valós betegekben egymástól függetlenül kialakuló rezisztencia-mechanizmusok közül többet is egyszerre azonosítani tudjunk. Külön kérdés, amit jó lenne modellezni, hogy a rezisztencia kialakulása után nem egyszer ugyanazzal a szerrel kezelnek, sokszor sikeresen. A tumorok progressziója során a klonális evolúció azt is eredményezi, hogy miközben lesznek lassan osztódó, egy adott szerrel szemben rezisztens klónok, eközben ezek mellett kialakulhatnak gyorsan osztódó további al-vonalak is. Mivel ezek szaporodása meghaladhatja a rezisztens klónt, ezért a tumor nagy tömegét adhatják és a terápiára való érzékenységük folytán a kezelés újból eredményes lehet. Mit ért tumortípustól független biomarker alatt? Ez a klinikumban alig képzelhető el. Alkalmasak ezek azonosítására az in vitro rendszerek? Itt utalnék a fentebb már említett, az EGFR-en ható erlotinibre, amelyet NSCLC mellett hasnyálmirigyrák esetében is jóváhagytak (illetve jelenleg még további más tumortípusok esetén is klinikai vizsgálat alatt van), tehát az EGFR ebben az esetben a tumor típusától független. Azzal egyetértek, hogy tisztább a megfogalmazás, ha a tumor típusa helyett a tumor szövettani/anatómiai eredetétől független biomarkerről beszélünk. A rezisztenciagének előrejelzésénél fontos említeni az EGFR1 rezisztenciagént, amit már elég jól ismerünk, és tipikus példáját kínálja annak, hogy ezt a gént próbálják gátolni. Ez belefér a koncepcióba? Ez pontosan így van, azonban az általunk vizsgált modellekben az EGFR nem volt a legjobb gének között, ezért ezt a gént nem vizsgáltuk részletesen. Az előrejelzés nehézségét a kombinációk jelentik. Jelölt számos módszer közül ennek megközelítésére melyik alkalmas? 3
4 Az első jelentős, az Oncogene-ben megjelent közleményünkben abban a szerencsés helyzetben voltunk, hogy valamennyi beteg monoterápiás kezelést kapott, ezek 2000 előtt Norvégiában operált betegek voltak. Ez ma már szinte teljesen elképzelhetetlen. Az általunk használt módszerek elviekben a kombinációkkal szembeni rezisztencia azonosítását is lehetővé teszik, azonban ehhez jóval több betegminta szükséges, mint amennyi jelenleg rendelkezésünkre áll. A jövőben nagyobb mintaszámú vizsgálatok lehetővé tehetik, hogy a betegeket az egyes kezelési kombinációk szerint további alcsoportokba osszuk, ami ezen csoportok vizsgálatának az alapját adhatja. A jelölt szerint az OncotypeDx-szel sem független, sem reprodukálható vizsgálat nem történt. Tudomásom szerint a klinikai reprodukálhatóság 95% körüli, az eladott tesztek a félmilliót közelítik. A teszt során az RT-PCR méréseket az USA-ban fizikálisan egy helyen végzik el. Ez azt jelenti, hogy valamennyi mérést ugyanazok az emberek végzik. További zavaró tényező, hogy a megrendelőnek nem csak a méréshez szükséges egyetlen mintát, de pld további metszeteket is be kell küldenie ezek alapján egy magasan képzett patológus már egyedül is jó hatékonysággal meg tudja a klinikai kérdést válaszolni. Eközben az egyes gének meghatározására az OncotypeDX teljesen alkalmatlan. Összesen 784 beteg vizsgálata során az IHC/FISH módszerrel HER2 pozitívnak mért 36 betegből az teszt elfogadhatatlanul keveset, mindössze 10-et talált meg (Ref: Dabbs, JCO, 2011). Véleményem szerinte egy diagnosztikai teszt csak onnantól megbízható, ha látjuk a nyers eredményeket, amelyeket egy független csoport is reprodukálni tudott. Ennek hiánya az oka annak, hogy az OncotypeDX-et az FDA nem hagyta jóvá. Németországban a teszt befogadását szintén az alacsony megbízhatóság miatt utasították el. Az, hogy ennek ellenére közel félmillió tesztet eladtak, arra vezethető vissza, hogy a teszt eredményeképpen kevesebb beteg esetében szükséges kemoterápia, amely a biztosítók számára nagyobb költségmegtakarítással jár, mint amibe maga a vizsgálat kerül (Ref: Lyman, Cancer, 2007). Van arra adat, hogy miért nem kezelnek daganatos betegeket akik így negatív kontrollként szolgálnak? A kezeletlen kifejezés az értekezésben nem arra vonatkozik, hogy a beteg nem részesült kezelésben, csupán azt tartalmazza, hogy a sebészet után nem részesült gyógyszeres kezelésben. A kutatásaink során vizsgált kezeletlen minták elsősorban emlőrákos betegek voltak, amely tumor esetében nem minden esetben szükséges kemoterápiát adni. A retrospektíven elvégzett gén-chip vizsgálatokba többször direkt azok a minták kerülnek be, ahol 4
5 a betegek nem kaptak szisztémás kezelést, mert ez teszi lehetővé, hogy a tumor természetes lefolyását tanulmányozni tudjuk. A transzkriptom mennyire veszi figyelembe a mikrorns-eket? A transzkriptom csak az mrns-ek mérését tartalmazza. Az általunk használt gén chipek sem mérték a mikrorns-ek kifejeződését - kivéve egy vizsgálatunkat, ahol azonban csak ezt mértük (Ref: Tchernitsa, J Pathol, 2010). Miért gondolja a jelölt, hogy független rezisztencia-markerek lennének, amikor a tumorok génexpressziós profilja is igen eltérő vagy csak ebben egyeznek? Négy tumortípus vizsgálata elegendő a függetlenség kimondásához? A vizsgálatban (Ref: Győrffy, Oncogene, 2005) nem egyszerűen négy különböző tumortípust vizsgáltunk, hanem négy sejtvonal párt. Mindegyik pár egy eredeti (kemoterápiára érzékeny) és egy ebből származó, a kemoterápiára rezisztens vonalat tartalmazott. Statisztikai elemzés során ezeket párba állítottuk, majd azokat a géneket kerestük, amelyek mind a négy párban eltérő expressziót mutattak. Ezzel a megközelítéssel azt akartuk elérni, hogy a tumorok közötti eredendő génexpressziós különbség csak minimálisan befolyásolja a végeredményt. A megközelítés hatásosságát alátámasztja, hogy a mintázat ezután független beteganyagban (amely csak egy tumortípust tartalmazott) is működött. A microarray rendszer által használt hibridizációs próbák figyelembe veszik e a splicing variánsok pontos kimutatásának szükségességét? Ma már vannak ilyen microarray rendszerek, azonban mi még nem ilyen gén chipet használtunk, mivel ezek az általunk végzett mérések időpontjában nem álltak rendelkezésre. Mi biztosítja, hogy ugyanarra a transzkriptomra tervezett oligo-szett és RT-PCR szett minden tumor minden állapotára használható lesz? Hogyan kezelhető az intraés intertumorális heterogenitás? A human genom array mindenkire alkalmazható? Az Affymetrix gén chipek (mint technológia) reprodukálhatósága és specificitása áll a mögött, hogy ezt a technológiát az FDA 2011-ben humán diagnosztikai alkalmazásra is jóváhagyta. Nagy valószínűséggel az egyes alanyokban levő eltérések (pld. SNP-k) miatt a chipeken levő egyes próbák alkalmazhatósága nem tökéletes, azonban nem ismerek olyan irodalmi hivatkozást, amely pontosan ezt a kérdést a már kereskedelmi forgalomban árult, FDA által jóváhagyott tesztek esetében megválaszolná (ezek a gén chip alapú MammaPrint és a Nanostring technológiát használó PAM50). 5
6 Ezen tesztek fejlesztése alatt az általunk is használt megközelítést alkalmazták: ennek során lényegében két korábbi csoporthoz hasonlítják a beteget. Más szóval a csoportok közötti különbséget használjuk fel arra, hogy az aktuális beteget pld a jó vagy rossz prognózisú csoportba soroljuk. A teszt fejlesztése során alkalmazott tanulóhalmaz nagy mérete teszi lehetővé, hogy az egy csoporton belüli tumorok közötti heterogenitás ellenére is megbízható legyen a végeredmény. Bár egy mérés alapján az intra-tumor heterogenitás pontosan nem mérhető, azonban a kialakulásának okait már lehet quantifikálni. Erre alkalmasak például a szintén Affymetrix microarray mérést felhasználó, a kromoszómális instabilitást mérő mintázatok (Ref: Carter, Nat Genet, 2006). Milyen tanácsot tud adni az in vitro rendszer eredményei alapján a gyógyszeriparnak? Segítenek az in vivo driver gének azonosítására? Amikor egy gén klinikai mintákban összefüggést mutat egy tumorral, annak alapvetően kettő oka lehet. Egyrészt a gén lehet egy oki (driver) gén, amely a tumor létrejöttének vagy progressziójának folyamatában közvetlenül is részt vesz erre példa az KRAS vagy az ösztrogén receptor; másrészt az is lehet, hogy a gén ugyan nem maga okozza a molekuláris elváltozást, azonban annak eredményeképpen eltérést mutat. Erre tipikus példa a KI67, amely a tumor proliferációjának mértékére enged következtetni. Ezen második csoport is kiválóan alkalmas biomarkernek, azonban a gyógyszeripar számára az első (driver) gének jelentik az igazi célpontot. Azt, hogy a kettő csoport közül egy gén melyikbe kerüljön, csak in vitro vizsgálatok segítségével lehet eldönteni. A betegek osztályozása a monoterápia (ami igen ritka) előtt történt, vagy retrospektíven? Hogyan magyarázza az ábrán a plató kialakulását? A doxorubicin monoterápiában részesült betegminták egy retrospektív biobankból származtak ma már szinte lehetetlen lenne ilyen beteganyagot összeállítani. A plató kialakulása véleményem szerint csak technikai eredetű. Bár öt év után egyik vizsgált csoportban sem volt esemény, azonban már csak 11 beteg volt itt a vizsgálatban és ezek is mind cenzorált értékkel rendelkeztek. Ki kell emelnem, hogy a betegek utánkövetése nem egyszerre kezdődött, hanem időben eltolva, a műtétek időpontjában, azonban magát a cenzorálást a vizsgálat időpontjában el kellett végeznünk. Más szóval nem várhattuk meg, hogy az összes betegben meglegyen a teljes utánkövetés. Emiatt nagy valószínűséggel a vizsgálat lezárása után lehetett még további relapszus a cenzorált betegek között is. Egy újabb esemény pld 75 hónap után a Kaplan-Meier görbe felépítése miatt (hogy a túlélők proporcionális arányát mutatja) a platófázist teljesen 6
7 megszüntetné, miközben a számolt szignifikancia csak minimálisan változna (mivel a teljes grafikon csak elenyésző mértékben változna). PSMB7 szerepel ez a gén az előzőekben prognosztikai képességekkel kimutatottak között? Ha nem, miért nem? Mi a sejtek relatív viabilitása? A PSMB7 nem szerepelt az első doxorubicin érzékenységgel foglalkozó cikkünkben. Ennek valószínűleg az az oka, hogy két eltérő gén-chip platformot használtunk a két vizsgálat során (az elsőben a Stanfordi Egyetem-en készített chipeket, a másodikban pedig kereskedelmi forgalomban kapható Affymetrix gén chipeket). Különböző platformok egy adott gént különböző dinamikus tartományban, eltérő érzékenységgel és specificitással határoznak meg. Nem ismerek olyan vizsgálatot, ahol a Stanfordi-i és az Affymetrix chipeket közvetlenül egymással hasonlították volna össze. A relatív viabilitás a kezeletlen kontrollhoz viszonyítva mutatott sejtvitalitást jelenti. Ennek értéke ezért a kontroll esetében 1 lenne, azonban ezt nem tüntettük fel a grafikonon. A parallel evolúciós modell érdekes lehetőség a rezisztenciához vezető mechanizmusok azonosítására. Ez a modell is jól illeszkedik a tumortípustól való függetlenségre? A parallel evolúciós modell során egyetlen tumortípust vizsgáltunk. Amennyiben azt találtuk volna, hogy valamennyi sejtvonal ugyanazzal a mechanizmussal alkalmazkodik a gyógyszeres kezeléshez, akkor ezt meg kellett volna erősítenünk más tumortípusok esetén is. Eredményeink ezzel szemben pont a tumorok heterogenitását emelik ki, ezért véleményem szerint ezek az eredmények más tumortípusokra való vonatkoztatás esetén is megállják a helyüket. Tudjuk, hogy a sunitinib több támadásponttal rendelkezik. Ezektől mennyire függnek vagy függetlenek a feltételezett rezisztenciagének? A rezisztenciagének nagy része független volt ezektől. Azonban még az RT-PCR-el validált gének között is találtunk olyat, amelyik a sunitinib célpontjaitól (VEGFR, C-KIT, FLT3, PDGFR) downstream helyezkedik el (pld a RAB17, amelyik a RAS onkogének családjába tartozik). A kutatás során ezen kívül sikerült több olyan gént is igazolnunk, amelyek a vizsgált szerek által modulált jelátviteli útvonalhoz kapcsolódnak (pld ERBB2, TGFA, PDGFA, AKT1). Figyelembe véve, hogy még nem ismerjük a TK gátlószerek valamennyi célpontját (ezt mutatja az úgynevezett off-target hatások feltérképezetlen volta), ezek a pozitív leletek is igazolják, hogy az általunk alkalmazott megközelítés helyes. Az eddig a rezisztenciával kapcsolatba nem hozott, de szingifikánsan 7
8 összefüggő gének részletes vizsgálatára lesz szükség a jövőben ahhoz, hogy a gén és a gyógyszer közötti kapcsolatot teljesen felderítsük. A génexpressziós mintázatokat generáló experimentális és klinikai vizsgálatok reprodukálhatósága alacsony. Vonatkozik ez az előbbiekben kimutatott rezisztenciagénekre is? A klinikai vizsgálatok alacsony reprodukálhatósága mögött nagy valószínűséggel az alacsony mintaszám áll. Az emlőtumor diagnosztikájában alkalmazott MammaPrint-et mindössze 78 betegben (Ref: van t Veer, Nature, 2002), a Genomic Grade Index-et pedig 64 beteg alapján (Ref: Sotiriou, J Natl Cancer Inst, 2006) azonosították. Ezzel szemben mi jóval nagyobb esetszámokkal dolgoztunk, pld a PSMB7 gén prognosztikai szerepét 1592 betegben igazoltuk. Emiatt bízunk abban, hogy az általunk azonosított rezisztenciagének a jövőben is jól reprodukálhatóak lesznek. A prognosztika mellett, vagy inkább előtt, a prediktív biomarkerek iránt nagy az igény beleértve a várható rezisztenciát is. Milyen esélyt lát az utóbbiak azonosítására? A rezisztencia biomarkereinek azonosítását megnehezíti, hogy az utóbbi tíz évben a célzott terápiás szerek rohamos terjedésével az onkológiai kezelés teljesen átalakulni látszik. Azonban klinikailag a várható választ előrejelző (mind pozitív mind negatív) biomarkerek szerepét mutatja, hogy míg egy átlagos kemoterápiás szer esetén a minőséggel korrigált életidő-hosszabbodás (QUALY) mindössze 0,1 év, addig trastuzumab esetén (ahol a HER2 személyében rendelkezünk egy hatásos biomarkerrel) ez már kettő év. Rövidesen a gyógyszeripar csak olyan gyógyszereket hozhat forgalomba, ahol meg tudjuk előre megmondani, hogy ki fog reagálni. Mindezek miatt a prediktív biomarkerek a következő évtized kutatásai során a slágertermékek között lehetnek. A világhálón elérhető rendszerekkel kapcsolatban kerül említésre, hogy génchipek segítségével direkt tumordiagnózis készíthető. Megmagyarázná ezt a definíciót a jelölt? Direkt tumordiagnózis alatt a közvetlen tumordiagnózist értettem. Egyes diagnosztikus tesztek (pld CT) esetén a mérés és a beteget kezelő onkológus között még egy további szakirányú továbbképzéssel rendelkező orvos is megvizsgálja az eredményt (a példa esetében egy radiológus). Mivel a gén chipek kiértékelése teljesen automatizálható, ezért megfelelő program birtokában az eredmény direkt a kezelőorvoshoz futhat be. 8
9 Cél lehet-e az, hogy az ilyen típusú adatok az egyes betegek számára is hasznosak legyenek-e? Vagy elégnek bizonyulnak a jelenlegi terápiát meghatározó, befolyásoló biomarkerek? Úgy néz ki, hogy az onkológiában elkezdődött az a forradalom, amire oly régóta vártunk. Évente a jóváhagyott onkológiai gyógyszerek száma több mint 10%-al nő (az elmúlt 1 év alatt 14-el 133-ra emelkedett). Eközben csak példaként említve a kolon- és rectum-tumor esetén a halálozás esélye 1990 óta 37%-al csökkent, emlőrák esetén pedig 33%-al. Ezen trendek alapján azt várhatjuk, hogy a továbbiakban is új gyógyszerekre és új biomarkerekre lesz igény. Még mindig nagyon sok kutatásra lesz szükség, ameddig eljutunk oda, hogy a gyógyszeres kezelés a sebészi kezelés alternatívájaként is szóba jöjjön. Végezetül még egyszer köszönöm a lelkiismeretes bírálatot, és köszönöm, hogy a dolgozat elfogadását javasolja. Budapest, Győrffy Balázs 9
Válasz Dr. Balázs Margit, az MTA doktora bírálatára
 Válasz Dr. Balázs Margit, az MTA doktora bírálatára Mindenek előtt tisztelettel köszönöm Balázs Margit Professzor Asszonynak, hogy elvállalta doktori munkám opponensi feladatát, valamint az elért eredményeinkre
Válasz Dr. Balázs Margit, az MTA doktora bírálatára Mindenek előtt tisztelettel köszönöm Balázs Margit Professzor Asszonynak, hogy elvállalta doktori munkám opponensi feladatát, valamint az elért eredményeinkre
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Válasz Dr. Szalai Csaba, az MTA doktora bírálatára
 Válasz Dr. Szalai Csaba, az MTA doktora bírálatára Hálásan köszönöm a dolgozat minden részletre kiterjedő kritikai bírálatát valamint a kutatásaink során elért eredmények elismerő méltatását. Válaszok
Válasz Dr. Szalai Csaba, az MTA doktora bírálatára Hálásan köszönöm a dolgozat minden részletre kiterjedő kritikai bírálatát valamint a kutatásaink során elért eredmények elismerő méltatását. Válaszok
OPPONENSI VÉLEMÉNY. Dr. Kulka Janina MTA doktori értekezéséről
 1 OPPONENSI VÉLEMÉNY Dr. Kulka Janina MTA doktori értekezéséről Az értekezés témaválasztása korszerű és megfelel a XXI. századi emlő onkológia elvárásainak. A patológusok szerepe az emlőrák kórismézésében
1 OPPONENSI VÉLEMÉNY Dr. Kulka Janina MTA doktori értekezéséről Az értekezés témaválasztása korszerű és megfelel a XXI. századi emlő onkológia elvárásainak. A patológusok szerepe az emlőrák kórismézésében
Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére
 MTA DOKTORI PÁLYÁZAT Akadémiai Doktori Értekezés Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére Dr. Győrffy Balázs,
MTA DOKTORI PÁLYÁZAT Akadémiai Doktori Értekezés Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére Dr. Győrffy Balázs,
Tumorprogresszió és előrejelzése. Statisztikák. Statisztika - USA Megbetegedés / 10 leggyakoribb (2012)
 Tumorprogresszió és előrejelzése 1. Statisztikák 2. Kezelési protokollok 3. Jövő 4. Teszt írása Megbetegedés / 1 leggyakoribb (212) Statisztikák Forrás: CA Halálozás / 1 leggyakoribb (212) Statisztika
Tumorprogresszió és előrejelzése 1. Statisztikák 2. Kezelési protokollok 3. Jövő 4. Teszt írása Megbetegedés / 1 leggyakoribb (212) Statisztikák Forrás: CA Halálozás / 1 leggyakoribb (212) Statisztika
GNTP. Személyre Szabott Orvoslás (SZO) Munkacsoport. Kérdőív Értékelő Összefoglalás
 GNTP Személyre Szabott Orvoslás (SZO) Munkacsoport Kérdőív Értékelő Összefoglalás Választ adott: 44 fő A válaszok megoszlása a válaszolók munkahelye szerint Személyre szabott orvoslás fogalma Kérdőív meghatározása:
GNTP Személyre Szabott Orvoslás (SZO) Munkacsoport Kérdőív Értékelő Összefoglalás Választ adott: 44 fő A válaszok megoszlása a válaszolók munkahelye szerint Személyre szabott orvoslás fogalma Kérdőív meghatározása:
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
OncotypeDX az emlőrák kezelésében
 OncotypeDX az emlőrák kezelésében Dr. Nagy Zoltán Med Gen-Sol Kft. Szenológiai Kongresszus Kecskemét 2018. 04. 13-14. Slide 1 Az Oncotype DX korai emlőrák teszt 16 tumorral kapcsolatos gén Ösztrogén csoprt
OncotypeDX az emlőrák kezelésében Dr. Nagy Zoltán Med Gen-Sol Kft. Szenológiai Kongresszus Kecskemét 2018. 04. 13-14. Slide 1 Az Oncotype DX korai emlőrák teszt 16 tumorral kapcsolatos gén Ösztrogén csoprt
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
OncotypeDX és más genetikai tesztek emlőrákban és azon túl. Dr. Nagy Zoltán Med Gen-Sol Kft.
 OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
OncotypeDX és más genetikai tesztek emlőrákban és azon túl Dr. Nagy Zoltán Med Gen-Sol Kft. 2 A betegek leggyakoribb kérdései! Kiújul a betegségem?! Kell kemoterápiát kapnom?! A beteg és környezete életét,
Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában. Nagy Tünde Országos Onkológiai Intézet B belosztály
 Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában Nagy Tünde Országos Onkológiai Intézet B belosztály A tüdőrák a vezető daganatos halálok USA-ban: férfiak daganatos mortalitása 1930-2000*
Pathologiai lelet értéke a tüdőrákok kezelésének megválasztásában Nagy Tünde Országos Onkológiai Intézet B belosztály A tüdőrák a vezető daganatos halálok USA-ban: férfiak daganatos mortalitása 1930-2000*
Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán
 Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán Dr. Gelencsér Viktória, Dr. Boér Katalin Szent Margit Kórház, Onkológiai
Metasztatikus HER2+ emlőrák kezelése: pertuzumab-trasztuzumab és docetaxel kombinációval szerzett tapasztalataink esetismertetés kapcsán Dr. Gelencsér Viktória, Dr. Boér Katalin Szent Margit Kórház, Onkológiai
Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére
 MTA Doktori Pályázat TÉZISEK Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére Dr. Győrffy Balázs, PhD Budapest, 2013 1
MTA Doktori Pályázat TÉZISEK Transzkriptom szintű adatok alkalmazása a rosszindulatú daganatos betegek várható terápiás válaszának és túlélésének előrejelzésére Dr. Győrffy Balázs, PhD Budapest, 2013 1
Daganatok Kezelése. Bödör Csaba. I. sz. Patológiai és Kísérleti Rákkutató Intézet november 30., ÁOK, III.
 Daganatok Kezelése Bödör Csaba I. sz. atológiai és Kísérleti Rákkutató Intézet 2017. november 30., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu Daganatok kezelése: Terápiás modalitások Sebészi kezelés
Daganatok Kezelése Bödör Csaba I. sz. atológiai és Kísérleti Rákkutató Intézet 2017. november 30., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu Daganatok kezelése: Terápiás modalitások Sebészi kezelés
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
Új utak az antipszichotikus gyógyszerek fejlesztésében
 Új utak az antipszichotikus gyógyszerek fejlesztésében SCHIZO-08 projekt Dr. Zahuczky Gábor, PhD, ügyvezető igazgató UD-GenoMed Kft. Debrecen, 2010. november 22. A múlt orvostudománya Mindenkinek ugyanaz
Új utak az antipszichotikus gyógyszerek fejlesztésében SCHIZO-08 projekt Dr. Zahuczky Gábor, PhD, ügyvezető igazgató UD-GenoMed Kft. Debrecen, 2010. november 22. A múlt orvostudománya Mindenkinek ugyanaz
Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9
 Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9 dr Kollár György Elvárás az egészségügytől Több hatékonyabb és biztonságosabb gyógyszer legyen elérhető 80 Kezelésre válaszolók
Roche Personalised Healthcare Megfelelő kezelést az egyénnek 2009 szeptember 9 dr Kollár György Elvárás az egészségügytől Több hatékonyabb és biztonságosabb gyógyszer legyen elérhető 80 Kezelésre válaszolók
Mellékhatás menedzsment költségének változása az onkoterápia fejlődésével nem-kissejtes tüdőrák esetében
 Mellékhatás menedzsment költségének változása az onkoterápia fejlődésével nem-kissejtes tüdőrák esetében 2017. 06. 23. BERKI JÚLIA 1, VÁRNAI MÁTÉ 1, DR. RUMSZAUER ÁGNES 1, DR. GERENCSÉR ZSOLT 1, RÓZSA
Mellékhatás menedzsment költségének változása az onkoterápia fejlődésével nem-kissejtes tüdőrák esetében 2017. 06. 23. BERKI JÚLIA 1, VÁRNAI MÁTÉ 1, DR. RUMSZAUER ÁGNES 1, DR. GERENCSÉR ZSOLT 1, RÓZSA
BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben
 Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
SZEMÉLYRE SZABOTT ORVOSLÁS II.
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 SZEMÉLYRE SZABOTT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 SZEMÉLYRE SZABOTT
A tüdőrák agyi metasztázisainak komplex kezelése az onkopulmonológus szemszögéből
 A tüdőrák agyi metasztázisainak komplex kezelése az onkopulmonológus szemszögéből Ostoros Gyula Országos Korányi TBC és Pulmonológiai Intézet 2007. október 6. Az onkológia jelenlegi legnagyobb kihívása
A tüdőrák agyi metasztázisainak komplex kezelése az onkopulmonológus szemszögéből Ostoros Gyula Országos Korányi TBC és Pulmonológiai Intézet 2007. október 6. Az onkológia jelenlegi legnagyobb kihívása
A tüdő adenocarcinomák szubklasszifikációja. Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5.
 A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
Modern terápiás szemlélet az onkológiában
 Modern terápiás szemlélet az onkológiában Dr. Horváth Anna Semmelweis Egyetem, III.Belgyógyászati Klinika Haemato-Onkológiai osztály Budapest, 1125. Kútvölgyi út 4. TERÁPIÁS SZEMLÉLET VÁLTOZÁSA AZ ONKOLÓGIÁBAN?
Modern terápiás szemlélet az onkológiában Dr. Horváth Anna Semmelweis Egyetem, III.Belgyógyászati Klinika Haemato-Onkológiai osztály Budapest, 1125. Kútvölgyi út 4. TERÁPIÁS SZEMLÉLET VÁLTOZÁSA AZ ONKOLÓGIÁBAN?
Dózis Gyógyszerforma Alkalmazási mód Tartalom (koncentráció) megnevezés. engedély jogosultja
 I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZIS, ALKALMAZÁSI MÓD, KÉRELMEZŐ ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN Tagállam Forgalomba hozatali engedély
I. MELLÉKLET FELSOROLÁS: MEGNEVEZÉS, GYÓGYSZERFORMA, GYÓGYSZERKÉSZÍTMÉNY- DÓZIS, ALKALMAZÁSI MÓD, KÉRELMEZŐ ÉS A FORGALOMBA HOZATALI ENGEDÉLY JOGOSULTJA A TAGÁLLAMOKBAN Tagállam Forgalomba hozatali engedély
Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése
 Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése Dr. Kerpel-Fronius Sándor Egyetemi tanár Farmakológiai és Farmakoterápiás Tanszék Semmelweis Egyetem Budapest Email: kerfro@pharma.sote.hu
Rosszindulatú daganatok célzott, molekuláris gyógyszeres kezelése Dr. Kerpel-Fronius Sándor Egyetemi tanár Farmakológiai és Farmakoterápiás Tanszék Semmelweis Egyetem Budapest Email: kerfro@pharma.sote.hu
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA. Dr. Győrffy Balázs
 A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
2. SZ. SZAKMAI ÖSSZEFOGLALÓ PIR 2
 Az Országos Onkológiai Intézet Norvég Finanszírozási mechanizmus keretében elnyert Kutatás Fejlesztési Pályázata Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon
Az Országos Onkológiai Intézet Norvég Finanszírozási mechanizmus keretében elnyert Kutatás Fejlesztési Pályázata Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon
Rovarméreg (méh, darázs) - allergia
 Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
OncotypeDX Korai emlőrák és a genetika biztosan mindent tudunk betegünkről a helyes terápia megválasztásához? Boér Katalin
 OncotypeDX Korai emlőrák és a genetika biztosan mindent tudunk betegünkről a helyes terápia megválasztásához? Boér Katalin Korai HR+, HER2- emlőrák kezelése ormonterápia emoterápia - előnye 4,4% lasszikus
OncotypeDX Korai emlőrák és a genetika biztosan mindent tudunk betegünkről a helyes terápia megválasztásához? Boér Katalin Korai HR+, HER2- emlőrák kezelése ormonterápia emoterápia - előnye 4,4% lasszikus
Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió
 Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió összefüggései Szentmártoni Gy., Zergényi É., Torgyík L., Tóth A., Szita A., Dank M. SE Radiológiai és Onkoterápiás
Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió összefüggései Szentmártoni Gy., Zergényi É., Torgyík L., Tóth A., Szita A., Dank M. SE Radiológiai és Onkoterápiás
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése
 Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Férfiemlőrák. Dr Kocsis Judit
 Férfiemlőrák Dr Kocsis Judit Bevezetés Ritka Összes emlőrák kevesebb, mint 1%-a (11% in situ-seer) Összes férfi malignitás kevesebb, mint 1%-a Gyakran előrehaladottabb stádiumban kerül felfedezésre Idősebb
Férfiemlőrák Dr Kocsis Judit Bevezetés Ritka Összes emlőrák kevesebb, mint 1%-a (11% in situ-seer) Összes férfi malignitás kevesebb, mint 1%-a Gyakran előrehaladottabb stádiumban kerül felfedezésre Idősebb
Genomikai Medicina és Ritka Betegségek Intézete Semmelweis Egyetem
 Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
S atisztika 2. előadás
 Statisztika 2. előadás 4. lépés Terepmunka vagy adatgyűjtés Kutatási módszerek osztályozása Kutatási módszer Feltáró kutatás Következtető kutatás Leíró kutatás Ok-okozati kutatás Keresztmetszeti kutatás
Statisztika 2. előadás 4. lépés Terepmunka vagy adatgyűjtés Kutatási módszerek osztályozása Kutatási módszer Feltáró kutatás Következtető kutatás Leíró kutatás Ok-okozati kutatás Keresztmetszeti kutatás
A.) Biopsziás mintavétel lehetőségei és a biopsziás anyagok kezelésével kapcsolatos tudnivalók.
 II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
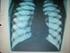 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
HORMONKEZELÉSEK. A hormonkezelés típusai
 HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
OPPONENSI VÉLEMÉNY. Dr. Lakatos Péter László köztestületi azonosító: 15893 az MTA Doktora cím elnyerése érdekében benyújtott,
 OPPONENSI VÉLEMÉNY Dr. Lakatos Péter László köztestületi azonosító: 15893 az MTA Doktora cím elnyerése érdekében benyújtott, GENETIKAI, SZEROLÓGIAI ÉS KLINIKAI TÉNYEZŐK SZEREPE A GYULLADÁSOS BÉLBETEGSÉGEK
OPPONENSI VÉLEMÉNY Dr. Lakatos Péter László köztestületi azonosító: 15893 az MTA Doktora cím elnyerése érdekében benyújtott, GENETIKAI, SZEROLÓGIAI ÉS KLINIKAI TÉNYEZŐK SZEREPE A GYULLADÁSOS BÉLBETEGSÉGEK
EGFR-tirozinkináz-inhibitorok alkalmazása tüdőrákban: szenzitivitás és rezisztencia
 38 Gyógyszergyári közlemény EGFR-tirozinkináz-inhibitorok alkalmazása tüdőrákban: szenzitivitás és rezisztencia Moldvay Judit 1, Peták István 2,3 1 Semmelweis Egyetem Pulmonológiai Klinika, 2 Semmelweis
38 Gyógyszergyári közlemény EGFR-tirozinkináz-inhibitorok alkalmazása tüdőrákban: szenzitivitás és rezisztencia Moldvay Judit 1, Peták István 2,3 1 Semmelweis Egyetem Pulmonológiai Klinika, 2 Semmelweis
1122 Budapest, Ráth Gy. u. 7-9. 1149 Budapest, Pillangó park 12/d.
 Magyar Onkológusok Gyógyszerterápiás Tudományos Társasága (MAGYOT) Tudományos Szimpóziuma Budapest, Danubius Hotel Flamenco 2013. május 9-11. PROGRAM 2013. május 9. (csütörtök) 14.00 Ebéd 16.00 16.10 Megnyitó
Magyar Onkológusok Gyógyszerterápiás Tudományos Társasága (MAGYOT) Tudományos Szimpóziuma Budapest, Danubius Hotel Flamenco 2013. május 9-11. PROGRAM 2013. május 9. (csütörtök) 14.00 Ebéd 16.00 16.10 Megnyitó
A 22C3 PD-L1 tesztek értékelése intézetünkben. Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs
 A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A terápiaeredményesség kockázatának átvétele, megosztása
 A terápiaeredményesség kockázatának átvétele, megosztása Dr. Bidló Judit Főosztályvezető Döntéshozói dilemma Klinikai vizsgálatok eredményei Hatásosság Biztonság Tolrálhatóság Életminőség Gazdasági kérdések
A terápiaeredményesség kockázatának átvétele, megosztása Dr. Bidló Judit Főosztályvezető Döntéshozói dilemma Klinikai vizsgálatok eredményei Hatásosság Biztonság Tolrálhatóság Életminőség Gazdasági kérdések
A Ritka Betegség Regiszterek szerepe a klinikai kutatásban Magyarósi Szilvia (SE, Genomikai Medicina és Ritka Betegségek Intézete)
 A Ritka Betegség Regiszterek szerepe a klinikai kutatásban Magyarósi Szilvia (SE, Genomikai Medicina és Ritka Betegségek Intézete) I. Ritka Betegség regiszterek Európában II. Ritka betegség regiszterek
A Ritka Betegség Regiszterek szerepe a klinikai kutatásban Magyarósi Szilvia (SE, Genomikai Medicina és Ritka Betegségek Intézete) I. Ritka Betegség regiszterek Európában II. Ritka betegség regiszterek
I. melléklet. Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása
 I. melléklet Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések,
I. melléklet Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések,
Esetbemutatás. Dr. Iván Mária Uzsoki Kórház 2013.11.07.
 Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
ALK+ tüdőrák a klinikai gyakorlatban. Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest
 ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
ALK+ tüdőrák a klinikai gyakorlatban Dr. Ostoros Gyula Országos Korányi Pulmonológiai Intézet Budapest Előadói megjegyzés Az előadás az előadó független szakmai véleményét tükrözi, ami nem feltétlenül
KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS
 KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS 1. Daganatos morbiditás és mortalitás Magyarországon 2. Kémiai és fizikai tényezők szerepe a daganatok kialakulásában
KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS 1. Daganatos morbiditás és mortalitás Magyarországon 2. Kémiai és fizikai tényezők szerepe a daganatok kialakulásában
1. Adatok kiértékelése. 2. A feltételek megvizsgálása. 3. A hipotézis megfogalmazása
 HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház. Emlő MR vizsgálatok korai eredményei kórházunkban
 DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekbe
 Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekben a korcsoportokban ez a leggyakoribb daganatos halálozási
Bár az emlőrák elsősorban a posztmenopauzális nők betegsége, a betegek mintegy 5,5%-a 40 évesnél, 2%-a 35 évesnél fiatalabb a diagnózis idején. Ezekben a korcsoportokban ez a leggyakoribb daganatos halálozási
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere
 I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
GYORSTESZTEK ALKALMAZÁSA A
 GYORSTESZTEK ALKALMAZÁSA A GYÓGYSZERTÁRAKBAN DR. MISETA ILDIKÓ GÖLLE, SZENT ISTVÁN GYÓGYSZERTÁR Rozsnyay Mátyás emlékverseny Debrecen, 2012. május 10-12. BEVEZETÉS - CÉLKITŰZÉS Miért kell a gyorstesztekkel
GYORSTESZTEK ALKALMAZÁSA A GYÓGYSZERTÁRAKBAN DR. MISETA ILDIKÓ GÖLLE, SZENT ISTVÁN GYÓGYSZERTÁR Rozsnyay Mátyás emlékverseny Debrecen, 2012. május 10-12. BEVEZETÉS - CÉLKITŰZÉS Miért kell a gyorstesztekkel
MAGYAR ONKOLÓGUSOK GYÓGYSZERTERÁPIÁS TUDOMÁNYOS TÁRSASÁGA ÉVI SZIMPÓZIUMA
 MAGYAR ONKOLÓGUSOK GYÓGYSZERTERÁPIÁS TUDOMÁNYOS TÁRSASÁGA 2017. ÉVI SZIMPÓZIUMA PROGRAM KIVONAT Radisson Blu Béke Hotel - 1067 Budapest, Teréz krt. 43. 1. NAP 2017. MÁJUS 5. (PÉNTEK) 08.30 17.00 Regisztráció
MAGYAR ONKOLÓGUSOK GYÓGYSZERTERÁPIÁS TUDOMÁNYOS TÁRSASÁGA 2017. ÉVI SZIMPÓZIUMA PROGRAM KIVONAT Radisson Blu Béke Hotel - 1067 Budapest, Teréz krt. 43. 1. NAP 2017. MÁJUS 5. (PÉNTEK) 08.30 17.00 Regisztráció
MAGYOT PROGRAMJA In memoriam Horti József dr. A prosztatadaganatok kezelése
 MAGYOT 2011. PROGRAMJA 2011. MÁJUS. 20. Péntek. 09. 30. Megnyitó, köszöntések: Dr. Géczi Lajos Dr. Cseh József Védnökök: Prof. Dr. Oláh Edit Prof. Dr. Kásler Miklós Prof. Dr. Eckhardt Sándor 09. 50. In
MAGYOT 2011. PROGRAMJA 2011. MÁJUS. 20. Péntek. 09. 30. Megnyitó, köszöntések: Dr. Géczi Lajos Dr. Cseh József Védnökök: Prof. Dr. Oláh Edit Prof. Dr. Kásler Miklós Prof. Dr. Eckhardt Sándor 09. 50. In
Áttekintő. Citotoxikus vs. célzott terápia. RAS jelátvitel. Onkogén-addikció. Célzott terápiás gyógyszerek (2013) 2014.11.12.
 Áttekintő Tumorprogresszió és előrejelzése Dr. Győrffy Balázs 1. RAS + Erbb család 2. Érújdonképződés- VEGF 3. 4. Biomarkerek RAS Mellékhetások 5. Heterogenitás 6. Összefoglalás Citotoxikus vs. célzott
Áttekintő Tumorprogresszió és előrejelzése Dr. Győrffy Balázs 1. RAS + Erbb család 2. Érújdonképződés- VEGF 3. 4. Biomarkerek RAS Mellékhetások 5. Heterogenitás 6. Összefoglalás Citotoxikus vs. célzott
Hivatalos bírálat Dr. Antus Balázs: A légúti gyulladás és az oxidatív stressz vizsgálata tüdőbetegségekben című MTA doktori értekezéséről
 Hivatalos bírálat Dr. Antus Balázs: A légúti gyulladás és az oxidatív stressz vizsgálata tüdőbetegségekben című MTA doktori értekezéséről Jelölt a fenti címen MTA doktori értekezést nyújtott be a Magyar
Hivatalos bírálat Dr. Antus Balázs: A légúti gyulladás és az oxidatív stressz vizsgálata tüdőbetegségekben című MTA doktori értekezéséről Jelölt a fenti címen MTA doktori értekezést nyújtott be a Magyar
San Antonio Breast Cancer Symposium. Dr. Tőkés Tímea
 San Antonio Breast Cancer Symposium Dr. Tőkés Tímea San Antonio, Texas, USA Henry B. Gonzalez Convention Center December 10-14, 2013 SABCS 2013 Több, mint 7500 résztvevő, több, mint 70 országból Továbbképzések,
San Antonio Breast Cancer Symposium Dr. Tőkés Tímea San Antonio, Texas, USA Henry B. Gonzalez Convention Center December 10-14, 2013 SABCS 2013 Több, mint 7500 résztvevő, több, mint 70 országból Továbbképzések,
Caronax - 4 féle gombakivonatot tartalmazó étrend-kiegészítő
 Caronax - 4 féle gombakivonatot tartalmazó étrend-kiegészítő Tisztelettel köszöntöm a kedves érdeklődőt! A Max-Immun Kft. 2013 júliusában bízta meg cégünket az angliai székhelyű Bujtar Medical Ltd.-t (Company
Caronax - 4 féle gombakivonatot tartalmazó étrend-kiegészítő Tisztelettel köszöntöm a kedves érdeklődőt! A Max-Immun Kft. 2013 júliusában bízta meg cégünket az angliai székhelyű Bujtar Medical Ltd.-t (Company
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban
 mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
mtorc1 and C2 komplexhez köthető aktivitás különbségek és ennek jelentősége humán lymphomákbanés leukémiákban Sebestyén A, Márk Á, Nagy N, Hajdu M, Csóka M*, SticzT, Barna G, Nemes K*, Váradi Zs*, KopperL
Finanszírozott indikációk:
 Bevacizumab Finanszírozott indikációk: 1. Inoperábilis előrehaladott, metasztatikus vagy kiújuló tüdő adenocarcinoma elsővonalbeli kezelése platinaalapú kemoterápiával kombinációban, majd azt követően
Bevacizumab Finanszírozott indikációk: 1. Inoperábilis előrehaladott, metasztatikus vagy kiújuló tüdő adenocarcinoma elsővonalbeli kezelése platinaalapú kemoterápiával kombinációban, majd azt követően
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Hipotézis STATISZTIKA. Kétmintás hipotézisek. Munkahipotézis (H a ) Tematika. Tudományos hipotézis. 1. Előadás. Hipotézisvizsgálatok
 STATISZTIKA 1. Előadás Hipotézisvizsgálatok Tematika 1. Hipotézis vizsgálatok 2. t-próbák 3. Variancia-analízis 4. A variancia-analízis validálása, erőfüggvény 5. Korreláció számítás 6. Kétváltozós lineáris
STATISZTIKA 1. Előadás Hipotézisvizsgálatok Tematika 1. Hipotézis vizsgálatok 2. t-próbák 3. Variancia-analízis 4. A variancia-analízis validálása, erőfüggvény 5. Korreláció számítás 6. Kétváltozós lineáris
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek?
 Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Daganat immunterápia molekuláris markereinek tanulmányozása biofizikai módszerekkel. Áramlási és képalkotó citometria
 Daganat immunterápia molekuláris markereinek tanulmányozása biofizikai módszerekkel. Áramlási és képalkotó citometria Szöllősi János, Vereb György Biofizikai és Sejtbiológiai Intézet Orvos- és Egészségtudományi
Daganat immunterápia molekuláris markereinek tanulmányozása biofizikai módszerekkel. Áramlási és képalkotó citometria Szöllősi János, Vereb György Biofizikai és Sejtbiológiai Intézet Orvos- és Egészségtudományi
III./5. GIST. Bevezetés. A fejezet felépítése. A.) Panaszok. B.) Anamnézis. Pápai Zsuzsanna
 III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
A, B, C, D, E a vállalat vizsgált termékei
 c) Vállalati versenyképesség-elemzés Az EU-felkészülésnek egyik kulcskérdése érthetô módon a versenyképesség. Minden olyan elemzési, tervezési módszer, vállalatirányítási és vezetési technika (és ennek
c) Vállalati versenyképesség-elemzés Az EU-felkészülésnek egyik kulcskérdése érthetô módon a versenyképesség. Minden olyan elemzési, tervezési módszer, vállalatirányítási és vezetési technika (és ennek
III./8.3. Lokálisan előrehaladott emlőrák. A fejezet felépítése
 III./8.3. Lokálisan előrehaladott emlőrák Kocsis Judit A fejezet célja, hogy megismerje a hallgató a helyileg előrehaladott emlődaganat fogalmát, diagnózisát és a terápiás lehetőségeket. A fejezet teljesítését
III./8.3. Lokálisan előrehaladott emlőrák Kocsis Judit A fejezet célja, hogy megismerje a hallgató a helyileg előrehaladott emlődaganat fogalmát, diagnózisát és a terápiás lehetőségeket. A fejezet teljesítését
A köpenysejtes limfómákról
 A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
A köpenysejtes limfómákról Dr. Schneider Tamás Országos Onkológiai Intézet Lymphoma Centrum Limfóma Világnap 2014. szeptember 15. Limfómám van! Limfómám van! Igen? De milyen típusú? Gyógyítható? Nem gyógyítható?
Diagnózis és prognózis
 Diagnózis, prognózis Általános vizsgálat Diagnózis és prognózis Fizikális vizsgálat Endoszkópia Képalkotás Sebészi feltárás A kezelés megválasztása Specifikus elemzés Kórszövettan/citológia Klinikai kémia
Diagnózis, prognózis Általános vizsgálat Diagnózis és prognózis Fizikális vizsgálat Endoszkópia Képalkotás Sebészi feltárás A kezelés megválasztása Specifikus elemzés Kórszövettan/citológia Klinikai kémia
Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet)
 Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet) I. Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist az ép
Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet) I. Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist az ép
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL
 ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a écsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMO-4.1.2-08/1/A-2009-0011 Az orvosi
III./8.4. Metasztatikus emlőrák
 III./8.4. Metasztatikus emlőrák Szentmártoni Gyöngyvér, Dank Magdolna A fejezet célja, hogy megismerje a hallgató az áttétes emlőrák kezelésének főbb állomásait, az egyénre szabott optimális ellátást.
III./8.4. Metasztatikus emlőrák Szentmártoni Gyöngyvér, Dank Magdolna A fejezet célja, hogy megismerje a hallgató az áttétes emlőrák kezelésének főbb állomásait, az egyénre szabott optimális ellátást.
Bírálat Dr. Igaz Péter című MTA doktori értekezéséről
 Bírálat Dr. Igaz Péter Endokrin daganatok és immun-endokrin kölcsönhatások molekuláris, bioinformatikai és klinikai vizsgálata című MTA doktori értekezéséről Igaz Péter MTA doktori értekezését 2011-ben
Bírálat Dr. Igaz Péter Endokrin daganatok és immun-endokrin kölcsönhatások molekuláris, bioinformatikai és klinikai vizsgálata című MTA doktori értekezéséről Igaz Péter MTA doktori értekezését 2011-ben
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3,
 Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
A II. kategória Fizika OKTV mérési feladatainak megoldása
 Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Cetuximab. Finanszírozott indikációk:
 Cetuximab Finanszírozott indikációk: 1. Lokálisan előrehaladott fej-nyak carcinoma kezelésére radioterápiával kombinálva, a készítmény alkalmazása a docetaxel-tartalmú kemoterápia és cisplatin-tartalmú
Cetuximab Finanszírozott indikációk: 1. Lokálisan előrehaladott fej-nyak carcinoma kezelésére radioterápiával kombinálva, a készítmény alkalmazása a docetaxel-tartalmú kemoterápia és cisplatin-tartalmú
A függetlenül kialakuló rezisztencia vizsgálata 29 rezisztens sejtvonalon
 A függetlenül kialakuló rezisztencia vizsgálata 29 rezisztens sejtvonalon Doktori értekezés Dr. Tegze Bálint Semmelweis Egyetem Patológiai Tudományok Doktori Iskola Témavezető: Dr. Győrffy Balázs, tudományos
A függetlenül kialakuló rezisztencia vizsgálata 29 rezisztens sejtvonalon Doktori értekezés Dr. Tegze Bálint Semmelweis Egyetem Patológiai Tudományok Doktori Iskola Témavezető: Dr. Győrffy Balázs, tudományos
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
ALÁÍRÁS NÉLKÜL A TESZT ÉRVÉNYTELEN!
 A1 A2 A3 (8) A4 (12) A (40) B1 B2 B3 (15) B4 (11) B5 (14) Bónusz (100+10) Jegy NÉV (nyomtatott nagybetűvel) CSOPORT: ALÁÍRÁS: ALÁÍRÁS NÉLKÜL A TESZT ÉRVÉNYTELEN! 2011. december 29. Általános tudnivalók:
A1 A2 A3 (8) A4 (12) A (40) B1 B2 B3 (15) B4 (11) B5 (14) Bónusz (100+10) Jegy NÉV (nyomtatott nagybetűvel) CSOPORT: ALÁÍRÁS: ALÁÍRÁS NÉLKÜL A TESZT ÉRVÉNYTELEN! 2011. december 29. Általános tudnivalók:
Termék azonosítási és nyomon követési szabvány alkalmazásának előnyei az egészségügyben
 Termék azonosítási és nyomon követési szabvány alkalmazásának előnyei az egészségügyben Molnár Attila az EGVE leköszönő elnöke Az üzleti élet közös nyelve Miért van szükség egy szabványra? Értünk egymás
Termék azonosítási és nyomon követési szabvány alkalmazásának előnyei az egészségügyben Molnár Attila az EGVE leköszönő elnöke Az üzleti élet közös nyelve Miért van szükség egy szabványra? Értünk egymás
A proteomika új tudománya és alkalmazása a rákdiagnosztikában
 BIOTECHNOLÓGIAI FEJLESZTÉSI POLITIKA, KUTATÁSI IRÁNYOK A proteomika új tudománya és alkalmazása a rákdiagnosztikában Tárgyszavak: proteom; proteomika; rák; diagnosztika; molekuláris gyógyászat; biomarker;
BIOTECHNOLÓGIAI FEJLESZTÉSI POLITIKA, KUTATÁSI IRÁNYOK A proteomika új tudománya és alkalmazása a rákdiagnosztikában Tárgyszavak: proteom; proteomika; rák; diagnosztika; molekuláris gyógyászat; biomarker;
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél
 Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Expressziós microarray. Dr. Győrffy Balázs
 Expressziós microarray Dr. Győrffy Balázs Áttekintő 1. A technológia 2. Feldolgozás 2.1. Minőség-ellenőrzés 2.2. Jellemző kiválasztás 2.3. Vizualizálás 2.4. Kereszt-elemzés 2.5. Online diagnosztika 3.
Expressziós microarray Dr. Győrffy Balázs Áttekintő 1. A technológia 2. Feldolgozás 2.1. Minőség-ellenőrzés 2.2. Jellemző kiválasztás 2.3. Vizualizálás 2.4. Kereszt-elemzés 2.5. Online diagnosztika 3.
Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában
 Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában Minőségi indikátorok az analitikai szakaszban Dr. Kocsis Ibolya Semmelweis Egyetem Laboratóriumi Medicina Intézet Központi Laboratórium
Indikátorok alkalmazása a labordiagnosztikai eljárások minőségbiztosításában Minőségi indikátorok az analitikai szakaszban Dr. Kocsis Ibolya Semmelweis Egyetem Laboratóriumi Medicina Intézet Központi Laboratórium
Kulka Janina: Prediktív és prognosztikai vizsgálatok emlőkarcinómában
 Opponensi bírálat Kulka Janina: Prediktív és prognosztikai vizsgálatok emlőkarcinómában című MTA doktori értekezéséről A Doktori Értekezés témája a nőkben leggyakoribb neoplázia, az emlőrák klinikopatológiai,
Opponensi bírálat Kulka Janina: Prediktív és prognosztikai vizsgálatok emlőkarcinómában című MTA doktori értekezéséről A Doktori Értekezés témája a nőkben leggyakoribb neoplázia, az emlőrák klinikopatológiai,
Fókuszált ultrahangvizsgálat gyermekkorban
 Fókuszált ultrahangvizsgálat gyermekkorban DrGőblGergely, SE AITK II.Gyermeksürgősségi Kongresszus Budapest 2017.09.15. POCUS = Pointof careultrasound Betegágy melletti UH-vizsgálat Fókuszált UH-vizsgálat
Fókuszált ultrahangvizsgálat gyermekkorban DrGőblGergely, SE AITK II.Gyermeksürgősségi Kongresszus Budapest 2017.09.15. POCUS = Pointof careultrasound Betegágy melletti UH-vizsgálat Fókuszált UH-vizsgálat
TNBC ÚJDONSÁGOK. Dr Kocsis Judit
 TNBC ÚJDONSÁGOK Dr Kocsis Judit Előzmények Emlőrák konszenzus 2016 Metasztatikus emlődaganat kemoterápia Javallat ER és PR negativitás HER2 pozitivitás ER/PR pozitívitás, de tüneteket okozó többszervi
TNBC ÚJDONSÁGOK Dr Kocsis Judit Előzmények Emlőrák konszenzus 2016 Metasztatikus emlődaganat kemoterápia Javallat ER és PR negativitás HER2 pozitivitás ER/PR pozitívitás, de tüneteket okozó többszervi
A szűrővizsgálatok változó koncepciója
 A szűrővizsgálatok változó koncepciója Magyar Tudomány Ünnepe 2010. Vályi Péter dr. 1997. évi CLIV. törvény az egészségügyről Szűrővizsgálat: olyan vizsgálat, amelynek célja a betegség tüneteit nem mutató
A szűrővizsgálatok változó koncepciója Magyar Tudomány Ünnepe 2010. Vályi Péter dr. 1997. évi CLIV. törvény az egészségügyről Szűrővizsgálat: olyan vizsgálat, amelynek célja a betegség tüneteit nem mutató
Hotel Novotel Budapest Centrum. 2006. november 23-25. PROGRAM
 A Magyar Tüdőgyógyász Társaság Rendezvénye A TÜDŐGYÓGYÁSZAT AKTUÁLIS KÉRDÉSEI Hotel Novotel Budapest Centrum 2006. november 23-25. PROGRAM A RENDEZVÉNY TÁMOGATÓI: Boehringer Ingelheim Pharma és a Pfizer
A Magyar Tüdőgyógyász Társaság Rendezvénye A TÜDŐGYÓGYÁSZAT AKTUÁLIS KÉRDÉSEI Hotel Novotel Budapest Centrum 2006. november 23-25. PROGRAM A RENDEZVÉNY TÁMOGATÓI: Boehringer Ingelheim Pharma és a Pfizer
Az Európai Unió Tanácsa Brüsszel, december 2. (OR. en)
 Az Európai Unió Tanácsa Brüsszel, 2016. december 2. (OR. en) 15193/16 FEDŐLAP Küldi: az Európai Bizottság Az átvétel dátuma: 2016. november 30. Címzett: Biz. dok. sz.: Tárgy: a Tanács Főtitkársága D048510_01
Az Európai Unió Tanácsa Brüsszel, 2016. december 2. (OR. en) 15193/16 FEDŐLAP Küldi: az Európai Bizottság Az átvétel dátuma: 2016. november 30. Címzett: Biz. dok. sz.: Tárgy: a Tanács Főtitkársága D048510_01
Hivatalos Bírálat Dr. Gődény Mária
 Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
