Egy hexamer acilpeptid-hidroláz szerkezete, a méretszelektivitás újszerű módja
|
|
|
- Bertalan Bodnár
- 5 évvel ezelőtt
- Látták:
Átírás
1 Tudományos Diákköri Dolgozat TICHY-RÁCS ÉVA ILONA Egy hexamer acilpeptid-hidroláz szerkezete, a méretszelektivitás újszerű módja Témavezető: Harmat Veronika, Szerkezeti Kémiai és Biológiai Laboratórium Eötvös Loránd Tudományegyetem Természettudományi Kar Budapest, 2009
2 Tartalomjegyzék Bevezetés Irodalmi áttekintés Az enzimek felosztása A szerin-proteázok katalitikus mechanizmusa A Prolil-oligopeptidáz család Az acilpeptid-hidroláz alcsalád Az acilpeptid hidroláz szerkezete... 7 Célkitűzések Módszerek Fehérjekrisztallográfia Kristályosítás, adatgyűjtés Modellépítés, finomítás A szerkezet elemzése A PhAAP fehérje szerkezete A monomer felépítése A β-propeller domén A hidroláz domén szerkezete, stabilitása A PhAAP komplex felépítése A monomerek közötti kölcsönhatások A hexamer dinamikája Az aktív hely PhAAP fehérje összehasonlítása más enzimekkel A propeller domén A hidroláz domén stabilitása Összefoglalás Köszönetnyilvánítás Rövidítések Irodalomjegyzék
3 Bevezetés A fehérjék az élő szervezetek megfelelő működésében létfontosságú szerepet töltenek be. Az élő szervezetben lezajló folyamatok túlnyomó része energetikai okok miatt csak katalizátorok segítségével mehet végbe. Ilyen katalizátor szerepet töltenek be az enzimek, melyek speciális funkciójú fehérjék. Az enzimek tanulmányozása fontos az emberi test és más szervezetek működésének legjobb megismeréséhez, és segítségünkre lehet az esetleges problémák orvoslásához. A szerkezet-meghatározás nagyon sokat segíthet a reakciómechanizmusok felderítésében, hiszen a 3D szerkezet, a fehérje konformációja determinálja, hogy az enzim milyen biológiai funkciót tud ellátni. Az elmúlt évtizedben hihetetlen mértékben fejlődtek a makromolekulák térszerkezetének meghatározásához alkalmazott módszerek, és meredeken nő az ismert szerkezetek száma, mely segítségünkre lehet a mai tudomány számos területén. E dolgozat témája is egy ilyen fontos, néhány éve felfedezett fehérje, az acilaminoacilpeptidáz (AAP) szerkezetének meghatározása és elemzése. Az AAP fehérje a szerinpeptidázokon belül a prolil-oligopeptidáz (POP) családba tartozik. Biológiai szerepe és jelentősége az, hogy katalizálja bizonyos oligopeptidek N-terminálisán lévő acilezett aminosav lehasítását, így részt vesz a peptidhormonok és a neuropeptidek szintjének szabályozásában. Ezenkívül kapcsolatba hozható egyes rákfajtákkal, valamint egyik célpontja a memórianövelő gyógyszerek kutatásának is. A Pyrococcus horikoshii nevű, termofil ősbaktériumból származó AAP fehérjét (PhAAP) E. coli baktériumban fejezték ki a, majd tisztítás után került az ELTE fehérjekrisztallográfiai laboratóriumába. Kristályosítás után a hamburgi szinkrotronban végezték a röntgendiffrakciós méréseket b, melyeknek a kiértékelésében vettem részt. Ez alapján vizsgáltam a fehérje egyedi, eddig ismert szerkezeteknél nem tapasztalt felépítését, ami a méretszelektivitást újszerű módon befolyásolja. Ezen kívül vizsgáltam a PhAAP fehérje egyéb sajátosságait a POP enzimcsaládon belül, illetve ennek a családnak az α/β hidroláz klánon belüli hasonlóságait és eltéréseit. a Polgár László professzor csoportja, MTA Enzimológiai Intézet b Harmat Veronika, ELTE Fehérjekrisztallográfiai Laboratórium 3
4 1. Irodalmi áttekintés 1.1. Az enzimek felosztása Az enzimeket hat nagy csoportra osztják az általuk katalizált reakciók alapján [1]. Az oxidoreduktázok egyik biomolekula redukálása közben egy másikat oxidálnak. Azokat az enzimeket, amelyek funkciós csoportokat visznek át egyik molekuláról a másikra, transzferázoknak nevezzük. A hidrolázok észter-, éter- vagy amidkötést bontanak el hidrolízissel. Ezek közé tartoznak az általunk tanulmányozott enzimcsalád tagjai is. A liázok vagy szintázok szubsztrátjaikon kettőskötéseket alakítanak ki. A testben lévő molekulák belső szerkezeti átalakulását (izomerizációját) az izomerázok segítik elő. A ligázok vagy szintetázok nagyenergiájú szintéziseket hajtanak végre. Egy-egy családot aszerint oszthatunk fel újabb csoportokra, hogy milyen szubsztrátok vesznek részt a reakcióban. E szempont szerint a hidrolázokat négy csoport alkotja: az észterspecifikus lipázok, a glikozidos kapcsolatokat hasító amilázok, a nukleinsavak foszfodiészterkötéseit hidrolizáló nukleázok és az amidkötéseket bontó proteázok. A proteázok fehérjéket, polipeptideket vagy módosult aminosav-származékokat hidrolizálnak kisebb molekulákká. A proteázokat reaktív csoportjukat alkotó aminosavak szerint négy családra választjuk szét: a szerin-proteázokra, a cisztein-proteázokra, illetve a metallo- és az aszparaginsav-proteázokra. Ez utóbbi kettőből egyelőre kevésnek határozták meg a szerkezetét, a legnagyobb irodalma a szerinnel katalizáló enzimcsaládnak van. A fenti fő csoportok másféle felosztása a szerkezet/feltekeredés szerint tesz különbséget. Az általunk vizsgált POP enzimek hidroláz doménje amint arról még szó esik egy központi β-redőből és a körülötte elhelyezkedő α-hélixekből áll, így az α/β hidroláz feltekeredés (α/β hidrolase fold) névre hallgató klán tagja [2]. Ez a klán 58 tagot számlál, melyek között különböző hidrolázok szerepelnek lipázok, észterázok, proteázok. A proliloligopeptidáz család tehát egyrészt a szerin-proteázok, másrészt az α/β hidroláz klán tagja A szerin-proteázok katalitikus mechanizmusa A mechanizmus [1] kezdő lépése az, hogy a szubsztrát beköt az enzim megfelelő szubsztrátkötő helyére, melyet a katalitikus triád (Asp, His, Ser) határoz meg. A hasadó kötéstől számítva a peptid N-terminálisa felé az aminosavak a P1, P2 jelölést kapják, amelyek rendre az S1, S2, S3, kötőzsebekbe kötődnek. A hasadó kötéstől a peptid C-terminálisa felé haladva a P1', P2' stb. aminosavak az S1', S2' helyekre kötnek. A szubsztrát optimális 4
5 pozícióban való stabilizálása a katalízis szempontjából rendkívül fontos, ezért az S1 zseb határozza meg az enzim elsődleges specificitását (1. ábra). 1. ábra: Aktív hely és szubsztrátkötő hely a szerin-proteázokban A katalitikus triád a névadó szerin, valamint az aszparaginsav és a hisztidin. A bekötés után a szerin hidroxil-csoportja nukleofil támadást intéz a peptid karbonil-csoportja ellen, ezáltal kovalens kötés jön létre a szubsztrát és a szerin között, létrehozva ezzel egy negatív töltésű, átmeneti, a volt karbonil szén körül tetraéderes konfigurációjú oxianiont. A hidroxiloldallánc disszociáló hidrogénjét a hisztidin köti meg. Az aszparaginsav polarizáló hatása segíti elő ezt a folyamatot. Az oxianion komplexet a volt karbonil oxigénjén keresztül két főláncbeli amid-hidrogén hidrogénkötésekkel stabilizál. A hidrogéndonor aminosavak alkotta szerkezeti elrendeződés az oxianion-kötő zseb. Az átmenet állapot felbomlásával kialakul az acil-enzim komplex, amelyben a P1 aminosav a szerinhez észterkötéssel kapcsolódik. Ennek a felbomlását és az enzim regenerálódását hasonló módon egy vízmolekula nukleofil támadása indítja el A Prolil-oligopeptidáz család A családot 1991-ben azonosították, amikor a prolil oligopeptidáz, a dipeptidil-peptidáz IV és az aminoacil-peptidáz aminosavsorrendjét összehasonlították [3]. Még ez évben Kanatani és munkatársai által proteáz II néven leírt oligopeptidáz B [4] lett az alapító fehérjék negyedik tagja. A csoportot több hasonló fehérjével együtt S9 családnak nevezték el [5], amely szerkezeti jellemzői alapján a szerin-proteázok SC klánjába tartoznak, azaz karboxipeptidázok, és a katalitikus triádot a szerin, a hisztidin és az aszparaginsav alkotja. A 5
6 katalitikus domén vizsgálatakor kiderült, hogy ez a család más jellegű fehérjékkel együtt például egyes lipázokkal, harmadlagos szerkezetét (feltekeredését) tekintve az α/βhidrolázokhoz tartozik [6]. A prolil-oligopeptidáz család tagjai a szerin-peptidáz csoport más családjaitól több ponton lényegesen eltérnek. A szerin-proteázok általános kda-os molekulatömegéhez képest a prolil-oligopeptidázoké ennek három-négyszerese, azaz kda, továbbá szintézisük során nem előenzim, hanem rögtön az aktív alak keletkezik [7]. A méretbeli anomáliánál is fontosabb újszerű szerkezetük. A monomer enzim két fő részből tevődik össze, a hidroláz és a β-propeller doménből. A harmadik megkülönböztető jegy az, hogy az enzimcsalád tagjai nem tudnak harminc aminosavnál hosszabb láncokat lebontani [7,8]. Ennek fontos következményei vannak: a méret-korlát megakadályozza a fehérjék esetleges lebontását, ezáltal az önemésztést is Az acilpeptid-hidroláz alcsalád A prolil-oligopeptidázok családjának negyedik ágát az acilpeptid hidrolázok, vagy más néven acilaminoacil peptidázok (AAP) alkotják, amelyek az N-terminusról acilezett aminosavakat hasítanak le [8], miáltal egy rövidebb, de szabad végű polipeptid keletkezik. Az eltávolított acilező csoport lehet szerves formil, acetil, kloroacetil, vagy éppen szervetlen, például foszfát [9]. Számos eukarióta élőlényben találtak AAP fehérjéket. A patkányból a sertésből és az emberből nyert tetramer enzimek teljes szekvenciáját meghatározták [10, 11, 12]. Mindegyik 732 aminosav hosszú, szerkezetük kilencven százalékban azonos és a katalitikus aminosavak helyei is megegyeznek [6, 7]. Miután kiderült, hogy az emberben is előforduló egyes foszfátészter típusú ingerületátvivő anyagok a fehérje specifikus szubsztrátjai [13], feltételezhetjük, hogy az enzim hasonló szerepet játszik a tudat kémiai folyamataiban, mint az acetilkolinészteráz [14]. Az acilpeptid hidroláz alcsalád képes a β-endorfin és más biológiailag aktív peptidek bontásával részt vesz azok testbéli koncentrációjának szabályozásában [15]. Az AAP termelésének csökkenése sok esetben együtt jár a tüdőben és vesében lévő, kissejtes rosszindulatú daganatok kialakulásával [16]. Mindezen funkciói miatt szerkezetének és működési mechanizmusának megismerése gyógyászati jelentőségű lehet. 6
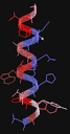
7 1.5. Az acilpeptid hidroláz szerkezete Az AAP fehérjék közül eddig egynek ismert a szerkezete, mely az Aeropyrum Pernix nevű termofil ősbaktériumból származik (ApAAP). A monomeren belül két domén található. Egyik a β-propeller domén, amely hét darab, egyenként négy antiparallel β-szálat tartalmazó lapátból áll. Ez a szerkezet sokféle funkciójú fehérjében előfordul. A POP család fehérjéiben az első és az utolsó lapát között nincs kovalens kapcsolat. A propellerben és a két domén között dinamikus mozgásra van lehetőség. Általában ez biztosítja az enzim belsejébe jutó peptidek méret szerinti szelektivitását. Másik a hidroláz domén, amelyben a központi nyolc β- szál körül α-hélixek helyezkednek el. Ezen belül a szélső β-szál után helyezkedik el a katalitikus triád (ApAAP: Ser445, Asp524, His556) hisztidinje. Az aktív hely a monomer belsejében van, így ebben a formában nem hozzáférhető, hanem a két doménnek oldatban szét kell nyílnia, hogy a szubsztrát be tudjon jutni. Az ApAAP enzim szimmetrikus homodimer, amelyben a két hidroláz domén úgy kapcsolódik, hogy a két β-élnél illeszkedve folytonos β-redőt képeznek (2. ábra). a) b) 2. ábra: Az ApAAP enzim szerkezete. a) A két monomer hidroláz doménje úgy illeszkedik, hogy folytonos β-redő jön létre. b) A szubsztrát (magenta színnel) csak a két domén szétnyílásával juthat be a katalitikus helyhez (metszeti kép). 7
8 Célkitűzések Az acilaminoacil peptidázok a POP családon belül nem túl rég lettek önálló csoportként elkülönítve. Az eddigi egyetlen meghatározott szerkezetű Aeropyrum Pernix ősbaktériumból származó enzim két monomerből áll, míg az általunk vizsgált Pyrococcus Horikoshii eredetű fehérje az első ismert hexamer szerkezetű. Emlősfehérjéből egyelőre még nem sikerült jól szóró AAP kristályt készíteni. Ezeknek a szekvenciája a hidroláz doméneket összevetve mintegy 25%-ban hasonlít az ősbaktériumokból származó enzimekéhez ez makromolekulás meghatározásnál elég nagy egyezésnek számít. Szerkezetükről annyi ismert, hogy tetramereket alkotnak. Ha sikerül megismernünk rokon fehérjék szerkezetét és működési mechanizmusát, akkor közelebb kerülhetünk az orvosi szempontból legfontosabbnak számító, ám közvetlenül nem vizsgálható emlősfehérje leírásához. 8
9 2. Módszerek 2.1. Fehérjekrisztallográfia Kristályosítás, adatgyűjtés A molekulák szerkezetéről, atomjaik pontos térbeli helyzetéről röntgendiffrakciós módszerrel nyerhetünk információt. A diffrakció jelenségének alapja a sugárzás rugalmas kölcsönhatása az anyaggal. Jelen esetben a röntgensugár szóródik az atomok elektronfelhőjén, ezt detektáljuk a diffrakciós képen, melyből a tárgy képét Fourier-transzformációval számítjuk, számítógép segítségével. Ennek eredményeként a molekulák elektronsűrűségi függvényét kapjuk. 3. ábra: A függőcsepp módszer A cseppben lévő kicsapószer koncentráció hígabb mint a kristályosító oldatban. A két oldat gőznyomása kiegyenlítődik, miközben a csepp fehérjére nézve lassan töményedik. A Pyrococcus horikoshii ősbaktériumból származó fehérjét E. Coli baktériumban fejezték ki, és tisztítás után került az ELTE fehérjekrisztallográfiai laboratóriumába. A kristályosítást a CrystalScreen II (Hampton Research) 39. számú elegyéből kiindulva függőcsepp módszerrel végezték (0. ábra). Ez a körülmény úgy áll össze, hogy µl 1M MgCl 2, 50 µl 1M Tris[hidroximetil]aminometán], µl 5M 1,6-hexándiol kerül 500 µl végtérfogatú kristályosító elegybe. Ebből a körülményből 2 µl-t 3 µl fehérjeoldattal elegyítve készült a csepp. A kristályokat UO 2 (OAc) 2, KI ill. K 2 PtCl 4 oldatokba áztatták. A nagy rendszámú atomok beépülése a kristályba a szórási mintázat megváltozását eredményezi, ami felhasználható a kezdeti fázisok kiszámításához. Ezt nevezzük izomorf helyettesítéses módszernek [17,18]. Később vált ismertté egy rokon enzimből származó β-propeller domén szerkezete, amelyet esetleg fel lehetett volna használni a fázisprobléma molekuláris 9
10 helyettesítéssel való megoldására [19]. Ez utóbbi módszer használatának az a feltétele, hogy a két fehérje aminosavsorrendje legalább 25-30%-ban megegyezzen. [20] Az adatgyűjtést 100 K-en végezték egy natív és három nehézatommal (U, Pt, I) származékolt egykristály felhasználásával. Sugárforrások: ESRF szinkrotron sugárforrás BM14-U nyaláb, a DESY EMBL X11 nyaláb és az ELTE Fehérjekrisztallográfiai Laboratóriumban található diffraktométere (réz Kα sugárzás, Rigaku RU-H2R forgó anódos generátor, Rigaku R-AXIS IIC image plate detektor). Az adatfeldolgozást az XDS programmal [21] illetve a CCP4 programcsomaggal (a MLPHARE és a DM programokkal [22, 23]) végezték. A fázisproblémát a MIRAS módszerrel oldották meg a SHELX csomag segítségével [24] Modellépítés, finomítás A kezdeti fáziskészletből számolt elektronsűrűségi térkép alapján úgy építjük fel a molekulaszerkezetet, hogy a nagy elektronsűrűségű régiókba illesztjük az atomokat. A kezdeti modellmolekulát a szekvencia elektronsűrűségi hálóba történő automatizált illesztésével kapjuk, ezek után igazítjuk a térképhez, a hozzáigazított modellből új fázisokat számítunk, ami alapján új térképet kapunk. A töredezett és a szekvenciában bizonytalan helyzetű fehérjeláncokat tartalmazó kezdeti modell felülvizsgálata, és a további modellépítési lépések manuálisan történnek. A modell lokális tökéletesítése a teljes elektronsűrűségi térkép javulását eredményezi, ezért modellépítési-finomítási ciklusok sorozatát végezzük. Ahogy egyre jobb lesz a modell, úgy csökken a térképek zajszintje (4. ábra). 4. ábra: modellépítés-finomítási ciklusok egymásutánja. A Coot programmal [26] megjelenített elektronsűrűségi térkép. Kiindulási modellt az ARP/wARP [25] segítségével építették fel. Ezután a modellépítési lépéseket a COOT programmal [26] végeztem. Ezzel a programmal építettem be 10
11 a szerkezetbe a vízmolekulákat, a kristályosítási körülményből származó 1,6-hexándiolokat, és a Mg 2+ -ionokat is. A program automatikusan csak vizet tud elhelyezni az elektronsűrűségi hálóban, ezért a többit manuálisan kell megkeresni, és kicserélni a térképen elhelyezett vízmolekulákkal. A Mg 2+ -ionokat a hatos koordinációs szféra, és az abban található negatív töltésú aminosav oldalláncok alapján azonosítottam (5. ábra). 5. ábra: Mg 2+ -ion koordinációja. Az első koordinációs szférában négy vízmolekula, és két aszparaginsav van. A finomítást az CCP4 (Collaborative Computing Project 4) programcsomag REFMAC5 programjával készítettem [27]. A felbontás (esetünkben 1,9 Å) meghatározza a mért adatok és atomok számának arányán keresztül az alkalmazandó finomítási stratégiát: A molekulákra geometriai kényszereket alkalmaztam. A fehérje atomokra individuális izotróp B-faktor finomítást alkalmaztam. Hogy modellezzem a fehérjemolekulák doménjeinek hőmozgási anizotrópiáját is, ún. TLS finomítást alkalmaztam [28]. Mivel a hidrogén atomok az elektronsűrűségi térképen nem látszanak ilyen felbontás esetén, kémiai ismeretek alapján generáltam őket, és rögzített geometriával, a kapcsolódó nemhidrogén atomon lovagolva finomítottam őket ( riding model ). A szerkezet validálását a CCP4 programcsomaggal végeztem. Ennek során vizsgáltam a szerkezet krisztallográfiai és fizikai-kémiai (pl. geometriai jellemzők, nemkötő kölcsönhatások) jóságát. Az adatgyűjtési (1. Táblázat) és szerkezetfinomítási (2. Táblázat) eredmények alább láthatók. 11
12 1. Táblázat: az adatgyűjtés eredményei. Adatgyűjtés Natív UO 2 (OAc) 2 KI K 2 PtCl 4 Tércsoport R32 R32 R32 R32 R32 Cellaparaméterek (a, c; Å) (Hexagonális tengelyválasztás) 183,0 144,63 182,95 143,94 182,82 144,44 184,80 145,73 184,68 145,48 Hullámhossz (Å) 1,5418 1,5418 1,5418 0,8162 1,0715 Felbontás 20,0-1,9 20,0-2,5 20,0-2,2 20,0-2,0 20,0-2,5 Független reflexiók száma I/σ(I) 12,79 10,94 9,65 15,35 31,14 R meas 0,158 0,141 0,137 0,112 0,071 Teljesség (%) 95,7 99,2 92,7 99,4 99,6 Nehézatomhelyek száma Fázismeghatározó erősség (acentrikus/centrikus reflexiók) - 0,74/0,48 1,01/0,69 2,01/1,25 1,77/1,07 2. Táblázat: a finomítás eredménye, Finomítás Felbontási tartomány 19,78-1,91 Reflexiók száma R 0,184 R free c Atomok száma: 0,212 fehérje ,6-hexándiol molekula 6 Mg 2+ -ion 3 vízmolekula 361 c Az R free számítására a reflexiók 5%-a lett véletlenszerűen kiválasztva. Átlagos négyzetes eltérés az ideális geometriától Kötéshossz (Å) 0,010 Kötésszög (º) 1,247 Trigonális / általános síkok (Å) 0,004 Átlagos B-faktor (Å 2 ) 17,79 Átlagos koordinátahiba (Å) d 0,122 Ramachandran térkép ϕ / ψ a legkedvezőbb régióban 462 ϕ / ψ a megengedett régióban 66 ϕ / ψ bővített megengedett és 4 / 2 tiltott régióban d R free alapján számolva 12
13 2.2 A szerkezet elemzése A fehérje szerkezete a PyMOL [29] programmal praktikusan megjeleníthető. Nem csak az atomok, aminosavak közti kötéseket, hanem a másodlagos szerkezeti elemeket, a feltekeredést is ábrázolja. Továbbá a fehérje szimmetriamásolatait is generálja, ezáltal az egész komplex szerkezetet is megjeleníthetjük vele. Amelyik ábránál külön nem jelzem, ott a molekulaszerkezet képét ezzel a programmal készítettem. Molekuladinamikai számításokat is végeztem, hogy kiderüljön, milyen mozgásokat végezhet az enzim oldatban. Az ElNémo [30] szerver makromolekulák mozgását a felhasználó által beküldött.pdb fájl (ami a kristályban lévő atomok koordinátáit tartalmazza) alapján normál módus analízissel végzi. A normál módus elemzés ún. elasztikus hálózat modellen alapul: több aminosavat tartalmazó nagyobb egységek elasztikus hálózatával modellezve a fehérjét a legalacsonyabb frekvenciájú normál módusok ugyanazok maradnak, így lehetővé válik nagy molekulák normál módus elemzése. Ezek a legalacsonyabb frekvenciájú normál módusok a domének közti és a fehérje multimeren belüli hajlékonyság jellemzésére használhatók. A számított eredményeket grafikusan, három irányból mutatva animált formátumban is megjeleníti (6. ábra). a) b) c) 6. ábra: Az ElNémo szerver által megjelenített irányok. a) x0, b) x90, c) y90.
14 3. A PhAAP fehérje szerkezete 3.1. A monomer felépítése A PhAAP enzim 622 aminosavból áll, amelyek két domént alkotnak. Ezek a komplexben egymáshoz képest félig nyitott helyzetben vannak rögzítve, szemben a POP család többi tagjával, ahol a domének szétnyílhatnak. Míg általában ennek a dinamikus mozgásnak a határai szabják meg, hogy mekkora oligopeptid fér a hidroláz domén katalitikus triádjának közelébe, addig itt a méretszelekció másféle, eddig egyedülálló módon valósul meg A β-propeller domén Sok, különböző funkciójú fehérjében megtalálható ez a jellegzetes doménszerkezet. 4-8 lapát építi fel, amik egyenként négy antiparallel β-szálból állnak (7. ábra). A proliloligopeptidáz családban 7 vagy 8 lapát építi fel ezt a domént. Az első és az utolsó lapát között nincs kovalens kapcsolat, vagy más extra stabilizáló kölcsönhatás, így a propelleren belül a dinamikus mozgást semmi nem gátolja, a közepén levő pórus átmérője változhat [31]. 7. ábra: A lapátok szerkezete, és a PhAAP a β-propeller doménjének felépítése. Az N-terminálistól (kék) számított 3. lapát 2. és 3. szála közé beékelődött hurok. A PhAAP fehérje propeller doménjének sajátossága az a hurok, ami a 3. lapát 2. és 3. β-szálja közé ékelődött be. Ez az inzerció szerepet játszik a fehérjekomplex struktúrájának rögzítésében, valamint a hidroláz doménnek is nagyfokú stabilitást biztosít. 14
15 A hidroláz domén szerkezete, stabilitása Az enzim másik eleme, a hidroláz domén, amely tulajdonképpen a peptidek bontását végzi. Ebben a központi nyolc β-szál körül α-hélixek helyezkednek el. Ezek közül a szélső β- szál után helyezkedik el a katalitikus triád (Ser466, Asp546, His578) hisztidinje (8. ábra). 8. ábra: A PhAAP monomer szerkezete A fehérje aktivitását feltehetően nagymértékben befolyásolja ennek a szélső β-szálnak a stabilitása, ezért külön vizsgáltuk ennek a kölcsönhatásait a hexameren belüli szomszédos AAP molekulákkal. Azt találtuk, hogy nem csak a monomer és az egymással érintkező hidroláz domének α-hélixei rögzítik, hanem a szomszédos fehérje β-propeller doménjének inzerciója is, mivel ez a hidroláz domén központi β-redőjének folytatásaként helyezkedik el. Ez az elhelyezkedés szimmetrikus, vagyis a hidroláz doménnel érintkező molekulák kölcsönösen rögzítik egymás β-élét. Vizsgáltam POP család többi tagjánál fellelhető β-él stabilizációs megoldásokat is. Azt találtam, hogy a prolil-oligopeptidázok közül mindegyikben nagyfokú stabilitás jellemzi a szélső β-szálat. Mint azt már láttuk, az ApAAP és a PhAAP fehérjéknél is folytatólagos a β- redő, az ApAAP-nél a két hidroláz domén kapcsolódása, míg a PhAAP-nél a szomszédos fehérje inzerciója következtében. 15
16 3.2. A PhAAP komplex felépítése A monomerek közötti kölcsönhatások A negyedleges szerkezet döntően befolyásolja egy enzim működési mechanizmusát. A teljes PhAAP enzim hat monomerből áll, melyek szimmetrikus hexamert alkotnak (11. ábra). Elegendő tehát egyetlen monomer szerkezetének a meghatározása, a többit az R32 krisztallográfiai szimmetria szerint képezzük. A monomerek közötti kölcsönhatások érintik mindkét domént. 3-3 fehérje β-propeller doménje érintkezik úgy, hogy a háromból páronként az egyik első lapátja a másik második lapátjához illeszkedik (10. ábra). A hidroláz domének közül 2-2 szorosan érintkezik, de nem alkot folytonos β-redőt. Ennek a párnak a kapcsolatát a fent említett inzerció következtében létrejövő propeller-hidroláz kölcsönhatás is erősíti (9. ábra). 10. ábra: A β-propellerek közötti kapcsolatok. 9. ábra: A hidroláz-propeller kölcsönhatás. Az 1. lapátok a 2. lapátokkal illeszkednek. A propeller inzerciója a hidroláz β-redőjének folytatása. Az ApAAP fehérje felépítésében a dimer két tagja között csak hidroláz-hidroláz kölcsönhatás van, ezért az ApAAP enzimben domének szét tudnak nyílni, és szét is nyílnak a szubsztrát bejutásához és az elbontott fragmensek kijutásához. Ezzel szemben a PhAAP komplex oldalán kb. 10X30 Å méretű rések vannak (11. ábra), az oligopeptidek ezeken át juthatnak el a szubsztrátkötő zsebig, ami, ellentétben az ApAAP-vel, a fehérjemolekula oldalról nyitott üregében helyezkedik el (8. ábra). Így a méretszelektivitás a POP család többi tagjától eltérően nem azáltal valósul meg, hogy a két domén dinamikusan szét tud nyílni, tehát az PhAAP fehérje esetében új működési mechanizmust ismerhetünk meg. 11. ábra: a hexamer oldalán található 10X30 Å méretű 16
17 A hexamer dinamikája Arra is kíváncsi voltam, hogy ezek a nyílások az oldatban, működés közben is nyitva maradnak-e, vagy be tudnak csukódni? Ennek felderítésére molekuladinamikai számításokra volt szükségem, amit az ElNémo szerveren keresztül végeztem. Ez a kiszolgáló kiszámolta a legalacsonyabb frekvenciájú normál módusokat (szám szerint ötöt) a PhAAP hexamer mozgására, amit animált formátumban is megjelenített, mindhárom tengely irányából. A dinamikus mozgásokat az x-tengely felől nézve az alábbi módon ábrázolom (12. ábra): a hat monomert a hat megfelelő szín jelöli, a rövid nyilak a monomerek mozgását, a hosszúak a dimerekét (ha a két monomer együtt mozog, csak az egyikük színével jelzem). A szaggatott vonalak az elmozdulás utáni helyzetüket mutatják, ahol szaggatott vonal/nyíl nem szerepel, abban a módusban az adott monomer/dimer mozdulatlan. Ezeken az látszik, hogy az oldalsó nyílások mérete és alakja hogyan változik. Az derült ki mindebből, hogy a pórusok ugyan lélegeznek, vagyis méretük változik a mozgás során, ám sosem záródnak be teljesen. Emellett a három pórus a hexamer oldalán sohasem szűkül egyszerre, tehát a szubsztrát bejutása és a termékek távozása mindig biztosított a hexamer mozgása során. 12. ábra: A pórusméret változása, a hexamer mozgása során az ElNémo szerver számításai szerint. 17
18 3.3. Az aktív hely A félig szétnyílt domének miatt az oldalsó nyílásokon belépő oligopeptidek mind a hat aktív helyet meg tudják közelíteni (13. ábra a)). Az aktív helyen a katalitikus triád (Ser466, His578, Asp546) és az oxianion hely konformációja hasonló az ApAAP szerkezetben találthoz, és aktí enzimkonformációnak felel meg. A szubsztrátkötő hely összehasonlítása azért érdekes, mert az ApAAP esetén kiderült, hogy az emlős enzimekkel ellentétben nemcsak egy láncvégi védett aminosavat tud eltávolítani az oligopeptidről, hanem láncközben is képes hasítani (endopeptidáz) [32]. Ez a PhAAP esetén is beigazolódott [33]. A PhAAP szubsztrátkötő régiójának molekuláris felszínét megvizsgálva (13. ábra c) részén bekeretezve) kiderül, hogy ennek az az oka, hogy az S2-S4 régió nyitott: sem térbeli, sem elektrosztatikus akadálya nincs hosszabb peptidlánc megkötésének. Az enzim S1 zsebének alján ellentétben az ApAAP-vel savas oldallánc is található (13. ábra b)), ami magyarázza a szubsztrát-specificitásbeli eltérést a két enzim között: mindkettő elsődlegesen fenilalanin után hasítja el a peptidláncot, de a PhAAP kisebb mértékben arginin után is. A B C 13. ábra: A PhAAP aktiv helye a) A komplex oldalán bejutó szubsztrát bármelyik aktív helyhez eljuthat. b) A molekuláris felszín a szubsztrátkötő helyen (propeller domén: barna, hidroláz domén: narancssárga). c) A katalitikus triád (zölddel aláhúzva) és az S1 zseb aminosavjai. PhAAP szerkezet: narancssárga C atomok, a zsebben található 1,6 hexándiol molekula magenta. ApAAP szerkezet: drapp C atomok, a zsebben kötött acetil-fenilalanin világoskék. d) Az S1 zseb kötrnyezetének molekuláris felszíne elektrosztatikus potenciál szerint színezve (kék: pozitív, piros: negatív) 18
19 4. PhAAP fehérje összehasonlítása más enzimekkel 4.1. A propeller domén Mint azt már említettem, az adatgyűjtés után publikálták egy β-propeller domén szerkezetet [19], ami nagymértékben hasonlít a PhAAP β-propeller doménjére. Ez rokon fajból, a Pyrococcus furiosus származó ún. háromlebenyű fehérje (TLP). Különbség csak a hidroláz doménnel érintkező hurokrégióknál, illetve a szomszédos fehérjemolekulákkal érintkező részen van (14. ábra). 14. ábra: A TLP és a PhAAP propellerjének egymásra illesztése. A bal oldali kép felülről jobb oldali alulnézetből, a hidroláz domén felől készült. A TLP molekula szürke, a PhAAP cián színnel van ábrázolva narancssárgával jelezve azokat a részeket, amik a molekulán belül a hidroláz doménnel, és magentával, amik a szomszédos fehérjével érintkeznek A hidroláz domén stabilitása A fent leírt sajátos megoldás a hexamer szerkezetének rögzítésére felvetette, hogy meg kellene vizsgálni, más enzimeknél is szerepel-e hidroláz domén β-redőjének kibővítése vagy a szélső β-szál valami egyéb módon stabilizálva van-e. Ugyanis az ez utáni hurkon helyezkedik el a katalitikus hisztidin, ezért a β-él destabilizációja az aktivitás rovására mehet. Első lépésben a POP enzimcsalád tagjait vizsgáltam meg (14. ábra), és azt találtam, hogy minden esetben található valamiféle erős kölcsönhatás a β-él és az enzimnek a fehérjemolekula hidroláz doménjén kívüli része között. Az acil-aminoacil peptidázoknál a hidroláz domén β-redője folytatódik, az ApAAP dimernél a két hidroláz kapcsolódásával, a PhAAP esetén pedig a szomszédos molekula inzerciójával. A prolil-oligopeptidáznál (POP) a 19
20 szélső β-szál a fehérje N-terminálisán levő α-hélix-szel van kölcsönhatásban. A dipeptidilpeptidáz IV (DPP4) dimerje esetén a két hidroláz domén úgy érintkezik a két szélső β-szálnál, hogy nem alkotnak folytonos β-redőt, hanem a két β-él egymást keresztezi (15. ábra). 15. ábra: A POP enzimcsaládban előforduló β-él stabilizáló megoldások Hidroláz domén: világoskék, propeller domén: sötétkék. A β-él széle és a katalitikus hisztidint tartalmazó hurok magenta. A második, kölcsönható fehérjemolekula megfelelő színei: sárga, zöldessárga, vörös. A katalitikus hisztidint térkitöltő ábrázolással jelenítettem meg. Az α/β hidroláz klánban megnéztem a POP családdal közvetlen rokonságban álló enzimcsaládokat is. Nem minden esetben, de találtam példákat hasonló β-él stabilizáló szerkezetekre. Az S10 peptidáz családban úgy valósul ez meg, hogy a molekula plusz egy vagy kettő - két β-szálat tartalmazó - inzerció beépülésével a központi β-redőt még kettő vagy négy β-szállal bővíti (16. ábra). 16. ábra: Az S10 család hidroláz domén Az 1ac5 jelű fehérje esetén négy, az 1whs jelűnél két β-szállal bővül a központi β-redő. 20
21 Összefoglalás Munkám során elsőként sikerült meghatározni a PhAAP enzim monomerjének és komplexének szerkezetét. Normál módus elemzést végeztem az enzim lehetséges mozgásának leírására. Ezek alapján elmondható, hogy az általam vizsgált fehérjénél újszerű módon valósul meg a méretszelektivitás. A szubsztrátmolekulák nem a domének szétnyílásával, hanem a komplex oldalán levő nyíláson keresztül jutnak el az aktív helyhez. Összehasonlítottam különböző enzimek hidroláz doménjében szélső β-szálak kölcsönhatásait, és azt tapasztaltam, hogy a POP család minden tagját nagyfokú β-él stabilizáció jellemzi. További tervek: Kutatási eredményeim publikálása folyamatban van. Köszönetnyilvánítás Mindenek előtt köszönet illeti témavezetőmet, Harmat Veronikát, aki munkámat irányította, hasznos tanácsokkal látott el és mindvégig biztatott. Szeretnék továbbá köszönetet mondani az Enzimológiai Intézetben dolgozó Polgár László csoportjának, köztük Kiss Andrásnak, akik a fehérjét előállították, és az oldatbeli vizsgálatokat végezték. Köszönettel tartozom az ELTE Fehérjekrisztallográfiai Laboratórium vezetőjének Náray-Szabó Gábornak, és Perczel Andrásnak, hogy lehetőséget adtak a csoportban a diákköri munka végzésére. S köszönet illeti még a csoport tagjait, Rádi Krisztinát és Hornung Balázst, akik a fehérjét kristályosították. 21
22 Rövidítések AAP: acil-aminoacil peptidáz, az acilpeptid hidroláz ennek a szinonimája ApAAP: Aeropyrum pernix AAP DPP4: dipeptidil-peptidáz IV PhAAP: Pyrococcus horikoshii AAP POP: prolil oligopeptid peptidáz TLP: Pyrococcus furiosus háromlebenyű proteáz (trilobed protease) Irodalomjegyzék [1] Boross László Sajgó Mihály A biokémia alapjai pp Mezőgazda, (2003) [2] Nardini, M. and Dijkstra, B. W.: α/β Hydrolase fold enzymes: the family keeps growing. [3] Rawlings N. D., Polgár, L. and Barrett, A. J. J. Biochem. 279; (1991). [4] Kanatani, A., Masuda, T., Shimoda, T., Misoka, F., Lin, X. S., Yoshimoto, T. et al. J. Biochem. 110; (1991). [5] Rawlings, N. D. and Barrett, A. J. Methods Enzymol. 244; 19-61, (1994). [6] Polgár, L. FEBS Lett. 311; (1992). [7] Polgár, L. Cell. Mol. Life Sci. 59; (2002). [8] Jones, W. M., Manning, L. R. and Manning J. M. Biochem. Biophys. Res. Comm. 139; (1986) [9] Tsunawa, S., Narita, K. and Ogata, K. J. Biochem (Tokyo) 77; (1975) [10] Scaloni, A., Jones, W.M., Pospischil, M., Scheewind, O., Popowicz, A., Bossa, F. et al. J. Lab Chin. Med. 120; (1992) [11] Mitta, M., Asada, k., Uchimura, Y., Kimizuka, F., Kato, I., Sakiyama, F. et al. J. Biochem. 106; (1989) [12] Kobayashi, K., Lin, L., Yeadon, J., Klickstein, L. and Smith, J. J. Biol. Chem. 264; (1989) [13] Richards, P. G., Johnson, M. K. and Ray, D. E. Mol. Pharmacol. 58; (2000) [14] Duysen, E. G., Li, B., Xie, W., Schopfer, L. M., Anderson, R. S., Broomfield, C. A. and Lockbridge, J. Pharmacol. Exp. Ther. 299; (2001) [15] Jones, W. M. and Manning, J. M. Biochim. Biophys. Acta 953; (1988) [16] Erlandsson, R., Boldog, F., Persson, B. et al Oncogene 6; (1991) 22
23 [17] Blundell, T.L. & Johnson, L.N. Protein Crystallography, Academic Press, London, (1976) [18] Robertson, J.M. J. Chem. Soc., (1935) [19] Bosch, J. et al. Acta Crystallographica D63, (2007) [20] Sanderson, M.R., Skelly, J.V.S. Macromolecular Crystallography conventional and high-throughput methods Oxford University Press (2007) [21] Kabsch, W. J. Appl. Cryst. 26, (1993) [22] Collaborative Computational Project, Number 4. (1994) Acta Cryst. D50, 760. [23] K. Cowtan, Joint CCP4 and ESF-EACBM Newsletter on Protein Crystallography, 31, p (1994) [24]Sheldrick, G.M., Acta Cryst. A (2008) [25] Langer, G., et al. Nature Protocols (2008) [26] "Coot: model-building tools for molecular graphics" Emsley P, Cowtan K Acta Crystallographica Section D-Biological Crystallography 60: [27] Vagin, A.A. and Dodson, E.J. "Refinement of Macromolecular Structures by the Maximum-Likelihood Method" G.N. Murshudov, Acta Cryst. D53, (1997) [28] Winn, M., Isupov, M. & Murshudov, G.N. Use of TLS parameters to model anisotropic displacements in macromolecular refinement. Acta Cryst D57: (2001) [29] DeLano, W.L. (2002) [30]Suhre, K. & Sanejouand, Y.H. ElNemo: a normal mode web-server for protein movement analysis and the generation of templates for molecular replacement. Nucleic Acids Research, 32, W610-W614, (2004) [31] V. Fülöp, D.T. Jones, Cur. Opin. Struct.Biol. 9, (1999) [32] Kiss, A.L., Hornung, B., Radi, K., Gengeliczki, Z., Sztaray, B., Juhasz, T., Szeltner, Z., Harmat, V., Polgar, L., J. Mol. Biol. 368, (2007) [33] Szeltner, Z., Kiss, A.L., Domokos, K., Harmat, V., Náray-Szabó, G. & Polgár, L. Biochim Biophys Acta 1794: (2009) 23
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
 A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
A polipeptidlánc szabályozott lebontása: mit mondanak a fehérjekristályok? Harmat Veronika ELTE Kémiai Intézet, Szerkezeti Kémia és Biológia Laboratórium MTA-ELTE Fehérjemodellező Kutatócsoport A magyar
Nyitott az újra, méretszelekció másképp, avagy a Pyrococcus horikoshii acilaminoacil-peptidáz vizsgálata
 Tudományos Diákköri Dolgozat Kiss-Szemán Anna Júlia Nyitott az újra, méretszelekció másképp, avagy a Pyrococcus horikoshii acilaminoacil-peptidáz vizsgálata Dr. Harmat Veronika és Dr. Karancsiné Menyhárd
Tudományos Diákköri Dolgozat Kiss-Szemán Anna Júlia Nyitott az újra, méretszelekció másképp, avagy a Pyrococcus horikoshii acilaminoacil-peptidáz vizsgálata Dr. Harmat Veronika és Dr. Karancsiné Menyhárd
Tudományos Diákköri Dolgozat. Orgován Zoltán
 Tudományos Diákköri Dolgozat Orgován Zoltán Egy oligopeptidáz méretszelektivitásának, szubsztrátkötésének és katalitikus mechanizmusának tanulmányozása röntgendiffrakcióval és in silico módszerekkel Dr.
Tudományos Diákköri Dolgozat Orgován Zoltán Egy oligopeptidáz méretszelektivitásának, szubsztrátkötésének és katalitikus mechanizmusának tanulmányozása röntgendiffrakcióval és in silico módszerekkel Dr.
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Enzimek. Enzimek! IUBMB: szisztematikus nevek. Enzimek jellemzése! acetilkolin-észteráz! legalább 10 nagyságrend gyorsulás. szubsztrát-specificitás
 Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
Enzimek acetilkolin-észteráz! Enzimek! [s -1 ] enzim víz carbonic anhydrase 6x10 5 10-9 karbonikus anhidráz acetylcholine esterase 2x10 4 8x10-10 acetilkolin észteráz staphylococcal nuclease 10 2 2x10-14
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Bioinformatika 2 6. előadás
 6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
6. előadás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2018.10.08. PDBj: http://www.pdbj.org/ Fehérjék 3D szerkezeti adatbázisai - PDBj 2 2018.10.08.
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Az oligopeptidázok szerkezete és működése: katalízis az S9A enzimcsaládban. A doktori értekezés tézisei. Juhász Tünde
 Az oligopeptidázok szerkezete és működése: katalízis az S9A enzimcsaládban A doktori értekezés tézisei Juhász Tünde Eötvös Loránd Tudományegyetem Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna,
Az oligopeptidázok szerkezete és működése: katalízis az S9A enzimcsaládban A doktori értekezés tézisei Juhász Tünde Eötvös Loránd Tudományegyetem Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna,
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk.
 .5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
.5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
Röntgen sugárzás. Wilhelm Röntgen. Röntgen feleségének keze
 Röntgendiffrakció Kardos Roland 2010.03.08. Előadás vázlata Röntgen sugárzás Interferencia Huygens teória Diffrakció Diffrakciós eljárások Alkalmazás Röntgen sugárzás 1895 röntgen sugárzás felfedezés (1901
Röntgendiffrakció Kardos Roland 2010.03.08. Előadás vázlata Röntgen sugárzás Interferencia Huygens teória Diffrakció Diffrakciós eljárások Alkalmazás Röntgen sugárzás 1895 röntgen sugárzás felfedezés (1901
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Röntgendiffrakció. Orbán József PTE, ÁOK, Biofizikai Intézet november
 Röntgendiffrakció Orbán József PTE, ÁOK, Biofizikai Intézet 2013. november Előadás vázlata Röntgen sugárzás Interferencia, diffrakció (elektromágneses hullámok) Kristályok szerkezete Röntgendiffrakció
Röntgendiffrakció Orbán József PTE, ÁOK, Biofizikai Intézet 2013. november Előadás vázlata Röntgen sugárzás Interferencia, diffrakció (elektromágneses hullámok) Kristályok szerkezete Röntgendiffrakció
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel
 Eötvös Loránd Tudományegyetem Természettudományi Kar Környezettudományi Centrum Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel készítette: Felföldi Edit környezettudomány szakos
Eötvös Loránd Tudományegyetem Természettudományi Kar Környezettudományi Centrum Anaerob fermentált szennyvíziszap jellemzése enzimaktivitás-mérésekkel készítette: Felföldi Edit környezettudomány szakos
Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis. Fehérjeszerkezet analízis
 Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Szerkezet Protein Data Bank (PDB) http://www.rcsb.org/pdb ~ 35 701 szerkezet közepes felbontás 1552 szerkezet d 1.5 Å 160 szerkezet d 1.0 Å 10 szerkezet d 0.8 Å (atomi felbontás) E globális minimum? funkció
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Imunnológiailag fontos fehérjék röntgendiffrakciós szerkezetvizsgálata: fehérje-ligandum kölcsönhatások a működés során Zárójelentés
 Imunnológiailag fontos fehérjék röntgendiffrakciós szerkezetvizsgálata: fehérje-ligandum kölcsönhatások a működés során Zárójelentés A fehérjék térszerkezetének meghatározása a fehérjeműködés atomi szintű
Imunnológiailag fontos fehérjék röntgendiffrakciós szerkezetvizsgálata: fehérje-ligandum kölcsönhatások a működés során Zárójelentés A fehérjék térszerkezetének meghatározása a fehérjeműködés atomi szintű
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
MedInProt Szinergia IV. program. Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére
 MedInProt Szinergia IV. program Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére Tantos Ágnes MTA TTK Enzimológiai Intézet, Rendezetlen fehérje kutatócsoport
MedInProt Szinergia IV. program Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére Tantos Ágnes MTA TTK Enzimológiai Intézet, Rendezetlen fehérje kutatócsoport
Fényhullámhossz és diszperzió mérése
 KLASSZIKUS FIZIKA LABORATÓRIUM 9. MÉRÉS Fényhullámhossz és diszperzió mérése Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. október 19. Szerda délelőtti csoport 1. A mérés célja
KLASSZIKUS FIZIKA LABORATÓRIUM 9. MÉRÉS Fényhullámhossz és diszperzió mérése Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. október 19. Szerda délelőtti csoport 1. A mérés célja
15. Fehérjeszintézis: transzláció. Fehérje lebontás (proteolízis)
 15. Fehérjeszintézis: transzláció Fehérje lebontás (proteolízis) 1 Transzláció fordítás A C G T/U A C D E F G H I K L M N P Q R S T V W Y 4 betűs írás (nukleinsavak) 20 betűs írás (fehérjék) 2 Amit már
15. Fehérjeszintézis: transzláció Fehérje lebontás (proteolízis) 1 Transzláció fordítás A C G T/U A C D E F G H I K L M N P Q R S T V W Y 4 betűs írás (nukleinsavak) 20 betűs írás (fehérjék) 2 Amit már
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Doktori értekezés. Kiss András László 2007. Témavezető: Polgár László professzor. 1. oldal
 Doktori értekezés Kiss András László 2007 Témavezető: Polgár László professzor 1. oldal Acylaminoacyl peptidáz enzimek katalízisének vizsgálata A dolgozatot készítette: Biológia Doktori Iskola Szerkezeti
Doktori értekezés Kiss András László 2007 Témavezető: Polgár László professzor 1. oldal Acylaminoacyl peptidáz enzimek katalízisének vizsgálata A dolgozatot készítette: Biológia Doktori Iskola Szerkezeti
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Fehérjék felépítése és struktúrája. Aminosav oldalláncok. A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel
 Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Fehérjék felépítése és struktúrája Aminosav oldalláncok A fehérjék királis elemekből (α-l-aminosavakból) épülnek fel Fehérjék szerkezete Anfinsen dogmája Anfinsen dogmája (vagy: termodinamikus hipotézis)
Bevezetés a bioinformatikába. Harangi János DE, TEK, TTK Biokémiai Tanszék
 Bevezetés a bioinformatikába Harangi János DE, TEK, TTK Biokémiai Tanszék Bioinformatika Interdiszciplináris tudomány, amely magába foglalja a biológiai adatok gyűjtésének,feldolgozásának, tárolásának,
Bevezetés a bioinformatikába Harangi János DE, TEK, TTK Biokémiai Tanszék Bioinformatika Interdiszciplináris tudomány, amely magába foglalja a biológiai adatok gyűjtésének,feldolgozásának, tárolásának,
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során
 Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során 1. projekt Kvaterner ammónium ligandot használó enzimek ligand kötőhelyének
Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során 1. projekt Kvaterner ammónium ligandot használó enzimek ligand kötőhelyének
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
[S] v' [I] [1] Kompetitív gátlás
![[S] v' [I] [1] Kompetitív gátlás [S] v' [I] [1] Kompetitív gátlás](/thumbs/93/114506146.jpg) 8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n. 2008. április 29.
 Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
2. Ismert térszerkezetű transzmembrán fehérjék adatbázisa: a PDBTM adatbázis. 3. A transzmembrán fehérje topológiai adatbázis, a TOPDB szerver
 A 2005 és 2007 között megvalósított project célja transzmembrán fehérjék vizsgálata és az ehhez szükséges eljárások kifejlesztése volt. Ez utóbbi magába foglalta új adatbázisok és szerkezet becslő módszerek
A 2005 és 2007 között megvalósított project célja transzmembrán fehérjék vizsgálata és az ehhez szükséges eljárások kifejlesztése volt. Ez utóbbi magába foglalta új adatbázisok és szerkezet becslő módszerek
Gépi tanulás és Mintafelismerés
 Gépi tanulás és Mintafelismerés jegyzet Csató Lehel Matematika-Informatika Tanszék BabesBolyai Tudományegyetem, Kolozsvár 2007 Aug. 20 2 1. fejezet Bevezet A mesterséges intelligencia azon módszereit,
Gépi tanulás és Mintafelismerés jegyzet Csató Lehel Matematika-Informatika Tanszék BabesBolyai Tudományegyetem, Kolozsvár 2007 Aug. 20 2 1. fejezet Bevezet A mesterséges intelligencia azon módszereit,
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól
 Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
Ragyogó molekulák: dióhéjban a fluoreszcenciáról és biológiai alkalmazásairól Kele Péter egyetemi adjunktus Lumineszcencia jelenségek Biolumineszcencia (biológiai folyamat, pl. luciferin-luciferáz) Kemilumineszcencia
A KAR-2, egy antimitotikus ágens egyedi farmakológiájának atomi és molekuláris alapjai
 A KAR-2, egy antimitotikus ágens egyedi farmakológiájának atomi és molekuláris alapjai A doktori értekezés tézisei Horváth István Eötvös Loránd Tudományegyetem Biológia Doktori Iskola (A Doktori Iskola
A KAR-2, egy antimitotikus ágens egyedi farmakológiájának atomi és molekuláris alapjai A doktori értekezés tézisei Horváth István Eötvös Loránd Tudományegyetem Biológia Doktori Iskola (A Doktori Iskola
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Farmakológus szakasszisztens Farmakológus szakasszisztens 2/34
 -06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
-06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
Modern Fizika Labor. 17. Folyadékkristályok
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. okt. 11. A mérés száma és címe: 17. Folyadékkristályok Értékelés: A beadás dátuma: 2011. okt. 23. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. okt. 11. A mérés száma és címe: 17. Folyadékkristályok Értékelés: A beadás dátuma: 2011. okt. 23. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
kutatás során legfőbb eredményeinket a szerin proteázok aktiválódásának mechanizmusával és az aktiválódás fiziológiai következményeinek
 Fehérjék konformációs flexibilitása mint a biomolekuláris felismerés és a jeltovábbítás alapvető eleme (OTKA NK 77978) Zárójelentés (2009. ápr. 1-től 2013. márc. 31-ig) A biológiai rendszerek önszerveződésének
Fehérjék konformációs flexibilitása mint a biomolekuláris felismerés és a jeltovábbítás alapvető eleme (OTKA NK 77978) Zárójelentés (2009. ápr. 1-től 2013. márc. 31-ig) A biológiai rendszerek önszerveződésének
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
Az élő sejt fizikai Biológiája:
 Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
KÖLCSÖNHATÁS ÉS DINAMIKA. az NMR spektroszkópia, mint a modern szem. Bodor Andrea
 KÖLCSÖNHATÁS ÉS DINAMIKA az NMR spektroszkópia, mint a modern szem Bodor Andrea ELTE Szerkezeti Kémiai és Biológiai Laboratórium A Magyar Tudomány Ünnepe, 2012.11.08. Edvard Munch: A Nap (1911-1916) AZ
KÖLCSÖNHATÁS ÉS DINAMIKA az NMR spektroszkópia, mint a modern szem Bodor Andrea ELTE Szerkezeti Kémiai és Biológiai Laboratórium A Magyar Tudomány Ünnepe, 2012.11.08. Edvard Munch: A Nap (1911-1916) AZ
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Biomolekuláris nanotechnológia. Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium
 Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Biomolekuláris nanotechnológia Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium Az élő szervezetek példája azt mutatja, hogy a fehérjék és nukleinsavak kiválóan alkalmasak önszerveződő molekuláris
Badari Andrea Cecília
 Nagy nitrogéntartalmú bio-olajokra jellemző modellvegyületek katalitikus hidrodenitrogénezése Badari Andrea Cecília MTA Természettudományi Kutatóközpont, Anyag- és Környezetkémiai Intézet, Környezetkémiai
Nagy nitrogéntartalmú bio-olajokra jellemző modellvegyületek katalitikus hidrodenitrogénezése Badari Andrea Cecília MTA Természettudományi Kutatóközpont, Anyag- és Környezetkémiai Intézet, Környezetkémiai
Flagellin alapú filamentáris nanoszerkezetek létrehozása
 Flagellin alapú filamentáris nanoszerkezetek létrehozása Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium MTA Enzimológiai Intézete MTA MFA Bakteriális flagellumok Flagelláris filamentum: ~10
Flagellin alapú filamentáris nanoszerkezetek létrehozása Vonderviszt Ferenc PE MÜKKI Bio-Nanorendszerek Laboratórium MTA Enzimológiai Intézete MTA MFA Bakteriális flagellumok Flagelláris filamentum: ~10
OH ionok LiNbO 3 kristályban (HPC felhasználás) 1/16
 OH ionok LiNbO 3 kristályban (HPC felhasználás) Lengyel Krisztián MTA SZFKI Kristályfizikai osztály 2011. november 14. OH ionok LiNbO 3 kristályban (HPC felhasználás) 1/16 Tartalom A LiNbO 3 kristály és
OH ionok LiNbO 3 kristályban (HPC felhasználás) Lengyel Krisztián MTA SZFKI Kristályfizikai osztály 2011. november 14. OH ionok LiNbO 3 kristályban (HPC felhasználás) 1/16 Tartalom A LiNbO 3 kristály és
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Cikloalkánok és származékaik konformációja
 1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
41. ábra A NaCl rács elemi cellája
 41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
Név: Pontszám: 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
A fehérjék hierarchikus szerkezete
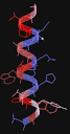 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
TRANSZPORTFOLYAMATOK A SEJTEKBEN
 16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Integráció. Csala Miklós. Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet
 Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
Integráció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet Anyagcsere jóllakott állapotban Táplálékkal felvett anyagok sorsa szénhidrátok fehérjék lipidek
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Modern Fizika Labor Fizika BSC
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. május 4. A mérés száma és címe: 9. Röntgen-fluoreszencia analízis Értékelés: A beadás dátuma: 2009. május 13. A mérést végezte: Márton Krisztina Zsigmond
Modern Fizika Labor. 12. Infravörös spektroszkópia. Fizika BSc. A mérés dátuma: okt. 04. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Immunológia alapjai előadás. Az immunológiai felismerés molekuláris összetevői.
 Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Immunológia alapjai 3 4. előadás Az immunológiai felismerés molekuláris összetevői. Az antigén fogalma. Antitestek, T- és B- sejt receptorok: molekuláris szerkezet, funkciók, alcsoportok Az antigén meghatározása
Kutatási programunk fő célkitűzése, az 2 -plazmin inhibitornak ( 2. PI) és az aktivált. XIII-as faktor (FXIIIa) közötti interakció felderítése az 2
 Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával. www.chem.elte.hu/pr
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1) Mikor kapott Paul Ehrlich orvosi Nobel-díjat? A) Idén. B) Pont 100 éve, 1908-ban. C) Nem
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1) Mikor kapott Paul Ehrlich orvosi Nobel-díjat? A) Idén. B) Pont 100 éve, 1908-ban. C) Nem
Gyalogos elütések szimulációs vizsgálata
 Gyalogos elütések szimulációs vizsgálata A Virtual Crash program validációja Dr. Melegh Gábor BME Gépjárművek tanszék Budapest, Magyarország Vida Gábor BME Gépjárművek tanszék Budapest, Magyarország Ing.
Gyalogos elütések szimulációs vizsgálata A Virtual Crash program validációja Dr. Melegh Gábor BME Gépjárművek tanszék Budapest, Magyarország Vida Gábor BME Gépjárművek tanszék Budapest, Magyarország Ing.
A kálium-permanganát és az oxálsav közötti reakció vizsgálata 9a. mérés B4.9
 A kálium-permanganát és az oxálsav közötti reakció vizsgálata 9a. mérés B4.9 Név: Pitlik László Mérés dátuma: 2014.12.04. Mérőtársak neve: Menkó Orsolya Adatsorok: M24120411 Halmy Réka M14120412 Sárosi
A kálium-permanganát és az oxálsav közötti reakció vizsgálata 9a. mérés B4.9 Név: Pitlik László Mérés dátuma: 2014.12.04. Mérőtársak neve: Menkó Orsolya Adatsorok: M24120411 Halmy Réka M14120412 Sárosi
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
