K oz ons eges termodinamika Matolcsi Tam as 1999
|
|
|
- Dávid Balázs
- 6 évvel ezelőtt
- Látták:
Átírás
1 Közönséges termodinamika Matolcsi Tamás 1999
2 2
3 Tartalomjegyzék Előszó 13 Bevezetés 19 I. EGYSZERŰ ANYAGOK Konstitúciós függvények Az alapvető termodinamikai mennyiségek Egyéb termodinamikai mennyiségek A termodinamikai mennyiségek közti összefüggések szabályai Az alapszabályok formalizálása Rendes egyszerű anyagok Entropikusság Egy speciális típusú entropikus anyag A Nernst-féle tulajdonság Feladatok Néhány speciális egyszerű anyag Az ideális gázok A van der Waals-féle anyagok A Clausius-féle anyagok A Berthelot-féle anyagok A Kammerlingh Onnes-féle anyagok Megjegyzések Feladatok Állapotváltozás-jellemzők Jelölési megállapodás Speciális típusú folyamatok Egyéb kényszerfolyamatok Hőtágulási együtthatók Rugalmassági együtthatók, kompresszibilitás Feszültségi együtthatók Fajhők Látens hők A hőtágulási tulajdonság Az állapotváltozás-jellemzők gyakorlati jelentősége Az ideális gáz állapotváltozás-jellemzői Halmazállapotváltozás-jellemzők Feladatok
4 4 TARTALOMJEGYZÉK 4. Állapotgörbék Általános tudnivalók Adiabaták Az ideális gáz állapotgörbéi A van der Waals-anyag állapotgörbéi Feladatok Kanonikus változók Alapvető összefüggések Egyszerű anyag kanonikus alakja Entropikusság a kanonikus változókban Ideális és van der Waals-féle anyagok kanonikus alakja Feladatok Fázisok Bevezető gondolatok A fázis definíciója A van der Waals-anyag fázisai Fázisok a kanonikus változókban A fázisok hőmérséklet nyomás-jellemzése A változók cserélgetése Egy hasznos formalizmus Feladatok Fáziskapcsolatok Bevezető gondolatok Nulladrendű fáziskapcsolatok Másodrendű fáziskapcsolatok λ-átmenetek A másodrendű fáziskapcsolatok osztályozásáról Elsőrendű fáziskapcsolatok A Clausius Clapeyron-egyenlet Átalakulási hő Kritikus pontok A van der Waals-anyag elsőrendű fáziskapcsolatai Feladatok Testek A test fogalma A teljes mennyiségek A teljes kanonikus változók Entropikusság a teljes kanonikus változókban Egy hasznos formalizmus Feladatok II. EGYSZERŰ TESTEK RENDSZERE; ÁTTEKINTÉS Folyamatok dinamikája Bevezető gondolatok A dinamikai egyenlet A munkavégzés és az energiaszállítás A fajlagos és a teljes dinamikai mennyiségek kapcsolata
5 TARTALOMJEGYZÉK Testek rendszere A kölcsönhatások függetlensége A dinamikai mennyiségek tulajdonságai Jelölési megállapodás A dinamikai mennyiségek pontos alakja Alaptulajdonságok A nem kompenzált hő Közvetett hővezetés Megállapodás a dinamikai mennyiségekről Kölcsönhatások szigetelése Az egyensúlyi tulajdonságok Még egyszer a jelölésekről Energiadisszipáció Bevezető gondolatok A dinamikai mennyiségek disszipációs tulajdonsága A disszipációs tulajdonság kanonikus alakja Termodinamikai erők Bevezető gondolatok Kanonikus termodinamikai erők Pszeudolineáris dinamikai mennyiségek A párközi vezetési mátrix Megjegyzés A párközi vezetési mátrixok nem egyértelműsége Mechanikailag erős rugódzás A kanonikus vezetési mátrix szimmetriatulajdonságai A disszipációs tulajdonság a pszeudolineáris esetben Feladatok III. SPECIÁLIS RENDSZEREK TÖMEGCSERE NÉLKÜL Egy test adott környezetben Bevezető megjegyzések Általános formulák Kényszer nélküli folyamatok Izochór folyamatok Adiabatikus folyamatok Izoterm folyamatok Izobár folyamatok Rugalmas burok Szélsőérték-tulajdonságok Megjegyezések az intenzív kényszerekről Kényszer helyett vezérlés Hőerőgépek Termikus hatásfok maximális teljesítmény mellett Megjegyzések a második főtételről Feladatok Két test adott környezetben Bevezető megjegyzések Általános formulák Kényszermentes rendszer
6 6 TARTALOMJEGYZÉK Rögzített együttes térfogat Rögzített együttes térfogat és együttes hőszigetelés Rögzített együttes térfogat és egyedi hőszigetelések Rögzített egyedi térfogatok Rögzített egyedi térfogatok és együttes hőszigetelés Egyedi hőszigetelések Együttes hőszigetelés Állandó hőmérséklet Állandó hőmérséklet és rögzített együttes térfogat Állandó nyomás Állandó nyomás és együttes hőszigetelés Szélsőérték-tulajdonságok Ismét a második főtételről Feladatok IV. EGYSZERŰ TESTEK RENDSZERE; ÁLTALÁNOS TÁRGYALÁS Rendszerek leírása Testek rendszerének pontos meghatározása Megjegyzések Az egyensúlyi és a disszipációs tulajdonság következményei Egyensúly Feladatok Összefoglaló formulák Bevezető megjegyzések A dinamikai egyenlet Kényszerek A pszeudolineáris eset A disszipációs tulajdonság Az egyensúly stabilitása Alkalmazás speciális rendszerekre Az egyensúlyok szigorú aszimptotikus stabilitása Az entrópia szélsőérték-tulajdonsága és produkciója Feladatok Megjegyzések néhány szokásos fogalomra Az Onsager-elmélet A Prigogine-elv Kölcsönhatások termodinamikai vonatkozásai Entrópia és belső stabilitás Feladatok V. SPECIÁLIS RENDSZEREK TÖMEGCSERÉVEL Diffúziós folyamatok és fázisátalakulások Egy test adott környezetben Általános formulák Kényszer nélküli folyamatok Rögzített térfogat Állandó hőmérséklet
7 TARTALOMJEGYZÉK Állandó nyomás Hőszigetelés Félig áteresztő fal, rögzített térfogat Feladatok Két test adott környezetben Általános formulák Kényszermentes rendszer Rögzített együttes térfogat Rögzített együttes részecskeszám Rögzített együttes térfogat és részecskeszám Rögzített együttes térfogat, részecskeszám és belső energia Rögzített egyedi térfogatok, együttes részecskeszám és belső energia Állandó hőmérséklet, rögzített együttes térfogat és részecskeszám Állandó nyomás, rögzített össz-részecskeszám Rögzített össz-részecskeszám és együttes hőszigetelés Rögzített össz-részecskeszám, együttes hőszigetelés és állandó nyomás Rögzített össz-részecskeszám, együttes hőszigetelés és mechanikai szétválasztás Gázok lehűtése Feladatok Nullad- és másodrendű fázisátalakulások Elsőrendő fázisátalakulások Általános formulák Fázisátalakulás adott környezetben Fázisátalakulás a környezettől elszigetelve Tűlhűtés, túlhevítés VI. ÖSSZETETT ANYAGOK (ELEGYEK, KEVERÉKEK, OLDATOK) Konstitúciós függvények A koncentrációk Az összetett anyagok pontos meghatározása Jelölési megállapodás Kanonikus változók Entropikusság Egy hasznos formalizmus Állapotváltozás-jellemzők Feladatok Ideális elegyek Az ideális elegyek fogalma A tisztasági határfeltételek A reguláris tartomány Entropikus anyagok ideális elegye Ideális gázok ideális elegye
8 8 TARTALOMJEGYZÉK Azonos anyagok ideális elegye A Gibbs-paradoxon Feladatok Nem ideális elegyek Parciális nyomások, Henry-törvény Fugacitások, Lewis Randall-szabály Elegyítéssel kapcsolatos néhány jelenség Tapasztalati tények Az állapotmennyiségek változása Elegyítési hő Fagyáspont-csökkenés Ozmózis Feladatok Fázisok, fáziskapcsolatok Fázisok Fáziskapcsolatok Fázisfelületek Különböző elegyek fáziskapcsolatai Feladatok Elegycsaládok Az elegycsaládok meghatározása Kanonikus változók Entropikus elegycsaládok Feladatok Testek A testek meghatározása A teljes mennyiségek A teljes kanonikus változók Entropikusság a teljes kanonikus változókban Egy hasznos formalizmus Feladatok Termodinamikai erők Az értelmezés problémája A probléma megoldása Testek rendszere Pontos meghatározás Korlátozások Összefoglaló formulák Entropikus testek Egy test adott környezetben A leírás kerete Kényszermentes rendszer Szelektív átvándorlás, rögzített térfogat Szelektív átvándorlás Feladatok Két test adott környezetben A leírás általános kerete Rögzített összenergia és össztérfogat Szelektív átvándorlás, rögzített összenergia és egyedi térfogatok
9 TARTALOMJEGYZÉK Szelektív átvándorlás Túltelített oldatok Feladatok VII. KÉMIAI REAKCIÓK A kémiai reakciók jellemzői Bevezető gondolatok Sztöchiometriai tényezők A kémiai affinitás A reakció mértéke Entropikus test Feladatok A kémiai reakciók dinamikája A dinamikai egyenlet Termodinamikai erők Az affinitás szerepe Katalizátorok A tömeghatás törvénye Feladatok Reakcióhők Elszigetelt test energiaváltozása Rögzített térfogatú és hőmérsékletű test energiaváltozása Rögzített hőmérsékletű és nyomású test energiaváltozása Kémiai rekciók leírása Bevezető gondolatok A kémiai reakciók pontos meghatározása Az egyensúlyi és a disszipációs tulajdonság következményei Összefoglaló formulák Speciális kémiai reakciók Kényszer nélküli reakciók Állandó térfogat Állandó hőmérséklet Állandó nyomás Hőszigetelés Feladatok VIII. KIBŐVÍTETT KÖZÖNSÉGES TERMODINAMIKA Termodinamikai test és mechanikai test kölcsönhatása A leírás problémái Egy új dinamikai egyenlet Feladatok Kibővített termodinamikai testek és folyamataik Bevezető gondolatok A kibővített termodinamikai anyag és test Folyamatok leírása Feladat
10 10 TARTALOMJEGYZÉK 41. Egy test adott környezetben A dinamikai mennyiségek Az egyensúlyi tulajdonság A disszipációs tulajdonság A dinamikai egyenlet Kényszer nélküli folyamatok Izoterm folyamatok Adiabatikus folyamatok Izobár folyamatok A kibővített dinamikai egyenletek határesete Feladatok A kibővített közönséges termodinamika korlátai IX. ELEKTROMÁGNESES JELENSÉGEK A TERMODINAMIKÁBAN Elektromosan tölthető termodinamikai testek A töltött test potenciálja A töltött test nyomása A töltött test belső energiája Extenzív és intenzív mennyiségek A tölthető test pontos meghatározása Kanonikus változók Entropikusság Közönséges tölthető test Megjegyzések az entropikusságról Két szokásos feltétel Feladatok Elektromosan tölthető testek folyamatai Dinamikai egyenlet, dinamikai mennyiségek Egyensúlyi tulajdonság, termodinamikai erők Disszipációs tulajdonság Megjegyzések Tölthető test adott környezetben Általános feltételek Rögzített térfogat Állandó nyomás Állandó hőmérséklet Egyenáramok Feladatok Néhány fontos termoelektromos jelenség Alapfeltevések A Seebeck-hatás A Peltier-hatás A Thomson-hatás Megjegyzés Feladat Kvázistacionárius áramok Kibővített tölthető testek Folyamatok dinamikája
11 TARTALOMJEGYZÉK Egy speciális rendszer folyamatai Állandó külső potenciál Periodikus külső potenciál A váltóáram hőhatása Komplex ellenállás Feladatok Ionokból álló testek Elektromosan polározható testek A polározott test elektromos mezője Polározottság adott külső mezőben A polározottság molekuláris vonatkozásai A Clausius Mosotti-formula Az indukált polározottság fogalma A polározható test pontos meghatározása Kanonikus változók Entropikusság Közönséges polározható test Két szokásos feltétel Feladatok Az indukált polározottság Dielektromos testek A Langevin Weiss-féle indukált polározottság A Langevin-függvény tulajdonságai Feladatok Egyéb tudnivalók Egyensúlyi összefüggések Megjegyzések a szokásos tárgyalásokról Vektormennyiségek Feladatok Polározható testek folyamatai Dinamikai egyenlet, dinamikai mennyiségek Egyensúlyi tulajdonság, termodinamikai erők Disszipációs tulajdonság Elektrostrikció Speciális folyamatok Általános feltételek Rögzített térfogat Állandó nyomás Állandó hőmérséklet Feladatok Kibővített polározható testek Pontos meghatározás Folyamatok Egy speciális rendszer folyamatai Állandó illetve periodikus külső mező Komplex szuszceptancia Feladatok Mágnesezhető testek Mágnesezett test és mágneses mező A mágnesezettség molekuláris vonatkozásai
12 12 TARTALOMJEGYZÉK A Clausius Mosotti-formula A mágnesezhető test pontos meghatározása Kanonikus változók, entropikusság Közönséges mágnesezhető test Két szokásos feltétel Feladatok Az indukált mágnesezettség Diamágnesség és paramágnesség A Langevin Weiss-féle indukált mágnesezettég A Langevin Weiss-egyenlet közelítő megoldása A Langevin Weiss-egyenlet megoldásai Feladatok Mágnesezhető testek folyamatai Dinamikai egyenlet, dinamikai mennyiségek Egyensúlyi tulajdonság, termodinamikai erők Disszipációs tulajdonság Mágneses hűtés A negatív hőmérsékletről Speciális folyamatok Általános feltételek Rögzített térfogat Hiszterézis Elmélet és tapasztalat Feladatok Szupravezetés Szupravezető testek A paramágneses és a szupravezető tartomány összekapcsolódása Átmenet a paramágneses és a szupravezető tartomány között Feladat A hősugárzás Az elektromágneses sugárzás hőhatása Üregbe zárt állóhullámok A frekvencia-eloszlás A Planck-féle eloszlás A fekete test sugárzása Az elektromágneses sugárzás szerepe a hőátadásban Feladatok Táblázatok 363 Függelék 373
13 Előszó 1. Tagadhatatlan tény, hogy az elméleti fizikának egy ága annál megbízhatóbb, minél pontosabban tudja matematikai formába önteni mondanivalóját. A matematizálás lényege az, hogy a matematika nyelvén fogalmazzunk, matematikailag szabatos fogalmakat használjunk, küszöböljük ki a hallgatólagos megállapodásokat. A hallgatólagos megállapodás természetesnek vett, magától értetődő, mindenki számára nyilvánvaló, pontosan körül nem határolt fogalmat, tulajdonságot, tényt jelent. Általában ezek az elmélet zavarainak, a félreértéseknek a forrásai. Ugyanis egyrészt különféle vonatkozásokban különféleképpen értelmezik a nyilvánvaló tulajdonságokat, másrészt előfordulhat, hogy a természetesnek vett tulajdonságok ellentmondanak egymásnak. Hallgatólagos megállapodás volt a régebbi matematikában a halmaz fogalma, ezen belül az összes halmazok halmaza, meg az a két természetes tény, hogy 1. két halmazban akkor van ugyanannyi elem, ha az egyik halmaz elemei kölcsönösen egyértelműen megfeleltethetők a másik halmaz elemeinek, 2. egy halmaz valódi részhalmazában kevesebb elem van, mint a halmazban. Ma már halmazelmélet pontos logikai felépítése birtokában jól tudjuk, hogy az összes halmazok halmaza nem létezik, és az említett két tény egyszerre nem állhat fenn: vagy az egyiket fogadjuk el, vagy a másikat (szokásosan az 1. tulajdonságot építjük be a halmazelméletbe). Persze nem minden hallgatólagos megállapodás félrevezető, de csak abban az elméletben bízhatunk meg, amelyben nincsenek ilyenek. A klasszikus mechanika, a kvantummechanika, a klasszikus elektromágnesség matematikailag fejlett ágai a fizikának és többnyire jól működnek, noha ezek az elméletek sem mentesek hallgatólagos megállapodásoktól. Mindezekkel éles ellentétben áll a termodinamika, amelyre éppen a hallgatólagos megállapodások kusza és sokszor ellentmondásos rendszere a jellemző, amint azt a következők jól mutatják. 2. A szokásos termodinamikában az egyensúly alapvető fogalom, sokszor hangsúlyozzák is, hogy minden egyéb termodinamikai fogalomnak például hőmérsékletnek csak egyensúlyban van értelme. Az egyensúly magától értetődő fogalom, mindenki tudja, mi az. Ha egy kicsit is odafigyelünk azonban, hamar észrevehetjük, hogy különféle értelemben használják ugyanazt a szót. Szerepel egy test egyensúlya, meg az is, hogy két test egyensúlyban van egymással. Persze ez annyira megszokott, hogy az olvasó talán észre sem veszi, mi itt a baj. Cseréljük ki a test és egyensúly szót másra, és mindjárt kiviláglik, hogy valami nincs rendjén: egy ember betegsége, két ember betegségben van egymással. Az egyensúly hallgatólagosan elfogadott tulajdonságai közé tartozik, hogy időben állandó, változatlan. Továbbá néhány egyszerű, hétköznapi megfigyelés alapján az egyensúlyok alapvető tulajdonságait a termodinamika nulladik 13
14 14 ELŐSZÓ főtételeként fogalmazzák meg: minden kölcsönhatáshoz tartozik egy intenzív állapotjelző, amelynek számszerű egyenlősége a kölcsönhatásban álló rendszerek egyensúlyának szükséges és elégséges feltétele. Ebből azt következtetik, hogy mivel a mondottak igazak a test bármely két részére is egy test egyensúlyának szükséges és elégséges feltétele az intenzív mennyiségek homogén eloszlása (vagyis azonos értéke a test minden pontjában). Ez azonban nem igaz, amint azt a következő példák mutatják. Egyszerű tény, hogy itt a Földön egy edénybe zárt nyugvó gáz (folyadék) nyomása nem homogén: lenn nagyobb, mint fenn (a hidrosztatikus nyomás miatt). A homogén eloszlás tehát kívülről eredő térfogati (azaz sűrűséggel arányos) erőhatás jelenlétében általában nem igaz. Egy elektromosan azonosan töltött részecskékből álló, gömb alakú nyugvó edénybe zárt gáz egyensúlyában a nyomás nem homogén eloszlású: a középponttól kifelé haladva növekszik, amint azt egyszerű elektrosztatikai és mechanikai számításokkal ellenőrizni lehet. A homogén eloszlás tehát belső térfogati erőhatás jelenlétében sem feltétlenül igaz. Vegyünk egy felfújt gumilabdát, amely nyugszik a levegőben, és tekintsünk el a gravitációs hatástól. Itt három test van egyensúlyban: a labdában levő levegő, a gumiburok és a kinti levegő, ezek nyomása azonban mind más. A benti levegő nyomása nagyobb, mint a kintié: megegyezik a kinti légnyomás és a gumi nyomásának összegével. Ez a furcsaság úgy valósul meg, hogy a gumi nyomása nem homogén eloszlású: a benti felületén nagyobb, mint a kinti felületén. A gumiburokra sem külső sem belső térfogati erő nem hat. A homogén eloszlás tehát külső és belső térfogati erőhatás híján sem szükségképpen igaz. Az előbbi példákban mindig kimondtuk, hogy a szóban forgó test nyugszik (értelemszerűen a Földhöz képest, amelyet tehetetlenségi rendszernek tekintettünk). Nem nehéz látni, hogy az egyensúly relatív, azaz vonatkoztatási rendszertől függő fogalom: nem mindegy, hogy a test mihez képest van nyugalomban. Nyugodjék egy semleges gázt tartalmazó edény egy forgó lemezjátszó korongján vagy körhintán, és tekintsünk el a gravitációs hatástól. A nyomás ismét nem lesz homogén eloszlású egyensúlyban: a forgás tengelyétől távolabbi részen nagyobb, mint a közelebbi részen. A homogén eloszlás tehát nem-tehetetlenségi rendszerhez viszonyított egyensúlyban sem mindenképppen igaz. Végül jegyezzük meg, hogy az egyensúly szükséges és elégséges feltételéül kimondott homogenitási tétel szerint egy test, amelynek a hőmérséklete és a nyomása minden pillanatban homogén eloszlású (vagy két kölcsönható test, amelyek hőmérséklete és nyomása minden pillanatban megegyezik), de változik az időben, egyensúlyban volna, amit viszont kizár az egyensúlyról alkotott másik hallgatólagos megállapodás: az egyensúlyban semmiféle változás nincs. 3. Egyszerű példák mutatják tehát, hogy a termodinamika nulladik főtétele általában nem teljesül. Ennek alapján megrendülhet a bizalmunk: vajon mennyire igaz az első és a második főtétel? Tovább növekszik a bizalmatlanságunk, amikor észrevesszük, hogy ezek megfogalmazásához szükség van állapotváltozásokra azaz nem-egyensúlyokra, noha a szokásos termodinamika csak az egyensúlyokat ismeri el értelmesnek. E nehézség áthidalására bevezetik a kvázisztatikus folyamat fogalmát; ez olyan folyamat, amelyben a test (rendszer) mindig egyensúlyban van: a kvázisztatikus folyamat egyensúlyok egymásutánja. Hiába említik meg, hogy természetesen a valóságban ilyen folyamat nincs, ez csak ideális határeset, amelyet azonban annál jobban megközelítünk, minél
15 15 lassúbb a változás, kételyeink támadnak, vajjon helyes-e ez az idealizáció. Tekintsünk ugyanis ennek a mechanikai megfelelőjét: egy test egyensúlyban van, ha a helyzete nem változik, a sebessége nulla (például áll egy vízszintes síkon). Vigyük el a testet egy egyensúlyából egy másikba úgy, hogy menet közben mindig közelítőleg egyensúlyban legyen, azaz nagyon lassan. Ezt megtehetjük bármilyen lassan, de a kvázisztatikus határesetben amikor mindig nulla a sebessége nincs valóságos változás. Vajon nem fából vaskarika-e a kvázisztatikus folyamat? Az első főtétel, majd látjuk, lényegében a szokásos formában helytálló. Azonban a második főtétel sokféle és nehezen megfogható alakja, a vele kapcsolatos félreértések megerősítik a gyanúnkat, hogy az elmélet itt is a hallgatólagos megállapodásoknak az áldozata. Érdemes idézni a második főtétel néhány formáját. Az eredeti, régebbi megfogalmazások: Kelvin Planck-féle: Nincs olyan periodikusan működő gép (nem létezik olyan körfolyamat), amely pusztán hőfelvétellel munkát végezne, Nincs olyan folyamat, amelynek egyetlen eredménye az, hogy hő teljes egészében munkává alakult. Clausius-féle: A hő önként sohasem áramlik a hidegebb helyről a melegebb felé, Nincs olyan folyamat, amelynek egyetlen eredménye az, hogy hő jutott át egy hidegebb testről egy melegebbre. Olykor bebizonyítják, hogy a fenti állítások egyenértékűek egymással; a pontban rávilágítunk az ilyen bizonyítás hibájára, és a pontban megmutatjuk, egyáltalán nem egyenértékű az a két kijelentés, hogy a hő sohasem alakítható tökéletesen munkává, és hogy a hő a melegebb hely felől áramlik a hidegebb felé. Egyes újabb megfogalmazások a nulladik főtételen alapszanak, amely, láttuk, nem igaz: Szigetelt rendszerben az inhomogenitások által létrehozott makroszkopikus folyamatok (spontán folyamatok) mindig csökkentik a rendszerben levő inhomogenitásokat. Hatásukra a rendszer egyensúlyi állapothoz közeledik. Ez a kiegyenlítődésre való törekvés a termodinamika második főtétele. A termodinamikai folyamatok irányát megszabó törvény: a jellemző intenzív mennyiségekben fennálló inhomogenitások kiegyenlítődésre törekednek, aminek kapcsán az extenzív mennyiségek olyan irányba áramlanak, amerre a homogenizálódást elősegítik. Carnot megfogalmazására alapozva, amely szerint 1. Minden termodinamikai rendszernek van egy (entrópiának nevezett) S állapotfüggvénye, és ezzel infinitezimális kvázisztatikus állapotváltozás esetén a rendszer által felvett hőre δq T ds teljesül, ahol egyenlőség csak reverzibilis folyamatokra áll fenn. 2. Zárt rendszerek entrópiája sohasem csökkenhet, a második főtételt mostanában leggyakrabban az entrópia segítségével mondják ki:
16 16 ELŐSZÓ Szigetelt rendszerben a stabil egyensúly elérésével az entrópiának maximuma van. Zárt rendszer entrópiája egyensúlyi állapotban maximális. Szigetelt rendszerben lejátszódó spontán folyamatok mindig csak olyan irányúak lehetnek, amelyek hatására a rendszer entrópiája nő. Többnyire egyenértékűnek tekintik az egyensúlyi állapotra vonatkozó entrópia-maximumot és az entrópia növekedését nem-egyensúlyi folyamatokban. Érdemes megemlíteni, hogy Fényes Imre magyar fizikus mutatta ki igen világosan, hogy ez nem igaz, ami nagyon jól látszik a mi tárgyalásunkból is (lásd és ). Az idézett megfogalmazások hiányosságait is azonnal látjuk. A szigetelt vagy zárt rendszer, a spontán folyamat, a folyamat iránya: ez mind hallgatólagos megállapodás, a második főtételnek ezekre hivatkozó formái teljesen megfoghatatlanok. Továbbá az egyensúlyi entrópia maximumának csak úgy van értelme, hogy nem-egyensúlyok entrópiájával hasonlítjuk össze, amik viszont az adott tárgyalásban értelmetlenek. Még inkább az elméleten kívüli objektumokra utal az entrópianövekedés törvénye. Itt érdemes megemlíteni H. B. Callen Thermodynamics c. könyvét, amelyben az entrópiamaximum említett hiányosságát formailag kiköszöbölte azáltal, hogy bevezette a belső kényszerekkel megvalósult egyensúlyokat, és az entrópiamaximumot a kényszermentes állapotra követelte meg. Ugyanakkor viszont magától értetődőnek vette, hogy a belső kényszerek feloldása olyan folyamatot indít el, amelyben az entrópia nő. Végül de nem utolsósorban megjegyezzük, a második főtétel ilyen megfogalmazásai természetellenesen féloldalasak: csak zárt (szigetelt) rendszerre vonatkoznak; elvárnánk például tapasztalataink is erre utalnak, hogy nem zárt rendszerekre is tudjunk mondani valamit a folyamatok irányáról. 4. A második főtételt mindegy miként fogalmazzák meg az irreverzibilitás törvényének tekintik. Érdemes erről is idéznünk szokásos fizikakönyvekből. Reverzibilis folyamatoknál az állapothatározók változásának az iránya nincsen meghatározva, tehát a folyamat megfordítható, minden irányban egyformán végbemehet. Az irreverzibilis vagy meg nem fordítható folyamatok esetében az állapothatározók változása korlátozott, a folyamat spontán csak az egyik irányban mehet végbe. Ha egy termodinamikai rendszer állapota oly módon változik meg, hogy található egy olyan folyamat, amely a közbülső állapotoknak ugyanazon a sorozatán fut le, de időben ellentétes irányban, akkor a folyamat reverzibilis, egyébként irreverzibilis. Ezek a kijelentések (állítások vagy meghatározások?) is megfoghatatlanok, semmitmondók: nincs körülhatárolva a lehetséges folyamatok, ezen belül a spontán folyamatok összessége, a folyamatok időbeli lefutása, mit jelent az, hogy egy folyamat valamely irányban végbemehet, stb. A reverzibilitást gyakran az időtükrözésre való invarianciával azonosítják, és megállapítják, hogy egy tisztán mechanikai folyamat mindig reverzibilis, minthogy a Newton-egyenlet invariáns az időtükrözésre. Ezzel kapcsolatban két megjegyzést kell tennünk. Az első az időtükrözés és a fenti reverzibilitás-definíció kapcsolatára vonatkozik. Az időtükrözött mechanikai folyamatban mindenki látja, hogy a
17 17 folyamat ugyanazokon az állapotokon fut végig ellentétes irányban. Nézzük például a Föld keringését a Nap körül. Látjuk (lelki szemünkkel) az ellipszispályát, amint halad rajta a Föld. Tükrözzük ezt a mozgást az időben: a Föld ellentétes irányban megy ugyanazon az ellipszispályán. Csakhogy egy mechanikai állapot nem egyszerűen a helyzet, hanem a helyzet és az impulzus együttese: a folyamat a fázistérben halad. Ha a tükrözött folyamat helyzete egy pillanatban megegyezik valamely eredeti helyzettel, akkor a tükrözött folyamat impulzusa nem egyezik meg a megfelelő eredeti impulzusal, hanem azzal ellentétes. A tükrözött folyamat nem ugyanazokon az állapotokon fut végig ellentétes irányban. Az időtükrözésre való invariancia nem fejezi ki az elképzelt reverzibilitás-fogalmat. A második arra vonatkozik, hogy kétséges, van-e egymáshoz köze egyáltalán az időtükrözésnek és a reverzibilitásnak. A reverzibilitásról még csak elképzeléseink vannak, még nem tudjuk, pontosan mi az, de úgy érezzük, nem lehet megfigyelőtől függő fogalom. Az időtükrözésre pontos definíciónk van, és azt is tudjuk, hogy megfigyelőtől függő fogalom. Anélkül, hogy ezt pontosan kifejtenénk, az előző példával szemléltetjük. Nézze valaki egy a Naphoz képest állandó sebességgel mozgó űrhajóból a Földet: azt látja, hogy a Föld egy mondjuk jobbmenetes spirális pályán halad előre. Tükrözi a mozgást: a Föld ugyanazon a pályán halad visszafelé. Az előzőekben tárgyalt, a Naphoz képest nyugvó megfigyelő szerint tükrözött mozgást viszont úgy látja, hogy a Föld egy balmenetes spirálison halad előre. 5. A fizika jól működő ágaiban klasszikus mechanikában, elektromágnességben, kvantummechanikában az alapvető fogalom a folyamat, amely egy differenciálegyenlet a Newton-egyenlet, a Maxwell-egyenletek, a Schrödingeregyenlet megoldásaként van értelmezve. Az egyensúlyok speciális, időben változatlan folyamatok. A folyamatok, speciálisan az egyensúlyok, jól meghatározott matematikai objektumok. A termodinamikában is felbukkannak valóságos, időben változó folyamatok az egyensúly közelében ; ezeket az úgynevezett Onsager-féle elmélet tárgyalja. Minthogy a nem-egyensúlyok nem értelmesek a termodinamikában, jól mutatja az Onsager-elmélet hiányosságait a következő kérdés: mik azok a nem értelmes objektumok, amelyek közel vannak az értelmeshez és milyen értelemben vannak közel? A termodinamika akkor nő fel a fizika többi ágához, ha úgy fogalmazzuk meg, hogy alapvető fogalma a folyamat, amelyet valamely differenciélegyenlet határoz meg. Ehhez először is túl kell lépnünk azon a beidegződésen, hogy a mennyiségeknek például a hőmérsékletnek csak egyensúlyban van értelme. A fizika majd minden mennyiségének mérési utasítása lassú változásra azaz közel egyensúlyra vonatkozik. Gondoljunk például az elektromos mező mérésére: meg kell határoznunk egy próbatöltésre ható erőt. Ilyen módon bizony ki nem mérjük az elektromos mezőt egy fénysugárban, de ez nem tart vissza minket attól, hogy a fénysugárban az elektromos mezőt értelmes létező mennyiségnek tartsuk. Hasonlóképpen elfogadhatjuk, hogy a hőmérséklet létező mennyiség nem-egyensúlyi folyamatokban is. Az úgynevezett kontinuum-termodinamika különféle elméletei jobb volna talán a kontinuum-fizika elnevezés, hiszen ez termodinamikai és mechanikai, esetleg elektromágneses stb. jelenségek együttesét írja le a fizika említett jól működő ágaival egyenrangú. Itt a testeket jellemző mennyiségeket pontról-pont-
18 18 ELŐSZÓ ra és időről-időre változónak tekintjük, a folyamat tehát a téridőben értelmezett valamely függvény, amelyet egy parciális differenciálegyenlet, az úgynevezett mérlegegyenletek rendszere határoz meg. Ennek az elméletnek csak technikai árnyoldala van: matematikailag meglehetősen bonyolult. Ha a kontinuum-fizikában figyelmen kívül hagyjuk a termodinamikai jelenségeket, akkor a kontinuum-mechanikára (deformálható testek mechanikájára) jutunk. Ezzel tulajdonképpen minden mechanikai jelenség leírható; bizonyos speciális esetekben amikor a deformáció elhanyagolható azonban a kontinuum-leírás feleslegesen bonyolult, és jól helyettesíthetjük egy sokkal egyszerűbbel, amelyben a testet merevnek tekintjük, és így parciális differenciálegyenlet helyett közönséges differenciálegyenlettel dolgozhatunk. Jól tudjuk persze, hogy a valóságban a test sohasem merev, erőhatásra mindig deformálódik, de ezt most elhanyagoljuk. Éppen ebben áll a modell-alkotás művészete: megtalálni azt a legegyszerűbb leírást, amely még jól tükrözi a valóságot. 6. A szokásos termodinamika helyes megfogalmazását amelyet közönséges termodinamikának hívunk a mechanika analógiájára érthetjük meg a fentiek szerint. Ha a jelenségek bizonyos körét elhanyagoljuk és a testeket homogénnek tekintjük (vagyis a testet jellemző bármely mennyiség ugyanazt az értéket mutatja a test minden pontjában), akkor a kontinuum-fizikai leírást helyettesíthetjük egy olyannal, amelyben a folyamatokat közönséges differenciálegyenlettel határozzuk meg. Láttuk, az egyensúlyt a szokásos termodinamikában a mennyiségek homogén eloszlásával azonosítják (helytelenül), és az ottani kvázisztatikus folyamat olyan, hogy a test minden pillanatban egyensúlyban van. Mondjunk most egyensúly helyett homogén eloszlást, és máris értelmet nyer a kvázisztatikus folyamat: olyan folyamat, amelyben minden mennyiség minden pillanatban homogén eloszlású. A kvázisztatikus jelző kompromittálódása miatt használjuk inkább a homogén folyamat elnevezést. Homogén folyamatokban a test tulajdonságai csak az időben változnak, a térben nem. A közönséges termodinamika tehát arra a feltételezésre épül, hogy a mennyiségek homogén eloszlásúak a folyamatok során. Láttuk, hogy ez még egyensúly esetén sem feltétlenül teljesül, ami azonban nem jelenti azt, hogy az elmélet értéktelen vagy hiábavaló. Mindössze azt kell jól látnunk, hogy csak bizonyos esetekben alkalmazható, mint minden elmélet. Felhívjuk a figyelmet, nem tartozik az elmélethez annak a kérdésnek a megválaszolása, hogy mikor ad jó leírást, azaz milyen körülmények között kapunk jó eredményeket azzal a feltevéssel, hogy a testek homogének; ugyanúgy, mint ahogy a merevtest-modell vagy a tömegpont-modell keretein is kívül esik az, hogy mikor tekinthető egy test merevnek, illetve pontszerűnek.
19 Bevezetés 1. Tudjuk jól, hogy a minket körülvevő testek mindegyike néhányszor molekulából áll, amelyek űzik, vonzzák, taszítják egymást, közben állandóan elektromágneses sugárzást bocsátanak ki és nyelnek el. Ez a kavargó, nyüzsgő, lármás belső élet kifelé többnyire egységes, csendes, viszonylagos nyugalomként jelentkezik, amit úgy foghatunk fel, hogy a mikroszkopikus tömegjelenségek nagyrészt kiegyensúlyozzák egymást és csak az átlaguk jelenik meg makroszkopikus szinten. A kontinuum-fizika az ilyen átlagos viselkedések leírásának az elmélete. Ahhoz, hogy a közönséges termodinamikát megértsük, képet kell alkotnunk a kontinuum-fizikáról. 2. Tekintsünk egy testet, amely azonos semleges molekulákból (atomokból) áll. Persze a semleges molekulák is elektromosan töltött részecskékből tevődnek össze, amelyek elektromos sugárzást bocsátanak ki és nyelnek el létezésük során, tehát az elektromágnesség ekkor is jelentős tényezője a molekulák együttesének. A test állapotára jellemző a molekulák átlagos sebessége. Gondoljuk el például, hogy a test (egy pohár víz) nyugszik hozzánk képest. Ekkor nagyban azt tapasztaljuk, hogy a test minden pontja nyugszik hozzánk képest: a test által kitöltött térrész minden pontjában és minden pillanatban az átlagsebesség nulla hozzánk viszonyítva. A Brown-mozgásról szerzett tapasztalatain alapján tudjuk, hogy ez valóban csak az átlagsebesség. A megkavart víz áramlani fog a pohárban, és az áramlást a test által kitöltött térrész pontjaiban megjelenő (átlagos) sebesség jellemzi, amely persze az időnek is függvénye. Látjuk tehát, hogy a test (kontinuum) áramlását, nyugalmát tér- és időpontokhoz rendelt sebességértékekkel jellemezhetjük. Nyugalom és áramlás relatív (megfigyelőtől függő) fogalmak (ami hozzánk képest nyugalom, az máshoz képest áramlás); a mögöttük levő abszolút (megfigyelőtől független) fogalom a létezés. Végül is megállapíthatjuk, hogy a kontinuum létezését a téridőben értelmezett (abszolút) sebesség értékű függvénnyel írhatjuk le, amelyet sebességmezőnek hívunk. A testre jellemző a sűrűsége is, vagyis az egységnyi térfogatban található anyagmennyiség azaz tömeg. A sűrűség általában pontonként és időpillanatonként változik, tehát a sűrűséget is a téridőben értelmezett függvénynek fogjuk fel. Nézzük továbbra is egy megfigyelő szempotjából a kontinuum áramlását. Az áramlásban tömeg, impulzus és energia kerül át egyik helyről a másikra. A tömeg, impulzus és energia megmaradását úgynevezett mérlegegyenletekkel fejezzük ki: egy térrészben levő mennyiség változása egyenlő a térrészből ki- illetve beáramlott mennyiséggel. A mennyiségek áramának két fajtáját különböztetjük meg: a szállítási (konvektív) és vezetési (konduktív) áramot. A szállítási áram a makroszkopikus mozgással, tehát a sebességmezővel kapcsolatos, a vezetési áram a mikroszkopikus mozgással kapcsolatos. Világos, hogy ha a test egy része 19
20 20 BEVEZETÉS egy helyről átkerül egy másik helyre, akkor tömeg és vele együtt impulzus és energia is szállítódik. Viszont áramlás nélkül is továbbítódhat impulzus és energia: a molekulák a mikroszkopikus mozgásuk folytán lökdösik egymást, ezzel impulzust és energiát adnak át egymásnak; elektromágneses sugárzást bocsátanak ki és nyelnek el, és ezzel is juthat impulzus és energia a test egyik részéből a másikba. Így jön létre a vezetési áram. Az áramokat tér- és időpontonként az adott pillanatban a tér pontjába helyezett egységnyi felületen az időegység alatt átáramlott mennyiséggel jellemezzük (ezt pontosabb matematikai formába is önthetjük, de nem lesz rá szükségünk), tehát ezek is a téridőben értelmezett különféle értékű függvények. A szállítási áram az adott mennyiség tömeg, impulzus és energia sűrűségének és a sebességmezőnek a szorzata. A tömeg sűrűségéről már szóltunk. Az impulzus sűrűsége a tömegsűrűség és a sebességmező szorzata: a molekulák mikroszkopikus mozgása nulla eredő impulzust ad. Egészen más a helyzet az energiával: a molekulák mikroszkopikus mozgása jelentős járulékot ad az energiasűrűségben. Az energiasűrűséget két részre bonthatjuk: egyrészt a makroszkopikus mozgási energia sűrűségére, amely a tömegsűrűség és a sebességmező négyzetének szorzata osztva kettővel, másrészt a belső energia sűrűségére, amely a mikroszkopikus mozgási energiából, a molekulák kölcsönhatási energiájából és a molekulák kémiai energiájából tevődik össze. A belső energia sűrűsége is a testre jellemző mennyiség. A vezetési áramok szintén jellemzők a testre. A mondottakból nyilvánvaló, hogy a tömegnek nincs vezetési árama. Az impulzus vezetési árama nem más, mint a nyomástenzor: az egységnyi felületen időegység alatt átadott impulzus éppen az egységnyi felületre ható erő. A belső energia vezetési áramát hőáramnak hívjuk, mert a szokásos hővezetés vagy hőátadás nem más, mint belső energia vezetési áramlása. Fogadjuk el ugyanis azt a durva képet, hogy a hőmérséklet a molekulák mikroszkopikus mozgási energiájával arányos. Egymásra teszünk két különböző hőmérsékletű testet. Az érintkezési felületen ütköznek a két test molekulái; a nagyobb hőmérsékletű test gyorsabb mikroszkopikus mozgást végző molekulái az ütközések során energiát adnak át a kisebb hőmérsékletű test lassabb molekuláinak. Belső energia vezetődött át az egyik testből a másikba, amit a szokásos makroszkopikus nézőpontból úgy fogalmazunk meg, hogy hő áramlott az egyik testből a másikba. 3. Célszerű a továbbaik miatt a tömegsűrűség helyett annak reciprokát használni, amely a tömegegységre eső térfogat, szokásos kifejezéssel a fajlagos térfogat. Ugyanakkor a belső energia sűrűsége helyett a tömegegységre eső belső energiát, a fajlagos belső energiát vesszük, ami nem más, mint a belső energia sűrűségének és a tömegsűrűségnek a hányadosa. Legyen e, u, v, k és P rendre a fajlagos belső energia, a sebességmező, a fajlagos térfogat, a hőáram és a nyomástenzor; ne feledjük, mindezek a tér időben értelmezett függvények, és hozzátesszük még, hogy nem-relativisztikus elméletet tekintünk. Az energia, az impulzus és a tömeg mérlegegyenlete (nem részletezzük, hogyan) rendre a D u e = v( k + P : u) D u u = v P D u v =v u
21 21 összefüggésre vezet. Itt D u az u sebességmező irányú deriváltat jelöli, amelyet szokásosan szubsztanciális időderiváltnak neveznek, mert a sebességmező által jellemzett testhez képesti időbeli változást írja le; a térszerű differenciálás, a pont vektorok skalárszorzatát, a kettőspont tenzorok skalárszorzatát jelöli. Mindezeket pontosabban is kifejthetnénk, de nem lesz rá szükségünk: a fenti egyenletek csak bizonyos motivációkhoz kellenek. Rögtön láthatjuk, hogy több az ismeretlen, mint az egyenlet: az egyértelmű megoldáshoz további összefüggések kellenek. Fogadjuk most el, hogy a kontinuum folyamatát egyértelműen jellemzik az egyenletek bal oldalán álló mennyiségek, azaz (e, u, v). Ekkor P-t és k-t meg kell és meg is lehet adni (e, u, v) függvényében, így az egyenletek és ismeretlenek száma meg fog egyezni (ami persze még csak reményt ad az egyértelmű megoldhatósághoz). 4. Azonkívül, hogy a belső energia áramát hőáramnak nevezzük, még nem látszik, miként vonatkoznak a fentiek a hőjelenségekre, hiszen az összes eddig bevezetett mennyiség mechanikai alapokon nyugszik. A hőáram-elnevezés indoklását úgy szemléltettük, hogy valamilyen kapcsolatot tételeztünk fel a hőmérséklet és a belső energia között. Valóban ez az a pont, ahol a hőjelenségek belépnek a fenti egyenletekbe. Közelebbről: a belső energia, noha szemléletes jelentése van, nem közvetlenül mérhető mennyiség. Helyette a T hőmérséklet áll a rendelkezésünkre. A hőmérséklet szerepel a vezetési áramok megadásában is. Gondoljunk például arra, hogy a gázok P sztatikus nyomása (amely része a nyomástenzornak) a fajlagos térfogattal és a hőmérséklettel ideális esetben P mv = kt formában áll kapcsolatban, ahol m egy molekula tömege és k a Boltzmann-állandó. Hasonlóképpen, azt a tapasztalatunkat, hogy a hő melegebb helyről a hidegebb felé áramlik a hőáramra vonatkozó k = λ T Fourier-féle összefüggéssel fejezhetjük ki, ahol λ pozitív állandó. Úgy bonyolódik tehát a helyzet, hogy a vezetési áramokat nem az (e, u, v) folyamat függvényében tudjuk természetes módon kifejezni, hanem (T, u, v) függvényében. Ugyanakkor persze kell egy kapcsolat T és e között is; pontosabban e-t kell előállítanunk (T, u, v) függvényében. 5. A termodinamika szokásos nulladik és második főtételének jelentése és igaz volta, láttuk az előszóban, bizonytalan. Ezzel szemben az első főtétel lényegében a szokásos formájában is helytálló. A belső energia fenti mérlegegyenletében felismerhetjük a termodinamika első főtételét: a belső energia változása a v k hőátadás és a vp : u munkavégzés eredményeként jön létre. Még közelebb jutunk az ismert formulához, ha feltesszük, hogy P = P I, ahol P a gázok vagy folyadékok szokásos rugalmas nyomása és I az egységtenzor (identitás). Ekkor ugyanis vp : u = vp u = P D u v. A mérlegegyenletek csak a kontinuumban azaz a test belsejében történő változást írják le pontról pontra; a test felületével kapcsolatos jelenségeket például hőelvezetést a testről matematikailag határfeltételekkel vesszük figyelembe. Ha csak a test egészét tekintjük, azaz például nem érdekel minket, hogyan oszlik el az energia a testen belül, csak az, mennyi a test összenergiája, akkor az energiára vonatkozó mérlegegyenlet integrálásával és a határfeltételek figyelembevételével azt kapjuk, hogy a test t 2 és t 1 pillanatbeli E(t 2 ) illetve E(t 1 ) energiájának különbsége megegyezik a [t 1, t 2 ] intervallumban a testnek hővezetés útján átadott Q(t 1, t 2 ) belső energia, a testen végzett W (t 1, t 2 ) munka és a test tömegének megváltozása (a testből való ki- és beáramlás) miatti L(t 1, t 2 )
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai
 3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
Termodinamika (Hőtan)
 Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
2. (d) Hővezetési problémák II. főtétel - termoelektromosság
 2. (d) Hővezetési problémák II. főtétel - termoelektromosság Utolsó módosítás: 2015. március 10. Kezdeti érték nélküli problémák (1) 1 A fél-végtelen közeg a Az x=0 pontban a tartományban helyezkedik el.
2. (d) Hővezetési problémák II. főtétel - termoelektromosság Utolsó módosítás: 2015. március 10. Kezdeti érték nélküli problémák (1) 1 A fél-végtelen közeg a Az x=0 pontban a tartományban helyezkedik el.
K oz ons eges termodinamika Matolcsi Tam as 2010
 Közönséges termodinamika Matolcsi Tamás 2010 2 Tartalomjegyzék Előszó 7 I. EGYSZERŰ ANYAGOK ÉS TESTEK 17 1. Konstitúciós függvények..................... 17 1.1. Az alapvető termodinamikai mennyiségek.........
Közönséges termodinamika Matolcsi Tamás 2010 2 Tartalomjegyzék Előszó 7 I. EGYSZERŰ ANYAGOK ÉS TESTEK 17 1. Konstitúciós függvények..................... 17 1.1. Az alapvető termodinamikai mennyiségek.........
Műszaki hőtan I. ellenőrző kérdések
 Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
Előszó.. Bevezetés. 1. A fizikai megismerés alapjai Tér is idő. Hosszúság- és időmérés.
 SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK
 ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
A TERMODINAMIKA I. AXIÓMÁJA. Egyszerű rendszerek egyensúlya. Első észrevétel: egyszerű rendszerekről beszélünk.
 A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont)
 Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
Hőtan I. főtétele tesztek
 Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Kérdések Fizika112. Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika
 Kérdések Fizika112 Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika 1. Adjuk meg egy tömegpontra ható centrifugális erő nagyságát és irányát!
Kérdések Fizika112 Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika 1. Adjuk meg egy tömegpontra ható centrifugális erő nagyságát és irányát!
Követelmények: f - részvétel az előadások 67 %-án - 3 db érvényes ZH (min. 50%) - 4 elfogadott laborjegyzőkönyv
 Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Légköri termodinamika
 Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
A munkavégzés a rendszer és a környezete közötti energiacserének a D hőátadástól eltérő valamennyi más formája.
 11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
11. Transzportfolyamatok termodinamikai vonatkozásai 1 Melyik állítás HMIS a felsoroltak közül? mechanikában minden súrlódásmentes folyamat irreverzibilis. disszipatív folyamatok irreverzibilisek. hőmennyiség
Molekuláris dinamika I. 10. előadás
 Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
A gáz halmazállapot. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Fizika feladatok. 1. Feladatok a termodinamika tárgyköréből november 28. Hővezetés, hőterjedés sugárzással. Ideális gázok állapotegyenlete
 Fizika feladatok 2014. november 28. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-23) Határozzuk meg egy 20 cm hosszú, 4 cm átmérőjű hengeres vörösréz
Fizika feladatok 2014. november 28. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-23) Határozzuk meg egy 20 cm hosszú, 4 cm átmérőjű hengeres vörösréz
Termodinamika. Belső energia
 Termodinamika Belső energia Egy rendszer belső energiáját az alkotó részecskék mozgási energiájának és a részecskék közötti kölcsönhatásból származó potenciális energiák teljes összegeként határozhatjuk
Termodinamika Belső energia Egy rendszer belső energiáját az alkotó részecskék mozgási energiájának és a részecskék közötti kölcsönhatásból származó potenciális energiák teljes összegeként határozhatjuk
6. Termodinamikai egyensúlyok és a folyamatok iránya
 6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
6. ermodinamikai egyensúlyok és a folyamatok iránya A természetben végbemenő folyamatok kizárólagos termodinamikai hajtóereje az entróia növekedése. Minden makroszkoikusan észlelhető folyamatban a rendszer
f = n - F ELTE II. Fizikus 2005/2006 I. félév
 ELTE II. Fizikus 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 2. (X. 25) Gibbs féle fázisszabály (0-dik fıtétel alkalmazása) Intenzív állapotothatározók száma közötti összefüggés: A szabad intenzív paraméterek
ELTE II. Fizikus 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 2. (X. 25) Gibbs féle fázisszabály (0-dik fıtétel alkalmazása) Intenzív állapotothatározók száma közötti összefüggés: A szabad intenzív paraméterek
Belső energia, hőmennyiség, munka Hőtan főtételei
 Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
1. Feladatok a termodinamika tárgyköréből
 . Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
Osztályozó vizsga anyagok. Fizika
 Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás Hőáramlás (konvekció) olyan folyamat,
 2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
Molekuláris dinamika. 10. előadás
 Molekuláris dinamika 10. előadás Mirőlis szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten? Hogyan tudjuk megérteni a folyadékok, gázok, szilárdtestek makroszkópikus
Molekuláris dinamika 10. előadás Mirőlis szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten? Hogyan tudjuk megérteni a folyadékok, gázok, szilárdtestek makroszkópikus
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok
 Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Vizsgatémakörök fizikából A vizsga minden esetben két részből áll: Írásbeli feladatsor (70%) Szóbeli felelet (30%)
 Vizsgatémakörök fizikából A vizsga minden esetben két részből áll: Írásbeli feladatsor (70%) Szóbeli felelet (30%) A vizsga értékelése: Elégtelen: ha az írásbeli és a szóbeli rész összesen nem éri el a
Vizsgatémakörök fizikából A vizsga minden esetben két részből áll: Írásbeli feladatsor (70%) Szóbeli felelet (30%) A vizsga értékelése: Elégtelen: ha az írásbeli és a szóbeli rész összesen nem éri el a
Mivel foglalkozik a hőtan?
 Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
Munka- és energiatermelés. Bányai István
 Munka- és energiatermelés Bányai István Joule tétele: adiabatikus munka A XIX. Sz. legnagyobb kihívása a munka Emberi erőforrás (rabszolga, szolga, bérmunkás, erkölcs?, ár!) Állati erőforrás (kevésbé erkölcssértő?,
Munka- és energiatermelés Bányai István Joule tétele: adiabatikus munka A XIX. Sz. legnagyobb kihívása a munka Emberi erőforrás (rabszolga, szolga, bérmunkás, erkölcs?, ár!) Állati erőforrás (kevésbé erkölcssértő?,
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Elméleti kérdések 11. osztály érettségire el ı készít ı csoport
 Elméleti kérdések 11. osztály érettségire el ı készít ı csoport MECHANIKA I. 1. Definiálja a helyvektort! 2. Mondja meg mit értünk vonatkoztatási rendszeren! 3. Fogalmazza meg kinematikailag, hogy mikor
Elméleti kérdések 11. osztály érettségire el ı készít ı csoport MECHANIKA I. 1. Definiálja a helyvektort! 2. Mondja meg mit értünk vonatkoztatási rendszeren! 3. Fogalmazza meg kinematikailag, hogy mikor
Az energia bevezetése az iskolába. Készítette: Rimai Anasztázia
 Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
Művelettan 3 fejezete
 Művelettan 3 fejezete Impulzusátadás Hőátszármaztatás mechanikai műveletek áramlástani műveletek termikus műveletek aprítás, osztályozás ülepítés, szűrés hűtés, sterilizálás, hőcsere Komponensátadás anyagátadási
Művelettan 3 fejezete Impulzusátadás Hőátszármaztatás mechanikai műveletek áramlástani műveletek termikus műveletek aprítás, osztályozás ülepítés, szűrés hűtés, sterilizálás, hőcsere Komponensátadás anyagátadási
9. évfolyam. Osztályozóvizsga tananyaga FIZIKA
 9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
Fizika. Fizika. Nyitray Gergely (PhD) PTE PMMIK március 27.
 Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 27. Az entrópia A természetben a mechanikai munka teljes egészében átalakítható hővé. Az elvont hő viszont nem alakítható át teljes egészében mechanikai
Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 27. Az entrópia A természetben a mechanikai munka teljes egészében átalakítható hővé. Az elvont hő viszont nem alakítható át teljes egészében mechanikai
összetevője változatlan marad, a falra merőleges összetevő iránya ellenkezőjére változik, miközben nagysága ugyanakkora marad.
 A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
Minek kell a matematika? (bevezetés)
 Tudomány Minek kell a matematika? (bevezetés) Osváth Szabolcs a tudomány az emberiségnek a világ megismerésére és megértésére irányuló vállalkozása Semmelweis Egyetem a szőkedencsi hétszáz éves hárs Matematika...
Tudomány Minek kell a matematika? (bevezetés) Osváth Szabolcs a tudomány az emberiségnek a világ megismerésére és megértésére irányuló vállalkozása Semmelweis Egyetem a szőkedencsi hétszáz éves hárs Matematika...
FIZIKA VIZSGATEMATIKA
 FIZIKA VIZSGATEMATIKA osztályozó vizsga írásbeli szóbeli időtartam 60p 10p arány az értékelésnél 60% 40% A vizsga értékelése jeles (5) 80%-tól jó (4) 65%-tól közepes (3) 50%-tól elégséges (2) 35%-tól Ha
FIZIKA VIZSGATEMATIKA osztályozó vizsga írásbeli szóbeli időtartam 60p 10p arány az értékelésnél 60% 40% A vizsga értékelése jeles (5) 80%-tól jó (4) 65%-tól közepes (3) 50%-tól elégséges (2) 35%-tól Ha
Komplex természettudomány 3.
 Komplex természettudomány 3. 1 A lendület és megmaradása Lendület (impulzus): A test tömegének és sebességének a szorzata. Jele: I. Képlete: II = mm vv mértékegysége: kkkk mm ss A lendület származtatott
Komplex természettudomány 3. 1 A lendület és megmaradása Lendület (impulzus): A test tömegének és sebességének a szorzata. Jele: I. Képlete: II = mm vv mértékegysége: kkkk mm ss A lendület származtatott
Lendület. Lendület (impulzus): A test tömegének és sebességének szorzata. vektormennyiség: iránya a sebesség vektor iránya.
 Lendület Lendület (impulzus): A test tömegének és sebességének szorzata. vektormennyiség: iránya a sebesség vektor iránya. Lendülettétel: Az lendület erő hatására változik meg. Az eredő erő határozza meg
Lendület Lendület (impulzus): A test tömegének és sebességének szorzata. vektormennyiség: iránya a sebesség vektor iránya. Lendülettétel: Az lendület erő hatására változik meg. Az eredő erő határozza meg
Egy részecske mozgási energiája: v 2 3 = k T, ahol T a gáz hőmérséklete Kelvinben 2 2 (k = 1, J/K Boltzmann-állandó) Tehát a gáz hőmérséklete
 Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
1. előadás. Gáztörvények. Fizika Biofizika I. 2015/2016. Kapcsolódó irodalom:
 1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
A mechanika alapjai. A pontszerű testek dinamikája
 A mechanika alapjai A pontszerű testek dinamikája Horváth András SZE, Fizika Tsz. v 0.6 1 / 26 alapi Bevezetés Newton I. Newton II. Newton III. Newton IV. alapi 2 / 26 Bevezetés alapi Bevezetés Newton
A mechanika alapjai A pontszerű testek dinamikája Horváth András SZE, Fizika Tsz. v 0.6 1 / 26 alapi Bevezetés Newton I. Newton II. Newton III. Newton IV. alapi 2 / 26 Bevezetés alapi Bevezetés Newton
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly
 Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Környezeti kémia: A termodinamika főtételei, a kémiai egyensúly Bányai István DE TTK Kolloid- és Környezetkémiai Tanszék 2013.01.11. Környezeti fizikai kémia 1 A fizikai-kémia és környezeti kémia I. A
Transzportjelenségek
 Transzportjelenségek Fizikai kémia előadások 8. Turányi Tamás ELTE Kémiai Intézet lamináris (réteges) áramlás: minden réteget a falhoz közelebbi szomszédja fékez, a faltól távolabbi szomszédja gyorsít
Transzportjelenségek Fizikai kémia előadások 8. Turányi Tamás ELTE Kémiai Intézet lamináris (réteges) áramlás: minden réteget a falhoz közelebbi szomszédja fékez, a faltól távolabbi szomszédja gyorsít
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Az előadás vázlata: Állapotjelzők: Állapotjelzők: Állapotjelzők: Állapotjelzők: nagy közepes kicsi. Hőmérséklet, T tapasztalat (hideg, meleg).
 Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Dinamikus modellek felállítása mérnöki alapelvek segítségével
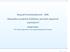 IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
IgyR - 3/1 p. 1/20 Integrált Gyártórendszerek - MSc Dinamikus modellek felállítása mérnöki alapelvek segítségével Hangos Katalin PE Villamosmérnöki és Információs Rendszerek Tanszék IgyR - 3/1 p. 2/20
Tárgymutató. dinamika, 5 dinamikai rendszer, 4 végtelen sok állapotú, dinamikai törvény, 5 dinamikai törvények, 12 divergencia,
 Tárgymutató állapottér, 3 10, 107 általánosított impulzusok, 143 147 általánosított koordináták, 143 147 áramlás, 194 197 Arisztotelész mozgástörvényei, 71 77 bázisvektorok, 30 centrifugális erő, 142 ciklikus
Tárgymutató állapottér, 3 10, 107 általánosított impulzusok, 143 147 általánosított koordináták, 143 147 áramlás, 194 197 Arisztotelész mozgástörvényei, 71 77 bázisvektorok, 30 centrifugális erő, 142 ciklikus
Evans-Searles fluktuációs tétel
 Az idő folyásának iránya Evans-Searles fluktuációs tétel Osváth Szabolcs Semmelweis Egyetem a folyamatok iránya a termodinamikai második főtétele alapján Nincs olyan folyamat, amelynek egyetlen eredménye,
Az idő folyásának iránya Evans-Searles fluktuációs tétel Osváth Szabolcs Semmelweis Egyetem a folyamatok iránya a termodinamikai második főtétele alapján Nincs olyan folyamat, amelynek egyetlen eredménye,
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet
 Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS 2013. Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet DIFFÚZIÓ 1. KÍSÉRLET Fizika-Biofizika I. - DIFFÚZIÓ 1. kísérlet: cseppentsünk tintát egy üveg vízbe 1. megfigyelés:
Fizika-Biofizika I. DIFFÚZIÓ OZMÓZIS 2013. Október 22. Vig Andrea PTE ÁOK Biofizikai Intézet DIFFÚZIÓ 1. KÍSÉRLET Fizika-Biofizika I. - DIFFÚZIÓ 1. kísérlet: cseppentsünk tintát egy üveg vízbe 1. megfigyelés:
2. Energodinamika értelmezése, főtételei, leírási módok
 Energetika 7 2. Energodinamika értelmezése, főtételei, leírási módok Az energia fogalmának kialakulása történetileg a munkavégzés definícióához kapcsolódik. Kezdetben az energiát a munkavégző képességgel
Energetika 7 2. Energodinamika értelmezése, főtételei, leírási módok Az energia fogalmának kialakulása történetileg a munkavégzés definícióához kapcsolódik. Kezdetben az energiát a munkavégző képességgel
Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola
 Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola 1047 Budapest, Langlet Valdemár utca 3-5. www.brody-bp.sulinet.hu e-mail: titkar@big.sulinet.hu Telefon: (1) 369 4917 OM: 034866 Osztályozóvizsga részletes
Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola 1047 Budapest, Langlet Valdemár utca 3-5. www.brody-bp.sulinet.hu e-mail: titkar@big.sulinet.hu Telefon: (1) 369 4917 OM: 034866 Osztályozóvizsga részletes
Azonos és egymással nem kölcsönható részecskékből álló kvantumos rendszer makrókanónikus sokaságban.
 Kvantum statisztika A kvantummechanika előadások során már megtanultuk, hogy az anyagot felépítő részecskék nemklasszikus, hullámtulajdonságokkal is rendelkeznek aminek következtében viselkedésük sok szempontból
Kvantum statisztika A kvantummechanika előadások során már megtanultuk, hogy az anyagot felépítő részecskék nemklasszikus, hullámtulajdonságokkal is rendelkeznek aminek következtében viselkedésük sok szempontból
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről
 A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
TANMENET FIZIKA. 10. osztály. Hőtan, elektromosságtan. Heti 2 óra
 TANMENET FIZIKA 10. osztály Hőtan, elektromosságtan Heti 2 óra 2012-2013 I. Hőtan 1. Bevezetés Hőtani alapjelenségek 1.1. Emlékeztető 2. 1.2. A szilárd testek hőtágulásának törvényszerűségei. A szilárd
TANMENET FIZIKA 10. osztály Hőtan, elektromosságtan Heti 2 óra 2012-2013 I. Hőtan 1. Bevezetés Hőtani alapjelenségek 1.1. Emlékeztető 2. 1.2. A szilárd testek hőtágulásának törvényszerűségei. A szilárd
Folyadékok és gázok mechanikája
 Folyadékok és gázok mechanikája A folyadékok nyomása A folyadék súlyából származó nyomást hidrosztatikai nyomásnak nevezzük. Függ: egyenesen arányos a folyadék sűrűségével (ρ) egyenesen arányos a folyadékoszlop
Folyadékok és gázok mechanikája A folyadékok nyomása A folyadék súlyából származó nyomást hidrosztatikai nyomásnak nevezzük. Függ: egyenesen arányos a folyadék sűrűségével (ρ) egyenesen arányos a folyadékoszlop
Bevezetés a modern fizika fejezeteibe. 1.(a) Rugalmas hullámok. Utolsó módosítás: szeptember 28. Dr. Márkus Ferenc BME Fizika Tanszék
 Bevezetés a modern fizika fejezeteibe 1.(a) Rugalmas hullámok Utolsó módosítás: 2012. szeptember 28. 1 A deformálható testek mozgása (1) A Helmholtz-féle kinematikai alaptétel: A deformálható test elegendően
Bevezetés a modern fizika fejezeteibe 1.(a) Rugalmas hullámok Utolsó módosítás: 2012. szeptember 28. 1 A deformálható testek mozgása (1) A Helmholtz-féle kinematikai alaptétel: A deformálható test elegendően
A modern fizika születése
 MODERN FIZIKA A modern fizika születése Eddig: Olyan törvényekkel ismerkedtünk meg melyekhez tapasztalatokat a mindennapi életből is szerezhettünk. Klasszikus fizika: mechanika, hőtan, elektromosságtan,
MODERN FIZIKA A modern fizika születése Eddig: Olyan törvényekkel ismerkedtünk meg melyekhez tapasztalatokat a mindennapi életből is szerezhettünk. Klasszikus fizika: mechanika, hőtan, elektromosságtan,
Az energia. Energia : munkavégző képesség (vagy hőközlő képesség)
 Az energia Energia : munkavégző képesség (vagy hőközlő képesség) Megjelenési formái: Munka: irányított energiaközlés (W=Fs) Sugárzás (fényrészecskék energiája) Termikus energia: atomok, molekulák véletlenszerű
Az energia Energia : munkavégző képesség (vagy hőközlő képesség) Megjelenési formái: Munka: irányított energiaközlés (W=Fs) Sugárzás (fényrészecskék energiája) Termikus energia: atomok, molekulák véletlenszerű
A Föld középpontja felé szabadon eső test sebessége növekszik, azaz, a
 a Matematika mérnököknek I. című tárgyhoz Függvények. Függvények A Föld középpontja felé szabadon eső test sebessége növekszik, azaz, a szabadon eső test sebessége az idő függvénye. Konstans hőmérsékleten
a Matematika mérnököknek I. című tárgyhoz Függvények. Függvények A Föld középpontja felé szabadon eső test sebessége növekszik, azaz, a szabadon eső test sebessége az idő függvénye. Konstans hőmérsékleten
Alkalmazás a makrókanónikus sokaságra: A fotongáz
 Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Összefoglaló kérdések fizikából 2009-2010. I. Mechanika
 Összefoglaló kérdések fizikából 2009-2010. I. Mechanika 1. Newton törvényei - Newton I. (a tehetetlenség) törvénye; - Newton II. (a mozgásegyenlet) törvénye; - Newton III. (a hatás-ellenhatás) törvénye;
Összefoglaló kérdések fizikából 2009-2010. I. Mechanika 1. Newton törvényei - Newton I. (a tehetetlenség) törvénye; - Newton II. (a mozgásegyenlet) törvénye; - Newton III. (a hatás-ellenhatás) törvénye;
Mechanika, dinamika. p = m = F t vagy. m t
 Mechanika, dinamika Mozgás, alakváltozás és ennek háttere Newton: a mozgás természetes állapot. A témakör egyik kulcsfontosságú fizikai mennyisége az impulzus (p), vagy lendület, vagy mozgásmennyiség.
Mechanika, dinamika Mozgás, alakváltozás és ennek háttere Newton: a mozgás természetes állapot. A témakör egyik kulcsfontosságú fizikai mennyisége az impulzus (p), vagy lendület, vagy mozgásmennyiség.
Gépészmérnöki alapszak, Mérnöki fizika ZH, október 10.. CHFMAX. Feladatok (maximum 3x6 pont=18 pont)
 1. 2. 3. Mondat E1 E2 Gépészmérnöki alapszak, Mérnöki fizika ZH, 2017. október 10.. CHFMAX NÉV: Neptun kód: Aláírás: g=10 m/s 2 Előadó: Márkus / Varga Feladatok (maximum 3x6 pont=18 pont) 1) Az l hosszúságú
1. 2. 3. Mondat E1 E2 Gépészmérnöki alapszak, Mérnöki fizika ZH, 2017. október 10.. CHFMAX NÉV: Neptun kód: Aláírás: g=10 m/s 2 Előadó: Márkus / Varga Feladatok (maximum 3x6 pont=18 pont) 1) Az l hosszúságú
Carnot körfolyamat ideális gázzal:
 ELTE II. Fizikus, 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 4. (XI. 8) Carnot körfolyamat ideális gázzal: p E körfoly. = 0 IV I III II V Q 1 + Q 2 + W I + W II + W III + W IV = 0 W I + W II + W III + W
ELTE II. Fizikus, 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 4. (XI. 8) Carnot körfolyamat ideális gázzal: p E körfoly. = 0 IV I III II V Q 1 + Q 2 + W I + W II + W III + W IV = 0 W I + W II + W III + W
-2σ. 1. A végtelen kiterjedésű +σ és 2σ felületi töltéssűrűségű síklapok terében az ábrának megfelelően egy dipól helyezkedik el.
 1. 2. 3. Mondat E1 E2 Össz Energetikai mérnöki alapszak Mérnöki fizika 2. ZH NÉV:.. 2018. május 15. Neptun kód:... g=10 m/s 2 ; ε 0 = 8.85 10 12 F/m; μ 0 = 4π 10 7 Vs/Am; c = 3 10 8 m/s Előadó: Márkus
1. 2. 3. Mondat E1 E2 Össz Energetikai mérnöki alapszak Mérnöki fizika 2. ZH NÉV:.. 2018. május 15. Neptun kód:... g=10 m/s 2 ; ε 0 = 8.85 10 12 F/m; μ 0 = 4π 10 7 Vs/Am; c = 3 10 8 m/s Előadó: Márkus
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 Nézd meg a képet és jelöld az 1. igaz állításokat! 1:56 Könnyű F sak a sárga golyó fejt ki erőhatást a fehérre. Mechanikai kölcsönhatás jön létre a golyók között. Mindkét golyó mozgásállapota változik.
Nézd meg a képet és jelöld az 1. igaz állításokat! 1:56 Könnyű F sak a sárga golyó fejt ki erőhatást a fehérre. Mechanikai kölcsönhatás jön létre a golyók között. Mindkét golyó mozgásállapota változik.
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 gázok hőtágulása függ: 1. 1:55 Normál de független az anyagi minőségtől. Függ az anyagi minőségtől. a kezdeti térfogattól, a hőmérséklet-változástól, Mlyik állítás az igaz? 2. 2:31 Normál Hőáramláskor
gázok hőtágulása függ: 1. 1:55 Normál de független az anyagi minőségtől. Függ az anyagi minőségtől. a kezdeti térfogattól, a hőmérséklet-változástól, Mlyik állítás az igaz? 2. 2:31 Normál Hőáramláskor
FIZIKA NYEK reál (gimnázium, 2 + 2 + 2+2 óra)
 FIZIKA NYEK reál (gimnázium, 2 + 2 + 2+2 óra) Tantárgyi struktúra és óraszámok Óraterv a kerettantervekhez gimnázium Tantárgyak 9. évf. 10. évf. 11. évf. 12. évf. Fizika 2 2 2 2 1 9. osztály B változat
FIZIKA NYEK reál (gimnázium, 2 + 2 + 2+2 óra) Tantárgyi struktúra és óraszámok Óraterv a kerettantervekhez gimnázium Tantárgyak 9. évf. 10. évf. 11. évf. 12. évf. Fizika 2 2 2 2 1 9. osztály B változat
DINAMIKA ALAPJAI. Tömeg és az erő
 DINAMIKA ALAPJAI Tömeg és az erő NEWTON ÉS A TEHETETLENSÉG Tehetetlenség: A testek maguktól nem képesek megváltoztatni a mozgásállapotukat Newton I. törvénye (tehetetlenség törvénye): Minden test nyugalomban
DINAMIKA ALAPJAI Tömeg és az erő NEWTON ÉS A TEHETETLENSÉG Tehetetlenség: A testek maguktól nem képesek megváltoztatni a mozgásállapotukat Newton I. törvénye (tehetetlenség törvénye): Minden test nyugalomban
Axiomatikus felépítés az axiómák megalapozottságát a felépített elmélet teljesítképessége igazolja majd!
 Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Mit nevezünk nehézségi erőnek?
 Mit nevezünk nehézségi erőnek? Azt az erőt, amelynek hatására a szabadon eső testek g (gravitációs) gyorsulással esnek a vonzó test centruma felé, nevezzük nehézségi erőnek. F neh = m g Mi a súly? Azt
Mit nevezünk nehézségi erőnek? Azt az erőt, amelynek hatására a szabadon eső testek g (gravitációs) gyorsulással esnek a vonzó test centruma felé, nevezzük nehézségi erőnek. F neh = m g Mi a súly? Azt
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 1. 2:29 Normál párolgás olyan halmazállapot-változás, amelynek során a folyadék légneművé válik. párolgás a folyadék felszínén megy végbe. forrás olyan halmazállapot-változás, amelynek során nemcsak a
1. 2:29 Normál párolgás olyan halmazállapot-változás, amelynek során a folyadék légneművé válik. párolgás a folyadék felszínén megy végbe. forrás olyan halmazállapot-változás, amelynek során nemcsak a
Elektromágneses hullámok
 Bevezetés a modern fizika fejezeteibe 2. (a) Elektromágneses hullámok Utolsó módosítás: 2015. október 3. 1 A Maxwell-egyenletek (1) (2) (3) (4) E: elektromos térerősség D: elektromos eltolás H: mágneses
Bevezetés a modern fizika fejezeteibe 2. (a) Elektromágneses hullámok Utolsó módosítás: 2015. október 3. 1 A Maxwell-egyenletek (1) (2) (3) (4) E: elektromos térerősség D: elektromos eltolás H: mágneses
Sztehlo Gábor Evangélikus Óvoda, Általános Iskola és Gimnázium. Osztályozóvizsga témakörök 1. FÉLÉV. 9. osztály
 Osztályozóvizsga témakörök 1. FÉLÉV 9. osztály I. Testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás; átlagsebesség, pillanatnyi sebesség 3. Gyorsulás 4. Szabadesés, szabadon eső test
Osztályozóvizsga témakörök 1. FÉLÉV 9. osztály I. Testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás; átlagsebesség, pillanatnyi sebesség 3. Gyorsulás 4. Szabadesés, szabadon eső test
Osztályozó, javító vizsga 9. évfolyam gimnázium. Írásbeli vizsgarész ELSŐ RÉSZ
 Írásbeli vizsgarész ELSŐ RÉSZ 1. Egy téglalap alakú háztömb egyik sarkából elindulva 80 m, 150 m, 80 m utat tettünk meg az egyes házoldalak mentén, míg a szomszédos sarokig értünk. Mekkora az elmozdulásunk?
Írásbeli vizsgarész ELSŐ RÉSZ 1. Egy téglalap alakú háztömb egyik sarkából elindulva 80 m, 150 m, 80 m utat tettünk meg az egyes házoldalak mentén, míg a szomszédos sarokig értünk. Mekkora az elmozdulásunk?
Atomok és molekulák elektronszerkezete
 Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Fizika. Tanmenet. 7. osztály. 1. félév: 1 óra 2. félév: 2 óra. A OFI javaslata alapján összeállította az NT számú tankönyvhöz:: Látta: ...
 Tanmenet Fizika 7. osztály ÉVES ÓRASZÁM: 54 óra 1. félév: 1 óra 2. félév: 2 óra A OFI javaslata alapján összeállította az NT-11715 számú tankönyvhöz:: Látta:...... Harmath Lajos munkaközösség vezető tanár
Tanmenet Fizika 7. osztály ÉVES ÓRASZÁM: 54 óra 1. félév: 1 óra 2. félév: 2 óra A OFI javaslata alapján összeállította az NT-11715 számú tankönyvhöz:: Látta:...... Harmath Lajos munkaközösség vezető tanár
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 1. 2:24 Normál Magasabb hőmérsékleten a részecskék nagyobb tágassággal rezegnek, s így távolabb kerülnek egymástól. Magasabb hőmérsékleten a részecskék kisebb tágassággal rezegnek, s így távolabb kerülnek
1. 2:24 Normál Magasabb hőmérsékleten a részecskék nagyobb tágassággal rezegnek, s így távolabb kerülnek egymástól. Magasabb hőmérsékleten a részecskék kisebb tágassággal rezegnek, s így távolabb kerülnek
FIZIKA II. Dr. Rácz Ervin. egyetemi docens
 FIZIKA II. Dr. Rácz Ervin egyetemi docens Fontos tudnivalók e-mail: racz.ervin@kvk.uni-obuda.hu web: http://uni-obuda.hu/users/racz.ervin/index.htm Iroda: Bécsi út, C. épület, 124. szoba Fizika II. - ismertetés
FIZIKA II. Dr. Rácz Ervin egyetemi docens Fontos tudnivalók e-mail: racz.ervin@kvk.uni-obuda.hu web: http://uni-obuda.hu/users/racz.ervin/index.htm Iroda: Bécsi út, C. épület, 124. szoba Fizika II. - ismertetés
Az Ampère-Maxwell-féle gerjesztési törvény
 Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
Fizika. Fizika. Nyitray Gergely (PhD) PTE PMMIK március 20.
 Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 20. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 20. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
FIZIKA KÖZÉPSZINTŐ SZÓBELI FIZIKA ÉRETTSÉGI TÉTELEK Premontrei Szent Norbert Gimnázium, Gödöllı, 2012. május-június
 1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
Fizika minta feladatsor
 Fizika minta feladatsor 10. évf. vizsgára 1. A test egyenes vonalúan egyenletesen mozog, ha A) a testre ható összes erő eredője nullával egyenlő B) a testre állandó értékű erő hat C) a testre erő hat,
Fizika minta feladatsor 10. évf. vizsgára 1. A test egyenes vonalúan egyenletesen mozog, ha A) a testre ható összes erő eredője nullával egyenlő B) a testre állandó értékű erő hat C) a testre erő hat,
Ábragyűjtemény levelező hallgatók számára
 Ábragyűjtemény levelező hallgatók számára Ez a bemutató a tanszéki Fizika jegyzet kiegészítése Mechanika I. félév 1 Stabilitás Az úszás stabilitása indifferens a stabil, b labilis S súlypont Sf a kiszorított
Ábragyűjtemény levelező hallgatók számára Ez a bemutató a tanszéki Fizika jegyzet kiegészítése Mechanika I. félév 1 Stabilitás Az úszás stabilitása indifferens a stabil, b labilis S súlypont Sf a kiszorított
Newton törvények, lendület, sűrűség
 Newton törvények, lendület, sűrűség Newton I. törvénye: Minden tárgy megtartja nyugalmi állapotát, vagy egyenes vonalú egyenletes mozgását (állandó sebességét), amíg a környezete ezt meg nem változtatja
Newton törvények, lendület, sűrűség Newton I. törvénye: Minden tárgy megtartja nyugalmi állapotát, vagy egyenes vonalú egyenletes mozgását (állandó sebességét), amíg a környezete ezt meg nem változtatja
Hajdú Angéla
 2012.02.22 Varga Zsófia zsofiavarga81@gmail.com Hajdú Angéla angela.hajdu@net.sote.hu 2012.02.22 Mai kérdés: Azt tapasztaljuk, hogy egy bizonyos fajta molekulának elkészített oldata áteső napfényben színes.
2012.02.22 Varga Zsófia zsofiavarga81@gmail.com Hajdú Angéla angela.hajdu@net.sote.hu 2012.02.22 Mai kérdés: Azt tapasztaljuk, hogy egy bizonyos fajta molekulának elkészített oldata áteső napfényben színes.
Fázisátalakulások vizsgálata
 KLASSZIKUS FIZIKA LABORATÓRIUM 6. MÉRÉS Fázisátalakulások vizsgálata Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. szeptember 28. Szerda délelőtti csoport 1. A mérés célja A mérés
KLASSZIKUS FIZIKA LABORATÓRIUM 6. MÉRÉS Fázisátalakulások vizsgálata Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. szeptember 28. Szerda délelőtti csoport 1. A mérés célja A mérés
Feladatlap X. osztály
 Feladatlap X. osztály 1. feladat Válaszd ki a helyes választ. Két test fajhője közt a következő összefüggés áll fenn: c 1 > c 2, ha: 1. ugyanabból az anyagból vannak és a tömegük közti összefüggés m 1
Feladatlap X. osztály 1. feladat Válaszd ki a helyes választ. Két test fajhője közt a következő összefüggés áll fenn: c 1 > c 2, ha: 1. ugyanabból az anyagból vannak és a tömegük közti összefüggés m 1
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA. A termodinamika alapproblémája
 A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA A termodinamika alapproblémája Első észrevétel: U, V és n meghatározza a rendszer egyensúlyi állapotát. Mi történik, ha változás történik a rendszerben? Mi lesz
A TERMODINAMIKA II., III. ÉS IV. AXIÓMÁJA A termodinamika alapproblémája Első észrevétel: U, V és n meghatározza a rendszer egyensúlyi állapotát. Mi történik, ha változás történik a rendszerben? Mi lesz
