Tumor specifikus DNS/gén dózis szerepe a papilláris vesetumor kialakulásában
|
|
|
- Klaudia Piroska Hegedűs
- 4 évvel ezelőtt
- Látták:
Átírás
1 Tumor specifikus DNS/gén dózis szerepe a papilláris vesetumor kialakulásában Doktori (PhD) értekezés tézisei Szerző: Dr. Sarlós Donát Péter Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, Doktori iskolavezetője: Prof. Dr. Bogár Lajos Programvezető: Prof. Dr.Pajor László Témavezetők: Prof. Dr. Kovács Gyula Dr. Szántó Árpád 1
2 Rövidítések jegyzéke: BAC-array: bacterial artificial chromosome array, Bakteriális artefíciális kromoszóma array CB: comma shape body CGH: comparative genomic hybridisation, DNS alapú összehasonlító genomikus hibridizáció CMM: cap metanpphrikus mesenchyma crcc: világossejtes veserák chrcc: kromofób veserák DNS: dezoxiribonukleinsav dntp: dezixiribonuleozid-trifoszfát EDTA: etilén-diamin-tetraecetsav HE: hematoxylin-eozin HNF1B: hepatocyte nuclear factor 1 homeobox B ISUP: Uropatológusok Nemzetközi Társasága, International Society of Urological Pathology KRT17: keratin 17 LRRK2: leucine-rich repeat kinase 2 MDE: mutation detection enhancement MET: hepatocyte growth factor receptor MEST: mesoderm-specific transcript MTSCC: Mucinous Tubular and Spindle Cell Carcinoma, Mucinózus tubuláris és orsósejtes daganat NCBI: National Center for Biotechnology Information NR: nephrogén rest PCDH: protokadherin PCR: polymerase chain reaction prcc: papilláris veserák PPL: papilláris prekurzor lézió RCC: renal cell carcinoma, vesesejtes rák SSCP: single-strand conformation polymorphism TCF2: transcription factor 2 TFE3: transcription factor E3 TGIF2LY: transforming growth factor-beta-induced factor 2-like, y-linked TMA: tissue micro array WHO: World Health Organisation, Egészségügyi Világszervezet 2
3 1.Bevezetés A vesesejtes rák (RCC) klasszifikációja hagyományosan a hematoxilin-eozinnal megfestett szövettani metszetek mikroszkopikus képén alapszik. A sejtek citológiai variabilitásán és növekedési formáján alapuló osztályozások után a 80-as évek végén és 90-es évek elején egy paradigmaváltás történt: az osztályozást a tumorokban előforduló specifikus kromoszóma eltérésekre alapozták (Kovacs, 1993 a,b). A Heidelbergi klasszifikáció a tumor-specifikus genetikai eltérésekre alapul, amik biztonsággal azonosítják a különböző vese tumorokat, még akkor is, ha szövettanilag nem egyértelműen kórismézhetők (Kovacs et al., 1997). A papilláris vesetumorokra szövettanilag heterogén megjelenés jellemző, azonban jól definiált kromoszómális és genetikai elváltozásokat mutat. A carcinogenezis során elsőként a 7-es és a 17-es kromoszóma tri-, illetve tetraszómiája jelenik meg, ezt követheti az Y kromoszóma elvesztése. Később a 3q, 8-as, 12-es, 16-as és a 20-as kromoszóma triszómiája is megjelenhet, ami az agresszívabb viselkedéső daganatok irányába való progressziót jelezheti (Kovacs 1993a, Szponar et al., 2009). Ezeknek az eredményeknek különös jelentősége van a mai WHO osztályozás tükrében, ahol a papilláris adenomát és karcinómát a tumorok mérete alapján különítik el, azaz papilláris tumorok 15mm alatt adenomának fölötte karcinómának kórisméznek (Moch et al., 2016). A papilláris adenoma és karcinóma azonosságát így elismerik, hiszen csak a méretük különböző. A WHO és ISUP által javasolt 15 mm-es határ (amelyet néhány éve még 5 mm-ben határoztak meg) alkamazása esetenként téves pronózis becsléshez vezet a papilláris vese tumorok biológiai-klinikai tulajdonságának megítélésénél. A papilláris vesetumor eredetéről kétféle elképzelés van. A WHO és ISUP (International Society of Urological Pathologists) szerint a papilláris veserák, a konvencionális veserákhoz hasonlóan, a felnőttkori vese differenciálódott tubulusainak hámsejtjeiből alakul ki (Moch et al., 2016). A másik elképzelés szerint a papilláris vesetumor hisztológiailag preneoplasztikus lézió-adenóma-karcinóma szekvenciát mutat (Kovacs, 1993 a,b), ahol azonban az éles határ az adenoma és karcinóma között nem húzható meg, így a malignitás meghatározása differenciáldiagnosztikai nehézséget jelent. A specifikus citogenetikai/dns elváltozások kimutatásán kívül nincs más olyan eszköz a kezünkben, amellyel az adenomát és karcinómát meg tudjuk különböztetni. 3
4 2. Célkitűzés Hipotézisünk szerint a papilláris vesetumor nem, vagy csak részben differenciálódott perzisztáló embrionális sejtcsoportokból indul ki, és ennek megfelelően egy preneoplasztikus lézió-adenóma-karcinóma fejlődési szekvenciát mutat. Korábbi eredmények azt mutatják, hogy a papilláris vese tumorok korai fejlődési szakaszában megjelenő, általános genomikus eltéréseknek (triszómia 7 és 17 és az Y kromoszóma vesztése) és a hozzájuk kapcsolódó gének időben és térben megváltozott expressziójának jelentős szerepe van az embrionális sejtek differenciálódási zavarában és így a pre-neoplasztikus léziók majd felnőtt korban a papilláris vesetumor kialakulásában. A munka célja az, hogy a papilláris veserákra jellemző kezdeti kromoszómális elváltozásokhoz kapcsolódó gének kifejeződését fötális vesékben, a papilláris vese tumorokhoz társuló, többnyire mikroszkópos méretű pre-neoplasztikus léziókban és nagyszámú papilláris vesetumort tartalmazó tissue microarray-n kimutassuk, és így a közös génexpressziók azonosításával alátámasszuk a papilláris vesetumor embrionális eredetét és igazoljuk a papilláris vesetumor megkülönböztető biológiai és klinikai viselkedését. 3. Vizsgálati anyagok és módszerek 3.1. Szövetminták Az RNS alapú vizsgálatokra a friss fötális veséket a Pécsi Tudományegyetem Nőgyógyászati Klinikáján gyűjtöttük, ezeket a feldolgozásig TRIzol-ban 80 C-on tároltuk. Hasonlóan a MET mutációhoz kötődő örökletes normál vese és vese tumor prekurzor lézió mintákat (HD1651) TRIzol-ban fagyasztva tároltuk. Az örökletes esetből származó tumor mintákat az RNS vizsgálatokhoz biztosított anyag biztosítása után 4%-os formaldehidben fixáltuk és rutin szövettani feldolgozásnak vetettük alá. A prekurzor léziók és papilláris vesetumor közötti összefüggés vizsgálatára 15 papilláris vesetumor valamint 15 konvencionális veserák miatt eltávolított vesét a tumor diagnózis biztosítása után teljes mértékben, több száz paraffin blokkban feldolgoztunk. Minden blokkból több hematoxilin eozin (HE) festett metszet készült, amelyekben mikroszkóp alatt prekurzor léziókat kerestünk. 4
5 A papilláris vese tumorok vizsgálatára a Pécsi Egyetem Urológiai Klinikán 2000 január és 2014 december között radikális vagy parciális nephrectómián átesett betegek tumorai közül válogattuk ki a papilláris vesetumornak kórismézett eseteket. A paraffin blokkokat, és HE festett metszeteket a Pécsi Egyetem Patológiai Intézete bocsájtotta rendelkezésünkre. A szövetminták gyűjtését és feldolgozását a PTE ÁOK Etikai Bizottság engedélyének birtokában végeztük (Etikai engedély száma: 5343/2014). A szövettani diagnózis minden esetben uropatológus (K.Gy.) által felülvizsgálatra került a heidelbergi klasszifikációs rendszernek megfelelően (Kovacs et al., 1997) A MET tirozin kináz domén mutáció analízise A MET tirozin kináz domén 16, 17, 18, és 19 exonját amplifikáltuk (Fischer et al., 1998). A PCR termékeket IR800 és IR700 jelölt primerrel szekvenáltuk Thermosequenase Cycle Sequencing kit segítségével (Amersham Pharmacia, Freiburg, Germany) a gyártó utasításai szerint. A jelölt PCR terméket mindkét irányból kettős lézer detektoros LICOR Long ReadIr 4200 szekvenáló géppel (MWG-Biotech, Ebersberg, Germany) a BaseImageIR software csomag segítségével vizsgáltuk A mutációk kimutatására összehasonlítottuk az így kapott szekvenciákat a vad típusú szekvenciával (J02958) A 19-es exon mutáció SSCP (Egyszálú DNS Konformációs Polimorfizmus) vizsgálata A genomikus AC MET szekvencia felhasználásával az exon 19 melletti régióhoz kapcsolódó primerokat készítettünk, amelynek segítségével egy olyan 198bp fragmentumot tudtunk amplifikálni, melynek középső része tartalmazta az A3954C mutációt. Kombináltuk a K2d (nt: ) cca cgg gta ata att ttg tcc intron primert a K1r (nt: ) cca cat ctg act tgg tgg tgg primerrel, ami az exon 19 3 végén található. A 20 µl PCR-reakció 100 ng DNS-t, 200 µm dntp-t, 1,5 mm MgCl 2 -t, mindegyik primerből 2 pmol-t (a K2d radioaktívan jelölt) és 0,5 ng Taqpolimerázt tartalmazott. 2 percig tartó kezdeti denaturálást hajtottunk végre 94 C-on, ezt 27 ciklus követte (30sec 94C-on, 30sec 55C-on és 40sec 72C-on). A végső fázis 5 percig tartott 72 C-on. Minden PCR-reakcióhoz 20 µl futtatópuffert, 2 µl 1M NaOH-t 5
6 és 2 µl 20 mm EDTA-t adtunk. A mintákat 2 percig 94 C-on denaturáltuk, majd 3 µl t 10%-os glicerolos MDE gélre töltöttük. Az elektroforézist 6 W-on állandó hőmérsékleten, éjszakán keresztül végeztük. Ezt követően a gélt megszárítottuk és egy éjszakán át röntgenfilmre exponáltuk A mutált és a vad típusú MET RT-PCR analízise Gyorsfagyasztott szövetmintákból, vagy sejtkultúrákból TRIzol (Invitrogen GmbH, Karlsruhe, Germany) segítségével RNS-t izoláltunk a gyártó utasítása szerint. A cdns első szálának szintézisét 2µg teljes RNA mintából, Superscript II reverz transzkriptáz (Invitrogen) felhasználásával a gyártó protokollja alapján végeztük el. A valós idejű PCR reakciót a DNA Engine Opticon rendszerrel (MJ Research Inc., Watertown, USA), Platinum SYBRGreen qpcr SuperMix-UDG (Invitrogen) végeztük el, kontrolként ß aktint használtunk. Az összes reakciót kétszeresen hajtottuk végre, a végeredményeket a két reakció eredményeiből átlagolva kaptuk. A pontban felsorolt vizsgálatok a Heidelbergi Ruprecht-Karls Egyetem Molekuláris Onkológiai Laboratóriumában történtek tudományos együttműködés keretében Tissue microarray (TMA) készítése A TMA készítéséhez paraffinba ágyazott szövetmintákat használtunk fel. HE metszetek részletes kiértékelésével választottunk ki megfelelő mintavételi helyeket. A blokkokból Manual Tissue Arrayer (MTA1, Beecher Instruments, Inc., Sun Prairie, USA) eszközzel 0,6 mm átmérőjű szövethengereket vettünk ki. Papilláris vesetumorokat, és a festés ellenőrzéséhez fötális veseszövetet és felnőtt normál veseszövetet is felhasználtunk a tissue microarray (TMA) készítéséhez. Eltérő morfológiájú és grádusú részeket tartalmazó tumorokból több mintát vettünk. Az így kiválasztott mintákat egy kombinált paraffin blokkba helyeztük, így akár 150 különböző minta is vizsgálható egy mikroszkópos metszeten. 6
7 3.6. Immunhisztokémia Az immunhisztológiai vizsgálatokra fötális és felnőttkori veséket, pre-neoplasztikus léziókat tartalmazó szövetmintákat és papilláris vesetumorokat tartalmazó TMA-t használtunk fel. A sorozatmetszetekben készült 4 µm vastagságú lemezeket alacsony forráspontú paraffinba mártottuk az epitóp megőrzésére. A paraffinba mártott metszeteket xilollal deparaffináltuk, és leszálló etil-alkohol sorozatban rehidráltuk. Az antigén feltárást 10 mm nátrium-citrát pufferben (ph 6,0) történő forralással értük el, a 2100-Retriever (Pick-Cell Laboratories, Amszterdam, Hollandia) készülék segítségével. A nem specifikus kötőhelyek és az endogén peroxidáz aktivitás blokkolása normál ló szérummal kevert (1%) hidrogén peroxidban (0,3%) történt szobahőmérsékleten 10 percig. Ezután a metszeteket a primer antitesttel fedtük le, és nedves kamrában inkubáltuk egy éjszakán keresztül 4 C-on. A felhasznált antitestek jegyzékét az 1. táblázat tartalmazza. Harminc percig történő HRP konjugált anti nyúl másodlagos antitest (DAKO) alkalmazását követően az előhívás AEC (3- amino-9-etilkarbazol) szubsztrát segítségével történt, majd a metszeteket Mayer hematoxilinnel festettük. A kiértékelést Leica LaborluxS mikroszkóppal végeztük a fotókat Leitz DMRBE mikroszkópra helyezett ProgRes C14 kamerával készítettük. Antitest Eredet Termékkód Puffer ph Hígítás anti-hnf1b nyúl HPA citrát ph 6.0 1:200 anti-met nyúl SC-12 citrát ph 6.0 1:100 anti-krt17 nyúl PA citrát ph 6.0 1:200 anti-pcdh11y nyúl PA citrát ph 6.0 1:50 1. Táblázat. Immunhisztokémiai vizsgálatok során használt antitestek 7
8 4. Eredmények 4.1. A papilláris pre-neoplasztikus léziók gyakorisága és szövettana A különböző típusú veserákot tartalmazó vesék teljes feldolgozása során több száz metszetet néztünk át a feltételezett pre-neoplasztikus léziók felismerésére. Amint az előzetes megfigyelésekből várható volt, a papilláris vese tumort hordozó vesékben találtuk meg a legtöbb mikroszkópos méretű, néha 1-2 mm átmérőjű tubulo-papilláris léziókat. 15 papilláris vesetumort hordozó vesében átlagosan 42 léziót figyeltünk meg. Ezekben a kis kék sejtektől a magasabb hámmal borított papilláris struktúrákig minden átmenet megtalálható volt. Ez a fokozatos átmenet a kis sejttől a nagy sejtig utánozza az embrionális vesefejlődés differenciálódási fázisait, azaz tubuláris epithel kialakulását metanephrogén blasztémából. Egyes szubkapszuláris léziók regresszív változáson mentek keresztül, ami a stroma fibrózisát, az epitheliális sejtek regresszióját és elmeszedését jelentheti. A konvencionális veserákot tartalmazó vesékben csak átlagosan 0.4 léziót figyeltünk meg, míg a vese onkocytómával átlagban 0.8 lézió társult. A kromofób veserák mellett egyetlen esetben sem találtunk tubulo-papilláris prekurzor léziót (2. táblázat). Egy korábbi, herediter papilláris tumort feldolgozó tanulmányban vesénként több, mint 1000 pre-neoplasztikus léziót találtak (Ornstein et al., 2000). Tumor típusa PNL/vese Konvencionális veserák 0.4 Kromofób veserák 0.0 Vese onkocytóma 0.8 Sporadikus papilláris veserák 42.0 Familiáris papilláris veserák >1000* 2. Táblázat. Mikroszkopikus prekurzor léziók (PNL) száma tumoros vesében (*Ornstein et al. 2000) 8
9 4.2. A papilláris vese tumorok szövettani heterogenitása A papilláris vese tumorok szövettani képe nagyfokú heterogenitást mutatott. A papilláris tumorok sok esetben hasonló szövettani képet mutattak, mint az azonos vesében talált pre neoplasztikus léziók legnagyobb része. Sok esetben azonban egyetlen tumoron belül is megfigyelhető volt a tumor sejtek növekedési formájának a heterogenitása. A jól differenciált, tisztán papilláris növekedésű tumor szabálytalan stromán ülő közepes grádusú sejteket mutatott, másik területen világossejtes papilláris növekedés valamint kromofób veserákra emlékeztető szerkezetek voltak felismerhetők. Időnként szabálytalan papilláris stromán ülő, magas eozinofil sejtekből álló tumort figyeltünk meg, amelyek sejtmagja a sejtek felszínén helyezkedett el. Ugyanez a tumor más területeken többmagsoros hámmal borított papillákat és cisztikus struktúrákat mutatott. Egy esetben a többmagsoros magas, bazofil sejtes primer tumor nyirokcsomó áttétében kissejtes forma fordult elő. A papilláris vese tumor, amennyiben jól differenciált kis sejtekből áll, az évek során nagyobb méretet is elérhet és vastag falú cisztaként kórismézhető. Azonban évek után szarkomatózus átalakulás mehet végbe, amely a gyors lefolyású és a beteg halálát okozza. A bemutatott példák diagnózisát minden esetben kromoszóma vizsgálat vagy array- CGH segítségével biztosítottuk A kromoszóma 7 duplikációja és a MET alterációja familiáris vesetumorban A MET tirozin kináz receptor szerepének igazolására módunkban állt egy csírasejtes MET mutációt hordozó 37 éves férfi multiplex tumorának vizsgálatát elvégezni. A MET szekvenálása során egy kontroll, vad típusú vese mintához képest a betegnél mind a normális veseszövetben és tumorokban egy A-C mutációt találtunk. Mutáció specifikus primerek segítségével kimutattuk, hogy a beteg nem tumoros vesesejtjeiben és a tumorokban a vad típusú és mutációt hordozó allél is kifejeződött. SSCP vizsgálat egyértelműen megmutatta, hogy minden egyes tumorban a mutációt hordozó allél duplikálódott. 9
10 4.4. A MET kifejeződése fötális vesében, pre-neoplasztikus lézióban és papilláris vese tumorban Immunhisztokémiai vizsgálattal MET expressziót láttunk a fötális vesében az ureterbimbóban, a cap metanephrikus mesenchymában (CMM), a kialakuló vese vezikulában (comma shape body, CB) valamint az S-forma disztális kompartmentjében. Ezt a kifejezett expressziót megtartották csírasejtes MET-mutációhoz társuló papilláris prekurzor léziók csak úgy, mint azok, amelyeket sporadikus papilláris veserák kapcsán figyeltünk meg. Felnőttkori vesében csak a disztális vese csatornákban fordult elő MET immun-reakció. A vizsgálat során 76 papilláris vese tumor közül közepes intenzitású MET expressziót találtunk 43 esetben (56,6%) A 17-es kromoszóma duplikációjához és amplifikációjához társuló HNF1B kifejeződése fötális vesében, prekurzor lézióban és tumorban Figyelembe véve a 17-es kromoszóma duplikációját, megvizsgáltuk a HNF1B (TCF2) transzkripciós factor kifejeződését ugyanezen szöveti anyagon. Fötális vesében az ureter bimbó végén valamint a komma- és S-forma disztális kompartmentjében, valamint a differenciálódó disztális tubulusokban volt erős immun-reakció, míg a proximális tubulusok és Henle kacs sejtjei csak gyenge sejtmag pozitivitást mutattak. Mind a MET mutációhoz társuló mind a sporadikus esetekből származó PPL erőteljes sejtmag pozitivitást mutatott a HNF1B antitesttel. A felnőttkori vesében a proximális és disztális tubulusokban figyeltünk meg gyenge sejtmag pozitivitást. A papilláris vese tumorok 75%-a (n=57) mutatott pozitív sejtmag festődést a HNF1B antitesttel. Pozitív reakció volt megfigyelhető mind a szolid és papillárisan növekvő tumorokban is. A pozitivitás sokkal erősebb volt a papilláris vese tumorok perifériás, ú.n. növekedési zónájában, és sok esetben a tumor közepén csak elvétve lehetett egyegy tumorsejtben magfestést látni. A MET és a HNF1B gén ko-expressziója 76-ból 32 esetben (42,1%) volt megfigyelhető. A MET és HNF1B szerepére a papilláris vese tumorok kialakulásának korai szakaszára utal az a megfigyelés, hogy míg a prekurzor léziókban mindkét gén kifejezett expressziója volt megfigyelhető, addig a tumorok centrális részein az immun- 10
11 pozitivitás általában gyengébb volt, mint a tumor széli részén, az ú.n. proliferációs zónában A 17-es kromoszóma duplikációjához társuló KRT17 kifejeződése normál vesében, prekurzor lézióban és papilláris vesetumorban A KRT17 elsőként a fötális vesében az ureterbimbóban és a gyűjtőcsatornában jelenik meg. Az ureterbimbó végénél az S-alakú test disztális részéhez csatlakozva láttunk gyenge festődést, de a jel a medulláris gyűjtőcsatorna mentén a vesepapilla irányába erősödik. A gyűjtőcsatorna és az ureterbimbó sejtjeinek mindegyike festődik, ami megfelel a fötális sejtek proliferációs állapotának. A felnőtt vesében, az összekötő csatornában membrán-attenuált és szelektív (a sejtek többsége, de nem minden sejt) festődést mutat. A medulláris gyűjtőcsatornák sejtjeinek többsége hasonló szelektív festődést mutat. A KRT17 pozitív sejtek vélhetően a principális sejtek az összekötő csatornákban és gyűjtőcsatornákban. A KRT17 expresszióját papilláris vesetumorokban egy 151 daganatos mintát tartalmazó TMA segítségével vizsgáltuk. Ezen kívül 17 sporadikus papilláris vesetumor mellett jelentkező papilláris prekurzor léziót vizsgáltunk, ezek között 8 olyat, ahol a betegnél ismert volt germ line MET mutáció. A KRT17 mind a 17 vizsgált 1-3mm-es papilláris lézióban kifejeződött. A 151 vizsgált papilláris vesetumor közül 116 esetben diffúz citoplazmatikus festődést észleltünk, ami a membrán alatti részeken kifejezettebb volt. Több daganatban a KRT17 erős kondenzációját figyeltük meg a sejtek apikális felszínén, néhol erős membrán pozitivitással. A papilláris vese tumorok összesen 76,8%-a (n=116) bizonyult pozitívnak KRT17 immunhosztokémia során, függetlenül a sejtek méretétől, amit I-es típusú, II-es típusú és kevert típusúként is klasszifikálnak Az X és Y kromoszóma elváltozása papilláris vese tumorokban Az Y kromoszóma vesztése familiáris papilláris vesetumorokban Az Y kromoszóma vesztését papilláris vesetumorokban már korábban kimutatták mind kromoszóma, Southern-blot és BAC-array vizsgálatokkal (Kovacs et al., 1994; Szponar et al., 2011). A fentebb tárgyalt familiáris papilláris tumor miatt vizsgált egyénnél, a 11
12 multiplex tumorok és pre-neoplasztikus léziók részletes genomikus vizsgálata során mind a kilenc lézióban előfordult a 7-es és 17-es kromoszómák duplikációjára utaló DNS elváltozás. Ezenkívül egy tumorban a 10-es kromoszóma és két további tumorban a 12-es kromoszóma duplikációja fordult elő. Ezek az eredmények egyértelműen igazolják a papilláris vese tumor diagnózisát. A tézisben tárgyalt, a papilláris vesetumorokban először megjelenő, alapvető genetikai elváltozások szempontjából fontos elváltozás volt továbbá az Y kromoszóma hiánya A PCDH11XY gén kifejeződése fötális vesében, pre-neoplasztikus léziókban és papilláris vesetumorokban Korábban az Yp11.2 régióhoz lokalizált legkisebb genomikus régióban két gén, a PCDH11Y és a homeobox gén TGIF2LY található, amelyek közül karcinogenezis szempontjából elsősorban a PCDH11Y-nak lehet jelentősége. A PCDH11Y az X kromoszómán előforduló homológ PCDH11X génhez képest egy 13 bázis pár (bp) deléciót mutat, ami megváltozott peptid szignált eredményez. Ezt a 13 bp különbséget fel tudtuk használni az X és Y specifikus PCDH11 szekvenciák kimutatására PCR reakcióval. Mind a PCDH11Y és PCDH11X génnek számos izoformája ismert. Az Y kromoszóma hiánya mellett az X kromoszómán elhelyezkedő PCDH11X gén 4-es izoforma kifejeződésének hiányát találtuk papilláris vesetumorokban, míg ez az izoforma az egészséges veseszövet mellett a placentában, fötális agyban, és hereszövetben magas fokon kifejeződött. Az 1-es, 2-es és 3-as izoformák a legtöbb papilláris vese tumorban is pozitív reakciót adnak. Immunhisztokémiai vizsgálattal a fötális vese kéregállományában jelentős PCDH11XY kifejeződést találtunk. A PCDH11XY protein az elágazódó ureterbimbó sejtek felszínén a kéregállomány aktív differenciálódási régiójában figyelhető meg, de a már differenciálódott kivezető csatornák sejtjeiben hiányzik a PCDH11XY protein. Feltűnő az ureterbimbó körül tömörült blasztémális sejteknek, azaz a CMM sejteknek a citoplazmájában látható PCDH11XY pozitivitása, ami a renális vezikula (az S-forma előalakja) kialakulása, azaz a mesenchyma-epithelium-transzformáció után már nagyrészt a sejtek felszínén jelenik meg. Az S-formában, különösen a disztális kompartmentben a PCDH11XY protein szintén többségében a sejtek felszínén található 12
13 meg. A PCDH11XY kifejlődő tubuláris rendszerben elsősorban a lenyúló Henle kacs és disztális tubulus kezdeményekben fejeződik ki, a proximális tubulus kezdemények csak gyenge pozitivitást mutatnak. A felszálló Henle kacs és a disztális tubulusok pozitív festődése következtében a macula densa sejtjei is pozitív reakciót adnak. A munkába bevont összes preneoplasztikus lézió és papilláris vesetumor a PCDH11XY immunhisztokémiával negatív reakciót mutatott. 5. Megbeszélés 5.1. Papilláris vesetumor eredete Mintegy 25 évvel ezelőtt javaslat született a papilláris vese tumorok embrionális maradványokból való kiindulására (Kovacs és Kovacs, 1993; Kovacs 1993a,b). Korábban közölték, hogy a csírasejtes MET mutációhoz társuló familiáris papilláris veserákhoz akár több ezer mikroszkópos méretű papilláris prekurzor lézió társul (Ornstein et al., 2000). Mi kimutattuk, hogy a sporadikus papilláris vese tumorok mellett is vesénként átlagban 42 hasonló prekurzor lézió fordul elő (Bányai, Sarlós et al., 2018). Ennek a jelentőségét alátámasztja az a tény, hogy a konvencionális veserákot tartalmazó vesékben átlagosan csak 0.4 hasonló jellegű PNL fordul elő (Bányai, Sarlós et al., 2018). A differenciálatlan epitheliális sejtekből álló prekurzor léziók morfológiája sok esetben hasonlít a Wilms tumorhoz társuló nephrogén maradványok (NR) szövettani képére. A papilláris vese tumorhoz társuló léziók eloszlása hasonló a perilobuláris NR-hez. A papilláris veserákot tartalmazó vesékben elsősorban a perilobuláris léziók dominálnak. Ezzel kapcsolatban érdemes megemlíteni, hogy mind a szövettani megfigyelések, gén expressziós és genetikai vizsgálatok alapján a Wilms tumorhoz társuló perilobuláris NR és interlobuláris NR szöveti formája meghatározza a belőlük kiinduló WT morfológiáját (Beckwith et al., 1990; Fukuzawa et al., 2008). Eredményeink alapján úgy véljük, hogy bizonyítottnak tekinthető a papilláris vese tumorok keletkezése és az embrionális szöveti differenciálódásának zavara közti összefüggés. Korábbi eredmények alapján már az 1-2 mm nagyságú papilláris preneoplasztikus léziókban minden esetben megtalálható 7-es és 17-es együttes triszómiája (Kovacs, 1989). A túlnyomóan férfiakban kiinduló papilláris vese tumorok 85%-ában a 7-es és 17-es kromoszómák triszómiájához az Y kromoszóma vesztése járul (Kovacs et al., 1994). Ezek az adatok arra utalnak, hogy a két kromoszómának és a rajtuk 13
14 elhelyezkedő gének elváltozásainak valamint az Y kromoszóma vesztésének a tumor kialakulásának korai fázisában van szerepe. A részletes szövettani vizsgálatok eredménye, és a papilláris vesetumorokhoz társuló pre-neoplasztikus léziók magas száma a két elváltozás közötti szoros összefüggésre utal. Továbbá nem hanyagolható el a pre-neoplasztikus léziók és a klinikailag észlelt tumorok hasonló citológiai megjelenése. A vizsgálatok során tett fontos megfigyelés volt, hogy a tumorokhoz társuló pre-neoplasztikus léziók minden esetben a tumorral azonos immunreakciót mutattak. A MET, HNF1B és KRT17 immunhisztológia mind a papilláris vesetumorban és a hozzá kapcsolódó pre-neoplasztikus lézióban pozitív volt. Az irodalomban korábban leirt ú.n. kortikális adenomák tulajdonképpen a prekurzor léziók már makroszkóposan is észlelhető formájának felel meg. Keyes (1890) több, mint 100 éve utalt ezen léziók gyakoriságára we do not regard it as extremely rare, since, owing the small size and inoffensive character of the growths, they are liable to be passed over without notice. Cristol és mtsai (1946) 22 veserák miatt eltávolított vese részletes vizsgálatával 37 papilláris szerkezetű adenomát figyeltek meg. Apitz (1944) több mint 4000 boncolásból 725 makroszkóposan észlelhető adenomát irt le. Mivel a papilláris veserák előfordulása férfiakban 5-10-szer gyakoribb, mint nőkben, és a férfiak és nők aránya Cristol és Apitz vizsgálatában 10:1 illetve 4.2:1 volt, feltételezhetjük, hogy mindkét szériában az adenomák papilláris vesetumorhoz társultak. Ezek az adatok megerősítik a prekurzor léziók és tumorok közti kapcsolatot, azt a feltevésünket, hogy a papilláris vesetumor embrionális eredetű prekurzor léziókból indul ki. Mindezek ellenére, a nemzetközi irodalomban a papilláris vese tumorok és társuló pre-neoplasztikus léziók szoros kapcsolatát figyelmen kívül hagyják és a papilláris vesetumor eredetét a vese differenciált tubulus sejtjeiben jelölik meg (Moch et al., 2016) A 7-es kromoszóma duplikációja/amplifikációja valamint a MET gén expressziója a papilláris vesetumor kialakulásában A MET szekvenálása vezetett a csirasejtes mutáció és a familiáris papilláris vese tumor közötti összefüggés felismerésére (Bentz et al. 1996; Schmidt et al., 1997). Mind a 14
15 familiáris mind a sporadikus papilláris vesetumorokban alapvető elváltozás a MET gén kópia számának változása és fokozott kifejeződése. A MET csírasejtes mutációja prekurzor léziók ezreinek, és papilláris vesetumoroknak a keletkezésével jár, amely fiatal korban, éves hordozókban jelentkezik (Ornstein et al., 2000, Schmidt et al., 1997, Fischer et al. 1998). A vizsgálatainkba bevont csírasejtes MET mutációt hordozó egyén 37 éves korában került mütétre multiplex kétoldali vese folyamat miatt. A klinikailag észlelt tumorok mellett számos mikroszkópos nagyságú papilláris léziókat találtunk. A fenti adatok arra utalnak, hogy a 7-es kromoszómán lokalizált MET lókusz duplikációjához, amplifikációjához társuló fokozott gén expressziónak valószínűleg fontos szerepe van az embrionális vese differenciálódási zavarában és a papilláris prekurzor léziók kialakulásában. A papilláris vesetumorokhoz hasonlóan a MET működésének zavarát a Wilms tumor kialakulásával is összefüggésbe hozták. A nephrogén restek 22%-ában és a belőlük kialakuló Wilms tumorok 54%-ában a MET expresszió növekedését észlelték (Vuononvirta et al., 2009). A HGF génje szintén a 7. kromoszómán található (7q21.11). Eddig nem mutatták ki HGF lokusz amplifikációját, így valószínűleg a papilláris vesetumorban, a 7. kromoszóma számbeli növekedésével csak egy extra HGF gén kópia fordul elő. Viszont a MET vad typusú allél amplifikációja sporádikus tumorokban felveti annak a lehetőségét, hogy a nagy sejtfelszíni denzitása miatt a MET receptor kináz a HGF interakciója nélkül is autofoszforilálódik és aktíválódik (Fischer et al., 1998; Zhuang et al., 1998; Glukhova et al., 2000). Immunhisztokémiával MET pozitivitás igazolódott a prekurzor léziókban és a tumorokban egyaránt. Kifejezett expresszió mutatkozott a periférián, a tubulárispapilláris struktúrák és a normál vesesejtek határán A 17-es kromoszóma duplikációja és a HNF1B (TCF2) transzkripciós faktor a papilláris vese tumorok kialakulásában A HNF1B (TCF2) gén a 17-es kromoszóma hosszú karján a q12 regióban egy bázispárnak megfelelő DNS szegmentben helyezkedik el. Ennek a körülírt DNS régiónak a papilláris vesetumorban felfedezett amplifikációja vezetett a gén felismeréséhez (Szponar et al., 2011). A HNF1B vese fejlődése során az ureterbimbó elágazódásában, a nephronok kialakulásának iniciálásában fontos szerepet játszik (Massa et al., 2013). A HNF1B felnőttekben kizárólag a polarizált epitheliális sejtekben 15
16 fejeződik ki (Fisher és Pontoglio, 2008). A vese tubuláris rendszer, a nefron a mesodermális blasztémából fejlődik ki és az ureter bimbó hatására alakul ki a tubuláris sejtek polarizációja. A HNF1B inaktiválása vagy a HNF1B domináns negatív formájának fokozott kifejeződése a vese tubulusok cisztikus kialakulásához vezet (Gresh et al., 2004; Hiesberger et al., 2004). A HNF1B funkciójának kiesése a vese és a húgyútrendszer komoly kongenitális fejlődési rendellenességet okozhatja (Nakayama et al., 2010). Vizsgálataink szerint a HNF1B először az epitelizáció során a renális vezikulában és az S forma disztális kompartmentjében valamint a disztális tubulusokban mutat erőteljes kifejeződést, míg az urterbimbó és a proximális tubulusok csak enyhe reakciót adnak a HNF1B antitesttel. A prekurzor léziók a mesenchyma epitheliális tranzíción átment polarizált embrionális képletekből indulnak ki. Vizsgálataink során a csirasejtes MET mutációhoz valamint a sporadikus papilláris vesetumorokhoz társult epitheliális prekurzor léziókban kifejezett HNF1B pozitivitást találtunk A 17-es kromoszóma duplikációja és a KRT17 expressziója a preneoplasztikus léziókban és papilláris vesetumorokban A keratinok intermedier filamentumok, amik a sejt integritásában és stabilitásában kulcsfontosságú szerepet játszanak. A KRT17 expresszióját kimutatták gyomor adenocarcinomában, petefészek- és emlő carcinomában, papilláris pajzsmirigy rákban, de e szervek ép szöveti körülményei között a KRT17 nem fejeződik ki. Ezek alapján a daganatokban a KRT17 neo-expressziójától beszélhetünk. A KRT17 kifejeződése egyes daganatok progressziójával és metasztázis hajlamával hozható összefüggésbe. A KRT17 kifejeződése a daganat progressziójával és metasztatizáló hajlamával korrelál. (van de Rijn et al., 1996; Ide et al., 2012; Escobar-Hoyos et al., 2014; Mockler et al., 2011; Wang et al., 2011; Kim et al., 2015; Hu et al., 2018). Kimutattuk, hogy a KRT17 megtalálható az ureterbimbóban és a fötális vese gyűjtőcsatornájában és a felnőtt vese összekötő csatornájában. Első alkalommal került leírásra egyszerű (egy sejtsoros) epitheliumban a KRT17 jelenléte. A papilláris tumorok 77%-ban megtalálható volt a KRT17, sejt morfológiától függetlenül. Figyelembe véve, hogy a papilláris vese tumorok döntő többségében megtalálható a KRT17, és, hogy ezen daganatok mindösszesen 6%-es mutatott metasztázis hajlamot 5 éves utánkövetési idő során, a KRT17 papilláris vese tumorok progressziójában játszott szerepe kétséges. 16
17 A KRT17-nek, mint a basalis epithelialis és myoepithelialis sejtek specifikus markerének kifejeződése egy egyszerű, egy rétegű epitheliumban a fötális és felnőtt vesében, önmagában érdekes felfedezés. Ez mellett a KRT17 folyamatos kifejeződése a fejlődő vesében, a prekurzor léziókban és a papilláris vese tumorok közel 80%-ában arra enged következtetni, hogy a KRT17 a papilláris vesedaganatok karcinogenezisében is szerepet játszhat Az Y kromoszóma hiánya és a PCDH11XY expressziója prekurzor léziókban és papilláris vesetumorban A PCDH11Y csakúgy, mint az Xq21.3 régióban lokalizált PCDH11X gén a protokadherin gének családjába tartozik, amelyeknek fontos szerepe van a sejt-sejt kapcsolatban és az agy szegmentális kifejlődésében és funkciójában (Hirano et al., 1999; Blanco et al., 2000). Immunhisztológiai vizsgálatunk arra utal, hogy a PCDH11Y génnek jelentős szerepe van a vese fejlődés korai szakaszában. A már kondenzálódott blasztémális sejtekben jelenik meg először és a mesenchyma epitheliális tranzíciója során egyre fokozott kifejeződését figyeltük meg. Ez arra utal, hogy a protocadherin PCDH11Y expressziója fontos a blasztémális sejtek epitelizációjához, a disztális tubuláris rendszer normális kifejlődéséhez. Feltételezésünk szerint a PCDH11Y hiánya a mesenchyma epitheliális tranzíciójának kezdeti szakaszán átment sejtek további differenciálódási zavarához és így a prekurzor léziók kialakulásához vezet Modell a papilláris vesetumor kialakulására A papilláris vese tumor embrionális eredete, a normális vesefejlődés során lokálisan kialakult differenciálódási zavar, a prekurzor léziók perzisztálása az élet folyamán és jóindulatú és azon túlmenően rosszindulatú tumor kialakulásához vezető későbbi proliferációja alapján javasoljuk a differenciálódási zavar - prekurzor lézió - adenómakarcinóma szekvenciát a papilláris vese tumorok kialakulására (Kovacs, 1993; Bányai, Sarlós et al., 2018). Ezeket a morfológiai/biológiai megjelenési formákat a papilláris léziókban kialakuló genetikai elváltozásokkal tudjuk alátámasztani. Az ú.n. klonális tumor fejlődés szerint nagyobb proliferációs képességgel rendelkező klónok túlnövik a 17
18 többi sejtek és a későbbiekben meghatározzák az egész tumor genetikai karakterét és biológiai viselkedését. Molekuláris patológiai szemlélet alapján helytelen, hogy a jelenleg érvényes tumor klasszifikáció szerint a jóindulatú adenomát és a rosszindulatú daganatot csupán mérete különbözteti meg egymástól (Moch et al., 2016). Ha következetesen a papilláris vesedaganat kifejezést használjuk, az mind az adenomát, mind a karcinómát magába foglalja. Korábban a genetikai vizsgálatokra alapozva papilláris vese tumorok osztályozására adenóma-karcinóma szekvencia volt javasolva (Szponar et al., 2009). Ez szerint az adenoma a 7-es és 17-es kromoszómák triszómiájával társul, míg karcinómában 8-as, 16-os és 20-as kromoszómák triszómiája, majd további aberrációk jelennek meg. A HNF1B és MET expressziója embrionális vesében, prekurzor lézióban és papilláris vesetumorban, ennek összefüggése a 7-es és 17-es kromoszómák triszómiájával, és a csírasejtes MET mutációs kromoszóma duplikációjával arra utal, hogy összefüggés van a megnövekedett gén-dózis és a génexpresszió közt. 6. Következtetések A WHO és ISUP klasszifikációja szerint a papilláris vese karcinóma a az epitheliális vese tubulusokból indul ki és az adenóma és karcinóma között csak a tumor mérete dönt: Papillary adenomas are uncapsulated tumours with papillary or tubular architecture of low grade (ISUP) and a diameter <15 mm (WHO, 2016). Papillary renal cell carcinoma is a malignant tumour derived from renal tubular epithelium. It has papillary or tubulopapillary architecture. (WHO, 2016) A vizsgálataink célja volt a papilláris vese tumorok eredetének tisztázása. Figyelembe véve a legkorábbi genetikai eltéréseket, azaz a 7-es és 17-es kromoszómák duplikációját és amplifikációját és a változásokba bevont gének, mint a MET, HNF1B, KRT17 folyamatos kifejeződését fötális vesékben, prekurzor léziókban és papilláris vesetumorokban, bizonyítottnak tekintjük a papilláris vese tumorok embrionális differenciálódási zavaron alapuló eredetét. Elméletünket támogatja a PCDH11XY gén 18
19 fokozott, időben és térben meghatározott kifejeződése az embryinális vesefejlődés során, amely a differenciálódott nefronban és papilláris vesetumorban már nem mutatható ki. Összefoglalva, véleményünk szerint a papilláris vesetumor specifikus genomikus és génexpressziós elváltozásokon alapuló embrionális differenciálódási zavar, prekurzor lézió, adenoma és karcinóma fejlődési szekvenciát mutat. 7. Közlemények 8.1. Az értekezés témájához kapcsolódó közlemények Sarlós DP, Bányai D, Péterfi L, Szántó Á, Kovacs G. Embryonal origin of metanephric adenoma and its differential diagnosis. Anticancer Res 38: , IF 1,86 Sarlós DP, Péterfi L, Szántó Á, Kovacs G. Shift of keratin expression profile in end-stage kidney increases the risk of tumor development. Anticancer Res 38(9): , IF 1,86 Bányai D, Sarlós DP, Nagy A, Kovacs G. Recalling Cohnheim's theory: Papillary renal cell tumor as a model of tumorigenesis from impaired embryonal development to malignant tumors in adults. Int J Biol Sci 14: , IF 3, Az értekezés témájához nem kapcsolódó közlemények Sarlós DP, Czétány P. Új laparoszkópos vesetumor-reszekció gyakorló modell kifejlesztése. Magyar Urológia 30:8-11, Pusztai Cs, Bányai D, Jávorházy A, Kenyeres B, Sarlós P, Szántó Á. Laparoszkópos parciális nephrectomia a technikailag komplex vesetumorok sebészi ellátásában. Magyar Urológia 27: , Tamás A, Jávorházy A, Reglődi D, Sarlós DP, Bányai D, Semjén D, Németh J, Lelesz B, Fülöp DB, Szántó Z. Examination of PACAP-like immunoreactivity in urogenital tumor samples. J Mol Neurosci 59: , IF 2,229 Pusztai Cs, Bányai D, Sarlós DP, Farkas L, Szántó Á, Semjén D. Laparoszkópia szerepe a vese angiomyolipomák sebészi kezelésében Magyar Urológia 27:2-6, Farkas N, Szabó A, Lóránd V, Sarlós DP, Minier T, Prohászka Z, Czirják L, Varjú C. Clinical usefulness of measuring red blood cell distribution width in patients with systemic sclerosis. Rheumatology (Oxford) 53: , IF Sarlós DP, Kispál ZF, Bíró E, Tornóczky T, Környey J, Sánta I, Pintér A, Vástyán A. Lézerbesugárzás hatása patkány gyomornyálkahártyára: szövettani és funkcionális vizsgálatok előzetes közlemény. Magyar Urológia 23(2):34-38, Impakt faktor: Első szerzős: 3,72 Kumulatív: 14,224 19
20 8. Köszönetnyilvánítás Köszönettel tartozom témavezetőimnek, Prof. Dr. Kovács Gyulának, hogy a lehetőséget adott a vesedaganatok molekuláris onkológiájával foglalkozó kutatócsoporthoz való csatlakozásra, és kutatási tevékenységemet segítőkészen irányította, és Dr. Szántó Árpádnak, hogy a kutatási tevékenységemet mindvégig támogatta. Köszönet illeti a Heidelbergi Egyetem Molekuláris Onkológiai Labor munkatársait kutatásunk több, fontos vizsgálatának elvégzéséért. Köszönöm a PTE KK Pathologiai Intézet munkatársainak (Dr. Tornóczki Tamás, Dr. Kálmán Endre, Dr. Semjén Dávid, Dr. Pap Anita, Dr. Fincsur András, Dr. Gyömörei Csaba, Halas Zsuzsanna, Szilágyi Imréné Judit) kutatásunkhoz nyújtott önzetlen segítségét. Köszönöm korábbi témavezetőimnek, Prof. Dr. Czirják Lászlónak, Prof. Dr. Balogh Péternek, Dr. Vástyán Attilának hogy munkájukkal nagyban hozzájárultak tudományos fejlődésemhez. Köszönöm a PTE KK Urológiai Klinika minden munkatársának a kutatásban, és a betegellátásban nyújtott segítségüket. Köszönöm családtagjaimnak, hogy mellettem álltak és szeretetükkel támogattak. 20
Tumor specifikus DNS/gén dózis szerepe a papilláris vesetumor kialakulásában
 Tumor specifikus DNS/gén dózis szerepe a papilláris vesetumor kialakulásában Doktori (PhD) értekezés Szerző: Dr. Sarlós Donát Péter Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2019.
Tumor specifikus DNS/gén dózis szerepe a papilláris vesetumor kialakulásában Doktori (PhD) értekezés Szerző: Dr. Sarlós Donát Péter Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2019.
Embryonális eredetű vesetumorok molekuláris pathologiája
 Embryonális eredetű vesetumorok molekuláris pathologiája Doktori (PhD) értekezés tézisei dr. Bányai Daniel Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2018 Doktori iskolavezetője: Prof.
Embryonális eredetű vesetumorok molekuláris pathologiája Doktori (PhD) értekezés tézisei dr. Bányai Daniel Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2018 Doktori iskolavezetője: Prof.
Embryonális eredetű vesetumorok molekuláris pathologiája
 Embryonális eredetű vesetumorok molekuláris pathologiája Doktori (PhD) értekezés Szerző: dr. Bányai Daniel Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2019 Doktori iskolavezetője: Prof.
Embryonális eredetű vesetumorok molekuláris pathologiája Doktori (PhD) értekezés Szerző: dr. Bányai Daniel Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2019 Doktori iskolavezetője: Prof.
NEM-VILÁGOSSEJTES VESERÁKOK
 NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
NEM-VILÁGOSSEJTES VESERÁKOK SomoráczÁron SEMMELWEIS EGYETEM Általános Orvostudományi Kar 2. sz. Patológiai Intézet http://semmelweis.hu/patologia2 A vesesejtes daganatok osztályozása - WHO 2016 I. Új entitások
A hólyagrák aktuális kérdései a pathologus szemszögéből. Iványi Béla SZTE Pathologia
 A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet. Frank Diagnosztika Szimpózium, DAKO workshop 2012.
 Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
67. Pathologus Kongresszus
 A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA. Dr. Kurgyis Zsuzsanna
 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Molekuláris genetikai vizsgáló. módszerek az immundefektusok. diagnosztikájában
 Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody
 CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében
 A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend)
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás
 Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján)
 pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3,
 Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet november 19., ÁOK, III.
 ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
Emlőpatológia. II. Sz. Patológiai Intézet Semmelweis Egyetem
 Emlőpatológia II. Sz. Patológiai Intézet Semmelweis Egyetem Emlőpatológia áttekintés - Benignus léziók - Acut mastitis - Plasmasejtes mastitis / ductectasia - Zsírnekrózis - Fibrocisztás / proliferatív
Emlőpatológia II. Sz. Patológiai Intézet Semmelweis Egyetem Emlőpatológia áttekintés - Benignus léziók - Acut mastitis - Plasmasejtes mastitis / ductectasia - Zsírnekrózis - Fibrocisztás / proliferatív
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában. Cifra János. Tolna Megyei Balassa János Kórház, Pathologia Osztály
 A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK
 Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK HISTORY Antitestet találtak egy koraszülött gyermek anyjának szérumában; ez lenne felelős a gyermek haláláért?
Rh VÉRCSOPORT RENDSZER GENETIKÁJA. Rh ANTIGÉNEK ÉS ANTITESTEK. EGYÉB VÉRCSOPORTRENDSZEREK HISTORY Antitestet találtak egy koraszülött gyermek anyjának szérumában; ez lenne felelős a gyermek haláláért?
Immunológia Alapjai. 13. előadás. Elsődleges T sejt érés és differenciálódás
 Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
Immunológia Alapjai 13. előadás Elsődleges T sejt érés és differenciálódás A T és B sejt receptor eltérő szerkezetű A T sejt receptor komplex felépítése + DOMÉNES SZERKEZET αβ ΤcR SP(CD4+ vagy CD8+) γδ
A pre-analitika szerepe a patológiai minták. Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet
 A pre-analitika szerepe a patológiai minták megőrz rzöttségében Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet A sebészeti anyagok útja Műtő OPTIMÁLIS HŐMÉRSÉKLET (20-22 C) IDŐFAKTOR (15
A pre-analitika szerepe a patológiai minták megőrz rzöttségében Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet A sebészeti anyagok útja Műtő OPTIMÁLIS HŐMÉRSÉKLET (20-22 C) IDŐFAKTOR (15
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok
 Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek?
 Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Általános daganattan II.
 Általános daganattan II. Benignus és malignus hámtumorok Semmelweis Egyetem II. Sz. Patológiai Intézet Neoplasia fogalma Kóros szövetszaporulat Genetikai és epigenetikai változásokon alapuló klonális proliferáció
Általános daganattan II. Benignus és malignus hámtumorok Semmelweis Egyetem II. Sz. Patológiai Intézet Neoplasia fogalma Kóros szövetszaporulat Genetikai és epigenetikai változásokon alapuló klonális proliferáció
Esetbemutatás. Dr. Iván Mária Uzsoki Kórház 2013.11.07.
 Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Engedélyszám: /2011-EAHUF Analitika követelménymodul szóbeli vizsgafeladatai
 1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK
 SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
Intraocularis tumorok
 Intraocularis tumorok 25 évvel ezelőtt, ha egy szemben chorioidea melanomát találtunk, akkor a szemet enucleáltuk. Szemben lévő festékes daganat (melanoma chorioideae) Chorioidea melanoma miatt eltávolított,
Intraocularis tumorok 25 évvel ezelőtt, ha egy szemben chorioidea melanomát találtunk, akkor a szemet enucleáltuk. Szemben lévő festékes daganat (melanoma chorioideae) Chorioidea melanoma miatt eltávolított,
A tüdő adenocarcinomák szubklasszifikációja. Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5.
 A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
A tüdő adenocarcinomák szubklasszifikációja Dr. Szőke János Molekuláris Patológiai Osztály Budapest, 2008 december 5. Háttér A tüdő ACA heterogén tumor csoport és a jelenlegi klasszifikáció elsősorban
Kappelmayer János. Malignus hematológiai megbetegedések molekuláris háttere. MOLSZE IX. Nagygyűlése. Bük, 2005 szeptember
 Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Dr. Máthéné Dr. Szigeti Zsuzsanna és munkatársai
 Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában
 Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
Adenoma-carcinoma szekvenciában szereplő polypoid elváltozások osztályozása
 Adenoma-carcinoma szekvenciában szereplő polypoid elváltozások osztályozása Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Henry D. Appelman recommends calling
Adenoma-carcinoma szekvenciában szereplő polypoid elváltozások osztályozása Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Henry D. Appelman recommends calling
A pajzsmirigy benignus és malignus daganatai
 A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
A pajzsmirigy benignus és malignus daganatai Dr. Boér András Országos Onkológiai Intézet 25 évesen az átlag népesség 10%-nak 70 évesen 55%-nak UH-gal van pajzsmirigy göbe, szoliter pajzsmirigygöb vagy
Invazív méhnyakrákos esetek az előzmények tükrében
 Invazív méhnyakrákos esetek az előzmények tükrében Márton Béla DE-ÁOK PA III. évfolyamos hallgató Témavezető: Dr. Kovács Ilona PhD. DE Kenézy Gyula Kórház Patológia Epidemiológiai adatok Méhnyakrák epidemiológiai
Invazív méhnyakrákos esetek az előzmények tükrében Márton Béla DE-ÁOK PA III. évfolyamos hallgató Témavezető: Dr. Kovács Ilona PhD. DE Kenézy Gyula Kórház Patológia Epidemiológiai adatok Méhnyakrák epidemiológiai
Mit is csinál pontosan a patológus?
 Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
A vesedaganatok sebészi kezelése
 A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
A 22C3 PD-L1 tesztek értékelése intézetünkben. Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs
 A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
A 22C3 PD-L1 tesztek értékelése intézetünkben Dr. László Terézia PTE ÁOK Patológiai Intézet, Pécs NSCLC NSCLC SCLC Előrehaladott tüdőrák kezelésének eredményessége az 1990-es évekig a kimenetel független
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
KERINGŐ EXTRACELLULÁRIS VEZIKULÁK ÁLTAL INDUKÁLT GÉNEXPRESSZIÓS MINTÁZAT VIZSGÁLATA TROPHOBLAST SEJTVONALBAN
 2016. 10. 14. KERINGŐ EXTRACELLULÁRIS VEZIKULÁK ÁLTAL INDUKÁLT GÉNEXPRESSZIÓS MINTÁZAT VIZSGÁLATA TROPHOBLAST SEJTVONALBAN Kovács Árpád Ferenc 1, Pap Erna 1, Fekete Nóra 1, Rigó János 2, Buzás Edit 1,
2016. 10. 14. KERINGŐ EXTRACELLULÁRIS VEZIKULÁK ÁLTAL INDUKÁLT GÉNEXPRESSZIÓS MINTÁZAT VIZSGÁLATA TROPHOBLAST SEJTVONALBAN Kovács Árpád Ferenc 1, Pap Erna 1, Fekete Nóra 1, Rigó János 2, Buzás Edit 1,
Új biomarkerek a konvencionális veserák progressziójának megítélésére. Doktori (PhD) értekezés tézisei. Szerző: Dr.
 Új biomarkerek a konvencionális veserák progressziójának megítélésére Doktori (PhD) értekezés tézisei Szerző: Dr. Jávorházy András Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2017 Doktori
Új biomarkerek a konvencionális veserák progressziójának megítélésére Doktori (PhD) értekezés tézisei Szerző: Dr. Jávorházy András Pécsi Tudományegyetem, Klinikai Központ Urológiai Klinika Pécs, 2017 Doktori
meghatározásának jelentősége
 A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
A HerHer-2 státusz meghatározásának jelentősége gyomorkarcinomában Tímár József, Szirtes Ildikó, Lotz Gábor, Kulka Janina SE 2.sz. Pathologiai Intézet 140 HER-2 fokozott expressziót mutató Emlőrák 20%
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata
 Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
A világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási eljárásrendje
 MGYRKÖZLÖNY 2010. évi 77. szám 16751 2. melléklet a 31/2010. (V. 13.) EüM rendelethez világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási eljárásrendje 1. z eljárásrend tárgyát
MGYRKÖZLÖNY 2010. évi 77. szám 16751 2. melléklet a 31/2010. (V. 13.) EüM rendelethez világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási eljárásrendje 1. z eljárásrend tárgyát
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Engedélyszám: 18211-2/2011-EAHUF Verziószám: 1. 2460-06 Humángenetikai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
1. eset. Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály
 1. eset Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Anamnézis 42 éves férfi véres széklet hátterében más intézetben az anustól3 cm-re kezdődően 11-12 cm hosszan
1. eset Dr. Strausz Tamás Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály Anamnézis 42 éves férfi véres széklet hátterében más intézetben az anustól3 cm-re kezdődően 11-12 cm hosszan
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén
 Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Országos Egészségbiztosítási Pénztár. A világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A világossejtes vesedaganatok diagnosztikájának és 2012-ben felülvizsgált TERVEZET 2013.05.24 Országos Egészségbiztosítási Pénztár Egészség, biztonság! 1. Azonosítószám: 5/2009 1.2. Az eljárásrend tárgyát
A világossejtes vesedaganatok diagnosztikájának és 2012-ben felülvizsgált TERVEZET 2013.05.24 Országos Egészségbiztosítási Pénztár Egészség, biztonság! 1. Azonosítószám: 5/2009 1.2. Az eljárásrend tárgyát
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában
 Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
A patológiai vizsgálatok metodikája. 1. Biopsziástechnikák 2. Speciális vizsgálatok
 A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
A patológiai vizsgálatok metodikája 1. Biopsziástechnikák 2. Speciális vizsgálatok Biopsziaindikációk Diffus/multifocalis eltérések Folyamat etiológiájának tisztázása Szisztémás kezeléshez szükséges paraméterek
Emlőbetegségek komplex diagnosztikája
 Emlőbetegségek komplex diagnosztikája Preoperatív citológiai-patológiai diagnosztika Dr. Hamar Sándor SZTE ÁOK Patológiai Intézet Emlőbetegségek diagnosztikája Az emlőbetegségek diagnosztikájában a nem
Emlőbetegségek komplex diagnosztikája Preoperatív citológiai-patológiai diagnosztika Dr. Hamar Sándor SZTE ÁOK Patológiai Intézet Emlőbetegségek diagnosztikája Az emlőbetegségek diagnosztikájában a nem
BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben
 Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
GRADING. Az emlő invazív és in situ carcinomái. Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet
 GRADING Az emlő invazív és in situ carcinomái Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet Invazív carcinoma Scarff-Bloom-Richardson grade Elston és Ellis által módosított Scarff- Bloom-Richardson
GRADING Az emlő invazív és in situ carcinomái Kulka Janina Semmelweis Egyetem II. sz. Pathologiai Intézet Invazív carcinoma Scarff-Bloom-Richardson grade Elston és Ellis által módosított Scarff- Bloom-Richardson
73. Patológus Kongresszus Siófok, szeptember Előzetes program
 2017. szeptember 28. csütörtök 09:00 10:30 Rezidens metszetszeminárium 73. Patológus Kongresszus 09:00 09:40 Prof.Dr. Kemény Éva: SZTE SZAKK Pathologiai Intézet, Szeged Glomerulonephritisek 09:40 10:20
2017. szeptember 28. csütörtök 09:00 10:30 Rezidens metszetszeminárium 73. Patológus Kongresszus 09:00 09:40 Prof.Dr. Kemény Éva: SZTE SZAKK Pathologiai Intézet, Szeged Glomerulonephritisek 09:40 10:20
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Opponensi Vélemény Dr. Nagy Bálint A valósidejű PCR alkalmazása a klinikai genetikai gyakorlatban ' című értekezéséről
 Opponensi Vélemény Dr. Nagy Bálint A valósidejű PCR alkalmazása a klinikai genetikai gyakorlatban ' című értekezéséről Dr. Nagy Bálint az MTA doktora fokozat megszerzéséhez a fenti címen nyújtott be a
Opponensi Vélemény Dr. Nagy Bálint A valósidejű PCR alkalmazása a klinikai genetikai gyakorlatban ' című értekezéséről Dr. Nagy Bálint az MTA doktora fokozat megszerzéséhez a fenti címen nyújtott be a
szerepe a gasztrointesztinális
 A calprotectin és egyéb biomarkerek szerepe a gasztrointesztinális gyulladásos betegségek differenciál diagnosztikájában 1 Halmainé Kiss Ilona, 2 Rutka Mariann, 1 Földesi Imre Szegedi Tudományegyetem 1
A calprotectin és egyéb biomarkerek szerepe a gasztrointesztinális gyulladásos betegségek differenciál diagnosztikájában 1 Halmainé Kiss Ilona, 2 Rutka Mariann, 1 Földesi Imre Szegedi Tudományegyetem 1
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Hasi tumorok gyermekkorban
 Hasi tumorok gyermekkorban Dr. Bartyik Katalin SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A gyermekkori tumorok a halálozási oki tényezői közül a 2. helyen állnak a balesetek,
Hasi tumorok gyermekkorban Dr. Bartyik Katalin SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A gyermekkori tumorok a halálozási oki tényezői közül a 2. helyen állnak a balesetek,
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL
 ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010.
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010.
DNS-szekvencia meghatározás
 DNS-szekvencia meghatározás Gilbert 1980 (1958) Sanger 3-1 A DNS-polimerázok jellemzői 5'-3' polimeráz aktivitás 5'-3' exonukleáz 3'-5' exonukleáz aktivitás Az új szál szintéziséhez kell: templát DNS primer
DNS-szekvencia meghatározás Gilbert 1980 (1958) Sanger 3-1 A DNS-polimerázok jellemzői 5'-3' polimeráz aktivitás 5'-3' exonukleáz 3'-5' exonukleáz aktivitás Az új szál szintéziséhez kell: templát DNS primer
Többgénes jellegek. 1. Klasszikus (poligénes) mennyiségi jellegek. 2.Szinte minden jelleg több gén irányítása alatt áll
 Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben
 DOKTORI (PHD) ÉRTEKEZÉS TÉZISEI Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben Bebes Attila Témavezető: Dr. Széll Márta tudományos tanácsadó Szegedi Tudományegyetem Bőrgyógyászati
DOKTORI (PHD) ÉRTEKEZÉS TÉZISEI Xenobiotikum transzporterek vizsgálata humán keratinocitákban és bőrben Bebes Attila Témavezető: Dr. Széll Márta tudományos tanácsadó Szegedi Tudományegyetem Bőrgyógyászati
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Többes malignus tumoros eseteink elemzése. Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya
 Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Antigén, Antigén prezentáció
 Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Antigén, Antigén prezentáció Biológiai Intézet Immunológiai Tanszék Bajtay Zsuzsa ELTE, TTK Biológiai Intézet Immunológiai Tanszék ORFI Klinikai immunológia tanfolyam, 2019. február. 26 Bev. 2. ábra Az
Neoplazma - szabályozottság nélküli osztódó sejt
 9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
mintasepcifikus mikrokapilláris elektroforézis Lab-on-Chip elektroforézis / elektrokinetikus elven DNS, RNS, mirns 12, fehérje 10, sejtes minta 6
 Agilent 2100 Bioanalyzer mikrokapilláris gélelektroforézis rendszer G2943CA 2100 Bioanalyzer system forgalmazó: Kromat Kft. 1112 Budapest Péterhegyi u. 98. t:36 (1) 248-2110 www.kromat.hu bio@kromat.hu
Agilent 2100 Bioanalyzer mikrokapilláris gélelektroforézis rendszer G2943CA 2100 Bioanalyzer system forgalmazó: Kromat Kft. 1112 Budapest Péterhegyi u. 98. t:36 (1) 248-2110 www.kromat.hu bio@kromat.hu
Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában
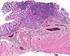 1 Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium
1 Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása.
 Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
Diagnosztikai célú molekuláris biológiai vizsgálatok
 Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás
 Kovács Ilona Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás (Hamberger et al. 1982) FNA használata mellett
Kovács Ilona Az FNA a leggyakrabban használt módszer a pajzsmirigy nodulusok tisztázásában Az FNA használata előtt a pajzsmirigy műtétek 14%-ban volt malignitás (Hamberger et al. 1982) FNA használata mellett
Immunhisztokémia: Előhívó rendszerek, problémák és megoldások
 Immunhisztokémia: Előhívó rendszerek, problémák és megoldások Dr. Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet Budapest Patológus Klasszikus patomorfológia Klinikai
Immunhisztokémia: Előhívó rendszerek, problémák és megoldások Dr. Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet Budapest Patológus Klasszikus patomorfológia Klinikai
Az Idegsebészeti Szövetbank jelentősége a neuro-onkológiai kutatásokban
 Az Idegsebészeti Szövetbank jelentősége a neuro-onkológiai kutatásokban Augusta - Idegsebészet Klekner Álmos 1, Bognár László 1,2 1 Debreceni Egyetem, OEC, Idegsebészeti Klinika, Debrecen 2 Országos Idegsebészeti
Az Idegsebészeti Szövetbank jelentősége a neuro-onkológiai kutatásokban Augusta - Idegsebészet Klekner Álmos 1, Bognár László 1,2 1 Debreceni Egyetem, OEC, Idegsebészeti Klinika, Debrecen 2 Országos Idegsebészeti
2354-06 Nőgyógyászati citodiagnosztika követelménymodul szóbeli vizsgafeladatai
 1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
Nagyon köszönöm a disszertáció alapvetően pozitív megítélését és a gondos bírálatot. A következőkben válaszolok a feltett kérdésekre.
 Válasz Dr. Tamás Gábor bírálói véleményére Tisztelt Professzor Úr, Nagyon köszönöm a disszertáció alapvetően pozitív megítélését és a gondos bírálatot. A következőkben válaszolok a feltett kérdésekre.
Válasz Dr. Tamás Gábor bírálói véleményére Tisztelt Professzor Úr, Nagyon köszönöm a disszertáció alapvetően pozitív megítélését és a gondos bírálatot. A következőkben válaszolok a feltett kérdésekre.
A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei
 Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Veserákok pathomorphologiája és molekuláris pathológiája
 Veserákok pathomorphologiája és molekuláris pathológiája WHO (2016) Classification Renal Cell Tumors Clear cell renal cell carcinoma Multilocular cystic renal neoplasm of low malignant potential Papillary
Veserákok pathomorphologiája és molekuláris pathológiája WHO (2016) Classification Renal Cell Tumors Clear cell renal cell carcinoma Multilocular cystic renal neoplasm of low malignant potential Papillary
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház. Emlő MR vizsgálatok korai eredményei kórházunkban
 DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
A göbös pajzsmirigy kivizsgálása, ellátása. Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika
 A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
PrenaTest Újgenerációs szekvenálást és z-score
 PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán
 A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
A stresszteli életesemények és a gyermekkori depresszió kapcsolatának vizsgálata populációs és klinikai mintán Doktori értekezés tézisei Dr. Mayer László Semmelweis Egyetem Mentális Egészségtudományok
