I./4. fejezet: Daganatos betegségek genetikai háttere
|
|
|
- Pál Fekete
- 6 évvel ezelőtt
- Látták:
Átírás
1 I./4. fejezet: Daganatos betegségek genetikai háttere Génhibák a daganatok kialakulásában Matolcsy András A fejezet legfőbb célja, hogy a daganatos betegségekben előforduló és a betegség diagnosztikájában vagy kezelésében meghatározó génhibákat a hallgató megismerje, és a genetikai eltérések kialakulásáról komplex képet alkothasson. A fejezetben foglaltak elsajátításával a hallgató értelmezni tudja az egyes génhibákat, azokat a megfelelő daganatos betegségekhez tudja kötni. Az egyes génhibákat használni tudja a daganatos betegségek diagnosztikájában és célzott terápiájában. Bevezetés A tumorsejtek genetikai hibák, mutációk sokaságát hordozzák. Ezen genetikai eltérések egy része a daganatok kialakulásában, mások a daganatok progressziójában vesznek részt. A genetikai eltérések ismerete fontos a betegségek diagnosztikájában és a betegség prognózisának megítélésében. A genetikai eltérések egy része terápiás célpontot képvisel a betegség kezelésében. A fejezetben a daganatos betegségekben leggyakrabban előforduló genetikai eltérések kerülnek bemutatásra. Kulcsszavak: Transzlokáció, kromoszomális imbalance, pontmutáció, genetikai instabilitás, mikro-rns eltérések A fejezet felépítése A. Transzlokáció B. Kromoszomális imbalance C. Pontmutációk D. Genetikai instabilitás E. Örökletes génhibák F. Mikro-RNS eltérések Epigenetikai hatások G. A genetikai léziók kialakulásának algoritmusa H. Összefoglalás Génhibák a daganatok kialakulásában Milyen nagy csoportokba oszthatók a génhibák típus szerint? A daganatok kialakulásában szerepet játszó genetikai eltérések két csoportra oszthatóak: egy részük (deletiok, pontmutációk és epigenetikai eltérések) a gének, általában a tumor suppressor gének inaktiválásában, másik csoportjuk (transzlokációk, amplificatiók, pontmutációk) a gének, általában az onkogének aktiválásában vagy regulációjuk megváltozásában játszik szerepet. A napjainkban széles körben elfogadott, Knudson által felvázolt két-találat elmélet alapján a malignus transzformációhoz legalább két genetikai lézió, vagyis az adott gén (általában tumor suppressor gén) mindkét alléljának inaktivációja szükséges. Az öröklődő daganatok esetében az első genetikai lézió csírasejtes mutáció, míg sporadikus daganatoknál szomatikus mutáció. A második genetikai lézió során a másik allél deletiója, heterozigota-vesztése (loss of heterozygosity, LOH), pontmutációja vagy hypermetilációja okozza az adott gén funkciójának teljes felfüggesztését. Ebből adódóan az esetek többségében az alábbiakban felsorolt genetikai léziók különböző kombinációkban együttesen is előfordulhatnak.
2 Az egyes betegségekre jellemző genetikai léziók fontos diagnosztikai markerek a daganatok diagnosztikájában és egyben fontos terápiás célpontok. A. Transzlokáció Az onkogének milyen módon aktiválódhatnak transzlokációk során? A transzlokációk elsősorban onkogének aktivációján keresztül játszanak szerepet a neoplasticus transzformáció folyamatában. A transzlokációk két úton aktiválhatják az onkogéneket. Egyrészről a transzlokáció során megváltozik az adott onkogén szabályozása azáltal, hogy elkerül normális regulátora mellől, és más gének promoterrégiójának irányítása alá kerül; másrészről a transzlokáció következtében új funkcióval rendelkező, kimera-proteint kódoló fúziós gének alakulhatnak ki. A promoterrégió cseréje során kialakuló onkogén-aktiváció nem változtatja meg az adott onkogén nukleinsav és fehérje szerkezetét, csupán a normális onkogén expressziós szintje változik meg. Ezzel ellentétben a fúziós onkoproteinek esetében egy új fehérje, és ebből adódóan egy új onkogénhatás alakul ki. A fúziós gének tirozin-kináz vagy transcriptiós faktorok kódolásán keresztül járulnak hozzá az onkogenezishez. 1. ábra. Translocatió okozta onkogén aktiváció sematikus ábrázolása. A: Promoterrégió-csere. B: Fúziós kimeragén kialakulása. A National Cancer Institute, Cancer Genome Anatomy Project keretében elkészített kromoszóma-transzlokációs térképből nyilvánvalóvá vált, hogy a humán kromoszómák gyakorlatilag minden régiója részt vesz a transzlokációkban, és ebből adódóan a neoplasticus transzformáció folyamatában részt vevő gének skálája rendkívül széles. A transzlokációk típusát tekintve jóval gyakoribbak a kiegyensúlyozott transzlokációk, mint a kiegyensúlyozatlanok. Jóllehet minden daganattípusban előfordulhatnak transzlokációk, a visszatérő, betegségtípusra jellemző transzlokációk elsősorban a hematológiai daganatokban és sarcomákban fordulnak elő. 1. táblázat. Gyakori kromoszóma-transzlokációk daganatos betegedésekben A transzlokációk kialakulásának mechanizmusában elsősorban a DNS-törések (doublestrand break, DSB) játszanak szerepet. Ezen DNS-törések fiziológiás körülmények között a lymphoid sejtek antigén receptorainak átrendeződése és a nehézlánc-gének izotípusváltása során alakulnak ki, de létrejöhetnek patológiás körülmények között is különböző DNS-károsító hatásokra (pl. irradiáció) is. Számos adat utal arra, hogy a transzlokáció az első lépés a daganatos transzformáció folyamatában, azonban az esetek többségében a daganatos klón kialakulásához további onkogén hatások szükségesek. Ezt az elképzelést támogatja, hogy az egészséges populációban érzékeny PCR technológiával tumorspecifikus transzlokációk [pl. a follicularis lymphomára jellemző t(14;18) translocatio] mutathatók ki, anélkül, hogy az adott betegben későbbiekben tumor fejlődne ki.
3 B. Kromoszomális imbalance A génamplifikáció és -deletio milyen módon járul hozzá a daganatok kialakulásához? A kromoszomális imbalance különböző nagyságú kromoszómaszegmensek nyerését (amplificatio) és/vagy elvesztését (deletio, allelvesztés) jelenti. A kromoszomális imbalance fontos szerepet játszik a tumorok kialakulásában és progressziójában tekintettel arra, hogy bizonyos gének elvesztése és mások felerősödése jelentős változásokat idéz elő a tumorsuppressor gének és az onkogének működésében. Kromoszómarégiók vesztése és nyerése ugyancsak szerepet játszik a nem-transzlálódó, regulatorikus funkcióval rendelkező RNS-ek (pl. mirns) expressióján keresztül a tumorok kialakulásában. A genetikai imbalance-ok többségében bizonyos daganattípusokra jellemző mintázatok ismerhetőek fel, illetve összefüggést mutatnak a tumor klinikai viselkedésével és a betegség prognózisával. Amplificatio: A génamplifikáció olyan folyamat, melynek során egy egyébként normális gén onkogénné válik. Az érintett gének elsősorban a sejtciklus szabályozásában vesznek részt. Ez a típusú onkogénhatás általában a tumorprogresszió során érvényesül, és általában egy amplifikálódott gén több, különböző daganat progressziójában is érintett. A génamplifikáció több gént is magában foglaló, több száz kilobázis nagyságú DNS-szekvencia megsokszorozódása. Az amplifikáció eredményeként egy gén kópiaszáma több százszorosára nő. A génamplifikációk kromoszomális szinten két különböző megjelenést mutathatnak: egyrészről mint homogénen festődő kromoszómarégiók, másrészről ún. double minutes formájában, a kromoszómáktól független, páros kromatin fragmentumok formájában jelenhetnek meg. 2. táblázat. Gyakori kromoszóma-amplifikációk daganatos betegségekben Deletio: A deléció különböző nagyságú kromoszómaszegmensek elvesztését jelenti. A deléciók elsősorban a tumorsuppressor gének elvesztésén keresztül járulnak hozzá a daganatok kialakulásához. A tumorsuppressor gének inaktivációjának egyik lépése az egyik allel elvesztése (loss of hetrozygosity, LOH), azonban a teljes onkogénhatás kialakulásához a másik allel elvesztése (biallelicus deletio) vagy a másik allélon lévő tumorsuppressor gén pontmutációval, hipermetilációval történő inaktivációja is szükséges. A nagyobb kromoszómaszegmenseket érintő deléciók esetében (pl. 1p, neuroblastoma; 3p, tüdőcarcinoma; 7p, myeloid leukaemia) a tumor kialakulásában szerepet játszó tumorsuppressor gén nem ismert, azonban számos esetben (pl. 11q, 13q, 17p, krónikus lymphocytás leukaemiában; 1p, 19q, oligodendroglioma) prognosztikai jelentőséggel bír. 3. táblázat. Gyakori deléciók daganatos betegségekben
4 C. Pontmutációk A pontmutációk egyaránt szerepet játszhatnak a tumorsuppressor gének inaktivációjában vagy onkogének aktivációjában. Az aktiváló mutációk során az adott gének olyan proteint kódolnak, melyek transzformáló aktivitása megnövekedett. Az aktiváló mutációk elsősorban a jelátviteli utak aktiválásán keresztül játszanak szerepet a daganatok kialakulásában. Az aktiváló mutációkat legjobban a K-RAS gén 12, 13 és 61-es kodonjának mutációja szemlélteti, ahol a mutációt szenvedett protein aktív állapotba kerül, és folyamatosan aktiválja a Raf és a MEK fehérjekináz útvonalakat. 4. táblázat. Gyakori aktiváló mutációk daganatos betegségekben D. Genetikai instabilitás A mismatch repair rendszer (MMR) zavara hogyan járul hozzá a daganatok kialakulásához? A genetikai instabilitás a sejtek és szövetek olyan állapota, ahol a genom teljes állományát érintő, multiplex genetikai léziók alakulnak ki. Ezekben az estekben kialakuló tumorokban halmozott genetikai léziók azonosíthatók, és a tumoron belül is eltérők a genetikai léziók az egyes sejtekben. A daganatok többségében a genetikai instabilitás a tumorprogresszió folyamán alakul ki. A genetikai instabilitás a nukleotidok és a kromoszómák szintjén jelenik meg. Nukleotidok szintjén kialakuló genetikai instabilitás. A nukleotidok szintjén jelentkező instabilitást a DNS hibajavító rendszerek zavara okozza. Ide tartozik a mismatch repair rendszer (MMR) és a nukleotidexciziós rendszer (NER) zavarai. A MMR a DNS-replikáció hibáit javítja, és meggátolja a hibás DNS-szekvenciák rekombinációját. Ide tartoznak a HMLH1, HMSH2 és HMSH6 gének által termelt fehérjék. A herediter nem-polyposus coloncarcinomák (HNPCC) magas százalékában azonosítható a MMR gének mutációs vagy hipermetilációs inaktivitálódása. A MMR rendszer zavara ezen tumorokban microsatellita instabilitást (a genomban konzervált tandem nukleotidszervenciák megváltozását) eredményez. A MMR rendszer zavara a colorectalis daganatokon túlmenően gyomor-, ovarium-, endometrium-, pancreas-, és egyéb daganatokban is kimutatható. A NER zavara esetén az UV-sugárzás hatására keletkező pirimidin dimerek javítása nem történik meg, így ezekben a betegekben (Xeroderma pigmentosum) megnő az UV-sugárzás hatására kialakuló bőrtumorok kockázata. Kromoszóma-instabilitás. A kromoszómainstabilitás a kromoszómák szegregációja során bekövetkezett zavarok, amelyek a kromoszómák számbeli eltéréséhez vagy más szóval aneuploiditáshoz vezet. Kromoszóma-instabilitás a legtöbb tumorban megfigyelhető, és általában a tumorprogresszió folyamata során alakul ki. Daganatok esetében leggyakrabban a bipolaris osztódási orsó felépítéséért felelős centrosoma amplificatio idézi elő a kromoszóma-instabilitást. A centrosoma aplifikáció halmozottan a p53 tumorsuppressor gén inaktivált tumorokban fordul elő, mivel p53 funkció hiányában aktiválódik a centromer duplikációt előidéző ciklin dependens kináz (CDK)2- ciklin E. E. Örökletes génhibák
5 Melyek a kritériumai az autosomalis dominans öröklődésű daganatszindrómáknak? Számos daganat kialakulását örökletes genetikai hajlam is befolyásolja. Ilyen esetekben a daganat kialakulásáért felelős génhiba a csírasejtekben alakul ki, és ebből adódóan minden somaticus utódsejt hordozza. Az esetek többségében az öröklött génhiba nem elégséges a daganatok kialakulásához és progressziójához, ahhoz további somaticus mutációk kialakulása is szükséges. Ezt támasztja alá az a megfigyelés is, hogy az öröklött genetikai lézió ellenére a tumorok a születést követően csak bizonyos idő elteltével alakulnak ki, amikorra a szervezet további szomatikus mutációkat szenvedett el. Az örökletes génhibákat hordozó egyénekben csupán a daganatos betegségre való hajlam fokozódik, és nem törvényszerű a daganatok kialakulása. Természetesen egyes genetikai léziók esetében igen magas a tumorkialakulási arány, míg másokban jóval alacsonyabb. Az örökletes daganatos megbetegedések két nagy csoportra, az autosomalis dominans öröklésmenetet mutató daganatszindrómákra és az autosomalis recessive öröklődésű DNS repair rendszer zavaraira oszthatók. A humán daganatos megbetegedések nem több mint 5-10%-a tartozik ebbe a két csoportba. 5. táblázat. Daganatok kialakulására predisponáló örökletes génhibák Autosomalis dominans öröklődésű daganatszindrómák. Ezekben az esetekben egyetlen gén mutációja idéz elő fokozott hajlamot a daganatos betegség kialakulására. Általában az érintett gének tumorsuppressor gének, és erős penetranciával rendelkeznek. A csoportra jellemző: (1) a daganatok korábbi életkorban alakulnak ki, mint sporadikus megfelelői; (2) a tumor multiplexen vagy páros szervekben bilaterálisan jelentkezik; (3) az érintettekben egyidejűleg több típusú tumor is kialakulhat; (4) a daganatok családi halmozódása; (5) a daganatos betegségek más, nem daganatos betegségekkel (pl. mentalis retardáció, melanin pigmentáció stb.) való társulása. Az autosomalis dominans öröklésmenetű daganatszindrómák további csoportokba, úgymint endokrin neoplasia szindrómák, intestinalis daganatszindrómák, emlő- és ovariumcarcinoma szindrómák, bőrcarcinoma szindrómák, neurofibromatosisok és vesecarcinoma szindromák sorolhatók. Autosomalis recessive öröklődésű daganatszindrómák. Ebbe a csoportba tartózó kórképekre jellemző a DNS repair zavaraiból adódó kromoszomális vagy DNS-instabilitás. A repairrendszerek közül érintett lehet a nucleotid excisios repair, a DNS repair/replicatios rendszer vagy a post-replicatiós repairrendszer. A csoportba tartozó betegségek közös jellemzője a daganatképződésre való fokozott hajlam mellett a csökkent fertilitás, az immundeficiencia, az alacsony testmagasság és a glükózintolerancia. Annak ellenére, hogy az egyes betegségeket különböző génhibák idézik elő, minden esetben azonosítható a DNS-repairhez nélkülözhetetlen p53 funkcionális károsodása. F. Micro-RNS eltérések A mirns-ek hogyan járulnak hozzá a daganatok kialakulásához? A humán genom egy jelentős része a fehérjeszintézisben szerepet nem játszó, azonban RNS-re átíródó, nem-kódoló szekvenciákat tartalmaz. A micro-rns-ek (mirns) a nem-kódló RNS-ek közé tartozó, nukleotidából álló, egyláncú, a gének negatív regulációjában résztvevő RNS-molekulák. A mirns-ek száma mintegy 1000-re tehető, ami nem több mint a jelenleg azonosított humán gének 3%-a. A mirns-ek a génexpressió post-transcriptionalis gátlásán, azaz a transzláció megakadályozásán keresztül szabályozzák a sejtek osztódást, differenciáját és túlélését. A mirns-ek a proteint kódoló gének mintegy 30%-át kontrolálják. A rendelkezésünkre álló mirns vizsgálatok alapján nyilvánvalóvá vált, hogy bizonyos mirns-ek, az ún. oncomirek fontos szerepet játszanak egyes daganattípusok
6 keletkezésében és progressziójában. A mirns-ek mintegy 50%-a a carcinogenesisben szerepet játszó gének, a deletiok, az amplificatiók és a translocatiók szempontjából forró pontoknak számító, fragilis kromoszómaterületek környezetében helyezkedik el. A mirns-ek az onkogének expressiójának elősegítésével vagy a tumorsuppressor gének expressiójának csökkentésével vesznek részt a malignus transzformáció folyamatában. Normális körülmények között a mirns-ek onkogének translatióját gátolják, ezen mirns-ek mennyiségének csökkenése az adott onkogének fokozott transzlációjához vezet. Tumorsuppressor gének esetében a fokozott mirns aktivitás csökkenti a tumorsuppressor gén aktivitását. Számos tumor esetében, köztük az emlő-, a prostata-, a colon-, az ovárium- és májcarcinoma esetében azonosították a mirns expressiók általános csökkenését. Más tumorok esetében, mint pl. lymphomák, tüdő-, hólyag- és prostatacarcinoma esetében bizonyos mirns-ek fokozott expressiója azonosítható. Néhány mirns molekuláris célpontja jól ismert. Így például bizonyos mirns-ek csökkent expressiója vagy deléciója az antiapoptotikus BCL2 fokozott expressióját idézik elő egyes leukémiákban és lymphomákban. Ily módon a BCL2 negatív szabályozásával ezen micro-rns-ek tumorsuppressor génként működnek. Hasonló módon mirns által fokozott RAS és MYC onkogén expressio mutatható ki tüdődaganatokban és bizonyos B-sejtes leukémiákban. A mirns-ek vizsgálata számos új aspektusát veti fel a daganatok diagnosztikájának, osztályozásának és prognosztizálásánál, ugyanakkor új daganatterápiás célpontot is szolgáltatnak a mirns-molekulák expressiójának regulálásán, blokkolásán és módosításán keresztül. 6. táblázat: Daganatos betegségekben kimutatható mirns eltérések Milyen génrégiók szabályzása történik DNS-metilációval? Epigenetikai hatások Az epigenetikai változások a génexpressiót befolyásoló olyan változások, melyek nem járnak DNS-szekvenciaváltozással. Az epigenetikai változások két csoportja a DNS-metiláció és a histon modifikáció. Mindkét folyamat fontos szerepet játszik a sejtregulációban, a differnciációban és a carcinogenesisben. DNS-metiláció. A DNS-metiláció a normális sejtműködés fontos regulátora. A DNS-metiláció kizárólag a citozin CpG dinucleotidjain fordul elő, melynek során a citidingyűrű 5 pozícióján lévő szénatomhoz metilcsoport kapcsolódik. A folyamatot a DNS-metiltranszferáz mediálja. A CpG-szervenciák eloszlása a genomban aszimmetrikus: az exon és intron régiókban számuk alacsony, a gének promoterrégiójában pedig ún. CpG-szigetek formájában halmozódnak fel. A genomban lévő CpG-szekvenciák általában metiláltak, míg a promoterrégiókban elhelyezkedő CpG-szigetek nem. Ily módon a transcriptionalisan inaktív génszakaszok (pl. pericentromericus régiók) hipermetiláltak, míg a trancriptionalisan aktív gének promoterrégiói hipometiláltak. A daganatok kialakulásában a hiper- és a hipormetiláció egyaránt szerepet játszhat. A hipermetiláció a promoterrégiók funkciójának felfüggesztésén és ebből adódóan a downstream gének inaktivációján keresztül járul hozzá a tumorok kialakulásához. A promoterrégió hipermetilációnak elsősorban a tumorsupressor gének inaktiválásában van szerepe. Számos adat utal arra, hogy a hipermetiláció okozta géninaktiváció fokozza a sejtek mutációs aktivitását. Például a DNS repair gének, köztük a MLH1 gén hipermetilációja és inaktivációja microsatellita-instabilitáshoz vezet. Az így kialakuló genetikai instabilitás következtében megnő egyes daganatos betegségek, köztük a coloncarcinoma és az endometrialis carcinoma kialakulásának kockázata.
7 2. ábra: Hipermetiláció okozta géninaktiváció. A: A normális gének promoterrégiójában a CpG-szigetek hipometiláltak, ami lehetővé teszi az adott gén expressióját és a fehérjeszintézist.b: A tumorsejtekben a promoterrégiókban lévő CpG-szigetek hipermetilációja felfüggeszti a gén expressióját. 7. táblázat: Daganatos betegségekben kimutatható hipermetilált gének A genomban elszórt CpG-szigetek hipermetilált állapota összecsapzódott, compact heterochromatin struktúrát eredményez, ami meggátolja a transcriptiót elősegítő faktorok kötődését. A daganatokban az általános metiláltsági szint jelentősen csökkent, ami azt jelzi, hogy a hipometilált állapot ugyancsak elősegíti a daganatok kialakulását. A hipometiláció számos mechanizmus alapján járulhat hozzá a daganatok kialakulásához és progressziójához. Egyrészről a pericentromerikus régiók hipometilációja fokozza a kromoszómák törékenységét, és ezáltal genetikai instabilitást idéz elő, másrészről az egyébként hypermetilált, nem funkcionáló onkogének aktiválódnak. Histon modifikáció. A histonok a magkromatinban elhelyezkedő bázikus fehérjék, melyek a deacetiláció és a metiláció folytán szerepet játszanak a gének post-translatiós szabályozásában. A histon acetiláció a magkromatint nyitott és ezáltal transcriptionalisan aktív állapotban tartja, míg a metiláció a heterokromatizáció fokozása révén trancripcionalisan depressalt állapotot idéz elő. A histon acetiláció és metiláció egyensúlyát a histon acetiltranszferázok (HAT), a histon metiltranszferáz (HMT) és a histon deacetilázok (HDEA) tartják fenn. Számos daganat esetében mutatták ki ezen enzimrendszerek olyan irányú eltoldását, mely különböző onkogének aktivizálása vagy tumorsuppressor gének inaktiválása révén járulhat hozzá a tumorgenesishez. G. A genetikai léziók kialakulásának algoritmusa Milyen sorrendiség állítható fel az onkogenetikai léziók kialakulásában? A daganatok kialakulása egy többlépcsős folyamat, melyben számos genetikai lézió kialakulása szükséges a malignus fenotípus kialakulásához. Ezen folyamatban többnyire az apoptosisban vagy a sejtöregedésben résztvevő onkogén és tumorsuppressor gének vesznek rész, de számos ezidáig ismeretlen funkcióval rendelkező gén is érintett. Számos daganat kialakulása során a malignus fenotípushoz vezető morfológiai változásokat meghatározott sorrendű molekuláris eltérések jellemzik. Ezen genetikai eltérések akkumulációja talán legjobban a coloncarcinoma esetében ismert, ahol az APC tumorsuppressor gén inaktivációja iniciálja a folyamatot, majd RAS aktivációt és p53 inaktivációt követően alakul ki a carcinoma. 3. ábra: A colorectalis carcinomák kialakulásának molekuláris algoritmusa (Seminars of Cancer Biology 2005, 15:484. alapján rajzolva)
8 H. Összefoglalás A daganatos betegségek szinte mindegyikében található genetikai lézió. Ezen genetikai léziók lehetnek öröklöttek vagy szerzettek, érvényre jutásukban az epigenetikai hatásoknak van szerepe. Számos esetben a tumorok kifejlődésében az egyes genetikai és epigenetikai léziók algoritmusa figyelhető meg. Hivatkozások: 1. Croce CM. Onkogénes and cancer. N. Engl. J. Med. 2008, 31:358: Fröhling S, Döhner H: Chromosomal abnormalities in cancer. N Engl J Med : Li M, Marin-Muller C, Bharadwaj U, Chow KH, Yao Q, Chen C. MicroRNAs: Control and Loss of Control in Human Physiology and Disease. World J. Surg Nov 22. [Epub ahead of print] 4. Marsh DM, Zori RT: Genetic insight into familial cancers update and recent discoveries. Cancer letters, :
Daganatok kialakulásában szerepet játszó molekuláris folyamatok
 Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
Daganatok kialakulásában szerepet játszó molekuláris folyamatok Genetikai változások Onkogének Tumorszuppresszor gének DNS hibajavító gének Telomer és telomeráz Epigenetikai változások DNS-metiláció Mikro-RNS
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere
 I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
I./1. fejezet: Jelátviteli utak szerepe a daganatok kialakulásában A daganatkeletkezés molekuláris háttere Kopper László A fejezet célja, hogy megismerje a hallgató a daganatok kialakulásában szerepet
Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon és Norvégiában
 Norvég Finanszírozási Mechanizmus által támogatott projekt Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon és Norvégiában Norvég Alap támogatással javul
Norvég Finanszírozási Mechanizmus által támogatott projekt Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon és Norvégiában Norvég Alap támogatással javul
I./6. fejezet: Praeblastomatosisok. Bevezetés
 I./6. fejezet: Praeblastomatosisok Zalatnai Attila A fejezet célja, hogy a hallgató megismerkedjen a praeblastomatosisok fogalmával, és lehetséges megjelenési formáival. A fejezet teljesítését követően
I./6. fejezet: Praeblastomatosisok Zalatnai Attila A fejezet célja, hogy a hallgató megismerkedjen a praeblastomatosisok fogalmával, és lehetséges megjelenési formáival. A fejezet teljesítését követően
Molekuláris genetikai vizsgáló. módszerek az immundefektusok. diagnosztikájában
 Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény
 A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A tumor-markerek alkalmazásának irányelvei BOKOR KÁROLY klinikai biokémikus Dr. Romics László Egészségügyi Intézmény 2016.10.17. 1 2016.10.17. 2 2016.10.17. 3 A TUMORMARKEREK TÖRTÉNETE I. ÉV FELFEDEZŐ
A melanocyták (naevussejtek) daganatai. Benignus. Malignus. Naevus pigmentosus (festékes anyajegy) szerzett veleszületett.
 A melanocyták (naevussejtek) daganatai Benignus Naevus pigmentosus (festékes anyajegy) szerzett veleszületett Malignus Melanoma malignum Szerzett NP barna, 6 mm-nél kisebb, éles határú NP junctionalis
A melanocyták (naevussejtek) daganatai Benignus Naevus pigmentosus (festékes anyajegy) szerzett veleszületett Malignus Melanoma malignum Szerzett NP barna, 6 mm-nél kisebb, éles határú NP junctionalis
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL
 ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
ZÁRÓJELENTÉS 2004-2007 A MOLEKULÁRIS ONKOGENEZIS MECHANIZMUSAI GYAKORI DAGANATOKBAN C. PÁLYÁZAT TELJESÍTÉSÉRŐL EREDMÉNYEK Munkacsoportunk úttörő szerepet játszott a molekuláris onkológiai (onkogenetikai)
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
GENETIKAI INSTABILITÁS VIZSGÁLATA A B-SEJTES KRÓNIKUS LYMPHOCYTÁS LEUKÉMIA RICHTER TRANSZFORMÁCIÓJA SORÁN
 GENETIKAI INSTABILITÁS VIZSGÁLATA A B-SEJTES KRÓNIKUS LYMPHOCYTÁS LEUKÉMIA RICHTER TRANSZFORMÁCIÓJA SORÁN PhD értekezés tézisei Dr. Fülöp Zsolt Témavezeto : Dr. Matolcsy András Programvezeto : Dr. Jeney
GENETIKAI INSTABILITÁS VIZSGÁLATA A B-SEJTES KRÓNIKUS LYMPHOCYTÁS LEUKÉMIA RICHTER TRANSZFORMÁCIÓJA SORÁN PhD értekezés tézisei Dr. Fülöp Zsolt Témavezeto : Dr. Matolcsy András Programvezeto : Dr. Jeney
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás
 Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
Mikroszatellita instabilitás immunhisztokémiai kimutatása colorectális carcinomában: antitestek, módszerek, standardizálás Dr. Krenács Tibor Semmelweis Egyetem I. sz. Patológiai és Kísérleti Rákkutató
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Többgénes jellegek. 1. Klasszikus (poligénes) mennyiségi jellegek. 2.Szinte minden jelleg több gén irányítása alatt áll
 Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Többgénes jellegek Többgénes jellegek 1. 1. Klasszikus (poligénes) mennyiségi jellegek Multifaktoriális jellegek: több gén és a környezet által meghatározott jellegek 2.Szinte minden jelleg több gén irányítása
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL
 Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Norvég Finanszírozási Mechanizmus által támogatott projekt HU-0115/NA/2008-3/ÖP-9 ÚJ TERÁPIÁS CÉLPONTOK AZONOSÍTÁSA GENOMIKAI MÓDSZEREKKEL KÖZÖS STRATÉGIA KIFEJLESZTÉSE MOLEKULÁRIS MÓDSZEREK ALKALMAZÁSÁVAL
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Neoplazma - szabályozottság nélküli osztódó sejt
 9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
9. előadás Rák Rák kialakulása: A szervezet 10 14 sejtet tartalmaz, ezek mutálnak és osztódnak A rákos sejt nem követi a sejtosztódás korlátait és végül a rákos sejtek elfoglalják a normál szövetek helyét.
11. Melanoma Carcinogenesis.
 A MELANOCYTÁK (NAEVUS SEJTEK) DAGANATAI NAEVUS PIGMENTOSUS (festékes anyajegy) Benignus; szerzett vagy veleszületett lehet A RAS jelátvivő ösvényen az NRAS vagy a BRAF gén aktiváló mutációja Barna,
A MELANOCYTÁK (NAEVUS SEJTEK) DAGANATAI NAEVUS PIGMENTOSUS (festékes anyajegy) Benignus; szerzett vagy veleszületett lehet A RAS jelátvivő ösvényen az NRAS vagy a BRAF gén aktiváló mutációja Barna,
A daganatok aetiológiai tényezői, genetikai háttere A daganatok képződése
 A daganatok aetiológiai tényezői, genetikai háttere A daganatok képződése Barna Gábor I.sz. Patológiai és Kísérleti Rákkutató Intézet A sejtek életének szabályozása növekedés differenciáció protoonkogének
A daganatok aetiológiai tényezői, genetikai háttere A daganatok képződése Barna Gábor I.sz. Patológiai és Kísérleti Rákkutató Intézet A sejtek életének szabályozása növekedés differenciáció protoonkogének
Epigenetikai Szabályozás
 Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Epigenetikai Szabályozás Kromatin alapegysége a nukleoszóma 1. DNS Linker DNS Nukleoszóma mag H1 DNS 10 nm 30 nm Nukleoszóma gyöngy (4x2 hiszton molekula + 146 nukleotid pár) 10 nm-es szál 30 nm-es szál
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
A daganat- és rákképződés május 5.
 A daganat- és rákképződés 2016. május 5. Jóindulatú (benignus) és rosszindulatú (malignus) tumorok tumor=daganat, malignus tumor = rák cső (pl. bél) ürege alaphártya normális hámsejtek benignus tumor malignus
A daganat- és rákképződés 2016. május 5. Jóindulatú (benignus) és rosszindulatú (malignus) tumorok tumor=daganat, malignus tumor = rák cső (pl. bél) ürege alaphártya normális hámsejtek benignus tumor malignus
http://www.rimm.dote.hu Tumor immunológia
 http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
http://www.rimm.dote.hu Tumor immunológia A tumorok és az immunrendszer kapcsolatai Tumorspecifikus és tumorasszociált antigének A tumor sejteket ölő sejtek és mechanizmusok Az immunológiai felügyelet
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában
 Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
Epigenetikai mintázatok biomarkerként történő felhasználási lehetőségei a toxikológiában Czimmerer Zsolt, Csenki-Bakos Zsolt, Urbányi Béla TOX 2017 Tudományos Konferencia 2017.10.12. Bükfürdő A sejtek
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Kappelmayer János. Malignus hematológiai megbetegedések molekuláris háttere. MOLSZE IX. Nagygyűlése. Bük, 2005 szeptember
 Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Kappelmayer János Malignus hematológiai megbetegedések molekuláris háttere MOLSZE IX. Nagygyűlése Bük, 2005 szeptember 29-30. Laboratóriumi vizsgálatok hematológiai malignómákban Általános laboratóriumi
Hátterükben egyetlen gén áll, melynek általában számottevő a viselkedésre gyakorolt hatása, öröklési mintázata jellegzetes.
 Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
A hólyagrák aktuális kérdései a pathologus szemszögéből. Iványi Béla SZTE Pathologia
 A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
A hólyagrák aktuális kérdései a pathologus szemszögéből Iványi Béla SZTE Pathologia Hólyagrák 7. leggyakoribb carcinoma Férfi : nő arány 3.5 : 1 Csúcsa: 60-80 év között Oka: jórészt ismeretlen Rizikótényezők:
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Mit tud a genetika. Génterápiás lehetőségek MPS-ben. Dr. Varga Norbert
 Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Mit tud a genetika Génterápiás lehetőségek MPS-ben Dr. Varga Norbert Oki terápia Terápiás lehetőségek MPS-ben A kiváltó okot gyógyítja meg ERT Enzimpótló kezelés Őssejt transzplantáció Genetikai beavatkozások
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Kromoszómák, Gének centromer
 Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Sporadikus vastag- és végbéldaganatok molekuláris genetikai markerei
 Sporadikus vastag- és végbéldaganatok molekuláris genetikai markerei Készítette: Kámory Enikő ELTE TTK Biológia Doktori Iskola Klasszikus és Molekuláris Genetika Doktori Program Témavezető: Dr. Csuka Orsolya
Sporadikus vastag- és végbéldaganatok molekuláris genetikai markerei Készítette: Kámory Enikő ELTE TTK Biológia Doktori Iskola Klasszikus és Molekuláris Genetika Doktori Program Témavezető: Dr. Csuka Orsolya
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
Daganatok fogalma, általános jellegzetességeik és osztályozásuk. Zalatnai Attila
 Daganatok fogalma, általános jellegzetességeik és osztályozásuk Zalatnai Attila Daganat: olyan kóros szövetszaporulat, mely a szervezet saját sejtjeiból kiindulva, fokozatosan függetlenedik a fiziológiás
Daganatok fogalma, általános jellegzetességeik és osztályozásuk Zalatnai Attila Daganat: olyan kóros szövetszaporulat, mely a szervezet saját sejtjeiból kiindulva, fokozatosan függetlenedik a fiziológiás
I. A sejttől a génekig
 Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
Gén A gének olyan nukleinsav-szakaszok a sejtek magjainak kromoszómáiban, melyek a szervezet működését és növekedését befolyásoló fehérjék szabályozásához és előállításához szükséges információkat tartalmazzák.
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2.
 A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
p16 - p21- p27- p53 - p63
 p16 - p21- p27- p53 - p63 Dako Szimpózium, 2010 december 3 Szentirmay Zoltán Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest A sejtciklus szabályozása Cyklin-Dependens
p16 - p21- p27- p53 - p63 Dako Szimpózium, 2010 december 3 Szentirmay Zoltán Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest A sejtciklus szabályozása Cyklin-Dependens
Daganatos betegségek megelőzése, a szűrés szerepe. Juhász Balázs, Szántó János DEOEC Onkológiai Tanszék
 Daganatos betegségek megelőzése, a szűrés szerepe Juhász Balázs, Szántó János DEOEC Onkológiai Tanszék Carcinogenesis mechanizmusa A daganatos átalakulás a normálistól eltérő DNS szintézisével kezdődik,
Daganatos betegségek megelőzése, a szűrés szerepe Juhász Balázs, Szántó János DEOEC Onkológiai Tanszék Carcinogenesis mechanizmusa A daganatos átalakulás a normálistól eltérő DNS szintézisével kezdődik,
HAPMAP -2010 Nemzetközi HapMap Projekt. SNP GWA Haplotípus: egy kromoszóma szegmensen lévő SNP mintázat
 HAPMAP -2010 Nemzetközi HapMap Projekt A Nemzetközi HapMap Project célja az emberi genom haplotípus* térképének(hapmap; haplotype map) megszerkesztése, melynek segítségével katalogizálni tudjuk az ember
HAPMAP -2010 Nemzetközi HapMap Projekt A Nemzetközi HapMap Project célja az emberi genom haplotípus* térképének(hapmap; haplotype map) megszerkesztése, melynek segítségével katalogizálni tudjuk az ember
Immunológia 4. A BCR diverzitás kialakulása
 Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
Immunológia 4. A BCR diverzitás kialakulása 2017. október 4. Bajtay Zsuzsa A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
- Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=>
 1 - Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=> a sejtek sorsa meg van határozva, mint egy üveggolyó,
1 - Conrad Hal Waddington számára a gének fizikai háttere még ismeretlen volt (Watson-Crick-Franklin 1953), így próbálta leírni a sejt specializációt=> a sejtek sorsa meg van határozva, mint egy üveggolyó,
Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására
 Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Szalma Katalin Biológiai módszerek alkalmazása környezeti hatások okozta terhelések kimutatására Témavezető: Dr. Turai István, OSSKI Budapest, 2010. október 4. Az ionizáló sugárzás sejt kölcsönhatása Antone
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
2. SZ. SZAKMAI ÖSSZEFOGLALÓ PIR 2
 Az Országos Onkológiai Intézet Norvég Finanszírozási mechanizmus keretében elnyert Kutatás Fejlesztési Pályázata Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon
Az Országos Onkológiai Intézet Norvég Finanszírozási mechanizmus keretében elnyert Kutatás Fejlesztési Pályázata Közös stratégia kifejlesztése molekuláris módszerek alkalmazásával a rák kezelésére Magyarországon
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
A kromoszómák kialakulása előtt a DNS állomány megkettőződik. A két azonos információ tartalmú DNS egymás mellé rendeződik és egy kromoszómát alkot.
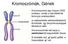 Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA. Dr. Győrffy Balázs
 A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
A ROSSZ PROGNÓZISÚ GYERMEKKORI SZOLID TUMOROK VIZSGÁLATA Dr. Győrffy Balázs ELŐADÁS ÁTTEKINTÉSE 1. Elmélet Gyermekkori tumorok Központi idegrendszer tumorai 2. Kutatás szakmai koncepciója 3. Együttműködés
Spinalis muscularis atrophia (SMA)
 Spinalis muscularis atrophia (SMA) Dr. Sztriha László SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A spinalis muscularis atrophia (SMA) a mucoviscidosis után a leggyakoribb
Spinalis muscularis atrophia (SMA) Dr. Sztriha László SZTE ÁOK Gyermekgyógyászati Klinika és Gyermekegészségügyi Központ, Szeged A spinalis muscularis atrophia (SMA) a mucoviscidosis után a leggyakoribb
A fejezet felépítése
 II./2.7. fejezet: A daganatok molekuláris diagnosztikája Kovalszky Ilona A fejezet célja, hogy megismerje a hallgató azokat a molekuláris diagnosztikai módszereket, melyek a napi gyakorlatban vagy kutatási
II./2.7. fejezet: A daganatok molekuláris diagnosztikája Kovalszky Ilona A fejezet célja, hogy megismerje a hallgató azokat a molekuláris diagnosztikai módszereket, melyek a napi gyakorlatban vagy kutatási
ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS
 ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS Mi az öregedés? Egyrészről az idő múlásával definiálható, a születéstől eltelt idővel mérhető, kronológiai sajátosságú, Másrészről az idő múlásához köthető biológiai,
ÖREGEDÉS ÉLETTARTAM, EGÉSZSÉGES ÖREGEDÉS Mi az öregedés? Egyrészről az idő múlásával definiálható, a születéstől eltelt idővel mérhető, kronológiai sajátosságú, Másrészről az idő múlásához köthető biológiai,
Hisztopatológiai és molekuláris patológiai prognosztikai faktorok vizsgálata béltumorokban. Dr. Tóth László
 EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS Hisztopatológiai és molekuláris patológiai prognosztikai faktorok vizsgálata béltumorokban Dr. Tóth László Témavezető: Dr. András Csilla DEBRECENI EGYETEM KLINIKAI ORVOSTUDOMÁNYOK
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS Hisztopatológiai és molekuláris patológiai prognosztikai faktorok vizsgálata béltumorokban Dr. Tóth László Témavezető: Dr. András Csilla DEBRECENI EGYETEM KLINIKAI ORVOSTUDOMÁNYOK
A sejtfelszíni receptorok három fő kategóriája
 A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001 Zárójelentés: 2001. május 15.-2004.
Többes malignus tumoros eseteink elemzése. Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya
 Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
4. A humorális immunválasz október 12.
 4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
4. A humorális immunválasz 2016. október 12. A klónszelekciós elmélet sarokpontjai: Monospecifictás: 1 sejt 1-féle specificitású receptor Az antigén receptorhoz kötődése aktiválja a limfocitát A keletkező
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A citológia és a genetika társtudománya Citogenetika A kromoszómák eredetét, szerkezetét, genetikai funkcióját,
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A citológia és a genetika társtudománya Citogenetika A kromoszómák eredetét, szerkezetét, genetikai funkcióját,
Dr. Máthéné Dr. Szigeti Zsuzsanna és munkatársai
 Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
A Lynch szindróma molekuláris genetikai háttere Magyarországon
 A Lynch szindróma molekuláris genetikai háttere Magyarországon A doktori értekezés tézisei Kovács Marietta Éva Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Doktori Iskola Klasszikus és
A Lynch szindróma molekuláris genetikai háttere Magyarországon A doktori értekezés tézisei Kovács Marietta Éva Eötvös Loránd Tudományegyetem Természettudományi Kar Biológiai Doktori Iskola Klasszikus és
Mutagenezis és s Karcinogenezis kutatócsoport. Haracska Lajos.
 Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
Mutagenezis és s Karcinogenezis kutatócsoport SZBK Genetikai Intézete (429 dolgozó,, Tel: 62-599666) haracska@brc.hu Haracska Lajos www.brc.hu/lajoslab Evolúci ció és s karcinogenezis: közös k s gyökerek
A sejtciklus szabályozása
 Molekuláris sejtbiológia A sejtciklus szabályozása? Dr. habil.. Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtciklus fázisai S G 2 G 0 G 1 M G = gap gap S = synthesis
Molekuláris sejtbiológia A sejtciklus szabályozása? Dr. habil.. Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtciklus fázisai S G 2 G 0 G 1 M G = gap gap S = synthesis
Az Ig génátrendeződés
 Az Ig génátrendeződés Háromféle változás játszódik le a molekula szerkezetét tekintve: B sejtek fejlődése alatt: VDJ átrendeződés (rekombináció) IgH izotípusváltás rekombináció (CSR) Szomatikus hipermutáció
Az Ig génátrendeződés Háromféle változás játszódik le a molekula szerkezetét tekintve: B sejtek fejlődése alatt: VDJ átrendeződés (rekombináció) IgH izotípusváltás rekombináció (CSR) Szomatikus hipermutáció
A rák, mint genetikai betegség
 A rák, mint genetikai betegség Diák: Ferencz Arnold-Béla la Felkész szítı tanár: József J Éva Bolyai Farkas Elméleti leti LíceumL Mi is a rák r tulajdonképpen? A rák r k egy olyan betegség g ahol sejt
A rák, mint genetikai betegség Diák: Ferencz Arnold-Béla la Felkész szítı tanár: József J Éva Bolyai Farkas Elméleti leti LíceumL Mi is a rák r tulajdonképpen? A rák r k egy olyan betegség g ahol sejt
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Terhesség és emlőrák genetikai szempontok. Kosztolányi György PTE Orvosi Genetikai Intézet
 erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
erhesség és emlőrák genetikai szempontok Kosztolányi yörgy PE Orvosi enetikai Intézet Előfordulás 1 emlőrák / 3000 várandós fokozódása várható: öröklődő emlőrák diagnózisa családon belül : I. generáció
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
Példák a független öröklődésre
 GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Nőgyógyászati daganatok carcinogenesis, szignálutak, célzott terápiák
 Nőgyógyászati daganatok carcinogenesis, szignálutak, célzott terápiák Tóth Erika Sebészeti és Molekuláris Patológiai Osztály Országos Onkológiai Intézet Az előadás vázlata 1. Célzott terápia definíció
Nőgyógyászati daganatok carcinogenesis, szignálutak, célzott terápiák Tóth Erika Sebészeti és Molekuláris Patológiai Osztály Országos Onkológiai Intézet Az előadás vázlata 1. Célzott terápia definíció
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
A genomiális medicina szép új világa
 A genomiális medicina szép új világa HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012 2014 2015. ÁPRILIS 16. Falus András Semmelweis Egyetem Genetikai Sejt és Immunbiológiai Intézet A medicina
A genomiális medicina szép új világa HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012 2014 2015. ÁPRILIS 16. Falus András Semmelweis Egyetem Genetikai Sejt és Immunbiológiai Intézet A medicina
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia. Dr. Sáfrány Géza OKK - OSSKI
 Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
A preventív vakcináció lényege :
 Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Vakcináció Célja: antigénspecifkus immunválasz kiváltása a szervezetben A vakcina egy olyan készítmény, amely fokozza az immunitást egy adott betegséggel szemben (aktiválja az immunrendszert). A preventív
Tudománytörténeti visszatekintés
 GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
Herediter Nonpolipózis Kolorektális Karcinóma elıfordulásával szerzett tapasztalataink. Igazolt mutáció hordozó családok családfa analízise.
 EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS Herediter Nonpolipózis Kolorektális Karcinóma elıfordulásával szerzett tapasztalataink. Igazolt mutáció hordozó családok családfa analízise. Dr. Tanyi Miklós Témavezetı:
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS Herediter Nonpolipózis Kolorektális Karcinóma elıfordulásával szerzett tapasztalataink. Igazolt mutáció hordozó családok családfa analízise. Dr. Tanyi Miklós Témavezetı:
A PKU azért nem hal ki, mert gyógyítják, és ezzel növelik a mutáns allél gyakoriságát a Huntington kór pedig azért marad fenn, mert csak későn derül
 1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós
 A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós Összefoglalás A humángenetika korunk egyik legdinamikusabban fejlődő tudományága. Ennek a fejlődésnek legfőbb mozgatórugója az, hogy a humángenetika,
A HUMÁNGENETIKA LEGÚJABB EREDMÉNYEI Péterfy Miklós Összefoglalás A humángenetika korunk egyik legdinamikusabban fejlődő tudományága. Ennek a fejlődésnek legfőbb mozgatórugója az, hogy a humángenetika,
A prostata sebészete. A prostata sebészeti jelentőségű. középkorú, ill. idős kanokban
 Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia --cysta -- tályog --daganat
Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia --cysta -- tályog --daganat
TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301)
 Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
Biokémia és molekuláris biológia I. kurzus (bb5t1301) Tematika 1 TEMATIKA Biokémia és molekuláris biológia IB kurzus (bb5t1301) 0. Bevezető A (a biokémiáról) (~40 perc: 1. heti előadás) A BIOkémia tárgya
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS A KI-67, FLT3 ÉS JAK2 GÉNEK MUTÁCIÓINAK VIZSGÁLATA TUMOROS SEJTVONALAKBAN ÉS COLORECTALIS CARCINOMÁS BETEGEK
 EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS A KI-67, FLT3 ÉS JAK2 GÉNEK MUTÁCIÓINAK VIZSGÁLATA TUMOROS SEJTVONALAKBAN ÉS COLORECTALIS CARCINOMÁS BETEGEK MINTÁIBAN DR. BUBÁN TAMÁS TÉMAVEZETŐ: DR. ANTAL-SZALMÁS PÉTER
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS A KI-67, FLT3 ÉS JAK2 GÉNEK MUTÁCIÓINAK VIZSGÁLATA TUMOROS SEJTVONALAKBAN ÉS COLORECTALIS CARCINOMÁS BETEGEK MINTÁIBAN DR. BUBÁN TAMÁS TÉMAVEZETŐ: DR. ANTAL-SZALMÁS PÉTER
Fehérje expressziós rendszerek. Gyógyszerészi Biotechnológia
 Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
E4 A Gyermekkori szervezett lakossági emlőszűrések hatása az emlőműtétek
 08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk.
 A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
A génterápia genetikai anyag bejuttatatása diszfunkcionálisan működő sejtekbe abból a célból, hogy a hibát kijavítsuk. A genetikai betegségek mellett, génterápia alkalmazható szerzett betegségek, mint
Molekuláris terápiák
 Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
