11. Előadás. Nukleinsavak, nukleinsav analitika. Nukleotidok, koenzimek, vitaminok.
|
|
|
- Gabi Kisné
- 6 évvel ezelőtt
- Látták:
Átírás
1 11. Előadás ukleinsavak, nukleinsav analitika. ukleotidok, koenzimek, vitaminok.
2 Történeti háttér Savas karakterű anyagok a sejtmagból DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, ) 1970: FM Insitute for Biomedical Research, Basel 1882 Walther Flemming: Chromatin elnevezés W. Waldeyer: CRM (szín) SZMA ( coloured body, festék láthatóvá tétel) DS polimer és molekulatömege kb E. ammersten, T. Caspersson - tisztított növényi vírusban (tobacco mosaic virus) is van W. M. Stanley (USA), obel dij, kémia, első elektronmikroszkópos kép (DS, pozitívan töltött fehérjék) nukleotid összetétel E. Chargaff (USA) 1953 kettős hélix J. Watson, F. Crick (UK) (.d. 1962) 1958 DS polimeráz I enzim (első DS készítő enzim) 1960 RS polimeráz; mrs felfedezése 1964 t RS Ala szekvenálása R. olley (USA) 1966 genetikai kód megfejtése 1968 védett nukleotidok összekapcsolása (A. Todd, Khorana) 1970 DS hasító enzim (restrikciós) felfedezése 1973 DS fragmensek beépítése plazmidba E. coli Androméda-törzs 1975 RS kromoszóma szekvenálása; MS2 fág (3 fehérje) 1977 GEETEC
3 1978 somatostatin: az első emberi hormon, rekombináns technológiával (W. Arber, D. athans,.. Smith, obel-díj: restrikciós enzimek) 1979 malignus sejtből származó DS-sel fertőzni lehet egészséges sejtvonalat 1980 obel-díj: DS szekvenálás; rekombináns DS szintézis F. Sanger; W. Gilbert humán inzulin (DS technológia) a piacon (humulin) - első onkogének izolálása, expresszálása, szekvenálása (egy aminosav különbség) 1983 DS a l baktérium fágból ( bázispár) UMA GEM projekt elfogadása (USA Kongresszus) kb. 3 x 109 bázispár 3 milliárd USD 1 USD/ bázispár 1992 The F. Sanger Centre, Cambridge (DA szekvenálás, UG) 2000 The F. Sanger Institute the role of genetics in health and disease 2009 obel-díj: Telomer/telomeráz védi a kromoszómát E.. Blackburn, C. W. Greider, J.W. Szostak 2015 Francis Crick Institute, London (1500, inc kutató, GB 100 millió) Felosztás ukleotid koenzimek AD, AT AD FAD Co-A UD-cukrok RS Mt: plazma vírusok lánchossz:> 3x10 3 DS Mt: sejtmag vírusok lánchossz: > 10 7 E. coli 0,4 % 6 % 1 %
4 A nukleinsavak primer szerkezete Alapkomponensek - szénhidrát-foszfát heterociklusos bázis 1. Szénhidrát: monoszacharid, aldopentóz n b-d-2-dezoxiribóz (DS) 1 C C2 D-2-dezoxiribóz b-d-2-dezoxiribóz 1 b-d-ribóz (RS) C C C C C 2 b-d-ribóz
5 2. Foszforsav(ak) R R2 R1 R R monoészter foszfodiészter - lineáris - ciklusos >300 o C metafoszforsav difoszforsav 160 o C foszforsav (ortofoszforsav) trifoszforsav difoszforsav-észter trifoszforsav-észter
6 3. eterociklusos bázis 2 1 R 1 3 citozin (C) timin R = - C 3 R = - (T) (U) (C) pirimidin adenin (A) 2 1 a b 7 9 e 5 c 3 guanin, (G) 1 2 purin (pirimidin(d)imidazol)
7 Keto-enol tautoméria C 3 3C 3C vagy guanin timin Amino-imino tautoméria citozin adenin
8 ukleozidok szénhidrát és heterobázis ( glikozid kötés) 2 3C 3 dezoxicitidin dezoxitimidin dezoxiadenozin dezoxiguanozin b--glikozid
9 3 -hidroxi 5 -foszfát ukleotidok szénhidrát és foszforsav (3,5 - diészter kötés) - 5 C C 2 3 bázis 1-2 bázis 2-5 C C 2 5 -vég észter (primer ) - 3 Ribonukleotidok ionizációs állandói (pk) bázis 1 szekunder () bázis 2 3 -vég Bázis Szekunder foszfát rimer foszfát Adenozin - 5 -foszfát (5 -AM) * 3,8 6,1 0,9 Uridin foszfát (5 -UM) 9,5 6,4 1,0 Citidin foszfát (5 -CM) 4,5 6,3 0,8 Guanin foszfát (5 -GM) 2,4, 9,4 6,1 0,7
10 A polinukleotid lánc primer szerkezete 5 -vég 3C - timin C2 C2 - C2 - C2-3 -vég 2 2 adenin pk = 3,8 pk = 4,5 citozin guanin 2 pk= 2,4 9,4
11 A kettős polinukleotid lánc primer szerkezete Rövidítések A C foszfodiészter kötés cukorrész bázis A C G papcpg [ACG] 5
12 ukleinsav térszerkezetek Francis Crick, James D. Watson, A Z c só (RA) A 72% Et alacsony só koncentráció 50% Et c só Z Minimális só (nem Li 2 +) B 0.7 M MgCl 2 vagy 2.5 M acl 3M acl Alacsony nedvességű szálakban. C Magas sókoncentráció
13 B-DS A-DS Z-DS ármas (triple) helix
14 A nukleinsavak térszerkezete (háttér) A 2-dezoxi-D-ribóz téralkata (a gyűrű síkja fölötti C atom szerint) C - 2 endo C 3 endo 0,5 Å C 3 endo C - 2 endo
15 A b-glikozidkötéshez kapcsolódó konformerek Rotáció a C - glikozid kötés körül
16 Értelmezés James D. Watson: A kettős spirál, Gondolat, 1970, 1972
17 A, B és Z típusú DS jellemzői A B Z élix irány Jobbmenetű Jobbmenetű Balmenetű Bázispár per kanyar 11 10,4 12 (6 dimers) Bázispárok távolsága 2.3 Å 3.4 Å 3.8 Å Menetemelkedés 25,3 Å 35,4 Å 45,6 Å Bázispár dőlésszög Glikozid konformáció Dezoxicitidin Anti Anti Anti Dezoxiguanozin Anti Anti Syn Szénhidrát konformáció Dezoxicitidin C-3 -endo C-2 -endo C-2 -endo Dezoxiguanozin C-3 -endo C-2 -endo C-3 -endo
18 A DS-től a kromoszómákig
19 Összevetés: RS és DS
20 RS mrs másodlagos szerkezete
21 trs trs másodlagos szerkezete éhány módositott bázis a trs-ben éhány módositott bázisok trs-ben (75-95 nukleotid) (méret: nukleotid) Aminosav kapcsolódása trs Ala (olley,.d. 1968)
22 Aminoacil-tRS keletkezése
23 ukleotid származékok vírusellenes hatóanyagok Acyclovir, első vírusellenes hatóanyag, SV (Gertrude B. Elion, obel-dij, 1988) Ganclovir, vírusellenes hatóanyag, CMV Zidovudin (AZT), retrovírus ellenes Mechanizmus: antimetabolit típus, foszforileződés, vírus-enzim inhibitor
24 ukleotid származékok tumorellenes hatóanyagok irimidin analógok 2 F 5 2 C 5 - fluoro uracil ( Cl, Br, I ) citozin arabinozid (Ara-C) 2 F 2 C 2 C 5 -fluoro - 2' dezoxiuridin 5 - aza - citidin urin analógok S S 2 6-merkapto-adenin 6-merkapto-guanin
25 ukleinsav/oligonukleotid analitika 1. Elválasztás: gélelektroforézis 2. Kimutatás interkaláció C25 Br - Etidiumbromid (3,8-diamino-5-etil-6-fenil-fenantrédiumbromid) l g = nm l e =590 nm
26 Szekvencia meghatározása 1. Fragmentálás restrikciós enzimekkel Cél: feldarabolás (W. Arber,. Smith, D. athans, 1978 obel-díj) baktériumokban, kékalgákban 5 GAATTC 3 3 CTTAAGC 5 EcoRI törzs E. coli 5 GGCC 3 3 CCGG 5 ae III éhány II-es típusú restrikciós (endonukleáz) enzim (>2000) Bam I G/GATCC Bacillus amyloliquefaciens Bst I G/GATCC Bacillus stearothermophilus1503-4r Eco RI G/AATTC Escherichia coli RY 13 Fok I GGATG 9 / CCTAC 13 / Flavobacterium okeanokoites ind II GTy/uAC aemophilus influenzae R d ind I A/AGCTT aemophilus influenzae R d pa II C/CGG aemophilus parainfluenzae Msp I C/CGG Moraxella spezies ot I GC/GGCCGC ocardia otitidiscaviarum Sac I GAGC/TC Streptomyces achromogenes Sau 3A /GATC Staphyllococcus aureus 3A Sma I 5'- 3' irányban CCC/GGG haladva a hasítás Serratia pontos marcecescens helye: '/' jelnél Sb ú Xma I C/CCGGG Xanthomonas malvacearum
27 2. uleotid sorrend meghatározás 2a. Kémiai módosítás/hasítás (A. Maxam, W.Gilbert, 1977) 2b. Didezoxi beépítés - enzimes módszer (F. Sanger et al., 1977)
28 2a. Kémiai módosítás/hasítás (A. Maxam, W. Gilbert, 1977) 1. lépés 2. lépés 5 ATTGACTTAGCC 3 omogén Single-stranded DS minta előállítása Jelölés a szabad 5 -végen 32 (*) (polinukleotid kináz, észter) *ATTGACTTAGCC 12-mer 3. lépés Kémiai hasítás G reakció A reakció + G reakció T reakció + C reakció C reakció *ATTGACTTAGCC *ATTGACTTA *ATT *ATTGACTTAGCC *ATTGACTTA *ATTGACTT *ATTG *ATT *ATTGACTTAGCC *ATTGACTTAGC *ATTGACTTAG *ATTGACT *ATTGAC *ATTGA *AT *A *ATTGACTTAGCC *ATTGACTTAGC *ATTGACTTAG *ATTGA
29 4. lépés: elektroforézis élda: G hasítás után elbomlás Fragmens hossz *ATTGAACTTAGCC *ATTGAACTTA AACTTAGCC *ATT AACTTA CC lépés: autoradiográfia 6. lépés: szekvencia leolvasás
30 5 G reakció 2 C Kémiai hasítás: urinok 3C S C3 Dimetilszulfát (metilezés) Bázis (gyűrűfelnyitás) C2-3 C3 + - C3 C3 C C C2 C iperidin 5 (-glikozidos kötés hasítás) C2 b a Bázis (Cukor-foszfát lánc hasítás) 2C C 5 C - C - C
31 A > G: A reakció 5 2-3C S C3 dimetilszulfát 0 o C, 0,1 M Cl, 2 óra C 3 - (-metilezés) - 3 -glikozidos kötés hasítás p 7 90 o C C + 2-3C 3 - Bázis (Cukor-foszfát lánc hasítás) 5 C 2 - C C - C C - 3 -
32 Kémiai hasítás: irimidinek 2 - timin 3C hidrazin (-metilezés) citozin 3C 4-Me-3-pirazolon 1 C Urea amino-pirazol dezoxiribozil-hidrazon piperidin - Bázis (Cukor-foszfát lánc hasítás a 3 - végen) 2 3 asítás a 3 végen
33 5 C reakció 5 C C C C C idrazin, 1 M acl (gátolja a timin metileződést) piperidin C C
34 5 C + T: T reakció - C3 2 2 hidrazin 5-2 C glikozidos kötés hasítás piperidin Bázis (Cukor-foszfát lánc hasítás) C C 2 C C C C
35 Maxam-Gilbert módszer - kiértékelés
36 2b. Didezoxi nuleotid beépítés enzimes módszer (F. Sanger et al., 1977) templát primer DS polimeráz +
37 1. lépés: Didezoxi nukleotid jelölése a) Radioaktív izotóp ( 32 ) B B b) Fluorofór (fluoreszcens jelölés, L. E. ood, 1986)
38 2. lépés A DS-polimeráz müködésének blokkolása 3 GAATTCGCTAATGC 5 CTTAA primer szekvenálandó DS DS polimeráz I dat, dtt, dct, dgt + didezoxi analóg (ddat) 3 GAATTCGCTAATGC 5 CTTAAGCGATTA + 3 GAATTCGCTAATGC 5 CTTAAGCGA 4 edény 4 analóg
39 Áttekintés 5 3 DS polimeráz 3 5 primer ( 32 ) ddgt ddat ddtt ddct DEATURÁLÁS
40 1. iroszekvenálás 2. Illumina/Solexa szekvenálás Új-generációs szekvenálás 3. SLiD (Sequencing by ligonucleotid Ligation and Detection) 4. TSMS (True Single Molecule Sequencing) Valódi egymolekulás szekvenálás) 5. SMRT (Single Molecule Real-time) Egymolekulás valósidejű szekvenálás /nanopore-sequencing/
41 ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban (1955) Tood (obel díj 1957), Khorana (obel díj 1975) Kapcsoló szer: DCC/iridin 8-12 tagszám 2. Foszfit módszer, szilárd hordozón Beaucage, Caruthers; (1981) (Merrifield obel dij, 1984)
42 1. Szintézis oldatban Kapcsoló szer: Védőcsoportok: DCC/iridin acetil, tritil 1. lépés: Védett komponensek kapcsolása C C3 Sir Alexander R. Todd ( ) -acetil (Ac) C 6 4 C C3 Tritil (Tr) C C C3, diciklohexil-karbodiimid (DCC) -acetil (Ac)
43 2. lépés: A védőcsoportok eltávolítása Tr Ac A Ac C 1. Lúg 2. Sav (80% Ac) A C Ac Tr A Lúg C + T Ac 3. lépés: Láncnövekedés Védőcsoportok C Me C védelem (MMTr) védelem (Bz) MMTr = monometoxi-tritil
44 2. Szintézis szilárd fázison Foszfit módszer Beaucage, Caruthers (1981) 2.1 Szilárd hordozó: szilika, üveggyöngy,műanyag, cellulóz, papir 3-aminopropanol szilika Si szilika Si (C2) borostyánkősavanhidrid 2. védett nukleotid savérzékeny DMTr Bz A 2 szilika Si (C2)3 C (C2)2 C bázis érzékeny + Bz A szilika Si (C2)3 C (C2)2 C + DMTr + l= 498 nm (karbokation)
45 2.2 Védőcsoportok DMTr + C3 DMTr A Bz 2 Si (C 2 ) 3 C (C 2 ) 2 C C + szilika C3 C3 2 C C benzoil -6-benzoil adenin [A Bz ] C3-4-benzoli citozin [C Bz ] 4,4 -dimetoxitritil (DMtr) -2-isobutil guanin [G IBu ] a) C 3 - b) b-c-c 2 -C 2 - (b-cianoetil) C izopropioil, diizopropil
46 2.3 Aktiválás A DMTr 3C A DMTr 3C tetrazol Bz Bz diizopropil foszforamidát 2.4 Kapcsolás A DMTr 3C Bz G Szilika IBu A DMTr 3C G Szilika IBu Bz + tetrazol
47 2.5 xidáció: foszforos sav (foszfonsav) foszforsav DMTr A Bz DMTr A Bz I 2, 2 IBu 3C G kollidin* C3 1 3 G IBu Szilika 2 Szilika *trimetil-piridin 2.6 asítás 1. C 3 eltávolítása (tiofenol) helyette 2. ligonukleotid lehasítása a hordozóról ( 3 ) 3. ukleozid bázis védőcsoport (Bz, IBu) eltávolítása ( 4 + hő) 2.7 Tisztítás LC Elektroforézis
48 Foszforsavak R R2 R1 R R monoészter foszfodiészter - lineáris - ciklusos >300 o C metafoszforsav difoszforsav 160 o C foszforsav (ortofoszforsav) trifoszforsav difoszforsav-észter trifoszforsav-észter
49 ligonukleotid szintézis ciklus ( phosphoramidite ) Kezdés Tritil-csoport hasítása Következő ciklus 1. lépés Aktiválás, kapcsolás 2. lépés Sapkázás (capping): reakció ecetsavanhidriddel, a szabad acetilezése ligonukleotid hasitása a hordozóról 4. lépés Tritil-csoport hasítása 3. lépés xidáció Védőcsoportok hasítása
50 DS/oligonukleotid chip (csip)
51 Expression levels of 50 genes most highly correlated with the acute lymphoblastic leukemia (ALL) and acute myeloid leukemia (AML) Expressed in ALL Expressed in AML Expression levels greater than the mean: red, below the mean: blue. TR Golub et al Science 286: 531 (1999)
52 Koenzimek Enzim = apoenzim (fehérje) + koenzim (nem-fehérje) Szubsztrátspecifitás Reakciótípus Felosztás ukleotid Fémion (példa) Egyéb Fe (citokróm oxidáz) AD Cu (aszkorbinsav oxidáz) B1 FAD Zn (alkohol dehidrogenáz) B6 AT Mn (hisztidin ammónia-liáz) B12 Koenzim A Co (glutamát mutáz) folsav i (ureáz) pantoténsav Mo (xantin oxidáz) biotin V (nitrát reduktáz) Se (glutation peroxidáz)
53 ukleotid koenzimek 1. Adenozin mono-, di- és trifoszfát felfedezés: Lohmann, Fiske (1929) észterkötés D-ribóz b--glikozid Adenozin-monofoszfát (AM) 2 ciklusos AM AT AD foszforsav D = -31 kj/mol
54 2. AD/AD: oxidáció 2 5 nikotinamid D-ribóz 2 5 adenin élda: nikotinamid-adenin-dinukleotid (AD + ) C 3 -C AD enzim C 3 -C + AD + AD = alkohol dehidrogenáz acetaldehid AD Mechanizmus e R R AD + AD
55 3. FAD/FAD 2 : oxidáció oxidált /enzimkötődés/ redukált Flavin-adenin-dinukleotid (FAD) Flavus (latin), sárga
56 4. Koenzim-A (CoA) felfedezés: Lipmann, 1946 adenozin-3,5 -difoszfát észter kötés 5 észter kötés 3 savamid kötés 2,4-dihidroxi-3,3- dimetil-vajsav b-alanin ciszteamin pantoténsav (vitamin) savamid kötés S-acetil koenzim-a (Ac-CoA) - (C 2 ) 2 - S - (C 2 ) 2 - S C C 3
57 5. Koenzim-Q (ubikinon, CoQ) (eukarióta sejtekben, mitokondriumok) szemikinon (Izoprén egységek) ubikinon Koenzim Q 4, n = 4 Koenzim Q 9, n = 9 Koenzim Q 10, n = 10 ubikinol eter D. Mitchell, 1961 (obel díj, kémia, 1978) for his contribution to the understanding of biological energy transfer through the formulation of the chemiosmotic theory". Később: elektrontranszport lánc koncepció CoQ10 protonvonzó
58 VITAMIK 1912: vitamin = vita amines (Casimir Funk) Kis mennyiségben kívülről kell felvenni. em vitaminok: esszenciális aminosavak esszenciális zsírsavak rovitaminok Antropocentrikus pl. C-vitamin: ember (tengeri malac) igen patkány nem p-amino-benzoesav: baktérium igen ember nem Kémiai szerkezet: heterogén Felosztás (oldékonyság alapján) Vízoldékony Zsírban oldódó B, C, és vitaminok A, D, E és K vitaminok - koenzimek is - bélből szívódnak fel - felesleg kiürül - májban raktározódnak 1958: féle vitamin
59 B1 vitamin (tiamin) szerkezet 1934, szintézis 1936 Beri-beri piroszőlősav nem bomlik le pirimidin tiazol észter kötés - - 3C 2 + tiamin C3 S C2C2 AT 2 C3 3 + C2C2 2 S 3C 1 tiamin-pirofoszfát (koenzim) - piroszőlősav: + 3C C piroszőlősav-dekarboxiláz C3 C2C2-3C S C 3C aktív piruvát brit tengerészek (1747) Ch. Eijkman (1897), F. G. opkins [orvosi obel-díj (1929)] C. Funk vita amin (1912)
60 B 2 -vitamin (riboflavin) ( ) for his work on carotenoids and vitamins obel-díj, 1938 izolálás: Richard Kuhn (1933), 4500 liter tejsavóból 1g (természetben 1-foszfát-észter) D-ribóz bőrbántalom növekedés 3C 3C Izo-alloxazin váz 1,3,5,8-tetraazanaftalin (pteridin) B 6 -vitamin (piridoxál, piridoxin) izolálás: Euler (1937) C C2 C C C 3C piridoxál (- C) piridoxin (- ) Bőrbántalmak, élesztő 5 -foszfát - észter (koenzim)
61 B 12 -vitamin (kobalamin) Lásd fémorganikus/porfirin vázas Kobalt ion Szerkezet: D. odgkin, xford, obel díj, 1964 (penicillin is) ational ortrait Galery London Folsav (pteroil-glutaminsav) izolálás: eterson (1940), vérszegénység (anémia, leukopénia) p-amino-benzoesav pteridin glutaminsav C formil-5,6,7,8-tetrahidrofolsav, folinsav (koenzim)
62 C-vitamin (L-aszkorbinsav) felfedezés: 1928 izolálás: Szentgyörgyi A. (1932) skorbut keto-L-gulonsav g-laktám 6 = 6 1 C 2 L-aszkorbinsav) -vitamin (biotin) izolálás: Kögl (1936) 2800 kg tojássárgája 390 mg 1 tojás 50 g, ebből 17 g sárgája 390 mg = db tojás imidazolidin * * * tetrahidrotiofén Avidin biotin K d = 10-15
63 ikotinsav(niacin)/ B 3 vitamin és a nikotinsavamid hiánya: pellagra (pelle agra = durva bőr) nikotinsavamid 2 niacin AD + (koenzim) Koleszterin szint szabályozó (?) antoténsav/b 5 vitamin 3C pantothen (πάντοθεν): mindenfelől koenzim A C3 élesztő b-alanin a,g - dihidroxi b,b- dimetil-vajsav Roger J. Williams 1933 stressz ellenes vitamin
64 C 3 C 2 =C-C=C 2 A-vitamin Kuhn, 1931, halak májából,farkasvakság, 0,5-1 mg/nap, 1 E = 0,6 mg provitamin: b-karotin világos sárga olaj, fp.: 136 C A 1 = retinol,a 2 = dehidroretinol A vitamin cisz-retinal rodopszin K 1 -vitamin (fillokinon) naftokinon C3 sárga olaj C3 C3 3C C3 C3 Szerepe: antioxidáns, gyulladásgátló, Koaguláció iánya: vérzékenység (koaguláció hiánya miatt) fitil-csoport 2-metil-3-fitil-1,4-naftokinon Bomlás: fény, hő (100 o C felett) Előfordulás: káposztafélék, spenót, saláta, brokkoli, tejtermék, máj
65 2 3 1 A 4 R B 6 19 C3 R C R D 3C C3 7-dehidrokoleszterin 20 Állati eredetű élelmiszerek alolaj, máj, tojás, tejtermék D-vitaminok C3 C3 napfény hn l = nm 3C C3 C2 D 3 -vitamin (kolekalciferol) C3 C3 op.: C C3 C3 3C C3 C3 3C C3 C3 C3 hn 3C C3 C2 ergoszterol övényi eredetű élelmiszerek Sörélesztő, gombák D 2 -vitamin (ergo)kalciferol op.: C 1 E = 0,025 mg Szerepe: Ca 2+ - és foszfát felszívódás, csontképződés sziv- és érrendszer védelme, immunhiányos állapot, osztódás iánya: angolkór (rickets), csontritkulás, csontosodási zavar ipervitamiózis: Csontszövet Ca2+- lerakódás, vesekőképződés
66 E-vitamin (tokoferol) τόκος [tókos], φέρειν [phérein] = születés, hordozni izolálás 1936 felfedezés 1927 szintézis 1938 R3 R2 7 C3 C3 C3 3C 5 R1 C3 C3 kromán váz C16 lánc halványsárga olaj R 1 =R 2 =R 3 =C 3 R 1 =R 3 =C 3, R 2 = R 2 =R 3 =C 3, R 1 = a-tokoferol (5,7,8-trimetil) b-tokoferol (5,8-dimetil) g-tokoferol (7,8-dimetil) Előfordulás: növényi olajok, napraforgó, oliva, tökmag hús, máj, tojás, tejtermék Szerepe: antioxidáns, gyulladásgátló iánya: vérszegénység, izomsorvadás, meddőség (embernél ritka) ipervitamiózis: Csontszövet Ca2+- lerakódás, vesekőképződés E-vitamin (tokotrienol) R3 R2 C3 C3 C3 3C R1 C3 C3 antisterilitás (patkány)
5. Előadás Nukleinsavak kimutatása, szekvenálás
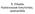 5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
CHO H H H OH H OH OH H CH2OH HC OH HC OH HC OH CH 2
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
6. Előadás Oligonukleotidok szintézise, koenzimek, vitaminok
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
CHO H H H OH H OH OH H CH2OH CHO OH H HC OH HC OH HC OH CH 2 OH
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895) 1970: FM Insitute
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895) 1970: FM Insitute
4. Előadás. Nukleozidok, nukleotidok, nukleinsavak
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895), izolálás 1970: FM
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895), izolálás 1970: FM
P O O O. OAc A O. OAc
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
Sir Alexander R. Todd ( )
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció 3 5 ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Fehérjék. SZTE ÁOK Biokémiai Intézet
 Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
Fehérjék Csoportosítás Funkció alapján Szerkezetük alapján Kapcsolódó nem peptid részek alapján Szintézisük Transzkripció - sejtmag Transzláció - citoplazma Poszttranszlációs módosítások (folding) - endoplazmatikus
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Néhány fontosabb vitamin
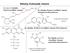 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
,:/ " \ OH OH OH - 6 - / \ O / H / H HO-CH, O, CH CH - OH ,\ / "CH - ~(H CH,-OH \OH. ,-\ ce/luló z 5zer.~ezere
 - 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
- 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
Dr. Mandl József BIOKÉMIA. Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek.
 Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
Nukleinsavak. Szerkezet, szintézis, funkció
 Nukleinsavak Szerkezet, szintézis, funkció Nukleinsavak, nukleotidok, nukleozidok 1869-ben Miescher a sejtmagból egy savas természetű, lúgban oldódó foszfortartalmú anyagot izolált, amit később, eredetére
Nukleinsavak Szerkezet, szintézis, funkció Nukleinsavak, nukleotidok, nukleozidok 1869-ben Miescher a sejtmagból egy savas természetű, lúgban oldódó foszfortartalmú anyagot izolált, amit később, eredetére
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Max. bekever és napi adagba. Max. életkor 13500 NE 13500 NE 13500 NE 13500 NE 13500 NE 13500 NE 25000 NE. nincs korlátozás nincs korlátozás
 1 Vitaminok és elővitaminok, 1831/2003/EC-ben 3.a csoport szám Egyedi név Kémiai képlet, leír Állatfaj, - életkor Egyéb előír E 672 E 160 a A vitamin - acetát - palmitát - propionát Béta-karotin C22H32O2
1 Vitaminok és elővitaminok, 1831/2003/EC-ben 3.a csoport szám Egyedi név Kémiai képlet, leír Állatfaj, - életkor Egyéb előír E 672 E 160 a A vitamin - acetát - palmitát - propionát Béta-karotin C22H32O2
A nukleinsavkémiai kisszótár:
 A nukleinsavkémiai kisszótár: DS: dezoxiribonukleinsav, DA : olyan nukleotidegységekből felépülő nukleinsavak gyűjtőneve, amelyek dezoxiribóz cukorrészt tartalmaznak. A gének kódolására, és továbbadására
A nukleinsavkémiai kisszótár: DS: dezoxiribonukleinsav, DA : olyan nukleotidegységekből felépülő nukleinsavak gyűjtőneve, amelyek dezoxiribóz cukorrészt tartalmaznak. A gének kódolására, és továbbadására
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
Vitaminok meghatározása és csoportosítása
 Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Mária. A pirimidin-nukleotidok. nukleotidok anyagcseréje
 Prof.. Sasvári Mária A pirimidin-nukleotidok nukleotidok anyagcseréje 1 A nukleobázisok szerkezete Nitrogéntartalmú, heterociklusos vegyületek; szubsztituált purin- és pirimidin-származékok purin Adenin
Prof.. Sasvári Mária A pirimidin-nukleotidok nukleotidok anyagcseréje 1 A nukleobázisok szerkezete Nitrogéntartalmú, heterociklusos vegyületek; szubsztituált purin- és pirimidin-származékok purin Adenin
Genomika. Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel. DNS szekvenálási eljárások. DNS ujjlenyomat (VNTR)
 Genomika (A genom, génállomány vizsgálata) Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel DNS szekvenálási eljárások DNS ujjlenyomat (VNTR) DNS chipek statikus és dinamikus információk vizsgálata
Genomika (A genom, génállomány vizsgálata) Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel DNS szekvenálási eljárások DNS ujjlenyomat (VNTR) DNS chipek statikus és dinamikus információk vizsgálata
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód)
 2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
Táplálék. Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz
 Étel/ital Táplálék Táplálék Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz Szénhidrát Vagyis: keményítő, élelmi rostok megemésztve: szőlőcukor, rostok Melyik élelmiszerben? Gabona, és feldolgozási
Étel/ital Táplálék Táplálék Szénhidrát Fehérje Zsír Vitamin Ásványi anyagok Víz Szénhidrát Vagyis: keményítő, élelmi rostok megemésztve: szőlőcukor, rostok Melyik élelmiszerben? Gabona, és feldolgozási
TAKARMÁNYOZÁSTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Vitaminok jelentősége kis mennyiségben előforduló biológiailag aktív anyagok esszenciálisak ( vital amines =létfontosságú
TAKARMÁNYOZÁSTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Vitaminok jelentősége kis mennyiségben előforduló biológiailag aktív anyagok esszenciálisak ( vital amines =létfontosságú
BIOLÓGIA VERSENY 10. osztály 2016. február 20.
 BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
Táplálkozás. SZTE ÁOK Biokémiai Intézet
 Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
Táplálkozás Cél Optimális, kiegyensúlyozott táplálkozás - minden szükséges bevitele - káros anyagok bevitelének megakadályozása Cél: egészség, jó életminőség fenntartása vagy visszanyerése Szükséglet és
A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan.
 A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan. A táplálékfelvétel célja: Nyersanyagok biztosítása a test számára a növekedéshez a szöveti regenerációhoz az ivarsejtek képzéséhez
A gasztrointesztinális (GI) rendszer élettana IV. Táplálkozás élettan. A táplálékfelvétel célja: Nyersanyagok biztosítása a test számára a növekedéshez a szöveti regenerációhoz az ivarsejtek képzéséhez
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE
 AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
TestLine - Biogén elemek, molekulák Minta feladatsor
 TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
Vitaminok csoportosítása
 Vitaminok A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe a vitaminokat a táplálékkal
Vitaminok A vitaminok az emberi szervezet számára nélkülözhetetlen, kis molekulájú, különféle kémiai összetételű biológiailag aktív szerves vegyületek. Az emberi szervezetbe a vitaminokat a táplálékkal
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig
 A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
10. Előadás. Heterociklusos vegyületek.
 0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
A vitaminok és az élelmiszerek kapcsolatáról
 A vitaminok és az élelmiszerek kapcsolatáról Rengeteg tévinformáció "marketing szöveg" és áltudományos szenzáció található a világhálón a vitaminokról és forrásaikról. Cikkünkben megpróbálunk a tényekre
A vitaminok és az élelmiszerek kapcsolatáról Rengeteg tévinformáció "marketing szöveg" és áltudományos szenzáció található a világhálón a vitaminokról és forrásaikról. Cikkünkben megpróbálunk a tényekre
elektrokémiai-, ozmózisos folyamatokban, sav bázis egyensúly fenntartásában, kolloidok állapotváltozásaiban, enzimreakciókban.
 Ásványi anyagok Ásványi anyagok Ami az elhamvasztás után visszamarad. Szerepük: elektrokémiai-, ozmózisos folyamatokban, sav bázis egyensúly fenntartásában, kolloidok állapotváltozásaiban, enzimreakciókban.
Ásványi anyagok Ásványi anyagok Ami az elhamvasztás után visszamarad. Szerepük: elektrokémiai-, ozmózisos folyamatokban, sav bázis egyensúly fenntartásában, kolloidok állapotváltozásaiban, enzimreakciókban.
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Human genome project
 Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód)
 2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
Nanotechnológia. Nukleinsavak. Készítette - Fehérvári Gábor
 Nanotechnológia Nukleinsavak Készítette - Fehérvári Gábor Bevezető A nukleinsavak az élő anyag alapvetően fontos komponensei. Meghatározó szerepet töltenek be az átöröklésben, a fehérjék szintézisében
Nanotechnológia Nukleinsavak Készítette - Fehérvári Gábor Bevezető A nukleinsavak az élő anyag alapvetően fontos komponensei. Meghatározó szerepet töltenek be az átöröklésben, a fehérjék szintézisében
Vitaminok Ásványi anyagok
 Táplálkozástan és gasztronómia 2012.04.23. 1 Védő tápanyagok Vitaminok Ásványi anyagok 2012.04.23. 2 Vitaminok! A szervezet számára nélkülözhetetlen, biológiailag aktív anyagok, energiát nem szolgáltatnak,
Táplálkozástan és gasztronómia 2012.04.23. 1 Védő tápanyagok Vitaminok Ásványi anyagok 2012.04.23. 2 Vitaminok! A szervezet számára nélkülözhetetlen, biológiailag aktív anyagok, energiát nem szolgáltatnak,
NUKLEINSAVAK. DNS (DNA) /dezoxiribonukleinsav/ -sejtplazmában -peptid / fehérje szintézis vezérlése (messenger-, transfer-rns)
 UKLEISAVAK Első elkülönítés: Miescher 189. (gennyből) vízben és híg savban oldhatatlan, de lúgban oldódó, foszfortartalmú anyag Két típus: RS (RA) /ribonukleinsav/ DS (DA) /dezoxiribonukleinsav/ -sejtplazmában
UKLEISAVAK Első elkülönítés: Miescher 189. (gennyből) vízben és híg savban oldhatatlan, de lúgban oldódó, foszfortartalmú anyag Két típus: RS (RA) /ribonukleinsav/ DS (DA) /dezoxiribonukleinsav/ -sejtplazmában
Kémiai Intézet Kémiai Laboratórium. F o t o n o k k e r e s z tt ü z é b e n a D N S
 Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK
 VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK KÉSZÍTETTE: GAÁL ELEONÓRA OKLEVELES TÁPLÁLKOZÁSTUDOMÁNYI SZAKEMBER DEBRECENI EGYETEM Egészséges alapanyagok egészséges táplálkozás mintaprojekt a közétkeztetés minőségi
VITAMINOK JELENTŐSÉGE ÉS FORRÁSAIK KÉSZÍTETTE: GAÁL ELEONÓRA OKLEVELES TÁPLÁLKOZÁSTUDOMÁNYI SZAKEMBER DEBRECENI EGYETEM Egészséges alapanyagok egészséges táplálkozás mintaprojekt a közétkeztetés minőségi
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Grilla Stúdiója - gyógytorna, szülésfelkészítés
 Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
Az éltetõ vitaminok A vitaminok olyan szerves vegyületek, amelyek feltétlenül szükségesek testünk kifogástalan mûködéséhez. A vitamin elnevezés a vita (élet) és az amin (NH2-tartalmú kémiai gyök) szavakból
A gyakorlat elméleti háttere A DNS molekula a sejt információhordozója. A DNS nemzedékről nemzedékre megőrzi az élőlények genetikai örökségét.
 A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
Vitaminok leírása, hatásai
 Vitaminok leírása, hatásai A vitaminok két nagyobb csoportra oszthatók, vízben oldódó és zsírban oldódó vitaminokra. &amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp
Vitaminok leírása, hatásai A vitaminok két nagyobb csoportra oszthatók, vízben oldódó és zsírban oldódó vitaminokra. &amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp;amp
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Poligénes v. kantitatív öröklődés
 1. Öröklődés komplexebb sajátosságai 2. Öröklődés molekuláris alapja Poligénes v. kantitatív öröklődés Azok a tulajdonságokat amelyek mértékegységgel nem, vagy csak nehezen mérhetők, kialakulásuk kevéssé
1. Öröklődés komplexebb sajátosságai 2. Öröklődés molekuláris alapja Poligénes v. kantitatív öröklődés Azok a tulajdonságokat amelyek mértékegységgel nem, vagy csak nehezen mérhetők, kialakulásuk kevéssé
2010. Vitaminok kézi- könyve. www.egeszsegeletmod.hu. Lőrincz Balázs 2010.03.20.
 2010. Vitaminok kézi- könyve Lőrincz Balázs www.egeszsegeletmod.hu 2010.03.20. Tartalomjegyzék Bevezető... 3 A vitamin retinol... 3 C vitamin aszkorbinsav... 3 D vitamin kalciferol... 4 E vitamin tokoferol...
2010. Vitaminok kézi- könyve Lőrincz Balázs www.egeszsegeletmod.hu 2010.03.20. Tartalomjegyzék Bevezető... 3 A vitamin retinol... 3 C vitamin aszkorbinsav... 3 D vitamin kalciferol... 4 E vitamin tokoferol...
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
alanin (Ala, A) valin (Val, V) leucin (Leu, L) izoleucin (Ile, I) szerin (Ser, S) treonin (Thr, T)
 Aminosavak I. (fehérjealkotó aminosavak) Az emberben előforduló fehérjealkotó aminosavak L-konfigurációjúak, a ahn Ingold relog-nevezéktan alapján pedig az S-sorozatba tartoznak a ys kivételével (ami R
Aminosavak I. (fehérjealkotó aminosavak) Az emberben előforduló fehérjealkotó aminosavak L-konfigurációjúak, a ahn Ingold relog-nevezéktan alapján pedig az S-sorozatba tartoznak a ys kivételével (ami R
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
Valin H 3 C. Treonin. Aszpartát S OH
 2 Glicin C 3 Alanin C 3 Valin 3 C Leucin 2 2 2 C 3 Izoleucin 2 zerin 2 Treonin 2 Tirozin 2 Cisztein Metionin Aszpartát 2 C 3 2 Glutamát 2 2 Aszparagin 2 Glutamin 2 Arginin 2 2 2 2 2 Lizin isztidin Fenilalanin
2 Glicin C 3 Alanin C 3 Valin 3 C Leucin 2 2 2 C 3 Izoleucin 2 zerin 2 Treonin 2 Tirozin 2 Cisztein Metionin Aszpartát 2 C 3 2 Glutamát 2 2 Aszparagin 2 Glutamin 2 Arginin 2 2 2 2 2 Lizin isztidin Fenilalanin
Biológus MSc. Molekuláris biológiai alapismeretek
 Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
A nukleinsavkémia koronázatlan királyai, kémiai és orvosi Nobel-díjak:
 A nukleinsavkémia koronázatlan királyai, kémiai és orvosi obel-díjak: Francis arry James Dewey ompton rick Watson Maurice ugh Frederick Wilkins 1962 DS molekuláris szerkezetének felismeréséért aul Berg
A nukleinsavkémia koronázatlan királyai, kémiai és orvosi obel-díjak: Francis arry James Dewey ompton rick Watson Maurice ugh Frederick Wilkins 1962 DS molekuláris szerkezetének felismeréséért aul Berg
Kun Ádám. Növényrendszertani, Ökológiai és Elméleti Biológiai Tanszék, ELTE MTA-ELTE-MTM Ökológiai Kutatócsoport. Tudomány Ünnepe,
 Kun Ádám Növényrendszertani, Ökológiai és Elméleti Biológiai Tanszék, ELTE MTA-ELTE-MTM Ökológiai Kutatócsoport Tudomány Ünnepe, 2016.11.22. Miskolc Kun Ádám: A víz szerepe az élet keletkezésében. Tudomány
Kun Ádám Növényrendszertani, Ökológiai és Elméleti Biológiai Tanszék, ELTE MTA-ELTE-MTM Ökológiai Kutatócsoport Tudomány Ünnepe, 2016.11.22. Miskolc Kun Ádám: A víz szerepe az élet keletkezésében. Tudomány
7. évfolyam kémia osztályozó- és pótvizsga követelményei Témakörök: 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2.
 7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
7. évfolyam kémia osztályozó- és pótvizsga követelményei 1. Anyagok tulajdonságai és változásai (fizikai és kémiai változás) 2. Hőtermelő és hőelnyelő folyamatok, halmazállapot-változások 3. A levegő,
Hús és hústermék, mint funkcionális élelmiszer
 Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
MAGYAR ÉLELMISZERKÖNYV. Codex Alimentarius Hungaricus
 MAGYAR ÉLELMISZERKÖNYV Codex Alimentarius Hungaricus 1-1-2001/15 számú előírás Különleges táplálkozási igényt kielégítő élelmiszerekhez adható tápértéknövelő anyagok Substances that may be added for specific
MAGYAR ÉLELMISZERKÖNYV Codex Alimentarius Hungaricus 1-1-2001/15 számú előírás Különleges táplálkozási igényt kielégítő élelmiszerekhez adható tápértéknövelő anyagok Substances that may be added for specific
Purin nukleotidok bontása
 Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
37/2004. (IV. 26.) ESzCsM rendelet. az étrend-kiegészítőkről
 Az élelmiszerekről szóló 2003. évi LXXXII. törvény 20. -a (11) bekezdésének b) pontjában kapott felhatalmazás alapján az alábbiakat rendelem el: 1. (1) E rendelet előírásait a Magyarországon forgalomba
Az élelmiszerekről szóló 2003. évi LXXXII. törvény 20. -a (11) bekezdésének b) pontjában kapott felhatalmazás alapján az alábbiakat rendelem el: 1. (1) E rendelet előírásait a Magyarországon forgalomba
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
4. SZERVES SAVAK. Az ecetsav biológiai előállítása SZERVES SAVAK. Ecetsav baktériumok. Az ecetsav baktériumok osztályozása ECETSAV. 04.
 Az ecetsav biológiai előállítása 4. SZERVES SAVAK A bor után legősibb (bio)technológia: a bor megecetesedik borecet keletkezik A folyamat bruttó leírása: C 2 H 5 OH + O 2 CH 3 COOH + H 2 O Az ecetsav baktériumok
Az ecetsav biológiai előállítása 4. SZERVES SAVAK A bor után legősibb (bio)technológia: a bor megecetesedik borecet keletkezik A folyamat bruttó leírása: C 2 H 5 OH + O 2 CH 3 COOH + H 2 O Az ecetsav baktériumok
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
AMINOK. Aminok rendűsége és típusai. Levezetés. Elnevezés. Alkaloidok (fiziológiailag aktív vegyületek) A. k a. primer RNH 2. szekunder R 2 NH NH 3
 Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
 3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Zsírsav szintézis. Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P. 2 i
 Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
MAGYAR ÉLELMISZERKÖNYV. Codex Alimentarius Hungaricus 1-1-90/496 számú előírás Az élelmiszerek tápértékének jelölése
 MAGYAR ÉLELMISZERKÖNYV Codex Alimentarius Hungaricus 1-1-90/496 számú előírás Az élelmiszerek tápértékének jelölése Nutrition labelling for foodstuffs Az előírás az Európai Közösségek Tanácsa 90/496/EGK
MAGYAR ÉLELMISZERKÖNYV Codex Alimentarius Hungaricus 1-1-90/496 számú előírás Az élelmiszerek tápértékének jelölése Nutrition labelling for foodstuffs Az előírás az Európai Közösségek Tanácsa 90/496/EGK
Az örökítőanyag. I. A tulajdonságokat meghatározó örökítőanyag/információ átadható/ transzformálható.(fred Griffith kísérlet, 1928.
 Az örökítőanyag I. A tulajdonságokat meghatározó örökítőanyag/információ átadható/ transzformálható.(fred Griffith kísérlet, 1928.) Kísérlet: Tüdőgyulladást okozó pneumococcus baktériumok vizsgálata. S
Az örökítőanyag I. A tulajdonságokat meghatározó örökítőanyag/információ átadható/ transzformálható.(fred Griffith kísérlet, 1928.) Kísérlet: Tüdőgyulladást okozó pneumococcus baktériumok vizsgálata. S
Géntechnológia és fehérjemérnökség
 Géntechnológia és fehérjemérnökség Szerkesztette: Nyitray László Alexa Anita (12. és 13. fejezet) Fodor Krisztián (3. és 9. fejezet) Garai Ágnes (4. és 5. fejezet) Glatz Gábor (6. és 7. fejezet) Radnai
Géntechnológia és fehérjemérnökség Szerkesztette: Nyitray László Alexa Anita (12. és 13. fejezet) Fodor Krisztián (3. és 9. fejezet) Garai Ágnes (4. és 5. fejezet) Glatz Gábor (6. és 7. fejezet) Radnai
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
Sejttenyésztési alapismeretek
 Sejttenyésztési alapismeretek 1. Bevezetés A sejteknek ún. sejtkultúrákban történő tenyésztése (a sejteket az eredeti helyükről eltávolítva in vitro tartjuk fenn ill. szaporítjuk) és tanulmányozása több
Sejttenyésztési alapismeretek 1. Bevezetés A sejteknek ún. sejtkultúrákban történő tenyésztése (a sejteket az eredeti helyükről eltávolítva in vitro tartjuk fenn ill. szaporítjuk) és tanulmányozása több
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Termékadat. Összetevők. 100 g por 1 adag (200 g) (50 g por ml víz) Tápanyagok. Összetevők. Sovány tej
 Termékadat Összetevők Összetevők Sovány tej 17,4% kekszliszt (búzaliszt, szacharóz, vaj, édes savópor, térfogatnövelő szer: kálium-karbonát, só, savanyúságot szabályozó anyag: citromsav, vanília) Növényi
Termékadat Összetevők Összetevők Sovány tej 17,4% kekszliszt (búzaliszt, szacharóz, vaj, édes savópor, térfogatnövelő szer: kálium-karbonát, só, savanyúságot szabályozó anyag: citromsav, vanília) Növényi
Szerves Kémia. Farmakológus szakasszisztens képzés 2012/2013 ősz
 Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
TR90 M-Bars & M-Shakes
 TR90 M-Bars & M-Shakes Válassza ki kedvencét! TERMÉKPOZICIONÁLÁS Világunkban az idő pénz. Elfoglalt mindennapjainkban, amelyek a család, munka, társasági élet és teendők közötti ingázással telnek, nem
TR90 M-Bars & M-Shakes Válassza ki kedvencét! TERMÉKPOZICIONÁLÁS Világunkban az idő pénz. Elfoglalt mindennapjainkban, amelyek a család, munka, társasági élet és teendők közötti ingázással telnek, nem
2. oldal (3)1 A tápérték jelölésben megadott vitaminnak, illetve ásványi anyagnak jelentős mennyiségben - a napi ajánlott bevitel legalább 15%-ában -
 1. oldal 37/2004. (IV. 26.) ESzCsM rendelet az étrend-kiegészítőkről Az élelmiszerekről szóló 2003. évi LXXXII. törvény 20. -a (11) bekezdésének b) pontjában kapott felhatalmazás alapján az alábbiakat
1. oldal 37/2004. (IV. 26.) ESzCsM rendelet az étrend-kiegészítőkről Az élelmiszerekről szóló 2003. évi LXXXII. törvény 20. -a (11) bekezdésének b) pontjában kapott felhatalmazás alapján az alábbiakat
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
