A nukleinsavkémiai kisszótár:
|
|
|
- Ilona Fodor
- 8 évvel ezelőtt
- Látták:
Átírás
1 A nukleinsavkémiai kisszótár: DS: dezoxiribonukleinsav, DA <ang.>: olyan nukleotidegységekből felépülő nukleinsavak gyűjtőneve, amelyek dezoxiribóz cukorrészt tartalmaznak. A gének kódolására, és továbbadására szolgálnak. RS: ribonukleinsav, RA <ang.>: olyan nukleotid egységekből felépülő nukleinsav, amely cukorrészként ribózt tartalmaz, előfordul minden élő sejtben, valamint egyes vírusokban. ukleotidok: (= bázis + cukor + foszfát) a nukleozidok foszforsav-észtereinek gyűjtőneve. A bennük szereplő cukorrész (D-ribóz v. 2-dezoxi-D-ribóz) alapján megkülönböztetik a ribonukleotidok és a dezoxiribonukleotidok csoportját. ukleozidok: (= bázis + cukor) szűkebb értelemben a nukleinsavakban előforduló pirimidin- és purinbázisok -ribozid, ill. -2 -dezoxiribozid típusú glikozidjainak gyűjtőneve ( citidin, uridin, timidin, adenozin, guanozin). A ~okban a cukorrész mindig furanóz szerekezetű, a glikozidos szénatom pedig β-konfigurációjú. ukleinsavak (DS, RS): <lat. nucleus mag >: (= bázis+cukor+foszfát -> polimer) nukleotidokból felépülő óriásmolekulák (biopolimerek), amelyek minden sejtben és a virusokban is megtalálhatók, azoknak esszenciális alkotórészei. ~akat először F. Miescher (1869) különített el a genny fehérvérsejtjeiből. Watson rick-modell: a DS térszerkezetét leíró térszerkezeti modell. A ~ szerint a DS-molekula kettős hélixét két, ellentétes lefutású (antiparalel) polinukleotid-lánc alkotja. A két láncot a komplementer bázispárok (adenin timin, guanin citozin) között létrejött hidrogénkötések tartják össze. A kettőshélix-szerkezetet J. D. Watson és F. rick javasolta 1953-ban. A ~ szerint a polinukleotid-láncokat helikális szerkezetű cukorfoszfátváz építi fel; a hélix tengelyére merőleges irányban, a hélix belseje felé helyezkednek el a nukleinsavbázisok. A ~ alapján jól magyarázható a genetikai információ megőrzése és átadása. DS kettős hélix/spirál: Két komplementer DS szál Watson-rick-modell szerint alkotott térszerkezete. DS-replikáció: A DS mindkét szálának megduplázódása, amely során egy DS kettős spirálból létrejön kettő, az eredetivel azonos DS kettős spirál. Transzkripció: Atírás (DS->RS) amely során a DS-függő RS polimeráz a rendelkezésére álló nukleozid 5 -trifoszfátokból RS-t hoz létre. Fontosabb lépései: iniciáció, elongáció és termináció. Transzláció: Fehérje bioszintézis (RS->Fehérje), amely során a riboszóma az RS alapján, a rendelkezésre álló (és megfelelő aminosavat hordozó) trs-ek segítségével megszintetizálja az adott fehérjét.
2 Mutáció: Az eredetihez képesti elváltozás a DS-ben (más vagy hiányzó nukleotid(ok)) Riboszóma: A fehérjeszintézist = transzlációt végző ribozim, mely 2 rrs és több fehérjéből áll. Ribozim: Egy bizonyos enzimatikus feladatot ellátó (egy bizonyos reakciót katalizáló) RS. Enzim: Egy bizonyos enzimatikus feladatot ellátó (bizonyos reakciót katalizáló) fehérje. mrs: hírvivő RS: átmeneti adathordozóként szolgál (DS -> mrs -> Fehérje) rrs: riboszomális RS: a riboszóma fő alkotóeleme, a katalitikusan aktív része. trs: átvivő RS: Antikodont és annak megfelelő aminosavat (ill. kötőhelyét) tartalmazó RS A genetikai kód: Kodon: ukleotid-hármas a DS/RS-en, mely egy-egy aminosavat kódol Antikodon: ukleotid-hármas a trs-en, mely reverz-komplementje a kodonnak (tehát Watson- rick párosítással illeszkedik a kodonhoz transzláció közben) Gén: Az öröklődő DS egy fehérjét kódoló része. Genom: A gének összesége (egy egyedben/fajban), pl. a humán (emberi) genom. Exon: Egy gén/mrs azon része(i), mely(ek) tényleges fehérjeszekvenciát kódól(nak) Intron: Egy gén/mrs azon része(i), mely(ek) nem kódolnak fehérjeszekvenciát, és az RS érés során (transzkripció és transzláció között) kivágódnak, pre-mrs -> m-rs. Restrikciós endonukleáz: DS-hasító enzim, mely csak egy meghatározott szekvencia egy meghatározott pontján hasítja a DS-t. alindrom szekvencia: DS szekvencia, mely megegyezik a reverz-komplementjével, pl. AATT, GGAT, stb. Antiszensz oligonukleotid: A kódoló DS szálhoz kapcsolódó oligonukleotid, amely speciális szakaszhoz kötődve gátolhatja a DS átíródását (transzkipciót). R: olimerase-hain-reaction: polimeráz-láncreakció, egy eljárás a sejten-kívüli (in vitro) DS sokszorosítására. (templát DS + primer + polimeráz + + nukleotidok(monomerek) + hőmérsékletváltakozás = sokszorozódás)
3 A nukleinsavkémia koronázatlan királyai: Francis arry James Dewey ompton rick Watson Maurice ugh Frederick Wilkins Friedrich Miescher német orvos-kémikus 1869-ban felfedezi és izolálja a DS-t. Lord Alexander R. Todd (angol biokémikus) 1957 obel-díj A nukleotidok és a nukleotid koenzimek felfedezéséért 1962 obel-díj a DS molekuláris szerkezetének felismeréséért Luis Federico Leloir (argentín biokkémikus) 1970 obel-díj a cukor nukleotidok felfedezéséért és a szénhidrátok bioszintézise kapcsán elért eredményeiért
4 A nukleinsavkémia koronázatlan királyai, kémiai és orvosi obel-díjak: Stanford Moore és William. Stein amerikai biokémikusok 1980 aul Berg Walter Gilbert rekombináns-ds Frederick Sanger A nukleinsavak szekvenálásáért 1972 obel-díj a ribonukleáz aktív centrumának katalitikus aktivitása és kémiai szerkezete közötti kapcsolat feltárásáért Aaron Klug (angol kémikus ) 1982 obel-díj a kristálygráfiai elektronmikroszkóp kifejlesztéséért illetve a bilológiai szempontból fontos nukleinsavfehérjekomplexek szerkezetfelderítéséért
5 Sir James W. Black Gertrude B. Elion George. itchings 1988 obel-díj a purin alapú kemoterápiás gyógyszerek kifejlesztéséért Sidney Altman és Thomas R. ech Amerikai/kanadai és amerikai kémikus 1989 obel-díj az RS katalitikus tulajdonságainak felfedezéséért. Kary B. Mullis Michael Smith 1993 obel-díj olimeráz Irányított láncreakció (R) mutagenezis
6 UKLEISAVAK - dezoxiribonukleinsavak (DS) - ribonukleinsavak (RS) memo: nucleus = sejtmag lyan molekulák, amelyek az átörökítendő információ tárolására, annak átírására (transzkripció) és átfordítására (transzláció) alkalmasak, aminek eredményeként a sejt összes fehérjéje megszintetizálódik. (Alkalmasak továbbá reakciók katalízisére is.) Kémiai építőelemek: nukleotidok és nukleozidok 4' 5' 3' 2' heterociklusos bázis β--glikozidos kötés 1' egy nukleotid hidrolízis heterociklusos bázis: purin vagy pirimidin ötszénatomos monoszacharid: D-ribóz vagy 2-dezoxi-D-ribóz foszfátion
7 146 bázispár 8 histon fehérje és ezt is - hidak tartják össze. A nukleoszóma komplexet stab. a 1 linker fehérje A supercoiling 15000* kondenzációt tesz lehetővé mindig jobb menetes, antiparallel, Z-DS az egészet a -hidak tartják egyben Eukarióta sejtek génjében van nemkódoló rész; intronok. (rokarióta sejtekben tipikusan nincs intron.) Az intron a pre-mrs-be átíródik, majd az RS érés során az kivágódik.
8 Foszforsavészterek hidrolízise: 2 Q Q= adenozin-5'-monof oszf át Q= dezoxiadenozin-5'-monof oszf át 2 ukleinsav (polinukleotid) nukleáz ukleotid (monomer) nukleotidáz enyhe degradáció 1 a, 25 cc. 3, 180 Q= Q= Q A -glikozidkötés hidrolízise: adenozin dezoxiadenozin ukleozid (glikozid) purin nukleozid foszforiláz* + ukleotidbázis + pentóz (nucleobase) * Ez a foszforiláz az valójában egy hidroláz
9 A cukorrész: D-ribóz D-arabinóz D-xilóz D-lixóz memo: pirán furán tetrahidro-2 -pirán tetrahidrofurán iklusos félacetál képződése, avagy hogyan rajzoljuk a furanózokat: A nyílt láncú D-fruktóz különbözö konformációi nyílt láncú D-ribóz nyílt láncú D-ribóz 2 1 ukleozidokban mindig 5 tagú (furanóz) gyűrű formájában van a cukor jelen β-d-ribofuranóz α-d-ribof uranóz 2 1
10 memo.: eterociklusos szénvegyületek: két heteroatomos hattagú gyűrűk (Bruckner. III/1.) Aromás vegyületek: em aromás származékok memo: gyenge bázisok: a piperazin 10%-os vizes oldatának p-ja
11 A nukleinsav építőelemek; a heterociklus: irimidinszármazékok Az uracil keto-enol tautomer egyensúlyi formái: memo: csak a laktim-laktám vagy a dilaktám forma jöhet szóba, az -glikozid kötés miatt.
12 A nukleinsav építőelemek; a heterociklus: urinszármazékok 2 6-amino-purin adenin A guanin keto-enol tautomer egyensúlyi formái: 2 2-amino-6-hidroxi-purin guanin Melyik tautomer forma a stabilabb?
13 em-rs és -DS alkotó purinszármazékok: A purin degradációs út: áz:= urin nukleozid foszforiláz AM nukleotidáz GM Adenozin dezamináz áz purinvázas alkaloidok: di- és trimetil xantinok:
14 ukleotidok: A nukleozidok foszforsavészterei 2 Q= Q= Q adenozin-5'-monofoszf át dezoxiadenozin-5'-monofoszf át ukleozidok: A megfelelő purinés pirimidinbázisok -glikozidjai Q Q= Q= 2 adenozin dezoxiadenozin
15 2 2 adenozin RS építőelem adenozin 9-(β-D-ribofuranozil)-adenin op= 235 o 2 2 adenozid - - adenozin-5'-foszfát 5'-AM - - adenozin-3'-foszfát 3'-AM dezoxiadenozin 2 2 DS építőelem dezoxiadenozin 9-(2'-dezoxi-β-D-ribofuranozil)-adenin op= 190 o 2 2 dezoxiadenozid - - dezoxiadenozin-5'-foszfát 5'-dAM - - dezoxiadenozin-3'-foszfát 3'-dAM
16 guanozin 2 2 RS építőelem guanozin 9-(β-D-ribof uranozil)-guanin op= 240 o guanozid guanozin-5'-foszfát 5'-GM - DS építőelem - guanozin-3'-foszfát 3'-GM dezoxiguanozin 2 dezoxiguanozin 9-(2'-dezoxi-β-D-ribofuranozil)-guanin 2 dezoxiguanozid dezoxiguanozin-5'-foszfát 5'-dGM - - dezoxiguanozin-3'-foszfát 3'-dGM
17 2 citidin 2 RS építőelem citidin 3-(β-D-ribof uranozil)-citozin op= 230 o citidinf oszfátok citidin-5'-foszfát 5'-M - DS építőelem - citidin-3'-f oszf át 3'-M dozoxicitidin 2 2 dezoxicitidin 3-(2'-dezoxi-β-D-ribofuranozil)-citozin dezoxicitidinfoszf átok dezoxicitidin-5'-foszfát 5'-dM - - dezoxicitidin-3'-f oszfát 3'-dM
18 uridinn RS építőelem uridin 3-(β-D-ribofuranozil)-uracil op= 165 o uridinnfoszfátok - - uridin-5'-foszfát 5'-UM - DS építőelem - uridin-3'-foszfát 3'-UM timidin 3 3 timidin 3-(2'-dezoxi-β-D-ribofuranozil)-timin op= 183 o timidinf oszfátok timidin-5'-foszfát 5'-TM - - timidin-3'-f oszfát 3'-TM
19 A DS kémiai szerkezete 2 citidin 5' 3' foszforsavdiészter típusú, nem-eléágazó, lineáris polimer, amit az 5 3 irányba írunk: 5 -A-T-G--3 guanozin Az RS kémiai szerkezete 5' 3' 3 2 timidin 5 5' 3' adenozin 2 5' 3' 3
20 is G is amino-laktám forma T dilaktám, míg az A amino (aromás) forma ribóz citozin ribóz amino-laktám-f orma guanin amino-laktám-f orma ukleotidok belső arányai a DS-ben; a hargaff-szabály (E. hargaff, 1940s): Σ(pur.)/Σ(pir.) (G+A)/(+T) 1 és A/T 1 és G/ 1 memo: (G+)/(A+T) változik (DS stabilitás) - A bázispárok miatt a DS két szála komplementer jellegű, - az intermolekuláris -hidak jelentősége nagy, - a cukor-foszforsav diészter gerinc teljesen konzervatív, míg a heterociklusok permutálódnak, - a heterociklusok pontos szekvenciája hordozza az információt. A kettős hélix (double hélix) 1953 Francis arry James Dewey ompton rick Watson
21 A DS térszerkezete: jobbmenetes kettős hélix, körülbelül 10 nukleotidpárral hélix menetenként. A spirálokat -hidak tartják össze. Az adenint és a timint 2, míg a guanint és a citozint 3- híd köti össze. Ezt a téralkatot először James Watson and Francis rick becsülték (határozták) meg helyesen 1953-ban. citozin 2,8 Â guanin timin 2,8 Â adenin 3,0 Â 3,0 Â ribóz citozin ribóz amino-laktám-f orma guanin amino-laktám-f orma
22 Mutáció I: ormális és abnormális bázispárok Rib guanin laktám tautomerje STABILABB Rib citozin amino-latkám f orma Replikáció #1 Replikáció #2 -G- -szülő gyerek -G- -- -G- -- unoka 3 mutáció Rib guanin laktim tautomerje LABILIS Rib timin dilaktámf orma -G*- -T- memo: ugyanúgy megvan a 3. -híd is, ám míg a normál esetben (felső) a purin bázis a 3. - hídban az akceptor, addig a mutációra vezető esetben ugyanitt a -híd donor szerepét tölti be. A két tautomer eltérő -híd mintázatú, s ezért eltérő partnerrel (pirimidin bázissal) képez W párt. -G- -- -G- -- -G- -- -G- -- -G- -- -A- -T-
23 Mutáció II: a kémiai reagensek indukálta mutációk Salétromossav a 2 + l magyarázat: mutáció indukált mutáció: memo: ugyanúgy megvan a 2. -híd, ám míg a normál esetben (alsó) a purin bázis a 2. -hídban donnor, addig a mutációra vezető esetben (felső eset) az akceptor szerepét tölti be. A két tautomer eltérő -híd mintázatú, s ezért eltérő partnerrel (pirimidin bázissal) képez W párt. -A- -T- -A- -T- -A- -A- -T- -Tszülő gyerek unoka -*- -- -A- -T- -A- -T- -G- -- -A- -T- -A- -T-
24 em-klasszikus DS szerkezetek: triplex DS: háromszálú DS quadruplex DS: négyszálú DS. pl. telomerek (kromoszómavégek) 4xG: négy guanidin helyezkedik el egy síkban, egy kation + 4x 2 hidrogénhíd (a purinváz 7-es -jével is) stabilizálja a szerkezetet.
25 A DS térszerkezete: A leggyakoribb forma a B-DS, amely jobbmenetes, a két szál antiparallel elhelyezkedésű 3 nagyárok kisárok 5 A G G G T 5 3 memo: Az A olyan mint a B-forma, csak tömörebb.
26 jobbmenetes hélix jobbmenetes hélix Az A-DS hélix tömzsibb és rövidebb, mint a B-DS, a főtengelyhez képest a bázispárok síkja döntött ( képest 19 o ). R -3' a sík felett -3' endo balmenetes hélix Az Z-DS hélix karcsúbb, főtengelyhez képest a bázispárok síkja döntött ( képest 9 o ). Az B-DS hélixben a főtengelyhez képest a bázispárok síkja merőleges ( képest 1 o ). R -2' a sík felett -2' endo
27 A DS hőstabilitása tétel: A DS T m pontja nő a G frakció növekedésével; T m1 < T m2 ha G 1 /total<g 2 /total! memo: mivel a G-ben 3- míg az AT-párban csak 2 -híd van bázispáronként. kérdés: mennyi a T m pont ha G = 0,4? válasz: T m 340K (ha c(al =0)) kérdés: mennyi a T m pont ha G = 0,4, de teszünk mellé al? válasz:t m 360K (ha c(al =150 mmol)) kérdés: miért nő a T m pont ugyanolyan G frakció mellett akkor, ha magasabb az oldat só koncentrációja? válasz: a DS felszíni negatív töltései - kompenzálódnak. Tm (K) ribóz citozin oxo-f orma guanin oxo-f orma 0 al 150mM al Lineáris (0 al) Lineáris (150mM al) ribóz 3 ribóz timin oxo-f orma adenin ribóz DS termostabilitás y = 39,7x R 2 = 0,996 y = 39,7x R 2 = 0,996 0,3 0,4 0,5 0,6 0,7 0,8 G- frakció megjegyzés: - Minnél több a belső -híd a DS 2 szála között az annál stabilabb dimert képez. (Fehérjék esetében ez nem igaz, ott a belső -hidakkal nem nő lineárisan a fehérje termostabilitása!) - A DS T m (60-80 o ) pontja lényegesen magasabb mint a testhőmérsékletünk, és jelentősen magasabb mint a legtöbb fehérjénkké! Atkins de aula 118
28 DS és RS hidrolízisének részletei: 1) Savas hidrolízis l. depurinálás (A v. G) memo: az RS és a DS kb. egyformán hidrolízál savban kérdés: a ribóz félacetálja savban felnyílik-e?
29 2) Lúgos hidrolízis (az RS lúgos hidrolízise): eredmény: lánchasadás memo: ezért az RS kevésbé, míg a DS jobban ellenáll a lúgos hidrolízisnek memo: azért van DS és nem csak RS(?), mert az előbbi jobban ellenáll a lúgos hidrolízisnek, azaz stabilabb!
30 DS szilárdfázisú szintézise: egyszerű észter kötés(ek) kialakítása, azaz ezek egyszerű S reakciók foszfor centrumon. Védőcsoportok I: a bázisok védelme permanens csoportokkal él a primer aminok védelme, avagy a nukleofil csoportok álcázása, hogy a majdani kapcsolásnál már csak a ribóz 5 legyen csupán az egyetlen u. A G Rib Rib 4 -benzoilezés Rib 6 -benzoilezés vagy 2 -izobutiril 3 4 -acetilezés Rib T 3 nem kell védeni Rib
31 Védőcsoportok II: a foszfodiészter védelme permanens csoporttal B cianoetilészter formában E B Mindkét típusú permanens védőcsoport típus (-benzoil vagy -acetil és a E) is eltávolítható: memo: a szintézis végén az összes állandó védőcsoportot vizes ammóniával kvantitatíve eltávolítható vizes 3 -val
32 Védőcsoport: az 5 - csoport ideiglenes védelme Dmtr Me Me (enyhén savas rendszer) B 2 l 2 + 3% l 3 - Me B narancs szín Me
33 Szilárd hordozó: G (controlled pore glass) kontrolált pórusú üveg -kémiailag inert -nem duzzad -amino funkcionalizált G Me Si ( 2 ) n 2 Me Linker : l. borostyánkősav 2 ( 2 ) n Me Si 3 / 2 hasító hely Me G 2
34 DS szintézis: -szilárdfázisú szintézis 3 -től 5 irányba a aruthers -módszer Dmtr B 1 memo: a bioszintézis iránya 5 -től 3 irányba 1. Dmtr hasítás (dimetoxi-tritil) ( 2 ) n Me Si Me G 2. Aktiválás és kapcsolás B 1 enyhe savas detritilezés (3% TA) ( 2 ) n Me Si Me G
35 2. Aktiválás és kapcsolás B 1 memo: a bioszintézis iránya 5 -től 3 irányba ( 2 ) n Me Si Me G Dmtr foszforamidit B 2 E Me + S (5' S reakciója) tetrazol (gyenge sav)
36 3. Lánczárás (az elreagálatlan 5 --t acetilezzük) 4. xidálás I 2 ( 2 vagy TF) iklus végén 4 -val: - minden permanens védőcsoport eltávolítása - gyantáról való lehasítás Legvégén: kromatográfiás tisztítás
37 Összefoglalás: oligonukleotidok laboratóriumi szintézisére Foszforamidit kapcsolási módszer DMTr B 3 R B 2 G B 1 DMTr R i r 2 tetrazol B 3 1. lépés Kapcsolás R R B 2 G B 1 B 1,B 2,B 3 : védett bázisok R: 2 2 β-cianoetil egy savra stabil, de bázisra érzékeny védõcsoport DMTr : tetrazol: G: "controlled pore glass" (porózus üveg) dimetoxitritil egy savra érzékeny védõcsoport
38 DMTr B 3 B 3 R B 2 R B 2 I 2 R B 1 A R B 1 2. lépés xidáció G 3. lépés Védõcsoport eltávolítása G 1., 2. és 3. lépés ismétlése 4 hasítás a szilárd hordozóról, a foszfát-észterek és a bázisok védõcsoportjainak egyidejû eltávolítása szintetikus uligonukleotid olimeráz láncreakció (R) egyszerű és hatékony módszer a DS-molekulák számának növelésére
39 Ízelítő a nukleotidok és nukleozidok laboratóriumi szintéziséből: 1) ilbert-johnson-nukleozid szintézisből -Bz: BSA: Si Si benzoilcsoport,-bisz(trimetilszilil)acetamid nukleofil - ill.-atomok szililezõ reagense
40 2) Ribozilaminhoz kapcsolás A reakció javasolt mechanizmusa: Bz 2 Bz Bz 2,3,5-tri--benzoil- -D-ribofuranózilamin + Michael addíció Et Et Et -etoxi--etoxikarbonil-akrilamid Rib Et gyûrûzáródás -Et Et Rib Et limináció -Et Rib Bz Bz benzoilcsoporttal védett uridin
41 l 3) Szubsztituált purinszármazékok továbbalakítása: 3 2 S 2 / i 2 S R R R adenozin R: β-d-ribofuranozil
42 4) Foszforilezés: dibenzil-foszfokloridáttal rvosi alkalmazások: S 6-merkapto-purin Gyerekeknél akut leukémia kezelésére 80%-os gyógyulás allopurinol köszvény kezelésére 2 l 2 2 dibenzil-foszfokloridát aciklovir erpes virus kezelésére 2 -atom hiányzik a ribózból
43 SZERKEZET A DS, RS építőelemei: bázisok, pentóz, foszfát (nukleozid nukleotid) Kétszálú DS szerkezete: Watson-rick párosítás em-klasszikus DS szerkezetek: triplex, quadruplex DS DS sokszorosítás: ÉLETTAI SZERESZTÁS a sejtben: replikáció A DS mint információhordozó: transzkripció (-> RS) transzláció (-> fehérje) RS fajták és funkciójuk a kémcsőben: szilárdfázisú DS szintézis R = DS másolás DS szekvenálás, leolvasás BIEERGETIKA AT / GT mint a sejt energiahordozója: elem akkumulátor
44 A DS replikációja A genetikai kód megkettőződése: A kettős hélix az egyik vége felől letekeredik, majd a templátok mentén a komplemnter szálak megszintetizálódnak.
45 DS polimeráz: 5 => 3 irányban szintetizálja az új láncot. Leading strand = vezető szál, folyamatos szálszintézis Lagging strand = sántikáló szál, darabonkénti szálszintézis, majd utólagos összekötés (DS ligáz)
46 Összefoglalás: oligonukleotidok laboratóriumi szintézisére Foszforamidit kapcsolási módszer DMTr B 3 R B 2 G B 1 DMTr R i r 2 tetrazol B 3 1. lépés Kapcsolás R R B 2 G B 1 B 1,B 2,B 3 : védett bázisok R: 2 2 β-cianoetil egy savra stabil, de bázisra érzékeny védõcsoport DMTr : tetrazol: G: "controlled pore glass" (porózus üveg) dimetoxitritil egy savra érzékeny védõcsoport
47 DMTr B 3 B 3 R B 2 R B 2 I 2 R B 1 A R B 1 2. lépés xidáció G 3. lépés Védõcsoport eltávolítása G 1., 2. és 3. lépés ismétlése 4 hasítás a szilárd hordozóról, a foszfát-észterek és a bázisok védõcsoportjainak egyidejû eltávolítása szintetikus uligonukleotid olimeráz láncreakció (R): ha van templát DS egyszerű és hatékony módszer a DS-molekulák számának növelésére
48 R: olymerase hain Reaction = olimeráz láncreakció egyszerű és hatékony módszer a DS-molekulák számának növelésére, (adott láncvégek primerek között) VIDE!
49 SZERKEZET A DS, RS építőelemei: bázisok, pentóz, foszfát (nukleozid nukleotid) Kétszálú DS szerkezete: Watson-rick párosítás em-klasszikus DS szerkezetek: triplex, quadruplex DS DS sokszorosítás: ÉLETTAI SZERESZTÁS a sejtben: replikáció A DS mint információhordozó: transzkripció (-> RS) transzláció (-> fehérje) RS fajták és funkciójuk a kémcsőben: szilárdfázisú DS szintézis R = DS másolás DS szekvenálás, leolvasás BIEERGETIKA AT / GT mint a sejt energiahordozója: elem akkumulátor
50 A DS mint információhordozó: A gének leolvasása: DS (transzlokáció és mrs érés) mrs 1. transzkripció átírás, másolás RS polimeráz (enzim) fehérje 2. transzláció fordítás, dekódolás riboszóma (ribozim)
51 1. Transzkripció: RS polimeráz iniciáció: promoter régió elongáció termináció: terminátor
52 Ribonukleinsav (RS) és fehérjeszintézis A genetikai kód áramlásának irány: transzkripció transzláció DS RS fehérje gén: olyan DS szegmens amely tartalmazza mindazon információk összességét amely az adott polipeptid vagy fehérje szintéziséhez szükséges. (pl egy egyszerű bacilus DS-e is legalább 3000 különböző enzimfehérjét kódol.) 1. lépés: a transzkripció: a hírvivő-rs (messenger-rs, mrs) szintézise A színdarab szereplői : RS- polimeráz: egy enzim amely széttekeri a DS kettős spirált romoter: a DS-nek az a része ahova az RS-polimeráz kötődik és ahol megkezdi a transzkripciót RS nukleotidok, mint építőelemek Terminátor: prokarióták azon DS része ami jezi a transzkripció végét Transzkripciós egység: Az a DS darab ami RS-é átíródik. Transzkripcós factorok: az eukarióta sejtek azon fehérjéi amelyek az RS-polimeráz kötését, illetve a transzkripció megkezdését elősegítik. Transzkripciós Iniciációs Komplex: A transzkripciós faktorok és a promoter régióhoz kapcsolódó RS-polimeráz II együttese. TATA Box: A DS promoter része
53 A hírvivő-rs (messenger-rs, mrs) szintézise: etc. DS A G Dezoxiribóz: G U G ribóz: RS polimeráz etc. DS A G U G G etc. láncszétválás komplementer RS etc. DS A G U G G etc. komplementer RS. Transzkripció a sejtmagban történik, a szintetizálódott RS-nek van fehérjét kódoló (exon: expressed sequence ) és nem-kódoló része (intron: intervening sequence.) Az intron a pre-mrs-be átíródik, majd az RS érés során az kivágódik. A kész m-rs elvándoról a citoplazmába ahol a fehérjeszintézis templátja lesz..
54 protein sequence DS: - nem kódoló részek - kódoló részek (gének) >>>>>> mrs: - nem kódoló részek (intron) - kódoló részek (exon) >>>>>>>>>> fehérje 1. transzkripció - mrs érés - 2. transzláció sejtmag - transzlokáció - citoplazma
55 RS fajták és funkciójuk: kódoló RS: mrs: hírvivő (angol: messenger) RS: DS-ből másolt RS, mely a genetikai információt hordozza, és ezt a riboszómához szállítja, ahol a rajta lévő információ alapján a fehérjék szintetizálódnak. árom egymás melletti bázis alkot egy-egy kodon-t, mely egy-egy aminosavat kódol. pre-mrs: éretlen mrs. Az érés során a nem-kódoló részek (intronok) kivágódnak, csak a kódoló részek (exonok) maradnak az érett mrs-ben. nem-kódoló RS: trs: transzfer RS: segít az mrs-en található kód (kodon) leolvasásában. Minden létező kodonhoz külön trs tartozik, mely a kodonnak megfelelő aminosavak hordozza, és a riboszómához szállítja, majd ott részt vesz a fehérjeszintézisben rrs: riboszomális RS: a riboszóma alkotoeleme, mely a fehérjeszintézis katalitikus centrumát alkotja. léteznek további nem-kódoló RS-ek is, mint például: sirs: (small interfering RA): gének kikapcsolásáért felelős rövid RS részek (a DS-hez kötődnek, és így meggátolják annak átíródását)
56 Az RS szerkezete: hairpin RS szerkezet Watson-rick párosítás, saját magával (az RS általában egyszálú) trs szerkezete E.coli rrs szerkezete, (kis alegység)
57 Szállító RS (transzfer RS, trs) feladata: hogy a megfelelő helyre eljuttassa az aminosavat aminosav akceptor kar antikodon hurok
58 Szállító RS (transzfer RS, trs) jellemzői: nukleotidból áll, -mindig a A- véghez kapcsolódik észterkötéssel az aminosav (pl. Tyr), -minden aminosavnak saját trs-e van, amelyen az annak az aminosavnak megfelelő antikodon található (egy vagy akár több trs is lehet/aminosav) - például: Met UA.tRS: antikodon (AU) AUG.mRS: kodon
59 A m-rs tripletjei a genetikai kód: egy aminosavhoz egynél több kodon (egynél több antikodonnal ellátott t-rs) tarozik: As. m-rs As. m-rs As. m-rs Ala GA is A Ser AG G AU AGU GG Ile AUA UA GU AU UG Arg AGA AUU U AGG Leu UA UU GA U Thr AA G UG A GG UU AG GU UUA AU Asn AA UUG Trp UGG AAU Lys AAA Tyr UA Asp GA AAG UAU GAU Met AUG Val GUA ys UG he UUU GUG UGU UU GU Gln AA ro A GUU AG Glu GAA G lánckezdő GAG U fmet AUG Gly GGA GG lánczárás UAA GGG UAG GGU UGA antikodon hurok S -formil-metionin (fmet)
60 Transzláció: Lefordítás fehérje nyelvre codon mrs anticodon trs aminosav fehérje
61 codon mrs anticodon trs aminosav fehérje
62 2. lépés: a transzláció a citoszólban a ribószóma által katalizált folyamat, a fehérjeszintézis. a ribószóma egy RS-fehérje komplex: két alegység: 30S és 50S, molekulaméret: MW= 2.6*10 6, funkció: 30S; köti az m-rs-t 50S; katalitikus aktivitás, fehérjét is tartalmaz a komplex. memo: nem a fehérje hanem az RS rész végzi a katalízist. Ezért a riboszóma nem enzim hanem ribozim! 50S
63 Transzláció (1 perc alatt kb.150 peptidkötés formálódik): 1. lépés: (itt kezdődjön a transzláció) mindig az AUG mrs triplet. 2. ide mindig az -For-Met aminosav kerül 3. szintézis irány -term.től a -term. felé 4. Lánczáró kodonok az mrs-en: UAA, UAG és UGA. ( a mondat végi pontot jelölik ) 5. a szintézis legvégén a For-csoportot egy enzim lehidrolizálja. 2 S 2 Lys For-Met trs Lys U U U trs For-Met m-rs U A A U G A A A G U A U U U G G A A G A
64 2 Lys 2 Val For-Met 2 trs Lys trs Val S A U trs For-Met U A U U U A U G A A A G U A U U U G G A A G A
65 Lys 2 Val 2 he For-Met 2 trs he S trs Val trs Lys A A A U U U A U A U G A A A G U A U U U G G A A G A
66 A ribozim katalizálta peptidszintézis elemi kémiai lépései: 2 2 riboszóma + tetraéderes intermedieren keresztül riboszóma trs peptidndbas. peptidndbas. R trs tetraéderes intermedier: A nukleofil addiciót segíti az 50S alegység 2486 adeninje: 1) Az adenin nemkötő elektronpárjának protonvonzása részlegesen deprotonálja az aminocsoportot, ezzel fokozva annak nukleofil jellegét. 2) A tertaéderes köztitermék elbomlását a proton visszaadása iniciálja, kialakítva így a peptidkötést. 2 trs R trs trs R 2 trs (Science 289; , 2000) R peptid
67 Transzláció áttekintése:
68 DS szekvenálás: A DS bázissorrendjének meghatározása első két szekvenálási módszer: Maxam-Gilbert módszer > a lánc (5 ) elejét jelöli ( 32 ) > 4-féle kémiai módszerrel bázisspecifikusan elhasítja a láncot > méret szerint elválaszt Walter Gilbert Frederick Sanger Sanger: didesoxy / láncterminációs módszer óbel díj 1980
69 Maxam Gilbert Method (Maxam, A., Gilbert, W.: AS, 1977, 74, 560.) Walter Gilbert obel-díj, ' 3' alkaline phosphatase polynucleotide kinase AT M e 2 S M l G A/G /T iperidine (leaves after modification site) AGE Autoradiography
70
71
72 DS szekvenálás: A DS bázissorrendjének meghatározása első két szekvenálási módszer: Maxam-Gilbert módszer > a lánc (5 ) elejét jelöli ( 32 ) > 4-féle kémiai módszerrel bázisspecifikusan elhasítja a láncot > méret szerint elválaszt Walter Gilbert Frederick Sanger Sanger: didesoxy / láncterminációs módszer óbel díj 1980 > 3 -véghez párosuló primerel és DS polimerázzal lemásolja a DS-t > az egyik bázisból didesoxynukleotidot is ad hozzá -> korai láncterminációt okoz annál a bázisnál (4x) > méret szerint elválaszt
73 Dideoxy Method hain Termination Method (Sanger, F., et al: AS, 1977, 74, 5463.) 5' 3' rimer DA polymerase I (Klenow fragment) no nuclease activity dat 32 dt dgt dtt ddat dat dt 32 dgt dtt ddt dat dt dgt 32 dtt ddgt dat dt dgt dtt 32 ddtt AGE Autoradiography
74 A DS bázissorrendjének meghatározása: A lánczáró didezoxynukleotid módszer Láncterminációs eljárás: festékkel jelölt didezoxi-nukleotidok 2 linker 2',3'-didezoxicitozin-trifoszfát a 3'-hidroxil hiánya lánctörést okoz
75 linker: nukleotid festék festék: linker + fluoreszcens donorcsoport donor-akceptor fluoreszcens festék fluoreszcens akceptorcsoport
76
77 1996. új módszer: piroszekvenálás egyetlen immobilizált DS szál a templát DS polimeráz + egyenként adagoljuk a dezoxi-nukleotidokat a megfelelő nukleotid adagolásakor fényfelvillanás, aminek intenzitása arányos a beépített bázisok számával al yrén / Mostafa Ronaghi (Stockholm)
78 SZERKEZET A DS, RS építőelemei: bázisok, pentóz, foszfát (nukleozid nukleotid) Kétszálú DS szerkezete: Watson-rick párosítás em-klasszikus DS szerkezetek: triplex, quadruplex DS DS sokszorosítás: ÉLETTAI SZERESZTÁS a sejtben: replikáció A DS mint információhordozó: transzkripció (-> RS) transzláció (-> fehérje) RS fajták és funkciójuk a kémcsőben: szilárdfázisú DS szintézis R = DS másolás DS szekvenálás, leolvasás BIEERGETIKA AT / GT mint a sejt energiahordozója: elem akkumulátor
79 AT: adenozin -5 - trifoszfát foszforanhidrid foszforészter A szervezetben az ELEM AT és GT G~ 30.5 kj G~ mol kj mol -1 AT + 2 AD + i AT + 2 AM + i G = 30.5 kj/mol ( 7.3 kcal/mol) G = 45.6 kj/mol ( 10.9 kcal/mol)
80 AT és GT mint energiahordozók: elem / akkumulátor (újrafeltölthető!) felhasználás: dirkekt módon: kapcsolt reakció A sejtben igényelt anyagok szintézisében az endoterm ill. endergonikus reakciókhoz a kapcsolódó AT/GT hidrolízis adja a megfelelő hajtóerőt a reakció lefutásához. pl. transzláció (fehérjeszintézis) kreatin (energiaraktár az izomban) feltöltés: dirkekt módon: szubsztrát szintű foszforiláció: a metabolizmus (ételek, raktározott zsírsavak, egyéb anyagok lebontása) során az exoterm ill. exergonikus reakciókban történő AD/GD foszforilációja. indirekt módon: oxidatív foszforiláció a metabolizmus során redox-reakciókban redukált koenzimek keletkeznek: AD + és FAD 2 Ezek a redukált koenzimek elektrontranszporttal egybekötött, szabályozott regenerálása (oxidációja) során keletkezik AT.
81 Biomolekulák energetikája: Atkins & de aula 99 kérdés: mennyi glükóz elégetése teszi lehetővé egy 30 g össztömegű madár számára hogy 10 m magasra repüljön? tapasztalat: 1 mol szilárd glükóz 2 gázzá és folyékony vízzé való oxidációja 25 -on ~ 2828 kj szabadentalpia ( G) felszabadulást eredményez. válasz: az elvégezendő munka nagysága mgh= (30*10-3 kg)* (9,81*ms -2 )* (10 m) = 2,943 kg m 2 s -2 = 2,943 J mivel 1 mol glükóz G ~ 2, J munka végzéséhez elegendő, 2,943 J munka elvégzéséhez 2,943 / 2, mol glükózra van szükség, ami 1,04 µmol cukrot jelent. Mivel a glükóz M W -je ~180g mol -1 ezért ez hozzávetőlegesen (180 gmol -1 * 1,04*10-6 mol) = 0,19 mg kérdés: a koncentráló emberi agy ~25 J energiát igényel másodpercenként. Mennyi cukor (glükóz) elégetése szükséges ehhez óránként? tapasztalat: 1 mol glükóz oxidációja 25 -on ~ 2828 kj szabadentalpia ( G) felszabadulását eredményezi. válasz: az elvégezendő munka nagysága óránként = (25 Js -1 )* (3,6*10 3 s) = J = 90 kj mivel 1 mol glükóz G ~ 2, kj munka végzéséhez elegendő, 90 kj munka elvégzéséhez 90 / 2, mol glükózra van szükség, ami 32 mmol glükózt jelent. Mivel a glükóz M W -je ~180g mol -1 ezért ez hozzávetőlegesen (180 * 32*10-3 g ) = 5,7 g/óra Tehát az emberi agy naponta ~ 24 * 5,7g ~140g glükózt igényel.
82 A napi g glükóz többsége AT-vé alakul és így hasznosul a sejtekben. Aerob körülmények között 1mol glükóz mintegy 38 mol AT eredményez. mivel M w (AT)/ M w (glükóz) 507/180 = 2,82 ezért 2,82 * 38 * 160g 17,1 kg AT Ténylegesen egy 70 kg-os ember napi AT fogyasztása ~ 145 kg (mivel nem csak szénhidrátot, de zsírt és fehérjét is fogyasztunk!) Ám a szervezetben egyszerre kb. 51 g össz AT áll rendelkezésre, ami a teljes szükséglet (51 g /1, g) kb. 0,035% -a. Ez az tartalékolt AT mennyiség tehát kb. (24* 3600s) * (3, ) ~ 30 s-ra elegendő mindössze! Tehát az ember AT szükséglete ~ 100g / perc (aktív mozgás esetén 500g /perc) AD/AT ciklus (a foszforiltranszfer) A kémiai reakció: AT 4 (aq) + 2 AD 2 (aq) (aq) G~ 30 kj mol -1 A biokémiai rész ciklus: ½ 2 2 AD AT 4 + G
83 A teljes biokémiai ciklus: 2 G +2 2 AD + + AD + FAD 2 FAD elektronátvitel AD + (ikotinamid-adenin-dinukleotid) ½ 2 2 AD AT 4 foszforilátvitel + G FAD (Flavin-adenin-dinukleotid)
84 éhány fontosabb foszfátvegyület foszfátcsoport(jai) hidrolízisének G- értékei 37 o -on: memo: foszfoenol-piruvát G~ 62 kj mol -1 AT AD G~ 31 kj mol -1 AD AM G~ 28 kj mol -1 AM G~ 14 kj mol -1 -D-(+)-glükopiranóz-1-f oszf át -D-(+)-glükopiranóz-6-foszfát glükóz-1-foszfát G~ 21 kj mol -1 glükóz-6-foszfát G~ 14 kj mol -1 fruktóz-6-foszfát G~ 16 kj mol D-(+)-fruktofuranóz-6-foszfát kérdés: mit takar az AT G~ 31 kj mol -1? A hidrolízis exergonikus G< 0 és éppen 31 kj mol -1 energiát ad más csatolt, esetleg endergonikus reakciók lefolytatásához. Ezért hívjuk a megfelelő savanhidrid kötést nagyenergiájú kötésnek. 2 2 memo: vegyük észre hogy az AT középen helyezkedik el, ezért lehet foszfát donor és akceptor is.
85 AT 4 (aq) + 2 AD 2 (aq) (aq) tény: az AT G~ 31 kj mol -1 valamint a ~ 20 kj mol -1 és S~ +34 JK -1 mol -1 memo: mivel G = T S T S~ 310 K *34 JK -1 mol -1 ~ +11 kj mol -1 ) memo: az 1 mol víz a hidrát burok része mivel a reakció nem vákuumban megy. Innen a formális mólszám növekedés (1-ből 2-ő), emiatt van az entrópia növekedés, avagy a komplexitás csökkenése is. A G értéke ( 31 kj mol -1 ) ezért is ilyen kedvező. Az AT hidrolízise felhasználható olyan csatolt endergonikus reakciókhoz amelyek G nem nagyobb mint +31 kj mol -1. pl. a peptidkötés szintézise erősen endergonikus: G~ +17 kj mol -1 memo: az 1 mol víz a hidrát burok része mivel a reakció nem vákuumban megy. Innen a nagy entrópia csökkenés (2-ből 1), a komplexitás növekedés. G ezért is ilyen kedvezőtlen. memo: nem csak az entalpiaváltozás, de az entrópia csökkenés (komplexitás növekedése) is jelentős! kérdés: hogy mehet végbe a reakció 37 o -on? válasz: AT csatolt a reakció. memo: a csatolt rendszer értelmében a két reakció össze van kapcsolva! (a a két reakció elkülönítve (2 edényben) megy végbe, vagy ha csak úgy összeöntjük a reagenseket akkor a folyamat nem fog végbemenni.)
86 megfigyelés: Itt nem részletezett okok miatt 1 peptidkötés kialakításához 3 AT szükséges. kérdés: hány gramm glükóz kell 1mol mioglobin bioszintéziséhez, ha az 153 aminosabvól épül fel? válasz: 153*3 = 459 AT szükséges. 1 mol glükóz 38 AT eredményez, tehát 459/38~ 12 mol glükóz szükséges. tehát: (12*180g)~ 2,2kg cukor kell 1 mol (16,7 kda) fehérje szintéziséhez (~16,7 kg)
87
88 ow to safely store genetic material: cable reels in the cell nucleus... Legend: The nucleosome ucleosomes are cable reels for genetic material. In the cell s nucleus, the genetic material (DA) is organized in different chromosomes and protectively packaged. In this storage packing, the DA is wound around nucleosomes, just as a cable on a reel. Each nucleosome consists of four pairs of proteins called histones. Apart from their role as cable reels, nucleosomes are also involved in gene regulation as they prevent DA from being read at wrong positions.
89 I am not giving away the original data! A copy is good enough... Legend: RA polymerase RA polymerase is essential for each cell. This protein reads the genetic code from the genetic material in the cell nucleus and copies it onto so-called mra molecules. These copies are then shipped to the ribosomes where they serve as blueprints for proteins. Thus, the precious original always stays in the vault of the nucleus, and only copies are
90 DA is long where does a gene begin and how to find it? Legend: The TATA-box binding protein (TB) in yellow The repetition of the amino acids threonine (T) and alanine (A) T-A-T-A marks the beginning of a TATA-box binding protein (TB) recognizes this specific genetic start sequence and allows correct RA polymerase. Without TB, genes could not be copied to mra and would, hence, not be read of TB is too long, it causes some of the most severe neurodegenerative diseases
Nukleinsavak. Szerkezet, szintézis, funkció
 Nukleinsavak Szerkezet, szintézis, funkció Nukleinsavak, nukleotidok, nukleozidok 1869-ben Miescher a sejtmagból egy savas természetű, lúgban oldódó foszfortartalmú anyagot izolált, amit később, eredetére
Nukleinsavak Szerkezet, szintézis, funkció Nukleinsavak, nukleotidok, nukleozidok 1869-ben Miescher a sejtmagból egy savas természetű, lúgban oldódó foszfortartalmú anyagot izolált, amit később, eredetére
CHO H H H OH H OH OH H CH2OH HC OH HC OH HC OH CH 2
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A nukleinsavkémia koronázatlan királyai, kémiai és orvosi Nobel-díjak:
 A nukleinsavkémia koronázatlan királyai, kémiai és orvosi obel-díjak: Francis arry James Dewey ompton rick Watson Maurice ugh Frederick Wilkins 1962 DS molekuláris szerkezetének felismeréséért aul Berg
A nukleinsavkémia koronázatlan királyai, kémiai és orvosi obel-díjak: Francis arry James Dewey ompton rick Watson Maurice ugh Frederick Wilkins 1962 DS molekuláris szerkezetének felismeréséért aul Berg
CHO H H H OH H OH OH H CH2OH CHO OH H HC OH HC OH HC OH CH 2 OH
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895) 1970: FM Insitute
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895) 1970: FM Insitute
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa. Gergely Pál 2009
 FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa Gergely Pál 2009 Fehérjeszintézis és poszttranszlációs módosítások A kódszótár A riboszóma szerkezete A fehérjeszintézis (transzláció)
FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa Gergely Pál 2009 Fehérjeszintézis és poszttranszlációs módosítások A kódszótár A riboszóma szerkezete A fehérjeszintézis (transzláció)
4. Előadás. Nukleozidok, nukleotidok, nukleinsavak
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895), izolálás 1970: FM
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense nuclein Friedrich Miescher (Svájc, 1844-1895), izolálás 1970: FM
FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa. Bay Péter
 FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa Bay Péter Fehérjeszintézis és poszttranszlációs módosítások A kódszótár A riboszóma szerkezete A fehérjeszintézis (transzláció)
FEHÉRJESZINTÉZIS: a transzláció mechanizmusa és a polipeptidlánc további sorsa Bay Péter Fehérjeszintézis és poszttranszlációs módosítások A kódszótár A riboszóma szerkezete A fehérjeszintézis (transzláció)
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
A replikáció mechanizmusa
 Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
Az öröklődés molekuláris alapjai A DNS megkettőződése, a replikáció Szerk.: Vizkievicz András A DNS-molekula az élőlények örökítő anyaga, kódolt formában tartalmazza mindazon információkat, amelyek a sejt,
,:/ " \ OH OH OH - 6 - / \ O / H / H HO-CH, O, CH CH - OH ,\ / "CH - ~(H CH,-OH \OH. ,-\ ce/luló z 5zer.~ezere
 - 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
- 6 - o / \ \ o / \ / \ () /,-\ ce/luló z 5zer.~ezere " C=,1 -- J - 1 - - ---,:/ " - -,,\ / " - ~( / \ J,-\ ribóz: a) r.yílt 12"('.1, b) gyürus íormája ~.. ~ en;én'. fu5 héli'(ef1e~: egy menete - 7-5.
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete
 Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
Peptid- és fehérjék másodlagos-, harmadlagos- és negyedleges szerkezete Polipeptidek térszerkezete Tipikus (rendezett) konformerek em tipikus (rendezetlen) konformerek Periodikus vagy homokonformerek Aperiodikus
CzB 2010. Élettan: a sejt
 CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék. elrendeződés, rend, rendszer, periodikus ismétlődés
 Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
A géntechnológia genetikai alapjai (I./3.)
 Az I./2. rész (Gének és funkciójuk) rövid összefoglalója A gének a DNS információt hordozó szakaszai, melyekben a 4 betű (ATCG) néhány ezerszer, vagy százezerszer ismétlődik. A gének önálló programcsomagként
Az I./2. rész (Gének és funkciójuk) rövid összefoglalója A gének a DNS információt hordozó szakaszai, melyekben a 4 betű (ATCG) néhány ezerszer, vagy százezerszer ismétlődik. A gének önálló programcsomagként
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
A nukleinsavkémiai kisszótár: aminoacil-trns szintetáz: adott aminosavat a megfelelő trns-hez kapcsoló enzim DNS: dezoxiribonukleinsav, DNA <ang.
 1 A nukleinsavkémiai kisszótár: aminoacil-trs szintetáz: adott aminosavat a megfelelő trs-hez kapcsoló enzim DS: dezoxiribonukleinsav, DA : olyan nukleotidegységekből felépülő nukleinsavak gyűjtőneve,
1 A nukleinsavkémiai kisszótár: aminoacil-trs szintetáz: adott aminosavat a megfelelő trs-hez kapcsoló enzim DS: dezoxiribonukleinsav, DA : olyan nukleotidegységekből felépülő nukleinsavak gyűjtőneve,
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
Mária. A pirimidin-nukleotidok. nukleotidok anyagcseréje
 Prof.. Sasvári Mária A pirimidin-nukleotidok nukleotidok anyagcseréje 1 A nukleobázisok szerkezete Nitrogéntartalmú, heterociklusos vegyületek; szubsztituált purin- és pirimidin-származékok purin Adenin
Prof.. Sasvári Mária A pirimidin-nukleotidok nukleotidok anyagcseréje 1 A nukleobázisok szerkezete Nitrogéntartalmú, heterociklusos vegyületek; szubsztituált purin- és pirimidin-származékok purin Adenin
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
DNS, RNS, Fehérjék. makromolekulák biofizikája. Biológiai makromolekulák. A makromolekulák TÖMEG szerinti mennyisége a sejtben NAGY
 makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
makromolekulák biofizikája DNS, RNS, Fehérjék Kellermayer Miklós Tér Méret, alak, lokális és globális szerkezet Idő Fluktuációk, szerkezetváltozások, gombolyodás Kölcsönhatások Belső és külső kölcsöhatások,
BIOLÓGIA VERSENY 10. osztály 2016. február 20.
 BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
BIOLÓGIA VERSENY 10. osztály 2016. február 20. Kód Elérhető pontszám: 100 Elért pontszám: I. Definíció (2x1 = 2 pont): a) Mikroszkopikus méretű szilárd részecskék aktív bekebelezése b) Molekula, a sejt
Transzláció. Leolvasás - fehérjeszintézis
 Transzláció Leolvasás - fehérjeszintézis Fehérjeszintézis DNS mrns Transzkripció Transzláció Polipeptid A trns - aminosav kapcsolódás 1 A KEZDETEK ELŐTT Az enzim aktiválja az aminosavat azáltal, hogy egy
Transzláció Leolvasás - fehérjeszintézis Fehérjeszintézis DNS mrns Transzkripció Transzláció Polipeptid A trns - aminosav kapcsolódás 1 A KEZDETEK ELŐTT Az enzim aktiválja az aminosavat azáltal, hogy egy
A TRANSZLÁCIÓ Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak?
 A TRANSZLÁCIÓ Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak? mrns, trns, riboszómák felfedezése A GENETIKAI KÓD 20 AS és csak 4 bázis, a kódolás hogy lehetséges?
A TRANSZLÁCIÓ Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak? mrns, trns, riboszómák felfedezése A GENETIKAI KÓD 20 AS és csak 4 bázis, a kódolás hogy lehetséges?
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
A fehérjék szerkezete és az azt meghatározó kölcsönhatások
 A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
A fehérjék szerkezete és az azt meghatározó kölcsönhatások 1. A fehérjék szerepe az élõlényekben 2. A fehérjék szerkezetének szintjei 3. A fehérjék konformációs stabilitásáért felelõs kölcsönhatások 4.
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód)
 2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
Bioinformatika 2 5.. előad
 5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
5.. előad adás Prof. Poppe László BME Szerves Kémia és Technológia Tsz. Bioinformatika proteomika Előadás és gyakorlat 2009. 03. 21. Fehérje térszerkezet t megjelenítése A fehérjék meglehetősen összetett
Makromolekulák. Fehérjetekeredé. rjetekeredés. Biopolimer. Polimerek
 Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Biopolimerek Makromolekulá Makromolekulák. Fehé Fehérjetekeredé rjetekeredés. Osztódó sejt magorsófonala 2011. November 16. Huber Tamá Tamás Dohány levél epidermális sejtjének aktin hálózata Bakteriofágból
Új irányok a biomolekuláris felismerés detektálásában
 Magyar Kémiai Folyóirat - Előadások 133 Új irányok a biomolekuláris felismerés detektálásában GYURCSÁNYI E. Róbert a* Budapesti Műszaki és Gazdaságtudományi Egyetem, Általános és Analitikai Kémiai Tanszék,
Magyar Kémiai Folyóirat - Előadások 133 Új irányok a biomolekuláris felismerés detektálásában GYURCSÁNYI E. Róbert a* Budapesti Műszaki és Gazdaságtudományi Egyetem, Általános és Analitikai Kémiai Tanszék,
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze
 Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze László Éva Babeş-Bolyai Tudományegyetem, Kolozsvár A polimeráz láncreakció (PCR) napjaink molekuláris biológiai (genetikai) kutatásának nélkülözhetetlen
Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze László Éva Babeş-Bolyai Tudományegyetem, Kolozsvár A polimeráz láncreakció (PCR) napjaink molekuláris biológiai (genetikai) kutatásának nélkülözhetetlen
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
(11) Lajstromszám: E 008 532 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000832T2! (19) HU (11) Lajstromszám: E 008 32 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 783231 (22) A bejelentés
!HU00000832T2! (19) HU (11) Lajstromszám: E 008 32 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 783231 (22) A bejelentés
Tutorial 1 The Central Dogma of molecular biology
 oday DN RN rotein utorial 1 he entral Dogma of molecular biology Information flow in genetics:» ranscription» ranslation» Making sense of genomic information Information content in DN - Information content
oday DN RN rotein utorial 1 he entral Dogma of molecular biology Information flow in genetics:» ranscription» ranslation» Making sense of genomic information Information content in DN - Information content
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
A biológiai mozgás molekuláris mechanizmusai
 BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
BIOLÓGIAI MOZGÁSOK A biológiai mozgás molekuláris mechanizmusai Kollektív mozgás Szervezet mozgása ( Az évszázad ugrása ) Szerv mozgás BIOLÓGIAI MOZGÁSOK BIOLÓGIAI MOZGÁSOK Ritmusosan összehúzódó szívizomsejt
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
TRANSZLÁCIÓ és fehérje transzport Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak?
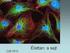 TRANSZLÁCIÓ és fehérje transzport Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak? mrns, trns, riboszómák felfedezése A GENETIKAI KÓD 20 AS és csak 4 bázis,
TRANSZLÁCIÓ és fehérje transzport Hogyan lesz a DNS-ben kódolt információból fehérje? A DNS felszínén az aminosavak sorba állnak? mrns, trns, riboszómák felfedezése A GENETIKAI KÓD 20 AS és csak 4 bázis,
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
(11) Lajstromszám: E 007 952 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
!HU00000792T2! (19) HU (11) Lajstromszám: E 007 92 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 04 73892 (22) A bejelentés napja:
Számolási feladatok. A = 17,5 % T = 17,5 % 32,5 % G és ugyanennyi C
 Számolási feladatok 1. Egy 200 bázispárt tartalmazó DNS szakaszról megállapították, hogy az egyik szálban 30 db A és 40 db T bázis, a másik szálban pedig 40 db C bázis van. Mekkora az egyes bázisok %-os
Számolási feladatok 1. Egy 200 bázispárt tartalmazó DNS szakaszról megállapították, hogy az egyik szálban 30 db A és 40 db T bázis, a másik szálban pedig 40 db C bázis van. Mekkora az egyes bázisok %-os
Ciklusok bűvöletében Katalizátorok a szintetikus kémia szolgálatában
 Ciklusok bűvöletében Katalizátorok a szintetikus kémia szolgálatában Novák Zoltán Eötvös oránd Tudományegyetem, Kémiai Intézet Szerves Kémiai Tanszék Alkímiai Ma, 2011. Március 17. Ciklusok - Katalízis
Ciklusok bűvöletében Katalizátorok a szintetikus kémia szolgálatában Novák Zoltán Eötvös oránd Tudományegyetem, Kémiai Intézet Szerves Kémiai Tanszék Alkímiai Ma, 2011. Március 17. Ciklusok - Katalízis
Szénhidrátok I. (Carbohydrates)
 sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban
 A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
A humán tripszinogén 4 expressziója és eloszlási mintázata az emberi agyban Doktori (PhD) értekezés Siklódi Erika Rozália Biológia Doktori Iskola Iskolavezető: Prof. Erdei Anna, tanszékvezető egyetemi
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód)
 2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
2. Sejtalkotó molekulák II. Az örökítőanyag (DNS, RNS replikáció), és az öröklődés molekuláris alapjai (gén, genetikai kód) 2.1 Nukleotidok, nukleinsavak Információátadás (örökítőanyag) Információs egység
Budapesti Műszaki és Gazdaságtudományi Egyetem Alkalmazott Biotechnológia és Élelmiszertudományi Tanszék
 Budapesti Műszaki és Gazdaságtudományi Egyetem Alkalmazott Biotechnológia és Élelmiszertudományi Tanszék PHD DOLGOZAT IN VITRO TRANSZLÁCIÓS VEKTOROK FEJLESZTÉSE ÉS ALKALMAZÁSA Készítette: Bardóczy Viola
Budapesti Műszaki és Gazdaságtudományi Egyetem Alkalmazott Biotechnológia és Élelmiszertudományi Tanszék PHD DOLGOZAT IN VITRO TRANSZLÁCIÓS VEKTOROK FEJLESZTÉSE ÉS ALKALMAZÁSA Készítette: Bardóczy Viola
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
CIÓ A GENETIKAI INFORMÁCI A DNS REPLIKÁCI
 A GENETIKAI INFORMÁCI CIÓ TÁROLÁSA ÉS S KIFEJEZŐDÉSE A DNS SZERKEZETE Két antiparalel (ellentétes lefutású) polinukleotid láncból álló kettős helix A két lánc egy képzeletbeli közös tengely körül van feltekeredve,
A GENETIKAI INFORMÁCI CIÓ TÁROLÁSA ÉS S KIFEJEZŐDÉSE A DNS SZERKEZETE Két antiparalel (ellentétes lefutású) polinukleotid láncból álló kettős helix A két lánc egy képzeletbeli közös tengely körül van feltekeredve,
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig
 A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
13. RNS szintézis és splicing
 13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
13. RNS szintézis és splicing 1 Visszatekintés: Az RNS típusai és szerkezete Hírvivő RNS = mrns (messenger RNA = mrna) : fehérjeszintézis pre-mrns érett mrns (intronok kivágódnak = splicing) Transzfer
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
A kémiai energia átalakítása a sejtekben
 A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
Fehérjeszerkezet, és tekeredés. Futó Kinga
 Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
Fehérjeszerkezet, és tekeredés Futó Kinga Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983 H 211861 N
TÉMAKÖRÖK. Ősi RNS világ BEVEZETÉS. RNS-ek tradicionális szerepben
 esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
esirna mirtron BEVEZETÉS TÉMAKÖRÖK Ősi RNS világ RNS-ek tradicionális szerepben bevezetés BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek BIOLÓGIAI MOLEKULÁK FEHÉRJÉK NUKLEINSAVAK DNS-ek RNS-ek
Genomadatbázisok Ld. Entrez Genome: Összes ismert genom, hierarchikus szervezésben (kromoszóma, térképek, gének, stb.)
 Genomika Új korszak, paradigmaváltás, forradalom: a teljes genomok ismeretében a biológia adatokban gazdag tudománnyá válik. Új kutatási módszerek, új szemlélet. Hajtóerõk: Genomszekvenálási projektek
Genomika Új korszak, paradigmaváltás, forradalom: a teljes genomok ismeretében a biológia adatokban gazdag tudománnyá válik. Új kutatási módszerek, új szemlélet. Hajtóerõk: Genomszekvenálási projektek
Kémiai Intézet Kémiai Laboratórium. F o t o n o k k e r e s z tt ü z é b e n a D N S
 Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
Szalay SzalayPéter Péter egyetemi egyetemi tanár tanár ELTE, ELTE,Kémiai Kémiai Intézet Intézet Elméleti ElméletiKémiai Kémiai Laboratórium Laboratórium F o t o n o k k e r e s z tt ü z é b e n a D N S
EMELT SZINTŰ ÍRÁSBELI VIZSGA
 ÉRETTSÉGI VIZSGA 2016. május 11. BIOLÓGIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 11. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA
ÉRETTSÉGI VIZSGA 2016. május 11. BIOLÓGIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2016. május 11. 8:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati EMBERI ERŐFORRÁSOK MINISZTÉRIUMA
1. Tömegszámváltozás nélkül milyen részecskéket bocsáthatnak ki magukból a bomlékony atommagok?
 A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának feladatlapja KÉMIÁBÓL I-II. kategória I. FELADATSOR Az I. feladatsorban húsz kérdés szerepel. Minden kérdés után
A 2004/2005. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) fordulójának feladatlapja KÉMIÁBÓL I-II. kategória I. FELADATSOR Az I. feladatsorban húsz kérdés szerepel. Minden kérdés után
A felvétel és a leadás közötti átalakító folyamatok összességét intermedier - köztes anyagcserének nevezzük.
 1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
H H 2. ábra: A diazometán kötésszerkezete σ-kötések: fekete; π z -kötés: kék, π y -kötés: piros sp-hibrid magányos elektronpár: rózsaszín
 3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
Nemzeti Akkreditáló Testület. SZŰKÍTETT RÉSZLETEZŐ OKIRAT (2) a NAT-1-1560/2012 nyilvántartási számú akkreditált státuszhoz
 Nemzeti Akkreditáló Testület SZŰKÍTETT RÉSZLETEZŐ OKIRAT (2) a NAT-1-1560/2012 nyilvántartási számú akkreditált státuszhoz A Bonafarm-Bábolna Takarmány Kft. Vizsgálólaboratórium (2942 Nagyigmánd, Burgert
Nemzeti Akkreditáló Testület SZŰKÍTETT RÉSZLETEZŐ OKIRAT (2) a NAT-1-1560/2012 nyilvántartási számú akkreditált státuszhoz A Bonafarm-Bábolna Takarmány Kft. Vizsgálólaboratórium (2942 Nagyigmánd, Burgert
Egy idegsejt működése
 2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
a III. kategória (11-12. évfolyam) feladatlapja
 2009/2010. tanév I. forduló a III. kategória (11-12. évfolyam) feladatlapja Versenyző neve:... évfolyama: Iskolája : Település : Felkészítő szaktanár neve:.. Megoldási útmutató A verseny feladatait nyolc
2009/2010. tanév I. forduló a III. kategória (11-12. évfolyam) feladatlapja Versenyző neve:... évfolyama: Iskolája : Település : Felkészítő szaktanár neve:.. Megoldási útmutató A verseny feladatait nyolc
Purin nukleotidok bontása
 Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
Dr. Sasvári MáriaM Purin nukleotidok bontása 24 1 Purin nukleotidok bontása AMP B r -p 5 nukleotidáz GMP P i adenozin (6-amino) ADA 2 adenozin deamináz 3 B r guanozin P i inozin (6-oxo) P i PP P i purin
Dr. Ottó Szabolcs Országos Onkológiai Intézet
 Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001. Részjelentés: 200. November 0.-2004.
Nemzeti Kutatási és Fejlesztési Program 1. Főirány: Életminőség javítása Nemzeti Onkológiai Kutatás-Fejlesztési Konzorcium a daganatos halálozás csökkentésére 1/48/2001. Részjelentés: 200. November 0.-2004.
Szerk.: Vizkievicz András A DNS örökítő szerepét bizonyító kísérletek
 Az öröklődés molekuláris alapjai Szerk.: Vizkievicz András A DNS örökítő szerepét bizonyító kísérletek A DNS-nek addig nem szenteltek különösebb figyelmet, amíg biológiai kísérlettel ki nem mutatták, hogy
Az öröklődés molekuláris alapjai Szerk.: Vizkievicz András A DNS örökítő szerepét bizonyító kísérletek A DNS-nek addig nem szenteltek különösebb figyelmet, amíg biológiai kísérlettel ki nem mutatták, hogy
Géntechnológia és fehérjemérnökség
 Géntechnológia és fehérjemérnökség Szerkesztette: Nyitray László Alexa Anita (12. és 13. fejezet) Fodor Krisztián (3. és 9. fejezet) Garai Ágnes (4. és 5. fejezet) Glatz Gábor (6. és 7. fejezet) Radnai
Géntechnológia és fehérjemérnökség Szerkesztette: Nyitray László Alexa Anita (12. és 13. fejezet) Fodor Krisztián (3. és 9. fejezet) Garai Ágnes (4. és 5. fejezet) Glatz Gábor (6. és 7. fejezet) Radnai
INFORMATIKA EMELT SZINT%
 Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
Szövegszerkesztés, prezentáció, grafika, weblapkészítés 1. A fényképezés története Táblázatkezelés 2. Maradékos összeadás Adatbázis-kezelés 3. Érettségi Algoritmizálás, adatmodellezés 4. Fehérje Maximális
A 2009/2010. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) forduló KÉMIA I-II. KATEGÓRIA FELADATLAP
 Oktatási Hivatal Munkaidő: 300 perc Elérhető pontszám: 100 pont A 2009/2010. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) forduló A VERSENYZŐ ADATAI KÉMIA I-II. KATEGÓRIA FELADATLAP A
Oktatási Hivatal Munkaidő: 300 perc Elérhető pontszám: 100 pont A 2009/2010. tanévi Országos Középiskolai Tanulmányi Verseny első (iskolai) forduló A VERSENYZŐ ADATAI KÉMIA I-II. KATEGÓRIA FELADATLAP A
1. Az élő szervezetek felépítése és az életfolyamatok 17
 Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
Élődi Pál BIOKÉMIA vomo; Akadémiai Kiadó, Budapest 1980 Tartalom Bevezetés 1. Az élő szervezetek felépítése és az életfolyamatok 17 Mi jellemző az élőre? 17. Biogén elemek 20. Biomolekulák 23. A víz 26.
Nanotechnológia. Nukleinsavak. Készítette - Fehérvári Gábor
 Nanotechnológia Nukleinsavak Készítette - Fehérvári Gábor Bevezető A nukleinsavak az élő anyag alapvetően fontos komponensei. Meghatározó szerepet töltenek be az átöröklésben, a fehérjék szintézisében
Nanotechnológia Nukleinsavak Készítette - Fehérvári Gábor Bevezető A nukleinsavak az élő anyag alapvetően fontos komponensei. Meghatározó szerepet töltenek be az átöröklésben, a fehérjék szintézisében
TRANSZPORTFOLYAMATOK 1b. Fehérjék. 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS
 1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
1b. FEHÉRJÉK TRANSZPORTJA A MEMBRÁNONOKBA ÉS A SEJTSZERVECSKÉK BELSEJÉBE ÁLTALÁNOS DIA 1 Fő fehérje transzport útvonalak Egy tipikus emlős sejt közel 10,000 féle fehérjét tartalmaz (a test pedig összesen
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor)
 2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL
 SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2011/12. II. félév 1 Tartalomjegyzék 1.
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2011/12. II. félév 1 Tartalomjegyzék 1.
BIOTECHNOLÓGIÁK EGYÉB IPARÁGAKBAN. Pókselyemfehérjék előállítása dohányban és burgonyában
 BIOTECHNOLÓGIÁK EGYÉB IPARÁGAKBAN Pókselyemfehérjék előállítása dohányban és burgonyában Tárgyszavak: selyemfehérje; transzgénikus növény; szintetikus pókselyem; selyemfehérjegén. A Nephila clavipes pók
BIOTECHNOLÓGIÁK EGYÉB IPARÁGAKBAN Pókselyemfehérjék előállítása dohányban és burgonyában Tárgyszavak: selyemfehérje; transzgénikus növény; szintetikus pókselyem; selyemfehérjegén. A Nephila clavipes pók
Molekuláris terápiák
 Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
Molekuláris terápiák Aradi, János Balajthy, Zoltán Csősz, Éva Scholtz, Beáta Szatmári, István Tőzsér, József Varga, Tamás Szerkesztette Balajthy, Zoltán és Tőzsér, József, Debreceni Egyetem Molekuláris
Adatok: Δ k H (kj/mol) metán 74,4. butadién 110,0. szén-dioxid 393,5. víz 285,8
 Relay feladatok 1. 24,5 dm 3 25 C-os, standardállapotú metán butadién gázelegyet oxigénfeleslegben elégettünk (a keletkező vízgőz lecsapódott). A folyamat során 1716 kj hő szabadult fel. Mennyi volt a
Relay feladatok 1. 24,5 dm 3 25 C-os, standardállapotú metán butadién gázelegyet oxigénfeleslegben elégettünk (a keletkező vízgőz lecsapódott). A folyamat során 1716 kj hő szabadult fel. Mennyi volt a
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B
 SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET 2013/14. II. félév 1 Tartalomjegyzék 1. Tantárgyleírás,
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET 2013/14. II. félév 1 Tartalomjegyzék 1. Tantárgyleírás,
Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA
 Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA Idei gyorsjelentés http://eduline.hu/erettsegi_felveteli/2 015/7/16/Az_elmult_7_ev_legrosszab b_eredmenye_szulet_azozlb
Kémia emelt szintű érettségi írásbeli vizsga ELEMZÉS (BARANYA) ÉS AJÁNLÁS KÉSZÍTETTE: NAGY MÁRIA Idei gyorsjelentés http://eduline.hu/erettsegi_felveteli/2 015/7/16/Az_elmult_7_ev_legrosszab b_eredmenye_szulet_azozlb
NUKLEINSAVAK. DNS (DNA) /dezoxiribonukleinsav/ -sejtplazmában -peptid / fehérje szintézis vezérlése (messenger-, transfer-rns)
 UKLEISAVAK Első elkülönítés: Miescher 189. (gennyből) vízben és híg savban oldhatatlan, de lúgban oldódó, foszfortartalmú anyag Két típus: RS (RA) /ribonukleinsav/ DS (DA) /dezoxiribonukleinsav/ -sejtplazmában
UKLEISAVAK Első elkülönítés: Miescher 189. (gennyből) vízben és híg savban oldhatatlan, de lúgban oldódó, foszfortartalmú anyag Két típus: RS (RA) /ribonukleinsav/ DS (DA) /dezoxiribonukleinsav/ -sejtplazmában
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését!
 I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
Sipos Ferenc. Új PNS oligomerek és P-királis mononukleotidok szintézise és szerkezetvizsgálata. Doktori (Ph.D.) értekezés
 Sipos Ferenc Új PS oligomerek és P-királis mononukleotidok szintézise és szerkezetvizsgálata Doktori (Ph.D.) értekezés Témavezető: Sági Gyula, C.Sc. MTA Kémiai Kutatóközpont, Bioekuláris Kémiai Intézet
Sipos Ferenc Új PS oligomerek és P-királis mononukleotidok szintézise és szerkezetvizsgálata Doktori (Ph.D.) értekezés Témavezető: Sági Gyula, C.Sc. MTA Kémiai Kutatóközpont, Bioekuláris Kémiai Intézet
A gyakorlat elméleti háttere A DNS molekula a sejt információhordozója. A DNS nemzedékről nemzedékre megőrzi az élőlények genetikai örökségét.
 A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
Biológus MSc. Molekuláris biológiai alapismeretek
 Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Szén-dioxid semleges elektromos energia előállítása szerves szennyezőanyagokból mikrobiológiai üzemanyagcellákban
 Szén-dioxid semleges elektromos energia előállítása szerves szennyezőanyagokból mikrobiológiai üzemanyagcellákban Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Alkalmazott
Szén-dioxid semleges elektromos energia előállítása szerves szennyezőanyagokból mikrobiológiai üzemanyagcellákban Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Alkalmazott
RNS-ek. 1. Az ősi RNS Világ: - az élet hajnalán. 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek
 RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
RNS-ek RNS-ek 1. Az ősi RNS Világ: - az élet hajnalán 2. Egy már ismert RNS Világ: - a fehérjeszintézis ben résztvevő RNS-ek 3. Egy újonnan felfedezett RNS Világ: - szabályozó RNS-ek 4. Transzkripció Ősi
