AFLP módszer alkalmazása növényi minták azonosításához
|
|
|
- Marcell Vass
- 8 évvel ezelőtt
- Látták:
Átírás
1 AFLP módszer alkalmazása növényi minták azonosításához Zubor Ákos 1 Surányi Gyula 2 Prokisch József 1 Győri Zoltán 1 Borbély György 2 1 Debreceni Egyetem Agrártudományi Centrum, Mezőgazdaságtudományi Kar, Mezőgazdasági Termékfeldolgozás és Minősítés Tanszék, Debrecen 2 Debreceni Egyetem, Természettudományi Kar, Növénytani Tanszék, Debrecen ÖSSZEFOGLALÁS A DNS-polimorfizmus meghatározásának egyik lehetséges módja a PCR-technikával kombinált AFLP (Amplified Fragment Length Polymorphism)-módszer alkalmazása. A Debreceni Egyetem Természettudományi Karának Növénytani Tanszékén ben sikeresen bevezetett módszert a jóféle sáfrány (Crocus sativus L.) rokonsági körének vizsgálatához használtuk. A jóféle sáfrány évezredek óta termesztett növény, amely a világon a legdrágább fűszert adja. A növény steril, triploid, csak vegetatív úton szaporodik, magokat nem terem. Eredete ismeretlen, csak termesztési kultúrákban létezik, feltételezhetően egy másik faj mutációja, amelyet az ember szelektált, vagy több fajból létrehozott, létrejött hibrid. Rokonsági vizsgálatára a hagyományos módszerek csak korlátozott mértékben alkalmasak, ésszerűnek tűnt a molekuláris biológia nyújtotta lehetőségeket alkalmazni esetében. Munkánk eredménye volt a módszer bevezetése és sokrétű alkalmazásának megismerése mellett, hogy az irodalmi adatoknak megfelelően a C. sativushoz leginkább hasonlító genetikai mintázatot a C. cartwrightianus esetében tapasztaltunk. SUMMARY One possible method for the determination of DNApolymorphism is the PCR-based AFLP (Amplified Fragment Length Polymorphism). This method had been succesfully introduced to the Department of Botany at University of Debrecen in with the examination of hay saffron (Crocus sativus L.) and its allies. Hay saffron is grown as a spice for some thousand years producing the most expensive spice in the world. This plant is sterile, triploid reproduces only vegetatively with no fertile seeds. However its origin is unknown it exists only in cultivation and it is a mutated variety of another species or an artificial or natural hybrid. Usual methods for the systematic examination are restricted hence it seemed to be reasonable to apply molecular biological methods in its case. Results of this work include the introduction and many fold application of the method beside ensuring the consequences of science literature with determining the C. cartwrightianus to give the most similar genetical pattern to C. sativus. BEVEZETÉS Napjainkban a növény- és állatrendszertan, a populációbiológia, és az ökológia egyre részletesebben tárja fel az élőlények, társulások, életközösségek közötti hasonlóságot, vagy azokat a tulajdonságokat, amelyek mérhető, jól meghatározható különbséget jeleznek közöttük. Ennek a kutatási iránynak a fejlődéséhez az utóbbi időben a molekuláris biológia is egyre növekvő mértékben hozzájárul. Ez a tudományterület a fenotípusosan megjelenő, egyszerűbb eszközökkel meghatározható tulajdonságokhoz hozzáteszi a genotípus, a genetikai variabilitás vizsgálatát. A DNS a földi élőlények túlnyomó százalékánál, mint általános információhordozó szerepel, amely az adott fajra, egyedre nézve jellemző, egyedi. Ezen a makromolekulán bizonyos mintázatok szabályosan ismétlődnek. Ezeket a mintázatokat egyes, baktériumokból izolált, enzimek képesek felismerni, sőt adott ponton szét is hasítják. Az így kapott DNS szakaszok, fragmentumok száma és hossza jellemző az adott fajra, egyedre (1-2. ábra). 1. ábra: DNS- lánc kettős (EcoRI és MseI) restrikciós hellyel GAATTC TTAA CTTAAG AATT Figure 1: DNA chain with two (EcoRI and MseI) restriction sites 2. ábra: Kettősen emésztett DNS fragmentum 5 AATTC T G AAT5 Figure 2: Double digested DNA fragment Ha ezeket a nagyon kis koncentrációban, de annál nagyobb számban lévő fragmentumokat rendszerezni tudjuk és ennek értékelhető megjelenítését is megoldjuk, nagyon hasznos eszközt nyerünk az egyes élőlények faji, egyedi különbségeinek vagy hasonlóságainak kimutatására. Az értékelhető megjelenítés egyik legáltalánosabb módja, ha a DNS szakaszokat megsokszorozzuk, és az így nyert, nagyobb mennyiségű fragmentum keveréket gélelektroforézissel rendezzük. A DNS molekula megsokszorozását a 80-as évek közepén végezték el először mesterségesen. Az eljárást Polymerase Chain Reaction-nak (PCR), azaz polimeráz láncreakciónak nevezték el. Lényege, hogy a Thermophilus aquaticus nevű baktériumból izolált, hőstabil DNS-polimeráz enzim, a Taq megfelelő körülmények között egymás után többször is képes az adott DNS lánc szintézisére és az újonnan másolt DNS láncokat is tovább másolja, tehát minden
2 másolási ciklusban az adott DNS mennyiség láncreakció szerűen megkétszereződik. Ezzel a módszerrel másfél, két óra alatt a DNS mennyiség több milliószorosára is növekedhet. Az így kapott nagy koncentrációjú nukleinsavat agaróz gélen elválasztva az azonos hosszúságú fragmentumok egy helyre rendeződnek, így akár meg is számolhatjuk, hogy hányféle és milyen nagyságú szakasz keletkezett ban Zabeau és Vos (Key Gene, Hollandia) szabadalmaztatott, majd 1995-ben publikált egy olyan eljárást, amely megoldja azt a problémát, mely a PCR-rel történő DNS polimerizálás esetében fellép, azaz ahhoz, hogy egy adott DNS szakaszt megtöbbszörözzünk, legalább egy, kezdeti részének a bázissorrendjét ismernünk kell. Ez a szekvenciaismeret azért nagyon fontos, mert a DNSpolimeráz enzim csak akkor tudja elkezdeni a működését, ha rendelkezésére áll egy olyan, kevés bázisból álló, egyszálú DNS szakasz, oligonukleotid, amely már előzőleg hozzákötődött a másolni kívánt DNS-hez. Ezt az oligonukleotidot primernek nevezzük, mely a nevében is hordozza, hogy a folyamat beindítására szolgál. Ezt a természetben egy másik enzim szintetizálja rá a szétnyílt DNS lánc azon pontjára, ahonnan az adott szakasz szintézise kezdődni fog. A PCR esetében ezt az enzimet nem használjuk, hanem az előre elkészített (szintetizált) primert adjuk a DNS fragmentumokhoz. Ahhoz azonban, hogy tudjuk, milyen bázissorrendű primert vigyünk be a rendszerbe, feltétlenül ismernünk kell az adott eredeti DNS szakasz kezdeti sorrendjét, aminek komplenetereként a primer bekötődhet. Ha belegondolunk, hogy egy élőlény DNS állományának szétszabdalásakor akár több százezer fragmentum is keletkezhet, láthatjuk, hogy ennek kiderítése bármelyik kutatólabor teljes kapacitásának is több mint megterhelő lenne. Erre kínál megoldást az Amplified Fragment Length Polymorphism (AFLP) azaz felerősített fragmenthossz polimorfizmus módszer (Vos et al., 1995). Ennek lényege, hogy mivel ismerjük a DNS-t felszabdaló, ún. restrikciós enzimek hasítási pontjainak bázissorrendjét, azt is tudjuk, hogy a fragmentumok végein milyen bázisok vannak. Ez csak néhány, 1-2, bázis ismeretét jelenti, de már elég ahhoz, hogy olyan adaptereket szintetizáljunk, amelyek a végekhez hozzá tudnak kötődni (3-4. ábra). 3. ábra: AFLP adapterek 5 CTCGTAGACTGCGTACC CATCTGACGCATGGTTAA5 EcoRI adpter 5 TACTCAGGACTCAT GAGTCCTGAGTAGCAG5 MseI adapter Figure 3: AFLP adapters 4. ábra: DNS fragmentum adapterekkel 5 CTCGTAGACTGCGTACCAATTC TTACTCAGGACTCAT CATCTGACGCATGGTTAAG AATGAGTCCTGAGTAGCAG5 Figure 4: DNA fragment with adapters Mivel a fragmentek végén lévő néhány tíz bázispárból álló adapterek teljes bázissorrendjét ismerjük, már csak olyan primereket kell hozzáadnunk, amelyek ezekhez az adapterekhez bekötődnek, és amelyeket már a Taq polimeráz is felismer (5. ábra). 5. ábra: AFLP primerek 5 GACTGCGTACCAATTCNNN EcoRI primer 5 GATGAGTCCTGAGTAANNN MseI primer Figure 5: AFLP primers Így szinte maradéktalanul fel tudjuk szaporatani az összes fragmentumot anélkül, hogy akár csak a kezdeti szekvenciájukat is ismernénk, a hasítási helyeket leszámítva (6. ábra). 6. ábra: Szintetizálódó DNS fragmentum primerekkel 5 CTCGTAGACTGCGTACCAATTC TTACTCAGGACTCAT3 NNNAATGAGTCCTGAGTAG5 5 GACTGCGTACCAATTCNNN 3 CATCTGACGCATGGTTAAG AATGAGTCCTGAGTAGCAG5 Figure 6: Synthesyzing DNA fragment with primers 2
3 Ezzel azonban még nem kapunk jól értékelhető mintázatokat, ugyanis a fragmentumok száma olyan nagy, hogy a gélelektroforézises képük még teljesen egybemosódik és értékelhetetlen. Az AFLP erre a problémára is megoldást kínál azzal, hogy a fragmentumok számát specifikusan, szelektíven lecsökkenti. Ezt több lépésben érhetjük el. Első lépésben a genomiális DNS-t kétféle restrikciós enzimmel, egy ritkán hasító és egy gyakori hasítási hellyel rendelkező enzimmel kezeljük. A ritkán hasító enzim (esetünkben az EcoRI) eleve csökkenti a szakaszok számát, míg a gyakran hasító enzim (MseI) biztosítja a megfelelő számú, ezáltal diverz és eléggé rövid fragmentum mennyiséget, amelyben előfordulnak az egyénre, fajra nézve egyedi DNS-szakaszok is. Az ily módon kezelt DNS tartalmazni fog olyan szakaszokat, amelyeknek mind a két végét ugyanaz az enzim alakította ki és olyat is, amelynek az egyik végét az egyik, a másikat a másik enzim. Második lépésben a primerek módosításával csökkentjük a felerősített szakaszok számát. A primerek úgy épülnek fel, hogy van egy központi, komplementer részük, amellyel az adott adapterhez be tudnak kötődni (az ábrákon vastaggal jelölve) és van egy olyan enzimspecifikus részük, amely a Taq polimeráz számára, mint felismerési szignál szerepel. Ezeken felül még van három olyan bázisuk, amely nem állandó, hanem bizonyos elképzeléseknek megfelelően módosítható (az ábrákon NNN-nel jelölve). Ennek a három, szelektív bázisnak a változtatásával egymástól némileg eltérő primereket hozhatunk létre. Az AFLP első PCR alkalmazásánál egy úgynevezett preszelektív amplifikációt végzünk, amikor csak az első ilyen bázis kiterjesztést határozzuk meg. Ekkor csak azok a fragmentumok fognak felerősödni, amelyeknél az adott enzim hasítási helye után közvetlenül a primeren lévő szelektív bázis komplementere található. A PCR további alkalmazásaikor már olyan primereket alkalmazunk, amelyeknél mind a három szelektív bázist megadjuk, így már csak azok a fragmentumok erősödnek fel, amelyeknél a hasítási hely után közvetlenül a primer kiterjesztésének megfelelő bázisok következnek. Ez a módszer olyan hatékonyan tud szelektálni a fragmentumok közül, hogy néhány darab primer-pár használatával szinte biztosan találunk olyan fragmentumokat, amelyek csak az adott fajra vagy egyedre jellemzőek. Ezen a módon egy olyan adatrendszert kapunk, ahol az egyes mintáknál szerepel, hogy az adott primer-párral hány egyedi, illetve egy másik mintával hány közös fragmentje volt. Ez alapján kiszámolható a minták relatív távolsága, amely aztán clusterként ábrázolva jól szemlélteti az egyes taxonok közti genetikai távolságot. A módszer nagy érzékenysége és általános működési elve miatt alkalmazható növények, állatok, prokarióták stb. fajok közötti és fajon belüli távolságainak felmérésére egyaránt ben a DE TTK Növénytani Tanszékén több növénycsoport vizsgálatával sikeresen bevezettük a módszert. Itt néhány mondatban ismertetjük az egyik ilyen vizsgálatunkat. ANYAG ÉS MÓDSZER Vizsgálatunkhoz sajnos nem tudtuk a Crocus sativus rokonsági körének teljes fajkészletét felsorakoztatni (MATHEW, 1982), de az összes vizsgált faj őszi virágzású és valamilyen szempontból (pl. mert egyes vidékeken szintén termesztették, mint szerényebb értékű fűszernövényt) kapcsolódik a jóféle sáfrányhoz. Munkánkhoz a következő fajokat reprezentáló mintákat használtuk fel: Crocus sativus L. 1 - a madridi Királyi Botanikus Kertből 1998 Crocus sativus L 2 - Priszter Szaniszló Crocus cartwrightianus Herbert - Priszter Szaniszló Crocus longiflorus Rafin. - Priszter Szaniszló Crocus goulimyi Turrill - Priszter Szaniszló Crocus goulimyi var. albus - Priszter Szaniszló Crocus serotinus ssp. Salzmannii Mathew - Priszter Szaniszló Crocus pulchellus Herbert - Priszter Szaniszló A minták 96%-os alkoholban, -20 o C-on tárolt levéldarabok voltak. DNS kivonás Az AFLP módszer alkalmazásához megfelelő tisztaságú DNS mintákra van szükség. A begyűjtött növények leveléből a Benner és mtsai (1995) által közölt kivonási módszerrel végeztük a DNS extrakciót. A restrikciós enzimekkel történő hasítás Az egyes Crocus fajokból származó DNS mintákat EcoRI, TruI, EcoRI+TruI, AluI illetve HindIII enzimekkel hasítottunk (Vos és mtsai, 1995; Reineke és Karlowsky, 2000). Itt kell megjegyezni, hogy az MseI és a TruI1 enzimek szekvencia felismerési és hasítási helyei megegyeznek, azaz izoschizomerek, egymást helyettesíthetik. Az enzimek és az emésztés során használt pufferek, reagensek a Fermentas cég készítményei voltak. Az adapterek ligálása A TruI, EcoRI, illetve EcoRI+TruI restrikciós enzimekkel emésztett DNS fragmentekhez kapcsoltuk a megfelelő adapter oligonukleotidokat (Reineke és Karlowsky, 2000; Briand és mtsai, 2000). A ligálás reagensei Fermentas készítmények. 3
4 A PCR reakcióelegy összeállítása A TruI és EcoRI adapterekkel ligált DNSfragmentek mennyiségének növelését a PCR alkalmazásával értük el (Briand és mtsai, 2000). A PCR reakcióban használt enzimek és pufferek Fermentas termékek. Az alkalmazott primerek nukleotid szekvenciái: EcoRI: 5 -GACTGCGTACCAATTCACG TruI: 5 -GATGAGTCCTGAGTAACAA A DNS minták elektroforézise és festése A restrikciós enzimekkel történő módosítások és a PCR-t követően kapott DNS fragmenteket akrilamid gélelektroforézissel választottuk el (Vos és mtsai, 1995; Briand és mtsai, 2000). A DNS mintázat meghatározásakor minden esetben 5% koncentrációjú poliakrilamid gélt használtunk, futtató pufferünk 1xTBE volt. A DNS fragmentek méretének meghatározásához a Fermentas cég HindIII emésztett lambda-dns molekulatömeg standardját használtuk (23,1; 9,4; 4,4; 2,3; 2,0 és 0,56 kbp). A molekulatömeg standard és különböző DNS minták gélrevitelekor is a Frementas 6x töménységű mintapufferét alkalmaztuk (végkoncentráció: 2x). Az általunk használt AFLP technika nem tartalmazott radioaktív jelölési lépéseket (pl. primerek), ezért a DNS fragmentek elválasztás utáni kimutatására minden esetben az ezüstfestés módszerét alkalmaztuk (Sammons et al., 1981; Schumacher et al., 1983), a kapott DNS mintázatokat szkennelés után jpeg formátumú képfájlokként rögzítettük. A PCR-technikán alapuló AFLP-módszerrel kapott eredmények statisztikai kiértékelése A különböző, összehasonlító populációkból származó DNS-minták az AFLP-PCR technika alkalmazása és a gélelektroforetikus elválasztás után az ezüsttel festett géleken egy-egy géloszlopként (lane) jelennek meg. Ezekben az oszlopokban a DNS fragmentek (band) számbavehetők. Ha egy adott csík jelen van, akkor 1-es értéket, ha nincs, akkor 0 értéket kap (Loh et al., 1999; Nybom és Kraft, 1995). Ha minden vizsgált objektumra (adott populáció DNS-mintázata) elvégezzük a fenti transzponációt, akkor egyértelműen képezhetjük az ún. Jaccardindexet (J): J = a/a+b+c, ahol a = két összehasonlítandó mintában, az azonos pozícióban lévő csíkok száma, b = csak az egyik összehasonlítandó mintára jellemző csíkok száma, c = csak a másik összehasonlítandó mintára jellemző csíkok száma. A Jaccard index, tehát annak a becsült valószínűsége, hogy két objektum megegyezik egy, legalább az egyiküket jellemző változóban (Podani, 1997). A J értéke 0 és 1 között mozoghat, tükrözve a két minta genetikai közelségét. A Jaccard-index értékeit hasonlósági mátrixokba rendeztük, amelyeket dendrogramokon is megjelenítettünk (1-6. táblázat). AZ EREDMÉNYEK ISMERTETÉSE ÉS ÉRTÉKELÉSE Eredményeink alapján megállapítható, hogy a két, különböző helyről származó C. sativus hasonlósági indexe volt a legnagyobb: J=0,9 (2. és 5. táblázat). A C. sativushoz a többi faj közül minden esetben a C. cartwrightianus állt a legközelebb. A 2. táblázatban két, eltérő helyről származó C. sativus szerepel. Ha ezek bármelyikét kiemeltük az adatsorunkból (3. és 4. táblázat), az előző eredmény akkor sem változott. Az 5. táblázat a két C. sativus és a C. cartwrightianus becsült hasonlóságát mutatja, melyből megállapítható, hogy a C. sativusok és az utóbbi közt lévő távolságok eltérése csekély, azaz majdnem ugyanolyan mértékben hasonlít a két eltérő élőhelyű C. sativus a C. cartwrightianusra. A 6. táblázat szintén azt a feltételezést erősíti, hogy a C. sativus legközelebbi rokona az itt szereplő öt faj közül a C. cartwrightianus. Eredményeinkből az is kitűnik, hogy a két eltérő helyről származó C. sativus hasonlósági értéke magasabb, mint az egy faj, két változatát adó C. goulimyi és C. goulimyi var. albus esetében, ám ez utóbbiak hasonlósága a restrikciós enzimtől függően magasabb, megegyezik vagy kisebb, mint a C. sativus C. cartwrightianus közötti hasonlóság (1., 3., 4. és 6. táblázat). Természetesen hangsúlyozni kell, hogy a fenti állításokat ugyan független, ismételt kísérletek alapján tesszük, de eddig csak egyetlen EcoRI/Tru1l primer párt próbáltunk ki PCR-os programjainkban; és itt kell megemlítenünk azt is, hogy a C. cartwrightianus csoport hiányzó taxonjaiból eddig nem sikerült mintát beszereznünk, ezért még ezen taxonok vizsgálatával is ki kívánjuk bővíteni kísérleti munkánkat. 4
5 1. táblázat EcoRI+Tru1I (kettős) emésztett Crocus DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája C.sativus1 C.cartwr. C.longifl. C.goulimyi C.gou.v.alb C.serotinus C.pulchell. C.sativus1 C.cartwr.,556 C.longifl.,364,433 C.goulimyi,375,235,324 C.gou.v.al,452,303,353,607 C.serotinu,406,303,353,324,353 C.pulchell,382,364,371,382,371,455 C.goulimyi 4 C.gou.v.alb 5 C.sativus1 1 C.cartwr. 2 C.longifl. 3 C.serotinus 6 C.pulchell. 7 Table 1: Double (EcoRI+Tru1I) digested Crocus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram 2. táblázat EcoRI emésztett Crocus DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája C.sativus2 C.sativus1 C.cartwr. C.longifl. Cgoulimyi C.cou.v.al C.serot. C.pulchell C.sativus2 C.sativus1,900 C.cartwr.,700,636 C.longifl.,286,267,308 C.goulimyi,333,417,250,231 C.gou.v.al.,250,231,400,250,625 C.serot.,353,412,294,278,500,333 C.pulchell,273,250,300,273,333,375,188 C.sativus2 1 C.sativus1 2 C.cartwr. 3 C.goulimyi 5 C.gou.v.alb 6 C.serotinus 7 C.pulchell. 8 C.longifl. 4 Table 2: EcoRI digested Crocus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram 5
6 3. táblázat EcoRI emésztett DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája a C. sativus 2 nélkül C.sativus1 C.cartw. C.longifl. C.goulimyi C.gou.v.al C. serot. C.pulchell C.sativus1 C.cartwr.,636 C.longifl.,267,308 C.goulimyi,417,250,231 C.gouv.al.,231,400,250,625 C.serot.,412,294,278,500,333 C.pulchell,250,300,273,333,375,188 C.sativus1 1 C.cartwr. 2 C.goulimyi 4 C.gou.v.al 5 C.seot. 6 C.pulchell 7 C.longifl. 3 Table 3: EcoRI digested Crocus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram without C. sativus 2 4. táblázat EcoRI emésztett DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája a C. sativus 1 nélkül C.cartwr. C.longifl C.goulimyi C.gou.v.al C.serot. C.pulchell C.sativus2 C.cartwr. C.longifl.,308 C.goulimyi,250,231 C.gou.v.al,400,250,625 C.serot.,294,278,500,333 C.pulchell,300,273,333,375,188 C.sativus2,700,286,333,250,353,273 C.cartwr. 1 C.sativus2 7 C.goulimyi 3 C.gou.v.al. 4 C.serot. 5 C.pulchell 6 C.longifl. 2 Table 4: EcoRI digested Crocus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram without C. sativus 1 6
7 5. táblázat EcoRI emésztett C.sativus 1, C.sativus 2 és C. cartwrightianus DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája C.cartwr. C.sativus2 C.sativus1 C.cartwr. C.sativus2,700 C.sativus1,636,900 C.sativus2 2 C.sativus1 3 C.cartwr. 1 Table 5: EcoRI digested Crocu sativus 1, C. sativus 2 and C. cartwrightianus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram 6. táblázat Tru1I emésztett DNS-mintázatok Jaccard-index alapján hasonlósági mátrixba rendezett és dendrogramon ábrázolt formája C.sativ.1 C.cartwr. C.longifl. C.goulimyi C.gou.v.al C.serot. C.pulchell C.sativus1 C.cartwr.,769 C.longifl.,235,265 C.goulimyi,237,200,457 C.gou.v.al,281,273,452,535 C.serot.,304,348,282,279,289 C.pulchell,222,250,488,500,465,268 C.sativus1 1 C.cartwr. 2 C.serot. 6 C.goulimyi 4 C.gou.v.al. 5 C.pulchell 7 C.longifl. 3 Table 6: Tru1I digested Crocus DNA patterns arranged in similarity matrix with Jaccard index and displayed on dendrogram IRODALOM Benner, M. S.-Braunstein, M. D.-Weisberg, M. U. (1995): Detection of DNA Polymorphisms Within the Genus Catteya (Orchidaceae). Plant Molecular Reporter, Briand, M.-Le Clers, V.-Grzebelus, D.-Senalik, D.-Simon, P. W. (2000): Modified Protocols for Rapid Carrot Genomic DNA Extraction and AFPL TM Analysis Using Silver Stain or Radioisotopes. Plant Molecular Biology Reporter, Loh, J. Ph.-Kiew, R.-Kee, A.-Gan, L. H.-Gan, Y. Y. (1999): Amplified Fragment Length Polymorphism (AFLP) Provides Molecular Markers for the Identification of Caladium bicolor Cultivars. Annals of Botany, Mathew, B. (1982): The Crocus. A Revision of the Genus Crocus (Iridaceae). B. T. Batsford Ltd., London Nybom, H.-Kraft, T. (1995): Application of NA fingerprinting to the taxonomy ofeuropean blackberry species. Electrophoresis, Podani J. (1997): Bevezetés a többváltozós biológiai adatfeltárás rejtelmeibe. Scientia Kiadó, Budapest Reineke, A.-Karlowsky, P. (2000): Simplified AFLP Protocol: Replacement of Primer Labeling by the Incorporation of α- Labeled Nucleotides during PCR. Biotechniques, Sammons, D. W.-Adams, L. P.-Nishazawa, E. E. (1981): Electrophoresis Schumacher, J.-Randles, J. W.-Reisner, D. (1983): Anal. Biochem Vos, P.-Hogers, R.-Bleeker, M.-Reijans, M.-van de Lee, Th.- Hornes, M.-Frijters, A.-Pot, J.-Peleman, J.-Kuiper, M.-Zabeau, M. (1995): AFLP: a new technique for DNA fingerprinting. Nucleid Acids Research
DNS-szekvencia meghatározás
 DNS-szekvencia meghatározás Gilbert 1980 (1958) Sanger 3-1 A DNS-polimerázok jellemzői 5'-3' polimeráz aktivitás 5'-3' exonukleáz 3'-5' exonukleáz aktivitás Az új szál szintéziséhez kell: templát DNS primer
DNS-szekvencia meghatározás Gilbert 1980 (1958) Sanger 3-1 A DNS-polimerázok jellemzői 5'-3' polimeráz aktivitás 5'-3' exonukleáz 3'-5' exonukleáz aktivitás Az új szál szintéziséhez kell: templát DNS primer
Engedélyszám: 18211-2/2011-EAHUF Verziószám: 1. 2460-06 Humángenetikai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén
 Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
Molekuláris biológiai eljárások alkalmazása a GMO analitikában és az élelmiszerbiztonság területén Dr. Dallmann Klára A molekuláris biológia célja az élőlények és sejtek működésének molekuláris szintű
A bioinformatika gyökerei
 A bioinformatika gyökerei 1944: Avery a transforming principle a DNS 1952: Hershey és Chase perdöntő bizonyíték: a bakteriofágok szaporodásakor csak a DNS jut be a sejtbe 1953: Watson és Crick a DNS szerkezete
A bioinformatika gyökerei 1944: Avery a transforming principle a DNS 1952: Hershey és Chase perdöntő bizonyíték: a bakteriofágok szaporodásakor csak a DNS jut be a sejtbe 1953: Watson és Crick a DNS szerkezete
ADATBÁNYÁSZAT I. ÉS OMICS
 Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére TÁMOP-4.1.1.C-13/1/KONV-2014-0001 ADATBÁNYÁSZAT
5. Molekuláris biológiai technikák
 5. Molekuláris biológiai technikák DNS szaporítás kémcsőben és élőben. Klónozás, PCR, cdna, RT-PCR, realtime-rt-pcr, Northern-, Southernblotting, génexpresszió, FISH 5. Molekuláris szintű biológiai technikák
5. Molekuláris biológiai technikák DNS szaporítás kémcsőben és élőben. Klónozás, PCR, cdna, RT-PCR, realtime-rt-pcr, Northern-, Southernblotting, génexpresszió, FISH 5. Molekuláris szintű biológiai technikák
Bakteriális identifikáció 16S rrns gén szekvencia alapján
 Bakteriális identifikáció 16S rrns gén szekvencia alapján MOHR ANITA SIPOS RITA, SZÁNTÓ-EGÉSZ RÉKA, MICSINAI ADRIENN 2100 Gödöllő, Szent-Györgyi Albert út 4. info@biomi.hu, www.biomi.hu TÖRZS AZONOSÍTÁS
Bakteriális identifikáció 16S rrns gén szekvencia alapján MOHR ANITA SIPOS RITA, SZÁNTÓ-EGÉSZ RÉKA, MICSINAI ADRIENN 2100 Gödöllő, Szent-Györgyi Albert út 4. info@biomi.hu, www.biomi.hu TÖRZS AZONOSÍTÁS
BALATONI NÁDASOK KLONÁLIS DIVERZITÁSÁNAK VIZSGÁLATA RAPD-PCR MÓDSZERREL
 Bot. Közlem. 94(1 2): 133 140, 2007. BALATONI NÁDASOK KLONÁLIS DIVERZITÁSÁNAK VIZSGÁLATA RAPD-PCR MÓDSZERREL LUKÁCS VIKTÓRIA 1, HERODEK SÁNDOR 1, MAJOR ÁGNES 2 1 MTA Balatoni Limnológiai Kutatóintézet,
Bot. Közlem. 94(1 2): 133 140, 2007. BALATONI NÁDASOK KLONÁLIS DIVERZITÁSÁNAK VIZSGÁLATA RAPD-PCR MÓDSZERREL LUKÁCS VIKTÓRIA 1, HERODEK SÁNDOR 1, MAJOR ÁGNES 2 1 MTA Balatoni Limnológiai Kutatóintézet,
Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 projekt
 Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 projekt ÁLLATGENETIKA Debreceni Egyetem Nyugat-magyarországi Egyetem Pannon Egyetem A projekt az Európai Unió támogatásával, az
Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 projekt ÁLLATGENETIKA Debreceni Egyetem Nyugat-magyarországi Egyetem Pannon Egyetem A projekt az Európai Unió támogatásával, az
Evolúcióbiológia. Biológus B.Sc tavaszi félév
 Evolúcióbiológia Biológus B.Sc. 2011. tavaszi félév A biológiában minden csak az evolúció fényében válik érthetővé Theodosius Dobzhansky : Nothing in biology makes sense except in the light of evolution.
Evolúcióbiológia Biológus B.Sc. 2011. tavaszi félév A biológiában minden csak az evolúció fényében válik érthetővé Theodosius Dobzhansky : Nothing in biology makes sense except in the light of evolution.
DNS-számítógép. Balló Gábor
 DNS-számítógép Balló Gábor Bevezetés A nukleinsavak az élő szervezetek egyik legfontosabb alkotórészei. Ezekben tárolódnak ugyanis az öröklődéshez, és a fehérjeszintézishez szükséges információk. Bár a
DNS-számítógép Balló Gábor Bevezetés A nukleinsavak az élő szervezetek egyik legfontosabb alkotórészei. Ezekben tárolódnak ugyanis az öröklődéshez, és a fehérjeszintézishez szükséges információk. Bár a
10. CSI. A molekuláris biológiai technikák alkalmazásai
 10. CSI. A molekuláris biológiai technikák alkalmazásai A DNS mint azonosító 3 milliárd bázispár az emberi DNS-ben (99.9%-ban azonos) 0.1%-nyi különbség elegendő az egyedek megkülönböztetéséhez Genetikai
10. CSI. A molekuláris biológiai technikák alkalmazásai A DNS mint azonosító 3 milliárd bázispár az emberi DNS-ben (99.9%-ban azonos) 0.1%-nyi különbség elegendő az egyedek megkülönböztetéséhez Genetikai
DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel
 DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel Gyakorlat helye: BIOMI Kft. Gödöllő, Szent-Györgyi A. u. 4. (Nemzeti Agrárkutatási és Innovációs Központ épülete volt
DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel Gyakorlat helye: BIOMI Kft. Gödöllő, Szent-Györgyi A. u. 4. (Nemzeti Agrárkutatási és Innovációs Központ épülete volt
Molekuláris biológiai módszerek alkalmazása a biológiai környezeti kármentesítésben
 Molekuláris biológiai módszerek alkalmazása a biológiai környezeti kármentesítésben Dr. Kovács Tamás, Kovács Árpád László Kármentesítés Aktuális Kérdései 2013 Budapest, 2013.03.21-22 Bioremediáció során
Molekuláris biológiai módszerek alkalmazása a biológiai környezeti kármentesítésben Dr. Kovács Tamás, Kovács Árpád László Kármentesítés Aktuális Kérdései 2013 Budapest, 2013.03.21-22 Bioremediáció során
A genetikai diverzitás vizsgálata sugárkezelt kukoricavonalakban és kapcsolata hibridjeik teljesítményével
 A genetikai diverzitás vizsgálata sugárkezelt kukoricavonalakban és kapcsolata hibridjeik teljesítményével Bódi Zoltán 1 Pepó Pál 1 Zubor Ákos 2 Tóth Szilárd 1 Prokisch József 2 Győri Zoltán 2 Debreceni
A genetikai diverzitás vizsgálata sugárkezelt kukoricavonalakban és kapcsolata hibridjeik teljesítményével Bódi Zoltán 1 Pepó Pál 1 Zubor Ákos 2 Tóth Szilárd 1 Prokisch József 2 Győri Zoltán 2 Debreceni
3. gyakorlat: nukleinsav-tisztítás, polimeráz láncreakció
 3. gyakorlat: nukleinsav-tisztítás, polimeráz láncreakció A vírus genetikai anyagának vizsgálata (direkt víruskimutatási módszer) biztosítja a legrészletesebb és legspecifikusabb információkat a kimutatott
3. gyakorlat: nukleinsav-tisztítás, polimeráz láncreakció A vírus genetikai anyagának vizsgálata (direkt víruskimutatási módszer) biztosítja a legrészletesebb és legspecifikusabb információkat a kimutatott
Az örökítőanyag. Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase
 SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
4.3. Mikrofluidikai csipek analitikai alkalmazásai
 367 4.3. Mikrofluidikai csipek analitikai alkalmazásai 4.3.1. DNS meghatározása A kettős szálú DNS példáján kiválóan demonstrálhatók a mikrofluidikai eszközökön (csip, lab-on-a-chip) elérhető gyors és
367 4.3. Mikrofluidikai csipek analitikai alkalmazásai 4.3.1. DNS meghatározása A kettős szálú DNS példáján kiválóan demonstrálhatók a mikrofluidikai eszközökön (csip, lab-on-a-chip) elérhető gyors és
5. Előadás Nukleinsavak kimutatása, szekvenálás
 5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
Fiatal kutatói beszámoló
 Talajbiológiai- és biokémiai osztály Fiatal kutatói beszámoló Gazdag Orsolya tudományos segédmunkatárs Témavezető: Dr. Ködöböcz László 2013.12.03. Témacím: Különböző gazdálkodási módok hatása a talaj baktérium-közösségeinek
Talajbiológiai- és biokémiai osztály Fiatal kutatói beszámoló Gazdag Orsolya tudományos segédmunkatárs Témavezető: Dr. Ködöböcz László 2013.12.03. Témacím: Különböző gazdálkodási módok hatása a talaj baktérium-közösségeinek
2011. január április 10. IPK Gatersleben (Németország) május 17. Kruppa Klaudia
 2011. január 10. 2011. április 10. IPK Gatersleben (Németország) Gatersleben (G-life) Country State District Town Administration Germany Saxony-Anhalt Salzlandkreis Seeland Basic statistics Area 16.00
2011. január 10. 2011. április 10. IPK Gatersleben (Németország) Gatersleben (G-life) Country State District Town Administration Germany Saxony-Anhalt Salzlandkreis Seeland Basic statistics Area 16.00
Algaközösségek ökológiai, morfológiai és genetikai diverzitásának összehasonlítása szentély jellegű és emberi használatnak kitett élőhelykomplexekben
 Algaközösségek ökológiai, morfológiai és genetikai diverzitásának összehasonlítása szentély jellegű és emberi használatnak kitett élőhelykomplexekben Duleba Mónika Környezettudományi Doktori Iskola I.
Algaközösségek ökológiai, morfológiai és genetikai diverzitásának összehasonlítása szentély jellegű és emberi használatnak kitett élőhelykomplexekben Duleba Mónika Környezettudományi Doktori Iskola I.
Genomika. Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel. DNS szekvenálási eljárások. DNS ujjlenyomat (VNTR)
 Genomika (A genom, génállomány vizsgálata) Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel DNS szekvenálási eljárások DNS ujjlenyomat (VNTR) DNS chipek statikus és dinamikus információk vizsgálata
Genomika (A genom, génállomány vizsgálata) Mutációk (SNP-k) és vizsgálatuk egyszerű módszerekkel DNS szekvenálási eljárások DNS ujjlenyomat (VNTR) DNS chipek statikus és dinamikus információk vizsgálata
SALMONELLA SSP. GYORS, MOLEKULÁRIS BIOLÓGIAI MÓDSZEREKKEL TÖRTÉNŐ DETEKTÁLÁSA
 SALMONELLA SSP. GYORS, MOLEKULÁRIS BIOLÓGIAI MÓDSZEREKKEL TÖRTÉNŐ DETEKTÁLÁSA Nyirő-Fekete B., Tabajdi-Bajza N., Kovácsné Kis É., Pocklán E., Zoller L., Micsinai A., Gasparikné Reichardt J. Hungalimentaria
SALMONELLA SSP. GYORS, MOLEKULÁRIS BIOLÓGIAI MÓDSZEREKKEL TÖRTÉNŐ DETEKTÁLÁSA Nyirő-Fekete B., Tabajdi-Bajza N., Kovácsné Kis É., Pocklán E., Zoller L., Micsinai A., Gasparikné Reichardt J. Hungalimentaria
GENOMIKA TÖBBFÉLE MAKROMOLEKULA VIZSGÁLATA EGYIDŐBEN
 GENOMIKA TÖBBFÉLE MAKROMOLEKULA VIZSGÁLATA EGYIDŐBEN Strukturális genomika Genomkönyvtárak DNS szekvenálás Genom programok Polimorfizmusok RFLP DNS könyvtár készítés humán genom 1. Emésztés RE-kal Emberi
GENOMIKA TÖBBFÉLE MAKROMOLEKULA VIZSGÁLATA EGYIDŐBEN Strukturális genomika Genomkönyvtárak DNS szekvenálás Genom programok Polimorfizmusok RFLP DNS könyvtár készítés humán genom 1. Emésztés RE-kal Emberi
Diagnosztikai célú molekuláris biológiai vizsgálatok
 Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
Diagnosztikai célú molekuláris biológiai vizsgálatok Dr. Patócs Attila, PhD MTA-SE Molekuláris Medicina Kutatócsoport, Semmelweis Egyetem II. sz. Belgyógyászati Klinika Laboratóriumi Medicina Intézet Genetikai
10. Genomika 2. Microarrayek és típusaik
 10. Genomika 2. 1. Microarray technikák és bioinformatikai vonatkozásaik Microarrayek és típusaik Korrelált génexpresszió mint a funkcionális genomika eszköze 2. Kombinált megközelítés a funkcionális genomikában
10. Genomika 2. 1. Microarray technikák és bioinformatikai vonatkozásaik Microarrayek és típusaik Korrelált génexpresszió mint a funkcionális genomika eszköze 2. Kombinált megközelítés a funkcionális genomikában
MIKROSZATELIT DNS- VIZSGÁLATOK A MOCSÁRI TEKNŐS NÉGY DUNÁNTÚLI ÁLLOMÁNYÁN
 MIKROSZATELIT DNS- VIZSGÁLATOK A MOCSÁRI TEKNŐS NÉGY DUNÁNTÚLI ÁLLOMÁNYÁN Molnár Tamás 1, Lanszki József 1, Magyary István 1, Jeney Zsigmond 2, Lehoczky István 2 1 Kaposvári Egyetem Állattudományi Kar,
MIKROSZATELIT DNS- VIZSGÁLATOK A MOCSÁRI TEKNŐS NÉGY DUNÁNTÚLI ÁLLOMÁNYÁN Molnár Tamás 1, Lanszki József 1, Magyary István 1, Jeney Zsigmond 2, Lehoczky István 2 1 Kaposvári Egyetem Állattudományi Kar,
Nagy Emese: Polimorfizmus és rokonsági körök vizsgálata kukoricában (Zea mays) Témavezetők: Cs. L. Marton G Gyulai
 Nagy Emese: Polimorfizmus és rokonsági körök vizsgálata kukoricában (Zea mays) Témavezetők: Cs. L. Marton G Gyulai BEVEZETÉS A molekuláris biológiai és genetikai módszerek gyors fejlődése egyre inkább
Nagy Emese: Polimorfizmus és rokonsági körök vizsgálata kukoricában (Zea mays) Témavezetők: Cs. L. Marton G Gyulai BEVEZETÉS A molekuláris biológiai és genetikai módszerek gyors fejlődése egyre inkább
ALMAFAJTÁK MOLEKULÁRIS ELKÜLÖNÍTÉSE ÉS
 Szent István Egyetem Gödöllő Növénytudományi Doktori Iskola Doktori Iskola vezetője: Dr. Heszky László Növénynemesítés genetikai és biotechnológiai módszerekkel Programvezető: Dr. Heszky László DOKTORI
Szent István Egyetem Gödöllő Növénytudományi Doktori Iskola Doktori Iskola vezetője: Dr. Heszky László Növénynemesítés genetikai és biotechnológiai módszerekkel Programvezető: Dr. Heszky László DOKTORI
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei)
 Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
Antiszenz hatás és RNS interferencia (a génexpresszió befolyásolásának régi és legújabb lehetőségei) Az antiszenz elv története Reverz transzkripció replikáció transzkripció transzláció DNS DNS RNS Fehérje
A Hardy-Weinberg egyensúly. 2. gyakorlat
 A Hardy-Weinberg egyensúly 2. gyakorlat A Hardy-Weinberg egyensúly feltételei: nincs szelekció nincs migráció nagy populációméret (nincs sodródás) nincs mutáció pánmixis van allélgyakoriság azonos hímekben
A Hardy-Weinberg egyensúly 2. gyakorlat A Hardy-Weinberg egyensúly feltételei: nincs szelekció nincs migráció nagy populációméret (nincs sodródás) nincs mutáció pánmixis van allélgyakoriság azonos hímekben
DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI VESZPRÉMI EGYETEM GEORGIKON MEZGAZDASÁGTUDOMÁNYI KAR KESZTHELY
 DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI VESZPRÉMI EGYETEM GEORGIKON MEZGAZDASÁGTUDOMÁNYI KAR KESZTHELY NÖVÉNYTERMESZTÉSI ÉS KERTÉSZETI TUDOMÁNYOK DOKTORI ISKOLA ALTERNARIA FAJOK ÖSSZEHASONLÍTÓ ELEMZÉSE KÉSZÍTETTE:
DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI VESZPRÉMI EGYETEM GEORGIKON MEZGAZDASÁGTUDOMÁNYI KAR KESZTHELY NÖVÉNYTERMESZTÉSI ÉS KERTÉSZETI TUDOMÁNYOK DOKTORI ISKOLA ALTERNARIA FAJOK ÖSSZEHASONLÍTÓ ELEMZÉSE KÉSZÍTETTE:
Genetikai panel kialakítása a hazai tejhasznú szarvasmarha állományok hasznos élettartamának növelésére
 Genetikai panel kialakítása a hazai tejhasznú szarvasmarha állományok hasznos élettartamának növelésére Dr. Czeglédi Levente Dr. Béri Béla Kutatás-fejlesztés támogatása a megújuló energiaforrások és agrár
Genetikai panel kialakítása a hazai tejhasznú szarvasmarha állományok hasznos élettartamának növelésére Dr. Czeglédi Levente Dr. Béri Béla Kutatás-fejlesztés támogatása a megújuló energiaforrások és agrár
Növényi minták GMO-tartalmának kvalitatív meghatározása
 Növényi minták GMO-tartalmának kvalitatív meghatározása Uri Csilla 1 Prokisch József 1 Sándor Erzsébet 2 Győri Zoltán 1 Debreceni Egyetem Agrártudományi Centrum, Mezőgazdaságtudományi Kar, 1 Élelmiszertudományi,
Növényi minták GMO-tartalmának kvalitatív meghatározása Uri Csilla 1 Prokisch József 1 Sándor Erzsébet 2 Győri Zoltán 1 Debreceni Egyetem Agrártudományi Centrum, Mezőgazdaságtudományi Kar, 1 Élelmiszertudományi,
A géntechnológiát megalapozó felfedezések
 2010. december BIOTECHNOLÓGIA Rova tvezető: Dr. Heszky László akadémikus A géntechnológia genetikai alapjai c. I. fejezet 1-5. részében azokat a tudományos eredményeket mutattuk be, melyek bizonyítják,
2010. december BIOTECHNOLÓGIA Rova tvezető: Dr. Heszky László akadémikus A géntechnológia genetikai alapjai c. I. fejezet 1-5. részében azokat a tudományos eredményeket mutattuk be, melyek bizonyítják,
12/4/2014. Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció. 1952 Hershey & Chase 1953!!!
 Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
Genetika 7-8 ea. DNS szerkezete, replikáció és a rekombináció 1859 1865 1869 1952 Hershey & Chase 1953!!! 1879 1903 1951 1950 1944 1928 1911 1 1. DNS szerkezete Mi az örökítő anyag? Friedrich Miescher
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
DI-, TETRA- ÉS HEXAPLOID TRITICUM FAJOK GENOMJAINAK ELEMZÉSE ÉS AZOK ÖSSZEHASONLÍTÁSA FLUORESZCENS IN SITU HIBRIDIZÁCIÓVAL
 Hagyomány és haladás a növénynemesítésben DI-, TETRA- ÉS HEXAPLOID TRITICUM FAJOK GENOMJAINAK ELEMZÉSE ÉS AZOK ÖSSZEHASONLÍTÁSA FLUORESZCENS IN SITU HIBRIDIZÁCIÓVAL VARGA MÓNIKA, MOLNÁR ISTVÁN ÉS KOVÁCS
Hagyomány és haladás a növénynemesítésben DI-, TETRA- ÉS HEXAPLOID TRITICUM FAJOK GENOMJAINAK ELEMZÉSE ÉS AZOK ÖSSZEHASONLÍTÁSA FLUORESZCENS IN SITU HIBRIDIZÁCIÓVAL VARGA MÓNIKA, MOLNÁR ISTVÁN ÉS KOVÁCS
Összehasonlító környezetmikrobiológiai. Böddi-szék vizében egy alga tömegprodukció idején
 Összehasonlító környezetmikrobiológiai vizsgálatok a Böddi-szék vizében egy alga tömegprodukció idején Czeibert Katalin Témavezető: Dr. Borsodi Andrea Eötvös Loránd Tudományegyetem, Mikrobiológiai Tanszék
Összehasonlító környezetmikrobiológiai vizsgálatok a Böddi-szék vizében egy alga tömegprodukció idején Czeibert Katalin Témavezető: Dr. Borsodi Andrea Eötvös Loránd Tudományegyetem, Mikrobiológiai Tanszék
7. A b-galaktozidáz indukciója Escherichia coliban
 7. A b-galaktozidáz INDUKCIÓJA ESCHERICHIA COLIBAN 7. A b-galaktozidáz indukciója Escherichia coliban dr. Bauer Pál 7.1. Az enzimindukció jelensége Az élõlények valamennyi génjének állandó és folyamatos
7. A b-galaktozidáz INDUKCIÓJA ESCHERICHIA COLIBAN 7. A b-galaktozidáz indukciója Escherichia coliban dr. Bauer Pál 7.1. Az enzimindukció jelensége Az élõlények valamennyi génjének állandó és folyamatos
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
Kettőnél több csoport vizsgálata. Makara B. Gábor
 Kettőnél több csoport vizsgálata Makara B. Gábor Három gyógytápszer elemzéséből az alábbi energia tartalom adatok származtak (kilokalória/adag egységben) Három gyógytápszer elemzésébô A B C 30 5 00 10
Kettőnél több csoport vizsgálata Makara B. Gábor Három gyógytápszer elemzéséből az alábbi energia tartalom adatok származtak (kilokalória/adag egységben) Három gyógytápszer elemzésébô A B C 30 5 00 10
NYÁR GENOTÍPUSOK AZONOSÍTÁSA DNS UJJLENYOMATUK ALAPJÁN
 1. évfolyam 1. szám 2 011 107 114 oldal NYÁR GENOTÍPUSOK AZONOSÍTÁSA DNS UJJLENYOMATUK ALAPJÁN Cseke Klára, Benke Attila és Borovics Attila Erdészeti Tudományos Intézet Kivonat Kutatásunk célja a nyár
1. évfolyam 1. szám 2 011 107 114 oldal NYÁR GENOTÍPUSOK AZONOSÍTÁSA DNS UJJLENYOMATUK ALAPJÁN Cseke Klára, Benke Attila és Borovics Attila Erdészeti Tudományos Intézet Kivonat Kutatásunk célja a nyár
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
3. HPV típusok meghatározása RFLP analízissel, típus-specifikus PCR módszerrel és blot assay módszerrel.
 OTKA zárójelentés 2007 Részletes összefoglaló Célkitűzések: 1. Human papillomavirusok (HPV) kimutatása colorectalis daganatok miatt eltávolított biopszia mintákból nukleinsav hybridizációs próbával. 2.
OTKA zárójelentés 2007 Részletes összefoglaló Célkitűzések: 1. Human papillomavirusok (HPV) kimutatása colorectalis daganatok miatt eltávolított biopszia mintákból nukleinsav hybridizációs próbával. 2.
DNS munka a gyakorlatban. 2012.10.12. Természetvédelmi genetika
 DNS munka a gyakorlatban 2012.10.12. Természetvédelmi genetika Munka fázisok DNS kivonás elektroforézis (fakultatív lépés) PCR Elektroforézis Szekvenálás Szekvencia elemzés faji azonosítás; variabilitás,
DNS munka a gyakorlatban 2012.10.12. Természetvédelmi genetika Munka fázisok DNS kivonás elektroforézis (fakultatív lépés) PCR Elektroforézis Szekvenálás Szekvencia elemzés faji azonosítás; variabilitás,
Mutáció detektáló módszerek
 Mutáció detektáló módszerek Molekuláris genetikai vizsgáló módszerek 2014.03.19. Bármilyen eltérés a referencia szekvenciától Lehet Egy bázispárnyi szubsztitúció, deléció, inzerció Kromoszóma deléció,
Mutáció detektáló módszerek Molekuláris genetikai vizsgáló módszerek 2014.03.19. Bármilyen eltérés a referencia szekvenciától Lehet Egy bázispárnyi szubsztitúció, deléció, inzerció Kromoszóma deléció,
DATURA STRAMONIUM ÉS DATURA ARBOREA DNS- ÉS TROPANOID MINTÁZATÁNAK NÉHÁNY JELLEMZÕJE
 Tájökológiai Lapok 3 (2): 275 280. (2005) 275 DATURA STRAMONIUM ÉS DATURA ARBOREA DNS- ÉS TROPANOID MINTÁZATÁNAK NÉHÁNY JELLEMZÕJE TÓVÖLGYI ZSUZSA 1,SZABÓ LÁSZLÓ GY. 2, STRANCZINGER SZILVIA 2 1 PTE ÁOK
Tájökológiai Lapok 3 (2): 275 280. (2005) 275 DATURA STRAMONIUM ÉS DATURA ARBOREA DNS- ÉS TROPANOID MINTÁZATÁNAK NÉHÁNY JELLEMZÕJE TÓVÖLGYI ZSUZSA 1,SZABÓ LÁSZLÓ GY. 2, STRANCZINGER SZILVIA 2 1 PTE ÁOK
Patogén mikroorganizmusok vizsgálata molekuláris biológiai módszerekkel
 Patogén mikroorganizmusok vizsgálata molekuláris biológiai módszerekkel Rohonczy Kata, Zoller Linda, Fodor Andrea, Tabajdiné, dr. Pintér Vera FoodMicro Kft. Célkitűzés Élelmiszerekben és takarmányokban
Patogén mikroorganizmusok vizsgálata molekuláris biológiai módszerekkel Rohonczy Kata, Zoller Linda, Fodor Andrea, Tabajdiné, dr. Pintér Vera FoodMicro Kft. Célkitűzés Élelmiszerekben és takarmányokban
Gyakorlati Forduló Fizika, Kémia, Biológia
 Gyakorlati Forduló Fizika, Kémia, Biológia Töltsd ki az alábbiakat! DIÁKOK NEVE: CSOPORT JELE: ORSZÁG: ALÁÍRÁSOK: Ennek a kísérletnek a célja a DNS kivonása csírázó búzából. Azután a kiadott mintában lévő
Gyakorlati Forduló Fizika, Kémia, Biológia Töltsd ki az alábbiakat! DIÁKOK NEVE: CSOPORT JELE: ORSZÁG: ALÁÍRÁSOK: Ennek a kísérletnek a célja a DNS kivonása csírázó búzából. Azután a kiadott mintában lévő
Animal welfare, etológia és tartástechnológia
 Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 424 A PROLAKTIN RECEPTOR GÉN HATÁSA A MANGALICÁK ALOMMÉRETÉRE Gajdócsi
Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 424 A PROLAKTIN RECEPTOR GÉN HATÁSA A MANGALICÁK ALOMMÉRETÉRE Gajdócsi
BEVEZETÉS CÉLKITŰZÉS
 BEVEZETÉS A molekuláris biológiai és genetikai módszerek gyors fejlődése egyre inkább tért hódít a növénynemesítés különböző területein, így a kukoricanemesítésben is. A növényi fenotípusos jellemzők és
BEVEZETÉS A molekuláris biológiai és genetikai módszerek gyors fejlődése egyre inkább tért hódít a növénynemesítés különböző területein, így a kukoricanemesítésben is. A növényi fenotípusos jellemzők és
Supporting Information
 Supporting Information Paired design of dcas9 as a systematic platform for the detection of featured nucleic acid sequences in pathogenic strains Yihao Zhang 1,2,8, Long Qian 4,8, Weijia Wei 1,3,7,8, Yu
Supporting Information Paired design of dcas9 as a systematic platform for the detection of featured nucleic acid sequences in pathogenic strains Yihao Zhang 1,2,8, Long Qian 4,8, Weijia Wei 1,3,7,8, Yu
Molekuláris markerek alkalmazása a szőlő magvatlanságának követésére és Rosa L. taxonok rokonsági viszonyainak vizsgálatára
 Doktori (PhD) értekezés Molekuláris markerek alkalmazása a szőlő magvatlanságának követésére és Rosa L. taxonok rokonsági viszonyainak vizsgálatára Deák Tamás Témavezető: Dr. Bisztray György Dénes, PhD
Doktori (PhD) értekezés Molekuláris markerek alkalmazása a szőlő magvatlanságának követésére és Rosa L. taxonok rokonsági viszonyainak vizsgálatára Deák Tamás Témavezető: Dr. Bisztray György Dénes, PhD
NANOTECHNOLOGIA 6. előadás
 NANOTECHNOLOGIA 6. előadás A plazmid: Ha meg akarjuk ismerni egy fehérje működését, akkor sokat kell belőle előállítanunk. Ezt akár úgy is megtehetjük, hogy a kívánt géndarabot egy baktérumba ültetjük
NANOTECHNOLOGIA 6. előadás A plazmid: Ha meg akarjuk ismerni egy fehérje működését, akkor sokat kell belőle előállítanunk. Ezt akár úgy is megtehetjük, hogy a kívánt géndarabot egy baktérumba ültetjük
(11) Lajstromszám: E 008 532 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU00000832T2! (19) HU (11) Lajstromszám: E 008 32 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 783231 (22) A bejelentés
!HU00000832T2! (19) HU (11) Lajstromszám: E 008 32 (13) T2 MAGYAR KÖZTÁRSASÁG Szellemi Tulajdon Nemzeti Hivatala EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 783231 (22) A bejelentés
A termesztett búza diploid őseinek molekuláris citogenetikai elemzése: pachytén- és fiber-fish.
 OTKA K67808 zárójelentés 2012. A termesztett búza diploid őseinek molekuláris citogenetikai elemzése: pachytén- és fiber-fish. A fluoreszcens in situ hibridizáció (FISH) olyan technikai fejlettséget ért
OTKA K67808 zárójelentés 2012. A termesztett búza diploid őseinek molekuláris citogenetikai elemzése: pachytén- és fiber-fish. A fluoreszcens in situ hibridizáció (FISH) olyan technikai fejlettséget ért
Biológus MSc. Molekuláris biológiai alapismeretek
 Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Biológus MSc Molekuláris biológiai alapismeretek A nukleotidok építőkövei A nukleotidok szerkezete Nukleotid = N-tartalmú szerves bázis + pentóz + foszfát N-glikozidos kötés 5 1 4 2 3 (Foszfát)észter-kötés
Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében
 Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében Szántó-Egész Réka 1, Mohr Anita 1, Sipos Rita 1, Dallmann Klára 1, Ujhelyi Gabriella 2, Koppányné Szabó Erika
Mangalica specifikus DNS alapú módszer kifejlesztés és validálása a MANGFOOD projekt keretében Szántó-Egész Réka 1, Mohr Anita 1, Sipos Rita 1, Dallmann Klára 1, Ujhelyi Gabriella 2, Koppányné Szabó Erika
SOLiD Technology. library preparation & Sequencing Chemistry (sequencing by ligation!) Imaging and analysis. Application specific sample preparation
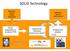 SOLiD Technology Application specific sample preparation Application specific data analysis library preparation & emulsion PCR Sequencing Chemistry (sequencing by ligation!) Imaging and analysis SOLiD
SOLiD Technology Application specific sample preparation Application specific data analysis library preparation & emulsion PCR Sequencing Chemistry (sequencing by ligation!) Imaging and analysis SOLiD
Alu-inszerciós polimorfizmus saját hajszálból izolált DNS mintákbon
 Alu-inszerciós polimorfizmus saját hajszálból izolált DNS mintákbon A kisérlet 60 perces előkészitő fázisra + 2 gyakorlati alkalomra tervezett. Előkészités: hajhagymák kiszedése, sejtek lizise, előkészités
Alu-inszerciós polimorfizmus saját hajszálból izolált DNS mintákbon A kisérlet 60 perces előkészitő fázisra + 2 gyakorlati alkalomra tervezett. Előkészités: hajhagymák kiszedése, sejtek lizise, előkészités
A Multi Locus Sequence Typing (MLST) alkalmazhatósága az élelmiszermikrobiológiában
 A Multi Locus Sequence Typing (MLST) alkalmazhatósága az élelmiszermikrobiológiában Sipos Rita, Lukács Alena, Simon Janka, Szántó-Egész Réka, Micsinai Adrienn 2100 Gödöllő, Szent-Györgyi Albert út 4. info@biomi.hu,
A Multi Locus Sequence Typing (MLST) alkalmazhatósága az élelmiszermikrobiológiában Sipos Rita, Lukács Alena, Simon Janka, Szántó-Egész Réka, Micsinai Adrienn 2100 Gödöllő, Szent-Györgyi Albert út 4. info@biomi.hu,
Adatok statisztikai értékelésének főbb lehetőségei
 Adatok statisztikai értékelésének főbb lehetőségei 1. a. Egy- vagy kétváltozós eset b. Többváltozós eset 2. a. Becslési problémák, hipotézis vizsgálat b. Mintázatelemzés 3. Szint: a. Egyedi b. Populáció
Adatok statisztikai értékelésének főbb lehetőségei 1. a. Egy- vagy kétváltozós eset b. Többváltozós eset 2. a. Becslési problémák, hipotézis vizsgálat b. Mintázatelemzés 3. Szint: a. Egyedi b. Populáció
Genetikailag módosított növények detektálása élelmiszerekben polimeráz láncreakcióval
 Genetikailag módosított növények detektálása élelmiszerekben polimeráz láncreakcióval Szabó Erika és Szamos Jenõ Központi Élelmiszeripari Kutató Intézet, Budapest Érkezett: 2001. június 20. A nemesítõk
Genetikailag módosított növények detektálása élelmiszerekben polimeráz láncreakcióval Szabó Erika és Szamos Jenõ Központi Élelmiszeripari Kutató Intézet, Budapest Érkezett: 2001. június 20. A nemesítõk
A PCR TECHNIKA ÉS ALKALMAZÁSI TERÜLETEI
 Polimeráz láncreakció A PCR TECHNIKA ÉS ALKALMAZÁSI TERÜLETEI Tetszõleges DNS-szakaszról (templát) rövid idõ alatt korlátlan számú másolatot készíthetünk két iniciáló oligonukleotid (primer) és a DNS-polimeráz
Polimeráz láncreakció A PCR TECHNIKA ÉS ALKALMAZÁSI TERÜLETEI Tetszõleges DNS-szakaszról (templát) rövid idõ alatt korlátlan számú másolatot készíthetünk két iniciáló oligonukleotid (primer) és a DNS-polimeráz
Matematikai alapok és valószínőségszámítás. Valószínőségi eloszlások Binomiális eloszlás
 Matematikai alapok és valószínőségszámítás Valószínőségi eloszlások Binomiális eloszlás Bevezetés A tudományos életben megfigyeléseket teszünk, kísérleteket végzünk. Ezek többféle különbözı eredményre
Matematikai alapok és valószínőségszámítás Valószínőségi eloszlások Binomiális eloszlás Bevezetés A tudományos életben megfigyeléseket teszünk, kísérleteket végzünk. Ezek többféle különbözı eredményre
Új temékek az UD- GenoMed Kft. kínálatában!
 Új temékek az UD- GenoMed Kft. kínálatában! Szolgáltatásaink: Medical Genomic Technologies Kft. Betegtoborzás és biobanking Bioinformatika o Adatelemzés/adatbányászás o Integrált adatbázis készítés Sejtvonal
Új temékek az UD- GenoMed Kft. kínálatában! Szolgáltatásaink: Medical Genomic Technologies Kft. Betegtoborzás és biobanking Bioinformatika o Adatelemzés/adatbányászás o Integrált adatbázis készítés Sejtvonal
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Animal welfare, etológia és tartástechnológia
 Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 468 EGYEDAZONOSÍTÁS ÉS SZÁRMAZÁSELLENİRZÉS HIPERPOLIMORF MIKROSZATELLITA
Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 4 Issue 2 Különszám Gödöllı 2008 468 EGYEDAZONOSÍTÁS ÉS SZÁRMAZÁSELLENİRZÉS HIPERPOLIMORF MIKROSZATELLITA
Természetvédelmi biológia
 Természetvédelmi biológia 1. A természetvédelmi biológia meghatározása, a biológiai sokféleség értelmezése A természetvédelmi biológia (konzervációbiológia) fı céljai 1. Az emberi tevékenység fajok populációra,
Természetvédelmi biológia 1. A természetvédelmi biológia meghatározása, a biológiai sokféleség értelmezése A természetvédelmi biológia (konzervációbiológia) fı céljai 1. Az emberi tevékenység fajok populációra,
DR. KOVÁCS ANDRÁS egyetemi tanár, az MTA doktora TÉMAVEZETŐ: Dr. Czeglédi Levente Ph.D. FAJAZONOSÍTÁS ÉLELMISZEREKBŐL PCR SSCP METODIKA FEJLESZTÉSÉVEL
 DEBRECENI EGYETEM Mezőgazdaság-, Élelmiszertudományi és Környezetgazdálkodási Kar ÁLLATTENYÉSZTÉSI TUDOMÁNYOK DOKTORI ISKOLA Doktori Iskola vezető: DR. KOVÁCS ANDRÁS egyetemi tanár, az MTA doktora TÉMAVEZETŐ:
DEBRECENI EGYETEM Mezőgazdaság-, Élelmiszertudományi és Környezetgazdálkodási Kar ÁLLATTENYÉSZTÉSI TUDOMÁNYOK DOKTORI ISKOLA Doktori Iskola vezető: DR. KOVÁCS ANDRÁS egyetemi tanár, az MTA doktora TÉMAVEZETŐ:
Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze
 Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze László Éva Babeş-Bolyai Tudományegyetem, Kolozsvár A polimeráz láncreakció (PCR) napjaink molekuláris biológiai (genetikai) kutatásának nélkülözhetetlen
Polimeráz láncreakció a géntechnológia nélkülözhetetlen eszköze László Éva Babeş-Bolyai Tudományegyetem, Kolozsvár A polimeráz láncreakció (PCR) napjaink molekuláris biológiai (genetikai) kutatásának nélkülözhetetlen
A gyakorlat elméleti háttere A DNS molekula a sejt információhordozója. A DNS nemzedékről nemzedékre megőrzi az élőlények genetikai örökségét.
 A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
A kísérlet megnevezése, célkitűzései: DNS molekula szerkezetének megismertetése Eszközszükséglet: Szükséges anyagok: színes gyurma, papírsablon Szükséges eszközök: olló, hurkapálcika, fogpiszkáló, cérna,
Fehérje expressziós rendszerek. Gyógyszerészi Biotechnológia
 Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
Fehérje expressziós rendszerek Gyógyszerészi Biotechnológia Expressziós rendszerek Cél: rekombináns fehérjék előállítása nagy tisztaságban és nagy mennyiségben kísérleti ill. gyakorlati (therapia) felhasználásokra
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A citológia és a genetika társtudománya Citogenetika A kromoszómák eredetét, szerkezetét, genetikai funkcióját,
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A citológia és a genetika társtudománya Citogenetika A kromoszómák eredetét, szerkezetét, genetikai funkcióját,
Magyar vakcsiga (Bythiospeum hungaricum (Soós, 1927)) egy szisztematikai probléma vizsgálata genetikai módszerekkel
 Földtan, őslénytan, flóra, fauna, természetvédelem www.mecsek.gportal.hu 2013.07.01. Szerkesztő: Fazekas Imre E-mail: fazekas.hu@gmail.com Magyar vakcsiga (Bythiospeum hungaricum (Soós, 1927)) egy szisztematikai
Földtan, őslénytan, flóra, fauna, természetvédelem www.mecsek.gportal.hu 2013.07.01. Szerkesztő: Fazekas Imre E-mail: fazekas.hu@gmail.com Magyar vakcsiga (Bythiospeum hungaricum (Soós, 1927)) egy szisztematikai
A Crocus vernus (Iridaceae) fajcsoport Kárpát-medencei fajainak molekuláris taxonómiája. Egyetemi doktori (PhD) értekezés. Mosolygó-Lukács Ágnes
 DE TTK 1949 A Crocus vernus (Iridaceae) fajcsoport Kárpát-medencei fajainak molekuláris taxonómiája Egyetemi doktori (PhD) értekezés Mosolygó-Lukács Ágnes Témavezető Dr. Surányi Gyula egyetemi adjunktus
DE TTK 1949 A Crocus vernus (Iridaceae) fajcsoport Kárpát-medencei fajainak molekuláris taxonómiája Egyetemi doktori (PhD) értekezés Mosolygó-Lukács Ágnes Témavezető Dr. Surányi Gyula egyetemi adjunktus
[S] v' [I] [1] Kompetitív gátlás
![[S] v' [I] [1] Kompetitív gátlás [S] v' [I] [1] Kompetitív gátlás](/thumbs/93/114506146.jpg) 8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor,
 1 A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor, (Debreceni Egyetem Állattenyésztéstani Tanszék) A bármilyen
1 A gidrán fajta genetikai változatosságának jellemzése mitokondriális DNS polimorfizmusokkal Kusza Szilvia Sziszkosz Nikolett Mihók Sándor, (Debreceni Egyetem Állattenyésztéstani Tanszék) A bármilyen
Filogenetikai analízis. Törzsfák szerkesztése
 Filogenetikai analízis Törzsfák szerkesztése Neighbor joining (szomszéd összevonó) módszer A fában egymás mellé kerülı objektumok kiválasztása a távolságmátrix értékei és az objektumoknak az összes többivel
Filogenetikai analízis Törzsfák szerkesztése Neighbor joining (szomszéd összevonó) módszer A fában egymás mellé kerülı objektumok kiválasztása a távolságmátrix értékei és az objektumoknak az összes többivel
STATISZTIKA. A maradék független a kezelés és blokk hatástól. Maradékok leíró statisztikája. 4. A modell érvényességének ellenőrzése
 4. A modell érvényességének ellenőrzése STATISZTIKA 4. Előadás Variancia-analízis Lineáris modellek 1. Függetlenség 2. Normális eloszlás 3. Azonos varianciák A maradék független a kezelés és blokk hatástól
4. A modell érvényességének ellenőrzése STATISZTIKA 4. Előadás Variancia-analízis Lineáris modellek 1. Függetlenség 2. Normális eloszlás 3. Azonos varianciák A maradék független a kezelés és blokk hatástól
Dobzhansky: In Biology nothing makes sense except in the light of Evolution.
 Dobzhansky: In Biology nothing makes sense except in the light of Evolution. Az Evolúcióbiológia Története Molnár István im54@invitel.hu Mai témák 1. Mi az evolúció? 2. Hogyan alakult ki a mai evolúciós
Dobzhansky: In Biology nothing makes sense except in the light of Evolution. Az Evolúcióbiológia Története Molnár István im54@invitel.hu Mai témák 1. Mi az evolúció? 2. Hogyan alakult ki a mai evolúciós
Szervrendszerek szintje. Szervek szintje. Atomok szintje. Sejtek szintje. Szöveti szint. Molekulák szintje
 Egyed szintje Ökoszisztéma Szervrendszerek szintje Szervek szintje Szöveti szint Sejtek szintje Atomok szintje Molekulák szintje TARTALOM: 1. Molekuláris biológiai/genetikai technikák 2. A genomika technikái
Egyed szintje Ökoszisztéma Szervrendszerek szintje Szervek szintje Szöveti szint Sejtek szintje Atomok szintje Molekulák szintje TARTALOM: 1. Molekuláris biológiai/genetikai technikák 2. A genomika technikái
Függvények II. Indítsuk el az Excel programot! A minta alapján vigyük be a Munka1 munkalapra a táblázat adatait! 1. ábra Minta az adatbevitelhez
 Bevezetés Ebben a fejezetben megismerkedünk a Logikai függvények típusaival és elsajátítjuk alkalmazásukat. Jártasságot szerzünk bonyolultabb feladatok megoldásában, valamint képesek leszünk a függvények
Bevezetés Ebben a fejezetben megismerkedünk a Logikai függvények típusaival és elsajátítjuk alkalmazásukat. Jártasságot szerzünk bonyolultabb feladatok megoldásában, valamint képesek leszünk a függvények
NUKLEINSAVAK. Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag
 NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
NUKLEINSAVAK Nukleinsav: az élő szervezetek sejtmagvában és a citoplazmában található, az átöröklésben szerepet játszó, nagy molekulájú anyag RNS = Ribonukleinsav DNS = Dezoxi-ribonukleinsav A nukleinsavak
Biomatematika 13. Varianciaanaĺızis (ANOVA)
 Szent István Egyetem Állatorvos-tudományi Kar Biomatematikai és Számítástechnikai Tanszék Biomatematika 13. Varianciaanaĺızis (ANOVA) Fodor János Copyright c Fodor.Janos@aotk.szie.hu Last Revision Date:
Szent István Egyetem Állatorvos-tudományi Kar Biomatematikai és Számítástechnikai Tanszék Biomatematika 13. Varianciaanaĺızis (ANOVA) Fodor János Copyright c Fodor.Janos@aotk.szie.hu Last Revision Date:
1. Adatok kiértékelése. 2. A feltételek megvizsgálása. 3. A hipotézis megfogalmazása
 HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
HIPOTÉZIS VIZSGÁLAT A hipotézis feltételezés egy vagy több populációról. (pl. egy gyógyszer az esetek 90%-ában hatásos; egy kezelés jelentősen megnöveli a rákos betegek túlélését). A hipotézis vizsgálat
Egész számok. pozitív egész számok: 1; 2; 3; 4;... negatív egész számok: 1; 2; 3; 4;...
 Egész számok természetes számok ( ) pozitív egész számok: 1; 2; 3; 4;... 0 negatív egész számok: 1; 2; 3; 4;... egész számok ( ) 1. Írd a következõ számokat a halmazábra megfelelõ helyére! 3; 7; +6 ; (
Egész számok természetes számok ( ) pozitív egész számok: 1; 2; 3; 4;... 0 negatív egész számok: 1; 2; 3; 4;... egész számok ( ) 1. Írd a következõ számokat a halmazábra megfelelõ helyére! 3; 7; +6 ; (
Animal welfare, etológia és tartástechnológia
 Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 5 Issue 4 Különszám Gödöllı 2009 459 MORFOLÓGIAI ÉS GENETIKAI VIZSGÁLATOK MAGYARORSZÁGI TÖRPEHARCSÁKON
Animal welfare, etológia és tartástechnológia Animal welfare, ethology and housing systems Volume 5 Issue 4 Különszám Gödöllı 2009 459 MORFOLÓGIAI ÉS GENETIKAI VIZSGÁLATOK MAGYARORSZÁGI TÖRPEHARCSÁKON
A GENOM MEGISMERÉSÉNEK MÓDSZEREI
 A GENOM MEGISMERÉSÉNEK MÓDSZEREI 20 GENETIKA ALAPOK 3-1 Jóslatok és a valóság a molekuláris biológiában. Mennyire látható előre a tudomány fejlődése? 1968 Simone de Beauvoir "Minden ember halandó" 1-2
A GENOM MEGISMERÉSÉNEK MÓDSZEREI 20 GENETIKA ALAPOK 3-1 Jóslatok és a valóság a molekuláris biológiában. Mennyire látható előre a tudomány fejlődése? 1968 Simone de Beauvoir "Minden ember halandó" 1-2
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban
 11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása - (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása - (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
Baranyáné Dr. Ganzler Katalin Osztályvezető
 Budapesti Műszaki és Gazdaságtudományi Egyetem Biokémiai és Élelmiszertechnológiai Tanszék Kapilláris elektroforézis alkalmazása búzafehérjék érésdinamikai és fajtaazonosítási vizsgálataira c. PhD értekezés
Budapesti Műszaki és Gazdaságtudományi Egyetem Biokémiai és Élelmiszertechnológiai Tanszék Kapilláris elektroforézis alkalmazása búzafehérjék érésdinamikai és fajtaazonosítási vizsgálataira c. PhD értekezés
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Supporting Information
 Supporting Information Plasmid Construction DNA cloning was carried out according to standard protocols. The sequence of all plasmids was confirmed by DNA sequencing and amplified using the E. coli strain
Supporting Information Plasmid Construction DNA cloning was carried out according to standard protocols. The sequence of all plasmids was confirmed by DNA sequencing and amplified using the E. coli strain
Human genome project
 Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
Human genome project Pataki Bálint Ármin 2017.03.14. Pataki Bálint Ármin Human genome project 2017.03.14. 1 / 14 Agenda 1 Biológiai bevezető 2 A human genome project lefolyása 3 Alkalmazások, kitekintés
A távérzékelt felvételek tematikus kiértékelésének lépései
 A távérzékelt felvételek tematikus kiértékelésének lépései Csornai Gábor László István Földmérési és Távérzékelési Intézet Mezőgazdasági és Vidékfejlesztési Igazgatóság Az előadás 2011-es átdolgozott változata
A távérzékelt felvételek tematikus kiértékelésének lépései Csornai Gábor László István Földmérési és Távérzékelési Intézet Mezőgazdasági és Vidékfejlesztési Igazgatóság Az előadás 2011-es átdolgozott változata
Molekuláris ökológia Általános Ökológia 2012
 Molekuláris ökológia Általános Ökológia 2012 Technikák Csak vázlatosan Technikák Allozim elektroforérizs Restrikciós fragmens méret polimorfizmus (RFLP) Miniszattelita DNS ujjlenyomat Random Amplification
Molekuláris ökológia Általános Ökológia 2012 Technikák Csak vázlatosan Technikák Allozim elektroforérizs Restrikciós fragmens méret polimorfizmus (RFLP) Miniszattelita DNS ujjlenyomat Random Amplification
Statisztika I. 8. előadás. Előadó: Dr. Ertsey Imre
 Statisztika I. 8. előadás Előadó: Dr. Ertsey Imre Minták alapján történő értékelések A statisztika foglalkozik. a tömegjelenségek vizsgálatával Bizonyos esetekben lehetetlen illetve célszerűtlen a teljes
Statisztika I. 8. előadás Előadó: Dr. Ertsey Imre Minták alapján történő értékelések A statisztika foglalkozik. a tömegjelenségek vizsgálatával Bizonyos esetekben lehetetlen illetve célszerűtlen a teljes
Expression analysis of PIN genes in root tips and nodules of Lotus japonicus
 Article Expression analysis of PIN genes in root tips and nodules of Lotus japonicus Izabela Sańko-Sawczenko 1, Dominika Dmitruk 1, Barbara Łotocka 1, Elżbieta Różańska 1 and Weronika Czarnocka 1, * 1
Article Expression analysis of PIN genes in root tips and nodules of Lotus japonicus Izabela Sańko-Sawczenko 1, Dominika Dmitruk 1, Barbara Łotocka 1, Elżbieta Różańska 1 and Weronika Czarnocka 1, * 1
