A gyógyszerhatás fizikaikémiai
|
|
|
- Hunor Pintér
- 8 évvel ezelőtt
- Látták:
Átírás
1 A gyógyszerhatás fizikaikémiai alapjai Rozmer Zsuzsanna Perjési Pál Az élettudományi-klinikai felsőoktatás gyakorlatorientált és hallgatóbarát korszerűsítése a vidéki képzőhelyek nemzetközi versenyképességének erősítésére Azonosítószám: TÁMOP C-13/1/KONV Pécsi Tudományegyetem Pécs, 2015 Rozmer Zsuzsanna, Perjési Pál, 2015 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásával valósul meg
2 Kézirat lezárva: július 30. A kiadásért felel a: Pécsi Tudományegyetem Felelős szerkesztő: Dr. Perjési Pál Egyéb fejlesztő: Erdősné Moravecz Zsuzsanna Műszaki szerkesztő: Bencze Zsolt és Erdősné Moravecz Zsuzsanna Lektorálta: Dr. Halmos Gábor Terjedelem: 143 oldal
3 Tartalom ÁBRAJEGYZÉK...7 ELŐSZÓ...9 I A GYÓGYSZERHATÁS MOLEKULÁRIS ALAPJAI. A GYÓGYSZERCÉLPONTOK ÉS SZERKEZETI JELLEGZETESSÉGEIK I.1 A GYÓGYSZERHATÁS MOLEKULÁRIS ALAPJAI I.1.1 Kémiai kölcsönhatás kialakítása nélkül ható vegyületek I.1.2 Kémiai kölcsönhatás kialakításával ható vegyületek I.2 A GYÓGYSZERCÉLPONTOK (CÉLMOLEKULÁK) SZERKEZETI JELLEGZETESSÉGEI I.2.1 A fehérjék szerkezete I.2.2 A lipidek tulajdonságai I.2.3 A sejtmembránok szerkezete I.3 IRODALOM II RECEPTOROK, MINT GYÓGYSZERCÉLPONTOK II.1 SEJTFELSZÍNI RECEPTOROK II.1.1 Ligandum-aktivált ioncsatornák (ionotróp receptorok) II.1.2 Saját enzimaktivitás nélküli receptorok (metabotróp receptorok) II.1.3 Saját enzimaktivitással bíró receptorok II.2 INTRACELLULÁRIS RECEPTOROK II.3 IRODALOM III ENZIMEK, MINT GYÓGYSZERCÉLPONTOK III.1 AZ ENZIMKATALÍZIS MECHANIZMUSA III.2 AZ ENZIMEK CSOPORTOSÍTÁSA III.3 AZ ENZIMREAKCIÓK KINETIKÁJA III.4 AZ ENZIMREAKCIÓK GÁTLÁSA III.5 IRODALOM IV TRANSZPORTEREK ÉS IONCSATORNÁK, MINT GYÓGYSZERCÉLPONTOK IV.1 FACILITÁLT DIFFÚZIÓ IV.2 A TRANSZPORTFOLYAMATOK ENERGIAVISZONYAI IV.3 AKTÍV TRANSZPORT IV.4 CSATORNAKÉPZŐ FEHÉRJÉK IV.4.1 Ionofórok IV.4.2 Feszültségfüggő ioncsatornák IV.4.3 Ligandumfüggő ioncsatornák Azonosító szám: TÁMOP C-13/1/KONV
4 IV.5 IRODALOM V NUKLEINSAVAK, MINT GYÓGYSZERCÉLPONTOK V.1 NUKLEOZIDOK, NUKLEOTIDOK V.2 DEZOXINUKLEINSAV (DNS) V.3 RIBONUKLEINSAVAK V.4 IRODALOM VI A HATÓANYAG-GYÓGYSZERCÉLPONT KÖLCSÖNHATÁS FIZIKAI-KÉMIAI JELLEGZETESSÉGEI VI.1 MÁSODLAGOS KÖLCSÖNHATÁSOK VI.1.1 Rövidtávú taszítás VI.1.2 Ion-Ion kölcsönhatás VI.1.3 Ion-Indukált dipól kölcsönhatás VI.1.4 Permanens dipól-permanens dipól (Keesom) kölcsönhatások VI.1.5 Permanens dipól- Indukált dipól (Debay) kölcsönhatás VI.1.6 Pillanatszerűen indukált dipól-indukált dipól (London) kölcsönhatás VI.1.7 Hidrogénhidas kölcsönhatás ( hidrogénkötés ) VI.2 AFFINITÁS ÉS AKTIVITÁS VI.3 HATÉKONYSÁG ÉS HATÁSERŐSSÉG VI.4 SZELEKTIVITÁS VI.5 IRODALOM VII A HATÓANYAG-GYÓGYSZERCÉLPONT KÖLCSÖNHATÁS FIZIKAI-KÉMIAI JELLEGZETESSÉGEI. SZERKEZET, TÉRSZERKEZET VII.1 DIASZTEREOIZOMEREK VII.2 ENANTIOSZTEREOIZOMEREK VII.3 A GYÓGYSZERHATÁS DIASZTEREO- ÉS ENANTIOSZTERO- SZELEKTIVITÁSA VII.4 IRODALOM VIII A GYÓGYSZERVEGYÜLETEK FIZIKAI-KÉMIAI JELLEMZŐI. SAV-BÁZIS TULAJDONSÁGOK VIII.1 A SAVAK ÉS BÁZISOK ERŐSSÉGE. A PK A ÉRTÉK FOGALMA VIII.2 HATÓANYAGOK SAVAS ÉS BÁZIKUS FUNKCIÓS CSOPORTJAI VIII.2.1 Savas funkciós csoportok VIII.2.2 Bázikus funkciós csoportok VIII.3 A PK A ÉRTÉK JELENTŐSÉGE VIII.4 A PK A ÉRTÉK MEGHATÁROZÁSÁNAK LEHETŐSÉGEI VIII.4.1 Potenciometriás titrálás A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
5 Tartalom VIII.4.2 UV-Vis spektrofotometriás titrálás VIII.4.3 Egyéb módszerek VIII.5 IRODALOM IX A GYÓGYSZERVEGYÜLETEK FIZIKAI-KÉMIAI JELLEMZŐI. OLDHATÓSÁG X IX.1 AZ OLDATOK DEFINÍCIÓJA IX.2 AZ OLDÓDÁS FOLYAMATA IX.3 AZ OLDHATÓSÁG DEFINÍCIÓJA, FAJTÁI IX.4 AZ OLDHATÓSÁGOT BEFOLYÁSOLÓ TÉNYEZŐK IX.4.1 Molekulaszerkezet és oldószer IX.4.2 Hőmérséklet IX.4.3 Az ionizálható vegyületek oldhatósága IX.4.4 Idegen anyagok jelenléte, az anyag és az oldószer tisztasága IX.5 AZ OLDHATÓSÁG MEGHATÁROZÁSÁNAK KÍSÉRLETES MÓDSZEREI IX.5.1 A kinetikai oldhatóság meghatározási módszerei IX.5.2 A termodinamikai oldhatóság meghatározási módszerei IX.6 IRODALOM A GYÓGYSZERVEGYÜLETEK FIZIKAI-KÉMIAI JELLEMZŐI. LIPOFILITÁS ÉS MEGOSZLÁSI HÁNYADOS X.1 A MEGOSZLÁSI HÁNYADOS FOGALMA X.2 A MEGOSZLÁSI HÁNYADOS SZEREPE X.3 A LIPOFILITÁS ÉS A FOSZFOLIPOFILITÁS X.3.1 Az oktanol/víz rendszer X.3.2 A foszfolipofilitás X.4 A MEGOSZLÁSI HÁNYADOS MEGHATÁROZÁSÁNAK MÓDSZEREI X.4.1 Direkt meghatározási módszerek X.4.2 Indirekt meghatározási módszerek X.4.3 Predikciós módszerek X.5 IRODALOM XI A GYÓGYSZERVEGYÜLETEK FIZIKAI-KÉMIAI JELLEMZŐI. PERMEÁBILITÁS XI.1 A PERMEÁBILITÁS FOGALMA XI.2 A BIOLÓGIAI MEMBRÁNOK ÉS TRANSZPORTFOLYAMATOK XI.2.1 A biológiai membránok felépítése XI.2.2 Penetrációs mechanizmusok XI.3 A PERMEÁBILITÁS JELENTŐSÉGE XI.4 A PERMEÁBILITÁS MEGHATÁROZÁSÁNAK KÍSÉRLETES MÓDSZEREI Azonosító szám: TÁMOP A/1-11/
6 XI.4.1 A PAMPA-modell XI.4.2 Sejtes modellek XI.5 IRODALOM XII METABOLIZMUS XII.1 FÁZIS I VAGY FUNKCIONALIZÁCIÓS REAKCIÓK XII.1.1 Oxidációs reakciók XII.2 FÁZIS II VAGY KONJUGÁCIÓS REAKCIÓK XII.2.1 Konjugáció glükuronsavval XII.2.2 Konjugáció szulfáttal XII.2.3 Konjugáció aminosavakkal XII.2.4 Konjugáció glutationnal XII.2.5 Acetilezés XII.2.6 Metilezés XII.3 IRODALOM A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
7 Ábrajegyzék I-1. ábra: A peptidkötés szerkezete I-2. ábra: A fehérjék alfa-hélix szerkezete I-3. ábra: A fehérjék béta-redő szerkezete I-4. ábra: A fehérjék béta-fordulat szerkezete I-5. ábra: A fehérjék harmadlagos szerkezete I-6. ábra: Az L- -foszfatidsav (2-(R)-foszfatidsav) szerkezete I-7. ábra: A szvingozin (D-eritro-4-szfingenin) szerkezete I-8. ábra: A koleszterin szerkezete I-9. ábra: A sejthártya mozaikmodellje I-10. ábra: A foszfolipidek megoszlása az emberi vörösvértest plazmamembránjában II-1. ábra: A receptor, a másodlagos hírvivő és az effektor fogalma II-2. ábra: A dózis-válasz görbe különböző formái II-3. ábra: A receptor ioncsatornák egyszerűsített szerkezete II-4. ábra: A G-fehérjéhez kapcsolt receptorok aktiválásának modellje II-5. ábra: A sejtmagreceptorok egyszerűsített felépítése II-6. ábra: Az ösztrogén receptor működési ciklusa III-1. ábra: Enzimkatalizált reakció sebességének (v) változása a szubsztrátkoncentráció [S] függvényében. (v max : maximális sebesség, K M : Michaelis-Menten állandó) IV-1. ábra: Az egyszerű diffúzió, a facilitált diffúzió és az aktív transzport egyszerűsített mechanizmusa IV-2. ábra: Az egyszerű diffúzió és a facilitált diffúzió sebességének és a transzportálandó anyag koncentrációjának összefüggése IV-3. ábra: Az uniport, a szimport és az antiport transzporterek működésének elve IV-4. ábra: A mobilis ionszállítók és a csatornaképző ionofórok működése IV-5. ábra: A nátriumion-csatorna nyugalmi, aktivált és inaktivált állapota IV-6. ábra: A helyi érzéstelenítők nátriumion csatornákra kifejtett hatásának Hille szerinti értelmezése V-1. ábra: A nukleinsav bázisok nukleozid származékainak szerkezete V-2. ábra: Az adenozin-trifoszfát (ATP) és a gyűrűs adenozin-monofoszfát (camp) szerkezete V-3. ábra: A DNS B-formája VI-1. ábra: A másodlagos kölcsönhatások energiájának távolságfüggése VI-2. ábra: A hidrogénhidas kölcsönhatás kialakulása VI-3. ábra: Teljes és részleges agonista dózis-válasz görbéi VI-4. ábra: A dózis-biológia válasz összefüggés lineáris és szemilogaritmikus koordinátarendszerben történő ábrázolása VI-5. ábra: Két különböző hatékonyságú ( A valamint B és C ) és két különböző hatáserősségű ( A és B valamint C ) hatóanyag dózisválasz görbéje VII-1. ábra: A 2-metil-pentán (1) és 3-metil-pentán (2), valamint az etanol (3) és dimetil-éter (4) szerkezete VII-2. ábra: A (Z)-2-butén (1) és az (E)-2-butén (2), valamint a cisz-1,2-dimetilciklopentán (3) és transz-1,2-dimetil-ciklopentán (4) szerkezete VII-3. ábra: Az alanin két enantiomerje Azonosító szám: TÁMOP A/1-11/
8 II-11. ábra: A D-szorbit mind a D-mannit szerkezete VII-5. ábra: A glicerinaldehid enantiomerek Fischer-féle projekciós képletei VII-6. ábra: A D-glicerinaldehid, a D-tejsav és az L-alanin projekciós képletei VII-7. ábra: A D/L és az R/S konfigurációs prefixumok közötti összefüggés VII-8. ábra: Az (E)-cinnarizin (1) és a (Z)-tamoxifén (2) szerkezete VII-9. ábra: A kinin (1) és a kinidin (2) szerkezete VII-10. ábra: A ligandum-receptor kölcsönhatás hárompontos illeszkedési modellje VIII-1. ábra: Potenciometriás titrálási görbe VIII-2. ábra: A potenciometriás titrálási görbe, valamint első és második differencia-hányados görbéi VIII-3. ábra: Potenciometriás titrálási görbék a paracetamol disszociációs állandójának meghatározása különbségi potenciometriás módszerrel VIII-4. ábra: Benzokain UV-Vis spektrumának ph-függése IX-1. ábra: A gyógyszerhatóanyag oldódását befolyásoló tényezők IX-2. ábra: Az oldódást kísérő hőváltozások IX-3. ábra: Egyértékű gyenge sav, egyértékű gyenge bázis és amfoter vegyület oldhatóság-ph profiljai IX-4. ábra: A gyomor és a patkóbél (duodenum) kémhatásának változása étkezés előtt, valamint étkezést követően X-1. ábra: Egyértékű gyenge sav, egyértékű gyenge bázis és amfoter vegyület lipofilitás-ph profiljai X-2. ábra: A ph-megoszlás hipotézis XI-1. ábra: A biológiai membránok felépítése XI-2. ábra: A BCS osztályozási rendszer XI-3. ábra: A PAMPA-modell sematikus vázlata XI-4. ábra: A sejtes-modell sematikus vázlata XII-1. ábra: A benzoesav hippursavvá történő átalakulásának reakciója XII-2. ábra: A xenobiotikumok átalakulásának két lehetséges útja XII-3. ábra: A propranolol metabolizmusa XII-4. ábra: A monoamin-oxidáz enzimek működésének mechanizmusa XII-5. ábra: A paracetamol és az ibuprofén glükuronsav-konjugátummá történő átalakulásának UDP-glükuronil-transzferáz (UGT) enzimek által katalizált reakciója XII-6. ábra: A paracetamol szulfát-konjugátummá történő átalakulásának szulfotranszferáz (SULT) enzimek által katalizált reakciója XII-7. ábra: A benzoesav glicin-konjugátuma (hippursav) képződésének reakciója XII-8. ábra: Az etakrinsav és a redukált glutation (GSH) glutation-s-transzferáz (GST) enzimek által katalizált reakciója XII-9. ábra: A glutation-konjugátumok merkaptursav-származékká történő metabolizmusának reakcióútja XII-10. ábra: A prokainamid acetilszármazékká történő átalakulásának N- acetiltranszferáz (NAT) enzimek által katalizált reakciója XII-11. ábra: A norepinefrin katechol-o-metiltranszferáz (COMT) enzimek által katalizált O-metilezési reakciója A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
9 Előszó A biztonságos, a lehető legkevesebb nemkívánt hatással rendelkező hatóanyagok fejlesztése, a hatóanyagok nemkívánt kölcsönhatásainak elkerülése, elengedhetetlenné teszi a vegyületek hatásainak molekuláris szintű megismerését. E terület e farmakológiai, a biokémiai és a gyógyszerkémiai vizsgálatok egyik legintenzívebben művelt terülte. A biológiai hatás kialakulásának komplex jellegéből eredően a jelenségek vizsgálatainak metodikái, célkitűzései a három különböző területen végzett vizsgálatok során különbözőek lehetnek. Az azonban közös kísérleti tapasztalat, hogy a testidegen vegyületek biológiai hatásait néhány alapvető fizikai-kémiai tulajdonsága, így többek között a (tér)szerkezet, az ionizációs készség, valamint a lipofil-hidrofil fázisok közötti megoszlási hányados határozza meg. Jelen elektronikus tananyag a PTE ÁOK Gyógyszertudományi Doktori Iskola keretében meghirdetett tantárgy főbb fejezeteinek alapján íródott. A tantárgy keretében a hallgatók megismerkednek a celluláris gyógyszercélpontok valamint a hatóanyagok szerkezetével és a hatás kialakulásával kapcsolatos legfontosabb fizikai-kémiai tulajdonságokkal, a hatóanyag-celluláris célmolekula kölcsönhatások természetével, valamint a kölcsönhatás és a biológiai hatás közötti kapcsolat alapjaival. Bár a tananyag elsősorban Ph.D. hallgatók képzése céljából készült, azt hasznosan tanulmányozhatják a Gyógyszerészi kémia tantárgy iránt érdeklődő graduális hallgatók is. A címben megjelölt terület összetettsége következtében, egy a fenti oktatási célkitűzésekkel összeállított tananyag szükségszerűen nem lehet teljes. Bizonyára kellő alapot nyújt azonban a gyógyszerek hatásmechanizmusát alaposabban megismerni vágyó és /vagy új hatóanyagok/gyógyszerformák fejlesztésén dolgozó munkatársak számára. A szerkesztők köszönetüket fejezik ki Dr. Halmos Gábor egyetemi tanár Úrnak (Debreceni Egyetem), aki lelkiismeretes lektori munkájával, építő jellegű megjegyzéseivel, javításaival járult hozzá, hogy a hallgatók hiteles, megbízható forrásból ismerkedjenek meg a gyógyszerek hatása és azok fizikai-kémiai tulajdonságai közti alapvető összefüggésekkel. A tananyag modulszerű felépítése lehetővé teszi, hogy a jövőben szükség szerint újabb területekkel, a gyógyszerhatás molekuláris alapjainak további kémiai, biokémiai, fizikai-kémiai aspektusainak további részletes tárgyalásával bővüljön. Ezzel kapcsolatban a tananyag szerkesztője örömmel vesz minden hozzá eljuttatott javaslatot. Természetesen a szerkesztő köszönettel vesz bármi, a javításra vonatkozó megjegyzést. Pécs, július. A szerkesztők Azonosító szám: TÁMOP A/1-11/
10 I A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik A testidegen anyagok élő szervezetekre gyakorolt hatásának vizsgálata egyike a legősibb természettudományos vizsgálatoknak. E vizsgálatok alapjait azok a mai is ismert ősi megfigyelések adták, melyek az ehető és nem-ehető (mérgező) növények, termések stb. megkülönböztetéséhez, valamint a fájdalmak enyhítését, a láz csökkentését, a sebek gyógyulását, stb. eredményező természetes anyagok (levelek, gyökerek, kövek, stb.) megismeréséhez vezettek. Az első időkben az adatgyűjtés korában a legfontosabb ismeretet a természetes hatóanyag felismerése és a szervezetre gyakorolt hatásának ismerete jelentette. Bár az első írásos dokumentumok az ókori Kínában születtek, az Európában legismertebbé vált korai dokumentumot G. Ebers 1874-ben Egyiptomban találta meg. Ez az egyik legrégebbi orvosi szöveg az i.e körül keletkezett, 21 m hosszú papirusztekercset, amely 1000 év orvosi történelmét írja le, és 876 gyógykészítményt valamint több mint 500 növényt sorol fel. Ezeknek a növényeknek a harmada ma is használt gyógynövény (például: kömény, szennalevél, kakukkfű, lenmag, fokhagyma). I.e. 500 körül az egyiptomi herbalistákat tekintették a legjobbaknak. Rómától Babilonig ők voltak az uralkodók orvosai. A görög és a római orvosok rendszerezték a gyógynövények ismeretét, fajtáit és felhasználásukat. Hippokratész (i. e ), az orvostudomány atyja könyvében, a Corpus Hippocratiumban több mint 200 gyógynövényt írt le. A különféle betegségeket az emberi létezés természetes velejárójának tartotta, melyek megfelelő készítményekkel gyógyíthatók. Arisztotelész (i. e ) szintén készített gyógynövényeket taglaló könyvet. A görög-római Dioszkoridész (i.sz ) az ismeretek összegzése és elemzése után, 78-ban megírta Európa első gyógynövény jegyzékét. A De Materia Medica című művében 600 gyógynövényt tárgyal. Könyve 1500 éven keresztül a herbalisták alapműve volt. Marcus Aurelius császár elismert orvosa, C. Galenus ( ) részletesen taglalt, többkötetes gyógynövény könyveket alkotott. A gyógynövényekből különböző gyógyszerformákat (főzetek, tinktúrák, kenőcsök, tapaszok stb.) készített, amiket ma galenusi készítményekként ismerünk. A modern gyógynövénygyógyászat alapjait a 16. század elején Paracelsus rakta le. Paracelsus Herbarius című könyvében írta le részletesen a különböző gyógynövényeket. Míg a középkorban a betegségeket isten büntetésének tartották, addig Paracelsus a korát megelőző különböző nézeteket összegezve úgy gondolta, hogy nem a lélek tisztátlansága, hanem a test pillanatnyi ásványi egyensúlyának megbomlása okozza a betegségeket, amelyeket a test kémiájának orvosolásával lehet meggyógyítani. Paracelsus volt az első orvos, aki gyógyszerként volt képes alkalmazni egyébként mérgező, például higany-, kén- vagy vasvegyületeket. Mondása: A mennyiség teszi a mérget. (Eredeti megfogalmazásban: Alle Ding' sind Gift und nichts ohn' Gift; allein die Dosis macht, das ein Ding kein Gift ist. : Minden dolog méreg, ha önmagában nem is az; csupán a mennyiség teszi, hogy egy anyag nem méreg. ) A gyógyszeres terápia tudományos alapjának megteremtése a C. Bernard ( ) nevéhez kapcsolódik, aki 1850-ben a kuráré vizsgálata során elvégezte az első pontos farmakológiai analízist, és ezzel lefektette az experimentális farmakológia alapköveit. Az első önálló farmakológiai tanszéket 1849-ben alapították a dorpati (ma Tartu, Észtország, akkor német nyelvű oroszországi univerzitás volt) egyetemen R. Buchheim ( ) vezetésével. Tanítványát, a lett származású O. Schmiedeberget ( ), tekintik a modern gyógyszertani oktatás megalapítójának. 10 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
11 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik A kísérletes farmakológia kezdettől fogva szorosan együtt fejlődött a szerves kémiával, ami előbb a növényi hatóanyagok izolálásával és szerkezet-felderítésével, majd a szintetikus módszerek fejlesztésével vitte előre a farmakológiai tudományok fejlődését. Az önálló tudománnyá nőtt gyógyszerkémia a kísérletes farmakológia molekuláris szinten történő értelmezésének fizikai-kémiai alapjait rendszerbe foglaló tudományág. A gyógyszerhatás molekuláris szinten történő első értelmezése P. Erlich ( ) és J.N. Langley ( ) munkáiban jelenik meg. Erlich koncepciója szerint a gyógyszerhatás alapfeltétele a hatást kiváltó molekula és valamely sejtalkotó elem ( receptor ) kapcsolódása ( Corpora non agunt nisi fixata ). Erlich elképzelése szerint a kórokozó mikroszkopikus élőlények sejtjeinek a protoplazmája számos oldalláncot, ún. receptort tartalmaz. Normális körülmények között ezeknek a funkciója a sejt metabolizmusához szükséges tápanyag és oxigén felvétele. Kedvező hatás esetén a gyógyszer molekulája, a szerkezetére jellemző sajátos csoportok (farmakofor csoportok) segítségével, éppen ezekhez a receptorokhoz kapcsolódik, és ezzel meggátolja a mikroorganizmus normális élettevékenységet. A kötődés a gyógyszer molekulája és a receptor között (tipikusan másodlagos) kémiai kötések kialakulásával történhetik. Például a bázikus tulajdonságú festékek a receptorok savas jellegű csoportjaival kapcsolódnak. Erlich munkahipotézise helyesnek bizonyult, bár elmélete az elmúlt időszakban tovább finomodott. Mindezek ellenére, Ehrlich egész munkásságát - a kemoterápia megalapozását és a receptor elmélet kidolgozását - határkőnek is, de talán még inkább iránymutatónak tekinthetjük a gyógyszerkutatásban. I.1 A gyógyszerhatás molekuláris alapjai Az eredeti elképzések mai ismereteink alapján sokat fejlődtek. Így a gyógyszervegyületek (testidegen anyagok) biológiai hatásaink kialakulása molekuláris alapjai szempontjából a vegyületek két nagy csoportba oszthatók: 1.) Endogén celluláris (makro)molekulákkal (célmolekulákkal) kémiai kölcsönhatás kialakítása nélkül biológiai hatást eredményező vegyületek, valamint 2.) Az endogén celluláris (makro)molekulákkal (célmolekulákkal) kémiai kölcsönhatás kialakítása révén biológiai hatást eredményező vegyületek. Ez utóbbi vegyületek csoportja két további alcsoportba osztható, az alapján, hogy a kölcsönhatás természete a.) kovalens, vagy b.) nem-kovalens természetű. I.1.1 Kémiai kölcsönhatás kialakítása nélkül ható vegyületek Ebbe a csoportba tartozó vegyületek hatásukat fizikai, illetve fizikai-kémiai tulajdonságaik alapján fejtik ki. E csoportba tartoznak például a bélfal síkosításával ható hashajtók, a sós hashajtók, az ozmotikus hashajtók, az ozmotikus diuretikumok, vagy az inhalációs általános érzéstelenítők (anesztetikumok). Azonosító szám: TÁMOP /1/A
12 Az indifferens, fel nem szívódó olajokat (pl. paraffinolaj) hashajtóként lehet használni. A béltartalommal emulziót képezve a bélfalat sikamlóssá teszi, így enyhe hashajtó hatást vált ki. A sós hashajtók fizikokémiai tulajdonságok alapján hatnak. A csoport jellegzetes képviselői a glaubersó (nátrium-szulfát-dekahidrát) és a keserűsó (magnézium-szulfátheptahidrát). A fenti sók jellemzője a szulfátion tartalom. A szulfátionok rosszul szívódnak fel és így a bélcsatornában maradnak. A béltartalom izotóniás a plazmával, így a nagy szulfátion-koncentráció miatt, a víz a béltraktusból nem szívódik fel. A belek víztartalma feszíti a bélfalakat és ezáltal növeli a perisztaltikát. Így a béltartalom gyorsabban távozik. Az ozmotikus hashajtók hatásának fizikai-kémiai alapja megegyezik a sós hashajtóékkal: a gyomor-bélrendszerből nem szívódnak fel, a belek víztartalma feszíti a bélfalakat és ezáltal növeli a perisztaltikát. E csoportba tartozó jellegzetes vegyületek a mannit, a szorbit, a glicerin, a metilcellulóz, a guargumi és a laktulóz. Az inhalációs anesztetikumok hatásmechanizmusát is fizikokémiai tulajdonságokkal lehet magyarázni. A csoport jellegzetes képviselői a dinitrogén-oxid, az éter, a halotán, az izoflurán, stb. L. Pauling elmélete szerint az inhalációs anesztetikumok a membránfehérjékhez kapcsolódó vízzel klatrát komplexet alkotnak. A vizet ezek a vegyületek megkötik, és így az idegtevékenységet biztosító ionok (nátriumion, kálium, klorid) mozgását gátolják. A feltevést a komplex létét röntgen diffrakciós mérésekkel igazolták. I.1.2 Kémiai kölcsönhatás kialakításával ható vegyületek I Kovalens kölcsönhatás kialakítása révén ható vegyületek Az ide sorolható vegyületeket további alcsoportokra oszthatjuk. Ezek egyikét azok a vegyületek képviselik, melyek a szervezet endogén kis molekulatömegű vegyületeivel lépnek kémiai reakcióba. E vegyületek egy gyakran alkalmazott csoportját képviselik az antacid szerek. Az antacid szerek (pl. nátrium-hidrogén-karbonát, kalcium-karbonát, bázisos magnézium-karbonát, alumínium-oxid) a fokozott gyomorsósav-termelés okozta panaszok enyhítésére szolgáló vegyületek. Általános jellemzőjük, hogy gyenge bázisok, melyek a gyomor sósavtartalmával sót képeznek. A csoport másik nagy alcsoportját azok a vegyületek képviselik, melyek a celluláris makromolekulákkal (célmolekulákkal) reagálnak kovalens kölcsönhatás kialakításával. E vegyületek legismertebb példái az (a) alkiláló hatású daganatellenes szerek, valamint az (b) irreverzibilis enzim inhibitorok. A biológiai alkilezőszerek fontosabb csoportjait a nitrogénmustár-származékok, a nitrózokarbamid- (nitrózourea-) származékok, valamint a mitomicinek képviselik. A vegyületek metabolikus átalakulása eredményeképpen reaktív elektrofil származékok keletkeznek, melyek képesek reagálni a célmolekulák (p. fehérjék, nukleinsavak, poliszacharidok) nukleofil csoportjaival. Az elektrofil metabolitok nagy reaktivitása eredményeképpen a vegyületek szelektivitása elsősorban a vegyületek megoszlásának és a reaktív metabolitok elsődleges képződési helyének különbözőségén alapul. A celluláris célmolekulákkal kovalens kötést kialakító vegyületek között kiemelkedő jelentőséggel bírnak a szelektív gátló hatással bíró származékok. E származékok legtöbbje, mint különböző enzimek irreverzibilis gátlója ismert. Az ide tartozó vegyületek legismertebb példái 12 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
13 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik az acetilszalicilsav (szelektív COX-1 gátló) a tranilcipromin (nem-szelektív MAO gátló) a szelegilin (szelektív MAO-B gátló) a diizopropil-fluor-foszfát (acetilkolin-eszteráz gátló) az allopurinol (xantin-oxidáz gátló) a penicillinek és kefalosporinok (DD-transzpeptidáz gátlók). I Nem-kovalens kölcsönhatás kialakítása révén ható vegyületek A legtöbb gyógyszerként alkalmazott vegyület kialakulásának molekuláris alapjait a vegyületek celluláris célmolekulákkal kialakított nem-kovalens kölcsönhatások képezik. A nem-kovalens kölcsönhatások nem eredményeznek új molekulákat. Meghatározó szerepet töltenek azonban be az ionok és molekulák egymás közötti kapcsolat kialakításában. A kapcsolat a kovalens kölcsönhatásoknál gyengébb, megfordítható (reverzibilis), érzékenyen változik a környezet molekuláris változásai függvényében. A legfontosabb nem-kovalens kölcsönhatásokat és rövid jellemzőit a I-1. táblázat foglalja össze. I-1 táblázat: Nem-kovalens kölcsönhatások és legfontosabb jellemzőik. Kölcsönhatás típusa Ion-Ion Ion-Permanens dipólus Permanens dipólus- Permanens dipólus Ion-Indukált dipólus Permanens dipólus Indukált dipólus London-féle diszperziós effektus Rövidtávú taszítás Jellemzés Példa Energia távolságfüggés leghosszabb ammóniumion - 1/r hatótáv, nem karboxilátion irányfüggő Erőssége függ a ammóniumion - 1/r 2 dipólus vízmolekula irányítottságától Erőssége függ a két dipólus egymáshoz viszonyított orientációjától Erőssége függ az indukálható molekula polarizálhatóságától Erőssége függ az indukálható molekula polarizálhatóságától Fluktuáló pillanatszerű töltések kölcsönös szinkronizációja Elektronpályák közeledésekor, rendkívül rövidtávú vízmolekula - vízmolekula ammóniumion - fenilcsoport 1/r 3 1/r 4 víz - fenilcsoport 1/r 6 fenilcsoport - fenilcsoport elektronpálya - elektronpálya 1/r 6 1/r 12 Hidrogénhidas kölcsönhatás Elektrosztatikus, részlegesen kovalens szekunder aminocsoport - karbonilcsoport kötéshossz Azonosító szám: TÁMOP /1/A
14 A celluláris célmolekulák tipikusan a szervezet makromolekulái lehetnek. Ezek a.) a fehérjék, b.) a nukleinsavak, c.) a lipidek (sejtmembránok) és d.) a szénhidrátok E makromolekulák mindegyike sokrétű funkciót tölt be az élő szervezetben. A gyógyszerhatás molekuláris szintű megismerése szempontjából legfontosabb csoportjai a fehérjék, a nukleinsavak, valamint a sejteket és a sejtorganellumokat körülvevő kettős lipidmembránok. Ez utóbbiakban számos fehérje természetű, különböző fiziológiás funkcióval rendelkező sejtalkotót is megtalálhatunk, melyek közül számos képezheti gyógyszermolekulák célpontjait. A terápiás szempontból legfontosabb celluláris célpontok funkcióinak gyógyszervegyületekkel történő módosításának lehetőségeit a II.-V. fejezetek tárgyalják. A makromolekulák esetén a kölcsönhatás kialakulásában résztvevő molekulaszakasz megnevezése az adott makromolekula celluláris funkciójától függően célmolekula, kötőhely, aktív centrum, stb. lehet. E fejezet keretében a fehérjék és a lipidek szerkezeti jellegzetességei kerülnek bemutatásra. A nukleinsavak szerkezeti jellegzetességeit az V. fejezet mutatja be. A nemkovalens kölcsönhatásokat meghatározó fizikai-kémiai tulajdonságokat a VIII.-XII. fejezetek mutatják be. I.2.1 I.2 A gyógyszercélpontok (célmolekulák) szerkezeti jellegzetességei A fehérjék szerkezete A fehérjék az aminosavak polimerjeinek tekinthetők és kémiai vagy enzimatikus hidrolízisükkor aminosavakra bomlanak. A fehérjék ún. elsődleges szerkezete maga az aminosav sorrend, amely az egymással peptidkötéssel kapcsolódó aminosavakból épül fel. A peptidkötés az egymást követő aminosavak karboxil- és aminocsoportjai között kialakuló savamid kötés (I-1. ábra). A kötésben a nitrogénatom nemkötő elektronpárja valamint a karbonilcsoport pi- és n-elektronjai konjugált rendszert képeznek, melynek következtében 1. A peptidkötés C-N kötésének kötésrendje megnő, a kötés körül a rotáció normál körülmények között gátolttá válik. A stabilisabb transz elrendeződés cisz térszerkezetté történő átrendeződéséhez (izomerizációjához) viszonylag nagy energia szükséges. A kedvezményezett transz formában a H-N-C=O atomok egy síkban helyezkednek el (lásd I-1. ábra). 2. A konjugáció eredményeképpen a savamid nitrogénatom vízzel szemben nem mutat bázikus tulajdonságot. I-1. ábra: A peptidkötés szerkezete. 14 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
15 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik A láncot felépítő aminosavak sorrendjét az N-terminálistól indulva adjuk meg, leggyakrabban az egyes aminosavakat szimbolizáló két- vagy hárombetűs kódok segítségével. A fehérjék egyenes láncú szerkezet energetikailag nem kedvező, ezért a fehérjeláncok egyes szakaszai egymással kölcsönhatásba kerülve, másodlagos, harmadlagos és oligomer fehérjék esetén negyedleges szerkezeti elemeket hoznak létre. A háromdimenziós elrendeződés (konformáció) kialakításában résztvevő kölcsönhatások közül megemlítendők a hidrogénkötések, az ionos kötések, a hidrofób kölcsönhatások, valamint a diszulfidhidak. Mint látható, a fehérjék térszerkezetét (konformációját) a környezet által aránylag könnyen módosítható kölcsönhatások (a diszulfid hidak kivételével nemkovalens kölcsönhatások) alakítják ki. Maguk a kölcsönhatások kooperativitást mutatnak: néhány kialakuló kapcsolat a továbbiak létrejöttét segíti. A fehérjék egyik alapvető tulajdonsága, hogy konformációjuk szoros kapcsolatban van a funkciójukkal; a funkció ellátása egy adott konformációhoz kötött. Így a konformáció módosulása (pl. testidegen anyagokkal történő kölcsönhatás kialakulása következtében) a fehérje funkcióját megváltoztathatja. A fehérjék ún. másodlagos szerkezetét a peptidkötések és karbonil- és amidocsoportjai között kialakuló hidrogénhidak stabilizálják. A szerkezet annál stabilabb, minél nagyobb számú hidrogénhíd kialakítására van lehetőség. A fehérjék szerkezetvizsgálata alapján megállapítható volt, hogy három kitüntetett ismétlődést (periodicitást) mutató másodlagos szerkezeti elem figyelhető meg: a csavarmenetes alfa hélix, a redőzött béta redő és a béta fordulat képezik. Az alfa-hélix esetében a peptidlánc NH és CO csoportjai között hidrogénhidak alakulnak ki oly módon, hogy minden negyedik aminosav egymáshoz kapcsolódik (I-2. ábra). A kialakuló stabil helikális szerkezet kialakításában leggyakrabban Ala, Cys, Leu, Met, Glu, Gln, His és Lys oldalláncok vesznek részt. I-2. ábra: A fehérjék alfa-hélix szerkezete. Azonosító szám: TÁMOP /1/A
16 A béta-redő esetében nem a láncon belül, hanem a láncok között alakulnak ki a hidrogénhidak, a polipeptidláncok nem tekerednek fel, lemezes szerkezet alakul ki. (I-3. ábra). A Val, Ile, Phe, Tyr, Trp, Thr aminosavak gyakrabban fordulnak elő a béta redős szerkezetekben. A résztvevő láncok orientációjának függvényében a béta-redő lehet paralel vagy antiparalel. I-3. ábra: A fehérjék béta-redő szerkezete. A béta-fordulat (kanyar) néhány aminosavból álló struktúra, amely két bétaredőt vagy alfa-hélixet köt össze (I-4. ábra). A Gly, Ser, Asp, Asn, Pro oldalláncok a béta fordulatos szerkezeteket preferálják. I-4. ábra: A fehérjék béta-fordulat szerkezete. A fehérjék feltekeredése során a másodlagos elemek összerendeződnek, először ún. szupermásodlagos elemek vagy modulok alakulnak ki, majd ezek további szerveződése alakítja ki a fehérjére jellemző háromdimenziós szerkezetet, a harmadlagos szerkezetet (I-5. ábra). Ezáltal alakulnak ki a fehérjemolekuláknak a funkció szempontjából kitüntetett kémiai struktúrái. A biológiailag aktív fehérjék funkciója csak ép (natív) harmadlagos szerkezet esetén biztosított. 16 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
17 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik I-5. ábra: A fehérjék harmadlagos szerkezete. Bizonyos fehérjék esetén nem egyetlen polipeptidlánc alkotja a funkcionáló molekulát. Az ilyen fehérjéket oligomer fehérjéknek hívjuk, míg az egyes alkotó polipeptidek a protomérek, illetve alegységek. Az ilyen típusú fehérjék esetén a fehérjék alegységükből történő felépítettségét negyedleges szerkezetnek nevezzük. Ez a több alegységes fehérjék esetében bír nagy jelentőséggel, ahol a harmadlagos szerkezettel rendelkező alegységek tovább rendeződnek és így nyerik el funkcionális formájukat (pl. hemoglobin). I.2.2 A lipidek tulajdonságai A lipidek az élő szervezet kémiailag igen heterogén csoportját alkotják. Közös fizikai-kémiai tulajdonságuk - ellentétben a fehérjékkel, a nukleinsavakkal és szénhidrátokkal különböző mértékű, de mindig meghatározó apolaritásuk. Vízoldékonyságuk csekély, következésképpen apoláris oldószerekben (pl. petroléter, kloroform, éter, benzol) jól oldódnak. A lipidek az élő szervezetben több fontosabb funkciót látnak el: 1.) Hatékony energiaforrások 2.) Jó hő- és elektromos szigetelő, valamint mechanikai védelmet nyújtó anyagok. 3.) Fehérjékkel képzett komplexeik (lipoproteinek) fontos sejtalkotórészek. 4.) A szervezet anyagcsere-folyamatait szabályozó anyagok (hormonok, vitaminok, stb.). A lipidek csoportosítása, mivel kémiailag különböző szerkezetű anyagok, meglehetősen önkéntes. A lipideket osztályozhatjuk az apoláris tulajdonságokért felelős komponensek szerkezete alapján. Így megkülönböztethetünk a.) zsírsav-származékokat (elszappanosítható lipideket) és b.) poliprenil-származékokat (nem-elszappanosítható lipideket). I Elszappanosítható lipidek Az elszappanosítható lipidek állandó összetevői a zsírsavak és a glicerin. További csoportosításuk alapját a két komponens mellett megtalálható szerkezeti elemek képezik. Ez alapján az elszappanosítható lipideket az alábbi csoportokba sorolhatjuk: 1. Egyszerű lipidek (trigliceridek) Neutrális zsírok (zsírok, növényi olajok) Azonosító szám: TÁMOP /1/A
18 Viaszok 2. Összetett lipidek 2a. Foszfolipidek Foszfogliceridek Szfingolipidek 2b. Glikolipidek Szfingolipidek Neutrális zsírok A neutrális zsírok az élőlények tartalék tápanyagai. Az állati (és emberi) sejtekben megtalálható neutrális zsírok páros szénatomszámú, szénatomot tartalmazó karbonsavak (zsírsavak) glicerinnel képzett észterei. Az emberi szervezetben a C 16 és a C 18 zsírsavak fordulnak elő legnagyobb mennyiségben. Közülük a legelterjedtebb a palmitinsav (16:0), a sztearinsav (18:0) és az olajsav (18:1 n-9). (Az 18:1 n-9 jelölés a 18 szénatomszámú zsírsavban megtalálható 1 darab C9-C10 atomok között elhelyezkedő szén-szén kettős kötés helyzetét jelöli.) A természetes zsírsavakban előforduló szén-szén kettős kötések konfigurációja a legtöbb esetben (Z). A szobahőmérsékleten szilárd triglicerideket zsíroknak, a folyadék állagúakat olajoknak nevezzük. Viaszok A viaszok hosszú szénláncú alkánok, és hosszú szénláncú alifás alkoholok telített zsírsavakkal képzett észtereinek az elegye. A viaszok gyümölcsök és külső rétegének védőhártyáját, madarak tollának víztaszító bevonatát képezik. Foszfogliceridek A foszfogliceridek elsősorban a biológiai membránok felépítésében vesznek részt. Szerkezeti jellemzőjük, hogy a glicerin két alkoholos hidroxilcsoportját zsírsav, míg az egyik láncvégi hidroxilcsoportját foszforsav észteresíti. Így alakul ki a foszfogliceridek alapvegyülete az L- -foszfatidsav (I-6. ábra). A celluláris foszfatidokban kizárólagosan L-konfigurációjú -foszfatidsav (2-(R)-foszfatidsav) fordul elő. I-6. ábra: Az L- -foszfatidsav (2-(R)-foszfatidsav) szerkezete. A foszfogliceridek egyik vége foszforsav részt és alkoholt tartalmaz, amelyek együttesen a poláros, míg a szénhidrogénláncot tartalmazó rész az apoláros részt alkotja; emiatt a foszfoglicerideket amfipatikus vegyületeknek hívjuk. A foszfogliceridek tehát poláros lipidek. A foszfogliceridek felépítésében a következő alkoholok vesznek részt: 18 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
19 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik Foszfoglicerid Alkoholkomponens Szerkezet/Összegképlet Foszfatidil-aminoetanol aminoetanol HOCH 2 CH 2 NH 2 (kefalin) Foszfatidil-kolin (lecitin) kolin HOCH 2 CH 2 N + (CH 3 ) 3 Foszfatidil-szerin szerin HOCH 2 CHNH 2 COOH Foszfatidil-inozitol mioinozitol C 6 H 12 O 6 Biszfoszfatidil-glicerin (kardiolipin) glicerin HOCH 2 CHOHCH 2 OH A foszfolipidek egy speciális csoportját képezik azok a származékok (plazmalogének), melyekben a glicerin C1-hidroxilcsoportjához éterkötéssel telített alifás láncú alkohol, vagy enoléter kötéssel, -helyzetben (E)-konfigurációjú kettős kötést tartalmazó telítetlen alkohol kapcsolódik. A vegyületek a foszfatidokhoz hasonló szerkezetű molekulákat képeznek, melyek elsősorban az izom- és idegmembránokban fordulnak elő nagyobb mennyiségben. Szfingolipidek A szfingolipidek olyan foszfolipidek, amelyeknek az alapvázát nem a glicerin, hanem egy 20 C-atomos aminoalkohol, a 4-szfingenin (szfingozin) alkotja. A szvingozin két aszimmetriás szénatomot tartalmaz. A természetben csak az egyik enantiomer (D-eritro-4-szfingenin) fordul elő (I-7. ábra). I-7. ábra: A szvingozin (D-eritro-4-szfingenin) szerkezete. A szfingolipidek általános felépítésében az aminocsoporthoz savamid kötéssel zsírsav, leggyakrabban sztearinsav kapcsolódik. Az alapváz C1-es pozíciójához glikozidos kötéssel cukorkomponens, vagy foszforsav-észter funkciós csoporton keresztül egyéb poláros csoport (pl. kolin) kapcsolódik. A kapcsolódó csoportok szerkezete alapján a szfingolipidek a (a) foszfolipidek vagy a (b) glikolipidek csoportjába sorolhatók. A foszfolipid csoportba sorolható, legelterjedtebb szfingomielinben a szvingozin aminocsoportját sztearinsav acilezi, míg a primer alkoholos hidroxilcsoporthoz foszforil-kolin (kolin-foszfát) kapcsolódik. A szfingolipidek legnagyobb csoportját azok molekulák képezik, melyekben a primer alkoholos hidroxilcsoporthoz glikozidos kötéssel cukorkomponens kapcsolódik. A cukorkomponens szerkezete alapján a vegyületek három csoportba sorolhatók: 1.) Neutrális glikoszfingolipidek (cerebrozidok), 2.) Negatív töltésű, sziálsavat tartalmazó szfingolipidek (gangliozidok), valamint 3.) Galaktocerebrozidok kénsavészterei (szulfatált glikolipidek). I Nem-elszappanosítható lipidek A nem-elszappanosítható lipidek főbb csoportjait a - terpének, Azonosító szám: TÁMOP /1/A
20 - szteroidok, - zsírban oldódó vitaminok (A, D, E, K), valamint a - prosztaglandinok képezik. A gyógyszerhatás fizikai-kémiai alapjainak megismerése szempontjából a nemelszappanosítható lipidek legfontosabb csoportját a szteroidok képezik. Ezért e tananyag keretében csak e származékok kerülnek tárgyalásra. A szteroidok összetett felépítésű, sokrétű biológiai funkcióval rendelkező vegyületek. Közös szerkezetük alapját a négy gyűrű kondenzációjával kialakult szteránvagy más néven gonánváz alkotja. A szervezetben szintetizálódó szteránvázas vegyületek (szteroidok) szintézisének előanyaga a koleszterin. A molekulában két metilcsoport (C10 és C13), egy alifás (izooktil) oldallánc (C17) valamint egy hidroxilcsoport (C3) található. A B gyűrűben egy kettős kötés van. A B/C és C/D gyűrűk transz-kapcsolódásúak, ezért a molekula elnyújtott térszerkezetű (I-8. ábra). A koleszterin szabad állapotban vagy zsírsavakkal képzett észterei formájában minden sejtben megtalálható. Részt vesz a sejtmembránok felépítésében is. I-8. ábra: A koleszterin szerkezete. HO H H 8 H A természetes szteroidok legfontosabb csoportjai a következők: 1. Szterinek. A koleszterinből származtatható, C3-helyzetben hidroxilcsoportot és C17-helyzetben szénhidrogénláncot hordozó vegyületek. 2. D-vitaminok. Vitaminhatású szterinszármazékok. Valójában nem vitaminok, mert prekurzoruk a szervezetben képződő koleszterin. 3. Epesavak. Alapvegyületük a C17-oldalláncban karboxilcsoportot hordozó kolánsav. Detergens hatású vegyületek. A zsírokat emulgeálják a gyomor-bél rendszerben. 4. Szteroid hormonok. A vegyületek két nagy csoportját a nemi hormonok, valamint a mellékvesekéreg-hormonok képviselik. 5. Szteroidglikozidok. Növényi szteroidszármazékok. A gyógyászatban szívelégtelenség kezelésére alkalmazható származékok (pl. digitoxin). 6. Szteroid-alkaloidok. Általában mérgező tulajdonságú, növényi származékok. Kiindulási anyagai lehetnek gyógyászatilag értékes szteroidszármazékok előállításának. I.2.3 A sejtmembránok szerkezete Az élő szervezetek alaki és működési egysége a sejt. A sejt belső terét a külső környezettől a sejthártya választja el, de egyben össze is köti azzal. Az általánosan elfogadott fluid-mozaik (folyékony-mozaik) membránmodell szerint a sejthártya váza egy foszfolipid kettősréteg. A foszfolipid molekulák apoláros részeikkel egymás fele néznek, köztük Van der Waals-erők összekötő kapocsként hatnak. A foszfatidokon 20 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
21 A gyógyszerhatás molekuláris alapjai. A gyógyszercélpontok és szerkezeti jellegzetességeik kívül más lipidek is megtalálhatók a membránban: a koleszterin a membránalkotók fixálását végzi, a glikolipidek (szfingomielin) a sejt azonosításában játszanak szerepet. A lipidalkotók függőleges irányban alig, oldalirányban azonban gyorsan mozognak, cserélnek helyet, egymással (laterális diffúzió), ezért a membrán félig folyékony (I-9. ábra). A sejthártya másik fontos összetevőjét a membránfehérjék csoportja adja. Ezek zömmel amfipatikus molekulák, azaz poláros és apoláros részeik is vannak. Ennek megfelelően strukturálódnak a membránba. A membránfehérjék lehetnek (a) perifériális fehérjék, vagy (b) integráns fehérjék. A perifériás fehérjék a membrán külső vagy belső felszínét képező hidrofil foszfatidrészekhez, vagy más membrán-fehérjékhez kötődnek. Az integráns fehérjék amfipatikusak, apoláros részeikkel beleolvadnak a kettős foszfatidréteg apoláros részébe. I-9. ábra: A sejthártya mozaikmodellje. A biológiai membránok kémiai összetételének tanulmányozása során felismerték, hogy a lipidek eltérő mennyiségben fordulnak elő a kettősréteg extracelluláris és intracelluláris oldalán. Így például az emberi vörösvértest membránjában a kolint tartalmazó foszfolipidek (szfingomielin és foszfatidil-kolin) szinte kizárólagosan az extracelluláris oldalon helyezkednek el. A primer aminocsoportot hordozó foszfolipidek (foszfatidil-etanolamin, foszfatidil-szerin) viszont az intracelluláris oldalon koncentráltabbak. A koleszterin szimmetrikus eloszlású, a plazmamembránok mindkét oldalán azonos mennyiségben mutatható ki (I-10. ábra) I-10. ábra: A foszfolipidek megoszlása az emberi vörösvértest plazmamembránjában. Azonosító szám: TÁMOP /1/A
22 I.3 Irodalom Guba F.: Orvosi biokémia. Medicina Könyvkiadó, Budapest (1988) Smith and Williams' Introduction to the Principles of Drug Design and Action. (Editor: Smith H.J.) Harwood Academic Publishers, Amsterdam (1998) Novák L., Nyitrai J., Hazai L.: Biomolekulák kémiája. MKE, Budapest (2001) Ádám V., Dux L., Faragó A., Fésüs L., Machovich R., Mandl J., Sümegi B.: Orvosi biokémia. Medicína Kiadó, Budapest (2001) Atkins P.W.: Fizikai kémia I-III. Nemzeti Tankönyvkiadó, Budapest (2002) Gergely P., Erdődi F., Vereb Gy.: Általános és bioszervetlen kémia. (Szerk.: Gergely P.) Semmelweis Kiadó, Budapest (2003) Gyógyszerészi kémia. Szerk.: Fülöp F., Noszál B., Szász Gy., Takácsné Novák K. Semmelweis Kiadó, Budapest (2010) A gyógyszerkutatás kémiája. Szerk. Keserű Gy. M. Akadémiai Kiadó, Budapest (2011) Gyógyszerek. Szerk. Faigl F. Elektronikus tankönyv. BME, Budapest (2011) Lemke T.L., Williams D.A., Roche V.F., Zito S.W.: Foye s Principles of Medicinal Chemistry, 7th Edition. Lippincott Williams and Wilkins, Philadelphia (2013) 22 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
23 Receptorok, mint gyógyszercélpontok II Receptorok, mint gyógyszercélpontok A receptorok az élővilág jelfelismerésre és továbbításra specializálódott makromolekulái. A szervezet receptorainak jelentős hányada ún. szenzoros receptor, melyek a látás, szaglás, hallás, mechanikai, kémiai vagy egyéb inger közvetítésében vesznek részt. Biokémiai értelemben a receptor olyan fehérje, amely egy bizonyos (általában kisméretű) molekulával kölcsönhatást alakít ki, és az annak következtében megváltozott háromdimenziós szerkezet a molekuláris környezetében további változásokat okoz. A receptorok jelfelismerő és jeltovábbító funkciója működési ciklus során valósul meg. Ennek első fázisa során egy extracelluláris eredetű szignál, vagy szignált indukáló molekula jut el/kötődik az (általában a sejtmembránba ágyazott) receptorhoz. Ennek eredményeképpen, megfelelő konformációs átrendeződés révén, a receptor továbbítja az információt az (elsődleges) effektornak, vagy egy jelátviteli molekulának (transducer). A jelátviteli molekulák intracellulárisan lokalizálódó ún. másodlagos hírvivő részeket (ionok, molekulák) aktiválnak, melyek a másodlagos effektorral történő kölcsönhatás eredményeképpen eredményezik a biológiai válaszreakciót (II-1. ábra). A receptorok a gyógyszeres terápiában használt hatóanyagok elsődleges célpontjai. A receptort specifikusan kötő anyagot ligandumnak, ezen belül a receptor aktivációját kiváltó anyagot agonistának, míg a receptor aktivációját gátló anyagot antagonistának nevezzük. II-1. ábra: A receptor, a másodlagos hírvivő és az effektor fogalma. Az eredeti receptor-teóriákban a receptor kémiai természete értelemszerűen nem volt részletes vizsgálatok tárgya. Az ismeretek szélesedésével és mélyülésével azonban ismertté vált, hogy az eredeti receptor fogalom számos celluláris makromolekulát, illetve makromolekulákból felépülő funkcionális egységet (célmolekulát) jelenthet. Így a gyógyszerhatást kiváltó gyógyszermolekula-celluláris célmolekula kölcsönhatások az alábbi fő csoportokba sorolhatók: 1. Kölcsönhatás receptorokkal 2. Kölcsönhatás metabolikus, regulatorikus enzimekkel 3. Kölcsönhatás transzporfehérjékkel, transzporterekkel 4. Kölcsönhatás strukturális fehérjékkel 5. Kölcsönhatás nukleinsavakkal Jelen fejezet a fenti beosztás szerint értelmezett receptorok természetével foglalkozik. Azonosító szám: TÁMOP /1/A
24 A gyógyszerek (testidegen anyagok) biológiai hatása gyakran egy ismert endogén vegyület (pl. acetilkolin, norepinefrin, szerotonin, gamma-aminovajsav, stb.) biológiai hatásának kialakulásában szerepet játszó receptorral kialakított kölcsönhatás eredménye. Így gyógyszerkutatás egyik fő célpontjai a receptorok, amelyeken ható gyógyszermolekulák a biológiai működéseket specifikusan befolyásolni képesek. Ahhoz, hogy egy testidegen molekula kötődése egy fehérjéhez receptorkötődésnek legyen tekinthető (más szóval, a fehérje receptornak legyen tekinthető) a következő legfontosabb kritériumnak kell megfelelnie: 1. A receptornak nagy affinitást kell mutatnia a ligandum iránt, 2. A receptornak nagyfokú szerkezeti és sztereospecificitást kell mutatnia a ligandummal szemben, 3. A receptor alacsony ligandum-koncentrációnál telíthető legyen, 4. A ligandum-receptor kölcsönhatás reverzibilis legyen, 5. A receptor expressziója mutasson megfelelő eloszlást és szöveti specificitást, 6. A ligandum megfelelő agonistákkal és antagonistákkal a receptor-kötődésből felszabadítható legyen, valamint 7. A ligandum in vitro receptor affinitása és in vivo farmakológiai hatásossága pozitív korrelációt mutasson. A receptorok működése és a receptorhoz kötődő anyagok hatáskiváltó képessége kvantitatív módon, ún. dózis-hatás összefüggésekkel is jellemezhető, melynek nagy jelentősége van a modern gyógyszerkutatásban. Ennek lényege, hogy amennyiben a ligandumot fokozatosan növekvő koncentrációban adjuk a receptorhoz, a kiváltott válasz mérteke először lassan, majd egyre meredekebben emelkedik - azzal párhuzamosan, hogy a receptorok kötőhelyeit elfoglalja - majd egy bizonyos koncentráció fölött már nem növelhető tovább, amikor már valamennyi kötőhely foglalt. A fokozatos dózis-hatás(válasz) görbe egyedi változást fejez ki egy adott gyógyszer növekvő koncentrációi mellett. A változás nagysága összefüggésben van a receptorok számával, melyekkel a gyógyszer kapcsolatba lép. E dózis-válasz görbék szemilogaritmikus (válasz-log dózis) formái jellegzetes szigmoid alakot öltenek, melyről leolvasható a ligandum hatékonysága (ED 50 ), vagyis a félmaximális hatáshoz szükséges ligandum dózis, illetve a hatáserőssége (E max ), ami a maximálisan kiváltható válasszal egyenlő (II-2. ábra). II-2. ábra: A dózis-válasz görbe különböző formái. A dózis-válasz görbe alakja és lefutása függ a ligandum (gyógyszer) receptorral szemben mutatott affinitásától és a belső aktivitástól. Az affinitás erősségét a dózisválasz görbe X tengelyhez viszonyított helyzete, míg a belső aktivitást a válasz nagysága határozza meg: 24 A projekt az Európai Unió támogatásával az Európai Szociális Alap társfinanszírozásávalvalósul meg
25 Receptorok, mint gyógyszercélpontok A hatékonyság (potency) az adott nagyságú hatás kiváltásához szükséges ligandum dózis (koncentráció). A gyógyszer hatékonysága azt fejezi ki, hogy mennyi gyógyszerre van szükség a hatás elérésére (pl. ED 50 ). A gyógyszer hatékonyságát a gyógyszer receptorhoz való affinitása határozza meg és az alkalmazott gyógyszer azon mennyisége, mely ahhoz szükséges, hogy a gyógyszer a receptort elérje. A gyógyszerhatás erőssége (efficacy) az a maximális gyógyszerhatás, amely egyáltalán elérhető az adott gyógyszerrel (E max ). A hatáserősséget számos tényező határozza meg, mint a gyógyszer-receptor komplexek száma, a gyógyszer képessége hogy aktiválja a receptort, ha kötődött (belső aktivitás) és a célszerv állapota. A meredekség (slope) a dózis-válasz görbe középső szakaszán mérhető. A meredekség gyógyszertől és hatástól függő. A különféle testidegen anyagok lipofil tulajdonságuktól függően extra vagy intracellulárisan lokalizálódó receptorokhoz kötődhetnek. A lipofil molekulák (pl. szteroid hormonok, tiroid hormonok, D 3 vitamin) a plazmamembrán lipid rétegén keresztül diffundálnak és intracelluláris receptorukhoz kötődnek. A hidrofil/vízoldékony vegyületek (pl. peptid hormonok, neurotranszmitterek), nem képesek áthatolni a lipidben gazdag rétegen, ezért hatásuk kiváltásához a membránba ágyazódó, a membrán felszínén lokalizálódó ligandum kötőhellyel bíró sejtfelszíni (extracelluláris) receptorokra van szükségük. A receptorok különböző típusait celluláris lokalizációik és funkcióik alapján a következő csoportokba sorolhatjuk 1.) Sejtfelszíni (extracelluláris) receptorok a.) Ligandum-aktivált ioncsatornák (ionotróp receptorok) b.) Saját enzimaktivitás nélküli receptorok (metabotróp receptorok) G-fehérje kapcsolt receptorok Tirozin-kinázhoz kapcsolt receptorok Proteolízisen keresztül szabályozó receptorok c.) Saját enzimaktivitással bíró receptorok (metabotróp receptorok) Tirozin-kináz receptorok Tirozin-foszfatáz receptorok Guanilát-cikláz receptorok Szerin/Treonin-kináz receptorok 2.).Intracelluláris receptorok d.) Intracelluláris sejtmag receptorok Homodimer receptorok Ösztrogén receptorok Androgén receptorok Progeszteron receptorok Glükokortikoid receptorok Mineralokortikoid receptorok Heterodimer receptorok Retinsav receptorok D 3 -vitamin receptorok Tiroid receptorok Azonosító szám: TÁMOP /1/A
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai
 Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
Dózis-válasz görbe A dózis válasz kapcsolat ábrázolása a legáltalánosabb módja annak, hogy bemutassunk eredményeket a tudományban vagy a klinikai gyakorlatban. Például egy kísérletben növekvő mennyiségű
neutrális zsírok, foszfolipidek, szteroidok karotinoidok.
 Lipidek A lipidek/zsírszerű anyagok az élőlényekben előforduló, változatos szerkezetű szerves vegyületek. Közös sajátságuk, hogy apoláris oldószerekben oldódnak. A lipidek csoportjába tartoznak: neutrális
Lipidek A lipidek/zsírszerű anyagok az élőlényekben előforduló, változatos szerkezetű szerves vegyületek. Közös sajátságuk, hogy apoláris oldószerekben oldódnak. A lipidek csoportjába tartoznak: neutrális
Lipidek. Lipidek. Viaszok. Lipidek csoportosítása. Csak apoláros oldószerben oldódó anyagok.
 Lipidek sak apoláros oldószerben oldódó anyagok. Lipidek (ak és származékaik, valamint olyan vegyületek, amelyek bioszintézisükben vagy biológiai szerepükben összefüggenek velük + szteroidok, zsíroldható
Lipidek sak apoláros oldószerben oldódó anyagok. Lipidek (ak és származékaik, valamint olyan vegyületek, amelyek bioszintézisükben vagy biológiai szerepükben összefüggenek velük + szteroidok, zsíroldható
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
BIOKÉMIA. Simonné Prof. Dr. Sarkadi Livia egyetemi tanár.
 BIOKÉMIA Simonné Prof. Dr. Sarkadi Livia egyetemi tanár e-mail: sarkadi@mail.bme.hu LIPIDEK Lipidek Lipidek ~ lipoidok ~ zsírszerű anyagok (görög lipos zsír ) kémiailag igen változatos vegyületcsoportok
BIOKÉMIA Simonné Prof. Dr. Sarkadi Livia egyetemi tanár e-mail: sarkadi@mail.bme.hu LIPIDEK Lipidek Lipidek ~ lipoidok ~ zsírszerű anyagok (görög lipos zsír ) kémiailag igen változatos vegyületcsoportok
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Dr. Mandl József BIOKÉMIA. Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek.
 Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
Dr. Mandl József BIOKÉMIA Aminosavak, peptidek, szénhidrátok, lipidek, nukleotidok, nukleinsavak, vitaminok és koenzimek Semmelweis Kiadó Semmelweis Orvostudományi Egyetem Orvosi Vegytani, Molekuláris
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
Biológiai membránok és membrántranszport
 Biológiai membránok és membrántranszport Biológiai membránok A citoplazma membrán funkciói: térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
Biológiai membránok és membrántranszport Biológiai membránok A citoplazma membrán funkciói: térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
Folyadékkristályok; biológiai és mesterséges membránok
 Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
Folyadékkristályok; biológiai és mesterséges membránok Dr. Voszka István Folyadékkristályok: Átmenet a folyadékok és a kristályos szilárdtestek között (anizotróp folyadékok) Fonal, pálcika, korong alakú
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
1. Előadás Membránok felépítése, mebrán raftok
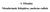 1. Előadás Membránok felépítése, mebrán raftok Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis biztosítása Klasszikus folyadékmozaik
1. Előadás Membránok felépítése, mebrán raftok Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis biztosítása Klasszikus folyadékmozaik
KARBONSAV-SZÁRMAZÉKOK
 KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
Szerkesztette: Vizkievicz András
 Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Fehérjék A fehérjék - proteinek - az élő szervezetek számára a legfontosabb vegyületek. Az élet bármilyen megnyilvánulási formája fehérjékkel kapcsolatos. A sejtek szárazanyagának minimum 50 %-át adják.
Kevéssé fejlett, sejthártya betüremkedésekből. Citoplazmában, cirkuláris DNS, hisztonok nincsenek
 1 A sejtek felépítése Szerkesztette: Vizkievicz András A sejt az élővilág legkisebb, önálló életre képes, minden életjelenséget mutató szerveződési egysége. Minden élőlény sejtes szerveződésű, amelyek
1 A sejtek felépítése Szerkesztette: Vizkievicz András A sejt az élővilág legkisebb, önálló életre képes, minden életjelenséget mutató szerveződési egysége. Minden élőlény sejtes szerveződésű, amelyek
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
térrészek elválasztása transzport jelátvitel Milyen a membrán szerkezete? Milyen a membrán szerkezete? lipid kettısréteg, hidrofil/hidrofób részek
 Biológiai membránok A citoplazma membrán funkciói: Biológiai membránok és membrántranszport térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
Biológiai membránok A citoplazma membrán funkciói: Biológiai membránok és membrántranszport térrészek elválasztása (egész sejt, organellumok) transzport jelátvitel Milyen a membrán szerkezete? lipidek
Szerkezet és funkció kapcsolata a membránműködésben. Folyadékkristályok típusai (1) Dr. Voszka István
 MODELLMEMBRÁNOK (LIPOSZÓMÁK) ORVOSI, GYÓGYSZERÉSZI ALKALMAZÁSA 2012/2013 II. félév II. 7. Szerkezet és funkció kapcsolata a membránműködésben Dr. Voszka István II. 21. Liposzómák előállítási módjai Dr.
MODELLMEMBRÁNOK (LIPOSZÓMÁK) ORVOSI, GYÓGYSZERÉSZI ALKALMAZÁSA 2012/2013 II. félév II. 7. Szerkezet és funkció kapcsolata a membránműködésben Dr. Voszka István II. 21. Liposzómák előállítási módjai Dr.
Szerkezet és funkció kapcsolata a membránműködésben. Folyadékkristályok típusai (1) Dr. Voszka István
 MODELLMEMBRÁNOK (LIPOSZÓMÁK) ORVOSI, GYÓGYSZERÉSZI ALKALMAZÁSA 2015/2016 II. félév Időpont: szerda 17 30-19 00 Helyszín Elméleti Orvostudományi Központ Szent-Györgyi Albert előadóterme II. 3. Szerkezet
MODELLMEMBRÁNOK (LIPOSZÓMÁK) ORVOSI, GYÓGYSZERÉSZI ALKALMAZÁSA 2015/2016 II. félév Időpont: szerda 17 30-19 00 Helyszín Elméleti Orvostudományi Központ Szent-Györgyi Albert előadóterme II. 3. Szerkezet
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
1. Bevezetés. Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei
 1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
1. Bevezetés Mi az élet, evolúció, információ és energiaáramlás, a szerveződés szintjei 1.1 Mi az élet? Definíció Alkalmas legyen különbségtételre élő/élettelen közt Ne legyen túl korlátozó (más területen
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE
 AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
Membrántranszport. Gyógyszerész előadás Dr. Barkó Szilvia
 Membrántranszport Gyógyszerész előadás 2017.04.10 Dr. Barkó Szilvia Sejt membránok A sejtmembrán funkciói Védelem Kommunikáció Molekulák importja és exportja Sejtmozgás Általános szerkezet Lipid kettősréteg
Membrántranszport Gyógyszerész előadás 2017.04.10 Dr. Barkó Szilvia Sejt membránok A sejtmembrán funkciói Védelem Kommunikáció Molekulák importja és exportja Sejtmozgás Általános szerkezet Lipid kettősréteg
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Farmakológus szakasszisztens Farmakológus szakasszisztens 2/34
 -06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
-06 Farmakológus szakasszisztens feladatok A 0/007 (II. 7.) SzMM rendelettel módosított /006 (II. 7.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés
3. Sejtalkotó molekulák III.
 3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
3. Sejtalkotó molekulák III. Fehérjék, fehérjeszintézis (transzkripció, transzláció, posztszintetikus módosítások). Enzimműködés 3.1 Fehérjék A genetikai információ egyik fő manifesztálódása Számos funkció
A sejtek élete. 5. Robotoló törpék és óriások Az aminosavak és fehérjék R C NH 2. C COOH 5.1. A fehérjeépítőaminosavak általános
 A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A sejtek élete 5. Robotoló törpék és óriások Az aminosavak és fehérjék e csak nézd! Milyen protonátmenetes reakcióra képes egy aminosav? R 2 5.1. A fehérjeépítőaminosavak általános képlete 5.2. A legegyszerűbb
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Élettan. előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45
 Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Membránszerkezet Nyugalmi membránpotenciál
 Membránszerkezet Nyugalmi membránpotenciál 2011.11.15. A biológiai membránok fő komponense. Foszfolipidek foszfolipid = diglicerid + foszfát csoport + szerves molekula (pl. kolin). Poláros fej (hidrofil)
Membránszerkezet Nyugalmi membránpotenciál 2011.11.15. A biológiai membránok fő komponense. Foszfolipidek foszfolipid = diglicerid + foszfát csoport + szerves molekula (pl. kolin). Poláros fej (hidrofil)
TRANSZPORTFOLYAMATOK A SEJTEKBEN
 16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
16 A sejtek felépítése és mûködése TRANSZPORTFOLYAMATOK A SEJTEKBEN 1. Sejtmembrán elektronmikroszkópos felvétele mitokondrium (energiatermelõ és lebontó folyamatok) citoplazma (fehérjeszintézis, anyag
Tel: ;
 BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
Bevezetés. Szénvegyületek kémiája Organogén elemek (C, H, O, N) Életerő (vis vitalis)
 Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
Hatóanyagok fizikai-kémiai tulajdonságai és a felszívódás összefüggése
 Hatóanyagok fizikai-kémiai tulajdonságai és a felszívódás összefüggése Völgyi Gergely Semmelweis Egyetem, Gyógyszerészi Kémiai Intézet Továbbképző előadás 2014. október 4. A gyógyszer szervezetbeni sorsát
Hatóanyagok fizikai-kémiai tulajdonságai és a felszívódás összefüggése Völgyi Gergely Semmelweis Egyetem, Gyógyszerészi Kémiai Intézet Továbbképző előadás 2014. október 4. A gyógyszer szervezetbeni sorsát
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
A fehérjék hierarchikus szerkezete
 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
BIOFIZIKA I OZMÓZIS Bugyi Beáta (PTE ÁOK Biofizikai Intézet) OZMÓZIS
 BIOFIZIKA I OZMÓZIS - 2010. 10. 26. Bugyi Beáta (PTE ÁOK Biofizikai Intézet) OZMÓZIS BIOFIZIKA I - DIFFÚZIÓ DIFFÚZIÓ - ÁTTEKINTÉS TRANSZPORTFOLYAMATOK ÁLTALÁNOS LEÍRÁSA ONSAGER EGYENLET lineáris, irreverzibilis
BIOFIZIKA I OZMÓZIS - 2010. 10. 26. Bugyi Beáta (PTE ÁOK Biofizikai Intézet) OZMÓZIS BIOFIZIKA I - DIFFÚZIÓ DIFFÚZIÓ - ÁTTEKINTÉS TRANSZPORTFOLYAMATOK ÁLTALÁNOS LEÍRÁSA ONSAGER EGYENLET lineáris, irreverzibilis
Szerves kémiai és biokémiai alapok:
 Szerves kémiai és biokémiai alapok: Másodlagos kémiai kötések: A másodlagos kötések energiája nagyságrenddel kisebb, mint az elsődlegeseké. Energiaközlés hatására a másodlagos kötések bomlanak fel először,
Szerves kémiai és biokémiai alapok: Másodlagos kémiai kötések: A másodlagos kötések energiája nagyságrenddel kisebb, mint az elsődlegeseké. Energiaközlés hatására a másodlagos kötések bomlanak fel először,
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT)
 BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
BIOLÓGIA ALAPJAI (BMEVEMKAKM1; BMEVEMKAMM1) Előadói: Dr. Bakos Vince, Kormosné Dr. Bugyi Zsuzsanna, Dr. Török Kitti, Nagy Kinga (BME ABÉT) Előadások anyaga: Dr. Pécs Miklós, Dr. Bakos Vince, Kormosné Dr.
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Gyógyszerészi kémia szigorlati tételek 2015/2016
 Gyógyszerészi kémia szigorlati tételek 2015/2016 1. Szedato-hipnotikus és anxiolitikus hatású vegyületek. A barbitursavszármazékok néhány képviselője. A benzodiazepinek típusai, példákkal. Szerkezet, fizikai
Gyógyszerészi kémia szigorlati tételek 2015/2016 1. Szedato-hipnotikus és anxiolitikus hatású vegyületek. A barbitursavszármazékok néhány képviselője. A benzodiazepinek típusai, példákkal. Szerkezet, fizikai
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék Szerkesztette: FAIGL FERENC Írta: FAIGL FERENC, SZEGHY LAJOS, KOVÁCS ERVIN, MÁTRAVÖLGYI
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék Szerkesztette: FAIGL FERENC Írta: FAIGL FERENC, SZEGHY LAJOS, KOVÁCS ERVIN, MÁTRAVÖLGYI
Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet
 Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet Az ioncsatorna fehérjék szerkezete, működése és szabályozása Panyi György www.biophys.dote.hu Mesterséges membránok
Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet Az ioncsatorna fehérjék szerkezete, működése és szabályozása Panyi György www.biophys.dote.hu Mesterséges membránok
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
LIPID ANYAGCSERE (2011)
 LIPID ANYAGCSERE LIPID ANYAGCSERE (2011) 5 ELİADÁS: 1, ZSÍRK EMÉSZTÉSE, FELSZÍVÓDÁSA + LIPPRTEINEK 2, ZSÍRSAVAK XIDÁCIÓJA 3, ZSÍRSAVAK SZINTÉZISE 4, KETNTESTEK BIKÉMIÁJA, KLESZTERIN ANYAGCSERE 5, MEMBRÁN
LIPID ANYAGCSERE LIPID ANYAGCSERE (2011) 5 ELİADÁS: 1, ZSÍRK EMÉSZTÉSE, FELSZÍVÓDÁSA + LIPPRTEINEK 2, ZSÍRSAVAK XIDÁCIÓJA 3, ZSÍRSAVAK SZINTÉZISE 4, KETNTESTEK BIKÉMIÁJA, KLESZTERIN ANYAGCSERE 5, MEMBRÁN
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások
 Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Gyógyszer-élelmiszer kölcsönhatások
 Gyógyszer-élelmiszer kölcsönhatások Dietetikus MSc. képzés Dr. Horváth Péter Semmelweis Egyetem Gyógyszerészi Kémiai Intézet TEMATIKA Bevezetés Alapfogalmak Gyógyszerhatás kialakulása Gyógyszerek tulajdonságait
Gyógyszer-élelmiszer kölcsönhatások Dietetikus MSc. képzés Dr. Horváth Péter Semmelweis Egyetem Gyógyszerészi Kémiai Intézet TEMATIKA Bevezetés Alapfogalmak Gyógyszerhatás kialakulása Gyógyszerek tulajdonságait
Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése
 Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése Előadó: Lihi Norbert Debreceni Egyetem Szervetlen és Analitikai Kémiai Tanszék Bioszervetlen Kémiai Kutatócsoport A bioszervetlen
Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése Előadó: Lihi Norbert Debreceni Egyetem Szervetlen és Analitikai Kémiai Tanszék Bioszervetlen Kémiai Kutatócsoport A bioszervetlen
A fehérjék hierarchikus szerkezete
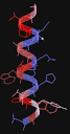 Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Fehérjék felosztása A fehérjék hierarchikus szerkezete Smeller László Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biológiai funkció alapján Enzimek (pl.: tripszin, citokróm-c ) Transzportfehérjék
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
 9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
9. Előadás Fehérjék Előzmények Peptidkémia Analitikai kémia Protein kémia 1901 E.Fischer : Gly-Gly 1923 F. Pregl : Mikroanalitika 1952 Stein and Moore : Aminosav analizis 1932 Bergman és Zervas : Benziloxikarbonil
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK A membránok minden sejtnek lényeges alkotórészei. Egyrészt magát a sejtet határolják - ez a sejtmembrán vagy
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA A BIOLÓGIAI MEMBRÁNOK 1. kulcsszó cím: MEMBRÁNOK A membránok minden sejtnek lényeges alkotórészei. Egyrészt magát a sejtet határolják - ez a sejtmembrán vagy
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
TestLine - Biogén elemek, molekulák Minta feladatsor
 TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
TestLine - iogén elemek, molekulák iogén elemek, szervetlen és szerves molekulák az élő szervezetben. gészítsd ki a mondatot! aminocsoportja kondenzáció víz ún. peptidkötés 1. 1:48 Normál fehérjék biológiai
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
A fehérjék szerkezeti hierarchiája. Fehérje-szerkezetek! Klasszikus szerkezet-funkció paradigma. szekvencia. funkció. szerkezet! Myoglobin.
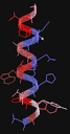 Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
Myoglobin Fehérje-szerkezetek! MGLSDGEWQLVLNVWGKVEADIPGGQEVLIRLFK GPETLEKFDKFKLKSEDEMKASE DLKKGATVLTALGGILKKKGEAEIKPLAQSA TKKIPVKYLEFISECIIQVLQSK PGDFGADAQGAMNKALELFRKDMASNYKELGFQG Fuxreiter Mónika! Debreceni
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
Szénhidrátok. Szénhidrátok. Szénhidrátok. Csoportosítás
 Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B
 SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET 2013/14. II. félév 1 Tartalomjegyzék 1. Tantárgyleírás,
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM229B TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET 2013/14. II. félév 1 Tartalomjegyzék 1. Tantárgyleírás,
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék. elrendeződés, rend, rendszer, periodikus ismétlődés
 Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
Az élő anyag szerkezeti egységei: víz, nukleinsavak, fehérjék Agócs Gergely 2013. december 3. kedd 10:00 11:40 1. Mit értünk élő anyag alatt? Az élő szervezetet felépítő anyagok. Az anyag azonban nem csupán
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
Gyógyszermetabolizmus és gyógyszertoxicitás
 Gyógyszermetabolizmus és gyógyszertoxicitás Perjési Pál Megújuló gyógyszerészi kompetenciák gyakorlatorientált elsajátítását szolgáló digitális tananyagok fejlesztése magyar és angol nyelven, az egyetemi
Gyógyszermetabolizmus és gyógyszertoxicitás Perjési Pál Megújuló gyógyszerészi kompetenciák gyakorlatorientált elsajátítását szolgáló digitális tananyagok fejlesztése magyar és angol nyelven, az egyetemi
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Az élő sejt fizikai Biológiája:
 Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
Az élő sejt fizikai Biológiája: Modellépítés, biológiai rendszerek skálázódása Kellermayer Miklós Fizikai biológia Ma már nem csak kvalitatív megfigyeléseket, hanem kvantitatív méréseket végzünk (biológiai
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Transzporterek vizsgálata lipidmembránokban Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest
 Transzporterek vizsgálata lipidmembránokban 2016. Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest Membrántranszport fehérjék típusok, lipid-kapcsolatok A membránok szerkezete
Transzporterek vizsgálata lipidmembránokban 2016. Sarkadi Balázs MTA-SE Molekuláris Biofizikai Kutatócsoport, MTA-TTK Budapest Membrántranszport fehérjék típusok, lipid-kapcsolatok A membránok szerkezete
