Elektrokémia 04. Cellareakció potenciálja, elektródreakció potenciálja, termodinamikai paraméterek meghatározása példa. Láng Győző
|
|
|
- Piroska Török
- 5 évvel ezelőtt
- Látták:
Átírás
1 Elektokémi 04. Cellekció potenciálj, elektódekció potenciálj, temodinmiki pméteek meghtáozás péld Láng Győző Kémii Intézet, Fiziki Kémii Tnszék Eötvös Loánd Tudományegyetem Budpest
2 Az elmélet lklmzás konkét cellekció A cellekcióekció: C 6 H 4(OH) Ag C6H 4O H Ag
3 A cellekció stndd szbdentlpi változás: G o FE 5 C MF RT ln Q H Q H Ag Ag A csk szilád fázisbn jelen lévő komponensek (Ag), eltív ktivitását egységnyi. A szilád fázisbn is jelenlévő komponenseke nézve z oldt telített (H Q, Q), ezét kémii potenciáljuk z oldtbn egyenlő szilád fázisbn vett kémii potenciálll. A szilád fázisbn kinon és hidokinon eltív ktívitásánk ány egységnyi, mint hogyn folydékfázisbn is.
4 A cellekció stndd szbdentlpi változás tehát: 5 C H FEMF RT ln G Ag [ ] 5 C H FEMF RT ln G [ ] [ Ag ] S F E T MF p R ln H [ Ag ] 5 C H FEMF FT Hiszen H G T S. E T MF p
5 AZ ELMÉLETI ÖSSZEFÜGGÉSEK ALKALMAZÁSA: TERMODINAMIKAI PARAMÉTEREK SZÁMÍTÁSA GALVÁNCELLA ELEKTROMOTOROS ERÉJÉNEK HŐMÉRSÉKLETFÜGGÉSÉBŐL (dott x -hez ttozó y éték hibhtáink becslése)
6 A 10-3 M Ag ion ttlmú glváncell elektomotoos eejének hőmésékletfüggésének méése soán kpott dtok: -0,015-0,00-0,05 E MF /V -0,030-0,035-0, T/ C Egy glváncell elektomotoos eejének hőmésékletfüggése
7 95%-os sttisztikus biztonság mellett: α 5 %, f n- 11, t α, Az illesztett egyenes egyenlete: E MF ( -4 4, V/ ) T 0, V C A szóások: meedekség szóás: 6 Sb 4, V / C eziduális szóás: S eziduális 1, V
8 A egessziós egyenletből számított E 5 C MF hibhtái A konfidencihtáok számításá vontkozó összefüggés: y, j ± t α S y S y * 1 Seziduális n n (, x x) ( x ) j x j 1 j, x j 5 C
9 Az Y szóásánk számítás és z hhoz szükséges segédmennyiségek képzése x 35,0 S y 1, ,5 6, V
10 Az elektomotoos eő hibhtái: E 5 C MF ( 5 0,0648 ±,0 6, ) ( 0,0648 ± 0,001395)V V E G hibhtáink számítás: ( 0,0648 0,00014)V 5 C MF ± G zfe 5 C MF ( 5110,6 ± 69,)J/mol ( 0,0648 ± 0,001395) J/mol G ( 5,11 0,7)kJ/mol ±
11 ± Ebből z dtból láthtó, hogy ebben cellábn ekció játszódik le önként! G ( 5,11 0,7)kJ/mol ( ) OH C6H 4O H Ag C6H 4 Ag
12 S hibhtáink számítás: EMF S zf zf b T ( ± t S ) ( , ±,0 4, ) ( ) ,089 ± 1,9664 J mol K p α b S (- 85,1± 1,9) J mol K vgy (-85 ± ) J mol K G hibhtáink számítás: A temodinmiki mennyiség számítás: G o FE 5 C MF RT ln [ ] H [ Ag ]
13 G hibhtáink számítás: Az elektomotoos eő hibhtáit is behelyettesítve: G 0, ( 0,0648 ± 0,001395) 8,314 98,15 ln 3 10 ([ ( 0,0648 ± 0,001395) ] 831) J/mol ( 1770 ± 69)J/mol J/mol (-17,7 0,7)kJ/mol G ± A szögletes záójelben lévő mennyiséget má G számításko megdtuk, így most kevesebb munkávl kpjuk végeedményt. A többi temodinmiki mennyiség számításánál fentiekkel nlóg módon jáunk el.
14 A temodinmiki egyensúlyi állndó hibhtái: Mivel G RT ln K hol K cellekció egyensúlyi állndój. Így K számíthtó következő egyenlet lpján: K exp G RT (Temészetesen G -t előjelhelyesen kell behelyettesíteni.) Itt háom lépésben kpjuk hibhtáokt. Előszö G -t helyettesítjük be, mjd hibhtál növelt, illetve csökkentett étéket. Ezzel háom db K -t kpunk. A hibhtáokt z elsőként kpott dthoz képest djuk meg pozitív és negtív iánybn.,
15 K exp ,314 98,15 17, K exp 1141,4 K exp 1415, 4 8,314 98,15 8,314 98,15 innen hibhtáok: K ( 0,14 ) 3 1,7 ± 0,13 10 Amint z eedmény muttj nem szimetikus hibhtáokt kpunk mint z előzőekben, met itt nemlineáis függvénynyel számolunk. A G hibhtáink növekedésével nő ez z sszimeti, csökkenésével pedig el is tűnhet (leglábbis hibhtá második jegyében nem jelentkezik).
16
17
AZ EGYENSÚLYI ÁLLANDÓ HMÉRSÉKLET ÉS NYOMÁSFÜGGÉSE
 AZ EGYENSÚLYI ÁLLANDÓ HMÉRSÉLE ÉS NYOMÁSFÜGGÉSE A mésékletfüggés Egyensúlybn: zz G + R ln egyensúlyi G + R ln Átlkítv: ln G R A stndd ekció szbdentli kifejezését sználv ideális gázok: ln R µ vgy áltlábn
AZ EGYENSÚLYI ÁLLANDÓ HMÉRSÉLE ÉS NYOMÁSFÜGGÉSE A mésékletfüggés Egyensúlybn: zz G + R ln egyensúlyi G + R ln Átlkítv: ln G R A stndd ekció szbdentli kifejezését sználv ideális gázok: ln R µ vgy áltlábn
Eredeti Veszprémi T. (digitálisan Csonka G) jegyzet: X. fejezet
 2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
2011/2012 tvsi félév 7. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyserű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 ) Másodfjú
Elektrokémia 05. Elektródreakciók kinetikája. Láng Győző. Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem Budapest
 Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W G v,,, G v,,, z ϕ αzf G G, ( ) ϕ zf α G G 1, ϕ αzf G
Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W G v,,, G v,,, z ϕ αzf G G, ( ) ϕ zf α G G 1, ϕ αzf G
Elektrokémia 03. (Biologia BSc )
 lektokéma 03. (Bologa BSc ) Cellaeakcó potencálja, elektódeakcó potencálja, Nenst-egyenlet Láng Győző Kéma Intézet, Fzka Kéma Tanszék ötvös Loánd Tudományegyetem Budapest Cellaeakcó Közvetlenül nem méhető
lektokéma 03. (Bologa BSc ) Cellaeakcó potencálja, elektódeakcó potencálja, Nenst-egyenlet Láng Győző Kéma Intézet, Fzka Kéma Tanszék ötvös Loánd Tudományegyetem Budapest Cellaeakcó Közvetlenül nem méhető
Elektrokémia 05. Elektródreakciók kinetikája. Láng Győző. Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
 Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W ,, G G v,, v, z, G G, αzf F ϕ, G G 1 ( α ) zf ϕ zf,,
Eletroém 5. Eletródreó netá Láng Győző Kém Intézet, Fz Kém Tnszé Eötvös Loránd Tudományegyetem Budpest Átlépés polrzáó ( z ) ( e z e ) ( e) S W ,, G G v,, v, z, G G, αzf F ϕ, G G 1 ( α ) zf ϕ zf,,
Elektrokémia 02. (Biologia BSc )
 Elektokéma 02. (Bologa BSc ) Elektokéma cella, Kapocsfeszültség, Elektódpotencál, Elektomotoos eő Láng Győző Kéma Intézet, Fzka Kéma Tanszék Eötvös Loánd Tudományegyetem Budapest Temodnamka paaméteek TERMODINAMIKAI
Elektokéma 02. (Bologa BSc ) Elektokéma cella, Kapocsfeszültség, Elektódpotencál, Elektomotoos eő Láng Győző Kéma Intézet, Fzka Kéma Tanszék Eötvös Loánd Tudományegyetem Budapest Temodnamka paaméteek TERMODINAMIKAI
1. feladat Oldja meg a valós számok halmazán a következő egyenletet: 3. x log3 2
 A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
A 004/005 tnévi Országos Középiskoli Tnulmányi Verseny második fordulójánk feldtmegoldási MATEMATIKÁBÓL ( I ktegóri ) feldt Oldj meg vlós számok hlmzán következő egyenletet: log log log + log Megoldás:
Elektrokémia Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı.
 Elektrokémia 2012. Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı Láng Gyızı Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
Elektrokémia 2012. Kiegészítés a praktikumhoz Elektrokémiai cella, Kapocsfeszültség, Elektródpotenciál, Elektromotoros erı Láng Gyızı Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym TMt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. évfolym TMt2 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 15:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
EA. Elektrokémia alap mérés: elektromotoros erő és kapocsfeszültség mérése a Daniell cellában, az EMF koncentráció függése
 EA. Elektrokémia alap mérés: elektromotoros erő és kapocsfeszültség mérése a Daniell cellában, az EMF koncentráció függése Előkészítő előadás 2018.02.19. Alapfogalmak Elektrokémiai cella: olyan rendszer,
EA. Elektrokémia alap mérés: elektromotoros erő és kapocsfeszültség mérése a Daniell cellában, az EMF koncentráció függése Előkészítő előadás 2018.02.19. Alapfogalmak Elektrokémiai cella: olyan rendszer,
Kémiai alapismeretek 11. hét
 Kémiai alapismeretek 11. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2011. május 3. 1/8 2009/2010 II. félév, Horváth Attila c Elektród: Fémes
Kémiai alapismeretek 11. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2011. május 3. 1/8 2009/2010 II. félév, Horváth Attila c Elektród: Fémes
Elektrokémia 03. Cellareakció potenciálja, elektródreakció potenciálja, Nernst-egyenlet. Láng Győző
 lektrokéma 03. Cellareakcó potencálja, elektródreakcó potencálja, Nernst-egyenlet Láng Győző Kéma Intézet, Fzka Kéma Tanszék ötvös Loránd Tudományegyetem Budapest Cellareakcó Közvetlenül nem mérhető (
lektrokéma 03. Cellareakcó potencálja, elektródreakcó potencálja, Nernst-egyenlet Láng Győző Kéma Intézet, Fzka Kéma Tanszék ötvös Loránd Tudományegyetem Budapest Cellareakcó Közvetlenül nem mérhető (
2012/2013 tavaszi félév 9. óra
 2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
2012/2013 tvszi félév 9. ór Elektródpotenciálok, Stndrd elektródpotenciál foglm Egyszerű fémelektródok, oxelektródok (pl. Sn 2+ /Sn 4+ ) ph-függő redoxelektródok (pl. Mn 2+ /MnO 4, Cr 3+ /Cr 2 O 7 2 )
Elektrokémiai gyakorlatok
 Elektrokémiai gyakorlatok Az elektromos áram hatására bekövetkezı kémiai változásokkal, valamint a kémiai energia elektromos energiává alakításának folyamataival, törvényszerőségeivel foglalkozik. A változást
Elektrokémiai gyakorlatok Az elektromos áram hatására bekövetkezı kémiai változásokkal, valamint a kémiai energia elektromos energiává alakításának folyamataival, törvényszerőségeivel foglalkozik. A változást
Általános Kémia GY 4.tantermi gyakorlat
 Általános Kémia GY 4.tantermi gyakorlat Csapadékképződési egyensúlyok, oldhatósági szorzat Termokémiai számítások Hess tétel Közömbösítési hő meghatározása kísérlet (példaszámítás: 4. labor leírásánál)
Általános Kémia GY 4.tantermi gyakorlat Csapadékképződési egyensúlyok, oldhatósági szorzat Termokémiai számítások Hess tétel Közömbösítési hő meghatározása kísérlet (példaszámítás: 4. labor leírásánál)
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
13 Elektrokémia. Elektrokémia Dia 1 /52
 13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
13 Elektrokémia 13-1 Elektródpotenciálok mérése 13-2 Standard elektródpotenciálok 13-3 E cella, ΔG és K eq 13-4 E cella koncentráció függése 13-5 Elemek: áramtermelés kémiai reakciókkal 13-6 Korrózió:
Ez a kifejezés ekvivalens a termokémia részben már megismert standard reakció szabadentalpiával! A termodinamikai egyensúlyi állandó: egyensúlyi
 ÜLÖNÖZ REACIÓ EGYENSÚLYI ÁLLANDÓ Egyensúlybn: r G + RT ln Az egyenlet els tgj különböz ódokon írhtó el stndrd állotok egválsztásától üggen Ezek szerint ásodik tg s így z állndó értéke is változik h különböz
ÜLÖNÖZ REACIÓ EGYENSÚLYI ÁLLANDÓ Egyensúlybn: r G + RT ln Az egyenlet els tgj különböz ódokon írhtó el stndrd állotok egválsztásától üggen Ezek szerint ásodik tg s így z állndó értéke is változik h különböz
Az előadás vázlata:
 Az előadás vázlata: I. emokémiai egyenletek. A eakcióhő temodinamikai definíciója. II. A standad állapot. Standad képződési entalpia. III. Hess-tétel. IV. Reakcióentalpia számítása képződési entalpia (képződéshő)
Az előadás vázlata: I. emokémiai egyenletek. A eakcióhő temodinamikai definíciója. II. A standad állapot. Standad képződési entalpia. III. Hess-tétel. IV. Reakcióentalpia számítása képződési entalpia (képződéshő)
TERMOELEKTROMOS HŰTŐELEMEK VIZSGÁLATA
 9 MÉRÉEK A KLAZKU FZKA LABORATÓRUMBAN TERMOELEKTROMO HŰTŐELEMEK VZGÁLATA 1. Bevezetés A termoelektromos jelenségek vizsgált etekintést enged termikus és z elektromos jelenségkör kpcsoltár. A termoelektromos
9 MÉRÉEK A KLAZKU FZKA LABORATÓRUMBAN TERMOELEKTROMO HŰTŐELEMEK VZGÁLATA 1. Bevezetés A termoelektromos jelenségek vizsgált etekintést enged termikus és z elektromos jelenségkör kpcsoltár. A termoelektromos
Általános Kémia, 2008 tavasz
 9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
9 Elektrokémia 9-1 Elektródpotenciálok mérése 9-1 Elektródpotenciálok mérése 9-2 Standard elektródpotenciálok 9-3 E cell, ΔG, és K eq 9-4 E cell koncentráció függése 9-5 Elemek: áramtermelés kémiai reakciókkal
7 Elektrokémia. 7-1 Elektródpotenciálok mérése
 7 Elektrokémia 7-1 Elektródpotenciálok mérése 7-2 Standard elektródpotenciálok 7-3 E cell, ΔG, és K eq 7-4 E cell koncentráció függése 7-5 Elemek: áramtermelés kémiai reakciókkal 7-6 Korrózió: nem kívánt
7 Elektrokémia 7-1 Elektródpotenciálok mérése 7-2 Standard elektródpotenciálok 7-3 E cell, ΔG, és K eq 7-4 E cell koncentráció függése 7-5 Elemek: áramtermelés kémiai reakciókkal 7-6 Korrózió: nem kívánt
KÉMIA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia emelt szint 1212 ÉRETTSÉGI VIZSGA 2013. október 22. KÉMIA EMELT SZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének
Kémia emelt szint 1212 ÉRETTSÉGI VIZSGA 2013. október 22. KÉMIA EMELT SZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének
 ó Ü ő É ó ó ő Ó Ó í ő ó ő Ö É ó ő ú Ü í ó Ú ő Ó Ó í ó ő ó É ó É ó ö ö ű Ö ő Ó ő ó ó Éó Ó É Ó Ó Ő ó É ó ó Ó É Ó ó ö í Ó ö í ű Ó í í ö Ü ű ó í ó ö ű Ó Ö Ö ó Ö Ó í ö ü ű ú ü ú ő ó í ó ó Ú ú í í í ó Ö ü ő
ó Ü ő É ó ó ő Ó Ó í ő ó ő Ö É ó ő ú Ü í ó Ú ő Ó Ó í ó ő ó É ó É ó ö ö ű Ö ő Ó ő ó ó Éó Ó É Ó Ó Ő ó É ó ó Ó É Ó ó ö í Ó ö í ű Ó í í ö Ü ű ó í ó ö ű Ó Ö Ö ó Ö Ó í ö ü ű ú ü ú ő ó í ó ó Ú ú í í í ó Ö ü ő
 Á Á Á Á Á ö ő ü Ü ö ő ú ű ő ü ü ő ű ö ű ő ö ö ő ö ő ő ő ő ő ő ő ő ő ű ő ő ű ö ö ö ő ő Ü ő ő ű ö ő ő Ü ű ö ö ö ö ö ö ö ü ö ö ú ü ő ü ű ö ö ü ű ő ö ő ö ő ű ő ö ő ü ö ű ő ö ö Ü ö ö ő ő ö ő ű ő ő ü ö ő ő ú
Á Á Á Á Á ö ő ü Ü ö ő ú ű ő ü ü ő ű ö ű ő ö ö ő ö ő ő ő ő ő ő ő ő ő ű ő ő ű ö ö ö ő ő Ü ő ő ű ö ő ő Ü ű ö ö ö ö ö ö ö ü ö ö ú ü ő ü ű ö ö ü ű ő ö ő ö ő ű ő ö ő ü ö ű ő ö ö Ü ö ö ő ő ö ő ű ő ő ü ö ő ő ú
 É ö í ö í í ű ö ö ú í í ú í ó Ó ö ú í ö ú í ű ö ü ó ü ó í ó ó ű ü í ű ö ó ó í ö Ü Ó í ó ű ó í ó ö ü ó í í ö ö í ó ö ú í ó ó í ó Ü ó í ü ű ö ü ó ó ö ö ö ö í ö ú Ó í í í ü ó ö ü í ó í Á Ó í ó ó ó ú Á ö í
É ö í ö í í ű ö ö ú í í ú í ó Ó ö ú í ö ú í ű ö ü ó ü ó í ó ó ű ü í ű ö ó ó í ö Ü Ó í ó ű ó í ó ö ü ó í í ö ö í ó ö ú í ó ó í ó Ü ó í ü ű ö ü ó ó ö ö ö ö í ö ú Ó í í í ü ó ö ü í ó í Á Ó í ó ó ó ú Á ö í
 ű ü ű ű ű ű ö Á ö ö ú ú ö ö ö ü ö ö ö ű ö ú ú ű ö ö ü ö ö ú ö ü ü ö ü ö ű ö ö ü ö ö ü ö ü ü ü ö ö ö ö ű ö ű ü ö ö ü ű ö ü ö ű ü ű ö ö ú ű ö ú ö ö ü ű ű ö ű ü ö ű ö ö ö ú ö ü ö ö ö ö ú ü ü ö ö ü ö ö ö ö
ű ü ű ű ű ű ö Á ö ö ú ú ö ö ö ü ö ö ö ű ö ú ú ű ö ö ü ö ö ú ö ü ü ö ü ö ű ö ö ü ö ö ü ö ü ü ü ö ö ö ö ű ö ű ü ö ö ü ű ö ü ö ű ü ű ö ö ú ű ö ú ö ö ü ű ű ö ű ü ö ű ö ö ö ú ö ü ö ö ö ö ú ü ü ö ö ü ö ö ö ö
 É á á á ö á á á á á á á á á ű á á á á á á á ű á á á ö á á á á á á á á á á á á á á á ű á ű á á á ö á á ú á á á á á ö ű á ű á á ü á á á É É ú É ü É ü Ú Á É ú Ú Á É Ü É Ú É Ú ű á ű á á ü Í Ú ü Á á É É ű á
É á á á ö á á á á á á á á á ű á á á á á á á ű á á á ö á á á á á á á á á á á á á á á ű á ű á á á ö á á ú á á á á á ö ű á ű á á ü á á á É É ú É ü É ü Ú Á É ú Ú Á É Ü É Ú É Ú ű á ű á á ü Í Ú ü Á á É É ű á
OPTIMALIZÁLÁS LAGRANGE-FÉLE MULTIPLIKÁTOR SEGÍTSÉGÉVEL
 OPTIMALIZÁLÁS LAGRANGE-FÉLE MULTIPLIKÁTOR SEGÍTSÉGÉVEL HAJDER LEVENTE 1. Bevezetés A Lgrnge-féle multiplikátoros eljárást Joseph Louis Lgrnge (1736-1813) olsz csillgász-mtemtikus (eredeti nevén Giuseppe
OPTIMALIZÁLÁS LAGRANGE-FÉLE MULTIPLIKÁTOR SEGÍTSÉGÉVEL HAJDER LEVENTE 1. Bevezetés A Lgrnge-féle multiplikátoros eljárást Joseph Louis Lgrnge (1736-1813) olsz csillgász-mtemtikus (eredeti nevén Giuseppe
Megjegyzések a mesterséges holdak háromfrekvenciás Doppler-mérésének hibaelemzéséhez
 H E L L E R MÁRTA DR. FERENCZ CSABA Megjegyzések esteséges holdk háofekvencás Dopple-éésének hbelezéséhez ETO 62.396.962.33.8.46: 629.783: 88.3.6 Mnt z á előző ckkünkből [] s set, kuttás bn és esteséges
H E L L E R MÁRTA DR. FERENCZ CSABA Megjegyzések esteséges holdk háofekvencás Dopple-éésének hbelezéséhez ETO 62.396.962.33.8.46: 629.783: 88.3.6 Mnt z á előző ckkünkből [] s set, kuttás bn és esteséges
Redox reakciók. azok a reakciók, melyekben valamely atom oxidációs száma megváltozik.
 Redox reakciók azok a reakciók, melyekben valamely atom oxidációs száma megváltozik. Az oxidációs szám megadja, hogy egy atomnak mennyi lenne a töltése, ha gondolatban a kötő elektronpárokat teljes mértékben
Redox reakciók azok a reakciók, melyekben valamely atom oxidációs száma megváltozik. Az oxidációs szám megadja, hogy egy atomnak mennyi lenne a töltése, ha gondolatban a kötő elektronpárokat teljes mértékben
Anyagvizsgálati módszerek Elektroanalitika. Anyagvizsgálati módszerek
 Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
Anyagvizsgálati módszerek Elektroanalitika Anyagvizsgálati módszerek Pannon Egyetem Mérnöki Kar Anyagvizsgálati módszerek Optikai módszerek 1/ 18 Potenciometria Potenciometria olyan analitikai eljárások
A REAKCIÓKINETIKA ALAPJAI
 A REAKCIÓKINETIKA ALAPJAI Egy kémiai reakció sztöchiometriai egyenletének általános alakja a következő formában adható meg k i=1 ν i A i = 0, (1) ahol A i a reakcióban résztvevő i-edik részecske, ν i pedig
A REAKCIÓKINETIKA ALAPJAI Egy kémiai reakció sztöchiometriai egyenletének általános alakja a következő formában adható meg k i=1 ν i A i = 0, (1) ahol A i a reakcióban résztvevő i-edik részecske, ν i pedig
Kémiai egyensúly. Fizikai kémia előadások 6. Turányi Tamás ELTE Kémiai Intézet. ν j sztöchiometriai együttható
 émiai egyensúly Fizikai kémia előadások 6. Tuányi Tamás ELTE émiai Intézet Sztöchiometiai együttható ν sztöchiometiai együttható általános kémiai eakció: (a temokémiában használtuk előszö) ν A 0 ν A eaktánsa
émiai egyensúly Fizikai kémia előadások 6. Tuányi Tamás ELTE émiai Intézet Sztöchiometiai együttható ν sztöchiometiai együttható általános kémiai eakció: (a temokémiában használtuk előszö) ν A 0 ν A eaktánsa
Általános Kémia GY 3.tantermi gyakorlat
 Általános Kémia GY 3.tantermi gyakorlat ph számítás: Erős savak, erős bázisok Gyenge savak, gyenge bázisok Pufferek, pufferkapacitás Honlap: http://harmatv.web.elte.hu Példatárak: Villányi Attila: Ötösöm
Általános Kémia GY 3.tantermi gyakorlat ph számítás: Erős savak, erős bázisok Gyenge savak, gyenge bázisok Pufferek, pufferkapacitás Honlap: http://harmatv.web.elte.hu Példatárak: Villányi Attila: Ötösöm
Jegyzőkönyv. Termoelektromos hűtőelemek vizsgálatáról (4)
 Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
Jegyzőkönyv ermoelektromos hűtőelemek vizsgáltáról (4) Készítette: üzes Dániel Mérés ideje: 8-11-6, szerd 14-18 ór Jegyzőkönyv elkészülte: 8-1-1 A mérés célj A termoelektromos hűtőelemek vizsgáltávl kicsit
Minta feladatsor I. rész
 Mint feldtsor I. rész. Írj fel z A számot htványként! A / pont/. Mekkor hosszúságú dróttl lehet egy m m-es tégllp lkú testet z átlój mentén felosztni két derékszögű háromszögre? Adj meg hosszúságot mértékegységgel!
Mint feldtsor I. rész. Írj fel z A számot htványként! A / pont/. Mekkor hosszúságú dróttl lehet egy m m-es tégllp lkú testet z átlój mentén felosztni két derékszögű háromszögre? Adj meg hosszúságot mértékegységgel!
1. feladat Összesen: 10 pont. 2. feladat Összesen: 6 pont. 3. feladat Összesen: 18 pont
 1. feladat Összesen: 10 pont Etil-acetátot állítunk elő 1 mol ecetsav és 1 mol etil-alkohol felhasználásával. Az egyensúlyi helyzet beálltakor a reakciót leállítjuk, és az elegyet 1 dm 3 -re töltjük fel.
1. feladat Összesen: 10 pont Etil-acetátot állítunk elő 1 mol ecetsav és 1 mol etil-alkohol felhasználásával. Az egyensúlyi helyzet beálltakor a reakciót leállítjuk, és az elegyet 1 dm 3 -re töltjük fel.
AZ ELEKTROKÉMIA VÁLOGATOTT ALKALMAZÁSI TERÜLETEI
 AZ ELEKTROKÉMIA VÁLOGATOTT ALKALMAZÁSI TERÜLETEI Elektrokémiai áramforrások Csoportosításuk: - primer elemek: nem tölthetk újra - szekunder elemek: újabb kisütési-feltöltési ciklus lehetséges - tüzelanyag
AZ ELEKTROKÉMIA VÁLOGATOTT ALKALMAZÁSI TERÜLETEI Elektrokémiai áramforrások Csoportosításuk: - primer elemek: nem tölthetk újra - szekunder elemek: újabb kisütési-feltöltési ciklus lehetséges - tüzelanyag
2. MECHANIKA-STATIKA GYAKORLAT (kidolgozta: Triesz Péter, egy. ts.; Tarnai Gábor, mérnök tanár) Erők eredője, fölbontása
 SZÉCHENYI ISTVÁN EGYETEM LKLMZOTT MECHNIK TNSZÉK. MECHNIK-STTIK GYKORLT (kidolgozt: Triesz Péter, eg. ts.; Trni Gábor, mérnök tnár) Erők eredője, fölbontás.1. Péld dott eg erő és eg egenes irán-egségvektor:
SZÉCHENYI ISTVÁN EGYETEM LKLMZOTT MECHNIK TNSZÉK. MECHNIK-STTIK GYKORLT (kidolgozt: Triesz Péter, eg. ts.; Trni Gábor, mérnök tnár) Erők eredője, fölbontás.1. Péld dott eg erő és eg egenes irán-egségvektor:
HIBAJEGYZÉK az Alapvető fizikai kémiai mérések, és a kísérleti adatok feldolgozása
 HIBAJEGYZÉK az Alapvető fzka kéma mérések, és a kísérlet adatk feldlgzása címü jegyzethez 2008-070 Általáns hba, hgy a ktevőben lévő negatív (-) előjelek mndenhnnan eltűntek a nymtatás srán!!! 2. Fejezet
HIBAJEGYZÉK az Alapvető fzka kéma mérések, és a kísérlet adatk feldlgzása címü jegyzethez 2008-070 Általáns hba, hgy a ktevőben lévő negatív (-) előjelek mndenhnnan eltűntek a nymtatás srán!!! 2. Fejezet
Általános Kémia GY, 2. tantermi gyakorlat
 Általános Kémia GY, 2. tantermi gyakorlat Sztöchiometriai számítások -titrálás: ld. : a 2. laborgyakorlat leírásánál Gáztörvények A kémhatás fogalma -ld.: a 2. laborgyakorlat leírásánál Honlap: http://harmatv.web.elte.hu
Általános Kémia GY, 2. tantermi gyakorlat Sztöchiometriai számítások -titrálás: ld. : a 2. laborgyakorlat leírásánál Gáztörvények A kémhatás fogalma -ld.: a 2. laborgyakorlat leírásánál Honlap: http://harmatv.web.elte.hu
Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása
 Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Javítókulcs (Kémia emelt szintű feladatsor)
 Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. A katalizátorok a kémiai reakciót gyorsítják azáltal, hogy az aktiválási energiát csökkentik, a reakció végén változatlanul megmaradnak. 2. Biológiai
Javítókulcs (Kémia emelt szintű feladatsor) I. feladat 1. A katalizátorok a kémiai reakciót gyorsítják azáltal, hogy az aktiválási energiát csökkentik, a reakció végén változatlanul megmaradnak. 2. Biológiai
100% = 100 pont A VIZSGAFELADAT MEGOLDÁSÁRA JAVASOLT %-OS EREDMÉNY: EBBEN A VIZSGARÉSZBEN A VIZSGAFELADAT ARÁNYA 40%.
 Az Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről szóló 133/2010. (IV. 22.) Korm. rendelet alapján. Szakképesítés, szakképesítés-elágazás, rész-szakképesítés,
Az Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről szóló 133/2010. (IV. 22.) Korm. rendelet alapján. Szakképesítés, szakképesítés-elágazás, rész-szakképesítés,
SCHWARTZ 2009 Emlékverseny A TRIÓDA díj-ért kitűzött feladat megoldása ADY Endre Líceum Nagyvárad, Románia 2009. november 7.
 SCHWARTZ 009 Emlékveseny A TRIÓA díj-ét kitűzött feldt megoldás AY Ende Líceum Ngyvád, Románi 009. novembe 7. Az elekton fjlgos töltésének meghtáozás mgneton módszeel A szező áltl jánlott teljes megoldás,
SCHWARTZ 009 Emlékveseny A TRIÓA díj-ét kitűzött feldt megoldás AY Ende Líceum Ngyvád, Románi 009. novembe 7. Az elekton fjlgos töltésének meghtáozás mgneton módszeel A szező áltl jánlott teljes megoldás,
Mozgás centrális erőtérben
 Mozgás centális eőtében 1. A centális eő Válasszunk egy olyan potenciális enegia függvényt, amely csak az oigótól való távolságtól függ: V = V(). A tömegponta ható eő a potenciális enegiája gaiensének
Mozgás centális eőtében 1. A centális eő Válasszunk egy olyan potenciális enegia függvényt, amely csak az oigótól való távolságtól függ: V = V(). A tömegponta ható eő a potenciális enegiája gaiensének
7. VIZES OLDATOK VISZKOZITÁSÁNAK MÉRÉSE OSTWALD-FENSKE-FÉLE VISZKOZIMÉTERREL
 7. VIZES OLDATOK VISZKOZITÁSÁNAK MÉRÉSE OSTWALD-FENSKE-FÉLE VISZKOZIMÉTERREL Számos technológiai folyamat, kémiai reakció színtere gáz, vagy folyékony közeg (fluid közeg). Gondoljunk csak a fémek előállításakor
7. VIZES OLDATOK VISZKOZITÁSÁNAK MÉRÉSE OSTWALD-FENSKE-FÉLE VISZKOZIMÉTERREL Számos technológiai folyamat, kémiai reakció színtere gáz, vagy folyékony közeg (fluid közeg). Gondoljunk csak a fémek előállításakor
Az ABCD köré írható kör egyenlete: ( x- 3) + ( y- 5) = 85. ahol O az origó. OB(; 912). Legyen y = 0, egyenletrendszer gyökei adják.
 5 egyes feldtok Az dott körök k : x + ( y- ) = és k : ( x- ) + y = K (; 0), r, K (; 0), r K K = 0 > +, két körnek nincs közös pontj Legyen (; ) Az egyenlô hosszú érintôszkszokr felírhtjuk következô egyenletet:
5 egyes feldtok Az dott körök k : x + ( y- ) = és k : ( x- ) + y = K (; 0), r, K (; 0), r K K = 0 > +, két körnek nincs közös pontj Legyen (; ) Az egyenlô hosszú érintôszkszokr felírhtjuk következô egyenletet:
Középiskolás leszek! matematika. 13. feladatsor 1. 2. 3. 4. 5. 6.
 Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
Középiskolás leszek! mtemtik Melyik számot jelentheti A h tudjuk hogy I felennyi mint S S egyenlõ K és O összegével K egyenlõ O és L különbségével O háromszoros L-nek L negyede 64-nek I + S + K + O + L
Összetettebb feladatok
 A szinusztétel és koszinusztétel lklmzás Összetettebb feldtok 055..,7 m háom kö közötti síkidom teülete. Kössük össze köök középpontjit, így kpunk egy háomszöget. Legyen m, b m, 5 m. Számítsuk ki koszinusztétellel
A szinusztétel és koszinusztétel lklmzás Összetettebb feldtok 055..,7 m háom kö közötti síkidom teülete. Kössük össze köök középpontjit, így kpunk egy háomszöget. Legyen m, b m, 5 m. Számítsuk ki koszinusztétellel
4. Hatványozás, gyökvonás
 I. Nulldik ZH-bn láttuk:. Htványozás, gyökvonás. Válssz ki, hogy z lábbik közül melyikkel egyezik meg következő kifejezés, h, y és z pozitív számok! 7 y z z y (A) 7 8 y z (B) 7 8 y z (C) 9 9 8 y z (D)
I. Nulldik ZH-bn láttuk:. Htványozás, gyökvonás. Válssz ki, hogy z lábbik közül melyikkel egyezik meg következő kifejezés, h, y és z pozitív számok! 7 y z z y (A) 7 8 y z (B) 7 8 y z (C) 9 9 8 y z (D)
VIII. Szélsőérték számítás
 Foglmk VIII. Szélsőéték számítás Az elem úton meghtáozhtó függvények jellemző: () ételmezés ttomány és étékkészlet megdás (b) zéushelyek (hol y ) és y tengelypontok (hol ) meghtáozás (c) folytonosság vzsgált
Foglmk VIII. Szélsőéték számítás Az elem úton meghtáozhtó függvények jellemző: () ételmezés ttomány és étékkészlet megdás (b) zéushelyek (hol y ) és y tengelypontok (hol ) meghtáozás (c) folytonosság vzsgált
Kémia OKTV 2006/2007. II. forduló. A feladatok megoldása
 Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
Kémia OKTV 2006/2007. II. forduló A feladatok megoldása Az értékelés szempontjai Csak a hibátlan megoldásokért adható a teljes pontszám. Részlegesen jó megoldásokat a részpontok alapján kell pontozni.
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI III.
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI III. OLDTOK EGYENSÚLYI: KORLÁTOZOTT OLDÓDÁS z elegyedés oldódás nem feltétlenül korlát, zz nem megy végbe teljes összetétel-trtománybn! H z oldódás korlátozott, kkor
Összetett hálózat számítása_1
 Összetett hálózat számítása_1 Határozzuk meg a hálózat alkatrészeinek feszültségeit, valamint a körben folyó áramot! A megoldás lépései: - számítsuk ki a kör eredő ellenállását, - az eredő ellenállás felhasználásával
Összetett hálózat számítása_1 Határozzuk meg a hálózat alkatrészeinek feszültségeit, valamint a körben folyó áramot! A megoldás lépései: - számítsuk ki a kör eredő ellenállását, - az eredő ellenállás felhasználásával
3. MECHANIKA STATIKA GYAKORLAT (kidolgozta: Triesz Péter; Tarnai Gábor, mérnök tanár) Három erő egyensúlya
 SZÉHENYI ISTVÁN EGYETEM LKLMZOTT MEHNIK TNSZÉK Péld: MEHNIK STTIK GYKORLT (kidolgozt: Tisz Pét; Tni Gábo ménök tná) Háom ő gynsúly dott gy mlőszkzt méti és thlés: m b 5 m c 5 m kn ldt: y c Htáozz mg z
SZÉHENYI ISTVÁN EGYETEM LKLMZOTT MEHNIK TNSZÉK Péld: MEHNIK STTIK GYKORLT (kidolgozt: Tisz Pét; Tni Gábo ménök tná) Háom ő gynsúly dott gy mlőszkzt méti és thlés: m b 5 m c 5 m kn ldt: y c Htáozz mg z
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA
 HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
HOMOGÉN EGYENSÚLYI ELEKTROKÉMIA: ELEKTROLITOK TERMODINAMIKÁJA I. Az elektrokémia áttekintése. II. Elektrolitok termodinamikája. A. Elektrolitok jellemzése B. Ionok termodinamikai képződési függvényei C.
5. Logaritmus. I. Nulladik ZH-ban láttuk: 125 -öt kapjunk. A 3 5 -nek a 3. hatványa 5, log. x Mennyi a log kifejezés értéke?
 . Logritmus I. Nulldik ZH-bn láttuk:. Mennyi kifejezés értéke? (A) Megoldás I.: BME 0. szeptember. (7B) A feldt ritmus definíciójából kiindulv gykorltilg fejben végiggondolhtó. Az kérdés, hogy -öt hánydik
. Logritmus I. Nulldik ZH-bn láttuk:. Mennyi kifejezés értéke? (A) Megoldás I.: BME 0. szeptember. (7B) A feldt ritmus definíciójából kiindulv gykorltilg fejben végiggondolhtó. Az kérdés, hogy -öt hánydik
Az integrálszámítás néhány alkalmazása
 Az integrálszámítás néhány lklmzás (szerkesztés ltt) Dr Toledo Rodolfo 4 november 4 Trtlomjegyzék Két függvények áltl htárolt terület Forgástestek térfogt és felszíne 5 3 Ívhosszszámítás 7 4 Feldtok 8
Az integrálszámítás néhány lklmzás (szerkesztés ltt) Dr Toledo Rodolfo 4 november 4 Trtlomjegyzék Két függvények áltl htárolt terület Forgástestek térfogt és felszíne 5 3 Ívhosszszámítás 7 4 Feldtok 8
Egy látószög - feladat
 Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
Ehhez tekintsük z 1. ábrát is! Egy látószög - feldt 1. ábr Az A pont körül kering C pont, egy r sugrú körön. A rögzített A és B pontok egymástól távolság vnnk. Az = CAB szöget folymtosn mérjük. Keressük
5. Sók oldáshőjének meghatározása kalorimetriás módszerrel. Előkészítő előadás 2016.02.01.
 5. Sók oldáshőjének meghatározása kalorimetriás módszerrel Előkészítő előadás 2016.02.01. Célja: hő mérése A kalorimetriás mérések Használatával meghatározható: átalakulási hő reakcióhő anyagok hőkapacitása
5. Sók oldáshőjének meghatározása kalorimetriás módszerrel Előkészítő előadás 2016.02.01. Célja: hő mérése A kalorimetriás mérések Használatával meghatározható: átalakulási hő reakcióhő anyagok hőkapacitása
Redox reakciók. azok a reakciók, melyekben valamely atom oxidációs száma megváltozik.
 Redox reakciók azok a reakciók, melyekben valamely atom oxidációs száma megváltozik. Az oxidációs szám megadja, hogy egy atomnak mennyi lenne a töltése, ha gondolatban a kötő elektronpárokat teljes mértékben
Redox reakciók azok a reakciók, melyekben valamely atom oxidációs száma megváltozik. Az oxidációs szám megadja, hogy egy atomnak mennyi lenne a töltése, ha gondolatban a kötő elektronpárokat teljes mértékben
Sűrűségmérés. 1. Szilárd test sűrűségének mérése
 Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Sűrűségérés. Szilárd test sűrűségének érése A sűrűség,, definíciój hoogén test esetén: test töege osztv test V térfogtávl: V A sűrűség SI értékegysége kg/, hsználtos ég kg/d, kg/l és g/c Ne hoogén testnél
Azonosító jel: KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA. 2009. október 28. 14:00. Az írásbeli vizsga időtartama: 240 perc
 É RETTSÉGI VIZSGA 2009. október 28. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2009. október 28. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati KTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
É RETTSÉGI VIZSGA 2009. október 28. KÉMIA EMELT SZINTŰ ÍRÁSBELI VIZSGA 2009. október 28. 14:00 Az írásbeli vizsga időtartama: 240 perc Pótlapok száma Tisztázati Piszkozati KTATÁSI ÉS KULTURÁLIS MINISZTÉRIUM
2012/2013 tavaszi félév 10. óra
 2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
2012/2013 tvszi félév 10. ór Glvánelemek, Elektromotoros erő számítás Cellfolymtok felírás, rendezése, ruttó folymt foglm Koncentrációs elemek Elektrokémii egyensúlyok Redoxrekciók irányánk megállpítás
9. Exponenciális és logaritmusos egyenletek, egyenlőtlenségek
 . Eponenciális és ritmusos egenletek, egenlőtlenségek Elméleti összefoglló H >, b>, és vlós számok, kkor + ( ) b ( b) H >, kkor z z ( ) ( ) f függvén szigorún monoton növekvő, míg h <
. Eponenciális és ritmusos egenletek, egenlőtlenségek Elméleti összefoglló H >, b>, és vlós számok, kkor + ( ) b ( b) H >, kkor z z ( ) ( ) f függvén szigorún monoton növekvő, míg h <
EGYENESFOGÚ HENGERESKERÉK GEOMETRIAI REKONSTRUKCIÓJA 4. jegyzőkönyv
 EGYENESFOGÚ HENGERESKERÉK GEOMETRIAI REKONSTRUKCIÓJA. jegyzőkönyv A mérés helye: DE-MK Gépelemek Lbortórium A mérés időpontj:... A mérést végezte:... Gykorltvezető:... Tételszám:... Feldt: Mérési dtok
EGYENESFOGÚ HENGERESKERÉK GEOMETRIAI REKONSTRUKCIÓJA. jegyzőkönyv A mérés helye: DE-MK Gépelemek Lbortórium A mérés időpontj:... A mérést végezte:... Gykorltvezető:... Tételszám:... Feldt: Mérési dtok
2012.05.02. 1 tema09_20120426
 9. Elektokémia kísélet: vasszög éz-szulfát oldatban cink eszelék éz-szulfát oldatban buttó eakció: + = + oxidációs folyamat: = + 2e edukciós folyamat: + 2e = Tegyünk egy ézlemezt éz-szulfát oldatba! Rövid
9. Elektokémia kísélet: vasszög éz-szulfát oldatban cink eszelék éz-szulfát oldatban buttó eakció: + = + oxidációs folyamat: = + 2e edukciós folyamat: + 2e = Tegyünk egy ézlemezt éz-szulfát oldatba! Rövid
Fizika A2E, 4. feladatsor
 Fizik AE, 4. feltso Vi Gyögy József vigyogy@gmil.com. felt: Közös pontbn zonos hosszúságú szigetel fonlkon felfüggesztett egyfom, g s ség golyók függnek, minkett töltése q. A golyók közötti teet ε eltív
Fizik AE, 4. feltso Vi Gyögy József vigyogy@gmil.com. felt: Közös pontbn zonos hosszúságú szigetel fonlkon felfüggesztett egyfom, g s ség golyók függnek, minkett töltése q. A golyók közötti teet ε eltív
VI. Kétismeretlenes egyenletrendszerek
 Mtemtik A 9. évfolm 7. modul: EGYENLETEK Tnári kézikönv VI. Kétismeretlenes egenletrendszerek Behelettesít módszer Mintpéld Két testvér érletpénztárnál jeget vásárol. Az egik vonljegért és eg átszálló
Mtemtik A 9. évfolm 7. modul: EGYENLETEK Tnári kézikönv VI. Kétismeretlenes egenletrendszerek Behelettesít módszer Mintpéld Két testvér érletpénztárnál jeget vásárol. Az egik vonljegért és eg átszálló
KÉMIA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia középszint 1512 ÉRETTSÉGI VIZSGA 2015. október 20. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
Kémia középszint 1512 ÉRETTSÉGI VIZSGA 2015. október 20. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
6. MECHANIKA-STATIKA GYAKORLAT Kidolgozta: Triesz Péter egy. ts. Négy erő egyensúlya, Culmann-szerkesztés, Ritter-számítás
 SZÉHENYI ISTVÁN EGYETE GÉPSZERKEZETTN ÉS EHNIK TNSZÉK 6. EHNIK-STTIK GYKORLT Kidolgozta: Tiesz Péte egy. ts. Négy eő egyensúlya ulmann-szekesztés Ritte-számítás 6.. Példa Egy létát egy veembe letámasztunk
SZÉHENYI ISTVÁN EGYETE GÉPSZERKEZETTN ÉS EHNIK TNSZÉK 6. EHNIK-STTIK GYKORLT Kidolgozta: Tiesz Péte egy. ts. Négy eő egyensúlya ulmann-szekesztés Ritte-számítás 6.. Példa Egy létát egy veembe letámasztunk
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakció kinetika és katalízis
 Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
Reakció kinetika és katalízis 1. előadás: Alapelvek, a kinetikai eredmények analízise Felezési idők 1/22 2/22 : A koncentráció ( ) időbeli változása, jele: mol M v, mértékegysége: dm 3. s s Legyen 5H 2
FELVÉTELI VIZSGA, július 15.
 BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
BABEŞ-BOLYAI TUDOMÁNYEGYETEM, KOLOZSVÁR MATEMATIKA ÉS INFORMATIKA KAR FELVÉTELI VIZSGA, 8. július. Írásbeli vizsg MATEMATIKÁBÓL FONTOS TUDNIVALÓK: ) A feleletválsztós feldtok (,,A rész) esetén egy vgy
MATEMATIKA FELADATLAP a 8. évfolyamosok számára
 8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
8. évfolym TMt1 feldtlp MATEMATIKA FELADATLAP 8. évfolymosok számár tehetséggondozó változt 11:00 ór NÉV: SZÜLETÉSI ÉV: HÓ: NAP: Tolll dolgozz! Zseszámológépet nem hsználhtsz. A feldtokt tetszés szerinti
KÉMIA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia középszint 1412 ÉRETTSÉGI VIZSGA 2015. május 14. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
Kémia középszint 1412 ÉRETTSÉGI VIZSGA 2015. május 14. KÉMIA KÖZÉPSZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
A 2013/2014. tanévi Országos Középiskolai Tanulmányi Verseny első forduló MATEMATIKA I. KATEGÓRIA (SZAKKÖZÉPISKOLA) Javítási-értékelési útmutató
 Okttási Hivtl A 013/014 tnévi Országos Középiskoli Tnulmányi Verseny első forduló MATEMATIKA I KATEGÓRIA (SZAKKÖZÉPISKOLA) Jvítási-értékelési útmuttó 1 Oldj meg vlós számok hlmzán egyenletet! 3 5 16 0
Okttási Hivtl A 013/014 tnévi Országos Középiskoli Tnulmányi Verseny első forduló MATEMATIKA I KATEGÓRIA (SZAKKÖZÉPISKOLA) Jvítási-értékelési útmuttó 1 Oldj meg vlós számok hlmzán egyenletet! 3 5 16 0
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam
 A feladatokat írta: Kódszám: Pócsiné Erdei Irén, Debrecen... Lektorálta: Kálnay Istvánné, Nyíregyháza 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam A feladatok megoldásához
A feladatokat írta: Kódszám: Pócsiné Erdei Irén, Debrecen... Lektorálta: Kálnay Istvánné, Nyíregyháza 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 9. évfolyam A feladatok megoldásához
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001
 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden
1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 JAVÍTÁSI ÚTMUTATÓ Az írásbeli felvételi vizsgadolgozatra összesen 100 (dolgozat) pont adható, a javítási útmutató részletezése szerint. Minden
A torokgerendás fedélszerkezet erőjátékáról 1. rész
 A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
A torokgerendás fedélszerkezet erőjátékáról. rész Bevezetés Az idő múlik, kívánlmk és lehetőségek változnk. Tegnp még logrléccel számoltunk, m már elektronikus számoló - és számítógéppel. Sok teendőnk
Elektrokémia B01. Mi a ph? Láng Győző. Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem Budapest
 Elektrokémia B01 Mi a ph? Láng Győző Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem Budapest Mi a ph? 1:48:51 Természetesen mindenki tudja, hogy mi az a ph, hiszen tanulta az iskolában...
Elektrokémia B01 Mi a ph? Láng Győző Kémiai Intézet, Fizikai Kémiai Tanszék Eötvös Loránd Tudományegyetem Budapest Mi a ph? 1:48:51 Természetesen mindenki tudja, hogy mi az a ph, hiszen tanulta az iskolában...
Érettségi eredmények 2005-től (Békéscsabai Andrássy Gyula Gimnázium és Kollégium)
 2005/db közép 2005/db emelt 2005/db összes 2005/jegy közép 2005/jegy emelt 2005/jegy összes 2005/% közép 2005/% emelt 2005/% összes 51 119 170 3,53 5,00 4,42 59,90 99,17 84,27 22 17 39 4,45 4,94 4,7 75,68
2005/db közép 2005/db emelt 2005/db összes 2005/jegy közép 2005/jegy emelt 2005/jegy összes 2005/% közép 2005/% emelt 2005/% összes 51 119 170 3,53 5,00 4,42 59,90 99,17 84,27 22 17 39 4,45 4,94 4,7 75,68
Vektorok. Vektoron irányított szakaszt értünk.
 Vektorok Vektoron irányított szkszt értünk A definíció értelmében tehát vektort kkor ismerjük, h ismerjük hosszát és z irányát A vektort kövér kis betűkkel (, b stb) jelöljük, megkülönböztetve z, b számoktól,
Vektorok Vektoron irányított szkszt értünk A definíció értelmében tehát vektort kkor ismerjük, h ismerjük hosszát és z irányát A vektort kövér kis betűkkel (, b stb) jelöljük, megkülönböztetve z, b számoktól,
Numerikus módszerek 2.
 Numerikus módszerek 2. 12. elődás: Numerikus integrálás I. Krebsz Ann ELTE IK 2015. május 5. Trtlomjegyzék 1 Numerikus integrálás 2 Newton Cotes típusú kvdrtúr formulák 3 Hibformulák 4 Összetett formulák
Numerikus módszerek 2. 12. elődás: Numerikus integrálás I. Krebsz Ann ELTE IK 2015. május 5. Trtlomjegyzék 1 Numerikus integrálás 2 Newton Cotes típusú kvdrtúr formulák 3 Hibformulák 4 Összetett formulák
Kémiai alapismeretek 7.-8. hét
 Kémiai alapismeretek 7.-8. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. október 16.-október 19. 1/12 2012/2013 I. félév, Horváth Attila
Kémiai alapismeretek 7.-8. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. október 16.-október 19. 1/12 2012/2013 I. félév, Horváth Attila
3. MECHANIKA STATIKA GYAKORLAT Kidolgozta: Triesz Péter egy. ts. Három erő egyensúlya
 SZÉHENYI ISTVÁN EGYETEM GÉPSZERKEZETTN ÉS MEHNIK TNSZÉK 3 MEHNIK STTIK GYKORLT Kdolgozt: Tsz Pét gy ts Háom ő gynsúly 3 Péld: dott gy mlőszkzt mét és thlés: m b 5 m c 5 m 0 kn ldt: y c Htáozz mg z és támsztóőkt
SZÉHENYI ISTVÁN EGYETEM GÉPSZERKEZETTN ÉS MEHNIK TNSZÉK 3 MEHNIK STTIK GYKORLT Kdolgozt: Tsz Pét gy ts Háom ő gynsúly 3 Péld: dott gy mlőszkzt mét és thlés: m b 5 m c 5 m 0 kn ldt: y c Htáozz mg z és támsztóőkt
KIMUTATÁS A TARTÓS BENTLAKÁSOS ÉS ÁTMENETI ELHELYEZÉST NYÚJTÓ INTÉZMÉNYEK MŰKÖDÉSI ADATAIRÓL
 KÖZPONTI STATISZTIKAI HIVATAL Az dtszolgálttás sttisztikáról szóló 1993. évi XLVI. törvény (Stt.) 8. (2) ekezdése lpján kötelező. Nyilvántrtási szám: KIMUTATÁS A TARTÓS BENTLAKÁSOS ÉS ÁTMENETI ELHELYEZÉST
KÖZPONTI STATISZTIKAI HIVATAL Az dtszolgálttás sttisztikáról szóló 1993. évi XLVI. törvény (Stt.) 8. (2) ekezdése lpján kötelező. Nyilvántrtási szám: KIMUTATÁS A TARTÓS BENTLAKÁSOS ÉS ÁTMENETI ELHELYEZÉST
Tevékenység: Olvassa el a fejezetet! Gyűjtse ki és jegyezze meg a ragasztás előnyeit és a hátrányait! VIDEO (A ragasztás ereje)
 lvassa el a fejezetet! Gyűjtse ki és jegyezze meg a ragasztás előnyeit és a hátrányait! VIDE (A ragasztás ereje) A ragasztás egyre gyakrabban alkalmazott kötéstechnológia az ipari gyakorlatban. Ennek oka,
lvassa el a fejezetet! Gyűjtse ki és jegyezze meg a ragasztás előnyeit és a hátrányait! VIDE (A ragasztás ereje) A ragasztás egyre gyakrabban alkalmazott kötéstechnológia az ipari gyakorlatban. Ennek oka,
Formális nyelvek I/2.
 Formális nyelvek I/2. Véges utomták minimlizálás Fülöp Zoltán SZTE TTIK Informtiki Intézet Számítástudomány Alpji Tnszék 6720 Szeged, Árpád tér 2. Véges utomták minimlizálás Két utomt ekvivlens, h ugynzt
Formális nyelvek I/2. Véges utomták minimlizálás Fülöp Zoltán SZTE TTIK Informtiki Intézet Számítástudomány Alpji Tnszék 6720 Szeged, Árpád tér 2. Véges utomták minimlizálás Két utomt ekvivlens, h ugynzt
26. HÁLÓZATI TÁPEGYSÉGEK. Célkitűzés: A hálózati egyenirányító és stabilizáló alapkapcsolások és jellemzőinek megismerése, illetőleg mérése.
 26. HÁLÓZATI TÁPEGYSÉGEK Célkiűzés: A hálózi egyenirányíó és silizáló lpkpcsolások és jellemzőinek megismerése, illeőleg mérése. I. Elmélei áekinés Az elekronikus készülékek működeéséhez legöször egyenfeszülségre
26. HÁLÓZATI TÁPEGYSÉGEK Célkiűzés: A hálózi egyenirányíó és silizáló lpkpcsolások és jellemzőinek megismerése, illeőleg mérése. I. Elmélei áekinés Az elekronikus készülékek működeéséhez legöször egyenfeszülségre
O k t a t á si Hivatal
 O k t a t á si Hivatal 0/0. tanévi Országos Középiskolai Tanulmányi Verseny Kémia II. kategória. forduló I. FELADATSOR Megoldások. A helyes válasz(ok) betűjele: B, D, E. A legnagyobb elektromotoros erejű
O k t a t á si Hivatal 0/0. tanévi Országos Középiskolai Tanulmányi Verseny Kémia II. kategória. forduló I. FELADATSOR Megoldások. A helyes válasz(ok) betűjele: B, D, E. A legnagyobb elektromotoros erejű
KÉMIA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ
 Kémia emelt szint 1411 ÉRETTSÉGI VIZSGA 2015. május 14. KÉMIA EMELT SZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
Kémia emelt szint 1411 ÉRETTSÉGI VIZSGA 2015. május 14. KÉMIA EMELT SZINTŰ ÍRÁSBELI ÉRETTSÉGI VIZSGA JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ EMBERI ERŐFORRÁSOK MINISZTÉRIUMA Az írásbeli feladatok értékelésének alapelvei
M. 2. Döntsük el, hogy a következő két szám közül melyik a nagyobb:
 Mgyr Ifjúság (Rábi Imre) Az előző években közöltük Mgyr Ifjúságbn közös érettségi-felvételi feldtok megoldását mtemtikából és fizikából. Tpsztltuk, hogy igen ngy volt z érdeklődés lpunk e szám iránt. Évente
Mgyr Ifjúság (Rábi Imre) Az előző években közöltük Mgyr Ifjúságbn közös érettségi-felvételi feldtok megoldását mtemtikából és fizikából. Tpsztltuk, hogy igen ngy volt z érdeklődés lpunk e szám iránt. Évente
Exponenciális és logaritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek
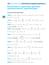 Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
Eponenciális és logritmikus egyenletek, Eponenciális és logritmikus egyenletek, egyenletrendszerek, egyenlôtlenségek Eponenciális egyenletek 60 ) = ; b) = ; c) = ; d) = 0; e) = ; f) = ; g) = ; h) =- 7
Jellemző redoxi reakciók:
 Kémia a elektronátmenettel járó reakciók, melynek során egyidejű elektron leadás és felvétel történik. Oxidáció - elektron leadás - oxidációs sám nő Redukció - elektron felvétel - oxidációs sám csökken
Kémia a elektronátmenettel járó reakciók, melynek során egyidejű elektron leadás és felvétel történik. Oxidáció - elektron leadás - oxidációs sám nő Redukció - elektron felvétel - oxidációs sám csökken
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996
 1996 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996 I. Az alábbiakban megadott vázlatpontok alapján írjon 1-1,5 oldalas dolgozatot! Címe: ALKÉNEK Alkének fogalma. Elnevezésük elve példával.
1996 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1996 I. Az alábbiakban megadott vázlatpontok alapján írjon 1-1,5 oldalas dolgozatot! Címe: ALKÉNEK Alkének fogalma. Elnevezésük elve példával.
