Zárójelentés A természet szénhidrátkémikusai: enzimatikus glikozilezések című OTKA pályázatról
|
|
|
- Ábel Csonka
- 5 évvel ezelőtt
- Látták:
Átírás
1 Zárójelentés A természet szénhidrátkémikusai: enzimatikus glikozilezések című OTKA pályázatról A szénhidrát- és zsíranyagcsere-zavar, valamint a magas vérnyomás betegség tünetegyüttes metabolikus szindróma néven ismert. A metabolikus szindróma mint kórkép az elmúlt két évtizedben az elhízás járványszerű megjelenésével került egyre inkább a figyelem központjába. A szénhidrátanyagcsere rendellenességei, mint pl. a cukorbetegség, elhízás, vagy a fogszuvasodás- igen széleskörűen elterjedt betegségekké váltak napjainkra és a népesség egyre nagyobb százalékát érintik. Így feltétlenül indokolt olyan új hatóanyagok vagy gyógymódok bevezetése, melyek hatással vannak a szénhidrátfelvétel fiziológiai szabályozására, a vércukor szintre és a különféle szájbetegségek megelőzésére. A szájbetegségek, köztük a fogszuvasodás, a periodontitis és a fog elvesztése jelentősen befolyásolja egy személy általános egészségi állapotát. A fogszuvasodás egy több tényezős fertőző betegség, melynek kialakulásában a táplálkozás, a diéta és a mikrobiális fertőzések fontos szerepet játszanak. A humán amilázok, mind a nyál (HSA), mind a pankreász eredetű (HPA) széleskörűen tanulmányozott enzimek klinikai kémiai szempontból, mivel fontos jellemzők a pankreász és nyálmirigy eredetű betegségek diagnosztizálásában. Olyan gyógyszerek tervezésének célpontjai, melyek a cukorbetegség, elhízás és a fogszuvasodás megelőzésére vagy gyógyítására irányulnak. A nyál amiláz enzime sokféle funkciót lát el a szájüregben. Részt vesz a keményítő kezdeti hidrolízisében, valamint bizonyított, hogy hozzákötődik a fogzománchoz, vagy a hidroxiapatithoz és így elősegíti a fogplakkok kialakulását. Továbbá, nagy affinitással kötődik a szájüregben található baktériumokhoz, melyek a keményítő lebontásából felszabaduló glükózt tejsavvá alakítják. Az összegyűlt tejsav a fogzománc feloldásához vezethet, ami egy kritikus lépés a fogszuvasodás kifejlődésében. Joggal merül fel az igény olyan inhibitorok (átmeneti állapot analógok és szubsztrát analóg származékok) tervezésére, melyek megelőzhetik a kellemetlen szájbetegségeket. Új inhibitor molekulák kifejlesztése, melyek nagy affinitással és specifikusan kötődnek az enzim aktív centrumában, és az inhibitor- enzim kötődés tanulmányozása nem könnyű feladat a biokémikus/kémikus számára. A tíz éve megkezdett kutatásainkat ezen célkitűzések motiválták.
2 Az OTKA által támogatott munkaterv több kutatócsoport közös érdeklődéséből fakadó multidiszciplináris pályázattá alakult. A részt vevő csoportok egymást kiegészítő tapasztalataik és képességeik egyesítésével, a szükséges berendezésekkel és a know-how lehetőségekkel együtt jelenleg is gyümölcsöző együttműködést alakítottak ki. Herczegh Pál és munkatársai (Debreceni Egyetem Gyógyszerészi Kémia Tanszék) egy 2,3- telítetlen hexapiranóz ismétlődő egységből felépülő új típusú poliszacharidot állítottak elő a 3,6-di-O-acetil-D-glükál polikondenzációjával. A dezacetilezett poliszacharid a humán nyál amiláz inhibitora, az inhibíciós állandók mm-os nagyságrendűek (Carbohydr. Polymers, 2005). Bár a glükálok a szubsztrát átmeneti állapotát mimikálják, gyenge affinitásuk feltehetően az OH csoportok hiányával magyarázható. A kis méretű D-glükál nem inhibitora a nyál amiláznak, de gátolja az Aspergillus oryzae eredetű -amilázt (IC 50 =43.5mM). A D-glükál az -glükozidázok hatékonyabb inhibitora. A sörélesztő (Brewers yeast Type VI. SIGMA) - glükozidáza által katalizált PNP -D-glükopiranozid hidrolízisre számolt IC 50 =1.82mM. Somsák László és csoportja (Debreceni Egyetem Szerves Kémiai Tanszék) széleskörű kutatásokat folytat a glikogén foszforiláz új glükózanalóg inhibitorainak tervezésére és szintézisére. A máj glikogén foszforiláz a glikogén metabolizmus kulcs enzime és közvetlenül felelős a vércukor szint szabályozásáért. Ezen megközelítést számos akadémiai csoport és gyógyszergyár vizsgálja, mint egy elképzelhető új lehetőséget a diabetes terápiában. A szintetizált vegyületek között a glükopiranozilidén-spiro-tio-hidantoin (GTH) igen kedvező hipoglikémiás hatása keltette fel érdeklődésünket, hogy tanulmányozzuk a GTH amilázra kifejtett hatását is. Méréseink szerint (Biochem. Biophys. Res. Commun., 2003) a GTH közepesen jó inhibitora a humán nyál amiláznak. Az inhibíciós állandók mm-os nagyságrendűek: K EI =7.3mM, K ESI =2.8 mm. A GTH szemben az akarbózzal nem metabolizálódik, ezáltal csökkenti az akarbóz kellemetlen mellékhatásait, és így a cukor metabolizmus rendellenességeinek kezelésére, valamint a fogszuvasodás megelőzésére alkalmas gyógyszerré fejleszthető igéretes vegyület. A glikogén foszforiláz gátlására tervezett vegyületek közül a diglükozil-biuret, a diglükozil-urea, valamint az N-N -diglükozil oxálsav amid típusúak a GTH-hoz hasonlóan jó inhibitorai a humán nyál amiláznak is. A vizsgált molekulák kis méretük miatt többféle produktív komplexet hozhatnak létre az enzim aktív centrumában, ami magyarázhatja a gyengébb inhibitor hatásukat. Úgy gondoltuk, hogy a hosszabb, több alhelyet elfoglaló molekulák hatásosabb enzimgátlók lesznek.
3 Feltételezésünket a GTH enzimatikus transzglikozilezésével bizonyítottuk (Carbohydr. Res., 2005). Kwan Hwa Park és munkatársai (Seoul National University, Korea) egy termostabil maltogén amilázt kódoló gént klónoztak és expresszáltak a B. stearothermophilus-ból. Az enzim (BSMA) hidrolizálja a keményítőt, a ciklodextrineket, a pullulánt valamint az akarbózt is. A BSMA úgy kötődik az akarbózhoz, hogy a maltóz közötti glikozidos kötést hasítja, ami egy pszeudotriszacharidot (PTS) eredményez. Ezt követően a BSMA képes transzferálni a PTS-t alkalmas akceptor molekulákra α-(1-6), α-(1-3) vagy α-(1-4) glikozidos kötések létrehozásával. A maltózt képző amilázok akceptor specifitása igen széles skálájú, mivel nemcsak mono- és diszacharidokra transzferálnak, hanem többféle, szerkezetileg különböző vegyületekre is; mint pl. cukoralkoholokra, flavonoidokra és az aszkorbinsavra. A transzglikozilezés számos biológiai és ipari szempontból fontos vegyület módosítására ad lehetőséget, melyek eredményeként azok tulajdonságai (oldékonyság, íz, biológiai aktivitás) előnyösen megváltoztathatók. Ezen ismeretek adták az ötletet, hogy kísérletet tegyünk egy új amiláz inhibitor előállítására a BSMA katalizálta glikozilezéssel. Az enzim K. H. Park professzor laboratóriumából (Dél- Korea) származott. Akarviozinil-izomaltozil-spiro-tiohidantoin (PTS-GTH) szintézise (Carbohydr. Res.,2005) Az enzimes glikozilezés akarbóz donor és glüko-spiro-tiohidantoin (GTH), mint akceptor jelenlétében történt. Az akarbózt Glucobay tablettából (Bayer) extraháltuk, a GTH-t kémiai szintézissel állítottuk elő. A reakciót TLC, HPLC és MALDI-TOF analízissel követtük. A TLC igazolta, hogy a BSMA hidrolizálja az akarbózt és glükóz valamint akarviozin-glükóz keletkezik. A GTH akceptor jelenlétében 2 UV-ben detektálható transzfertermék tűnt fel, közülük az egyik kisebb mennyiségben. Az újonnan képződött akceptortermékeket HPLC-vel detektáltuk. A két termék képződését 10 óra után észleltük, majd 48 óra elteltével mennyiségük szignifikánsan növekedett. A reakcióelegy MALDI-TOF analízise azonban csak egy olyan csúcsot eredményezett, melynek m/z értéke nagyobb volt, mint az akarbózé, s ez izomer termékek keletkezésére utalt. Azonosítottuk a spektrumban az akarbóz, az akarviozin-glükóz és az újonnan képződött akceptortermék [M+Na + ] ionizált csúcsait, 669, 506 és 752 m/z értékkel.
4 A HPLC analízis fő termékét izoláltuk és félpreparatív HPLC-vel tisztítottuk, majd szerkezetét NMR-rel igazoltuk. Az, hogy az újonnan képződött termék a PTS és GTH közötti transzglikozilezés eredménye, a számított (752.22) és mért (752.27) molekulatömegek közötti igen jó egyezés bizonyította. A proton és szén NMR spektrumok teljes jelhozzárendelését a COSY, TOCSY, ROESY, HSQC és HMBC módszerekkel végeztük el és ennek alapján igazoltuk a fő akceptortermék szerkezetét. A HMBC spektrum valamennyi interglikozidos és köztük az újonnan képződött C1 O-D 6 kötést egyértelműen igazolja. A glikozilezés helyét, azaz az 1-6 interglikozidos kötést (67,5 ppm) a D6 szén kémiai eltolódása is megerősíti. A gyűrűk kapcsolódását, vagyis az interglikozidos kötésben részt vevő hidrogének téren át ható kölcsönhatását a ROESY spektrum alapján is igazoltuk. Az α-amilázokhoz hasonlóan az anomer konfigurációt megtartó enzimek mechanizmusa egy kétlépéses reakció. Első lépésben a glikozil enzim intermedier képződik, majd ezt követi a víz vagy az akceptor molekula támadása, ami a hidrolízis termékeket (PTS + Glükóz) vagy a transzglikozilezés termékeit eredményezi. A GTH akceptor jelenlétében a PTS a C6-OH-ra tevődik át, ami az akarviozinil-izomaltozil-spiro-tiohidantoin képződéséhez vezet. A másik, minor komponens feltehetően α (1-4) kötésű, de az 1-3 kötés képződése sincs kizárva. Narayanan Ramasubbu és munkatársai (University of Medicine and Dentistry,New Jersey, USA) a humán nyál amiláz és mutánsaik szerkezeti és kinetikai tulajdonságát vizsgálják krisztallográfiás és enzimkinetikai módszerekkel. Igazolták, hogy az aktív hely konzervált aminosavai szerepet játszanak az átmeneti állapot stabilizálásában, valamint tisztázták a hidrolízis mechanizmusát is. A keményítő szubsztrát megkötődése az amiláz felületén található aktív helyen történik. A röntgenkrisztallográfiás vizsgálatokat az általunk kifejlesztett alhely térképezés (subsite mapping) eredményei egyértelműen megerősítették. A nyál amiláz (HSA) aktív centrumában 4 glikon és 3 aglikon kötőhelyet azonosítottunk, amely alapja lett az inhibitorok tervezésének. A fehérje szerkezetvizsgálata felfedte az aromás aminosavak jelentőségét a szubsztrát kötődésben és hidrolízisben. Az alhely térképezés az egyes kötőhelyek specifitásáról és kötési energiáiról nyújtott információt. A (-3), (-2) és (+2) alhelyek nagy energia értékei igazolták ezen kötőhelyek fontosságát a szubsztrát kötődésben. (FEBS Letters, 2003 és Theochem.,2003).
5 A humán nyál amiláz aktív centrumát három aromás aminosav Trp58, Trp59 és Tyr151 veszi körül, melyek kölcsönhatást létesítenek egymással (stacking or ring to ring interaction) és a kötött glükóz molekulával. Bizonyítottuk, hogy a Tyr151 a (+2) aglikon kötőhelyen található és befolyásolja a távozó csoport méretét. Azért, hogy megvizsgáljuk a (+2) kötőhely szerepét a szubsztrátok terminális egységének felismerésében, egy olyan mutánst hoztunk létre, ahol a tirozint a 151 pozícióban metioninra cseréltük ki. A mutáció lényegesen lecsökkentette a HSA specifikus aktivitását, valamint a szubsztrát bekötődés erősségét, ami az aromás gyűrűk közötti kölcsönhatások csökkenésével vagy hiányával magyarázható a (+2) alhelyen. A vad típusú és az Y151M mutáns amiláz által katalizált hidrolízisek termékanalízise azt mutatta, hogy a mutáns enzimben a maltóz, mint minimális távozó csoport glükózra cserélődött. A monomer glükozid CNP-G1 lett a hidrolízis domináns terméke a rövid szubsztrátok (DP 3-5) esetében, de szignifikánsan megjelent a hosszabb (DP 6-10) oligomerek hidrolízisekor is, azonban nem keletkezett a vad típusú amiláz katalizálta reakcióban. Ez a metionin jelenlétével magyarázható, mivel nem mutat kedvezményezett affinitást a glükózhoz a (+2) kötőhelyen. A mutáció lecsökkentette a kötőhelyek glükóz iránti affinitását, de a legfeltűnőbb csökkenés a számított kötési energiákban a (+2) alhelyen (-2,6 kj/mol a -12,0 kj/mol helyett), a mutáció helyén történt. Ez a szignifikáns redukció a Met oldallánc jelenlétével magyarázható, amely feltehetően egy olyan konformációt vesz fel, ami részben elfoglalja a glükóz kötődési helyét. Végül, a Tyr Met-ra történő cseréje jelentősen megnövelte a mutáns enzim transzferáz aktivitását, és így lehetővé tette az enzimatikus transzglikozilezésekhez történő felhasználását. Az Y151M mutáns enzimet elsőként alkalmaztuk sikerrel transzglikozilezésekhez. A szubsztrátkötő árok nem-redukáló végén két aromás aminosav, a Trp58 és a Trp59 található, melyek a katalitikus (β/α) 8 hordó β2-α2 hurok részei. A két aromás oldallánc különböző mértékű kapcsolatot alakít ki a kötött akarbózzal. A Trp59 stacking kölcsönhatást létesít a 4-amino-4,6-didezoxi-glükóz molekulával a (-3) kötőhelyen és a glükóz molekulával a (-2) kötőhelyen, továbbá a glükózhoz hidrogén kötéssel is kapcsolódik. Ezzel ellentétben a Trp58 nem létesít stacking kölcsönhatásokat az említett kötőhelyeken. A Trp58 úgy helyezkedik el a Trp59 mellett, hogy számos aminosavval alakít ki kapcsolatot mind kötetlen, mind komplex szerkezetekben a HSA-ban és más emlős amilázban is. Így pl. hidrofób kapcsolatokat létesít a Trp59, His299 és His305 aminosavakkal és hidrogén kötést az Asp356- tal, melyek dominánsak a Trp58 környezetében. Mivel a Trp58 a (-2) alhely közelében helyezkedik el, s ezen alhelynek a legnagyobb a kötőaffinitása a glikon kötőhelyek között,
6 tanulmányoztuk a HSA aktivitásában betöltött szerepét. Trp58Ala, Trp58Leu és Trp58Tyr mutánsokat állítottunk elő és kinetikai tulajdonságaikat összevetettük a vad típusú enzimével. Az Ala és Leu helyettesítésekkel a Trp nagy hely igényének csökkentését céloztuk meg, míg a Tyr csere az aromás karakter egy részének megtartására irányult. A mutáns enzimek keményítő szubsztráton mért specifikus aktivitásaik szorosára csökkentek a vad típusú amilázhoz képest. A k cat értékek jelentős csökkenését tapasztaltuk a rövidebb oligoszacharidok esetében is. A k cat /K m érték jóllehet alacsonyabb a W58Y mutánsnál a vad típushoz képest, de tízszer nagyobb a W58L vagy a W58A-ra kapott értékeknél, ami arra utal, hogy egy aromás aminosavra szükség van ebben a pozícióban. A triptofán-leucin csere lecsökkentette az összes alhely energia értékét, azonban a legjelentősebb csökkenés a számított kötési energiákban a (-3) alhelyen jelentkezett, ahol a mutáció történt. Érdekes, hogy az egyes alhelyek energia csökkenése nagyobb mértékű mint az Y151M mutáns esetében, ami arra utal, hogy a W58 aminosavnak több alhelyre kiterjedő koordináló szerepe lehet. Eredményeink azt a hipotézist támogatják, hogy az aktív centrum aromás aminosavai egy olyan vázat alakítanak ki, mely lehetővé teszi a szubsztrát befogadását, majd további stabilizáló kölcsönhatások létrejöttét. Ezen megállapításaink novumnak számítanak az irodalomban, melyeket a mutánsok alhely térképeivel együtt elsőként publikáltunk.(eur. J. Biochem.,2004). A triptofán leucinra történő cseréje megnövelte a HSA transzferáz aktivitását. Már alacsony szubsztrát koncentrációknál is a hidrolízis mellett transzglikozilezés is végbemegy. Transzferáz aktivitás bevezetése mutációval a HSA-ba [Organic Letters, 2003 és Biologia Bratislava, 2005] A nyál amiláz Y151M mutánsának alapos elemzése során arra a következtetésre jutottunk, hogy az aglikon kötőhelyen létrehozott szerkezeti változás növelheti a nyál amiláz szintetikus aktivitását, és a PNP-glikozidok jobb akceptorai lesznek az Y151M enzimnek, mint a vad típusú amiláznak. A PNP, mint aglikon használata azért is igen előnyös, mivel a reakciótermékek azonosítását és mennyiségi meghatározását érzékennyé és egyszerűvé teszi. Vizsgálataink arra irányultak, hogy tanulmányozzuk ezen új mutáns enzim alkalmazhatóságát oligoszacharidok szintézisére.
7 Maltotetraóz mint donor jelenlétében számos PNP-glikozidot, mint akceptort próbáltunk ki transzglikozilezésre, köztük néhányat említve; PNP α-glc, PNP β-glc, PNP 1-S- β-glc, PNP α-man, PNP α-xyl; melyek akceptortermékei jó hozammal képződtek. A transzglikozilezés a donor oligoszacharid egységeinek (maltóz vagy maltotrióz) átvitelével történt az akceptor glikozidra. Kísérleti körülményeink között a donor donorra történő transzfere (self transfer) nem fordult elő és a transzglikozilezés aktivitásának ph optimuma nem különbözött az Y151M által katalizált reakció ph optimumától. Megállapítottuk, hogy a glükozidok és a xilozid igen hatásos akceptorok a kitermelést illetően. Ha figyelembe vesszük, hogy az Y151M enzim az akceptorok alacsony koncentrációinál (15 mm) már transzglikozilez, továbbá, hogy a glikozilezés mellett a donor és az akceptortermékek víz jelenlétében végbemenő hidrolízise is állandóan jelen van, a kapott kitermelések igen jó eredménynek számítanak. Ez arra utal, hogy a használt akceptorok viszonylag erősen kötődnek az enzim aglikon kötőhelyéhez. A metionin jelenléte előnyösnek tűnik a nem poláris fenil csoport számára a (+2) kötőhelyen. Azt tapasztaltuk, hogy az α-glükozid akceptortermékek jobb kitermeléssel képződtek (48.6%) mint a megfelelő β-glükozid termékek (40%). Az Y151M enzim hatékonyabban viszi át a donor oligoszacharid egységet az α-glükozid akceptor 4-OH-jára, mint a megfelelő β- glükozid 4-OH-jára. Ez feltételezi, hogy a hidrofób PNP-csoport orientációja az akceptorban befolyásolja a transzglikozilezés hatékonyságát. A β-tio-glikozid hasonló kitermelést adott, mint a megfelelő O-glikozid. Így a glikozidos oxigén kénre történő cseréje lényegesen nem változtatja meg a kihozatalt. A β-xilozid is jó akceptornak bizonyult (27,8%), bár nem volt olyan hatékony, mint a β-glükozid. Ez feltehetően a 6-OH hiányának tulajdonítható, ami fontos a bekötődéshez. A β-mannozid akceptortermékek kisebb mértékű képződése (5%) feltehetően a mannopiranóz axiális OH-jának tulajdonítható, és ez azt jelzi, hogy a mannopiranóz kedvezőtlen kölcsönhatást létesít a (+1) kötőhelyen. A PNP-N-acetilglükózaminid, mint akceptor jelenlétében glikozilezett termék nem képződik. Ez is megerősíti az ekvatoriális 2-OH jelenlétének fontosságát a (+1) kötőhelyen. Ezen eredmények rámutatnak az Y151M mutáns enzimmel katalizált vizes fázisban történő szintézisek változatosságára és sokoldalúságára. Oligoszacharidok preparatív mértékű szintézisére a PNP 1-S- -Glc-t választottuk akceptorként, mivel ellenáll az Y151M katalizálta hidrolízisnek, valamint jó aktivátor az anomer pozícióban az egymást követő glikozilezési reakciókban. A tio-glikozidok hatásos glikozilező ágensek specifikus tiofil reagensekkel történő kémiai szintézisekhez. Részletes enzimológiai vizsgálatok rámutattak arra, hogy az idő és a hőmérséklet a legfontosabb
8 tényező a szintézis irányítására. A termékeket preparatív HPLC-vel fordított fázisú oszlopon választottuk szét. A termékek szerkezeti analízisét MALDI-TOF MS adatokkal és 13 C illetve 1 H NMR spektroszkópiával valósítottuk meg. A MALDI-TOF MS spektrum igen jó egyezést adott a mért és a számított molekula tömegekkel. Az interglikozidos kötés típusát valamint az anomer konfigurációt egy- és kétdimenziós 1 H és 13 C NMR spektroszkópiával határoztuk meg: Az 1D 1 H NMR spektrumban két dublett jelenik meg; az egyik 3.5 Hz, a másik 10.3 Hz J 1,2 csatolási állandóval. A 10.3 Hz érték a β- glikozidos kötésre utal, míg a 3.5 Hz az újonnan képződött α konfigurációt igazolja. Ezek az adatok megerősítik, hogy az Y151M mutáns enzim megtartotta α-sztereoszelektivitását, és nem változtatta meg az akceptor tio-glikozid anomer konfigurációját. Ezt az eredményt a 13 C NMR spektrumban a C-1 és a C-1 szén atomok kémiai eltolódás értékei is alátámasztják, melyek illetve 99.2 ppm értéknek adódtak. Az interglikozidos kötés típusára vonatkozóan, a C-6 és a C-6 szénatomok kémiai eltolódása alapján megállapítható, hogy a glikozilezésben a C-6 és a C-6 nem vesz részt. A C-4 kémiai eltolódása (78.18 ppm) a legnagyobb a váz szenek között, kivéve a két anomer szén kémiai eltolódásának értékét. Ez megerősíti az α(1-4) interglikozidos kötések jelenlétét, és arra utal, hogy az Y151M megőrzi nemcsak sztereo-, de regiospecifitását is a glikozilezési reakciókban. Az izolált diszacharid úgy írható le, mint α-d-glp (1 4)-β-D-Glp-(1-S-PNP). Összegezve: mutációval sikerült bevezetni transzferáz aktivitást a vad típusú amilázba, ami lehetővé tette enzimatikus transzglikozilezésekhez történő felhasználását. Az Y151M mutáns enzim képes a donor maltotetraóz nem redukáló végi szegmensének, a maltóznak vagy maltotrióznak alkalmas akceptorra történő átvitelére, ami a trimer és tetramer glikozidok képződéséhez vezetett. A tetramer glikozid enzimatikus hidrolízise eredményezi a dimer mint másodlagos transzfertermék képződését. A kísérleti körülmények optimalizálásával igen kényelmes és elegáns szintézis startégiát sikerült kidolgozni a rövidebb (DP 2-4) kromoforral szubsztituált homológ maltooligomerek előállítására, melyek humán amilázok szubsztrátjai vagy inhibitorai lehetnek. Az Y151M mutáns enzimet elsőként alkalmaztuk sikerrel transzglikozilezésekhez. A 4-nitrofenil 1-tio-β-maltooligoszacharidok (DP 2-4) NMR analízise igazolta, hogy az Y151M megtartotta regio-és sztereoszelektivitását. A glikozilezés a glikozil akceptor 4-es OH-ján történt és kizárólagosan α(1-4) glikozidos kötéseket eredményezett. Eredményeink igazolják, hogy mutáns enzimek használatával növelhető a transzglikozilezés/hidrolízis aránya, így a glikozilezés hozama. Ezen tapasztalatok
9 bátorítottak arra, hogy olyan újabb HSA mutánsok transzferáz aktivitását vizsgáljuk, melyek reményt keltőek lehetnek oligoszacharidok szintézisére. N. Ramasubbu laboratóriumában (UMD New Jersey, USA) egy új, exo-enzimet izoláltak, amely a biofilmet felépítő N-acetil-glükózamin (GlcNAc) egységekből álló poliszacharid lebontásáért felelős, és a szájban előforduló patogén mikroorganizmus az Actinobacillus actinomicetemcomitans termeli. Az enzim fontos szerepet tölt be a mikroorganizmus biofilmből való kiszabadulásában (diszperziójában), ezért a diszperzinb nevet kapta. Az enzim vizsgálatához szubsztrát sorozatokat terveztünk, melyeket a Debreceni Egyetem-MTA Szénhidrátkémiai Kutatócsoportjában Lipták András munkatársai szintetizáltak. A DP 2,4,6 tagszámú, 1-6) glikozidos kötésekkel összekapcsolódó GlcNAc egységeket tartalmazó, a redukáló végen 4-metoxi-fenil (PMP) kromofor csoportottal jelzett oligoszacharidok hidrolízis termékeinek HPLC analízise azt mutatja, hogy az enzim a szubsztrát nem redukáló végéről monomer egységet hasít. Megállapítottuk, hogy diszperzinb enzim egy (1-6) kötésekre specifikus exo hatásmechanizmusú hexózaminidáz. Az aktív hely feltérképezéséhez mutáns fehérjék és egy DP 2-5 tagszámú, tiofenil aglikont tartalmazó szubsztrát sorozat áll rendelkezésünkre. Eddigi eredményeinket két szénhidrátkémiai konferencián mutattuk be (Mátrafüred 2007, 2008) és egy közleményben foglaltuk össze (Acta Biologica Hungarica, 2008). Birte Svensson és kutatócsoportja (BioCentrum-DTU, Dánia) az ipari szempontból fontos árpa amilázokat tanulmányozza. A hosszú szubsztrátkötő árokkal rendelkező izoenzimek (AMY1 és AMY2 ) aktív centrumának feltérképezését a DP 3-12 tagszámú szubsztrát sorozatunk tette lehetővé. Elsőként közöltük az izoenzimek alhely térképeit (FEBS Letters, 2006). Bár mindkét izoenzim aktív centruma a alhely modellel írható le, azonban az egyes alhelyek energiaértékében szignifikás különbségek adódtak. Az alhely térképek a külső és belső gáthelyek jelenlétét is felfedték. A rendelkezésünkre álló aktív hely mutánsok vizsgálatával igazoltuk, hogy a (-6) alhely közelében elhelyezkedő Tyr105 aromás gyűrűje kulcsfontosságú a szubsztrát kötésében. Az árpa amilázokban a szubsztrát kötődése nemcsak a katalízisben részt vevő aktív helyen, hanem ún. másodlagos kötőhelyeken is végbemehet. Jelenleg az aktív hely és a másodlagos kötőhelyek mutáns fehérjéit vizsgáljuk a kötőhelyek ill. a módosított aminosavak szerepének tisztázása céljából.
10 Az AMY1 és izoenzimeinek figyelemreméltó tulajdonsága, hogy a hidrolitikus aktivitás mellett transzferáz aktivitással is rendelkeznek, vagyis a hidrolízis termékek mellett a szubsztrátnál hosszabb transzfertermékek is képződnek. Míg a hidrolízis/transzfer arány a vad típusú enzimben 8%, ez az arány 10 és 18 %-ra nő az Y105A ill. T212Y egyszeres mutánsokban, és tovább nő az Y105A/T212Y, valamint a V47K/S48G és a V47G/S48D kettős mutánsokban 20, 32 ill. 43%-ig. A mutáns enzimek transzferáz aktivitását enzimatikus glikozilezésekhez használjuk. Árpa amilázok, a természet szénhidrátkémikusai Az árpa amilázok transzferáz aktivitásának felismerése igen örvendetes, mert lehetővé teszi biotechnológiai alkalmazásukat különféle szintézisekhez. Jelenlegi kutatásaink a mutáns enzimek akceptor és donor specifitásainak tanulmányozására irányulnak. Maltopentaóz mint donor és PNP - és -Glc mint akceptor jelenlétében maltooligoszacharid glükozidok sorozatát állítottuk elő preparatív méretben. Jó hozamú transzglikozilezésre azonban a PNP -GlcNAc, -Xyl, Man és a szalicin is alkalmasnak bizonyult, ami lehetőséget ad heterooligoszacharidok enzimatikus szintézisére. Az izolált vegyületek szerkezetvizsgálata folyamatban van. Nyál amiláz inhibitorok tanulmányozása (BBRC 2004,2005, CR 2006, BBA 2008) A pályázati periódusban számos különböző szerkezetű szénhidrát, fehérje és polifenol típusú, köztük természetes eredetű, szintetikus és félszintetikus úton előállított vegyület inhibitor sajátságait vizsgáltuk. A természetes eredetű tanninok, valamint a kemoenzimatikus szintézissel nyert PTS-GTH szerkezetét MALDI-TOF MS, MALDI-TOF PSD MS, ESI MS, proton és szén NMR módszerekkel határoztuk meg. Megállapítottuk, hogy a kocsányos tölgy eredetű tanninban a központi kínasavhoz galluszsav dimer és trimer egységek kapcsolódnak, míg az allepói tölgy eredetű tanninban a glükózt monomer galluszsavak észteresítik, ami az aleppói tanninnak egy kompaktabb struktúrát ad igen kedvező enzim-inhibitor kölcsönhatással. A kellő számú OH csoport jelenléte lehetővé teszi a hidrogén hidak kialakulását az enzimmel, míg a galluszsav csoportok stacking kölcsönhatást létesítenek a HSA aromás aminosavaival, melynek erdményeként az aleppói tannin kitűnő inhibitora a humán nyál amiláznak, az akarbóz és a PTS-GTH-hoz hasonló inhibiciós állandóval.
11 A fehérje-inhibitor kölcsönhatás létrejöttét a pentagalloil-glükózzal (PGG), mint modell vegyülettel STD NMR és SPR módszerekkel igazoltuk. A PGG hozzákötődik a fehérje hidrofób régióihoz, feltehetően az aktív centrumot felépítő aromás aminosavak (Tyr151, Trp58, Trp59, Tyr62) a galluszsavak aromás gyűrűivel stacking kölcsönhatásokat létesítenek. A mutációt követően az aromás aminosavak környezetében domináló hidrofób kölcsönhatások és hidrogén híd kötések megszűnnek, így a PGG gátló hatása minimálisra csökken a Tyr151Met és Trp58Leu mutánsokban a vad típusú enzimhez képest. Eredményeink egyértelműen igazolják, hogy a gátlási mechanizmus egyrészt az aktív centrum közvetlen blokkolásán keresztül történik a (+2) és (-2) alhelyeknél, valamint a hidrofób kölcsönhatások és a hidrogénkötés hálózat kialakítása igen fontos tényező az inhibitor hatás létrejöttéért. Eredményeink feltehetően megadják az esélyt a lehető legjobb amiláz inhibitor vegyület kifejlesztésére, ami áldásos következményekkel járhat a diabetes, obesitas és fogszuvasodás megelőzésére és gyógyítására.
Oligoszacharidok előállítása kemoenzimatikus szintézissel. Doktori (Ph.D.) értekezés tézisei. Gálné Remenyik Judit. Témavezető: Dr.
 ligoszacharidok előállítása kemoenzimatikus szintézissel Doktori (Ph.D.) értekezés tézisei Gálné Remenyik Judit Témavezető: Dr. Kandra Lili Synthesis of oligosaccharides by chemoenzymatic methods Ph.D.
ligoszacharidok előállítása kemoenzimatikus szintézissel Doktori (Ph.D.) értekezés tézisei Gálné Remenyik Judit Témavezető: Dr. Kandra Lili Synthesis of oligosaccharides by chemoenzymatic methods Ph.D.
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Oligoszacharidok előállítása kemoenzimatikus szintézissel Doktori (Ph.D.) értekezés. Gálné Remenyik Judit
 ligoszacharidok előállítása kemoenzimatikus szintézissel Doktori (Ph.D.) értekezés Gálné Remenyik Judit Debreceni Egyetem, TEK, TTK MTA Szénhidrátkémiai Kutatócsoport Biokémiai Tanszék Debrecen, 2007.
ligoszacharidok előállítása kemoenzimatikus szintézissel Doktori (Ph.D.) értekezés Gálné Remenyik Judit Debreceni Egyetem, TEK, TTK MTA Szénhidrátkémiai Kutatócsoport Biokémiai Tanszék Debrecen, 2007.
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Az elvégzett munka összefoglalása a munkatervben megadott témák szerint:
 Zárójelentés a T043499 nyilvántartási számú Kutatások a MALDI-TOF tömegspektrometria szénhidrátkémiai alkalmazási lehetőségeinek kiszélesítésére című OTKA pályázatról A tömegspektrometria rendkívül hasznos
Zárójelentés a T043499 nyilvántartási számú Kutatások a MALDI-TOF tömegspektrometria szénhidrátkémiai alkalmazási lehetőségeinek kiszélesítésére című OTKA pályázatról A tömegspektrometria rendkívül hasznos
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
EXO GLIKOZID HIDROLÁZ ENZIMEK MŰKÖDÉSÉNEK TANULMÁNYOZÁSA AZ ÉDESBURGNYA β-amiláz ÉS A DISZPERZINB ENZIM VIZSGÁLATA
 Egyetemi doktori (PhD) értekezés tézisei EXO GLIKOZID HIDROLÁZ ENZIMEK MŰKÖDÉSÉNEK TANULMÁNYOZÁSA AZ ÉDESBURGNYA β-amiláz ÉS A DISZPERZINB ENZIM VIZSGÁLATA Fazekas Erika Témavezető: Dr. Gyémánt Gyöngyi
Egyetemi doktori (PhD) értekezés tézisei EXO GLIKOZID HIDROLÁZ ENZIMEK MŰKÖDÉSÉNEK TANULMÁNYOZÁSA AZ ÉDESBURGNYA β-amiláz ÉS A DISZPERZINB ENZIM VIZSGÁLATA Fazekas Erika Témavezető: Dr. Gyémánt Gyöngyi
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
[S] v' [I] [1] Kompetitív gátlás
![[S] v' [I] [1] Kompetitív gátlás [S] v' [I] [1] Kompetitív gátlás](/thumbs/93/114506146.jpg) 8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
8. Szeminárium Enzimkinetika II. Jelen szeminárium során az enzimaktivitás szabályozásával foglalkozunk. Mivel a klinikai gyakorlatban használt gyógyszerhatóanyagok jelentős része enzimgátló hatással bír
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Kutatási programunk fő célkitűzése, az 2 -plazmin inhibitornak ( 2. PI) és az aktivált. XIII-as faktor (FXIIIa) közötti interakció felderítése az 2
 Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
Kutatási programunk fő célkitűzése, az -plazmin inhibitornak ( PI) és az aktivált XIII-as faktor (FXIIIa) közötti interakció felderítése az PI N-terminális szakaszának megfelelő különböző hosszúságú peptidek
BIOLÓGIA DOKTORI ISKOLA Szénhidrátbontó enzimek gátlásának vizsgálata STZ indukált diabetes mellitus egérmodellben
 BIOLÓGIA DOKTORI ISKOLA Szénhidrátbontó enzimek gátlásának vizsgálata STZ indukált diabetes mellitus egérmodellben Takács István Gábor Doktori értekezés Témavezetők: Dr. Pósa Anikó Egyetemi adjunktus Dr.
BIOLÓGIA DOKTORI ISKOLA Szénhidrátbontó enzimek gátlásának vizsgálata STZ indukált diabetes mellitus egérmodellben Takács István Gábor Doktori értekezés Témavezetők: Dr. Pósa Anikó Egyetemi adjunktus Dr.
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise
 Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
Véralvadásgátló hatású pentaszacharidszulfonsav származék szintézise Varga Eszter IV. éves gyógyszerészhallgató DE-GYTK GYÓGYSZERÉSZI KÉMIAI TANSZÉK Témavezető: Dr. Borbás Anikó tanszékvezető, egyetemi
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
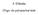 3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Definició: Két monoszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésben résztvevő C-atomok
A polifenol vegyületek rendszerezése
 A polifenol vegyületek rendszerezése Nem flavonoid fenolok tulajdonságai: Kevésbé összehúzó ízűek Hidroxi-fahéjsav és származékai (kávésav, ferulasav, kumársav) Szabad állapotban és antocianinokkal acilezett
A polifenol vegyületek rendszerezése Nem flavonoid fenolok tulajdonságai: Kevésbé összehúzó ízűek Hidroxi-fahéjsav és származékai (kávésav, ferulasav, kumársav) Szabad állapotban és antocianinokkal acilezett
Humán nyál amiláz inhibitorok vizsgálata doktori (PhD) értekezés tézisei. Zajácz Ágnes (Témavezet: Dr. Kandra Lili)
 Humán nyál amiláz inhibitorok vizsgálata doktori (PhD) értekezés tézisei Zajácz Ágnes (Témavezet: Dr. Kandra Lili) The study of human salivary amylase inhibitors theses of doctoral (PhD) dissertation Ágnes
Humán nyál amiláz inhibitorok vizsgálata doktori (PhD) értekezés tézisei Zajácz Ágnes (Témavezet: Dr. Kandra Lili) The study of human salivary amylase inhibitors theses of doctoral (PhD) dissertation Ágnes
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
II. IRODALMI ÁTTEKINTÉS
 I. BEVEZETÉS Az enzimek az él szervezet számára nélkülözhetetlenek, hiszen biokatalizátorok lévén lehetvé teszik az anyagcsere-folyamatok gyors végbemenetelét. Mai ismereteink szerint a természetben több
I. BEVEZETÉS Az enzimek az él szervezet számára nélkülözhetetlenek, hiszen biokatalizátorok lévén lehetvé teszik az anyagcsere-folyamatok gyors végbemenetelét. Mai ismereteink szerint a természetben több
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk.
 .5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
.5.Több szubsztrátos reakciók Több szubsztrátos enzim-reakciókról beszélve két teljesen különbözõ rekció típust kell megismernünk. A.) Egy enzim, ahhoz, hogy terméket képezzen, egyszerre több különbözõ
Kiss Tünde. ASPERGILLUS CARBONARIUS-BÓL IZOLÁLT EXTRACELLULÁRIS β-d-xilozidáz. doktori (Ph.D.) értekezés tézisei. Témavezető: Dr.
 ASPERGILLUS CARBONARIUS-BÓL IZOLÁLT EXTRACELLULÁRIS β-d-xilozidáz MŰKÖDÉSI MECHANIZMUSÁNAK VIZSGÁLATA doktori (Ph.D.) értekezés tézisei Kiss Tünde Témavezető: Dr. Kiss László Debreceni Egyetem, TTK Biokémiai
ASPERGILLUS CARBONARIUS-BÓL IZOLÁLT EXTRACELLULÁRIS β-d-xilozidáz MŰKÖDÉSI MECHANIZMUSÁNAK VIZSGÁLATA doktori (Ph.D.) értekezés tézisei Kiss Tünde Témavezető: Dr. Kiss László Debreceni Egyetem, TTK Biokémiai
DE Szerves Kémiai Tanszék
 DE Szerves Kémiai Tanszék Patonay Tamás Oxigéntartalmú heterociklusok fémkatalizált nitrilezése. kémia BSc; 1 fő Somsák László Kaszás Tímea Anhidro-aldóz tozilhidrazonok átalakítási lehetőségeinek vizsgálata
DE Szerves Kémiai Tanszék Patonay Tamás Oxigéntartalmú heterociklusok fémkatalizált nitrilezése. kémia BSc; 1 fő Somsák László Kaszás Tímea Anhidro-aldóz tozilhidrazonok átalakítási lehetőségeinek vizsgálata
α-amilázok termékanalízisen és molekuláris modellezésen alapuló alhelytérképezése és transzglikozidáz aktivitásuk vizsgálata
 Egyetemi doktori (Ph.D.) értekezés tézisei α-amilázok termékanalízisen és molekuláris modellezésen alapuló alhelytérképezése és transzglikozidáz aktivitásuk vizsgálata Mótyán János András Témavezető: Dr.
Egyetemi doktori (Ph.D.) értekezés tézisei α-amilázok termékanalízisen és molekuláris modellezésen alapuló alhelytérképezése és transzglikozidáz aktivitásuk vizsgálata Mótyán János András Témavezető: Dr.
A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban. doktori (PhD) értekezés.
 A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban doktori (PhD) értekezés Gyémánt Gyöngyi Debreceni Egyetem, TTK Biokémiai Tanszék Debrecen, 2001.
A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban doktori (PhD) értekezés Gyémánt Gyöngyi Debreceni Egyetem, TTK Biokémiai Tanszék Debrecen, 2001.
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
R-OH H + O H O H OH H O H H OH O H OH O H OH H H
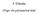 3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
3. Előadás ligo- és poliszacharidok Diszacharidok Defiició: Két mooszacharid kapcsolódása éter kötéssel Leírás: Összetevők, kötéstípus, térállás R- + R glikozid Csoportosítás a kötésbe résztvevő C-atomok
Szénhidrátkémiai kutatások bioinformatikai esetek. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Szénhidrátkémiai kutatások bioinformatikai esetek Dr. Harangi János DE, TTK, Biokémiai Tanszék Intranet http://dspace.lib.unideb.hu:8080/dspace/handle/2437/2815 Fő kutatási területek Enzimek vizsgálata
Szénhidrátkémiai kutatások bioinformatikai esetek Dr. Harangi János DE, TTK, Biokémiai Tanszék Intranet http://dspace.lib.unideb.hu:8080/dspace/handle/2437/2815 Fő kutatási területek Enzimek vizsgálata
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE
 Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
Glükoproteinek (GP) ELŐADÁSVÁZLAT ORVOSTANHALLGATÓK RÉSZÉRE SZTE ÁOK Biokémia Intézet összeállította: dr Keresztes Margit Jellemzők - relative rövid oligoszacharid láncok ( 30) (sok elágazás) (1-85% GP
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során
 Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során 1. projekt Kvaterner ammónium ligandot használó enzimek ligand kötőhelyének
Kutatási eredményeim a 2014 február 1- augusztus 31. a Varga József Alapítvány Pungor Ernő doktorjelölti ösztöndíjas időszak során 1. projekt Kvaterner ammónium ligandot használó enzimek ligand kötőhelyének
FEHÉRJÉK A MÁGNESEKBEN. Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium. Alkímia Ma, Budapest,
 FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
FEHÉRJÉK A MÁGNESEKBEN Bodor Andrea ELTE, Szerkezeti Kémiai és Biológiai Laboratórium Alkímia Ma, Budapest, 2013.02.28. I. FEHÉRJÉK: L-α aminosavakból felépülő lineáris polimerek α H 2 N CH COOH amino
Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás
 Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás kockázatát mérik fel. Annak érdekében, hogy az anyavegyületével
Az Ames teszt (Salmonella/S9) a nemzetközi hatóságok által a kémiai anyagok minősítéséhez előírt vizsgálat, amellyel az esetleges genotoxikus hatás kockázatát mérik fel. Annak érdekében, hogy az anyavegyületével
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
SZÉNHIDRÁTOK. Biológiai szempontból legjelentősebb a hat szénatomos szőlőcukor (glükóz) és gyümölcscukor(fruktóz),
 SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
SZÉNHIDRÁTOK A szénhidrátok döntő többségének felépítésében három elem, a C, a H és az O atomjai vesznek részt. Az egyszerű szénhidrátok (monoszacharidok) részecskéi egyetlen cukormolekulából állnak. Az
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
Oligoszacharid-fehérje konjugátumok elöállítása OTKA ny.sz.: 35128
 ligoszacharid-fehérje konjugátumok elöállítása TKA ny.sz.: 35128 A kutatási idöszakban elért eredmények három csoportba sorolhatók: 1. Mikobakteriális eredetü sejtfelszíni oligoszacharidok elöállítása,
ligoszacharid-fehérje konjugátumok elöállítása TKA ny.sz.: 35128 A kutatási idöszakban elért eredmények három csoportba sorolhatók: 1. Mikobakteriális eredetü sejtfelszíni oligoszacharidok elöállítása,
A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban. doktori (PhD) értekezés tézisei
 A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban doktori (PhD) értekezés tézisei Gyémánt Gyöngyi Debreceni Egyetem, TTK Biokémiai Tanszék Debrecen,
A nagyhatékonyságú-folyadékkromatográfia alkalmazása szénhidrátkémiai és szénhidrát-biokémiai kutatásokban doktori (PhD) értekezés tézisei Gyémánt Gyöngyi Debreceni Egyetem, TTK Biokémiai Tanszék Debrecen,
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Gyógyszerrezisztenciát okozó fehérjék vizsgálata
 Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Gyógyszerrezisztenciát okozó fehérjék vizsgálata AKI kíváncsi kémikus kutatótábor 2017.06.25-07.01. Témavezetők : Telbisz Ágnes, Horváth Tamás Kutatók : Dobolyi Zsófia, Bereczki Kristóf, Horváth Ákos Gyógyszerrezisztencia
Szénhidrátok I. (Carbohydrates)
 sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
sztályozás: Szénhidrátok I. (arbohydrates) Polihidroxi-aldehidek (aldózok) vagy polihidroxi-ketonok (ketózok) és származékaik. általános képlet: ( ) n / n ( ) m ; n, m 3 (egész számok) monoszacharidok:
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások
 ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
Intelligens molekulákkal a rák ellen
 Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Intelligens molekulákkal a rák ellen Kotschy András Servier Kutatóintézet Rákkutatási kémiai osztály A rákos sejt Miben más Hogyan él túl Áttekintés Rákos sejtek célzott támadása sejtmérgekkel Fehérjék
Exo glikozid hidroláz enzimek működésének tanulmányozása
 DE TTK 1949 Exo glikozid hidroláz enzimek működésének tanulmányozása Az édesburgonya β-amiláz és a DiszperzinB enzim vizsgálata Egyetemi doktori (PhD) értekezés Szerző neve: Fazekas Erika Témavezető neve:
DE TTK 1949 Exo glikozid hidroláz enzimek működésének tanulmányozása Az édesburgonya β-amiláz és a DiszperzinB enzim vizsgálata Egyetemi doktori (PhD) értekezés Szerző neve: Fazekas Erika Témavezető neve:
Leukotriénekre ható molekulák. Eggenhofer Judit OGYÉI-OGYI
 Leukotriénekre ható molekulák Eggenhofer Judit OGYÉI-OGYI Mik is azok a leukotriének? Honnan ered az elnevezésük? - először a leukocitákban mutatták ki - kémiai szerkezetükből vezethető le - a konjugált
Leukotriénekre ható molekulák Eggenhofer Judit OGYÉI-OGYI Mik is azok a leukotriének? Honnan ered az elnevezésük? - először a leukocitákban mutatták ki - kémiai szerkezetükből vezethető le - a konjugált
Fehérjeszerkezet, és tekeredés
 Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
Fehérjeszerkezet, és tekeredés Futó Kinga 2013.10.08. Polimerek Polimer: hasonló alegységekből (monomer) felépülő makromolekulák Alegységek száma: tipikusan 10 2-10 4 Titin: 3,435*10 4 aminosav C 132983
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK
 POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
POSZTTRANSZLÁCIÓS MÓDOSÍTÁSOK: GLIKOZILÁLÁSOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék 1 Glikozilálás A rekombináns fehérjék
Aspergillus carbonarius-ból izolált extracelluláris β D-glükozidáz működési mechanizmusának vizsgálata. doktori (PhD) értekezés tézisei.
 Aspergillus carbonarius-ból izolált extracelluláris β D-glükozidáz működési mechanizmusának vizsgálata doktori (PhD) értekezés tézisei Jäger Szilvia Témavezető: Dr. Kiss László Investigation the mechanism
Aspergillus carbonarius-ból izolált extracelluláris β D-glükozidáz működési mechanizmusának vizsgálata doktori (PhD) értekezés tézisei Jäger Szilvia Témavezető: Dr. Kiss László Investigation the mechanism
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
Általános megjegyzések
 ZÁRÓJELENTÉS Általános megjegyzések A T 048713 sz. kutatási pályázat futamideje során az eredeti munkatervhez képest több módosulás / módosítást történt; ezeket túlnyomó részben a külső körülmények előre
ZÁRÓJELENTÉS Általános megjegyzések A T 048713 sz. kutatási pályázat futamideje során az eredeti munkatervhez képest több módosulás / módosítást történt; ezeket túlnyomó részben a külső körülmények előre
Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése
 Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése Előadó: Lihi Norbert Debreceni Egyetem Szervetlen és Analitikai Kémiai Tanszék Bioszervetlen Kémiai Kutatócsoport A bioszervetlen
Fémionok szerepe az élő szervezetben: a bioszervetlen kémia alapjainak megismerése Előadó: Lihi Norbert Debreceni Egyetem Szervetlen és Analitikai Kémiai Tanszék Bioszervetlen Kémiai Kutatócsoport A bioszervetlen
OTKA nyilvántartási szám: F Töltéssel rendelkező oldalláncok szerepe retrovirális proteinázok szubsztrát-specificitásában Az elmúlt évtizedek
 Az elmúlt évtizedek intenzív kutatásai ellenére is ma még komoly kihívást jelent az emberiség számára az évről évre egyre több áldozatot szedő betegség a szerzett immunhiányos szindróma (AIDS), amit a
Az elmúlt évtizedek intenzív kutatásai ellenére is ma még komoly kihívást jelent az emberiség számára az évről évre egyre több áldozatot szedő betegség a szerzett immunhiányos szindróma (AIDS), amit a
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
ENZIMSZINTŰ SZABÁLYOZÁS
 ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
ENZIMEK 1833.: Sörfőzés kapcsán kezdtek el vele foglalkozni (csírázó árpa vizsgálata) valamilyen anyag katalizátorként működik (Berzelius, 1835.) 1850. körül: ez valamilyen N-tartalmú szervesanyag 1874.:
MedInProt Szinergia IV. program. Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére
 MedInProt Szinergia IV. program Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére Tantos Ágnes MTA TTK Enzimológiai Intézet, Rendezetlen fehérje kutatócsoport
MedInProt Szinergia IV. program Szerkezetvizsgáló módszer a rendezetlen fehérjék szerkezetének és kölcsönhatásainak jellemzésére Tantos Ágnes MTA TTK Enzimológiai Intézet, Rendezetlen fehérje kutatócsoport
ZÁRÓJELENTÉS. OAc. COOMe. N Br
 ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
ZÁRÓJELETÉS A kutatás előzményeként az L-treoninból kiindulva előállított metil-[(2s,3r, R)-3-( acetoxi)etil-1-(3-bróm-4-metoxifenil)-4-oxoazetidin-2-karboxilát] 1a röntgendiffrakciós vizsgálatával bizonyítottuk,
Hús és hústermék, mint funkcionális élelmiszer
 Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Hús és hústermék, mint funkcionális élelmiszer Szilvássy Z., Jávor A., Czeglédi L., Csiki Z., Csernus B. Debreceni Egyetem Funkcionális élelmiszer Első használat: 1984, Japán speciális összetevő feldúsítása
Májer Gábor (Témavezető: Dr. Borbás Anikó)
 Anionos oligoszacharidok szintézise 1-dezoxi-1-etoxiszulfonil-hept--ulopiranozil építőelemek felhasználásával. Ketopiranozil-glikozidok anomer konfigurációjának vizsgálata doktori (PhD) értekezés tézisei
Anionos oligoszacharidok szintézise 1-dezoxi-1-etoxiszulfonil-hept--ulopiranozil építőelemek felhasználásával. Ketopiranozil-glikozidok anomer konfigurációjának vizsgálata doktori (PhD) értekezés tézisei
Reakciókinetika és katalízis
 Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
Reakciókinetika és katalízis 14. előadás: Enzimkatalízis 1/24 Alapfogalmak Enzim: Olyan egyszerű vagy összetett fehérjék, amelyek az élő szervezetekben végbemenő reakciók katalizátorai. Szubsztrát: A reakcióban
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Biotechnológiai alapismeretek tantárgy
 Biotechnológiai alapismeretek tantárgy A biotechnológiai alapismeretek tantárgy magába foglalja a kémia, fizikai kémia és a biológia tantárgyak témaköreit. 1. A) Ismertesse az atomok elektronszerkezetét!
Biotechnológiai alapismeretek tantárgy A biotechnológiai alapismeretek tantárgy magába foglalja a kémia, fizikai kémia és a biológia tantárgyak témaköreit. 1. A) Ismertesse az atomok elektronszerkezetét!
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Vízben oldott antibiotikumok (fluorokinolonok) sugárzással indukált lebontása
 Vízben oldott antibiotikumok (fluorokinolonok) sugárzással indukált lebontása Doktori beszámoló 5. félév Készítette: Tegze Anna Témavezető: Dr. Takács Erzsébet ÓBUDAI EGYETEM ANYAGTUDOMÁNYOK ÉS TECHNOLÓGIÁK
Vízben oldott antibiotikumok (fluorokinolonok) sugárzással indukált lebontása Doktori beszámoló 5. félév Készítette: Tegze Anna Témavezető: Dr. Takács Erzsébet ÓBUDAI EGYETEM ANYAGTUDOMÁNYOK ÉS TECHNOLÓGIÁK
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek.
 Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Szénhidrátok Szerkesztette: Vizkievicz András A szénhidrátok az élet szempontjából rendkívül fontos, nélkülözhetetlen vegyületek. A bioszféra szerves anyagainak fő tömegét adó vegyületek. A szénhidrátok
Spektroszkópiai módszerek 2.
 Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
VEBI BIOMÉRÖKI MŰVELETEK
 VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
VEBI BIOMÉRÖKI MŰVELETEK KÖVETELMÉNYEK. Pécs Miklós: Vebi Biomérnöki műveletek. 1. előadás: Bevezetés és enzimkinetika
 VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
VEB BOMÉRÖK MŰVELETEK Műszaki menedzser BSc hallgatók számára 3 + 1 + 0 óra, részvizsga Előadó: dr. Pécs Miklós egyetemi docens Elérhetőség: F épület, FE lépcsőház földszint 1 (463-) 40-31 pecs@eik.bme.hu
A flavonoidok az emberi szervezet számára elengedhetetlenül szükségesek, akárcsak a vitaminok, vagy az ásványi anyagok.
 Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
SZÉNHIDRÁTOK (H 2. Elemi összetétel: C, H, O. O) n. - Csoportosítás: Poliszacharidok. Oligoszacharidok. Monoszacharidok
 Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
Szénhidrátok SZÉNIDRÁTK - soportosítás: Elemi összetétel:,, n ( 2 ) n Monoszacharidok (egyszerű szénhidrátok) pl. ribóz, glükóz, fruktóz ligoszacharidok 2 6 egyszerű szénhidrát pl. répacukor, tejcukor
Inzulinutánzó vanádium-, és cinkkomplexek kölcsönhatásának vizsgálata vérszérum fehérjékkel
 Inzulinutánzó vanádium-, és cinkkomplexek kölcsönhatásának vizsgálata vérszérum fehérjékkel Mivel a vizsgált komplexek inzulinutánzó hatása összetett és a hatásmechanizmusuk csak részben feltárt az irodalomban,
Inzulinutánzó vanádium-, és cinkkomplexek kölcsönhatásának vizsgálata vérszérum fehérjékkel Mivel a vizsgált komplexek inzulinutánzó hatása összetett és a hatásmechanizmusuk csak részben feltárt az irodalomban,
Szénhidrátok. Szénhidrátok. Szénhidrátok. Csoportosítás
 Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
Szénhidrátok Definíció: Szénhidrátok Polihidroxi aldehidek vagy ketonok, vagy olyan vegyületek, melyek hidrolízisével polihidroxi aldehidek vagy ketonok keletkeznek. Elemi összetétel: - Mindegyik tartalmaz
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Záróvizsga követelmények (Vegyész mesterképzési szak)
 Záróvizsga követelmények (Vegyész mesterképzési szak) A záróvizsga célja: A végzős hallgató szakmai ismereteinek ellenőrzése, különös tekintettel az ismeretek alkalmazásában nyújtott képességeire. A záróvizsgán
Záróvizsga követelmények (Vegyész mesterképzési szak) A záróvizsga célja: A végzős hallgató szakmai ismereteinek ellenőrzése, különös tekintettel az ismeretek alkalmazásában nyújtott képességeire. A záróvizsgán
1. feladat. Versenyző rajtszáma: Mely vegyületek aromásak az alábbiak közül?
 1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
1. feladat / 5 pont Mely vegyületek aromásak az alábbiak közül? 2. feladat / 5 pont Egy C 4 H 8 O összegképletű vegyületről a következő 1 H és 13 C NMR spektrumok készültek. Állapítsa meg a vegyület szerkezetét!
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
