N-metilezés (példa egy S N reakcióra):
|
|
|
- Rudolf Orsós
- 9 évvel ezelőtt
- Látták:
Átírás
1 Tartalomjegyzék -metilezés (példa S reakcióra) DS szintézis: (példa észter kötés kialakítására, egy S reakció foszfor centrumon) A koleszterin bioszintézise (addíció, izomerizáció, anionotrópia, elimináció) Biológiai oxidáció (epoxidképződés, addíció) Alkohollebontás (oxido-redukció, aromatizáció) A látás fotokémiája (addíció, elimináció, izomerizáció) Biodegradáció: amidok hidrolízise (addíció, elimináció) Peptidek szintézise (sav- és báziskatalizált elimináció) Jódfelvétel, a tiroxin bioszintézise (aromás elektrofil szubsztitúció) Sztereokémiai inverzió (elimináció báziskatalízissel) ogyan működik, amíg hat a penicillin (aciltranszfer) Biológiai környezetvédelem (aromás nukleofil szubsztitúció) Milyen kémiaimechanizmussal világít a szentjánosbogár? ovokain totálszintézise A szacharin totálszintézise:
2 -metilezés (példa egy S reakcióra): tapasztalat: Állati és növényi sejtekben a - 3 csoport átvihető a metioninról (Met) a megfelelő molekula nitrogénatomjára. A reakció 14 tartalmú Met-tel nyomon követhető: az izotóppal jelölt metilcsoport egy sor molekulában kimutatható: memo: kolin (neuron ingerület átvitel), adrenalin (vérnyomás emelő), nikotin (AD, alkaloid, méreg) a tényleges metilezőszer: S-adenozilmetionin (SAM)
3 Az S-adenozilmetionin képződése (S reakció): mechanizmus: a metionin kénatomja mint nukleofil megtámadja az ATP-t, és az S -reakcióban a trifoszfát anion a távozó csoport. A reakció során a szulfid metilszulfónium kationná alakul. TD = a.u. EPS töltés 0.08
4 A tényleges metilezés: az etanolamin,-dimetil származékának metilezése 1. memo: az etanolamin,-dimetilszármazéka - és nem -nukleofil. A szulfóniumsó metil- (és nem a metilén-) szénatomján megy végbe a reakció, mivel az utóbbi sztérikusan gátolt. 2. memo: azért nem támad az közvetlenül az S + -ra mert akkor nincs jó távozó csoport. Viszont a szulfid (tioéter, - 2 -S- 2 -) az jó távozó csoport. megjegyzés: Az -metilezés nem közvetlenül megy végbe, hanem S-adenozil- metionin (SAM, újabban AdoMet, lásd növényélettan) közvetítésével R? R' R 2 S 2 3
5 DS szintézis: észter kötés kialakítása (egy S reakció foszfor centrumon) A DS és RS hidrolizálhatósága savas hidrolízis RS lúgos hidrolízis eredmény: lánchasadás memo: ezért az RS kevésbé, míg a DS jobban ellenáll a lúgos hidrolízisnek
6 Védőcsoportok I: a bázisok védelme permanens csoportokkal. él: a primer aminok védelme, avagy a nukleofil csoportok (pl. aminok) álcázása, hogy a kapcsolásnál már csak a ridóz 5 legyen az egyetlen nukleofil. 6 -benzoilezés G 2 -izobutiril 4 -benzoilezés 4 -acetilezés vagy nem kell védeni
7 Védőcsoportok II: a foszfodiészter védelme permanens csoporttal Mindkét típusú permanens védőcsoport (mind az -acil, mind a cianoetilészter) eltávolítható vizes ammóniával ( 3 / 2 ). memo: a szintézis végén az összes állandó védőcsoportot vizes ammóniával kvantitatív módon eltávolítható. Védőcsoport: az 5 - csoport ideiglenes védelme cianoetilészter formában E P B B Dmtr (enyhén savas rendszer) 2 l 2 + 3% l (narancs szín)
8 Szilárd hordozó: PG (controlled pore glass) kontrolált pórusú üveg -kémiailag inert -nem duzzad -amino funkcionalizált Me PG Si ( 2 ) n 2 Me Linker : Pl. borostyánkősav 2 ( 2 ) n Me Si Me PG 2 3 / 2 hasító hely
9 DS kémiai szintézise: -szilárdfázisú szintézis 3 -től 5 irányba halad: McBride, L. J.; aruthers, M ) 1. Dmtr hasítás (dimetoxi-tritil) memo: a DS bioszintézise 5 -től 3 irányba megy enyhe savas detritilezés (3% TA) 2. Aktiválás és kapcsolás foszforamidit tetrazol (gyenge sav) E S (5' S reakciója)
10 dialkilamin amely jó távozócsoport 3. Lánczárás (az elreagálatlan 5 --t acetilezzük) 4. xidálás I 2 ( 2 vagy TF) iklus végén: - minden permanens védőcsoport eltávolítása - gyantáról való lehasítás - kromatográfiás tisztítás 4 -val
11 ligonukleotid szintézis:foszforamidit kapcsolási módszer McBridge és aruthers Dmtr hasítás (dimetoxi-tritil) 2. Aktiválás és kapcsolás xidálás I2 (2 vagy TF) Lánczárás (az elreagálatlan 5 --t acetilezzük) 3.
12 d da da - A Szilárdfázisú DS szintézise: Jelmagyarázat: da da := Dmtr, 5 -védőcsoport := hordozó gyanta := szabad 3 -vég := szabad 5 -vég := linker 2'-deoxinukleozidok (da, d, dg, and dt) 5 3 da d kapcsolás d d da da d hasítás dg dt 12
13 d da d da da d da terminálás da d da következő ciklus
14 d d da da da da d da d da következő ciklus
15 Koleszterin bioszintézise (addíció, izomerizáció, anionotrópia, elimináció): szkvalén szteroidok bioszintézise: a szkvalénbol egy enzim ( terpenoid cikláz) alakítja ki a 4-gyűrűs szteránvázat lanoszterin királis (asszimetriás) szénatom 2 7 = 128 lehetséges sztereoizomer közül csupán egyetlen egy keletkezik memo: cholesterol, lanosterol (alkohol jellegre utaló angol nevek) hol itt a szerves kémia? koleszterin 8 asszimetriás szénatom 2 8 = 256 lehetséges sztereoizomer
16 A szkvalén (polién) egy oxidációs lépést követően 3(S)-2,3-epoxiszkvalénné (egy epoxiddá) alakul amely protonálódik. A gyűrűhasadással kialakuló karbokation egy alkénaddíció-szerű láncreakcióban vesz részt. szkvalén- epoxid szkvalén protonált szkvalén-epoxid memo: izoprénből keletkező triterpén (Bruckner II/2 1628) egy S 1 reakció első lépése karbokation típusú szkvalénszármazék (gyűrűfelnyílással képződik egy intramolekuláris S 1 során) intramolekuláris Ad E I intramolekuláris Ad E II még két hasonló lépés kell a végleges térszerkezet kialakításához Ad E III é s Ad E IV
17 A szkvalén (polién) egy oxidációs lépést követően 3(S)-2,3-epoxiszkvalénné (egy epoxiddá) alakul amely protonálódik. A gyűrűhasadással kialakuló karbokation egy alkénaddíció-szerű láncreakcióban vesz részt. Bruttó addíciós séma:
18 memo: Markovnyikov szabály Érvényesül a Markovnyikov-szabály: a tercier karbokation képzõdik memo: a 3. számú szénatom konfigurációja szekunder karbokation (a kevésbé stabil) nem képződik A gyűrűzárást eredményező négy lépésből (Ad E ) a harmadik nem követi a Markovnyikov-szabályt (kivétel erősíti a szabályt): szekunder karbokation tercier karbokation 3
19 A lanoszterin képződésének második szakaszában bázis hatására képződő karbokation stabilizálódik : (Bruckner II/2 1394)
20 Biológiai oxidáció (epoxidképződés, addíció): xidáció hatására karcinogén metabolitok képződnek a májban és a belekben.
21 memo: nukleofil (amin, imin, tiol, stb.) reakciója epoxidokkal: peroxisavas oxidáció KMn 4 -os oxidáció Az epoxidok erős elektrofilek és ezért rákkeltőek - ha pl. glutationhoz (-S) kapcsolódik, akkor vízoldhatóvá válik és távozik a szervezetből, - ha dezoxiguanozinnal (- 2 ) találkozik, akkor ahhoz kapcsolódva negatív hatást fejthet ki.
22 1) Az oxidáció a normál méregtelenítő metabolizmus része: Az oxidálódott aflatoxin nukleofil szubsztitúciós reakció során kapcsolódik a glutationhoz, s így jóval polárisabbá válik. A vízoldható tioéter kiürül.
23 2) A normál méregtelenítő metabolizmus kísérője a karcinogén vegyület képződése: A dezoxiguanozin-származék képződése miatt a helyes DS bázispár térbeli okok miatt már nem tud kialakulni biológiai alkilezés helye 2,8 Â citozin 3,0 Â guanin
24 A citosztatikumok egyik fajtájának, a mustároknak gyógyító hatása hasonló típusú reakción alapszik mint a karcinogén hatás kiváltása (ismét egy S -reakció): memo: a kémiailag összekötött DS apoptózist indukál
25 Alkohollebontás (oxido-redukció, aromatizáció): A AD egyensúlyi reakciója az acetaldehidet etil-alkohollá redukálja. alkohol-dehidrogenáz enzim (AD + inhibitor komplex) leírás: a nikotinsav-amid nitrogénjének nemkötő elektronpárja delokalizálódik, a dihidropiridin gyűrű aromássá válik az egyik 4-es hidrogénatomot anionként leadva. A hidridion redukálja az acetaldehidet, majd a képződő alkoholát anion protonálódik. A cink, mint Lewis-sav fokozza a karbonil-szén pozitív polározottságát s így annak elektrofil jellegét. méregtelenítés: ha nagy az alkoholkoncentráció, akkor az egyensúlyi reakció megfordul és az etil-alkohol acetaldehidé oxidálódik
26 az alkohol-dehidrogenáz enzim apoenzim + koenzim + inhibitor (80 kda dimer, az emberben legalább 6 variánsa van, előfordulás, máj és gyomor) memo: Miért mérgezők az alkohol végzetes adalékai: metanol, etilénglikol? 2 feladatuk: - egyensúlyt tartani az alkoholok aldehidek és ketonok között. P P 2 - méregtelenítés (emlősben): a toxikus alkoholt aldehidé oxidálja - fermentálás (baci és élesztő): aldehidből alkoholt készít (redukció) A AD+ (ikotinsavamid-adenin-dinukleotid) (az élő sejt egyik oxidáló vagy dehidrogénező szere)
27 A látás fotokémiája (addíció, elimináció, izomerizáció): Az emberi szem kétfajta receptorsejtet tartalmaz: pálcikákat és csapokat Pálcikák: retina peremén helyezkednek el, gyenge fényviszonyoknál aktívak színlátásra nem alkalmasak. sapok: retina központi részén találhatók, erős fényviszonyok között aktívak, színlátásért felelősek. galambok (csak csapok s ezért csak nappal látnak), baglyok (csak pálcikák, s ezért színvakok, viszont szürkületben is remekül látnak) A pálcikákban található rodopszin kromofórja a 11-cisz-retinal. A rodopszin kialakulása során a retinal karbonilcsoportjára addícionálódik a fehérje egy aminocsoportja (Ad -reakció), majd egy molekula víz eliminálásaval jön létre az imin (ez a rodopszin). 27
28 Schiff-bázis: aldehid + amino - víz Ad + E R 2 R R R R 2
29 Eredeti megfigyelés: fényre a békák retinájának pigmentanyaga szint vált: vörös-liláról sárgára (1877-ben Franz Boll) A 11-cisz-retinal a kromofór, ez köti meg a fényt: cisz 3 rodopszin abszorpciós max = 498 nm (vöröses lila szín) Fehérje rodopszin h (foton) 150 kj/mol 3 batorodopszin 3 3 néhány lépés 3 11-transz 3 Fehérje metarodopszin Ad és E 2 3 opszin + all-transz retinal max = 387 nm (sárga szín) 11-transz 3 all-transz retinal + 2 Fehérje (opszin)
30 Ad + E 2 R + - R R R R 2 2 2
31 11-cisz retinal all-transz retinal all-transz retinalt tartalmazó szarvasmarha rodopszin (a metarodopszin elméleti modellje)
32 Delokalizált elektronok száma (dobozhossz [L] ) 2 ( 2Â) 4 ( 5Â) 24 ( 30Â) ( 2n) ( 3nÂ) 7 ev 5 ev 2-3 ev 1,5 ev 2 n Gerjesztési energia ( M-LUM átmenet) UV vörös ibolya IR látható molekula módszer M LUM de (artree) de (kcal/mol) de (ev) hullám hossz (nm) etilén rhf6/3-21g -0,380 0,187 0, ,5 80 etilén rhf/ gdp -0,380 0,049 0, ,8 106 etilén b3lyp/ gdp -0,282-0,011 0, ,4 168 butadién (cisz) butadién (transz) b3lyp/ gdp -0,242-0,053 0, ,2 241 b3lyp/ gdp -0,243-0,043 0, ,5 227 retinal b3lyp/ gdp// (11-cisz) rhf/3-21g retinal b3lyp/ gdp// (all-transz) rhf/3-21g -0,219-0,090 0, , ,217-0,091 0, ,5 360
33 Biodegradáció: amidok hidrolízise (addíció, elimináció) Szerinproteázok (sok egymással nem feltétlenül rokon fehérje) A fehérjék lebontó enzimek (proteázok): pl. kimotripszin, tripszin és elasztáz. (Azért szerinproteáz, mert van benne egy a katalízis szempontjából döntő fontosságú Ser.) A Kimotripszin: specificitása: főleg Trp, Tyr, Phe, de Leu, Met után is hasítja az amidkötést memo: észtereket is hidrolizál memo: a tripszin más specificitású: Arg vagy Lys után hasít. Az inaktív kimotripszinogénből (245 as.) két dipeptid kihasadása és egy refolding során képződik az enzim. A konformációs átrendeződés eredményeként sztérikusan közel kerül a katalitikus triád 3 eleme. A katalitikus triád: Asp is Ser
34 Szubsztrátkötő hely Aktív hely, benne a katalitikus triáddal oxianion üreg ez a peptidkötés fog elhasadni szubsztrátkö tő zseb egy aromás (R1) csoporttal rendelkező szubsztrát - terminális része
35 Biodegradáció: amidok hidrolízise (addíció, elimináció) Szerin-proteázok működési mechanizmusa: Asp is 57 2 Ser 195 R 2 R nukleofil addíció Asp is 57 2 Ser 195 szubsztrátkötő zseb R 2 R tetraéderes intermedier
36 Asp is 57 2 Ser Az aktív hely regenerálódása R 2 R acilezett szerin Asp is 57 2 Ser 195 R 2 2 R acilezett szerin
37 memo: lehet készíteni olyan enzimet, amelyik a fordított folyamatot katalizálja a riboszómán a fehérjeszintézis során (RS-részek közreműködésével) feltehetőleg ilyen fordított folyamat zajlik. Asp is 57 2 Ser R tetraéderes intermedier Asp is 57 2 Ser regenerált aktív centrum karbonsav termék R
38 Összefoglalás: A kimotripszin irreverzibilis inhibitora: pl. DIPF
39 A kimotripszin két alegysége és a katalitikus triád A kimotripszin és a hozzá kötött inhibitor
40 Peptidek szintézise (sav- és báziskatalizált elimináció, ): -terminális védőcsoportok: korábban: Boc-stratégia R ma: Fmoc-stratégia hasítás TFA hasítás F 2 R hasítás 20% DMF hasítás TFA Alkalmazott hordozó: Wang -linker (600 polimer gyanta) : hordozó R- : polimer gyöngy R
41 A Boc-védőcsoport hasításának mechanizmusa (savval-kiváltott (elektrofil) elimináció) : peptid
42 Az Fmoc-védőcsoport hasításának mechanizmusa (Bázissal (nukleofillal) -kiváltott elimináció): : peptid 2 proton transzfer + memo: a hajtóerő oka, hogy a kialakuló anion esetében az aromacitás kiterjed a molekula egészére + + +
43 Egy példa a -terminális karboxilát aktiválására: Bt -hidroxi-benztriazol PF 6 BTU 2-(1-benzotriazol-1-il)-1,1,3,3-tetramethiluronium-hexafluorofoszfát PF 6 R R + deprotonált Bt R + -alkilurea aktívészter
44 4) Polipeptidek szintézise: a --B-A- tripeptid szintézismenete: Jelmagyarázat: B A := -terminális védőcsoport := -terminális védőcsoport := szabad -terminális := szabad -terminális B A kapcsolás -term. hasítás B A kapcsolás B A -term. majd -term. hasítás B A 44
45 Peptid szintézis lépései: Fmoc-A linker Linkerre kötés: Fmoc-A 1 ---linker piperidines hasítás 2 -A 1 ---linker Fmoc-A 2 -Bt Fmoc-A 2 -A 1 ---linker + Bt piperidines hasítás 2 -A 2 -A 1 ---linker hasítás a gyantáról védõcsoport eltávolítás kromatográfiás tisztítás
46 Jódfelvétel, a tiroxin bioszintézise (aromás elektrofil szubsztitúció): A jódfelvétel első lépése a reaktív jódvegyület képződése: I I- + típusú reakció a jódperoxidáz enzim katalizál. Az aktivált jódot (a I--t) a tiroglobin fehérje tirozinjainak hidroxifenil-csoportjai kötik meg az alábbi reakcióban: Tyr Tyr 2 S E (aromás) jódperoxidáz I I I 2 I S E (alifás) jódperoxidáz I I I 2 I I A két tirozil-oldallánc ugyanahhoz a fehérjemolekulához tartozik! I I S (aromás) - I 3 2 a fehérje hidrolízise 2 majd S (alifás) 2 I I I I I I I I I I I 2 2 tiroxin I
47 1. lépés S E 2 (aromás) + + I EPS töltés TD = a.u. hidroxilcsoport: orto-, para-irányítás, aktiválás (para-helyzet foglalt) alkilcsoport: orto-, para-irányítás, aktiválás (para-helyzet foglalt, orto-helyzet térben gátolt) 2. lépés S E (alifás) I I + I I I I + I I I 3. lépés S (aromás) + S (alifás) Elektrofil szubsztitúció az oxigén centrumon I I I I I I I I I I I I I I I
48 Sztereokémiai inverzió (elimináció báziskatalízissel): A B 6 -viatmin egyik származéka, a piridoxál-foszfát (PLP) enzimhez kötött formában egy sor reakciótípus katalizálásában vesz részt: - transzaminálás (amino- és oxocsoportok kicserélése) - dekarboxilezés - sztereokémiai inverzió (konfiguráció megváltoztatása) - elimináció példa: Tekintsük a sztereokémiai inverziót pl. baktérium-sejtfalhoz (R)-alanin szükséges, amely a természetben elterjedtebb (S)-alaninból a következő módon szintetizálódik: Az aktív forma a piridoxál-5-foszfát és a megfelelő enzim alkotta imin: (S)-(+)-alanin (L-alanin) Enzim- 2
49 Az alapvegyület és a foszforsav-észter szerkezete: protontranszfer 5 3-hidroxi-5-hidroximetil- 2-metilpiridin-4-karbaldehid piridoxál piridoxál-5-foszfát
50 Az aktív forma kialakulása egy Ad + E reakció, amelyet egy intramolekuláris protonálódás egészít ki: P 3 Enzim- 2 Ad + E - 2 P Enzim 3 Ad + E R R 2 2 R R R 2
51 A megfelelő aminosavszármazék (R-alanin-piridoxál-foszfát) előállítása: (aciltranszfer lépés) P Enzim (S)-(+)-alanin (L-alanin) 3 2 P 3 3 Enzim- 2 3
52 A sztereokémiai inverzió: Az enzimkatalízis nélkül végbemenő (bázis katalizált) racemizáció mechanizmusa igen hasonló:
53 ogyan működik, amíg hat a penicillin (aciltranszfer): A penicillin és fontosabb típusai: ogyan inaktiválja a penicillin a bakteriális sejtfal egyik enzimét (E): R Aktív enzim + S 3 3 β-laktám gyűrű (térbeli feszültség miatt aktív amid) R Inaktív enzim S 3 3
54 kérdés: hogyan lesz penicillin-rezisztens a baktérium? A rezisztens törzsekben megjelenik a penicillináz amely elhidrolozálja a reaktív β-laktámgyűrűt: (az így keletkező aminokarbonsav már nem tud acilezni) R S R penicillináz ( -laktamáz) S 3 3
55 Biológiai környezetvédelem (aromás nukleofil szubsztitúció): Korábban számos polihalogénezett bifenilszármazékot használtunk (pl. polimerekben, elektromos készülékekben). gond: toxikusak, valamint beépültek a táplálékláncba. (1979 óta betiltva) megfigyelés: az egyik bomlástermék a 4-klórbenzoesav, amelyet egyes baktériumok dehalogéneznek és így méregtelenítenek: 3,4'-diklórbifenil SoA SoA SoA leírás: a megfelelő enzim egy karboxilátcsoportja a 4-klórbenzoesav-tioészter származékot S (Ar) reakcióba viszi. A Meisenheimer-komplexen át képződő aromás 4-hidroxibenzoesav-származék acilenzim-komplexe báziskatalizálta észterhidrolízist (Ad + E) szenved. l Enzim S Ar l Enzim Ad + E Enzim B SoA SoA Enzim B Enzim B
56 memo: a koenzim (spec. kofaktor) olyan segéd-molekula, amely nincs permanensen az enzimhez kötve. adenozin ys (dekarboxilezett) pantoténsa v 56
57 S 2 aromás SoA SoA SoA SoA l Enz l Enz l Enz Enz l Ad + E SoA SoA SoA Ad E Enz B Enz B Enz B
58 Milyen kémiaimechanizmussal világít a szentjánosbogár? Avagy a luciferin szubsztrát átalakulása Lucifer lux + fero fénythozó A reakció folyamatának biokémiai áttekintése MgATP Enzim + Luc- I. Aktiválási lépés: Az enzim köti a luciferint, egy ATP felhasználásával pedig aktiválja a karboxilcsoporton keresztül a szubsztrátot. PP i Enzim:Luc--AMP II. xidáció: Az oxidáció α-peroxilaktámon keresztül megy végbe, mely az enzimhez kötött gerjesztett terméket eredményez. 2 AMP 2 2 Enzim:Luc= * III. Kisugárzás (relaxáció): Az aktivált komplex a reakció végső lépéseként fénykibocsájtás révén relaxál, létrehozva az alapállapotú végterméket. Enzim + Luc= h
59 A luciferin gyűjtőnév a luciferináz enzim szubsztrátjait jelenti: oxigén jelenlétében az enzim biolumineszcenciát eredményez. ypridina Luciferin 2 Latia Luciferin Renilla Luciferin hromophore of Aequorin
60 R-luciferin Az aktiválás mechanizmusa 2-(6-ydroxy-benzothiazol-2-yl)-4,5-dihydro-thiazole-4-carb oxylic acid Az R forma a természetben elõforduló, de az S forma is mutatja a kemolumineszcencia jelenségét S S bogárból izoláltak néhány mg luciferint P P Mg 2+ P ATP 2 S R-luciferin S P AMP + P P pirofoszfát
61 Az oxidációs lépés - S S - AMP 18 Aktivált R-luciferin S 2 (bázikus közeg) - 18 nukleofil addició S S S AMP lazitott hidrogén AMP Et polimerizáció polimer peroxid (szilárd, robban) n - S - S 18 AMP - S elimináció és dekarboxileződés S AMP
62 A relaxáció az oxidált termék gerjesztett elektronállapota felelős a fénykibocsájtásért A pontos szint a fehérje módosítja -terminális domén: kék (A β-réteg), lila (B β-réteg), zöld (β-hordó). -terminális domén: sárga
63 Az elsődleges szerkezet Invariáns szekvencia (piros), 50%-nál nagyobb homológia: rózsaszín (Az összehasonlítás alapját 38 rokon fehérje szekvenciája képezi.)
64 A másodlagos szerkezet
65 A luciferáz aktív centruma Piros: invariábilis aminosavak (Lys206, Glu344, Asp422) Kék: variábilis aminosavak
66 A luciferin kötődése az árokba
67 ovokain totálszintézise: 3 8 (kokainhoz hasonló helyi érzéstelenítőszer) ox. 3 kokain 3-benzoiloxi-8-metil-8-aza- biciklo[3.2.1]oktán- 2-karbonsav-metil-észter (Bruckner III 913) Ad +E Pl 5 / Sl l l Ad +E - l l S Et l 2 Et 2 red Et 2 l
68 Savklorid előállítása (S [szén vagy kéncentrumon], elimináció ) Ad +E l S l Ad l S E l l S l kokain l l S Ad l Sl E S l l novokain (S 2 + l)
69 Az adrenalin szintézise (Bruckner 543) (meszkalinhoz hasonló molekula) pirokatechin + l 2 l + S E (aromás) Friedel-rafts 2 l (nem jól megy) Pl 3 All 3 2 l S /kat. * 2 3 Me Me adrenalin (neurotranszmitter) hallucinogén (kábítószer) meszkalin (Bruckner II/1 922) Anhalonium lewinni növénybõl Me
70 A klóracilezés részletei (Ad + E), S E (oxigén centrumon), S E (aromás): 2 l 2 l 2 l 2 2 l -acilszármazék Fries- átrendeződés (Pl 3 vagy All 3 ) 2 l All 3 2 l All 3 All 3 2 l elektrofil acilium kation 2 l All 3 + l a klóracetil-csoport vándorlásának végterméke memo: analóg vegyületek * noradrenalin hidroxi-fenilalanin
71 A szacharin totálszintézise: 3 3 S 2 l 3 (Bruckner II/1 851) édes ízű molekula (Remsen és Fahlberg 1879) toluol S E S 2 l o-toluolszulfonil-klorid (és tozil-klorid) képzõdik S 3 S 2 2 o-toluolszulfonamid S KMn 4 ox. S 2 2 S - 2 Ad + E laktám képzõdik a Szacharin (5-ször édesebb mint a szacharóz) memo: a szacharóz (nádcukor, répacukor) 2 -D-glükozil- -D-fruktozid 2
72 Függelék néhány fontosabb vitamin: all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin, ) tiaminpirofoszfát prekurzora l 3 -difoszfát: kokarboxiláz koenzim 3 3 l S 2 2
73 B 2 -vitamin: riboflavin (vízoldható vitamin) FAD prekurzora B 6 -vitamin: piridoxin (vízoldható vitamin) piridoxalfoszfát prekurzora hidroxi-4,5-bis(hidroximetil)- 2-metil-piridinium kation
74 B 12 -vitamin: cianokobalamin (vízoldható vitamin) Bruckner III/2 867, Solom.1087 X-ray: Dorothy rowfoot odgkin ( ) [1964 obel-díj] A o B totál szintézis (11 évig tartott): Robert Burns Woodward ( , [1965 obel-díj]) D P G 2 F E 3 3
75 -vitamin: L-aszkorbinsav (vízoldható vitamin) avitaminózis: skorbut Bruckner I/ D-gulonsav 2 L-gulonsav 2 L-aszkorbinsav 2 2 Szent-Györgyi Albert ( ) [1937 obel-díj]
76 D 3 -vitamin: kalcitrol (zsíroldható vitamin) D 3 -vitamin aktív formája kalcitrol D 3 -vitamin kolekalciferol 3 D 3 -provitamin UV-fény dehidrokoleszterin
77 D 2 -vitamin: ergokalciferol (zsíroldható vitamin) avitaminózis: angolkór D 2 -vitamin ergokalciferol 3 ergoszterin E-vitamin: tokoferol (zsíroldható vitamin) avitaminózis: terhesség megszakadása 3 K-vitamin: fillokinon (zsíroldható vitamin) avitaminózis: vérzékenység
78
79
80
81 Bioenergetika Elektromágneses energia forrása lehet hőerőgép és belsőégésű motor, amelyekben a hőenergia égésből, azaz kémiai átalakulásból származik, ami az atomok és molekulák elektronszerkezetéhez köthető átalakulás, azaz elektromágneses folyamat. Az élőlények számára is kémiai folyamatok, azaz az elektromágneses kölcsönhatás biztosítja az energiatárolást és energiafelhasználást, tehát a biológiai energiák is elektromágneses eredetűek. Memo: Az energiaformákat vissza lehet vezetni a fizika négy alapvető kölcsönhatásának valamelyikére. A négy alapvető kölcsönhatás a gravitációs, az elektromágneses, a gyenge és az erős kölcsönhatás. 81
82 ATP: adenozin -5 - trifoszfát foszforsavanhidrid foszfátészter DG~ 30.5 kj DG~ mol kj mol -1 ATP + 2 ADP + P i ΔG = 30.5 kj/mol ( 7.3 kcal/mol) ATP + 2 AMP + PP i ΔG = 45.6 kj/mol ( 10.9 kcal/mol) 82
83 ATP és GTP mint energiahordozók: elem / akkumulátor (újrafeltölthető!) (ATP) felhasználás: direkt módon: kapcsolt reakció A sejtben igényelt anyagok szintézisében az endoterm ill. endergonikus reakciókhoz a kapcsolódó ATP/GTP hidrolízis adja a megfelelő hajtóerőt a reakció lefutásához. pl.a felhasználásra: - transzláció (fehérjeszintézis) - kreatin (energiaraktár az izomban) - (ATP) feltöltés: direkt módon: szubsztrát szintű foszforiláció: a metabolizmus (ételek, raktározott zsírsavak, egyéb anyagok lebontása) során az exoterm ill. exergonikus reakciókban történő ADP/GDP foszforilációja. indirekt módon: oxidatív foszforiláció a metabolizmus során redox-reakciókban redukált koenzimek keletkeznek: AD + és FAD 2 Ezek a redukált koenzimek elektrontranszporttal egybekötött, szabályozott regenerálása (oxidációja) során keletkezik ATP. 83
84 Atkins & de Paula 99 kérdés: mennyi glükóz elégetése teszi lehetővé egy 30 g össztömegű madár számára, hogy 10 m magasra repüljön? tapasztalat: 1 mol szilárd glükóz 2 gázzá és folyékony vízzé való oxidációja 25 -on ~ 2828 kj (2,8 E6 J) szabadentalpia (DG) felszabadulást eredményez. válasz: az elvégezendő munka nagysága mgh= (30*10-3 kg)* (9,81*ms -2 )* (10 m) = 2,943 kg m 2 s -2 = 2,943 J mivel 1 mol glükóz DG ~ 2, J munka végzéséhez elegendő, 2,943 J munka elvégzéséhez 2,943 / 2, mol glükózra van szükség, ami 1,04 μmol cukrot jelent. Mivel a glükóz M W -je ~180 g/mol ezért ez hozzávetőlegesen (180 g/mol * 1,04*10-6 mol) = 0,19 mg kérdés: a koncentráló emberi agy ~25 J energiát igényel másodpercenként. Mennyi cukor (glükóz) elégetése szükséges ehhez óránként? tapasztalat: 1 mol glükóz oxidációja 25 -on ~ 2828 kj szabadentalpia (DG) felszabadulását eredményezi. válasz: az elvégezendő munka nagysága óránként = (25 Js -1 )* (3,6*10 3 s) = J = 90 kj mivel 1 mol glükóz DG ~ 2, kj munka végzéséhez elegendő, 90 kj munka elvégzéséhez 90 / 2, mol glükózra van szükség, ami 32 mmol glükózt jelent. Mivel a glükóz M W -je ~180g mol -1 ezért ez hozzávetőlegesen (180 * 32*10-3 g ) = 5,7 g/óra Tehát az emberi agy naponta ~ 24 * 5,7g ~140g glükózt igényel. 84
85 A napi g glükóz többsége ATP-vé alakul és így hasznosul a sejtekben. Aerob körülmények között 1 mol glükóz mintegy 38 mol ATP eredményez. mivel M w (ATP)/ M w (glükóz) 507/180 = 2,82 ezért 2,82 * 38 * 160g 17,1 kg ATP Ténylegesen egy 70 kg-os ember napi ATP fogyasztása ~ 145 kg (mivel nem csak szénhidrátot, de zsírt és fehérjét is fogyasztunk!) Ám a szervezetben egyszerre kb. 51 g össz ATP áll rendelkezésre, ami a teljes szükséglet (51 g /1, g) kb. 0,035% -a. Ez az tartalékolt ATP mennyiség tehát kb. (24* 3600s) * (3, ) ~ 30 s-ra elegendő mindössze! Tehát az ember ATP szükséglete ~ 100g / perc (aktív mozgás esetén 500g /perc) ADP/ATP ciklus (a foszforiltranszfer) A kémiai reakció: ATP 4 (aq) + 2 ADP 2 (aq) +P 4 2 (aq) DG~ 30 kj mol -1 A biokémiai rész ciklus: ½ 2 2 ADP 2 + P 4 2 ATP 4 DG 85
86 A teljes biokémiai ciklus: égetés DG + DG AD + + AD + FAD 2 FAD AD + (ikotinamid-adenin-dinukleotid) DG elektronátvitel ½ 2 + DG 2 ADP 2 + P 4 2 ATP 4 foszforilátvitel DG memo: a félkövér résztvevők (, AD+ +, FAD 2, ATP) azok a nagyobb energiájú molekulák a megfelelő párokban. memo: A negatív DG-s reakciók hajtják a velük összekapcsolt ( csatolt ) pozitív DG-s (piros nyíl) reakciókat. Tűz, ami melegíti a levest csatolt rendszert képeznek a levegőn keresztül. FAD (Flavin-adenin-dinukleotid) 86
87 éhány fontosabb foszfátvegyület foszfátcsoport(jai) hidrolízisének DG- értékei 37 o -on: memo: foszfoenol-piruvát DG~ 62 kj mol -1 ATP ADP DG~ 31 kj mol -1 ADP AMP DG~ 28 kj mol -1 AMP DG~ 14 kj mol -1 glükóz-1-foszfát DG~ 21 kj mol -1 glükóz-6-foszfát DG~ 14 kj mol -1 fruktóz-6-foszfát DG~ 16 kj mol -1 kérdés: mit takar az ATP DG~ 31 kj mol -1? A hidrolízis exergonikus DG< 0 és éppen 31 kj mol -1 energiát ad más csatolt, esetleg endergonikus reakciók lefolytatásához. Ezért hívjuk a megfelelő savanhidrid kötést nagyenergiájú kötésnek. memo: vegyük észre hogy az ATP középen helyezkedik el, ezért lehet foszfát donor és akceptor is. 87
88 ATP 4 (aq) + 2 ADP 2 (aq) +P 4 2 (aq) tény: az ATP DG~ 31 kj mol -1 valamint a D~ 20 kj mol -1 és DS~ +34 JK -1 mol -1 memo: mivel DG = D TDS TDS~ 310 K *34 JK -1 mol -1 ~ +11 kj mol -1 ) memo: az 1 mol víz a hidrát burok része, mivel a reakció nem vákuumban megy. Innen a formális mólszám növekedés (1-ből 2-re), emiatt van az entrópia növekedés, avagy a komplexitás csökkenése is, ami egy további kedvező komponens. A DG értéke ( 31 kj mol -1 ) ezért is ilyen kedvező. Az ATP hidrolízise felhasználható olyan csatolt endergonikus reakciókhoz, amelyek DG-je nem nagyobb mint +31 kj mol -1. pl. a peptidkötés szintézise erősen endergonikus: DG~ +17 kj mol -1 memo: az 1 mol víz a hidrát burok része, mivel a reakció nem vákuumban megy. Innen a nagy entrópia csökkenés (2-ből 1-re), a komplexitás növekedés. DG ezért is ilyen kedvezőtlen. memo: nem csak az entalpiaváltozás, de a szint entrópia csökkenése (komplexitás növekedése) is jelentős! kérdés: hogy mehet végbe a reakció 37 o -on? válasz: ATP csatolt a reakció. memo: a csatolt rendszer értelmében a két reakció össze van kapcsolva! (a a két reakció elkülönítve (2 edényben) megy végbe, vagy ha csak úgy összeöntjük a reagenseket, akkor a folyamat nem fog végbemenni.) 88
89 megfigyelés: Itt nem részletezett okok miatt 1 peptidkötés kialakításához 3 ATP szükséges. kérdés: hány gramm glükóz kell 1 mol mioglobin bioszintéziséhez, ha az 153 aminosavból épül fel? válasz: 153*3 = 459 ATP szükséges. 1 mol glükóz 38 ATP eredményez, tehát 459/38~ 12 mol glükóz szükséges. tehát: (12*180 g)~ 2,2 kg cukor kell 1 mol (16,7 kda) fehérje szintéziséhez (~16,7 kg) 89
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
Néhány fontosabb vitamin
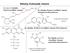 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
N-metilezés (példa egy S N
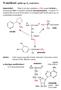 -metilezés (példa egy S reakcióra): tapasztalat: Állati és növényi sejtekben a - 3 csoport átvihető a metioninról (Met) a megfelelő molekula nitrogénatomjára. A reakció 14 tartalmú Met-tel nyomon követhető:
-metilezés (példa egy S reakcióra): tapasztalat: Állati és növényi sejtekben a - 3 csoport átvihető a metioninról (Met) a megfelelő molekula nitrogénatomjára. A reakció 14 tartalmú Met-tel nyomon követhető:
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
A fehérjék harmadlagos vagy térszerkezete. Még a globuláris fehérjék térszerkezete is sokféle lehet.
 A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A fehérjék harmadlagos vagy térszerkezete Még a globuláris fehérjék térszerkezete is sokféle lehet. A ribonukleáz redukciója és denaturálódása Chrisian B. Anfinsen A ribonukleáz renaturálódása 1972 obel-díj
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Az enzimek katalitikus aktivitású fehérjék. Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás.
 Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
Enzimek Az enzimek katalitikus aktivitású fehérjék Jellemzőik: bonyolult szerkezet, nagy molekulatömeg, kolloidális sajátságok, alakváltozás, polaritás. Az enzim lehet: csak fehérje: Ribonukleáz A, lizozim,
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R H + H 2 Q R Q + H 2 H R H + H 2 Q R + H 3 Q sav-bázis reakció már nem nukleofil Amidkötés kialakítása
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek
 Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
Több oxigéntartalmú funkciós csoportot tartalmazó vegyületek Hidroxikarbonsavak α-hidroxi karbonsavak -Glikolsav (kézkrémek) - Tejsav (tejtermékek, izomláz, fogszuvasodás) - Citromsav (citrusfélékben,
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
KARBONSAV-SZÁRMAZÉKOK
 KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
KABNSAV-SZÁMAZÉKK Karbonsavszármazékok Karbonsavak H X Karbonsavszármazékok X Halogén Savhalogenid l Alkoxi Észter ' Amino Amid N '' ' Karboxilát Anhidrid Karbonsavhalogenidek Tulajdonságok: - színtelen,
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Peptidek (savamidok) szintézise. feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik.
 Peptidek (savamidok) szintézise feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik. 1 avamidok (peptidek) szintézise és hidrolízise megfigyelés:
Peptidek (savamidok) szintézise feladat: a szintéziskor elvben csak egy mól vizet kell elvonni peptidkötésenként, ám az ördög a részletekben rejlik. 1 avamidok (peptidek) szintézise és hidrolízise megfigyelés:
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
O S O. a konfiguráció nem változik O C CH 3 O
 () ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
() ()-butanol [α] D = a konfiguráció nem változik () 6 4 ()--butil-tozilát [α] D = 1 a konfiguráció nem változik inverzió Na () () ()--butil-acetát [α] D = 7 ()--butil-acetát [α] D = - 7 1. Feladat: Milyen
9. Szilárdfázisú szintézisek. oligopeptidek, oligonukleotidok
 9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
9. Szilárdfázisú szintézisek oligopeptidek, oligonukleotidok Peptidszintézis Amidkötés kialakítása R O OH + H 2 N Q R O Q N + H 2 O H R O OH + H 2 N Q R O O + H 3 N Q sav-bázis reakció már nem nukleofil
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
Aromás vegyületek II. 4. előadás
 Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
P O O O. OAc A O. OAc
 6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
6. Előadás ligonukleotidok szintézise, koenzimek, vitaminok ligonukleotidok szintézise Elv: ( ) 1. Kondenzáció ( ) 5 - + (3 ) 2. Vízmentes közeg 3. Védőcsoportok Módszerek 1. Karbodiimid módszer, oldatban
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
Bevezetés. Szénvegyületek kémiája Organogén elemek (C, H, O, N) Életerő (vis vitalis)
 Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
HALOGÉNEZETT SZÉNHIDROGÉNEK
 ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
H H 2. ábra: A diazometán kötésszerkezete σ-kötések: fekete; π z -kötés: kék, π y -kötés: piros sp-hibrid magányos elektronpár: rózsaszín
 3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
3. DIAZ- ÉS DIAZÓIUMSPRTT TARTALMAZÓ VEGYÜLETEK 3.1. A diazometán A diazometán ( 2 2 ) egy erősen mérgező (rákkeltő), robbanékony gázhalmazállapotú anyag. 1. ábra: A diazometán határszerkezetei A diazometán
1. változat. 4. Jelöld meg azt az oxidot, melynek megfelelője a vas(iii)-hidroxid! A FeO; Б Fe 2 O 3 ; В OF 2 ; Г Fe 3 O 4.
 1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
1. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
Transzláció. Szintetikus folyamatok Energiájának 90%-a
 Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Transzláció Transzláció Fehérje bioszintézis a genetikai információ kifejeződése Szükséges: mrns: trns: ~40 Riboszóma: 4 rrns + ~ 70 protein 20 Aminosav aktiváló enzim ~12 egyéb enzim Szintetikus folyamatok
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ
 1 oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ I A VÍZ - A víz molekulája V-alakú, kötésszöge 109,5 fok, poláris kovalens kötések; - a jég molekularácsos, tetraéderes elrendeződés,
1 oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 1995 JAVÍTÁSI ÚTMUTATÓ I A VÍZ - A víz molekulája V-alakú, kötésszöge 109,5 fok, poláris kovalens kötések; - a jég molekularácsos, tetraéderes elrendeződés,
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ AMINOSAVAK ANYAGCSERÉJE 1. kulcsszó cím: Az aminosavak szerepe a szervezetben A szénhidrátokkal és a lipidekkel ellentétben szervezetünkben nincsenek aminosavakból
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben?
 Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI AZ AMINOSAVAK ÉS FEHÉRJÉK 1. kulcsszó cím: Aminosavak Egy átlagos emberben 10-12 kg fehérje van, mely elsősorban a vázizomban található.
Mire költi a szervezet energiáját?
 Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások
 Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Oktatási Hivatal Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia I. kategória 2. forduló Megoldások I. FELADATSOR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
Részletes tematika: I. Félév: 1. Hét (4 óra): 2. hét (4 óra): 3. hét (4 óra): 4. hét (4 óra):
 Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Részletes tematika: I. Félév: 1. Hét (4 óra): Szerves Vegyületek Szerkezete. Kötéselmélet Lewis kötéselmélet; atompálya, molekulapálya; molekulapálya elmélet; átlapolódás, orbitálok hibridizációja; molekulák
Vitaminok meghatározása és csoportosítása
 Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
Vitaminok Vitaminok meghatározása és csoportosítása A vitaminok a(z emberi) szervezet számára nélkülözhetetlen, kis molekulatömegű, változatos összetételű szerves vegyületek, melyeket a táplálékkal kell
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
AMINOK. Aminok rendűsége és típusai. Levezetés. Elnevezés. Alkaloidok (fiziológiailag aktív vegyületek) A. k a. primer RNH 2. szekunder R 2 NH NH 3
 Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
IX. Szénhidrátok - (Polihidroxi-aldehidek és ketonok)
 IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
IX Szénhidrátok - (Polihidroxi-aldehidek és ketonok) A szénhidrátok polihidroxi-aldehidek, polihidroxi-ketonok vagy olyan vegyületek, amelyek hidrolízisekor az előbbi vegyületek keletkeznek Növényi és
MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 3. Alifás szén-szén egyszeres kötések kialakítása báziskatalizált reakciókban Kovács Lajos 1 C-H savak Savas hidrogént tartalmazó szerves vegyületek H H 2 C α C -H H 2
Szerves kémiai szintézismódszerek 3. Alifás szén-szén egyszeres kötések kialakítása báziskatalizált reakciókban Kovács Lajos 1 C-H savak Savas hidrogént tartalmazó szerves vegyületek H H 2 C α C -H H 2
Országos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások
 ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
ktatási Hivatal rszágos Középiskolai Tanulmányi Verseny 2010/2011. tanév Kémia II. kategória 2. forduló Megoldások I. FELADATSR 1. C 6. C 11. E 16. C 2. D 7. B 12. E 17. C 3. B 8. C 13. D 18. C 4. D 9.
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások)
 3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
3. Sejtalkotó molekulák III. Fehérjék, enzimműködés, fehérjeszintézis (transzkripció, transzláció, poszt szintetikus módosítások) 3.1 Fehérjék, enzimek A genetikai információ egyik fő manifesztálódása
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A SZÉNHIDRÁTOK 1. kulcsszó cím: SZÉNHIDRÁTOK A szénhidrátok általános képlete (CH 2 O) n. A szénhidrátokat két nagy csoportra oszthatjuk:
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll.
 KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
KÉMIA II. (BMEVESZAKM1) A tárgy heti 2 2 óra előadásból és heti 1 óra laboratóriumi (kummulált) gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele, hogy a félévközben
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
Laboratóriumi technikus laboratóriumi technikus Drog és toxikológiai
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
