2018. MÁRCIUS Családtervezés és hemofília
|
|
|
- Krisztina Balogné
- 6 évvel ezelőtt
- Látták:
Átírás
1 MÁRCIUS Családtervezés és hemofília
2 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Tartalomjegyzék Bevezető...3 Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén...5 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Marci mese Hemofíliás gyermek a családban Impresszum Magyar Hemofília Egyesület: Alapítva 1990-ben, közhasznú jogállású 1998-tól. A Hemofília Világszövetség (WFH) és az Európai Hemofília Konzorcium (EHC) magyarországi tagszervezete és hivatalos képviselője, az EURORDIS és a RIROSZ tagja. Az Egyesület elnöksége: Keszthelyi Zoltán elnök Csaba Attila elnökhelyettes Gömbös Erzsébet vezetőségi tag Hadházy Tímea vezetőségi tag Nagy Péter vezetőségi tag A Hemofília magazin szerkesztősége: Virágh Via főszerkesztő A kiadványban szereplő fényképeket és ábrákat a szerzők bocsátották rendelkezésünkre. Az Egyesület és a szerkesztőség címe: 1088 Budapest, Rákóczi út 29., II/7. Telefon: Honlap: mhe@mhe.hu Adószám: Bankszámlaszám: OTP Az újságot terjeszti és a felelős kiadó: Magyar Hemofília Egyesület, Keszthelyi Zoltán elnök 2
3 Bevezető Kiadványaink legfőbb célja, hogy a hemofília betegséggel közvetlenül vagy közvetetten érintettek, valamint családtagjaik első kézből jussanak hozzá minden olyan információhoz, amely alapvető fontosságú lehet bizonyos élethelyzetekben: ilyen a gyermekvállalás, családtervezés. Az Egyesület fennállása során folyamatosan épít, és tart fenn kapcsolatokat a különböző egészségügyi szakintézményekkel, így a hemofília kezelőközpontokkal, az Országos Vérellátó Szolgálattal, az Istenhegyi Géndiagnosztikai, Nőgyógyászati és Családtervezési Centrummal, melyeknek munkatársai segítségével jöhetett létre ez a tájékoztató füzet, a legújabb kötete az Egyesület ismeretterjesztő sorozatának. Bár a vérzékenység, mint örökletes betegség, hosszú évszázadok óta ismert, az öröklődés folyamatát korábban mégsem lehetett befolyásolni. Ma már azonban több út is kínálkozik a döntés előtt álló családoknak: Elfogadják a betegség lehetőségét születendő gyermeküknél. Egy hemofíliás gyerek nevelésének sajátosságaival foglalkozik dr. Kardos Mária, a mohácsi kórház osztályvezető főorvosának cikke, a hemofília gondozó szakorvos szemszögéből. Élnek azzal a lehetőséggel, hogy a normál módon létrejött terhesség után, hemofíliás magzat esetében megszakíttatják a terhességet. A magzatról néhány hónapos korban hasfalon keresztüli méhlepény-mintavétel alapján megállapítható, hogy fiú-e, és szerencsés körülmények esetén kisebb-nagyobb valószínűséggel az is, hogy hemofíliás-e. A megszületendő lány magzatok hemofilia hordozósága nem zárható ki ezzel a módszerrel. Mind a vizsgálatot, mind a terhesség megszakítást a társadalombiztosítás támogatja. Tervezett lombikbébi programban vesznek részt, melynek lehetőségeit és részletes folyamatát Varga Tünde, az Istenhegyi Géndiagnosztikai Centrumának és Bors András, az Országos Vérellátó Szolgálat, Molekuláris Diagnosztikai Laboratóriumának szempontjából írja le. Keszthelyi Bori cikke egy érintett anyuka gyakorlati tapasztalatait foglalja össze. Társadalombiztosítás által csak részben támogatott eljárás. A világ, de Európa országaiban is, a magzatok genetikai vizsgálatát eltérő módon kezelik, bizonyos országokban jogi akadályok, más országokban az egészségügyi ellátás hiányosságai miatt nincs lehetőség a születés előtti vizsgálatokra. Magyarországon 3
4 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS néhány éve már a jogi szabályozás és az egészségügyi intézmények felkészültsége is lehetővé teszi, hogy amennyiben a szülők úgy döntenek hemofília hordozó nőknek se kelljen hemofíliás gyermeket szülniük. A lombikbébi program teszi lehetővé, hogy az úgynevezett előembriók (megtermékenyített és osztódásnak indult petesejt 14 napos korig) vizsgálhatóak legyenek már néhány napos korukban. Első lépésben a leendő anyától és apától levett ivarsejteket mesterséges körülmények között megtermékenyítik. Azután az előembriókat néhány napos korukban megvizsgálják, hogy hemofíliás betegek, vagy hordozóak-e. Végül csak a hemofíliával nem érintett előembriókból ültetnek vissza egyet vagy többet, hogy azután egy normál terhesség után megszülethessen a hemofília mentes kisbaba. Az előembriók vizsgálata két bonyolultságában, időtartamában és árában különböző diagnosztikai eljárással történhet: Nemi szelekció. Ebben az esetben csak az előembrió nemét vizsgálják meg és csak lány előembriót ültetnek vissza, függetlenül attól, hogy hemofília hordozó-e. Hibás gén kimutatása. Ebben az esetben minden előembrióról megállapítják, hogy tartalmazza-e a hibás hemofíliáért felelős gént, tehát kiderül az is, hogy egy lány előembrió hemofília hordozó-e, és csak a hemofília mentes előembriókat ültetik vissza. Ez a vizsgálat jelentősen bonyolultabb és drágább, több hónapos előkészítést igényel, hogy az előembrióból kivett egyetlen sejtből eldönthető legyen a beteg gén jelenléte. A lehetséges eljárások fenti rövid összefoglalója mutatja, hogy a gyermeket tervező párok komoly nehézségeket és terheket vállalnak az egészséges utódok érdekében. Akik a lombikbébi programot választják, nyilván a családi előtörténetük miatt vállalják a sokszor kemény küzdelmet, hogy gyermeküknek már ne kelljen ezzel a betegséggel megbirkóznia. A gyermekvállalás egészséges emberek számára is nehéz és nagy felelősséggel járó döntés. Amennyiben a családban már felbukkant a hemofília, ez a döntés még nehezebbé válik, hiszen szerencsére ma már több út is kínálkozik a leendő szülők számára. A döntés meghozatalához segítséget tudnak nyújtani külső támogatók, de a végső döntés joga és felelőssége minden esetben a gyermeket vállaló családé. A maga eszközeivel egyesületünk is támogatni szeretné a gyermeket tervező családokat, ezért 2017-ben programot indítottunk, amelynek keretében anyagi segítséget is tudunk nyújtani a rászoruló családoknak. Támogatásunk másik megjelenési formája ez a kiadvány, amelyet jó szívvel ajánlunk. 4
5 Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén 2000-ben szereztem biológusi diplomát, majd 2008-ban PhD fokozatot az ELTE-n. A laboratóriumban, ahol 17 éve dolgozom, 1995 óta foglalkozunk hemofíliás családok molekuláris genetikai vizsgálataival. Kezdetben az Országos Hematológia és Immunológiai Intézetben, majd intézet átalakítások következtében az OGYK-ban, illetve az OVSz-ben, 2018 óta pedig a Délpesti Centrumkórház Országos Hematológiai és Infektológiai Intézetben. dr. Bors András biológus Személy szerint azt szeretném, hogy a betegek kezelése és tájékoztatása minél hamarabb olyan szintet érjen el, hogy egyértelművé váljon: a hemofíliások is teljes életet élhetnek, ne legyen szükség a prenatális vizsgálatok elvégzésére, hanem minden családban bátran vállalható legyen minden kisfiú megszületése. dr. Bors András, dr. Andrikovics Hajnalka Országos Vérellátó Szolgálat, Molekuláris Diagnosztikai Laboratórium Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén Öröklődő betegségek Az emberi élet során sokféle betegség kialakulhat. Ezek lehetnek súlyosak, vagy csak kellemetlenek, tarthatnak egy-két napig, vagy akár élethosszig, lehetnek fertőzőek, vagy személyre szabottak. A betegségek között előfordulnak olyanok, amelyek örökletesek, vagyis az illetőnek a betegség típusa és a genetika öröklődési szabályai szerint valamelyik leszármazottja ugyanolyan betegségben fog szenvedni, mint ő maga. Ezek a betegségek jelenleg jó esetben csak kezelhetők, de nem gyógyíthatók. Az ilyen típusú betegségek hátterében az örökítő anyag (dezoxiribonukleinsav DNS) hibája áll. Ez a molekula minden sejtünkben megtalálható, a szervezetet felépítő fehérjék elkészítéséhez szolgáltatja az információt a sejtek számára. Az egy fehérje felépítésre vonatkozó információt génnek nevezzük. Minden sejtben minden fehérjére vonatkozó információ megvan, még akkor is, ha a sejt akár egész életében soha nem készíti azt el. Ha a gén hibás, a felhasználásával elkészített összes fehérje is hibás lesz, ezen alapul az adott betegség (szakszóval a megjelenő fenotípus). 5
6 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS A DNS a sejt életének bizonyos szakaszaiban összecsomagolva, jól látható kromoszómák formájában van jelen. A testünket felépítő sejtekben minden kromoszómából két példány található, méretük és alakjuk alapján huszonhárom párt lehet elkülöníteni. Kivételt az ivarsejtek, és az úgynevezett ivari kromoszómák jelentenek. Ugyanis míg a nőknél a 23. pár kromoszóma ténylegesen két hasonló, úgynevezett X-kromoszóma, addig a férfiak esetében egy X, és egy attól lényegesen különböző Y kromoszóma található minden sejtben. Az ivarsejtekben pedig minden kromoszómapárból csak egy található meg, értelemszerűen a férfiak hímivarsejtjeiben a 23. párból vagy egy X, vagy egy Y. Ha az ivarsejtekben, a DNS-ben valamilyen hiba (mutáció) van jelen, akkor ez a mutáció a megszülető gyermek minden testi sejtjében, és ivarsejtjeinek felében is megtalálható lesz, és kialakul(hat) az élete során a mutációnak megfelelő betegség. Fontos megemlíteni, hogy egy beteg ivarsejtjeit nem lehet egyesével megvizsgálni, hogy hibás, vagy jó kromoszómát tartalmaznak-e. Viszont azt, hogy egy betegnél milyen hiba okozta a betegséget, elvileg bármely testi sejtének vizsgálatával meg lehet állapítani. Legegyszerűbb módszer a vérben keringő fehérvérsejtek DNS-ének vizsgálata. Miért fontos a genetikai vizsgálat? A genetikai vizsgálat egyértelművé teheti a kezelőorvos számára, hogy a beteg pontosan milyen betegségben szenved, illetve hogy esetében milyen kockázati tényezőkkel kell számolni. Ha a vizsgálat még a tünetek megjelenése előtt megtörténik, egyes betegségeknél megelőző kezeléssel elkerülhető a betegség kialakulása. Segítségével azonosíthatók a tünetmentes, de a mutációt hordozó, és azt tovább örökítő családtagok. Sok esetben egy gyermekről már a megszületése előtt kideríthető, hogy beteg lesz-e, (prenatális diagnosztika) illetve egyes betegségek esetén a mesterséges megtermékenyítés folyamatának egy speciális időszakában az embriót a beültetés előtt is meg lehet vizsgálni (preimplantációs diagnosztika). E füzet témája a hemofília A és hemofília B betegségek esetében elérhető molekuláris genetikai diagnosztika. Hemofília: Ha a véralvadás a normálisnál hosszabb időt vesz igénybe, vérzékenységről beszélünk. A vérzékenység hátterében a véralvadás fehérjéi (véralvadási faktorok), a vérlemezkék, és az érfal szerzett, illetve örökletes betegségei egyaránt állhatnak. A VIII. véralvadási faktor hiányos működése miatt alakul ki a hemofília A, 6
7 Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén a IX. véralvadási faktor hiányos működése következtében pedig a hemofília B betegség. A hiányos termelődést az adott fehérje felépítését meghatározó gén (hemofília A esetén a VIII. alvadási faktorért felelős F8 gén, hemofília B esetén a IX. alvadási faktorért felelős F9 gén) mutációi okozzák. Mindkét gén az X kromoszómán található. Magyarországon több mint 2700 vérzékeny beteg él, ebből kb. 800 HA, kb. 200 HB, kb von Willebrand betegségben, további kb. 400 ember egyéb vérzési rendellenességben szenved. Ebben a tájékoztatóban az öröklődő vérzékenységek közül az A és B típusú hemofíliáról lesz szó részletesen. Öröklődés hordozó vizsgálatok Már az ókorban is felismerték, hogy a hemofília nemhez kötött recesszív öröklődésmenetű betegség, így néhány ritka kivételtől eltekintve férfiaknál alakul ki, nők nem betegek, csak hordozzák, és örökítik a betegséget. (Ahhoz, hogy nőknél is kialakulhasson, az szükséges, hogy egy beteg apa és egy hordozó anya házasságából szülessen az utód, aki az anyától a hibás X kromoszómát örökli.) Az X-hez kötött öröklődésmenetből adódóan egy beteg apának valamennyi fia egészséges, viszont valamennyi lánya hordozó (carrier, más néven konduktor) lesz. Egészen biztosan hordozónak (obligát hordozó) tekinthető egy hemofíliás férfi lánya, az az anya, akinek legalább két beteg fia van (akik nem egypetéjű ikrek) vagy akinek egy beteg fia és egy olyan lánya van, aki hemofíliában szenvedő fiút szült, illetve az az anya, akinek egy hemofíliás fia van, de családjában anyai oldalon még másvalaki is hemofíliás. A hordozók lányai az esetek felében szintén hordozók, míg fiai az esetek felében betegek lesznek. Lehetséges (potenciális) hordozónak tekintjük azokat a nőket, akiknek az anyja hordozó, de ők maguk nem obligát hordozók, illetve azokat, akiknek csak egy hemofíliás fia van, és a családban még nem fordult elő a betegség. Ez utóbbi esetben is az anya kb %-os valószínűséggel hordozó. A hordozók az esetek túlnyomó többségében tünetmentesek, faktorszintjük átlagosan a normál faktor aktivitás 50%-a (a normál érték 70 és 150% között van), azonban nagy az átfedés az obligát hordozók, és az egészséges nők faktoraktivitása között. A potenciális hordozók vizsgálatakor talált alacsony faktor aktivitás (<50%) a hordozói állapotot valószínűsíti, a normál %-os aktivitás viszont nem zárja ki a hordozó státuszt. A faktorszint normál esetben is változik (pl. az életkorral növekszik) és szintjét bizonyos gyógyszerek (pl. ösztrogéntartalmú fogamzásgátló tabletták), illetve a terhesség jelentősen befolyásolják. Az obligát hordozók esetében nem szükséges genetikai vizsgálat annak bizonyí- 7
8 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS tására, hogy örökíthetik a betegséget. Azonban potenciális hordozói státusz esetén a hordozói állapot kimutatására a faktor aktivitás meghatározása gyakran nem megbízható, így hemofília A-ban és B-ben a genetikai diagnosztika célja legtöbbször a hordozók azonosítása (carrier-diagnosztika). Hemofíliás beteg genetikai vizsgálata Azt, hogy valaki hemofíliás-e, a vér alvadási paramétereinek vizsgálatával egyértelműen meg lehet állapítani, tehát ehhez nem szükséges genetikai vizsgálat. A maradék faktoraktivitás alapján a hemofiliáknak súlyossági fokuk szerint három csoportja ismert: súlyos (faktoraktivitás: <1%); középsúlyos (1-5%) és enyhe (5-30%). A tünetek kialakulását rendszeres faktorpótlással meg lehet előzni. A kóroki mutáció ismerete alapvetően nem befolyásolja a beteg kezelését, a csecsemőkori, első kezelésektől eltekintve. Legtöbbször az esetleges potenciálisan hordozó családtagok genetikai vizsgálatához szükséges a családból egy hemofíliás beteg vizsgálata. Mutáció típusok, alkalmazott molekuláris biológiai módszerek Egy betegség molekuláris genetikai vizsgálatánál alapvető feladat a kóroki mutáció azonosítása (direkt mutáció kimutatás). Egy különleges a súlyos hemofília A esetek felében előforduló mutáció a VIII-as véralvadási faktor génjét érintő úgynevezett 22. intron inverzió. Ennél a mutációnál az érintett gén egy darabja a 22. intronnál kitörik, és fordított irányban épül vissza. A VIII-as véralvadási faktor gén 22. intron inverziója sok esetben egy egészséges férfi hímivarsejtjeinek érése során alakul ki véletlenszerűen, aminek következtében hordozó lánya születhet az illetőnek, a vérzékenység pedig majd csak az ezt követő generációban, az illető férfi unokájánál jelenik meg. Ez a mechanizmus magyarázhatja a családban újonnan megjelenő, ún. de novo hemofília A esetek jelentős részét. A súlyos hemofília A-s betegek kis részénél hasonló módon 1. intron inverzió alakul ki. Azokban a súlyos hemofília A-s esetekben, ahol nem géninverzió áll a betegség hátterében, valamint az összes középsúlyos és enyhe hemofília A, és minden hemofília B esetben nagyon sok különböző mutáció okozhatja a betegséget. Ahhoz, hogy a családra jellemző mutációt megtaláljuk, az egész gént végig kell vizsgálni, mintha egy hosszú könyvet kellene elolvasni. Ez hemofília B esetén könnyen kivitelezhető, hemofília A esetén azonban mivel a VIII-as véralvadási faktor génje nagyon hosszú jelentős munka- és időbefektetéssel jár. 8
9 Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén Ilyen esetekben lehetőség van azonban indirekt módon arra, hogy egy családon belül megkülönböztessük a beteg gént hordozó kromoszómát, és nyomon követhessük öröklődésmenetét, anélkül, hogy a családra jellemző mutációt pontosan azonosítanánk. Az indirekt módszerek családvizsgálaton alapulnak. Az esetek többségében szükség van a családból legalább egy beteg, és az összes olyan családtag vizsgálatára, akitől a kérdéses személy örökölhette az X kromoszómáját. Korrekt diagnózis indirekt módszerekkel csak pontos családfa esetén adható, ami aláhúzza a genetikai tanácsadás fontosságát, beleértve az apaság kérdését is. Távoli oldalági rokonok vizsgálatakor szükség lehet az anyai nagyszülők, illetve dédszülők vizsgálatára is. Direkt mutáció azonosításkor nincs szükség a teljes család vizsgálatára, elegendő a mutáció azonosítása a betegnél vagy egy obligát hordozónál, hiszen ugyanaz a mutáció okozza a betegséget egy családon belül. Távoli, oldalági rokonok is biztonsággal vizsgálhatók. A kérdéses személyeket akkor is vizsgálhatjuk, ha a családban az érintett (beteg) személytől valamilyen okból nem áll rendelkezésre minta. Különösen nagy jelentőségű továbbá sporadikus családokban, vagyis ahol a családban csak egy hemofíliás beteg ismert. Ezekben az esetekben ugyanis csak 70-80% a valószínűsége annak, hogy a beteg édesanyja hordozó (az esetek 20-30%-ában a mutáció újonnan, de novo keletkezett), ezért az indirekt módszerek sem adhatnak 95-99%-os valószínűségi eredményt. Ezen kívül fontos azokban a családokban, ahol az indirekt módszer szempontjából fontos családtag nem elérhető, és a módszer ezért nem alkalmazható. A direkt mutáció elemzéssel az inverzió kimutatástól eltekintve csak akkor nyújtható prenatális diagnosztika, ha a hordozó nő családjában még a terhessége előtt megtörtént a mutáció azonosítása. Az inverziók szempontjából negatív családokban a mutáció azonosítása időigényes folyamat, ezért ha nagyon sürgősen van szükség carrier-, vagy prenatális diagnosztikára, és a családban még nem történt direkt mutáció azonosítás, a gyorsan kivitelezhető indirekt módszerek alkalmazhatóak. Vizsgálati lehetőségek 1. Mit kell tennie, ha a családjában van hemofíliás beteg, és Ön attól fél, hogy esetleg Önnek is beteg gyermeke születik? Először meg kell bizonyosodni arról, hogy Ön hordozónak számít-e. Ha Önre illik a korábban az obligát hordozóra felsorolt lehetőségek egyike, akkor bizto- 9
10 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS san hordozó, és a genetikai vizsgálatra csak akkor van szükség, ha Ön a születendő gyermekénél magzati korban tudni akarja, hogy hemofíliás lesz-e. Ha Önre a potenciális hordozókra vonatkozó felsorolásból illik az egyik lehetőség, akkor a genetikai vizsgálattal először arra adunk választ, hogy hordozza-e egyáltalán a betegségért felelős kromoszómát? Ha igen, akkor Ön bizonyítottan hemofília hordozó, hasonlóan az obligát hordozókhoz. Ha nem hordozza a betegségért felelős kromoszómát, akkor az Ön esetében hemofília irányú prenatalis vizsgálatra nincs szükség. 2. Mit kell tennie, ha a családban még nem fordult elő ez a betegség, és Ön attól fél, hogy esetleg beteg gyermeke születik? Genetikai vizsgálattal erre a kérdésre nem tudjuk egyértelműen azt mondani, hogy Ön egészen biztosan nem hordozó. Azonban annak a valószínűsége, hogy Önnek ilyen helyzetben hemofíliás fia születik, hemofília A esetén 0,02%, hemofília B esetén 0,003%. 3. Mit kell tennie, ha beteg gyermeke született, és a családjában eddig nem fordult elő ez a betegség? Ezt az esetet sporadikus megjelenésnek nevezzük. Ilyen esetben Ön potenciális hordozónak számít, az irodalmi adatok szerint 70-80% annak az esélye, hogy ténylegesen hordozó, míg az esetek 20-30%-ában a mutáció újonnan, de novo keletkezett az anyai ivarsejt képződés során. Genetikai vizsgálat szükséges annak kiderítésére, hogy következő gyermekénél fennáll-e a betegség kialakulásnak lehetősége. Indirekt módszerek használatával ezekben a sporadikus családokban a kizáró diagnózis 95-99%- os biztonsággal, a megerősítő diagnózis csak 70-80%-os biztonsággal állítható fel. Direkt mutáció azonosítással a sporadikus betegek családjában is 100%- os biztonsággal nyújtható prenatális diagnosztika. Sporadikus családokban különösen fontos, hogy még a következő gyermekvállalás előtt kivizsgálásra kerüljön direkt mutáció kimutatással a génhiba. Prenatális vizsgálat igénye esetén keresse fel a hemofília gondozót a következő gyerekvállalás előtt lehetőleg legalább 6-12 hónappal, hogy a direkt mutációvizsgálatra elegendő idő álljon a genetikai laboratórium rendelkezésére. A genetikai vizsgálat folyamata Bármilyen esetben merül is fel a genetikai vizsgálat szükségessége, első lépésben egy genetikai tanácsadót kell felkeresnie. Az adott szakember fogja eldönteni, hogy milyen vizsgálatok, illetve milyen további családtagok vizsgálata szükséges. Sok esetben a genetikai tanácsadást a beteg családtag kezelőorvosa végzi. 10
11 Molekuláris diagnosztika A és B típusú öröklődő vérzékenység esetén Ha korábban még nem vizsgálták véralvadási probléma miatt, akkor először várhatóan a vérének az alvadási paramétereit fogják megvizsgálni, és ez után kerül sor a genetikai irányú mintavételre, ami egy egyszerű vérvételt jelent. Ezt a mintát az esetleges további családtagok mintájával együtt a kezelőorvos eljuttatja a genetikai laboratóriumba, ahol megtörténik a genetikai vizsgálat. Magyarországon jelenleg az Országos Vérellátó Szolgálat Molekuláris Diagnosztikai Laboratóriumában folynak hemofilia A és B genetikai vizsgálatok. A laboratórium óta foglalkozik a hemofilia genetikai vizsgálatával. Először mindig a hemofíliás beteg genetikai vizsgálata történik meg. A vizsgálat eredményről a kezelőorvos írásos leletet kap. Bármilyen súlyossági fokú hemofilia B, és súlyos hemofília A esetén, valamint a sporadikus hemophilia A családokban és a beteg családtag elérhetetlensége esetén a kóroki mutáció azonosítására törekszünk direkt mutáció azonosítással, míg középsúlyos és az enyhe hemofília A családokban alapvetően indirekt módszereket alkalmazunk. Indirekt módszerek alkalmazásakor előfordulhat, hogy további családtagok vizsgálata is szükséges az Önre vonatkozó egyértelmű eredményhez. A vizsgálatokat a társadalombiztosítás finanszírozza, Önnek nem kell értük fizetnie. A vizsgálatok többsége nem sürgős, mivel a genetikai vizsgálat eredménye nem befolyásolja a hemofíliás beteg vagy a tünetmentes hordozó kezelését. Ezekben az esetekben a laboratórium a beérkező mintákat csoportosan dolgozza fel, és több hónap is eltelhet a mintavétel és a genetikai eredmény megszületése között. Ideális esetben a potenciális vagy az obligát hordozók korán, még terhesség előtt felkeresik a genetikai tanácsadást, és a genetikai laboratórium kimutatja a beteg családtagban a betegségért felelős mutációt, vagy azonosítja a prenatális diagnosztikában vizsgálható, betegségért felelős kromoszómát. Potenciális hordozóknál a vizsgálatok akár ki is zárhatják a hordozói státuszt, így elkerülhető az invazív prenatális vizsgálat. Az azonosított hordozóknál prenatális diagnózis igénye esetén chorion boholy mintavétellel akár a terhesség hetes időszakában megtörténhet a magzati sex-kromoszóma meghatározás, és fiú magzat esetén a genetikai vizsgálat is egy-két héten belül elvégezhető. 11
12 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS 2004-ben végeztem a Pécsi Tudományegyetemen óta dolgozom az Istenhegyi Géndiagnosztikai és Családtervezési Központban, ahol elsősorban a monogénes betegséggel küzdő családoknak segítek családtervezés tekintetében. Hordozósági vizsgálatokkal, prenatális (magzati) és preimplantációs (embrionális) vizsgálatokkal foglalkozom. Varga Tünde molekuláris biológus Szívügyem a monogénes betegségek preimplantációs genetikai diagnosztikája (PGD), ami munkám gyümölcseként került bevezetésre intézetünkben. A mai napig szívemen viselem minden hozzánk forduló család sorsát, és velük együtt örülök a közösen elért sikernek, amikor sokszor nagyon nehéz előzmények után végre megszületik a várva-várt egészséges baba. Varga Tünde, Kékesi Anna Istenhegyi Géndiagnosztikai Centrum Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Mi a PGD? A PGD egy mozaikszó, a Preimplantációs (azaz beültetés előtti) Genetikai Diagnosztika rövidítése. PGD olyan pároknál kerülhet alkalmazásra, akiknek a családjában egy ismert, az életminőséget jelentősen csökkentő genetikai rendellenesség öröklődik, és magas a kockázatuk arra, hogy születendő gyermekük is érintett lesz a betegségben. A preimplantációs genetikai diagnosztika a prenatális (születés előtti) vizsgálatok legkorábban elvégezhető formája. Ilyenkor a hagyományos prenatális vizsgálatokkal szemben (chorion-boholy/ magzatvíz mintavétel) nem a terhesség alatt, hanem a terhesség létrejötte előtt történik meg a genetikai vizsgálat. PGD vizsgálatoknál mesterséges megtermékenyítést követően, még beültetés előtt álló preembriókat vizsgálunk azzal a céllal, hogy az adott családban öröklődő genetikai eltérést még a ter- 12
13 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában hesség létrejötte előtt azonosítsuk. A PGD vizsgálattal meghatározható, hogy mely embriók örökölték a betegséget, és melyek nem. Ezzel az eljárással lehetőség nyílik arra, hogy csak olyan embriók kerüljenek beültetésre, amelyek nem érintettek az adott betegségben. A PGD olyan pároknak is lehetőséget nyújt a gyermekvállalásra, akik számára a hagyományos prenatális vizsgálatot követő esetleges terhességmegszakítás nem elfogadható alternatíva. Milyen esetekben végezhető PGD vizsgálat egy hemofíliával érintett családban? PGD vizsgálat kizárólag olyan esetekben végezhető, ha a születendő gyermeknél magas egy adott betegség tényleges kialakulásának kockázata. Hemofília-A és -B esetében a fenti kritérium miatt PGD vizsgálat csak abban az esetben indokolt, ha az anya hordozója a betegségnek. Amennyiben a pár férfi tagja érintett, PGD vizsgálat nem végezhető, mert ilyenkor a gyermekeknél nem kell a betegség kialakulására számítani, hiszen az apa minden lánya tünetmentes hordozó lesz, míg a fiai egészségesek. Az okok megértéséhez tisztában kell lennünk az öröklődés főbb törvényszerűségeivel. A hemofília-a és -B betegségek X kromoszómához kötött recesszív módon öröklődnek, az alábbi főbb sajátosságokkal: a betegséget okozó mutáció az X kromoszómán helyezkedik el az öröklés recesszív, azaz csak akkor alakul ki a betegség, ha kizárólag hibás génpéldányt hordozó X kromoszóma van jelen a szervezetben jellemzően a férfiak érintettek, mert nekik csak egy X kromoszómájuk van nők csak abban a ritka esetben lesznek betegek, ha mindkettő szülőtől hibás X kromoszómát örökölnek (beteg apa + hordozó anya) ha az anya hordozó, a fiú utódok kockázata a betegség megjelenésére 50% ha az apa érintett, minden lánya tünetmentes hordozó, míg minden fia egészséges lesz Ahogy a következő ábrákon is látható, a hemofília megjelenésére csak az első esetben (hordozó anya) kell számítani, ezért PGD vizsgálat csak ekkor végezhető. A második esetben, beteg apa esetén az utódoknál nem alakul ki a betegség, viszont az apa összes lánya obligát hordozó lesz. Ilyenkor a prenatális/ preimplantációs vizsgálat egy generációval később, a beteg apa lányainak gyermekvállalásakor válik indokolttá. 13
14 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Az X-kromoszómához kötött recesszív öröklésmenet sematikus ábrái A két leggyakoribb eset, amikor a nő a hordozója a betegségnek, míg a férfi egészséges (A. ábra), illetve, amikor a férfi érintett, és a nő egészséges (B. ábra) Az A. esetben a nőnek egy normál és egy hibás génpéldánya van a betegségért felelős génből, míg a férfi egyetlen normál génpéldánnyal rendelkezik az X-kromoszómáján, az Y-kromoszóma nem hordozza az adott gént. A szülői nemi kromoszómák a nyilakkal jelzett módon 4-féleképpen kombinálódhatnak az utódokban. A gyerekek 25%-a a normál anyai X-kromoszómát örökli az apai Y-kromoszómával kombináltan, és egészséges fiú lesz. A gyerekek 25%-a a normál anyai X-kromoszómát örökli az apai X-kromoszómával kombináltan, és egészséges lány lesz. A gyerekek 25%-a a hibás anyai X-kromoszómát örökli az apai Y-kromoszómával kombináltan, és beteg fiú lesz. A gyerekek 25%-a a hibás anyai X-kromoszómát örökli az apai X-kromoszómával kombináltan, és tünetmentes hordozó lány lesz. Az B. esetben a férfinak egyetlen hibás génpéldánya van az X-kromoszómáján a betegségért felelős génből, mellette pedig egy Y-kromoszóma, ami nem hordozza az adott gént, míg a nő két normál génpéldánynyal rendelkezik. Ilyenkor az anya minden utódnak normál X-kromoszómát örökít, így attól függően, hogy az apa melyik nemi kromoszómáját örökíti tovább, kétféle lehetőség adódik. Az apa hibás X-kromoszómáját öröklő utódok a betegséget tünetmentesen hordozó lányok lesznek (50%) míg az apa Y-kromoszómáját öröklő utódok egészséges fiúk lesznek (50%). 14
15 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Milyen lehetőségek állnak rendelkezésre a hemofília PGD-vel történő megelőzésére? Hemofília-A és -B betegségek esetében az X-hez kötött recesszív öröklődésből adódóan kétféle módszer választható a PGD-vel történő megelőzésre: a. Az embriók nemének meghatározása FISH módszerrel Ebben az esetben a vizsgálat csak kromoszómák szintjén zajlik. Az X- és Y-kromoszómák vizsgálatával meghatározzuk az embriók nemét (XX - lány, XY - fiú), és visszaültetésre csak a lány embriókat javasoljuk a fiú utódok 50%- os kockázata miatt. Ennél a vizsgálatnál így nem lesz információnk arról, hogy a visszaültetésre javasolt lány embriók közül melyik hordozója a betegségnek, és melyik nem, továbbá nem tudjuk azt sem, hogy a visszaültetésre nem javasolt fiú embriók közül melyik valóban beteg és melyik lenne egészséges. Ezzel a módszerrel az öröklésből minden fiú utód kizárásra kerül a rájuk vonatkozó 50%-os kockázat miatt. A FISH-módszer mellett szólhat, hogy uniform, azaz nem igényel speciális előkészületet, ezért gyorsabb és olcsóbb, mint a betegség génszintű vizsgálata, hátránya viszont, hogy nem ismert a tényleges genotípus, ezért az egészséges fiú embriók is kizárásra kerülnek az öröklésből. b. Az embriók mutációs státuszának meghatározása PCR módszerrel. Ebben az esetben a vizsgálat során a konkrét kóroki mutáció, ill. hibás gén kimutatása történik, és mind a négy lehetséges genotípus (egészséges lány, hordozó lány, egészséges fiú, beteg fiú) egyértelműen azonosítható. Visszaültetésre ilyenkor csak a beteg fiú embriókat (25%) nem javasoljuk, így a módszerrel magasabb a visszaültetésre javasolható embriók aránya. PCR módszerrel a hordozó anyának egészséges fia és lánya is születhet. A PCR-módszer mellett szól, hogy nagyobb az információtartalma, ezáltal több embrió is visszaültetésre javasolható, és mindkét nemű egészséges utód is születhet a segítségével. Hátránya lehet, hogy speciális előkészületet igényel, ezért lassabb és drágább, mint az előkészületet nem igénylő, pusztán az embriók nemét meghatározó FISH vizsgálat. 15
16 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS PGD ciklus hemofília betegségben a nemi kromoszómák vizsgálatával (PGD-FISH) Az anya hordozója a betegségnek (egyik X-kromoszómája mutáns, a másik egészséges), míg az apa egészséges (egy normál X- kromoszómája mellett egy Y-kromoszómával). A 2-2 szülői nemi kromoszóma 4-féleképpen kombinálódhat az utódokban (egészséges lány, hordozó lány, egészséges fiú, beteg fiú). Mivel FISH technikánál a vizsgálat csak kromoszóma szinten zajlik, a pontos genotípusról nincs információnk. Az XX kromoszómával rendelkező embriók (1., 4. és 6.) mindegyike visszaültetésre javasolt (egészséges/ hordozó lányok), míg az XY kromoszómával rendelkező embriók (2., 5. és 7.) egyike sem javasolt visszaültetésre (egészséges/beteg fiúk). A 3. embrióból nincs megbízható eredmény, visszaültetésre nem javasolt. A nemi kromoszómák vizsgálatán alapuló hemofília PGD (FISH módszer) esetében statisztikai alapon 50% a visszaültetésre javasolt (lány) és 50% a visszaültetésre nem javasolt (fiú) embriók várható aránya, bár ezektől az arányoktól egy-egy ciklusban jelentős eltérések lehetnek. 16
17 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában PGD ciklus hemofília betegségben, a kóroki mutáció vizsgálatával (PGD-PCR) Az anya hordozója a betegségnek (egyik X-kromoszómája mutáns, a másik egészséges), míg az apa egészséges (egy normál X- kromoszómája mellett egy Y-kromoszómával). A 2-2 szülői nemi kromoszóma 4-féleképpen kombinálódhat az utódokban (egészséges lány, hordozó lány, egészséges fiú, beteg fiú). PCR technika esetében mind a 4 kombináció egyértelműen azonosítható. Az 1. embrió az anyai mutáns X-kromoszóma mellett a normál apai X-kromoszómát örökölte. Az embrió tünetmentes hordozó lány, visszaültetésre javasolt. A 2. embrió az anyai mutáns X-kromoszóma mellett Y-kromoszómát örökölt az apától. Az embrió beteg fiú, visszaültetésre nem javasolt. A 3. embrió genotípusa nem határozható meg. Az embrió genetikai eredmény hiányában visszaültetésre nem javasolt. A 4. embrió mindkét szülőjétől egészséges génpéldányt hordozó X-kromoszómát örökölt. Az embrió egészséges lány, visszaültetésre javasolt. 17
18 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Az 5. embrió az egészséges anyai X-kromoszóma mellett Y-kromoszómát örökölt az apától. Az embrió egészséges fiú, visszaültetésre javasolt. A 6. embrió az anyai mutáns X-kromoszóma mellett a normál apai X-kromoszómát örökölte. Az embrió tünetmentes hordozó lány, visszaültetésre javasolt. A 7. embrió az egészséges anyai X-kromoszóma mellett Y-kromoszómát örökölt az apától. Az embrió egészséges fiú, visszaültetésre javasolt. A hibás gén vizsgálatán alapuló hemofília PGD (PCR módszer) esetében statisztikai alapon az embrióknak kb. 75%-a várható visszaültetésre javasolhatónak (25% egészséges fiú, 25% hordozó lány, 25% egészséges lány), míg kb. 25%-a visszaültetésre nem javasoltnak (beteg fiú), bár ezektől az arányoktól egy-egy ciklusban jelentős eltérések lehetnek. A PGD eljárás menete A PGD eljárás szervezeten kívüli megtermékenyítést (IVF - in vitro fertilizáció) igényel, ezáltal a genetikai vizsgálatot végző, ill. a lombikkezelések végzésére specializálódott centrumok együttműködésében valósul meg. A genetikai tanácsadást, az előkészítő genetikai vizsgálatokat, illetve az embriókból kiemelt sejtek genetikai vizsgálatát az Istenhegyi Géndiagnosztikai Centrum, míg a lombikkezelés előkészítését, kivitelezését, az embriókból történő mintavételt, és az embrióbeültetést az IVF centrum (Kaáli Intézetek, Szent János Kórház Budai Meddőségi Centrum) végzi. Ennek megfelelően egyes lépések az Istenhegyi Géndiagnosztikai Centrumban, mások a lombikcentrumban történnek. A PGD eljárás lépései időrendi sorrendben a következők: I. Genetikai tanácsadás az Istenhegyi Géndiagnosztikai Centrumban A PGD vizsgálatot minden esetben számos előkészítő lépés előzi meg. Ezek közül az első a Géndiagnosztikai Centrumban tartott genetikai tanácsadás. A konzultáción jelen van a PGD vizsgálatra jelentkező pár, a klinikai genetikus szakorvos, és a PGD vizsgálatokban jártas biológus szakember. A konzultáción áttekintjük a családi előzményeket, a rendelkezésre álló genetikai leleteket, melyek alapján meghatározható, hogy az adott esetben indokolt-e a PGD vizsgálat elvégzése, ill. szükség van-e esetleg kiegészítő genetikai vizsgálatokra. PCR alapú vizsgálathoz szükség van a betegséget okozó mutáció pontos ismeretére. Ha a családban öröklődő mutáció beazonosítása koráb- 18
19 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában ban nem történt meg, akkor azt a PGD vizsgálat előtt szükséges elvégezni (ld. molekuláris diagnosztika fejezet). Amennyiben indokolt a PGD vizsgálat elvégzése, és ahhoz minden előzetes vizsgálati dokumentáció rendelkezésre áll, kiállítunk egy szakvéleményt arra vonatkozóan, hogy az adott párnál a PGD eljárás genetikai szempontból indokolt, technikailag kivitelezhető, és a pár kérésére elvégezhető. A párnak el kell döntenie, hogy melyik módszerrel (embriók nemének meghatározása/ mutációvizsgálat) kéri a PGD vizsgálatot, ugyanis az előkészületek, és az eljárás további lépései a két módszer esetében különbözőképpen alakulnak. A tanácsadáson a következő témaköröket járja körül a pár a jelenlévő szakemberekkel: 1) családi kórtörténet, családfa analízis 2) a születendő utód genetikai kockázata 3) a szülők gyermekvállalási lehetőségei (prenatális és preimplantációs vizsgálatok) 4) amennyiben a párnál PGD vizsgálat indokolt, annak részletei (előnyök, kockázatok, az eljárás menete, a két PGD lehetőség közötti különbségek) 5) a PGD ciklus indítása előtt szükséges laboratóriumi vizsgálatok 6) egyéb felmerülő kérdések II. Szakorvosi konzultáció a választott centrumban A PGD vizsgálathoz szükséges IVF kezelésre több IVF centrumban (Kaáli Intézetek, Szent János Kórház Budai Meddőségi Centrum) is lehetőség van, melyek közül a páciens választhatja ki a számára megfelelőbbet. A vizsgálat előkészítéséhez a választott lombikcentrumban is konzultációs időpontot kell egyeztetni. A konzultáción szükség lesz az I. pontban ismertetett genetikai tanácsadáson kiállított, a PGD indokoltságát alátámasztó szakvéleményre. A konzultáción a szakorvossal áttekintik a reproduktív előzményeket, egyeztetnek a kezelés indítása előtt elvégzendő orvosi és laboratóriumi vizsgálatokról, meghatározzák, hogy nincs-e egészségügyi akadálya a lombikkezelésnek. A szakorvos ismerteti az IVF eljárás menetét, és a konzultáción lehetőség van a kezeléssel kapcsolatos bármilyen további kérdés megvitatására. III. Laboratóriumi előkészületek LABORATÓRIUMI ELŐKÉSZÜLETEK AZ ISTENHEGYI GÉNDIAGNOSZTIKAI CENTRUMBAN a. Ha a pár az embriók nemének meghatározását kéri (PGD-FISH), speciális előkészületre nincs szükség, az IVF kezelés rövid időn belül indítható. 19
20 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS b. Ha a pár az embriók génszintű vizsgálatát (PGD-PCR) kéri, az IVF kezelést speciális, molekuláris genetikai laboratóriumi előkészületek előzik meg, melyek átlagosan 2-4 hónapot vesznek igénybe. Ez idő alatt az IVF centrum részéről kért vizsgálatok párhuzamosan végezhetők. A génszintű PGD vizsgálatok laboratóriumi előkészületeihez mintavétel szükséges a pár mindkét tagjától, ill. a genetikai tanácsadáson meghatározott hozzátartozó(k)tól. A leendő szülőktől helyben történik vérvétel, míg a hozzátartozóknak nem szükséges személyesen ellátogatnia centrumunkba, tőlük elegendő a szájnyálkahártyából történő otthoni mintavétel is. A családtagok DNS mintáit ezután a molekuláris genetikai labor a PGD-beállításnak nevezett előkészítési munka keretében feldolgozza, és segítségükkel felkészül az embriók vizsgálatára. A PGD-beállítás keretében végzett laboratóriumi munka részleteiről a fejezet utolsó pontjában olvashat. ELŐKÉSZÜLETEK AZ IVF CENTRUMBAN Az IVF kezelés előtt elvégzendő szakorvosi, ill. laboratóriumi vizsgálatokról a II. pontban ismertetett konzultáción egyeztetnek a szakorvossal. A rutinszerűen elvégzendő vizsgálatok között van a nőgyógyászati vizsgálat, citológia, hormonvizsgálatok a női ciklus különböző időpontjaiban, spermavizsgálat, és különböző kórokozó szűrések (pl. hepatitis-b, -C, HIV). A rutin teszteken felül egyéb, speciális vizsgálatokra is szükség lehet (endokrinológia, immunológia, meddőségi genetika), melyeket az IVF centrum szakorvosa rendel el a konzultáción feltárt előzmények alapján. IV. Az IVF-PGD ciklus lépésről-lépésre Az előkészületek lezárását követően indítható el az IVF-PGD ciklus, mely az IVF centrum és a Géndiagnosztikai Centrum szoros együttműködésében valósul meg. A kezelés indítása előtt mindig egyeztetni szükséges a vizsgálatban résztvevő mindkét centrummal az ütemezésről, hogy a PGD mintavétel időpontjában a genetikai laboratórium rendelkezésre tudjon állni a vizsgálathoz. 1. HORMONÁLIS STIMULÁCIÓ (IVF CENTRUM) A pár női tagjánál az előzetes vizsgálatok alapján személyre szabott hormonális petefészek stimulációt indítanak, melynek célja a többszörös, időzített tüszőérés. A tüszők érését segítő hormonkészítmények típusa, adagolása, a kezelés hossza egyénenként változhat. A tüszőérés folyamatát vérvételekkel és ultrahangos vizsgálatokkal követik, hogy a legmegfelelőbb időpontban végezzék el a petesejt leszívást. 20
21 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában 2. PETESEJT LESZÍVÁS (IVF CENTRUM) A petesejt leszívás altatásban, ultrahang kontroll mellett végzett beavatkozás. Ennek során az érett tüszőkből leszívják a petesejtet is tartalmazó folyadékot, majd a petesejteket megtisztítják és megfelelő táptalajba helyezve előkészítik a megtermékenyítéshez. 3. MESTERSÉGES MEGTERMÉKENYÍTÉS (IVF CENTRUM) PGD eljárás során a megtermékenyítésnek egy speciális formáját, az intracitoplazmatikus spermium injekciót (ICSI) alkalmazzák. ICSI eljárásnál egy mikroszkóp alatt kiválasztott, ép és szabályos hímivarsejttel termékenyítik meg a petesejtet, úgy, hogy a spermiumot egy kapilláris segítségével beinjektálják a petesejtbe. Ezzel az eljárással biztosítható, hogy nem kerül a genetikai vizsgálatot zavaró, külső DNS szennyezés a mintába a megtermékenyítésben részt nem vevő, de a petesejt burkához tapadó további spermiumok miatt. 4. MINTAVÉTEL (IVF CENTRUM) A megtermékenyült petesejteket számukra ideális környezetbe helyezik, és figyelik az első osztódásaikat. A szabályosan osztódó preembriókból a vizsgálat típusától függően a 3. vagy 5-6. napon mintát vesznek a PGD vizsgálathoz. Ilyenkor az embriót körülvevő külső burkot lézerrel megnyitják, és egy üvegkapilláris segítségével eltávolítanak az embrióból néhány sejtet a célzott genetikai vizsgálat céljára. A sejtek eltávolítása az embriót nem károsítja, a kiemelt sejtek szerepét a többi sejt gond nélkül képes átvenni. a. Blastomer biopszia (3. napi mintavétel) Blastomer biopsziát alkalmazunk abban az esetben, ha a PGD vizsgálat a nemi kromoszómák elemzésére irányul (PGD- FISH). Az embriók a fejlődésük 3. napján hat-nyolc sejtből, ún. blastomerekből állnak. 3. napi mintavétel esetén a fejlődő embrió sejtszámától függően 1 vagy 2 blastomer kerül eltávolításra a genetikai vizsgálathoz. 3. napon végzett mintavétel A megtermékenyítést követő 3. napon az embrió jellemzően 6-8 sejtből áll, melyekből egy üvegkapilláris segítségével 1 vagy 2 sejt kerül eltávolításra a genetikai vizsgálathoz. 21
22 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS b. Trofektoderma biopszia (5-6. napi mintavétel) Trofektoderma biopsziát alkalmazunk abban az esetben, ha a PGD vizsgálat a konkrét génmutáció elemzésére irányul (PGD-PCR). Az embriók a fejlődésük 5-6. napján hólyagcsíra állapotúak, és néhány száz sejtből állnak. A hólyagcsírán belül elkülöníthető az embriócsomó, melyből a magzat fog fejlődni, és egy külső sejtréteg (trofektoderma réteg), melyből a méhlepény fog fejlődni. A mintavétel a trofektoderma rétegből történik, átlagosan 6 sejt eltávolításával napon végzett mintavétel A megtermékenyítést követő 5-6. napra az embrió hólyagcsíra állapotig fejlődik. A hólyagcsírán belül elkülöníthető az embriócsomó, melyből a magzat fog fejlődni, és egy külső sejtréteg, melyből a méhlepény fog fejlődni. A külső sejtrétegből egy üvegkapilláris segítségével 5-6 sejt kerül eltávolításra a genetikai vizsgálathoz. Az embriók fagyasztása 5-6. napi mintavétel esetében a biopsziát követően minden embrió fagyasztásra kerül, és visszaültetésre egy későbbi ciklusban kerül majd sor a genetikai eredmény függvényében. 3. napi mintavételkor az embriókat tovább tenyésztik az 5. napig, amikor már a genetikai eredmény ismeretében el tudják végezni a visszaültetést. Amennyibben számfeletti visszaültethető embrió áll rendelkezésre, azok későbbi használatra fagyasztva tárolhatók. A fagyasztás egy modern eljárással, ún. vitrifikációval történik, mely a korábban alkalmazott technikával szemben sokkal nagyobb túlélési arányt biztosít, minimális veszteséggel. 5. GENETIKAI VIZSGÁLAT (ISTEN- HEGYI GÉNDIAGNOSZTIKAI CENTRUM) Az embriókból kiemelt sejtek genetikai vizsgálata az Istenhegyi Géndiagnosztikai Centrum laboratóriumában történik a választott PGD típusnak megfelelő módszerrel. a. Nemi kromoszómák vizsgálata (FISH technika) Amennyiben a pár az embriók nemének vizsgálata mellett döntött, az embriók- 22
23 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában ból kiemelt sejteket fluoreszcens in situ hibridizáció (FISH) technikával vizsgálja a laboratórium. Ez a vizsgálattípus 3. napi mintavétellel történik, és 2 napon belül eredményt ad. A vizsgálatról kiállított leleten szerepel, hogy az egyes embriókban milyen nemi kromoszómák detektálhatók, és hogy a vizsgálat alapján mely embriók javasolhatók visszaültetésre. b. Génhibák vizsgálata (PCR technika) Amennyiben a pár az embriók genotípusának meghatározása mellett döntött, az embriókból kiemelt sejteket polimeráz láncreakció (PCR) technikával vizsgálja a laboratórium. A vizsgálat mindig a PGDbeállítás során előzetesen kidolgozott, személyre szabott molekuláris genetikai módszerrel történik. Ez a vizsgálattípus 5. napi mintavételt követően történik, és 1-2 héten belül ad eredményt. A vizsgálatról kiállított leleten szerepel az embriók genotípusa, és hogy az alapján melyik embriók javasolhatók visszaültetésre. 6. EMBRIÓTRANSZFER (IVF CENTRUM) Az embriók visszaültetése (transzfer) során 1 vagy 2, a genetikai vizsgálat alapján visszaültetésre javasolt embriót helyeznek fel egy rugalmas katéter segítségével ultrahang kontroll mellett az anyaméhbe. A transzfer történhet a stimulált ciklusban (friss embrió transzfer), vagy egy későbbi spontán ciklusban (fagyasztott embrió transzfer). A 3. napi mintavételeket jellemzően friss embriótranszfer követi, míg az 5. napi mintavételek után mindig fagyasztott embrió transzferre kerül sor. A PGD eljárás eredményessége szempontjából kiemelten fontos, hogy abban a ciklusban, amikor a beültetés történik, kerüljék a spontán teherbeesés lehetőségét. Ha ugyanis fennáll a természetes fogantatás lehetősége is, előfordulhat, hogy nem a PGD keretében megvizsgált és beültetett embrióból fejlődik a magzat, hanem egy másik, spontán megtermékenyült, és nem vizsgált petesejtből. Ilyenkor a magzat genetikai kockázata a PGD ellenére magas, és csak a terhesség alatti hagyományos prenatális vizsgálattal tisztázható, hogy érintett-e a betegségben. 7. A TERHESSÉGI MEGERŐSÍTÉSE (IVF CENTRUM) A beültetést követő napon végzett vérvétellel, a szérum β-hcg szintjének mérése alapján megállapítható, hogy létrejött-e terhesség. Pozitív teszteredmény esetén, újabb 2 hét elteltével már ultrahanggal is ellenőrizhető a petezsák(ok) jelenléte, és megállapítható, hogy egyes vagy ikerterhesség fogant-e. 23
24 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS V. Terhesség alatti kontroll genetikai vizsgálat (Istenhegyi Géndiagnosztikai Centrum) Terhesség esetén javasolt a 12. héten méhlepény mintavétellel kontroll genetikai vizsgálatot végezni. Ilyenkor sor kerül a PGD eredményességének megerősítésére, valamint kromoszómavizsgálat is készül, amivel a véletlenszerűen kialakuló számbeli kromoszómarendellenességek (pl. Down- Edwards- és Patau-szindróma) is észlelhetők. A kétféle PGD módszer közötti főbb különbségek: Mire irányul a PGD vizsgálat? nemi kromoszómák kóroki mutáció Módszer PGD-FISH (mikroszkópos vizsgálat) PGD-PCR (molekuláris genetikai analízis) Lehetséges kimenetel Visszaültethető embriók várható aránya Genetikai laboratóriumi előkészület Mintavétel (biopszia) Beültetés legkorábbi időpontja XX lány (visszaültetésre javasolt) XY fiú (visszaültetésre nem javasolt) nincs eredmény (visszaültetésre nem javasolt) ~ 50% ~75% nem szükséges megtermékenyítést követő 3. napon (blasztomer biopszia) megtermékenyítést követő 5. napon egészséges lány (visszaültetésre javasolt) hordozó lány (visszaültetésre javasolt) egészséges fiú (visszaültetésre javasolt) beteg fiú (visszaültetésre nem javasolt) nincs eredmény (visszaültetésre nem javasolt) 2-4 hónap megtermékenyítést követő 5-6. napon (trofektoderma biopszia) következő ciklusban Embriófagyasztás számfeletti embriók összes embrió Ár olcsóbb drágább 24
25 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Mennyire megbízható a PGD vizsgálat eredménye? A PGD megbízhatósága magas, de a minimális sejtszámból adódó korlátozott vizsgálati lehetőségek miatt sajnos nem éri el a 100%-ot. Szakirodalmi adatok alapján a PGD kb. 98%-os megbízhatósággal detektálja az adott genetikai rendellenességet. A lehető legnagyobb biztonság érdekében minden PGD-vel fogant terhesség esetében javasolt a 12. terhességi héten végzett chorion-boholy mintavétel és kontroll genetikai vizsgálat. A kontroll vizsgálattal igazolható a PGD eredményessége, és emellett sor kerül olyan véletlenszerűen kialakuló kromoszóma-rendellenességek (pl. Down-, Edwards-, Patau-szindróma) vizsgálatára is, melyekre vonatkozóan a PGD vizsgálat nem nyújt információt. Mekkora az esély a PGD eljárással történő sikeres fogantatásra? A sikeres fogantatás esélyét számos tényező befolyásolja a PGD eljárás során. A PGD során alkalmazott eljárással az érett petesejteknek kb. 90%-a megtermékenyül. A megtermékenyült petesejtek közül azonban némelyek fejlődése a korai osztódások során leáll. Az embriók töredékénél előfordulhat, hogy nem élik túl a mintavételt vagy a fagyasztást, és a beültetésre kerülő embriók közül sem mind indul fejlődésnek az anyaméhben. Az esélyek a vizsgált embriók számával, minőségével arányosan nőnek. Eddigi tapasztalataink szerint FISH módszer esetén az embrióbeültetések kb. 30 %-ában, míg PCR módszer esetén az embrióbeültetések kb. 40 %-ában jön létre terhesség, ugyanakkor a PGD ciklusra vonatkoztatott terhességi arány ennél magasabb (ha egy ciklusban több visszaültetésre javasolt embrió van, akkor egy esetlegesen sikertelen beültetés után a fagyaszott embriók felhasználásával újabb beültetés végezhető a teljes eljárás ismétlése nélkül). Előfordulhat, hogy a terhesség létrejöttéhez több kezelésre van szükség. A technikai részletekről 1. Az embriók nemének meghatározása FISH módszerrel A nemi kromoszómák vizsgálata esetén az embriókból kiemelt sejtek X- és Y-kromoszómáihoz fluoreszcens in situ hibridizáció (FISH) módszert alkalmazva különböző színű fluoreszcens jelölő molekulákat (próbákat) kötünk. A kromoszóma-specifikus próbák segítségével az X-kromoszómát zöld, míg az Y-kromoszómát piros színnel jelöljük meg, majd a sejteket fluoreszcens mikroszkóp alatt vizsgáljuk. Értékeléskor a fluoreszcens jelek színe és száma alapján állapítható 25
26 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS meg a vizsgált embrió neme. A két zöld jel lány embriót (XX), míg a zöld/piros jelkombináció fiú embriót (XY) jelez. PGD vizsgálat FISH módszerrel A bal oldali képen egy fiú embrióból származó sejt látható mikroszkóp alatt egy zöld és egy piros jellel (XY). A jobb oldali képen egy lány embrióból származó sejt látható mikroszkóp alatt két zöld jellel (XX). 2. Az embriók mutációs státuszának meghatározása PCR módszerrel Mi történik a genetikai laboratóriumban a génszintű PGD vizsgálatot megelőző beállítás során? A hemofília génszintű PGD vizsgálata esetén a DNS kód építőköveit, az ún. bázisokat (A, C, G és T betűk) vizsgáljuk. A PGD vizsgálathoz szükség van a családi mutáció előzetes azonosítására, azaz tudnunk kell, hogy pontosan hol és milyen eltérés található az F8 vagy F9 génekben a normál génváltozathoz képest (a VIII-as faktor génje 187 ezer, a IX-es faktor génje 33 ezer betűből áll, és a két génben eddig összesen megközelítőleg 4000-féle különböző, hemofíliát okozó mutációt írtak le). A génszintű hemofília PGD egy összetett vizsgálat, melyet mindig egy beállítási szakasz (kb. 2-4 hónap laboratóriumi felkészülés) előz meg. Ennek során olyan személyre szabott diagnosztikai tesztet dolgozunk ki, mely nemcsak az adott párnál betegséget okozó mutáció kimutatására képes, hanem a hibás gént hordozó anyai X-kromoszómát indirekt módon is azonosítja. De miért van erre szükség? Miért nem elegendő a mutáció vizsgálata az embriókban? Míg a kromoszómák megfelelő nagyítás mellett mikroszkóppal láthatóvá tehetők és vizsgálhatók, a hemofíliát okozó génmutációk mikroszkóppal már nem vizsgálható mérettartományba esnek. A DNS betűsorrendjét csak közvetett módon, a vizsgálandó szakasz polimeráz láncreakcióval (PCR) történő felsokszorozását követően, speciális műszeres mérések segítségével tudjuk vizsgálni. A PGD vizsgálatok technikai kihívása, hogy a vérből végzett általános molekuláris diagnosztikához képest kb ed annyi DNS áll rendelkezésünkre a genetikai vizsgálathoz. A minimális mintamennyiség miatt néha előfordulhat, hogy egy-egy DNS szakaszt nem sikerül hatékonyan felsokszorozni, így arról elveszik a jel (ez az allélkiesésnek nevezett jelenség). 26
27 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Allékiesés (ADO) PCR alapú PGD vizsgálatok esetében, amikor minimális mennyiségből kiindulva kell felsokszorozni a vizsgálandó DNS-t, előfordulhat, hogy az egyik DNS szál sérülés vagy hozzáférhetetlenség miatt nem sokszorozódik megfelelően, és így az adott DNS szakaszról származó jel elveszik Ahhoz, hogy az allélkiesés ne vezessen téves diagnózishoz, a PGD vizsgálat keretében ún. haplotípus analízist végzünk az embriókon. Ilyenkor nem csak a betegséget okozó mutációt vizsgáljuk, hanem a mutáció környezetében elhelyezkedő további molekuláris azonosítókat, ún. markereket is felhasználunk a vizsgálat során. Ezek a markerek olyan pontok a DNS-en, amelyeket korábbi, népesség szintű vizsgálatok során azonosítottak. Ezeken a pontokon természetes változatosság tapasztalható az egyes kromoszómák között. Ezek a változások olyan DNS szakaszokra esnek, melyek nem befolyásolják a szervezet, ill. a gének működését. Az egyes markerek kombinációi egyediek minden kromoszómán - ez a haplotípus, ami elképzelhető egy molekuláris vonalkódként, vagy ujjlenyomatként is. Ezt a molekuláris ujjlenyomatot használva biztonsággal követhető az egészséges és hibás géneket hordozó szülői kromoszómák öröklődése, még abban az esetben is, ha a mutáció egy esetleges allélkiesés miatt közvetlenül nem detektálható. SNV és STR markerek A DNS szálak azonosítására használható markereknek alapvetően két típusát különböztetjük meg. 1. Az SNV (single nucleotid variant) markerek esetében a DNS egy bizonyos pozíciójában betűcsere történik (pl A>T), így egyes kromoszómák az adott helyen A betűt, mások T betűt fognak hordozni. 2. Az STR (small tandem repeat) markerek esetében a DNS egy bizonyos régiójában változó számú rövid ismétlődés fordul elő (pl közötti CTA ismétlődés egy-egy kromoszómán), mely miatt az ismétlődést hordozó DNS szakasz hossza is megváltozik. 27
28 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Haplotípus analízis Az allélkiesés nem marad észrevétlenül, ha az embriókon haplotípus analízist végzünk. Ezen az ábrán a mutáció mellett két informatív markert látunk az egyes kromoszómákon. A középső DNS szakasz hordozza a kóroki mutációt (a mutáció pirossal, a normál változat zölddel jelölve), a fölötte lévő szakaszon egy STR marker látható (a mutáns kromoszómán rövidebb, a normálon hoszszabb), míg a mutáció alatti szakaszon egy SNV marker látható (a mutáns kromoszómán sötéttel, az egészségesen világossal jelölve). Az ábrán 2 eshetőség szerepel. Az első esetben a DNS szál minden vizsgált szakasza jól értékelhető, az embrió heterozigóta mutáns. A második esetben a mutációról származó jel elveszik, csak a normál allél látható, a kapcsolt markerek azonban felhívják a figyelmet a hibás kromoszóma és az allélkiesés miatt láthatatlanná vált mutáció jelenlétére (a rövidebb STR marker és a sötéttel jelölt SNV marker csak a beteg kromoszómáról származhat). A markerek adatai (kromoszómákon belüli pozíciójuk, az eltérés típusa, a lehetséges variációk, azok gyakorisága) genetikai adatbázisokban hozzáférhetők. A PGDbeállítás során az adatbázisban tárolt információk alapján azonosítjuk azokat a markereket, melyek közel esnek a vizsgálandó kóroki mutációhoz, és melyekben a népességen belül viszonylag nagy változatosság tapasztalható. A kiválasztott DNS szakaszokat ezt követően meg kell vizsgálni a PGD-re jelentkező párnál. Nem biztos, hogy a vizsgált markernél valóban tapasztalunk eltérést az egyes családtagok X-kromoszómái között, ezért számos markert kell tesztelnünk ahhoz, hogy rátaláljunk azokra, melyek támogathatják a PGD vizsgálatot. A tesztelt markerek egy részénél nincs eltérés a szülők kromoszómái között (ezek a markerek nem informatívak a vizsgált családra), míg másoknál igen (ezek az informatív markerek). Egy-egy PGD-beállítás során jellemzően 20-30, a mutáció közvetlen környezetében elhelyezkedő markert kell megvizsgálunk ahhoz, hogy megfelelő számú (3-6), az adott párra informatív markert azonosítsunk, melyek egyedi kombinációja alapján követhetővé válnak a normál és hibás génpéldányokat hordozó szülői X-kromoszómák. A beállítás során a családtagok mintáinak segítségével felállítjuk a haplotípusokat, melyekre támaszkodva később nagy biztonsággal végezhető el a pár embrióinak PGD vizsgálata. Minden egyes beállítás egyedi, nincs két azonos eset. 28
29 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Egy PGD-PCR beállítás végeredménye hemofíliával sújtott családban A PGD beállításhoz számos SNV és STR markert tesztelünk a családtagokon. A tesztelt markerek közül azok használhatók az embriók későbbi vizsgálatánál, amelyeknél eltérést tapasztalunk az egyes kromoszómák között. Az itt bemutatott ábrán a leendő szülők és a nő beteg édesapjának a PGD szempontjából informatív markerei láthatók. A kóroki mutáció mellett 6 további informatív markert azonosítottunk a PGD-beállítás során. A fenti család PGD-PCR ciklusa Az embriókból vett mintákon vizsgáljuk a kóroki mutációt, és valamennyi, a PGD beállítás során azonosított informatív markert is. Az így nyert haplotípus információ alapján állapítható meg, hogy mely embriók javasolhatók visszaültetésre. Az 5. embriónál allélkiesés figyelhető meg (a kóroki mutációról származó jel hiányzik), de a többi marker egyértelműen jelzi a hibás X-kromoszóma jelenlétét. 29
30 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Dióhéjban a DNS vizsgálatához használt műszeres technikákról A DNS műszeres analíziséhez a vizsgálandó szakaszt először polimeráz láncreakció (PCR) segítségével felsokszorozzuk, majd különböző fluoreszcens technikákat alkalmazva elemezzük. Szekvenálás Olvadáspont-analízis A DNS olvadásának nevezzük azt a jelenséget, amikor a DNS kettős spirálja hő hatására kicsavarodik, és a két párhuzamosan futó lánc elválik egymástól. A DNS olvadáspontja függ a bázissorrendtől. DNS olvadáspont analízist alkalmazhatunk már ismert báziscserék gyors kimutatására. A DNS kód betűinek (A, C, G és T) leolvasása szekvenálással lehetséges. Ezt a módszert használjuk, ha egy vagy néhány betű megváltozását szeretnénk kimutatni a DNS-en. Pontmutáció vizsgálata olvadáspont analízissel Amennyiben a mutációt hordozó DNS szakaszhoz fluoreszcens festéket kötünk, mely a kicsavarodó spirálból adott hőmérsékleti ponton kiszabadul, a fluoreszcens jelintenzitás változásaiból következtethetünk a szekvenciára. Pontmutáció analízise szekvenálással Az ábrán a nyíllal jelölt pozícióban egy C>G báziscsere (mutáció) látható. Az egészséges génpéldány az adott pozícióban C bázist tartalmaz (kék színű csúcs), míg a mutáns G-t (fekete színű csúcs). Az 1. mintában csak a normál génváltozat detektálható (csak kék színű csúcs látható a nyíllal jelölt pozícióban), a 2. minta heterozigóta C/G genotípusú, azaz egyik szülőtől normál, míg a másiktól hibás génváltozatot örökölt (egy kék és egy fekete csúcs is látható a nyíllal jelölt pozícióban), a 3. mintában csak a mutáns génváltozat van jelen (csak fekete színű csúcs látható a nyíllal jelölt pozícióban) Az ábrán egy C>T báziscsere olvadáspontanalízis alapú vizsgálata látható. A C allél 71 fokon olvad, a T allél 65 fokon. A kékkel jelölt minta az olvadásgörbe alapján csak C allélt tartalmaz (71 fokon, egy csúccsal olvad), a pirossal jelölt minta heterozigóta C/T genotípusú (65 és 71 fokon, két csúccsal olvad), míg a zölddel jelölt mintában csak T allél detektálható (65 fokon, egy csúccsal olvad). 30
31 Preimplantációs Genetikai Diagnosztika A- és B típusú hemofíliában Fluoreszcens fragmenthossz analízis A fluoreszcens fragmenthossz analízist többnyire STR markerek vizsgálatához használjuk. A változó számú rövid ismétlődést hordozó régiók vizsgálatakor a régió két végpontja közötti szakaszt felsokszo- rozzuk, fluoreszcens festékkel jelöljük, és ún. kapilláris gélelekroforézis módszerrel vizsgáljuk a hosszúságát. A szakaszok hosszából következtethetünk az ismétlődések számára. Fluoreszcens fragmenthossz analízis Fent egy változó számú GT ismétlődést hordozó STR régió bázissorrendje látható. Az egyes szálakon eltér a GT ismétlődések száma, ezáltal a zölddel és pirossal határolt szakasz hossza is különbözik. Lent egy STR régió műszeres analízisét láthatjuk. A vízszintes tengelyen a hosszúság, a függőlegesen a fluoreszcens jelintenzitás látható. A két kék színű csúcs jelzi, hogy a vizsgált STR marker az egyik kromoszómán 279 bázispár, a másikon 287 bázispár hosszú (4 GT ismétlődésnek megfelelő hosszkülönbség van a két kromoszóma között). 31
32 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS A Budapesti Corvinus Egyetemen végeztem közgazdászként és egy multinacionális vállalatnál helyezkedtem el HR területen. Keszthelyi Bori önkéntes Az Egyesületben közel 10 éve szervezem és vezetem a nyári rehabilitációs gyermektáborokat. Számos alkalommal képviseltem Egyesületünket hazai és külföldi konferenciákon. Az Egyesületben végzett munkám során láthattam, hogyan szerveződik és alakul ki egy közösség, amelynek tagjait alapvetően a betegség köti össze, de túllépve a mindennapok kihívásain, mégis egy összetartó, egymást támogató csapat jön létre. A közösséghez való tartozás napjainkban egyre jobban felértékelődik hazai és nemzetközi szinten is. Olyan kapcsolatokra, ismeretségekre tehetünk szert világszerte, amelyek lehetővé teszik a gyors és hatékony információ áramlást a legújabb kutatásokról, gyógyszerekről, a betegséggel összefüggő kezelési módokról. A gyerektáborokban pedig a kezelés gyakorlása, az információátadás, és a közös élmények mellett, szinte észrevétlenül, életre szóló barátságok szövődnek. Keszthelyi Bori Magyar Hemofília Egyesület Marci mese Közel három éve a párommal eldöntöttünk egy nagyon fontos dolgot: kisbabát szeretnénk. Ezt a döntést viszonylag hamar és egyszerűen meghoztuk, csakhogy ezután egy sokkal súlyosabb kérdés következett: vállalunk-e hemofíliás babát. Én hemofília A hordozó vagyok, a súlyosabb fajtából (1% alatti faktorszintű betegséget hordozok). Tudom, hogy milyen súlyos hemofíliással együtt élni, mivel apukám érintett ebben a betegségben, komoly mozgásszervi szövődménnyel. Sokszor láttam, amikor injekciózta magát, sőt kiskoromban gyakran segítettem is neki. Ez volt a természetes, sosem merült fel bennem, hogy másképp is lehetne. Amikor elkezdtem a hemofíliás gyerektáborok szervezését, vezetését, láttam, milyen ez a betegség ma, a hemofíliás gyerekek szemével. Teljesen más. A profilaxisnak köszönhetően szinte nincs különbség a hemofíliás és a nem hemofíliás gyerekek életvitele között. Szinte... Hiszen ott vannak a hegek a kézfejen, a könyök hajlatban, és ott van a heti 2-3-szori vénázás, nem beszélve a nagyobbaknál a lelki nehézségekről. A gyerekek alapvetően elfogadják a betegséget, ehhez szoktak eddigi életük során, és megpróbálnak kihozni belőle mindent, amit csak lehet. Egy kicsit máshogyan látják ők a világot, egymást. 32
33 MARCI MESE Fontosnak éreztem, hogy a párom is lássa mindazt, amivel én együtt élek. Eljött a táborba velünk, figyelte a gyerekeket, játszott velük és rengeteget tanult tőlük. Ezek után közösen úgy döntöttünk, hogy amennyiben erre lehetőség van, belevágunk a lombik programba és kihasználjuk a modern orvostudomány adta lehetőségeket, egészséges babát szeretnénk. Nagyon fontos, hogy ezt a döntést közösen kell meghozni, hiszen együtt kell felnevelnünk a gyerekünket. Én könnyen mondom, hogy vállalom/nem vállalom, hiszen alaposan ismerem a helyzetet, egy kívülállónak ez nehezebb. Először a Géndiagnosztikai Intézetbe mentünk, ahol rögtön egy újabb döntést kellett meghoznunk, ugyanis kétféle diagnosztikai eljárás létezik. Az egyik esetben nemi szelekcióval kiválasztják a fiú embriókat (hiszen elsősorban ők lehetnek betegek), a másik esetben magára a génhibára keresnek rá és a beteg, illetve hordozó embriókat szűrik ki. Az első esetben csak lányunk lehet, a másodikban fiú is, lány is. Költségesebb eljárás, de mi a másodikat választottuk, vagyis kisfiút is szeretnénk. Ezzel párhuzamosan bejelentkeztünk a Kaáli Intézetbe TB támogatott lombik programra, ahol a várakozási idő fél év. Ezalatt számtalan vizsgálatot kellett elvégeztetni, elsősorban nekem, de a hemofília központon keresztül ez viszonylag könnyen, és nagyjából költségmentesen ment. Vannak ugyan olyan vizsgálatok, amelyeket csak magánúton lehet elvégeztetni, de ez nem jelent nagy költséget. A felkészülés során azt is figyelembe kell venni, hogy a lombik program feltétele az élettársi vagy házastársi viszony (házasságot kötni adminisztratív szempontból egyszerűbb, mint az élettársi viszony bejegyzése). Mivel konkrétan a hemofíliáért felelős génhibára voltunk kíváncsiak, a Géndiagnosztikai Intézetnek meg kellett néznie, hogy a mi családunknál hol van ez, és pontosan mi az eltérés. Így hát családosan bevonultunk az Istenhegyi úti Intézetbe, ahol mindenkitől vért vettek és megnézték, hogy hol a génhiba (eredményként egy kódsort kell elképzelni, amit leginkább R2D2 tudna kimondani). Ehhez nagy szükség van a hemofíliás rokonra is, nálunk apukámra, hiszen nála sokkal szembetűnőbb a hiba. Ez a vizsgálat is időt igényel (néhány hónap), így érdemes mielőbb elkezdeni. Közeledve a Kaáli Intézetben kapott időpontunkhoz, elkezdődtek az injekciók a szervezetem stimulálására, több héten keresztül minden este hormon injekciók, hasfalba, változatosságképpen néha tabletták is, szájon át. Volt, hogy már nagyon rosszul éreztem magam, türelmetlen voltam, és persze volt, hogy belilult a szúrás helye, jó hemofíliáshoz illően. 33
34 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Aztán csak eljött a nap, amikor leszívták a felturbózott petesejteket, szám szerint 27-et. Ezt altatásban végzik, a beavatkozási idő nagyon rövid. Nem lett mindegyik petesejtből embrió, de így is volt kiket vizsgálni. Megtermékenyítés után, 5 napos korukban mintát vettek belőlük, amit a Géndiagnosztikai Intézet vizsgált meg (a korábban említett génhibára kerestek). Ha az első esetet választottuk volna, vagyis nemi szelekcióval kiszűrik a fiúkat, akkor már 3 napos korukban vettek volna tőlük mintát. Az élet kiszámíthatatlanságai közé tartozik, hogy 15 embrióból 1 beteg fiú lett, viszont a lányok mind hordozók. Eközben újabb döntési pont: hány embriót ültessenek vissza. Mivel nálunk nem nőgyógyászati oka volt a lombik programnak, ezért azt a tanácsot kaptuk, hogy egy embrió visszaültetése javasolt. Van több egészséges fiú is az embriók között, így elsőnek fiút választottunk visszaültetésre. Esetünkben, egyrészt a magas petesejtszám, másrészt amiatt, hogy a Géndiagnosztikai Intézet által végzett vizsgálat több hónapot vesz igénybe, nem lehetett a leszívás ciklusában visszaültetni embriót. Tehát várnunk kellett még. (A nemi szelekció vizsgálata gyorsabban megvan és adott esetben lehetőség van a leszívás-megtermékenyítés ciklusában az embrió(k) visszaültetésére.) Miután megkaptuk az eredményt az embriókról, bejelentkeztünk visszaültetésre a Kaáli Intézetbe. A visszaültetéshez is kellenek hormon injekciók, de lényegesen kevesebb, mint a petesejt leszíváshoz. A visszaültetés nagyjából 3 perc, és utána fél óra pihenés következik. Hihetetlen érzés látni a pici embriót a mikroszkóp alatt közvetlenül a beültetés előtt. Csak egy pici pötty és baba lesz belőle. A többi embrió lefagyasztva várja, hogy ugyan kevéssé romantikus módon, de növekedésnek indulhassanak majd a pocakomban. Mi volt az egészben a legnehezebb? A várakozás. Várni az időpontokra, várni a helyekre, várni a vizsgálatokra, eredményekre. Várni, hogy a gyógyszerek kifejtsék a hatásukat. Néha úgy éreztük, sosem lesz vége. Emlékszem a pillanatra, amire oly régen készültünk, a bizonyos csíkok megjelenésére a terhességi teszten. Akkor éreztem azt, hogy jó úton haladunk. A terhesség nagyon jó volt, minimális rosszullét esténként, a szülés is egészen simán és gyorsan ment, de ez már egy másik történet. Aztán 9 hónappal később, amikor megszületett Marci egészségesen, tudtam, hogy megérte! (Akit további részletek érdekelnek a programmal kapcsolatban, kérdések merülnek fel benne, szívesen megválaszolom azokat, ha az egyesület címére mhe@mhe.hu levelet küld.) 34
35 HemofíLIÁS GYERMEK A CSALÁDBAN A Pécsi Orvostudományi Egyetemen summa cum laude minősítéssel szerzett általános orvosi diplomát. Végzést követően a POTE Gyermekklinikán dolgozott, ahol csecsemő- és gyermekgyógyászatból, hematológiából szakorvosi képesítést és PhD fokozatot kapott óta a Mohácsi Kórház Csecsemő- és Gyermekgyógyászati Osztályának osztályvezető főorvosa. Dr. Kardos Mária PhD osztályvezető főorvos Fő érdeklődési területe a csecsemő- és gyermekkori vérzékenység, thromboemboliák, valamint gyermekkori malignitásokhoz társuló hemosztázis zavarok, mely utóbbi PhD munkájának a témája is volt. Számos hazai és külföldi publikáció mellett több könyvfejezet, oktatófilm és elfogadott minisztériumi szakmai irányelv kidolgozója. Tagja hazai és nemzetközi tudományos szervezeteknek, és a MTA Pécsi területi Bizottsága hematológiai munkacsoportjának között vezetőségi tagként a Magyar Hemofília Egyesületben dolgozott ben Magyarországon elsőként alkalmazta és vezette be a rfviia (inj. NovoSeven) terápiát nagy inhibitor titerű, súlyos B hemofíliás gyermek kisműtétje (port a cath beültetés), majd 2001-ben jobb térdízületi synovectomiája kapcsán ban implementálta, és azóta irányítása mellett sikeresen alkalmazzák hazánkban a német gyermekgyógyászok által kidolgozott, a korábban még nem kezelt, súlyos A hemofíliás kisgyermekekben az inhibitor kialakulás csökkentését célzó korai kisdózisú, rendszeres profilaxist (Bréma- München protokoll) től szervezi a magyarországi súlyos vérzékeny betegek gyógytorna/ joint mobility programját. 35
36 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Dr. Kardos Mária PhD Mohácsi Kórház Csecsemő- és Gyermekosztály Hemofíliás gyermek a családban Felfogásom szerint melyet gondozottjaimban is mindig tudatosítok a hemofília nem hagyományos értelemben vett betegség, hanem veleszületett állapot, mely egy életre szól. Oka a véralvadás folyamatában kulcs szerepet játszó véralvadási fehérjék (VIII-as, vagy IX-es faktor) X kromoszómára lokalizálódó génjében bekövetkezett mutáció, melynek súlyossága a véralvadási faktorok termelődésének teljes vagy részleges hiányát okozza. Ennek eredménye a véralvadási folyamat elhúzódása: tehát a hemofíliásoknak is megalvad a vére, csak lassabban. A hemofília kezelésének alapja a hiányzó véralvadási faktor napjainkban még kizárólagosan intravénásan történő adása. során jelentkeznek, amikor a kisgyermek már mozgékonyabb. Döntően a nehezen felszívódó bőrvérzések a kék foltok, vagy a sérülés (esés) kapcsán kialakuló szájüregi vérzés (típusosan a felsőajak és fogíny közötti szövetsérülés) hívja fel rá a figyelmet. A közepesen súlyos, vagy enyhe formák döntően sokkal később általában baleset okozta sérülések, vagy műtétek során kerülnek felismerésre. A hemofília öröklődő kórkép, egy családon belül a generációk egymásnak átadhatják. Fontos azonban tudni, hogy az esetek %-ában újonnan kialakult genetikai hiba (mutáció) is okozhatja. Ha a szülők családjában már előfordult hemofília, a diagnózis már méhen belül, vagy megszületéskor megállapítható. Ha viszont a családban nem fordult elő, vagy nem emlékeznek rá, a súlyos hemofília tünetei általában az első életév Azok az édesanyák, akiknek családjában előfordult a hemofília aggódhatnak amiatt, hogy mi történhet babájukkal a terhesség, és különösen a szülés során. Az anyaméh és a magzatburok tökéletesen védi a magzatot, így a várandósság ideje alatt a magzat teljesen biztonságban van. Bár a normális lefolyású 36
37 HemofíLIÁS GYERMEK A CSALÁDBAN hüvelyi szülés során az anya és megszületendő vérzékeny újszülött fejének szövetei egymáshoz idomulnak, és nem okoznak sérülést (vérzést), különösen a súlyos hemofíliás újszülött biztonsága érdekében mérlegelendő a császármetszéses szülés. A szüléssel összefüggő, kezelést igénylő vérzések ritkák, mégis egy elhúzódó, nehéz szülést követően különösen központi idegrendszeri vérzés veszélyekor az újszülöttet faktorpótlásban kell részesíteni a hemofília diagnózisának megerősítését követően, vagy ha az már prenatálisan ismert volt. A szülőket még akkor is, ha már a várandósság ideje alatt ismert, vagy valószínűsíthető, hogy hemofíliás fiúnak adnak életet szinte kivétel nélkül elkeseríti, ha gyermeküknél a (súlyos) hemofília diagnosztizálásra kerül. Önmagában a betegség tényét is nehéz feldolgozni, elfogadása időbe telik. Részlet egy jelenleg 7 éves, kortársaival azonos életet élő súlyos A hemofíliás gyermek édesanyjának viszszaemlékezéséből: Amikor megtudtam, hogy a kisfiam hemofíliás beteg lett, főleg egy teljesen egészséges fiúgyermek után, egy világ omlott össze bennem, borzasztó érzés volt, azt sem tudtam, hogy mihez fogok vele kezdeni, mivel tudtam, tisztában voltam vele, hogy milyen betegséggel állunk szemben, hisz a családomban volt egy beteg Iszonyú nehéz volt elfogadni, beletörődni, hogy soha nem gyógyulhat meg. De már sikerült, túl vagyunk a nehézségeken, profilaxis mellett ugyanúgy élünk, mint más egészséges család! Amíg pici volt, iszonyúan féltettük mindentől, még a széltől is óvtuk, főleg mikor elkezdett járni tanulni, minden percben ott voltam mellette, sosem hagytam egyedül, hogy elkerüljük a balesetet. A hegyes, éles tárgyak kifejezetten nagy veszélyt jelentettek számára, és már pici korától kezdve tanítottam neki, hogy kerülje a veszélyes dolgokat, hogy ne kelljen kórházba kerülnie! Mostanra már kicsit nyugodtabb az életünk, mert hála Istennek, és a profi doktor néninek semmi gond nincs, csak vizsgálatokra, ellenőrzésekre járunk be a kórházba! :-) A diagnózis tényének ismerete után fontos, hogy a szülőkben tudatosuljon: gyermeküknek ma hazánkban biztosított az a korszerű, a vérzések kialakulását megelőző kezelés, a profilaxis, melynek révén elérhető, hogy az életminőség ne különbözzön lényegesen az egészséges kortársaktól. A tudatosításban döntő szerepe van a hemofília ellátásban jártas, nagy tapasztalattal rendelkező hematológus szakorvosnak, aki a kezelést és a gondozást végzi, irányítja. Ugyanakkor nem nélkülözhető a háziorvossal való szoros 37
38 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS kapcsolat kialakítása sem. A háziorvoson kívül, a gyereket vizsgáló orvosoknak és a fogorvosnak is tudni kell a gyermek hemofíliájáról. Kisgyermekkortól rendszeresen kell járni fogorvoshoz! A szülőkben tudatosítani kell, hogy orvoshoz kerüléskor ha nem a hemofília gondozó orvosukról van szó mindig hangsúlyozzák, hogy gyermekük vérzékenységben szenved, és faktor készítmény adását igényli! Ma a kezelés miatt csak ritkán kell a kórházba befeküdni. A kezelés járóbetegellátásban történik mindaddig, amíg a család el nem sajátítja az otthoni kezelést. Általánosságban az ajánlható, hogy a gyerekeket kezelés során sosem szabad elválasztani szüleiktől. Sokkal egyszerűbb egy gyereket úgy kezelni, hogy valamelyik szülő ölében ül. A profilaxist kontrollált otthoni kezelés (KOK) formájában javasolt folytatni, melyet megfelelő edukáció után az érintett családtagok biztonságosan, saját maguk, otthonukban tudnak végezni. Megkezdésének időpontját a vénás hozzáférés befolyásolja. 38
39 HemofíLIÁS GYERMEK A CSALÁDBAN A faktorkészítmény (plazma eredetű vagy rekombinált) biztosítása a hemofília gondozó orvos kompetenciája, a szülővel való egyeztetés alapján. Napjainkban a modern inaktiválási módszereknek köszönhetően a plazma eredetű faktorkészítmények vírus fertőzés szempontjából biztonságosak. A hemofília ellátás alapja, arany standardja a rendszeres, primér profilaxis az adott egyénre szabva. Ez az ún. személyre szabott profilaxis általában 2 éves életkor körül kezdődik, és a hemofília súlyosságán kívül főként későbbi életkorban figyelembe veszi az egyén életmódját, fizikai (sport) aktivitását is. Míg korábban a profilaxis célja a vérzések megelőzése volt, napjainkban a fő cél egyre inkább a teljes vérzésmentesség elérése, azaz az éves vérzésszám nullá - hoz közelítése. A rendszeres primér (ízületvédő) profilaxis megkezdését súlyos A hemofíliás kisgyermekben megelőzi az ún. inhibitor kialakulást megelőző profilaxis. Az inhibitorok (gátlótestek) az A és B hemofília kezelése során a beadott faktor ellen képződő ellenanyagok, melyek a molekula különböző részeihez kötődve gátolni tudják a faktor aktivitását, illetve lerövidítik annak féléletidejét a keringésben. Ennek következtében kiszámíthatatlanná, hatástalanná válik a VIII-as vagy IX-es faktorpótlás, az érintettek a véralvadás megkerülő útján ható ún. bypass kezelést igényelnek. Idézet egy inhibitoros, súlyos A hemofíliás gyermek édesanyjától: Sajnos kisfiam szervezete nem fogadta jól a 8-as faktort, ellenanyagot termelt, így inhibitoros lett, és nem hatott így a 8-as faktor. Ezek után csak akkor kaptunk faktort, NOVOSEVENT, amikor bevérzett pl. a lába, könyöke, bokája. Sokszor későn vettük észre, mert el is titkolta, hogy ne kelljen menni a kórházba. Nagyon nehéz észrevenni, mert alattomosan lassan vérzik be pl. az ízület vagy izomzat. Sok idő kellett ahhoz, hogy tudatosuljon, igenis nagyon komolyan kell venni a betegséget főleg az izom, ízület, fej vérzéseket. Először akkor ijedtünk meg, amikor 2-3 évesen beütötte a száját és a fogínye elkezdett vérezni és nem akart elállni. Az inhibitoros hemofília tehát súlyos, és költséges szövődmény, így megelőzése döntő fontosságú. Az inhibitor megelőzését célzó kezelés Magyarországon általában hónapos kor körül kezdődik és kb. 1 évig tart heti egyszeri, kis dózisú VIII-as faktor adásával, és az inhibitor képződését elősegíthető kockázati tényezők (döntően a vérzés) egyidejű kerülésével. 39
40 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS A 6-7 hónapos kortól kúszó, majd 11 hónapos kora körül felkapaszkodó és fenekére eső csecsemőkön a sérülésnek megfelelően bőrvérzések jelenhetnek meg, főként karokon, lábakon, csípőn, farpofákon, melyek csaknem mindig felületesek, mivel a zsírpárna védelmet nyújt. Bár csak ritkán fájdalmasak és veszélyesek, valamint az ízületi bevérzések is ritkák, a kúszó-mászó, totyogó kisgyermekeknek mégis ajánlott az ízületvédők (térd, boka) használata. Az ízületek bekötözése azonban kerülendő, mert izom hypotoniát (izomvesztést) és instabilitást eredményezhet. A mozgás koordináció hiánya miatt a totyogó kisgyermek gyakorta elveszítheti egyensúlyát, mely fejsérülést, következményes koponyaűri vérzést okozhat, ezért fontos a kutacsvédő használata. A későbbi életkorban is fontos a koponya védelme szorosan a fejhez illeszkedő sisakkal, különösen sportolás, vagy autóban való utazás esetén. Az utóbbi esetben fontos a biztonsági gyermekülés használata, még rövid utakon is! A hemofíliás csecsemők és kisgyermekek védőoltását subcután (bőr alá) kell adni. Az izomba történő védőoltás tilos! A fogzás, majd később a fogváltás is ugyanúgy zajlik, mint az egészséges gyermekeknél. Általában kezelést nem igénylő, kis vérzéssel járnak. A család életében az egyik legnagyszerűbb dolog, ahogy végig követheti, hogyan bontakozik ki gyermekük értelme, hogyan fedezi fel világot azáltal, hogy mindent döntően potenciálisan veszélyes dolgokat kipróbál. Nem kivétel ez alól a hemofíliás gyermek sem! A normális fejlődéshez szükség van a felfedezés ösztönző hatására, melyhez szerető biztonságos, szorongás nélküli környezetre van szükség. Ahogy a hemofíliás kisgyermek nő, meg kell tanulnia játszani, és más gyerekekkel kapcsolatot teremteni. Erre nagyon jó alkalmat teremt az óvodai környezet. Fontos azonban, hogy az óvónők, gondozónők ugyanúgy, mint később, iskolába kerüléskor az osztályfőnök, tanárok tisztában legyenek azzal, hogy óvodásuk/tanítványuk vérzékeny, és hogy az mivel jár. Saját gondozási gyakorlatomban mindig rendkívül hasznosnak bizonyult A tanítványom vérzékeny címet viselő találkozók megszervezése, ahol barátságos helyen (sohasem kórházban!) a hemofíliás gyermek és családja, a hemofília gondozó team tagjai, és az óvodapedagógusok, tanárok, testnevelő tanárok, osztályfőnökök (ha lehetőség van rá az intézmény igazgatója) kötetlen beszélgetése, kérdések-válaszok feltevése és adása kölcsönösen segíthet a vérzékenység lényegének megértésében, és abban, hogyan lehet egyensúlyt kialakítani óvodai-iskolai elvárásokkal. 40
41 HemofíLIÁS GYERMEK A CSALÁDBAN A gyermekközösségbe való kerülés után az óvodapedagógusokon, tanárokon, családtagokon kívül fontos, hogy a közösség tagjai, maguk a gyerekek is tudják, vérzékeny óvoda/iskolatársuk van. Ma Magyarországon a hemofíliások biztonságos véralvadási faktor ellátását az állam ingyenesen biztosítja. Az évente 1 főre jutó 10 NE/fő/év faktormennyiséggel az összehasonlítás alapja hazánk a fejlett hemofília ellátást nyújtó európai országok között van! Ennek köszönhetően a személyre szabott, rendszeres profilaxissal a hemofíliás gyermekek nemcsak, hogy igen ritkán hiányoznak az iskolából (döntően nem a vérzés, hanem egyéb gyermekkori betegség következtében), de napjainkban már lehetőség nyílik az iskolai testnevelésben, illetve sporttevékenységben való részvételre is. Néhány alapszabály: Hemofíliás gyermek versenyszerűen nem sportolhat (kivéve sakk)! 41
42 MAGYAR HEMOFÍLIA EGYESÜLET HEMOFÍLIA FÜZETEK MÁRCIUS Kerülni kell a küzdősportokat! Mindig egyénileg kell meghatározni, azt a sporttevékenységet, mely biztonsággal végezhető! A fizikai aktivitás és sporttevékenység sérüléssel járhat, ezért a biztonságos faktorszint mellett a megfelelő védőfelszerelésre is szükség van! Az iskolai tanulmányok magántanulóként való végzése még inhibitoros hemofíliásokban is kerülendő, nem javasolt! Az iskolában, a kortársakkal való együtt tanulás segít az emberi kapcsolatok, barátságok kialakításában, az életre szóló vérzékenységgel való együttélés elfogadásában, és a pályaválasztás megkönynyítésében. Fontos, hogy a pályaválasztás folyamata már korai tinédzserkorban megkezdődjön a tanárok, szülők és a gondozó orvosok bevonásával, szoros együttműködésével. Egy gyermek érkezése a családba az élet csodáinak egyike. Egy hemofíliás gyermek születése is ugyanolyan öröm, mint bármely más gyermeké, hiszen napjainkban megvan a lehetősége arra, hogy teljes életet éljen. Az orvos feladata a korrekt, érzelmektől mentes, a szülői döntést nem irányító, nem befolyásoló tájékoztatás. A döntés joga kizárólagosan a szülőké! Hogyan is vélekedik az egyik hemofíliás gyermek édesanyja? 42
43 HemofíLIÁS GYERMEK A CSALÁDBAN Fiúnk már 10 éves nagyfiú lett, szeret iskolába járni, szeretik az osztálytársak, védik minden akadálytól, és segítik, akárcsak a tanárok! A testvérek is segítik mindenben, nagyon jó testvérek! Apuka sokat dolgozik, de szabadidejében sokat beszélgetnek, játszanak, kirándulnak. A mi feladatunk vigyázni rá, óvni, jó útra terelni! Mindenben segíteni fogjuk örökké! Sokszor kívántam, bárcsak átvehetném a betegségét, és ő egészséges lehetne! Ha tudtam volna a terhességem alatt, hogy ilyen súlyos betegséggel születik, a sok nehézség ellenére is ugyanígy a legboldogabban vállaltam volna minden felelősséget, és újból így tennék, mert nélküle nem lenne teljes az életünk, és nagyon örülünk, hogy van egy csodálatos FIÚNK! 43
44 Honlap: Telefon: Cím: 1088 Budapest, Rákóczi út 29. Bank: Magyar Hemofília Egyesület A Magyar Hemofília Egyesület a különféle veleszületett vérzékenységben szenvedő betegek országos, közhasznú érdekvédelmi társadalmi szervezete, a Hemofília Világszövetség és az Európai Hemofília Konzorcium hivatalos magyarországi képviselője. Az egyesületet hemofíliás betegek alapították 1990-ben, jelenlegi taglétszáma hatszáz fő. Egyesületünk lassan harminc éve az orvostársadalommal együttműködve fejti ki tevékenységét az országosan egységes, egyenlő esélyeket biztosító, európai standardoknak megfelelő magas színvonalú és biztonságos faktorellátás és hemofília-gondozás megteremtése, valamint a betegek, az orvosok és a magyar társadalom felvilágosítása és képzése érdekében. Egyesületünknek fontos szerepe volt a vírusinaktivált véralvadási faktorkészítmények hazai bevezetésében, a preventív kezelés elfogadtatásában, az otthoni önkezelés bevezetésében, és a legbiztonságosabbnak tartott rekombináns készítmények térnyerésében. A Magyar Hemofília Egyesület tevékenysége: vérzékeny betegek közösségi és egyéni érdekképviselete ismeretterjesztő kiadványok, könyvek megjelentetése, edukáció, konferenciák szervezése online ismeretterjesztés, felvilágosítás a betegek és az orvosok körében ingyenes nyári rehabilitációs tábor vérzékeny gyermekeknek öninjekciózás és otthoni kezelés megtanítása otthoni gyógytorna szolgáltatás idős, mozgássérült, rászoruló hemofíliás betegeknek vérzékeny betegek összefogása, közösségi programok szervezése kezelőorvosok, gyógytornászok, nővérek munkájának támogatása, továbbképzésük elősegítése együttműködés a hazai, határon túli és külföldi betegszervezetekkel, a Hemofília Világszövetséggel és az Európai Hemofília Konzorciummal ISSN
genetikai diagnosztika IGD
 PreimPlantációs genetikai diagnosztika tartalomjegyzék I. MI A PGD? 4 II. MILYEN ESETEKBEN INDOKOLT A PGD VIZSGÁLAT ELVÉGZÉSE? 5 III. MIK A PGD ELJÁRÁS LÉPÉSEI? 6 1. GENETIKAI TANÁCSADÁS 6 2. SZAKORVOSI
PreimPlantációs genetikai diagnosztika tartalomjegyzék I. MI A PGD? 4 II. MILYEN ESETEKBEN INDOKOLT A PGD VIZSGÁLAT ELVÉGZÉSE? 5 III. MIK A PGD ELJÁRÁS LÉPÉSEI? 6 1. GENETIKAI TANÁCSADÁS 6 2. SZAKORVOSI
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály
 Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
Prenatalis diagnosztika lehetőségei mikor, hogyan, miért? Dr. Almássy Zsuzsanna Heim Pál Kórház, Budapest Toxikológia és Anyagcsere Osztály Definíció A prenatális diagnosztika a klinikai genetika azon
genetikai diagnosztika
 PreimPlantációs genetikai diagnosztika tartalomjegyzék I. MI A PD? 4 II. MILYEN ESETEKBEN INDOKOLT A PD VIZSÁLAT ELVÉZÉSE? 5 III. MIK A PD ELJÁRÁS LÉPÉSEI? 6 1. ENETIKAI TANÁCSADÁS 6 2. SZAKORVOSI KONZULTÁCIÓ
PreimPlantációs genetikai diagnosztika tartalomjegyzék I. MI A PD? 4 II. MILYEN ESETEKBEN INDOKOLT A PD VIZSÁLAT ELVÉZÉSE? 5 III. MIK A PD ELJÁRÁS LÉPÉSEI? 6 1. ENETIKAI TANÁCSADÁS 6 2. SZAKORVOSI KONZULTÁCIÓ
Genetikai szótár. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 Genetikai szótár Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A London IDEAS Genetikai Tudáspark, Egyesült Királyság szótárából módosítva. A munkát
12 Genetikai szótár Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A London IDEAS Genetikai Tudáspark, Egyesült Királyság szótárából módosítva. A munkát
Jelentés asszisztált reprodukciós eljárásokról
 Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. Az intézetek az adatszolgáltatást
Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. Az intézetek az adatszolgáltatást
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2011. évi tevékenységéről
 Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2011. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2011. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Recesszív öröklődés. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 Recesszív öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
12 Recesszív öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2010. évi tevékenységéről
 Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2010. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2010. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Embriószelekció PGD-vel genetikai terheltség esetén. Kónya Márton Istenhegyi Géndiagnosztika
 Embriószelekció PGD-vel genetikai terheltség esetén Kónya Márton Istenhegyi Géndiagnosztika A praeimplantatiós genetikai diagnosztika (PGD) a praenatalis diagnosztika legkorábbi formája, a beágyazódás
Embriószelekció PGD-vel genetikai terheltség esetén Kónya Márton Istenhegyi Géndiagnosztika A praeimplantatiós genetikai diagnosztika (PGD) a praenatalis diagnosztika legkorábbi formája, a beágyazódás
Jelentés asszisztált reprodukciós eljárásokról
 Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. A hatályos, asszisztált
Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. A hatályos, asszisztált
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI
 KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
KARNYÚJTÁSNYIRA, MAGYARORSZÁGI LABORATÓRIUMMAL KOCKÁZATMENTES GENETIKAI VIZSGÁLAT A MAGZATI KROMOSZÓMA-RENDELLENESSÉGEK KIMUTATÁSÁRA ÚJ KORSZAK A MAGZATI DIAGNOSZTIKÁBAN Ma már a várandós anya vérében
Jelentés asszisztált reprodukciós eljárásokról
 Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. A hatályos, asszisztált
Jelentés asszisztált reprodukciós eljárásokról Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet szabályozza. A hatályos, asszisztált
Jelentés asszisztált reprodukciós eljárásokat végző intézmények évi tevékenységéről
 Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2012. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2012. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
X-hez kötött öröklődés
 12 Pécsi Tudományegyetem Orvosi Genetikai Intézet H-7623 Pécs, József A.u.7. Tel.. (36)-72-535-976 Fax.: (36)-72-536-427 Honlap: www.genetics.aok.pte.hu/ Pécsi Tudományegyetem Szülészeti és Nőgyógyászati
12 Pécsi Tudományegyetem Orvosi Genetikai Intézet H-7623 Pécs, József A.u.7. Tel.. (36)-72-535-976 Fax.: (36)-72-536-427 Honlap: www.genetics.aok.pte.hu/ Pécsi Tudományegyetem Szülészeti és Nőgyógyászati
PrenaTest Újgenerációs szekvenálást és z-score
 PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
PrenaTest Újgenerációs szekvenálást és z-score számítást alkalmazó, nem-invazív prenatális molekuláris genetikai teszt a magzati 21-es triszómia észlelésére, anyai vérből végzett DNS izolálást követően
Az ember összes kromoszómája 23 párt alkot. A 23. pár határozza meg a nemünket. Ha 2 db X kromoszómánk van ezen a helyen, akkor nők, ha 1db X és 1db
 Testünk minden sejtjében megtalálhatók a kromoszómák, melyek a tulajdonságok átörökítését végzik. A testi sejtekben 2 x 23 = 46 db kromoszóma van. Az egyik sorozat apánktól, a másik anyánktól származik.
Testünk minden sejtjében megtalálhatók a kromoszómák, melyek a tulajdonságok átörökítését végzik. A testi sejtekben 2 x 23 = 46 db kromoszóma van. Az egyik sorozat apánktól, a másik anyánktól származik.
A (human)genetika alapja
 A (human)genetika alapja Genom diagnosztika - születés elött - tünetek megjelenése elött - hordozó diagnosztika Prenatalis genetikai diagnosztika indikációi emelkedett valószinüség egy gén betegségre egyik
A (human)genetika alapja Genom diagnosztika - születés elött - tünetek megjelenése elött - hordozó diagnosztika Prenatalis genetikai diagnosztika indikációi emelkedett valószinüség egy gén betegségre egyik
Genetikai szótár. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 Genetikai szótár Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A London IDEAS Genetikai Tudáspark, Egyesült Királyság szótárából módosítva. A munkát
12 Genetikai szótár Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A London IDEAS Genetikai Tudáspark, Egyesült Királyság szótárából módosítva. A munkát
A domináns öröklődés. Tájékoztató a betegek és családtagjaik számára. Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem
 12 A domináns öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
12 A domináns öröklődés Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság
Jelentés asszisztált reprodukciós eljárásokat végző intézmények évi tevékenységéről
 Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2013. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Jelentés asszisztált reprodukciós eljárásokat végző intézmények 2013. évi tevékenységéről Az asszisztált reprodukciós beavatkozásokat végző intézetek kötelező adatgyűjtését a 339/2008 (XII.30.) Kormányrendelet
Bevezetés az egészségügyi jogi ismeretekbe I. 13. hét
 Bevezetés az egészségügyi jogi ismeretekbe I. 13. hét Az emberi reprodukcióra irányuló különleges eljárások általános feltételei Emberi reprodukcióra irányuló különleges eljárásként testen kívüli megtermékenyítés
Bevezetés az egészségügyi jogi ismeretekbe I. 13. hét Az emberi reprodukcióra irányuló különleges eljárások általános feltételei Emberi reprodukcióra irányuló különleges eljárásként testen kívüli megtermékenyítés
Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra.
 Egészséges magzat, biztonságos jövő Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra. A veleszületett fejlődési
Egészséges magzat, biztonságos jövő Minden leendő szülő számára a legfontosabb, hogy születendő gyermeke egészséges legyen. A súlyosan beteg gyermek komoly terheket ró a családra. A veleszületett fejlődési
PANNON REPRODUKCIÓS INTÉZET KFT
 PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Hány
PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Hány
Példák a független öröklődésre
 GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
GENETIKAI PROBLÉMÁK Példák a független öröklődésre Az amelogenesis imperfecta egy, a fogzománc gyengeségével és elszíneződésével járó öröklődő betegség, a 4-es kromoszómán lévő enam gén recesszív mutációja
Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT
 Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT A terhességek kb. 1%-ában az újszülött teljesen egészséges szülőktől súlyos szellemi vagy testi fogyatékkal születik. A veleszületett értelmi
Tájékoztató a Down szűrésről Első trimeszteri KOMBINÁLT TESZT A terhességek kb. 1%-ában az újszülött teljesen egészséges szülőktől súlyos szellemi vagy testi fogyatékkal születik. A veleszületett értelmi
Kromoszóma transzlokációk
 16 Kromoszóma transzlokációk A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság és a London IDEAS Genetikai Tudáspark kiadványainak módosítása alapján készült a minőségbiztosítási
16 Kromoszóma transzlokációk A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság és a London IDEAS Genetikai Tudáspark kiadványainak módosítása alapján készült a minőségbiztosítási
Genomikai Medicina és Ritka Betegségek Intézete Semmelweis Egyetem
 Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
Tisztelt Hölgyem, Tisztelt Uram! Örömmel jelentjük be Önöknek, hogy a Genomikai Medicina és Ritka Betegségek Intézetének egyik új projektje azon betegségek genetikai hátterének feltérképezésére irányul,
Vizsgált kromoszóma-rendellenességek
 Vizsgált kromoszóma-rendellenességek A 21-es kromoszóma számbeli többlete okozza a Downkórt (21-es triszómia), mely a leggyakoribb, értelmi és testi fogyatékossággal járó kromoszóma-rendellenesség. Születési
Vizsgált kromoszóma-rendellenességek A 21-es kromoszóma számbeli többlete okozza a Downkórt (21-es triszómia), mely a leggyakoribb, értelmi és testi fogyatékossággal járó kromoszóma-rendellenesség. Születési
A genetikai lelet értelmezése monogénes betegségekben
 A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
A genetikai lelet értelmezése monogénes betegségekben Tory Kálmán Semmelweis Egyetem, I. sz. Gyermekklinika A ~20 ezer fehérje-kódoló gén a 23 pár kromoszómán A kromoszómán található bázisok száma: 250M
Biológiai feladatbank 12. évfolyam
 Biológiai feladatbank 12. évfolyam A pedagógus neve: A pedagógus szakja: Az iskola neve: Műveltségi terület: Tantárgy: A tantárgy cél és feladatrendszere: Tantárgyi kapcsolatok: Osztály: 12. Felhasznált
Biológiai feladatbank 12. évfolyam A pedagógus neve: A pedagógus szakja: Az iskola neve: Műveltségi terület: Tantárgy: A tantárgy cél és feladatrendszere: Tantárgyi kapcsolatok: Osztály: 12. Felhasznált
Kromoszóma rendellenességek
 16 Kromoszóma rendellenességek Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A munkát az EuroGentest támogatta, mely az Európai Unió FP6 keretprogramja
16 Kromoszóma rendellenességek Fordította: Dr. Komlósi Katalin Orvosi Genetikai Intézet, Pécsi Tudományegyetem 2009. május 15. A munkát az EuroGentest támogatta, mely az Európai Unió FP6 keretprogramja
Mi az a genetikai teszt?
 12 Mi az a genetikai teszt? Fordította: Dr. Komlósi Katalin Orvosi Genetikai és Gyermekfejlődéstani Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház kiadványainak módosítása
12 Mi az a genetikai teszt? Fordította: Dr. Komlósi Katalin Orvosi Genetikai és Gyermekfejlődéstani Intézet, Pécsi Tudományegyetem 2009. május 15. A londoni Guy s and St Thomas kórház kiadványainak módosítása
Molekuláris genetikai vizsgáló. módszerek az immundefektusok. diagnosztikájában
 Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Molekuláris genetikai vizsgáló módszerek az immundefektusok diagnosztikájában Primer immundefektusok A primer immundeficiencia ritka, veleszületett, monogénes öröklődésű immunhiányos állapot. Családi halmozódást
Hátterükben egyetlen gén áll, melynek általában számottevő a viselkedésre gyakorolt hatása, öröklési mintázata jellegzetes.
 Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
Múlt órán: Lehetséges tesztfeladatok: Kitől származik a variáció-szelekció paradigma, mely szerint az egyéni, javarészt öröklött különbségek között a társadalmi harc válogat? Fromm-Reichmann Mill Gallton
Domináns-recesszív öröklődésmenet
 Domináns-recesszív öröklődésmenet Domináns recesszív öröklődés esetén tehát a homozigóta domináns és a heterozigóta egyedek fenotípusa megegyezik, így a három lehetséges genotípushoz (példánkban AA, Aa,
Domináns-recesszív öröklődésmenet Domináns recesszív öröklődés esetén tehát a homozigóta domináns és a heterozigóta egyedek fenotípusa megegyezik, így a három lehetséges genotípushoz (példánkban AA, Aa,
Tudománytörténeti visszatekintés
 GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
GENETIKA I. AZ ÖRÖKLŐDÉS TÖRVÉNYSZERŰSÉGEI Minek köszönhető a biológiai sokféleség? Hogyan történik a tulajdonságok átörökítése? Tudománytörténeti visszatekintés 1. Keveredés alapú öröklődés: (1761-1766,
MUTÁCIÓK. A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik.
 MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
MUTÁCIÓK A mutáció az örökítő anyag spontán, maradandó megváltozása, amelynek során új genetikai tulajdonság keletkezik. Pontmutáció: A kromoszóma egy génjében pár nukleotidnál következik be változás.
A neurofibromatózis idegrendszeri megnyilvánulása
 A neurofibromatózis idegrendszeri megnyilvánulása Molekuláris Medicina Mindenkinek Fókuszban a Neurofibromatózis Varga Edina Tímea SE Genomikai Medicina és Ritka Betegségek Intézete Neurofibromatózis I.
A neurofibromatózis idegrendszeri megnyilvánulása Molekuláris Medicina Mindenkinek Fókuszban a Neurofibromatózis Varga Edina Tímea SE Genomikai Medicina és Ritka Betegségek Intézete Neurofibromatózis I.
K L A S S Z I K U S H U M Á N G E N E T I K A
 K L A S S Z I K U S H U M Á N G E N E T I K A 1 1. Családfa-analízis (Dr. Fülöp A. Kristóf) A. A családfa-ábrázolásnál használt jelölések A családfa-analízis során használt jelölések igen változatosak.
K L A S S Z I K U S H U M Á N G E N E T I K A 1 1. Családfa-analízis (Dr. Fülöp A. Kristóf) A. A családfa-ábrázolásnál használt jelölések A családfa-analízis során használt jelölések igen változatosak.
Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára. Nagy Melinda. MART VII. kongresszusa Sümeg,
 Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára Nagy Melinda MART VII. kongresszusa Sümeg, 215.5.8-9 Bevezetés Intézetünk egyik feladata a férfi infertilitás alapos kivizsgálása,
Fagyasztás, felolvasztás, preparálás hatása a humán DNS fragmentáltságára Nagy Melinda MART VII. kongresszusa Sümeg, 215.5.8-9 Bevezetés Intézetünk egyik feladata a férfi infertilitás alapos kivizsgálása,
A meddőség a páciensek szemszögéből. Borján Eszter Semmelweis Egyetem Egészségtudományi Kar Ápolástan Tanszék
 A meddőség a páciensek szemszögéből Borján Eszter Semmelweis Egyetem Egészségtudományi Kar Ápolástan Tanszék Egészség - betegség Az egészség nem csupán a betegség és nyomorékság hiánya, hanem a teljes
A meddőség a páciensek szemszögéből Borján Eszter Semmelweis Egyetem Egészségtudományi Kar Ápolástan Tanszék Egészség - betegség Az egészség nem csupán a betegség és nyomorékság hiánya, hanem a teljes
Vizsgálatkérő és adatlapok a Zalaegerszegi Területi Vérellátóban Hatályos szeptember verzió
 Vizsgálatkérő és adatlapok a Zalaegerszegi Területi Vérellátóban Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap Beküldő intézmény/osztály azonosító kódja: Nem választott vérkészítmény igénylőlap
Vizsgálatkérő és adatlapok a Zalaegerszegi Területi Vérellátóban Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap Beküldő intézmény/osztály azonosító kódja: Nem választott vérkészítmény igénylőlap
FELHASZNÁLÓI KÉZIKÖNYV
 Pécsi Tudományegyetem Klinikai Központ Az ában végzett vizsgálatokkal kapcsolatos legfontosabb információk a vizsgálatot kérők számára Készítette: Dr. Berenténé Dr. Bene Judit minőségirányítási vezető
Pécsi Tudományegyetem Klinikai Központ Az ában végzett vizsgálatokkal kapcsolatos legfontosabb információk a vizsgálatot kérők számára Készítette: Dr. Berenténé Dr. Bene Judit minőségirányítási vezető
Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje
 1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
1 Az omnipotens kutatónak, Dr. Apáti Ágotának ajánlva, egy hálás ex-őssejtje Írta és rajzolta: Hargitai Zsófia Ágota Munkában részt vett: Dr. Sarkadi Balázs, Dr. Apáti Ágota A szerkesztésben való segítségért
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM
 INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
INCZÉDY GYÖRGY SZAKKÖZÉPISKOLA, SZAKISKOLA ÉS KOLLÉGIUM Szakközépiskola Tesztlapok Biológia - egészségtan tantárgy 12. évfolyam Készítette: Perinecz Anasztázia Név: Osztály: 1. témakör: Az élet kódja.
A DOWN-KÓR SZŰRÉSE. Down-kór szűrés az egészséges babákért és a boldog kismamákért. Mi az a Down szindróma? A Down szindróma tünetei:
 A DOWN-KÓR SZŰRÉSE Kedves Kismama! Gratulálunk születendő gyermekéhez! Ön és családja bizonyára örömmel várják az újszülött érkezését, azonban a legtöbb kismamához hasonlóan Önben is felmerül, hogy a szülés
A DOWN-KÓR SZŰRÉSE Kedves Kismama! Gratulálunk születendő gyermekéhez! Ön és családja bizonyára örömmel várják az újszülött érkezését, azonban a legtöbb kismamához hasonlóan Önben is felmerül, hogy a szülés
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van.
 In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
In Situ Hibridizáció a pathologiai diagnosztikában és ami mögötte van. Kneif Józsefné PTE KK Pathologiai Intézet Budapest 2017. 05. 26 Kromoszóma rendellenesség kimutatás PCR technika: izolált nukleinsavak
1. GnRH antagonista Cetrorelix-szel szerzett tapasztalataink IVF ciklusok során
 Előadások jegyzéke Első szerzőként: 1. GnRH antagonista Cetrorelix-szel szerzett tapasztalataink IVF ciklusok során Dr. Zeke J., Kanyó K., Márta E., Dr. Konc J. III. Családcentrikus Szülészet Kongresszus
Előadások jegyzéke Első szerzőként: 1. GnRH antagonista Cetrorelix-szel szerzett tapasztalataink IVF ciklusok során Dr. Zeke J., Kanyó K., Márta E., Dr. Konc J. III. Családcentrikus Szülészet Kongresszus
mi a cukorbetegség? DR. TSCHÜRTZ NÁNDOR, DR. HIDVÉGI TIBOR
 mi a cukorbetegség? DR. TSCHÜRTZ NÁNDOR, DR. HIDVÉGI TIBOR az OkTaTÓaNyag a magyar DiabeTes Társaság vezetôsége megbízásából, a sanofi TámOgaTásával készült készítette a magyar DiabeTes Társaság edukációs
mi a cukorbetegség? DR. TSCHÜRTZ NÁNDOR, DR. HIDVÉGI TIBOR az OkTaTÓaNyag a magyar DiabeTes Társaság vezetôsége megbízásából, a sanofi TámOgaTásával készült készítette a magyar DiabeTes Társaság edukációs
XV. DOWN SZIMPÓZIUM Korszakváltás a klinikai genetikában
 XV. DOWN SZIMPÓZIUM Korszakváltás a klinikai genetikában Kötelező szinten tartó tanfolyam Szervező: A Szegedi Tudományegyetem Általános Orvostudományi Kar Orvosi Genetikai Intézete PROGRAMFÜZET Helyszín:
XV. DOWN SZIMPÓZIUM Korszakváltás a klinikai genetikában Kötelező szinten tartó tanfolyam Szervező: A Szegedi Tudományegyetem Általános Orvostudományi Kar Orvosi Genetikai Intézete PROGRAMFÜZET Helyszín:
A PKU azért nem hal ki, mert gyógyítják, és ezzel növelik a mutáns allél gyakoriságát a Huntington kór pedig azért marad fenn, mert csak későn derül
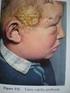 1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
1 Múlt órán: Genetikai alapelvek, monogénes öröklődés Elgondolkodtató feladat Vajon miért nem halnak ki az olyan mendeli öröklődésű rendellenességek, mint a Phenylketonuria, vagy a Huntington kór? A PKU
Humán genom variációk single nucleotide polymorphism (SNP)
 Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
Humán genom variációk single nucleotide polymorphism (SNP) A genom ~ 97 %-a két különböző egyedben teljesen azonos ~ 1% különbség: SNP miatt ~2% különbség: kópiaszámbeli eltérés, deléciók miatt 11-12 millió
DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI. 2013 szeptemberi MLDT-tagozati ülésen elhangzottak
 DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI 2013 szeptemberi MLDT-tagozati ülésen elhangzottak 21-es triszómia: Mi az a Down kór Down-kór gyakorisága: 0,13% Anya életkora (év) 20 25 30 35 40 45 49 Down-kór
DOWN-KÓR INTRAUTERIN SZŰRÉSI LEHETŐSÉGEI 2013 szeptemberi MLDT-tagozati ülésen elhangzottak 21-es triszómia: Mi az a Down kór Down-kór gyakorisága: 0,13% Anya életkora (év) 20 25 30 35 40 45 49 Down-kór
Engedélyszám: 18211-2/2011-EAHUF Verziószám: 1. 2460-06 Humángenetikai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
1. feladat Ismertesse a gyakorlaton lévő szakasszisztens hallgatóknak a PCR termékek elválasztása céljából végzett analitikai agaróz gélelektroforézis során használt puffert! Az ismertetés során az alábbi
BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben
 Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
Norvég Finanszírozási Mechanizmus által támogatott projekt mus által támogatott projekt BETEGTÁJÉKOZTATÓ Genetikai szűrés lehetőségei az Országos Onkológiai Intézetben Kedves Betegeink! A daganatokról
Rácz Olivér, Ništiar Ferenc, Hubka Beáta, Miskolci Egyetem, Egészségügyi Kar 2010
 Kromoszóma eltérések Rácz Olivér, Ništiar Ferenc, Hubka Beáta, Miskolci Egyetem, Egészségügyi Kar 2010 20.3.2010 genmisk6.ppt 1 Alapfogalmak ismétlése Csak a sejtosztódás közben láthatóak (de természetesen
Kromoszóma eltérések Rácz Olivér, Ništiar Ferenc, Hubka Beáta, Miskolci Egyetem, Egészségügyi Kar 2010 20.3.2010 genmisk6.ppt 1 Alapfogalmak ismétlése Csak a sejtosztódás közben láthatóak (de természetesen
Vizsgálatkérő és adatlapok a Soproni Területi Vérellátóban Hatályos 2009. szeptember 1-1.0. verzió
 Vizsgálatkérő és adatlapok a Soproni Területi Vérellátóban Hatályos 2009. szeptember 1-1.0. verzió 1. sz. adatlap VÁLASZTOTT VÖRÖSVÉRSEJT KÉSZÍTMÉNY IGÉNYLŐ LAP Beteg neve:... Születési neve:... Anyja
Vizsgálatkérő és adatlapok a Soproni Területi Vérellátóban Hatályos 2009. szeptember 1-1.0. verzió 1. sz. adatlap VÁLASZTOTT VÖRÖSVÉRSEJT KÉSZÍTMÉNY IGÉNYLŐ LAP Beteg neve:... Születési neve:... Anyja
BIOLÓGIA HÁZIVERSENY 1. FORDULÓ BIOKÉMIA, GENETIKA BIOKÉMIA, GENETIKA
 BIOKÉMIA, GENETIKA 1. Nukleinsavak keresztrejtvény (12+1 p) 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 1. A nukleinsavak a.-ok összekapcsolódásával kialakuló polimerek. 2. Purinvázas szerves bázis, amely az
BIOKÉMIA, GENETIKA 1. Nukleinsavak keresztrejtvény (12+1 p) 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 1. A nukleinsavak a.-ok összekapcsolódásával kialakuló polimerek. 2. Purinvázas szerves bázis, amely az
Intelligens Rendszerek Elmélete. Párhuzamos keresés genetikus algoritmusokkal
 Intelligens Rendszerek Elmélete Dr. Kutor László Párhuzamos keresés genetikus algoritmusokkal http://mobil.nik.bmf.hu/tantargyak/ire.html login: ire jelszó: IRE0 IRE / A természet általános kereső algoritmusa:
Intelligens Rendszerek Elmélete Dr. Kutor László Párhuzamos keresés genetikus algoritmusokkal http://mobil.nik.bmf.hu/tantargyak/ire.html login: ire jelszó: IRE0 IRE / A természet általános kereső algoritmusa:
Terhesgondozás, ultrahangvizsgálat Dr. Tekse István. www.szulesz-nogyogyaszt.hu
 Terhesgondozás, ultrahangvizsgálat Dr. Tekse István www.szulesz-nogyogyaszt.hu 1. Fogamzás előtti ( praeconceptionalis ) tanácsadás, gondozás 2. Kismamák gondozása a szülésig 1. A kismama és fejlődő magzatának
Terhesgondozás, ultrahangvizsgálat Dr. Tekse István www.szulesz-nogyogyaszt.hu 1. Fogamzás előtti ( praeconceptionalis ) tanácsadás, gondozás 2. Kismamák gondozása a szülésig 1. A kismama és fejlődő magzatának
Dr. Máthéné Dr. Szigeti Zsuzsanna és munkatársai
 Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Kar: TTK Tantárgy: CITOGENETIKA Kód: AOMBCGE3 ECTS Kredit: 3 A tantárgyat oktató intézet: TTK Mikrobiális Biotechnológiai és Sejtbiológiai Tanszék A tantárgy felvételére ajánlott félév: 3. Melyik félévben
Az ember szaporodása
 Az ember szaporodása Az ember szaporodásának általános jellemzése Ivaros szaporodás Ivarsejtekkel történik Ivarszervek (genitáliák) elsődleges nemi jellegek Belső ivarszervek Külső ivarszervek Váltivarúság
Az ember szaporodása Az ember szaporodásának általános jellemzése Ivaros szaporodás Ivarsejtekkel történik Ivarszervek (genitáliák) elsődleges nemi jellegek Belső ivarszervek Külső ivarszervek Váltivarúság
Chorionbiopszia. Tájékoztató a betegek és családtagjaik számára
 12 Chorionbiopszia A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak módosítása
12 Chorionbiopszia A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak módosítása
A kromoszómák kialakulása előtt a DNS állomány megkettőződik. A két azonos információ tartalmú DNS egymás mellé rendeződik és egy kromoszómát alkot.
 Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Kromoszómák, Gének A kromoszóma egy hosszú DNS szakasz, amely a sejt életének bizonyos szakaszában (a sejtosztódás előkészítéseként) tömörödik, így fénymikroszkóppal láthatóvá válik. A kromoszómák két
Mi történik a genetikai laboratóriumban?
 12 Mi történik a genetikai laboratóriumban? A brossúra elkészítéséhez segítséget nyújtottak: Dr Ian M Frayling, Orvosi Genetikai Intézet (Institute of Medical Genetics), Walesi Egyetemi Klinika (University
12 Mi történik a genetikai laboratóriumban? A brossúra elkészítéséhez segítséget nyújtottak: Dr Ian M Frayling, Orvosi Genetikai Intézet (Institute of Medical Genetics), Walesi Egyetemi Klinika (University
PRAEIMPLANTATIÓS GENETIKAI DIAGNOSZTIKA A HUMÁN REPRODUKCIÓS BIZOTTSÁG ÁLLÁSFOGLALÁSA
 PRAEIMPLANTATIÓS GENETIKAI DIAGNOSZTIKA A HUMÁN REPRODUKCIÓS BIZOTTSÁG ÁLLÁSFOGLALÁSA (Elfogadva a HRB 2008. november 17-i ülésén) I. A PGD MEGHATÁROZÁSA A praenatalis diagnosztika alkalmazásával lehetővé
PRAEIMPLANTATIÓS GENETIKAI DIAGNOSZTIKA A HUMÁN REPRODUKCIÓS BIZOTTSÁG ÁLLÁSFOGLALÁSA (Elfogadva a HRB 2008. november 17-i ülésén) I. A PGD MEGHATÁROZÁSA A praenatalis diagnosztika alkalmazásával lehetővé
Egészségügyi genetikai tesztek
 Egészségügyi genetikai tesztek MILYEN ESETBEN INDOKOLT GENETIKAI TESZTET VÉGEZNI? SZAKSZERŰ GENETIKAI TANÁCSADÁS MIRE KERES VÁLASZT A GENETIKAI TESZT? AZ ÖN DÖNTÉSE Egészségügyi genetikai tesztek Mindannyian
Egészségügyi genetikai tesztek MILYEN ESETBEN INDOKOLT GENETIKAI TESZTET VÉGEZNI? SZAKSZERŰ GENETIKAI TANÁCSADÁS MIRE KERES VÁLASZT A GENETIKAI TESZT? AZ ÖN DÖNTÉSE Egészségügyi genetikai tesztek Mindannyian
PANNON REPRODUKCIÓS INTÉZET KFT
 PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Betegtájékoztató
PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Betegtájékoztató
Kinek javasolt a genetikai tanácsadás?
 Kinek javasolt a genetikai tanácsadás? Az elmúlt években gyakori jelenség, hogy a házaspárok minden ok nélkül veszik igénybe a genetikai tanácsadást, mindössze a biztonságos családtervezés miatt. Ezekben
Kinek javasolt a genetikai tanácsadás? Az elmúlt években gyakori jelenség, hogy a házaspárok minden ok nélkül veszik igénybe a genetikai tanácsadást, mindössze a biztonságos családtervezés miatt. Ezekben
1 Egészségügyi államigazgatási szerv: Ehitv. 1. (1) bekezdése szerint: A közegészségügyi, a járványügyi, az egészségügyi igazgatási
 Az alapvető jogok biztosának Jelentése az AJB-368/2016. számú ügyben (Kapcsolódó ügy: AJB-3174/2015; 2890/2015; 3227/2015; 3362/2015; 3859/2015; 3904/2015; 4712/2015; 463/2016; 861/2016;) Előadó: dr. Kussinszky
Az alapvető jogok biztosának Jelentése az AJB-368/2016. számú ügyben (Kapcsolódó ügy: AJB-3174/2015; 2890/2015; 3227/2015; 3362/2015; 3859/2015; 3904/2015; 4712/2015; 463/2016; 861/2016;) Előadó: dr. Kussinszky
Az X kromoszóma inaktívációja. A kromatin szerkezet befolyásolja a génexpressziót
 Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
Az X kromoszóma inaktívációja A kromatin szerkezet befolyásolja a génexpressziót Férfiak: XY Nők: XX X kromoszóma: nagy méretű több mint 1000 gén Y kromoszóma: kis méretű, kevesebb, mint 100 gén Kompenzációs
VHL (von Hippel-Lindau) szindrómával élők gondozási füzete
 VHL (von Hippel-Lindau) szindrómával élők gondozási füzete A VHL szindróma egy nagyon ritka (1/100 000) örökletes genetikai rendellenesség, aminek a betegségként történő megjelenése (manifesztálódása)
VHL (von Hippel-Lindau) szindrómával élők gondozási füzete A VHL szindróma egy nagyon ritka (1/100 000) örökletes genetikai rendellenesség, aminek a betegségként történő megjelenése (manifesztálódása)
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban
 11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
11. Dr. House. Biokémiai és sejtbiológiai módszerek alkalmazása az orvoslásban HIV fertőzés kimutatása (fiktív) esettanulmány 35 éves nő, HIV fertőzöttség gyanúja. Két partner az elmúlt időszakban. Fertőzött-e
BIOLÓGIA 11. ÉVFOLYAM I. beszámoló. A genetika alaptörvényei
 BIOLÓGIA 11. ÉVFOLYAM 2015-2016. I. beszámoló A genetika alaptörvényei Ismétlés: a fehérjék fölépítése Új fogalom: gének: a DNS molekula egységei, melyek meghatározzák egy-egy tulajdonság természetét.
BIOLÓGIA 11. ÉVFOLYAM 2015-2016. I. beszámoló A genetika alaptörvényei Ismétlés: a fehérjék fölépítése Új fogalom: gének: a DNS molekula egységei, melyek meghatározzák egy-egy tulajdonság természetét.
Chorionbiopszia. Tájékoztató a betegek és családjaik számára
 12 Chorionbiopszia A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak módosítása
12 Chorionbiopszia A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak módosítása
MEGRENDELŐ TERHESGONDOZÁSI CSOMAG SZOLGÁLTATÁSHOZ
 MEGRENDELŐ TERHESGONDOZÁSI CSOMAG SZOLGÁLTATÁSHOZ páciens neve címe TAJ száma kezelőorvos neve, ha a páciens választott orvost Szüless nálunk! Otthonos és biztonságos! A MAI NAPON MEGRENDELEM A RÓBERT
MEGRENDELŐ TERHESGONDOZÁSI CSOMAG SZOLGÁLTATÁSHOZ páciens neve címe TAJ száma kezelőorvos neve, ha a páciens választott orvost Szüless nálunk! Otthonos és biztonságos! A MAI NAPON MEGRENDELEM A RÓBERT
NALP-12-Höz Társult Visszatérő Láz
 www.printo.it/pediatric-rheumatology/hu/intro NALP-12-Höz Társult Visszatérő Láz Verzió 2016 1. MI A NALP-12-HÖZ TÁRSULT VISSZATÉRŐ LÁZ 1.1 Mi ez? A NALP-12-höz társult visszatérő láz egy genetikai betegség.
www.printo.it/pediatric-rheumatology/hu/intro NALP-12-Höz Társult Visszatérő Láz Verzió 2016 1. MI A NALP-12-HÖZ TÁRSULT VISSZATÉRŐ LÁZ 1.1 Mi ez? A NALP-12-höz társult visszatérő láz egy genetikai betegség.
Mi lenne ha az MPS is része lenne az újszülöttkori tömegszűrésnek?
 Mi lenne ha az MPS is része lenne az újszülöttkori tömegszűrésnek? Dr. Jávorszky Eszter, Kánnai Piroska Dr. Szőnyi László Semmelweis Egyetem, I. Gyermekklinika, Budapest Anyagcsere szűrőközpont 2 Ritka
Mi lenne ha az MPS is része lenne az újszülöttkori tömegszűrésnek? Dr. Jávorszky Eszter, Kánnai Piroska Dr. Szőnyi László Semmelweis Egyetem, I. Gyermekklinika, Budapest Anyagcsere szűrőközpont 2 Ritka
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Általános asszisztens szakképesítés. 2375-06 Diagnosztizálás monitorozás előkészítés modul. 1.
 Nemzeti Erőforrás Minisztérium Korlátozott terjesztésű! Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Vízvári László A minősítő beosztása: főigazgató JAVÍTÁSI-ÉRTÉKELÉSI
Nemzeti Erőforrás Minisztérium Korlátozott terjesztésű! Érvényességi idő: az írásbeli vizsgatevékenység befejezésének időpontjáig A minősítő neve: Vízvári László A minősítő beosztása: főigazgató JAVÍTÁSI-ÉRTÉKELÉSI
Hordozóság szűrés. Tájékoztató a betegek és családtagjaik számára
 16 Hordozóság szűrés Köszönettel tartozunk mindazoknak, akik interjút adtak számunkra a brosúra elkészítése során. Adatvédelmi okokból az interjúalanyok neveit megváltoztattuk. A segédanyagot közreadta
16 Hordozóság szűrés Köszönettel tartozunk mindazoknak, akik interjút adtak számunkra a brosúra elkészítése során. Adatvédelmi okokból az interjúalanyok neveit megváltoztattuk. A segédanyagot közreadta
PANNON REPRODUKCIÓS INTÉZET KFT
 PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Betegtájékoztató
PANNON REPRODUKCIÓS INTÉZET KFT 8300 TAPOLCA, BARTÓK BÉLA U. 1.-3. Tel.: 06-87 510365 Fax:06-87 510366 Email: pritap@t-online.hu Honlap: www.pri.hu, www.pri.com Ügyvezető igazgató: Dr.Török Attila Betegtájékoztató
3. Általános egészségügyi ismeretek az egyes témákhoz kapcsolódóan
 11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
11. évfolyam BIOLÓGIA 1. Az emberi test szabályozása Idegi szabályozás Hormonális szabályozás 2. Az érzékelés Szaglás, tapintás, látás, íz érzéklés, 3. Általános egészségügyi ismeretek az egyes témákhoz
Az anus atresia diagnosztikája, kezelése és gondozása. Dr. Máttyus István SE I. sz. Gyermekklinika
 Az anus atresia diagnosztikája, kezelése és gondozása Dr. Máttyus István SE I. sz. Gyermekklinika Bevezető kérdés-1: melyik szerv rendellenessége nem szokott társulni anus atresiával? A. szív B. vese C.
Az anus atresia diagnosztikája, kezelése és gondozása Dr. Máttyus István SE I. sz. Gyermekklinika Bevezető kérdés-1: melyik szerv rendellenessége nem szokott társulni anus atresiával? A. szív B. vese C.
Vizsgálatkérő és adatlapok a Péterfy Területi Vérellátóban Hatályos 2011. szeptember 1-1.1. verzió
 Vizsgálatkérő és adatlapok a Péterfy Területi Vérellátóban Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap VÁLASZTOTT VÖRÖSVÉRSEJT KÉSZÍTMÉNY IGÉNYLŐ LAP Beteg neve:... Anyja neve:...... A beteg
Vizsgálatkérő és adatlapok a Péterfy Területi Vérellátóban Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap VÁLASZTOTT VÖRÖSVÉRSEJT KÉSZÍTMÉNY IGÉNYLŐ LAP Beteg neve:... Anyja neve:...... A beteg
Vizsgálatkérő és adatlapok a Szekszárdi Területi Vérellátónál Hatályos 2011. szeptember 1-1.1. verzió
 Vizsgálatkérő és adatlapok a Szekszárdi Területi Vérellátónál Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap Országos Vérellátó Szolgálat Tel./Fax.:06-74-501-628 Szekszárdi Területi Vérellátó e-mail:
Vizsgálatkérő és adatlapok a Szekszárdi Területi Vérellátónál Hatályos 2011. szeptember 1-1.1. verzió 1. sz. adatlap Országos Vérellátó Szolgálat Tel./Fax.:06-74-501-628 Szekszárdi Területi Vérellátó e-mail:
Quartett-teszt. a Down-kór, egyéb más számbeli kromoszóma-rendellenességek és az idegcsôzáródási rendellenességek kiszûrésére
 www.fetalmedicine.hu Quartett-teszt a Down-kór, egyéb más számbeli kromoszóma-rendellenességek és az idegcsôzáródási rendellenességek kiszûrésére Komplex megoldások a Down-kór szûrésében A szûrôvizsgálatot
www.fetalmedicine.hu Quartett-teszt a Down-kór, egyéb más számbeli kromoszóma-rendellenességek és az idegcsôzáródási rendellenességek kiszûrésére Komplex megoldások a Down-kór szûrésében A szûrôvizsgálatot
Genetika 2. előadás. Bevezető
 Genetika 2. előadás Genetikai alapelvek: hogyan öröklődnek a tulajdonságok Mendeli genetika Bevezető Mi okozza a hasonlóságokat és különbségeket a családtagok között? Gének: biológiai információ alapegysége
Genetika 2. előadás Genetikai alapelvek: hogyan öröklődnek a tulajdonságok Mendeli genetika Bevezető Mi okozza a hasonlóságokat és különbségeket a családtagok között? Gének: biológiai információ alapegysége
ÚJSÁGÍRÓ ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT
 ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT Dömötörfy Zsolt PÁLYÁZÓ Dömötörfy Zsolt Istenhegyi Géndiagnosztikai Centrum www.hpv-mehnyakrak.hu A méhnyakrák áldozatai Magyarországon napjainkban
ISMERETTERJESZTŐ/PROMÓCIÓS HONLAP A MÉHNYAKRÁK MEGELŐZÉSÉÉRT Dömötörfy Zsolt PÁLYÁZÓ Dömötörfy Zsolt Istenhegyi Géndiagnosztikai Centrum www.hpv-mehnyakrak.hu A méhnyakrák áldozatai Magyarországon napjainkban
Gebhardt Nóra. 12 hét. Mindent az abortuszról (azt is, amit az orvosok nem közölnek)
 Gebhardt Nóra 12 hét Mindent az abortuszról (azt is, amit az orvosok nem közölnek) Csak erős idegzetűeknek ajánlott! A könyv a nyugalom megzavarására alkalmas elemeket, felkavaró képeket tartalmaz. Előszó
Gebhardt Nóra 12 hét Mindent az abortuszról (azt is, amit az orvosok nem közölnek) Csak erős idegzetűeknek ajánlott! A könyv a nyugalom megzavarására alkalmas elemeket, felkavaró képeket tartalmaz. Előszó
Súlyos infekciók differenciálása a rendelőben. Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza
 Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
Súlyos infekciók differenciálása a rendelőben Dr. Fekete Ferenc Heim Pál Gyermekkórház Madarász utcai Gyermekkórháza Miért probléma a lázas gyermek a rendelőben? nem beteg - súlyos beteg otthon ellátható
Transzgénikus. nikus állatok. Transzgénikus nikus minden olyan állat, melynek genomja emberi közremk bejuttatott DNS-t t tartalmaz.
 Transzgénikus nikus állatok Transzgénikus nikus minden olyan állat, melynek genomja emberi közremk zremüködéssel bejuttatott DNS-t t tartalmaz. I. A KONKRÉT T GÉNSEBG NSEBÉSZETI SZETI TECHNIKA A beavatkozást
Transzgénikus nikus állatok Transzgénikus nikus minden olyan állat, melynek genomja emberi közremk zremüködéssel bejuttatott DNS-t t tartalmaz. I. A KONKRÉT T GÉNSEBG NSEBÉSZETI SZETI TECHNIKA A beavatkozást
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL
 MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
Bán Zoltán. Papp Zoltán
 Magyar Tudomány 2006/3 Prenatális és preimplantációs diagnosztika Bán Zoltán PhD, egyetemi tanársegéd, Semmelweis Egyetem Általános Orvostudományi Kar I. sz. Szülészeti és Nõgyógyászati Klinika banz@noi1.sote.hu
Magyar Tudomány 2006/3 Prenatális és preimplantációs diagnosztika Bán Zoltán PhD, egyetemi tanársegéd, Semmelweis Egyetem Általános Orvostudományi Kar I. sz. Szülészeti és Nõgyógyászati Klinika banz@noi1.sote.hu
Down-szindrómás babák születése, születés előtti kommunikáció, szűrések. Dr. Tóth Ágnes RE-PoD Záró konferencia 2014.09.25.
 Down-szindrómás babák születése, születés előtti kommunikáció, szűrések Dr. Tóth Ágnes RE-PoD Záró konferencia 2014.09.25. Mottó Egy civilizáció minőségét a leggyengébb tagjaival szemben tanúsított tisztelete
Down-szindrómás babák születése, születés előtti kommunikáció, szűrések Dr. Tóth Ágnes RE-PoD Záró konferencia 2014.09.25. Mottó Egy civilizáció minőségét a leggyengébb tagjaival szemben tanúsított tisztelete
2354-06 Nőgyógyászati citodiagnosztika követelménymodul szóbeli vizsgafeladatai
 1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek
 Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek Nagy V. Endre Endokrinológia Tanszék Debreceni Egyetem Orvos- és Egészségtudományi Centrum Belgyógyászati Intézet, I. Belklinika A pajzsmirigybetegségek
Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek Nagy V. Endre Endokrinológia Tanszék Debreceni Egyetem Orvos- és Egészségtudományi Centrum Belgyógyászati Intézet, I. Belklinika A pajzsmirigybetegségek
Vizsgálatkérő és adatlapok a Pécsi Regionális Vérellátó Központban Hatályos szeptember verzió
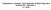 Vizsgálatkérő és adatlapok a ban Hatályos 2011. szeptember 1-1.1. verzió 1.sz. adatlap Országos Vérellátó Szolgálat Tel./Fax.:72/215-634, 211-920 IGÉNYLŐLAP NEM VÁLASZTOTT VÉRKÉSZÍTMÉNY NÉVRE SZÓLÓ IGÉNYLÉSÉHEZ
Vizsgálatkérő és adatlapok a ban Hatályos 2011. szeptember 1-1.1. verzió 1.sz. adatlap Országos Vérellátó Szolgálat Tel./Fax.:72/215-634, 211-920 IGÉNYLŐLAP NEM VÁLASZTOTT VÉRKÉSZÍTMÉNY NÉVRE SZÓLÓ IGÉNYLÉSÉHEZ
Tesztkérdések. 1 A nem fertőző betegségek halálozási aránya az európai régióban: a) 77% b) 68% c) 86%
 Tesztkérdések 1 A nem fertőző betegségek halálozási aránya az európai régióban: a) 77% b) 68% c) 86% 2. Az étkezés és az életmód megváltoztatásával milyen arányban előzhetők meg a szívérrendszeri betegségek?
Tesztkérdések 1 A nem fertőző betegségek halálozási aránya az európai régióban: a) 77% b) 68% c) 86% 2. Az étkezés és az életmód megváltoztatásával milyen arányban előzhetők meg a szívérrendszeri betegségek?
A magzatvízvizsgálat (amniocentesis)
 12 A magzatvízvizsgálat (amniocentesis) A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak
12 A magzatvízvizsgálat (amniocentesis) A londoni Guy s and St Thomas kórház, a Királyi Nőgyógyászati és Szülészeti Társaság www.rcog.org.uk/index.asp?pageid=625 és a London IDEAS Genetikai Tudáspark kiadványainak
