A Raoult és Dalton- törvényeket felhasználva kapjuk az egyensúlyi görbét (lencsegörbét), amelynek egyenlete:
|
|
|
- Márk Bodnár
- 9 évvel ezelőtt
- Látták:
Átírás
1 14. Ismertesse a desztillálási műveletek biztonságtechnikáját! - A lepárlás fogalma - A folyadékelegyek egyensúlyi viszonyainak ismertetése egy mellékelt egyensúlyi görbe használatával - Az egyensúlyi desztilláció és a rektifikálás folyamata diagram segítségével - Az egyszerű, a frakcionált, a vákuum- és a vízgőzdesztilláció berendezései - A laboratóriumi desztilláló berendezések használatának főbb szabályai - Példák a különböző desztillálási módszerek kiválasztására - Az alkalmazott védőfelszerelések I. Lepárlás (desztilláció): 1. Fogalma: folyadékelegyek szétválasztására, oldatokból a tiszta oldószer kinyerésére, folyadékok tisztítására szolgáló művelet, amely a komponensek illékonyságának különbözőségén alapul. Lepárlással olyan elegyeket választunk szét, amelyekben minden komponens illékony (ha a szétválasztásra kerülő elegy illékony és nem illékony komponenseket tartalmaz, akkor bepárlással is komponenseire választható). Az elegyet részben vagy egészben elpárologtatjuk, majd a keletkező gőzöket térben elkülönítve hűtőn átvezetve kondenzáltatjuk. Az elegyek gőzének összetétele általában nem azonos a folyadékéval, hanem az illékonyabb komponensek feldúsulnak a gőzben. A folyadékkal érintkező, vele termodinamikai egyensúlyban lévő gőzfázisban a két, vagy több, eltérő illékonyságú vegyületet tartalmazó rendszer esetén a nagyobb tenziójú (alacsonyabb forráspontú) komponens(ek) koncentrációja nagyobb, mint a folyadékban. Ezt a dúsulási lehetőséget hasznosítjuk a desztilláció (és a rektifikáció) művelete során, laboratóriumi és ipari méretekben egyaránt. A desztillációt a művelettanon belül a diffúziós vegyipari műveletek közé soroljuk. A művelet a vegyipar egyik legfontosabb szeparációs művelete: - kőolajfeldolgozás - élelmiszer és növényolajipar - gyógyszeripar - szerves anyagok desztillatív szétválasztása 2. Célja - folyadékelegyek szétválasztása alkotórészeikre - elegyekből, oldatokból anyag kinyerése. - oldószerek tisztítása II. Folyadékelegyek törvényszerűségei 1. Gőz- folyadék egyensúlyok törvényei - Raoult-törvény: egy anyag parciális nyomása (egyensúlyi gőznyomása) egyenesen arányos folyadékfázisbeli móltörtjével. p A = p A x A, ahol p A az A komponens parciális nyomása, p A a tiszta A komponens gőznyomása, x A az A komponens folyadékfázisbeli móltörtje. - Dalton-törvény: egy anyag parciális nyomása (egyensúlyi gőznyomása) egyenesen arányos gőzfázisbeli móltörtjével. p A = p Ö y A, ahol p Ö a teljes gőznyomás, y A az A komponens gőzfázisbeli móltörtje. - Konovalov I. törvénye: A gőzfázis azzal a komponenssel dúsul, amelyet a folyadékfázishoz adva a folyadék feletti gőzfázis nyomása növekszik és/vagy a folyadékelegy forráspontja csökken. Másképpen: a gőzfázis mindig az illékonyabb komponensben gazdagabb. - Konovalov II. törvénye: azeotróp elegy gőzének összetétele azonos a folyadék összetételével. Pl. 95,57% etanol-víz azeotróp elegy forráspontja 10 5 Pa nyomáson 78,2 o C, (azeotróp = változás nélkül forró). Ilyen összetétel mellet a folyadék már nem választható el, mert a kondenzátum (a gőzök cseppfolyósodásakor nyert folyadék) megtartja összetételét, desztillációs szempontból úgy viselkedik, mintha tiszta komponens lenne. 2. Illékonyság kritériuma: Az A komponens illékonyabb, mint a B: - Állandó hőmérsékleten (T=áll.). Ha az A komponens egyensúlyi gőznyomása nagyobb, mint a B komponensé. - Állandó nyomáson (p=áll.). Ha az A komponens forráspontja alacsonyabb, mint a B komponensé. - Ha az A komponens párolgáshője kisebb, mint a B komponensé. - relatív illékonyság (α i j : i-nek j-re vonatkoztatott relatív illékonysága): i j p 0 i 0 p j y y i j x x i j A Raoult és Dalton- törvényeket felhasználva kapjuk az egyensúlyi görbét (lencsegörbét), amelynek egyenlete: i j xi yi i 1 ( j 1) xi 1
2 Ábrázolva ezeket a görbéket különböző α értékek mellett: Azeotróp rendszer egyensúlyi diagramja (lencsegörbéje) Ha α=1, akkor nem lehet a két komponenst elválasztani, mert a folyadékfázisbeli összetétel megegyezik a gőzfázisbeli összetétellel. α=1 esettel találkozhatunk azeotróp elegyek képződésénél (pl: etanol víz) ahol az egyensúlyi görbe egy adott összetételnél metszi a diagonálist. Ezeket az elegyeket csak speciális desztillációs eljárásokkal, vagy kombinált műveletekkel lehet elválasztani egymástól. III. A desztilláció folyamata 1. A lepárló berendezés részei: forralóedény (kiforraló), kondenzátor (hűtő) és szedőedény(ek). 2. A lejátszódó folyamat - Az elegy elpárologtatása: ekkor a folyadék felett egy gőzfázis keletkezik. - A gőz hűtése (kondenzáltatása): a lecsapódás után a keletkező folyadékot szedőedénybe gyűjtjük. Az összegyűjtött párlat (desztillátum) összetétele közelítőleg azonos a forralóban fejlesztett gőz összetételével, de a kiindulási elegynél töményebb. - a kiindulási elegy forralóedényben maradó részét, amely túlnyomórészt a nehezebben illó komponenseket tartalmazza, desztillációs maradéknak nevezzük. 3. Probléma: egyszeri desztillálással nem lehet tökéletesen szétválasztani az alkotórészeket, mert a gőz nemcsak a kívánt forráspontú alkotórészt tartalmazza, hanem az alacsonyabb és magasabb forráspontúakat is. IV. A desztilláció fajtái 1. A műveletek száma szerint: - Egyszeri lepárlás egy műveleti egység. - Ismételt lepárlás: többször egymás után elvégzett desztillációs művelet. 2. Az áramló anyagok iránya szerint: - Egyenáramú lepárlás (egyszerű desztilláció): az elegy (vagy egy részének) elpárologtatása után a gőz egy irányban halad a hűtőn át a szedőedénybe. - Ellenáramú lepárlás (rektifikáció): a felszálló gőz a készülék hidegebb pontjain lecsapódott lefelé haladó kondenzátummal (reflux) ellentétes irányban halad. Egyszeri lepárlás lencsegörbéje 2
3 3. Üzemmódot tekintve van: - Szakaszos üzemű: a műveletek között kevesebb-több idő telik el. - Folyamatos (folytonos) üzemű: a két vagy több komponenst tartalmazó folyadékelegyet felmelegítés után, állandó áramban táplálják be egy lepárló rendszerbe és a keletkezett egyensúlyi összetételű gőz- és folyadékfázisokat folyamatosan, külön-külön elvezetik. Ezt a műveletet gyakran flash lepárlásnak is nevezik. Biner elegy szakaszos desztillációja Biner elegy folyamatos desztillációja IV. A desztilláció megvalósítása 1. Egyszeri lepárlás 1.1. Egyensúlyi desztilláció: a folyadékot forráspontra melegítjük, egy része gőzzé alakul, a gőz teljes mennyisége egész idő alatt érintkezik a folyadékkal Differenciális desztilláció: a lepárló készülékbe adott mennyiségű anyagot táplálunk be és ennek egy részét párologtatjuk el. A gőzöket elvezetjük a folyadék fölül, majd lecsapatva szedőbe gyűjtjük. 3.Az egyszeri lepárlás típusai - Egyszerű desztilláció (egyenáramú lepárlás): azt a műveletet, amelynek, során a folyadékelegyet forraljuk, a gőzeit elvezetve lehűtjük, kondenzáltatjuk, egyszerű desztillációnak nevezzük. Ha egy nem illékony, szilárd anyagot tartalmazó oldatot felforralunk, belőle az oldószermolekulák eltávoznak, az oldott anyag visszamarad a forraló edényben. Az eltávozó gőzöket hűtőben (kondenzátorban) lehűtjük, a gőz kondenzálódik, és a hűtő végen elhelyezett edényben, az un. szedőedény(ek)ben gyűlik össze a tiszta oldószer. Egyszerű desztilláló készülékek 3
4 Az egyszerű desztillációt általában két feladat megoldására használjuk: - az oldószernek nem illékony szennyeződéstől való elválasztására - kis mennyiségű, az oldószertől jelentősen eltérő forráspontú illékony szennyeződés eltávolítására Az egyszerű desztillácó során először előpárlat keletkezik. Ez követi a főpárlat elvezetése, végül az utópárlat desztillálódik át. Ezeket nem szabad összekeverni. - Kíméletes desztilláció: azokat a desztillációs műveleteket, amelyek alkalmasak az anyagok forráspont alatti hőmérsékleten való desztillációjára, kíméletes desztillációnak nevezzük. Ezt a módszert akkor alkalmazzuk, ha az anyagok hőre érzékenyek, a forráspontjuk körüli hőmérsékleten bomlanak vagy a levegőn meggyulladnak stb. A szerves vegyületek nagy része egyszerű desztillációval nem választható le a kísérő szennyező anyagoktól. A kíméletes desztillációknak két módja terjedt el: a) vákuumdesztilláció a csökkentett ( az atmoszférikusnál alacsonyabb) nyomáson végzett desztillációs művelet. A folyadékok forráspontja a külső nyomástól függ. Ha a folyadék felett csökkentjük a nyomást, a folyadék gőztenziója (egyensúlyi gőznyomása) már alacsonyabb hőmérsékleten is elérheti ezt a csökkentett nyomást: a folyadék már alacsonyabb hőmérsékleten is forrni kezd. A vákuumdesztilláció során a várható forráspontot becsléssel megállapíthatjuk. A tapasztalat szerint a nyoma s felére csökkentése a folyadék forráspontját 15 o C-kal csökkenti. - molekuláris desztilláció: számtalan hőérzékeny anyag (pl.: kőolaj- és növényolajszármazékok, vitaminok, gyógyszerhatóanyagok ) nem desztillálhatók a saját forrponti hőmérsékletükön, mert bomlást vagy károsodást szenvedhetnek (pl.: izomer átalakulás). Ezen anyagok desztillálását igen alacsony hőmérsékleten és nyomáson kell végezni, amelyre a vákuumdesztilláció alkalmas, amelynek egy különleges esete a molekuláris desztilláció. b) vivőgőzös desztilláció: nagy molekulatömegű, nem illékony anyagok gőznyomása kicsi, szobahőmérsékleten messze a külső nyomás alatt marad a tenzió értékük. Ha kis rnolekulatömegű, illékony anyag gőzét buborékoltatjuk át a folyadékon, a gőztérben a folyadék molekulái mellett nagy mennyiségben megjelennek az átbuborékoló gőzök is, és ott p V tenzió értéket alakítanak ki. A folyadékfázis felett levő gőztérben az összenyomást a tenziótörvény értelmében a két tenzió együttesen adja: p ö = p g + pv A két tenzió együttes értéke már a desztillálandó anyag forráspontjánál alacsonyabb hőmérsékleten is elérheti a külső nyomás értékét: a folyadékfázis forrni kezd. p ö = p külső Vivőgőzként olyan anyagok alkalmasak, melyek: - nem reagálnak a desztillálandó folyadékkal, - nem elegyednek a desztillálandó folyadékkal, így a gőzök kondenzálás után a vivőanyag és a desztillálandó folyadék választótölcsérben szétválasztható. - lehetőleg alacsony forráspontú, illékony anyagok - vízgőzdesztilláció: olyan desztilláció, ahol ha vivőgőzként vízgőzt használnak. A desztillálandó folyadékon átbuborékoltatott vízgőz tenziója segít elérni a külső nyomás értékét, így a magas forráspontú anyagok alacsony hőfokon is átdesztillálhatók. 2.Frakcionált desztilláció Azon ismert jelenségen alapul, hogy a gőz mindig dúsabb az illékonyabb komponensben. A frakcionált desztilláció hatékonyabb elválasztást tesz lehetővé. Az elválasztás hatásfokát azzal növelik, hogy a gőzöket hosszabb útra kényszerítik, miközben a gőz kénytelen áthaladni a már lecsapódott gőzök egy részén. A lecsapódott és folyamatosan visszacsurgó folyadékot refluxnak nevezzük. Ha a desztilláló lombikot egy feltéttel zárjuk le a hűtőhatás miatt a feltét tetején csak az illékony komponens távozik, a kevésbé illékony lecsapódik,és visszafolyik a forralólombikba. Az ilyen feltételeket frakcionáló félteteknek nevezzük. A lecsurgó folyadék és a felszálló gőzök között anyagcsere megy végbe. Az illékonyabb komponens a lecsurgó folyadék áramból a felszálló gőzáramba kerül, így a lecsurgó folyadék egyre kevesebb illékony komponenst tartalmaz. Az anyagcsere fordítva is végbemegy, így a feltét tetején távozó gőzük alig tartalmaznak nehezen illő komponenst. A frakcionáló feltétek hatásfoka jobb az egyszerű desztillálóknál, de még ezzel is csak min 10 o C forráspont-különbségű 4
5 folyadékok választhatok el. A frakcionált desztillációval több komponensű anyagokat tudunk szétválasztani. Ha a forraláskor keletkező gőzök és a reflux érintkezését fokozzuk, többkomponensű rendszerek is szétválaszthatok. 3. Ismételt lepárlás Egyszerű lepárlás esetén valójában nem válik szét a két komponens, csak megnő a keletkezett desztillátumban az illékonyabb komponens mennyisége. Ismételt lepárlásnál a desztillátumot újradeszilláljuk. Az ismételt lepárlás típusai - Egyenáramú ismételt lepárlás hátránya, hogy az újradesztillációk számának növelésével a desztillátum mennyisége csökken. - Rektifikálás= ellenáramú ismételt lepárlás A gőzből a magasabb forráspontú alkotórész egy hányada a készülék hidegebb pontjain cseppfolyósodik. A visszafolyt lefelé haladó kondenzátum (reflux) és a felfelé haladó gőz között a többszöri desztillálással egyenértékű folyamat játszódik le. Az egymással szemben haladó reflux és a gőz között komponenscsere játszódik le: a folyadék az illékonyabb komponensben elszegényedik, a gőz dúsul, mivel az alulról felfelé áramló gőzből főleg a magasabb forráspontú (kevésbé illékony) komponens kondenzálódik a lefelé folyó refluxból pedig az alacsonyabb forráspontú (illékonyabb) komponens újból elpárolog. Vagyis: a rektifikáláskor a reflux az alacsonyabb hőmérsékletű helyről a magasabb hőmérsékletű helyre vezető útján a magasabb forráspontú alkotórészeket felveszi, az alacsonyabb forráspontú alkotórészeket pedig a gőzáramnak átadja. Az eredmény: élesebb elválasztást érünk el. A rektifikáló oszlop alján és tetején eltérő összetételű elegyeket kapunk. Ezek a fenéktermék és a fejtermék. A fenékterméket az oszlop alján a magasabb hőmérséklet és a magasabb forráspontú komponens(ek) nagyobb koncentrációja jellemzi. A fejterméket az alacsonyabb hőmérséklet és a kisebb forráspontú komponens(ek) nagyobb koncentrációja jellemzi A rektifikáló berendezés lényegében több desztilláló berendezés egymásra építésével alakítható ki. Ha a berendezés forralóedényből, rektifikáló oszlopból, kondenzátorból és szedőedény(ek)ből áll, akkor ez a berendezés az ellenáramú desztilláció műveletének végrehajtására alkalmas. A reflux és a felszálló gőz közötti cserefolyamatot a bensőséges érintkeztetés elősegíti. Ezért a rektifikálás berendezései nem üresek, hanem különböző szerkezeti elemek biztosítják a felszálló gőz és a reflux bensőséges érintkeztetését. Az olyan rektifikáló oszlopot, amely különböző módon kialakított testekkel (gyűrűkkel, hengerpalástokkal, nyergekkel, csillagokkal, golyókkal stb.) van megtöltve a lecsurgó folyadék (=reflux) és a hézagokban felszálló gőz közötti komponens- és hőcsere elősegítése végett; töltetes (tölteléktestes) oszlopnak nevezzük. Ellenáramú ismételt lepárlás esetén az egyes üstökből eltávozó gőzök hőmérséklete mindig nagyobb, mint a magasabban elhelyezett szomszédos üstben az elegy forráspontja. Így lehetővé válik az egyes üstökből távozó gőz felhasználása: fűteni lehet vele a magasabban fekvő üstöt. A folyamat hátránya, hogy minden üstnél melegíteni kell, ill. hűtőt kell alkalmazni. A rektifikálás elve: 5
6 A rektifikálást a folyadékelegyek szétválasztását a gyakorlatban nem különálló üstökben, hanem ún. kolonnákban végzik. A kolonnákban az egymás fölé helyezett tányérok, (rektifikációs feltét) töltik be az üstök szerepét. A torony minden egyes tálcája úgy működik, mintha külön desztilláló berendezés lenne. A gőzök így az illékonyabb komponensben egyre dúsulnak, és a torony tetején a tiszta anyag gőzei távoznak. A rektifikálás hatékonyságát két tényező határozza meg: (1) a reflux arány és (2) a tálcák száma. Reflux arányon a szedőbe kerülő gőz és a lecsapatott gőz arányát értjük. Minél több a folyadék visszavezetés, annál tisztább lesz rektifikáló oszlop tetejéről elvezetett termék, az un. fejtermék, de annál költségesebb a művelet. Az optimális arányt kísérleti úton határozzák meg. A tálcaszám a reflux függvénye. Ha egy toronyban sok tálcát helyezünk el, egyre tisztább anyagot nyerünk, de a berendezés ára egyre drágább lesz, a művelet pedig egyre veszélyesebb. A tálcaszámot elméleti számítással és grafikus úton határozzák meg. - Deflegmáció: a valóságban a gőz összetétele a desztilláló berendezés különböző pontjaiban nem azonos a folyadékból távozó gőzzel, mert a folyadékfelülettől a hűtőig vezető úton a gőz a gőz egy része cseppfolyósodik. Természetes, hogy ezen az úton a kevésbé illékony összetevőből aránylag több cseppfolyósodik, mint az illékonyabból. Miközben tehát a gőz a folyadékfelülettől a hűtőig jut, az illékonyabb komponensben gazdagabbá válik. 4. Azeotróp desztilláció Az azeotróp desztilláció lényege, hogy a nehezen szétválasztható komponenseket (pl. azeotróp elegyet képző komponenseket) tartalmazó elegyhez olyan vegyületet adnak, amely minimális forráspontú azeotrópot képez valamelyik komponenssel. (A víz (fp.: 100,0 C) és az etanol fp.: 78,4 C minimális forráspontú (biner) azeotróp elegyet képeznek, amelynek forráspontja 78,1 C, összetétele 95,5 m/m % etanol és 4,5 m/m % víz. Harmadik komponensként benzolt adva a rendszerhez, egy 64,9 C minimális forráspontú terner azeotróp elegy (összetétel: 18,5 m/m % etanol, 7,4 m/m % víz, 74,1 m/m % benzol) és egy 68,2 C minimális forráspontú biner azeotróp elegy (összetétel: 32,4 m/m % etanol, 67,6 m/m % benzol) képződik. A desztillációs oszlopból a 64,9 C, és a 68,2 C forráspontú azeotróp elegyek fejtermékként távoznak, fenéktermékként marad a 78,4 C forráspontú abszolút etanol (benzolt nyomokban tartalmaz.)) (Aromások és nemaromások elválasztása is történhet azeotróp desztillációval. Az azeotróp desztilláció erősen poláros komponensek (pl.: alkoholok, ketonok, aminok, víz) hozzáadásával lehetővé teszi alkánok és cikloalkánok eltávolítását desztillációval; segédanyagokkal képezett alacsonyabb forráspontú azeotróp elegyek formájában. Az erősen poláros segédanyagok (mint az aceton vagy metanol) növelik a nemaromások illékonyságát (alacsonyabb forráspontú azeotrópképzéssel) és azokkal együtt desztillálnak, mint fejtermékek, míg az aromások a fenéktermékben maradnak.). 6
7 5. Extraktív desztilláció Az extraktív desztilláció lényege, hogy a desztilláló kolonnában felfelé áramló gőzökkel szemben ellenáramban egy olyan oldószer áramlik lefelé, amely a komponenseket szelektíven oldja, és így relatív illékonyságukat megnöveli. (Aromások és nemaromások elválasztása extraktív desztillációval is megvalósítható. Az extraktív desztilláció esetében (is) segédanyagot alkalmaznak az aromások és a nemaromások illékonysága közötti különbség növelésére, úgy, hogy az aromásfrakció illékonyságát csökkentik. A szelektív aromás oldószerek (pl.: poliglikolok) csökkentik az aromások illékonyságát, és azokkal együtt visszamaradnak a fenéktermékben, míg a nemaromások a fejtermékkel távoznak.) V. A desztillácio berendezései 1. Egyszerű desztilláció A desztillációs műveletek végrehajtásakor előfordulhat, hogy a folyadék a desztilláció alatt nagyon habzik. A habzást szilikon olajjal vagy habzásgátló feltéttel szoríthatjuk vissza. 2. Vákuumdesztilláció. A vákuumdesztillációs feltétek használatukkal a szedő folyamatosan, működés közben cserélhető. 7
8 3. Vízgőzdesztilláció Vízgőzfejlesztő kazánnal kibővített egyszerű desztilláló berendezés. A laboratóriumi munkában a kazánt gyakran hosszúnyakú lombikkal helyettesítik (gőzfejlesztő lombik). A nyomáskiegyenlítő cső a biztonsági szelep szerepét tölti be. Hűtésre Liebig hűtőt használunk. Vízgőzdesztillációs berendezés 4. Frakcionált desztilláció A desztilláló lombik és a szedő közé feltéteket iktatunk be. 8
9 Kétszeres vízdesztilláló berendezés 5. Rektifikálás Rektifikációs feltét 9
10 Hickmann-féle centrifugális rendszerű molekuláris desztillálókészülék VI.Desztillálási műveletek biztonságtechnikája (szerelési szabályok, desztillálás kivitelezése, alkalmazott védőfelszerelések) 1.Légköri desztillálás: Desztilláló készülék részei: - desztilláló (elpárologtató) edény páraelvezetővel, hőmérővel, - a hűtő és - szedő Nagyon tisztán és kényelmesen lehet dolgozni olyan üvegkészülékekben, amelyeket szabványos csiszolatos részekből állítanak össze. A csiszolatos készülékek szerelésekor azonban vigyázni kell arra, 10
11 hogy az egymáshoz illeszkedő csiszolatos eszközöket feszültségmentesen kell befogni, mert könnyen eltörhetnek. A lombikot félig, kétharmadáig töltjük a desztillálandó folyadékkal. A túlhevülés elkerülésére, az egyenletes forrás biztosítására még a lepárlás megkezdése előtt néhány darab forrkövet teszünk a lombikba. Ha a forrás közeli hőmérsékletű anyagba dobnánk forrkövet, akkor az felhabzik, kifuthat és égési sérülést, tüzet okozhat. Ha mégis ilyen helyzetbe kellene ezt megtenni, akkor az anyagot előbb vissza kell hűteni és úgy beadagolni a forrkövet. A hűtőbe a hűtővizet az alsó csonkon kell bevezetni, és a felsőn kivezetni, ellenkező esetben a köpeny nem telik fel, a víz a falon csak lecsorog. A gőz és a hűtővíz ellenáramú haladása tökéletesebb kondenzálást tesz lehetővé. A lepárlólombik melegítését úgy szabályozzuk, hogy a lepárlás sebessége ne legyen túl nagy. Gyors lepárlásnál a lombikban túlnyomás jön létre, aminek következtében a leolvasott hőmérséklet nem felel meg az atmoszférikus forráspontnak. A lombikba helyezett folyadékot alkalmas fürdővel vagy elektromos fűtéssel melegítjük. A desztilláció kezdetén a hőmérő higanyszála emelkedik, az ilyenkor átdesztillálódó gőzök összetétele változó. Ezt a terméket előpárlatnak nevezzük. Ha a hőmérő állandó értékre beáll, és legfeljebb csak 1 2 o C az ingadozás, új szedőbe gyűjtsük össze az un. főpárlatot. A főpárlat állandó összetételű termék. A forralás ütemét úgy válasszuk meg, hogy a szedőbe a párlat csepp/perc sebességgel csepegjen. Ha a desztillált folyadék nagyon illékony, célszerű a szedőt is hűteni. A desztilláció befejezése előtt a hőmérséklet emelkedni fog, ilyenkor az un. utópárlat desztillálódik át. Az utópárlatot ne engedjük a főpárlathoz, új szedőbe gyűjtsük össze. Előfordulhat, hogy a folyadék a desztilláció alatt nagyon habzik. A habzást vizes oldat esetén néhány csepp szilikon olajjal szoríthatjuk vissza. Ha az egyes desztillációs elegyekben a habzás veszélye fennáll, akkor a biztonság kedvéért a desztilláló lombik és a hűtő közé habzásgátló feltéteket iktatunk. A desztillálás megindulása után itt is közel állandó a hőmérséklet, amely a tiszta oldószer forráspontjánál kissé magasabb. A lepárlást úgy fejezzük be, hogy a lombikban még maradjon folyadék. Egészségre ártalmas, vagy tűzveszélyes anyag desztillálásakor légzőcsővel ellátott, zárt szedőedényt kell alkalmazni, amely a vegyifülke elszívókürtőjébe szellőzik. A desztillálás eredménye: desztilláló lombikban a maradék (tömény oldat), a szedő lombikban a párlat (illékony folyadék). 2.Vákuumdesztillálás: Csak sértetlen és jól illeszkedő berendezéseket szabad összeilleszteni, a csatlakozásoknál a feszülés nem engedhető meg. A készülékeket az esetleges széttörés esetére körül kell határolni védőlemezekkel. A vákuumot óvatosan kell rákapcsolni, el kell kerülni a hirtelen nyomásváltozást. Ugyanígy kell eljárni a megszívás megszüntetése után a levegő beengedésekor is. Így elkerülhető a gyors nyomásváltozásból származó szétrobbanás. Ha a szerelés hibátlan, a gömblombik feltölthető de csak 2/3 térfogatig, majd a kapillárist és a hőmérőt kell elhelyezni. Ezután a gömblombik alá kell helyezni a hideg fürdőt, amelyben annyi hőközlő anyagnak szabad csak lennie, hogy a szabad térfogatban elférjen a lombik széttörésekor kifolyó anyag is. A rendszer fokozatos megszívatása úgy történjék, hogy a kapillárisnál buborékolás jelentkezzen. A melegítést elkezdeni csak a kívánt vákuum beállítása után szabad. Számítani kell minden óvatosság ellenére a rendszer váratlan összeroppanására is, ezért a berendezés közelében is arcvédő pajzsot kell használni. Tűzveszélyes anyag desztillálásakor a nyílt lángot kerülni kell. Ha ez nem oldható meg, akkor az égéses kézsérülések elkerülésére, azbesztkesztyűt célszerű használni. Védeni kell a rendszert a beáramló hideg levegőtől is, de leginkább a ráfröccsenő víztől! Leálláskor ha a desztillációnak vége van, vagy más miatt abba kell hagyni, pl. áramkimaradáskor meg kell szüntetni a fűtést, el kell zárni a desztillálórendszer és a vákuumrendszer közötti csapot. A sorrendet nem szabad felcserélni. A levegőt a kapillárison keresztül lehet beengedni, nyomáskiegyenlítés céljából. Más megoldás pl. ha a vákuumrendszer tömlőjét Hoffmann- szorítóval elzárjuk, majd megbontjuk a csővezetéket és a szorító fokozatos lazításával engedünk levegőt a rendszerbe. Ujraindítás előtt az anyagot szobahőmérsékletre kell hűteni, mert könnyen felhabzik. Abban az esetben, ha szüneteltettük a folyamatot és úgy indítjuk újra, hogy a rendszer még meleg, akkor a vákuumtömlőn keresztül csak óvatosan csökkenthetjük a légnyomást, mert a meleg anyag könnyen felhabozhat a hirtelen nyomáscsökkenés következtében. Ez megoldható a szorító fokozatos lazításával, vagy úgy is, hogy a kellően hosszú gumicsövet kézzel megtörjük az indításkor és a szorítást enyhítve, befolyásoljuk a vákuum kialakulását. Csak akkor szabad a fűtést folytatni, ha a forrás normálissá válik. Az egyenletes forrás érdekében forrkő helyett a desztillálás során levegőző kapillárist használunk. A levegőző kapilláris fojtás, amin keresztül a szívott rendszerbe levegő áramolhat be.egyes esetekben a kapilláris állítható, szűkíthető ill. bővíthető. Amikor a forrás intenzitása megnő, a kapillárison keresztül beáramló levegő mennyiségét csökkenthetjük. 11
12 Ha a folyadékból kilépő gőz mennyisége megnő, a folyadékelegy kissé lehűl a forrás intenzitása csökken. A kapillárison beáramló levegő mennyiségét növelve, a folyadéktér felett a nyomás megnő, a folyadékelegy hőmérséklet is nőni fog, és a forrás intenzitása ismét megnövekszik.ily módon a gőztér nyomásának egy kis mértékű változtatásával a forrás egyenletessé tehető. A kapillárist a lombikban úgy helyezzük el, hogy annak alsó vége majdnem érintse az edény legmélyebb pontját. A vákuum alkalmazásakor nehezen oldható meg a szedőcsere, mert ilyenkor az egész berendezést vákuummentesíteni kell. Szedőfeltétek alkalmazásakor a szedő folyamatosan, működés közben cserélhető. Desztillálás alatt állandóan figyeljük a nyomásmérőt mert megváltoztatásával változik a forráspont is. A vákuumgép elé mindig tegyünk csapdát az oldószergőzök felfogására, mert azok a gépet tönkreteszik. 3.Vízgőzdesztilláció: Legtöbbször a forráspontján bomló anyagok desztillációjára, tisztítására használják. Berendezése: egy vízgőzfejlesztő kazánnal kibővített egyszerű desztilláló berendezés. A laboratóriumi munkában a kazánt gyakran hosszúnyakú lombikkal helyettesítik. A nyomáskiegyenlítő cső a biztonsági szelep szerepét tölti be. Ha a gőzbevezető cső valamilyen okból eltömődne, a gőz nem a kazánt veti szét, hanem a folyadékot nyomja ki a nyomáskiegyenlítő csövön keresztül. A vízgőzfejlesztő kazánt 2/3 részéig töltjük meg vízzel és a nyomáskiegyenlítő csövet úgy állítják be, hogy csaknem az edény fenekéig érjen. A kazánban levő víz melegítése közben megkezdjük a desztilláló berendezés összeszerelését. A kazánt csak akkor kapcsoljuk a berendezésre, ha a bevezető cső már jól átmelegedett, és a fejlődött gőz nagy része kondenzálódás nélkül áramlik ki rajta.a kondenzálódás elkerülése érdekében célszerű a desztillálandó anyagot előmelegíteni. A desztillálandó anyag tulajdonságai megszabják a desztilláló lombik alakját. A lehető legkisebb lombikot válasszuk, de a desztillálandó anyag max. 1/3-ad részét veheti csak igénybe. Habzásra hajlamos anyagokhoz hosszúnyakú lombikot használjunk. Szinte kivétel nélkül Liebig hűtőt használunk. Ha a desztillátum a hűtőben fagy, rövid időre zárjuk le a hűtővizet. A desztilláció végét az olajos fázis eltünése jelzi. A szedőből a vízzel kevert párlatot választótölcsérbe téve kettéválasztjuk. 12
Gépészeti Eljárástechnika Tanszék. Szakaszos rektifikálás mérés
 BME Gépészeti Eljárástechnika Tanszék zakaszos rektifikálás mérés Budapest, 006 1. Elméleti összefoglaló A mérés célja: laboratóriumi rektifikáló oszlopban szakaszos rektifikálás elvégzése, etanol víz
BME Gépészeti Eljárástechnika Tanszék zakaszos rektifikálás mérés Budapest, 006 1. Elméleti összefoglaló A mérés célja: laboratóriumi rektifikáló oszlopban szakaszos rektifikálás elvégzése, etanol víz
Desztilláció: gyakorló példák
 Desztilláció: gyakorló példák 1. feladat Számítsa ki egy 40 mol% benzolt és 60 mol% toluolt tartalmazó folyadékelegy egyensúlyi gőzfázisának összetételét 60 C-on! Az adott elegyre érvényes Raoult törvénye.
Desztilláció: gyakorló példák 1. feladat Számítsa ki egy 40 mol% benzolt és 60 mol% toluolt tartalmazó folyadékelegy egyensúlyi gőzfázisának összetételét 60 C-on! Az adott elegyre érvényes Raoult törvénye.
8.8. Folyamatos egyensúlyi desztilláció
 8.8. olyamatos egyensúlyi desztilláció 8.8.1. Elméleti összefoglalás olyamatos egyensúlyi desztillációnak vagy flash lepárlásnak nevezzük azt a desztillációs műveletet, amelynek során egy folyadék elegyet
8.8. olyamatos egyensúlyi desztilláció 8.8.1. Elméleti összefoglalás olyamatos egyensúlyi desztillációnak vagy flash lepárlásnak nevezzük azt a desztillációs műveletet, amelynek során egy folyadék elegyet
Gőz-folyadék egyensúly
 Gőz-folyadék egyensúly UNIFAC modell: csoport járulék módszer A UNIQUAC modellből kiindulva fejlesztették ki A molekulákat különböző csoportokból építi fel - csoportokra jellemző, mért paraméterek R és
Gőz-folyadék egyensúly UNIFAC modell: csoport járulék módszer A UNIQUAC modellből kiindulva fejlesztették ki A molekulákat különböző csoportokból építi fel - csoportokra jellemző, mért paraméterek R és
Általános és szervetlen kémia Laborelıkészítı elıadás I.
 Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Általános és szervetlen kémia Laborelıkészítı elıadás I. Halmazállapotok, fázisok Fizikai állapotváltozások (fázisátmenetek), a Gibbs-féle fázisszabály Fizikai módszerek anyagok tisztítására - Szublimáció
Kiegészítő desztillációs példa. 1. feladatsor. 2. feladatsor
 Kiegészítő desztillációs példa D3. példa: Izopropanol propanol elegy rektifikálása tányéros oszlopon 2104 kg/h 45 tömeg% izopropanol-tartalmú propanol izopropanol elegyet folyamatos üzemű rektifikáló oszlopon,
Kiegészítő desztillációs példa D3. példa: Izopropanol propanol elegy rektifikálása tányéros oszlopon 2104 kg/h 45 tömeg% izopropanol-tartalmú propanol izopropanol elegyet folyamatos üzemű rektifikáló oszlopon,
Szénhidrogén elegy rektifikálásának modellezése
 Hőmérséklet C Szénhidrogén elegy rektifikálásának modellezése 1. Elméleti összefoglalás Napjainkban a kőolaj az egyik legfontosabb bányászott és feldolgozott nyersanyag, meghatározó primer energia hordozó.
Hőmérséklet C Szénhidrogén elegy rektifikálásának modellezése 1. Elméleti összefoglalás Napjainkban a kőolaj az egyik legfontosabb bányászott és feldolgozott nyersanyag, meghatározó primer energia hordozó.
8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon.
 8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon. 8.9.1. Bevezetés. Az egyszerű, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon. 8.9.1. Bevezetés. Az egyszerű, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
Az extrakció. Az extrakció oldószerszükségletének meghatározása
 Az extrakció Az extrakció oldószerszükségletének meghatározása Az extrakció fogalma és fajtái olyan szétválasztási művelet, melynek során szilárd vagy folyadék fázisból egy vagy több komponens kioldását
Az extrakció Az extrakció oldószerszükségletének meghatározása Az extrakció fogalma és fajtái olyan szétválasztási művelet, melynek során szilárd vagy folyadék fázisból egy vagy több komponens kioldását
Technológiai hulladékvizek kezelése fiziko-kémiai módszerekkel a körforgásos gazdaság jegyében
 Technológiai hulladékvizek kezelése fiziko-kémiai módszerekkel a körforgásos gazdaság jegyében Ipari Szennyvíztisztítás Szakmai Nap Budapest, 2017. 11. 30. Mizsey Péter 1,2, Tóth András József 1, Haáz
Technológiai hulladékvizek kezelése fiziko-kémiai módszerekkel a körforgásos gazdaság jegyében Ipari Szennyvíztisztítás Szakmai Nap Budapest, 2017. 11. 30. Mizsey Péter 1,2, Tóth András József 1, Haáz
Kémia fogorvostan hallgatóknak Munkafüzet 3. hét
 Kémia fogorvostan hallgatóknak Munkafüzet 3. hét Desztillálás, vákuumbepárlás, liofilizálás (Gyakorlatos jegyzet: 17-35. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás,
Kémia fogorvostan hallgatóknak Munkafüzet 3. hét Desztillálás, vákuumbepárlás, liofilizálás (Gyakorlatos jegyzet: 17-35. o.) Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus Péter, Lóránd Tamás,
8. Gőz-folyadék egyensúly tanulmányozása kétkomponensű elegyekben. Előkészítő előadás 2015.02.09.
 8. Gőz-folyadék egyensúly tanulmányozása kétkomponensű elegyekben Előkészítő előadás 2015.02.09. Elméleti áttekintés Gőznyomás: adott hőmérsékleten egy anyag folyadék fázisával egyensúlyt tartó gőzének
8. Gőz-folyadék egyensúly tanulmányozása kétkomponensű elegyekben Előkészítő előadás 2015.02.09. Elméleti áttekintés Gőznyomás: adott hőmérsékleten egy anyag folyadék fázisával egyensúlyt tartó gőzének
A jegyzőkönyvvezetés formai és tartalmi követelményei
 A jegyzőkönyvvezetés formai és tartalmi követelményei A szerves kémiai laboratóriumi gyakorlatokon irodalmi leírás szerint a kiindulási anyagokból a reakciót végrehajtva, a feldolgozás lépései után kapjuk
A jegyzőkönyvvezetés formai és tartalmi követelményei A szerves kémiai laboratóriumi gyakorlatokon irodalmi leírás szerint a kiindulási anyagokból a reakciót végrehajtva, a feldolgozás lépései után kapjuk
ZÁRÓJELENTÉS Újtípusú félfolyamatos szétválasztó műveletek, OTKA T (4 év) Témavezető: Rév Endre
 ZÁRÓJLNTÉS Újtípusú félfolyamatos szétválasztó műveletek, OTK T 037191 (4 év) Témavezető: Rév ndre lsősorban a szakaszos extraktív desztilláció különféle változatait vizsgáltuk, beleértve a kulcskomponensek
ZÁRÓJLNTÉS Újtípusú félfolyamatos szétválasztó műveletek, OTK T 037191 (4 év) Témavezető: Rév ndre lsősorban a szakaszos extraktív desztilláció különféle változatait vizsgáltuk, beleértve a kulcskomponensek
BEPÁRLÁS. A bepárlás előkészítő művelet is lehet, pl. porlasztva szárításhoz, kristályosításhoz.
 Bepárlás fogalma: Az olyan oldatok esetében amelyekben az oldott anyag gőztenziója gyakorlatilag nulla, az oldatot forrásban tartva, párologtatással az oldószer eltávolítható, az oldat besűríthető. Az
Bepárlás fogalma: Az olyan oldatok esetében amelyekben az oldott anyag gőztenziója gyakorlatilag nulla, az oldatot forrásban tartva, párologtatással az oldószer eltávolítható, az oldat besűríthető. Az
8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon.
 8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon. 8.9.1. Bevezetés Az egyszerű, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
8.9. Folyamatos rektifikálás vizsgálata félüzemi méretű rektifikáló oszlopon. 8.9.1. Bevezetés Az egyszerű, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
1. feladat Összesen 8 pont. 2. feladat Összesen 18 pont
 1. feladat Összesen 8 pont Az ábrán egy szállítóberendezést lát. A) Nevezze meg a szállítóberendezést!... B) Milyen elven működik a berendezés?... C) Nevezze meg a szállítóberendezést számokkal jelölt
1. feladat Összesen 8 pont Az ábrán egy szállítóberendezést lát. A) Nevezze meg a szállítóberendezést!... B) Milyen elven működik a berendezés?... C) Nevezze meg a szállítóberendezést számokkal jelölt
Olefingyártás indító lépése
 PIROLÍZIS Olefingyártás indító lépése A legnagyobb mennyiségben gyártott olefinek: az etilén és a propilén. Az etilén éves világtermelése mintegy 120 millió tonna. Hazánkban a TVK-nál folyik olefingyártás.
PIROLÍZIS Olefingyártás indító lépése A legnagyobb mennyiségben gyártott olefinek: az etilén és a propilén. Az etilén éves világtermelése mintegy 120 millió tonna. Hazánkban a TVK-nál folyik olefingyártás.
Oldatok - elegyek. Elegyek: komponensek mennyisége azonos nagyságrendű
 Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
SZAKASZOS REKTIFIKÁLÁS
 SZAKASZOS REKTIFIKÁLÁS mérési segédlet Mérés helyszíne: Stokes Laboratórium Ellenőrizte: Dr. Hégely László Készítette: Deák Gábor, Kádár Péter, Tőzsér Eszter, Verrasztó László Budapest, 2018.05.17. Budapesti
SZAKASZOS REKTIFIKÁLÁS mérési segédlet Mérés helyszíne: Stokes Laboratórium Ellenőrizte: Dr. Hégely László Készítette: Deák Gábor, Kádár Péter, Tőzsér Eszter, Verrasztó László Budapest, 2018.05.17. Budapesti
Folyamattan gyakorlat. 2017/ félév BME-KKFT Készítette: Stelén Gábor
 Folyamattan gyakorlat 2017/18. 1. félév BME-KKFT Készítette: Stelén Gábor 1 Gőz-folyadék egyensúly Folyadékelegyek szétválasztása rektifikálás Szükségesek a gőz-folyadék egyensúlyi adatok Ideális elegyek
Folyamattan gyakorlat 2017/18. 1. félév BME-KKFT Készítette: Stelén Gábor 1 Gőz-folyadék egyensúly Folyadékelegyek szétválasztása rektifikálás Szükségesek a gőz-folyadék egyensúlyi adatok Ideális elegyek
Előadó: Varga Péter Varga Péter
 Abszorpciós folyadékhűtők Abszorpciós folyadékhűtők alkalmazási lehetőségei alkalmazási lehetőségei a termálvizeink világában a termálvizeink világában Előadó: Varga Péter Varga Péter ABSZORPCIÓS FOLYADÉKHŰTŐ
Abszorpciós folyadékhűtők Abszorpciós folyadékhűtők alkalmazási lehetőségei alkalmazási lehetőségei a termálvizeink világában a termálvizeink világában Előadó: Varga Péter Varga Péter ABSZORPCIÓS FOLYADÉKHŰTŐ
Fázisátalakulások. A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek.
 Fázisátalakulások A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek. Fából vaskarika?? K Vizes kalapács Ha egy tartályban a folyadék fölötti térrészből
Fázisátalakulások A víz fázisai. A nem közönséges (II-VIII) jég kristálymódosulatok csak több ezer bar nyomáson jelentkeznek. Fából vaskarika?? K Vizes kalapács Ha egy tartályban a folyadék fölötti térrészből
Hütökészülékek. Oktatás - II. rész. BUDAPEST - Attila Kovács. ESSE - Wilhelm Nießen
 Hütökészülékek Oktatás - II. rész 1 Hömérséklet Mi az a hideg? 2 Hömérséklet Fizikailag a hideg kifejezés nem helyes. Csak hö-röl beszélhetünk. A hö az energia egy formája. Minden anyag rendelkezik több
Hütökészülékek Oktatás - II. rész 1 Hömérséklet Mi az a hideg? 2 Hömérséklet Fizikailag a hideg kifejezés nem helyes. Csak hö-röl beszélhetünk. A hö az energia egy formája. Minden anyag rendelkezik több
8. oldaltól folytatni
 TARTÁLY ÉS TORONY JELLEGŰ KÉSZÜLÉKEK KIVÁLASZTÁSA, MEGHIBÁSODÁSA, KARBANTARTÁSA 8. oldaltól folytatni 2015.09.15. Németh János Tartály jellegű készülékek csoportosítása A készülékekben uralkodó maximális
TARTÁLY ÉS TORONY JELLEGŰ KÉSZÜLÉKEK KIVÁLASZTÁSA, MEGHIBÁSODÁSA, KARBANTARTÁSA 8. oldaltól folytatni 2015.09.15. Németh János Tartály jellegű készülékek csoportosítása A készülékekben uralkodó maximális
Folyadékok és szilárd anyagok sűrűségének meghatározása különböző módszerekkel
 Folyadékok és szilárd anyagok sűrűségének meghatározása különböző módszerekkel Név: Neptun kód: _ mérőhely: _ Labor előzetes feladatok 20 C-on különböző töménységű ecetsav-oldatok sűrűségét megmérve az
Folyadékok és szilárd anyagok sűrűségének meghatározása különböző módszerekkel Név: Neptun kód: _ mérőhely: _ Labor előzetes feladatok 20 C-on különböző töménységű ecetsav-oldatok sűrűségét megmérve az
8.9. Folyamatos rektifikálás vizsgálata félüzemi mérető rektifikáló oszlopon.
 8.9. Folyamatos rektifikálás vizsgálata félüzemi mérető rektifikáló oszlopon. 8.9.1. Bevezetés. Az egyszerő, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
8.9. Folyamatos rektifikálás vizsgálata félüzemi mérető rektifikáló oszlopon. 8.9.1. Bevezetés. Az egyszerő, egyfokozatú reflux nélküli desztillációnál az elválasztás egyetlen egyensúlyi fokozatnak felel
Művelettan 3 fejezete
 Művelettan 3 fejezete Impulzusátadás Hőátszármaztatás mechanikai műveletek áramlástani műveletek termikus műveletek aprítás, osztályozás ülepítés, szűrés hűtés, sterilizálás, hőcsere Komponensátadás anyagátadási
Művelettan 3 fejezete Impulzusátadás Hőátszármaztatás mechanikai műveletek áramlástani műveletek termikus műveletek aprítás, osztályozás ülepítés, szűrés hűtés, sterilizálás, hőcsere Komponensátadás anyagátadási
Fiziko-kémiai módszerek a finomkémiai ipar hulladékvizeinek kezelésére
 Fiziko-kémiai módszerek a finomkémiai ipar hulladékvizeinek kezelésére Környezettudományi Doktori Iskolák Konferenciája 2012. 08. 31. Tóth András József 1 Dr. Mizsey Péter 1, 2 andras86@kkft.bme.hu 1 Kémiai
Fiziko-kémiai módszerek a finomkémiai ipar hulladékvizeinek kezelésére Környezettudományi Doktori Iskolák Konferenciája 2012. 08. 31. Tóth András József 1 Dr. Mizsey Péter 1, 2 andras86@kkft.bme.hu 1 Kémiai
1. feladat Összesen 17 pont
 1. feladat Összesen 17 pont Két tartály közötti folyadékszállítást végzünk. Az ábrán egy centrifugál szivattyú- és egy csővezetéki (terhelési) jelleggörbe látható. A jelleggörbe alapján válaszoljon az
1. feladat Összesen 17 pont Két tartály közötti folyadékszállítást végzünk. Az ábrán egy centrifugál szivattyú- és egy csővezetéki (terhelési) jelleggörbe látható. A jelleggörbe alapján válaszoljon az
Oldatok - elegyek. Többkomponensű homogén (egyfázisú) rendszerek. Elegyek: komponensek mennyisége azonos nagyságrendű
 Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
Oldatok - elegyek Többkomponensű homogén (egyfázisú) rendszerek Elegyek: komponensek mennyisége azonos nagyságrendű Oldatok: egyik komponens mennyisége nagy (oldószer) a másik, vagy a többihez (oldott
(2006. október) Megoldás:
 1. Állandó hőmérsékleten vízgőzt nyomunk össze. Egy adott ponton az edény alján víz kezd összegyűlni. A gőz nyomását az alábbi táblázat mutatja a térfogat függvényében. a)ábrázolja nyomás-térfogat grafikonon
1. Állandó hőmérsékleten vízgőzt nyomunk össze. Egy adott ponton az edény alján víz kezd összegyűlni. A gőz nyomását az alábbi táblázat mutatja a térfogat függvényében. a)ábrázolja nyomás-térfogat grafikonon
Lemezeshőcserélő mérés
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM GÉPÉSZMÉRNÖKI KAR Épületgépészeti és Gépészeti Eljárástechnika Tanszék Lemezeshőcserélő mérés Hallgatói mérési segédlet Budapest, 2014 1. A hőcserélők típusai
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM GÉPÉSZMÉRNÖKI KAR Épületgépészeti és Gépészeti Eljárástechnika Tanszék Lemezeshőcserélő mérés Hallgatói mérési segédlet Budapest, 2014 1. A hőcserélők típusai
Folyadékok. Molekulák: Gázok Folyadékok Szilárd anyagok. másodrendű kölcsönhatás növekszik. cseppfolyósíthatók hűtéssel és/vagy nyomással
 Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Mekkora az égés utáni elegy térfogatszázalékos összetétele
 1) PB-gázelegy levegőre 1 vonatkoztatott sűrűsége: 1,77. Hányszoros térfogatú levegőben égessük, ha 1.1. sztöchiometrikus mennyiségben adjuk a levegőt? 1.2. 100 % levegőfelesleget alkalmazunk? Mekkora
1) PB-gázelegy levegőre 1 vonatkoztatott sűrűsége: 1,77. Hányszoros térfogatú levegőben égessük, ha 1.1. sztöchiometrikus mennyiségben adjuk a levegőt? 1.2. 100 % levegőfelesleget alkalmazunk? Mekkora
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
- anyagmérlegek felírása a szakaszos üzemű berendezés teljes üzemidejére;
 Szakaszos rektifikálás üveg harangtányéros kolonnán A laboratóriumi méretű, üveg harangtányérokkal ellátott rektifikáló kolonnán heptán-toluol elegy szétválasztásának vizsgálata, valamint az oszlop hatásfokának
Szakaszos rektifikálás üveg harangtányéros kolonnán A laboratóriumi méretű, üveg harangtányérokkal ellátott rektifikáló kolonnán heptán-toluol elegy szétválasztásának vizsgálata, valamint az oszlop hatásfokának
1. feladat Összesen 25 pont
 1. feladat Összesen 25 pont Centrifugál szivattyúval folyadékot szállítunk az 1 jelű, légköri nyomású tartályból a 2 jelű, ugyancsak légköri nyomású tartályba. A folyadék sűrűsége 1000 kg/m 3. A nehézségi
1. feladat Összesen 25 pont Centrifugál szivattyúval folyadékot szállítunk az 1 jelű, légköri nyomású tartályból a 2 jelű, ugyancsak légköri nyomású tartályba. A folyadék sűrűsége 1000 kg/m 3. A nehézségi
5. Laboratóriumi gyakorlat
 5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Ni 2+ Reakciósebesség mol. A mérés sorszáma
 1. feladat Összesen 10 pont Egy kén-dioxidot és kén-trioxidot tartalmazó gázelegyben a kén és oxigén tömegaránya 1,0:1,4. A) Számítsa ki a gázelegy térfogatszázalékos összetételét! B) Számítsa ki 1,0 mol
1. feladat Összesen 10 pont Egy kén-dioxidot és kén-trioxidot tartalmazó gázelegyben a kén és oxigén tömegaránya 1,0:1,4. A) Számítsa ki a gázelegy térfogatszázalékos összetételét! B) Számítsa ki 1,0 mol
doktori (Ph.D.) értekezés
 Kótai Barnabás Szakaszos extraktív és azeotrop desztilláció optimális tervezése doktori (Ph.D.) értekezés Témavezető: Dr. Láng Péter Budapesti Műszaki és Gazdaságtudományi Egyetem 2008 - 2 - TARTALOMJEGYZÉK
Kótai Barnabás Szakaszos extraktív és azeotrop desztilláció optimális tervezése doktori (Ph.D.) értekezés Témavezető: Dr. Láng Péter Budapesti Műszaki és Gazdaságtudományi Egyetem 2008 - 2 - TARTALOMJEGYZÉK
Többjáratú hőcserélő 3
 Hőcserélők Q = k*a*δt (a szoftver U-val jelöli a hőátbocsátási tényezőt) Ideális hőátadás Egy vagy két bemenetű hőcserélő Egy bemenet: egyszerű melegítőként/hűtőként funkcionál Design mód: egy specifikáció
Hőcserélők Q = k*a*δt (a szoftver U-val jelöli a hőátbocsátási tényezőt) Ideális hőátadás Egy vagy két bemenetű hőcserélő Egy bemenet: egyszerű melegítőként/hűtőként funkcionál Design mód: egy specifikáció
Folyadékok. Molekulák: Gázok Folyadékok Szilárd anyagok. másodrendű kölcsönhatás növekszik. cseppfolyósíthatók hűtéssel és/vagy nyomással
 Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Folyadékok Molekulák: másodrendű kölcsönhatás növekszik Gázok Folyadékok Szilárd anyagok cseppfolyósíthatók hűtéssel és/vagy nyomással Folyadékok Molekulák közti összetartó erők: Másodlagos kötőerők: apoláris
Desztilláció. Tartalomjegyzék. A Wikipédiából, a szabad enciklopédiából.
 Page 1 of 10 Desztilláció A Wikipédiából, a szabad enciklopédiából. A Desztilláció vagy lepárlás egyrészt egy régóta óta használt laboratóriumi technika, másrészt a kémiai ipar folyadékelegyeinek leggyakrabban
Page 1 of 10 Desztilláció A Wikipédiából, a szabad enciklopédiából. A Desztilláció vagy lepárlás egyrészt egy régóta óta használt laboratóriumi technika, másrészt a kémiai ipar folyadékelegyeinek leggyakrabban
A 27/2012 (VIII. 27.) NGM rendelet (12/2013 (III.28) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján.
 A 27/2012 (VIII. 27.) NGM rendelet (12/2013 (III.28) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. 54 524 01 Laboratóriumi technikus Tájékoztató A vizsgázó az első lapra írja fel
A 27/2012 (VIII. 27.) NGM rendelet (12/2013 (III.28) NGM rendelet által módosított) szakmai és vizsgakövetelménye alapján. 54 524 01 Laboratóriumi technikus Tájékoztató A vizsgázó az első lapra írja fel
2018. MAGYAR KERESKEDELMI ÉS IPARKAMARA. Országos Szakmai Tanulmányi Verseny. Elődöntő KOMPLEX ÍRÁSBELI FELADATSOR MEGOLDÁSA.
 MAGYAR KERESKEDELMI ÉS IPARKAMARA Országos Szakmai Tanulmányi Verseny Elődöntő KOMPLEX ÍRÁSBELI FELADATSOR MEGOLDÁSA Szakképesítés: SZVK rendelet száma: Komplex írásbeli: Vegyipari műszaki feladatok Elérhető
MAGYAR KERESKEDELMI ÉS IPARKAMARA Országos Szakmai Tanulmányi Verseny Elődöntő KOMPLEX ÍRÁSBELI FELADATSOR MEGOLDÁSA Szakképesítés: SZVK rendelet száma: Komplex írásbeli: Vegyipari műszaki feladatok Elérhető
1. feladat Összesen 21 pont
 1. feladat Összesen 21 pont A) Egészítse ki az alábbi, B feladatrészben látható rajzra vonatkozó mondatokat! Az ábrán egy működésű szivattyú látható. Az betűk a szivattyú nyomócsonkjait, a betűk pedig
1. feladat Összesen 21 pont A) Egészítse ki az alábbi, B feladatrészben látható rajzra vonatkozó mondatokat! Az ábrán egy működésű szivattyú látható. Az betűk a szivattyú nyomócsonkjait, a betűk pedig
Elegyek. Csonka Gábor 2008 Általános Kémia: oldatok 1 dia
 Elegyek 7-1 Elegyek fajtái 7-2 Koncentrációk 7-3 Intermolekuláris erők, az elegyedés folyamata 7-4 Elegyek keletkezése, egyensúly 7-5 Gázok oldhatósága 7-6 Elegyek gőznyomása 7-7 Ozmózis nyomás 7-8 Fagyáspont
Elegyek 7-1 Elegyek fajtái 7-2 Koncentrációk 7-3 Intermolekuláris erők, az elegyedés folyamata 7-4 Elegyek keletkezése, egyensúly 7-5 Gázok oldhatósága 7-6 Elegyek gőznyomása 7-7 Ozmózis nyomás 7-8 Fagyáspont
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Elegyek, ldatk A bemutatót összeállíttta: Fgarasi József, Petrik ajs SZKI, 20 Elegyek fgalma Elegyek az lyan hmgén, többkmpnensű rendszerek, amelyekben az alktórészek arányát tetszőlegesen váltztathatjuk
Elegyek, ldatk A bemutatót összeállíttta: Fgarasi József, Petrik ajs SZKI, 20 Elegyek fgalma Elegyek az lyan hmgén, többkmpnensű rendszerek, amelyekben az alktórészek arányát tetszőlegesen váltztathatjuk
100 o C víz forrása 212 o F 0 o C víz olvadása 32 o F T F = 9/5 T C Példák: 37 o C (láz) = 98,6 o F 40 o C = 40 o F 20 o C = 68 o F
 III. HőTAN 1. A HŐMÉSÉKLET ÉS A HŐ Látni fogjuk: a mechanika fogalmai jelennek meg mikroszkópikus szinten 1.1. A hőmérséklet Mindennapi általános tapasztalatunk van. Termikus egyensúly a résztvevők hőmérséklete
III. HőTAN 1. A HŐMÉSÉKLET ÉS A HŐ Látni fogjuk: a mechanika fogalmai jelennek meg mikroszkópikus szinten 1.1. A hőmérséklet Mindennapi általános tapasztalatunk van. Termikus egyensúly a résztvevők hőmérséklete
Méréstechnika. Hőmérséklet mérése
 Méréstechnika Hőmérséklet mérése Hőmérséklet: A hőmérséklet a termikus kölcsönhatáshoz tartozó állapotjelző. A hőmérséklet azt jelzi, hogy egy test hőtartalma milyen szintű. Amennyiben két eltérő hőmérsékletű
Méréstechnika Hőmérséklet mérése Hőmérséklet: A hőmérséklet a termikus kölcsönhatáshoz tartozó állapotjelző. A hőmérséklet azt jelzi, hogy egy test hőtartalma milyen szintű. Amennyiben két eltérő hőmérsékletű
Égéshő: Az a hőmennyiség, amely normál állapotú száraz gáz, levegő jelenlétében CO 2
 Perpetuum mobile?!? Égéshő: Az a hőmennyiség, amely normál állapotú száraz gáz, levegő jelenlétében CO 2,- SO 2,-és H 2 O-vá történő tökéletes elégetésekor felszabadul, a víz cseppfolyós halmazállapotban
Perpetuum mobile?!? Égéshő: Az a hőmennyiség, amely normál állapotú száraz gáz, levegő jelenlétében CO 2,- SO 2,-és H 2 O-vá történő tökéletes elégetésekor felszabadul, a víz cseppfolyós halmazállapotban
NATRII AUROTHIOMALAS. Nátrium-aurotiomalát
 Natrii aurothiomalas Ph.Hg.VIII. Ph.Eur.5.8-1 07/2007:1994 NATRII AUROTHIOMALAS Nátrium-aurotiomalát DEFINÍCIÓ A (2RS)-2-(auroszulfanil)butándisav mononátrium és dinátrium sóinak keveréke. Tartalom: arany
Natrii aurothiomalas Ph.Hg.VIII. Ph.Eur.5.8-1 07/2007:1994 NATRII AUROTHIOMALAS Nátrium-aurotiomalát DEFINÍCIÓ A (2RS)-2-(auroszulfanil)butándisav mononátrium és dinátrium sóinak keveréke. Tartalom: arany
Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció. Rabi István 2013. 09.18
 Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció Rabi István 2013. 09.18 Agenda Bevezetés Desztilláció Kőolaj desztilláció A Finomítás célja Agenda Bevezetés Desztilláció Kőolaj desztilláció
Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció Rabi István 2013. 09.18 Agenda Bevezetés Desztilláció Kőolaj desztilláció A Finomítás célja Agenda Bevezetés Desztilláció Kőolaj desztilláció
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
IV. Pervaporáció 1. Bevezetés
 IV. Pervaporáció 1. Bevezetés A pervaporáció a membrán-elválasztás és az elpárologtatás energiahatékony kombinációja ( membrane permeation + evaporation = pervaporation ). Azeotrop, közeli forrpontú, izomer
IV. Pervaporáció 1. Bevezetés A pervaporáció a membrán-elválasztás és az elpárologtatás energiahatékony kombinációja ( membrane permeation + evaporation = pervaporation ). Azeotrop, közeli forrpontú, izomer
Az α értékének változtatásakor tanulmányozzuk az y-x görbe alakját. 2 ahol K=10
 9.4. Táblázatkezelés.. Folyadék gőz egyensúly kétkomponensű rendszerben Az illékonyabb komponens koncentrációja (móltörtje) nagyobb a gőzfázisban, mint a folyadékfázisban. Móltört a folyadékfázisban x;
9.4. Táblázatkezelés.. Folyadék gőz egyensúly kétkomponensű rendszerben Az illékonyabb komponens koncentrációja (móltörtje) nagyobb a gőzfázisban, mint a folyadékfázisban. Móltört a folyadékfázisban x;
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
Az egyensúly 10-1 Dinamikus egyensúly 10-2 Az egyensúlyi állandó 10-3 Az egyensúlyi állandókkal kapcsolatos összefüggések 10-4 Az egyensúlyi állandó számértékének jelentősége 10-5 A reakció hányados, Q:
MŰSZAKI ISMERETEK, VEGYIPARI GÉPEK II.
 MŰSZAKI ISMERETEK, VEGYIPARI GÉPEK II. Vegyipari szakmacsoportos alapozásban résztvevő tanulók részére Ez a tankönyvpótló jegyzet a Petrik Lajos Két Tanítási Nyelvű Vegyipari, Környezetvédelmi és Informatikai
MŰSZAKI ISMERETEK, VEGYIPARI GÉPEK II. Vegyipari szakmacsoportos alapozásban résztvevő tanulók részére Ez a tankönyvpótló jegyzet a Petrik Lajos Két Tanítási Nyelvű Vegyipari, Környezetvédelmi és Informatikai
Fluidum-kőzet kölcsönhatás: megváltozik a kőzet és a fluidum összetétele és új egyensúlyi ásványparagenezis jön létre Székyné Fux V k álimetaszo
 Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
2.11. A kétkomponensű rendszerek fázisegyensúlyai
 Fejezetek a fizikai kémiából 2.11. kétkomonensű rendszerek fázisegyensúlyai kétkomonensű rendszerekben (C=2), amikor mind a nyomás, mint a hőmérséklet befolyásolja a rendszer állaotát (n=2), Gibbs törvénye
Fejezetek a fizikai kémiából 2.11. kétkomonensű rendszerek fázisegyensúlyai kétkomonensű rendszerekben (C=2), amikor mind a nyomás, mint a hőmérséklet befolyásolja a rendszer állaotát (n=2), Gibbs törvénye
Működésbiztonsági veszélyelemzés (Hazard and Operability Studies, HAZOP) MSZ
 Működésbiztonsági veszélyelemzés (Hazard and Operability Studies, HAZOP) MSZ-09-960614-87 Célja: a szisztematikus zavar-feltárás, nyomozás. A tervezett működési körülményektől eltérő állapotok azonosítása,
Működésbiztonsági veszélyelemzés (Hazard and Operability Studies, HAZOP) MSZ-09-960614-87 Célja: a szisztematikus zavar-feltárás, nyomozás. A tervezett működési körülményektől eltérő állapotok azonosítása,
Szerves laboratóriumi gyakorlatok 12. évfolyam. 2013. szeptember 12. 4. javított kiadás. Tanulói jegyzet és recept leírás
 szeptember 12. 4. javított kiadás Szerves laboratóriumi gyakorlatok 12. évfolyam Tanulói jegyzet és recept leírás [ Szerves kémiai alapfolyamatok és a hozzájuk kapcsolódó szerves és szervetlen preparátumok
szeptember 12. 4. javított kiadás Szerves laboratóriumi gyakorlatok 12. évfolyam Tanulói jegyzet és recept leírás [ Szerves kémiai alapfolyamatok és a hozzájuk kapcsolódó szerves és szervetlen preparátumok
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK
 ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció
 Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció Rabi István 2014. 09.24. A dokumentum nem sokszorosítható semmilyen formában az előadó írásos engedélye nélkül! Agenda Bevezetés Desztilláció
Szénhidrogén ipari technológiák Szétválasztó eljárások, Desztilláció Rabi István 2014. 09.24. A dokumentum nem sokszorosítható semmilyen formában az előadó írásos engedélye nélkül! Agenda Bevezetés Desztilláció
AUTOMATA REAKTOR. Kémiai Technológia Gyakorlat
 AUTOMATA REAKTOR Kémiai Technológia Gyakorlat Az iparban számos különböző reaktor típust használnak a laboratóriumi munkában is megszokott reakciók kivitelezésére. A reaktorokban lejátszódó folyamatok
AUTOMATA REAKTOR Kémiai Technológia Gyakorlat Az iparban számos különböző reaktor típust használnak a laboratóriumi munkában is megszokott reakciók kivitelezésére. A reaktorokban lejátszódó folyamatok
1. feladat Összesen: 8 pont. 2. feladat Összesen: 11 pont. 3. feladat Összesen: 7 pont. 4. feladat Összesen: 14 pont
 1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
1. feladat Összesen: 8 pont 150 gramm vízmentes nátrium-karbonátból 30 dm 3 standard nyomású, és 25 C hőmérsékletű szén-dioxid gáz fejlődött 1800 cm 3 sósav hatására. A) Írja fel a lejátszódó folyamat
Szabadentalpia nyomásfüggése
 Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
hőátadás, hőátvitel, hőcsere Pécsi Tudományegyetem Gyógyszertechnológiai Intézet
 hőátadás, hőátvitel, hőcsere Pécsi Tudományegyetem Gyógyszertechnológiai Intézet 1 A hő minden olyan energiaváltozás ami nem fordítódik munkára termodinamikai rendszerek kölcsönhatása során. Pécsi Tudományegyetem
hőátadás, hőátvitel, hőcsere Pécsi Tudományegyetem Gyógyszertechnológiai Intézet 1 A hő minden olyan energiaváltozás ami nem fordítódik munkára termodinamikai rendszerek kölcsönhatása során. Pécsi Tudományegyetem
1. feladat Összesen 20 pont
 É 047-06/1/D 1. feladat Összesen 0 pont Csőköteges hőcserélőben óránként 1,5 m anyagot melegítenek 0 C-ról 95 C-ra bar nyomású telített vízgőz rejtett hője segítségével. Az anyag sűrűsége 985 kg/m, fajhője,0
É 047-06/1/D 1. feladat Összesen 0 pont Csőköteges hőcserélőben óránként 1,5 m anyagot melegítenek 0 C-ról 95 C-ra bar nyomású telített vízgőz rejtett hője segítségével. Az anyag sűrűsége 985 kg/m, fajhője,0
Kémia I. 6. rész. Halmazállapotok, halmazállapot változások
 Kémia I. 6. rész Halmazállapotok, halmazállapot változások HALMAZÁLLAPOTOK I a körülöttünk lévő anyagok többsége a körülményektől függően háromféle halmazállapot -ban létezhet: elvileg minden anyag mindhárom
Kémia I. 6. rész Halmazállapotok, halmazállapot változások HALMAZÁLLAPOTOK I a körülöttünk lévő anyagok többsége a körülményektől függően háromféle halmazállapot -ban létezhet: elvileg minden anyag mindhárom
Extrakció. Vegyipari és biomérnöki műveletek segédanyag Simándi Béla, Székely Edit BME, Kémiai és Környezeti Folyamatmérnöki Tanszék
 Extrakció Vegyipari és biomérnöki műveletek segédanyag Simándi Béla, Székely Edit BME, Kémiai és Környezeti Folyamatmérnöki Tanszék 1 . fázis 2. fázis Anyagátmenet iránya áz (G) Folyadék G L (L) G L L
Extrakció Vegyipari és biomérnöki műveletek segédanyag Simándi Béla, Székely Edit BME, Kémiai és Környezeti Folyamatmérnöki Tanszék 1 . fázis 2. fázis Anyagátmenet iránya áz (G) Folyadék G L (L) G L L
Folyamatábra és anyagforgalmi diagram készítése
 Folyamatábra és anyagforgalmi diagram készítése Egy szintézis kivitelezése átgondolt tervezést igényel, ezen kívül a megvalósítás számszerű adatokkal alátámasztott kontrollja is elengedhetetlen. Az előbbi
Folyamatábra és anyagforgalmi diagram készítése Egy szintézis kivitelezése átgondolt tervezést igényel, ezen kívül a megvalósítás számszerű adatokkal alátámasztott kontrollja is elengedhetetlen. Az előbbi
Szabadonálló gázüzemű főzőüst
 A 700XP sorozat több, mint 100 modellt foglal magába. Minden készülékek nagy teljesítményű, megbízható, energiatakarékos, biztonságos és ergonómikus. A modul rendszer megszámlálhatatlan konfigurációban
A 700XP sorozat több, mint 100 modellt foglal magába. Minden készülékek nagy teljesítményű, megbízható, energiatakarékos, biztonságos és ergonómikus. A modul rendszer megszámlálhatatlan konfigurációban
1. feladat Összesen 15 pont. 2. feladat Összesen 6 pont. 3. feladat Összesen 6 pont. 4. feladat Összesen 7 pont
 1. feladat Összesen 15 pont Egy lombikba 60 g jégecetet és 46 g abszolút etanolt öntöttünk. A) Számítsa ki a kiindulási anyagmennyiségeket! B) Határozza meg az egyensúlyi elegy összetételét móltörtben
1. feladat Összesen 15 pont Egy lombikba 60 g jégecetet és 46 g abszolút etanolt öntöttünk. A) Számítsa ki a kiindulási anyagmennyiségeket! B) Határozza meg az egyensúlyi elegy összetételét móltörtben
Atomok. szilárd. elsődleges kölcsönhatás. kovalens ionos fémes. gázok, folyadékok, szilárd anyagok. ionos fémek vegyületek ötvözetek
 Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
LACTULOSUM. Laktulóz
 Lactulosum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1230 LACTULOSUM Laktulóz és C* epimere C 12 H 22 O 11 M r 342,3 [4618-18-2] DEFINÍCIÓ 4-O-(β-D-galaktopiranozil)-D-arabino-hex-2-ulofuranóz- Tartalom: 95,0 102,0
Lactulosum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1230 LACTULOSUM Laktulóz és C* epimere C 12 H 22 O 11 M r 342,3 [4618-18-2] DEFINÍCIÓ 4-O-(β-D-galaktopiranozil)-D-arabino-hex-2-ulofuranóz- Tartalom: 95,0 102,0
Tájékoztató. Használható segédeszköz: -
 A 29/2016 (VIII.26.) NGM rendelet szakmai és vizsgakövetelménye alapján. Szakképesítés, azonosító száma és megnevezése Tájékoztató 54 544 03 Gázipari technikus A vizsgázó az első lapra írja fel a nevét!
A 29/2016 (VIII.26.) NGM rendelet szakmai és vizsgakövetelménye alapján. Szakképesítés, azonosító száma és megnevezése Tájékoztató 54 544 03 Gázipari technikus A vizsgázó az első lapra írja fel a nevét!
2011/2012 tavaszi félév 2. óra. Tananyag:
 2011/2012 tavaszi félév 2. óra Tananyag: 2. Gázelegyek, gőztenzió Gázelegyek összetétele, térfogattört és móltört egyezősége Gázelegyek sűrűsége Relatív sűrűség Parciális nyomás és térfogat, Dalton-törvény,
2011/2012 tavaszi félév 2. óra Tananyag: 2. Gázelegyek, gőztenzió Gázelegyek összetétele, térfogattört és móltört egyezősége Gázelegyek sűrűsége Relatív sűrűség Parciális nyomás és térfogat, Dalton-törvény,
Problémás regressziók
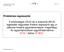 Universitas Eotvos Nominata 74 203-4 - II Problémás regressziók A közönséges (OLS) és a súlyozott (WLS) legkisebb négyzetes lineáris regresszió egy p- változós lineáris egyenletrendszer megoldása. Az egyenletrendszer
Universitas Eotvos Nominata 74 203-4 - II Problémás regressziók A közönséges (OLS) és a súlyozott (WLS) legkisebb négyzetes lineáris regresszió egy p- változós lineáris egyenletrendszer megoldása. Az egyenletrendszer
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
A halmazállapot-változások
 A halmazállapot-változások A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Halmazállapotok Energia Kondenzáció Kondenzációs hő Kondenzáció Párolgás Gőz Fagyáshő Párolgáshő Folyadék
A halmazállapot-változások A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Halmazállapotok Energia Kondenzáció Kondenzációs hő Kondenzáció Párolgás Gőz Fagyáshő Párolgáshő Folyadék
A fűtési rendszer kiválasztása a hőközlő közeg gőz vagy folyadék legyen?
 ENERGIATERMELÉS, -ÁTALAKÍTÁS, -SZÁLLÍTÁS ÉS -SZOLGÁLTATÁS 2.6 A fűtési rendszer kiválasztása a hőközlő közeg vagy folyadék legyen? Tárgyszavak: fűtés; kondenzátumfelhalmozódás; hőteljesítmény; szabályozás;
ENERGIATERMELÉS, -ÁTALAKÍTÁS, -SZÁLLÍTÁS ÉS -SZOLGÁLTATÁS 2.6 A fűtési rendszer kiválasztása a hőközlő közeg vagy folyadék legyen? Tárgyszavak: fűtés; kondenzátumfelhalmozódás; hőteljesítmény; szabályozás;
FIZIKA. Ma igazán belemelegszünk! (hőtan) Dr. Seres István
 FIZIKA Ma igazán belemelegszünk! (hőtan) Dr. Seres István Hőtágulás, kalorimetria, Halmazállapot változások fft.szie.hu 2 Seres.Istvan@gek.szi.hu Lineáris (vonalmenti) hőtágulás L L L 1 t L L0 t L 0 0
FIZIKA Ma igazán belemelegszünk! (hőtan) Dr. Seres István Hőtágulás, kalorimetria, Halmazállapot változások fft.szie.hu 2 Seres.Istvan@gek.szi.hu Lineáris (vonalmenti) hőtágulás L L L 1 t L L0 t L 0 0
Atomok. szilárd. elsődleges kölcsönhatás. kovalens ionos fémes. gázok, folyadékok, szilárd anyagok. ionos fémek vegyületek ötvözetek
 Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Hőtan I. főtétele tesztek
 Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
54 582 01 0000 00 00 Épületgépész technikus Épületgépész technikus
 A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
A 10/2007 (II. 27.) SzMM rendelettel módosított 1/2006 (II. 17.) OM rendelet Országos Képzési Jegyzékről és az Országos Képzési Jegyzékbe történő felvétel és törlés eljárási rendjéről alapján. Szakképesítés,
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
1. feladat Összesen 5 pont. 2. feladat Összesen 19 pont
 1. feladat Összesen 5 pont Válassza ki, hogy az alábbi táblázatban olvasható állításokhoz mely szivattyúcsővezetéki jelleggörbék rendelhetők (A D)! Írja a jelleggörbe betűjelét az állítások utáni üres
1. feladat Összesen 5 pont Válassza ki, hogy az alábbi táblázatban olvasható állításokhoz mely szivattyúcsővezetéki jelleggörbék rendelhetők (A D)! Írja a jelleggörbe betűjelét az állítások utáni üres
Szakmai fizika Gázos feladatok
 Szakmai fizika Gázos feladatok 1. *Gázpalack kivezető csövére gumicsövet erősítünk, és a gumicső szabad végét víz alá nyomjuk. Mennyi a palackban a nyomás, ha a buborékolás 0,5 m mélyen szűnik meg és a
Szakmai fizika Gázos feladatok 1. *Gázpalack kivezető csövére gumicsövet erősítünk, és a gumicső szabad végét víz alá nyomjuk. Mennyi a palackban a nyomás, ha a buborékolás 0,5 m mélyen szűnik meg és a
Halmazállapot-változások
 Halmazállapot-változások A halmazállapot-változások fajtái Olvadás: szilárd anyagból folyékony a szilárd részecskék közötti nagy vonzás megszűnik, a részecskék kiszakadnak a rácsszerkezetből, és kis vonzással
Halmazállapot-változások A halmazállapot-változások fajtái Olvadás: szilárd anyagból folyékony a szilárd részecskék közötti nagy vonzás megszűnik, a részecskék kiszakadnak a rácsszerkezetből, és kis vonzással
Halmazállapot változások. Folyadékok párolgása. Folyadékok párolgása
 Halmazállapot változások 6. hét Egy anyag különböző halmazállapotai közötti átmenet - elsőfajú fázisátalakulások A kémiai összetétel nem változik meg Adott nyomáson meghatározott hőmérsékleten megy végbe
Halmazállapot változások 6. hét Egy anyag különböző halmazállapotai közötti átmenet - elsőfajú fázisátalakulások A kémiai összetétel nem változik meg Adott nyomáson meghatározott hőmérsékleten megy végbe
B TÉTEL A túró nitrogéntartalmának kimutatása A hamisított tejföl kimutatása A keményítő kimutatása búzalisztből
 2011/2012. B TÉTEL A túró nitrogéntartalmának kimutatása A kémcsőben levő túróra öntsön tömény nátrium-hidroxid oldatot. Melegítse enyhén! Jellegzetes szagú gáz keletkezik. Tartson megnedvesített indikátor
2011/2012. B TÉTEL A túró nitrogéntartalmának kimutatása A kémcsőben levő túróra öntsön tömény nátrium-hidroxid oldatot. Melegítse enyhén! Jellegzetes szagú gáz keletkezik. Tartson megnedvesített indikátor
Ecetsav koncentrációjának meghatározása titrálással
 Ecetsav koncentrációjának meghatározása titrálással A titrálás lényege, hogy a meghatározandó komponenst tartalmazó oldathoz olyan ismert koncentrációjú oldatot adagolunk, amely a reakcióegyenlet szerint
Ecetsav koncentrációjának meghatározása titrálással A titrálás lényege, hogy a meghatározandó komponenst tartalmazó oldathoz olyan ismert koncentrációjú oldatot adagolunk, amely a reakcióegyenlet szerint
5/12/2010. Elegyek. 4-1 Az elegyek fajtái. 10% etanol oldat (v/v) 4-2 Koncentrációk. Mol koncentrációk. 4-3 intermolekuláris kölcsönhatások
 Elegyek 4-1 Az elegyek fajtái 4-1 Elegyek fajtái 4-2 Koncentrációk 4-3 Intermolekuláris erők, az elegyedés folyamata 4-4 Elegyek keletkezése, egyensúly 4-5 Gázok oldhatósága 4-6 Elegyek gőznyomása 4-7
Elegyek 4-1 Az elegyek fajtái 4-1 Elegyek fajtái 4-2 Koncentrációk 4-3 Intermolekuláris erők, az elegyedés folyamata 4-4 Elegyek keletkezése, egyensúly 4-5 Gázok oldhatósága 4-6 Elegyek gőznyomása 4-7
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
