11. Előadás. Heterociklusos vegyületek
|
|
|
- Réka Orbán
- 8 évvel ezelőtt
- Látták:
Átírás
1 11. Előadás eterociklusos vegyületek
2 ETECIKLUSS VEGYÜLETEK Felosztás: 1. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos, egy heteroatomos vegyületek C C 3 C C C 1 C C S C 1 furán* tiofén* pirrol* piridin* oxol tiol azol azin S C C C C C C C C C C C C S C C C C C tetrahidrofurán* oxolán tetrahidrotiofén* tiolán pirrolidin* azolidin piperidin* perhidroazin
3 II.Monociklusos, két heteroatomos vegyületek 1 3 S Azolok: -tagú gyűrű +legalább 1 más heteroatom oxazol tiazol imidazol (hisztidinben) Azinok: 6-tagú gyűrű +legalább 1 más heteroatom () pirimidin (1,3-diazin) (DS, S-ben) pirazin (1,-diazin) piridazin (1,-diazin) III. Biciklusos, kondenzált heteroatomos vegyületek 8 1 triazinok (3), tetrazinok () pirimidin imidazol pirazin pirimidin 3 indol (triptofánban) purin (DS, S-ben) pteridin (folsavban) kinolin (benzopiridin) Festék alapanyag, tartósítószer, fertőtlenítő, oldószer izokinolin izokinolinvázas alkaloidok
4 IV. Tri-,...-ciklusos, heteroatomos vegyületek C 3 akridin 9-aminoakridin: erős fertőtlenítő szer fluoreszcens tulajdonságú C C lizergsav-dietilamid (LSD) op C (anyarozs alkaloid) indol pteridin gyűrű 1 Folsav analógok C C - C (C ) C C 1 =, = folsav; B9-vitamin, M-vitamin. 1 =, = aminopterin 1 =, = C 3 amethopterin, methotrexat glutaminsav Folsav: terhesség korai szakaszában a fejlődő embrió gerincét, a velőcsövet lezáró folyamat fehérvérsejtek, vörösvértestek, vérlemezkék képzésében, az aminosavak, és nukleinsavak anyagcseréjében Metotrexát: tumorellenes szer, alkalmazzák reumatoid artritisz esetés is
5 Elektronszerkezet Aromás jelleg (pirrol, furán, tiofén) (ückel szabály: n+ elektron) Q - I effektus (hetero atom E-nak megfelelő mértékben vonzza az elektronokat Q = :S:, :, :: E =,6 3,0 3, S < < Tiofén hasonlít legjobban a benzolra,de az elektrofil szubsztitúciós reakció gyorsabbak. K effektus 0, 0, + 0,8 + 0, 0, δ- δ- + δ+ - 0,1 + S δ+ 0, δ+ 0,3 δ+ 0,38 egyenletes valóságos elektroneloszlás csak határszerkezetekből - 0,0 + határszerkezetek! nem bázis, nem proton kedvelő piridin + 0,18 + 0,0 + 0,1-0,8 + 0,1 bázis, proton kedvelő
6 Téralkat pm: 10-1 m Å: m izolált egyes kötés izolált kettős kötés Konjugált kettős kötés esetén az egyes és kettős kötés hossza aromás rendszer Kötéshossz : S-C > -C > -C
7 Fizikai tulajdonságok a a molekulában van -donor és -akceptor egyben, akkor tud -kötést kialakítani pirazol
8 Kémiai reakciók 1. Sav-bázis sajátság (sav: protont tud leadni; bázis: protont tud felvenni) tiofén: S nem bázis, nem sav (C- nem proton donor, a kén atom E nem elég nagy, hogy vonzza a -t) pirrol: K ½ K + (pk = 1) megszűnik az aromás jelleg aromás marad (tehát gyenge - sav) furán: piridin: -híd: pirrol, imidazol, purin pk b = 8,8 gyenge bázis
9 piridin piridin pirrol amfoter pirazol imidazol pirimidin bázikus bázikus piridin
10 . Elektrofil szubsztitúciók Feltétel: elektronban gazdag gyűrűk A. pirrol, furán, tiofén, indol pozitív töltés vagy parciális pozitív töltésű rész támad elektronban gazdag helyre δ- Irányítás - 0,0 δ- δ+ - 0,1 Q eaktivitás σ-komplexek lehetséges határszerkezete -es és 3-as helyzetű szubsztitúció esetén: jobb elektron eloszlás, stabilabb σ-komplex o C -nitropirrol -acetilpirrol 0 o C
11 B. piridin Irányítás eaktivitás + 0,1 + 0,18-0,8 + 0,0 + 0,1 legkevésbé + helyre igyekszik kötődni. De kölcsönhatás, ezért sokkal nehezebb a reakció, mint a benzol esetén stabilabb σ-komplex
12 Példák (kénsav protonálódás) 3-brómpiridin 3-nitropiridin piridin-3 szulfonsav Áttekintés benzol pirrol furán tiofén piridin nitrálás * + szulfonálás S * diazo kapcsolás Friedel- Crafts acilezés Ar- + + C 3 -C-Q brómozás Br * protonálás után
13 Példa: triptofán szintézise (indol S E reakció) CEt Ac C C - CEt Ac CEt nátrium-etilát (igen erős bázis) Et CEt acetamidomalonészter (C- sav) Aminometilezés + + C 3C C3 S E C C3 3C Alkilezés C C3 3C + C 3 I S C3 C + C3 3C I - (jó távozó csoport, ld. offman elimináció) C3 C + C3 3C + Ac C - CEt CEt S CEt C EtC Ac CEt C EtC Ac 1. észter hidrolízis. dekarboxilezés C C triptofán
14 3. ukleofil szubsztitúciók Feltétel: elektronban szegény gyűrűk C 6 - Li + C6 Összehasonlítás
15 Kétheteroatomos vegyületek reaktivitása δ + piridin szerű δ- - 0,0 δ + δ- - 0,1 δ+ + 0,18 δ - pirrol szerű δ - (tautoméria) + 0,0 + 0,1-0,8 + 0,1 b a piridin szerű Pozíció a b δ+ δ+ δ+ δ+ δ- δ- 6 δ+ δ+ elatív elektronhiány: = 6 > > Magyarázat: a parciális töltések szuperponálódnak S E S E S S E S E S S pirazol imidazol pirimidin
16 Tautoméria egy kettős kötés és egy proton helyzetének megváltozása Imidazol Szubsztituált imidazol
17 Piridin származékok keto-enol amino-imino citozin (pirimidin) adenin (purin)
18 Furán, tiofén, pirrol vázas vegyületek szintézise (Paal-Knorr) cc. S ' 3 1 ' 3 nyomás ' 1,-dioxo-vegyület (1,-dienol is jó) P S 10 Foszfor-pentaszulfid S ' Példák α amidin-származék karbonsavamid-származék imidazolszármazék oxazolszármazék tiazolszármazék α bróm - keton tioamid-származék
19 Piridin szintézis (antzsch) ' aldehid EtC α β 3 β-oxo karbonsav észter CEt - 3 EtC ' CEt EtC ' CEt ox. EtC ' CEt - piridin-származék
20 Purin szintézis,,6-trihidroxi-pirimidin (barbitursav) dilaktám-enol dilaktám-keto /Cl /red,,6-trihidroxi--aminopirimidin 1. KC. Wöhlerizomerizáció - Cl (0%) pszeudohúgysav keto enol tautoméria Cl Cl ,6,8-triklór-purin Cl PCl 3 10 o C,6,8-trihidroxi-purin (húgysav)
21 Purin szintézis (folytatás) eaktivitási sorrend 6 > > 8 Cl 1 Cl ,6,8-triklór-purin 8 Cl eduktív dehalogénezés purin a + Et K. 3 Et Cl Cl Cl Et Cl 1. Elfőzés (cc. Cl). red.dehalogénezés red. dehal. red. dehal. xantin 6-aminopurin (adenin) guanin
22 Antibiotikumok 198 Alexander Fleming ( ) Penicillium notatum / Staphylococus aureus 1938.W. Florey: tiszta penicillin 19 obel-díj (orvosi): Fleming, Florey
23 Penicillinek S C3 Gram-pozitív baktériumokra C Penicillin G Penám váz transzpeptidáz S C C3 C C3 C3 C C rezisztens törzsben: penicillináz (hidrolízis) C Ampicillin S C3 C3 C enzim (Thr,Ser) Kefalosporin C ezisztencia: a β-laktám gyűrű hidrolizál, mielőtt a transzpeptidázzal reagálna C S C C3
10. Előadás. Heterociklusos vegyületek.
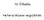 0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
0. Előadás eterociklusos vegyületek. ETECIKLUSS VEGYÜLETEK Felosztás:. telített telítetlen. heteroatomok száma 3. gyűrűk száma. heteroatomok milyensége (,, S, P, As, Si) oxa- S tia- aza- I. Monociklusos,
10. Előadás. Szerves vegyületek kénatommal. Heterociklusos (porfinvázas) vegyületek.
 10. Előadás zerves vegyületek kénatommal. eterociklusos (porfinvázas) vegyületek. ZEVE VEGYÜLETEK KÉATMMAL Példák: C 2 =C-C 2 ---C 2 -C=C 2 diallil-diszulfid (fokhagyma olaj) szacharin merkapto-purin tiofén
10. Előadás zerves vegyületek kénatommal. eterociklusos (porfinvázas) vegyületek. ZEVE VEGYÜLETEK KÉATMMAL Példák: C 2 =C-C 2 ---C 2 -C=C 2 diallil-diszulfid (fokhagyma olaj) szacharin merkapto-purin tiofén
HETEROCIKLUSOS VEGYÜLETEK
 ETERCIKLU VEGYÜLETEK ETERCIKLU VEGYÜLETEK Csoportosítás eteroatom minősége:,, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Telítettség mértéke szerint: - heteroaromás - heteroalkén - heteroalkán - Elnevezés: elsősorban
ETERCIKLU VEGYÜLETEK ETERCIKLU VEGYÜLETEK Csoportosítás eteroatom minősége:,, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Telítettség mértéke szerint: - heteroaromás - heteroalkén - heteroalkán - Elnevezés: elsősorban
Nitrogéntartalmú szerves vegyületek. 6. előadás
 Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Nitrogéntartalmú szerves vegyületek 6. előadás Aminok Funkciós csoport: NH 2 (amino csoport) Az ammónia (NH 3 ) származékai Attól függően, hogy hány H-t cserélünk le, kapunk primer, szekundner és tercier
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Heterociklusos vegyületek
 eterociklusos vegyületek ETERCIKLUSS VEGYÜLETEK eteroatom minősége:, S, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Elnevezés: elsősorban triviális nevek piridin furán izokinolin 2 evezéktan szabályai 5 4 3 R β'
eterociklusos vegyületek ETERCIKLUSS VEGYÜLETEK eteroatom minősége:, S, Gyűrű tagszáma: 3, 4, 5, 6, 7 stb. Elnevezés: elsősorban triviális nevek piridin furán izokinolin 2 evezéktan szabályai 5 4 3 R β'
Szerves kémiai nevezéktan IV.
 zerves kémiai nevezéktan IV. A magyar kémiai elnevezés és helyesírás szabályai, az IUPAC (International Union of Pure and Applied Chemistry) zerves Kémiai ómenklatúrabizottságának 99-as ajánlása alapján.
zerves kémiai nevezéktan IV. A magyar kémiai elnevezés és helyesírás szabályai, az IUPAC (International Union of Pure and Applied Chemistry) zerves Kémiai ómenklatúrabizottságának 99-as ajánlása alapján.
CH 2 =CH-CH 2 -S-S-CH 2 -CH=CH 2
 10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
10. Előadás zerves vegyületek kénatommal Példák: ZEVE VEGYÜLETEK KÉATMMAL CH 2 =CH-CH 2 ---CH 2 -CH=CH 2 diallil-diszulfid (fokhagyma olaj) H H H szacharin merkapto-purin tiofén C H2 H szulfonamid (Ultraseptyl)
Nitrogé ntartalmú hétérociklúsos végyú léték
 itrogé ntartalmú hétérociklúsos végyú léték A nitrogéntartalmú heterociklusos vegyületek a természetben előforduló jelentős vegyületek közé tartoznak. Piridin C55 Szerkezete o A benzolhoz hasonló a felépítése,
itrogé ntartalmú hétérociklúsos végyú léték A nitrogéntartalmú heterociklusos vegyületek a természetben előforduló jelentős vegyületek közé tartoznak. Piridin C55 Szerkezete o A benzolhoz hasonló a felépítése,
AROMÁS SZÉNHIDROGÉNEK
 AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
AROMÁS SZÉNIDROGÉNK lnevezés C 3 C 3 3 C C C 3 C 3 C C 2 benzol toluol xilol (o, m, p) kumol sztirol naftalin antracén fenantrén Csoportnevek C 3 C 2 fenil fenilén (o,m,p) tolil (o,m,p) benzil 1-naftil
Tantárgycím: Szerves kémia
 Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
Eötvös Loránd Tudományegyetem Természettudományi Kar Biológia Szak Kötelező tantárgy TANTÁRGY ADATLAP és tantárgykövetelmények 2005. Tantárgycím: Szerves kémia 2. Tantárgy kódja félév Követelmény Kredit
Szénhidrogének III: Alkinok. 3. előadás
 Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Szénhidrogének III: Alkinok 3. előadás Általános jellemzők Általános képlet C n H 2n 2 Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C C kötést
Részletes tematika: 1 hét (3 óra)
 Részletes tematika: 1 hét (3 óra) Telített Heterociklusos Vegyületek Előállítás. Konformációs Viszonyok. Reaktivitás Fontosabb N-, O- és S-Telített Heterociklusok. Penicillinek Nevezéktan, triviális név,
Részletes tematika: 1 hét (3 óra) Telített Heterociklusos Vegyületek Előállítás. Konformációs Viszonyok. Reaktivitás Fontosabb N-, O- és S-Telített Heterociklusok. Penicillinek Nevezéktan, triviális név,
ALKOHOLOK ÉS SZÁRMAZÉKAIK
 ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
ALKLK ÉS SZÁRMAZÉKAIK Levezetés R R alkohol R R R éter Elnevezés Nyíltláncú, telített alkoholok általános név: alkanol alkil-alkohol 2 2 2 metanol etanol propán-1-ol metil-alkohol etil-alkohol propil-alkohol
HALOGÉNEZETT SZÉNHIDROGÉNEK
 ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
ALOGÉNEZETT SZÉNIDOGÉNEK Elnevezés Nyíltláncú, telített általános név: halogénalkán alkilhalogenid l 2 l 2 2 l klórmetán klóretán 1klórpropán l metilklorid etilklorid propilklorid 2klórpropán izopropilklorid
Helyettesített karbonsavak
 elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
elyettesített karbonsavak 1 elyettesített savak alogénezett savak idroxisavak xosavak Dikarbonsavak Aminosavak (és fehérjék, l. Természetes szerves vegyületek) 2 alogénezett savak R az R halogént tartalmaz
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 3
O 2 R-H 2 C-OH R-H 2 C-O-CH 2 -R R-HC=O
 Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
Funkciós csoportok, reakcióik II C 4 C 3 C 2 C 2 R- 2 C- R- 2 C--C 2 -R C 2 R-C= ALKLK, ÉTEREK Faszesz C 3 Toxikus 30ml vakság LD 50 értékek alkoholokra patkányokban LD 50 = A populáció 50%-ának elhullásához
AMINOK. Aminok rendűsége és típusai. Levezetés. Elnevezés. Alkaloidok (fiziológiailag aktív vegyületek) A. k a. primer RNH 2. szekunder R 2 NH NH 3
 Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
Levezetés AMIK 2 primer 2 2 3 2 3 3 2 3 2 3 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 1aminobután butánamin nbutilamin Aminok rendűsége és típusai 2amino2metilpropán 2metil2propánamin tercierbutilamin
COOCH 3. Ca + O - NH 2 OCH 2 CH 2 CH 3 NO 2 N H H 3 CO N OCH 3 COOH
 9. Előadás itrogéntartalmú vegyületek 26. ITGÉTATALMÚ VEGYÜLETEK épszerű származékok 3 2 metil-antranilát (szőlő) 300 S szacharin (1977) S - kalcium-ciklamát (1970: rák) a + 2 2 3 2 2 3 2 2 3 2 2 2 glükóz:
9. Előadás itrogéntartalmú vegyületek 26. ITGÉTATALMÚ VEGYÜLETEK épszerű származékok 3 2 metil-antranilát (szőlő) 300 S szacharin (1977) S - kalcium-ciklamát (1970: rák) a + 2 2 3 2 2 3 2 2 3 2 2 2 glükóz:
β-dikarbonil-vegyületek szintetikus alkalmazásai
 β-dikarbonil-vegyületek szintetikus alkalmazásai A β-dikarbonil vegyületek tipikus szerkezeti egysége a két karbonilcsoport, melyeket egy metilén híd köt össze. Ezek a származékok két fontos tulajdonsággal
β-dikarbonil-vegyületek szintetikus alkalmazásai A β-dikarbonil vegyületek tipikus szerkezeti egysége a két karbonilcsoport, melyeket egy metilén híd köt össze. Ezek a származékok két fontos tulajdonsággal
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBONILCSOPORTOT TARTALMAZÓ VEGYÜLETEK
 1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
1. KARBILSPRTT TARTALMAZÓ VEGYÜLETEK 1.1. A karbonilcsoport szerkezete A szénsav acilcsoportja a karbonilcsoport: vagy 1. ábra: A karbonilcsoport A karbonilcsoport az alábbi vegyületcsaládokban fordul
Összefoglaló előadás. Sav-bázis elmélet
 Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
Összefoglaló előadás Sav-bázis elmélet SAV-BÁZIS TULAJDNSÁGKAT BEFLYÁSLÓ TÉNYEZŐK Elméletek: 1. Brönsted Lowry elmélet: sav - + donor; bázis - + akceptor; Konjugálódó (vagy korrespondáló) sav-bázis pár:
szerotonin idegi mûködésben szerpet játszó vegyület
 3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
3 2 2 3 2 3 2 3 2 2 3 3 1 amin 1 amin 2 amin 3 amin 2 3 3 2 3 1-aminobután butánamin n-butilamin 2-amino-2-metil-propán 2-metil-2-propánamin tercier-butilamin 1-metilamino-propán -metil-propánamin metil-propilamin
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 4. hét Szerves kémia ismétlése, a szerves kémiai ismeretek gyakorlása a biokémiához Írták: Agócs Attila, Berente Zoltán, Gulyás Gergely, Jakus
(11) Lajstromszám: E 005 785 (13) T2 EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA
 !HU000005785T2! (19) HU (11) Lajstromszám: E 005 785 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 753349 (22) A bejelentés napja:
!HU000005785T2! (19) HU (11) Lajstromszám: E 005 785 (13) T2 MAGYAR KÖZTÁRSASÁG Magyar Szabadalmi Hivatal EURÓPAI SZABADALOM SZÖVEGÉNEK FORDÍTÁSA (21) Magyar ügyszám: E 03 753349 (22) A bejelentés napja:
Bevezetés. Szénvegyületek kémiája Organogén elemek (C, H, O, N) Életerő (vis vitalis)
 Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
Szerves kémia Fontos tudnivalók Tárgy neve: Kémia alapjai I. Neptun kód: SBANKE1050 Előadó: Borzsák István C121 szerda 11-12 e-mail: iborzsak@ttk.nyme.hu http://www.bdf.hu/ttk/fldi/iborzsak/dokumentumok/
MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Szerves Kémia és Technológia Tanszék MECHANIZMUSGYŰJTEMÉNY a Szerves kémia I. előadáshoz Készítette: Kormos Attila Lektorálta:
Néhány fontosabb vitamin
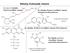 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) 3 3 2 B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora 3 3 l 3 -difoszfát: kokarboxiláz koenzim 3 3 2
Toluol (Bruckner II/1 476) µ= 0.33 Debye
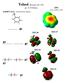 E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
E(RHF/3-21G= -268.24021020 Hartree Toluol (Bruckner II/1 476) µ= 0.33 Debye -0.04 töltés. 0.04 φ6 MO 26 MO 27 φ4 φ5 MO 24 MO 25 φ2 MO 21 φ1 TD ρ= 0.0004 a.u. Anilin (Bruckner II/1 476) µ= 1.44 Debye E(RHF/6-311++G(d,p))=
KARBONSAVAK. A) Nyílt láncú telített monokarbonsavak (zsírsavak) O OH. karboxilcsoport. Példák. pl. metánsav, etánsav, propánsav...
 KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
KABNSAVAK karboxilcsoport Példák A) Nyílt láncú telített monokarbonsavak (zsírsavak) "alkánsav" pl. metánsav, etánsav, propánsav... (nem használjuk) omológ sor hangyasav 3 2 2 2 valeriánsav 3 ecetsav 3
Budapest, június 15. Dr. Hornyánszky Gábor egyetemi docens
 SZERVES KÉMIA BIOMÉRNÖKÖKNEK B.Sc. képzés, kód: BMEVESZA204 Tantárgy követelményei 2016/2017 tanév I. félév A tárgy heti előadásból és 2 óra tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul.
SZERVES KÉMIA BIOMÉRNÖKÖKNEK B.Sc. képzés, kód: BMEVESZA204 Tantárgy követelményei 2016/2017 tanév I. félév A tárgy heti előadásból és 2 óra tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul.
Javító vizsga követelményei kémia tantárgyból augusztus osztály
 Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Javító vizsga követelményei kémia tantárgyból 2019. augusztus 29. 10. osztály I. Szerves kémia-bevezetés 1. A szerves kémia kialakulása, tárgya (Tk. 64-65 old.) - Lavoisier: organogén elemek (C, H, O,
Budapest, augusztus 22. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
Néhány fontosabb vitamin
 éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
éhány fontosabb vitamin all-transz A-vitamin: retinol (zsíroldható vitamin) B 1 -vitamin: thiamin (vízoldható vitamin) tiaminpirofoszfát prekurzora l -difoszfát: kokarboxiláz koenzim 3 l S B 2 -vitamin:
SZERVES KÉMIAI REAKCIÓEGYENLETEK
 SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIAI REAKCIÓEGYENLETEK Budapesti Reáltanoda Fontos! Sok reakcióegyenlet több témakörhöz is hozzátartozik. Szögletes zárójel jelzi a reakciót, ami más témakörnél található meg. Alkánok, cikloalkánok
SZERVES KÉMIA biomérnököknek B.Sc. képzés, kód: BMEVESZA204 Tantárgy követelményei 2017/2018 tanév II. félév
 SZERVES KÉMIA biomérnököknek B.Sc. képzés, kód: BMEVESZA204 Tantárgy követelményei 2017/2018 tanév II. félév A tárgy heti előadásból és 2 óra tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul.
SZERVES KÉMIA biomérnököknek B.Sc. képzés, kód: BMEVESZA204 Tantárgy követelményei 2017/2018 tanév II. félév A tárgy heti előadásból és 2 óra tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul.
CHO CH 2 H 2 H HO H H O H OH OH OH H
 2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
2. Előadás A szénhidrátok kémiai reakciói, szénhidrátszármazékok Áttekintés 1. Redukció 2. xidáció 3. Észter képzés 4. Reakciók a karbonil atomon 4.1. iklusos félacetál képzés 4.2. Reakció N-nukleofillel
KARBONSAVSZÁRMAZÉKOK
 KABNSAVSZÁMAZÉKK Levezetés Kémiai rokonság 2 2 2 N 3 N A karbonsavszármazékok típusai l karbonsavklorid karbonsavanhidrid karbonsavészter N N 2 karbonsavnitril karbonsavamid Példák karbonsavkloridok 3
KABNSAVSZÁMAZÉKK Levezetés Kémiai rokonság 2 2 2 N 3 N A karbonsavszármazékok típusai l karbonsavklorid karbonsavanhidrid karbonsavészter N N 2 karbonsavnitril karbonsavamid Példák karbonsavkloridok 3
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Budapest, augusztus 26. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból áll. A tárgy szóbeli vizsgával zárul. A vizsgára bocsáthatóság feltétele:
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
8. HETEROCIKLUSOS VEGYÜLETEK
 8. ETERIKLU VEGYÜLETEK 8.1. A heterociklusos vegyületek csoportosítása és elnevezése eterociklusos vegyületeknek nevezzük azokat a gyűrűs vegyületeket, amelyek gyűrűjében az egy vagy több szénatom mellett
8. ETERIKLU VEGYÜLETEK 8.1. A heterociklusos vegyületek csoportosítása és elnevezése eterociklusos vegyületeknek nevezzük azokat a gyűrűs vegyületeket, amelyek gyűrűjében az egy vagy több szénatom mellett
Aromás vegyületek II. 4. előadás
 Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
Aromás vegyületek II. 4. előadás Szubsztituensek irányító hatása Egy következő elektrofil hova épül be orto, meta, para pozíció CH 3 CH 3 CH 3 CH 3 E E E orto (1,2) meta (1,3) para (1,4) Szubsztituensek
szabad bázis a szerves fázisban oldódik
 1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
1. feladat Oldhatóság 1 2 vízben tel. Na 2 CO 3 oldatban EtOAc/víz elegyben O-védett protonált sóként oldódik a sóból felszabadult a nem oldódó O-védett szabad bázis a felszabadult O-védett szabad bázis
Gyűrűs vegyületek. - Monociklusos. - Policiklusos. Izolált gyűrűs. Kondenzált policiklusos. orto. orto és peri. Áthidalt gyűrűs.
 Gyűrűs vegyületek - Monociklusos - Policiklusos Izolált gyűrűs Kondenzált policiklusos orto orto és peri Áthidalt gyűrűs Spirociklusos egyszeres/kétszeres kötés kapcsolódási szám eggyel kevesebb a gyűrűk
Gyűrűs vegyületek - Monociklusos - Policiklusos Izolált gyűrűs Kondenzált policiklusos orto orto és peri Áthidalt gyűrűs Spirociklusos egyszeres/kétszeres kötés kapcsolódási szám eggyel kevesebb a gyűrűk
OXOVEGYÜLETEK. Levezetés. Elnevezés O CH 2. O R C H aldehid. O R C R' keton. Aldehidek. propán. karbaldehid CH 3 CH 2 CH 2 CH O. butánal butiraldehid
 XVEGYÜLETEK Levezetés 2 aldehid ' keton Elnevezés Aldehidek propán karbaldehid 3 2 2 butánal butiraldehid oxo karbonil formil Példák 3 3 2 metanal etanal propanal formaldehid acetaldehid propionaldehid
XVEGYÜLETEK Levezetés 2 aldehid ' keton Elnevezés Aldehidek propán karbaldehid 3 2 2 butánal butiraldehid oxo karbonil formil Példák 3 3 2 metanal etanal propanal formaldehid acetaldehid propionaldehid
Szerves Kémia II. Dr. Patonay Tamás egyetemi tanár E 405 Tel:
 Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
Szerves Kémia II. TKBE0312 Előfeltétel: TKBE03 1 Szerves kémia I. Előadás: 2 óra/hét Dr. Patonay Tamás egyetemi tanár E 405 Tel: 22464 tpatonay@puma.unideb.hu A 2010/11. tanév tavaszi félévében az előadás
CHO H H H OH H OH OH H CH2OH HC OH HC OH HC OH CH 2
 4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
4. Előadás ukleozidok, nukleotidok, nukleinsavak Történeti háttér Savas karakterű anyagok a sejtmagból 1869-71 DS a sejtmag fő komponense F. Miescher (Svájc) 1882 Flemming: Chromatin elnevezés Waldeyer:
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2018/2019tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Tantárgy követelményei 2016/2017tanév II. félév Az alaptárgy heti 3 óra előadásból és heti tantermi gyakorlatból áll. A tárgy szóbeli vizsgával zárul. A
8. Előadás. Karbonsavak. Karbonsav származékok.
 8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
Osztályozó vizsgatételek. Kémia - 9. évfolyam - I. félév
 Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Kémia - 9. évfolyam - I. félév 1. Atom felépítése (elemi részecskék), alaptörvények (elektronszerkezet kiépülésének szabályai). 2. A periódusos rendszer felépítése, periódusok és csoportok jellemzése.
Halogénezett szénhidrogének
 Halogénezett szénhidrogének - Jellemző kötés (funkciós csoport): X X = halogén, F, l, Br, I - soportosítás: - halogénatom(ok) minősége szerint (X = F, l, Br, I) - halogénatom(ok) száma szerint (egy-, két-
Halogénezett szénhidrogének - Jellemző kötés (funkciós csoport): X X = halogén, F, l, Br, I - soportosítás: - halogénatom(ok) minősége szerint (X = F, l, Br, I) - halogénatom(ok) száma szerint (egy-, két-
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
8. Előadás Karbonsavak. Karbonsav származékok.
 8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
8. Előadás Karbonsavak. Karbonsav származékok. 24. Karbonsavak α H X H H X N karbonsav nitril X Név F, Br, l halogénsav H hidroxisav oxosav NH 2 aminosav X Név F, Br, l savhaloid R észter R anhidrid NH
IV. Elektrofil addíció
 IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
IV. Elektrofil addíció Szerves molekulákban a kettős kötés kimutatására ismert analitikai módszer a 2 -os vagy a KMnO 4 -os reakció. 2 2 Mi történik tehát a brómmolekula addíciója során? 2 2 ciklusos bromónium
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 4. Szén-szén egyszeres kötések kialakítása savkatalizált reakciókban Kovács Lajos 1 Karbokationok képz dése Brønsted- vagy Lewis-savak jelenlétében P Alkil karbokationok
Szerves kémiai szintézismódszerek 4. Szén-szén egyszeres kötések kialakítása savkatalizált reakciókban Kovács Lajos 1 Karbokationok képz dése Brønsted- vagy Lewis-savak jelenlétében P Alkil karbokationok
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Savak bázisok 12-1 Az Arrhenius elmélet röviden 12-2 Brønsted-Lowry elmélet 12-3 A víz ionizációja és a p skála 12-4 Erős savak és bázisok 12-5 Gyenge savak és bázisok 12-6 Több bázisú savak 12-7 Ionok
Gyűrűs vegyületek. - Monociklusos. - Policiklusos. Izolált gyűrűs. Kondenzált policiklusos. orto. orto és peri. Áthidalt gyűrűs.
 Gyűrűs vegyületek - Monociklusos - Policiklusos Izolált gyűrűs Kondenzált policiklusos orto orto és peri Áthidalt gyűrűs pirociklusos egyszeres/kétszeres kötés kapcsolódási szám eggyel kevesebb a gyűrűk
Gyűrűs vegyületek - Monociklusos - Policiklusos Izolált gyűrűs Kondenzált policiklusos orto orto és peri Áthidalt gyűrűs pirociklusos egyszeres/kétszeres kötés kapcsolódási szám eggyel kevesebb a gyűrűk
Szerves Kémia. Farmakológus szakasszisztens képzés 2012/2013 ősz
 Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
Szerves Kémia Farmakológus szakasszisztens képzés 2012/2013 ősz Általános tudnivalók Kele Péter (ELTE Északi tömb, Kémia, 646. szoba) kelep@elte.hu sütörtök 17 15 19 45 Szeptember 27. elmarad Őszi szünet
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor)
 2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
2001 pótfeladatsor 1. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2001 (pótfeladatsor) Útmutató! Ha most érettségizik, az I. feladat kidolgozását karbonlapon végezze el! Figyelem! A kidolgozáskor
Eredményes vizsga esetén a tárggyal 5 kreditpont szerezhető. A félév csak aláírással zárul, ha
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2017/2018 tanév I. félév Az alaptárgy heti 3 óra előadásból és heti 2
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2017/2018 tanév I. félév Az alaptárgy heti 3 óra előadásból és heti 2
Szerves Kémia II. 2016/17
 Szerves Kémia II. 2016/17 TKBE0301 és TKBE0312 4 kr Előfeltétel: TKBE0301 Szerves kémia I. Előadás: 2 óra/hét Dr. Juhász László egyetemi docens E 409 Tel: 22464 juhasz.laszlo@science.unideb.hu A 2016/17.
Szerves Kémia II. 2016/17 TKBE0301 és TKBE0312 4 kr Előfeltétel: TKBE0301 Szerves kémia I. Előadás: 2 óra/hét Dr. Juhász László egyetemi docens E 409 Tel: 22464 juhasz.laszlo@science.unideb.hu A 2016/17.
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL
 SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2011/12. II. félév 1 Tartalomjegyzék 1.
SZERVES KÉMIA ANYAGMÉRNÖK BSc NAPPALI TÖRZSANYAG MAKKEM 229BL TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2011/12. II. félév 1 Tartalomjegyzék 1.
Budapest, szeptember 6. Dr. Huszthy Péter egyetemi tanár
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESKA202 és BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESKA202 és BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2016/2017 tanév I. félév Az alaptárgy heti 3 óra előadásból
Eredményes vizsga esetén a tárggyal 5 kreditpont szerezhető. A félév csak aláírással zárul, ha
 SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból és heti 2
SZERVES KÉMIA I. B.Sc. képzés, kód: BMEVESZA301 Válogatott fejezetek a szerves kémiából I., kód: BMEVESKA002 Tantárgy követelményei 2018/2019 tanév I. félév Az alaptárgy heti 3 óra előadásból és heti 2
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk.
 1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
1. feladat Aromás: 1, 3, 5, 6, 8, 9, 10, 11, 13, (14) Az azulén (14) szemiaromás rendszert alkot, mindkét választ (aromás, nem aromás) elfogadtuk. 2. feladat Etil-metil-keton (bután-2-on) Jelek hozzárendelése:
Szerves kémia Fontosabb vegyülettípusok
 Fontosabb vegyülettípusok Szénhidrogének: alifás telített (metán, etán, propán, bután, ) alifás telítetlen (etén, etin, ) aromás (benzol, toluol, naftalin) Oxigéntartalmú vegyületek: hidroxivegyületek
Fontosabb vegyülettípusok Szénhidrogének: alifás telített (metán, etán, propán, bután, ) alifás telítetlen (etén, etin, ) aromás (benzol, toluol, naftalin) Oxigéntartalmú vegyületek: hidroxivegyületek
KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 2000
 Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Megoldás 000. oldal KÉMIA ÍRÁSBELI ÉRETTSÉGI- FELVÉTELI FELADATOK 000 JAVÍTÁSI ÚTMUTATÓ I. A NITROGÉN ÉS SZERVES VEGYÜLETEI s s p 3 molekulák között gyenge kölcsönhatás van, ezért alacsony olvadás- és
Nukleinsavak építőkövei
 ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
ukleinsavak Szerkezeti hierarchia ukleinsavak építőkövei Pirimidin Purin Pirimidin Purin Timin (T) Adenin (A) Adenin (A) Citozin (C) Guanin (G) DS bázisai bázis Citozin (C) Guanin (G) RS bázisai bázis
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) dihidrofolsav tetrahidrofolsav N CH 2 N H H 2 N COOH
 folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
folsav, (a pteroil-glutaminsav vagy B 10 vitamin) 2 2 2 2 pirimidin rész pirazin rész aminobenzoesav rész glutaminsav rész pteridin rész dihidrofolsav 2 2 2 2 tetrahidrofolsav 2 2 2 2 A dihidrofolát-reduktáz
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig
 A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
A pillangóktól a folsavon és a metotrexáton át a programozott sejthalálig Kezdeti lépések (opkins 1889-95): Lepkék szárnyából sárga és narancsvörös pigmentet izolált: megállapította hogy ezek hidroxipurinokhoz
Szerves kémia kommunikációs dosszié SZERVES KÉMIA ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ
 SZERVES KÉMIA ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŐSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyzı, óraszám, kreditérték
SZERVES KÉMIA ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŐSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI TANSZÉK Miskolc, 2008 Tartalomjegyzék 1. Tantárgyleírás, tárgyjegyzı, óraszám, kreditérték
KÉMIA FOGORVOSTAN HALLGATÓKNAK II. VIZSGA TÉTELSORA
 KÉMIA FOGORVOSTAN HALLGATÓKNAK II. VIZSGA TÉTELSORA ÁLTALÁNOS KÉMIA 1. Az atomok felépítése. Tömegszám, rendszám. Kémiai elemek, vegyületek. Izotópok. Radioaktivitás, radioaktív izotópok. Avogadro-állandó.
KÉMIA FOGORVOSTAN HALLGATÓKNAK II. VIZSGA TÉTELSORA ÁLTALÁNOS KÉMIA 1. Az atomok felépítése. Tömegszám, rendszám. Kémiai elemek, vegyületek. Izotópok. Radioaktivitás, radioaktív izotópok. Avogadro-állandó.
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Szerves kémiai reakciók csoportosítása Kinetikus és termodinamikus kontroll Szubsztituens hatások Sav-bázis tulajdonságokat befolyásoló tényezők
 Alapismeretek 4. Szerves kémiai reakciók csoportosítása Kinetikus és termodinamikus kontroll Szubsztituens hatások Sav-bázis tulajdonságokat befolyásoló tényezők Reaktivitás és stabilitás Kísérlettervezés
Alapismeretek 4. Szerves kémiai reakciók csoportosítása Kinetikus és termodinamikus kontroll Szubsztituens hatások Sav-bázis tulajdonságokat befolyásoló tényezők Reaktivitás és stabilitás Kísérlettervezés
Budapest, szeptember 5. Dr. Tóth Tünde egyetemi docens
 SZERVES KÉMIA I. levelező B.Sc. képzés, kód: BMEVESZAL17 Tantárgy követelményei 2016/2017. tanév I. félév Az alaptárgy heti 2,5 óra (páratlan héten 2 óra, páros héten 3 óra) előadásból és ezzel integrált
SZERVES KÉMIA I. levelező B.Sc. képzés, kód: BMEVESZAL17 Tantárgy követelményei 2016/2017. tanév I. félév Az alaptárgy heti 2,5 óra (páratlan héten 2 óra, páros héten 3 óra) előadásból és ezzel integrált
Víz. Az élő anyag szerkezeti egységei. A vízmolekula szerkezete. Olyan mindennapi, hogy fel sem tűnik, milyen különleges
 Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Az élő anyag szerkezeti egységei víz nukleinsavak fehérjék membránok Olyan mindennapi, hogy fel sem tűnik, milyen különleges A Föld felszínének 2/3-át borítja Előfordulása az emberi szövetek felépítésében
Helyettesített Szénhidrogének
 elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
elyettesített Szénhidrogének 1 alogénezett szénhidrogének 2 3 Alifás halogénvegyületek Szerkezet Kötéstávolság ( ) omolitikus disszociációs energia (kcal/mol) Alkil-F 1,38 116 Alkil-l 1,77 81 Alkil-Br
Szemináriumi feladatok (alap) I. félév
 Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szemináriumi feladatok (alap) I. félév I. Szeminárium 1. Az alábbi szerkezet-párok közül melyek reprezentálják valamely molekula, vagy ion rezonancia-szerkezetét? Indokolja válaszát! A/ ( ) 2 ( ) 2 F/
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 3. Alifás szén-szén egyszeres kötések kialakítása báziskatalizált reakciókban Kovács Lajos 1 C-H savak Savas hidrogént tartalmazó szerves vegyületek H H 2 C α C -H H 2
Szerves kémiai szintézismódszerek 3. Alifás szén-szén egyszeres kötések kialakítása báziskatalizált reakciókban Kovács Lajos 1 C-H savak Savas hidrogént tartalmazó szerves vegyületek H H 2 C α C -H H 2
Szénhidrát-alapú koronaéterek szintézise és alkalmazása enantioszelektív reakciókban
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁYI EGYETEM SZERVES KÉMIAI TECLÓGIA TASZÉK Szénhidrát-alapú koronaéterek szintézise és alkalmazása enantioszelektív reakciókban PhD. dolgozat Készítette: Bakó Tibor Témavezető:
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDMÁYI EGYETEM SZERVES KÉMIAI TECLÓGIA TASZÉK Szénhidrát-alapú koronaéterek szintézise és alkalmazása enantioszelektív reakciókban PhD. dolgozat Készítette: Bakó Tibor Témavezető:
Feladatok haladóknak
 Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Megoldások H136. Az elektrolízis során vízbontás történik, melynek bruttó egyenlete:
Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Megoldások H136. Az elektrolízis során vízbontás történik, melynek bruttó egyenlete:
Budapest, február 1. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2017 tanév II. félév Az alaptárgy heti 3 óra ( hetente
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2017 tanév II. félév Az alaptárgy heti 3 óra ( hetente
Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel
 Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel Benke Zsanett, Nonn Melinda, Fülöp Ferenc, Kiss Loránd Szegedi Tudományegyetem, Gyógyszerkémiai Intézet
Funkcionalizált, biciklusos heterociklusok átalakításai sztereokontrollált gyűrűnyitó metatézissel Benke Zsanett, Nonn Melinda, Fülöp Ferenc, Kiss Loránd Szegedi Tudományegyetem, Gyógyszerkémiai Intézet
Budapest, február 1. Dr. Nagy József egyetemi docens
 SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2018 tanév II. félév Az alaptárgy heti 3 óra ( hetente
SZERVES KÉMIA II. B.Sc. képzés, kód: BMEVESZA401 Válogatott fejezetek a szerves kémiából II. B.Sc. képzés, kód: BMEVESKA003 Tantárgy követelményei 2017/2018 tanév II. félév Az alaptárgy heti 3 óra ( hetente
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
KARBONIL-VEGY. aldehidek. ketonok O C O. muszkon (pézsmaszarvas)
 KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
KABNIL-VEGY VEGYÜLETEK (XVEGYÜLETEK) aldehidek ketonok ' muszkon (pézsmaszarvas) oxocsoport: karbonilcsoport: Elnevezés Aldehidek szénhidrogén neve + al funkciós csoport neve: formil + triviális nevek
5. Előadás Nukleinsavak kimutatása, szekvenálás
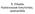 5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
5. Előadás ukleinsavak kimutatása, szekvenálás A nukleinsav kimutatás etidiumbromid 3,8-diamino-5-etil-6-fenil-fenantrédiumbromid λ g =254-366 nm λ e =590 nm 2 2 + C25 Br - X + C3 C3 C3 C (C3)2 + (C2)3
Szerves kémiai szintézismódszerek
 Szerves kémiai szintézismódszerek 7. Átrendez dések. Szén-nitrogén kötések kialakítása. Kovács Lajos 1 Átrendez dések elektronhiányos szénre 1. A Wagner-erwein-átrendez ı dés 3 C 3 C 3 C 1 3 C 3 C 3 C
Szerves kémiai szintézismódszerek 7. Átrendez dések. Szén-nitrogén kötések kialakítása. Kovács Lajos 1 Átrendez dések elektronhiányos szénre 1. A Wagner-erwein-átrendez ı dés 3 C 3 C 3 C 1 3 C 3 C 3 C
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
A tételek: Elméleti témakörök. Általános kémia
 A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
A tételek: Elméleti témakörök Általános kémia 1. Az atomok szerkezete az atom alkotórészei, az elemi részecskék és jellemzésük a rendszám és a tömegszám, az izotópok, példával az elektronszerkezet kiépülésének
Savak bázisok. Csonka Gábor Általános Kémia: 7. Savak és bázisok Dia 1 /43
 Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
Savak bázisok 121 Az Arrhenius elmélet röviden 122 BrønstedLowry elmélet 123 A víz ionizációja és a p skála 124 Erős savak és bázisok 125 Gyenge savak és bázisok 126 Több bázisú savak 127 Ionok mint savak
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Krajsovszky Gábor. Heterociklusos vegyületek
 Krajsovszky Gábor: eterociklusos vegyületek IB: 978-615-5722-04-2 Krajsovszky Gábor Felelős kiadó: Krajsovszky Gábor Lektor: Mándity István emmelweis Egyetem Gyógyszerésztudományi Kar zerves Vegytani Intézet
Krajsovszky Gábor: eterociklusos vegyületek IB: 978-615-5722-04-2 Krajsovszky Gábor Felelős kiadó: Krajsovszky Gábor Lektor: Mándity István emmelweis Egyetem Gyógyszerésztudományi Kar zerves Vegytani Intézet
