BELSİ ÉS KÜLSİ TÉNYEZİK HATÁSA A VÖRÖSVÉRSEJTEK (vvs) LIPIDPEROXIDÁCIÓS (LP) ÉS ANTIOXIDÁNS FOLYAMATAIRA
|
|
|
- Károly Kerekes
- 9 évvel ezelőtt
- Látták:
Átírás
1 BELSİ ÉS KÜLSİ TÉNYEZİK HATÁSA A VÖRÖSVÉRSEJTEK (vvs) LIPIDPEROXIDÁCIÓS (LP) ÉS ANTIOXIDÁNS FOLYAMATAIRA (szarvasmarhákban, juhokban, kutyákban és patkányokban végzett vizsgálatok) Vajdovich Péter Témavezetı: Mézes Miklós tanszékvezetı egyetemi tanár, a mezıgazdaságtudomány kandidátusa, Szent István Egyetem, Mezıgazdaság és Környezettudományi Kar, Takarmányozástani Tanszék 0
2 Jelölések és rövidítések jegyzéke αt. : oxidált E-vitamin αth: α-tokoferol, E-vitamin αtq: tokoferolkinon 1 O 2 : szinglet-oxigén 3HAA: 3-hidroxiantranilsav A: dehidro-alkohol vegyület (aldehid) A: dehidro-aszkorbinsav ADP: adenozin-difoszfát AH - : aszkorbát-anion AH. : mono(dehidro)aszkorbát-gyök AH 2: alifás alkohol vegyület AH 2 : aszkorbinsav Alb: albumin ALKP: alkalikus-foszfatáz ALT: alanin-aminotranszferáz AMP: adenozin-monofoszfát Amyl: α-amiláz AST: aszparaginsav-aminotranszferáz ATP: adenozin-trifoszfát BHA-butil-hidroxi-anizol BHT: butil-hidroxi-toluol Br-LOO. : bilirubin-lipidperoxid Br-LOOH: bilirubin-lipidhidroperoxid Br. : bilirubin-gyök Br: bilirubin BU: Bergmeyer-egység (-unit) C5a: komplemet-5a (kemotaktikus peptid) C9: komplemet-9 Ca: összkalcium CAT: kataláz CCl 3. : triklórmetil-szabadgyök CCl 4 : széntetraklorid CClOO 3. : triklórmetil-peroxid-szabadgyök Koleszt: összkoleszterin CK: kreatinin-foszfokináz CN: cián vagy cianid-csoport cnos: konstitutív nitrogénoxid-szintetáz CoA: koenzim-a Crea: kreatinin CuZnSOD: réz-, cinktartalmú szuperoxiddizmutáz D: dalton (molekulatömeg mértékegysége) dirbr: direktbilirubin DNS: dezoxi-ribonukleinsav DPPD: N,N-difenil-p-feniléndiamin DTNB: ditiobisz-2-nitrobenzoesav e - : eletron EDTA: etiléndiamin-tetraecetsav EKG: elektrokardiográfia EMQ: ethoxiquin (etoxi-metil-kinolin) FAD: flavin-adenin-dinukleotid Fe: vas Fe-kötı kap.: vaskötı kapacitás FeS-: vas- és kénközpontú rész FMN: flavin-adenin-mononukleotid fvs: fehérvérsejt G6P: glükóz-6-foszfát G6PD: glükóz-6-foszfát-dehidrogenáz GDP: guanozin-difoszfát GGT: γ-glutamil-transzferáz Glob: globulin GMP: guanozin-monofoszfát GS - : glutation-tiolát-anion GS. : glutationil-gyök vagy tiil-gyök GSH-Px: glutation-peroxidáz GSH-red: glutation-reduktáz GSH: redukált-glutation GSSG: oxidált-glutation, glutation-diszulfid GST: glutation-s-transzferáz GTP: guanozin-trifoszfát H + : hidrogén-ion H 2 O: víz H 2 O 2 : hidrogén-peroxid H 3 N + : protonált amingyök Hb: hemoglobin HCl: sósav HCO 3 - : hidrogénkarbonát-ion HDL: high density lipoprotein HO 2.- : perhidroxi-gyök HPETE: hidroxieikozatetraénsav Ht: hematokrit IgA: immunglobulin-a 1
3 IgG: immunglobulin-g IL-1: interleukin-1 inos: indukálható nitrogénoxid-szintetáz K + : kálium-ion (koncentráció) Karb: karbamid L-NAME: N G nitro-l-arginin-metilészter L. : lipid-szabadgyök vagy lipd-alkilgyök LDL: low density lipoprotein Lipa: Lipáz LH: zsírsav LOO. : lipid-peroxidgyök LOOH: lipidhidroperoxid LP: lipidperoxidáció M: mól MAC: membrane attack complex (membránkárosító komplex) MCH: mean corpuscular hemoglobin, a vvs-ek átlagos hemoglobintartalma MCHC: mean corpuscular hemoglobin concentration, a vvs-ek átlagos hemoglobinkoncentrációja MCV: mean corpuscular volume, a vvs-ek átlagos térfogata MDA: malondialdehid Me: átmeneti fém MnSOD: mangántartalmú szuperoxiddizmutáz MPO: mieloperoxidáz MTDQ: 5,6-metilén-bisz/-2,2,3-trimetil- 1,2-dihidrokinolin n= töltések száma NAD + : oxidált nikotinamidadenindinukleotid NADH + H + : redukált nikotinamidadenindinukleotid NADP + : oxidált nikotinamidadenindinukleotid-foszfát NADPH + H + : redukált nikotinamidadenindinukleotid-foszfát NAPH-ox: redukált nikotinamidadenindinukleotid-foszfát-oxidáz NO. : nitrogénoxid-gyök NO: nitrogénoxid NOS: nitrogénoxid-szintetáz O 2.- : szuperoxid-aniongyök O 2 : oxigénmolekula OH - : hidroxil-anion-csoport OH.- : hidroxil-gyök ONO 2.- : peroxinitrit-anion-gyök OD: optikai sőrőség (denzitás) OD 532 : 532 nm-en mért optikai sőrőség összbr: összbilirubin oxidált-6pg: oxidált 6-foszfoglukonát P ~ : makroergfoszfát-csoport pco 2 : parciális széndioxid-nyomás PGE 2 : prosztaglandin-e 2 PGF 2 : prosztaglandin-f 2 PGG 2 : prosztaglandin-g 2 PGH 2 : prosztaglandin-h 2 PGI 2 : prosztaciklin PHS: pulmonáris hipertenzió szindróma Pi: anorganikus-foszfát po 2 : parciális oxigén-nyomás PUFA: többszörösen telítetlen szabadzsírsav (polyunsaturated fatty acid) Q: ubi(szemi)kinon QH. : szemiquinon-gyök R - : anion-molekula R-CH 2 OH: alkoholmolekula R-CHO: aldehidmolekula R. : szabadgyök vagy lipid-szabadgyök RNS: ribonukleinsav ROH: hidroxilipid ROI: reaktív oxigén intermedier ROOH: lipid-hidroperoxid SeGSH-Px: szeléntartalmú glutationperoxidáz SH-: szulfhidril-csoport SOD: szuperoxid-dizmutáz TBA: tiobarbitursav Thrc: thrombocyta TNF: tumor nekrózis faktor TP: összfehérje ttkg: testtömeg kilogram TXA 2 : tromboxán-a 2 V minta : a minta össztérfogata V össz : az oldatok össztérfogata vvs: vörösvérsejt X - : halid-anion XO - : hipohalit-ion vagy halogenit-ion 2
4 I. BEVEZETÉS I. 1. A téma jelentısége A szabadgyökök hatásait széles körben vizsgálják. Az utóbbi idıben a kutatások nyomán a szabadgyökök vizsgálata, szinte önálló tudományterületté fejlıdött. A kutatások elsısorban alapkutatási, kísérleti jellegőek (101) (323) (324) (325) (399), másodsorban alkalmazott szintőek. Ezek nagy része humánorvoslási vonatkozásúak (61) (149) (320) (400), azonban az elmúlt évben azonban az agrár és veteriner szférában is figyelemre méltó eredmények születtek (14) (15) (171) (287) (338), de a biológiai, a növénytani, a vegyészeti és a gyógyszertani tudományterületeken belül is egyre nagyobb tért hódítanak a gyökös folyamatokkal kapcsolatos kutatások. A szabadgyökös reakciók a biológiai rendszerek számos élettani biokémiai folyamatában részt vesznek a reakciók fı-, vagy részlépéseiben, de nem csak élettani szerepük lehet. A szabadgyökök keletkezhetnek ugyanis számos idegen anyag vagy gyógyszer hatására fıvagy melléktermékként, és megjelenésükkel alapvetıen befolyásolhatják a biológiai rendszerek mőködését. A szabadgyökök reakciói általában a többi biokémiai folyamathoz hasonlóan a szervezetben szabályozottan zajlanak le, de kóros mértékben fokozódva, vagy csökkent módon is végbe mehetnek. A szabadgyökös folyamatok szoros összefüggésben állnak a sejtek anyagcseréjével. A legelterjedtebb gyökök az oxigén eredető ún. reaktív oxigén intermedierek (ROI), amelyek elsısorban a légzési lánc lépéseiben keletkeznek. Ezek "in loco", sejten belül képesek a funkciójukat ellátó molekulákkal reagálni, esetleg azokat károsítani. Egy-egy gyökös reakció azonban nem marad helyhez kötötten. Láncreakciók sorozata alakul ki és terjed szét a környezı szövetekben, ill. a szervezetben, ami révén további gyökök képzıdnek és befolyásolják a természetes biokémiai reakciókat, ezáltal jelentısen károsíthatják az adott biológiai rendszert. A metabolikus folyamatokon belül az ROI-k zsíranyagforgalommal való kapcsolata azért emelhetı ki, mert a sejtorganellumok alaphártyája az ún. lipid kettısréteg nagy mennyiségő többszörösen telítetlen zsírsavat (polyunsaturated fatty acid, PUFA) tartalmaz, és a PUFA-k a legnagyobb mértékben vannak kitéve az ROI-k károsító hatásainak. A többszörösen telítetlen zsírsavakban lévı kettıs kötések láncolata "jó talajt" biztosít a gyökökként mőködı molekulák vagy molekulafragmensek kötıdéséhez. A lipidek gyökreakciói ezért speciális szerepet játszanak az említett folyamatokban, oxidációjuk során oxid-, peroxid-, hidroperoxidderivátumok képzıdnek. Ezt a folyamatot nevezzük lipidperoxidációnak (LP). A sejtek és a sejtorganellumok hártyáinak károsodása permeabilitási zavarokat hozhat létre a sejten belül, illetve a sejt és a külsı környezet között. A védekezı rendszer enzimatikus vagy nem enzimatikus tagjai azonban olyan széles körben mőködnek sejt- és szövetszinten egyaránt, hogy élettani körülmények között nem találkozunk jelentıs mértékő membránkárosodással. A védekezı mechanizmust antioxidáns rendszernek nevezzük, mert a kóros oxidáció megelızését, esetleg hatástalanítását célozza. E rendszer egyes elemei (pl. az E-vitamin, a β-karotin stb.) a már képzıdött szabadgyökök 3
5 "eltakarításáért" felelısek, ezért ezeket "scavenger"-eknek nevezzük (scavenger = söprögetı). A gyökös folyamatok felgyorsulása, esetleg lelassulása, és/vagy a védekezı rendszer elégtelensége kóros folyamatokat eredményezhet. A mezıgazdasági és az állatorvosi kutatásokban Magyarországon eddig elsısorban az élettani reakciók, a szelén- és az E-vitamin-hiányos betegségek, valamint egyes toxikológiai vonatkozások vagy speciális kórképek tanulmányozása keretében foglalkoztak a szabadgyökös reakciókkal, illetve változásaival (47) (171) (172) (257) (284) (338) (404) (405) (475) (476). E korábbi kutatásokhoz kívántam csatlakozni vizsgálataimmal, melyek célját az alábbiakban foglalom össze. I. 2. A kitőzött célok és a megoldandó feladatok Kutatómunkámban a vörösvérsejtek (vvs) egyes LP-s reakciókban részt vevı paraméterei alapján kívántam adatokat nyerni a szervezetben zajló szabadgyökös folyamatokról élettani és kóros esetekben. A vizsgálatokat részben kérıdzıkön (szarvasmarha, juh), részben kutyákon, valamint két modellkísérlet esetében patkányokon végeztem. Négy fı témakörben végeztem vizsgálatokat: 1. a szarvasmarhák és a kutyák vvs-jeiben zajló LP-s reakciók kor függı és a kutyák esetében ivar függı vizsgálata; 2. a juhok és a kutyák vvs-jeiben a xenobiotikumok (CCl 4, alloxán) hatására bekövetkezı LP-s reakciók vizsgálata; 3. a hypoxia - reperfusio okozta fokozott LP-s reakciók vizsgálata kutyák és patkányok vvs-jeiben; 4. egyes anyagforgalmi és szervi kórfolyamatok hatására bekövetkezı LP-s reakciók vizsgálata szarvasmarhák és kutyák vvs-jeiben. A hypoxia-reperfusiós vizsgálatok fejezetben, a kutya mellett szereplı faj nem kérıdzı, mint a többi fejezetben, hanem a patkány. Ebben a két kísérletben a mőtéti megoldások bonyolultsága miatt a patkány alkalmasabb fajnak bizonyult. Olyan módszereket választottam, amelyek gyorsak, viszonylag könnyen, kis mőszerezettséggel elvégezhetık és rutinvizsgálatokban felhasználhatók. Ezen okokból kutatási módszerként több lehetıség közül állati vérmintákból a vvs-ek feldolgozása került elıtérbe. Ennek részletes okait az alábbiakban foglalom össze: 1. A vérminták vétele rutinszerő és egyszerően kivitelezhetı. 2. A vvs-ek membránja gazdag PUFA-kban, amelyek érzékenyek az LP-s folyamatokra és ezek a reakciók (elsıdlegesen vagy másodlagosan) viszonylag gyorsan kialakulnak bennük. 3. A vvs-ek a szabadgyökök szempontjából és a bennük lévı antioxidánsok révén raktározó és szállító szerepet is betöltenek, hiszen mind a bennük keletkezı gyökös vegyületek, mind az antioxidánsok a vérkeringés révén idıben és térben különbözıen fejthetik ki hatásaikat. A vvs-ek minden szervbe és szövetbe eljutnak, ahol LP-s reakciók folyhatnak, így a keletkezett gyökök a vvs-ek révén eljuthatnak a keletkezés helyérıl, egy addig még fokozott gyökös reakcióban részt nem vevı területre. Ezekbıl a megfontolásokból kiindulva érthetı, hogy nemcsak a fokozott LP-ben részt vevı szövetekbıl, hanem a vvs-ekbıl mérhetı gyökök, ill. a gyökreakciók elemei is jelzik a 4
6 szervezet szabadgyökös reakcióit. Az antioxidánsokat a szervezet szükség esetén azonnal mozgósítja, és azok felhasználódnak az adott igényeknek megfelelıen az adott helyen, így a vvs-ekben az antioxidáns enzimek aktivitásváltozása és az antioxidáns szubsztrátok koncentrációváltozása is jelzi a megváltozott szöveti, szervezeti igényt. 4. Egyes kóros folyamatokban, a vvs-ekbıl vizsgálható szabadgyökös paraméterek elemzése információt szolgáltathat a kórképek súlyosságának megítéléséhez is. A kísérletek során a szabadgyökös folyamatok vizsgálatára alkalmas egyszerőbb laboratóriumi módszereket alkalmaztam. Ezeket a biokémiai paramétereket a vvs-ek hemolizátumából végeztem. A szabadgyökös paraméterek vizsgálatát kiegészítettem a vérbıl, tejbıl, takarmányokból mérhetı egyéb biokémiai, valamint egyes esetekben hematológiai paraméterekkel, sıt a kísérleti alanyok egyéb élettani paramétereinek és klinikai tüneteinek vizsgálatával. A kísérletek elrendezése során alapelvként szerepelt, hogy a laboratóriumi paraméterek változását nem egy elıre meghatározott normálértékhez hasonlítottam, hanem minden esetben a vizsgálati eredmények egymáshoz viszonyított változását értékeltem. Az alapértékek felvétele céljából általában minden beavatkozás elıtt mintavétel történt, majd a beavatkozások után további mintákat vettem azok hatásának megállapítása céljából. 5
7 6
8 II. IRODALMI ÁTTEKINTÉS II. 1. A szabadgyök fogalma Ismeretes, hogy a legtöbb kémiai anyag elektronorbitálján két elektron kering, amelyeknek ellenkezı elıjelő spinjük (azaz pályamenti mozgásuktól független saját impulzusmomentumuk) van. Szabadgyöknek nevezünk minden molekulát vagy molekula-fragmenst, amelynek külsı orbitálján egy párosítatlan elektron van (130) (398). Mivel az elektronok párképzıdésre hajlamosak, a párosítatlan elektron jelenléte miatt a szabadgyökök kifejezett reaktivitást mutatnak, és mint gyökök, rövid az élettartamuk. Biradikálisnak nevezzük azokat a molekulákat, amelyek külsı elektronhéjukon két párosítatlan elektront tartalmaznak, ilyen pl. a molekuláris oxigén és a szuperoxid aniongyök (O -. 2 ) is (398). Ismeretes a gyökion elnevezés is, ami arra utal, hogy az adott gyök pozitív vagy negatív töltéső (H 3 N + - protonált amingyök, O szuperoxid aniongyök) (398). A kémiai kötés hasadhat szimmetrikusan (A:B A. + B. ), amikor szabadgyökök keletkeznek, vagy aszimmetrikusan (A:B A - + B + ), amikor ionok jönnek létre. II. 2. Az oxigén eredető szabadgyökök és a képzıdésükhöz vezetı néhány folyamat A molekuláris oxigén alapállapotban "biradikális", külsı orbitálján két paralel spinő párosítatlan elektront tartalmaz. A paralel elektronok spinelrendezıdése megakadályozza az elektronpár direkt addícióját egy adott molekulához, meggátolva a kémiai kötés képzıdését. A kötésképzıdéshez elıbb egy elektronspin megfordulásának kell létrejönnie. Mivel a spin megfordulási folyamata lassú, a molekuláris oxigén alapállapotában relatíve gyenge oxidáns. A kémiai reakciók létrejöttéhez aktiválás szükséges. Az aktiválás révén az oxigénmolekulából elıbb aktiválási komplexek, oxigén eredető gyökök keletkeznek, ezek már gyors reakciókra képesek. Az oxigén reaktív közbülsı termékei az ún. reaktív oxigén intermedierek (ROI) (149). A molekuláris oxigénbıl keletkezı gyökök az élettelen természetre és az élıvilágra egyaránt nagy veszélyt jelenthetnek. Az élettelen természetben elıforduló szabadgyökös reakciók: pl. a motorokban a benzin vagy a gázolaj égése, a szmogképzıdés, a fémek és a mőanyagok korróziója, a zsírok, az olajok, a vaj avasodása (210). Az oxigén komplett, tetravalens (4 elektronnal történı) redukciója során víz keletkezik: O 2 4e - + 4H + 2H 2 O. Ha azonban univalens (1 elektronos) redukcióban vesz részt, ami a természetben energetikai okokból könnyebben végbemegy, akkor ROI keletkezik, mint pl. a szuperoxid anion gyök (O 2 -. ). A divalens (2 elektronos) redukció során pl. a szinglet-oxigén, a hidrogén peroxid (H 2 O 2 ) és a hidroxil gyök (OH. ) keletkezik (266). Az O 2 uni-, és divalens redukciója az alábbiakban látható: O 2 +e - O 2.- +e - +2H + H 2 O 2 +e - +H + -H 2 O OH.- +e - + H + H 2 O. Kismennyiségő ROI képzıdése történhet enzimatikus úton, például olyan enzimek révén, amelyek képesek az oxigén (energetikailag kedvezıtlenebb) divalens és tetravalens redukciójára. Az egyik legfıbb ilyen enzim a citokrómoxidáz, amely az 7
9 oxigén tetravalens redukcióját hajtja végre a sejtlégzés során. Ez a folyamat az ROI-k keletkezésének egyik (fı) forrása. További ROI-k esetenként nagyobb mennyiségben egyéb oxido-redukciós enzimatikus folyamatok (pl. a xantin-oxidáz katalizálta reakció) révén keletkeznek a sejtorganellumokban, a thrombocyták és a fagocita sejtek mőködése során stb. (329). Az élılényekben az ROI-k másik forrása nem enzimatikus úton jön létre a különbözı kémiai vegyületek autooxidációja, vagyis az O 2 univalens redukciója révén, pl. az ubiszemikinon O 2 -vel zajló reakciója során O 2.- képzıdik (180). II Szuperoxidanion-gyök (O 2.- ) Jelentısebb mennyiségő O 2.- képzıdik nem enzimatikus úton (pl. a hidrokinonokból (348)), és enzimatikus úton a molibdoflavoprotein-oxidázok (pl. a xantin-oxidáz) révén. A xantin-oxidáz hatelektronos redukált formája mobilizálható elektronjait két kételektronos és két egyelektronos lépésben adhatja le. A hat- és a négyelektronos redukált forma H 2 O 2 -ot, míg a két- és az egyelektronos redukált forma O 2.- -t képez. Ha a szubsztrát (xantin) koncentrációja nagy, akkor megmarad az enzim redukált formája. Ez az enzimnek az O 2 -vel zajló reakciója révén a H 2 O 2 képzıdésének kedvez. Az alkalikus ph, az alacsony xantin-, és a magas O 2 -koncentráció az O 2.- képzıdését erısíti (221). Az O 2.- a flavoprotein-dehidrogenázok mőködése révén is képzıdhet. Ilyen enzimek pl. a mikroszómális NADPH-citokróm-P 450 (497), a mitokondriális NADHdehidrogenáz (496), a dihidroorotsav-dehidrogenáz (158), a ribulóz-1,5-difoszfátkarboxiláz (55) és az ubiszemikinon (158). A gyökképzı reakciókban katalizátor hatású fémek (pl. vas) mellett egyes enzimek is részt vesznek. A NADPH-citokróm-P 450 -reduktáz révén O 2.- keletkezhet NADPH és ADP-hez kapcsolódott vas (Fe 3+ ) jelenlétében a mikroszómákban és a liposzómákban (156). Ez az enzim (NADPH-citokróm-P 450 -reduktáz) az alábbi reakciót katalizálja (383): 2O 2 + NADPH NADP + + H + + 2O 2.-. Izolált májsejtmagok képesek voltak a NADPH jelenlétében O 2.- -t képezni, Patton és mtsai. szerint ennek a hátterében egy FAD-monooxigenáz enzim áll (381). Az O 2.- keletkezhet különbözı vegyületek autooxidációja esetén. Autooxidációra képes vegyület pl. a mitokondriumokon belül a légzési lánc tagja a redukált citokróm-c (91), a vvs-ekben a hemoglobin (346), az izomsejtekben a mioglobin (187), valamint egyéb sejtekben a leukoflavinok (29), a tetrahidropterinek (361), a katekolaminok (347), a polihidrofenolok (313) és a tiolok (349). Az O 2.- maga kevésbé reaktív, de az átmeneti fémeket, azok komplexeit és egyéb organikus szubsztrátokat oxidálni képes. Kapcsolódhat egyes fémekhez így más reaktívabb ROI keletkezését készítheti elı. Az O 2.- perhidroxi gyökké (HO 2.- ) való alakulása, szintén könnyen végbemegy, ha az O 2.- a vizes közegbıl a lipidfázisba jut. A lipidmicellák, membránok kisebb ph-jú környezete teremti meg a protonáció feltételeit. A membránok felszínének polianionokat tartalmazó része az ellentétes töltéső H + - ionokat vonzza a felszín közelébe, így az O 2 -. protonálódik perhidroxi gyökké (HO 2.- ): H + + O HO2.- (167). A képzıdött HO 2.- könnyen reagál tovább linolén és arachidonsavval (179). 8
10 II Hidrogén-peroxid (H 2 O 2 ) A H 2 O 2 képzésében a legfontosabbak az intracelluláris flavin-kötı oxidázok, és a flavoenzimek (337). Ezeknek a szubsztrátja az O 2, végtermékük a H 2 O 2 és csak elenyészı mennyiségő O 2.- -t képeznek (459). Ezek közé az enzimek közé tartoznak a majdnem minden sejtben a mitokondriumok külsı membránján lévı monoaminooxidázok (162). Néhány H 2 O 2 -t képzı flavoprotein a peroxiszómákban fordul elı (490). Ilyen az emlısık peroxiszómáiban elıforduló urát-oxidáz, aminek "magjában" egy réztartalmú cuproprotein helyezkedik el (128). Hidrogén peroxidot képzı flavoenzimek közé tartozik továbbá a glikolát-oxidáz, az aminosav-oxidáz és a zsírsav-oxidáz is (422). Hidrogén-peroxidot képzı enzimek az amin-oxidázok és a tiol-oxidázok (288) is. Az egyik legfontosabb H 2 O 2 -képzı enzim azonban a szuperoxid-dizmutáz (SOD) (166). II Hidroxil(anion)-gyök (OH.- ) Az OH.- a legreaktívabb oxigéngyök. Ez az ROI az O 2 -bıl és az O 2.- -bıl képzıdik a vas- vagy rézkatalizálta Haber-Weiss reakció révén (59) (196). A biológiai rendszerekben a vas szállító vagy raktározó fehérjékhez kapcsolódik (transzferrin, ferritin), és ezekben a formákban nem képes katalizálni az OH.- -t képzı reakciókat (202). Az O 2.- képes a ferritinbıl felszabadítani a vasat, míg a transzferrinbıl erre nem képes (57). A sejtekben a vas az ATP-hez, a GTP-hez és a citráthoz kötıdik. Ezek a vaskelátok az Fe 3+ gyorsabb redukciója révén még a szabad vasnál is jobban katalizálják az OH. -t képzı reakciót. Ezek a kelátok vízben jelentısen jobban oldhatók, mint a szabad vas, ami valójában Fe(H 2 O) 6 3+ precipitátum formájában fordul elı. Egyes megfigyelések szerint a szabad vas koncentrációját csökkentı, azt kelát formájában megkötı anyagok, mint pl. az etiléndiamin-tetraecetsav (EDTA), bár csökkentik az Fe 3+ -szintet, azonban az OH.- képzıdését nem (199). Az említett OH.- képzıdésére vezetı reakcióút az ún. Haber-Weiss-reakció (167) (196): O H 2 O 2 O 2 + OH - + OH.-. Ebben az esetben a reakcióhoz szükséges H 2 O 2 a molekuláris oxigén divalens redukciójával a glükóz-oxidáz mőködése révén vagy az O 2.- -bıl a SOD hatására (2O H + H 2 O 2 + O 2 ) keletkezik. Ebben a formában csak néhány esetben alakulnak ki a fenti reakciók, fıként ha katalizálja más vegyület, pl. a tiolok (423). A Haber-Weiss reakció lejátszódhat a májsejtek mikroszómáinak nem specifikus alkohol-oxidázának mőködése révén (93), valamint a neutrophil granulocytákban (415) is. Az alloxán diabetogén hatása is gyaníthatóan e reakció révén keletkezı OH.- miatt alakul ki (214). A Haber-Weiss-reakció az élı szervezetekben lassú folyamat, de fémkatalízis hatására felgyorsul. Ez következik be pl. a laktoferrinben lévı vas (Fe 2+ ) (6) és a réz (Cu 2+ ) (433) hatására. A vas nagymértékben felgyorsítja a reakciót pl. EDTÁ-val kötött formájában (Fe-EDTA), vagy a hem részeként porfirin-vas formában (200). A fémkatalizálta Haber-Weiss reakció az ún. Fenton-reakció (167): O Me (n+1)+ Me n+ + O 2 Me n+ + H 2 O 2 Me (n+1)+ + OH.- + OH - O H 2 O 2 O 2 + OH.- + OH - (Me = átmeneti fém, n = + töltések száma). 9
11 Ha a vas a katalízisért szereplı átmeneti fém, a Fenton-reakció az alábbiak szerint alakul (18): O Fe 3+ Fe 2+ + O 2 Fe 2+ + H 2 O 2 Fe 3+ + OH.- + OH - Ezen az úton jelentıs mennyiségő OH.- keletkezhet. A Fenton-reakció analógiájára a H 2 O 2 -ot hidroperoxidok is helyettesíthetik (jelen esetben a katalízisért a vas-ion felelıs): Fe 2+ + ROOH Fe 3+ + RO. + OH -. II Alkoxi-gyökök (RO. ) Az RO. -k kevésbé reaktívak, mint a OH.-, de jelentıs lehet a károsító hatásuk fıként, ha egy H-atom áttevıdik és hidroxialkil-gyökök képzıdnek belılük: RO. + RH ROH + R. (143). II Szinglet-oxigén ( 1 O 2 ) Az 1 O 2 akkor képzıdik, amikor energia-abszorpcióval a molekuláris oxigén két párosítatlan elektronja közül az egyik spin-inverzióval egy nagyobb orbitálra kerül (266). A szinglet-oxigén képzıdésének legjelentısebb módja, amikor a laktoperoxidáz (252), a kloroperoxidáz (251), vagy a mieloperoxidáz (262) a H 2 O 2 -t halidok közremőködésével bontja. Az 1 O 2 képzıdésében részt vesz továbbá, a prosztaglandinendoperoxid-szintáz (87), a citokróm-p 450 -enzimrendszer (86) és a tormaperoxidáz is (amely a késıbbiekben említésre kerülı malondialdehid oxidációját is katalizálja) (504). Szinglet-oxigén keletkezik a késıbb kifejtésre kerülı lipidperoxidációs reakciók terminális lépésében is: LOO. + LOO. LO + LOH + 1 O 2 (471); az oxigénnek a triplet-karboxilvegyületekkel (pl. 4-hidroxi-2,3-transznonenal /RO. /) történı reakciója révén: RO. + O 2 RO + 1 O 2 (527); valamint a xenobiotikumok NADPH-citokróm- P 450 -reduktáz által katalizált univalens redox-ciklus melléktermékeként (253), amire a késıbbiekben szintén utalok. II. 3. Az ROI-k keletkezésének sejtszintő forrásai Michaelis már 1946-ban azt feltételezte, hogy a bivalens szerves molekulák oxidációját meg kell elıznie intermedierek keletkezésének (344). Eszerint a teória szerint az O 2 redukciójából származó intermedierek univerzálisak az aerob életben, és szükségszerően létre kell jönniük olyan toxikus, erısen reaktív anyagoknak is, mint az O 2.- és a H 2 O 2. Az élı szervezetekben számos enzim és szubsztrát mőködik közre az ROI-k képzésében, de ezeknek csak egy része mutatható ki közvetlenül. A sejtek organellumaiban a szabadgyök-képzésben részt vevı fontosabb elemeket az alábbiakban foglalom össze: 10
12 II Mitokondriumok A legtöbb ROI a mitokondriumokban képzıdik, mert a mitokondriumokban zajlanak a légzési lánc lépései (66). A légzési láncban az O 2.- képzıdésének fı helye a szukcinát-dehidrogenáz-citokróm-b-szegmens (222), de az O 2 -. képzıdésében a NADHubikinon-reduktáz és az ubikinol-citokróm-c-reduktáz (85) és a flavoproteindihidroorotsav-dehidrogenáz (159) mőködése is szerepet játszik. A szabadgyökök képzıdésére vezetı reakcióutak légzési láncban való megjelenésének sematikus ábrázolása az 1. ábrán látható. 1. ábra A mitokondriumban mőködı légzési lánc sematikus ábrázolása (132) NADH FeS-FMN-FeS 2 KoenzimQ citokróm b, c 1 -FeS citokróm a és a 3 -réz O 2 FeS-FAD Szukcinil-dehidrogenáz rövidítések: NADH = redukált nikotinamid-adenin-dinukleotid FeS = nem hembıl származó vas- és kén-tartalmú fehérjeközpontok FMN = flavinadenin-mononukleotid FAD = flavinadenin-dinukleotid = szabadgyök-képzıdésre vezetı reakcióutak (az FeS-központok, a flavincsoportok és a KoenzimQ interakciói) II Peroxiszómák A peroxiszómákban a flavoproteinek, a D-amino-oxidáz, az L-α-hidroxisav-oxidáz, a zsírsav-acil-coa-oxidáz és egyes fajokban (nem primatákban) a réztartalmú húgysavoxidáz mőködése révén jön létre az ROI-k döntı hányada (317). A peroxiszómák kataláza hozza létre a H 2 O 2 nagy részét, mégis a képzıdött H 2 O %-a kijut a citoszolba (67). II Endoplazmatikus retikulum Az endoplazmatikus retikulum membránjában szintén képzıdnek ROI-k (181). Itt a flavoprotein-nadph-citokróm-c-reduktáz rendszer és a citokróm-p 450 mőködése a fıbb forrás (220). II Citoszol A citoszol enzimjei közül a xantin-oxidáz és az aldehid-oxidáz a fıbb ROI-képzık. Ezek az enzimek a sejtek által képzıdött H 2 O 2, mintegy 5%-ának képzıdéséért felelısek 11
13 (67). Itt említhetı meg, hogy a nem enzimatikus forrásokból, a tiolok autooxidációja révén szintén keletkezhetnek ROI-k, így H 2 O 2 is (349). II Sejtmag A sejtmag szintén rendelkezik energiafüggı légzési aktivitással (114). Patkány májsejtmagból (115) és ascitesbıl származó tumorsejtbıl (39) flavinokat és citokrómokat mutattak ki, melyek elektrontraszferként is mőködnek. Az említett sejtek magjaiból O 2.- és H 2 O 2 képzıdést, sıt SOD-aktivitást is kimutattak (40). II. 4. A lipidperoxidáció (LP) fogalma és folyamata A biomolekulák közül azok, amelyeknek telítetlen kettıskötései vannak (pl. acilláncok, zsírsavak, foszfolipidek, koleszterin) kifejezetten érzékenyek a patológiás gyökreakciók károsító hatásaira (448). Ennek három fı oka van: (1.) a PUFA-k α- metilén szénatomja a kettıskötések szénatomjai mellett igen könnyen reakcióba lépnek a szabadgyökökkel (131); (2.) a molekuláris oxigénnek hétszer nagyobb az oldékonysága az apoláros közegben, mint a vizes fázisban (290); (3.) a molekuláris oxigénnek külsı orbitálján párosítatlan elektronok vannak, amelyek révén az O 2 könnyen iniciálhat szabadgyökös láncreakciókat (398). A lipidek in vivo (pl. az öregedési pigmentekben található peroxidált lipidek) és in vitro (pl. a zsír avasodása) is oxidálódhatnak. Ha egy adott lipidet egy szabadgyökiniciátor segítségével hidrogénelvonással lipid-szabadgyök (R. ) állapotba hozunk, könnyebben képes reakcióba lépni a molekuláris oxigénnel. A reakció során peroxiszabadgyök (ROO. ) keletkezik. Ezt a folyamatot nevezzük lipidperoxidációnak. A peroxidációra fıleg a PUFA-k hajlamosak, mivel a kettıs kötés melletti ún. α-metilén szénatomjaik C-H kötése gyengébb, így részlegesen aktiváltnak tekinthetık. Az LP kezdeti lépéseként errıl a szénatomról történik a hidrogénelvonás. Az α-metilén szénatom hidrogénjét allil-hidrogénnek is nevezik (398). A kezdeti lépések láncreakciót indítanak el, amely a környezı molekulákat tovább károsíthatják. A lipidek autooxidációja során új C-C-kötések, és keresztkötések képzıdnek. Ezek fıképp a membránok lipid-kettısrétegének sérülését eredményezhetik. Az autooxidációt meggyorsítja az egyes fémek jelenléte, mert fokozzák a hidroperoxidok bomlását. A láncreakcióban létrejövı, a fémek által is katalizált oxidációs lépésekben részt vesznek az egyébként kevésbé reakcióképes, nem lipid-típusú, más sejt- ill. membránalkotó vegyületek. Élettani körülmények között ez azonban igen lassú folyamat, patológiás körülmények között azonban extrém felgyorsulása következhet be (132). Az LP során kelekezı ún. metastabil lipidperoxidok, aldehidek (pl. a malondialdehid), vagy más végtermékek (2-alkenálok, 4-hidroxil-2-alkenálok) is keletkeznek, amelyek noha nem szabadgyökök, mégis rendelkeznek bizonyos reaktivitással. Ezek relatív stabilitásuk révén a keringési rendszeren keresztül eljuthatnak a keletkezésük helyétıl távol esı szövetekbe, így ott is súlyos károsodásokat okozhatnak (149). 12
14 Az LP mechanizmusát a következıkben Aust és mtsai. (1982) által közöltek felhasználása alapján foglalom össze (18), a más szerzıktıl származó kiegészítéseket külön jelölöm: Az alábbiakban alkalmazott, eddig nem szereplı rövidítések: LH = zsírsav, LOOH = lipidhidroperoxid, L. = lipid-alkilgyök, LOO. = lipid-peroxigyök. II Iniciáció (bevezetı szakasz) I. lehetıség LH + O 2 L. + HO 2. Ez lipid-hidroperoxid képzıdése nélkül lejátszódó iniciáció, vagyis LOOH-independens folyamat. Ez a reakció önmagában nem zajlik le, mert kifejezetten endoterm, igen magas aktivációs energájú, élettani körülmények között ilyen nem jöhet létre, de bekövetkezhet, ha egy fémion katalizálja a folyamatot. II. lehetıség A másik esetben az iniciáció egyik reakcióalanya egy olyan lipidmolekula, amely már tartalmaz egy peroxid-csoportot, ilyen pl. a PUFA-hidroperoxid. Ebben a reakcióban PUFA-alkoxi- vagy PUFA-peroxi-gyökök keletkeznek. LOOH szabadgyök A lipid-hidroperoxidok ilyen típusú reakciója az ún. terminális homolízis. Önmagában szintén lassú folyamat, annak ellenére, hogy következményesen iniciált reakció, és a katalízisben szereplı részben aktivált komponensek már eleve jelen vannak. E folyamatot is felgyorsítja a fémkatalízis. A reakcióban részt vevı vas pl. az oxidált hembıl származhat. II Propagáció (tovaterjedés szakasza) Az iniciáció után a propagáció következik amely több lépést foglal magában és közben nagyszámú szabadgyök jön létre. L. + O 2 LOO. LOO. + LH LOOH + L. Ha az iniciáció hidrogénelvonással történt, és PUFA-alkil-gyök jött létre, a propagáció során következı lépésként arra két oxigénatom kapcsolódik. A propagáció lezajlása függ a reakcióelegyben lévı oxigén parciális nyomásától is. Ez alapján tehát, a lipidperoxidáció propagációs lépése magában foglalja a PUFAmetilén-hidrogén elvonását a PUFA-peroxigyök által. Ennek a rekciónak a terméke a PUFA-hidroperoxid és a PUFA-alkilgyök. A PUFA-alkilgyökhöz ezután oxigén kapcsolódik és újraképzıdik a PUFA-peroxigyök. A propagáció egyik módosulata során egy PUFA-peroxigyök belülrıl generál egy cirkulációs folyamatot és PUFA-endoperoxid-gyök jön létre. Ez az ún. belsı endoperoxid formáció. A PUFA-endoperoxid-gyökhöz O 2 kapcsolódik és PUFA- 13
15 endoperoxid-peroxigyök alakul ki. A PUFA-endoperoxid-peroxi-gyök részt vesz azután a propagáció lépéseiben hasonlóképpen, mint bármely más PUFA-peroxigyök. A belsı endoperoxid formáció és a ß-helyzető C-atomhoz történı oxigénkapcsolódás alakítja ki azt a tulajdonságot, hogy az endoperoxidok kimutathatóvá válnak a tiobarbitursavas módszerrel. Az endoperoxidok az ún. tiobarbitursav-reaktív anyagok. Felhalmozódásuk a lipidperoxidáció folyamatát és kiterjedését jelzi. A tiobarbitursavval oxo-, vagy dioxo-vegyületek is képesek reagálni, és sárgás-vöröses színő komplexet hoznak létre hevítés hatására savanyú közegben (391). II Termináció (befejezı szakasz) A harmadik fázis a termináció, amelynek végtermékei nem szabadgyökök, de rendelkeznek bizonyos reaktivitással. Ilyen stabil termékek a kilélegzett levegıbıl mérhetı etán és pentán (134) valamint a testfolydékokból és a szövetekbıl kimutatható metastabil tiobarbitursav-reaktív malondialdehid (31). További stabil végtermék például a 8-epi-prosztaglandin-F 2 -α (413) is. A biológiai membránokban a terminációs lépés reakcióiba beletartoznak a PUFAgyökök és a membránalkotók (α-tokoferol, koleszterin, glutation, fehérjék) reakciói is. Az LP összefoglaló folyamatának rövid áttekinthetı összegzése Demopoulos és mtsai. (1980) nyomán (132), a Mellékletek fejezetben található. II. 5. Az LP sejtszintő következményei A sejtekben és a szövetekben létrejövı LP-s folyamatoknak számos károsító hatása van, amik nagymértékben befolyásolják az élı szervezet mőködését, sıt gyakran morfológiai elváltozásokat is okoznak. Az alábbiakban rövid összefoglalását kívánom adni a sejtek szintjén jelentkezı LP okozta káros behatásoknak. II Membránok mikroarchitektúrájának károsodása Ez a folyamat azáltal alakul ki, hogy hidrofil részek jönnek létre az alaphártyában. A membránkárosodás olyan mértékő lehet, hogy a lipidek szénláncai megszakadhatnak és végsı következményként fokozott (esetleg csökkent) membránpermeabilitás alakulhat ki. A vvs-ek membránkárosodása következtében pl. hemolízis alakulhat ki (145). II A sejtenzimek mőködésének gátlása A sejtenzimek gátlása elsısorban a hidroperoxidok hatására következik be, pl. az izocitrát-dehidrogenáz-aktivitás szinte teljesen megszőnik a májsejtek mitokondriumaiban a vas-ionok által indukált linolénsav-hidroperoxidok károsító hatása miatt (334). A szulfhidril-(sh-) csoportok és/vagy a cisztein-tartalmú fehérjék oxidációja is közrejátszik az enzimaktivitások megváltozásában (109) (110). 14
16 II A lebontási (vég)termékek károsító hatásai A metastabil végtermékek közül a malondialdehidnek (MDA-nak) ismertek a károsító hatásai. Degradációjának két lehetséges útja van. Az egyik út az MDA oxidációja az aldehid-dehidrogenázok révén, egyéb metabolikus változások kíséretben (226), a másik út az ún. Schiff-bázisok kialakulása mellett, pl. a lizin ε-amino csoportjaival történı reakció révén jöhet létre (103). Ebben a reakcióban keresztkötések alakulhatnak ki különbözı enzimeken belül is. Kimutatták, hogy pl. a ribonukleáz-a-ban keresztkötések alakultak ki az MDA hatására csakúgy, mint más LP-t iniciáló anyag jelenlétében. II Fehérjék és nukleinsavak károsodása Az albuminban, ami jelentıs mennyiségő PUFA-t szállíthat, hasonlóan egyéb fehérjékhez, szintén keresztkötések alakulhatnak ki az LP hatására. Más amino csoportot tartalmazó anyagok esetében is létrejöhetnek ezek a reakciók, pl. RNS-ben, DNS-ben stb. A keresztkötéses sejtszintő komponensek fluoreszcens tulajdonságai hasonlítanak a lipofuszcin (idıs kori pigment) tulajdonságaira (101). II. 6. A szabadgyökökkel szembeni védekezés és elemeinek intracelluláris lokalizációja A szabadgyökök, lipidperoxidok hatását az E-vitamin (α-tokoferol) általánosan kivédi (445). Élettani körülmények között azonban, a védekezı rendszer fı tagjai, a kataláz (CAT), a glutation-peroxidáz (GSH-Px) és a szuperoxid-dizmutáz (SOD) eliminálja a szabadgyököket, és a kis mennyiségben jelen lévı E-vitamin a második védelmi vonalat képviseli (481). II Mitokondrium A mitokondriumban keletkezı O 2.- és H 2 O 2 a mitokondriumot magát is károsíthatja. A légzési lánc, mint gyökképzı folyamat szintén károsodhat a gyökök által okozott esszenciális zsírsavak oxidációja miatt. Tyler kimutatta, hogy az O 2.- a NADHdehidrogenáz aktivitását is gátolta (498). Ezért lényeges, hogy az antioxidánsvédekezésben szereplı enzimek (GSH-Px, SOD) jelen legyenek a mitokondriumon belül. A mitokondriális citokróm-c-peroxidáz, amelyet pl. élesztı mitokondriumban találtak, a következı reakciót katalizálja (531): H 2 O citokróm-c H + 2H 2 O + 2 citokróm c 3+. A mitokondriumok mátrixában a légzési láncban keletkezı O 2.- -t a Mn-t tartalmazó SOD alakítja H 2 O 2 -vé (519). II Citoszol Nohl és Hegner feltételezik, hogy a képzıdött O %-a "megszökik" a mitokondriális SOD elıl és kilép a citoszolba (364). Más vizsgálatok azt bizonyítják, 15
17 hogy a mitokondriumból jelentıs mennyiségő H 2 O 2 képes távozni (301). Ezért nagy jelentısége van a citoszolban lévı antioxidáns enzimek, anyagok jelenlétének is. A SOD két formában jelenik meg az eukaryota sejtekben. A citoszol réz- és cinktartalmú SOD-ot (CuZnSOD) tartalmaz (519). A GSH-Px szintén megtalálható a citoszolban és a mitokondrium mátrixában. A nem szelén tartalmú GSH-Px elsısorban a citoszolban található és kisebb affinitást mutat a H 2 O 2 iránt (82). II Szubcelluláris struktúrák A sejtek szubcelluláris struktúrái közé tartoznak a peroxiszómák, az endoplazmatikus retikulum, a Golgi-apparátus stb. A CAT fıként a peroxiszómákban vagy más szubcelluláris mikrotestecskékben jelenik meg, de nem a mitokondriumban (128). Az említett enzimek, folyamatok intracelluláris lokalizációja látható a leegyszerősített ábrán (2. ábra). 2. ábra A O 2.- és H 2 O 2 metabolizmusának intracelluláris lokalizációja (157) rövidítések: szuperoxid-aniongyök: O 2.- ; szeléntartalmú glutation-peroxidáz: SeGSH-Px; nem szeléntartalmú glutation-peroxidáz: GSH-Px; mangántartalmú szuperoxid dizmutáz: MnSOD; réz- és cinktartalmú szuperoxid-dizmutáz: CuZnSOD; kataláz: CAT; alifás alkohol vegyület: AH 2 ; dehidro-alkohol vegyület (aldehid): A * Ebben a folyamatábrában a szerzık jelölnek H-donort a CAT számára, amire csak bizonyos esetekben van szükség az enzim mőködéséhez. II. 7. Az antioxidáns enzimek lokalizációja a vvs-ekben A keringı Hb 3%-a oxidálódik és redukálódik naponta a methemoglobin-reduktáz segítségével. Ebben a reakcióban folyamatosan képzıdnek O 2.- -k, amelyek az oxihb-t methemoglobinná oxidálhatják. A O 2.- -bıl a peroxidokkal való interakció révén OH.- is képzıdhet, amely a legveszélyesebb vvs-membrán-károsító (487). A vvs-ekben az antioxidáns védelemért felelıs a szelénfüggı GSH-Px, a SOD, a CAT. A GSH-Px hidrofób része a vvs-ek sejthártyájához kapcsolódik és redukálja az itt képzıdött lipidhidroperoxidokat (104). A szelén GSH-Px-be való beépülése az erythropoiesis során következik be (197). 16
18 A CAT a vvs-ekben a membránhoz kapcsolódik, és részt vesz a GSH-Px-el együtt a Hb oxidatív károsító folyamatainak gátlásában (104). A vvs-ek antioxidáns védekezırendszerének mőködésének fıbb elemeit lásd még a 8. ábrán. II. 8. Regulációs mechanizmusok II A szervezet védekezése a fokozott oxigéntenzióval szemben A szervezet a szöveti oxigéntenziót viszonylag stabilan alacsony szinten tartja egyrészt a mikrovascularis rendszeren keresztül másrészt a nagy oxigén grádiens fenntartása révén. Az arteriolák constrictióval reagálnak a magas oxigéntenzióra, így a keringést csökkentik az életfontosságú szervek, mint pl. az agy irányába. Ezáltal a magas nyomású oxigén káros hatásai az agyban sokkal késıbb jelentkeznek, mint pl. a tüdıben (96). Lényeges, hogy a létfontosságú szervekben (szív, agy) nagy az interkapilláris távolság. Ezzel a kapilláris és a szövet közötti oxigénkoncentrácó grádiens, akár 100- vagy 1000-szeres is lehet (278). A többi védekezési lépés az antioxidáns enzimek és szubsztrátok mőködésének útján megy végbe (371). Fontos szerep hárul a már említett citokrómoxidázra is az antioxidáns védekezés szempontjából. A sejten belüli oxigénredukciós lánc fı elektron-transzfere, a citokrómoxidáz ("zsebe" segítségével) a mitokondriumból nem engedi ki a közbülsı termékeket (pl. az O 2.- -t). A lekötött termékekbıl a folyamatban végül víz képzıdik (99). II Az antioxidáns védekezés regulációja Lotscher és mtsai. kimutatták, hogy a H 2 O 2 és más hidroperoxidok szerepet játszanak a megfelelı NAD(P)H / NAD(P) arány kialakulásában (303). Az összefüggés a szelénfüggı GSH-Px és a NADPH-függı glutation-reduktáz mőködése révén jelentkezik: H 2 O 2 (ROOH) + 2 GSH H 2 O 2 (ROH) + GSSG GSSG + NADPH + H + 2 GSH + NADP Májsejteken végzett vizsgálatok azt valószínősítik, hogy a májsejtek mitokondriumjai és a citoszolja között létrejövı Ca 2+ egyensúly szintén az adott NAD(P)H + H + / NAD(P) arány kontrollja alatt áll (294). A Ca 2+ felvétele az ATPhidrolízis közvetítette energia révén jöhet létre (442). A NAD(P)H + H + / NAD(P) + párok mőködése összekapcsolódik egy energia-függı transzhidrogenázzal a mitokondriumon belül: NADH + ATP + NADP + NAD + + ADP + P ~ + NADPH A NAD(P)H + H + /NAD(P) + párok és a H 2 O 2 egymásra is hatnak. Ez az egymásra hatás úgy jön létre, hogy a H 2 O 2 termelıdésének mértéke szabályozza a redukáló rendszer (NAD(P)H + H + /NAD(P) + ) mőködését a Ca 2+ -felvétel, a GSH-Px, a glutationreduktáz és a mitokondriális transzhidrogenáz mőködése által. A H 2 O 2 -produkciót a 17
19 mitokondrium állapota szabályozza, vagyis amikor ADP van jelen és amikor a NADH oxidációja maximális szinten van, akkor a H 2 O 2 -produkció leáll. Az O 2.- és a H 2 O 2 hatása révén keletkezı lipid-hidroperoxidok szintén befolyásolják a mitokondriális funkciót (260). Watanabe és Nakamura kimutatták, hogy a linolsav-hidroperoxidok gátolták a mitokondriumban zajló oxidatív foszforilációt, fokozták az Mg-ATP-áz aktivitását és "uncoupling"-ként mőködtek (513). Mások bizonyították, hogy a lipidhidroperoxidok megváltoztatták a mitokondriumok permeabilitását egyes kationokkal szemben (17). Érdekes tapasztalat, hogy a szubmitokondriális partikulumok nem képeznek O 2.- -t, ha nincs jelen SOD. Bizonyítást nyert, hogy a SOD jelenlétében az energetikailag kedvezıtlenebb O 2.- -képzı reakció játszódik le. A SOD ezáltal gátolja a szemikinongyök (QH. ) reakcióit és H 2 O 2 -t képez (157): O 2 + QH. O Q + H + ; 2O H + H 2 O 2 + O 2. II. 9. Antioxidáns és prooxidáns enzimek II Kataláz (CAT) (EC: ) Briggs és Haldane 1925-ben feltételezték olyan enzimek jelenlétét, amelyek H 2 O 2 -t használnak fel (73). Theorell 1951-ben ezeket az enzimeket hidroperoxidázoknak nevezte (483). Kimutatták a H 2 O 2 reakcióinak szerepét a mikroszómákban, mitokondriumokban és a peroxiszómákban (127). A mitokondriumoknak a peroxidok termelıdésben betöltött szerepét vizsgáló kutatások adták az alapját a mitokondriális hidrogéntranszfer reakciók feltérképezésének (66). A H 2 O 2 bontásáért elsısorban a szubcelluláris frakcióban lévı CAT a felelıs. A kataláz szinte minden állati sejtben megtalálható, molekulatömege D, négy alegysége van, aktív centruma az Fe 3+ -at tartalmazó protoporfirin-ix (483). Mőködését az O 2.- gátolni képes (270). A kataláz az egyetlen olyan enzim, amely kettıs funkciót képes ellátni teljesen különbözı kinetikus karakterrel. Fıbb reakcióinak a magyarázatát az ún. I. komponens, mint köztianyag (aktiválási komplex) felfedezése segítette elı (94). Az I. komponens teljes kémiai struktúráját pontosan nem ismerjük, de biztos, hogy a vas és a peroxid oxidációs terméke (35). A reakció végén a szabad kataláz újjáalakul, és molekuláris oxigén képzıdik. Az összes oxigén 0,5 %-a szinglet-oxigénként kerül ki a rendszerbıl (392). A kataláznak nagy a specifitása egyes peroxidokra nézve, pl. a hidrogén-peroxidra, a metil- és az etilhidroperoxidokra. A H 2 O 2 helyi koncentrációja és a kataláz aktivitása biológiai rendszerekben általában egyenesen arányos, így az enzim megfelelı szinten képes tartani az intracelluláris H 2 O 2 koncentrációt (101). A kataláz két kinetikailag is eltérı funkciója úgy változik, hogy amikor a H 2 O 2 koncentráció kicsi, akkor a peroxidatív mőködés lép elıtérbe, amikor pedig nagy, akkor a katalitikus út dominál (98). Az enzim mennyisége (és aktivitása) más enzimek mellett hormonális, táplálkozási, farmakológiai körülményektıl függ (227). A "peroxiszóma koncepciót" De Duve és Baudhuin dolgozta ki (128). Immunológiai módszerekkel igazolást nyert, hogy a kataláz 18
20 a peroxiszómákon kívül szintetizálódó prekurzorokból a peroxiszómában válik aktív enzimmé (126). A vörösvérsejtekben a kataláz enzimnek csekély jelentısége van élettani viszonyokban, mivel a képzıdı gyökök degradációját a glutation-rendszer végzi (104). Bizonyítást nyert azonban, hogy nagyobb H 2 O 2 koncentrációnak kitett sejtekben a kataláz gyorsabban bontja a H 2 O 2 -ot, mint a GSH-Px, gyaníthatóan annak következtében, hogy ennek az enzimnek a mőködéséhez nincs minden esetben szükség hidrogén donorra (2). Egy leegyszerősített reakciósorozat látható a 3. ábrán, amely a CAT két reakcióciklusát ábrázolja. A felsı rész a katalitikus, az alsó pedig a peroxidatív reakciót ábrázolja. A peroxidatív reakcióban az I. komponens és az alkohol reakcióterméke egy aldehid molekula (444). 3. ábra A CAT I. komponensének feltételezett reakciója (444) rövidítések: X: szubsztrátkötı, az enzimhez tartozó fehérje molekula; L: az enzim struktúrális, vaskötı része; R-CH 2 OH: alkohol-molekula, mely H-donorként mőködik; R- CHO: aldehidmolekula, a peroxidatív reakció végterméke; a nyilak a reakcióutakat és az elektronátadást jelölik. II Glutation-peroxidáz(ok) (GSH-Px) (EC: ) és a glutation-s-transzferáz (GST) (EC: ) A GSH-Px-et és biokémiai funkcióját Mills 1957-ben fedezte fel (345). A szelénfüggı enzimnek (molekulatömege: D) négy alegysége van, aktív centruma a szelén, amelybıl alegységenként egyet tartalmaz (154). A szelénfüggı GSH-Px aktív centrumában a katalízisért felelıs csoport a szelenocisztein, redukált formában SeHcsoport található (161). A GSH-Px a H 2 O 2 és a hidroperoxidok katalitikus bontását végzi azáltal, hogy a redukált glutationt (GSH) oxidálja glutation diszulfiddá (GSSG) (303): H 2 O GSH 2H 2 O + GSSG ROOH + 2 GSH H 2 O + ROH + GSSG A képzıdött hidroxi-lipid a késıbbiekben a β-oxidációban további bontásra kerülhet (104). 19
21 A GSH-Px aktivitása nagy a májban és az erythrocytákban, kicsi a szívben és a tüdıben valamint az izomszövetben. A GSH-Px specifikus a hidrogén donorjára, a GSHra nézve, és nem specifikus a hidroperoxidokra nézve, hiszen azok széles spektrumával (a H 2 O 2 -tıl kezdve a szerves hidroperoxidokig, a zsírsav hidroperoxidokat, a nukleotidés szteroid hidroperoxid derivátumokat beleértve) képes reagálni. A GSH-Px "osztozik" a H 2 O 2 -on a kataláz enzimmel és egyedül képes hatékonyan reagálni a szerves hidroperoxidokkal. Patkány májsejtjein belül a GSH-Px 2/3 része a citoszolban, 1/3-a pedig a mitokondriumban található. A peroxiszómákból nem mutatható ki (153). A sejten belüli migrációja során kapcsolódik a membránstruktúrában lévı hidrofób lipidhidroperoxidokhoz. A szervezetbe juttatott LP-t fokozó szubsztrát adása a szöveti GSH-Px aktivitását jelentısen növeli. Lipidperoxidok felvétele után a bélnyálkahártya és a májszövet GSH- Px aktivitása nı (410) csakúgy, mint a tüdıszöveté ózon belélegeztetése után vagy 85-90%-os oxigén 14 napig történı inhalálását követıen (265). Patkányok májának GSH- Px-aktivitása nı ösztrogén adagolása után is (390). A Se-bevitellel a GSH-Px aktivitása is nı egy adott szintig, és Se-hiányában pedig az enzim aktivitása csökken. Ezt a folyamatot számos szervben és a vvs-ekben is ki lehet mutatni (197) (169). Megemlítendı azonban, hogy a GSH-Px mérésével inkább a Sehiány mutatható ki, mint a Se-túladagolás. A Se-bevitel fokozása esetén ugyanis nem szoros korrelációban emelkedik az enzim aktivitása. Megemlítendı, hogy a GSH-Px aktivitásában jelentıs faji diverzitás is jelentkezik (169) (338), sıt ivari differenciát is igazoltak (a nıstény patkányok mája kisebb aktivitási értékeket mutat) (390). Létezik egy nem szelénfüggı GSH-Px is. Megfigyelték, hogy a szelénhiányos patkányokban a hidroperoxidok eliminálása nem vált teljesen gátolttá. Ennek a felfedezésnek a nyomán mutatták ki a szelén-independens glutation peroxidázt, melyet glutation transzferáz B-nek, vagy glutation-s-transzferáznak (GST) neveztek el (396). Lawrence és Burk patkányok májhomogenizátumán végzett vizsgálatai is bizonyították ennek az enzimnek a meglétét (291). A lipidhidroperoxidok és a H 2 O 2 bontását vizsgálták és kimutatták, hogy molekulatömegük alapján egészséges állatokban két enzim figyelhetı meg. Az egyik enzim mindkét anyag bontását képes volt katalizálni, míg a másik csak lipid-hidroperoxidokat bontott. A nem szelénfüggı GSH-Px molekulatömege D, dimer struktúrájú, a két alegység önmagában is funkcióképes (396). Sárvári összefoglaló munkájában részletezi a GST szerepét és mérésének jelentıségét a klinikai diagnosztikában. A GST-nek számos funkcióját ismerjük: a szerves hidroperoxidokat közömbösíti, peroxidáz-aktivitása van, a glutation tiolát-anion (GS - ) konjugációját végzi számos hidrofób molekula elektrofil centrumával, alkil-, aralkil-, aril-, alkán- és epoxidtranszferáz aktivitása van, katalizálja a tiolízist, nitrocsoportot hasít le egyes szubsztrátokról, ketoszteroid izomeráz aktivitása van, a szerves halogenizált benzolszármazékok károsító csoportjait átalakítja. Számos reaktív metabolit képes a GST-hez kovalensen kötıdni, ezért feltételezik intracelluláris transzport protein, illetve receptor szerepét is (435). A GST szubcelluláris szinten megtalálható a citoszolban, az endoplazmatikus retikulumban, a mikroszómákban, és a mitokondriumok külsı membránján (292). 20
22 Ismeretes egy a klasszikus Se-dependens, GSH-Px-hez hasonló aminosavszekvenciájú és kinetikájú, D molekulatömegő monomer enzim is az ún.: foszfolipid-hidroperoxid glutation-peroxidáz (PHGSH-Px), eredeti nevén: "peroxidation-inhibiting-protein" (PIP), amelyet sertések májszövetébıl izoláltak. Ez az enzim képes redukálni a kumén- és a t-butil-hidroperoxidot, valamint a klasszikus GSH- Px-tıl eltérıen a foszfolipid-hidroperoxidokat is. Fıleg a sejtmembrán védelmében játszik szerepet (499). Emberi vérplazmából izoláltak egy, az elızıekhez hasonló, glutation-peroxidáz funkciójú enzimet, a plazma-gsh-px-et, amit vese eredetőnek tartanak. Szintén négy Setartalmú alegységbıl áll, azonban aminosavszekvenciája eltér a "klasszikus" GSH-Px-tıl (169). II Hem-peroxidázok A hem-peroxidázok természetben széles körben elıforduló enzimek, amelyek a növényekben (pl. a tormában) jelennek meg különösen nagy mennyiségben (95). Az emlısökben elıforduló peroxidázok prosztetikus csoportja a hem (529). A laktoperoxidáz az emlı- és a nyálmirigyben fordul elı (351), hidrogéndonorjai a pirogallol, a guajakol, az aszkorbinsav és a benzidin (440), de a tirozint is képes jodinálni (42). A laktoperoxidázokhoz hasonló tulajdonságokkal rendelkeznek azok a peroxidázok, amelyek az eozinofil sejtekben (12) és a bél nyálkahártyában (466) találhatók. Sokféle peroxidázt izoláltak állati szövetekbıl, bár sokak szerint ezek nem olyanok, amelyek az adott helyen termelıdnek (thyreoid-peroxidáz és a mieloperoxidáz /MPO/ kivételével), hanem pl. az eosinophil granulocyták szállítják az adott szövethez (424). Mégis, egy bizonyítottan szöveti eredető enzim az ún. uterin-peroxidáz, amelynek fokozódik az aktivitása ösztrogén és luteinizáló hormon hatására (4). A thyreoid-peroxidáz szorosan kötıdik a szövethez (kísérletes körülmények között a pajzsmirigy szövethomogenizátumhoz), katalizálja a jód oxidációját a mirigyen belül és fontos feladatot lát el a thyreoid hormonok szintézisében (440). Az MPO a neutrophil granulocytákban található, két vas atomot tartalmaz egy-egy hemcsoportjában és reagálni képes a H 2 O 2 -vel és a cianidokkal is (3). Az MPO fenolokat, kinonokat, aszkorbinsavat stb. használ fel hidrogéndonorként. Legfıbb szerepe a fagocitózisban van (101). II Tiol-transzferázok A fehérjék és a kis molekulatömegő tiolok tiol-diszulfid cserereakciói enzimatikusan és enzimatikus reakciók nélkül is létrejöhetnek (275) (535). Jól ismertek azok az enzimatikus reakciók, amelyek során a protein-diszulfidok kis molekulatömegő tiolok által történı redukciója zajlik (163), azonban kevésbé ismertek azok, amelyek során a protein-tiolok kis molekulatömegő diszulfidokkal történı reakciói zajlanak. Ezeket a folyamatokat nevezik S-tiolációnak (108) (190). Patkányok májából izolált tioltranszferáz katalizálja a reverzibilis tiol-diszulfid cserét a GSSG és a patkánymájból származó tiol-tartalmú fehérje között (311). A tiol-transzferázok képesek a fehérjék 21
A bioenergetika a biokémiai folyamatok során lezajló energiaváltozásokkal foglalkozik.
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA BIOENERGETIKA I. 1. kulcsszó cím: Energia A termodinamika első főtétele kimondja, hogy a különböző energiafajták átalakulhatnak egymásba ez az energia megmaradásának
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Energiatermelés a sejtekben, katabolizmus. Az energiaközvetítő molekula: ATP
 Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Energiatermelés a sejtekben, katabolizmus Az energiaközvetítő molekula: ATP Elektrontranszfer, a fontosabb elektronszállító molekulák NAD: nikotinamid adenin-dinukleotid FAD: flavin adenin-dinukleotid
Citrátkör, terminális oxidáció, oxidatív foszforiláció
 Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
Citrátkör, terminális oxidáció, oxidatív foszforiláció A citrátkör jelentősége tápanyagok oxidációjának közös szakasza anyag- és energiaforgalom központja sejtek anyagcseréjében elosztórendszerként működik:
A KOLESZTERIN SZERKEZETE. (koleszterin v. koleszterol)
 19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
19 11 12 13 C 21 22 20 18 D 17 16 23 24 25 26 27 HO 2 3 1 A 4 5 10 9 B 6 8 7 14 15 A KOLESZTERIN SZERKEZETE (koleszterin v. koleszterol) - a koleszterin vízben rosszul oldódik - szabad formában vagy koleszterin-észterként
Szabadgyök-reakciók és az antioxidáns rendszer gasztroenterológiai betegségekben és diabetes mellitusban dr. Szaleczky Erika
 Szabadgyök-reakciók és az antioxidáns rendszer gasztroenterológiai betegségekben és diabetes mellitusban dr. Szaleczky Erika Programvezető: Prof. Dr. Fehér János Témavezető: Dr. Prónai László Ph.D. Dr.
Szabadgyök-reakciók és az antioxidáns rendszer gasztroenterológiai betegségekben és diabetes mellitusban dr. Szaleczky Erika Programvezető: Prof. Dr. Fehér János Témavezető: Dr. Prónai László Ph.D. Dr.
Stressz és a reaktív oxigénformák
 Stressz és a reaktív oxigénformák Oxigénformák A földi élet egyik paradoxonja: Az oxigén, amely az aerob életfolyamatokhoz szükséges, és a az energia termelés és légzés alapvetı feltétele, sok betegség
Stressz és a reaktív oxigénformák Oxigénformák A földi élet egyik paradoxonja: Az oxigén, amely az aerob életfolyamatokhoz szükséges, és a az energia termelés és légzés alapvetı feltétele, sok betegség
A piruvát-dehidrogenáz komplex. Csala Miklós
 A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
A piruvát-dehidrogenáz komplex Csala Miklós szénhidrátok fehérjék lipidek glikolízis glukóz aminosavak zsírsavak acil-koa szintetáz e - piruvát acil-koa légz. lánc H + H + H + O 2 ATP szint. piruvát H
ZSÍRSAVAK OXIDÁCIÓJA. FRANZ KNOOP német biokémikus írta le először a mechanizmusát. R C ~S KoA. a, R-COOH + ATP + KoA R C ~S KoA + AMP + PP i
 máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
máj, vese, szív, vázizom ZSÍRSAVAK XIDÁCIÓJA FRANZ KNP német biokémikus írta le először a mechanizmusát 1 lépés: a zsírsavak aktivációja ( a sejt citoplazmájában, rövid zsírsavak < C12 nem aktiválódnak)
A légzési lánc és az oxidatív foszforiláció
 A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
A légzési lánc és az oxidatív foszforiláció Csala Miklós Semmelweis Egyetem Orvosi Vegytani, Molekuláris Biológiai és Patobiokémiai Intézet intermembrán tér Fe-S FMN NADH mátrix I. komplex: NADH-KoQ reduktáz
Bevezetés a biokémiába fogorvostan hallgatóknak
 Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Bevezetés a biokémiába fogorvostan hallgatóknak Munkafüzet 14. hét METABOLIZMUS III. LIPIDEK, ZSÍRSAVAK β-oxidációja Szerkesztette: Jakus Péter Név: Csoport: Dátum: Labor dolgozat kérdések 1.) ATP mennyiségének
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Az oxidatív stressz és a fizikai erőkifejtés kapcsolata
 Az oxidatív stressz és a fizikai erőkifejtés kapcsolata Doktori értekezés Dékány Miklós Semmelweis Egyetem Sporttudományi Doktori Iskola Témavezető: Dr. Pucsok József egyetemi tanár, az MTA doktora Hivatalos
Az oxidatív stressz és a fizikai erőkifejtés kapcsolata Doktori értekezés Dékány Miklós Semmelweis Egyetem Sporttudományi Doktori Iskola Témavezető: Dr. Pucsok József egyetemi tanár, az MTA doktora Hivatalos
vvs) LIPIDPEROXIDÁCI CIÓS S (LP) ÉS S ANTIOXIDÁNS Vajdovich Péter
 BELSİ ÉS S KÜLSK LSİ TÉNYEZİK K HATÁSA A VÖRÖSVV SVÉRSEJTEK (vvs( vvs) LIPIDPEROXIDÁCI CIÓS S (LP) ÉS S ANTIOXIDÁNS NS FOLYAMATAIRA (szarvasmarhákban, juhokban, kutyákban kban és s patkányokban végzett
BELSİ ÉS S KÜLSK LSİ TÉNYEZİK K HATÁSA A VÖRÖSVV SVÉRSEJTEK (vvs( vvs) LIPIDPEROXIDÁCI CIÓS S (LP) ÉS S ANTIOXIDÁNS NS FOLYAMATAIRA (szarvasmarhákban, juhokban, kutyákban kban és s patkányokban végzett
LIPID ANYAGCSERE (2011)
 LIPID ANYAGCSERE LIPID ANYAGCSERE (2011) 5 ELİADÁS: 1, ZSÍRK EMÉSZTÉSE, FELSZÍVÓDÁSA + LIPPRTEINEK 2, ZSÍRSAVAK XIDÁCIÓJA 3, ZSÍRSAVAK SZINTÉZISE 4, KETNTESTEK BIKÉMIÁJA, KLESZTERIN ANYAGCSERE 5, MEMBRÁN
LIPID ANYAGCSERE LIPID ANYAGCSERE (2011) 5 ELİADÁS: 1, ZSÍRK EMÉSZTÉSE, FELSZÍVÓDÁSA + LIPPRTEINEK 2, ZSÍRSAVAK XIDÁCIÓJA 3, ZSÍRSAVAK SZINTÉZISE 4, KETNTESTEK BIKÉMIÁJA, KLESZTERIN ANYAGCSERE 5, MEMBRÁN
Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből.
 Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Vércukorszint szabályozása: Szénhidrátok monoszacharidok formájában szívódnak fel a vékonybélből. Szövetekben monoszacharid átalakítás enzimjei: Szénhidrát anyagcserében máj központi szerepű. Szénhidrát
Tárgyszavak: citokróm P450, oxidatív stressz; reaktív oxigénvegyületek; szabad gyök.
 BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN A citokróm P450 szerepe az oxidatív stresszben Tárgyszavak: citokróm P450, oxidatív stressz; reaktív oxigénvegyületek; szabad gyök. A sejtekben és szövetekben végbemenő
BIOTECHNOLÓGIA AZ EGÉSZSÉGÜGYBEN A citokróm P450 szerepe az oxidatív stresszben Tárgyszavak: citokróm P450, oxidatív stressz; reaktív oxigénvegyületek; szabad gyök. A sejtekben és szövetekben végbemenő
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI
 PH.D. ÉRTEKEZÉS AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI RENDSZER VIZSGÁLATA NEHÉZFÉM KEZELÉST KÖVETŐEN PONTYBAN ÉS STREPTOZOTOCIN-INDUKÁLTA DIABÉTESZES PATKÁNY MODELLBEN JANCSÓ ZSANETT TÉMAVEZETŐ:
PH.D. ÉRTEKEZÉS AZ OXIDATÍV STRESSZ ÉS AZ ANTIOXIDÁNS VÉDELMI RENDSZER VIZSGÁLATA NEHÉZFÉM KEZELÉST KÖVETŐEN PONTYBAN ÉS STREPTOZOTOCIN-INDUKÁLTA DIABÉTESZES PATKÁNY MODELLBEN JANCSÓ ZSANETT TÉMAVEZETŐ:
Fotoszintézis. 2. A kloroplasztisz felépítése 1. A fotoszintézis lényege és jelentısége
 Fotoszintézis 2. A kloroplasztisz felépítése 1. A fotoszintézis lényege és jelentısége Szerves anyagok képzıdése energia felhasználásával Az élıvilág szerves anyag és oxigénszükségletét biztosítja H2 D
Fotoszintézis 2. A kloroplasztisz felépítése 1. A fotoszintézis lényege és jelentısége Szerves anyagok képzıdése energia felhasználásával Az élıvilág szerves anyag és oxigénszükségletét biztosítja H2 D
A felépítő és lebontó folyamatok. Biológiai alapismeretek
 A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
A felépítő és lebontó folyamatok Biológiai alapismeretek Anyagforgalom: Lebontó Felépítő Lebontó folyamatok csoportosítása: Biológiai oxidáció Erjedés Lebontó folyamatok összehasonlítása Szénhidrátok
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekIKözgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekIKözgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Növényélettani Gyakorlatok A légzés vizsgálata
 Növényélettani Gyakorlatok A légzés vizsgálata /Bevezető/ Fotoszintézis Fény-szakasz: O 2, NADPH, ATP Sötétszakasz: Cellulóz keményítő C 5 2 C 3 (-COOH) 2 C 3 (-CHO) CO 2 Nukleotid/nukleinsav anyagcsere
Növényélettani Gyakorlatok A légzés vizsgálata /Bevezető/ Fotoszintézis Fény-szakasz: O 2, NADPH, ATP Sötétszakasz: Cellulóz keményítő C 5 2 C 3 (-COOH) 2 C 3 (-CHO) CO 2 Nukleotid/nukleinsav anyagcsere
Az eukarióta sejt energiaátalakító organellumai
 A mitokondrium és a kloroplasztisz hasonlósága Az eukarióta sejt energiaátalakító organellumai mitokondrium kloroplasztisz eukarióta sejtek energiaátalakító és konzerváló organellumai Működésükben alapvető
A mitokondrium és a kloroplasztisz hasonlósága Az eukarióta sejt energiaátalakító organellumai mitokondrium kloroplasztisz eukarióta sejtek energiaátalakító és konzerváló organellumai Működésükben alapvető
R R C X C X R R X + C H R CH CH R H + BH 2 + Eliminációs reakciók
 Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
Eliminációs reakciók Amennyiben egy szénatomhoz távozó csoport kapcsolódik és ugyanazon a szénatomon egy (az ábrákon vel jelölt) bázis által protonként leszakítható hidrogén is található, a nukleofil szubsztitúció
A kémiai energia átalakítása a sejtekben
 A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
A kémiai energia átalakítása a sejtekben A sejtek olyan mikroszkópikus képződmények amelyek működése egy vegyi gyárhoz hasonlítható. Tehát a sejtek mikroszkópikus vegyi gyárak. Mi mindenben hasonlítanak
Kémiai reakciók. Kémiai reakció feltételei: Aktivált komplexum:
 Kémiai reakció feltételei: részecskék ütközése nagyobb koncentrációban gyakoribb: a részecskék megfelelı térhelyzetben legyenek Aktivált komplexum: részecskék ütközés utáni nagyon rövid ideig tartó összekapcsolódása
Kémiai reakció feltételei: részecskék ütközése nagyobb koncentrációban gyakoribb: a részecskék megfelelı térhelyzetben legyenek Aktivált komplexum: részecskék ütközés utáni nagyon rövid ideig tartó összekapcsolódása
Mire költi a szervezet energiáját?
 Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
Glükóz lebontás Lebontó folyamatok A szénhidrátok és zsírok lebontása során széndioxid és víz keletkezése közben energia keletkezik (a széndioxidot kilélegezzük, a vizet pedig szervezetünkben felhasználjuk).
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
Glikolízis. emberi szervezet napi glukózigénye: kb. 160 g
 Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis Minden emberi sejt képes glikolízisre. A glukóz a metabolizmus központi tápanyaga, minden sejt képes hasznosítani. glykys = édes, lysis = hasítás emberi szervezet napi glukózigénye: kb. 160
Glikolízis. Csala Miklós
 Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Glikolízis Csala Miklós Szubsztrát szintű (SZF) és oxidatív foszforiláció (OF) katabolizmus Redukált tápanyag-molekulák Szállító ADP + P i ATP ADP + P i ATP SZF SZF Szállító-H 2 Szállító ATP Szállító-H
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA LIPIDEK ANYAGCSERÉJE 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA LIPIDEK ANYAGCSERÉJE 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai védelem, hőszigetelés,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA LIPIDEK ANYAGCSERÉJE 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai védelem, hőszigetelés,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015
 Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
Kollokviumi vizsgakérdések biokémiából humánkineziológia levelező (BSc) 2015 A kérdés 1. A sejtről általában, a szervetlen alkotórészeiről, a vízről részletesen. 2. A sejtről általában, a szervetlen alkotórészeiről,
A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim. tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek
 1 A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek a./ Csak fehérjébıl állók b./ Fehérjébıl (apoenzim)
1 A biokémiai folyamatokat enzimek (biokatalizátorok) viszik véghez. Minden enzim tartalmaz fehérjét. Két csoportjukat különböztetjük meg az enzimeknek a./ Csak fehérjébıl állók b./ Fehérjébıl (apoenzim)
09. A citromsav ciklus
 09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
09. A citromsav ciklus 1 Alternatív nevek: Citromsav ciklus Citrát kör Trikarbonsav ciklus Szent-Györgyi Albert Krebs ciklus Szent-Györgyi Krebs ciklus Hans Adolf Krebs 2 Áttekintés 1 + 8 lépés 0: piruvát
Túledzés és oxidatív stressz
 Semmelweis Egyetem Doktori Iskola Semmelweis Egyetem, Testnevelési és Sporttudományi Kar Nevelés- és Sporttudományi Doktori Iskola Kollárné Ogonovszky Helga Túledzés és oxidatív stressz Témavezető: Dr.
Semmelweis Egyetem Doktori Iskola Semmelweis Egyetem, Testnevelési és Sporttudományi Kar Nevelés- és Sporttudományi Doktori Iskola Kollárné Ogonovszky Helga Túledzés és oxidatív stressz Témavezető: Dr.
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
A koenzim Q10 fél évszázados története
 A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
A koenzim Q10 fél évszázados története A koenzim Q10 a sejtek optimális működéséhez nélkülözhetetle A koenzim Q10 (KoQ10) vitaminszerű vegyület. Az ubikinonok k 1 / 8 A Nobel-díjas Dr. Peter Mitchell Kémiailag
BIOGÉN ELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %)
 BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
BIOGÉN ELEMEK ELSŐDLEGES BIOGÉN ELEMEK(kb. 95%) ÁLLANDÓ BIOGÉN ELEMEK MAKROELEMEK MÁSODLAGOS BIOGÉN ELEMEK (> 0,005 %) C, H, O, N P, S, Cl, Na, K, Ca, Mg MIKROELEMEK (NYOMELEMEK) (< 0,005%) I, Fe, Cu,
Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában SZARKA ANDRÁS
 Semmelweis Egyetem, Molekuláris Orvostudományok Doktori Iskola PATHOBIOKÉMIA DOKTORI PROGRAM Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában Doktori (Ph.D.) értekezés tézisei SZARKA ANDRÁS
Semmelweis Egyetem, Molekuláris Orvostudományok Doktori Iskola PATHOBIOKÉMIA DOKTORI PROGRAM Antioxidánsok szerepe a fehérje diszulfid kötések kialakulásában Doktori (Ph.D.) értekezés tézisei SZARKA ANDRÁS
Orvosi biokémia, molekuláris és sejtbiológia II. Az intermedier anyagcsere
 Orvosi biokémia, molekuláris és sejtbiológia II. Az intermedier anyagcsere www.ovi.sote.hu Intézeti tanulmányi felelős: Dr. Müllner Nándor egyetemi docens II. évfolyam orvosi biokémia oktatási felelős:
Orvosi biokémia, molekuláris és sejtbiológia II. Az intermedier anyagcsere www.ovi.sote.hu Intézeti tanulmányi felelős: Dr. Müllner Nándor egyetemi docens II. évfolyam orvosi biokémia oktatási felelős:
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN. Somogyi János -- Vér Ágota Első rész
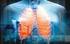 A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
A MITOKONDRIUMOK SZEREPE A SEJT MŰKÖDÉSÉBEN Somogyi János -- Vér Ágota Első rész Már több mint 200 éve ismert, hogy szöveteink és sejtjeink zöme oxigént fogyaszt. Hosszú ideig azt hitték azonban, hogy
 Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
Az élő szervezetek felépítése I. Biogén elemek biomolekulák alkotóelemei a természetben előforduló elemek közül 22 fordul elő az élővilágban O; N; C; H; P; és S; - élő anyag 99%-a Biogén elemek sajátosságai:
MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben
 Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
Modul cím: MEDICINÁLIS ALAPISMERETEK AZ ÉLŐ SZERVEZETEK KÉMIAI ÉPÍTŐKÖVEI A LIPIDEK 1. kulcsszó cím: A lipidek szerepe az emberi szervezetben Tartalék energiaforrás, membránstruktúra alkotása, mechanikai
A nukleinsavak polimer vegyületek. Mint polimerek, monomerekből épülnek fel, melyeket nukleotidoknak nevezünk.
 Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
Nukleinsavak Szerkesztette: Vizkievicz András A nukleinsavakat először a sejtek magjából sikerült tiszta állapotban kivonni. Innen a név: nucleus = mag (lat.), a sav a kémhatásukra utal. Azonban nukleinsavak
A felvétel és a leadás közötti átalakító folyamatok összességét intermedier - köztes anyagcserének nevezzük.
 1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
1 Az anyagcsere Szerk.: Vizkievicz András Általános bevezető Az élő sejtekben zajló biokémiai folyamatok összességét anyagcserének nevezzük. Az élő sejtek nyílt anyagi rendszerek, azaz környezetükkel állandó
neutrális zsírok, foszfolipidek, szteroidok karotinoidok.
 Lipidek A lipidek/zsírszerű anyagok az élőlényekben előforduló, változatos szerkezetű szerves vegyületek. Közös sajátságuk, hogy apoláris oldószerekben oldódnak. A lipidek csoportjába tartoznak: neutrális
Lipidek A lipidek/zsírszerű anyagok az élőlényekben előforduló, változatos szerkezetű szerves vegyületek. Közös sajátságuk, hogy apoláris oldószerekben oldódnak. A lipidek csoportjába tartoznak: neutrális
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2014.10.01. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA
 A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
A METABOLIZMUS ENERGETIKÁJA Futó Kinga 2013.10.02. Metabolizmus Metabolizmus = reakciók együttese, melyek a sejtekben lejátszódnak. Energia nyerés szempontjából vannak fototrófok ill. kemotrófok. szervesanyag
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
DER (Felületén riboszómák találhatók) Feladata a biológiai fehérjeszintézis Riboszómák. Az endoplazmatikus membránrendszer. A kódszótár.
 Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
Az endoplazmatikus membránrendszer Részei: DER /durva (szemcsés) endoplazmatikus retikulum/ SER /sima felszínű endoplazmatikus retikulum/ Golgi készülék Lizoszómák Peroxiszómák Szekréciós granulumok (váladékszemcsék)
KEDVEZMÉNYES VIZSGÁLATI CSOMAGOK
 C-1 es ár Élni jó csomag Páros csomag D-vitamin csomag Manager csomag Egészség 50+ csomag hölgyeknek Egészség 50+ csomag férfiaknak Vérkép automatával (kvalitatív vérképpel) (GGT), Alkalikus foszfatáz
C-1 es ár Élni jó csomag Páros csomag D-vitamin csomag Manager csomag Egészség 50+ csomag hölgyeknek Egészség 50+ csomag férfiaknak Vérkép automatával (kvalitatív vérképpel) (GGT), Alkalikus foszfatáz
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Átmenetifém-komplexek ESR-spektrumának jellemzıi
 Átmenetifém-komplexek ESR-spektrumának jellemzıi A párosítatlan elektron d-pályán van. Kevéssé delokalizálódik a fémionról, a fém-donoratom kötések meglehetısen ionos jellegőek. A spin-pálya csatolás viszonylag
Átmenetifém-komplexek ESR-spektrumának jellemzıi A párosítatlan elektron d-pályán van. Kevéssé delokalizálódik a fémionról, a fém-donoratom kötések meglehetısen ionos jellegőek. A spin-pálya csatolás viszonylag
jobb a sejtszintű acs!!
 Metabolikus stresszválasz jobb a sejtszintű acs!! dr. Ökrös Ilona B-A-Z Megyei Kórház és Egyetemi Oktató Kórház Miskolc Központi Aneszteziológiai és Intenzív Terápiás Osztály Az alkoholizmus, A fiziológiás
Metabolikus stresszválasz jobb a sejtszintű acs!! dr. Ökrös Ilona B-A-Z Megyei Kórház és Egyetemi Oktató Kórház Miskolc Központi Aneszteziológiai és Intenzív Terápiás Osztály Az alkoholizmus, A fiziológiás
Általános és szervetlen kémia 3. hét Kémiai kötések. Kötések kialakítása - oktett elmélet. Lewis-képlet és Lewis szerkezet
 Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Kémiai reakciók sebessége
 Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Kémiai reakciók sebessége reakciósebesség (v) = koncentrációváltozás változáshoz szükséges idő A változás nem egyenletes!!!!!!!!!!!!!!!!!! v= ± dc dt a A + b B cc + dd. Melyik reagens koncentrációváltozását
Zárójelentés OTKA 37321. A téma címe: Az antioxidáns rendszer ontogenezisének vizsgálata emlős állatfajokban A kutatás időtartama: 2002-2005
 Témavezető neve: Dr. Gaál Tibor Zárójelentés OTKA 37321 A téma címe: Az antioxidáns rendszer ontogenezisének vizsgálata emlős állatfajokban A kutatás időtartama: 22-25 A kutatásban vizsgáltuk az antioxidáns
Témavezető neve: Dr. Gaál Tibor Zárójelentés OTKA 37321 A téma címe: Az antioxidáns rendszer ontogenezisének vizsgálata emlős állatfajokban A kutatás időtartama: 22-25 A kutatásban vizsgáltuk az antioxidáns
4. változat. 2. Jelöld meg azt a részecskét, amely megőrzi az anyag összes kémiai tulajdonságait! A molekula; Б atom; В gyök; Г ion.
 4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
4. változat z 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Melyik sor fejezi be helyesen az állítást:
A szénhidrátok lebomlása
 A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
A disszimiláció Szerk.: Vizkievicz András A disszimiláció, vagy lebontás az autotróf, ill. a heterotróf élőlényekben lényegében azonos módon zajlik. A disszimilációs - katabolikus - folyamatok mindig valamilyen
M E G O L D Ó L A P. Egészségügyi Minisztérium
 Egészségügyi Minisztérium Szolgálati titok! Titkos! Érvényességi idı: az írásbeli vizsga befejezésének idıpontjáig A minısítı neve: Vízvári László A minısítı beosztása: fıigazgató M E G O L D Ó L A P szakmai
Egészségügyi Minisztérium Szolgálati titok! Titkos! Érvényességi idı: az írásbeli vizsga befejezésének idıpontjáig A minısítı neve: Vízvári László A minısítı beosztása: fıigazgató M E G O L D Ó L A P szakmai
Energia források a vázizomban
 Energia források a vázizomban útvonal sebesség mennyiség ATP/glükóz 1. direkt foszforiláció igen gyors igen limitált - 2. glikolízis gyors limitált 2-3 3. oxidatív foszforiláció lassú nem limitált 36 Izomtípusok
Energia források a vázizomban útvonal sebesség mennyiség ATP/glükóz 1. direkt foszforiláció igen gyors igen limitált - 2. glikolízis gyors limitált 2-3 3. oxidatív foszforiláció lassú nem limitált 36 Izomtípusok
BIOMOLEKULÁK KÉMIÁJA. Novák-Nyitrai-Hazai
 BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
BIOMOLEKULÁK KÉMIÁJA Novák-Nyitrai-Hazai A tankönyv elsısorban szerves kémiai szempontok alapján tárgyalja az élı szervezetek felépítésében és mőködésében kulcsfontosságú szerves vegyületeket. A tárgyalás-
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL
 TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
TRIPSZIN TISZTÍTÁSA AFFINITÁS KROMATOGRÁFIA SEGÍTSÉGÉVEL Az egyes biomolekulák izolálása kulcsfontosságú a biológiai szerepük tisztázásához. Az affinitás kromatográfia egyszerűsége, reprodukálhatósága
A nitrogén körforgalma. A környezetvédelem alapjai május 3.
 A nitrogén körforgalma A környezetvédelem alapjai 2017. május 3. A biológiai nitrogén körforgalom A nitrogén minden élő szervezet számára nélkülözhetetlen, ún. biogén elem Részt vesz a nukleinsavak, a
A nitrogén körforgalma A környezetvédelem alapjai 2017. május 3. A biológiai nitrogén körforgalom A nitrogén minden élő szervezet számára nélkülözhetetlen, ún. biogén elem Részt vesz a nukleinsavak, a
Az enzimműködés termodinamikai és szerkezeti alapjai
 2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
2017. 02. 23. Dr. Tretter László, Dr. Kolev Kraszimir Az enzimműködés termodinamikai és szerkezeti alapjai 2017. február 27., március 2. 1 Mit kell(ene) tudni az előadás után: 1. Az enzimműködés termodinamikai
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
A flavonoidok az emberi szervezet számára elengedhetetlenül szükségesek, akárcsak a vitaminok, vagy az ásványi anyagok.
 Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Amit a FLAVIN 7 -ről és a flavonoidokról még tudni kell... A FLAVIN 7 gyümölcsök flavonoid és más növényi antioxidánsok koncentrátuma, amely speciális molekulaszeparációs eljárással hét féle gyümölcsből
Zsírsav szintézis. Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P. 2 i
 Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Zsírsav szintézis Az acetil-coa aktivációja: Acetil-CoA + CO + ATP = Malonil-CoA + ADP + P 2 i A zsírsav szintáz reakciói Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14 H = Palmitát + 8 CoA-SH + 7 CO 2 + 7
Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája
 Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája A) Az etanol metabolizmusa emberben A metabolizmus átlagos sebessége: 10 g etanol/óra Az etanol energiatartalma: 30 kj/g (7,1 kcal/g) Az
Az Etanol Metabolizmusa és az Alkoholos Májkárosodás Biokémiája A) Az etanol metabolizmusa emberben A metabolizmus átlagos sebessége: 10 g etanol/óra Az etanol energiatartalma: 30 kj/g (7,1 kcal/g) Az
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE
 AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
AZ ÉLET KÉMIÁJA... ÉLŐ ANYAG SZERVEZETI ALAPEGYSÉGE A biológia az élet tanulmányozásával foglalkozik, az élő szervezetekre viszont vonatkoznak a fizika és kémia törvényei MI ÉPÍTI FEL AZ ÉLŐ ANYAGOT? HOGYAN
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
BEVEZETÉS ::11:: BEVEZETÉS
 A szervezetben a molekulákat alkotó elemeket páros számú elektronokból álló kötések kapcsolják össze, amelyek a molekula stabilitását biztosítják. Ezek a molekulák többnyire a békés egymás mellett élés
A szervezetben a molekulákat alkotó elemeket páros számú elektronokból álló kötések kapcsolják össze, amelyek a molekula stabilitását biztosítják. Ezek a molekulák többnyire a békés egymás mellett élés
CzB 2010. Élettan: a sejt
 CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
CzB 2010. Élettan: a sejt Sejt - az élet alapvető egysége Prokaryota -egysejtű -nincs sejtmag -nincsenek sejtszervecskék -DNS = egy gyűrű - pl., bactériumok Eukaryota -egy-/többsejtű -sejmag membránnal
Elválasztástechnikai és bioinformatikai kutatások. Dr. Harangi János DE, TTK, Biokémiai Tanszék
 Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Elválasztástechnikai és bioinformatikai kutatások Dr. Harangi János DE, TTK, Biokémiai Tanszék Fő kutatási területek Enzimek vizsgálata mannozidáz amiláz OGT Analitikai kutatások Élelmiszer analitika Magas
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Aktív életerő HU/KAR/0218/0001
 Aktív életerő HU/KAR/0218/0001 A bizonyítottan javítja az idősödő kutyák életminőségét: élénkebbé teszi az állatokat és ezáltal aktívabb életmódot tesz lehetővé számukra. Az oxigenizáció mellett a szív-
Aktív életerő HU/KAR/0218/0001 A bizonyítottan javítja az idősödő kutyák életminőségét: élénkebbé teszi az állatokat és ezáltal aktívabb életmódot tesz lehetővé számukra. Az oxigenizáció mellett a szív-
A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban
 A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés tézisek Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
A FAD transzportjának szerepe az oxidatív fehérje foldingban patkány máj mikroszómákban PhD értekezés tézisek Varsányi Marianne 2005 Témavezető: Dr. Bánhegyi Gábor Semmelweis Egyetem Orvosi Vegytani, Molekuláris
39. Elmeszesedés (calcificatio)
 Elmeszesedés 39. Elmeszesedés (calcificatio) élettani elmeszesedés (calcificatio phisiologia) aktív calcifikációs folyamat csontokban Ca 3 (PO 4 ) 2 9 rész CaCO 3... 1 rész kóros elmeszesedés (calcificatio
Elmeszesedés 39. Elmeszesedés (calcificatio) élettani elmeszesedés (calcificatio phisiologia) aktív calcifikációs folyamat csontokban Ca 3 (PO 4 ) 2 9 rész CaCO 3... 1 rész kóros elmeszesedés (calcificatio
15. elıadás SZERVES ÜLEDÉKES KİZETEK
 15. elıadás SZERVES ÜLEDÉKES KİZETEK A KİSZÉN A kıszén növényi eredető, szilárd, éghetı, fosszílis üledékes kızet. A kıszénképzıdés szakaszai: Biokémiai szénülési folyamatok: kis mélységben huminsavak
15. elıadás SZERVES ÜLEDÉKES KİZETEK A KİSZÉN A kıszén növényi eredető, szilárd, éghetı, fosszílis üledékes kızet. A kıszénképzıdés szakaszai: Biokémiai szénülési folyamatok: kis mélységben huminsavak
Kémiai reakciók. Közös elektronpár létrehozása. Általános és szervetlen kémia 10. hét. Elızı héten elsajátítottuk, hogy.
 Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
Általános és szervetlen kémia 10. hét Elızı héten elsajátítottuk, hogy a kémiai reakciókat hogyan lehet csoportosítani milyen kinetikai összefüggések érvényesek Mai témakörök a közös elektronpár létrehozásával
A krómvegyületek hatásmechanizmusának vizsgálata eukarióta élesztő sejteken. Ph.D. disszertáció Gazdag Zoltán
 A krómvegyületek hatásmechanizmusának vizsgálata eukarióta élesztő sejteken Ph.D. disszertáció Gazdag Zoltán Ph.D. program: Mikroorganizmusok életfolyamatainak molekuláris analízise Program és témavezető:
A krómvegyületek hatásmechanizmusának vizsgálata eukarióta élesztő sejteken Ph.D. disszertáció Gazdag Zoltán Ph.D. program: Mikroorganizmusok életfolyamatainak molekuláris analízise Program és témavezető:
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
A tananyag felépítése: A BIOLÓGIA ALAPJAI. I. Prokarióták és eukarióták. Az eukarióta sejt. Pécs Miklós: A biológia alapjai
 A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A BIOLÓGIA ALAPJAI A tananyag felépítése: Környezetmérnök és műszaki menedzser hallgatók számára Előadó: 2 + 0 + 0 óra, félévközi számonkérés 3 ZH: október 3, november 5, december 5 dr. Pécs Miklós egyetemi
A vér élettana 1./12 Somogyi Magdolna. A vér élettana
 A vér élettana 1./12 Somogyi Magdolna A vér folyékony kötőszövet Mesenchymális eredetű A vér élettana A) Szerepe: 1. transzport vérgázok, tápanyagok és végtermékek hormonok és vitaminok hőenergia víz szervetlen
A vér élettana 1./12 Somogyi Magdolna A vér folyékony kötőszövet Mesenchymális eredetű A vér élettana A) Szerepe: 1. transzport vérgázok, tápanyagok és végtermékek hormonok és vitaminok hőenergia víz szervetlen
SZÉRUM KOLESZTERIN ÉS TRIGLICERID MEGHATÁROZÁS
 SZÉRUM KOLESZTERIN ÉS TRIGLICERID MEGHATÁROZÁS A koleszterin, a koleszterin észterek, triacilglicerolok vízben oldhatatlan vegyületek. E lipidek a májból történő szintézist, és/vagy táplálék abszorpciót
SZÉRUM KOLESZTERIN ÉS TRIGLICERID MEGHATÁROZÁS A koleszterin, a koleszterin észterek, triacilglicerolok vízben oldhatatlan vegyületek. E lipidek a májból történő szintézist, és/vagy táplálék abszorpciót
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén
 ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
A sejtek lehetséges sorsa. A sejtek differenciálódása. Sejthalál. A differenciált sejtek tulajdonságai
 A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
A sejtek lehetséges sorsa A sejtek differenciálódása, öregedése Sejthalál osztódás az osztódási folyamatok befejezése és specializálódás egy (összetett) funkra: differenciá elöregedés (szeneszcencia) elhalás
A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év
 Témavezető neve: Dr. Csala Miklós A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év Háttér A glutation (GSH) és a glutation diszulfid
Témavezető neve: Dr. Csala Miklós A téma címe: Antioxidáns anyagcsere és transzportfolyamatok az endo/szarkoplazmás retikulumban A kutatás időtartama: 4 év Háttér A glutation (GSH) és a glutation diszulfid
Immunológia alapjai. 16. előadás. Komplement rendszer
 Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Immunológia alapjai 16. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Plazma enzim mediátorok: - Kinin rendszer - Véralvadási rendszer Lipid mediátorok Kemoattraktánsok: - Chemokinek:
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
A fotoszintézis molekuláris biofizikája (Vass Imre, 2000) 39
 A fotoszintézis molekuláris biofizikája (Vass Imre, 2000) 39 6. A citokróm b 6 f komplex A két fotokémiai rendszer közötti elektrontranszportot a citokróm b 6 f komplex közvetíti. Funkciója a kétszeresen
A fotoszintézis molekuláris biofizikája (Vass Imre, 2000) 39 6. A citokróm b 6 f komplex A két fotokémiai rendszer közötti elektrontranszportot a citokróm b 6 f komplex közvetíti. Funkciója a kétszeresen
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak
 BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
BIOGÉN ELEMEK Azok a kémiai elemek, amelyek az élőlények számára létfontosságúak A több mint száz ismert kémiai elem nagyobbik hányada megtalálható az élőlények testében is, de sokuknak nincsen kimutatható
MÉRGEK SORSA AZ ÉLŐ SZERVEZETBEN ELŐADÓ DR. LEHEL JÓZSEF
 MÉRGEK SORSA AZ ÉLŐ SZERVEZETBEN ELŐADÓ DR. LEHEL JÓZSEF 2006.09.13. 1 MÉREGHATÁS FELTÉTELE 1 kapcsolat (kémiai anyag biológiai rendszer) helyi hatás szisztémás Megfelelő koncentráció meghatározó tényező
MÉRGEK SORSA AZ ÉLŐ SZERVEZETBEN ELŐADÓ DR. LEHEL JÓZSEF 2006.09.13. 1 MÉREGHATÁS FELTÉTELE 1 kapcsolat (kémiai anyag biológiai rendszer) helyi hatás szisztémás Megfelelő koncentráció meghatározó tényező
Függelék Laboratóriumi referenciaértékek. Írta Gaál Tibor és Vajdovich Péter
 Függelék Laboratóriumi referenciaértékek Írta Gaál Tibor és Vajdovich Péter A referenciaértékek jelentősége A klinikus állatorvos számára a laboratóriumi diagnosztikai könyvek egyik leggyakrabban forgatott
Függelék Laboratóriumi referenciaértékek Írta Gaál Tibor és Vajdovich Péter A referenciaértékek jelentősége A klinikus állatorvos számára a laboratóriumi diagnosztikai könyvek egyik leggyakrabban forgatott
