Érzékelők és beavatkozók
|
|
|
- Léna Gáspárné
- 6 évvel ezelőtt
- Látták:
Átírás
1 Érzékelők és beavatkozók A tárgy előadói: Dr. Bársony István akadémikus, egyetemi tanár, kutatóprofesszor MTA EK Műszaki Fizikai és Anyagtudományi Intézet Dr. Battistig Gábor MTA Dr.,tud. osztályvezető, az MTA Elektronikus Eszközök és Technológiák Tud. Biz. elnöke valamint alkalmanként a MOGI egy-egy munkatársa
2 Érzékelés: Transducer: jelátalakítás jelátalakító
3 A folyamatszabályozás elve Érzékelés Jelfeldolgozás Beavatkozás analóg digitális analóg
4 Az elektronikus folyamatszabályzás vázlata
5 Tematika 1. Anyagismeret a) Atomszerkezet b) Kötések, kristályszerkezet c) Sávszerkezet, félvezetők d) Fémek 2. Érzékelési elvek, fizikai jelenségek a) Termikus elvek b) Ellenállás c) Kapacitás d) Mágneses indukció e) Piezo-elvek f) Optikai elvek 3. Érzékelési módszerek, alkalmazások a) Hossz, elmozdulás b) Sebesség, gyorsulás c) Nyomás, erő, nyomaték d) Kémiai érzékelés 4. Integrált érzékelő rendszerek a) Technológiai alapok, MEMS, NEMS, OEMS b) Szenzorhálózatok, IoT
6 1. Anyagismeret a. Atomszerkezet (ismétlés)
7 Elemi részecskék jellemzői Töltés Nyugalmi tömeg Forgási impulzus Mágneses momentum
8 A Bohr-féle atommodell Pozitív töltésű atommag Negatív töltésű elektron Niels Bohr ( ) Az elektron diszkrét pályákon kering a mag körül. Coulomb erő Probléma (a klasszikus fizika törvényei szerint): Centripetális erő A körpályán mozgó elektron energiát sugároz le elektromágneses hullámok formájában.
9 Bohr-féle posztulátumok 1.) Az atomon belül az elektronok meghatározott E n (n=1,2,3...) diszkrét körpályákon mozognak. 2.) Az elektronok mozgása sugárzásmentesen történik, a magasabb energiájú pályáról egy alacsonyabbra történő átmenet energiájú foton kibocsátásával, ill. fordított esetben annak elnyelésével jár. 3.) Stacionárius állapotban az elektron forgási impulzusa csak diszkrét értékeket vehet fel:
10 Bohr-féle atommodell A hidrogénatom sajátértékei Legalacsonyabb energiaszint: n=1 (a szabad elektronra vonatkoztatva) A hidrogénatom ionizációs energiája H H + + e: 13,6eV
11 Klasszikus részecskék: kicsiny tömör golyók, Kvantummechanika Hullám - részecske dualizmus tartózkodási helyük mindig pontosan ismert, impulzusuk és energiájuk meghatározott, interferencia ill. elhajlási jelenség fellépése kizárt. Klasszikus hullám: az energia és impulzus a térben folytonosan oszlik el, interferencia és elhajlás jelenségét mutatja. a klasszikus modellek nem kielégítően írják le az elektronok tulajdonságait, Schrödinger (1926) a részecskének feltételezett elektronok interferencia és elhajlási jelenséget mutatnak A saját tömeggel rendelkező részecskék hullámegyenlete Erwin Schrödinger
12 Részecske egydimenziós mozgása (dobozmodell) Modell Megoldás A részecske hullámfüggvénye Potenciális energiája A részecske energiaállapotai Schrödinger egy. V=0-ra n: az energia kvantáltsága Nullponti energia Részecske végtelen nagy doboz-potenciálon belül x=0 és x=l esetén
13 Az elektron 2 tartózkodási valószínűségsűrűsége egy adott gömbfelületen Pályák orientációja Lehetséges pályák száma Elektron héj
14 Kvantummechanika Az elektron tartózkodási valószínűsége a hidrogénatomban Tarózkodási valószínűség Bohr modell Kvantummechanikai modell az atommagtól mért távolság Mag Figyelem: Az elektronsűrűség a centrumban a legnagyobb!
15 Kvantummechanikailag megengedett elektron energiaállapotok Fő kvantumszám Héj Alhéj Állapotok Elektronok az n száma alhéjon héjon stb.
16 Kvantummechanika Az energiaszintek betöltésének szabályai az atomon belül Pauli elv: Az egy atomon belüli elektronok mind a négy kvantumszámukban nem egyezhetnek meg! Wolfgang Ernst Pauli Egy adott főhéjon elhelyezkedő elektronok maximális száma:
17 Energia / ev Energia / J Kvantummechanika Az elektron energiája a hidrogénatomban Bohr modell Kvantummechanikai modell
18 Kvantummechanika Az elektronpályák 3 dimenziós ábrázolása héj héj Az elektron 2 tartózkodási valószínűség-függvénye
19 Kvantummechanika Az elektronhéjak betöltésének szabályai Atom orbitális pálya: n és l kombinációja pályánként két elektron ellentétes irányú spinnel Hund-féle szabály (a legnagyobb multiplicitásról): a pályák betöltése először a pár nélküli elektronokkal
20 Az elemek elektronkonfigurációja
21 Energia Kvantummechanika Az állapotok energiaszintjei Az elektronok először mindig a legalacsonyabb energiaszintű üres pályákat töltik be Fő kvantumszám n: Elektronhéj l : Az elemek periódusos rendszere
22 Az elemek periódusos rendszere Dmitri Ivanovich Mendeleev
23 Az elemek periódusos rendszere Gázok Fémek Félvezetők Fémek Félfémek
24 Ionizációs energia Energiamennyiség egyetlen atom ionizálásához (ev) Kation (pozitív ion) Rendszám
25 Ionizációs energia Egyetlen atom ionizálásához szükséges energia (ev) Kation (pozitív ion) Nemesgázok
26 Elektronaffinitás Egyetlen elektron beépüléséhez szükséges energia Anion (negatív ion) Rendszám
27 Elektronaffinitás Egyetlen elektron beépüléséhez szükséges energia (ev) Lantanidák Aktinidák Anion (negatív ion)
28 1. Anyagismeret b. Kémiai kötések, kristályszerkezet (ismétlés)
29 Kémiai kötések A kötések kialakulásának oka: az atomok között ható erőhatások valamennyi kötéstípus esetében az elektrosztatikus vonzás és taszítás közötti egyensúly Vegyületképzés: az atomok külső elektronpályáinak kölcsönhatása révén (ionizálás, elektronfelvétel, elektronfelhők átlapolása) Típusai: (határesetek) kovalens kötés ionos kötés fémes kötés
30 erő Az atomok közötti kölcsönhatás távolságuk függvényében vonzás effektív erő atomtávolság taszítás Pl. pozitív és negatív ionok között Pl. a teljesen betöltött belső elektronhájak között Erőegyensúly: taszítóerő összenergia atomtávolság Egyensúlyi atomtávolság: Eredő kötési energia: vonzóerő
31 Hidrogénmolekula
32 Kovalens kötés: (homeopoláros kötés) Részben betöltött elektronhéjak ill. elektronpályák átfedése A szomszédos atom(ok) elektronjai segítenek a teljes héjbetöltöttség elérésében Növekszik az elektronsűrűség az atommagok között atomtávolság Példa: Hidrogén molekula molekula átmeneti állapot
33 Ionos (heteropoláros) kötés: NaCl
34 Ionos kötések: atom- és ionsugarak az I. oszlop elemei Kationok a VII. oszlop elemei Anionok rendszám rendszám Atomsugár Ionsugár
35 Tipikus hibridizációs struktúrák Atomtörzs Hibridpálya (kötés) lineáris háromszögű planáris tetraéderes négyzetes planáris trigon. kettős piramis oktaéderes
36 Koordináció, ionsugarak aránya és geometriák Koordináció, Geometria: Koordináció, (Atomsugarak aránya (Atomsugarak aránya
37 Kovalens kötés: gyémántszerkezetű szén (C) Gyémántszerkezetű: C, Si, Ge (izomorf) Alapállapot hibridizált állapot Koordináció: 4 hibridpálya Az elektronok Az elektronok energia-sémája energia-sémája a C atomban a gyémántban
38 Ionos kötés (heteropoláros kötés) Kis ionizációs energia Nagy elektronaffinitás
39 Kristályképződés a kötéstípusok és koordináció (kötésszög) függvényében Ionos kötés pl:nacl Kovalens kötés pl: GaAs
40 Kötéstípusok összehasonlítása ionos kovalens fémes I.+VII. : NaCL II.+VI.: MgO oszlopok elemeinek vegyületei Félvezetők: Molekulák: Intermetallikusv.: SiC, GaAs, CH 4 InP, InSb, Elemi félvezetők: GaN Si, Ge, C Elemi fémek
41
42 Anyagtudományi tetréder Szerkezet Jellemzés Tulajdonságok Technológia Viselkedés
43 1. Anyagismeret c. Sávszerkezet, félvezetők
44 Vonzó erő Taszító erő Az atomok közötti erőhatások Coulomb erő pontszerű töltések között: F qq 4 r 0 2 Az atomok közötti távolság Taszító erő: a kölcsönhatásba lépő atomok azonos töltésű részecskéi, pl. elektronhéjai között F taszító ~ 1/r Vonzó erő: egyik atom atommagja és a szomszédos atom elektronjai között F vonzó ~ 1/r 2 a Az elektrosztatikus kölcsönhatás eredményeképp az az egyensúlyi távolság alakul ki, ahol legkisebb az eredő potenciális energia
45 Ún. vákuumenergiaszint Megengedett energiaállapotok az atomon belül a 11-es rendszámú Na két atomja egymástól távol E 1, E 2, : az adott energiaszint állapotaiban lévő elektronok kiszakításához szükséges energia E E 3s 1 2p 6 2s 2 E 1 E 2 E 3 E 4 2s 2 2p6 3s 1 Potenciálgát 1s 2 1s 2 r»a Távolság a két atommag között Nincs elektroncsere a két azonos felépítésű atom között, amik külön rendszert alkotnak!
46 A két (ill. több) atom immár egy rendszert alkot, erre kell teljesülnie a Pauli-elvnek, azaz az azonos energiaszintek felhasadnak, ezek sokasága energiasávot alkot! E 1 E 2 Energiaszintek felhasadása Az energiasávok kialakulása: sávmodell A 11-es rendszámú Na két szomszédos atomja a kristályrácsban A potenciálgát maximuma: az atomtávolság csökkenésével csökken Ún. vákuumenergiaszint E E 3 } rácsállandó E a = 4,3 Ångstrom A vezetési sávban az elektronok mozgó töltéshordozók, azaz szabadon közlekednek a rendszerben :! } 1s 2 } 2s 2 2p6 3s 1 Vezetési sáv (szabad elektronok) Vegyértéksáv (legkülső teljesen betöltött energiaszintig: benne az elektronok kötöttek)
47 Az anyagok osztályozása a sávmodell alapján A sávok relatív helyzete és az egyes sávokban megengedett elektronállapotok betöltöttsége szerint Fermi-energiaszint E F A Fermi-energiaértéknél alacsonyabb energiájú megengedett elektronállapotok nagy valószínűséggel fel vannak töltve elektronokkal. E F E F elektromos viselkedésük alapján
48 E E Vezetők: Vezetési sáv Félvezetők: vezetési sáv * * * vegyértéksáv E F E L E G <4,5 ev E L E V Szilárd testek osztályozása: vezetők, félvezetők, szigetelők vezetési sáv vegyértéksáv Szigetelők: vezetési sáv E G >4,5 ev vegyértéksáv E F E V E L E L E V E F Vegyértéksáv (valenciasáv) a legfelső, (vegyérték)elektronokkal teljesen telített energiasáv (T 0 = 0 K) E v :a vegyértéksáv felső szélének energiaszintje Vezetési sáv a legalsó üres, vagy (vezetési) elektronokkal csak részben telített energiasáv (T 0 = 0 K) E L : a vezetési sáv alsó szélének energiaszintje Tiltott sáv E G E V és E L közötti távolság, azon energiaértékek, amelyeket elektronok nem foglalhatnak el
49 Szilárd testek sávmodellje Elektronok: Fermi-eloszlás, állapot-eloszlás, tényleges elektron-sűrűség Fermi-eloszlás szigetelők félvezetők fémek VS üres VS üres VS félig tele VÉS tele tele T=0 T=0 T=0 z(e): Megengedett elektronállapot-eloszlás f (E)z(E) : tényleges elektron-sűrűség f(e): Fermi-eloszlás: adott E állapot betöltöttségi valószinűsége T hőmérsékleten E F : Fermi-szint: vezető elektronok maximális energiaszintje (0 K-en, külső erőtér nulla)
50 Félvezetők a periódusos rendszerben Periódus Oszlop Tiltott sávszélesség W G (ev) akceptor donor Si-ban és Ge-ban
51 energia Sávszerkezet: az energiaszintek helyzete a gyémántban, Ge-ban, Si-ban (szigetelő félvezető) üres teli törzs atomonként három állapot atomonként három állapot atomonként egy állapot valencia elektronok atomonként egy állapot anyag gyémánt (C) szilícium germánium tiltott sáv az atomtörzs átmérője r (nm)
52 A félvezetők felosztása Félvezetők Elektron félvezető Vegyes félvezető Ion félvezető Sajátvezetéses (intrinsic-vezető) Elektrontöbblet (n-vezető) Adalékolt (szennyezéses) Elektronhiány (p-vezető) Gyakorlati félvezetőkkel szembeni követelmények: Sávszélesség: 0,1 4,5eV Ionvezetés nem megengedett elektronvezetés a vezetési-, lyukvezetés a valenciasávban kémiai és termikus stabilitás adalékanyagok oldékonysága K o v a l e n s
53 Energia A Si rács- és sávszerkezete Indirekt átmenet gyémántrács impulzus
54 Energia A Ge rács- és sávszerkezete Indirekt átmenet gyémántrács impulzus
55 Energia A GaAs rács- és sávszerkezete Direkt átmenet cinkblende impulzus
56 A Si rács kétdimenziós ábrázolása (T=0K) Egyszerű sávmodell Vezetési sáv Vegyérték sáv valencia elektron hibridizáció nincs elektron a vezetési sávban
57 A Si kétdimenziós rácsszerkezete (T>0K) Egyszerű sávszerkezet Vezetési sáv Vegyértéksáv Energiaközlés szabad elektronok a vezetési sávban lyukak (elektronhiány) a vegyértéksávban
58 Sajátvezetés Fermi-szint a sajátvezetésnél Termikus egyensúly a félvezetőben sajátvezetésnél Töltéshordozó-koncentráció a sajátvezetésnél Intrinsic félvezető vezetési (szabad) elektronok lyukak (elektronhiány)
59 Sajátvezetés Sajátvezetés termikusan gerjesztett lyuk-elektron párok révén Intrinsic vezetőképesség: Az elektronok és lyukak mozgékonysága: A mozgékonyság hőmérséklet függése:
60 Fermi-függvény, Fermi-szint, állapotsűrűség-függvény, elektronsűrűség-eloszlás intrinsic félvezetőben Fermi-szint W Fi Fermi-függvény Állapotsűrűség eloszlás Szabad állapotok a valenciasávban betöltött állapotok a vezetési sávban Betöltöttségi valószínűség (Fermi-) függvény, állapotsűrűség- és elektronsűrűség-eloszlás T>0K esetén sajátvezetésnél
61 Az elemi és vegyület-félvezetők izoelektronikus vázlata Elemi- és Vegyület-félvezetők IV-IV III-V II-VI Egy atomra jutó elektronok átlagos száma
62 Periodus Félvezető (alkotó-)elemek a periódusos rendszerben és tiltott sáv szélességük W G (ev) értéke Oszlop
63 A legfontosabb félvezetők adatai (T=300K) Félvezető Tilos sáv Dielektromos állandó eff. állapotsűrűség a vezetési sávban eff. állapotsűrűség a valencia sávban elektronmozgékonyság lyukmozgékonyság elektron effektív/nyugalmi tömeg aránya lyuk effektív/nyugalmi tömeg aránya
64 Sávszélesség Intrinsic koncentráció Tilos sávszélesség (W G ) és intrinsic koncentráció (n i ) a hőmérséklet (T) függvényében
65 A Fermi-energia (W Fi ) hőmérsékletfüggése Fermi-energia W Fi nem degenerált félvezető degenerált félvezető Si-ban, Ge-ban és GaAs-ben degeneráció csak magas hőmérsékleten vagy extrém nagy adalékolás mellett lép fel!
66 Szennyezéses félvezetők Reális kristályok mindig tartalmaznak kristályhibákat: Ponthibák: hiányzó rácsatomok, atomok rácsközi helyeken, idegen atomok véletlenszerű szennyeződés célzottan bevitt adalékolás Diszlokációk: rácsatomok távolságának periodicitása sérül; a keletkező mechanikaia feszültség vonzza a beépülő idegen atomokat getterezés A félvezető egykristályok tisztasága: kristályhibasűrűség = cm -3 a diszlokációsűrűség max. megengedett értéke: műszakilag gyártható diszlokáció-mentes kristályban:
67 Az i-, n- és p-vezetés összehasonlítása félvezetőkben i-vezetés (sajátvezető) n-vezetés (donoradalékolt) p-vezetés (akceptoradalékolt) vezetési sáv vezetési sáv vezetési sáv donor nívók akceptor nívók vegyérték sáv vegyérték sáv vegyérték sáv
68 Adalékolt félvezetők: állapotsűrűség (z), elektron- (n) és lyukkoncentráció (p) sajátvezetés n-adalékolás p-adalékolás
69 Adalékolt félvezetők, donor- és akceptor, sekély és mély nívók Donor Akceptor Olyan ponthiba a kristályrácsban, amely szabad elektront ad le a vezetési sávba és a félvezetőt n-vezetésre teszi alkalmassá. Ionizációs energia*: Olyan ponthiba a kristályrácsban, amely elektront vesz fel a vegyérték sávból és a félvezetőt p-vezetésre teszi alkalmassá. Ionizációs energia*: Sekély (adalék) és mély (csapda) állapotok (nívók) kategórizálás a valós ionizációs energia szerint *Az ionizációs energiát a H-modell alapján számíthatjuk ki:
70 A szennyező-elemek energiaszintjei Si-ban donor szint vezetés akceptor szint vezetés
71 A szennyező-elemek energiaszintjei GaAs-ben donor szint vezetés akceptor szint vezetés
72 Mély nívók, elektron csapdaszintek GaAs-ben Gyakorlati alkalmazás: Kvázi-szigetelő tarto-mányok kialakítása a félvezetőben (pl. FET) Generáció a sekély állapoton és elektron csapdázódás a mély nívón A befogási folyamat eredményeképp csökkent a vezetési elektronok száma
73 Rekombinációs centrumok A rekombinációs centrumok technológiai hasznosítása: pl. gyors kapcsolóeszközökben (p-nátmenet) Generáció (elektron ill. lyuk) a sekély nívókon (D ill. A); rekombináció a mély nívón (RC) A rekombinációs folyamatban Megsemmisül egy szabad töltéshordozó pár
74 Adalékolt (extrinsic) félvezetők Extrinsic azaz adalékolt félvezetők n-típusú félvezető - donor adalékolással p-típusú félvezető - akceptor adalékolással Az adalékatomok sekély energiájú megengedett állapotokat generálnak a félvezető tiltott sávjában Állapotsűrűség ill. Többségi / kisebbségi töltéshordozó Termodinamikus egyensúlyban a félvezető kristály semleges: Az egyensúlyi lyuk- és elektronkoncentráció meghatározása: Elektronkoncentráció (n) a vezetési sávban Lyukkoncentráció (p) a valencia sávban
75 Az effektív adalékolás hőmérsékletfüggése Hőmérsékletfüggő szabad elektronkoncentráció extrinsic félvezetőben eltérő donor adalékolás esetén A hőmérséklet függvényében részleges n<n D (R), vagy teljes n=n D (E) ionizációval, azaz effektív adalékolással számolhatunk a W D ionizációs energiának megfelelően.
76 A Fermi-szint helyzete az extrinsic Si-ban Fermi-szint az intrinsic esetben
77 A vezetőképesség hőmérsékletfüggése intrinsic és extrinsic félvezetőben adalékkoncentráció mozgékonyság vezetőképesség I: intrinsic E: teljes ionizáció R: részleges ionizáció
78 A félvezetők alkalmazhatóságának maximális hőmérséklete félvezető T T max n i N A ill. N D
79 Félvezetők több minimummal az E(k) diagramban A Gunn-effektus Gunn-hatás vezetési sáv valencia sáv A szabad elektronok az energetikailag magasabb mellékminimumokba gerjesztődnek, ahol mozgékonyságuk drasztikusan csökken. impulzus
80 Töltéskiegyenlítődési folyamatok időben és térben Többlet lyuk-koncentráció felépülése és lecsengése állandó generációs ráta mellett Lyuk-koncentráció többlet térbeli lecsengése, ha a kezdeti lyuk-többlet
81 Galvanomágneses hatások a félvezetőkben n-félvezető p-félvezető A töltéshordozók eltérítése a B mágneses térben: Hall-effektus n- és p- típusú félvezetőben Az elektromos ellenállás megváltozása mágneses térben - B mérés
82 A Seebeck-effektus Vezető fém Félvezető Félvezető Vezető fém
83 1. Anyagismeret d. Fémek elektromágneses viselkedése
84 Fémek elektromos tulajdonságai j áramsűrűség és elektromos vezetőképesség definíciója Áramsűrűség: ahol driftsebesség elemi töltés töltéshordozó-sűrűség töltési szám z e = -1 Ohm törvénye: Elektromos térerősség a töltéshordozók mozgékonysága Lyukakkal (defektelektronokkal) kiegészítve: Ált. vezetőképesség: össz
85 Fémek elektromos tulajdonságai Az elektron gyorsulása az elektromos erőtérben, mozgékonyság Az elektron sebességének időbeli alakulása E>0 esetén (t 1 - t 4 között) Az M n effektív tömegű elektron gyorsuló mozgása Az elektron repülési (ütközési) ideje Az elektron átlagsebessége Az elektron mozgékonysága n Áramsűrűség
86 Fémek elektromos tulajdonságai Matthiessen-szabály =f (T) a valós fémekben Hőmérsékleti összetevő Maradék összetevő Matthiessen-szabály Rácsionok hőmozgása (egyéb paraméterek) Szennyeződések stb. R/R 290K 3 féle különböző mértékben szennyezett Na-mintára más hőmérséklet-független paraméterek: idegen atomok diszlokációk más rácshibák (szemcsehatárok, szekunder halmazállapotok )
87 Fémek elektromos tulajdonságai Az ellenállás megnövekedése a beépült idegen atomok miatt Rendszám Rendszám
88 Fémek elektromos tulajdonságai fémek fajlagos ellenállása a hőmérséklet függvényében Hőmérséklet / C A fajlagos ellenállás hőmérsékletfüggése = (1 + T) T hőmérséklet C-ban Hőmérséklet / K
89 Fémek elektromos tulajdonságai Termoelektromos hatások fémekben és félvezetőkben hatás hatás hatás Vezető 1 Vezető 1 Vezető Vezető 2 Vezető 2 Vezető Az A és B közötti hőmérsékletkülönbség miatt potenciálkülönbség lép fel és elektromos áram folyik: U th = AB T Seebeck-tényező Felmelegedés ill. lehűlés (+Q, -Q) A-ban és B-ben az áthajtott elektromos áram miatt = AB I Peltier-tényező Felmelegedés vagy lehűlés homogén vezetőben, ha kívülről áramot és hőmérsékletváltozást is rákényszerítünk dp th = th I grad(t)dv Thomson-tényező
90 Fémek elektromos tulajdonságai Különböző Fermi-energiájú fémek kontaktusfeszültsége Szabad elektronok Fém Fém 1 Fém 2 Fém 1 Fém 2 Két különböző Fermienergiájú (W F1 és W F2 ) fém energiaállapota és a kilépési energiák: W A1 és W A2 Érintkezés esetén (W F közös Fermi-energia) a kiegyenlítő-töltés potenciálkülönbséget eredményez U 12 kontaktus-feszültség
91 Fémek elektromos tulajdonságai Termikus vezetőképesség fémekben Nem fémes szilárdtestekben: a hővezetést rácsrezgések képezik Fémekben: a szabad elektronok által képviselt plusz energiaáramlás jelentősebb Hőáram-sűrűség Energia elektrononként Egy elektronra ható erő Mozgásegyenlet: Hővezetési képesség Hőáram-sűrűség Hő- és töltésáramlás összekapcsolódása fémekben és félvezetőkben: termo-erő
92 Fémek a méréstechnikában Alkalmazási elvek Fémek a méréstechnikában Hőmérséklet T F erő, M nyúlás T 0 viszonyítási hőmérséklettel anyag A U H segédfeszültséggel Ellenálláshőmérő B anyag Termoelem Nyúlásmérő bélyeg
93 Fémek a méréstechnikában Termoelektromos hatások: Seebeck-effektus A hőmérsékletkülönbség potenciálkülönbséget generál: Vezető 1 Vezető 2 Seebeck-tényező (termoerő) termofeszültség Az A, B anyagok abszolút termoereje termoelem Termopárban a fémek bizonyulnak előnyösebbnek, mivel a félvezetőkkel ellentétben rugalmas huzal formában gyárthatók
94 Fémek a méréstechnikában Termoelemek (termopárok) a hőmérséklet méréséhez Hőelemek (termopárok) kiválasztásának szempontjai: nagy termikus-feszültség U th U th és T között lineáris összefüggés magas olvadáspont kémiai rezisztencia magas hőmérsékleteken Előnyök: nincs szükség külső áramellátásra egyszerű, áttekinthető mérőrendszer viszonylag erős mechanikai igénybevételt is elvisel (hajlítható drótok) viszonylag olcsó a felhasználható anyagok széles skálája nagy hőmérsékletátfogás Hátrányok: nemlineáris hőmérséklet-jelleggörbe referenciahőmérséklet szükséges hosszú távú stabilitása más hőmérséklet-szenzorokhoz képest alacsony kisebb érzékenységű más hőmérséklet-szenzorokhoz képest
DR. KOVÁCS ERNŐ ELEKTRONIKA II. (DISZKRÉT FÉLVEZETŐK, ERŐSÍTŐK) ELŐADÁS JEGYZET
 MISKOLCI EGYETEM VILLAMOSMÉRNÖKI INTÉZET ELEKTROTECHNIKAI- ELEKTRONIKAI TANSZÉK DR. KOVÁCS ERNŐ ELEKTRONIKA II. (DISZKRÉT FÉLVEZETŐK, ERŐSÍTŐK) ELŐADÁS JEGYZET 2003. 2.0. Diszkrét félvezetők és alkalmazásaik
MISKOLCI EGYETEM VILLAMOSMÉRNÖKI INTÉZET ELEKTROTECHNIKAI- ELEKTRONIKAI TANSZÉK DR. KOVÁCS ERNŐ ELEKTRONIKA II. (DISZKRÉT FÉLVEZETŐK, ERŐSÍTŐK) ELŐADÁS JEGYZET 2003. 2.0. Diszkrét félvezetők és alkalmazásaik
Szilárdtestek sávelmélete. Sávelmélet a szabadelektron-modell alapján
 Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Szilárdtestek el e ek e tr t o r n o s n zer e k r ez e et e e t
 Szilárdtestek elektronszerkezete Kvantummechanikai leírás Ismétlés: Schrödinger egyenlet, hullámfüggvény, hidrogén-atom, spin, Pauli-elv, periódusos rendszer 2 Szilárdtestek egyelektron-modellje a magok
Szilárdtestek elektronszerkezete Kvantummechanikai leírás Ismétlés: Schrödinger egyenlet, hullámfüggvény, hidrogén-atom, spin, Pauli-elv, periódusos rendszer 2 Szilárdtestek egyelektron-modellje a magok
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
1. SI mértékegységrendszer
 I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
Thomson-modell (puding-modell)
 Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Fogorvosi anyagtan fizikai alapjai 9. Hőtani, elektromos és kémiai tulajdonságok
 Fogorvosi anyagtan fizikai alapjai 9. Hőtani, elektromos és kémiai tulajdonságok Kiemelt témák: Elektromosságtan alapfogalmai Szilárdtestek energiasáv modelljei Félvezetők és alkalmazásaik Tankönyv fej.:
Fogorvosi anyagtan fizikai alapjai 9. Hőtani, elektromos és kémiai tulajdonságok Kiemelt témák: Elektromosságtan alapfogalmai Szilárdtestek energiasáv modelljei Félvezetők és alkalmazásaik Tankönyv fej.:
Fermi Dirac statisztika elemei
 Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Közös minimum kérdések és Vizsgatételek a Fizika III tárgyhoz
 Közös minimum kérdések és Vizsgatételek a Fizika III tárgyhoz 2005. Fizika C3 KÖZÖS MINIMUM KÉRDÉSEK Kvantummechanika 1. Rajzolja fel a fekete test sugárzását jellemző kísérleti görbéket T 1 < T 2 hőmérsékletek
Közös minimum kérdések és Vizsgatételek a Fizika III tárgyhoz 2005. Fizika C3 KÖZÖS MINIMUM KÉRDÉSEK Kvantummechanika 1. Rajzolja fel a fekete test sugárzását jellemző kísérleti görbéket T 1 < T 2 hőmérsékletek
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
FELADATMEGOLDÁS. Tesztfeladat: Válaszd ki a helyes megoldást!
 FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
FÉLVEZETŐ ESZKÖZÖK I. Elektrotechnika 4. előadás
 FÉLVEZETŐ ESZKÖZÖK I. Elektrotechnika 4. előadás FÉLVEZETŐ ESZKÖZÖK A leggyakrabban használt félvezető anyagok a germánium (Ge), és a szilícium (Si). Félvezető tulajdonsággal rendelkező elemek: szén (C),
FÉLVEZETŐ ESZKÖZÖK I. Elektrotechnika 4. előadás FÉLVEZETŐ ESZKÖZÖK A leggyakrabban használt félvezető anyagok a germánium (Ge), és a szilícium (Si). Félvezető tulajdonsággal rendelkező elemek: szén (C),
Az anyagszerkezet alapjai. Az atomok felépítése
 Az anyagszerkezet alapjai Az atomok felépítése Kérdések Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Az anyagszerkezet alapjai Az atomok felépítése Kérdések Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Atomfizika. Az atommag szerkezete. Radioaktivitás Biofizika, Nyitrai Miklós
 Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
dinamikai tulajdonságai
 Szilárdtest rácsok statikus és dinamikai tulajdonságai Szilárdtestek osztályozása kötéstípusok szerint Kötések eredete: elektronszerkezet k t ionok (atomtörzsek) tö Coulomb- elektronok kölcsönhatás lokalizáltak
Szilárdtest rácsok statikus és dinamikai tulajdonságai Szilárdtestek osztályozása kötéstípusok szerint Kötések eredete: elektronszerkezet k t ionok (atomtörzsek) tö Coulomb- elektronok kölcsönhatás lokalizáltak
Az anyagszerkezet alapjai. Az atomok felépítése
 Az anyagszerkezet alapjai Az atomok felépítése Kérdések Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Az anyagszerkezet alapjai Az atomok felépítése Kérdések Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Mérés és adatgyűjtés
 Mérés és adatgyűjtés 7. óra Mingesz Róbert Szegedi Tudományegyetem 2013. április 11. MA - 7. óra Verzió: 2.2 Utolsó frissítés: 2013. április 10. 1/37 Tartalom I 1 Szenzorok 2 Hőmérséklet mérése 3 Fény
Mérés és adatgyűjtés 7. óra Mingesz Róbert Szegedi Tudományegyetem 2013. április 11. MA - 7. óra Verzió: 2.2 Utolsó frissítés: 2013. április 10. 1/37 Tartalom I 1 Szenzorok 2 Hőmérséklet mérése 3 Fény
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
A FÉMES KÖTÉS ÉRTELMEZÉSE A SZABADELEKTRON MODELL ALAPJÁN
 A FÉMES KÖTÉS ÉRTELMEZÉSE A SZABADELEKTRON MODELL ALAPJÁN Energia (W) és erőhatás (F) az anyagi rácsban Rácstípusok: ionrács, atomrács, molekularács. A részecskék azokat a helyeket foglalják el a rácsban,
A FÉMES KÖTÉS ÉRTELMEZÉSE A SZABADELEKTRON MODELL ALAPJÁN Energia (W) és erőhatás (F) az anyagi rácsban Rácstípusok: ionrács, atomrács, molekularács. A részecskék azokat a helyeket foglalják el a rácsban,
A periódusos rendszer, periodikus tulajdonságok
 A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Általános és szervetlen kémia 3. hét Kémiai kötések. Kötések kialakítása - oktett elmélet. Lewis-képlet és Lewis szerkezet
 Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Bevezetés az anyagtudományba II. előadás
 Bevezetés az anyagtudományba II. előadás 010. febuá 11. Boh-féle atommodell 1914 Niels Henik David BOHR 1885-196 Posztulátumai: 1) Az elekton a mag köül köpályán keing. ) Az elektonok számáa csak bizonyos
Bevezetés az anyagtudományba II. előadás 010. febuá 11. Boh-féle atommodell 1914 Niels Henik David BOHR 1885-196 Posztulátumai: 1) Az elekton a mag köül köpályán keing. ) Az elektonok számáa csak bizonyos
9. évfolyam. Osztályozóvizsga tananyaga FIZIKA
 9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
Az elektronpályák feltöltődési sorrendje
 3. előadás 12-09-17 2 12-09-17 Az elektronpályák feltöltődési sorrendje 3 Az elemek rendszerezése, a periódusos rendszer Elsőként Dimitrij Ivanovics Mengyelejev és Lothar Meyer vette észre az elemek halmazában
3. előadás 12-09-17 2 12-09-17 Az elektronpályák feltöltődési sorrendje 3 Az elemek rendszerezése, a periódusos rendszer Elsőként Dimitrij Ivanovics Mengyelejev és Lothar Meyer vette észre az elemek halmazában
 http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
Sugárzások kölcsönhatása az anyaggal
 Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Az anyagszerkezet alapjai
 Kérdések Az anyagszerkezet alapjai Az atomok felépítése Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Kérdések Az anyagszerkezet alapjai Az atomok felépítése Mik az építőelemek? Milyen elvek szerint épül fel az anyag? Milyen szintjei vannak a struktúrának? Van-e végső, legkisebb építőelem? A legkisebbeknél
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet
 Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
A kémiai kötés. Kémiai kölcsönhatás
 A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE
 AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008.
 Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
A kovalens kötés polaritása
 Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
AZ ATOM. Atom: atommag + elektronfelhő = proton, neutron, elektron. Elemi részecskék
 AZ ATOM Atom: atommag + elektronfelhő = proton, neutron, elektron Elemi részecskék Atomok Dalton elmélete (1805): John DALTON 1766-1844 1. Az elemek apró részecskékből, atomokból állnak. Atom: görög szó
AZ ATOM Atom: atommag + elektronfelhő = proton, neutron, elektron Elemi részecskék Atomok Dalton elmélete (1805): John DALTON 1766-1844 1. Az elemek apró részecskékből, atomokból állnak. Atom: görög szó
Periódusosság. Általános Kémia, Periódikus tulajdonságok. Slide 1 of 35
 Periódusosság 3-1 Az elemek csoportosítása: a periódusos táblázat 3-2 Fémek, nemfémek és ionjaik 3-3 Az atomok és ionok mérete 3-4 Ionizációs energia 3-5 Elektron affinitás 3-6 Mágneses 3-7 Az elemek periodikus
Periódusosság 3-1 Az elemek csoportosítása: a periódusos táblázat 3-2 Fémek, nemfémek és ionjaik 3-3 Az atomok és ionok mérete 3-4 Ionizációs energia 3-5 Elektron affinitás 3-6 Mágneses 3-7 Az elemek periodikus
3. (b) Kereszthatások. Utolsó módosítás: április 1. Dr. Márkus Ferenc BME Fizika Tanszék
 3. (b) Kereszthatások Utolsó módosítás: 2013. április 1. Vezetési együtthatók fémekben (1) 1 Az elektrongáz hővezetési együtthatója A levezetésben alkalmazott feltételek: 1. Minden elektron ugyanazzal
3. (b) Kereszthatások Utolsó módosítás: 2013. április 1. Vezetési együtthatók fémekben (1) 1 Az elektrongáz hővezetési együtthatója A levezetésben alkalmazott feltételek: 1. Minden elektron ugyanazzal
Atommodellek. Az atom szerkezete. Atommodellek. Atommodellek. Atommodellek, A Rutherford-kísérlet. Atommodellek
 Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
Elektromos áram. Vezetési jelenségek
 Elektromos áram. Vezetési jelenségek Emlékeztető Elektromos áram: töltéshordozók egyirányú áramlása Áramkör részei: áramforrás, vezető, fogyasztó Áramköri jelek Emlékeztető Elektromos áram hatásai: Kémiai
Elektromos áram. Vezetési jelenségek Emlékeztető Elektromos áram: töltéshordozók egyirányú áramlása Áramkör részei: áramforrás, vezető, fogyasztó Áramköri jelek Emlékeztető Elektromos áram hatásai: Kémiai
Egyenáram. Áramkörök jellemzése Fogyasztók és áramforrások kapcsolása Az áramvezetés típusai
 Egyenáram Áramkörök jellemzése Fogyasztók és áramforrások kapcsolása Az áramvezetés típusai Elektromos áram Az elektromos töltéshordozók meghatározott irányú rendezett mozgását elektromos áramnak nevezzük.
Egyenáram Áramkörök jellemzése Fogyasztók és áramforrások kapcsolása Az áramvezetés típusai Elektromos áram Az elektromos töltéshordozók meghatározott irányú rendezett mozgását elektromos áramnak nevezzük.
ω mennyiségek nem túl gyorsan változnak
 Licenszvizsga példakérdések Fizika szak KVANTUMMECHANIKA Egy részecskére felírt Schrödinger egyenlet szétválasztható a három koordinátatengely irányában levő egydimenziós egyenletre ha a potenciális energiára
Licenszvizsga példakérdések Fizika szak KVANTUMMECHANIKA Egy részecskére felírt Schrödinger egyenlet szétválasztható a három koordinátatengely irányában levő egydimenziós egyenletre ha a potenciális energiára
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK. Kalocsai Angéla, Kozma Enikő
 ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
Orvosi jelfeldolgozás. Információ. Információtartalom. Jelek osztályozása De, mi az a jel?
 Orvosi jelfeldolgozás Információ De, mi az a jel? Jel: Információt szolgáltat (információ: új ismeretanyag, amely csökkenti a bizonytalanságot).. Megjelent.. Panasza? információ:. Egy beteg.. Fáj a fogam.
Orvosi jelfeldolgozás Információ De, mi az a jel? Jel: Információt szolgáltat (információ: új ismeretanyag, amely csökkenti a bizonytalanságot).. Megjelent.. Panasza? információ:. Egy beteg.. Fáj a fogam.
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis-elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis-elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
8. AZ ATOMMAG FIZIKÁJA
 8. AZ ATOMMAG FIZIKÁJA Az atommag szerkezete (40-44 oldal) A tömegspektrométer elve Az atommag komponensei Izotópok Tömeghiány, kötési energia, stabilitás Magerők Magmodellek Az atommag stabilitásának
8. AZ ATOMMAG FIZIKÁJA Az atommag szerkezete (40-44 oldal) A tömegspektrométer elve Az atommag komponensei Izotópok Tömeghiány, kötési energia, stabilitás Magerők Magmodellek Az atommag stabilitásának
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
MIKROELEKTRONIKA, VIEEA306
 Budaesti Műszaki és Gazdaságtudomáyi Egyetem Elektroikus Eszközök Taszéke MIKROELEKTRONIKA, VIEEA306 Félvezető fizikai alaok htt://www.eet.bme.hu/~oe/miel/hu/03-felvez-fiz.tx htt://www.eet.bme.hu Budaesti
Budaesti Műszaki és Gazdaságtudomáyi Egyetem Elektroikus Eszközök Taszéke MIKROELEKTRONIKA, VIEEA306 Félvezető fizikai alaok htt://www.eet.bme.hu/~oe/miel/hu/03-felvez-fiz.tx htt://www.eet.bme.hu Budaesti
Elektronok, atomok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
2. (d) Hővezetési problémák II. főtétel - termoelektromosság
 2. (d) Hővezetési problémák II. főtétel - termoelektromosság Utolsó módosítás: 2015. március 10. Kezdeti érték nélküli problémák (1) 1 A fél-végtelen közeg a Az x=0 pontban a tartományban helyezkedik el.
2. (d) Hővezetési problémák II. főtétel - termoelektromosság Utolsó módosítás: 2015. március 10. Kezdeti érték nélküli problémák (1) 1 A fél-végtelen közeg a Az x=0 pontban a tartományban helyezkedik el.
Periódusosság. Általános Kémia, Periódikus tulajdonságok. Slide 1 of 35
 Periódusosság 11-1 Az elemek csoportosítása: a periódusos táblázat 11-2 Fémek, nemfémek és ionjaik 11-3 Az atomok és ionok mérete 11-4 Ionizációs energia 11-5 Elektron affinitás 11-6 Mágneses 11-7 Az elemek
Periódusosság 11-1 Az elemek csoportosítása: a periódusos táblázat 11-2 Fémek, nemfémek és ionjaik 11-3 Az atomok és ionok mérete 11-4 Ionizációs energia 11-5 Elektron affinitás 11-6 Mágneses 11-7 Az elemek
Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty
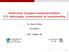 Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty Dr. Berta Miklós bertam@sze.hu 2017. október 26. 1 / 11 Tekintsünk egy olyan kristályrácsot, amelynek minden mérete sokkal
Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty Dr. Berta Miklós bertam@sze.hu 2017. október 26. 1 / 11 Tekintsünk egy olyan kristályrácsot, amelynek minden mérete sokkal
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Atomszerkezet, kötések
 Anyagszerkezettan és anyagvizsgálat 016/17 Atomszerkezet, kötések Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük: a két alapvető atommodell alapjait, és a modellek közötti különbségeket;
Anyagszerkezettan és anyagvizsgálat 016/17 Atomszerkezet, kötések Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük: a két alapvető atommodell alapjait, és a modellek közötti különbségeket;
Vezetési jelenségek, vezetőanyagok
 Anyagszerkezettan és anyagvizsgálat 2015/16 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők
Anyagszerkezettan és anyagvizsgálat 2015/16 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők
Bevezetés a modern fizika fejezeteibe. 4. (a) Kvantummechanika. Utolsó módosítás: november 15. Dr. Márkus Ferenc BME Fizika Tanszék
 Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Periódusos rendszer (Mengyelejev, 1869) nemesgáz csoport: zárt héj, extra stabil
 s-mezı (fémek) Periódusos rendszer (Mengyelejev, 1869) http://www.ptable.com/ nemesgáz csoport: zárt héj, extra stabil p-mezı (nemfém, félfém, fém) d-mezı (fémek) Rendezés elve: növekvı rendszám (elektronszám,
s-mezı (fémek) Periódusos rendszer (Mengyelejev, 1869) http://www.ptable.com/ nemesgáz csoport: zárt héj, extra stabil p-mezı (nemfém, félfém, fém) d-mezı (fémek) Rendezés elve: növekvı rendszám (elektronszám,
Elektronika Alapismeretek
 Alapfogalmak lektronika Alapismeretek Az elektromos áram a töltéssel rendelkező részecskék rendezett áramlása. Az ika az elektromos áram létrehozásával, átalakításával, befolyásolásával, irányításával
Alapfogalmak lektronika Alapismeretek Az elektromos áram a töltéssel rendelkező részecskék rendezett áramlása. Az ika az elektromos áram létrehozásával, átalakításával, befolyásolásával, irányításával
Kémiai alapismeretek 3. hét
 Kémiai alapismeretek 3. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2013. szeptember 17.-20. 1/15 2013/2014 I. félév, Horváth Attila c : Molekulákon
Kémiai alapismeretek 3. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2013. szeptember 17.-20. 1/15 2013/2014 I. félév, Horváth Attila c : Molekulákon
Elektromos vezetés, mágneses ellenállás és Hall-effektus vizsgálata félvezetőkben
 Elektromos vezetés, mágneses ellenállás és Halleffektus vizsgálata félvezetőkben 1. A mérés célja a félvezetők néhány fontos vezetési tulajdonságának, és a mágneses tér által okozott néhány effektusnak
Elektromos vezetés, mágneses ellenállás és Halleffektus vizsgálata félvezetőkben 1. A mérés célja a félvezetők néhány fontos vezetési tulajdonságának, és a mágneses tér által okozott néhány effektusnak
Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola
 Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola 1047 Budapest, Langlet Valdemár utca 3-5. www.brody-bp.sulinet.hu e-mail: titkar@big.sulinet.hu Telefon: (1) 369 4917 OM: 034866 Osztályozóvizsga részletes
Újpesti Bródy Imre Gimnázium és Ál tal án os Isk ola 1047 Budapest, Langlet Valdemár utca 3-5. www.brody-bp.sulinet.hu e-mail: titkar@big.sulinet.hu Telefon: (1) 369 4917 OM: 034866 Osztályozóvizsga részletes
BME, Anyagtudomány és Technológia Tanszék. Trendek az anyagtudományban Vezetési jelenségek Dr. Mészáros István 2013.
 BME, nyagtudomány és Technológia Tanszék Trendek az anyagtudományban Vezetési jelenségek Dr. Mészáros István 03. Elektromos vezetési tulajdonságok Vezetési jelenségek (transzportfolyamatok) fenomenologikus
BME, nyagtudomány és Technológia Tanszék Trendek az anyagtudományban Vezetési jelenségek Dr. Mészáros István 03. Elektromos vezetési tulajdonságok Vezetési jelenségek (transzportfolyamatok) fenomenologikus
Zárthelyi dolgozat I. /A.
 Zárthelyi dolgozat I. /A. 1. Az FCC rács és reciprokrácsa (és tudjuk, hogy: V W.S. * V B.z. /() 3 = 1 / mindig!/) a 1 = ½ a (0,1,1) ; a = ½ a (1,0,1) ; a 3 = ½ a (1,1,0) b 1 = (/a) (-1,1,1); b = (/a) (1,-1,1);
Zárthelyi dolgozat I. /A. 1. Az FCC rács és reciprokrácsa (és tudjuk, hogy: V W.S. * V B.z. /() 3 = 1 / mindig!/) a 1 = ½ a (0,1,1) ; a = ½ a (1,0,1) ; a 3 = ½ a (1,1,0) b 1 = (/a) (-1,1,1); b = (/a) (1,-1,1);
Kémiai alapismeretek 2. hét
 Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Atomok, elektronok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 , elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
, elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
XI. előad. 2010. április 22. Definíci. Elektromos tulajdonságok: az anyagok elektromos tér hatására adott válasza
 Bevezetés s az anyagtudományba nyba XI. előad adás 2010. április 22. Definíci ciók Elektromos tulajdonságok: az anyagok elektromos tér hatására adott válasza Az anyag válasza lehet: töltésmozgás (vezetés)
Bevezetés s az anyagtudományba nyba XI. előad adás 2010. április 22. Definíci ciók Elektromos tulajdonságok: az anyagok elektromos tér hatására adott válasza Az anyag válasza lehet: töltésmozgás (vezetés)
Bevezetés a lézeres anyagmegmunkálásba
 Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
5. elıadás KRISTÁLYKÉMIAI ALAPOK
 5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
5. elıadás KRISTÁLYKÉMIAI ALAPOK KRISTÁLYKÉMIAI ALAPFOGALMAK Atomok: az anyag legkisebb olyan részei, amelyek még hordozzák a kémiai elem jellegzetességeit. Részei: atommag (mely protonokból és neutronokból
Bevezetés az analóg és digitális elektronikába. V. Félvezető diódák
 Bevezetés az analóg és digitális elektronikába V. Félvezető diódák Félvezető dióda Félvezetőknek nevezzük azokat az anyagokat, amelyek fajlagos ellenállása a vezetők és a szigetelők közé esik. (Si, Ge)
Bevezetés az analóg és digitális elektronikába V. Félvezető diódák Félvezető dióda Félvezetőknek nevezzük azokat az anyagokat, amelyek fajlagos ellenállása a vezetők és a szigetelők közé esik. (Si, Ge)
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Vezetési jelenségek, vezetőanyagok. Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék:
 nyagtudomány 2014/15 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők fémek ötvözetek elektrolitok
nyagtudomány 2014/15 Vezetési jelenségek, vezetőanyagok Dr. Szabó Péter János szpj@eik.bme.hu Elektromos vezetési folyamatban töltést továbbító (elmozdulni képes) részecskék: Vezetők fémek ötvözetek elektrolitok
Mézerek és lézerek. Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19.
 és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
2. Érzékelési elvek, fizikai jelenségek. a. Termikus elvek
 2. Érzékelési elvek, fizikai jelenségek a. Termikus elvek Az érzékelés célja Open loop: A felhasználó informálására (mérés) Más felhasználó rendszer informálása Felügyelet Closed loop Visszacsatolás (folyamatszabályzás)
2. Érzékelési elvek, fizikai jelenségek a. Termikus elvek Az érzékelés célja Open loop: A felhasználó informálására (mérés) Más felhasználó rendszer informálása Felügyelet Closed loop Visszacsatolás (folyamatszabályzás)
Félvezetk vizsgálata
 Félvezetk vizsgálata jegyzkönyv Zsigmond Anna Fizika BSc III. Mérés vezetje: Böhönyei András Mérés dátuma: 010. március 4. Leadás dátuma: 010. március 17. Mérés célja A mérés célja a szilícium tulajdonságainak
Félvezetk vizsgálata jegyzkönyv Zsigmond Anna Fizika BSc III. Mérés vezetje: Böhönyei András Mérés dátuma: 010. március 4. Leadás dátuma: 010. március 17. Mérés célja A mérés célja a szilícium tulajdonságainak
Általános Kémia, BMEVESAA101
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Magfizika tesztek. 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem
 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
Anyagismeret 2016/17. Diffúzió. Dr. Mészáros István Diffúzió
 Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
A SZILÁRDTEST FOGALMA. Szilárdtest: makroszkópikus, szilárd, rendezett anyagdarab. molekula klaszter szilárdtest > σ λ : rel.
 A SZILÁRDTEST FOGALMA Szilárdtest: makroszkópikus, szilárd, rendezett anyagdarab. a) Méret: b) Szilárdság: molekula klaszter szilárdtest > ~ 100 Å ideálisan rugalmas test: λ = 1 E σ λ : rel. megnyúlás
A SZILÁRDTEST FOGALMA Szilárdtest: makroszkópikus, szilárd, rendezett anyagdarab. a) Méret: b) Szilárdság: molekula klaszter szilárdtest > ~ 100 Å ideálisan rugalmas test: λ = 1 E σ λ : rel. megnyúlás
A kémiai és az elektrokémiai potenciál
 Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Dr. Báder Imre A kémiai és az elektrokémiai potenciál Anyagi rendszerben a termodinamikai egyensúly akkor állhat be, ha a rendszerben a megfelelő termodinamikai függvénynek minimuma van, vagyis a megváltozása
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár. Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár,
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Stern Gerlach kísérlet. Készítette: Kiss Éva
 Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Diffúzió. Diffúzió sebessége: gáz > folyadék > szilárd (kötőerő)
 Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
-A homogén detektorok közül a gyakorlatban a Si és a Ge egykristályból készültek a legelterjedtebbek.
 Félvezető detektorok - A legfiatalabb detektor család; a 1960-as évek közepétől kezdték alkalmazni őket. - Működésük bizonyos értelemben hasonló a gáztöltésű detektorokéhoz, ezért szokták őket szilárd
Félvezető detektorok - A legfiatalabb detektor család; a 1960-as évek közepétől kezdték alkalmazni őket. - Működésük bizonyos értelemben hasonló a gáztöltésű detektorokéhoz, ezért szokták őket szilárd
Kémiai kötés: több atom reakcióba lépése során egy közös, stabil (telített) külső elektronhéj alakul ki.
 19. Kémiai kötések (Elsődleges és másodlagos kötések. Elektronegativitás, elektronaffinitás, ionizációs energia. Ionos, fémes és kovalens kötés. A kovalens kötések fajtái, működésük, osztályozásuk, hibridizáció.
19. Kémiai kötések (Elsődleges és másodlagos kötések. Elektronegativitás, elektronaffinitás, ionizációs energia. Ionos, fémes és kovalens kötés. A kovalens kötések fajtái, működésük, osztályozásuk, hibridizáció.
Az ionizáló sugárzások fajtái, forrásai
 Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Az atom felépítése Alapfogalmak
 Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
a Bohr-féle atommodell (1913) Niels Hendrik David Bohr ( )
 a Bohr-féle atommodell (1913) Niels Hendrik David Bohr (1885-1962) atomok gerjesztése és ionizációja elektronnal való bombázással (1913-1914) James Franck (1882-1964) Gustav Ludwig Hertz (1887-1975) Nobel-díj
a Bohr-féle atommodell (1913) Niels Hendrik David Bohr (1885-1962) atomok gerjesztése és ionizációja elektronnal való bombázással (1913-1914) James Franck (1882-1964) Gustav Ludwig Hertz (1887-1975) Nobel-díj
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Osztályozó vizsga anyagok. Fizika
 Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
