Az MM2 erőtérben használt vegyérték jellegű kölcsönhatások Az MM2 erőtérben használt nemkötő jellegű kölcsönhatások...
|
|
|
- Károly Lukács
- 9 évvel ezelőtt
- Látták:
Átírás
1 TARTALOMJEGYZÉK KIVO AT...3 ABSTRACT...4 AUSZUG BEVEZETÉS SZAKIRODALMI ÖSSZEFOGLALÓ ALKOXIKARBONIL-METIL-TRIKARBONIL-TRIFENILFOSZFÁN-KOBALT KOMPLEXEK JELLEGZETESSÉGEI Királis információk Autoszolvatáció, spektroszkópia NANOTECNOLÓGIA Molekuláris propellerek, kúpfogaskerekek MOLEKULAMECANIKA Kötő kölcsönhatások emkötő kölcsönhatások Az MM2 erőtér Az MM2 erőtérben használt vegyérték jellegű kölcsönhatások Az MM2 erőtérben használt nemkötő jellegű kölcsönhatások Molekulamechanikai erőterek paraméterezése Kvantumkémiai alapokon történő erőtérfejlesztés Empirikus erőterek fejlesztése KÍSÉRLETI MÓDSZEREK AZ MM2 ERŐTÉR BŐVÍTÉSE ÉS PARAMÉTEREZÉSE [KE45, KE46, KE47] Erőtér- és szoftverválasztás Paraméterkészlet bővítés Kísérleti szerkezeti információk gyűjtése Referencia-adatbázis összeállítása A kezdeti paraméterkészlet meghatározása Kiindulási paraméterkészlet meghatározása PARAMÉTEROPTIMALIZÁCIÓ Az erőtér tesztelése, ellenőrzése mért vs. számított hiba KONFORMÁCIÓANALÍZIS Egydimenziós/egyváltozós konformációanalízis Kétdimenziós konformációanalízisek
2 Etilészter származék (EtOC(O)C 2 Co(CO) 3 (PPh 3 )) kétdimenziós konformációanalízise [K60, K61] A fenilgyűrűk inverziója AZ [(ETILOXIKARBONIL)METIL]KOBALT TETRAKARBONIL KOMPLEX REAKCIÓJA TRIFENILFOSZFÁNNAL [KE63] A komplexek szintézise Reakcióút hipotézis A reakció számítása számításos kémiai módszerekkel A trifenilfoszfán ligandum támadása C komplex D komplex átalakulás Dekarbonileződés, D komplex E komplex átalakulás Cisz-alkil (F komplex) transz-alkil (A komplex) átalakulás A reakció lejátszódása A BENZILÉSZTER SZÁRMAZÉK (POC(O)C 2 CO(CO) 3 (PP 3 ), IX) KÉTDIMENZIÓS KONFORMÁCIÓ ANALÍZISE [KE73, KE74] A FOGASKERÉK MODELL KITEKI TÉS ÖSSZEFOGLALÁS ÚJ TUDOMÁ YOS EREDMÉ YEK ÖSSZEFOGLALÁSA MAJOR RESULTS KÖSZÖ ET YILVÁ ÍTÁS IVATKOZÁSOK
3 KIVO AT KIRÁLIS I FORMÁCIÓK TERJEDÉSI MECA IZMUSA ALKIL-KOBALT- TRIKARBO IL-FOSZFÁ KOMPLEXEKBE KURDI RÓBERT A dolgozat az alkoxikarbonil-metil-trikarbonil-kobalt-tercierfoszfán komplexek sajátos önszerveződése révén keletkező, trigonális-bipiramidális szerkezetű molekulák speciális tulajdonságainak vizsgálatával foglalkozik. A vizsgált komplexekben, a koordinációs kölcsönhatások révén, több sztereogén részegység található, amelyek gátolt rotációk révén atropizomerként, konformerként, konfigurációként viselkednek. Ennek következtében a szintézis során abszolút diasztereoszelektivitás, sőt enantioszelektivitás is érvényesül. A szerző a királis információk terjedését vizsgálja fenti komplexekben a számításos kémia eszközeivel. Egy szerkezeti adatbázis felhasználásával empirikus molekulamechanikai erőteret készített, amellyel a vizsgált molekulaszerkezetek nagy pontossággal reprodukálhatók. Adatokat gyűjtött az enantiomerek közti átalakulás során lejátszódó intermolekuláris mozgásokra, ezek csatolt jellegére, energetikai színezetére és az indukciós mechanizmusok működésére. Ezen eredmények felhasználásával modellezte és igazolta az enantiomerpárok egymásba történő átalakulása során lejátszódó clockwork mechanizmust és bővítette ezt a tercierfoszfán ligandum inverziójának 2:1 típusú mechanizmusával. Felismerte, hogy a vizsgált vegyületek egy jól elkülönített része a közönséges fogaskerék áttétel kapcsolt rotációjának mechanizmusát követve invertálódhat. A sztereoszelektivitás eredetét sikeresen bizonyította a komplexek kialakulásainak vizsgálatával. Ezáltal segítve a preparatív munkát végző kutatókat az eddig még nem izolált termékek geometriai és energiai adataival. A dolgozat eredményeinek hatására bővültek az interdiszciplináris kutatási kapcsolatok. Pozitív eredményeik közé tartozik még a szponzori támogatás megjelenése is. 3
4 ABSTRACT SPREAD MECA ISM OF CIRAL I FORMATIO S I ALKYLCOBALT TRICARBO YL POSPI E COMPLEXES RÓBERT KURDI This study focuses on the investigation of special properties of alkylcobalt tricarbonyl phosphine molecules. In the complexes absolute diastereoselectivity, moreover enantioselectivity was obtained during the synthesis. The author studies the spread of chiral informations in the complexes mentioned by means of calculating chemistry. Using a structural database, an empirical molecular mechanical force field was created by which the molecule structures examined can be reproduced precisely. Clockwork- and gear-transmission mechanisms, taken place during the transformation of enantiomers into each other, were modelled and confirmed. The origin of stereoselectivity was proved successfully by investigating the formation of complexes. This could contribute to the work of preparative researchers with geometric and energetic data of compounds not isolated so far. 4
5 AUSZUG AUSBREITMECA ISMUS DER KIRALE I FORMATIO E I DE ALKYL- KOBALT-TRIKARBO YL-POSPA E KOMPLEXE RÓBERT KURDI Die Dissertation beschäftigt sich mit dem Untersuchen der speziellen Eigenschaften der Alkyl-Kobalt-Phosphane Molekülen. Absolute Diastereoselektivität und sogar Enantioselektivität geht in den geprüften Komplexen während der Synthese durch. Der Autor prüft mit den Methoden der rechnerischen Chemie den Ausbreiten der kiralen Informationen in den oben genannten Komplexen. Er schaffte mit der Anwendung einer strukturellen Datenbank ein empirisches molekularmechanisches Feld, mit dem die geprüften Molekularstrukturen mit grossen Präzision reproduziert werden können. Er modellte und bestätigte den während der Ineinander-Konvertierung der Enantiomerpaaren abrollenden sogenannten Uhrwerk-Zahnrad Mechanismus. Er bewiese erfolgreich den Ursprung der Stereoselektivität mit dem Untersuchen der erausbildung der Komplexen. Er hilft mit den geometrischen und energetischen Daten der bis jetzt noch nicht isolierten Produkten der präparativen Arbeit der Forscher. 5
6 1 Bevezetés A kobalt-karbonil vegyületeket gyakran használják homogén katalizátorként a fémorganikus kémiában. Tanulmányozásuk igen hasznos, mind gyakorlati, mind elméleti kémiai szempontból től a nyolcvanas évekig zászlóshajója volt ez a Markó László nevével fémjelzett, a Pannon Egyetem (egykori Veszprémi Egyetem) Kémia Intézet, Szerves Kémia Intézeti Tanszék keretei között működő kémiai iskolának. Számos kiváló tudós szerzett nemzetközi elismerést az itt folyó kutatásokból (Markó L., Ungváry F., eil B, Sisak A., Pályi Gy. Váradi Gy., orváth I., Kovács I., Kollár L. stb.). Napjainkban már alig lehet összefüggést találni az említett tudósok mai kutatási tematikáival. Egy kivétel azért van; Professzor Pályi Gyula (University of Modena and Reggio Emilia, Olaszország) tanszékén még mindig, sőt, megint folyik az egykoron kobalt katalizált hidroformilezési mechanizmus intermedierének tekintett alkil- és acil-karbonilkomplexek újabb és újabb képviselőinek szintézise. Az eredeti cél már lassan elfelejtődik. A preparatív munka hajtóereje ma már e vegyültek tulajdonságaiból és azok interdiszciplináris aspektusaiból fakad. A szintetikus munka (Prof. C. Zucchi, University of Modena and Reggio Emilia, Olaszország) és a biológiai homokiralitás eredetével kapcsolatos elméleti kutatás (Prof. Pályi Gy.) a modenai csoportban, a röntgen szerkezetvizsgálat Essenben (Prof. R. Boese, University of Essen, Németország), a molekulák motorikus tulajdonságainak vizsgálata, pedig a Pannon Egyetem (Prof Bencze L, Kurdi R.) keretei között folyik. A kutatási vertikum középpontjában az alkoxikarbonil-metil-trikarbonil-kobalttercierfoszfán komplexek sajátos önszerveződése révén keletkező, trigonális-bipiramidális szerkezetek állnak. A koordinációs kölcsönhatások révén több sztereogén részegységet hoznak létre, amelyek gátolt rotációk révén atropizomerként, konformerként, konfigurációként viselkednek. Ennek következtében a szintézis során abszolút diasztereoszelektivitás, sőt enantioszelektívitás is érvényesül. Az enantiomerek interkonverziója is a szeteroszelektivitás megmaradásával jár, ami a folyamat során rendkívül effektív intramolekuláris információcserét feltételez. Kutatásaimat a Veszprémi Egyetem (ma Pannon Egyetem) Szerves Kémia Tanszékén, a Kémia Doktori Iskola Elméleti Kémia alprogram keretében, 1998 őszén kezdtem TDK hallgatóként. Akkor már készen állt, hazai és nemzetközi fórumokon is megmérettetett, a fent említett témakörökben összegyűlt kísérleti adatok és kémiai számítások szintézisét átfogó kompakt logikai rendszer, egy hipotézis, amelyet a helyi zsargonban klokkvörk (clockwork 6
7 - óramű) mechanizmusként emlegettek. Érdekes módon e hipotézis bírálata szinte kizárólag a csoporton belül született, miután a kémiai számításokkal nem lehetett értelmezni az intramolekuláris átalakulásokat, így szimulációjuk is sikertelen maradt. A vita hatalmi szóval végződött: a kísérleti tapasztalat az első, vissza az empíriához. Lévén a legkisebb, és még egyik fronton sem elkötelezett, ez a feladat természetesen nekem jutott. Szerencsémre. Dolgozatomban a királis információk molekulán belüli terjedésével foglalkozom. Az adatgyűjtés elsősorban a szerkezetekre vonatkozott, de sok más egyéb között többlet információforrássá vált egy- egy rendezettlen Röntgen-spektrum és a szintetikus receptúrák olyan fizikai paraméterei is, mint a reakcióidő vagy a reakcióhőmérséklet. Munkámat főként a számításos kémia eszközeivel végeztem. Az adatbázis felhasználásával elkészítettem egy, a molekulaszerkezetek nagy pontosságú reprodukálását szolgáló empirikus molekulamechanikai erőteret. A realitáshoz közeli energiaértékeket kvantumkémiai módszerekkel számítottam. Adatokat gyűjtöttem az enantiomerek közti átalakulás során lejátszódó intermolekuláris mozgásokra, ezek csatolt jellegére, energetikai színezetére, a szintézis során észlelt királis jelenségek eredetére, (tandem jellegű) indukciós mechanizmusok működésére. Kutatási eredményeim felhasználásával modelleztem és igazoltam az enantiomerpárok interkonverziójának óraműszerű mechanizmusát és bővítettem ezt a tercierfoszfán-ligandum inverziójának 2:1 típusú mechanizmusával. Felismertem, hogy az ismert vegyületek egy jól elhatárolható része a közönséges fogaskerék-áttétel (gear) kapcsolt rotációjának mechanizmusát követve invertálódhat. Osztályozásuk a kristályfázisú konfigurációik révén clockwork (rep, sim) vagy gear (sip, rem) csoportba könnyen megoldható, de az alkoxilcsoport szerkezete alapján is jól megbecsülhető. A kétezredik év végén még bátortalanul, de egy konferencián már megjelent a kutatási eredményeink gyakorlati hasznosíthatóságának lehetősége. Az érdeklődés meglepően élénk volt, az eredmények is szaporák. Az örömkémia (belső és külső) kommunikációs kényszere ellentétébe fordult. Külföldi partnereinket is publikációs moratóriumra, de legalább is kontrollált kéziratok benyújtására kértük. Lassan meginduló publikációink java a fiókban várakozik, és csak e dolgozat révén juthat szűkrétű szakértői nyilvánossághoz. Pozitív eredmények közé tartozik a kutatás pragmatizmusa, a molekulatervezés és szelekció intenzitása, az interdiszciplináris kutatási kapcsolatok bővülése, és a szponzori támogatás megjelenése. A kutatási spektrum is bővült, elsősorban a molekulák kiroptikai tulajdonságainak számításával, tervezésével és vizsgálatával. A változások mértékét és minőségét jelképesen ez a kis példa is jelezheti: az etoxikarbonil-metil-trikarbonil-kobalttrifenilfoszin, (vizsgálataink kedvenc modellje) ez utóbbi témacsoportban a rotalicén-2e 7
8 nevet kapta. Munkámnak ezt a részét már nem tekintem a dolgozat részének, ezért erre csak egy rövid kitekintést nyújtok az olvasónak. 8
9 2 Szakirodalmi összefoglaló 2.1 Alkoxikarbonil-metil-trikarbonil-trifenilfoszfán-kobalt komplexek jellegzetességei A 80-as évek elejétől kezdve Pályi és munkatársai számos érdekes tulajdonságú komplexet állítottak elő (RO(O)CC2Co(CO)3PR'3 R, R' = alkil-, arilcsoport) [1]. Ezek a vegyületek közti termékként fontos szerepet játszanak számos homogén-katalitikus szintézis (oxószintézis, hidroformilezés, hidrogénezés) katalitikus ciklusában Királis információk Nagyszámú ilyen komplexet állítottak elő akirális és királis R és R' ligandumokat használva, amelyek közül 14-nek a kristály és molekula szerkezetét is meghatározták [2]. Érdekes tulajdonságokra figyeltek fel a vegyületek analitikai elemzése (IR, CD, röntgen diffrakció) során [3]. Akirális komplexek reakcióiban királis szerkezetek, konformációk alakultak ki (1. táblázat), amelyek a következő tulajdonságokkal rendelkeznek (a-j): 1. táblázat: Alkoxi-karbonil-metil-trikarbonil-tercierfoszfán-kobalt komplexek (ROC(O)C 2 Co(CO) 3 PR' 3 ) kristályaikban kialakuló királis konformációk [4] R R' Tércsoport rep sip rem sim I Me PPh 3 P II Et PPh 3 P2 1 /n 3 4 III n-pr PPh 3 P2 1 /n 5 6 IV i-pr PPh 3 P V s-bu PPh 3 P2 1 /n 9 10 VI t-bu PPh 3 P2 1 /c VII c-ex PPh 3 P2 1 /c VIII c-ex PPh 3 P IX C2Ph h PPh 3 g P-1 17(?) 18(?) 17(?) 18(?) X (S)-Lact a PPh 3 P XI D-Menth b PPh 3 P XII L-Menth c PPh 3 P XIII i-pr PPh 2 (n-menth) P XIV Gluc e PPh 3 g P (?) XV (Bis-Me) f PPh 3 P2 1 /n a (S)-{α-[EtOC(O)]C(C 3 )}; b (1S,2R,5S)-mentil; c (1R,2S,5R)-mentil; d (1S,2S,5R)-mentil; e 1,2:5,6-di-O-izopropilidén-α-D-glükofuranóz; f 1,2-bis(metoxikarbonil)etil-kobalt (Ungváry féle komplex); g A foszfán kiralitása nem határozható meg egyértelműen a fenilgyűrűk rendezetlensége miatt 9
10 (a) A vizsgált komplexek jellegzetesen torzított trigonális bipirimidális szerkezetében az ekvatoriális síkban három CO ligandum, a két átellenes axiális pozícióban pedig egy trifenilfoszfán 1 és egy alkoxi-karbonil-metilén ligandum helyezkedik el (1. ábra). triphenylphosphane ligandcarbonylcobalt fragment Észter rész Trikarbonil rész Trifenilfoszfin ligandum 1. ábra: A komplex szerkezeti egységei az R=Et példáján (II) keresztül (b) A kristályokban egymással fedésbe nem hozható, tükörképi viszonyban lévő molekulák vannak, melyek az axiális ligandumokon legalább egy-egy sztereogén egységgel rendelkeznek. (c) A kiralitás forrása az észtercsoportnak a kobalthoz viszonyított térállása (re vagy si) és a trifenilfoszfán csavarodottsága (P vagy M), helicitása (2. ábra). Az észtercsoport királis konformációinak meghatározásakor [4] használt elnevezések a CIP konvencióra épülnek. Ehhez azonban elengedhetetlenül szükség volt egy olyan kötés feltételezésére, mely a kobaltatom és az észtercsoport sp 2 -es szénatomja között alakul ki. Így az sp 2 -es szénatom királis atommá válik, ezáltal az egyes konfigurációk, (R) re vagy (S) si könnyen meghatározhatók. 1 A XIII komplex kivételével. 10
11 O O R R O O C C 2 C C 2 Co re si Co P P P M 2. ábra: A királis konformációk jelölésrendszere az alkil és a foszfán ligandumon (d) Az észtercsoport síkja és a Co(CO) 3 tárcsa síkja közel párhuzamos helyzetű. A Co-Csp 2 kötés körüli elforgatással létrehozható egyéb orientációk nem kedvezményezettek. (e) Az észtercsoport Csp 2 atomjának a kobalthoz viszonyított távolsága <3 Å, ami a van der Waals erőket meghaladó mértékű kölcsönhatást "autoszolvatációt" feltételez [5]. Ezáltal mind a kobalt atom, mind pedig a karboxilcsoport Csp 2 atomja királissá válik. (f) Minden komplex esetében hiányzik a statisztikusan lehetséges izomereknek legalább az 50% -a, de a si/re és a P/M konformációk kombinációja molekulánként változó lehet. (g) Királis R esetén még nagyobb a szelektivitás mértéke, több a lehetséges izomer. Az s- butil-észter (V) származék esetében az alkilcsoporton egy további aszimmetriacentrum is található, amely centrális kiralitását tekintve R és S lehet. Statisztikailag 2 3, tehát 8 szerkezet lehetséges, ezzel szemben a kristályszerkezetben csak kettő található meg (reps, simr) [2, 6]. A tejsav (X) és glükofuranóz (XIV) származékok esetében még nagyobb a szelektivitás. A lehetséges 8 szerkezetből csupán egyetlen módosulat (sims az X-es illetve sipd a XIV-es komplexnél) képződik. 11
12 (h) Királis R esetén (R=i-Pr és R =PPh 2 (n-menth), XIII) szintén csak egy királis konformáció alakul ki (3. ábra). 3. ábra: R=i-Pr, R =PPh 2 (n-menth) (XIII) származék szerkezete (i) A ciklohexil-észter (VII, VIII) származék esetében két különböző polimorf kristálymódosulat (P-1 és P21/c) alakul ki. (j) A kristálycellák felépítése jelentős számú intra- és intermolekuláris hidrogénkötés kialakulására enged következtetni. A Pannon Egyetem Müller Laboratóriumában Tóth Gergely erre irányulóan előrehaladott munkákat végez [7]. A kobalt katalizált homogénkatalitikus reakciók az egyik legrégebben vizsgált reakciók közé tartoznak [8]. Számtalan új vegyületet szintetizáltak, azonban Pályi és munkatársai által előállítottakhoz hasonló, csak egyetlen egy található még az irodalomban. Kobalt-katalizált hidroformilezési reakciók mechanizmusának vizsgálata közben Ungváry Ferenc egy újabb alkoxi-karbonil-metil-tercierfoszfán-kobalt származék szerkezetét írta le (4. ábra) (R=(Bis-Met), XV) [9]. Ez a komplex is tökéletesen beleillik a vizsgált vegyületeink sorába, hiszen az összefoglalt (a)-(d) jellegzetességeknek megfelel. 12
13 4. ábra: Az R =(Bis-Met) komplex (XV) szerkezete A vizsgált komplexek legmeglepőbb tulajdonsága az, hogy a trifenilfoszfán ligandum egy bizonyos konformációjához (P vagy M) az észter csoportnak mindig csak egy adott konformációja (re vagy si) tartozhat. Ez alól kivétel a benzil-észter származék (IX), amelyben a kristályszerkezet rendezetlensége kiterjed a benziloxikarbonil-csoportra, ezáltal lehetővé téve mind a 4 lehetséges szerkezet megjelenését Autoszolvatáció, spektroszkópia Kiroptikai vizsgálatok során felfigyeltek arra, hogy az RO(O)CC 2 Co(CO) 3 PR' 3 (R, R' = alkil, aril) vegyületek királis R és/vagy R' csoportokkal olyan cirkuláris dikroizmus (CD) színképeket adnak [10]; (a) amelyek gyökeresen különböznek a szabad ligandumok CD színképeitől; (b) amelyekben olyan CD-sávok jelentkeznek, melyek a komplexekben jelenlévő átmenetifém valamely átmenetének részvételével magyarázhatók. Ezek a megfigyelések azt jelentik, hogy a CD színképekben nem csak a klasszikus vegyérték kapcsolatok elektronátmeneteit találták, hanem egy ezeken túlmenő kölcsönhatást is, amely a fémet királisan perturbálja. Ekkor a vegyületcsoportból csak a PhC 2 OC(O)C 2 Co(CO) 3 PPh 3 (benzil származék) molekulaszerkezete állt rendelkezésükre. A komplexben az észtercsoportban található C(sp 2 ) 13
14 és a kobalt távolsága 292 pm, amely némileg alátámasztja a vegyérték kapcsolatokon túli kölcsönhatás, (Pályi professzor terminológiája szerint) az autoszolvatáció jelenlétét is. A feltételezett kötést a Müller Laboratórium munkatársainak sikerült kvantumkémiai vizsgálatokkal is bizonyítani [11]. A röntgenszerkezetek elemzése, spektroszkópiai eredmények, és a DFT számítások egybehangzóan azt bizonyítják, hogy az α-észter csoport és a kobalt atom között egy η 3 -típusú parciális koordinatív kötés alakul ki, mely felelős a vegyületekben létrejövő sztereoszelektív önszerveződés és királis konfigurációk kialakulásáért. Bencze és munkatársai már a 2000-ben leírták [12] a röntgen szerkezetekben talált enantiomerek egymás közötti átalakulásának, általuk lehetséges útját. Munkájukban tüzetesebben az etoxi származékot (II) vizsgálták. Meghatározták, hogy az észter csoport sp 3 - as és az sp 2 -es szén körüli átfordulása energetikailag sokkal kedvezőbb akkor, ha az a karbonilos oxigén atomjával fordul a CO tárcsa felé. Az átfordulás további mozgásokat gerjeszthet a molekulában. Amikor az észtercsoport re állásból jobbra fordul, eltaszítja a Co(CO) 3 fragmenst, ami ezáltal az óramutató járásával megegyező irányba fordul el. A CO tárcsa viszont olyan közel található a PPh 3 ligandum orto hidrogénjeihez, hogy ezeket P állásból M állásba sodorja át (5. ábra). Tehát az eredeti rep szerkezetből kialakul enantiomerje, a sim szerkezet. A molekulán belüli mozgások összehangoltságából ( koncertikus jellegéből) következtettek arra, hogy miért hiányzik a másik két kombináció. Felfigyeltek továbbá arra is, hogy ez a molekulán belüli összehangolt mozgás nagyon hasonlít a klasszikus óraszerkezetek működéséhez, sőt ezzel lényegében azonos [13]. Eszerint az óraszerkezet és a molekula, hasonló tulajdonságú részekkel rendelkezik. Az észtercsoport az anker+ankerkerék, a CO tárcsa a potenciális energia változó irányú továbbítására szolgáló anker, míg a trifenilfoszfán ligandum az ún. billegő kerékkel rokonítható (6. ábra). Kvantumkémiai számolásokkal bizonyították, hogy az egyensúlyi szerkezeteknél mind a négy variáns (rep, sip, rem és sim) energiája a számítások hibahatárán belül azonosnak adódott [14]. Ezzel azt feltételezték, hogy a szelektivitás oka nem pusztán a termodinamikai. Az irodalomban számos érdekes elképzelést találhatunk molekuláris óraműszerű vegyületek előállítására [15]. Azonban a fentiekben ismertetett óramű (clockwork) modell az eddigi legteljesebb szerkezet, melyben a klasszikus, mechanikus óraszerkezet valamennyi 14
15 15 lényeges alkatrésze megvan. A kutatás, a jelenség jellege folytán természetszerűen a hasonló molekuláris szerkezetek kutatására és fejlesztésére hivatott új tudományág, a nanotechnológia területére sodródott. Co P O O O O O P Co O O O O O re,p si,m 5. ábra: Az EtOC(O)C 2 Co(CO) 3 (PPh 3 ) átalakulásának sémája 6. ábra: Az óraszerkezet és a molekuláris óramodell összehasonlítása
16 2.2 anotechnológia 1959-ben Richard P. Feynman azt mondta, hogy egy napon a tudomány segítségével képesek leszünk egy enciklopédia tartalmát egyetlen tűhegyre felírni. Ez a módszer a gyakorlatban már évmilliárdok óta jól működik. A természet már ennyi ideje használja a nanotechnológiát. a nem is atomokból, de néhány atomos molekulákból épülnek fel az élethez szükséges anyagok. Ezek a folyamatok már ismertek voltak, de csak elképzelni tudták őket. Ahhoz, hogy Feynman tervét megvalósítsák olyan eszközre volt szükség, amivel a molekulákat, atomokat láthatják. Gerd Karl Binnig az IBM gyárral közösen 1981-re elkészítette a pásztázó alagút(áram)mikroszkópot (Scanning Tunneling Microscope, STM). Ezért a felfedezésért 1985-ben megkapta a fizikai Nobel díjat. Kiderült, hogy nem csak az egyes atomokat, hanem a köztük lévő kötéseket is látják, sőt az atomokat is tudják vele mozgatni. Ekkor született meg a modernkori nanotechnológia. A nanotechnológia lehetőségei határtalanok. Alkalmazási területei lehetnek például az orvostudomány (mesterséges izmok), számítástechnika (memóriák), elektronika (chipek), űrtechnológia (könnyű és stabil anyagok), nanomotorok (molekulákból felépülő kerekek, fogaskerekek, pumpák, jeltároló, jelátalakító eszközök), stb. Nem célom a nanotechnológia összes ágának bemutatása, csak a dolgozatom témájához legközelebb álló ún. nanomotorokkal foglalkozom itt. A nanomotorok felhasználási köre sokrétű lehet az optikai kapcsolóktól egészen a mikrofolyadékokig Molekuláris propellerek, kúpfogaskerekek Mislow és Gust [16, 17] olyan molekuláris propellereket állítottak elő, amelyekben kettő vagy több aril csoport (Ar) kapcsolódik egy egyszerű centrumhoz (Z). Az egyik arilcsoport C-Z kötés menti forgatására a molekulában a többi csoport (Ar n Z) is mozog (7. ábra). 16
17 z z 7. ábra: Ar 3 Z típusú molekuláris propellerek Mislow [18] és Iwamura [19] érdekes tulajdonságokat figyeltek meg Tp 2 Z (8. ábra) rendszerekben, ahol a két tripticén (Tp) oxigén vagy metilén hídon keresztül kapcsolódik egymáshoz (Z=O, C 2 ). Meglepődve tapasztalták, hogy egy gyors belső forgás következtében a molekula úgy viselkedik, mint egy ideális kúpfogaskerék. 1 - és 13 C-NMR vizsgálatokkal kimutatták, hogy a C-O kötés körüli forgás a bis(1-triptycycl) éterben -94 Con is kimutatható, és a rotációs gát nagysága nem nagyobb, mint 8 kcal/mól. Oxigén híd esetében (Tp 2 O), ha a tripticén 4-es pozícióiba egy klór atomot, vagy a Tp 2 C 2 -nél a 3-as és a 4-es pozíciókba egy-egy metil csoportot tettek, akkor megakadályozták a fogaskerekek elcsúszását egymáson, tehát egy igazi háromfogú fogaskerék-rendszert kaptak. 8. ábra: A molekuláris és a mechanikus kúpfogaskerék sémája Mislow és munkatársai későbbi kutatatásaikban [20] három tripticil csoportot kapcsoltak hozzá egy GeCl molekulához. Olyan három fogaskerékből álló rendszert kaptak, ahol két Tp csoport egyirányba a harmadik, pedig ellentétes irányba forog (9. ábra). 17
18 9. ábra: árom tripticénből álló fogaskerék rendszer Fuji [21] és munkatársai olyan kísérleteket hajtottak végre, amelyben a Tp helyett szubsztituált naftil csoportokat használtak. Ezáltal elsőként állítottak elő optikailag aktív kétfogú fogaskerekeket (10. ábra). 10. ábra: Kétfogú fogaskerék-rendszer Az analóg molekula rendszerekben, a nagy amplitúdójú mozgásokat külső stimulációval (fotokémiai, kémiai, elektrokémiai stb.) érik el. Ezáltal a csoportok egyes részei valóban átrendeződnek és ezt a reverzibilis átrendeződést számos módon tudják kimutatni (abszorpció, NMR, elektrokémiai potenciál stb.) [22]. Richards és munkatársai [23] [(9-tripticil-etinil)ciklopentadienil](tetrafenilciklobutadién)-kobalt komplexet (11. ábra) állítottak elő. A molekulában a ciklobutadiénhez kapcsolódó fenilgyűrűk egy négyfogú, az etin csoporthoz kapcsolódó tripticén pedig egy háromfogú fogaskereket hozott létre. Azonban a két forgó csoport kapcsolt rotációját nem tudták megoldani. 18
19 11. ábra: Metallocén típusú molekuláris fogaskerék Az eddig ismertetett vegyületek sok tekintettben hasonlítanak az általunk vizsgált alkilkobalt-trikarbonil-foszfán komplexre. 2.3 Molekulamechanika Az informatika fejlődésével a számításos kémia lehetőségei kitárultak. Sokféle módszert alkalmazhatunk a molekulaszintű motorok, masinák tulajdonságainak feltérképezéséhez. Az általunk vizsgált molekulacsalád legkisebb tagja is több mint 50 atomból áll. Ilyen nagy molekulákra, a konformációs viszonyok számolásához ezért célszerű volt a molekulamechanika eszközeit választani. A molekulamechanika témakörében számos érdekes és értékes könyv [24], valamint cikk jelent már meg. Nem célom ezen írások részletes összefoglalása - egy pontos, részletes munka meg is haladná a dolgozat kereteit, inkább kiemelném a munkám számára fontos részeket, részleteket és lehetőségeket. A molekulamechanika nem kvantumkémiai szerkezetvizsgáló módszer. A molekulamechanikai módszerek a magok helyzetét úgy vizsgálják, hogy az elektronokat csak az általuk létesített erőtér révén veszik figyelembe. Egy rendszer leírásának két fontos pillére van. Az egyik az erőteret leíró egyenletek matematikai alakja, a másik pedig az ezekben szereplő paraméterek megválasztása. Mindkét esetben a választás kritériuma az, hogy minél pontosabban tudjuk leírni a vizsgált modellek kísérletileg meghatározott jellemzőit. Az erőtér módszer alapötlete abból adódott, hogy a kísérleti módszerek fejlesztésével a kisméretű molekulákról egyre több adat állt rendelkezésre. Ismertek lettek az atomok közti kötéstávolságok, kötésszögek, valamint még számos molekulageometriai és energetikai 19
20 jellemző. A kérdés az volt, hogy leírható-e egy nagy molekula a kisebbekkel modellezett szerkezeti egységek kombinációjaként. Erre szolgál az erőtér eljáráson alapuló molekulamechanikai számítási módszer. Az erőtér eljárás alapjait Andrews 1930-ban közölt mechanikai modellje [25] képezi, amely szerint a molekulák merev, gömbszerű atomokból állnak. Az atomok közti kötéseket úgy szemléltetik, mintha rúgókkal kapcsolnánk őket össze. A molekulát felépítő atomok állandóan mozognak. A fellépő szerkezeti változások pedig, a molekula teljes energiájának a megváltozását vonják maguk után. Ezek az egyszerű erőtörvények alapján számíthatóak. A molekulamechanikában használatos erőterekben alkalmazott energiatagok kötő és nemkötő kölcsönhatások leírására szolgálnak, E összes = E + E. vegyérték nem kötő Vegyérték jellegű- vagy kötőkölcsönhatások közé többek közt az egymással közvetlen kötésben lévő atomok között fellépő kötésnyújtási, a geminális (1-3 vagy kötéshajlítási) és a vicinális (1-4 vagy torziós) kölcsönhatások tartoznak, E E + E + E vegyérték = nyújtási hajlítási torziós Az egymáshoz közel lévő atomok között tapasztalható taszítás, az egymástól távol lévő atomok között kialakuló diszperziós vonzás, valamit az elektrosztatikus effektusok a nemkötő kölcsönhatások közé tartoznak, E nem kötő EvdW + ECoulomb + = E. kötés Kötő kölcsönhatások Andrews molekulamechanikai modellje alapján a kovalens kötés irányában és az arra merőlegesen ébredő erőket a ooke-törvény segítségével számolhatjuk. Minden egyes kötéstávolságnak és kötésszögnek definiálhatunk egy egyensúlyi értéket (kötéstávolság: két egymással kötésben lévő atom távolságának leírására szolgál; kötésszög: a központi atomtól a szomszédos atomok felé húzott szakaszok (=kötések) által bezárt szög leírására szolgál). a 20
21 egy kötéstávolság vagy egy kötésszög eltér annak egyensúlyi értékétől, akkor ez energianövekedést eredményez. Ezt, a kötéstávolságnál az E r 1 k 2 r ( r r ) 2 =, 0 kötésszögeknél pedig az E θ 1 = k 2 θ ( θ θ ) 2 0 egyenlettel írhatjuk le. Ahol r 0 és θ 0 az egyensúlyi, r és θ a számított kötéstávolság, ill. kötésszög értékek. Nagy deformációk esetén alkalmazható lenne a Morse-függvény [26], de ezt a nagy időszükséglete miatt nem alkalmazzák. A számítás pontosítására mind a kötésnyújtási, mind a kötéshajlítási tagot kiegészíthetjük egy harmadrendű taggal. Ez azonban veszélyekkel járhat olyan molekulák esetében, ahol a geometriai jellemzők (kötéstávolság, kötésszög, stb.) jelentősen eltérnek az egyensúlyi értékektől. a egy molekula részei a kötések kölcsönös taszítása miatt egymáshoz képest nem fordulhatnak el szabadon, akkor torziós gátról beszélünk. Kezdetben ennek a leírására a van der Waals paramétereket használták, de ez megnehezítette a van der Waals kölcsönhatások leírását. Ezért vezették be a torziós gátra jellemző energiatagot, a torziós energiát [27]. Első lépésben definiálni kellett egy függő változót. Ez a torziós szög. Az A,B,C,D atomok által meghatározott torziós szög az AB és CD egyenesek által bezárt szög a BC tengelyen keresztül nézve (12. ábra) [28]. 12. ábra: A torziós szög definíciója 21
22 Mivel a torziós energiagátat leíró görbe a torziós szög koszinuszával arányos, ezért a molekulamechanikában az E ω = k ω ( 1 3cosω) egyszerű képlettel írják le az energiát. Bonyolultabb rendszereknél, szerkezeteknél ez az egyenlet csak részben alkalmas. Részletesebben az alábbi Fourier-sorral felírva az E ω = j 1 E j j 2 ( 1 cos( ω) ) egyenletet kapjuk. a az első három tagra kifejtjük, akkor megkapjuk a molekulamechanikában használt egyenletet: E E E2 3 = ( 1+ cosω) + ( 1 cos2ω) + ( 1+ cos ω) E ω 3. Az egyes tagoknak szemléletes fizikai értelmet is lehet adni. Az első tag a dipólus-dipólus kölcsönhatásból származik. A második tag telített kötés körüli gátolt rotáció esetén hiperkonjugációra, telítetlen kötés esetén, pedig konjugációra utal. A harmadik tag a térbeli hatásoknak tulajdonítható. A molekula egyes részei, amelyekben sp2-es hibridállapotú atomok találhatóak, planáris elrendeződést mutatnak. a a trigonális centrumban elhelyezkedő atom a sík alatt vagy felett helyezkedik el, akkor ez energianövekedést eredményez a síkbéli szerkezethez képest. Ez a kihajlás szögével (χ) arányos és a következő egyenlettel írható le [29]: E χ = k χ χ. A χ koordináta definíciója az irodalomban nem egyértelmű, többféle leírás ismert. Egy gyakori definíció szerint, egy a centrumból kiinduló kötés körüli ún. hamis torzió segítségével írja le (13. ábra). 22
23 13. ábra: A síkból történő kihajlásra vonatkozó koordináták definíciója emkötő kölcsönhatások Molekulamechanika a molekulaszerkezet pontosabb energetikai jellemzésére a nyújtási-hajlítási taggal közelített 1,3 nemkötő kölcsönhatás mellett egyéb intramolekuláris kölcsönhatásokat is figyelembe vesz. Ezek közül a van der Waals kölcsönhatás [30] a legfontosabb. A van der Waals kölcsönhatás három részből tevődik össze, melyek a következők. Az első a dipólusnyomatékkal és töltéssel nem rendelkező molekulákra jellemző diszperziós kölcsönhatás. A második a dipólusnyomatékkal rendelkező atomok dipól-dipól kölcsönhatásának energiája, és végül az effektív töltések között fellépő Coulomb-erők energiája. A van der Waals-jellegű másodlagos kölcsönhatások egyidejű számítására több összefüggés is alkalmas. asználják az ún. ill-összefüggést [31], de a molekulamechanikai eljárásokban az általánosabb érvényű Lennard-Jones potenciált [32] alkalmazzák: ij ij EvdW = ij vdw Rij Rij A B Ennek oka az is, hogy a ill-összefüggésben található exponenciális kifejezés számítása jóval időigényesebb. A töltések között kialakuló nemkötő kölcsönhatások számolására az erőterek többségében a Coulomb-potenciált használják: E Coulomb = i, j Coulomb qiq DR j ij, 23
24 ahol q i és q j atomi töltések, R ij a köztük lévő távolság és D a dielektromos állandó. [33]: Az intra- vagy intermolekuláris -kötés leírására a következő egyenletet használják E kötés = i, j kötés C R D ij ij ij Rij Ezt a tagot nem minden molekulamechanikai erőtérbe építették be. Kvantumkémiai számításokkal bizonyították, hogy az ilyen másodlagos kötések leírhatóak egyszerű elektrosztatikus kölcsönhatásokkal is [34] Az MM2 erőtér Az előzőekben leírtak alapján elmondható, hogy egyes kölcsönhatások kiszámítására több módszer ismeretes. Szinte minden erőtér más és más formában használja ezeket az egyenleteket. A szervetlen vegyületekre végzett molekulamechanikai számítások a szimulációs eszközök fejlődésével a 80-as évek közepétől kerültek be a kutatói gyakorlatba. Az átmenetifém atomokat tartalmazó vegyületek molekulamechanikai kezelése két jól definiált csoportra osztható, a koordinációs- és a (számunkra fontosabb) fémorganikus vegyületek szimulációjára ben egy átfogó tanulmány [35] jelent meg fémorganikus komplexek molekulamechanikai kezeléséről. Több mint 250 hivatkozás segítségével tekintik át a 90-es évek elejétől megindult erőtérfejlesztéseket. Az első igazán jól alkalmazható módszer a PCMODEL [36] programkörnyezetében megvalósított MMX erőtér, amelyben az átmenetifém komplexek modellezése vegyérték jellegű kölcsönhatásokkal történik. A paraméterkészletet a vas atom különböző vegyületeire fejlesztették ki. Más fémek komplexeinek kezeléséhez szükséges paramétereket a fématomok van der Waals sugarainak különbsége alapján határozza meg. Nagy előnye, hogy a hiányzó paramétereket meg tudja becsülni. A becslés pontossága azonban kapcsolatban van a hiányzó paraméterek számával. Munkám során a Cerius 2 program MM2 [37] erőterét alkalmaztam. (Döntésemet a kísérleti részben indokolom.) Az MM2 erőteret Allinger és munkatársai fejlesztették ki. Ez volt az első általánosan is alkalmazható erőtér. Dolgozatomban az egyes energiatagok számítási módszereit ismertettem röviden. 24
25 Az MM2 erőtérben használt vegyérték jellegű kölcsönhatások Kötésnyújtási kölcsönhatás Ez az energia csak a két atom távolságától függ. Ennek számolására a program a köbös potenciál függvényt használja, E nyújtási 2 = / 2K ( R R ) [1+ d( R )], (E1) 1 b 0 R0 ahol R 0 a kötéstávolság (Å), K b az erőállandó ((kcal/mól)/å 2 ) és a d pedig a köbös korrekciós tag (1/Å). Szöghajlítási kölcsönhatás Az MM2 szög potenciált, vagy más néven Allinger potenciált használja a program ennek a kölcsönhatásnak a számítására. 2 4 E hajlítási = 1/ 2K ( θ θ ) [1+ d( θ ) ], (E2) θ 0 θ0 ahol θ 0 a bezárt szög (º), d hatos term (1/rad 4 ) és K θ az erőállandó. Torziós kölcsönhatás A torziós energia számítása a következő egyenlettel történik, E torziós = p n= 1 [ 1 d ( n )] 1/ 2K θ θ, n cos, (E3) ahol K θ,n a rotációs gát (kcal/mól), n a periodicitás (n=1,2,3,4,5,6) és d a fázis faktor (±1) Az MM2 erőtérben használt nemkötő jellegű kölcsönhatások Van der Waals kölcsönhatás Az MM2 erőtérben a van der Waals kölcsönhatás számítására egy módosított Lennard-Jones potenciált használnak, E vdw CR 6 ( R) = ( Ae BR ) = D 0 exp γ 6 6 R γ 1 R 0 6 γ R 0, (E4) γ 6 R 25
26 ahol a γ rendszerint 12, hogy a Lennard-Jones 12-6 potenciál esetében a nagy atomtávolságoknál fellépő hibákat kiküszöböljék [38]. R 0 a kötéserősség (kcal/mól), D 0 pedig a kötéstávolság (Å). Coulomb kölcsönhatás A teljes elektrosztatikus energiát a következő egyenlettel tudjuk leírni, E coulomb QiQ j = C0, (E5) εr i j> i ij ahol Q i és Q j az atomok töltése, R ij az atomok közti távolság (Å), ε a dielektromos állandó és C 0 a konverziós faktor (C 0 =332,0637) Molekulamechanikai erőterek paraméterezése Az erőterek paraméterezésén a bennük előforduló paraméterek beállítását értjük. Bár a molekulamechanikában használatos általános erőterekben a szerzők a lehető legszélesebb paraméterkészlet fejlesztésére törekednek, az alkalmazások sokszínűsége folytán egyes paraméterek hiányára hamar fény derül. Az ilyen esetekben gondoskodni kell a hiányzó paraméterek pótlásáról. A molekulamechanikai erőtér pontosságát, az erőteret alkotó potenciálegyenleteken túl, a kísérleti szerkezetek száma is biztosítja. A korábban végzett manuális elemzések alkalmazása már technikai problémákat vet fel, miszerint a sok paraméter és belső koordináta együttes kezelése már csak számítógépes célszoftverek segítségével oldható meg. A molekulamechanikai paraméterek fejlesztésére az irodalomban két fő irányt tartanak megfelelőnek. Az egyik módszer lényege az, hogy a paraméterezéshez csak kvantumkémiai számításokat használnak fel. A másik módszer, ezt használtuk mi is, csupán kísérleti eredményeket használ a fejlesztéshez Kvantumkémiai alapokon történő erőtérfejlesztés Ezen módszeren alapuló molekulamechanikai paraméterkészlet előállítására számos példa található az irodalomban [39]. A fejlesztések során volt, amikor még együtt alkalmazták a kísérleti és elméleti adatokat, de a sokak által ismert és használt Merk erőtér [40] már csak tisztán kvantumkémiai számításokon alapul. A szerzők a paraméteroptimalizációhoz közel 1500 F és MP2/6-31G* szinten optimalizált molekulaszerkezetet használtak fel. A 26
27 kvantumkémiai számításokon alapuló erőtérfejlesztés előnye, hogy a számításokkal lényegében minden olyan adat előállítható, ami a paraméteroptimalizációhoz kell. Azonban ahhoz, hogy egy pontos, használható paraméterkészletet elkészítsünk, rengeteg kvantumkémiai számításra van szükség. Ez, a számítástechnika rendkívüli mértékű fejlődésével is, csak egyedi, kis molekulacsoportok részére kidolgozott erőterek esetében lehetséges Empirikus erőterek fejlesztése A molekulamechanika, eredeti definícióját is alapul véve, szinte kizárólag kísérleti adatokat használ a paraméterezéshez. Ennek a módszernek a legfontosabb és a legidőigényesebb része a kísérleti adatok összegyűjtése és azok elemzése. Két olyan nagy kutatócsoportot ismerünk, akik tisztán kísérleti alapokon keresztül készítik el a molekulamechanikai paraméterek optimalizációját. Allinger és munkatársai a 1991-ben megjelent munkáikban elsősorban az MM2 és MM3 erőterek eltéréseit mutatják be, viszont magáról a paraméterezésről kevés szót szólnak. Kidolgoztak viszont egy olyan becslési módszert, amellyel a hiányzó paramétereket kvantitatív úton tudják pótolni [41]. Rasmussen és munkatársai a molekulamechanikai paramétereket a legkisebb négyzetek módszerével optimalizálták a Lewenberg-Marquardt algoritmus alkalmazásával [42]. Ezzel a módszerrel egyszerre lehet optimalizálni a belső koordinátákat, kondenzált fázis cellaparamétereit és rácsenergiáját, valamint a dipólus momentumokat. Ezzel egyidőben az Allinger-csoport egy új kvalitatív becslési módszert dolgozott ki, amellyel az új paramétereket lehet kiválasztani [43]. A közlemény nagy értéke, hogy tartalmazza az MM2 és MM3 erőterekben alkalmazható van der Waals paramétereket az egész periódusos rendszerre nézve. Így ezeket a paramétereket nem kell feltétlenül optimalizálni a későbbi erőtérfejlesztésekben. A tanulmányban részletesen elemzik, hogy a vegyérték jellegű kölcsönhatások paramétereit milyen kísérleti geometriákból lehet pontosabban megbecsülni. A legalkalmasabb a jó minőségű elektrondiffrakciós szerkezet, amennyiben ez nem áll rendelkezésre akkor használhatók a mikrohullámú és a röntgendiffrakciós szerkezetek is. Fémorganikus komplexeknél általában csak az utóbbiak ismertek. Mivel mi elsősorban kísérleti szerkezeteken alapuló molekulamechanikai erőteret kívánunk létrehozni, a röntgendiffrakciós szerkezeteket részesítjük előnyben. A szakirodalmat átvizsgálva megállapíthatjuk, hogy a gyakorlatban is használható, jól reprodukálható optimalizálási módszer - egyet kivéve - nincs publikálva. A Veszprémi 27
28 Egyetem (Pannon Egyetem) Müller Laboratóriumában Szilágyi Róbert dolgozott ki [44] egy olyan paraméterezési eljárást, amelyet már sikerrel alkalmaztak más molekulacsoportok paramétereinek előállítására is. A paraméterezési algoritmus előnye az, hogy kémiai és számítógépes környezettől független és nem tartalmaz a felhasználótól függő algoritmusparamétereket. A módszert a dolgozat kísérleti részében mutatom be a vizsgált vegyületcsalád példáján keresztül. 28
29 3 Kísérleti módszerek A kutatások, a bevezetésben említettek szerint, egy nemzetközi konzorcium keretében folynak. Ezen belül, a munkánk célja és jellege, a számítási kémia eszközrendszerével végzett molekulaszerkezet-vizsgálat, a molekuláris tulajdonságok számítása, modellezése és a molekulatervezés. Konkrétabban: a korábbi munkákban főleg DFT és PM3 számításokat végeztek el, Gaussian és Spartan programokkal. A kvantumkémiai számítások eszközrendszerét és alkalmazását változatlanuk megtartottuk. A molekulák mérete miatt azonban szükségünk volt egy gyorsabb számítási módszerre, amely eléri a műszeres vizsgálatok, pl. Röntgenspektroszkópia pontosságát. Ennek megfelelően egy host (gazda) szoftverből és egy új erőtérből felépített molekulamechanikai számítást vezettünk be, amelynek gyorsasága három nagyságrenddel haladja meg a korábban alkalmazott számítási módszerekét és geometriai pontossága is megfelel az eredményes munka követelményeinek. (A konformációanalízis alatt előállítottunk majdnem 15 ezer szerkezetet. Molekulamechanikai módszerrel 1 geometriai optimalizáció ~1 perc alatt lesz kész, kvantumkémiai módszerrel, a rendelkezésünkre álló számítókapacitás maximális kihasználásával is, ez az idő megközelítette az 1 napot.) Munkánk során többféle szoftvert és számítógépet használtunk. A molekulamechanikai paraméterezést egy INDY R4000-es munkaállomáson, Cerius 2 szoftverrel végeztük el. Az eredmények kiértékeléséhez Microsoft EXCEL makrót használtuk. A reakcióút számításához a Spartan 02 program Windows-ós változatát használtuk. 3.1 Az MM2 erőtér bővítése és paraméterezése [KE45, KE46, KE47] Erőtér- és szoftverválasztás Ahhoz, hogy molekulamechanikai módszerrel tudjuk vizsgálni az alkoxikarbonilmetil-trikarbonil-trifenilfoszfán-kobalt típusú komplexeket, olyan erőteret kellett választani, amelyik tartalmazza az összes szükséges paramétert. A rendelkezésünkre álló számítógépes modellező szoftverek közül (Spartan 5.0 [48], Cerius [49]) mindegyik tartalmaz MM erőtereket, de sajnos ezeknek az erőtereknek egyike sem tartalmazta az összes szükséges paramétert. Döntenünk kellett, hogy melyik szoftver, melyik erőterét bővítjük, paraméterezzük. 29
30 A szoftver választásánál két okból döntöttünk a Cerius 2 mellett. Az első ok az volt, hogy a Veszprémi Egyetemen Bencze és munkatársai már korábban végeztek ezzel a programmal paraméterezési munkákat. A második, hogy a programcsomagban az erőtér nyitott az energiafüggvények és paramétereik szabad változtatására, mint ezt már a neve is mutatja: Cerius 2 Open Force Field (C2-OFF). A Cerius 2 Anyagtudományi Szakértői rendszerben jelentős számú molekulamechanikai erőtér található, többek közt a Dreiding I és II [50], az Universal FF [51, 52], az AMBER [53] és az MM2, valamint számos kisebb paraméterkészlet a speciális munkákhoz ( például: bks [54] szilikát és alumino-foszfátok kvantumkémiai vizsgálata, msxx [55] halogénezett polimerek). Programkörnyezetében csak egyetlen erőtér képes az átmenetifém komplexek szerkezetét modellezni. Ez az Universal FF, amely a teljes periódusos rendszerre alkalmazható atomi paramétereket tartalmaz. A lefedett tartomány növelésével növekszik a számolási hiba is. Ebből is következik, hogy ezzel az erőtérrel nem lehet olyan pontosságot elérni, amilyet a kutatások megkívánnak. A Pannon Egyetem Müller Laboratóriumában korábban már bebizonyították [56], hogy az MMX második generációs erőtér [57] alkalmas átmenetifém komplexek szerkezetének leírására. Mivel a Cerius 2 programban megtalálható MM2 erőtér, ami az MMX erőtér alapja, ezért munkám során az MM2 erőteret használtam Paraméterkészlet bővítés A szakirodalom többféle paraméterezési eljárást említ. Az irodalmi összefoglalóban már többet bemutattam. Választásunk a már említett okokból - a Szilágyi Róbert által kidolgozott eljárásra esett. Az eljárás algoritmusát az 1.sémán mutatom be, majd az egyes lépéseket fejtem ki részletesebben. 30
31 START Kiindulási szerkezetoptimalizáció Kísérleti szerkezeti információk gyûjtése Referencia-adatbázis összeállítása Kezdeti paraméterkészlet meghatározása Kiindulási paraméterkészlet meghatározása Eltolási mûvelet Szerkezetoptimalizáció Erõállandókszerinti skálázás Illesztési hibák elemzése nem megfelelõ Atomtípusok ellenörzése megfelelõ Konvergencia nem igen STOP 1. séma: Paraméteroptimalizálás algoritmusa Kísérleti szerkezeti információk gyűjtése Molekulamechanikai számítások paramétereit szerkezeti adatokból származtatjuk. A megfelelő kísérleti adatbázis létrehozásához elegendő mennyiségű és minőségű szerkezeti információ kell. Összegyűjtésükhöz számos forrás és módszer áll rendelkezésünkre. Többek közt a rezgési-spektroszkópia (IR), mágneses magrezonancia (NMR), elektron- (ED) és röntgendiffrakciós (XD) eljárások. A munkánk során a kristályos, szerves és fémorganikus anyagok szerkezeti adatbázisát, a Cambridge Crystallographic Database-t (CSD) használtuk. A kristályos anyagok szerkezete így a fémorganikus komplexeké is röntgen diffrakciós technikával vizsgálható. A mérés a nem-hidrogén atomok pozícióját 0,1 Å pontossággal adja meg. Ez megegyezik a molekulamechanikai módszer általánosan elfogadott, maximálisan megengedett hibahatárával [58], ezért jól használható e molekulák paraméterezésekor. 31
32 Referencia-adatbázis összeállítása Mivel más szerkezeteket nem találtunk, azon komplexek szerkezeteit gyűjtöttük ki, amelyeket Pályi és munkatársai, valamint Ungváry és munkatársai állítottak elő (1. táblázat). Mivel a ciklohexil származék (VII, VIII) esetében megjelent a polimorfia, a kétféle tércsoport közül csak az egyiket (P2 1 /c) használtuk fel a paraméterezés során. A teljes adatbázis végül 25 alkoxi-karbonil-metil-kobalt-trikarbonil-tercier foszfán molekulaszerkezetre duzzadt (2. táblázat). 2. táblázat: A paraméterezéshez felhasznált röntgenszerkezetek (ROC(O)C 2 Co(CO) 3 PR' 3 ) R R' Me PPh 3 1, 2 Et PPh 3 3, 4 n-pr PPh 3 5, 6 i-pr PPh 3 7, 8 s-bu PPh 3 9, 10 t-bu PPh 3 11, 12 c-ex PPh 3 13, 14 C 2 Ph PPh 3 g 17, 18 (S)-Lact PPh 3 19 D-Menth PPh 3 20, 21 L-Menth PPh 3 22, 23 i-pr PPh 2 (n-menth) 24 Gluc PPh 3 25 (Bis-Me) PPh 3 26, 27 32
33 A kezdeti paraméterkészlet meghatározása A gazdaerőtérnek választott C2-MM2 molekulamechanikai paraméterkészlet nagy pontossággal képes leírni a fémorganikus komplexeket. Tesztszámításokat végeztünk annak a kiderítésére, hogy melyek azok a belső koordináták, amelyeket a fejlesztendő MM2-es paraméterkészlet nem tud kezelni. Az adatok elemzését statisztikai módszerrel végeztem el. A hiányzó paraméterek 1 kivételével (C_1 O karbonil kötéstávolság) az átmenetifém környezetét leíró belső koordinátákhoz kapcsolódnak (3. táblázat). 3. táblázat: A C2-MM2 paraméterkészletből hiányzó belső koordináták Kötéstávolságok Kötésszögek Torziósszögek Co_5 C_1 Co_5 C_3 Co_5 P_3 C_1 O karbonil C_1 Co_5 C_1 C_1 Co_5 C_3 C_1 Co_5 P_3 C_ar P_3 Co_5 C_2CO C_3 Co_5 C_3 Co_5 P_3 C_2CO C_3 Co_5 C_1 _C C_3 Co_5 C_1 C_1 Co_5 P_3 C_ar O_3 C_2CO C_3 Co_5 O_2 C_2CO C_3 Co_5 C_ar C_ar P_3 Co_5 Co_5 C_1 O karbonil Co_5 C_3 _C C_3 C_3 Co_5 C_3 P_3 Co_5 Kötéstávolságok A kapott értékek statisztikai elemzéséből kiderül, hogy az egyes kötéstávolságokhoz tartozó értékek megközelítően azonosak, a szórás nagyon kicsi (4. táblázat). 33
34 4. táblázat: A paraméterkészletből hiányzó kötéstávolságok statisztikai elemzése Kötéstávolságok (Å) C_1 - Co C_1 - O karbonil C_3 - Co_5 Co_5 - P_3 Átlag 1,784 1,139 2,086 2,217 Eltérés 0,006 0,005 0,008 0,006 Szórás 0,008 0,007 0,011 0,009 Minimum 1,771 1,130 2,065 2,205 Maximum 1,803 1,156 2,116 2,239 Darabszám Kötésszögek A molekulák szerkezeti tulajdonságaiból következik, hogy a C(sp 3 ) - C(sp 3 ) Co és a C(sp 3 ) P Co szög nem mindegyik molekulában szerepel (5. táblázat). Az előbbi a (XV, R=1,2-bis(metoxikarbonil)etil-kobalt; 4. ábra) komplexben, az utóbbi, pedig abban, amelyikben az egyik fenilgyűrű helyén mentil csoport található (XIII, R =PPh 2 Menth; 3. ábra). 5. táblázat: A kobalt környezetében található kötésszögek statisztikai elemzése Kötésszögek (º) C_1 C_1 C_1 C_ar C_2CO C_3 Co_5 Co_5 C_3 C_3 Co_5 Co_5 Co_5 P_3 C_3 Co_5 C_1 C_3 C_3 P_3 C_1 C_3 P_3 Co_5 Co_5 P_3 O karb. _C Co_5 Co_5 Átlag 119,82 87,59 92,44 114,39 110,29 176,84 177,62 109,34 114,09 112,84 Eltérés 0,04 0,28 0,28 0,36 1,63 1,10 0,74 0,27 0,00 Szórás 0,05 0,36 0,36 0,46 2,02 1,32 0,98 0,39 0,00 Min. 119,69 86,83 91,75 112,95 106,04 174,82 175,15 108,58 114,09 Max. 119,91 88,27 93,20 114,99 113,46 179,16 178,59 110,10 114,09 Darab
35 Torziósszögek A torziós szögek a legkisebb energia-befektetéssel változtatható belső koordináták, amelyeknél a kísérleti és a számított értékek közötti tökéletes egyezést szinte lehetetlen elérni. A torziós kölcsönhatások lépésenkénti elemzése feleslegesen terheli az optimalizációt, ezért csak az illesztési hiba jelentős növekedésekor kell ezeket korrigálni. A torziós paraméterek megadásánál fontos szempont a periodicitás meghatározása. (Periodicitás: A 360 -os forgatás alatt felvett maximumok száma, ismétlődése) A röntgen szerkezeti adatokból kigyűjtöttük a számunkra fontos torziókra vonatkozó értékeket és a gyakoriságokból következtettünk a periodicitásra. Mivel az összes torzió részletes elemzésének bemutatása túlságosan megnövelné a dolgozat méreteit, ezért itt csak a Co-P-C(ar)-C(ar) torziós szögek elemzését mutatom be. A meghatározást úgy végeztük, hogy a röntgenszerkezetekben megmértük az összes említett torziós szöget. Mivel a fenilgyűrűk aromás szén atomjai nincsenek megkülönböztetve egymástól, ezért gyűrűnként kettő, molekulánként pedig hat torziósszög értéket kaptunk. Ezeket az értékeket ábrázoltuk gyakoriság szerint (1. diagram). A diagramon négy gyakoriság maximum látható, -130º, -40º, +50º és -140º környékén. Ez nem meglepő, hiszen ez a komplexek tulajdonságaiból egyértelműen következik. A négy maximum értékből tehát négyes periodicitásra következtettünk. isztogram Gyakoriság Gyakoriság Rekesz 1. diagram: A Co P-C(ar)-C(ar) torziósszög értékeinek gyakorisága 35
Cikloalkánok és származékaik konformációja
 1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
1 ikloalkánok és származékaik konformációja telített gyűrűs szénhidrogének legegyszerűbb képviselője a ciklopropán. Gyűrűje szabályos háromszög alakú, ennek megfelelően szénatomjai egy síkban helyezkednek
KIRÁLIS I FORMÁCIÓK TERJEDÉSI MECHA IZMUSA ALKIL-KOBALT-TRIKARBO IL- FOSZFÁ KOMPLEXEKBE. Doktori (PhD) értekezés tézisei. Kurdi Róbert.
 KIRÁLIS I FORMÁCIÓK TERJEDÉSI MECHA IZMUSA ALKIL-KOBALT-TRIKARBO IL- FOSZFÁ KOMPLEXEKBE Doktori (PhD) értekezés tézisei Kurdi Róbert Pannon Egyetem 2008 1. Bevezetés A kobalt-karbonil vegyületeket gyakran
KIRÁLIS I FORMÁCIÓK TERJEDÉSI MECHA IZMUSA ALKIL-KOBALT-TRIKARBO IL- FOSZFÁ KOMPLEXEKBE Doktori (PhD) értekezés tézisei Kurdi Róbert Pannon Egyetem 2008 1. Bevezetés A kobalt-karbonil vegyületeket gyakran
A kovalens kötés elmélete. Kovalens kötésű molekulák geometriája. Molekula geometria. Vegyértékelektronpár taszítási elmélet (VSEPR)
 4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
4. előadás A kovalens kötés elmélete Vegyértékelektronpár taszítási elmélet (VSEPR) az atomok kötő és nemkötő elektronpárjai úgy helyezkednek el a térben, hogy egymástól minél távolabb legyenek A központi
3. A kémiai kötés. Kémiai kölcsönhatás
 3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
3. A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS OVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Kémiai kötések Na Ionos kötés Kovalens kötés Fémes
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Molekuláris dinamika I. 10. előadás
 Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
A kovalens kötés polaritása
 Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
Általános és szervetlen kémia 4. hét Kovalens kötés A kovalens kötés kialakulásakor szabad atomokból molekulák jönnek létre. A molekulák létrejötte mindig energia csökkenéssel jár. A kovalens kötés polaritása
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n. 2008. április 29.
 Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
Kvalitatív elemzésen alapuló reakciómechanizmus meghatározás
 Kvalitatív elemzésen alapuló reakciómechanizmus meghatározás Varga Tamás Pannon Egyetem, Folyamatmérnöki Intézeti Tanszék IX. Alkalmazott Informatika Konferencia ~ AIK 2011 ~ Kaposvár, Február 25. Tartalom
Kvalitatív elemzésen alapuló reakciómechanizmus meghatározás Varga Tamás Pannon Egyetem, Folyamatmérnöki Intézeti Tanszék IX. Alkalmazott Informatika Konferencia ~ AIK 2011 ~ Kaposvár, Február 25. Tartalom
Kémiai kötés Lewis elmélet
 Kémiai kötés 10-1 Lewis elmélet 10-2 Kovalens kötés: bevezetés 10-3 Poláros kovalens kötés 10-4 Lewis szerkezetek 10-5 A molekulák alakja 10-6 Kötésrend, kötéstávolság 10-7 Kötésenergiák Általános Kémia,
Kémiai kötés 10-1 Lewis elmélet 10-2 Kovalens kötés: bevezetés 10-3 Poláros kovalens kötés 10-4 Lewis szerkezetek 10-5 A molekulák alakja 10-6 Kötésrend, kötéstávolság 10-7 Kötésenergiák Általános Kémia,
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit
 SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
SZAK: KÉMIA Általános és szervetlen kémia 1. A periódusos rendszer 14. csoportja. a) Írják le a csoport nemfémes elemeinek az elektronkonfigurációit b) Tárgyalják összehasonlító módon a csoport első elemének
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén
 ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
ESR-spektrumok különbözı kísérleti körülmények között A számítógépes értékelés alapjai anizotróp kölcsönhatási tenzorok esetén A paraméterek anizotrópiája egykristályok rögzített tengely körüli forgatásakor
Intra- és intermolekuláris reakciók összehasonlítása
 Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Intra- és intermolekuláris reakciók összehasonlítása Intr a- és inter molekulár is r eakciok összehasonlítása molekulán belüli reakciók molekulák közötti reakciók 5- és 6-tagú gyűrűk könnyen kialakulnak.
Műszeres analitika. Abrankó László. Molekulaspektroszkópia. Kémiai élelmiszervizsgálati módszerek csoportosítása
 Abrankó László Műszeres analitika Molekulaspektroszkópia Minőségi elemzés Kvalitatív Cél: Meghatározni, hogy egy adott mintában jelen vannak-e bizonyos ismert komponensek. Vagy ismeretlen komponensek azonosítása
Abrankó László Műszeres analitika Molekulaspektroszkópia Minőségi elemzés Kvalitatív Cél: Meghatározni, hogy egy adott mintában jelen vannak-e bizonyos ismert komponensek. Vagy ismeretlen komponensek azonosítása
A II. kategória Fizika OKTV mérési feladatainak megoldása
 Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Molekuláris dinamika. 10. előadás
 Molekuláris dinamika 10. előadás Mirőlis szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten? Hogyan tudjuk megérteni a folyadékok, gázok, szilárdtestek makroszkópikus
Molekuláris dinamika 10. előadás Mirőlis szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten? Hogyan tudjuk megérteni a folyadékok, gázok, szilárdtestek makroszkópikus
FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI
 FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI statisztika 9 IX. ROBUsZTUs statisztika 1. ROBUsZTUssÁG Az eddig kidolgozott módszerek főleg olyanok voltak, amelyek valamilyen értelemben optimálisak,
FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI statisztika 9 IX. ROBUsZTUs statisztika 1. ROBUsZTUssÁG Az eddig kidolgozott módszerek főleg olyanok voltak, amelyek valamilyen értelemben optimálisak,
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
A kémiai kötés eredete; viriál tétel 1
 A kémiai kötés ereete; viriál tétel 1 Probléma felvetés Ha egy molekula atommagjai közötti távolság csökken, akkor a közöttük fellép elektrosztatikus taszításhoz tartozó energia n. Ugyanez igaz az elektronokra
A kémiai kötés ereete; viriál tétel 1 Probléma felvetés Ha egy molekula atommagjai közötti távolság csökken, akkor a közöttük fellép elektrosztatikus taszításhoz tartozó energia n. Ugyanez igaz az elektronokra
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer A kémiai kötés Kémiai
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Elektrosztatikus számítások. Elektrosztatikus számítások. Elektrosztatikus számítások. Elektrosztatikus számítások Definíciók
 Jelentősége szubsztrát kötődés szolvatáció ionizációs állapotok (pka) mechanizmus katalízis ioncsatornák szimulációk (szerkezet) all-atom dipolar fluid dipolar lattice continuum Definíciók töltéseloszlás
Jelentősége szubsztrát kötődés szolvatáció ionizációs állapotok (pka) mechanizmus katalízis ioncsatornák szimulációk (szerkezet) all-atom dipolar fluid dipolar lattice continuum Definíciók töltéseloszlás
Kutatási beszámoló. 2015. február. Tangens delta mérésére alkalmas mérési összeállítás elkészítése
 Kutatási beszámoló 2015. február Gyüre Balázs BME Fizika tanszék Dr. Simon Ferenc csoportja Tangens delta mérésére alkalmas mérési összeállítás elkészítése A TKI-Ferrit Fejlsztő és Gyártó Kft.-nek munkája
Kutatási beszámoló 2015. február Gyüre Balázs BME Fizika tanszék Dr. Simon Ferenc csoportja Tangens delta mérésére alkalmas mérési összeállítás elkészítése A TKI-Ferrit Fejlsztő és Gyártó Kft.-nek munkája
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz Programajánlatok október 18. 16:00 ELTE Kémiai Intézet 065-ös terem Észbontogató (www.chem.elte.hu/pr)
Ütközések vizsgálatához alkalmazható számítási eljárások
 Ütközések vizsgálatához alkalmazható számítási eljárások Az eljárások a kiindulási adatoktól és a számítás menetétől függően két csoportba sorolhatók. Az egyik a visszafelé történő számítások csoportja,
Ütközések vizsgálatához alkalmazható számítási eljárások Az eljárások a kiindulási adatoktól és a számítás menetétől függően két csoportba sorolhatók. Az egyik a visszafelé történő számítások csoportja,
Fizikai kémia 2. Előzmények. A Lewis-féle kötéselmélet A VB- és az MO-elmélet, a H 2+ molekulaion
 06.07.5. Fizikai kémia. 4. A VB- és az -elmélet, a H + molekulaion Dr. Berkesi ttó ZTE Fizikai Kémiai és Anyagtudományi Tanszéke 05 Előzmények Az atomok szerkezetének kvantummehanikai leírása 90-30-as
06.07.5. Fizikai kémia. 4. A VB- és az -elmélet, a H + molekulaion Dr. Berkesi ttó ZTE Fizikai Kémiai és Anyagtudományi Tanszéke 05 Előzmények Az atomok szerkezetének kvantummehanikai leírása 90-30-as
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Fémorganikus vegyületek
 Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
Fémorganikus vegyületek A fémorganikus vegyületek fém-szén kötést tartalmaznak. Ennek polaritása a fém elektropozitivitásának mértékétől függ: az alkálifém-szén kötések erősen polárosak, jelentős százalékban
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával.
 ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1. Mely mennyiségek között teremt kapcsolatot a bizonytalansági reláció? A) a koordináta értéke
ALKÍMIA MA Az anyagról mai szemmel, a régiek megszállottságával www.chem.elte.hu/pr Kvíz az előző előadáshoz 1. Mely mennyiségek között teremt kapcsolatot a bizonytalansági reláció? A) a koordináta értéke
Robotika. Relatív helymeghatározás Odometria
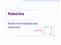 Robotika Relatív helymeghatározás Odometria Differenciális hajtás c m =πd n /nc e c m D n C e n = hány mm-t tesz meg a robot egy jeladó impulzusra = névleges kerék átmérő = jeladó fölbontása (impulzus/ford.)
Robotika Relatív helymeghatározás Odometria Differenciális hajtás c m =πd n /nc e c m D n C e n = hány mm-t tesz meg a robot egy jeladó impulzusra = névleges kerék átmérő = jeladó fölbontása (impulzus/ford.)
Akusztikai tervezés a geometriai akusztika módszereivel
 Akusztikai tervezés a geometriai akusztika módszereivel Fürjes Andor Tamás BME Híradástechnikai Tanszék Kép- és Hangtechnikai Laborcsoport, Rezgésakusztika Laboratórium 1 Tartalom A geometriai akusztika
Akusztikai tervezés a geometriai akusztika módszereivel Fürjes Andor Tamás BME Híradástechnikai Tanszék Kép- és Hangtechnikai Laborcsoport, Rezgésakusztika Laboratórium 1 Tartalom A geometriai akusztika
PhD DISSZERTÁCIÓ TÉZISEI
 Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis-elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis-elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
41. ábra A NaCl rács elemi cellája
 41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
41. ábra A NaCl rács elemi cellája Mindkét rácsra jellemző, hogy egy tetszés szerint kiválasztott pozitív vagy negatív töltésű iont ellentétes töltésű ionok vesznek körül. Különbség a közvetlen szomszédok
Regresszió számítás. Tartalomjegyzék: GeoEasy V2.05+ Geodéziai Kommunikációs Program
 Regresszió számítás GeoEasy V2.05+ Geodéziai Kommunikációs Program DigiKom Kft. 2006-2010 Tartalomjegyzék: Egyenes x változik Egyenes y változik Egyenes y és x változik Kör Sík z változik Sík y, x és z
Regresszió számítás GeoEasy V2.05+ Geodéziai Kommunikációs Program DigiKom Kft. 2006-2010 Tartalomjegyzék: Egyenes x változik Egyenes y változik Egyenes y és x változik Kör Sík z változik Sík y, x és z
6) Az átmenetifémek szerves származékai
 Rendszeres fémorganikus kémia 2009-2010 (134) Átmenetifém-átmenetifém kötések és klaszterek Történet: A. Werner (1866-1919) oligonukleáris komplexekben ligandum-hidakat tételezett fel: (H 3 N)(Cl)Pt(µ-Cl)
Rendszeres fémorganikus kémia 2009-2010 (134) Átmenetifém-átmenetifém kötések és klaszterek Történet: A. Werner (1866-1919) oligonukleáris komplexekben ligandum-hidakat tételezett fel: (H 3 N)(Cl)Pt(µ-Cl)
Összefoglalók Kémia BSc 2012/2013 I. félév
 Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Összefoglalók Kémia BSc 2012/2013 I. félév Készült: Eötvös Loránd Tudományegyetem Kémiai Intézet Szerves Kémiai Tanszékén 2012.12.17. Összeállította Szilvágyi Gábor PhD hallgató Tartalomjegyzék Orgován
Atomok és molekulák elektronszerkezete
 Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Erőterek. Erőterek. Erőterek. Erőterek. Erőterek. Erőterek. Probléma: fehérjéknél nagy dimenziók értelmetlen QM eredmények.
 fehérjéknél nagy dimenziók értelmetlen QM eredmények Megoldás: egyszerűsítés dimenzió-csökkentés Közelítések Born-Oppenheimer közelítés (Ψ mol = Ψ el Ψ mag ; E tot =E el +E mag ) az energia párkölcsönhatások
fehérjéknél nagy dimenziók értelmetlen QM eredmények Megoldás: egyszerűsítés dimenzió-csökkentés Közelítések Born-Oppenheimer közelítés (Ψ mol = Ψ el Ψ mag ; E tot =E el +E mag ) az energia párkölcsönhatások
Fémorganikus kémia 1
 Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Fémorganikus kémia 1 A fémorganikus kémia tárgya a szerves fémvegyületek előállítása, szerkezetvizsgálata és kémiai reakcióik tanulmányozása A fémorganikus kémia fejlődése 1760 Cadet bisz(dimetil-arzén(iii))-oxid
Problémás regressziók
 Universitas Eotvos Nominata 74 203-4 - II Problémás regressziók A közönséges (OLS) és a súlyozott (WLS) legkisebb négyzetes lineáris regresszió egy p- változós lineáris egyenletrendszer megoldása. Az egyenletrendszer
Universitas Eotvos Nominata 74 203-4 - II Problémás regressziók A közönséges (OLS) és a súlyozott (WLS) legkisebb négyzetes lineáris regresszió egy p- változós lineáris egyenletrendszer megoldása. Az egyenletrendszer
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése
 Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Célkitűzés/témák Fehérje-ligandum kölcsönhatások és a kötődés termodinamikai jellemzése Ferenczy György Semmelweis Egyetem Biofizikai és Sugárbiológiai Intézet Biokémiai folyamatok - Ligandum-fehérje kötődés
Folyadékszcintillációs spektroszkópia jegyz könyv
 Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Modern fizika laboratórium
 Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
I. BESZÁLLÍTÓI TELJESÍTMÉNYEK ÉRTÉKELÉSE
 I. BESZÁLLÍTÓI TELJESÍTMÉNYEK ÉRTÉKELÉSE Komplex termékek gyártására jellemző, hogy egy-egy termékbe akár több ezer alkatrész is beépül. Ilyenkor az alkatrészek általában sok különböző beszállítótól érkeznek,
I. BESZÁLLÍTÓI TELJESÍTMÉNYEK ÉRTÉKELÉSE Komplex termékek gyártására jellemző, hogy egy-egy termékbe akár több ezer alkatrész is beépül. Ilyenkor az alkatrészek általában sok különböző beszállítótól érkeznek,
A kémiai kötés. Kémiai kölcsönhatás
 A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
A kémiai kötés Kémiai kölcsönhatás ELSŐDLEGES MÁSODLAGOS KOVALENS IONOS FÉMES HIDROGÉN- KÖTÉS DIPÓL- DIPÓL, ION- DIPÓL, VAN DER WAALS v. DISZPERZIÓS Ionos kötés Na Cl Ionpár képződése e - Na + Cl - Na:
Modern Fizika Labor. 2. Elemi töltés meghatározása
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2011.09.27. A mérés száma és címe: 2. Elemi töltés meghatározása Értékelés: A beadás dátuma: 2011.10.11. A mérést végezte: Kalas György Benjámin Németh Gergely
Modern Fizika Labor Fizika BSC A mérés dátuma: 2011.09.27. A mérés száma és címe: 2. Elemi töltés meghatározása Értékelés: A beadás dátuma: 2011.10.11. A mérést végezte: Kalas György Benjámin Németh Gergely
A periódusos rendszer, periodikus tulajdonságok
 A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
A periódusos rendszer, periodikus tulajdonságok Szalai István ELTE Kémiai Intézet 1/45 Az előadás vázlata ˆ Ismétlés ˆ Történeti áttekintés ˆ Mengyelejev periódusos rendszere ˆ Atomsugár, ionsugár ˆ Ionizációs
Modern Fizika Labor. 12. Infravörös spektroszkópia. Fizika BSc. A mérés dátuma: okt. 04. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Érdekes geometriai számítások Téma: A kardáncsukló kinematikai alapegyenletének levezetése gömbháromszögtani alapon
 Érdekes geometriai számítások 7. Folytatjuk a sorozatot. 7. Téma: A kardáncsukló kinematikai alapegyenletének levezetése gömbháromszögtani alapon Korábbi dolgozatainkban már többféle módon is bemutattuk
Érdekes geometriai számítások 7. Folytatjuk a sorozatot. 7. Téma: A kardáncsukló kinematikai alapegyenletének levezetése gömbháromszögtani alapon Korábbi dolgozatainkban már többféle módon is bemutattuk
SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG
 SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2019/20. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás
SZÁMÍTÓGÉPES KÉMIA ALAPJAI VEGYÉSZMÉRNÖK BSc. NAPPALI TÖRZSANYAG TANTÁRGYI MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR KÉMIAI INTÉZET Miskolc, 2019/20. tanév I. félév 1 Tartalomjegyzék 1. Tantárgyleírás
Kurtán Tibor. Természetes eredetű és szintetikus heterociklusok sztereokémiai vizsgálata. című akadémiai doktori értekezésének bírálata
 Kurtán Tibor Természetes eredetű és szintetikus heterociklusok sztereokémiai vizsgálata című akadémiai doktori értekezésének bírálata Bírálatomat egy vallomással kell kezdenem. Amikor a Doktori Tanácstól
Kurtán Tibor Természetes eredetű és szintetikus heterociklusok sztereokémiai vizsgálata című akadémiai doktori értekezésének bírálata Bírálatomat egy vallomással kell kezdenem. Amikor a Doktori Tanácstól
Szénhidrogének II: Alkének. 2. előadás
 Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Szénhidrogének II: Alkének 2. előadás Általános jellemzők Általános képlet C n H 2n Kevesebb C H kötés van bennük, mint a megfelelő tagszámú alkánokban : telítetlen vegyületek Legalább egy C = C kötést
Altalános Kémia BMEVESAA101 tavasz 2008
 Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Folyadékok és szilárd anayagok 3-1 Intermolekuláris erők, folyadékok tulajdonságai 3-2 Folyadékok gőztenziója 3-3 Szilárd anyagok néhány tulajdonsága 3-4 Fázisdiagram 3-5 Van der Waals kölcsönhatások 3-6
Modern Fizika Labor. 5. ESR (Elektronspin rezonancia) Fizika BSc. A mérés dátuma: okt. 25. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. okt. 25. A mérés száma és címe: 5. ESR (Elektronspin rezonancia) Értékelés: A beadás dátuma: 2011. nov. 16. A mérést végezte: Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. okt. 25. A mérés száma és címe: 5. ESR (Elektronspin rezonancia) Értékelés: A beadás dátuma: 2011. nov. 16. A mérést végezte: Szőke Kálmán Benjamin
Al-Mg-Si háromalkotós egyensúlyi fázisdiagram közelítő számítása
 l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
Infobionika ROBOTIKA. X. Előadás. Robot manipulátorok II. Direkt és inverz kinematika. Készült a HEFOP P /1.0 projekt keretében
 Infobionika ROBOTIKA X. Előadás Robot manipulátorok II. Direkt és inverz kinematika Készült a HEFOP-3.3.1-P.-2004-06-0018/1.0 projekt keretében Tartalom Direkt kinematikai probléma Denavit-Hartenberg konvenció
Infobionika ROBOTIKA X. Előadás Robot manipulátorok II. Direkt és inverz kinematika Készült a HEFOP-3.3.1-P.-2004-06-0018/1.0 projekt keretében Tartalom Direkt kinematikai probléma Denavit-Hartenberg konvenció
A KLT (Kanade Lucas Tomasi) Feature Tracker Működése (jellegzetes pontok választása és követése)
 A KL (Kanade Lucas omasi) Feature racker Működése (jellegzetes pontok választása és követése) Készítette: Hajder Levente 008.11.18. 1. Feladat A rendelkezésre álló videó egy adott képkockájából minél több
A KL (Kanade Lucas omasi) Feature racker Működése (jellegzetes pontok választása és követése) Készítette: Hajder Levente 008.11.18. 1. Feladat A rendelkezésre álló videó egy adott képkockájából minél több
A cukrok szerkezetkémiája
 A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
A cukrok szerkezetkémiája A cukrokról,szénhidrátokról általánosan o o o Kémiailag a cukrok a szénhidrátok,vagy szacharidok csoportjába tartozó vegyületek. A szacharid arab eredetű szó,jelentése: édes.
Gyenge kölcsönhatások karbonilezési reakciók során Záróbeszámoló (2007)
 Gyenge kölcsönhatások karbonilezési reakciók során Záróbeszámoló (2007) Az olefinek hidroformilezése több mint 50 éve ismert ipari jelentőségű homogénkatalitikus eljárás, melynek során az átmenetifém katalizátor
Gyenge kölcsönhatások karbonilezési reakciók során Záróbeszámoló (2007) Az olefinek hidroformilezése több mint 50 éve ismert ipari jelentőségű homogénkatalitikus eljárás, melynek során az átmenetifém katalizátor
A kémiatanári zárószigorlat tételsora
 1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
1. A. tétel A kémiatanári zárószigorlat tételsora Kémiai alapfogalmak: Atom- és molekulatömeg, anyagmennyiség, elemek és vegyületek elnevezése, jelölése. Kémiai egyenlet, sztöchiometria. A víz jelentősége
BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011.
 BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011. 1 Mérési hibák súlya és szerepe a mérési eredményben A mérési hibák csoportosítása A hiba rendűsége Mérési bizonytalanság Standard és kiterjesztett
BAGME11NNF Munkavédelmi mérnökasszisztens Galla Jánosné, 2011. 1 Mérési hibák súlya és szerepe a mérési eredményben A mérési hibák csoportosítása A hiba rendűsége Mérési bizonytalanság Standard és kiterjesztett
STATISZTIKAI PROBLÉMÁK A
 STATISZTIKAI PROBLÉMÁK A HULLÁMTÉR REPRODUKCIÓ TERÜLETÉN 2012. május 3., Budapest Firtha Gergely PhD hallgató, Akusztikai Laboratórium BME Híradástechnikai Tanszék firtha@hit.bme.hu Tartalom A hangtér
STATISZTIKAI PROBLÉMÁK A HULLÁMTÉR REPRODUKCIÓ TERÜLETÉN 2012. május 3., Budapest Firtha Gergely PhD hallgató, Akusztikai Laboratórium BME Híradástechnikai Tanszék firtha@hit.bme.hu Tartalom A hangtér
Kvantumszimulátorok. Szirmai Gergely MTA SZFKI. Graphics: Harald Ritsch / Rainer Blatt, IQOQI
 Kvantumszimulátorok Szirmai Gergely MTA SZFKI Graphics: Harald Ritsch / Rainer Blatt, IQOQI A kvantummechanika körülvesz tranzisztor számítógép, mobiltelefon A kvantummechanika körülvesz tranzisztor számítógép,
Kvantumszimulátorok Szirmai Gergely MTA SZFKI Graphics: Harald Ritsch / Rainer Blatt, IQOQI A kvantummechanika körülvesz tranzisztor számítógép, mobiltelefon A kvantummechanika körülvesz tranzisztor számítógép,
A dinamikus geometriai rendszerek használatának egy lehetséges területe
 Fejezetek a matematika tanításából A dinamikus geometriai rendszerek használatának egy lehetséges területe Készítette: Harsányi Sándor V. matematika-informatika szakos hallgató Porcsalma, 2004. december
Fejezetek a matematika tanításából A dinamikus geometriai rendszerek használatának egy lehetséges területe Készítette: Harsányi Sándor V. matematika-informatika szakos hallgató Porcsalma, 2004. december
Abszorpciós spektroszkópia
 Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
A szárazmegmunkálás folyamatjellemzőinek és a megmunkált felület minőségének vizsgálata keményesztergálásnál
 1 A szárazmegmunkálás folyamatjellemzőinek és a megmunkált felület minőségének vizsgálata keményesztergálásnál A keményesztergálás, amelynél a forgácsolás 55 HRC-nél keményebb acélon, néhány ezred vagy
1 A szárazmegmunkálás folyamatjellemzőinek és a megmunkált felület minőségének vizsgálata keményesztergálásnál A keményesztergálás, amelynél a forgácsolás 55 HRC-nél keményebb acélon, néhány ezred vagy
Gnädig Péter: Golyók, labdák, korongok és pörgettyűk csalafinta mozgása április 16. Pörgettyűk különböző méretekben az atomoktól a csillagokig
 Gnädig Péter: Golyók, labdák, korongok és pörgettyűk csalafinta mozgása 2015. április 16. Pörgettyűk különböző méretekben az atomoktól a csillagokig Egyetlen tömegpont: 3 adat (3 szabadsági fok ) Példa:
Gnädig Péter: Golyók, labdák, korongok és pörgettyűk csalafinta mozgása 2015. április 16. Pörgettyűk különböző méretekben az atomoktól a csillagokig Egyetlen tömegpont: 3 adat (3 szabadsági fok ) Példa:
A Hamilton-Jacobi-egyenlet
 A Hamilton-Jacobi-egyenlet Ha sikerül olyan kanonikus transzformációt találnunk, amely a Hamilton-függvényt zérusra transzformálja akkor valamennyi új koordináta és impulzus állandó lesz: H 0 Q k = H P
A Hamilton-Jacobi-egyenlet Ha sikerül olyan kanonikus transzformációt találnunk, amely a Hamilton-függvényt zérusra transzformálja akkor valamennyi új koordináta és impulzus állandó lesz: H 0 Q k = H P
A racionális gyógyszertervezés lehetőségei. A racionális gyógyszertervezés lehetőségei. A racionális gyógyszertervezés lehetőségei
 Cél: kis koncentrációban kötődő célvegyület tervezése Agonista: segíti az enzim működését, hatékonyabb, mint a természetes szubsztrát Antagonista: gátolja az enzim működését, ellentétes hatású, mint a
Cél: kis koncentrációban kötődő célvegyület tervezése Agonista: segíti az enzim működését, hatékonyabb, mint a természetes szubsztrát Antagonista: gátolja az enzim működését, ellentétes hatású, mint a
1.7. Felületek és katalizátorok
 Mobilitás és Környezet Konferencia Magyar Tudományos Akadémia Budapest, 2012. január 23. 1.7. Felületek és katalizátorok Polimer töltőanyagként alkalmazható agyagásvány nanostruktúrák előállítása Horváth
Mobilitás és Környezet Konferencia Magyar Tudományos Akadémia Budapest, 2012. január 23. 1.7. Felületek és katalizátorok Polimer töltőanyagként alkalmazható agyagásvány nanostruktúrák előállítása Horváth
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban
 1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
1. feladat (3 pont) Írjon példát olyan aminosav-párokra, amelyek részt vehetnek a következő kölcsönhatásokban a, diszulfidhíd (1 példa), b, hidrogénkötés (2 példa), c, töltés-töltés kölcsönhatás (2 példa)!
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
Vegyületek - vegyületmolekulák
 Vegyületek - vegyületmolekulák 3.Az anyagok csoportosítása összetételük szerint Egyszerű összetett Azonos atomokból állnak különböző atomokból állnak Elemek vegyületek keverékek Fémek Félfémek Nemfémek
Vegyületek - vegyületmolekulák 3.Az anyagok csoportosítása összetételük szerint Egyszerű összetett Azonos atomokból állnak különböző atomokból állnak Elemek vegyületek keverékek Fémek Félfémek Nemfémek
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI
 SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
SZAKÁLL SÁNDOR, ÁsVÁNY- És kőzettan ALAPJAI 6 KRISTÁLYTAN VI. A KRIsTÁLYOs ANYAG belső RENDEZETTsÉGE 1. A KRIsTÁLYOs ÁLLAPOT A szilárd ANYAG jellemzője Az ásványok néhány kivételtől eltekintve kristályos
Atomszerkezet. Atommag protonok, neutronok + elektronok. atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok
 Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
Atomszerkezet Atommag protonok, neutronok + elektronok izotópok atompályák, alhéjak, héjak, atomtörzs ---- vegyérték elektronok periódusos rendszer csoportjai Periódusos rendszer energia szintek atomokban
3D - geometriai modellezés, alakzatrekonstrukció, nyomtatás
 3D - geometriai modellezés, alakzatrekonstrukció, nyomtatás 15. Digitális Alakzatrekonstrukció Méréstechnológia, Ponthalmazok regisztrációja http://cg.iit.bme.hu/portal/node/312 https://www.vik.bme.hu/kepzes/targyak/viiiav54
3D - geometriai modellezés, alakzatrekonstrukció, nyomtatás 15. Digitális Alakzatrekonstrukció Méréstechnológia, Ponthalmazok regisztrációja http://cg.iit.bme.hu/portal/node/312 https://www.vik.bme.hu/kepzes/targyak/viiiav54
Tartalmi követelmények kémia tantárgyból az érettségin K Ö Z É P S Z I N T
 1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
1. Általános kémia Atomok és a belőlük származtatható ionok Molekulák és összetett ionok Halmazok A kémiai reakciók A kémiai reakciók jelölése Termokémia Reakciókinetika Kémiai egyensúly Reakciótípusok
FELADATMEGOLDÁS. Tesztfeladat: Válaszd ki a helyes megoldást!
 FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
Q 1 D Q 2 (D x) 2 (1.1)
 . Gyakorlat 4B-9 Két pontszerű töltés az x tengelyen a következőképpen helyezkedik el: egy 3 µc töltés az origóban, és egy + µc töltés az x =, 5 m koordinátájú pontban van. Keressük meg azt a helyet, ahol
. Gyakorlat 4B-9 Két pontszerű töltés az x tengelyen a következőképpen helyezkedik el: egy 3 µc töltés az origóban, és egy + µc töltés az x =, 5 m koordinátájú pontban van. Keressük meg azt a helyet, ahol
Modern Fizika Labor. 2. Az elemi töltés meghatározása. Fizika BSc. A mérés dátuma: nov. 29. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 29. A mérés száma és címe: 2. Az elemi töltés meghatározása Értékelés: A beadás dátuma: 2011. dec. 11. A mérést végezte: Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 29. A mérés száma és címe: 2. Az elemi töltés meghatározása Értékelés: A beadás dátuma: 2011. dec. 11. A mérést végezte: Szőke Kálmán Benjamin
Transzformációk síkon, térben
 Transzformációk síkon, térben Leképezés, transzformáció Leképezés: Ha egy A ponttér pontjaihoz egy másik B ponttér pontjait kölcsönösen egyértelműen rendeljük hozzá, akkor ezt a hozzárendelést leképezésnek
Transzformációk síkon, térben Leképezés, transzformáció Leképezés: Ha egy A ponttér pontjaihoz egy másik B ponttér pontjait kölcsönösen egyértelműen rendeljük hozzá, akkor ezt a hozzárendelést leképezésnek
KÖSZÖNTJÜK HALLGATÓINKAT!
 2010. november 10. KÖSZÖNTJÜK HALLGATÓINKAT! Önök Dr. Horváth Zoltán Módszerek, amelyek megváltoztatják a világot A számítógépes szimuláció és optimalizáció jelentősége c. előadását hallhatják! 1 Módszerek,
2010. november 10. KÖSZÖNTJÜK HALLGATÓINKAT! Önök Dr. Horváth Zoltán Módszerek, amelyek megváltoztatják a világot A számítógépes szimuláció és optimalizáció jelentősége c. előadását hallhatják! 1 Módszerek,
Folyadékok és szilárd anyagok
 Folyadékok és szilárd anyagok 7-1 Intermolekuláris erők, folyadékok tulajdonságai 7-2 Folyadékok gőztenziója 7-3 Szilárd anyagok néhány tulajdonsága 7-4 Fázisdiagram 7-5 Van der Waals kölcsönhatások 7-6
Folyadékok és szilárd anyagok 7-1 Intermolekuláris erők, folyadékok tulajdonságai 7-2 Folyadékok gőztenziója 7-3 Szilárd anyagok néhány tulajdonsága 7-4 Fázisdiagram 7-5 Van der Waals kölcsönhatások 7-6
Röntgendiffrakció. Orbán József PTE, ÁOK, Biofizikai Intézet november
 Röntgendiffrakció Orbán József PTE, ÁOK, Biofizikai Intézet 2013. november Előadás vázlata Röntgen sugárzás Interferencia, diffrakció (elektromágneses hullámok) Kristályok szerkezete Röntgendiffrakció
Röntgendiffrakció Orbán József PTE, ÁOK, Biofizikai Intézet 2013. november Előadás vázlata Röntgen sugárzás Interferencia, diffrakció (elektromágneses hullámok) Kristályok szerkezete Röntgendiffrakció
FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI
 FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI statisztika 10 X. SZIMULÁCIÓ 1. VÉLETLEN számok A véletlen számok fontos szerepet játszanak a véletlen helyzetek generálásában (pénzérme, dobókocka,
FEGYVERNEKI SÁNDOR, Valószínűség-sZÁMÍTÁs És MATEMATIKAI statisztika 10 X. SZIMULÁCIÓ 1. VÉLETLEN számok A véletlen számok fontos szerepet játszanak a véletlen helyzetek generálásában (pénzérme, dobókocka,
Mozgatható térlefedő szerkezetek
 Mozgatható térlefedő szerkezetek TDK Konferencia 2010 Szilárdságtani és tartószerkezeti szekció Tartalomjegyzék 1 Absztrakt 2 Bevezetés 3 Az alakzat mozgásának görbületre gyakorolt hatása 4 Teljes összenyomódás
Mozgatható térlefedő szerkezetek TDK Konferencia 2010 Szilárdságtani és tartószerkezeti szekció Tartalomjegyzék 1 Absztrakt 2 Bevezetés 3 Az alakzat mozgásának görbületre gyakorolt hatása 4 Teljes összenyomódás
Versenyző rajtszáma: 1. feladat
 1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
1. feladat / 5 pont Jelölje meg az alábbi vegyület valamennyi királis szénatomját, és adja meg ezek konfigurációját a Cahn Ingold Prelog (CIP) konvenció szerint! 2. feladat / 6 pont 1887-ben egy orosz
Szabó Dénes Molekulák és reakciók három dimenzióban
 Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
Szabó Dénes Molekulák és reakciók három dimenzióban Alkímia ma, 2012. április 19. Egy kis tudománytörténet -O azonos kémiai szerkezet -O Scheele (1769) -O különböző tulajdonságok -O Kestner (1822) borkősav
