Immunológiai Gyakorlatok II április
|
|
|
- Regina Gál
- 9 évvel ezelőtt
- Látták:
Átírás
1 Immunológiai Gyakorlatok II április T- és B-limfociták szeparálása (dúsítása) egér lépsejt-szuszpenzióból; neutrofil extracelluláris csapda (NET) vizsgálata Anyagok: steril fülke, olló, csipesz, fecskendő, petri csésze, Falcon cső, szűrő (mind steril), centrifuga, pipetta, Bürker kamra GKN (fiziológiás NaCl, glukóz és fenolvörös tartalmú foszfát puffer, ph 7.2) RPMI 1640 komplett médium (2-merkapto-etanollal, piruváttal és antibiotikumokkal kiegészített, 10 % FCS-t tartalmazó tápoldat) ACK (KCl és EDTA tartalmú 0,83 %-os ammóniumklorid oldat) Anti-Thy-1.2 (HO-13.4 egér monoklonális IgM) tartalmú sejttenyészet felülúszó Friss (legfeljebb egyszer lefagyasztott és felolvasztott) nyúlsavó Tripánkék (festék sejtszámoláshoz, élő/pusztult arány megállapításához) A lép feldolgozása: 1. A lép és a combcsontok steril körülmények között történő kivétele az egerekből GKN oldatot tartalmazó petricsészékbe. A csontvelő izolálása a D. pontban! 2. Sejtszuszpenzió készítése és 50 ml-es Falcon csövekbe töltése majd a sejtek lecentrifugálása (7 perc, 1200 rpm, 4 C) 3. A felülúszó leöntése után a sejtüledék fellazítása (vortex), majd ml ACK oldat hozzáadásával a vörösvérsejtek lízise. 1,5 perc inkubálás után a csövek feltöltése GKN-nel (50 ml), majd a sejtek lecentrifugálása (7 perc, 1200 rpm, 4 C). 4. A sejtek felvétele 10 ml RPMI-ben, átszűrése (70µm-es sejtszűrő), majd a sejtszám megállapítása Bürker-kamrával. 5. A sejtszuszpenzió kettéosztása: 7 ml szuszpenzió a T-sejt deplécióhoz, 3 ml a sejtszortírozáshoz. A. B-limfociták dúsítása T-sejt deplécióval A/6. A 7 ml lépsejtszuszpenzió kiegészítése 1 ml anti-thy-1 tartalmú sejttenyészet felülúszóval és 2 ml tápoldattal, majd 20 perc inkubálás szobahőmérsékleten. A/7. A sejteket lecentrifugálása (7 perc, 1200 rpm, 20 C) után a felülúszó elöntése és a sejtüledék fellazítása, majd a sejtek felvétele 9 ml GKN oldatban. 1 ml friss nyúlsavó (komplement forrás) hozzáadása, majd inkubálás percig 37 C-os vízfürdőben. A/8. A sejtek lecentrifugálása (7 perc, 1200 rpm, 20 C), mosása 50ml GKN oldatban (centrifugálás: 7 perc, 1200 rpm, 20 C) majd a sejtek felvétele 5 ml tápoldatban, sejtszámolás. 1
2 B. T-sejt dúsítás szorterrel és a T-sejt depléció ellenőrzése áramlási citometriával Hozzávalók: - teljes lépsejt szuszpenzió és T-sejt depletált lépsejt szuszpenzió - FACS puffer (PBS, 1% FCS, 0,1% Na-azid) - FACS csövek - előre kihígított FcγR blokkoló ellenanyag 50 ul / cső - előre kihígított konjugált ellenanyagok (ea): anti-cd3-fitc 50 μl / cső anti-cd19-apc 50 μl / cső A módszer leírása: A T-sejt-depletált szuszpenzió egy részét (~10 6 sejtet) és a teljes szuszpenziót is lecentrifugáljuk (7 perc,1200 rpm, 4 C), majd leöntjük róluk a médiumot. Enyhe vortexelés után µl FcγR blokkoló ellenanyagot pipettázunk a sejtpelletekre (5 perc inkubáció jégen). Ezek után felvesszük a sejteket 1-1 ml FACS pufferben, és szétosztjuk őket FACS csövekbe 250µl-enként. Minden csőhöz a táblázat alapján hozzáadjuk a megfelelő antitesteket (50 µl / cső). 20 perc inkubáció, fénytől elzárva, 4 C. cső minta Antitestek (20 perc jégen) 1. teljes lép - 2. teljes lép anti-cd19-apc 3. teljes lép anti-cd3-fitc 4. teljes lép anti-cd19-apc + anti-cd3-fitc 5. T-sejt depletált - 6. T-sejt depletált anti-cd19-apc 7. T-sejt depletált anti-cd3-fitc 8. T-sejt depletált anti-cd19-apc + anti-cd3-fitc Mosás 3ml FACS pufferrel, a mosási lépést követően a fellazított sejtpellethez 500 μl FACS puffert adunk. A sejtek lemérése FACS ARIA III. sejtszortírozó berendezéssel. Feladat: Határozzuk meg a B-sejt dúsítás hatékonyságát az egyes mintákban a B- és T-sejtek %-os arányának megállapításával! C. Proliferációs teszt CFSE jelöléssel Hozzávalók: T-sejt depletált lépsejtek CFSE (Carboxyfluorescein succinimidyl ester) 10 mm-os oldata PBS-5 %FCS stimuláló ellenanyag: kecskében termelt anti-egér IgM (0,5 mg/ml) A sejtek feltöltése CFSE-vel: A T-sejt deplécióval tisztított B-sejtek koncentrációját 2-5x10 7 /ml-re állítsuk be 1 ml végtérfogatban, PBS/5%FCS oldatban, 15 ml-es Falcon csőben. Adjunk a sejtekhez 5 µm 2
3 végkoncentrációban CFSE-t, majd inkubáljuk sötétben, szobahőmérsékleten 10 percig. Mossuk a sejteket 2x PBS-5%FCS oldattal (10 ml, 7 perc,1200 rpm, 20 C) majd vegyük fel a sejteket tápfolyadékban és állítsuk be a sejtszámot 2x10 6 /ml-re. A sejtek stimulálása: Tegyük ki a sejteket 96 lyukú platre ( µl sejtszuszpenzió/lyuk, mintánként 3 párhuzamos), adjuk hozzá a stimuláló ellenanyagot (anti-igm) 100 ul-ben, 10 és 1 µg/ml végkoncentrációban, majd 5 napra, 37 C-ra, CO2 termosztátba helyezzük a sejteket. A sejtproliferációt FACS segítségével, 5 nap elteltével mérjük. A B tápoldat tápoldat tápoldat C a-igm 1 a-igm 1 a-igm 1 D a-igm 10 a-igm 10 a-igm 10 E F G H D. Neutrofil granulociták kinyerése és stimulálása A combcsontokat kiszedjük az egerekből, majd Petri-csészében GKN-oldattal injekciós tű segítségével kimossuk a csontvelőt a combcsontokból. A szuszpenziót lecentrifugáljuk (7 perc,1200 rpm, 4 C), a vörösvértesteket a lépnél leírtak szerint ACK oldattal lizáljuk, majd mosás után a sejteket 1ml tápoldatban felvesszük. 8-lyukú kamrás lemezen két lyukba 5x10 5 sejtet mérünk, és 20 percig hagyjuk őket kitapadni (37 C, CO2 inkubátor). A tápoldatot óvatosan leszívjuk, majd a kontrollhoz 150 µl tápoldatot, a stimulált mintához 150 µl 100 nm phorpbol-miristoyl-acetátot (PMA; protein kináz C aktivátor) tartalmazó tápoldatot pipettázunk. A kamrát 3 órára 37 C-os CO2 inkubátorba rakjuk. Festés: A lyukakból kiszívjuk a folyadékot, majd PBS-sel óvatosan 2x mossuk. Lyukanként 120 µl Sytox orange festéket tartalmazó oldatot pipettázunk, 20 percig állni hagyjuk a mintákat, majd CLSM-mel értékeljük. 3
4 A B-sejtek antigénreceptor-közvetített aktivációja: Intracelluláris fehérjék foszforilációjának kimutatása Western blot módszerrel Anyagok, pufferek, reagensek, eszközök: BL41 sejtvonal (humán, érett B sejtek) aktiváló ellenanyag (anti-humán IgG+M F(ab )2 ), előzetesen titrálva szérummentes RPMI 1640 médium lízis puffer (a sejtek szolubilizálására alkalmas, detergens tartalmú oldat): Tris 50mM, NaCl 150mM, EDTA 5mM, 0,1% NP40, ph 7,6 A pufferhez mindig frissen adjuk a proteáz- és foszfatázgátlókat: Proteázinhibitor koktél hígítás: 1:20 Foszfatázinhibitor koktél hígítás: 1:50 folyékony nitrogén Gélöntéshez: akrilamid-biszakrilamid 33 %-os oldata. 0,5 M-os Tris/HCl puffer ph 6.8 1,5 M-os Tris/HCl puffer ph %-os SDS oldat 10%-os ammónium perszulfát oldat (APS) N,N,N',N'-tetrametil-etiléndiamin (TEMED) 2-szeres redukáló minta-puffer a poliakrilamid gélelektroforézis (PAGE)-hez: (0.5 M Tris/HCl ph 6.8, SDS, glicerin, 2-merkapto-etanol, brómfenolkék) Elektroforézis futtató puffer: (14.4 g/l glicin, 3 g/l Tris/HCl, 0.1 % SDS ph: 8,3) Blottoló puffer: (14.4 g/l glicin, 3 g/l Tris/HCl ph: 8,3) Membrán-mosó puffer (TWB): 1 literre (ph: 7.6): 2.42 g/l Tris (20 mm) 8.00 g/l NaCl (137 mm) 3.8 ml 1 M HCl 0.05 % TWEEN - Blokkoló puffer: 5% BSA oldat TWB-ben - szűrőpapír, nitrocellulóz membrán (0.45 µm pórusméret) a blottoláshoz - Eppendorf-csövek, pipetták, centrifugacsövek, automata pipetták - molekula-tömeg standard - anti-foszfotirozin monoklonális ellenanyag - anti-egér IgG-tormaperoxidázzal konjugálva - kemiluminescens szubsztrát (ECL-reagens) - röntgen film - előhívó és fixáló oldatok - elektroforézis és blottoló készülék 4
5 A sejtek aktiválása: - Mossuk a B-sejteket szérum-mentes médiumban, és állítsuk a sejtek számát 1x10 7 /ml-re. - Tartsuk a mintákat (200 µl/ Eppendorf-cső) szérum-mentes médiumban 37 C-on percig, majd aktiváljuk a sejteket 2, 5, 20 és 60 percig 5 µg anti-humán IgG+M-el + készítsünk egy 60 perces aktivált mintát, amit foszfatázinhibitor mentes lízis pufferben fogunk lizálni. (A reakció pontos leállítása érdekében az egyes mintákat az idő visszaszámlálásával stimuláljuk, vagyis a 2-perces aktivációt az 58. percben kezdjük el.) - Centrifugáljuk a mintákat rögtön az inkubációs idő elteltével (14000 g, 30 mp), szívjuk le a felülúszót és tegyük a sejtüledéket tartalmazó Eppendorf-csövet lezárva folyékony nitrogénbe. Így az adott időpontban a sejtekre jellemző aktivitást befagyasztjuk. Minták: - Kontroll (nem aktivált) foszfatáz-gátló mentes lízis pufferrel A sejtek szolubilizálása - Vegyük ki a csöveket a nitrogénből csipesszel és minden mintához azonnal mérjünk 100 µl szolubilizáló puffert. Vortex segítségével azonnal keverjük össze, amíg nem marad üledék a cső alján. - Hagyjuk állni a mintákat jég között 30 percig. - A detergensben oldhatatlan frakciót (törmelék membrán, mag, stb.) ülepítsük g-vel 15 percig centrifugálva 4 oc-on. - Vigyünk át 90 µl felülúszót újabb Eppendorf-csövekbe és mérjünk hozzá 90 µl 2X redukáló mintapuffert. SDS-PAGE és Western blot - Futtassunk meg SDS-PAGE-sel minden mintából 20 µl-t, redukáló közegben. - Blottoljuk a szétválasztott fehérje-elegyet nitrocellulóz membránra. - Blokkoljuk a sejtlizátum fehérjéit tartalmazó nitrocellulóz membrán szabadon maradt kötőhelyeit szobahőmérsékleten 5 % BSA-t tartalmazó TWB-vel 1 órán át billegőasztalon. - Adjunk egy újabb adag 5% BSA-t tartalmazó TWB-hez monoklonális anti-foszfotirozin ellenanyagot (1:8000 hígításban) és inkubáljuk 4 C-on éjszaka, állandó mozgatással, billegő asztalon. Fontos, hogy a teljes membránt fedje az ellenanyag tartalmú oldat. (ált ml térfogat szükséges.) - Másnap mossuk a nitrocellulóz membránt 3 x 10 percig TWB Tween pufferrel. - Adjuk a nitrocellulóz membránhoz az anti-egér IgG F(ab )2-HRPO konjugátumot 3% BSA tartalmú pufferben, 8000-szeres hígításban és inkubáljuk 1 órán át szobahőmérsékleten, állandó mozgatás közben. - Mossuk a nitrocellulóz membránt 5-6x 5 percig TWB-Tween pufferrel, majd kemilumineszcencia (ECL) reagens alkalmazásával detektáljuk a tirozinon foszforilált fehérjéket. Az ECL mindkét komponenséből 1-1 ml-t keverünk össze, majd a blottot kissé leitatva, 1 percig állandóan mozgatva tartjuk a reagensben. 5
6 - 1 perc elteltével a reagens leöntése és leitatása utána a membránt helyezzük röntgenkazettába, fóliák közé, sötétkamrában tegyünk rá filmet, és 30 sec -5 perc közötti időtartamig való expozíció után hívjuk elő a filmet. Feladat: Értékeljük az előhívott Western-blotot a tirozin foszforiláció intenzitása (denzitás) szempontjából az aktiváció körülményei és az idő függvényében! 6
7 A B limfocita aktiváció jellemzői II.: a B sejt receptor internalizációja A B sejtek B sejt receptoron (BCR) keresztüli aktivációjakor hasonlóan a T sejtek TCR-en keresztüli aktivációjához - két fontos folyamat indul be. Az egyik a gyakorlaton is vizsgált foszforilációs kaszkád, a másik pedig a receptor-antigén komplex internalizálódása (más néven receptor-közvetített endocitózis), vagyis a citoplazmába kerülése. Ez utóbbi folyamat eredményeképpen megy végbe az antigén processzálása, majd az antigénből származó peptidek MHCII-molekulákon keresztüli újraprezentálása a T-sejtek felé. Az endocitózis kezdeti szakaszának vizsgálatát a gyakorlaton áramlási citofluoriméterrel végezzük. A kísérletben a BCR-aktivációt követően a sejtfelszíni BCR-molekulák mennyiségét detektáljuk, és a kapott adatokból következtetünk az idő folyamán eltűnő, azaz internalizálódott BCR-molekulák mennyiségére. A gyakorlat menete: Mintánként 5x10 5 RAMOS sejtet 500 μl szérummentes médiumban veszünk fel, FACScsövekbe rakjuk, percig inkubátorban tartjuk 37 C-on, majd 2-3 percig jégre helyezzük. Ezután anti-humán IgG+M F(ab )2 ellenanyagot 5 µg/ml végkoncentrációban adunk a megfelelő mintákhoz, a csöveket pedig 45 percig jégen hagyjuk. Ez a szinkronizációs lépés biztosítja, hogy az ellenanyag minden mintában egyformán telítse a BCR-eket. Az aktivációhoz a mintákat adott időközönként 37 C-ra (CO2-termosztát) tesszük. Az aktiválást a leghosszabb idejű mintával kezdjük, és a legrövidebbel fejezzük be, hogy az aktivációs időknek egyszerre legyen végük. Ezután a sejteket hideg FACS pufferben 2x mossuk (1ml rpm 4 C), majd anti-humán IgM-FITC ellenanyagot adunk hozzájuk (2 µl/cső), és 20 percig fénytől védve, jégen hagyjuk. A sejteket ezután 1x mossuk, majd 300 µl ml FACS pufferben felvesszük, és elvégezzük az áramlási citofluoriméteres mérést. A minták: anti-humán IgG+M Aktiváció (37 C) α-humán IgM-FITC F(ab )2 1. Ø Ø Ø 2. Ø Ø Ø Feladat: Ábrázoljuk a sejtfelszínen expresszált BCR mennyiségét melyet áramlási citometriával határoztunk meg az aktiválást követően az idő függvényében és értelmezzük a görbét. 7
8 Fas-független apoptózis indukciója T sejtekben membrán stressz révén: az apoptózis néhány szelektív markerének áramlási citometriás és konfokális mikroszkópiás vizsgálata Az apoptózis az immunrendszerben különösen gyakran fellépő programozott sejthalál folyamat, melynek révén a funkcionálisan nem megfelelő, a szervezet sejtjeire veszélyes (autoreaktív) ill. a feladatukat már ellátott, vagy arra egyáltalán nem képes sejtek eliminálódnak az immunrendszer sejtkészletéből. Ez naponta akár több száz millió sejt (nagyrészt limfociták) folyamatos elhalását jelenti. Az apoptózis során a sejtek citotoxikus anyagokat nem ürítenek a környezetükbe, szemben a nekrotikus sejthalállal (ami a sejtek lízisével jár). Az apoptotikus sejteket a makrofágok felismerik sejtfelszíni lipid (ill. fehérje) mintázataik alapján és fagocitózis útján eltávolítják őket az immunrendszerből. Az apoptózis folyamán bekövetkező DNS fragmentálódás eredményeként megjelenő csökkent mértékű propidium-jodid festődést mutató, ún. szubdiploid (apoptotikus) populáció %-os arányát áramlási citométer segítségével vizsgálhatjuk. A folyamat beindulásának több jellegzetes markere is megfigyelhető mikroszkópiásan, többek között a sejtek plazma membránjának hólyagosodása (blebbing), majd késői fázisban a DNS fragmentálódása, apoptotikus testek képződése és leválása a sejtekről, valamint a plazma membrán permeabilizálódása ( szekunder nekrózis ). Ezeket a folyamatokat a membrán lipidek (pl. GM1 gangliozid) fluoreszcens jelzésével (Alexa-488 cholera toxin B alegység), ill. a spontán módon csak a permeabilizálódott sejtek által felvett viabilitás marker festék, a propidium jodid (DNS-be interkalálódik) fluoreszcenciája alapján vizsgálhatjuk. Sejtek, anyagok, eszközök: IP12-7 egér TH-hibridoma sejtek (2.5x10 5 /ml, RPMI komplett médiumban) RPMI komplett médium propidium-jodid törzsoldat (1 mg/ml) VIGYÁZAT, MUTAGÉN HATÁSÚ!!! PBS pufferoldat hipotóniás DNS-extraháló/festő oldat: 0.1 % Na-citrát, 0.1 % Triton X-100, 50 µg/ml propidium-jodid steril csövek; 24-lyukú sejttenyésztő lemez; 5 ml-es FACS csövek 5 μl (40 μg/ml törzsoldatból) Alexa488-cholera toxin B oldattal Metodika A: Az IP12-7 T sejteket RPMI médiumban inkubálunk (5x10 5 sejt/ml) apoptózis indukció céljából (37 C-on, CO2 termosztátban) 24 lyukú mikroplateben, kb. 24 órán át, 0, 12.5, 25 és 50 µm C2 ceramiddal, ami a sejthalál receptor (Fas) független apoptózis jelátvitel egyik mediátora. Az apoptotikusan indukált sejteket centrifugáljuk és mossuk hideg PBS-ben. A sejteket 5 ml-es FACS csövekbe pipettázzuk, PBS-sel egyszer mossuk (1200 rpm, 8 min), majd a fellazított sejtpelletre 500 µl propidium-jodid tartalmú DNS-extraháló/festő oldatot mérünk (KESZTYŰ AJÁNLATOS!!!), majd a mintákat +4 o C-on 3-4 óráig inkubáljuk, óránként felszuszpendálva (vortex). Áramlási citométeren mérjük a propidium-jodid fluoreszcencia intenzitását (gerjesztés 488 nm-en Ar + -lézerrel, detektálás a vörös (FL3) csatornában). Meghatározzuk az apoptotikus (DNS fragmentáción átesett, szubdiploid) sejtek százalékát, marker jel alkalmazásával 8
9 Metodika B: Az IP12-7 T sejteket RPMI médiumban inkubálunk (5x10 5 sejt/ml) apoptózis indukció céljából (37 C-on, CO2 termosztátban) 24 lyukú mikroplateben, kb. 24 órán át, 0, 12.5, 25 és 50 µm C2 ceramiddal, ami a sejthalál receptor (Fas) független apoptózis jelátvitel egyik mediátora. Az apoptotikusan indukált sejteket centrifugáljuk és mossuk hideg PBS-ben, majd festjük a sejt pelletet 5 μl (40 μg/ml törzsoldatból) Alexa-488 cholera toxin B oldattal, 5 percig 37 C-os vízfürdőben vagy 20 percig jégen, mindkét esetben letakarva, hogy fény ne érje. A sejteket mossuk 2 x hideg PBS-ben, majd hideg médiumban felszuszpendáljuk (kb. 500 μl) és közvetlenül mérés előtt 1 μl propidium jodid törzsoldatot (1 mg/ml) adunk hozzá a DNS festése céljából. Feladat: A membrán és DNS festett apoptotikus T sejtmintáról felvett CLSM képek elemzése. A mintában várhatóan találhatók ép sejtek (folytonos, gyűrűszerű membránfestés), ill. olyan sejtek melyekben már beindult az apoptózis, ill. a kb. 20 órás inkubáció alatt már el is jutott a DNS fragmentáció fázisába. Így a vörös színű magfestés alapján ezen sejtek egymás mellett jól értékelhetőek. A membrán festés alapján a membrán permeabilizálódása/propidium jodid pozitivitás, folytonossági hiányok, valamint a gyengébb vagy nem észlelhető festődés alapján a késői apoptózis/szekunder nekrózis azonosítható. A fragmentáció a DNS-t festő propidium jodid foltos intracelluláris festődése alapján deteketálható, szemben a még nem fragmentálódott sejtmagok homogén vörös festődésével.) A bleb -ek (hólyagok) képződése a morfológiai (DIC) kép alapján detektálható és jelzi a korai apoptotikus sejteket. 9
10 B-limfociták aktiválása a B-sejt receptoron keresztül anti-humán IgG+M F(ab )2 ellenanyaggal: az intracelluláris Ca 2+ válasz áramlási citometria segítségével. Sejtek, anyagok, eszközök: RAMOS humán IgM+ B-sejtvonal RPMI 1640 komplett médium GKN-oldat (NaCl, glükóz és fenolvörös tartalmú fiziológiás foszfátpuffer) tripánkék festék Anti-humán IgG+M F(ab )2 kecskében termelt poliklonális ellenanyag Fluo-4 AM törzsoldata (1 mg/ml), Pluronic F-127 tartalmú DMSO-ban oldva propidium-jodid törzsoldat (1 mg/ml) VIGYÁZAT, MUTAGÉN HATÁSÚ!!! Ionomycin (1 mg/ml) steril csövek; 5 ml-es FACS csövek Feladat: Aktiváljuk a B sejteket BCR-en keresztül anti-humán IgG+M ellenanyaggal. Alkalmazzunk egyre növekvő dózist a stimulálásra: 0, 1, 2,5 5, 10 µg/ml végkoncentrációk(!). Mérjük meg a kontroll (kezeletlen) és a kezelt sejtek intracelluláris Ca2+-szintjét (mérés: az FL1 csatornában, idő függvényében, 6 percig; halott sejtek negatívan kikapuzva PI DNS-festék segítségével (PI-pozitív sejtek az FL3 csatornában). Ábrázoljuk a görbék maximumát az anti- IgG+M dózis függvényében. Metodika: 1. A sejtek feltöltése Fluo-4 AM Ca2+-szenzitív fluoreszcens festékkel: 5x10 6 sejtet 0,5 ml médiumban felveszünk és 5 µl Fluo-4 AM festék hozzáadását követően 30 percig 37 oc-os vízfürdőben enyhe rázatás mellett inkubálunk. Ezután médiummal 10 ml-re egészítjük ki a sejtszuszpenzió térfogatát, és további 30 percig inkubáljuk 37 C-os vízfürdőben. Egyszeri hideg GKN-nel történő mosás után a sejteket 4 ml hideg médiumban vesszük fel, majd 0,5 ml-enként FACS méréshez használatos csövekbe mérjük és jégre helyezzük. 2. Az 5 perces 37 C-on való előmelegítés után a 0,5 ml sejtszuszpenzióhoz 1 µl propidiumjodid törzsoldatot adunk a halott sejtek mérés során való elkülöníthetősége érdekében. 3. A 0,5 ml térfogatú előmelegített sejtszuszpenziókhoz az alapjel (kb. 30 sec) regisztrálása után pipettázzunk anti-igg+m-t, hogy annak a végkoncentrációja rendre 0, 1, 2,5, 5 és 10 µg/ml legyen, majd folytassuk a Ca 2+ jel regisztrálását sec-os alapjel felvétele után 2 µl ionomycin (ionofór vegyület) hozzáadásával mérjük meg B-sejtek maximális Ca 2+ -jelét. 10
11 Molekuláris kolokalizáció (pl. MHCII glikoprotein és GM1 gangliozid raft lipid között) kimutatása A20 egér B limfóma (APC) sejtek membránjában konfokális lézerpásztázó mikroszkópiával (CLSM). Bevezetés, elméleti háttér: Receptorok, membránfehérjék kolokalizációjának analízise konfokális fluoreszcens mikroszkópiával A receptorok és egyéb membránfehérjék sejtfelszíni eloszlása gyakran informatív az aktivációs folyamatokhoz kötött un. aktivációs fehérje clusterek (több tíz-száz fehérje molekula csoportosulása) ill. funkcionális membrán mikrodomének kialakulása szempontjából. Ezeket a molekulacsoportosulásokat, ill. tetszőleges membránfehérjék előfordulását bennük, a konfokális fluoreszcens mikroszkópia segítségével is vizsgálhatjuk, természetesen az optikai mikroszkópia térbeli feloldási korlátai (min. 250 nm) mellett. Ez azt jelenti, hogy csak ilyen vagy az ennél nagyobb méretű clusterek/mikrodomének feloldására van lehetőség, a clustereken belüli molekuláris kapcsolatokat ezeken képeken közvetlenül nem tudjuk feloldani. A konfokális mikroszkóp tulajdonképpen a tárgylemezen elhelyezett, immuncitokémiai úton fluoreszcensen jelzett sejteken egy függőleges z irányú optikai szeletelést végez (az immunrendszer különféle sejtjeinél a vastagság, azaz a z irányú kiterjedés kb.1030 mikrométer, egy szelet tipikus vastagsága 200 nm, de ez tetszés szerint változtatható), azaz több fókuszsíkból gyűjt be információt a szelet x,y irányú, pontszerű lézersugárral történő pásztázásával, miközben az éppen pásztázott síkon kívüli térrészből érkező fluoreszcens fényt (háttérzaj) optikai úton (pontszerű rés, pinhole a detektor előtt) kiszűri. Az így előállt optikai szelet képek számítógép segítségével 3 dimenziós kép formájában rekonstruálhatók. Ez a vizsgálati módszer előnyösen alkalmazható teszőleges sejtfelszíni (vagy akár intracelluláris) fehérje lokalizálására, kolokalizására más fehérjékkel (vagy intracelluláris organellumokkal), ill. membrán mikrodoménekkel (pl. caveola, lipid raft). A módszer alkalmazását itt az MHCII molekula lipid raftokkal (marker: GM1 gangliozid, fluoreszcens cholera toxin B-vel jelölve) való kolokalizációjának demonstrálásán keresztül mutatjuk be, de bármely két tetszőleges fehérje között is hasonló módon végezhető el a vizsgálat. Anyagok, Reagensek, Eszközök: a vizsgálni kívánt sejt/sejtvonal szuszpenzióban izotóniás, foszfátpufferelt sóoldat (PBS, ph: 7.4) fluoreszcens festékkel konjugált monoklonális ellenanyag (FmAb) a vizsgálni kívánt fehérje ellen fluoreszcens festékkel konjugált cholera toxin B (40 μg/ml, frissen hígitva 1 mg/ml törzsoldatból, mely utóbbi aliquotjai 200Con 6 hónapig tárolhatók) Fc receptort expresszáló sejtek esetén Fc receptor blokkolására alkalmas ellenanyag vagy Fc preparátum 50 ml-es Falcon cső, 1.5 ml-es Eppendorf csövek hűthető centrifuga 4 vagy 8 osztatú microplate, amely alkalmas a mikroszkópra felszerelt hőmérséklet és CO 2 szabályozó egység használatára 10µg/ml fibronectin a microplate-ek felszínének bevonására inverz fluoreszcens mikroszkóp konfokális pásztázó egységgel és megfelelő hullámhosszakra érzékeny fotomultiplier detektorokkal ellátva 11
12 lézer fényforrások (488 nm Argon, 543 nm HeNe-Green és 632nm HeNe-Red lézer) és megfelelő szűrőkockák (dichroikus tükör/ emissziós szűrő kombináció) a kétféle fluoreszcencia detektálására A digitális képek felvételére és kiértékelésére alkalmas szoftver Zeiss LSM5/Axiovert 200, Olympus Fluoview 300/500/IX81. A módszer leírása: A sejteket megszámoljuk, és mintánként 5x10 5 sejt/ml koncentrációt állítunk be, 1.5 ml-es Eppendorf csövekben, majd lecentrifugáljuk (1300g, 7 perc, 4 C). A sejtpellethez megfelelő (telítési) mennyiségű fluoreszcens ellenanyagot (pl. FITC anti MHCII) és egyidejűleg 5 μl Alexa-647 cholera toxin B-t adunk, majd összekeverést követően, jégen 20 percig inkubáljuk. A jelölést követően a sejteket saját médiumban 2x mossuk. A kettősen jelölt sejtmintát 4% formaldehiddel fixáljuk (szobahőmérsékleten, kb. 20 perc), majd a fibronectinnel előkezelt (ON, szobahőn) microplate lyukaiba pipettázzuk. A microplate-et a hőmérséklet és CO2 szabályozó készülékbe majd a konfokális mikroszkóp tárgyasztalára helyezzük. A konfokális mikroszkópban a minta fluoreszcens képe alapján megkeressük a lemezzel érintkező ún. fenék síkot (csökkenés után éppen eltűnő fluoreszcencia), majd felfelé lépegetve a tetősíkot, és meghatározzuk, hogy milyen szeletvastagságot kívánunk beállítani. Erre a kb. 200 nm érték javasolt. Ezután a mikroszkóp automatikusan pásztázza a kijelölt síkokat, ill. összeállítja a síkokból a 3D rekonstrukciót. A kettősen jelzett sejtek fluoreszcens képét regisztráljuk a mikroszkóp optikai csatornáiban, digitális formában, az előző pontban említett módon. (A festékek esetleges spektrális áthallásának ellenőrzésére a felvételeket szekvenciális üzemmódban készítsük.) Célszerű ezen mérésekhez nagy numerikus appertúrájú, immerziós olajos objektívet (60 x nagyítás) alkalmazni. Vizsgáljuk a kolokalizáció mértékét a két optikai csatornában felvett képek pixelhelyes fedésbe hozásával /overlay/ vizuálisan (pl. zöld és vörös szín esetén az adott pixelben történő együttes előfordulás esetén narancssárga szín észlelhető). A kolokalizáció mértéke kvantitatívan is értékelhető, a két képen kijelölt, adott koordinátájú pixelben megjelenő, a detektálási küszöböt meghaladó zöld ill. vörös fluoreszcencia intenzitásának keresztkorreláció analízisével (pl. Image J (NIH, USA) szoftver, vagy az adott mikroszkóp kolokalizációs index értékelő programja). A módszer kritikus pontjai Célszerű a vizsgált fehérjékre nézve specifikus, keresztreakciót nem mutató, monoklonális antitestek használata. Fontos az ellenanyaggal való jelöléseket hidegen végezni, ill. a sejtek azonnali fixálása, az antitest internalizáció minimalizálása céljából. Fontos olyan festékek választása, melyek emissziós spektrumai jól elkülönülnek egymástól (nincs áthallás egymás optikai csatornáiba). A kiértékelést (ld. alább) szokásos ekvatoriális optikai szeleten (a sejt középmagasságában) is elvégezni, de célszerűbb a kétféle szín (szomszédos, szeleten belüli síkokból történő) véletlenszerű egymásravetülését kiküszöbölendő egy a sejt felszínéhez közeleső szeleten (is) elvégezni azt. Az eredmények értékelése A két, spektrálisan izolált, csatornában (pl. zöld:x,vörös:y) a kettősen jelölt sejtmintáról digitálisan rögzített képek esetén a kolokalizációt a keresztkorrelációs koefficiens (C) értéke alapján kvantitatívan is megítélhetjük. A koefficiens definíciója C = Σ i Σ j (x i,j - <x>) (y i,j - <y>) / Σ i Σ j (x i,j - <x>) 2 Σ i Σ j (y i,j - <y>) 2, ahol x i,j ill. y i,j az i és j koordinátákkal jellemzett pixel fluoreszcencia értékei az x (zöld) ill. y (vörös) képen. A kiértékeléskor csak a detektálási küszöb fölötti értékekkel rendelkező pixeleket vesszük figyelembe a summázás során. A C elméleti 12
13 felső értéke 1, ami két teljesen azonos kép esetén adódik, míg a 0 ill. ahhoz közeli érték a kétféle festék (jelölt molekula) szeparált lokalizációjára utal. A módszer alkalmazási lehetőségei A módszer alkalmas az immunrendszer legtöbb sejtje (pl. T, B limfociták, hízósejtek, makrofágok) esetén két tetszőleges sejtmembránban expresszált fehérje (vagy lipid) kolokalizációjának vizsgálatára pixelenként. A módszer 10 4 fehérje/sejt expresszió alatt korlátozottan alkalmazható az esetleges alacsony fluoreszcencia jelszint miatt. Kísérlet: A20 egér B sejteket anti-mhcii (IA) ellenanyaggal jelöljük a fentiekben leírt módon, egyidejűleg a fluoreszcens cholera toxin B-vel, mely utóbbi a plazma membrán GM1 gangliozidok (raft marker lipid) jelölésére szolgál. A sejteket a jelölés után fixáljuk, majd a sejtkamra lyukaiba cseppentjük. Konfokális mikroszkóp két szeparált optikai csatornájában (zöld és vörös fluoreszcencia) vizsgáljuk a sejtek fluoreszcencia képét ( ekvatoriális, tető és fenék szelet fókuszsíkok), majd a leírt módon pixelenként értékeljük a kétféle fluoreszcencia együttes előfordulását. Megjegyzés: A kolokalizáció magas foka nem jelent bizonyítékot a kétféle molekula fizikai asszociáciációjára/kölcsönhatására (ez csak a fluoreszcencia rezonancia energia transzfer /FRET/ technikával vizsgálható megbízhatóan), pusztán azt jelzi, hogy a két molekula milyen mértékben fordul együttesen elő egy pixel méretnyi térelemben (min. 0.1 x 0.1 mikrométernyi terület, amely a membrán raft mikrodomének mérettartományával összemérhető). 13
Immunhisztokémiai módszerek
 Immunhisztokémiai módszerek Fixálás I. Fixálás I. A szövet eredeti szerkezetének megőrzéséhez, az enzimatikus lebontó folyamatok gátlásához: fixálószerek! kompromisszumkeresés - alkoholok: vízelvonók!!!
Immunhisztokémiai módszerek Fixálás I. Fixálás I. A szövet eredeti szerkezetének megőrzéséhez, az enzimatikus lebontó folyamatok gátlásához: fixálószerek! kompromisszumkeresés - alkoholok: vízelvonók!!!
INTERFERONI GAMMA-1B SOLUTIO CONCENTRATA. Tömény gamma-1b-interferon-oldat
 01/2008:1440 javított 7.0 INTERFERONI GAMMA-1B SOLUTIO CONCENTRATA Tömény gamma-1b-interferon-oldat C 734 H 1166 N 204 O 216 S 5 M r 16 465 DEFINÍCIÓ A tömény gamma-1b-interferon-oldat a gamma interferon
01/2008:1440 javított 7.0 INTERFERONI GAMMA-1B SOLUTIO CONCENTRATA Tömény gamma-1b-interferon-oldat C 734 H 1166 N 204 O 216 S 5 M r 16 465 DEFINÍCIÓ A tömény gamma-1b-interferon-oldat a gamma interferon
POSEIDON DNS PRÓBÁK. Felhasználói Kézikönyv. Használati útmutató. Használati útmutató
 POSEIDON DNS PRÓBÁK Felhasználói Kézikönyv Használati útmutató Használati útmutató A Poseidon fluoreszcensen jelölt próbáinak használata A fluoreszcens in situ hibridizáció (FISH) genomi célszekvenciákat
POSEIDON DNS PRÓBÁK Felhasználói Kézikönyv Használati útmutató Használati útmutató A Poseidon fluoreszcensen jelölt próbáinak használata A fluoreszcens in situ hibridizáció (FISH) genomi célszekvenciákat
PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM. Humán plazma, kevert, vírus-inaktiválás céljából kezelt
 conditumque ad exstinguendum virum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1646 PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM Humán plazma, kevert, vírus-inaktiválás céljából kezelt DEFINÍCIÓ
conditumque ad exstinguendum virum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:1646 PLASMA HUMANUM COAGMENTATUM CONDITUMQUE AD EXSTIGUENDUM VIRUM Humán plazma, kevert, vírus-inaktiválás céljából kezelt DEFINÍCIÓ
 PÉCSI TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNYI KAR Áramlási citometria, sejtszeparálás ÁRAMLÁSI CITOMETRIA, SEJTSZEPARÁLÁS BIOFIZIKA 2. 2015. március 3. Dr. Bugyi Beáta Biofizikai Intézet ÁRAMLÁSI folyadékáramban
PÉCSI TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNYI KAR Áramlási citometria, sejtszeparálás ÁRAMLÁSI CITOMETRIA, SEJTSZEPARÁLÁS BIOFIZIKA 2. 2015. március 3. Dr. Bugyi Beáta Biofizikai Intézet ÁRAMLÁSI folyadékáramban
Sejttenyésztési alapismeretek
 Sejttenyésztési alapismeretek 1. Bevezetés A sejteknek ún. sejtkultúrákban történő tenyésztése (a sejteket az eredeti helyükről eltávolítva in vitro tartjuk fenn ill. szaporítjuk) és tanulmányozása több
Sejttenyésztési alapismeretek 1. Bevezetés A sejteknek ún. sejtkultúrákban történő tenyésztése (a sejteket az eredeti helyükről eltávolítva in vitro tartjuk fenn ill. szaporítjuk) és tanulmányozása több
Egyetemi doktori (PhD) értekezés tézisei
 Egyetemi doktori (PhD) értekezés tézisei A HUMÁN PLAZMAPROTEOMOT REPREZENTÁLÓ ANALITKÖNYVTÁR LÉTREHOZÁSA, JELLEMZÉSE ÉS FELHASZNÁLÁSA MONOKLONÁLIS ANTITESTEK ANTIGÉNJEINEK AZONOSÍTÁSÁRA Kovács András Témavezető:
Egyetemi doktori (PhD) értekezés tézisei A HUMÁN PLAZMAPROTEOMOT REPREZENTÁLÓ ANALITKÖNYVTÁR LÉTREHOZÁSA, JELLEMZÉSE ÉS FELHASZNÁLÁSA MONOKLONÁLIS ANTITESTEK ANTIGÉNJEINEK AZONOSÍTÁSÁRA Kovács András Témavezető:
Kis molekulás NADPH-oxidáz 4 inhibitorok azonosítása és karakterizálása az oxidatív stressz kivédésére
 Kis molekulás NADPH-oxidáz 4 inhibitorok azonosítása és karakterizálása az oxidatív stressz kivédésére Doktori tézisek Borbély Gábor Semmelweis Egyetem Gyógyszertudományok Doktori Iskola Témavezető: Dr.
Kis molekulás NADPH-oxidáz 4 inhibitorok azonosítása és karakterizálása az oxidatív stressz kivédésére Doktori tézisek Borbély Gábor Semmelweis Egyetem Gyógyszertudományok Doktori Iskola Témavezető: Dr.
HEPARINA MASSAE MOLECULARIS MINORIS. Kis molekulatömegű heparinok
 01/2014:0828 HEPARINA MASSAE MOLECULARIS MINORIS Kis molekulatömegű heparinok DEFINÍCIÓ A kis molekulatömegű heparinok olyan, 8000-nél kisebb átlagos relatív molekulatömegű szulfatált glükózaminoglikánok
01/2014:0828 HEPARINA MASSAE MOLECULARIS MINORIS Kis molekulatömegű heparinok DEFINÍCIÓ A kis molekulatömegű heparinok olyan, 8000-nél kisebb átlagos relatív molekulatömegű szulfatált glükózaminoglikánok
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 7. előadás Immunizálás. Poliklonális és monoklonális ellenanyag előállítása, tisztítása, alkalmazása Az antigén (haptén + hordozó) sokféle specificitású ellenanyag
Immunológiai módszerek a klinikai kutatásban 7. előadás Immunizálás. Poliklonális és monoklonális ellenanyag előállítása, tisztítása, alkalmazása Az antigén (haptén + hordozó) sokféle specificitású ellenanyag
2.6.17. IMMUNGLOBULIN ANTIKOMPLEMENT- AKTIVITÁSÁNAK VIZSGÁLATA
 vizsgálata Ph.Hg.VIII. - Ph.Eur.6.6 1 2.6.17. IMMUNGLOBULIN ANTIKOMPLEMENT- AKTIVITÁSÁNAK VIZSGÁLATA Az immunglobulin antikomplement-aktivitásának (ACA) méréséhez meghatározott mennyiségű vizsgálati anyagot
vizsgálata Ph.Hg.VIII. - Ph.Eur.6.6 1 2.6.17. IMMUNGLOBULIN ANTIKOMPLEMENT- AKTIVITÁSÁNAK VIZSGÁLATA Az immunglobulin antikomplement-aktivitásának (ACA) méréséhez meghatározott mennyiségű vizsgálati anyagot
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
BIOKÉMIA GYAKORLATI JEGYZET
 BIOKÉMIA GYAKORLATI JEGYZET ELTE Biokémiai Tanszék összeállította: Tanszéki munkaközösség többszörösen javított kiadás: 2010 1. gyakorlat 1. gyakorlat SPEKTROFOTOMETRIA FEHÉRJEKONCENTRÁCIÓ MÉRÉSE A. Fotometria
BIOKÉMIA GYAKORLATI JEGYZET ELTE Biokémiai Tanszék összeállította: Tanszéki munkaközösség többszörösen javított kiadás: 2010 1. gyakorlat 1. gyakorlat SPEKTROFOTOMETRIA FEHÉRJEKONCENTRÁCIÓ MÉRÉSE A. Fotometria
HYPROMELLOSUM. Hipromellóz
 Hypromellosum Ph.Hg.VIII. Ph.Eur. 8.0-1 01/2014:0348 [9004-65-3] HYPROMELLOSUM Hipromellóz DEFINÍCIÓ Hidroxipropilmetilcellulóz. Cellulóz, 2-hidroxipropilmetiléter. Részlegesen O-metilezett és O-(2-hidroxipropilezett)
Hypromellosum Ph.Hg.VIII. Ph.Eur. 8.0-1 01/2014:0348 [9004-65-3] HYPROMELLOSUM Hipromellóz DEFINÍCIÓ Hidroxipropilmetilcellulóz. Cellulóz, 2-hidroxipropilmetiléter. Részlegesen O-metilezett és O-(2-hidroxipropilezett)
3.1.14. VIZES INFÚZIÓS OLDATOK TARTÁLYAINAK ELŐÁLLÍTÁSÁHOZ HASZNÁLT LÁGYÍTOTT POLI(VINIL- KLORID)-ALAPÚ ANYAGOK
 3.1.14. Vizes infúziós oldatok tartályainak előállításához Ph.Hg.VIII. Ph.Eur.7.5-1 01/2008:30114 javított 7.5 3.1.14. VIZES INFÚZIÓS OLDATOK TARTÁLYAINAK ELŐÁLLÍTÁSÁHOZ HASZNÁLT LÁGYÍTOTT POLI(VINIL-
3.1.14. Vizes infúziós oldatok tartályainak előállításához Ph.Hg.VIII. Ph.Eur.7.5-1 01/2008:30114 javított 7.5 3.1.14. VIZES INFÚZIÓS OLDATOK TARTÁLYAINAK ELŐÁLLÍTÁSÁHOZ HASZNÁLT LÁGYÍTOTT POLI(VINIL-
Virológia gyakorlatok
 Virológia gyakorlatok A virológia gyakorlatok célja, hogy a hallgatók betekintést nyerhessenek az állatorvosi virológiai diagnosztika különböző módszereibe. A hallgatók a gyakorlatokon esetfeldolgozás
Virológia gyakorlatok A virológia gyakorlatok célja, hogy a hallgatók betekintést nyerhessenek az állatorvosi virológiai diagnosztika különböző módszereibe. A hallgatók a gyakorlatokon esetfeldolgozás
APROTININUM. Aprotinin
 Aprotinin Ph.Hg.VIII. Ph.Eur.6.3-1 APROTININUM Aprotinin 01/2009:0580 javított 6.3 C 284 H 432 N 84 O 79 S 7 M R 6511 DEFINÍCIÓ Az aprotinin 58 aminosavból álló polipeptid, mely sztöchiometrikus arányban
Aprotinin Ph.Hg.VIII. Ph.Eur.6.3-1 APROTININUM Aprotinin 01/2009:0580 javított 6.3 C 284 H 432 N 84 O 79 S 7 M R 6511 DEFINÍCIÓ Az aprotinin 58 aminosavból álló polipeptid, mely sztöchiometrikus arányban
LACTULOSUM LIQUIDUM. Laktulóz-szirup
 Lactulosum liquidum Ph.Hg.VIII. Ph.Eur.7.7-1 04/2013:0924 LACTULOSUM LIQUIDUM Laktulóz-szirup DEFINÍCIÓ A laktulóz-szirup a 4-O-(β-D-galaktopiranozil)-D-arabino-hex-2-ulofuranóz vizes oldata, amelyet általában
Lactulosum liquidum Ph.Hg.VIII. Ph.Eur.7.7-1 04/2013:0924 LACTULOSUM LIQUIDUM Laktulóz-szirup DEFINÍCIÓ A laktulóz-szirup a 4-O-(β-D-galaktopiranozil)-D-arabino-hex-2-ulofuranóz vizes oldata, amelyet általában
A basidiomycota élesztőgomba, a Filobasidium capsuligenum IFM 40078 törzse egy olyan
 A basidiomycota élesztőgomba, a Filobasidium capsuligenum IFM 40078 törzse egy olyan fehérjét (FC-1 killer toxint) választ ki a tápközegbe, amely elpusztítja az opportunista patogén Cryptococcus neoformans-t.
A basidiomycota élesztőgomba, a Filobasidium capsuligenum IFM 40078 törzse egy olyan fehérjét (FC-1 killer toxint) választ ki a tápközegbe, amely elpusztítja az opportunista patogén Cryptococcus neoformans-t.
Az Oxidatív stressz hatása a PIBF receptor alegységek összeszerelődésére.
 Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
Újabban világossá vált, hogy a Progesterone-induced blocking factor (PIBF) amely a progesteron számos immunológiai hatását közvetíti, nem csupán a lymphocytákban és terhességgel asszociált szövetekben,
ADEPS LANAE. Gyapjúviasz
 Adeps lanae Ph.Hg.VIII. Ph.Eur.7.4-1 04/2012:0134 ADEPS LANAE Gyapjúviasz DEFINÍCIÓ Juhok (Ovis aries) gyapjából nyert, tisztított, vízmentes, viasszerű anyag. Megfelelő antioxidánst tartalmazhat. SAJÁTSÁGOK
Adeps lanae Ph.Hg.VIII. Ph.Eur.7.4-1 04/2012:0134 ADEPS LANAE Gyapjúviasz DEFINÍCIÓ Juhok (Ovis aries) gyapjából nyert, tisztított, vízmentes, viasszerű anyag. Megfelelő antioxidánst tartalmazhat. SAJÁTSÁGOK
Konfokális mikroszkópia elméleti bevezetõ
 Konfokális mikroszkópia elméleti bevezetõ A konfokális mikroszkóp fluoreszcensen jelölt minták vizsgálatára alkalmas. Jobb felbontású képeket ad, mint a hagyományos fluoreszcens mikroszkópok, és képes
Konfokális mikroszkópia elméleti bevezetõ A konfokális mikroszkóp fluoreszcensen jelölt minták vizsgálatára alkalmas. Jobb felbontású képeket ad, mint a hagyományos fluoreszcens mikroszkópok, és képes
ANTICANCER RESEARCH [Rákkutatás]
![ANTICANCER RESEARCH [Rákkutatás] ANTICANCER RESEARCH [Rákkutatás]](/thumbs/39/19250750.jpg) ANTICANCER RESEARCH [Rákkutatás] Nemzetközi rákkutatási és rákgyógyászati folyóirat Az MGN-3/Biobran rizskorpából kivont módosított arabinoxilán in vitro növeli a metasztatikus emlőráksejtek érzékenységét
ANTICANCER RESEARCH [Rákkutatás] Nemzetközi rákkutatási és rákgyógyászati folyóirat Az MGN-3/Biobran rizskorpából kivont módosított arabinoxilán in vitro növeli a metasztatikus emlőráksejtek érzékenységét
A sejtmembrán molekuláris szerveződése, membrán mikrodomének
 A sejtmembrán molekuláris szerveződése, membrán mikrodomének A sejtmembrán molekuláris szerveződése A membránfehérjék globális szerkezete és kapcsolódása a lipid kettősréteghez: Ext. 1 2 8 3 GPI 4 membrán
A sejtmembrán molekuláris szerveződése, membrán mikrodomének A sejtmembrán molekuláris szerveződése A membránfehérjék globális szerkezete és kapcsolódása a lipid kettősréteghez: Ext. 1 2 8 3 GPI 4 membrán
Kalcium szabályozta sejtosztódás és túlélés vizsgálata mieloeritroid
 Kalcium szabályozta sejtosztódás és túlélés vizsgálata mieloeritroid sejtekben Doktori (Ph.D.) értekezés Jánossy Judit, Okleveles Biológus EÖTVÖS LORÁND TUDOMÁNY EGYETEM, TERMÉSZETTUDOMÁNY KAR Biológia
Kalcium szabályozta sejtosztódás és túlélés vizsgálata mieloeritroid sejtekben Doktori (Ph.D.) értekezés Jánossy Judit, Okleveles Biológus EÖTVÖS LORÁND TUDOMÁNY EGYETEM, TERMÉSZETTUDOMÁNY KAR Biológia
Immunhisztokémia: Előhívó rendszerek, problémák és megoldások
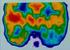 Immunhisztokémia: Előhívó rendszerek, problémák és megoldások Dr. Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet Budapest Patológus Klasszikus patomorfológia Klinikai
Immunhisztokémia: Előhívó rendszerek, problémák és megoldások Dr. Krenács Tibor Semmelweis Egyetem I.sz. Patológiai és Kísérleti Rákkutató Intézet Budapest Patológus Klasszikus patomorfológia Klinikai
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai
 Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
Az áramlási citométer és sejtszorter felépítése és működése, diagnosztikai alkalmazásai Az áramlási citométer és sejtszorter felépítése és működése Kereskedelmi forgalomban kapható készülékek 1 Fogalmak
Az AT 1A -angiotenzinreceptor G-fehérjétől független jelátvitelének vizsgálata C9 sejtekben. Doktori tézisek. Dr. Szidonya László
 Az AT 1A -angiotenzinreceptor G-fehérjétől független jelátvitelének vizsgálata C9 sejtekben Doktori tézisek Dr. Szidonya László Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető:
Az AT 1A -angiotenzinreceptor G-fehérjétől független jelátvitelének vizsgálata C9 sejtekben Doktori tézisek Dr. Szidonya László Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola Témavezető:
Áramlási citometria 2011. / 4. Immunológiai és Biotechnológiai Intézet PTE KK
 Áramlási citometria 2011. / 4 Immunológiai és Biotechnológiai Intézet PTE KK Az áramlási citometria elve Az áramlási citometria ( Flow cytometria ) sejtek gyors, multiparaméteres vizsgálatára alkalmas
Áramlási citometria 2011. / 4 Immunológiai és Biotechnológiai Intézet PTE KK Az áramlási citometria elve Az áramlási citometria ( Flow cytometria ) sejtek gyors, multiparaméteres vizsgálatára alkalmas
ZINCI ACEXAMAS. Cink-acexamát
 Zinci acexamas Ph.Hg.VIII. Ph.Eur.6.8-1 07/2010:1279 ZINCI ACEXAMAS Cink-acexamát C 16 H 28 N 2 O 6 Zn M r 409,8 [70020-71-2] DEFINÍCIÓ Cink-bisz[6-(acetilamino)hexanoát]. Tartalom: 97,5 101,0% (szárított
Zinci acexamas Ph.Hg.VIII. Ph.Eur.6.8-1 07/2010:1279 ZINCI ACEXAMAS Cink-acexamát C 16 H 28 N 2 O 6 Zn M r 409,8 [70020-71-2] DEFINÍCIÓ Cink-bisz[6-(acetilamino)hexanoát]. Tartalom: 97,5 101,0% (szárított
SUCRALFATUM. Szukralfát
 01/2011:1796 SUCRALFATUM Szukralfát C 12 H 30 Al 8 O 51 S 8 [Al(OH) 3 ] n [H 2 O] n' ahol n = 8 10 és n' = 22 31. DEFINÍCIÓ β-d-fruktofuranozil-α-d-glükopiranozid-oktakisz(dihidroxi-alumínium-szulfát)
01/2011:1796 SUCRALFATUM Szukralfát C 12 H 30 Al 8 O 51 S 8 [Al(OH) 3 ] n [H 2 O] n' ahol n = 8 10 és n' = 22 31. DEFINÍCIÓ β-d-fruktofuranozil-α-d-glükopiranozid-oktakisz(dihidroxi-alumínium-szulfát)
XANTHANI GUMMI. Xantán gumi
 Xanthani gummi Ph.Hg.VIII. Ph.Eur.6.4-1 [11138-66-2] DEFINÍCIÓ XANTHANI GUMMI Xantán gumi 04/2009:1277 A xantán gumi nagy molekulatömegű anionos poliszacharid, melyet szénhidrátok Xanthomonas campestris-szel
Xanthani gummi Ph.Hg.VIII. Ph.Eur.6.4-1 [11138-66-2] DEFINÍCIÓ XANTHANI GUMMI Xantán gumi 04/2009:1277 A xantán gumi nagy molekulatömegű anionos poliszacharid, melyet szénhidrátok Xanthomonas campestris-szel
Gyors DNS alapú mangalica specifikus kimutatási rendszer kidolgozás a MANGFIELD projekt keretében
 Gyors DNS alapú mangalica specifikus kimutatási rendszer kidolgozás a MANGFIELD projekt keretében SZÁNTÓ-EGÉSZ RÉKA 1, MOHR ANITA 1, SIPOS RITA 1, MICSINAI ADRIENN 1, KOPPÁNYNÉ SZABÓ ERIKA 2, JÁNOSI ANNA
Gyors DNS alapú mangalica specifikus kimutatási rendszer kidolgozás a MANGFIELD projekt keretében SZÁNTÓ-EGÉSZ RÉKA 1, MOHR ANITA 1, SIPOS RITA 1, MICSINAI ADRIENN 1, KOPPÁNYNÉ SZABÓ ERIKA 2, JÁNOSI ANNA
EGYETEMI DOKTORI (PhD) ÉRTEKEZÉS
 EGYETEMI DOKTORI (PhD) ÉRTEKEZÉS AZ ILLEGÁLIS FORRÁSOKBÓL SZÁRMAZÓ TÖMÉNY SZESZESITALOKBAN ELŐFORDULÓ ALIFÁS ALKOHOLOK HATÁSA GRANULOCITÁK ÉS MONOCITÁK FUNKCIONÁLIS ÁLLAPOTÁRA PÁL LÁSZLÓ TÉMAVEZETŐ: DR.
EGYETEMI DOKTORI (PhD) ÉRTEKEZÉS AZ ILLEGÁLIS FORRÁSOKBÓL SZÁRMAZÓ TÖMÉNY SZESZESITALOKBAN ELŐFORDULÓ ALIFÁS ALKOHOLOK HATÁSA GRANULOCITÁK ÉS MONOCITÁK FUNKCIONÁLIS ÁLLAPOTÁRA PÁL LÁSZLÓ TÉMAVEZETŐ: DR.
TÚLÉRZÉKENYSÉGI I. TÍPUSÚ TÚLÉRZÉKENYSÉGI REAKCIÓ 2013.04.21. A szenzitizáció folyamata TÚLÉRZÉKENYSÉGI REAKCIÓK ÁTTEKINTÉSE TÚLÉRZÉKENYSÉGI REAKCIÓK
 TÚLÉRZÉKENYSÉGI REAKCIÓK TÚLÉRZÉKENYSÉGI REAKCIÓK Ártalmatlan anyagok bejutása egyes emberekben túlérzékenységi reakciókat válthat ki Nemkívánatos gyulladáshoz, sejtek és szövetek károsodásához vezet Az
TÚLÉRZÉKENYSÉGI REAKCIÓK TÚLÉRZÉKENYSÉGI REAKCIÓK Ártalmatlan anyagok bejutása egyes emberekben túlérzékenységi reakciókat válthat ki Nemkívánatos gyulladáshoz, sejtek és szövetek károsodásához vezet Az
OPIUM CRUDUM. Nyers ópium
 Opium crudum Ph.Hg.VIII. Ph.Eur.4. - 1 01/2015:0777 OPIUM CRUDUM Nyers ópium A nyers ópium csak mint galenusi készítmények kiindulási anyaga használható. Önmagában nem adható ki. DEFINÍCIÓ A nyers ópium
Opium crudum Ph.Hg.VIII. Ph.Eur.4. - 1 01/2015:0777 OPIUM CRUDUM Nyers ópium A nyers ópium csak mint galenusi készítmények kiindulási anyaga használható. Önmagában nem adható ki. DEFINÍCIÓ A nyers ópium
A vér vizsgálata. 12. B. biológia fakultációsainak projektje 2015.03.30-31.
 A vér vizsgálata 12. B. biológia fakultációsainak projektje 2015.03.30-31. Vérkenet készítése Menete: Alkoholos vattával letörölt ujjbegyünket szúrjuk meg steril tűvel.töröljük le az első vércseppet, majd
A vér vizsgálata 12. B. biológia fakultációsainak projektje 2015.03.30-31. Vérkenet készítése Menete: Alkoholos vattával letörölt ujjbegyünket szúrjuk meg steril tűvel.töröljük le az első vércseppet, majd
01/2008:40202 4.2.2. MÉRŐOLDATOK
 Ph.Hg.VIII. Ph.Eur.5.6-6.0-1 4.2.2. MÉRŐOLDATOK 01/2008:40202 A mérőoldatokat a szokásos kémiai analitikai eljárások szabályai szerint készítjük. A mérőoldatok előállításához használt eszközök megfelelő
Ph.Hg.VIII. Ph.Eur.5.6-6.0-1 4.2.2. MÉRŐOLDATOK 01/2008:40202 A mérőoldatokat a szokásos kémiai analitikai eljárások szabályai szerint készítjük. A mérőoldatok előállításához használt eszközök megfelelő
Trypsinum Ph.Hg.VIII. Ph.Eur.6.3-1 TRYPSINUM. Tripszin
 1 TRYPSINUM Tripszin 01/2009:0694 [9002-07-7] DEFINÍCIÓ A tripszin proteolitikus enzim, melyet az egészséges emlõsök hasnyálmirigyébõl kivont tripszinogén aktiválásával nyernek. Szárított anyagra vonatkoztatott
1 TRYPSINUM Tripszin 01/2009:0694 [9002-07-7] DEFINÍCIÓ A tripszin proteolitikus enzim, melyet az egészséges emlõsök hasnyálmirigyébõl kivont tripszinogén aktiválásával nyernek. Szárított anyagra vonatkoztatott
Vércsoportszerológiai alapfogalmak. Dr. Csépány Norbert Transzfúziós tanfolyam Debrecen
 Vércsoportszerológiai alapfogalmak Dr. Csépány Norbert Transzfúziós tanfolyam Debrecen 1 Vércsoportszerológia Az immunológia tudományának speciális ága, mely a vörösvérsejtek felületi antigénjeivel, és
Vércsoportszerológiai alapfogalmak Dr. Csépány Norbert Transzfúziós tanfolyam Debrecen 1 Vércsoportszerológia Az immunológia tudományának speciális ága, mely a vörösvérsejtek felületi antigénjeivel, és
1. Az immunrendszer működése. Sejtfelszíni markerek, antigén receptorok. 2. Az immunrendszer szervei és a leukociták
 Sejtfelszíni markerek, antigén receptorok A test őrei 1. Az immunrendszer működése Az individualitás legjobban az immunitásban mutatkozik meg. Feladatai: - a saját és idegen elkülönítése, felismerése -
Sejtfelszíni markerek, antigén receptorok A test őrei 1. Az immunrendszer működése Az individualitás legjobban az immunitásban mutatkozik meg. Feladatai: - a saját és idegen elkülönítése, felismerése -
AMOXICILLINUM TRIHYDRICUM. Amoxicillin-trihidrát
 Amoxicillinum trihydricum Ph.Hg.VIII. Ph.Eur.7.6-1 01/2013:0260 AMOXICILLINUM TRIHYDRICUM Amoxicillin-trihidrát C 16 H 19 N 3 O 5 S.3H 2 O M r 419,4 [61336-70-7] DEFINÍCIÓ (2S,5R,6R)-6-[[(2R)-2-Amino-2-(4-hidroxifenil)acetil]amino]-3,3-dimetil-7-oxo-4-tia-1-azabiciklo[3.2.0]heptán-2-
Amoxicillinum trihydricum Ph.Hg.VIII. Ph.Eur.7.6-1 01/2013:0260 AMOXICILLINUM TRIHYDRICUM Amoxicillin-trihidrát C 16 H 19 N 3 O 5 S.3H 2 O M r 419,4 [61336-70-7] DEFINÍCIÓ (2S,5R,6R)-6-[[(2R)-2-Amino-2-(4-hidroxifenil)acetil]amino]-3,3-dimetil-7-oxo-4-tia-1-azabiciklo[3.2.0]heptán-2-
CALCII STEARAS. Kalcium-sztearát
 Calcii stearas Ph.Hg.VIII. Ph.Eur.6.3-1 CALCII STEARAS Kalcium-sztearát 01/2009:0882 DEFINÍCIÓ Különböző zsírsavak kalciumsóinak keveréke; a savkomponenst főként sztearinsav (oktadekánsav) [(C 17 H 35
Calcii stearas Ph.Hg.VIII. Ph.Eur.6.3-1 CALCII STEARAS Kalcium-sztearát 01/2009:0882 DEFINÍCIÓ Különböző zsírsavak kalciumsóinak keveréke; a savkomponenst főként sztearinsav (oktadekánsav) [(C 17 H 35
A sejtfelszíni FasL és szolubilis vezikulakötött FasL által indukált sejthalál gátlása és jellemzése
 A sejtfelszíni FasL és szolubilis vezikulakötött FasL által indukált sejthalál gátlása és jellemzése Doktori értekezés tézisei Hancz Anikó Témavezetők: Prof. Dr. Sármay Gabriella Dr. Koncz Gábor Biológia
A sejtfelszíni FasL és szolubilis vezikulakötött FasL által indukált sejthalál gátlása és jellemzése Doktori értekezés tézisei Hancz Anikó Témavezetők: Prof. Dr. Sármay Gabriella Dr. Koncz Gábor Biológia
2.6.13. NEM STERIL TERMÉKEK MIKROBIOLÓGIAI VIZSGÁLATA: VIZSGÁLAT MEGHATÁROZOTT MIKROORGANIZMUSOKRA
 2.6.13. Nem steril termékek mikrobiológiai vizsgálata Ph.Hg.VIII. - Ph.Eur.6.0. 1 01/2008:20613 javított 6.0 2.6.13. NEM STERIL TERMÉKEK MIKROBIOLÓGIAI VIZSGÁLATA: VIZSGÁLAT MEGHATÁROZOTT MIKROORGANIZMUSOKRA
2.6.13. Nem steril termékek mikrobiológiai vizsgálata Ph.Hg.VIII. - Ph.Eur.6.0. 1 01/2008:20613 javított 6.0 2.6.13. NEM STERIL TERMÉKEK MIKROBIOLÓGIAI VIZSGÁLATA: VIZSGÁLAT MEGHATÁROZOTT MIKROORGANIZMUSOKRA
A VÉR BIOKÉMIÁJA VÉRKÉSZÍTMÉNYEK, PLAZMADERIVÁTUMOK A VÉR BIOKÉMIÁJA A VÉR ÖSSZETÉTELE VÉRKÉSZÍTMÉNYEK VÉRKÉSZÍTMÉNYEK
 VÉRKÉSZÍTMÉNYEK, PLAZMADERIVÁTUMOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék A VÉR BIOKÉMIÁJA Áramló folyadék, amely anyagokat
VÉRKÉSZÍTMÉNYEK, PLAZMADERIVÁTUMOK Dr. Pécs Miklós Budapesti Műszaki és Gazdaságtudományi Egyetem, Alkalmazott Biotechnológia és Élelmiszertudomány Tanszék A VÉR BIOKÉMIÁJA Áramló folyadék, amely anyagokat
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody
 CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
PHENOXYMETHYLPENICILLINUM KALICUM. Fenoximetilpenicillin-kálium
 Phenoxymethylpenicillinum kalicum Ph.Hg.VIII. Ph.Eur.6.1-1 01/2008:0149 javított 6.1 PHENOXYMETHYLPENICILLINUM KALICUM Fenoximetilpenicillin-kálium C 16 H 17 KN 2 O 5 S M r 388,5 [132-98-9] DEFINÍCIÓ A
Phenoxymethylpenicillinum kalicum Ph.Hg.VIII. Ph.Eur.6.1-1 01/2008:0149 javított 6.1 PHENOXYMETHYLPENICILLINUM KALICUM Fenoximetilpenicillin-kálium C 16 H 17 KN 2 O 5 S M r 388,5 [132-98-9] DEFINÍCIÓ A
Az örökítőanyag. Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase
 SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
SZTE, Orv. Biol. Int., Mol- és Sejtbiol. Gyak., VIII. Az örökítőanyag Az élőlények örökítőanyaga minden esetben nukleinsav (DNS,RNS) (1)Griffith, (2)Avery, MacLeod and McCarty (3)Hershey and Chase Ez az
Hús romlási folyamatból izolált Candida zeylanoides törzsek extracelluláris lipáz termelése és az enzim jellemzése
 Hús romlási folyamatból izolált Candida zeylanoides törzsek extracelluláris lipáz termelése és az enzim jellemzése Berkics Adrienn Bajcsi Nikolett, Kovács Mónika, Belák Ágnes, Renata Teparič, Vladimir
Hús romlási folyamatból izolált Candida zeylanoides törzsek extracelluláris lipáz termelése és az enzim jellemzése Berkics Adrienn Bajcsi Nikolett, Kovács Mónika, Belák Ágnes, Renata Teparič, Vladimir
Tudományos Diákköri Konferencia. Dobrotka Paula
 Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Tudományos Diákköri Konferencia Dobrotka Paula Biomérnök MSc szak Egészségvédő szakirány Staphylococcus aureus transzkripciós
Budapesti Műszaki és Gazdaságtudományi Egyetem Vegyészmérnöki és Biomérnöki Kar Tudományos Diákköri Konferencia Dobrotka Paula Biomérnök MSc szak Egészségvédő szakirány Staphylococcus aureus transzkripciós
2.9.10. ETANOLTARTALOM
 07/2012:20910 2.9.10. ETANOLTARTALOM Az itt előírt módszerek etanoltartalmú folyékony gyógyszerkészítmények vizsgálatára vonatkoznak. Valamely folyadék etanoltartalmát a folyadék 100 térfogategységében
07/2012:20910 2.9.10. ETANOLTARTALOM Az itt előírt módszerek etanoltartalmú folyékony gyógyszerkészítmények vizsgálatára vonatkoznak. Valamely folyadék etanoltartalmát a folyadék 100 térfogategységében
Immunpatológia kurzus, - tavaszi szemeszter
 Immunpatológia kurzus, - tavaszi szemeszter Prof. Sármay Gabriella, Dr. Bajtay Zsuzsa, Dr. Józsi Mihály, Prof. Kacskovics Imre Prof. Erdei Anna Szerdánként, 10.00-12.00-ig, 5-202-es terem 1 2016. 02. 17.
Immunpatológia kurzus, - tavaszi szemeszter Prof. Sármay Gabriella, Dr. Bajtay Zsuzsa, Dr. Józsi Mihály, Prof. Kacskovics Imre Prof. Erdei Anna Szerdánként, 10.00-12.00-ig, 5-202-es terem 1 2016. 02. 17.
Fludezoxiglükóz( 18 F) injekció
 07/2008:1325 javított 7.0 FLUDEOXYGLUCOSI ( 18 F) SOLUTIO INIECTABILIS Fludezoxiglükóz( 18 F) injekció DEFINÍCIÓ A készítmény a nukleofil szubsztitúcióval előállított 2-[ 18 F]fluor-2-dezoxi-D-glükopiranóz
07/2008:1325 javított 7.0 FLUDEOXYGLUCOSI ( 18 F) SOLUTIO INIECTABILIS Fludezoxiglükóz( 18 F) injekció DEFINÍCIÓ A készítmény a nukleofil szubsztitúcióval előállított 2-[ 18 F]fluor-2-dezoxi-D-glükopiranóz
3. ANYAGOK ÉS MÓDSZEREK
 1 1. BEVEZETÉS A szív- és érrendszeri kórképek után a tumoros megbetegedések képezik a második leggyakoribb halálokot világszerte. A daganatok kialakulását a kontroll nélküli sejtproliferáció és a sejthalál
1 1. BEVEZETÉS A szív- és érrendszeri kórképek után a tumoros megbetegedések képezik a második leggyakoribb halálokot világszerte. A daganatok kialakulását a kontroll nélküli sejtproliferáció és a sejthalál
MTA Doktori értekezés
 MTA Doktori értekezés Összefoglaló-Tézis füzet Egyes gazdasági haszonhalaink hímivartermékeinek mélyhűtése, a technológia standardizálásának kidolgozása és gyakorlati alkalmazása Dr. Urbányi Béla Gödöllő
MTA Doktori értekezés Összefoglaló-Tézis füzet Egyes gazdasági haszonhalaink hímivartermékeinek mélyhűtése, a technológia standardizálásának kidolgozása és gyakorlati alkalmazása Dr. Urbányi Béla Gödöllő
NADROPARINUM CALCICUM. Nadroparin-kalcium
 1 01/2008:1134 NADROPARINUM CALCICUM Nadroparin-kalcium R = H vagy SO 3 (½Ca), R' = H vagy SO 3 (½Ca), vagy CO-CH 3 R2 = H és R3 = CO 2 (½Ca), vagy R2 = CO 2 (½Ca), és R3 = H DEFINICIÓ A nadroparin-kalcium
1 01/2008:1134 NADROPARINUM CALCICUM Nadroparin-kalcium R = H vagy SO 3 (½Ca), R' = H vagy SO 3 (½Ca), vagy CO-CH 3 R2 = H és R3 = CO 2 (½Ca), vagy R2 = CO 2 (½Ca), és R3 = H DEFINICIÓ A nadroparin-kalcium
MTA Doktori Értekezés tézisei
 1 MTA Doktori Értekezés tézisei Az ér-endothel működési zavarai, vasculáris agressziv tényezők és a keringés rendellenességei tápcsatornai betegségekben. Dr. Altorjay István 2013 A Debreceni Egyetem Orvos-
1 MTA Doktori Értekezés tézisei Az ér-endothel működési zavarai, vasculáris agressziv tényezők és a keringés rendellenességei tápcsatornai betegségekben. Dr. Altorjay István 2013 A Debreceni Egyetem Orvos-
4. SZÉRUMFEHÉRJÉK MENNYISÉGI MEGHATÁROZÁSA ÉS FRAKCIONÁLÁSA (BGY:15-18 old.)
 Név: Csoport: Dátum: 4. SZÉRUMFEHÉRJÉK MENNYISÉGI MEGHATÁROZÁSA ÉS FRAKCIONÁLÁSA (BGY:15-18 old.) A GYAKORLAT CÉLJA:........ Meghatározások: Elméletileg a szérum 60-80 mg/ml fehérjét tartalmaz: 60% (30-50mg/ml)
Név: Csoport: Dátum: 4. SZÉRUMFEHÉRJÉK MENNYISÉGI MEGHATÁROZÁSA ÉS FRAKCIONÁLÁSA (BGY:15-18 old.) A GYAKORLAT CÉLJA:........ Meghatározások: Elméletileg a szérum 60-80 mg/ml fehérjét tartalmaz: 60% (30-50mg/ml)
Megnövekedett fagocitózis és gyulladásos válasz glükokortikoid kezelés hatására humán dendritikus sejtekben. Hodrea Judit
 EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI Megnövekedett fagocitózis és gyulladásos válasz glükokortikoid kezelés hatására humán dendritikus sejtekben Hodrea Judit Témavezető: Prof. Dr. Fésüs László, akadémikus
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI Megnövekedett fagocitózis és gyulladásos válasz glükokortikoid kezelés hatására humán dendritikus sejtekben Hodrea Judit Témavezető: Prof. Dr. Fésüs László, akadémikus
Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában
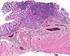 1 Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium
1 Az Egészségügyi Minisztérium módszertani levele Immunhisztokémiai és immuncitokémiai módszerek alkalmazása a patológiában Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium
Modern mikroszkópiai módszerek 2 2011 2012
 FLUORESZCENCIA MIKROSZKÓPIA A mintának a megvilágító fény által kiváltott fluoreszcencia emisszióját képezzük le. 1 Bugyi Beáta - PTE ÁOK Biofizikai Intézet 2 FLUOROFÓROK BELSŐ (INTRINSIC) FLUORESZCENCIA
FLUORESZCENCIA MIKROSZKÓPIA A mintának a megvilágító fény által kiváltott fluoreszcencia emisszióját képezzük le. 1 Bugyi Beáta - PTE ÁOK Biofizikai Intézet 2 FLUOROFÓROK BELSŐ (INTRINSIC) FLUORESZCENCIA
I. Szennyvizekben, szennyezett talajokban a biológiai oxigénigény mérése
 Talajok, természetes vizek, szennyvizek állapotának felmérése, a szennyezett területek tisztulási folyamatának nyomonkövetése Talajok, vizek minıségének meghatározása fizikai, kémiai, biológai vizsgálatok
Talajok, természetes vizek, szennyvizek állapotának felmérése, a szennyezett területek tisztulási folyamatának nyomonkövetése Talajok, vizek minıségének meghatározása fizikai, kémiai, biológai vizsgálatok
FLUDARABINI PHOSPHAS. Fludarabin-foszfát
 Fludarabini phosphas Ph.Hg.VIII. Ph.Eur.7.7-1 04/2013:1781 FLUDARABINI PHOSPHAS Fludarabin-foszfát C 10 H 13 FN 5 O 7 P M r 365,2 [75607-67-9] DEFINÍCIÓ 2-Fluor-9-(5-O-foszfono-β-D-arabinofuranozil)-9H-purin-6-amin.
Fludarabini phosphas Ph.Hg.VIII. Ph.Eur.7.7-1 04/2013:1781 FLUDARABINI PHOSPHAS Fludarabin-foszfát C 10 H 13 FN 5 O 7 P M r 365,2 [75607-67-9] DEFINÍCIÓ 2-Fluor-9-(5-O-foszfono-β-D-arabinofuranozil)-9H-purin-6-amin.
Száloptika, endoszkópok
 Száloptika, endoszkópok Optikai mikroszkópok a diagnosztikában Elektronmikroszkópia, fluorescens és konfokális mikroszkópia PTE-ÁOK Biofizikai ntézet Czimbalek Lívia 2009.03.16. Száloptika, endoszkópok
Száloptika, endoszkópok Optikai mikroszkópok a diagnosztikában Elektronmikroszkópia, fluorescens és konfokális mikroszkópia PTE-ÁOK Biofizikai ntézet Czimbalek Lívia 2009.03.16. Száloptika, endoszkópok
A BIZOTTSÁG HATÁROZATA
 L 336/36 Az Európai Unió Hivatalos Lapja 2009.12.18. A BIZOTTSÁG HATÁROZATA (2009. december 15.) az enzootiás szarvasmarha-leukózis diagnosztikai vizsgálatai tekintetében a 64/432/EGK tanácsi irányelv
L 336/36 Az Európai Unió Hivatalos Lapja 2009.12.18. A BIZOTTSÁG HATÁROZATA (2009. december 15.) az enzootiás szarvasmarha-leukózis diagnosztikai vizsgálatai tekintetében a 64/432/EGK tanácsi irányelv
CARBOMERA. Karbomerek
 04/2009:1299 CARBOMERA Karbomerek DEFINÍCIÓ A karbomerek cukrok vagy polialkoholok alkenil-étereivel térhálósított, nagy molekulatömegű akrilsav-polimerek. Tartalom: 56,0 68,0% karboxil-csoport (-COOH)
04/2009:1299 CARBOMERA Karbomerek DEFINÍCIÓ A karbomerek cukrok vagy polialkoholok alkenil-étereivel térhálósított, nagy molekulatömegű akrilsav-polimerek. Tartalom: 56,0 68,0% karboxil-csoport (-COOH)
Avidin biotin rendszer
 Avidin biotin rendszer Avidin: 4 alegység, 16 400 Da 66 000 Da glikoprotein Green M Avidin Adv Prot Chem 29 85 (1975) biotin kötőhely/alegység; CH kötőhely/alegység pi ~ 10 avidin biotin 1.3*10-15 M (Trp,
Avidin biotin rendszer Avidin: 4 alegység, 16 400 Da 66 000 Da glikoprotein Green M Avidin Adv Prot Chem 29 85 (1975) biotin kötőhely/alegység; CH kötőhely/alegység pi ~ 10 avidin biotin 1.3*10-15 M (Trp,
A vesebiopszia standard laboratóriumi vizsgálata. Daru Krisztián, Dr. Iványi Béla SZTE ÁOK Pathologiai Intézet Szeged
 A vesebiopszia standard laboratóriumi vizsgálata Daru Krisztián, Dr. Iványi Béla SZTE ÁOK Pathologiai Intézet Szeged Mintavétel Intézetek között előre egyeztetett időpontban Percutan biopszia, vese alsó
A vesebiopszia standard laboratóriumi vizsgálata Daru Krisztián, Dr. Iványi Béla SZTE ÁOK Pathologiai Intézet Szeged Mintavétel Intézetek között előre egyeztetett időpontban Percutan biopszia, vese alsó
A PROTEIN KINÁZ C IZOENZIMEK SZEREPE HUMÁN HaCaT KERATINOCYTÁK SEJTM KÖDÉSEINEK SZABÁLYOZÁSÁBAN
 EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI A PROTEIN KINÁZ C IZOENZIMEK SZEREPE HUMÁN HaCaT KERATINOCYTÁK SEJTM KÖDÉSEINEK SZABÁLYOZÁSÁBAN Papp Helga DEBRECENI EGYETEM ORVOS-ÉS EGÉSZSÉGTUDOMÁNYI CENTRUM
EGYETEMI DOKTORI (Ph.D.) ÉRTEKEZÉS TÉZISEI A PROTEIN KINÁZ C IZOENZIMEK SZEREPE HUMÁN HaCaT KERATINOCYTÁK SEJTM KÖDÉSEINEK SZABÁLYOZÁSÁBAN Papp Helga DEBRECENI EGYETEM ORVOS-ÉS EGÉSZSÉGTUDOMÁNYI CENTRUM
GYÓGYSZERTECHNOLÓGIA 1. MUNKAFÜZET
 GYÓGYSZERTECHNOLÓGIA 1. MUNKAFÜZET 0 TARTALOMJEGYZÉK FELADATLAPOK 1 Vizek paramétereinek vizsgálata és összehasonlítása 1 A ph befolyása az oldékonyságra 3 Hidrotróp és komplexképző anyagok oldásközvetítése
GYÓGYSZERTECHNOLÓGIA 1. MUNKAFÜZET 0 TARTALOMJEGYZÉK FELADATLAPOK 1 Vizek paramétereinek vizsgálata és összehasonlítása 1 A ph befolyása az oldékonyságra 3 Hidrotróp és komplexképző anyagok oldásközvetítése
V. A MIKROSZKÓP. FÉNYMIKROSZKÓPOS VIZSGÁLATOK A MIKROSZKÓP FELÉPÍTÉSE ÉS MŐKÖDÉSE
 V. A MIKROSZKÓP. FÉNYMIKROSZKÓPOS VIZSGÁLATOK A MIKROSZKÓP FELÉPÍTÉSE ÉS MŐKÖDÉSE Minden olyan optikai eszközt, amely arra szolgál, hogy a tiszta látás távolságán belül megnövelje a látószöget abból a
V. A MIKROSZKÓP. FÉNYMIKROSZKÓPOS VIZSGÁLATOK A MIKROSZKÓP FELÉPÍTÉSE ÉS MŐKÖDÉSE Minden olyan optikai eszközt, amely arra szolgál, hogy a tiszta látás távolságán belül megnövelje a látószöget abból a
DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel
 DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel Gyakorlat helye: BIOMI Kft. Gödöllő, Szent-Györgyi A. u. 4. (Nemzeti Agrárkutatási és Innovációs Központ épülete volt
DNS molekulák elválasztása agaróz gélelektroforézissel és kapilláris elektroforézissel Gyakorlat helye: BIOMI Kft. Gödöllő, Szent-Györgyi A. u. 4. (Nemzeti Agrárkutatási és Innovációs Központ épülete volt
Immundiagnosztikai módszerek
 Western blot/immunoblot Immundiagnosztikai módszerek Katona Éva 2015-03-24 Ag Enzim/Fluorochrome/ izotóp Másodlagos, jelzett At Primer At Western Blotting fehérje/ag preparálás (1) Fehérje tisztítás/extrahálás
Western blot/immunoblot Immundiagnosztikai módszerek Katona Éva 2015-03-24 Ag Enzim/Fluorochrome/ izotóp Másodlagos, jelzett At Primer At Western Blotting fehérje/ag preparálás (1) Fehérje tisztítás/extrahálás
ALOE BARBADENSIS. Barbadoszi aloé
 Aloe barbadensis Ph.Hg.VIII. Ph.Eur.8.3-1 01/2015:0257 ALOE BARBADENSIS Barbadoszi aloé DEFINÍCIÓ A drog az Aloe barbadensis Miller leveleiből kinyert, betöményített és szárított sejtnedv. Tartalom: legalább
Aloe barbadensis Ph.Hg.VIII. Ph.Eur.8.3-1 01/2015:0257 ALOE BARBADENSIS Barbadoszi aloé DEFINÍCIÓ A drog az Aloe barbadensis Miller leveleiből kinyert, betöményített és szárított sejtnedv. Tartalom: legalább
IMMUNOGLOBULINUM HUMANUM NORMALE AD USUM INTRAVENOSUM. Humán normál immunglobulin intravénás alkalmazásra
 ad usum intravenosum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:0918 IMMUNOGLOBULINUM HUMANUM NORMALE AD USUM INTRAVENOSUM Humán normál immunglobulin intravénás alkalmazásra DEFINÍCIÓ Az intravénás alkalmazásra
ad usum intravenosum Ph.Hg.VIII. Ph.Eur.6.3-1 01/2009:0918 IMMUNOGLOBULINUM HUMANUM NORMALE AD USUM INTRAVENOSUM Humán normál immunglobulin intravénás alkalmazásra DEFINÍCIÓ Az intravénás alkalmazásra
1. EGFP transzfektált HEK sejtek sortolása NFAT jelátviteli vizsgálatokhoz.
 Elemi kutatási témák a Multiparaméteres Fluoreszcencia Aktivált Sejtanalízis és Szortírozás (FACS) 2.4. TÁMOP részprojekt keretében: 2011-02-05 és 2011-07-07 között 1. EGFP transzfektált HEK sejtek sortolása
Elemi kutatási témák a Multiparaméteres Fluoreszcencia Aktivált Sejtanalízis és Szortírozás (FACS) 2.4. TÁMOP részprojekt keretében: 2011-02-05 és 2011-07-07 között 1. EGFP transzfektált HEK sejtek sortolása
A vér folyékony sejtközötti állományú kötőszövet. Egy átlagos embernek 5-5,5 liter vére van, amely két nagyobb részre osztható, a vérplazmára
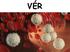 VÉR A vér folyékony sejtközötti állományú kötőszövet. Egy átlagos embernek 5-5,5 liter vére van, amely két nagyobb részre osztható, a vérplazmára (55-56%) és az alakos elemekre (44-45%). Vérplazma: az
VÉR A vér folyékony sejtközötti állományú kötőszövet. Egy átlagos embernek 5-5,5 liter vére van, amely két nagyobb részre osztható, a vérplazmára (55-56%) és az alakos elemekre (44-45%). Vérplazma: az
2 HASZNÁLATI ÚTMUTATÓ
 PLATELIA ASPERGILLUS Ag 1 микроплака 96 62794 A Platelia Aspergillus Ag immuno-enzimatikus szendvics mikrolemez vizsgálat az aspergillus galaktomannan antigén kimutatására szérumban és bal folyadékban
PLATELIA ASPERGILLUS Ag 1 микроплака 96 62794 A Platelia Aspergillus Ag immuno-enzimatikus szendvics mikrolemez vizsgálat az aspergillus galaktomannan antigén kimutatására szérumban és bal folyadékban
Ellenanyagok kimutatása diagnosztikai/prognosztikai célból
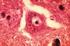 Ellenanyagok kimutatása diagnosztikai/prognosztikai célból Dr. Prohászka Zoltán Az MTA doktora Semmelweis Egyetem III. Sz. Belgyógyászati Klinika 2012-03-27 prohoz@kut.sote.hu Mennyiség Előfordulás (szekréció)
Ellenanyagok kimutatása diagnosztikai/prognosztikai célból Dr. Prohászka Zoltán Az MTA doktora Semmelweis Egyetem III. Sz. Belgyógyászati Klinika 2012-03-27 prohoz@kut.sote.hu Mennyiség Előfordulás (szekréció)
Röntgendiffrakció, tömegspektrometria, infravörös spektrometria.
 A biomolekuláris szerkezet és dinamika vizsgálómódszerei: Röntgendiffrakció, tömegspektrometria, infravörös spektrometria. Smeller László A molekuláris szerkezet és dinamika vizsgáló módszereinek áttekintése
A biomolekuláris szerkezet és dinamika vizsgálómódszerei: Röntgendiffrakció, tömegspektrometria, infravörös spektrometria. Smeller László A molekuláris szerkezet és dinamika vizsgáló módszereinek áttekintése
Kutatási beszámoló 2006-2009. A p50gap intracelluláris eloszlásának és sejtélettani szerepének vizsgálata
 Kutatási beszámoló 6-9 Kutatásaink alapvetően a pályázathoz benyújtott munkaterv szerint történtek. Először ezen eredményeket foglalom össze. z eredeti tervektől történt eltérést a beszámoló végén összegzem.
Kutatási beszámoló 6-9 Kutatásaink alapvetően a pályázathoz benyújtott munkaterv szerint történtek. Először ezen eredményeket foglalom össze. z eredeti tervektől történt eltérést a beszámoló végén összegzem.
LAVANDULAE AETHEROLEUM. Levendulaolaj
 Lavandulae aetherolaeum Ph.Hg.VIII. Ph.Eur.6.8-1 07/2010:1338 LAVANDULAE AETHEROLEUM Levendulaolaj DEFINÍCIÓ A Lavandula angustifolia Miller (Lavandula officinalis Chaix) virágzó ágvégződéseiből vízgőzdesztillációval
Lavandulae aetherolaeum Ph.Hg.VIII. Ph.Eur.6.8-1 07/2010:1338 LAVANDULAE AETHEROLEUM Levendulaolaj DEFINÍCIÓ A Lavandula angustifolia Miller (Lavandula officinalis Chaix) virágzó ágvégződéseiből vízgőzdesztillációval
Növényi sejtek által előállított monoklonális antitesttöredékek jellemzése
 BIOTECHNOLÓGIÁK MŰSZAKI HÁTTERE Növényi sejtek által előállított monoklonális antitesttöredékek jellemzése Tárgyszavak: idegen fehérje; monoklonális antitest; fehérjestabilitás; növényisejt-szuszpenzió;
BIOTECHNOLÓGIÁK MŰSZAKI HÁTTERE Növényi sejtek által előállított monoklonális antitesttöredékek jellemzése Tárgyszavak: idegen fehérje; monoklonális antitest; fehérjestabilitás; növényisejt-szuszpenzió;
2011.11.25. Modern Biofizikai Kutatási Módszerek 2011.11.03. Kereskedelmi forgalomban kapható készülékek. Áramlási citometria (flow cytometry)
 Modern Biofizikai Kutatási Módszerek 2011.11.03. Kereskedelmi forgalomban kapható készülékek Áramlási citometria (flow cytometry) Eljárás vagy mérési módszer, amellyel folyadékáramban lévő önálló részecskék,
Modern Biofizikai Kutatási Módszerek 2011.11.03. Kereskedelmi forgalomban kapható készülékek Áramlási citometria (flow cytometry) Eljárás vagy mérési módszer, amellyel folyadékáramban lévő önálló részecskék,
ETHANOLUM (96 PER CENTUM) (1) 96 %-os Etanol
 Ethanolum (96 per centum) Ph.Hg.VIII. Ph.Eur.8.1-1 04/2014:1317 ETHANOLUM (96 PER CENTUM) (1) 96 %-os Etanol DEFINÍCIÓ Tartalom: etanol (C 2 H 6 O; M r 46,07): 95,1 96,9 %V/V (92,6 95,2 %m/m), 20 C-on,
Ethanolum (96 per centum) Ph.Hg.VIII. Ph.Eur.8.1-1 04/2014:1317 ETHANOLUM (96 PER CENTUM) (1) 96 %-os Etanol DEFINÍCIÓ Tartalom: etanol (C 2 H 6 O; M r 46,07): 95,1 96,9 %V/V (92,6 95,2 %m/m), 20 C-on,
Feladatok haladóknak
 Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
HYDROXYPROPYLBETADEXUM. Hidroxipropilbetadex
 Hydroxypropylbetadexum Ph.Hg.VIII. Ph.Eur.6.2-1 07/2008:1804 HYDROXYPROPYLBETADEXUM Hidroxipropilbetadex C 42 H 70 O 35 (C 3 H 6 O) x x = 7 MS DEFINÍCIÓ A hidroxipropilbetadex (β-ciklodextrin, 2-hidroxipropil-éter)
Hydroxypropylbetadexum Ph.Hg.VIII. Ph.Eur.6.2-1 07/2008:1804 HYDROXYPROPYLBETADEXUM Hidroxipropilbetadex C 42 H 70 O 35 (C 3 H 6 O) x x = 7 MS DEFINÍCIÓ A hidroxipropilbetadex (β-ciklodextrin, 2-hidroxipropil-éter)
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE VPRIV 200 egység por oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 200 egység* velagluceráz-alfát tartalmaz.
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE VPRIV 200 egység por oldatos infúzióhoz. 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 200 egység* velagluceráz-alfát tartalmaz.
SZABVÁNYMŰVELETI ELŐÍRÁS
 SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tű zoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS Készítette: 2008.10.31. A dokumentáció kódja: SE-OBI-H-MU-01 Fodor Gábor laborasszisztens Dátum Változat
SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tű zoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS Készítette: 2008.10.31. A dokumentáció kódja: SE-OBI-H-MU-01 Fodor Gábor laborasszisztens Dátum Változat
Szerelési, üzemeltetési útmutató
 PULSER triak szabályzó egy- vagy kétfázisú elektromos fűtőelemek folyamatos teljesítmény szabályozására Szerelési, üzemeltetési útmutató ÁLTALÁNOS LEÍRÁS A PULSER egy-, vagy két-fázisú elektromos fűtőelemek
PULSER triak szabályzó egy- vagy kétfázisú elektromos fűtőelemek folyamatos teljesítmény szabályozására Szerelési, üzemeltetési útmutató ÁLTALÁNOS LEÍRÁS A PULSER egy-, vagy két-fázisú elektromos fűtőelemek
Immunológia. Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun
 Immunológia Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun Hogyan működik az immunrendszer? Milyen stratégiája van? Milyen szervek / sejtek alkotják?
Immunológia Hogyan működik az immunrendszer? http://www.szote.u-szeged.hu/mdbio/oktatás/immunológia password: immun Hogyan működik az immunrendszer? Milyen stratégiája van? Milyen szervek / sejtek alkotják?
Rubella-IgG-ELISA PKS medac. Magyar 136-PKS-VPU/010512
 RubellaIgGELISA PKS medac Magyar 0123 136PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
RubellaIgGELISA PKS medac Magyar 0123 136PKSVPU/010512 GYÁRTÓ medac Gesellschaft für klinische Spezialpräparate mbh Fehlandtstraße 3 D20354 Hamburg FORGALMAZÓ medac Gesellschaft für klinische Spezialpräparate
EURÓPAI UNIÓ Az Európai Unió Hivatalos Lapjának Kiegészítő Kiadványa 2, rue Mercier, 2985 Luxembourg, LUXEMBOURG Fax +352 2929-42670 E-mail:
 EURÓPAI UNIÓ Az Európai Unió Hivatalos Lapjának Kiegészítő Kiadványa 2, rue Mercier, 2985 Luxembourg, LUXEMBOURG Fax +352 2929-42670 E-mail: ojs@publications.europa.eu Információ és online formanyomtatványok:
EURÓPAI UNIÓ Az Európai Unió Hivatalos Lapjának Kiegészítő Kiadványa 2, rue Mercier, 2985 Luxembourg, LUXEMBOURG Fax +352 2929-42670 E-mail: ojs@publications.europa.eu Információ és online formanyomtatványok:
L Ph 1. Az Egyenlítő fölötti közelítőleg homogén földi mágneses térben a proton (a mágneses indukció
 A 2008-as bajor fizika érettségi feladatok (Leistungskurs) Munkaidő: 240 perc (A vizsgázónak két, a szakbizottság által kiválasztott feladatsort kell kidolgoznia) L Ph 1 1. Kozmikus részecskék mozgása
A 2008-as bajor fizika érettségi feladatok (Leistungskurs) Munkaidő: 240 perc (A vizsgázónak két, a szakbizottság által kiválasztott feladatsort kell kidolgoznia) L Ph 1 1. Kozmikus részecskék mozgása
SZABVÁNYMŰVELETI ELŐÍRÁS. A tejsavdehidrogenáz enzim izoenzimeinek vizsgálata című gyakorlat előkészítése
 SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tűzoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS című gyakorlat előkészítése Készítette: 2011.02.21. A dokumentáció kódja: SE-OBI-OKT- MU-16 Dr. Bauer
SEMMELWEIS EGYETEM Orvosi Biokémiai Intézet 1094 Budapest, Tűzoltó u. 37-47. SZABVÁNYMŰVELETI ELŐÍRÁS című gyakorlat előkészítése Készítette: 2011.02.21. A dokumentáció kódja: SE-OBI-OKT- MU-16 Dr. Bauer
Gyógyszervegyületek elektrofiziológiai szűrése nagy hatáskereszt-metszetű ( semi high-troughput ) rendszereken
 Gyógyszervegyületek elektrofiziológiai szűrése nagy hatáskereszt-metszetű ( semi high-troughput ) rendszereken Szegedi Tudományegyetem, Általános Orvostudomány Kar Farmakológiai és Farmakoterápiai Intézete
Gyógyszervegyületek elektrofiziológiai szűrése nagy hatáskereszt-metszetű ( semi high-troughput ) rendszereken Szegedi Tudományegyetem, Általános Orvostudomány Kar Farmakológiai és Farmakoterápiai Intézete
A CD44 ÉS L-SZELEKTIN LEUKOCITA-ENDOTÉL INTERAKCIÓKBAN BETÖLTÖTT SZEREPÉNEK VIZSGÁLATA GYULLADÁSOS EGÉRMODELLEKBEN GONDA ANDREA DR.
 Doktori (Ph.D.) értekezés A CD44 ÉS L-SZELEKTIN LEUKOCITA-ENDOTÉL INTERAKCIÓKBAN BETÖLTÖTT SZEREPÉNEK VIZSGÁLATA GYULLADÁSOS EGÉRMODELLEKBEN Készítette: GONDA ANDREA DR. Programvezetı: Prof. Dr. Zeher
Doktori (Ph.D.) értekezés A CD44 ÉS L-SZELEKTIN LEUKOCITA-ENDOTÉL INTERAKCIÓKBAN BETÖLTÖTT SZEREPÉNEK VIZSGÁLATA GYULLADÁSOS EGÉRMODELLEKBEN Készítette: GONDA ANDREA DR. Programvezetı: Prof. Dr. Zeher
CINtec PLUS Cytology Kit
 CINtec PLUS Cytology Kit 605-100 06889565001 100 1. ábra: Cervicalis epithelialis sejt, p16 INK4a pozitív (barna citoplazmás festődés) és Ki-67 pozitív (piros magfestődés) FELHASZNÁLÁSI TERÜLET A CINtec
CINtec PLUS Cytology Kit 605-100 06889565001 100 1. ábra: Cervicalis epithelialis sejt, p16 INK4a pozitív (barna citoplazmás festődés) és Ki-67 pozitív (piros magfestődés) FELHASZNÁLÁSI TERÜLET A CINtec
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül.
 7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
