Extraszinaptikus proteinek szerepe a szinaptikus átvitelben
|
|
|
- Pál Orsós
- 9 évvel ezelőtt
- Látták:
Átírás
1 Extraszinaptikus proteinek szerepe a szinaptikus átvitelben Szakdolgozat biológia alapszak, biológus szakirány készítette: GYÖRFFY BALÁZS ANDRÁS témavezető: DR. KÉKESI ADRIENNA KATALIN, egyetemi docens Élettani és Neurobiológiai Tanszék EÖTVÖS LORÁND TUDOMÁNYEGYETEM TERMÉSZETTUDOMÁNYI KAR BIOLÓGIAI INTÉZET Budapest, 2010.
2 Tartalomjegyzék Rövidítésjegyzék... 3 Bevezetés Sejtadhéziós molekulák N-CAM típusú fehérjék Az L1/CHL1 molekulák közvetítette szignalizációs útvonal Az N-CAM fehérje indukálta intracelluláris folyamatok Egyéb sejtadhéziós molekulák Integrin fehérjék Dystroglycan molekulák Extraszinaptikus receptorok Az AMPA-receptorok transzlokációja A receptorok alegység-összetételében megnyilvánuló különbségek A periszinaptius receptorok intracelluláris és a periszinaptikus membránban való transzportja a glicin receptorán bemutatva Kainát receptorok funkciói A szinapszisból kijutó neurotranszmitterek hatása Az extracelluláris mátrix elemei A neuronok környezetébe szekretált molekulák Egyéb proteoglikánok Következtetés, modell Összefoglalás Summary Hivatkozások Köszönetnyilvánítás
3 Rövidítésjegyzék Az egyes molekulák hivatalos elnevezései: ABP: AMPA receptor-binding protein AMPA receptor: α-amino-3-hydroxyl-5-methyl-4-isoxazole-propionate receptor CHL1: neural cell adhesion molecule L1-like protein CREB: Cyclic AMP-responsive element-binding protein EAAT1: excitatory amino acid transporter 1 ERK: extracellular signal-regulated kinase FAK: focal adhesion kinase FARP2: FERM, RhoGEF and pleckstrin domain-containing protein 2 FGF-receptor: fibroblast growth factor receptor GABA receptor: γ-aminobutyric acid receptor GEF: guanine nucleotide exchange factor GlyR: glycine receptor GRIP: glutamate receptor-interacting protein L1 (L1-CAM): neural cell adhesion molecule L1 MAGUK: membrane-associated guanylate kinase MAPKK/MEK: mitogen-activated protein kinase kinase MGLUR: metabotropic glutamate receptor MHC: myosin heavy chain N-cadherin: neural cadherin N-CAM: neural cell adhesion molecule NMDA receptor: N-methyl-D-aspartate NrCAM: neuronal cell adhesion molecule PAK1: hivatalos név: serine/threonine-protein kinase PAK 1; alternatív elnevezés: p-21 activated kinase 1 PDZ domén: a PSD-95 a DlgA és a zo-1 fehérjék kezdőbetűiből képzett betűszó PI 3-kináz: phosphatidylinositol 3-kinase PICK1: hivatalos név: PRKCA-binding protein; alternatív elnevezés: protein kinase C-alphabinding protein 3
4 PSD-95: hivatalos név: disks large homolog 4; alternatív elnevezés: postsynaptic density protein 95 Rac1 GTP-áz: Rac1: Ras-related C3 botulinum toxin substrate 1; GTP: guanosine triphosphate Raf: RAF proto-oncogene serine/threonine-protein kinase RGD: az arginin (R), glicin (G) és az aszparaginsav (D) aminosavak egybetűs kódjai alapján képzett betűszó Rnd1: Rho-related GTP-binding protein Rho6 R-Ras: Ras-related protein SAP102: hivatalos név: disks large homolog 3; alternatív elnevezés: synapse-associated protein 102 Src: proto-oncogene tyrosine-protein kinase Src SynCAM: synaptic cell adhesion molecule TAG-1/axonin-1: hivatalos név: contactin-2; alternatív elnevezések: axonal glycoprotein TAG-1, transient axonal glycoprotein 1 VAV2 GEF: guanine nucleotide exchange factor VAV2 Bevezetés A dolgozat célja az extraszinaptikus helyzetű fehérjék, molekuláris struktúrák jelentőségének, a szinaptikus átvitelben való szerepének a megmutatása, az újabb kutatások fényében. Ezek az eredmények a neuronok molekuláris komponenseinek még pontosabb megismeréséhez és az idegsejtek működésének megértéséhez segíthetnek hozzá. Az intenzív kutatómunka következtében szükséges lehet a neuronok közötti kapcsolatok új modelljének a megalkotása. Különösen nagy hangsúlyt fektettek az utóbbi időben a szinapszisok és a periszinaptikus régiók fehérjekészletének meghatározására. A molekuláris biológián belül nemrégiben megjelent új tudományterület, a proteomika foglalkozik egy vizsgálati objektum fehérjéinek kimutatásával, azok struktúrájának és funkciójának meghatározásával, valamint a köztük lévő kapcsolatok, hálózatok megismerésével. A szakdolgozatban terjedelmi okok miatt nem térhettem ki a plasztikus szinaptikus struktúra létrehozásában részt vevő szinaptikus, extraszinaptikus és intracelluláris komponensek egészére. Ezért néhány, a neuronok élettani folyamatait nagymértékben befolyásoló extraszinaptikus protein (pl.: sejtadhéziós molekulák, extraszinaptikus 4
5 receptorok) funkciójának, szerepének leírásán keresztül szeretném bemutatni az egymással kapcsolódó idegsejtek hálózatának mai, korszerű modelljét. Ugyanakkor több esetben szükség van még a molekuláris kapcsolatok felderítésére, és a napjainkban is tartó ez irányú kutatások akár a neuronok közti szinapszisokról, és egyéb sejtes kölcsönhatásokról alkotott mai szemléletünket is átalakíthatják a jövőben. A két idegsejt (pre- és posztszinaptikus neuron) között létrejött, jellemző strukturális és funkcionális tulajdonságokkal bíró kapcsolatokat szinapszisoknak nevezzük. Ez a specifikus kölcsönhatás a két résztvevő sejt közötti ingerülettovábbítást, információ-átadást teszi lehetővé. A dolgozat a neuronok közötti kémiai szinapszisokat körülvevő és befolyásoló extraszinaptikus molekuláris komponenseken keresztül megvalósuló folyamatokat tárgyalja, ugyanakkor más típusú szinaptikus kapcsolatok is léteznek. Egy-egy idegsejt szinapszist hozhat létre akár izom-, vagy mirigysejtekkel, míg a kémiai szinapszisoktól lényegesen eltérnek az úgynevezett elektromos és immunszinapszisok. A szinapszisok tulajdonképpen a soksejtű élőlények ideg- illetve immunsejtjei közötti kommunikáció rendkívül speciális csatornái, de rajtuk kívül működnek az idegsejtek között más kommunikációs csatornák is. Az intercelluláris kommunikációnak több fajtája is létezik, amelyek csoportosítása több szempont szerint lehetséges. Megkülönböztethetünk direkt és indirekt kommunikációt. A direkt kapcsolat a két sejt között kialakuló gap junction-ökön keresztül valósul meg. Ebben a struktúrában a sejtek plazmamemránjai rendkívül közel kerülnek egymáshoz az átnyúló connexin fehérjéken keresztül. A keletkező pórusokon a kisebb méretű molekulák és ionok átjutnak, valamint bizonyos izom- és idegsejtek között elektromos szinapszisként funkcionálnak ezek a rés-kapcsolódások. Az indirekt kommunikáció mindig valamilyen szignálként szereplő kémiai anyag közvetítésével valósul meg. A kémiai szempontból rendkívül változatos jelmolekulák kibocsátására a legkülönbözőbb sejtek képesek. A szignál terjedése több csatornán keresztül lehetséges. Endokrin jeltovábbítás esetén a hormonoknak nevezett jelmolekulákat mirigy-, vagy idegsejtek bocsátják a véráramba, és ezen a szerteágazó csatornán keresztül a szignál széles körben kifejtheti hatását. A parakrin jelátvitelben a szövetközti tér tölti be a csatorna szerepét, és a kibocsátó sejthez közeli, szomszédos sejtek képesek a jelmolekulákat receptoraikkal felfogni. Ennek a kommunikációs típusnak egy szélsőséges eseteként is értelmezhető az autokrin jeltovábbítás. Ebben az esetben a jeladó sejt funkcionál egyben a jelfogó célsejtként is. Végül az indirekt kommunikációs típusok közé sorolható még a neurokrin jelátvitel, ami a szinapszisokon keresztül valósul meg. A neurokrin kommunikáció során egy jeladó funkcióval bíró idegsejt neurotranszmittereknek nevezett szignálmolekulákat bocsát ki a 5
6 rendkívül szűk, mindössze nm-es szinaptikus résbe. Ezen a csatornán áthaladva a neurotranszmitterek eljutnak a posztszinaptikus sejt felszínéhez, és a plazmamembránon lévő receptorfehérjékhez kötődhetnek. A posztszinaptikus sejtben a receptor-ligandum kapcsolódás intracelluláris változások sorozatát váltja ki. A két kapcsolódó neuron intracelluláris komponenseit, és plazmamembránjaik fehérjeösszetételét tekintve is különbözik. A preszinaptikus neuron szinapszisban résztvevő régiója (amelyet többnyire az idegsejt axonjának végződése képez) intracellulárisan, a sejttest felől anterográd transzporttal érkező szinaptikus vezikulumokat tartalmaz. A vezikulumok a dokkolás során a preszinaptikus végződés membránjához kapcsolódnak különböző fehérjék közvetítésével, majd az ingerület hatására exocitózissal bocsátják ki a szinaptikus résbe tartalmukat. A posztszinaptikus sejtek a neurotranszmitterek megkötésére képes membránreceptorokat hordoznak a felszínükön. Intracelluláris helyzetben a membrán fehérjéivel kapcsolatban álló citoszkeletális régió, a posztszinaptikus denzitás található, amely a jelátvitelben játszik szerepet. A szinapszis nem rigid struktúra, változására a különböző receptorfehérjék és sejtadhéziós molekulák mozgása, internalizációja, és sejtfelszíni megjelenése jellemző. Az extraszinaptikus proteinek laterális diffúzióval megvalósuló mozgásukkal befolyásolhatják a szinaptikus hatékonyságot, a szinapszis erősségét. A dolgozatban magával a szinaptikus molekuláris jelátvivő mechanizmussal nem foglalkozom, hanem a szinapszisokba szorosan nem beletartozó, de funkciójukat befolyásoló molekuláris komponensek rendkívül sokrétű szerepének bemutatását végzem el. Ezen elemek közé extraszinaptikus sejtadhéziós proteinek, periszinaptikus receptorok és az extracelluláris mátrix molekulái sorolhatók. Ezenkívül a témához szorosan nem kapcsolódó, a gliasejtek felszínén lokalizált molekulák szinaptikus átvitelre gyakorolt hatásainak megértése is elengedhetetlen a neuronális folyamatok korszerű modelljének megalkotásához. A sejtek közti szinapszisokon keresztül zajló kommunikációban rendkívül nagy befolyásoló tényezőnek bizonyult - az újabb vizsgálatok értelmében az extraszinaptikus környezet. Az egymásra kölcsönösen ható szinaptikus és extraszinaptikus régió közül ez utóbbi szerepének tárgyalását végzem el. 6
7 1. Sejtadhéziós molekulák A szinapszisok kialakításában nagy jelentősége van a pre- és posztszinaptikus neuronon elhelyezkedő több különböző sejtadhéziós molekulának. Az adhéziós molekulák rendkívül sok - és egymástól nagymértékben eltérő - tagból álló csoportjának öt nagyobb típusa különíthető el: az immunglobulin szuperfamíliába tartozók, az integrinek, a cadherinek, a szelektinek és a limfocita homing receptorok. A sejtadhéziós molekulákat a partner adhéziós molekulák alapján két csoportra oszthatjuk. Az azonos típusú adhéziós molekulák kapcsolata homofil (például a cadherinek közti kapcsolat), míg az eltérő típusú molekulák közti interakció heterofil típusú (például az integrin és a mátrix egy fehérje molekulája közötti kölcsönhatás során). E molekulák közül a neuronok közötti, és az idegsejt-mátrix kapcsolatok létrehozásában több cadherin (N-cadherin), immunglobulin típusú fehérjék (például: SynCAM, NCAM), valamint integrinek játszanak szerepet N-CAM típusú fehérjék A neuronális sejtadhéziós molekulák (N-CAM proteinek) több sejttípusra is jellemző fehérjék, amelyek jelenlétét a neuronokon és gliasejteken kívül vázizom sejteken és az immunrendszer részét képező NK-sejteken is kimutatták. Az idegrendszerben a szinaptogenezisben játszanak fontos szerepet, valamint hatással vannak a szinaptikus plaszticitásra, és így a tanulás folyamatára is. Az N-CAM fehérjék az immunglobulin proteincsaládba tartozó molekulák. A csoportba tartozó fehérjék közül az N-CAM, az L1, és a CHL1 sejtadhéziós molekulák a leginkább ismertek. Az L1-CAM fehérjék közé négy különböző, ám szerkezetileg nagyfokú hasonlóságot mutató molekula tartozik: az L1, a CHL1 ( close homolog of L1, tehát az L1 proteinnel homológ fehérje), az NrCAM, és a Neurofascin. Ezekre a proteinekre általánosságban jellemző a kiterjedt extracelluláris domén, valamint a csoport tagjai közt meglévő konzervatív intracelluláris szakasz. Az N-CAM transzmembrán protein extracelluláris régiója egy öt immunglobulin-szerű (Ig) doménből, valamint két fibronectin III-as típusú szakaszból álló részletből épül fel. Az L1-CAM csoport tagjai 6 darab Ig-típusú, és 4-5 fibronectin III-as, a sejt felszínén lévő doménnel bírnak (Schmid és Maness, 2008) (1). 7
8 A központi idegrendszerben jelen lévő CAM fehérjék úgynevezett homofil, és heterofil kapcsolatokon keresztül - tehát, azonos típusú, valamint különböző ligandumokkal létesített kölcsönhatás során - töltik be rendkívül sokrétű funkcióikat. Az összetett extracelluláris domén-struktúrával bíró L1-CAM fehérjék homofil kölcsönhatása nemcsak a sejt-sejt kapcsolódást teszik lehetővé, hanem a neuritek növekedését is indukálhatják. A vizsgálatok szerint az L1-CAM proteinek homofil interakciójához egy bizonyos Ig-2 domén szükséges. Az L1-CAM típusú fehérjék ugyanakkor a sejt környezetének sok egyéb tagjával képesek heterofil kölcsönhatást biztosítani, mint például az N-CAM, TAG-1/axonin-1 ligandumok, valamint különböző proteoglikánok (Zhao és Siu, 1995) (2). A sejtadhéziós fehérjék intracelluláris szakaszai különböző sejten belüli molekuláris változásokat indukálnak. A citoszkeletális komponensekre gyakorolt hatásuk teszi lehetővé a neuronális sejtmigráció folyamatát, az axonok, és dendritek növekedését, fejlődését, és a környező idegsejtekkel való szinaptikus kapcsolatok képzését. Az N-CAM fehérjék intracelluláris szakasza spektrin proteineken keresztül áll kapcsolatban a sejt plazmamembránja alatt elhelyezkedő aktin filamentumok citoszkeletális hálózatával. Az L1- típusú adhéziós fehérjék a spektrin-adaptor, ankyrin molekulával valósítják meg mindezt Az L1/CHL1 molekulák közvetítette szignalizációs útvonal Az újabb feltételezések szerint ezek a neuronális sejtadhéziós molekulák koreceptorokként is funkcionálnak bizonyos növekedési faktorok, integrinek és egyéb, az extracelluláris mátrix tagjait képező molekulák számára. Vizsgálták az L1 sejtadhéziós protein β1-integrinnel kialakított kölcsönhatását az idegsejtek migrációjának, és a neuritek növekedésének folyamatában (Schmid és Maness, 2008) (1). Ezen kapcsolat létrejöttében az L1 fehérje RGD-kötő szekvenciája játszik szerepet. Az RGD az arginin, a glicin és az aszparaginsav aminosavak egybetűs kódjaiból származó rövidítés. Az L1-β1 fehérjék közötti kis affinitású kölcsönhatás egy közös intracelluláris jelátviteli folyamatot indít el. Az L1/CHL1 (és N-CAM) által indukált szignáltranszdukciót az 1. ábra mutatja be. Az L1 (CHL1) sejtadhéziós fehérje ligandumának megkötése után a c-src tirozin kináz, a PI 3- kináz, a Vav2 GEF (VAV2 guanin nukleotid kicserélő faktor), a Rac1 GTP-áz, a PAK1 protein (a p21 fehérje aktiválta kináz), majd a MEK (más néven MAPKK), és végül az ERK fehérje aktiválódik. A szignáltranszdukciós folyamat a nukleáris DNS-ről való transzkripciót eredményezi (Schmid és Maness, 2008) (1). 8
9 1. ábra (Schmid és Maness, 2008) Az L1 fehérjecsaládba tartozó adhéziós molekulák a spektrinnel asszociált aktin filamentumokkal az úgynevezett ankyrin adaptor fehérjén keresztül állnak kapcsolatban. A spektrin/ankyrin komplex citoszkeletális hálózattal alkotott együttesének sok esetben nélkülözhetetlen szerepe van. A mielinhüvellyel burkolt axonok feszültségfüggő ioncsatornáinak vizsgálata során arra mutattak rá, hogy ezen fehérjék lokalizálásában kiemelt funkcióval bír a fent említett molekuláris komplex. A citoszkeletonnal kapcsolatban álló spektrin és ankyrin fehérjék hozzájárulnak a transzmembrán helyzetű ioncsatornák helyének stabilizálásában, a laterális irányú mozgásuk gátlásában, és a membrán integritásának megőrzésében (Susuki és Rasband, 2008) (3). A transzmembrán L1 fehérjék citoszkeletális elemekkel való kapcsolata reverzibilis, és a fent említett molekuláris kaszkád ezt a kölcsönhatást befolyásolni tudja. A szignalizációs útvonal utolsó citoplazmatikus komponense, a szerin/treonin protein kinázok közé tartozó ERK, aktiválódása után képessé válik az L1 fehérje intracelluláris doménjének egy kritikus 9
10 pontján (az FIGQY motívumon) történő foszforiláció indukálására. Az ERK indirekt módon vesz részt a folyamatban, a foszforilációt közvetlenül katalizáló fehérje még nem ismert. Az L1-CAM protein ezen a területén - egy tirozin oldalláncon bekövetkező foszforilációja az ankyrin molekulától, és így az aktin filamentumtól való disszociációját eredményezi. A folyamat a ligandumkötést követően, az egyes receptorok szintjén megvalósuló visszacsatolási mechanizmushoz szükséges (Whittard és mtsai, 2006) (4). A fentiekben részletezett mechanizmus alapján egyfajta magyarázatot kaphatunk az idegsejtek migrációjakor és a neuritek növekedésekor megfigyelt jelenségekre. Az idegsejtek nyúlványai ekkor dinamikusan váltakozva kapcsolódnak az extracelluláris mátrix komponenseihez, és a szomszédos sejtekhez, vagy megszüntetik kölcsönhatásukat a környező elemekkel. A folyamatban résztvevő sejtadhéziós molekulák (ez esetben az L1-CAM fehérjék), a sejtet körülvevő mátrixban lévő, vagy egy másik neuron felszínén található ligandumuk megkötése után, az intracelluláris doménjükön keresztül aktiválják azt a molekuláris kaszkádot, amely végső soron az L1 fehérje ankyrin molekulától való elszakadásához vezethet. Az L1 fehérje FIGQY motívumon való foszforilációja az aktin filamentumoktól való disszociációt, míg defoszforilációja az újabb kapcsolódást eredményezi. A modell értelmében, az egyelőre még ismeretlen kináz foszforilációs aktivitása, és a ciklikus foszforiláció/defoszforiláció folyamata teszi lehetővé a neuron megfelelő sejtrégiójának a környező neuronokhoz való kapcsolódását, és azoktól való elválását. Az idegsejtek felszínén található sejtadhéziós molekulák közötti kölcsönhatás egyik érdekes példája az L1/CHL1 és a neuropilin-1 molekulák közt létrejövő interakció. A már ismertetett L1-típusú adhéziós proteinek ko-receptorokként szolgálnak egy bizonyos extracellulárisan szekretált fehérje, a semaphorin3a (sema3a) számára, amelynek megkötésére az L1-CAM molekulák közelében elhelyezkedő neuropilin-1 proteinek képesek. A semaphorin fehérjék elsődleges funkciója, hogy megakadályozzák a fejlődő idegrendszerben a növekvő axonok helytelen kapcsolódását a környező sejtekhez, extracelluláris elemekhez. Az L1-CAM fehérje az egyik Ig-doménjén keresztül egy, a plazmamembránban lévő integrin adhéziós molekulával is kapcsolatban áll. A neuropilin-1 szubsztrátjának megkötését követő szignáltranszdukciós változásokat a 2. ábra mutatja be. Az L1-CAM, és közvetve az integrin molekulákkal kapcsolatban lévő neuropilin-1 fehérje egy újabb transzmembrán fehérjével, a citoplazmatikus szignalizációt mediáló plexina ko-receptorral is kölcsönhatásban van. A neuropilin-1 fehérje rendkívül kis méretű citoplazmatikus régiója nem tartalmaz az intracelluláris szignalizációhoz szükséges motívumot, szerepe inkább a transzmembrán receptorokból álló komplex létrehozásában van. 10
11 A sema3a ligandum kötése után a GEF-ként funkcionáló FARP2 fehérje aktiválódik a plexina-n keresztül. A FARP2 molekula ezután a Rac1 proteint aktiválja, amely az Rnd1 fehérje plexina-hoz való kötődését váltja ki. Ez a folyamat vezet előbb az R-Ras, majd ezen keresztül az integrin fehérje gátlásához. A leírt mechanizmus az adott sejtfelszín eltávolodását váltja ki a környező elemektől, és így a növekvő axon megtapadásának gátlását okozza (Schmid és Maness, 2008) (1), (Goshima és mtsai, 2000) (5). 2. ábra (Schmid és Maness, 2008) Az N-CAM fehérje indukálta intracelluláris folyamatok Az N-CAM sejtadhéziós fehérjék hasonló módon vesznek részt a neuronok felszínén megvalósuló adhéziós folyamatokban, mint a rokon L1-CAM típusú fehérjék. Az extracelluláris régióban történő ligandumkötést követően azonban egy kissé eltérő szignalizációs útvonal aktiválódik. A molekuláris kaszkád első tagja ez esetben a tirozin kináz szerepet betöltő Fyn molekula. Ez a fehérje ezután aktiválja az úgynevezett fokális adhéziós kinázt (FAK), amit azután a Ras, a Raf, és a MEK fehérje aktivációja követ. Ezen a ponton az előzőleg már említett L1-CAM jelátviteli útvonallal közös úton folytatódik tovább a kaszkád, 11
12 és előbb az ERK, majd a transzkripciós faktorként funkcionáló CREB fehérjék aktiválódnak. A FAK fehérjék különböző hatást gyakorolhatnak a sejtre, a neuronokban azonban leginkább a dendritek és axonok növekedését gátolják. A FAK adaptor fehérjék a legkülönbözőbb molekulákkal képesek kölcsönhatásba lépni, többek között növekedési faktorok receptoraival, PI 3-kinázokkal, az Src fehérjével, az Rho GTP-ázok regulátoraival, és citoszkeletális elemekkel. Így fontos megjegyezni, hogy a FAK proteinek aktiválása több, eltérő szignalizációs útvonal eredménye is lehet (Rico és mtsai, 2004) (6). A sejtfelszíni receptorok interakciójában bizonyos esetekben szerepe lehet a lipid raftoknak is. A kutatások során megvizsgálták az N-CAM fehérje három különböző izoformájának, az N-CAM 120-nak, N-CAM 140-nek, és N-CAM 180-nak az előfordulását a membránban, valamint ezek kölcsönhatását az FGF-receptorral. A kutatók azt találták, hogy az N-CAM 140 raftok megszüntetése a FAK, valamint az ERK fehérjék aktivációját gátolja, és megakadályozza a neuritek növekedését. Ehhez hasonlóan, a neurit-növekedés blokkolását okozta egy bizonyos FGF-receptor inhibitor komponens használata. Ezek alapján a lipid raftokban jelenlévő, különböző típusú N-CAM, és FGF-receptorok közötti szoros kapcsolatot feltételezhetünk (Niethammer és mtsai, 2002) (7). A lipid raftok szerepére az NrCAM sejtadhéziós molekulák esetében is rámutattak. A raftok felbontásához használt metil-β-ciklodextrin (MBCD) kezelést követően az NrCAM molekulák F-actin polimerrel való kapcsolatának felbomlását figyelték meg. Az MBCDkezelés hatással volt az NrCAM fehérje ligandum-kötésére is. A lipid raftok roncsolásával lecsökkent az aggregálódó NrCAM proteinek száma, és sokkal kisebb mértékben voltak képesek ligandumuk, az úgynevezett TAG-1 gyöngyök megkötésére (Falk és mtsai, 2004) (8) Egyéb sejtadhéziós molekulák Integrin fehérjék Az integrinek minden bizonnyal fontos funkcióval rendelkeznek az extracelluláris mátrix és a sejtek közötti kapcsolatok biztosításában. Az integrin fehérjék családjába legalább 21 különböző heterodimer protein tartozik, amelyek egy α-, valamint egy β-alegységből épülnek fel. A kimutatott nyolcféle β-alegység nemkovalens kapcsolat kialakítására képes a 12 féle α-alegység tagjaival. A kilencféle, β 1 -alegységgel rendelkező integrin fehérje 12
13 mindegyike megtalálható az idegszövetben. Példaként említhető az α 8 β 1 szerkezettel jellemezhető fehérje, amely jelenlétét kimutatták a növekvő axonokon, és feltételezik az axonok és az extracelluláris mátrix közötti kapcsolat kialakításában való szerepét (Venstrom és Reichardt, 1993) (9) Dystroglycan molekulák A dystroglycan fehérjék izomrostokban betöltött szerepe jól ismert, ugyanakkor más szövetekben, és így az idegszövetben is kimutatták expressziójukat. Komplexet képeznek az izomrostokban intracellulárisan elhelyezkedő dystrophin fehérjével, valamint az extracelluláris mátrix komponenseivel (a fehérje laminin receptorként funkcionál). Amennyiben a dystroglycan fehérjén keresztül megvalósuló kapcsolat nem jön létre, úgy izomdisztrófia, és az izomszövet nekrózisa következhet be. A fehérjének rendkívül fontos szerepe lehet a központi idegrendszerben is, mivel a Duchenne-féle izomdisztrófiában szenvedő páciensek egy részénél mentális betegségek is megjelentek (Venstrom és Reichardt, 1993) (9). 2. Extraszinaptikus receptorok A szinapszisban résztvevő sejtek plazmamembránján elhelyezkedő, neurotranszmittereket érzékelő receptorok a legnagyobb sűrűségben a szinaptikus rést kialakító felszíneken helyezkednek el. Helyzetük nem állandó, a szinaptikus és extraszinaptikus régiók közötti folyamatos mozgásuk mutatható ki. A szinapszis területén lokalizált receptorok speciális állványzat fehérjék segítségével, a posztszinaptikus denzitáson (PSD) keresztül kapcsolódnak az intracelluláris sejtvázhoz, és ezek az elemek mintegy kihorgonyozzák a receptorokat a megfelelő pozícióban. A PSD komponensei a szinapszisok plaszticitását eredményezve csak átmenetileg kötik a sejt felszínére kerülő fehérjéket. Ez a dinamikusan változó struktúra modulálja a kibocsátott neurotranszmitterek megkötésére képes receptorok számát, sűrűségét, elhelyezkedését. A jelenséget leginkább az NMDA, AMPA, GABA és a glicin receptorait vizsgálva figyelték meg, de minden bizonnyal ezek a folyamatok több más szinaptikus receptor esetén megvalósulnak. Az egyes receptorok eltérő mértékben képesek a posztszinaptikus struktúrákhoz való stabil kötődésre, így például az 13
14 NMDA-receptorok kisebb, míg az AMPA-receptorok intenzívebb mozgást mutatnak a szinaptikus és periszinaptikus régiók között (Sheng, 2001) (10). A receptorok a transzlokáció során a szintézisük intracelluláris helyéről exocitózissal a periszinaptikus plazmamembránba épülnek be, így extracelluláris doménjük képes a környezetben megtalálható specifikus ligandumok megkötésére. Megfelelő intracelluláris hatások következtében a receptorok laterális irányban mozogva a membránban a szinaptikus rés területére juthatnak. Ezzel lehetővé válik a szinaptikus vezikulumokból felszabaduló neurotranszmitterek hatékonyabb megkötése. Bizonyos esetekben megfigyelhető a szintetizált receptorok közvetlen transzlokációja a szinaptikus rés régiójába, az extraszinaptikus területeken való megjelenés nélkül is. A receptorok eltávolítása klatrin-mediált endocitózissal történik, majd bekövetkezhet a fehérjék intracelluláris degradációja (Lévi és Triller, 2006) (11). A receptorok transzlokációját a sematikus 3. ábra mutatja. 3. ábra (Lévi és Triller, 2006), 1: a receptor intracelluláris transzportja a szintézis helyéről; 2: a receptor megjelenése a szinaptikus résben; 3: a receptor kihelyezése a periszinaptikus területre; 4: laterális mozgás a periszinaptikus régióban; 5: a receptor endocitózisa; 6: a receptor lebontása; scaffold=állványzat fehérjék csoportja 14
15 2.1. Az AMPA-receptorok transzlokációja Az extraszinaptikus receptorok felismerése elektrofiziológiai módszerekkel végzett vizsgálatok eredménye volt. A későbbiekben a fagyasztva törés és immuncitokémiai eljárások használatával lehetővé vált az idegsejtek plazmamembránján elhelyezkedő receptorok számának és lokalizációjának pontos detektálása. Egy vizsgálat során ezen technikák kombinálásával sikerült megbecsülni a kísérleti állat (fiatal patkány) kisagyából származó posztszinaptikus helyzetű Purkinje-sejtek membránján lokalizált AMPA receptorok számát. Az AMPA-receptorok a glutaminsav neurotranszmitter megkötésére képes ionotróp transzmembrán receptor molekulák. A vizsgálat során megfigyelt Purkinje-sejtek csak egyféle serkentő bemenetet kaptak a preszinaptikus sejtektől. A mérések által a szinaptikus rés területén lévő AMPA receptorok száma 910 ± 36 receptor/µm 2 -nek, míg az extraszinaptikus régiókban a jóval alacsonyabb 19 ± 2 receptor/µm 2 értéknek adódott. A receptorok sűrűsége között tehát szignifikáns különbség volt kimutatható. Ennek ellenére a neuronok extraszinaptikus plazmamembránja jóval nagyobb receptor készlettel bír, mint a szinapszisokban szereplő területek, mivel az extraszinaptikus membrán teszi ki a sejtet határoló teljes felület 98 %-át (Tanaka és mtsai, 2005) (12). Kutatók vizsgálták a serkentő szinapszisokra jellemző plaszticitásért nagymértékben felelős AMPA-receptorok lateralis mozgásakor egyéb fehérjékkel létrejövő kölcsönhatásait. A hippocampalis neuronokon végzett megfigyelések során kimutatták, hogy a periszinaptikus AMPA-receptorok szinaptikus régióba jutása során kölcsönhatás alakul ki a receptorhoz asszociált stargazin fehérje, és a PSD-95 fehérje első két PDZ doménje között. A vizsgálatok alkalmával ezen komponensek mennyiségének változtatásával több esetet is modelleztek. Amennyiben a neuron posztszinaptikus régiójában megnövelték a PSD-95 fehérjék koncentrációját, úgy az AMPA-receptorok nagyobb mértékű toborzását figyelték meg a szinapszis területén. Ezzel szemben változatlan PSD-95 fehérjekészlet, és a stargazin fehérje koncentrációjának növelése esetén a kontrollnál jóval több extraszinaptikus AMPA-receptor jelent meg. Ekkor a receptorok szinapszisban való kihorgonyzása az intracelluláris molekuláris körülmények változása miatt nem valósulhatott meg. Az AMPA-receptorok toborzásában, a szinapszisban való lokalizálásában több, még nem teljesen ismert fehérjefehérje kölcsönhatás is szerepet játszik. Minden bizonnyal egyéb, a MAGUK fehérjék (membrane-associated guanylate kinase) közé tartozó molekula is szükséges a kapcsolat 15
16 kialakításához. Ezek közé tartozik például a SAP 102 protein is, amely funkcióját tekintve a PSD-95 fehérjéhez hasonló. Ehhez hasonlóan kimutathatóak AMPA-receptorok a plazmamembránban stargazint nem tartalmazó neuronokban, ami a hiányzó fehérjével azonos szerepű egyéb molekulák jelenlétét feltételezi. Az AMPA-receptorok szállításában résztvevő molekuláris mechanizmusok még ismeretlen folyamatairól több lehetséges modell is létezik. Egyesek a PSD-95 és a stargazin komplexének szerepét a receptorok extraszinaptikus területekről a szinapszisokba történő szállításában látják. Úgy vélik, hogy a periszinaptikus régiókból a posztszinaptikus membrán területére érkező receptorok disszociálnak a PSD-95/stargazin komplextől, és újabb fehérjékhez kötődnek, így megtartva posztszinaptikus lokalizáltságukat. Az újonnan létrejövő kapcsolatokban AMPA-receptorok kötésére képes GRIP, ABP, vagy PICK1 fehérjék szerepelhetnek. Ezt a modellt alátámasztják azok a megfigyelések, amelyek szerint az AMPAreceptorok GluR1 és GluR2 alegységeinek PDZ-kötő doménnel nem rendelkező változatai a szinapszisba szállítódnak ugyan, de tartósan nem képesek ott maradni, mivel a posztszinaptikus denzitás egyéb fehérjéihez nem képesek kötődni. Fluoreszcensen jelölt stargazin fehérjék vizsgálatakor viszont azt tapasztalták, hogy a szinapszisba jutó AMPAreceptorokkal való kölcsönhatásuk nem szűnik meg. A szállítás, és kihorgonyzás pontos mechanizmusa tehát még nem ismert (Schnell és mtsai, 2002) (13). A kutatások kimutatták, hogy a theta, vagy nagy frekvenciájú ingerléssel való stimulálás az AMPA receptorok átmeneti megjelenéséhez vezet a periszinaptikus régióban. Alacsony frekvenciájú ingerléssel, stimulálással elérhető a plazmamembránon lokalizált AMPA receptorok mobilizálása. Ez a jelenség annak a következménye, hogy a szinaptikus résben lokalizált receptorok a posztszinaptikus denzitással való kapcsolatuk következtében stabilabban helyezkednek el a sejt membránján, mint a periszinaptikus helyzetben lévő fehérjék, amelyek így transzlokációra képesek bizonyos intracelluláris változások eredményeként. Nagy jelentősége van a neuronokat körülvevő sejteknek is a szinaptikus átvitelben. A periszinaptikusan elhelyezkedő AMPA receptorok szignifikánsan kisebb mennyiségben képesek ligandumukat, a preszinaptikus sejt által kibocsátott glutaminsavat megkötni a szinapszist körülvevő gliasejtek jelenléte miatt. Abban az esetben viszont, ha a gliasejtek glutaminsav-transzporter fehérjéjét (Glutamate Aspartate Transporter, GLAST vagy Excitatory Amino Acid Transporter 1, EAAT1) gátolják, akkor a szinapszis területéről kijutó glutaminsav megkötése már lehetségessé válik (Yang és mtsai, 2008) (14). 16
17 2.2. A receptorok alegység-összetételében megnyilvánuló különbségek Néhány receptor esetében a kutatók különbségeket írtak le a receptorok szerkezetében. Patkány hippocampusából származó neuronok vizsgálata során eltéréséket találtak az extraszinaptikus és szinaptikus helyzetű NMDA receptorok alegységeinek szerkezetében. Az NMDA-receptorok rendkívül intenzíven kutatott ionotróp, glutaminsav neurotranszmitter megkötésére képes receptor fehérjék. A vizsgálatok során azt tapasztalták, hogy amíg az NR2A alegység megtalálható mindkét régió receptoraiban, addig az NR2B alegység csak extraszinaptikusan mutatható ki. Feltevések szerint a szinaptogenezis során többek között az NMDA receptorok gyors átalakulása is bekövetkezik (Tovar és Westbrook, 1999) (15). A kisagy szemcsesejteket tartalmazó rétegében a GABA A receptorok vizsgálata során szintén eltéréseket találtak a neuron plazmamembránjának különböző régióiban elhelyezkedő fehérjék alegység szerkezetében. A GABA receptorok a központi idegrendszer legfontosabb gátló neurotranszmitterének, a gamma-aminovajsavnak a megkötésére képesek. Két típusuk különíthető el: a ligandfüggő ioncsatornaként funkcionáló GABA A receptor, valamint a metabotróp, G-fehérjével kapcsolt GABA B receptorok. A GABA A receptorok öt alegységből épülnek fel, és ezen alegységeknek több izoformája is kimutatható. A fehérjében jelen lévő alegységtípusok jelentősen befolyásolják többek között a receptorok ligandumkötési affinitását, a csatorna nyitási valószínűségét. A vizsgálat során a felnőtt patkány kisagyi szemcsesejtjeinek felszínén lévő GABA A receptorok α1, α6, β2, β3, γ2 és δ alegységeit mutatták ki. Ezek a fehérje alegységek 4-6 különböző típusú GABA A receptor megjelenését tették lehetővé. Ezen szemcsesejtek a GABAerg szinaptikus kapcsolataikat kizárólag Golgisejtekkel valósítják meg. Az elvégzett immunarany-jelöléses lokalizálás során azt találták, hogy az α1, α6, β2, β3 és γ2 alegységek a szinaptikus és extraszinaptikus régiókban egyaránt jelen vannak, bár az extraszinaptikus területeken kisebb koncentrációban. Szintén ezzel a technikával mutatták ki azt is, hogy a δ-alegységek csak az extraszinaptikus receptorok felépítésében vesznek részt. A kísérletek tanúsága szerint a különböző alegység szerkezettel rendelkező, szinaptikus és extraszinaptikus helyzetű receptorokon keresztül a szemcsesejt eltérő típusú gátlása valósul meg. A δ-alegységgel rendelkező GABA A receptorok nagyobb affinitást mutatnak ligandumaikkal, a GABA neurotranszmitterekkel szemben. Ezen kívül képesek a neurotranszmitter tartós jelenléte esetén is aktiválódni, szemben a szinaptikus típusú GABA A receptorral. Ezzel lehetőség nyílik a posztszinaptikus neuron tartós, tonikus gátlására. A fázikus inhibíció a kutatások eredményei alapján a szinaptikus GABA A 17
18 receptorok közvetítésével valósul meg (Nusser és mtsai, 1998) (16). Mindezek alapján látható, hogy a szinaptikus résből a sejtek közötti extracelluláris térbe jutó GABA neurotranszmitterek megkötésére specifikus receptorok szolgálnak, amelyek kinetikai paramétereikben szignifikánsan eltérnek a szinapszisban lévő típusoktól, és így eltérő befolyást gyakorolnak a posztszinaptikus sejtre A periszinaptius receptorok intracelluláris és a periszinaptikus membránban való transzportja a glicin receptorán bemutatva A receptorok periszinaptikus és szinaptikus területek közötti lateralis mozgásán kívül jelentős intracelluláris transzport is létezik. A membránon lévő receptorok internalizációja endocitózissal megy végbe. Ez a folyamat nem mutatható ki a posztszinaptikus denzitás régiójában (tehát a szinaptikus junkció területén), hanem ezt a szinaptikus receptorfehérjék perifériás irányba, az extraszinaptikus területek felé tartó mozgása előzi meg. Miután egy-egy fehérje bejutott a sejtbe, a körülményektől függően a lizoszómák segítségével degradálódhatnak, vagy ismét felhasználódhatnak, újból kijutva a plazmamembrán egy meghatározott pontjára. A vizsgálatok alanyául a glicin receptort (GlyR) kiválasztva, a kutatók leírták a posztszinaptikus sejtben zajló receptorfehérje-szintézis folyamatát. A GlyR-ok a központi idegrendszer gátló szinapszisaiban jelen lévő, a glicin neurotranszmittert kötő fehérjék. Általánosságban elmondható, hogy a létrejövő neurotranszmitter-receptorok plazmamembránon való elhelyezkedését a szintetizáló rendszer subcelluláris lokalizációja nagymértékben befolyásolja bár a későbbiekben lehetőség van a receptor lateralis irányú transzlokálására a membránban. A vizsgálatok során a patkány gerincvelőjének mellső szarvában lévő neuronokban immuncitokémiai módszerekkel, fény- és elektronmikroszkópos technikát is felhasználva figyelték meg a posztszinaptikus sejtek fehérjeszintézisének folyamatát. A kutatók a GlyR α alegységét kódoló mrns nukleinsavat mutatták ki az idegsejt dendritikus régiójában, és a posztszinaptikus területeken. Az mrns molekulák sejten belüli lokalizációja szerepet játszik a transzlálódó fehérjék megjelenési helyének determinálásában. Az idegsejtek bizonyos, proximális helyzetű dendritjeiben mrns nukleinsavmolekulák, valamint intracelluláris membránrendszerek (endoplazmatikus retikulum, Golgi-ciszternák), és riboszómák jelenlétét mutatták ki (Gardiol és mtsai, 1999) (17). 18
19 A legkorábbi vizsgálatok során a lokális fehérjeszintetizáló folyamatok bizonyítékául a neuronok dendritjében megfigyelt poliriboszómák szolgáltak. A morfológiai megfigyeléseken kívül később biokémiai módszerekkel is igazolták a szintetizáló rendszer jelenlétét a neuronok dendritjeiben, valamint kimutatták a fehérjék glikozilációjához szükséges enzimeket is ezen régiókban. Mindezek alapján azt feltételezik, hogy a neuronok sejttestjén kívül a dendritekben is képződnek transzmembrán proteinek, neurotranszmitterreceptorok. Azon riboszómák és iniciációs faktorok, amelyek nem állnak kapcsolatban a neuron ciszternáival minden bizonnyal a periszinaptikus proteinek keletkezésében játszanak szerepet, mivel a proteineket kódoló mrns-eket ezekben a régiókban mutatták ki (Gardiol és mtsai, 1999) (17). A kutatások során megvizsgálták a patkány gerincvelőjéből származó neuronok dendritjeinek plazmamembránjában elhelyezkedő transzmembrán GlyR fehérjék diffúziós mozgását. A mérések során a fehérjék sebessége a membránban 1-2 µm/min értékű volt. Ezenkívül meghatározták az extraszinaptikus receptorok diffúziós koefficiensét is, amely 0,029 ± 0,005 µm 2 /sec-nak adódott. Ezen proteinek esetében a véletlenszerű Brownmozgások jelenlétét is ki tudták mutatni (Lévi és Triller, 2006) (11). Ez a szüntelenül folyó mozgás a közeg hőmérsékletének növelésével intenzívebbé válik. A membránt alkotó lipidmolekulák rotációs vagy flip-flop mozgása, valamint laterális irányú diffúziója mind befolyásolja a közeg állapotát és így a fehérjék Brown-mozgását. A gyors Brown-mozgásokat a glicinreceptorokon kívül több más receptorfehérje vizsgálata során is kimutatták, mint például a metabotróp glutaminsav-, NMDA-, és AMPA-receptorok esetében. A megfigyelések során a glicin receptorainak mozgása lelassult, majd (bizonyos időre) megszűnt, amikor a fluoreszcensen megjelölt gephyrin fehérjékkel kerültek kapcsolatba. A gephyrin a gátló szinapszisban résztvevő posztszinaptikus neuron szinapszishoz közeli régiójában mutatható ki, és a glicin- és GABA receptoraival van kölcsönhatásban. A fehérjék mozgását egyéb intracelluláris állványzat fehérjék, a citoszkeleton komponensei, és a plazmamembránban lévő transzmembrán proteinek is akadályozhatják. A glicin- és GABAreceptorok gephyrin fehérjével kialakított kölcsönhatásán kívül a metabotróp glutaminsav receptorok homer proteinnel, és az AMPA-receptorok PSD-95 fehérjével kialakított kapcsolatát mutatták ki. Ezen tényezők hatására a fehérjék váltakozva, hol gyors Brownmozgással, máskor pedig lassabban, gátat jelentő molekulákkal övezve haladnak a membránban (Lévi és Triller, 2006) (11). 19
20 2.4. Kainát receptorok funkciói A kainát receptorok a glutaminsav neurotranszmitterekre érzékeny ionotróp receptorok. Ezek a fehérjék az NMDA- és az AMPA-receptorok mellett az ionotróp glutaminsav receptorok harmadik csoportját képezik. A posztszinaptikus sejt plazmamembránján lokalizált receptorok a serkentő szinaptikus átvitelben játszanak szerepet, míg a preszinaptikus neuron felszínén lévő proteinek a gátló szinapszisokban zajló GABA neurotranszmitter-kibocsátást szabályozzák. A tetramer kainát receptorok öt különböző fehérje alegység, a GluR5, GluR6, GluR7, KA1 és KA2 közül felhasznált négy komponens megfelelő elrendezésben kialakított együtteséből épülnek fel (Eder és mtsai, 2003) (18). A kainát receptorok alegység-összetétele sejtenként eltérő jellemzőket mutat. A receptor fehérjék jelenlétét a legkorábbi kutatások során különböző hippocampalis sejtpopulációkon figyelték meg. A CA3 piramidális sejtek esetében azt találták, hogy a receptorokat a GluR6 alegységek építik fel, és ez befolyással van a receptor kötési affinitására. Az ettől eltérő alegység-szerkezettel rendelkező, a CA1 areából származó piramidális neuronok például a CA3-as típusú hippocampus sejteken lokalizált receptorokénál kisebb szenzitivitást mutatnak a ligandumuk irányában (Bureau és mtsai, 1999) (19). A posztszinaptikusan elhelyezkedő kainát receptorok, az újabb kutatások szerint részt vesznek a serkentő posztszinaptikus áram létrehozásában. A vizsgálatok során a kutatók azt tapasztalták, hogy a kainát receptorok aktiválásához a preszinaptikus sejt felől érkező ismétlődő szinaptikus ingerlés szükséges. Ezen kívül azt a megfigyelést tették, hogy a kainát receptorokon keresztül kialakuló serkentő posztszinaptikus áram más receptorokhoz viszonyítva kisebb amplitúdóval bír. Ezek az eredmények vetették fel annak a gondolatát, hogy a kainát receptorok esetlegesen az extraszinaptikus régiókban helyezkednek el, és a szinaptikus résből kijutó glutaminsav neurotranszmitterek megkötésére képesek. Egy kutatás során patkányok neokortikális 5. rétegbeli piramidális neuronjainak szomatodendritikus sejtfelszínén vizsgálták a kainát receptorok jellemzőit és eloszlását a membránon. A receptorok jelenlétét kimutatták mind a neuron sejttestén (soma), mind a dendrit nyúlványokon, és az eltérő elhelyezkedésű kainát receptorok tulajdonságaiban, funkciójukban nem találtak különbségeket. A disztálisan elhelyezkedő dendriteken a receptorokat nagyobb számban mutatták ki. Érdekes eredményként szolgált, hogy ezeken a területeken a szintén glutaminsav megkötésére képes AMPA-receptorok ugyancsak nagy mennyiségben fordultak elő (Eder és mtsai, 2003) (18). 20
21 A vizsgálatok során kimutatták, hogy az AMPA- és kainát receptorok közel azonos glutaminsav affinitással bírnak. A posztszinaptikus sejtet ért stimulus által kiváltott molekuláris változások pontosabb megértéséhez egy AMPA-receptorokat szelektíven gátló kémiai vegyületet (a GYKI kóddal ellátott anyagot) használtak fel. A neuronhoz ekkor hozzáadott glutaminsav neurotranszmitter képes volt a szinaptikus és extraszinaptikus régiókban lokalizált receptorokhoz egyaránt kötődni, és a stimulusra adott válasz alapján a kutatók arra a következtetésre jutottak, hogy a kainát receptorok legnagyobb mennyiségben az extraszinaptikus területeken helyezkednek el (Eder és mtsai, 2003) (18). Az extraszinaptikus kainát receptorok neuronok közötti kommunikációban betöltött funkciójának egyre pontosabb leírásán, megértésén kívül fontos lehet még az ideg- és gliasejtek közti kapcsolatban játszott szerepük feltárása is. A gliasejtek közé tartozó corticalis és hippocampalis asztrociták képesek az intracelluláris Ca 2+ -koncentrációtól függő glutaminsav kibocsátásra. Az asztrocitákban a Ca 2+ mennyiségének oszcillációja által kiváltott neurotranszmitter-exocitózis pedig hatással van a környező gliasejtekre, valamint a neuronokra is. Ebben az esetben nagy szerepe lehet az idegsejtek felszínén lokalizált extraszinaptikus glutaminsav-receptoroknak, és így többek közt a kainát receptoroknak is (Liu és mtsai, 2004) (20). 3. A szinapszisból kijutó neurotranszmitterek hatása A gyors serkentő szinapszisok bizonyos feltevések szerint zárt kommunikációt tesznek lehetővé a pre- és posztszinaptikus neuronok között. A kutatások alapján viszont az a modell tűnik helyesnek, amely szerint a preszinaptikus idegsejtből exocitózissal felszabaduló glutaminsav neurotranszmitter diffúzióval kijuthat a szinaptikus résből, és extraszinaptikus receptorokhoz kötődhet akár egy szomszédos neuronon is. Ezt bizonyítja például az, hogy kimutathatóak metabotróp glutaminsav receptorok (mglur1) a posztszinaptikus denzitástól, a szinaptikus réstől távolabb, tehát periszinaptikus helyzetben, valamint a preszinaptikus sejt plazmamembránján, a neurotranszmitterek exocitózisának helyéhez képest perifériásan (mglur2) is. Mindkét receptorfehérje megtalálható a gliasejteken is. A preszinaptikus sejt axonterminális régiójának membránján lokalizált mglur2 típusú protein gátló hatást fejt ki a neuron további glutaminsav kibocsátására. Ezt igazolja, hogy a receptorra szelektív antagonista képes megakadályozni ezen funkciójának betöltését. A jelenségből, a neurotranszmitter kibocsátás ezen az úton való szabályozásából következik, hogy a 21
22 glutaminsav diffúziója lehetséges a szinaptikus kommunikáció során. A metabotróp glutaminsav receptorokról szólva meg kell említeni, hogy szemben a gyors serkentő szinaptikus átvitelben szerepet játszó ionotróp glutaminsav receptorokkal, az mglur fehérjék csoportjának tagjai leginkább moduláló funkcióval bírnak (Flor és mtsai, 2002) (21), (Rusakov és Kullmann, 1998) (22). A glia- és idegsejteken elhelyezkedő mglur fehérjéket a 3. ábra mutatja be. 4. ábra (Flor és mtsai, 2002) Mivel a glutaminsav kibocsátást követő diffúzió jelentős hatással van a szinaptikus transzmisszióra, és befolyásolja a környező sejteket is, ezért fontos megismerni ezt a jelenséget. A folyamat megfelelő modellezéséhez tisztában kell lenni az extracelluláris tér geometriai viszonyaival, a környező gliasejtek és neuronok nyúlványainak helyzetével, és természetesen a neurotranszmitter diffúziójának jellemzőivel, és a sejtfelszíni receptorokkal, transzporter fehérjékkel való interakcióinak tulajdonságaival. Az exocitózis helyétől távol elhelyezkedő glutaminsav transzporter fehérjék jelentősen befolyásolhatják a neurotranszmitter extraszinaptikus régiók felé történő terjedését. Ez a hatás a vizsgálatok során leginkább alacsony glutaminsav koncentrációnál volt érzékelhető. Abban az esetben, amikor a kibocsátott neurotranszmitter koncentrációja elegendően nagy volt ahhoz, hogy aktiválja a posztszinaptikus sejt AMPA és NMDA receptorait, a glutaminsav molekulák gyors eltűnése volt tapasztalható, a szabad receptorok nagy sebességgel való telítődése következtében. 22
23 A kutatások eredményei alapján szimulálhatóvá vált az exocitózissal kibocsátott egyetlen vezikula hatása az extraszinaptikus receptorokra. A modellben az extracelluláris mátrix tulajdonságait, és a neurotranszmitterre vonatkozó diffúziós koefficiens értékét is figyelembe vették. Egyetlen vezikula átmérőjét kb. 40 nm-nek tekintették, amelyből kb glutaminsav molekula szabadulhat fel a szinaptikus résben. Ezen paraméterek alapján egyetlen vezikulában a neurotranszmitterek koncentrációja hozzávetőlegesen 250 mm, amely alatta van a hipotetikus maximum (kb. 320 mm) értékének. Az egyetlen vezikulából felszabaduló glutaminsav mennyiség elegendőnek bizonyult ahhoz, hogy megnyissa a szinaptikus rés központjától 200 nm-nél nem távolabbi, periszinaptikusan lokalizált NMDA receptorokat. Ebből az eredményből arra következtethetünk, hogy az NMDA receptorokkal megegyező glutaminsav affinitású, extraszinaptikus mglur1 transzporter fehérjék is aktiválódnak egyetlen vezikula exocitózisa által. A nagyobb távolságban, szomszédos sejteken elhelyezkedő nagy affinitású receptorok ligandumkötése már nagymértékben függ a diffúziós koefficienstől (D). Amennyiben a glutaminsav neurotranszmittert a közegben D 0,1 µm 2 /msec érték jellemezte, abban az esetben a szinapszishoz legközelebb elhelyezkedő, szomszédos sejteken lokalizált NMDA receptorok jelentős hányada aktiválódott a ligandum hatására. Ebből az eredményből arra a következtetésre juthatunk, hogy egy neuronok között jelenlévő, átlagosnak tekinthető szinapszisból felszabaduló glutaminsav képes arra, hogy az extracelluláris mátrixon áthaladva megnyissa a szomszédos sejtek NMDA receptorait. Az AMPA receptorok esetében viszont kisebb kötési affinitásuk következtében sokkal kevésbé tapasztalták a csatornák megnyílását a ligandumaik felszabadulása után. A vizsgálatok tanúsága szerint az extraszinaptikus glutaminsav receptorok által ezen a diffúziós úton megvalósuló interszinaptikus kommunikáció 0,3 µm 2 /msec érték feletti diffúziós koefficiens esetén már nem jelentős. Ennek ellenére egymáshoz közelebb elhelyezkedő szinapszisok vizsgálatakor nagyobb diffúziós együttható mellett is számottevő a szomszédos sejten lévő receptorok aktivációja. Vizsgálták az egyetlen vezikulából felszabaduló neurotranszmitterek hatását más szinaptikus és extraszinaptikus helyzetű receptorokra is. Azonban a preszinaptikus helyzetű mglur2, valamint a GABAerg szinapszisok posztszinaptikus membránján lokalizált kainát típusú fehérjék aktivációjának kutatásakor akadályt jelentett a receptorok és a neurotranszmitter kibocsátás helye közötti távolság nem elég pontos ismerete (Rusakov és Kullmann, 1998) (22). Fontos még megemlíteni, hogy a szinapszist kialakító sejtrégiók (mint például a dendrittüske) időben változó helyzete és struktúrája is befolyással bír a neurotranszmitterek 23
24 kijutására, diffúziójára és így az interszinaptikus kommunikációra, a szinaptikus hatékonyságra. 4. Az extracelluláris mátrix elemei Az extracelluláris mátrix fehérjéi rendkívül sokrétű funkcióval bíró komponensei az élő szervezetnek, így fontos szerepet töltenek be a központi idegrendszerben is. Ezek a molekulák befolyásolják az egyes neuronok, valamint az egymással kapcsolatban álló sejtek fejlődését, növekedését, differenciálódását. Az egyedfejlődés alatt szerepük van az idegsejtek axonjainak növekedési folyamataiban, a neuronális migrációban, a szinapszisok képzésében, valamint bizonyos régiókban a sérüléseket követő regenerációt is befolyásolják A neuronok környezetébe szekretált molekulák Az agrin proteoglikánok fontos funkciót töltenek be a szinaptogenezisben. Az egyedfejlődés során (illetve denervációt követően) a motoneuronok által kibocsátott agrin molekulák a neuromuszkuláris junkcióba jutnak, majd az acetilkolin receptorok aggregációját hozzák létre az izomrost felszínén. A molekulák expresszálását a központi idegrendszer több neuron típusában is kimutatták, és minden bizonnyal esszenciális szerepet töltenek be az idegsejtek közti szinaptogenezisben is. A laminin fehérjék az ontogenezis során a neuronok axonjainak növekedését segítik. Az idegsejtek felszínén jelenlévő β 1 -típusú integrinek sejtadhéziós molekulák, amelyek képesek az extracelluláris mátrixban található lamininokhoz kötődni a neuritek fejlődése, növekedése során. A β 1 -alegységgel több különböző α-alegység (α 1, α 2, α 3, α 6, α 7 ) is létrehozhat a lamininokat ligandumukként felismerni képes integrineket. Ezen kívül egyéb molekulák is funkcionálhatnak laminin-receptorként, mint például a dystroglycan, a laktózkötő lektin, és egyéb proteoglikánok. A fibronectin extracelluláris glikoproteinek a neuronális migrációban és a neuritek növekedésében játszanak szerepet az egyedfejlődés, valamint a regeneráció során. A mátrixban lévő dimer struktúrájú fibronectin molekulák a sejtek felszínén lévő integrin fehérjékhez képesek kötődni. 24
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az idegsejtek kommunikációja. a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus PERIFÉRIÁS IDEGRENDSZER Receptor
a. Szinaptikus jelátvitel b. Receptorok c. Szignál transzdukció neuronokban d. Neuromoduláció. Szinaptikus jelátvitel.
 Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
Az idegsejtek kommunikációja a. Szinaptikus jelátvitel b. eceptorok c. Szignál transzdukció neuronokban d. Neuromoduláció Szinaptikus jelátvitel Terjedő szignál 35. Stimulus eceptor végződések Érző neuron
Egy idegsejt működése. a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza
a. Nyugalmi potenciál b. Transzport proteinek c. Akciós potenciál. Nyugalmi potenciál. 3 tényező határozza meg:
 Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
Egy idegsejt működése a. Nyugalmi potenciál b. Transzport proteinek c. Nyugalmi potenciál Az ionok vándorlása 5. Alacsonyabb koncentráció ioncsatorna membrán Passzív Aktív 3 tényező határozza meg: 1. Koncentráció
2. A jelutak komponensei. 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája 1. Receptor fehérje Jel molekula (ligand; elsődleges
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Gyógyszerészeti neurobiológia. Idegélettan
 Az idegrendszert felépítő sejtek szerepe Gyógyszerészeti neurobiológia. Idegélettan Neuronok, gliasejtek és a kémiai szinapszisok működési sajátságai Neuronok Információkezelés Felvétel Továbbítás Feldolgozás
Az idegrendszert felépítő sejtek szerepe Gyógyszerészeti neurobiológia. Idegélettan Neuronok, gliasejtek és a kémiai szinapszisok működési sajátságai Neuronok Információkezelés Felvétel Továbbítás Feldolgozás
A sejtek közöti kommunikáció formái. BsC II. Sejtélettani alapok Dr. Fodor János
 A sejtek közöti kommunikáció formái BsC II. Sejtélettani alapok Dr. Fodor János 2010. 03.19. I. Kommunikáció, avagy a sejtek informálják egymást Kémiai jelátvitel formái Az üzenetek kémiai úton történő
A sejtek közöti kommunikáció formái BsC II. Sejtélettani alapok Dr. Fodor János 2010. 03.19. I. Kommunikáció, avagy a sejtek informálják egymást Kémiai jelátvitel formái Az üzenetek kémiai úton történő
Jelutak. 2. A jelutak komponensei Egy tipikus jelösvény sémája. 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék
 Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Jelutak 2. A jelutak komponensei 1. Egy tipikus jelösvény sémája 2. Ligandok 3. Receptorok 4. Intracelluláris jelfehérjék Egy tipikus jelösvény sémája Receptor fehérje Jel molekula (ligand; elsődleges
Szignalizáció - jelátvitel
 Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Jelátvitel autokrin Szignalizáció - jelátvitel Összegezve: - a sejt a,,külvilággal"- távolabbi szövetekkel ill. önmagával állandó anyag-, információ-, energia áramlásban áll, mely autokrin, parakrin,
Egy idegsejt működése
 2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
2a. Nyugalmi potenciál Egy idegsejt működése A nyugalmi potenciál (feszültség) egy nem stimulált ingerelhető sejt (neuron, izom, vagy szívizom sejt) membrán potenciálját jelenti. A membránpotenciál a plazmamembrán
Receptorok, szignáltranszdukció jelátviteli mechanizmusok
 Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
Receptorok, szignáltranszdukció jelátviteli mechanizmusok Sántha Péter 2016.09.16. A sejtfunkciók szabályozása - bevezetés A sejtek közötti kommunikáció fő típusai: Endokrin Parakrin - Autokrin Szinaptikus
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi- és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM. Jelutak. 1. a sejtkommunikáció alapjai
 Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
Jelutak ÖSSZ TARTALOM 1. Az alapok 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi és hormonális kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés
A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban
 A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban 17. Központi idegrendszeri neuronok ingerületi folyamatai és szinaptikus összeköttetései 18. A kalciumháztartás zavaraira
A sejtmembrán szabályozó szerepe fiziológiás körülmények között és kóros állapotokban 17. Központi idegrendszeri neuronok ingerületi folyamatai és szinaptikus összeköttetései 18. A kalciumháztartás zavaraira
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav,
 MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
MULTICELLULÁRIS SZERVEZŐDÉS: SEJT-SEJT (SEJT-MÁTRIX) KÖLCSÖNHATÁSOK 1. Bevezetés (2.)Extracelluláris mátrix (ECM) (Kollagén, hialuron sav, proteoglikánok) (3.)Multiadhéziós fehérjék és sejtfelszíni receptorok
KÉSZÍTETTE: BALOGH VERONIKA ELTE IDEGTUDOMÁNY ÉS HUMÁNBIOLÓGIA SZAKIRÁNY MSC 2015/16 II. FÉLÉV
 KÉSZÍTETTE: BALOGH VERONIKA ELTE IDEGTUDOMÁNY ÉS HUMÁNBIOLÓGIA SZAKIRÁNY MSC 2015/16 II. FÉLÉV TÉNYEK, CÉLOK, KÉRDÉSEK Kísérlet központja Neuronok és réskapcsolatokkal összekötött asztrocita hálózatok
KÉSZÍTETTE: BALOGH VERONIKA ELTE IDEGTUDOMÁNY ÉS HUMÁNBIOLÓGIA SZAKIRÁNY MSC 2015/16 II. FÉLÉV TÉNYEK, CÉLOK, KÉRDÉSEK Kísérlet központja Neuronok és réskapcsolatokkal összekötött asztrocita hálózatok
ÖSSZ-TARTALOM. 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3.
 Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Jelutak ÖSSZ-TARTALOM 1. Az alapok - 1. előadás 2. A jelutak komponensei 1. előadás 3. Főbb jelutak 2. előadás 4. Idegi kommunikáció 3. előadás Jelutak 1. a sejtkommunikáció alapjai 1. Bevezetés 2. A sejtkommunikáció
Sejt - kölcsönhatások az idegrendszerben
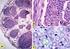 Sejt - kölcsönhatások az idegrendszerben dendrit Sejttest Axon sejtmag Axon domb Schwann sejt Ranvier mielinhüvely csomó (befűződés) terminális Sejt - kölcsönhatások az idegrendszerben Szinapszis típusok
Sejt - kölcsönhatások az idegrendszerben dendrit Sejttest Axon sejtmag Axon domb Schwann sejt Ranvier mielinhüvely csomó (befűződés) terminális Sejt - kölcsönhatások az idegrendszerben Szinapszis típusok
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
9. előadás Sejtek közötti kommunikáció
 9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
9. előadás Sejtek közötti kommunikáció Intracelluláris kommunikáció: Elmozdulás aktin szálak mentén miozin segítségével: A mikrofilamentum rögzített, A miozin mozgékony, vándorol az aktinmikrofilamentum
S-2. Jelátviteli mechanizmusok
 S-2. Jelátviteli mechanizmusok A sejtmembrán elválaszt és összeköt. Ez az információ-áramlásra különösen igaz! 2.1. A szignál-transzdukció elemi lépései Hírvivô (transzmitter, hormon felismerése = kötôdés
S-2. Jelátviteli mechanizmusok A sejtmembrán elválaszt és összeköt. Ez az információ-áramlásra különösen igaz! 2.1. A szignál-transzdukció elemi lépései Hírvivô (transzmitter, hormon felismerése = kötôdés
1. Mi jellemző a connexin fehérjékre?
 Sejtbiológia ea (zh2) / (Áttekintés) (1. csoport) : Start 2019-02-25 20:35:53 : Felhasznált idő 00:01:02 Név: Minta Diák Eredmény: 0/121 azaz 0% Kijelentkezés 1. Mi jellemző a connexin fehérjékre? (1.1)
Sejtbiológia ea (zh2) / (Áttekintés) (1. csoport) : Start 2019-02-25 20:35:53 : Felhasznált idő 00:01:02 Név: Minta Diák Eredmény: 0/121 azaz 0% Kijelentkezés 1. Mi jellemző a connexin fehérjékre? (1.1)
A sejtek közötti közvetett (indirekt) kapcsolatok
 A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
A sejtek közötti közvetett (indirekt) kapcsolatok kémiai anyag közvetítése a jeladó - jel - csatorna - jelfogó rendszerben szöveti hormon hormon szövet közötti tér véráram neurotranszmisszió neurotranszmitter
Kommunikáció. Sejtek közötti kommunikáció
 Kommunikáció Sejtek közötti kommunikáció soksejtűekben elengedhetetlen összehangolni a sejtek működését direkt és indirekt kommunikáció direkt kommunikáció: rés-illeszkedés (gap junction) 6 connexin =
Kommunikáció Sejtek közötti kommunikáció soksejtűekben elengedhetetlen összehangolni a sejtek működését direkt és indirekt kommunikáció direkt kommunikáció: rés-illeszkedés (gap junction) 6 connexin =
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét. Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet
 Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Sejtmozgás és adhézió Molekuláris biológia kurzus 8. hét Kun Lídia Genetikai, Sejt és Immunbiológiai Intézet Sejtmozgás -amőboid - csillós - kontrakció Sejt adhézió -sejt-ecm -sejt-sejt MOZGÁS A sejtmozgás
Idegsejtek közötti kommunikáció
 Idegsejtek közötti kommunikáció Idegrendszer funkcionális alapegysége: neuron (idegsejt) Neuronok morfológiája: Morfológia leírása: Soma és dendritek geometria leírása: dendritek száma, elágazások száma
Idegsejtek közötti kommunikáció Idegrendszer funkcionális alapegysége: neuron (idegsejt) Neuronok morfológiája: Morfológia leírása: Soma és dendritek geometria leírása: dendritek száma, elágazások száma
TDK lehetőségek az MTA TTK Enzimológiai Intézetben
 TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
TDK lehetőségek az MTA TTK Enzimológiai Intézetben Vértessy G. Beáta egyetemi tanár TDK mind 1-3 helyezettek OTDK Pro Scientia különdíj 1 második díj Diákjaink Eredményei Zsűri különdíj 2 első díj OTDK
A sejtfelszíni receptorok három fő kategóriája
 A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
A sejtfelszíni receptorok három fő kategóriája 1. Saját enzimaktivitás nélküli receptorok 1a. G proteinhez kapcsolt pl. adrenalin, szerotonin, glukagon, bradikinin receptorok 1b. Tirozin kinázhoz kapcsolt
MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet
 Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Modul cím: MEDICINÁLIS ALAPISMERETEK BIOKÉMIA AZ IZOMMŰKÖDÉS 1. kulcsszó cím: A SZERVEZETBEN ELŐFORDULÓ IZOM- SZÖVETEK TÍPUSAI 1. képernyő cím: Sima izomszövet G001 akaratunktól függetlenül működik; lassú,
Sejtadhézió. Sejtkapcsoló struktúrák
 Sejtadhézió Sejtkapcsoló struktúrák Sejtadhézió jelentősége: Sejtlemezek kialakulása Sejtadhézió jelentősége: Többrétegű sejtsorok kialakulása Limfociták kilépése az endotélen Rolling Adhézió Belépés homing
Sejtadhézió Sejtkapcsoló struktúrák Sejtadhézió jelentősége: Sejtlemezek kialakulása Sejtadhézió jelentősége: Többrétegű sejtsorok kialakulása Limfociták kilépése az endotélen Rolling Adhézió Belépés homing
IDEGSZÖVET 1. neuronok felépítése, típusai, végszervei 2. gliasejtek típusai és funkciója
 IDEGSZÖVET 1. neuronok felépítése, típusai, végszervei 2. gliasejtek típusai és funkciója A Golgi-impregnáció kulcsfontosságú módszer a struktúra megismerésében rer: tigroid vs Nissl rögök Tigroid: Lenhossék
IDEGSZÖVET 1. neuronok felépítése, típusai, végszervei 2. gliasejtek típusai és funkciója A Golgi-impregnáció kulcsfontosságú módszer a struktúra megismerésében rer: tigroid vs Nissl rögök Tigroid: Lenhossék
A citoszkeletális rendszer
 A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
A citoszkeletális rendszer A citoszkeletális filamentumok típusai, polimerizációja, jellemzıik, mechanikai tulajdonságaik. Asszociált fehérjék 2013.09.24. Citoszkeleton Fehérjékbıl felépülı, a sejt vázát
1. Előadás Membránok felépítése, mebrán raftok
 1. Előadás Membránok felépítése, mebrán raftok Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis biztosítása Klasszikus folyadékmozaik
1. Előadás Membránok felépítése, mebrán raftok Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis biztosítása Klasszikus folyadékmozaik
AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN
 AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN c. PhD-értekezés magyar nyelvű összefoglalója Csákvári Eszter Témavezető: Dr. Párducz Árpád Magyar Tudományos Akadémia Szegedi
AZ ÖSZTROGÉN ÉS A DEHIDROEPIANDROSZTERON SZEREPE A SZINAPTIKUS ÁTRENDEZŐDÉSBEN c. PhD-értekezés magyar nyelvű összefoglalója Csákvári Eszter Témavezető: Dr. Párducz Árpád Magyar Tudományos Akadémia Szegedi
IONCSATORNÁK. I. Szelektivitás és kapuzás. III. Szabályozás enzimek és alegységek által. IV. Akciós potenciál és szinaptikus átvitel
 IONCSATORNÁK I. Szelektivitás és kapuzás II. Struktúra és funkció III. Szabályozás enzimek és alegységek által IV. Akciós potenciál és szinaptikus átvitel V. Ioncsatornák és betegségek VI. Ioncsatornák
IONCSATORNÁK I. Szelektivitás és kapuzás II. Struktúra és funkció III. Szabályozás enzimek és alegységek által IV. Akciós potenciál és szinaptikus átvitel V. Ioncsatornák és betegségek VI. Ioncsatornák
A kémiai szinapszis (alapok)
 A preszinapszis A kémiai szinapszis (alapok) preszinaptikus neuron 1 akciós potenciál 2 Ca 2+ axon végbunkó (preszinapszis) Ca 2+ szinaptikus vezikula feszültség-függő Ca 2+ csatorna citoplazma szinaptikus
A preszinapszis A kémiai szinapszis (alapok) preszinaptikus neuron 1 akciós potenciál 2 Ca 2+ axon végbunkó (preszinapszis) Ca 2+ szinaptikus vezikula feszültség-függő Ca 2+ csatorna citoplazma szinaptikus
A transzportfolyamatok és a sejtek közötti kommunikáció
 A transzportfolyamatok és a sejtek közötti kommunikáció A sejtmembrán I.véd II.szelektál (átmenő anyagtranszport szigorúan szabályozott) III.elválaszt (barrier) extracelluláris (sejten kívüli) intracelluláris
A transzportfolyamatok és a sejtek közötti kommunikáció A sejtmembrán I.véd II.szelektál (átmenő anyagtranszport szigorúan szabályozott) III.elválaszt (barrier) extracelluláris (sejten kívüli) intracelluláris
Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet
 Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet Az ioncsatorna fehérjék szerkezete, működése és szabályozása Panyi György www.biophys.dote.hu Mesterséges membránok
Debreceni Egyetem Orvos- és Egészségtudományi Centrum Biofizikai és Sejtbiológiai Intézet Az ioncsatorna fehérjék szerkezete, működése és szabályozása Panyi György www.biophys.dote.hu Mesterséges membránok
Az idegi működés strukturális és sejtes alapjai
 Az idegi működés strukturális és sejtes alapjai Élettani és Neurobiológiai Tanszék MTA-ELTE NAP B Idegi Sejtbiológiai Kutatócsoport Schlett Katalin a kurzus anyaga elérhető: http://physiology.elte.hu/agykutatas.html
Az idegi működés strukturális és sejtes alapjai Élettani és Neurobiológiai Tanszék MTA-ELTE NAP B Idegi Sejtbiológiai Kutatócsoport Schlett Katalin a kurzus anyaga elérhető: http://physiology.elte.hu/agykutatas.html
AZ IDEGSZÖVET Halasy Katalin
 1 AZ IDEGSZÖVET Halasy Katalin Az idegszövet elektromos impulzusok generálására és gyors továbbítására specializálódott szövetféleség, idegsejtekből és gliasejtekből épül fel. Az egyedfejlődés során a
1 AZ IDEGSZÖVET Halasy Katalin Az idegszövet elektromos impulzusok generálására és gyors továbbítására specializálódott szövetféleség, idegsejtekből és gliasejtekből épül fel. Az egyedfejlődés során a
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: TÁMOP-4.1.2-08/1/A-2009-0011 Az orvosi
8. előadás. Sejt-sejt kommunikáció és jelátvitel
 8. előadás Sejt-sejt kommunikáció és jelátvitel A sejt-sejt szignalizáció evolúciója A Saccharomyces cerevisiae (sörélesztő) élesztőnek két párosodási típusa van: a és α A különböző párosodási típusokba
8. előadás Sejt-sejt kommunikáció és jelátvitel A sejt-sejt szignalizáció evolúciója A Saccharomyces cerevisiae (sörélesztő) élesztőnek két párosodási típusa van: a és α A különböző párosodási típusokba
A posztszinapszis és a PSD (posztszinaptikus. szinaptikus plaszticitásban játszott szerepük
 A posztszinapszis és a PSD (posztszinaptikus denzitás), valamint a szinaptikus plaszticitásban játszott szerepük A posztszinapszis szimmetrikus (Gray II): variábilis, nagy vezikulák; ált. gátló aszimmetrikus
A posztszinapszis és a PSD (posztszinaptikus denzitás), valamint a szinaptikus plaszticitásban játszott szerepük A posztszinapszis szimmetrikus (Gray II): variábilis, nagy vezikulák; ált. gátló aszimmetrikus
Apoptózis. 1. Bevezetés 2. Külső jelút 3. Belső jelút
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag 1. Kondenzálódó sejtmag apoptózis autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita
Ca 2+ Transients in Astrocyte Fine Processes Occur Via Ca 2+ Influx in the Adult Mouse Hippocampus
 Ca 2+ Transients in Astrocyte Fine Processes Occur Via Ca 2+ Influx in the Adult Mouse Hippocampus Ravi L. Rungta, Louis-Philippe Bernier, Lasse Dissing-Olesen, Christopher J. Groten,Jeffrey M. LeDue,
Ca 2+ Transients in Astrocyte Fine Processes Occur Via Ca 2+ Influx in the Adult Mouse Hippocampus Ravi L. Rungta, Louis-Philippe Bernier, Lasse Dissing-Olesen, Christopher J. Groten,Jeffrey M. LeDue,
Jelutak. Apoptózis. Apoptózis Bevezetés 2. Külső jelút 3. Belső jelút. apoptózis autofágia nekrózis. Sejtmag. Kondenzálódó sejtmag
 Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
Jelutak Apoptózis 1. Bevezetés 2. Külső jelút 3. Belső jelút Apoptózis Sejtmag Kondenzálódó sejtmag 1. autofágia nekrózis Lefűződések Összezsugorodás Fragmentálódó sejtmag Apoptotikus test Fagocita bekebelezi
A T sejt receptor (TCR) heterodimer
 Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
Immunbiológia - II A T sejt receptor (TCR) heterodimer 1 kötőhely lánc lánc 14. kromoszóma 7. kromoszóma V V C C EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL lánc: VJ régió lánc: VDJ régió Nincs szomatikus
16. A sejtek kommunikációja: jelátviteli folyamatok (szignál-transzdukció)
 16. A sejtek kommunikációja: jelátviteli folyamatok (szignál-transzdukció) 2016. február 25. Lippai Mónika lippai@elte.hu Minden sejt érzékel többféle, más sejtek által kibocsájtott jelmolekulát. - A jeleket
16. A sejtek kommunikációja: jelátviteli folyamatok (szignál-transzdukció) 2016. február 25. Lippai Mónika lippai@elte.hu Minden sejt érzékel többféle, más sejtek által kibocsájtott jelmolekulát. - A jeleket
A transzportfolyamatok és a sejtek közötti kommunikáció
 A transzportfolyamatok és a sejtek közötti kommunikáció A sejtmembrán protektív és szelektív barrier kompartmentalizáció: sejtfelszín és sejtorganellumok borítása 1926 szénhidrát 1943 zsírsav 1972 poláros
A transzportfolyamatok és a sejtek közötti kommunikáció A sejtmembrán protektív és szelektív barrier kompartmentalizáció: sejtfelszín és sejtorganellumok borítása 1926 szénhidrát 1943 zsírsav 1972 poláros
A tanulási és emlékezési zavarok pathofiziológiája. Szeged,
 A tanulási és emlékezési zavarok pathofiziológiája Szeged, 2015.09.09 Szerkezet, működés, információáramlás, memória, tanulás: 1. Neokortex 2. Limbikus rendszer Limbikus rendszer és a memória Paul Broca
A tanulási és emlékezési zavarok pathofiziológiája Szeged, 2015.09.09 Szerkezet, működés, információáramlás, memória, tanulás: 1. Neokortex 2. Limbikus rendszer Limbikus rendszer és a memória Paul Broca
A somatomotoros rendszer
 A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
A somatomotoros rendszer Motoneuron 1 Neuromuscularis junctio (NMJ) Vázizom A somatomotoros rendszer 1 Neurotranszmitter: Acetil-kolin Mire hat: Nikotinos kolinerg-receptor (nachr) Izom altípus A parasympathicus
Receptorok és szignalizációs mechanizmusok
 Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Molekuláris sejtbiológia: Receptorok és szignalizációs mechanizmusok Dr. habil Kőhidai László Semmelweis Egyetem Genetikai, Sejt- és Immunbiológiai Intézet Sejtek szignalizációs kapcsolatai Sejtek szignalizációs
Élettan. előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45
 Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
Élettan előadás tárgykód: bf1c1b10 ELTE TTK, fizika BSc félév: 2015/2016., I. időpont: csütörtök, 8:15 9:45 oktató: Dr. Tóth Attila, adjunktus ELTE TTK Biológiai Intézet, Élettani és Neurobiológiai tanszék
A sejtek közötti kommunikáció módjai és mechanizmusa. kommunikáció a szomszédos vagy a távoli sejtek között intracellulári jelátviteli folyamatok
 A sejtek közötti kommunikáció módjai és mechanizmusa kommunikáció a szomszédos vagy a távoli sejtek között intracellulári jelátviteli folyamatok A kommunikáció módjai szomszédos sejtek esetén autokrin
A sejtek közötti kommunikáció módjai és mechanizmusa kommunikáció a szomszédos vagy a távoli sejtek között intracellulári jelátviteli folyamatok A kommunikáció módjai szomszédos sejtek esetén autokrin
Sejt - kölcsönhatások. az idegrendszerben és az immunrendszerben
 Sejt - kölcsönhatások az idegrendszerben és az immunrendszerben A sejttől a szervezetig A sejtek között, ill. a sejtek és környezetük közötti jelátviteli folyamatok összessége az a struktúrált kölcsönhatásrendszer,
Sejt - kölcsönhatások az idegrendszerben és az immunrendszerben A sejttől a szervezetig A sejtek között, ill. a sejtek és környezetük közötti jelátviteli folyamatok összessége az a struktúrált kölcsönhatásrendszer,
Signáltranszdukciós útvonalak: Kívülről jövő információ aktiválja őket Sejtben keletkező metabolit aktiválja őket (mindkettő)
 Szignáltranszdukció Signáltranszdukciós útvonalak: Kívülről jövő információ aktiválja őket Sejtben keletkező metabolit aktiválja őket (mindkettő) Információ átvitel másodlagos hírvivőkkel vagy fehérje-fehérje
Szignáltranszdukció Signáltranszdukciós útvonalak: Kívülről jövő információ aktiválja őket Sejtben keletkező metabolit aktiválja őket (mindkettő) Információ átvitel másodlagos hírvivőkkel vagy fehérje-fehérje
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA NOVEMBER
 Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
Asztroglia Ca 2+ szignál szerepe az Alzheimer kórban FAZEKAS CSILLA LEA 2017. NOVEMBER Az Alzheimer kór Neurodegeneratív betegség Gyógyíthatatlan 65 év felettiek Kezelés: vakcinákkal inhibitor molekulákkal
A Földön előforduló sejtek (pro- és eukarioták) közös és eltérő tulajdonságai. A sejtes szerveződés evolúciója.
 A tárgy neve: Sejtbiológia előadás 1. Jellege: Törzs Gazda tanszék: Állattani és Sejtbiológiai Tanszék Felelős oktató: Dr. Gulya Károly Kredit: 2 Heti óraszám: 2 Típus: előadás Számonkérés: K A Földön
A tárgy neve: Sejtbiológia előadás 1. Jellege: Törzs Gazda tanszék: Állattani és Sejtbiológiai Tanszék Felelős oktató: Dr. Gulya Károly Kredit: 2 Heti óraszám: 2 Típus: előadás Számonkérés: K A Földön
-Két fő korlát: - asztrogliák rendkívüli morfológiája -Ca szignálok értelmezési nehézségei
 Nature reviewes 2015 - ellentmondás: az asztrociták relatív lassú és térben elkent Ca 2+ hullámokkal kommunikálnak a gyors és pontos neuronális körökkel - minőségi ugrás kell a kísérleti és analitikai
Nature reviewes 2015 - ellentmondás: az asztrociták relatív lassú és térben elkent Ca 2+ hullámokkal kommunikálnak a gyors és pontos neuronális körökkel - minőségi ugrás kell a kísérleti és analitikai
NÖVÉNYGENETIKA. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP /1/A
 NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
NÖVÉNYGENETIKA Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 A NÖVÉNYI TÁPANYAG TRANSZPORTEREK az előadás áttekintése A tápionok útja a növényben Növényi tápionok passzív és
2006 1. Nemszinaptikus receptorok és szubmikronos Ca2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra.
 2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
2006 1. Nemszinaptikus receptorok és szubmikronos Ca 2+ válaszok: A két-foton lézermikroszkópia felhasználása a farmakológiai vizsgálatokra. A kutatócsoportunkban Közép Európában elsőként bevezetett két-foton
(1) A T sejtek aktiválása (2) Az ön reaktív T sejtek toleranciája. α lánc. β lánc. V α. V β. C β. C α.
 Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
Immunbiológia II A T sejt receptor () heterodimer α lánc kötőhely β lánc 14. kromoszóma 7. kromoszóma 1 V α V β C α C β EXTRACELLULÁRIS TÉR SEJTMEMBRÁN CITOSZÓL αlánc: VJ régió β lánc: VDJ régió Nincs
A posztszinapszis és a PSD (posztszinaptikus. szinaptikus plaszticitásban játszott szerepük
 A posztszinapszis és a PSD (posztszinaptikus denzitás), valamint a szinaptikus plaszticitásban játszott szerepük A posztszinapszis szimmetrikus (Gray II): variábilis, nagy vezikulák; ált. gátló aszimmetrikus
A posztszinapszis és a PSD (posztszinaptikus denzitás), valamint a szinaptikus plaszticitásban játszott szerepük A posztszinapszis szimmetrikus (Gray II): variábilis, nagy vezikulák; ált. gátló aszimmetrikus
NÖVÉNYÉLETTAN. Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010
 NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
NÖVÉNYÉLETTAN Az Agrármérnöki MSc szak tananyagfejlesztése TÁMOP-4.1.2-08/1/A-2009-0010 Sejtfal szintézis és megnyúlás Környezeti tényezők hatása a növények növekedésére és fejlődésére Előadás áttekintése
JELUTAK 1. A Sejtkommunikáció Alapjai: Általános lapelvek
 JELUTAK 1. A Sejtkommunikáció Alapjai: Általános lapelvek 1 ÖSSZ-TARTALOM: 1. Az alapok 1. Előadás 2. A jelutak komponensei 1. Előadás 3. Főbb jelutak 2. Előadás 4. Idegi kommunikáció 3. Előadás TARTALOM
JELUTAK 1. A Sejtkommunikáció Alapjai: Általános lapelvek 1 ÖSSZ-TARTALOM: 1. Az alapok 1. Előadás 2. A jelutak komponensei 1. Előadás 3. Főbb jelutak 2. Előadás 4. Idegi kommunikáció 3. Előadás TARTALOM
Hemoglobin - myoglobin. Konzultációs e-tananyag Szikla Károly
 Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
Hemoglobin - myoglobin Konzultációs e-tananyag Szikla Károly Myoglobin A váz- és szívizom oxigén tároló fehérjéje Mt.: 17.800 153 aminosavból épül fel A lánc kb 75 % a hélix 8 db hélix, köztük nem helikális
sejt működés jovo.notebook March 13, 2018
 1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
1 A R É F Z S O I B T S Z E S R V E Z D É S I S E Z I N E T E K M O I B T O V N H C J W W R X S M R F Z Ö R E W T L D L K T E I A D Z W I O S W W E T H Á E J P S E I Z Z T L Y G O A R B Z M L A H E K J
Natív antigének felismerése. B sejt receptorok, immunglobulinok
 Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
Natív antigének felismerése B sejt receptorok, immunglobulinok B és T sejt receptorok A B és T sejt receptorok is az immunglobulin fehérje család tagjai A TCR nem ismeri fel az antigéneket, kizárólag az
transzláció DNS RNS Fehérje A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti fehérjék, transzportfehérjék
 Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
Transzláció A molekuláris biológia centrális dogmája transzkripció transzláció DNS RNS Fehérje replikáció Reverz transzkriptáz A fehérjék jelenléte nélkülözhetetlen minden sejt számára: enzimek, szerkezeti
3. Főbb Jelutak. 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3.
 Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Jelutak 3. Főbb Jelutak 1. G protein-kapcsolt receptor által közvetített jelutak 2. Enzim-kapcsolt receptorok által közvetített jelutak 3. Egyéb jelutak I. G-protein-kapcsolt receptorok 1. által közvetített
Immunológia alapjai. 10. előadás. Komplement rendszer
 Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
Immunológia alapjai 10. előadás Komplement rendszer A gyulladás molekuláris mediátorai: Miért fontos a komplement rendszer? A veleszületett (nem-specifikus) immunválasz része Azonnali válaszreakció A veleszületett
A glükóz reszintézise.
 A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
A glükóz reszintézise. A glükóz reszintézise. A reszintézis nem egyszerű megfordítása a glikolízisnek. A glikolízis 3 irrevezibilis lépése más úton játszódik le. Ennek oka egyrészt energetikai, másrészt
Az idegsejtek diverzitása
 Az idegsejtek diverzitása Készítette Dr. Nusser Zoltán előadása és megadott szakirodalma alapján Walter Fruzsina II. éves PhD hallgató A neurobiológia hajnalán az első idegtudománnyal foglalkozó kutatók
Az idegsejtek diverzitása Készítette Dr. Nusser Zoltán előadása és megadott szakirodalma alapján Walter Fruzsina II. éves PhD hallgató A neurobiológia hajnalán az első idegtudománnyal foglalkozó kutatók
Szinaptikus folyamatok
 Szinaptikus folyamatok Jelátvitel az idegrendszerben Elektromos szinapszisok Kémiai szinapszisok Neurotranszmitterek és receptoraik Szinaptikus integráció Szinaptikus plaszticitás Kettős információátvitel
Szinaptikus folyamatok Jelátvitel az idegrendszerben Elektromos szinapszisok Kémiai szinapszisok Neurotranszmitterek és receptoraik Szinaptikus integráció Szinaptikus plaszticitás Kettős információátvitel
Az ioncsatorna fehérjék szerkezete, működése és szabályozása. A patch-clamp technika
 Az ioncsatorna fehérjék szerkezete, működése és szabályozása. A patch-clamp technika Panyi György 2014. November 12. Mesterséges membránok ionok számára átjárhatatlanok Iontranszport a membránon keresztül:
Az ioncsatorna fehérjék szerkezete, működése és szabályozása. A patch-clamp technika Panyi György 2014. November 12. Mesterséges membránok ionok számára átjárhatatlanok Iontranszport a membránon keresztül:
Degeneráció és regeneráció az idegrendszerben
 Degeneráció és regeneráció az idegrendszerben Axonális sérülés és regeneráció August Waller, 1850: Waller-féle degeneráció (Wallerian degeneration) disztális axonális csonk: degeneráció 24-36 órán belül
Degeneráció és regeneráció az idegrendszerben Axonális sérülés és regeneráció August Waller, 1850: Waller-féle degeneráció (Wallerian degeneration) disztális axonális csonk: degeneráció 24-36 órán belül
Vezikuláris transzport
 Molekuláris Sejtbiológia Vezikuláris transzport Dr. habil KŐHIDAI László Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. november 3. Intracelluláris vezikul uláris transzport Kommunikáció
Molekuláris Sejtbiológia Vezikuláris transzport Dr. habil KŐHIDAI László Semmelweis Egyetem, Genetikai, Sejt- és Immunbiológiai Intézet 2005. november 3. Intracelluláris vezikul uláris transzport Kommunikáció
A GLIASEJTEK ÉS AZ EPILEPTIKUS AKTIVITÁS KAPCSOLATA GÁSPÁR ATTILA GLIA SEJTEK ÉLETTANA EA
 A GLIASEJTEK ÉS AZ EPILEPTIKUS AKTIVITÁS KAPCSOLATA GÁSPÁR ATTILA GLIA SEJTEK ÉLETTANA EA 2017.11.14. AZ ASZTROGLIA SEJTEK FONTOSABB TULAJDONSÁGAI AZ EPILEPTIKUS AKTIVITÁS SZEMPONTJÁBÓL (Devinsky és mtsai.,
A GLIASEJTEK ÉS AZ EPILEPTIKUS AKTIVITÁS KAPCSOLATA GÁSPÁR ATTILA GLIA SEJTEK ÉLETTANA EA 2017.11.14. AZ ASZTROGLIA SEJTEK FONTOSABB TULAJDONSÁGAI AZ EPILEPTIKUS AKTIVITÁS SZEMPONTJÁBÓL (Devinsky és mtsai.,
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói
 1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
1. előadás Membránok felépítése, mebrán raftok, caveolák jellemzője, funkciói Plazmamembrán Membrán funkciói: sejt integritásának fenntartása állandó hő, energia, és információcsere biztosítása homeosztázis
Új szignalizációs utak a prodromális fázisban. Oláh Zita
 Új szignalizációs utak a prodromális fázisban Oláh Zita 2015.10.07 Prodromális fázis Prodromalis fázis: De mi történik?? Beta-amiloid: OK vagy OKOZAT? Beta-amiloid hogyan okozhat neurodegenerációt? Tau
Új szignalizációs utak a prodromális fázisban Oláh Zita 2015.10.07 Prodromális fázis Prodromalis fázis: De mi történik?? Beta-amiloid: OK vagy OKOZAT? Beta-amiloid hogyan okozhat neurodegenerációt? Tau
A citoszkeleton Eukarióta sejtváz
 A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
A citoszkeleton Eukarióta sejtváz - Alak és belső szerkezet - Rugalmas struktúra sejt izomzat - Fehérjékből épül fel A citoszkeleton háromféle filamentumból épül fel Intermedier filamentum mikrotubulus
Jelátviteli útvonalak 1
 Jelátviteli útvonalak 1 Információ metabolizmus Szignál transzdukció 1 Jelátviteli séma Mi lehet a jel? Hormonok Növekedési faktorok Fejlődési szignálok Neurotranszmitterek Antigének Sejtfelszíni glikoproteinek
Jelátviteli útvonalak 1 Információ metabolizmus Szignál transzdukció 1 Jelátviteli séma Mi lehet a jel? Hormonok Növekedési faktorok Fejlődési szignálok Neurotranszmitterek Antigének Sejtfelszíni glikoproteinek
Immunológia alapjai. Az immunválasz szupressziója Előadás. A szupresszióban részt vevő sejtes és molekuláris elemek
 Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Immunológia alapjai 19 20. Előadás Az immunválasz szupressziója A szupresszióban részt vevő sejtes és molekuláris elemek Mi a szupresszió? Általános biológiai szabályzó funkció. Az immunszupresszió az
Ioncsatorna szerkezetek
 Jellegzetes Ioncsatorna szerkezetek Ördög Balázs Farmakológiai és Farmakoterápiai Intézet Kapuzás Feszültség szabályozott Voltage-gated Fesz. szab. Na +, +, Ca 2+ 2+,, K + + csatornák channels Transiens
Jellegzetes Ioncsatorna szerkezetek Ördög Balázs Farmakológiai és Farmakoterápiai Intézet Kapuzás Feszültség szabályozott Voltage-gated Fesz. szab. Na +, +, Ca 2+ 2+,, K + + csatornák channels Transiens
JELUTAK 2. A Jelutak Komponensei
 JELUTAK 2. A Jelutak Komponensei TARTALOM - 1. Előadás: A jelutak komponensei 1. Egy egyszerű jelösvény 2. Jelmolekulák 3. Receptorok 4. Intracelluláris jelmolekulák 1 1.1. Egy tipikus jelösvény sémája
JELUTAK 2. A Jelutak Komponensei TARTALOM - 1. Előadás: A jelutak komponensei 1. Egy egyszerű jelösvény 2. Jelmolekulák 3. Receptorok 4. Intracelluláris jelmolekulák 1 1.1. Egy tipikus jelösvény sémája
Immunológiai módszerek a klinikai kutatásban
 Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
Immunológiai módszerek a klinikai kutatásban 3. előadás Az immunrendszer molekuláris elemei: antigén, ellenanyag, Ig osztályok Az antigén meghatározása Detre László: antitest generátor - Régi meghatározás:
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, )
 A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
A CITOSZKELETÁLIS RENDSZER (Nyitrai Miklós, 2010.11.30.) 1. Mi a citoszkeleton? 2. Polimerizá, polimerizás egyensúly 3. ilamentumok osztályozása 4. Motorfehérjék Citoszkeleton Eukariota sejtek dinamikus
Darvas Zsuzsa László Valéria. Sejtbiológia. Negyedik, átdolgozott kiadás
 Darvas Zsuzsa László Valéria Sejtbiológia Negyedik, átdolgozott kiadás Írták: DR. DARVAS ZSUZSA egyetemi docens Semmelweis Egyetem Genetikai, Sejtés Immunbiológiai Intézet DR. LÁSZLÓ VALÉRIA egyetemi docens
Darvas Zsuzsa László Valéria Sejtbiológia Negyedik, átdolgozott kiadás Írták: DR. DARVAS ZSUZSA egyetemi docens Semmelweis Egyetem Genetikai, Sejtés Immunbiológiai Intézet DR. LÁSZLÓ VALÉRIA egyetemi docens
Az endomembránrendszer részei.
 Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
Az endomembránrendszer Szerkesztette: Vizkievicz András Az eukarióta sejtek prokarióta sejtektől megkülönböztető egyik alapvető sajátságuk a belső membránrendszerük. A belső membránrendszer szerkezete
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül.
 7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
7. előadás: A plazma mebrán szerkezete és funkciója. Anyagtranszport a plazma membránon keresztül. A plazma membrán határolja el az élő sejteket a környezetüktől Szelektív permeabilitást mutat, így lehetővé
Membránpotenciál, akciós potenciál
 A nyugalmi membránpotenciál Membránpotenciál, akciós potenciál Fizika-Biofizika 2015.november 3. Nyugalomban valamennyi sejt belseje negatív a külső felszínhez képest: negatív nyugalmi potenciál (Em: -30
A nyugalmi membránpotenciál Membránpotenciál, akciós potenciál Fizika-Biofizika 2015.november 3. Nyugalomban valamennyi sejt belseje negatív a külső felszínhez képest: negatív nyugalmi potenciál (Em: -30
Idegrendszer egyedfejlődése. Az idegszövet jellemzése
 Idegrendszer egyedfejlődése. Az idegszövet jellemzése Központi idegrendszer egyedfejlődése: Ektoderma dorsális részéből velőcső Velőcső középső és hátsó részéből: gerincvelő Velőcső elülső részéből 3 agyhólyag:
Idegrendszer egyedfejlődése. Az idegszövet jellemzése Központi idegrendszer egyedfejlődése: Ektoderma dorsális részéből velőcső Velőcső középső és hátsó részéből: gerincvelő Velőcső elülső részéből 3 agyhólyag:
AZ IDEGSEJTEK KÖZTI SZINAPTIKUS KOMMUNIKÁCIÓ Hájos Norbert. Összefoglaló
 AZ IDEGSEJTEK KÖZTI SZINAPTIKUS KOMMUNIKÁCIÓ Hájos Norbert Összefoglaló Az idegsejtek közt az ingerületátvitel döntően kémiai természetű, míg az idegsejten belül az elektromos jelterjedés a jellemző. A
AZ IDEGSEJTEK KÖZTI SZINAPTIKUS KOMMUNIKÁCIÓ Hájos Norbert Összefoglaló Az idegsejtek közt az ingerületátvitel döntően kémiai természetű, míg az idegsejten belül az elektromos jelterjedés a jellemző. A
SZAGLÁS 2
 AZ ÉRZÉKELÉS BIOLÓGIÁJA 1 SZAGLÁS 2 ÍZLELÉS 3 HALLÁS 4 ÉRINTÉS EGYENSÚLY 5 FÁJDALOM 6 túl az emberi érzékelésen 7 HOGYAN ALAKÍTJÁK ÁT A RECEPTOR SEJTEK A KÜLÖNBÖZŐ STIMULUSOKAT AKCIÓS POTENCIÁLLÁ? HOGYAN
AZ ÉRZÉKELÉS BIOLÓGIÁJA 1 SZAGLÁS 2 ÍZLELÉS 3 HALLÁS 4 ÉRINTÉS EGYENSÚLY 5 FÁJDALOM 6 túl az emberi érzékelésen 7 HOGYAN ALAKÍTJÁK ÁT A RECEPTOR SEJTEK A KÜLÖNBÖZŐ STIMULUSOKAT AKCIÓS POTENCIÁLLÁ? HOGYAN
Speciális működésű sejtek
 Speciális működésű sejtek Mirigysejt Izomsejt Vörösvérsejt Idegsejt Mirigysejt Kémiai anyagok termelése Váladék kibocsátása A váladék anyaga lehet: Fehérje Szénhidrát Lipid Víz+illatanyag Vörösvérsejt
Speciális működésű sejtek Mirigysejt Izomsejt Vörösvérsejt Idegsejt Mirigysejt Kémiai anyagok termelése Váladék kibocsátása A váladék anyaga lehet: Fehérje Szénhidrát Lipid Víz+illatanyag Vörösvérsejt
A jel-molekulák útja változó hosszúságú lehet. A jelátvitel. hírvivő molekula (messenger) elektromos formában kódolt információ
 A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
A jelátvitel hírvivő molekula (messenger) elektromos formában kódolt információ A jel-molekulák útja változó hosszúságú lehet 1. Endokrin szignalizáció: belső elválasztású mirigy véráram célsejt A jelátvitel:
