Bevezetés az atomfizikába
|
|
|
- Margit Bognárné
- 8 évvel ezelőtt
- Látták:
Átírás
1 az atomfizikába Berta Miklós SZE, Fizika és Kémia Tsz október 25.
2 Bevezetés Bevezetés 2 / 57
3 Bevezetés Bevezetés Makrovilág Klasszikus fizika Mikrovilág Jó-e a klasszikus fizika itt is? Túl kell lépni a klasszikus fizika keretein! 3 / 57
4 Bevezetés Bevezetés Makrovilág Klasszikus fizika Mikrovilág Jó-e a klasszikus fizika itt is? Túl kell lépni a klasszikus fizika keretein! Ezek a kísérleti tények a következő jelenségek során merültek fel: Abszolút fekete test sugárzása Fényelektromos jelenség Gázok fénykibocsájtása és fényelnyelése 3 / 57
5 Bevezetés Bevezetés Makrovilág Klasszikus fizika Mikrovilág Jó-e a klasszikus fizika itt is? Túl kell lépni a klasszikus fizika keretein! Ezek a kísérleti tények a következő jelenségek során merültek fel: Abszolút fekete test sugárzása Fényelektromos jelenség Gázok fénykibocsájtása és fényelnyelése Nincs magyarázat a klasszikus fizika keretein belül! 3 / 57
6 Bevezetés Bevezetés Makrovilág Klasszikus fizika Mikrovilág Jó-e a klasszikus fizika itt is? Túl kell lépni a klasszikus fizika keretein! Ezek a kísérleti tények a következő jelenségek során merültek fel: Abszolút fekete test sugárzása Fényelektromos jelenség Gázok fénykibocsájtása és fényelnyelése Nincs magyarázat a klasszikus fizika keretein belül! Általánosabb érvényű elmélet szükséges! 3 / 57
7 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség 4 / 57
8 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! 5 / 57
9 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! izzó vasdarab a környezettől eltérő hőmérsékletű anyagok megfigyelése infratávcsövekkel 5 / 57
10 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! izzó vasdarab a környezettől eltérő hőmérsékletű anyagok megfigyelése infratávcsövekkel Azt a sugárzót amelyik elnyeli az összes ráeső elektromágneses sugárzást abszolút fekete testnek nevezzük. 5 / 57
11 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! izzó vasdarab a környezettől eltérő hőmérsékletű anyagok megfigyelése infratávcsövekkel Azt a sugárzót amelyik elnyeli az összes ráeső elektromágneses sugárzást abszolút fekete testnek nevezzük. Az abszolút fekete test csak a rá jellemző, hőmérsékletétől függő, hőmérsékleti sugárzást bocsájt ki. 5 / 57
12 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! izzó vasdarab a környezettől eltérő hőmérsékletű anyagok megfigyelése infratávcsövekkel Azt a sugárzót amelyik elnyeli az összes ráeső elektromágneses sugárzást abszolút fekete testnek nevezzük. Az abszolút fekete test csak a rá jellemző, hőmérsékletétől függő, hőmérsékleti sugárzást bocsájt ki. Az elektromágneses sugárzás u(ν) spektrális intenzitásán az I intenzitás ν frekvencia szerinti eloszlását értjük. 5 / 57
13 Hőmérsékleti sugárzás Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az anyag T hőmérsékleten elektromágneses sugárzás forrása! izzó vasdarab a környezettől eltérő hőmérsékletű anyagok megfigyelése infratávcsövekkel Azt a sugárzót amelyik elnyeli az összes ráeső elektromágneses sugárzást abszolút fekete testnek nevezzük. Az abszolút fekete test csak a rá jellemző, hőmérsékletétől függő, hőmérsékleti sugárzást bocsájt ki. Az elektromágneses sugárzás u(ν) spektrális intenzitásán az I intenzitás ν frekvencia szerinti eloszlását értjük. u(ν) dν megadja, hogy az I intenzitású sugárzásban mekkora intenzitást képviselnek a (ν, ν + d ν) frekvenciaintervallumba eső frekvenciájú elektromágneses sugarak. 5 / 57
14 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség u(ν) T 1 < T 2 < T 3 T 1 T 2 T 3 ν 6 / 57
15 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség u(ν) T 1 < T 2 < T 3 T 1 T 2 T 3 ν Wien-féle eltolódási törvény: ν max T = konstans 6 / 57
16 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség u(ν) T 1 < T 2 < T 3 T 1 T 2 T 3 ν Wien-féle eltolódási törvény: ν max T = konstans Stefan-Boltzmann törvény: u(t) = σt 4 6 / 57
17 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség u(ν) T 1 < T 2 < T 3 T 1 T 2 T 3 ν Wien-féle eltolódási törvény: ν max T = konstans Stefan-Boltzmann törvény: u(t) = σt 4 6 / 57
18 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az abszolút fekete test mért spektrális intenzitása csak akkor magyarázható, ha feltesszük, hogy az elektromágneses mező energiakvantummal (foton) rendelkezik, melynek energiája: E ν = hν 7 / 57
19 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az abszolút fekete test mért spektrális intenzitása csak akkor magyarázható, ha feltesszük, hogy az elektromágneses mező energiakvantummal (foton) rendelkezik, melynek energiája: h-a Planck-állandó E ν = hν h = 6, Js 7 / 57
20 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Az abszolút fekete test mért spektrális intenzitása csak akkor magyarázható, ha feltesszük, hogy az elektromágneses mező energiakvantummal (foton) rendelkezik, melynek energiája: h-a Planck-állandó E ν = hν h = 6, Js Ekkor u(ν,t) = 2πhν3 c 2 (e hν kt 1) 7 / 57
21 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Compton-effektus Hullám-részecske kettősség 8 / 57
22 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Megoldás: I(T) = 0 u(ν,t)dν = 2πh c 2 0 ν 3 e hν kt 1 dν 8 / 57
23 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Megoldás: I(T) = 0 u(ν,t)dν = 2πh c 2 0 Vezessük be az x = hν kt I(T) = 2πk4 T 4 c 2 h 3 0 helyettesítést! Ekkor: x 3 e x 1 dx ν 3 e hν kt 1 dν 8 / 57
24 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Megoldás: I(T) = 0 u(ν,t)dν = 2πh c 2 0 Vezessük be az x = hν kt I(T) = 2πk4 T 4 c 2 h 3 0 helyettesítést! Ekkor: A határozott integrálok táblázatából 0 x 3 e x 1 dx x 3 e x 1 ν 3 e hν kt 1 dx = π4 15. dν 8 / 57
25 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Megoldás: I(T) = 0 u(ν,t)dν = 2πh c 2 0 Vezessük be az x = hν kt I(T) = 2πk4 T 4 c 2 h 3 0 helyettesítést! Ekkor: A határozott integrálok táblázatából 0 Tehát: I(T) = σt 4, x 3 e x 1 dx x 3 e x 1 ν 3 e hν kt 1 dx = π4 15. dν ahol σ = 2π5 k 4 15c 2 h 3 = 5, W.m 2.K 4. 8 / 57
26 Példa Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Határozza meg az abszolút fekete test sugárzásának intenzitását T hőmérsékleten! Megoldás: I(T) = 0 u(ν,t)dν = 2πh c 2 0 Vezessük be az x = hν kt I(T) = 2πk4 T 4 c 2 h 3 0 helyettesítést! Ekkor: A határozott integrálok táblázatából 0 Tehát: I(T) = σt 4, x 3 e x 1 dx x 3 e x 1 ν 3 e hν kt 1 dx = π4 15. dν ahol σ = 2π5 k 4 15c 2 h 3 = 5, W.m 2.K 4. A Planck által a kvantumhipotézis alapján talált összefüggésből tehát következik a Stefan-Boltzmann törvény. 8 / 57
27 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. 9 / 57
28 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. Csak bizonyos frekvenciánál nagyobb frekvenciájú sugárzás hatására válnak ki az anyagból a fotoelektronoknak elnevezett részecskék. 9 / 57
29 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. Csak bizonyos frekvenciánál nagyobb frekvenciájú sugárzás hatására válnak ki az anyagból a fotoelektronoknak elnevezett részecskék. A kilépő elektronok mozgási energiája csak a beeső monokromatikus sugárzás frekvenciájától függ, és független a sugárzás intenzitásától. 9 / 57
30 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. Csak bizonyos frekvenciánál nagyobb frekvenciájú sugárzás hatására válnak ki az anyagból a fotoelektronoknak elnevezett részecskék. A kilépő elektronok mozgási energiája csak a beeső monokromatikus sugárzás frekvenciájától függ, és független a sugárzás intenzitásától. Az intenzitás növelése csak a kilépő elektronok számát növelte, és semmilyen hatással nem volt az energiájukra. 9 / 57
31 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. Csak bizonyos frekvenciánál nagyobb frekvenciájú sugárzás hatására válnak ki az anyagból a fotoelektronoknak elnevezett részecskék. A kilépő elektronok mozgási energiája csak a beeső monokromatikus sugárzás frekvenciájától függ, és független a sugárzás intenzitásától. Az intenzitás növelése csak a kilépő elektronok számát növelte, és semmilyen hatással nem volt az energiájukra. Albert Einstein a kvantumhipotézist használta a fényelektromos jelenség magyarázatára. 9 / 57
32 Fényelektromos jelenség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Jelenség: Elektromágneses sugarak anyaggal (fémekkel) való kölcsönhatása. Csak bizonyos frekvenciánál nagyobb frekvenciájú sugárzás hatására válnak ki az anyagból a fotoelektronoknak elnevezett részecskék. A kilépő elektronok mozgási energiája csak a beeső monokromatikus sugárzás frekvenciájától függ, és független a sugárzás intenzitásától. Az intenzitás növelése csak a kilépő elektronok számát növelte, és semmilyen hatással nem volt az energiájukra. Albert Einstein a kvantumhipotézist használta a fényelektromos jelenség magyarázatára. hν = A m ev 2 9 / 57
33 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Fény Fotocella Anód G U 10 / 57
34 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Fény Fotocella Anód G U Kísérleti elrendezés, amelyik lehetővé teszi a fotoelektronok mozgási energiájának mérését. 10 / 57
35 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Fény Fotocella Anód G U Kísérleti elrendezés, amelyik lehetővé teszi a fotoelektronok mozgási energiájának mérését. A fémből készült anódra beeső fény váltja ki a fotoelektronokat. 10 / 57
36 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Fény Fotocella Anód G U Kísérleti elrendezés, amelyik lehetővé teszi a fotoelektronok mozgási energiájának mérését. A fémből készült anódra beeső fény váltja ki a fotoelektronokat. Ezek a változtatható feszültségű ellentérben lassulnak, míg egy bizonyos feszültség mellett, amit lezárási feszültségnek hívunk (U 0 ), az áram az áramkörben nullára esik, amit a galvanométer jelez. 10 / 57
37 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Amikor az áram az aramkörben nulla, akkor az ellentérrel szemben végzett munka egyenlő az elektronok mozgási energiájával. 11 / 57
38 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Amikor az áram az aramkörben nulla, akkor az ellentérrel szemben végzett munka egyenlő az elektronok mozgási energiájával. eu 0 = 1 2 mv2 A fotoeffektus kísérleti tanulmányozása során vizsgálták azt is, hogy miként függ a lezárási feszültség a beeső fény frekvenciájától. 11 / 57
39 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Amikor az áram az aramkörben nulla, akkor az ellentérrel szemben végzett munka egyenlő az elektronok mozgási energiájával. eu 0 = 1 2 mv2 A fotoeffektus kísérleti tanulmányozása során vizsgálták azt is, hogy miként függ a lezárási feszültség a beeső fény frekvenciájától. U 0 α A e tan (α) = h e ν 11 / 57
40 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Amikor az áram az aramkörben nulla, akkor az ellentérrel szemben végzett munka egyenlő az elektronok mozgási energiájával. eu 0 = 1 2 mv2 A fotoeffektus kísérleti tanulmányozása során vizsgálták azt is, hogy miként függ a lezárási feszültség a beeső fény frekvenciájától. U 0 α A e tan (α) = h e ν U 0 (ν) = h e ν + A e 11 / 57
41 Compton-effektus Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Meglepetést jelentett az a megfigyelés, hogy az anyag elektronjain a néhány kev energiájú fotonok szóródásakor megváltozik azok frekvenciája, és így energiája is. 12 / 57
42 Compton-effektus Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Meglepetést jelentett az a megfigyelés, hogy az anyag elektronjain a néhány kev energiájú fotonok szóródásakor megváltozik azok frekvenciája, és így energiája is. 1 ev energiára tesz szert egy elektron, ha 1 V feszültség gyorsítja. 1 ev = 1, J. 12 / 57
43 Compton-effektus Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Meglepetést jelentett az a megfigyelés, hogy az anyag elektronjain a néhány kev energiájú fotonok szóródásakor megváltozik azok frekvenciája, és így energiája is. 1 ev energiára tesz szert egy elektron, ha 1 V feszültség gyorsítja. 1 ev = 1, J. szórt foton E γ E γ beeső foton Θ ϕ elektron E e 12 / 57
44 Compton-effektus Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Meglepetést jelentett az a megfigyelés, hogy az anyag elektronjain a néhány kev energiájú fotonok szóródásakor megváltozik azok frekvenciája, és így energiája is. 1 ev energiára tesz szert egy elektron, ha 1 V feszültség gyorsítja. 1 ev = 1, J. szórt foton E γ E γ beeső foton Θ ϕ elektron E e 12 / 57
45 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. 13 / 57
46 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. Feltette, hogy a fotonnak hν impulzusa van, és tökéletesen c = h λ rugalmasan ütközik az elektronnal. 13 / 57
47 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. Feltette, hogy a fotonnak hν impulzusa van, és tökéletesen c = h λ rugalmasan ütközik az elektronnal. Compton tehát feltételezte az energiamegmaradás tételének és az impulzusmegmaradás tételének érvényességét a folyamatban. 13 / 57
48 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. Feltette, hogy a fotonnak hν impulzusa van, és tökéletesen c = h λ rugalmasan ütközik az elektronnal. Compton tehát feltételezte az energiamegmaradás tételének és az impulzusmegmaradás tételének érvényességét a folyamatban. p γ = p γ + p e 13 / 57
49 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. Feltette, hogy a fotonnak hν impulzusa van, és tökéletesen c = h λ rugalmasan ütközik az elektronnal. Compton tehát feltételezte az energiamegmaradás tételének és az impulzusmegmaradás tételének érvényességét a folyamatban. p γ = p γ + p e E γ + m e c 2 = E γ + E e 13 / 57
50 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton a jelenség magyarázatakor a kvantumhipotézisből indult ki. Feltette, hogy a fotonnak hν impulzusa van, és tökéletesen c = h λ rugalmasan ütközik az elektronnal. Compton tehát feltételezte az energiamegmaradás tételének és az impulzusmegmaradás tételének érvényességét a folyamatban. p γ = p γ + p e E γ + m e c 2 = E γ + E e A relativitás elméletéből tudjuk, hogy egy részecske energiája és impulzusa között a következő összefüggés áll fenn: E 2 = p 2 c 2 + m 2 0c / 57
51 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Θ p γ ϕ Θ ϕ p γ p e 14 / 57
52 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Θ p γ ϕ Θ ϕ p γ p e Írjuk át az energia megmaradásának tételét az impulzus és energia közötti relativisztikus összefüggés felhasználásával: p γ c + m e c 2 = p γc + m 2 e c4 + p 2 e c2. 14 / 57
53 Hőmérsékleti sugárzás Fényelektromos jelenség Θ ϕ Θ p γ Compton-effektus Hullám-részecske kettősség p γ ϕ p e Írjuk át az energia megmaradásának tételét az impulzus és energia közötti relativisztikus összefüggés felhasználásával: p γ c + m e c 2 = p γc + m 2 e c4 + p 2 e c2. Rendezés után: p 2 e = (p γ p γ) 2 2m e c(p γ p γ). 14 / 57
54 Hőmérsékleti sugárzás Fényelektromos jelenség Θ ϕ Θ p γ Compton-effektus Hullám-részecske kettősség p γ ϕ p e Írjuk át az energia megmaradásának tételét az impulzus és energia közötti relativisztikus összefüggés felhasználásával: p γ c + m e c 2 = p γc + m 2 e c4 + p 2 e c2. Rendezés után: p 2 e = (p γ p γ) 2 2m e c(p γ p γ). A koszinusz-tétel felhasználásával az ábra alapján: p 2 e = p 2 γ + p 2 γ 2p γ p γ cos. 14 / 57
55 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség A kifejezéseket egyenlővé téve, és a kapott egyenletből a szórt foton lendületét kifejezve: p γ = 1+ p γ mec p γ (1 cos Θ). 15 / 57
56 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség A kifejezéseket egyenlővé téve, és a kapott egyenletből a szórt foton lendületét kifejezve: Mivel p = E c alakul: p γ = 1+ p γ mec p γ (1 cos Θ)., a szórt foton energiája a következő egyenlet szerint E γ = E γ 1+ E γ mec2 (1 cos Θ). 15 / 57
57 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség A kifejezéseket egyenlővé téve, és a kapott egyenletből a szórt foton lendületét kifejezve: Mivel p = E c alakul: p γ = 1+ p γ mec p γ (1 cos Θ)., a szórt foton energiája a következő egyenlet szerint E γ = 1+ E γ mec2 (1 cos Θ). Az előzőek alapján kiszámítható a foton hullámhosszának megváltozása is: E γ λ = h m e (1 cos). c 15 / 57
58 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség A kifejezéseket egyenlővé téve, és a kapott egyenletből a szórt foton lendületét kifejezve: Mivel p = E c alakul: p γ = 1+ p γ mec p γ (1 cos Θ)., a szórt foton energiája a következő egyenlet szerint E γ = 1+ E γ mec2 (1 cos Θ). Az előzőek alapján kiszámítható a foton hullámhosszának megváltozása is: A h m e c E γ λ = h m e (1 cos). c kifejezést az elektron Compton-hullámhosszának nevezzük. 15 / 57
59 Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség A kifejezéseket egyenlővé téve, és a kapott egyenletből a szórt foton lendületét kifejezve: Mivel p = E c alakul: p γ = 1+ p γ mec p γ (1 cos Θ)., a szórt foton energiája a következő egyenlet szerint E γ = 1+ E γ mec2 (1 cos Θ). Az előzőek alapján kiszámítható a foton hullámhosszának megváltozása is: A h m e c E γ λ = h m e (1 cos). c kifejezést az elektron Compton-hullámhosszának nevezzük. Compton az elektromágneses hullámokhoz részecsketulajdonságokat rendelt. 15 / 57
60 Hullám-részecske kettősség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton elgondolását Louis de Broglie tette szimmetrikussá, amikor a klasszikus értelemben vett részecskékhez hullámtulajdonságokat rendelt. 16 / 57
61 Hullám-részecske kettősség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton elgondolását Louis de Broglie tette szimmetrikussá, amikor a klasszikus értelemben vett részecskékhez hullámtulajdonságokat rendelt. A foton esetében a Compton-féle hozzárendelés a következő: E = hν p = h λ. 16 / 57
62 Hullám-részecske kettősség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton elgondolását Louis de Broglie tette szimmetrikussá, amikor a klasszikus értelemben vett részecskékhez hullámtulajdonságokat rendelt. A foton esetében a Compton-féle hozzárendelés a következő: E = hν p = h λ. Louis de Broglie nem tett mást mint megfordította Compton gondolatmenetét. 16 / 57
63 Hullám-részecske kettősség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton elgondolását Louis de Broglie tette szimmetrikussá, amikor a klasszikus értelemben vett részecskékhez hullámtulajdonságokat rendelt. A foton esetében a Compton-féle hozzárendelés a következő: E = hν p = h λ. Louis de Broglie nem tett mást mint megfordította Compton gondolatmenetét. Ennek értelmében egy p impulzusú részecskének λ = h p hullámhosszúságú hullám feleltethető meg. 16 / 57
64 Hullám-részecske kettősség Bevezetés Hőmérsékleti sugárzás Fényelektromos jelenség Compton-effektus Hullám-részecske kettősség Compton elgondolását Louis de Broglie tette szimmetrikussá, amikor a klasszikus értelemben vett részecskékhez hullámtulajdonságokat rendelt. A foton esetében a Compton-féle hozzárendelés a következő: E = hν p = h λ. Louis de Broglie nem tett mást mint megfordította Compton gondolatmenetét. Ennek értelmében egy p impulzusú részecskének λ = h p hullámhosszúságú hullám feleltethető meg. 16 / 57
65 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet 17 / 57
66 Rutherford-féle atommodell Bevezetés Az elektron az elemi negatív töltés hordozója. Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet 18 / 57
67 Rutherford-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az elemi negatív töltés hordozója. Hogyan oszlik el az anyagban az elektronok negatív töltését kompenzáló pozitív töltésű alkotórész, melynek léteznie kell, mert az anyag általában elektromosan semleges? 18 / 57
68 Rutherford-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az elemi negatív töltés hordozója. Hogyan oszlik el az anyagban az elektronok negatív töltését kompenzáló pozitív töltésű alkotórész, melynek léteznie kell, mert az anyag általában elektromosan semleges? Már a kinetikus gázelméletből meg lehetett becsülni az atomok méretét. Ez m nagyságrendűnek adódott. 18 / 57
69 Rutherford-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az elemi negatív töltés hordozója. Hogyan oszlik el az anyagban az elektronok negatív töltését kompenzáló pozitív töltésű alkotórész, melynek léteznie kell, mert az anyag általában elektromosan semleges? Már a kinetikus gázelméletből meg lehetett becsülni az atomok méretét. Ez m nagyságrendűnek adódott. Thomson feltételezte, hogy a pozitív anyagrész kitölti az atomok teljes térfogatát, és az elektronok ebben vannak kötve az elektromos erők által. 18 / 57
70 Rutherford-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az elemi negatív töltés hordozója. Hogyan oszlik el az anyagban az elektronok negatív töltését kompenzáló pozitív töltésű alkotórész, melynek léteznie kell, mert az anyag általában elektromosan semleges? Már a kinetikus gázelméletből meg lehetett becsülni az atomok méretét. Ez m nagyságrendűnek adódott. Thomson feltételezte, hogy a pozitív anyagrész kitölti az atomok teljes térfogatát, és az elektronok ebben vannak kötve az elektromos erők által. A XX. század elején fedezték fel a természetes radioaktivitást. Ennek egyik komponense az α sugárzás, amely kétszeres elemi pozitív töltést hordozó részecskék árama. 18 / 57
71 Rutherford-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az elemi negatív töltés hordozója. Hogyan oszlik el az anyagban az elektronok negatív töltését kompenzáló pozitív töltésű alkotórész, melynek léteznie kell, mert az anyag általában elektromosan semleges? Már a kinetikus gázelméletből meg lehetett becsülni az atomok méretét. Ez m nagyságrendűnek adódott. Thomson feltételezte, hogy a pozitív anyagrész kitölti az atomok teljes térfogatát, és az elektronok ebben vannak kötve az elektromos erők által. A XX. század elején fedezték fel a természetes radioaktivitást. Ennek egyik komponense az α sugárzás, amely kétszeres elemi pozitív töltést hordozó részecskék árama. Ezekkel sokkal effektívebben tanulmányozható az atomszerkezet. Az α sugárzásban terjedő részecskék tömege mintegy 7340-szerese az elektron tömegének, töltésük pedig kétszeres pozitív elemi töltés. 18 / 57
72 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Rutherford az új sugárzással bombázott vékony fémfóliákat, és arra volt kíváncsi, mennyiben tér el a fólia mögötti szórási kép attól, amit katódsugarak esetében tapasztaltak. 19 / 57
73 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Rutherford az új sugárzással bombázott vékony fémfóliákat, és arra volt kíváncsi, mennyiben tér el a fólia mögötti szórási kép attól, amit katódsugarak esetében tapasztaltak. A várakozásokkal ellentétben átlagosan minden dik α rész visszapattant a fóliáról. 19 / 57
74 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Rutherford az új sugárzással bombázott vékony fémfóliákat, és arra volt kíváncsi, mennyiben tér el a fólia mögötti szórási kép attól, amit katódsugarak esetében tapasztaltak. A várakozásokkal ellentétben átlagosan minden dik α rész visszapattant a fóliáról. Rutherford a jelenséget azzal a feltételezéssel magyarázta, hogy az atom pozitív része nem tölti ki az atom teljes térfogatát, hanem az atom közepén helyezkedik el. Ez az atommag. 19 / 57
75 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Rutherford az új sugárzással bombázott vékony fémfóliákat, és arra volt kíváncsi, mennyiben tér el a fólia mögötti szórási kép attól, amit katódsugarak esetében tapasztaltak. A várakozásokkal ellentétben átlagosan minden dik α rész visszapattant a fóliáról. Rutherford a jelenséget azzal a feltételezéssel magyarázta, hogy az atom pozitív része nem tölti ki az atom teljes térfogatát, hanem az atom közepén helyezkedik el. Ez az atommag. A Rutherford-féle kísérlet azt mutatja, hogy az alkalmazott E α energiájú α részeket az atommag képes teljesen lefékezni és visszalökni. 19 / 57
76 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Rutherford az új sugárzással bombázott vékony fémfóliákat, és arra volt kíváncsi, mennyiben tér el a fólia mögötti szórási kép attól, amit katódsugarak esetében tapasztaltak. A várakozásokkal ellentétben átlagosan minden dik α rész visszapattant a fóliáról. Rutherford a jelenséget azzal a feltételezéssel magyarázta, hogy az atom pozitív része nem tölti ki az atom teljes térfogatát, hanem az atom közepén helyezkedik el. Ez az atommag. A Rutherford-féle kísérlet azt mutatja, hogy az alkalmazott E α energiájú α részeket az atommag képes teljesen lefékezni és visszalökni. Az α rész akkor áll meg, amikor kezdeti mozgási energiája felhasználódik az atommag taszításának leküzdésére, azaz amikor: E α = Z αze 2 4πε 0 R 19 / 57
77 U c Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet 1 r E α R mag R r 20 / 57
78 U c Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet 1 r E α R mag R r Határozzuk meg R értékét, ha az egyik kísérletben E α = 8 MeV energiájú α sugárzás visszalökődését figyelték meg aranyfóliáról (Z = 79). R = Z αze 2 4πε 0 E α = 2, m 20 / 57
79 Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet 21 / 57
80 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m 21 / 57
81 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. 21 / 57
82 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. Az atommag körül körpályákon keringenek a könnyű elektronok elektronburkot alkotva. 21 / 57
83 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. Az atommag körül körpályákon keringenek a könnyű elektronok elektronburkot alkotva. Sajnos ez a modell nem egyeztethető össze egyszerre a kísérleti tapasztalatokkal és a klasszikus elektrodinamikával. 21 / 57
84 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. Az atommag körül körpályákon keringenek a könnyű elektronok elektronburkot alkotva. Sajnos ez a modell nem egyeztethető össze egyszerre a kísérleti tapasztalatokkal és a klasszikus elektrodinamikával. A körpályán keringő töltött elektronnak a klasszikus elmélet szerint sugároznia kell, mivel gyorsulással mozog. 21 / 57
85 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. Az atommag körül körpályákon keringenek a könnyű elektronok elektronburkot alkotva. Sajnos ez a modell nem egyeztethető össze egyszerre a kísérleti tapasztalatokkal és a klasszikus elektrodinamikával. A körpályán keringő töltött elektronnak a klasszikus elmélet szerint sugároznia kell, mivel gyorsulással mozog. A kisugárzott energia csökkenti a keringő elektron mozgási energiáját, ezért annak bele kéne zuhannia a magba, miközben folytonos spektrumú elektromágneses sugárzást kéne kibocsátania. 21 / 57
86 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Nyilván az atommag sugara ennél az értéknél csak kisebb lehet. R mag m Rutherford a kísérleti eredmények alapján egy új atommodellt javasolt. Az atommag körül körpályákon keringenek a könnyű elektronok elektronburkot alkotva. Sajnos ez a modell nem egyeztethető össze egyszerre a kísérleti tapasztalatokkal és a klasszikus elektrodinamikával. A körpályán keringő töltött elektronnak a klasszikus elmélet szerint sugároznia kell, mivel gyorsulással mozog. A kisugárzott energia csökkenti a keringő elektron mozgási energiáját, ezért annak bele kéne zuhannia a magba, miközben folytonos spektrumú elektromágneses sugárzást kéne kibocsátania. A kísérletek azonban azt mutatják, hogy az atomok különösképpen stabil képződmények, továbbá az általuk kibocsátott sugárzás spektruma vonalas. 21 / 57
87 A hidrogén színképe Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A XIX. század végén az optikából jól ismert módon, spektroszkópiai módszerekkel vizsgálták az atomok által kibocsátott látható fényt, vagy az infravörös és ultraibolya sugárzásokat. 22 / 57
88 A hidrogén színképe Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A XIX. század végén az optikából jól ismert módon, spektroszkópiai módszerekkel vizsgálták az atomok által kibocsátott látható fényt, vagy az infravörös és ultraibolya sugárzásokat. A mért spektrumok kivétel nélkül vonalas jellegűek voltak. 22 / 57
89 A hidrogén színképe Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A XIX. század végén az optikából jól ismert módon, spektroszkópiai módszerekkel vizsgálták az atomok által kibocsátott látható fényt, vagy az infravörös és ultraibolya sugárzásokat. A mért spektrumok kivétel nélkül vonalas jellegűek voltak. A fizika további fejlődésének szempontjából különösen fontos a legegyszerűbb elem, a hidrogén spektruma. 22 / 57
90 A hidrogén színképe Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A XIX. század végén az optikából jól ismert módon, spektroszkópiai módszerekkel vizsgálták az atomok által kibocsátott látható fényt, vagy az infravörös és ultraibolya sugárzásokat. A mért spektrumok kivétel nélkül vonalas jellegűek voltak. A fizika további fejlődésének szempontjából különösen fontos a legegyszerűbb elem, a hidrogén spektruma. A spektrumvonalak hullámhosszára a következő tapasztalati képletet találták: ( 1 1 λ = R n 1 ) 2 m 2 R = 1, m 1 - a Rydberg állandó n,m > n- természetes számok 22 / 57
91 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Hidrogén színképének első sikeres magyarázatát Niels Bohr dán fizikus adta meg. 23 / 57
92 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Hidrogén színképének első sikeres magyarázatát Niels Bohr dán fizikus adta meg. Elfogadta Rutherford atommodelljét, de hiányosságainak kiküszöbölésére bevezetett három posztulátumot. 23 / 57
93 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Hidrogén színképének első sikeres magyarázatát Niels Bohr dán fizikus adta meg. Elfogadta Rutherford atommodelljét, de hiányosságainak kiküszöbölésére bevezetett három posztulátumot. 1. posztulátum Az elektron az atomburokban csak olyan körpályán (stacionárius pályán) mozoghat, amelyre teljesül a következő kvantumfeltétel: m e vr = n h 2π. 23 / 57
94 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Hidrogén színképének első sikeres magyarázatát Niels Bohr dán fizikus adta meg. Elfogadta Rutherford atommodelljét, de hiányosságainak kiküszöbölésére bevezetett három posztulátumot. 1. posztulátum Az elektron az atomburokban csak olyan körpályán (stacionárius pályán) mozoghat, amelyre teljesül a következő kvantumfeltétel: 2. posztulátum m e vr = n h 2π. Ha az elektron az említett stacionárius pálya valamelyikén kering, nem sugároz ki elektromágneses sugárzást. 23 / 57
95 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Hidrogén színképének első sikeres magyarázatát Niels Bohr dán fizikus adta meg. Elfogadta Rutherford atommodelljét, de hiányosságainak kiküszöbölésére bevezetett három posztulátumot. 1. posztulátum Az elektron az atomburokban csak olyan körpályán (stacionárius pályán) mozoghat, amelyre teljesül a következő kvantumfeltétel: 2. posztulátum m e vr = n h 2π. Ha az elektron az említett stacionárius pálya valamelyikén kering, nem sugároz ki elektromágneses sugárzást. 3. posztulátum Az elektron csak akkor sugároz, ha nagyobb sugarú pályáról kisebb sugarúra áll. Ekkor a pályáknak megfelelő energiák különbségét egy foton formájában adja le. hν = E m E n 23 / 57
96 Bohr-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet r 2 v 1 r 1 foton v 2 24 / 57
97 Bohr-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet r 2 v 1 r 1 foton v 2 Írjuk fel az elektron mozgásegyenletét az n-dik pályán: m e v 2 r = e2 4πε 0 r 2 24 / 57
98 Bohr-féle atommodell Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet r 2 v 1 r 1 foton v 2 Írjuk fel az elektron mozgásegyenletét az n-dik pályán: v m 2 e r = e2 4πε 0 r 2 Bohr 1. posztulátuma alapján: 2πm e vr = nh. 24 / 57
99 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A két egyenletből a pályasugár és a kerületi sebesség kifejezhető: r n = ε 0h 2 πm e e 2 n 2, v n = e2 2ε 0 nh. 25 / 57
100 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A két egyenletből a pályasugár és a kerületi sebesség kifejezhető: r n = ε 0h 2 πm e n 2, e 2 v n = e2 2ε 0 nh. Mivel az elektron a mag elektromos terében mozog, összenergiája a mozgási és a helyzeti energiájának összege: E = 1 2 m ev 2 e2 4πε 0 r. 25 / 57
101 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A két egyenletből a pályasugár és a kerületi sebesség kifejezhető: r n = ε 0h 2 πm e n 2, e 2 v n = e2 2ε 0 nh. Mivel az elektron a mag elektromos terében mozog, összenergiája a mozgási és a helyzeti energiájának összege: E = 1 2 m ev 2 e2 4πε 0 r. Behelyettesítve a sugár és sebesség helyére: E n = m ee 4 8ε 0 2 h 2 1 n / 57
102 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet A két egyenletből a pályasugár és a kerületi sebesség kifejezhető: r n = ε 0h 2 πm e n 2, e 2 v n = e2 2ε 0 nh. Mivel az elektron a mag elektromos terében mozog, összenergiája a mozgási és a helyzeti energiájának összege: E = 1 2 m ev 2 e2 4πε 0 r. Behelyettesítve a sugár és sebesség helyére: E n = m ee 4 8ε 0 2 h 2 1 n 2. Bohr 3. posztulátuma alapján kiszámolható az m-dik pályáról az n-dik pályára való átmenetkor kisugárzott foton hullámhossza: 1 λ = m ee 4 8ε 2 0 h 3 c ( 1 n 1 ). 2 m 2 25 / 57
103 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. 26 / 57
104 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. Behelyettesítve az állandók számértékeit, a kísérleti és elméleti érték meglepő egyezést mutat. 26 / 57
105 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. Behelyettesítve az állandók számértékeit, a kísérleti és elméleti érték meglepő egyezést mutat. A Bohr elmélet értelmezni képes a hidrogén színképében fellelt különböző sorozatokat. 26 / 57
106 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. Behelyettesítve az állandók számértékeit, a kísérleti és elméleti érték meglepő egyezést mutat. A Bohr elmélet értelmezni képes a hidrogén színképében fellelt különböző sorozatokat. Sajnos Bohr-elmélete csak a H-atomra használható. A többi atom esetében a tapasztalattal nem megegyező eredményre vezet. 26 / 57
107 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. Behelyettesítve az állandók számértékeit, a kísérleti és elméleti érték meglepő egyezést mutat. A Bohr elmélet értelmezni képes a hidrogén színképében fellelt különböző sorozatokat. Sajnos Bohr-elmélete csak a H-atomra használható. A többi atom esetében a tapasztalattal nem megegyező eredményre vezet. Írjuk át Bohr 1. posztulátumát a következő alakba: 2πr = n h m e v. 26 / 57
108 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Látjuk, hogy Bohr elmélete a Rydberg állandóra a következő összefüggést adja: R = m ee 4 8ε 0 2 h 3 c. Behelyettesítve az állandók számértékeit, a kísérleti és elméleti érték meglepő egyezést mutat. A Bohr elmélet értelmezni képes a hidrogén színképében fellelt különböző sorozatokat. Sajnos Bohr-elmélete csak a H-atomra használható. A többi atom esetében a tapasztalattal nem megegyező eredményre vezet. Írjuk át Bohr 1. posztulátumát a következő alakba: A h m e v 2πr = n h m e v. mennyiség az elektron de-broglie hullámhossza, így a fenti felírásnak van egy másik jelentése is. 26 / 57
109 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Ez a feltétel azt mondja ki, hogy az atomokba zárt elektronok olyan állóhullámok, melyeknek hullámhossza a stacionárius pálya kerületére n-szer fér rá. (n = 1, 2, 3,...) Mag r elektron 27 / 57
110 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Ez a feltétel azt mondja ki, hogy az atomokba zárt elektronok olyan állóhullámok, melyeknek hullámhossza a stacionárius pálya kerületére n-szer fér rá. (n = 1, 2, 3,...) Mag r elektron Ez a Bohr-féle posztulátum arra szolgál, hogy a klasszikus elmélet alapján számított eredményekből kiválassza a mikrovilág számára megfelelőeket. kvantált fizikai mennyiségeket. 27 / 57
111 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az n = 1 kvantumszámú pálya sugaránál nem kerülhet közelebb a maghoz. Ezt az állapotot nevezzük alapállapotnak. 28 / 57
112 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az n = 1 kvantumszámú pálya sugaránál nem kerülhet közelebb a maghoz. Ezt az állapotot nevezzük alapállapotnak. Az elektron összenergiája csak a kvantumfeltételnek eleget tevő diszkrét érték lehet. 28 / 57
113 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az n = 1 kvantumszámú pálya sugaránál nem kerülhet közelebb a maghoz. Ezt az állapotot nevezzük alapállapotnak. Az elektron összenergiája csak a kvantumfeltételnek eleget tevő diszkrét érték lehet. n = 3 n = 2 E 0. E 3 = 1, 51 ev E 2 = 3, 40 ev n = 3 E 0. E 3 n = 2 E 2 n = 1 E 1 = 13, 605 ev a) n = 1 E 1 b) 28 / 57
114 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Az elektron az n = 1 kvantumszámú pálya sugaránál nem kerülhet közelebb a maghoz. Ezt az állapotot nevezzük alapállapotnak. Az elektron összenergiája csak a kvantumfeltételnek eleget tevő diszkrét érték lehet. n = 3 n = 2 E 0. E 3 = 1, 51 ev E 2 = 3, 40 ev n = 3 E 0. E 3 n = 2 E 2 n = 1 E 1 = 13, 605 ev a) n = 1 E 1 b) Az anyagba zárt mikrorészecskék általános tulajdonsága, hogy energiáik csak diszkrét értékeket vehetnek fel. 28 / 57
115 Franck-Hertz kísérlet Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet R K A G Hg-gőz U r U a / 57
116 Franck-Hertz kísérlet Bevezetés Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet R K A G Hg-gőz U r U a + + A kísérlet során változtatjuk a katód és rács közé kapcsolt gyorsítófeszültséget, és ennek függvényében mérjük a G galvanométerrel az anódáramot. 29 / 57
117 I Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet V 0 2V 0 3V 0 4V 0 V r 30 / 57
118 I Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet V 0 2V 0 3V 0 4V 0 V r Az elektronok tökéletesen rugalmasan ütköznek a higanyatomokkal. 30 / 57
119 I Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet V 0 2V 0 3V 0 4V 0 V r Az elektronok tökéletesen rugalmasan ütköznek a higanyatomokkal. Mivel azok tömege több ezerszer nagyobb az elektronok tömegénél, az elektronok gyakorlatilag energiaveszteség nélkül pattannak vissza róluk, és elérik az anódot. Az anódáram a gyorsítófeszültséggel arányosan nő. 30 / 57
120 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Amikor a gyorsítófeszültség eléri a V 0 = 4,9 V értéket az anódáram hirtelen csökkenni kezd. Mi lehet ennek az oka? 31 / 57
121 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Amikor a gyorsítófeszültség eléri a V 0 = 4,9 V értéket az anódáram hirtelen csökkenni kezd. Mi lehet ennek az oka? A 4, 9 ev energiájú elektronok ütközése a higanyatomokkal nem rugalmas ütközés. Az ilyen energiájú elektronok a higany atomjaival ütközve átadják energiájukat a higany egyik elektronjának, és az magasabb energiaszintre ugrik. 31 / 57
122 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Amikor a gyorsítófeszültség eléri a V 0 = 4,9 V értéket az anódáram hirtelen csökkenni kezd. Mi lehet ennek az oka? A 4, 9 ev energiájú elektronok ütközése a higanyatomokkal nem rugalmas ütközés. Az ilyen energiájú elektronok a higany atomjaival ütközve átadják energiájukat a higany egyik elektronjának, és az magasabb energiaszintre ugrik. Mivel ez a folyamat 4,9 V feszültség mellett játszódik le, a higany alapállapota és első gerjesztett állapota közötti energiakülönbség 4,9 ev kell legyen. 31 / 57
123 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Amikor a gyorsítófeszültség eléri a V 0 = 4,9 V értéket az anódáram hirtelen csökkenni kezd. Mi lehet ennek az oka? A 4, 9 ev energiájú elektronok ütközése a higanyatomokkal nem rugalmas ütközés. Az ilyen energiájú elektronok a higany atomjaival ütközve átadják energiájukat a higany egyik elektronjának, és az magasabb energiaszintre ugrik. Mivel ez a folyamat 4,9 V feszültség mellett játszódik le, a higany alapállapota és első gerjesztett állapota közötti energiakülönbség 4,9 ev kell legyen. A további csúcsok a többszöri rugalmatlan ütközésekkel magyarázhatóak. 31 / 57
124 Rutherford-féle atommodell A hidrogén színképe Bohr-féle atommodell Franck-Hertz kísérlet Amikor a gyorsítófeszültség eléri a V 0 = 4,9 V értéket az anódáram hirtelen csökkenni kezd. Mi lehet ennek az oka? A 4, 9 ev energiájú elektronok ütközése a higanyatomokkal nem rugalmas ütközés. Az ilyen energiájú elektronok a higany atomjaival ütközve átadják energiájukat a higany egyik elektronjának, és az magasabb energiaszintre ugrik. Mivel ez a folyamat 4,9 V feszültség mellett játszódik le, a higany alapállapota és első gerjesztett állapota közötti energiakülönbség 4,9 ev kell legyen. A további csúcsok a többszöri rugalmatlan ütközésekkel magyarázhatóak. A gerjesztett állapotban lévő elektron az energiaminimum elve miatt nagyon rövid idő eltelte után (kb s) visszaugrik az alapállapotba, miközben 4, 9 ev energiájú fotont sugároz ki. A Franck-Hertz kísérletben ezeket a fotonokat megfigyelték. 31 / 57
125 Hullámfüggvény Dobozba zárt elektron Alagút-effektus 32 / 57
126 Hullámfüggvény Bevezetés Ψ(r, t) Hullámfüggvény Dobozba zárt elektron Alagút-effektus 33 / 57
127 Hullámfüggvény Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Ψ(r, t) Ψ(r, t)-csak a hely és idő komplex függvénye 33 / 57
128 Hullámfüggvény Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Ψ(r, t) Ψ(r, t)-csak a hely és idő komplex függvénye Ψ 2 dv annak a valószínűsége, hogy a vizsgált objektum a t időpillanatban az r helyvektorral jellemzett dv térfogatban található. 33 / 57
129 Hullámfüggvény Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Ψ(r, t) Ψ(r, t)-csak a hely és idő komplex függvénye Ψ 2 dv annak a valószínűsége, hogy a vizsgált objektum a t időpillanatban az r helyvektorral jellemzett dv térfogatban található. A hullámfüggvény normálási feltétele: (V ) Ψ(r, t) 2 dv = 1 33 / 57
130 Hullámfüggvény Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Ψ(r, t) Ψ(r, t)-csak a hely és idő komplex függvénye Ψ 2 dv annak a valószínűsége, hogy a vizsgált objektum a t időpillanatban az r helyvektorral jellemzett dv térfogatban található. A hullámfüggvény normálási feltétele: (V ) Ψ(r, t) 2 dv = 1 Az állapotfüggvény időbeli fejlődését a Schrödinger-egyenlet írja le. 33 / 57
131 Hullámfüggvény Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Ψ(r, t) Ψ(r, t)-csak a hely és idő komplex függvénye Ψ 2 dv annak a valószínűsége, hogy a vizsgált objektum a t időpillanatban az r helyvektorral jellemzett dv térfogatban található. A hullámfüggvény normálási feltétele: (V ) Ψ(r, t) 2 dv = 1 Az állapotfüggvény időbeli fejlődését a Schrödinger-egyenlet írja le. Stacionárius esetben mindig felírható: Ψ(r,t) = ϕ(r)e iē h t h = h 2π 33 / 57
132 Dobozba zárt elektron Bevezetés Elektron egy dimenzióban, ha mozgását egy a hosszúságú szakaszra korlátozzuk. Hullámfüggvény Dobozba zárt elektron Alagút-effektus 34 / 57
133 Dobozba zárt elektron Bevezetés Hullámfüggvény Dobozba zárt elektron Alagút-effektus Elektron egy dimenzióban, ha mozgását egy a hosszúságú szakaszra korlátozzuk. Az elektron időben állandósult állapotát leíró állapotfüggvény tértől függő ϕ(x) része eleget kell tegyen az állóhullám-egyenletnek. 34 / 57
Atomfizika. A hidrogén lámpa színképei. Elektronok H atom. Fényképlemez. emisszió H 2. gáz
 Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Atomfizika A hidrogén lámpa színképei - Elektronok H atom emisszió Fényképlemez V + H 2 gáz Az atom és kvantumfizika fejlődésének fontos szakasza volt a hidrogén lámpa színképeinek leírása, és a vonalas
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés J.J. Thomson (1897) Katódsugárcsővel végzett kísérleteket az elektron fajlagos töltésének (e/m) meghatározására. A katódsugarat alkotó részecskét
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet
 Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atomfizika. Fizika kurzus Dr. Seres István
 Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Atomfizika Fizika kurzus Dr. Seres István Történeti áttekintés 440 BC Democritus, Leucippus, Epicurus 1660 Pierre Gassendi 1803 1897 1904 1911 19 193 John Dalton Joseph John (J.J.) Thomson J.J. Thomson
Bevezetés a modern fizika fejezeteibe. 4. (a) Kvantummechanika. Utolsó módosítás: november 15. Dr. Márkus Ferenc BME Fizika Tanszék
 Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atommodellek. Az atom szerkezete. Atommodellek. Atommodellek. Atommodellek, A Rutherford-kísérlet. Atommodellek
 Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
Démokritosz: a világot homogén szubsztanciájú oszthatatlan részecskék, atomok és a közöttük lévı őr alkotja. Az atom szerkezete Egy atommodellt akkor fogadunk el érvényesnek, ha megmagyarázza a tapasztalati
OPTIKA. Fénykibocsátás mechanizmusa fényforrás típusok. Dr. Seres István
 OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
A hőmérsékleti sugárzás
 A hőmérsékleti sugárzás Felhevített tárgyak több száz fokos hőmérsékletet elérve először vörösen majd még magasabb hőmérsékleten sárgán izzanak, tehát fényt (elektromágneses hullámokat a látható tartományban)
A hőmérsékleti sugárzás Felhevített tárgyak több száz fokos hőmérsékletet elérve először vörösen majd még magasabb hőmérsékleten sárgán izzanak, tehát fényt (elektromágneses hullámokat a látható tartományban)
A hőmérsékleti sugárzás
 A hőmérsékleti sugárzás Alapfogalmak 1. A hőmérsékleti sugárzás Értelmezés (hőmérsékleti sugárzás): A testek hőmérsékletével kapcsolatos, a teljes elektromágneses spektrumra kiterjedő sugárzást hőmérsékleti
A hőmérsékleti sugárzás Alapfogalmak 1. A hőmérsékleti sugárzás Értelmezés (hőmérsékleti sugárzás): A testek hőmérsékletével kapcsolatos, a teljes elektromágneses spektrumra kiterjedő sugárzást hőmérsékleti
Thomson-modell (puding-modell)
 Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
Atommodellek Thomson-modell (puding-modell) A XX. század elejére világossá vált, hogy az atomban található elektronok ugyanazok, mint a katódsugárzás részecskéi. Magyarázatra várt azonban, hogy mi tartja
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről
 A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
A fény korpuszkuláris jellegét tükröző fizikai jelenségek
 A fény korpuszkuláris jellegét tükröző fizikai jelenségek A fény elektromágneses sugárzás, amely hullámjelleggel és korpuszkuláris sajátosságokkal is rendelkezik. A fény hullámjellege elsősorban az olyan
A fény korpuszkuláris jellegét tükröző fizikai jelenségek A fény elektromágneses sugárzás, amely hullámjelleggel és korpuszkuláris sajátosságokkal is rendelkezik. A fény hullámjellege elsősorban az olyan
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK. Kalocsai Angéla, Kozma Enikő
 ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
FIZIKA. Sugárzunk az elégedettségtől! (Atomfizika) Dr. Seres István
 Sugárzunk az elégedettségtől! () Dr. Seres István atommagfizika Atommodellek 440 IE Democritus, Leucippus, Epicurus 1803 1897 John Dalton J.J. Thomson 1911 Ernest Rutherford 19 Niels Bohr 3 Atommodellek
Sugárzunk az elégedettségtől! () Dr. Seres István atommagfizika Atommodellek 440 IE Democritus, Leucippus, Epicurus 1803 1897 John Dalton J.J. Thomson 1911 Ernest Rutherford 19 Niels Bohr 3 Atommodellek
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE
 AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
AZ ELEKTROMÁGNESES SUGÁRZÁS KETTŐS TERMÉSZETE A Planck-féle sugárzási törvény Hipotézis 1.: A hősugárzást (elektromágneses hullámokat) kis, apró rezgő oszcillátorok hozzák létre. Egy ilyen oszcillátor
2, = 5221 K (7.2)
 7. Gyakorlat 4A-7 Az emberi szem kb. 555 nm hullámhossznál a Iegnagyobb érzékenységű. Adjuk meg annak a fekete testnek a hőmérsékletét, amely sugárzásának a spektrális teljesitménye ezen a hullámhosszon
7. Gyakorlat 4A-7 Az emberi szem kb. 555 nm hullámhossznál a Iegnagyobb érzékenységű. Adjuk meg annak a fekete testnek a hőmérsékletét, amely sugárzásának a spektrális teljesitménye ezen a hullámhosszon
Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag?
 Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
Atomfizika I. Az anyagszerkezetről alkotott kép változása Ókori görög filozófusok régi kérdése: Miből vannak a testek? Meddig osztható az anyag? Platón (i.e. 427-347), Arisztotelész (=i.e. 387-322): Végtelenségig
Az elektromágneses hullámok
 203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
Kvantummechanikai alapok I.
 Kvantummechanikai alapok I. Dr. Berta Miklós bertam@sze.hu 2017. szeptember 21. 1 / 41 Állapotfüggvény. Dinamikai egyenlet. Ψ(r, t) 2 / 41 Állapotfüggvény. Dinamikai egyenlet. Ψ(r, t) Ψ(r, t)-csak a hely
Kvantummechanikai alapok I. Dr. Berta Miklós bertam@sze.hu 2017. szeptember 21. 1 / 41 Állapotfüggvény. Dinamikai egyenlet. Ψ(r, t) 2 / 41 Állapotfüggvény. Dinamikai egyenlet. Ψ(r, t) Ψ(r, t)-csak a hely
Atomfizika tesztek. 2. Az elektrolízis jelenségére vonatkozóan melyik összefüggés helytelen?
 Atomfizika tesztek 1. Melyik állítás nem helyes? a) Azonos tömegű ideális gázok azonos számú részecskét tartalmaznak. b) Normál állapotú, 22,41 liter térfogatú ideális gázok 6. 10 23 db részecskét tartalmaznak.
Atomfizika tesztek 1. Melyik állítás nem helyes? a) Azonos tömegű ideális gázok azonos számú részecskét tartalmaznak. b) Normál állapotú, 22,41 liter térfogatú ideális gázok 6. 10 23 db részecskét tartalmaznak.
Kifejtendő kérdések június 13. Gyakorló feladatok
 Kifejtendő kérdések 2016. június 13. Gyakorló feladatok 1. Adott egy egyenletes térfogati töltéssel rendelkező, R sugarú gömb, melynek felületén a potenciál U 0. Az elektromos potenciál definíciója (1p)
Kifejtendő kérdések 2016. június 13. Gyakorló feladatok 1. Adott egy egyenletes térfogati töltéssel rendelkező, R sugarú gömb, melynek felületén a potenciál U 0. Az elektromos potenciál definíciója (1p)
Modern fizika vegyes tesztek
 Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
ATOMFIZIKA. óravázlatok
 ATOMFIZIKA óravázlatok A fizika felosztása 1. Klasszikus fizika Olyan jelenségekkel és törvényekkel foglalkozik, amelyekről a mindennapi életben is szerezhetünk tapasztalatokat. 2. Modern fizika A fizikának
ATOMFIZIKA óravázlatok A fizika felosztása 1. Klasszikus fizika Olyan jelenségekkel és törvényekkel foglalkozik, amelyekről a mindennapi életben is szerezhetünk tapasztalatokat. 2. Modern fizika A fizikának
Kvantummechanika. - dióhéjban - Kasza Gábor július 5. - Berze TÖK
 Kvantummechanika - dióhéjban - Kasza Gábor 2016. július 5. - Berze TÖK 1 / 27 Mire fogunk választ kapni az előadásból? Miért KVANTUMmechanika? Miért részecske? Miért hullám? Mit mond a Schrödinger-egyenlet?
Kvantummechanika - dióhéjban - Kasza Gábor 2016. július 5. - Berze TÖK 1 / 27 Mire fogunk választ kapni az előadásból? Miért KVANTUMmechanika? Miért részecske? Miért hullám? Mit mond a Schrödinger-egyenlet?
Alkalmazás a makrókanónikus sokaságra: A fotongáz
 Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
1. Az üregsugárzás törvényei
 1. Az üregsugárzás törvényei 1.1. A Wien féle eltolódási törvény és a Stefan-Boltzmann törvény Egy zárt, belül üres fémdoboz kis nyílása az úgynevezett abszolút fekete test. A nyílás elektromágneses sugárzást
1. Az üregsugárzás törvényei 1.1. A Wien féle eltolódási törvény és a Stefan-Boltzmann törvény Egy zárt, belül üres fémdoboz kis nyílása az úgynevezett abszolút fekete test. A nyílás elektromágneses sugárzást
KVANTUMMECHANIKA. a11.b-nek
 KVANTUMMECHANIKA a11.b-nek HŐMÉRSÉKLETI SUGÁRZÁS 1 Hősugárzás: elektromágneses hullám A sugárzás által szállított energia: intenzitás I, T és λkapcsolata? Példa: Nap (6000 K): sárga (látható) Föld (300
KVANTUMMECHANIKA a11.b-nek HŐMÉRSÉKLETI SUGÁRZÁS 1 Hősugárzás: elektromágneses hullám A sugárzás által szállított energia: intenzitás I, T és λkapcsolata? Példa: Nap (6000 K): sárga (látható) Föld (300
Röntgensugárzás az orvostudományban. Röntgen kép és Komputer tomográf (CT)
 Röntgensugárzás az orvostudományban Röntgen kép és Komputer tomográf (CT) Orbán József, Biofizikai Intézet, 2008 Hand mit Ringen: print of Wilhelm Röntgen's first "medical" x-ray, of his wife's hand, taken
Röntgensugárzás az orvostudományban Röntgen kép és Komputer tomográf (CT) Orbán József, Biofizikai Intézet, 2008 Hand mit Ringen: print of Wilhelm Röntgen's first "medical" x-ray, of his wife's hand, taken
Név... intenzitás abszorbancia moláris extinkciós. A Wien-féle eltolódási törvény szerint az abszolút fekete test maximális emisszióképességéhez
 A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
Kémiai alapismeretek 2. hét
 Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. február 14. 1/15 2011/2012 II. félév, Horváth Attila c XIX sz. vége,
Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2012. február 14. 1/15 2011/2012 II. félév, Horváth Attila c XIX sz. vége,
A modern fizika születése
 MODERN FIZIKA A modern fizika születése Eddig: Olyan törvényekkel ismerkedtünk meg melyekhez tapasztalatokat a mindennapi életből is szerezhettünk. Klasszikus fizika: mechanika, hőtan, elektromosságtan,
MODERN FIZIKA A modern fizika születése Eddig: Olyan törvényekkel ismerkedtünk meg melyekhez tapasztalatokat a mindennapi életből is szerezhettünk. Klasszikus fizika: mechanika, hőtan, elektromosságtan,
FIZIKA II. Dr. Rácz Ervin. egyetemi docens
 FIZIKA II. Dr. Rácz Ervin egyetemi docens Fontos tudnivalók e-mail: racz.ervin@kvk.uni-obuda.hu web: http://uni-obuda.hu/users/racz.ervin/index.htm Iroda: Bécsi út, C. épület, 124. szoba Fizika II. - ismertetés
FIZIKA II. Dr. Rácz Ervin egyetemi docens Fontos tudnivalók e-mail: racz.ervin@kvk.uni-obuda.hu web: http://uni-obuda.hu/users/racz.ervin/index.htm Iroda: Bécsi út, C. épület, 124. szoba Fizika II. - ismertetés
A kvantumelmélet kísérletes háttere
 A kvantumelmélet kísérletes háttere A hőmérsékleti sugárzás A fényelektromos hatás A fény kettős természete. Anyaghullámok A XIX. század végén és a XX. század elején olyan kísérleti eredmények születtek,
A kvantumelmélet kísérletes háttere A hőmérsékleti sugárzás A fényelektromos hatás A fény kettős természete. Anyaghullámok A XIX. század végén és a XX. század elején olyan kísérleti eredmények születtek,
ELEMI RÉSZECSKÉK ATOMMODELLEK
 ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
ELEMI RÉSZECSKÉK ATOMMODELLEK Az atomok felépítése Készítette: Horváthné Vlasics Zsuzsanna Mi van az atomok belsejében? DÉMOKRITOSZ (Kr.e. 460-370) az anyag nem folytonos parányi, tovább nem bontható,
ELEKTRONIKAI ALKATRÉSZEK
 ELEKTRONIKAI ALKATRÉSZEK VEZETÉS VÁKUUMBAN (EMISSZIÓ) 2. ELŐADÁS Fémek kilépési munkája Termikus emisszió vákuumban Hideg (autoelektromos) emisszió vákuumban Fotoelektromos emisszió vákuumban KILÉPÉSI
ELEKTRONIKAI ALKATRÉSZEK VEZETÉS VÁKUUMBAN (EMISSZIÓ) 2. ELŐADÁS Fémek kilépési munkája Termikus emisszió vákuumban Hideg (autoelektromos) emisszió vákuumban Fotoelektromos emisszió vákuumban KILÉPÉSI
Kémiai alapismeretek 2. hét
 Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Kémiai alapismeretek 2. hét Horváth Attila Pécsi Tudományegyetem, Természettudományi Kar, Kémia Intézet, Szervetlen Kémiai Tanszék 2014. szeptember 9.-12. 1/13 2014/2015 I. félév, Horváth Attila c Hullámtermészet:
Szilárd testek sugárzása
 A fény keletkezése Szilárd testek sugárzása A szilárd test melegítés hatására fényt bocsát ki A sugárzás forrása a közelítőleg termikus egyensúlyban lévő kibocsátó test atomi részecskéinek véletlenszerű
A fény keletkezése Szilárd testek sugárzása A szilárd test melegítés hatására fényt bocsát ki A sugárzás forrása a közelítőleg termikus egyensúlyban lévő kibocsátó test atomi részecskéinek véletlenszerű
 http://www.flickr.com Az atommag állapotait kvantummechanikai állapotfüggvénnyel írjuk le. A mag paritását ezen fv. paritása adja meg. Paritás: egy állapot tértükrözéssel szemben mutatott viselkedését
http://www.flickr.com Az atommag állapotait kvantummechanikai állapotfüggvénnyel írjuk le. A mag paritását ezen fv. paritása adja meg. Paritás: egy állapot tértükrözéssel szemben mutatott viselkedését
Theory hungarian (Hungary)
 Q3-1 A Nagy Hadronütköztető (10 pont) Mielőtt elkezded a feladat megoldását, olvasd el a külön borítékban lévő általános utasításokat! Ez a feladat a CERN-ben működő részecskegyorsító, a Nagy Hadronütköztető
Q3-1 A Nagy Hadronütköztető (10 pont) Mielőtt elkezded a feladat megoldását, olvasd el a külön borítékban lévő általános utasításokat! Ez a feladat a CERN-ben működő részecskegyorsító, a Nagy Hadronütköztető
Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus
 Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus Melyik egyenlet nem hullámot ír le? a) y = A sin 2π(ft x/λ) b) y = A
Jelöljük meg a kérdésnek megfelelő válaszokat! 1, Hullámokról általában: alapösszefüggések a harmonikus hullámra. A Doppler-effektus Melyik egyenlet nem hullámot ír le? a) y = A sin 2π(ft x/λ) b) y = A
Biofizika. Sugárzások. Csik Gabriella. Mi a biofizika tárgya? Mi a biofizika tárgya? Biológiai jelenségek fizikai leírása/értelmezése
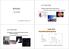 Mi a biofizika tárgya? Biofizika Csik Gabriella Biológiai jelenségek fizikai leírása/értelmezése Pl. szívműködés, membránok szerkezete és működése, érzékelés stb. csik.gabriella@med.semmelweis-univ.hu
Mi a biofizika tárgya? Biofizika Csik Gabriella Biológiai jelenségek fizikai leírása/értelmezése Pl. szívműködés, membránok szerkezete és működése, érzékelés stb. csik.gabriella@med.semmelweis-univ.hu
A fény mint elektromágneses hullám és mint fényrészecske
 A fény mint elektromágneses hullám és mint fényrészecske Segítség az 5. tétel (Hogyan alkalmazható a hullám-részecske kettősség gondolata a fénysugárzás esetében?) megértéséhez és megtanulásához, továbbá
A fény mint elektromágneses hullám és mint fényrészecske Segítség az 5. tétel (Hogyan alkalmazható a hullám-részecske kettősség gondolata a fénysugárzás esetében?) megértéséhez és megtanulásához, továbbá
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
A gamma-sugárzás kölcsönhatásai
 Ref. [3] A gamma-sugárzás kölcsönhatásai Az anyaggal való kölcsönhatás kis valószínűségű hatótávolság nagy A sugárzás gyengülését 3 féle kölcsönhatás okozza. fotoeffektus Compton-szórás párkeltés A gamma-fotonok
Ref. [3] A gamma-sugárzás kölcsönhatásai Az anyaggal való kölcsönhatás kis valószínűségű hatótávolság nagy A sugárzás gyengülését 3 féle kölcsönhatás okozza. fotoeffektus Compton-szórás párkeltés A gamma-fotonok
Fermi Dirac statisztika elemei
 Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Fermi Dirac statisztika elemei A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra érvényes klasszikus statisztika
Elektromágneses hullámegyenlet
 Elektromágneses hullámegyenlet Valódi töltésektől és vezetési áramoktól mentes szigetelőkre felírva az első két egyenletet: Az anyagegyenletek továbbá: Ezekből levezethetők a homogén hullámegyenletek a
Elektromágneses hullámegyenlet Valódi töltésektől és vezetési áramoktól mentes szigetelőkre felírva az első két egyenletet: Az anyagegyenletek továbbá: Ezekből levezethetők a homogén hullámegyenletek a
FIZIKA KÖZÉPSZINTŐ SZÓBELI FIZIKA ÉRETTSÉGI TÉTELEK Premontrei Szent Norbert Gimnázium, Gödöllı, 2012. május-június
 1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
Radioaktív sugárzások tulajdonságai és kölcsönhatásuk az elnyelő közeggel. A radioaktív sugárzások detektálása.
 Különböző sugárzások tulajdonságai Típus töltés Energia hordozó E spektrum Radioaktí sugárzások tulajdonságai és kölcsönhatásuk az elnyelő közeggel. A radioaktí sugárzások detektálása. α-sugárzás pozití
Különböző sugárzások tulajdonságai Típus töltés Energia hordozó E spektrum Radioaktí sugárzások tulajdonságai és kölcsönhatásuk az elnyelő közeggel. A radioaktí sugárzások detektálása. α-sugárzás pozití
Biofizika tesztkérdések
 Biofizika tesztkérdések Egyszerű választás E kérdéstípusban A, B,...-vel jelölt lehetőségek szerepelnek, melyek közül az egyetlen megfelelőt kell kiválasztani. A választ írja a kérdés előtt lévő kockába!
Biofizika tesztkérdések Egyszerű választás E kérdéstípusban A, B,...-vel jelölt lehetőségek szerepelnek, melyek közül az egyetlen megfelelőt kell kiválasztani. A választ írja a kérdés előtt lévő kockába!
Röntgensugárzás. Röntgensugárzás
 Röntgensugárzás 2012.11.21. Röntgensugárzás Elektromágneses sugárzás (f=10 16 10 19 Hz, E=120eV 120keV (1.9*10-17 10-14 J), λ
Röntgensugárzás 2012.11.21. Röntgensugárzás Elektromágneses sugárzás (f=10 16 10 19 Hz, E=120eV 120keV (1.9*10-17 10-14 J), λ
Az atom felépítése Alapfogalmak
 Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Anyagszerkezeti vizsgálatok 2017/2018. 1. félév Az atom felépítése Alapfogalmak Csordás Anita E-mail: csordasani@almos.uni-pannon.hu Tel:+36-88/624-924 Pannon Egyetem Radiokémiai és Radioökológiai Intézet
Gyorsítók. Veszprémi Viktor ATOMKI, Debrecen. Supported by NKTH and OTKA (H07-C 74281) 2009. augusztus 17 Hungarian Teacher Program, CERN 1
 Gyorsítók Veszprémi Viktor ATOMKI, Debrecen Supported by NKTH and OTKA (H07-C 74281) 2009. augusztus 17 Hungarian Teacher Program, CERN 1 Az anyag felépítése Részecskefizika kvark, lepton Erős, gyenge,
Gyorsítók Veszprémi Viktor ATOMKI, Debrecen Supported by NKTH and OTKA (H07-C 74281) 2009. augusztus 17 Hungarian Teacher Program, CERN 1 Az anyag felépítése Részecskefizika kvark, lepton Erős, gyenge,
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008.
 Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Fizika II. segédlet táv és levelező
 Fizika II. segédlet táv és levelező Horváth Árpád 2012. június 9. A 284/6. alakú feladatsorszámok a Lökös Mayer Sebestyén Tóthné féle Kandós Fizika példatárra, a 38C-28 típusúak a Hudson Nelson: Útban
Fizika II. segédlet táv és levelező Horváth Árpád 2012. június 9. A 284/6. alakú feladatsorszámok a Lökös Mayer Sebestyén Tóthné féle Kandós Fizika példatárra, a 38C-28 típusúak a Hudson Nelson: Útban
Orvosi Biofizika I. 12. vizsgatétel. IsmétlésI. -Fény
 Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
Az atom felépítése, fénykibocsátás (tankönyv 68.o.- 86.o.)
 Az atom felépítése, fénykibocsátás (tankönyv 68.o.- 86.o.) Atomok, atommodellek (tankönyv 82.o.-84.o.) Már az ókorban Démokritosz (i. e. 500) úgy gondolta, hogy minden anyag tovább nem osztható alapegységekből,
Az atom felépítése, fénykibocsátás (tankönyv 68.o.- 86.o.) Atomok, atommodellek (tankönyv 82.o.-84.o.) Már az ókorban Démokritosz (i. e. 500) úgy gondolta, hogy minden anyag tovább nem osztható alapegységekből,
Mézerek és lézerek. Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19.
 és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
Stern Gerlach kísérlet. Készítette: Kiss Éva
 Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
19. A fényelektromos jelenségek vizsgálata
 19. A fényelektromos jelenségek vizsgálata PÁPICS PÉTER ISTVÁN csillagász, 3. évfolyam Mérőpár: Balázs Miklós 2006.04.19. Beadva: 2006.05.15. Értékelés: A MÉRÉS LEÍRÁSA Fontos megállapítás, hogy a fénysugárzásban
19. A fényelektromos jelenségek vizsgálata PÁPICS PÉTER ISTVÁN csillagász, 3. évfolyam Mérőpár: Balázs Miklós 2006.04.19. Beadva: 2006.05.15. Értékelés: A MÉRÉS LEÍRÁSA Fontos megállapítás, hogy a fénysugárzásban
Az elektron hullámtermészete. Készítette Kiss László
 Az elektron hullámtermészete Készítette Kiss László Az elektron részecske jellemzői Az elektront Joseph John Thomson fedezte fel 1897-ben. 1906-ban Nobel díj! Az elektronoknak, az elektromos és mágneses
Az elektron hullámtermészete Készítette Kiss László Az elektron részecske jellemzői Az elektront Joseph John Thomson fedezte fel 1897-ben. 1906-ban Nobel díj! Az elektronoknak, az elektromos és mágneses
Mit értünk a termikus neutronok fogalma alatt? Becsüljük meg a sebességüket 27 o C hőmérsékleten!
 Országos Szilárd Leó fizikaverseny Elődöntő 04. Minden feladat helyes megoldása 5 pontot ér. A feladatokat tetszőleges sorrenen lehet megoldani. A megoldáshoz bármilyen segédeszköz használható. Rendelkezésre
Országos Szilárd Leó fizikaverseny Elődöntő 04. Minden feladat helyes megoldása 5 pontot ér. A feladatokat tetszőleges sorrenen lehet megoldani. A megoldáshoz bármilyen segédeszköz használható. Rendelkezésre
 http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
9. évfolyam. Osztályozóvizsga tananyaga FIZIKA
 9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
9. évfolyam Osztályozóvizsga tananyaga A testek mozgása 1. Egyenes vonalú egyenletes mozgás 2. Változó mozgás: gyorsulás fogalma, szabadon eső test mozgása 3. Bolygók mozgása: Kepler törvények A Newtoni
KOVÁCS ENDRe, PARIpÁS BÉLA, FIZIkA II.
 KOVÁCS ENDRe, PARIpÁS BÉLA, FIZIkA II. 10 A MODERN FIZIKa ELEMEI X. A MODeRN fizikához vezető TApASZTALATOk 1. BeVeZeTÉS A fizika történetének egyik legnagyobb kérdése az volt, hogy az anyag a végtelenségig
KOVÁCS ENDRe, PARIpÁS BÉLA, FIZIkA II. 10 A MODERN FIZIKa ELEMEI X. A MODeRN fizikához vezető TApASZTALATOk 1. BeVeZeTÉS A fizika történetének egyik legnagyobb kérdése az volt, hogy az anyag a végtelenségig
XX. századi forradalom a fizikában
 XX. századi forradalom a fizikában magfizika részecskefizika 1925 1913 1900 1896 radioaktivitás lumineszcencia kvantummechanika Bohr-modell! színk nkép hőmérsékleti sugárz rzás!?? 1873 elektrodinamika
XX. századi forradalom a fizikában magfizika részecskefizika 1925 1913 1900 1896 radioaktivitás lumineszcencia kvantummechanika Bohr-modell! színk nkép hőmérsékleti sugárz rzás!?? 1873 elektrodinamika
Modern Fizika Laboratórium Fizika és Matematika BSc 8. Alkáli spektrumok
 Modern Fizika Laboratórium Fizika és Matematika BSc 8. Alkáli spektrumok Mérést végezték: Bodó Ágnes Márkus Bence Gábor Kedd délelőtti csoport Mérés ideje: 03/7/0 Beadás ideje: 04/0/0 Érdemjegy: . A mérés
Modern Fizika Laboratórium Fizika és Matematika BSc 8. Alkáli spektrumok Mérést végezték: Bodó Ágnes Márkus Bence Gábor Kedd délelőtti csoport Mérés ideje: 03/7/0 Beadás ideje: 04/0/0 Érdemjegy: . A mérés
Sugárzások kölcsönhatása az anyaggal
 Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
a Bohr-féle atommodell (1913) Niels Hendrik David Bohr ( )
 a Bohr-féle atommodell (1913) Niels Hendrik David Bohr (1885-1962) atomok gerjesztése és ionizációja elektronnal való bombázással (1913-1914) James Franck (1882-1964) Gustav Ludwig Hertz (1887-1975) Nobel-díj
a Bohr-féle atommodell (1913) Niels Hendrik David Bohr (1885-1962) atomok gerjesztése és ionizációja elektronnal való bombázással (1913-1914) James Franck (1882-1964) Gustav Ludwig Hertz (1887-1975) Nobel-díj
Fizika 2 - Gyakorló feladatok
 2015. június 19. ε o =8.85 10-12 AsV -1 m -1 μ o =4π10-7 VsA -1 m -1 e=1,6 10-19 C m e =9,11 10-31 kg m p =1,67 10-27 kg h=6,63 10-34 Js 1. Egy R sugarú gömbben -ρ állandó töltéssűrűség van. a. Határozza
2015. június 19. ε o =8.85 10-12 AsV -1 m -1 μ o =4π10-7 VsA -1 m -1 e=1,6 10-19 C m e =9,11 10-31 kg m p =1,67 10-27 kg h=6,63 10-34 Js 1. Egy R sugarú gömbben -ρ állandó töltéssűrűség van. a. Határozza
Színképelemzés. Romsics Imre 2014. április 11.
 Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
Színképelemzés Romsics Imre 2014. április 11. 1 Más néven: Spektrofotometria A színképből kinyert információkból megállapítható: az atomok elektronszerkezete az elektronállapotokat jellemző kvantumszámok
Atommodellek. Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Rausch Péter kémia-környezettan tanár
 Atommodellek Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Ernest Rutherford Rausch Péter kémia-környezettan tanár Modellalkotás A modell a valóság nagyított
Atommodellek Ha nem tudod egy pincérnőnek elmagyarázni a fizikádat, az valószínűleg nem nagyon jó fizika. Ernest Rutherford Rausch Péter kémia-környezettan tanár Modellalkotás A modell a valóság nagyított
Bevezetés az atomfizikába
 1 Bevezetés az atomfizikába A XIX. század végén és a XX. század elején számos, az anyag szerkezetével kapcsolatos, új tényt fedeztek fel. Kiderült például, hogy az atomok elektronokból és magból állnak,
1 Bevezetés az atomfizikába A XIX. század végén és a XX. század elején számos, az anyag szerkezetével kapcsolatos, új tényt fedeztek fel. Kiderült például, hogy az atomok elektronokból és magból állnak,
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
A +Q töltés egy L hosszúságú egyenes szakasz mentén oszlik el egyenletesen (ld ábra ábra
 . Gyakorlat 4B-9 A +Q töltés egy L hosszúságú egyenes szakasz mentén oszlik el egyenletesen (ld. 4-6 ábra.). Számítsuk ki az E elektromos térerősséget a vonal irányában lévő, annak.. ábra. 4-6 ábra végpontjától
. Gyakorlat 4B-9 A +Q töltés egy L hosszúságú egyenes szakasz mentén oszlik el egyenletesen (ld. 4-6 ábra.). Számítsuk ki az E elektromos térerősséget a vonal irányában lévő, annak.. ábra. 4-6 ábra végpontjától
1. A KLASSZIKUS FIZIKA ÉRVÉNYESSÉGÉNEK
 1. A KLASSZIKUS FIZIKA ÉRVÉNYESSÉGÉNEK HATÁRAI A XIX. század végén mindössze néhány probléma maradt megoldatlanul a fizika egyes fejezeteiből. Ilyen volt például a hőmérsékleti sugárzás problémaköre, a
1. A KLASSZIKUS FIZIKA ÉRVÉNYESSÉGÉNEK HATÁRAI A XIX. század végén mindössze néhány probléma maradt megoldatlanul a fizika egyes fejezeteiből. Ilyen volt például a hőmérsékleti sugárzás problémaköre, a
1. ábra. 24B-19 feladat
 . gyakorlat.. Feladat: (HN 4B-9) A +Q töltés egy hosszúságú egyenes szakasz mentén oszlik el egyenletesen (ld.. ábra.). Számítsuk ki az E elektromos térerősséget a vonal. ábra. 4B-9 feladat irányában lévő,
. gyakorlat.. Feladat: (HN 4B-9) A +Q töltés egy hosszúságú egyenes szakasz mentén oszlik el egyenletesen (ld.. ábra.). Számítsuk ki az E elektromos térerősséget a vonal. ábra. 4B-9 feladat irányában lévő,
Az atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen.
 MGFIZIK z atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. Z TOMMG SZERKEZETE, RDIOKTIVITÁS PTE ÁOK Biofizikai Intézet Futó Kinga magfizika azonban még nem lezárt tudomány,
MGFIZIK z atomhéj (atommag körüli elektronok) fizikáját a kvantumfizika írja le teljes körűen. Z TOMMG SZERKEZETE, RDIOKTIVITÁS PTE ÁOK Biofizikai Intézet Futó Kinga magfizika azonban még nem lezárt tudomány,
Elektromos alapjelenségek
 Elektrosztatika Elektromos alapjelenségek Dörzselektromos jelenség: egymással szorosan érintkező, vagy egymáshoz dörzsölt testek a szétválasztásuk után vonzó, vagy taszító kölcsönhatást mutatnak. Ilyenkor
Elektrosztatika Elektromos alapjelenségek Dörzselektromos jelenség: egymással szorosan érintkező, vagy egymáshoz dörzsölt testek a szétválasztásuk után vonzó, vagy taszító kölcsönhatást mutatnak. Ilyenkor
Az atom felépítése, fénykibocsátás (tankönyv 90.o o.)
 Az atom felépítése, fénykibocsátás (tankönyv 90.o.- 128.o.) Atomok, atommodellek (tankönyv 116.o.-120.o.) Már az ókorban Démokritosz (i. e. 500) úgy gondolta, hogy minden anyag tovább nem osztható alapegységekből,
Az atom felépítése, fénykibocsátás (tankönyv 90.o.- 128.o.) Atomok, atommodellek (tankönyv 116.o.-120.o.) Már az ókorban Démokritosz (i. e. 500) úgy gondolta, hogy minden anyag tovább nem osztható alapegységekből,
Az Ampère-Maxwell-féle gerjesztési törvény
 Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
1. Bevezetés az atomfizikába
 1. Bevezetés az atomfizikába A múlt század végén és századunk elején számos, az anyag szerkezetével kapcsolatos, új tényt fedeztek fel. Kiderült például, hogy az atomok elektronokból és magból állnak,
1. Bevezetés az atomfizikába A múlt század végén és századunk elején számos, az anyag szerkezetével kapcsolatos, új tényt fedeztek fel. Kiderült például, hogy az atomok elektronokból és magból állnak,
1. tétel A Az elektromágneses színkép tartományai.
 1. tétel z elektromágneses színkép tartományai. I. z elektromágneses sugárzás: z elektromágneses sugárzás egymásra merőlegesen haladó, oszcilláló elektromos és mágneses tér, mely hullám formájában terjed,
1. tétel z elektromágneses színkép tartományai. I. z elektromágneses sugárzás: z elektromágneses sugárzás egymásra merőlegesen haladó, oszcilláló elektromos és mágneses tér, mely hullám formájában terjed,
AZ ELEKTRON MÁGNESES MOMENTUMA. H mágneses erœtérben az m mágneses dipólmomentummal jellemzett testre M = m H forgatónyomaték hat.
 AZ ELEKTRON MÁGNESES MOMENTUMA Mágneses dipólmomentum: m H mágneses erœtérben az m mágneses dipólmomentummal jellemzett testre M = m H forgatónyomaték hat. M = m H sinϕ (Elektromos töltés, q: monopólus
AZ ELEKTRON MÁGNESES MOMENTUMA Mágneses dipólmomentum: m H mágneses erœtérben az m mágneses dipólmomentummal jellemzett testre M = m H forgatónyomaték hat. M = m H sinϕ (Elektromos töltés, q: monopólus
A sugárzás kvantumos természete. A hőmérsékleti sugárzás
 A sugárzás kvantumos természete A hőmérsékleti sugárzás Bevezetés A következőkben azokat a századorduló táján kutatott őbb jelenségeket tekintjük át, amelyek megértése a klasszikus izika alapján nem volt
A sugárzás kvantumos természete A hőmérsékleti sugárzás Bevezetés A következőkben azokat a századorduló táján kutatott őbb jelenségeket tekintjük át, amelyek megértése a klasszikus izika alapján nem volt
Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty
 Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty Dr. Berta Miklós bertam@sze.hu 2017. október 26. 1 / 11 Tekintsünk egy olyan kristályrácsot, amelynek minden mérete sokkal
Elektronok mozgása nanostruktúrákban 2-D elektrongáz, kvantumdrót és kvantumpötty Dr. Berta Miklós bertam@sze.hu 2017. október 26. 1 / 11 Tekintsünk egy olyan kristályrácsot, amelynek minden mérete sokkal
A fizika története (GEFIT555-B, GEFIT555B, 2+0, 2 kredit) 2018/2019. tanév, 1. félév Dr. Paripás Béla. 7. Előadás ( )
 A fizika története (GEFIT555-B, GEFIT555B, 2+0, 2 kredit) 2018/2019. tanév, 1. félév Dr. Paripás Béla 7. Előadás (2018.11.08.) Óracsere Itt tartandó rendezvény miatt a 10. előadás (2018. november 29. azaz
A fizika története (GEFIT555-B, GEFIT555B, 2+0, 2 kredit) 2018/2019. tanév, 1. félév Dr. Paripás Béla 7. Előadás (2018.11.08.) Óracsere Itt tartandó rendezvény miatt a 10. előadás (2018. november 29. azaz
Magfizika tesztek. 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem
 1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
1. Melyik részecske nem tartozik a nukleonok közé? a) elektron b) proton c) neutron d) egyik sem 2. Mit nevezünk az atom tömegszámának? a) a protonok számát b) a neutronok számát c) a protonok és neutronok
Sugárzások és anyag kölcsönhatása
 Sugárzások és anyag kölcsönhatása Az anyaggal kölcsönhatásba lépő részecskék Töltött részecskék Semleges részecskék Nehéz Könnyű Nehéz Könnyű T D p - + n Radioaktív sugárzás + anyag energia- szóródás abszorpció
Sugárzások és anyag kölcsönhatása Az anyaggal kölcsönhatásba lépő részecskék Töltött részecskék Semleges részecskék Nehéz Könnyű Nehéz Könnyű T D p - + n Radioaktív sugárzás + anyag energia- szóródás abszorpció
Elektronok, atomok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
Elektronok, atomok 2-1 Elektromágneses sugárzás 2-2 Atomi Spektrum 2-3 Kvantumelmélet 2-4 A Bohr Atom 2-5 Az új Kvantummechanika 2-6 Hullámmechanika 2-7 Kvantumszámok Dia 1/61 Tartalom 2-8 Elektronsűrűség
Folyadékszcintillációs spektroszkópia jegyz könyv
 Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Molekulák világa 1. kémiai szeminárium
 GoBack Molekulák világa 1. kémiai szeminárium Szilágyi András 2008. október 6. Molekulák világa 1. kémiai szeminárium Molekuláris bionika szak I. év 1 Kvantummechanika Klasszikus fizika eszközei tömegpont
GoBack Molekulák világa 1. kémiai szeminárium Szilágyi András 2008. október 6. Molekulák világa 1. kémiai szeminárium Molekuláris bionika szak I. év 1 Kvantummechanika Klasszikus fizika eszközei tömegpont
Koherens fény (miért is különleges a lézernyaláb?)
 Koherens fény (miért is különleges a lézernyaláb?) Inkoherens fény Atomok egymástól függetlenül sugároznak ki különböző hullámhosszon, különböző fázissal fotonokat. Pl: Termikus sugárzó Koherens fény Atomok
Koherens fény (miért is különleges a lézernyaláb?) Inkoherens fény Atomok egymástól függetlenül sugároznak ki különböző hullámhosszon, különböző fázissal fotonokat. Pl: Termikus sugárzó Koherens fény Atomok
Atommodellek. Készítette: Sellei László
 Atommodellek Készítette: Sellei László Démokritosz Kr. e. V. sz. Az egyik legnehezebb kérdés, amire már az ókori görög tudomány is megpróbált választ adni: miből áll a világ? A világot homogén szubsztanciájú
Atommodellek Készítette: Sellei László Démokritosz Kr. e. V. sz. Az egyik legnehezebb kérdés, amire már az ókori görög tudomány is megpróbált választ adni: miből áll a világ? A világot homogén szubsztanciájú
Kvantumos információ megosztásának és feldolgozásának fizikai alapjai
 Kvantumos információ megosztásának és feldolgozásának fizikai alapjai Kis Zsolt Kvantumoptikai és Kvantuminformatikai Osztály MTA Wigner Fizikai Kutatóközpont H-1121 Budapest, Konkoly-Thege Miklós út 29-33
Kvantumos információ megosztásának és feldolgozásának fizikai alapjai Kis Zsolt Kvantumoptikai és Kvantuminformatikai Osztály MTA Wigner Fizikai Kutatóközpont H-1121 Budapest, Konkoly-Thege Miklós út 29-33
Az ionizáló sugárzások fajtái, forrásai
 Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
Az ionizáló sugárzások fajtái, forrásai magsugárzás Magsugárzások Röntgensugárzás Függelék. Intenzitás 2. Spektrum 3. Atom Repetitio est mater studiorum. Röntgen Ionizációnak nevezzük azt a folyamatot,
Atomok, elektronok. Általános Kémia - Elektronok, Atomok. Dia 1/61
 , elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
, elektronok 2-1 Elektromágneses sugárzás 2-2 Atomi spektrum 2-3 Kvantumelmélet 2-4 Bohr-atom 2-5 Az új kvantummechanika 2-6 Hullámmechanika 2-7 A hidrogénatom hullámfüggvényei Dia 1/61 , elektronok 2-8
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 5. mérés: Elektronspin rezonancia. 2008. március 18.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
Röntgen. W. C. Röntgen. Fizika-Biofizika
 Röntgen Fizika-Biofizika 2014. 11. 11. Thomas Edison (1847-1931, USA) Első működő fluoroszkóp (röntgen-készülék) feltalálása, 1896 Sugárvédelem hiánya égési sérülések Clarence Madison Dally (Edison aszisztense):
Röntgen Fizika-Biofizika 2014. 11. 11. Thomas Edison (1847-1931, USA) Első működő fluoroszkóp (röntgen-készülék) feltalálása, 1896 Sugárvédelem hiánya égési sérülések Clarence Madison Dally (Edison aszisztense):
Sugárzások kölcsönhatása az anyaggal. Dr. Vincze Árpád vincze@oah.hu
 Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
Sugárzások kölcsönhatása az anyaggal Dr. Vincze Árpád vincze@oah.hu Mitől függ a kölcsönhatás? VÁLASZ: Az anyag felépítése A sugárzások típusai, forrásai és főbb tulajdonságai A sugárzások és az anyag
