Válasz Lovas Antal által benyújtott Akadémiai doktori értekezés bírálatára.
|
|
|
- Jakab Bognár
- 6 évvel ezelőtt
- Látták:
Átírás
1 Dr. Radnóczi György MTA doktora Úrnak Válasz Lovas Antal által benyújtott Akadémiai doktori értekezés bírálatára. Tisztelt Bíráló! Megköszönöm a dolgozat bírálatában részletesen kifejtett kritikai véleményét, amely a kivételesen alapos elolvasást tükrözi. Nem csupán a formai és szerkesztési hiányosságokra hívta fel figyelmemet, hanem részletesen megfogalmazta a tartalmi kérdések vonatkozásában is a kérdéseit. E bevezető mondatok nem udvariassági fordulatok. Néhány megjegyzését a jelenleg készülő összefoglaló publikációmban is hasznosítani tudom. Mindenekelőtt a koncepcionális kérdéseire adom meg válaszaimat, lehetőleg tömbösítve, egy-egy problémakör köré csoportosítva. Csak ezek után reflektálok a formai kifogásaira. Válasz az általános megjegyzésekre A dolgozat az utóbbi 15 év kísérleti munkáinak összegezése, de ez nem jelenti az eredmények egyszerű, tényszerű felsorolását. Ilyen jellegű lehetne pl. a dolgozat, ha a szerző egy bővített tézisfüzet formájában nyújtotta volna be pályázatát. Ehelyett, amint azt a bevezetőben is leírtam egységes értelmezést kívántam adni a kísérleti eredményekhez. Ennek megfelelően nagy hangsúlyt helyeztem az eredmények értelmezésére. A vonatkozó közlemények zömmel szerzői kollektívák munkái, több fizikai tulajdonságot és kísérleti módszert érintenek. A vonatkozó közlemények időbeni megjelenésük, és az alkalmazott mérési módszereinek tekintetében is nagy változatosságot mutatnak. Főként ezzel magyarázható, hogy az eredmények konkrét publikációkból kerültek átmásolásra. Stílusbeli, vagy grafikai különbözőségük homogenizálása időben is kivihetetlen szerkesztői feladat elé állította volna a dolgozat szerzőjét. A dolgozat kiindulási koncepciói között két fogalom játszik alapvető szerepet: a klaszter és a relaxáció. Mindkettő az üvegképződés jelenségével kapcsolatban kerül értelmezésre. Mindenekelőtt a klaszterjelenség (a dolgozat címében is szereplő) fogalom értelmezésére térek ki. A klaszter fogalmát napjainkban gyakran használják a gazdasági életben is: többnyire adott üzleti, vagy termelési célok elérésére történő (pl. pénzügyi, piacpolitikai stb.) szövetkezést (tehát gazdasági kapcsolat) jelent a gazdasági élet egységei, szereplői között. A fogalom tartalmilag tehát széles, többféle tevékenységre kiterjedhet. Jellegzetessége éppen az időlegesség és a közös cselekvési tér határainak lazasága. Ez a fogalmi rugalmasság jellemzi a fizikában, kémiában, vagy az anyagtudományban alkalmazott klaszter szót is. Legáltalánosabban definíció szerint: klaszter az atomoknak olyan halmaza, amelyek a megfigyelés ideje alatt valamilyen szempontból összetartoznak. A megfigyelés ideje esetünkben maga a mérési folyamat. Kondenzált anyagokban az összetartozás leggyakrabban kötési kapcsolatot jelent, de eredet, vagy méret szerint is megkülönböztethetjük a klasztereket. Méret, vagy eredet szerint a klaszterek tulajdonságai nagymértékben különbözhetnek: (pl. gőzök kondenzációja során, vagy az olvadékokban keletkező, ultra-nagy sebességgel befagyasztott, szabad felülettel nem rendelkező klaszterek tulajdonságai lényeges eltérést mutatnak. Egy dologban azonban közösek: méreteiknél fogva metastabil képződmények. 1
2 Nanométeres kiterjedésűek, hasonlóan, mint a kristályos fázisok kritikus csírái a megfelelő ötvözetben. Metastabilitásuk következménye, hogy a hőkezelési folyamatokban, vagy akár valamely mágneses tulajdonság meghatározása során (pl. Curie-hőmérséklet mérése, ami legtöbbször a hőmérséklet növelését jelenti) átalakulnak, vagy megsemmisülhetnek. Amint fent említettem, a klasztereknek, mint metastabil képződménynek fő jellemzője a tulajdonságaik méretfüggése. E méretfüggés univerzális, bármilyen eredetű klaszteregyüttesről van szó. Példaként erre mutattam rá a 2/a és 2/b ábrákon, ahol a szilárd fémes fázisokra jellemző egyik legalapvetőbb tulajdonság, az ionizációs energia is megváltozik a klaszter méretével. A 2/b ábra pedig arra világít rá, hogy pusztán a mérethatások miatt a nanométeres méret-tartományban a fő kémiai kötéstípusok is megváltozhatnak (pl. a gyémántra jellemző sp3 hibridállapot fokozatosan átalakul a grafitra jellemző kötésállapottá, pusztán mérethatások miatt). Éppen ez az érdekes univerzalitás a feltett kérdéssel kapcsolatban. A kritikus méretű csíra kialakulása sem jelenti a makroszkópos (fázisfogalom által megkövetelt) tulajdonságok megjelenését. Csak a növekedés képességet jelölik meg termodinamikai kritériumként. Dolgozatomban a klaszterek szerkezet- és tulajdonságformáló szerepét vizsgáltam, és jelenlétük feltételezésével bizonyos folyamatokat, átalakulásokat is értelmeztem. Eredet szempontjából kétféle klasztertípussal foglalkoztam: Az egyik típus az olvadék szerkezetének, ill. a szerkezet hőmérséklettel történő változásának következménye, a jelenlévő eltérő kötéstípusok (kovalens, fémes) miatt alakulnak ki gyorshűtés során, bizonyos hőmérséklet-tartományban. A fizikai tulajdonságok és átalakulások vizsgálata során ezeket összefoglalóan fázis-emlékezések -nek neveztem. A másik klaszter-típus H-oldódás hatására alakul ki, rendszerint o C-os hőkezelések során. Ezek a klaszterek nanométeres kiterjedésűek, és mikro-fázisszeparációknak is nevezi az irodalom. Ez utóbbiak nagyfelbontású elektronmikroszkópos vizsgálattal jól megfigyelhetők. A klaszterek szerkezetformáló szerepét Bakai [16] univerzális jelenségként tárgyalta. Munkái elméleti, termodinamikai meggondolásokon alapulnak. A gyakorlati szempontból fontos fizikai tulajdonságokkal, valamint a metallurgiai háttérrel történő kapcsolat megteremtése jelentette dolgozatom fő vállalkozását. E kapcsolatok kifejtésére, indoklására külön-külön is kitértem az egyes jelenségek ismertetése során. Feltehetően ezért érzékeli a bíráló a dolgozatot mozaikszerűnek. A másik alapvető fogalom a relaxáció. Termodinamikai szempontból a relaxáció minden esetben az egyensúlyra törekvés folyamatát jelenti. A klaszterszerkezet eredetének vonatkozásában (az olvadékszerkezetben lejátszódó atomi szintű folyamatokra való tekintettel) azonban ezt a fogalmat ma általánosabban használják, mint azt korábban, a fémüvegek hőkezelése során megfigyelt jelenségek értelmezése kapcsán tették (az üvegátalakulási hőmérséklet alatt megfigyelt tulajdonság változások). E kérdéskör megvilágítására idéztem dolgozatom irodalmi összefoglalójában az alábbi ábrákat is: 2
3 V, H, S Tg 1 Tg 2 olvadék G(v 1) G(v ) 2 v 1 >v 2 kristály Hőmérséklet Tolv 5.a. ábra A fajtérfogat, entalpia és entrópia hőmérséklet-függése a kristályos és az üvegátalakulás során. G(v 1 ) és G(v 2 ), a (v 1 > v 2 ) sebességgel hűtött olvadékokra vonatkozó üvegátalakulásokat, ill. üvegállapotokat ábrázolják 17. ábra Reverzibilis ( H r ) és irreverzibilis ( H irr ) entalpia relaxáció az előállításkor alkalmazott hűtési sebesség függvényében Fe 82,5 B 17,5 összetételű mintánál. [60] Az 5/a ábra az üvegátalakulás jelenségét ábrázolja (T g1, T g2 ). Látható, hogy a nagyobb sebességgel (v 1 ) hűtött olvadék nagyobb hőmérsékleten esik ki a termodinamikai egyensúlyból, ennek következtében hőtartalma, entrópiája és fajtérfogata is nagyobb, mint a lassabban hűtött olvadéké. Jól mutatja ezt a különbséget az 17. ábra, ahol a hűtési sebesség függvényében ábrázolták az irreverzibilis és reverzibilis entalpia-relaxációt. Ebből látható, hogy a többlet entalpia és entrópia tekintélyes része az üvegátalakulás hőmérséklet-tartományában fagy be. Az üvegátalakulás lényegi kijelentése tehát, hogy nem határozott hőmérsékleten, hanem hőmérséklettartományban történik meg. E tartományon belül, a szóban forgó termodinamikai állapotfüggvények gyorsan, de folyamatosan változnak, és a rendszer a termodinamikai egyensúlyból kiesik. 3
4 4. ábra Az üvegátalakulás fenomenológiáját összefoglaló ábra: A hőmérséklettartomány a belső egyensúly állapotát, B a relaxációs események tartományát, C a teljesen befagyott állapot hőmérséklet-tartományát jelöli [25] A jelenségkörnek részletesebb elemzése látható a 4. ábrán, amely már rávilágít a túlhűtött olvadék és a fokozatosan befagyó rendszer termodinamikai különbségére is: Három tartományt különböztethető meg itt: az A tartományt az jellemzi, hogy a hőelvonás (beavatkozás, megfigyelés!) időtartománya sokkal nagyobb, mint az atomi transzlációs mozgások elemi lépéseinek időtartama, ezért a konfigurációs entrópia változása maximális, vagyis a hűlés során szabadenergia minimumokon halad át a rendszer. Ekkor nevezik ergodikusnak. Magát a folyamatot, ami az energiaminimum eléréséhez vezet, relaxációnak hívjuk. A növekvő túlhűlés során azonban az atomi mozgások elemi lépései lelassulnak, és a hőmérsékletváltoztatás (a hőelvonás) sebességéhez közelítenek. Ekkor érünk a B tartományba, ahol már a megfigyelés, vagyis a makroszkópos beavatkozás ideje alatt is érzékelhető átrendeződés (vagyis a relaxációs folyamat) zajlik. A rendszer, mikroszkópos szinten itt már nem tudja lekövetni a hőmérséklet változása által megkövetelt szabadenergia minimumot és fokozatosan befagy ( C állapot). Itt kell megjegyezni újból, hogy ebben az állapotban végrehajtott termikus beavatkozásokat (amelyek rendszerint hosszú idejű hőkezelések) nevezik gyakorlati szempontból szerkezeti relaxációnak. Ezekben a folyamatokban beszélünk a tulajdonság formálásának lehetőségéről (tailoring), amelyeknek nagy szerepük van a lágymágneses jellemzők optimalizálásában. Ami a 12. oldal 6. ábráját illeti, azt hiszem, világosan leírtam, hogy az ábra a túlhűlő olvadékok viszkozitásának változását ábrázolja (logaritmikus léptékben) a T g -vel normált hőmérséklet függvényében. Két olvadék-alaptípusról van szó: az egyikre tipikus példa a szilicium-dioxid (SiO 2 ) olvadék. Ebben egyetlen fő (kovalens) kötéstípus van, ennek megfelelően a viszkozitás hőmérsékletfüggése az egész hőmérséklet-tartományon belül egyetlen aktiválási energiával közelíthető: ez az u.n. Arrheniusz-jellegű viselkedés. Hasonló viselkedést mutatnak egyébként más, kovalens oxidok is. Az irodalom az ilyen olvadékokat jellemzi strong (erős) jelzővel, amivel arra utalnak, hogy az olvadék szerkezetében (rövidtávú atomi koordinációs környezet) nincs változás az olvadék túlhűlése során, miközben a viszkozitás változik [30]. Az atomok transzlációs mobilitását biztosító mechanizmus (Stokes-Einstein összefüggés) a Si-O kötések hőmérséklettől függő, felszakadási és rekombinációs gyakorisága következtében teljesül. Az ilyen olvadéktípusok üvegképző hajlama igen nagy, úgyhogy olvadékból a kristályos állapot elérése jelent nehézséget. 4
5 6. ábra A strong és fragile üvegképző olvadékok viszkozitás-hőmérsékletfüggé-sének összehasonlítása túlhűtött olvadékál-lapotban [30] A fenti típustól gyökeresen eltérő viselkedést mutatnak az u.n. fragile olvadékok, amelyekben a viszkozitás hőmérséklet függése nem írható le egyetlen aktiválási energiával a túlhűlés során (u.n. Vogel Tammann Fulcher-közelítés). Ezeknek az üvegképző hajlama kicsi. Tipikusan ebbe a kategóriába sorolhatók a fémes, üvegképző olvadékok. Az üvegképződéshez itt nagy hűtési sebesség szükséges ( K/sec). Megjegyeznem, hogy az egyébként fémes olvadékok üvegképző hajlama is széles tartományban változhat, amint ezt a sokkomponensű, u.n. bulk amorphous rendszerek felfedezése óta tudjuk. Az üvegképző hajlam itt megközelíti a kovalens olvadékokét. A dolgozat 7. ábráján ilyen (Arrheniuszjellegű) viszkozitás-változásra is láthatunk példát. Az u.n. fragile olvadéktípusokban figyelhető meg túlhűlés folyamán a klaszterekre történő szétesés. Ez térben is elkülönülő atomhalmazok megjelenését jelenti a túlhűlés növekedésével. Az egyes klasztertípusokban a relaxáció (az egyensúlyi állapot irányában történő átrendeződés) is különböző sebességgel zajlik. A térben is elkülönülő atomcsoportokban az atomi mozgások dinamikája tehát eltérő [36]. A jelenséget több komponensű, polimerolvadékokban mutatták ki először. A lokálisan eltérő atomi mobilitás okát az eltérő kötéstípusokban látják (pl. kovalens és másodlagos kötések). Ezt a gondolatot vittem tovább dolgozatomban, kiterjesztve az üvegképző fémes olvadékokra is annak okán, hogy az általam vizsgált fémes olvadékokban is legalább két, vagy többféle kötéstípus és szimmetria különül el (az egyensúlyi kristályos fázisok között ugyanis átmenetifém boridok, szilicidek és szilárd oldatok egyaránt megtalálhatók). A dolgozatban szereplő ötvözetekre, ill. olvadékaikra a fenti klaszter-fogalom jól alkalmazható. 5
6 A bíráló a 34. oldalra vonatkozóan írja: A 26. ábrát nem használja stb. Az ábrát igenis használom, éppen az ábra fölötti bekezdésben utalok rá, pontosan azért, hogy a FINEMET típusú ötvözetekben a kettős nukleációs mechanizmusra vonatkozóan elképzelésemet kifejtsem. (összefoglalása a II tézispontban!) 34. oldal: A 26/a,b ábrák a biner Fe-B hypo-eutektikus ötvözet kristályosodási folyamatát ábrázolják termomágneses és DSC mérések során. Mindkét mérés közös jellemzője, hogy a minta hőmérsékletét állandó sebességgel növeljük, miközben folyamatosan mérjük a minta mágnesezettségét (26/a ábra) ill. a kristályosodási folyamatban észlelhető hőfelszabadulást. (26/b ábra). Eszerint tehát az x tengelyen az idő függvényében regisztrált hőmérséklet látható. Ami a két fizikai mennyiség hőmérséklet szerinti változását illeti, meg kell jegyezni, hogy a mérések helye és időpontja is lényegesen különböző. Lényeges ezen kívül, hogy a két fizikai mennyiség változása az egyes hőmérsékleti tartományokban (természetükből következően) eltérő érzékenységgel követhetők nyomon. A két mérés összehasonlításához az alábbi értelmezést fűzöm: A mágneses mérésekből levonható információk: szobahőmérséklet és kb. 600K között az amorf minta ferromágneses, de mágnesezettsége folyamatosan csökken és a Curiehőmérsékleten 0 értéket ér el. A Curie-hőmérsékleten azonban az amorf állapot termikus bomlása még nem kezdődik el (ennél az összetételnél), vagyis a mágnesezettség egy ideig még 0 értéken marad. Ha a minta termikus bomlása (kristályosodása) elkezdődik, a hőmérséklet függvényében mérhető mágnesezettség változása attól függ, hogy a kristályosodáskor keletkező fázisok (keletkezésük hőmérsékletén) ferromágnesesek-e, ill. képződésük milyen sebességgel zajlik? a b 26 ábra (a) Biner, hypo-eutektikus Fe 85 B 15 ötvözet kristályosodását ábrázoló termomágneses görbék különböző hűtési sebességű, azonos összetételű hipo-eutektikus Fe 85 B 15 fémüveg esetében. A (b) ábrán látható DSC termogramon a bomlási folyamatban a primer -Fe kiválását jelzi az első kristályosodási lépcső. A második kristályosodási lépésben Fe 3 B intermetallikus vegyület keletkezik. (A két csúcs távolsága nemcsak összetételtől, hanem az előállításkor alkalmazott hűtési sebességtől is függ [27] Minthogy hypo-eutektikus Fe-B ötvözetről van szó (Fe 85 B 15 ), a kétlépcsős kristályosodáskor keletkező primer termék, az Fe (ferrit) még ferromágneses (ennek a fázisnak Curiehőmérséklete ugyanis 1040 K) 6
7 A bomlási folyamat első felében keletkező második kristályos fázis a Fe 3 B. Keletkezésének hőmérsékletén ez ugyancsak ferromágneses, (Curie hőmérséklete kb 800 K) ez utóbbi fázis azonban metastabil, és csak a FeB amorf ötvözetek kristályosodási folyamataiban figyelhető meg, ezért nincs is feltüntetve az egyensúlyi fázisdiagramokon [6]. A termomágneses görbe második maximumát az Fe 3 B -Fe+Fe 2 B reakció lezajlásának tulajdonítja az irodalom. Az Fe 2 B ugyanis, miként az Fe, még ebben a hőmérséklettartományban is ferromágneses (disszertációban a 34 old. III. reakció). Meg kell jegyezni azonban, hogy ez utóbbi reakció termikusan alig mutatható ki, ezért a 26/b ábrán látható DSC termogramokon ezt a folyamatot már nem ábrázolják. A 26. ábrák közös kijelentése hogy mind a termomágneses, mind a DSC termogramok alakjára hatással van az olvadék gyorshűtésekor alkalmazott hűtési sebesség, amelyet relatív léptékben (v/v o = 5, ill. 10) a (b) ábrán tüntettem fel. Másik fontos kijelentése az ábráknak, hogy csökkenő B-tartalommal, a hypo-eutektikus tartományban az első és második kristályosodási lépcső fokozódóan elkülönül (a dolgozatban 27. ábra). Ez utóbbi jelenség képezi alapját a FINEMET típusú ötvözetek kifejlesztésének. Az alábbiakban ezt részletezem: A dolgozat 34. oldalán látható reakciósémák, valamint a 36. oldal reakciósémáinak összehasonlítása alapján nyilvánvaló, hogy a FINEMET ötvözetekben lezajló amorfnanokristályos átalakulás őstípusa a hypo-eutektikus Fe-B ötvözet kristályos átalakulásának első lépcsője, vagyis az Fe kiválását eredményező primer reakció. E reakciónak le kell zajlania mielőtt a második kristályosodási lépcsőben keletkező mágnesesen kemény boridok képződése elkezdődne. Ehhez a két kristályosodási lépcsőnek biztonságosan el kell különülnie. Hasznos útmutatásul szolgál ehhez a már idézett 27. ábra: a két kristályosodási lépcső annál inkább elkülönül a hőmérsékleti skálán, minél kisebb a fémüveg B-tartalma. Problémát jelent azonban, hogy a szükséges mértékű elkülönüléshez a B-tartalom csökkentése nem elegendő, mivel az üvegképző hajlam is jelentősen lecsökken kis B-tartalom esetén, ezzel az alapanyagul szolgáló amorf ötvözet üzemi méretű előállíthatósága meghiúsul. További adalékanyagokat alkalmaznak ezért az amorf prekurzor-ötvözet gyárthatóságának, és a nano-kristályosító hőkezelés technikai biztonságának növelésére (üvegképző hajlamot növelő és a primer Fe nukleációját elősegítő komponensek adagolása). Közismert adalékanyagok: Cu: nukleációt elsősegítő komponens Nb: a Tx2 borid fázis megjelenésének hőmérsékletét növeli, A Si (a B-al együttesen) üvegképző hajlamot növelő komponens. Az adalékanyagok szerepének vizsgálata témakörben elsősorban a Cu-nukleációt elősegítő hatásának mechanizmusával foglalkoztam, mert ez tekinthető a célkitűzéseimben megnevezett klaszterjelenségnek : A nukleációt elősegítő hatás lényege az első kristályosodási lépcső hőmérsékletének csökkentése, vagyis a kritikus csíra megjelenéséhez szükséges termikus aktiválás csökkentése. A dolgozat 47. ábrája jól mutatja a Cu kristályosodási lépcsők elkülönülésére kifejtett hatását. Ez a hatás a konkrét B-tartalomtól független jelenségnek bizonyul (hypo-eutektikus tartományról van szó!). A Cu hatásmechanizmusának szerepét az alábbi érvelés alapján érthetjük meg: Az alább látható fázisdiagram szerint a Cu oldékonysága a mezőben (fcc!) jelentékeny, míg a kis hőmérsékleten stabil -fázisban (bcc!) (különösen o C tartományban, tehát ott, ahol a nanokristályosító hőkezeléseket végzik) már elhanyagolható. 7
8 P (W/g) 3 Fe 85 Cu 1 B 14 Fe 86 B 14 2 v = 20 K/perc Hõmérséklet ( o C) a b 47. ábra (a) A Fe 86 B 14 és Fe 85 Cu 1 B 14 fémüvegek kristályosodásának DSC termogramja (a Cu ötvöző hatása a kristályosodási lépcsők közötti hőmérséklet különbség növekszik) [141] (b) A Fe-Cu ötvözetrendszer fázisdiagramja Az olvadékból történő gyorshűtés során -jellegű környezetek dermednek bele az amorf matrixba. Azt is mondhatjuk, hogy a bekvencselt Cu-atomok szimmetriájú-környezeteket létesítenek maguk körül, ezek azonban mágneses szempontból feszültségcentrumokat jelentenek (a koercitív erőt növelik!) Ezek a környezetek ugyanakkor metastabilak is, hiszen kis hőmérsékleten a Fe mátrix bcc módosulata a termodinamikailag stabil fázis. Termikus aktiválással ezek a -centrumok (klaszterek) eutektoidos reakcióval -Fe és Cunukleuszokra bomlanak le, ezzel a stabil fázisok csíráit hozzák létre. A két nukleuszból (most már heterogén nukleációval!), nyilván az -Fe szemcsék növekednek nagyobb sebességgel, (többségi matrix-atomok!) ugyanakkor ezekből a Cu-atomok oldékonysági okokból már kiszorulnak. A vázolt elképzelést alátámasztja az a kísérleti tény, hogy a koercitív erő már jóval a nanokristályos Fe-szemcsék kifejlődése alatti hőmérsékleteken lényegesen lecsökken [5,6 :tézisekhez tartozó publikációk] Így válik érthetővé hogy Cu atomok kilépnek a kristályosodási folyamatból. 8
9 Kísérleti eredmények és értelmezésük Miért ezeket az anyagrendszereket választotta.? A ötvözetek kiválasztását több szempont is motiválta: - mindenekelőtt az, hogy a vizsgált jelenségek szempontjából a Fe-alapú amorf ötvözetek a leginkább alkalmasak az u.n fázisemlékezések típusú klaszterszerkezetek kialakulásához, így a bevezetésben is megfogalmazott célkitűzésnek (egységes értelmezés) leginkább megfelelnek. Az előzőekben már említettem, hogy a klaszterek keletkezésének metallurgiai hátterében a Fe allotróp módosulatai ( - és -Fe) jelentős szerepet játszanak. Különösen jelentőssé válik ez a tulajdonság, ha az ötvözőelemek eltérő oldékonyságát is szemügyre vesszük a szóban forgó allotróp módosulatokban. Erre a tényre jól rávilágítanak a dolgozat (33, 34.) ábrái. Jelentőségük kiemelkedő az acél metallurgiájában is. (pl edzhetőség, edzési folyamatok mechanizmusa stb) 33. ábra 34. ábra 33. ábra Különböző fémek hidrogénoldó képessége (ill. egyensúlyi H-tartalma) a hőmérséklet függvényében [91] 34. ábra A 3d átmenetifémek maximális karbonoldó képességének összehasonlítása a bcc és fcc módosulatokban Bár a 34. ábra a karbon maximális oldhatóságáról ad információt, üzenete világosan utal más metalloidok oldékonyságára is. (pl.h, N oldékonysága a Fe fcc módosulatában jelentősen nagyobb, mint a bcc módosulatban. Közismert, ugyanakkor az is, hogy ennek nem csupán kristálytani, hanem elektronszerkezeti okai is vannak. (a 34. ábrán látható ugyanis, hogy d- elektronpályák növekvő feltöltődésével, az fcc típusú u.n. 3d átmenetifémekben is fokozatosan 9
10 csökken az oldékonyság). Ismételten felhívom a figyelmet arra, hogy a H oldékonysága is nagyobb a Fe fcc módosulatában (33. ábra). Ennek szerepe a -centrumok és az oldott hidrogén közötti kölcsönhatás vonatkozásában lényeges. A dolgozat irodalmi összefoglalójában ezt kifejtettem. Az ötvözetek kiválasztásának másik motivációját a gyakorlati alkalmazás jelenti. A Fe-alapú fémüvegek (FeSiB), kisveszteségű hálózati transzformátorok (lágymágneses) alapanyagai. Ugyancsak Fe alapúak a már előzőekben ismertetett FINEMET nanokristályos prekurzorötvözetek (a dolgozat 1. ábrája) A nanokristályosító hőkezelések technológiájának hazai kidolgozásában a szerzőnek szerepe volt. (lásd: Varga B PhD munkája és a csatlakozó közlemények). Néhány kiegészítő értelmezés az ábrákhoz és a klaszterszerkezet kialakulásához. Ami az eutektikus összetételre vonatkozó pontatlanság -ot illeti, a szakmai közélet természetesnek tartja, hogy csakis a Fe-hoz közeli eutektikumról lehet szó, hiszen lágymágneses anyagokról és ezek alkalmazásáról már a dolgozat bevezetőjében is utaltam. A 44/a és b kifogásolt ábrákon szereplő összetételi értékekből ugyancsak nyilvánvaló, hogy melyik eutektikumról van szó. Az ábrákon egyébként valóban nem következetes a hőmérséklet jelölése. Az egyiken K, a másikon o C ban adtam meg a hőmérsékletet. Itt ismét a különböző időben és társszerzőkkel megjelent publikációkból történő, sajnálatos ábra-beemelésről van szó. A b ábrán látható számok egyébként különböző forrásmunkákból történő hivatkozást jelölnek. A forrásmunkák eltérő eredete egyébként növeli annak a kijelentésnek bizonyító erejét, amely szerint a Curiehőmérséklet (a várakozással ellentétben!) csökken a Fe-tartalom növekedésével. Ennek az ellentmondásnak feloldására éppen a klaszterszerkezeten alapuló érvelés nyújt lehetőséget. Amikor centrumokról beszélünk, nem nano-kristályos méretű, kristályos fáziscsírák befagyására gondolunk, hanem a topológiai rend helyi megváltozásáról van szó. Ezekben a klaszterekben a Fe-atomok atomi térfogata helyileg kisebb, mint a matrix többi részében. Az ilyen rendkívül kis sűrűségváltozások ugyanakkor nem mutathatók ki makroszkópos módszerekkel. Elméleti következtetések vannak viszont arra vonatkozóan, hogy miként kell viselkednie mágneses szempontból a Fe-atomoknak az ilyen környezetben. Erre vonatkozó meggondolásokat tartalmaz az u.n. Bethe-Slater görbe, amely megadja kicserélődési integrál (J) változását az atomok közötti (normált) távolság függvényében: 42. ábra A Bethe Slater-görbe, amely megadja a kicserélődési integrál (J) értékét az atomok közötti távolság (a) és a d héj sugarának (d) függvényében [120] Látható a 42. ábra alapján, hogy a ferromágnesség megjelenése szorosan összefügg az atomok közötti távolsággal. A J értéke gyorsan változik (előjelet is váltva!). Az előjel váltás megfelel a Fe 10
11 és módosulatainak megfelelő makroszkópos mágneses viselkedésnek, vagyis annak, hogy a Fe lokális, atomi térfogat változásával (az atomi térfogat csökkenésével) a ferromágneses csatolás helyileg akár meg is szűnhet ( -Fe). Ennek az elméleti meggondolásnak helyességét alátámasztják azok a makroszkópos mérések, amelyek szerint az Fe Curie-hőmérséklete (ami függvénykapcsolatban van a J kicserélődési integrállal) a makroszkópos hidrosztatikus nyomás növelésével csökkenthető, míg a Ni esetében a T Curie növekszik a hidrosztatikus nyomás hatására. Az olvadék gyorshűtésének lényegéből következik, hogy nagy hőmérsékleten (a túlhűtött olvadékfázisban, vagyis a T g fölött) nagy számban keletkeznek olyan klaszterek, amelyekben a Fe atomok atomi térfogata kicsi, ill. közel áll a -Fe-ra jellemző tömörebb illeszkedéshez, ill. szimmetriához. A befagyott szerkezetben a -Fe -Fe típusú, rövidtávú átrendeződés csak termikus aktiválás hatására történhetnek meg. Ez a folyamat a fémüveg relaxációs hőkezelése során folyamatosan történik meg a hőmérséklet növelésével, de ugyanez játszódik le akár a Curie-hőmérséklet mérésével járó felfűtési folyamatban is. Ennek az lesz a következménye, hogy a T am c irreverzibilisen növekszik, mert ebben a hőmérséklet-tartományban termodinamikailag az -Fe típusú környezetek ill. szimmetriák a stabilak. Ennek az irreverzibilis változásnak a termikus alátámasztását mutatja a 17. ábra, amely szerint az irreverzibilis relaxáció során felszabaduló u.n. relaxációs entalpia nagymértékben függ az olvadék gyorshűtése során alkalmazott hűtési sebességtől. Összefoglalva, a fenti (fázis-emlékezés) típusú klaszterek jelenlétére nem közvetlen szerkezetvizsgálatból jutottam, hanem, számos mágneses tulajdonság elemzése és értelmezése révén, e következtetéseket azonban Mössbauer-vizsgálatok is megerősítik. A 48 a,b ábrákon nincs felcserélés a Cr-tartalomban: éppen azt akartam megmutatni, hogy változatlan B-tartalom mellett, a Fe-matrixfém fokozatos lecserélésével nincs monoton változása sem a termofeszültségnek, sem pedig az amorf Curie-hőmérsékletnek, noha az egyszerű elektronszerkezeti modell alapján ezt várnánk. Ehelyett, egészen kis Cr-tartalmak esetén pozitív irányban tolódik el a termofeszültség, változása ellenkező irányba fordul a tiszta binner Fe-B hoz képest. Ugyancsak törés mutatkozik a Curie hőmérsékletben (hypoeutektikus ötvözet) a Cr-tartalom függvényében. Azért kell feltételeznünk az amorf állapoton belüli rejtett szerkezetváltást, mert az általánosan elfogadott elméleti meggondolásokból következő homogén, egyfázisú szerkezeti kép az egy atomra eső d-elektronszám, (e d /a) folytonos változásából következően monoton változást jósol mind a mágneses, mind a termikus tulajdonságokban. Tehát nem egyszerűen csak tényként tárgyalom az ábrákon látható ötvözőhatást, hanem annak megmutatására is, hogy az általánosan elfogadott elméleti meggondolásokkal ellentétben a vizsgált jellemzők nem mutatnak monoton változást. Tény ugyanakkor, hogy e változásokat jelenleg csak kvalitatív módon tudjuk szerkezetváltozáshoz (klaszter-szerkezet) hozzárendelni. Ilyen értelemben beszélek rejtett szerkezetváltozásról. Hangsúlyozom, hogy a változások több tulajdonságban azonos koncentrációtartományban következnek be (kristályosodási hőmérséklet, energia, keménység) (47/a, 48/a ábrák). Összegezve: állításom az, hogy az üvegállapot homogén-kontínuum elképzelésén alapuló, akár szerkezeti, akár elektronszerkezeti képhez kötődő leírások nem nyújtanak lehetőséget több fizikai tulajdonság összetételfüggésének értelmezéséhez. A tulajdonságokban mutatkozó anomáliák, így indokolttá tették a már ismertetett klaszter-felépítés feltételezését. A oldal kérdései ismét az amorf nanokristályos átalakulás kezdő (nukleációs) jelenségeivel kapcsolatosak: 11
12 Erre vonatkozóan ismételten hangsúlyozom, hogy a Cu szerepe a kettős nukleációs mechanizmusban van, aminek lényege az fcc jellegű környezetek eutektoidos bomlása. Ebben az értelmezésben a klaszter nem más, mint fcc szilárd oldathoz közeli szimmetriájú, kb. nanométeres kiterjedésű olvadékállapotból származó, bekvencselt atomhalmaz, amely szobahőmérséklet közelében már metastabil. Ezek a centrumok alakulnak át csatolt mechanizmussal kristályos -ferrit és Cu nukleuszokká. Hasonló jellegű ez a mechanizmus a szénacélokban megfigyelhető ausztenit-perlites átalakuláshoz. Ami a diffúzió irányát, annak termodinamikai hátterét illeti, azt nem a koncentrációk, hanem a kémiai potenciálok irányítják. Ennek megfelelően, adott hőmérsékleten nem szükségszerűen a homogén szilárd oldat a stabilabb fázis. A mechanizmus igazolására diffrakciós evidenciákat a jelen dolgozat nem tartalmaz, a szerző nem tűzte ki célul, mivel e területen nem járatos. A Cu katalizáló szerepét viszont a 47. ábra is bemutatja. (DSC vizsgálat, 141 publ.). Nyilvánvaló, hogy Cu-nek, hatása a kristályosodás két fő lépcsőjének elkülönítésében kap szerepet, így teret enged a nanokristályos Fe(Si)-fázis kialakulásának anélkül, hogy mágnesesen kemény boridok is képződnének. A bíráló többször is kifogásolta a kísérleti evidenciák hiányát a -centrumok (fázis emlékezések) alapján az indirekt érvelést elégtelennek tartja. Ezzel kapcsolatban több dolgot le kell szögeznem: 1. A dolgozatban szereplő kísérleti eredmények publikált kísérleti tények, amelyeket ugyan lehet vitatni, de zömükben önmagukban is megálló, lektorált folyóiratokban közölt eredmények 2. csak direkt, diffrakciós bizonyítékok ilyen méretű (nanométeres kiterjedésű) szerkezeti tényezők kimutatása tudomásom szerint igen nagy költségigényű, atomi felbontású mikroszkópos technikát igényelne. Ezek nem álltak rendelkezésemre. 3. A dolgozatot célkitűzésében megfogalmazott értelmezést ugyanakkor számos indirekt bizonyíték támasztja alá, melyek az alábbiak: A lágymágneses fémüvegek hőkezelése során tapasztalható koercitív erő csökkenés, még az amorf állapotban. Ez a megfigyelés egyezésben van az irodalommal. Saját eredmények közül erre utalnak pl. a már említett 5. táblázat adatai: 400 o C hőkezelés hatására a H c már közel azonos a nanokristályos állapotra jellemző értékkel. Ilyen hőmérsékleten pedig még kifejlett nanokristályos szerkezetről nem beszélhetünk. Erre viszont direkt, diffrakciós evidenciák is vannak. Hasonló következtetések vonhatók le a veszteség csökkenéséből is: pl. 350 o C-os izoterm hőkezelés több mint 50%-al csökkenti a veszteséget, noha ezen a hőmérsékleten bizonyíthatóan csak feszültség-relaxáció zajlik. (52. sz ábra, 132 hivatkozás) A hidrogén abszorpciója a relaxált (hőkezelt, de nem nanokristályosított) FINEMET mintában gyakorlatilag megszűnik. E jelenség a H-atomok által preferált rövidtávú (fcc) környezetekbe történő befogásával magyarázható. Amint az előzőekben már említettem, ezek a környezetek relaxációs hőkezelések hatására leépülnek. (19.saját publ.) Mi lehet az a szerkezetváltozás, amit direkt diffrakciós módszerekkel nem lehet nyomon követni? Válaszom: van ilyen szerkezetváltozás: pl. kristályos, híg szilárd oldatokban (főleg atomi szintű szerkezetváltozásra gondolok.) Pl. oldott atomok környezetében a méretkülönbség és 12
13 az elektronszerkezet helyi megváltozása miatt lokális feszültségtér keletkezik. Vagy: pl. fémüvegekben a szerkezeti relaxáció hatására a diffrakciós gyűrű szélessége megváltozik, (rendszerint csökken) azonban ebből kvantitatív következtetések nehezen vonhatók le. A szerkezeti relaxáció jelenségköre és a fázisemlékezések viszonya (a következő reflexiók a T c am mérésekből származó információkkal és azok értelmezésével kapcsolatosak.) Mindenekelőtt a T am c mérés pontosságára, ill. a mérés technikai kivitelezésének kapcsolatából levonható következtetésekre reflektálok. A mérések az u.n. FONER-típusú magnetométerben történtek, amelyben a mintát egy ellenállás fűtésű kályhába helyezték el és programozható sebességű fűtést alkalmazva határozták meg a Curie-hőmérséklet. am A termomágneses görbére illesztett egyenes és a T tengely metszéspontját fogadták el a T c -nek (ez egyébként megegyezés kérdése, a lényeg, hogy minden esetben azonos elvek alapján történjen a mérés kivitelezése és kiértékelése). A mérés pontossága szempontjából lényeges szerepe van a felfűtés sebességének is, mivel az hőátadási okok miatt nem lehet túl gyors. Ugyanakkor, a T am am c környezetében már relaxáció is történhet a mintában, ami szintén T c változást eredményezhet, ezért minden mérést ugyanolyan felfűtési programmal kell végezni. Lényeges lehet a minta pozicionálása is. A tapasztalat szerint akkor legpontosabb a mérés, ha a mintát (ismételt, reprodukciós mérések során) nem vesszük ki a berendezésből, és így ismételjük meg a mérést. Ilyen esetben a T am c 1C o -on belüli szórással meghatározható. Etalon anyagként azonos súlyú és geometriájú Ni-fóliát használnak, mert abban nincs szerkezetváltozás, ami a Curie-hőmérséklet befolyásolná. Annak bemutatására, hogy miként hat a mintában lezajló szerkezet (vagy feszültség állapot) változás, méréseket végeztünk Fe-Ni ötvözeteken (54-55 ábrák), ahol gyorshűtött, de egyébként kristályos mintákon T c meghatározásokat végeztünk oly módon, hogy a mintát a Curie-hőmérséklet fölé hevítve, hűtési módban is megmértük a Curie-hőmérsékletet. Tudjuk, hogy ezekben a mintákban átalakulás is lezajlik a T c -hez közeli hőmérséklettartományában, ezért az ábrákon látható jelenség, miszerint a T c a hőmérsékletváltozás irányától is függ, világosan bizonyítja, hogy amennyiben a háttérben fázisátalakulás is zajlik, a T c itt nem valós, hanem fázisviszonyokat is tükröző állapotot mutat. Ezzel a méréssorozattal arra akartunk példát mutatni, hogy milyen problémák merülnek fel a T c méréssel kapcsolatban, ha a mérés közben szerkezetváltozás is lezajlik. Bizonyos mértékben ez történik ugyanis a fémüvegek Curie-hőmérsékletének mérésekor is, noha itt csak szerkezeti relaxáció fordulhat elő mérés során. Abból adódóan tehát, hogy a mérés periódikus megismétlésének hatására milyen irányba mozdul el a T am c, a relaxációs folyamat tényére és mikroszkópos atomi mechanizmusára is következtethetünk. A fent említett tájékozódó mérések így segítséget nyújtottak a fémüvegek T am c relaxációja során lezajló atomi szintű elmozdulások értelmezéséhez. 13
14 Ezek után rátérek néhány, a bíráló által feltett kérdések tényleges tárgyalására. 58. ábra A Fe Ni egyensúlyi diagram és a Fe 40 Ni 40 Si 6 B 14 összetételű üvegfém üvegátalakulását sematikusan ábrázoló TTT diagram (A T g hőmérsékletet közel azonosnak tekinthetjük a T krist -tel) [168] Hőkezelések hatására, a T am c megváltozik, de hatással lehet rá magával a méréssel járó am hevítési folyamat is, tehát maga a mérési folyamat is változtathatja a T c értékét. A mérésnek, mint termikus beavatkozásnak a hatására tehát a T am c fölfelé is, vagy akár lefelé is elmozdulhat attól függően, hogy milyen hőmérsékleten hőkezelünk, vagy mérjük magát a T am c - et.. A változás iránya attól függ, hogy milyen hőmérsékletre hevítjük fel a mintát, és ezzel milyen irányban befolyásoljuk az üvegátalakulási hőmérsékleten befagyasztott klaszterszerkezetet. Más szóval: egy mérési folyamatban meghatározott T c értéke tükrözi az előző am teljes termikus előéletet. Magát a jelenséget már Egami is közölte [66], de atomi szintű szerkezetmagyarázatot nem fűzött a jelenséghez. Az általam publikált értelmezés éppen a már többször idézett és vitatott -centrumok (fázis-emlékezések) segítségével történik. Az érvelést nagymértékben elősegíti a disszertáció 58 ábrája,- amelyet fentebb, ismét bemutatok. A Fe-Ni egyensúlyi fázisdiagram lényeges átalakulásait láthatjuk itt, összekötve a Fe 40 Ni 40 Si 6 B 14 amorf ötvözet olvadáspontját, valamint az üvegátalakulási hőmérsékletét ábrázoló vízszintesekkel (az olvadási és a kristályosodási hőmérsékletek saját kísérleti adatataim). Látható, hogy az üvegátalakulási hőmérséklet (T g ) környezetében az egyensúlyi rendszer már kétfázisú (fcc és bcc). Feltehető tehát, hogy az olvadékban ez a kétféle szimmetriájú klaszter tendenciaszerűen megjelenik. Nagyobb hőmérsékleten inkább az fcc, kisebb hőmérsékleten inkább a bcc jellegű klaszterek túlsúlya a domináns, a fázisdiagram jellegéből következően. Ezt mutatja az alábbi reakcióséma: 14
15 növekvő hőmérséklet T( ) [Fe,Ni(B)]bcc [Fe,Ni(B)]fcc csökkenő hőmérséklet T( ) am A klaszter-arány bedermedése természetesen a T g -en történik, a T c pedig 350 o C körül van, ami lényegesen kisebb, mint a minta Curie-hőmérséklete. Amikor tehát a T am c -et mérjük, (különösen a hevítési folyamat első szakaszában) ebben a hőmérséklet tartományban nyilván a bcc jellegű környezetek jelentik a stabilabb konfigurációkat, ezért rövidtávú atomi szimmetria-váltásokkal az erősebb ferromágneses csatolású környezetek száma növekszik, vagyis a T am c növekedni fog (lásd a fenti reakció-sémát). Nagyobb hőmérsékleteken hőkezelve, (de még mindig a T g alatt!) az egyensúly egyre inkább az fcc-jellegű környezetek irányába tolódik el, így ezek határozzák meg a csatolás erősségét, így kisebb T am c -et mérünk. Jól mutatja ezt a tendenciát a disszertáció 63. ábrája is, ahol a minta Curie-hőmérsékletét fűtési és hűtési módban egyaránt meghatároztuk: látható hogy a mérések során (önmagában a méréssel járó hőkezelés hatására a T am c felfelé tolódik. Hasonló logikával érthető meg az a tény, hogy a gyorshűtési folyamatban alkalmazott hűtési sebesség változtatásával miért csökken a T c am a hűtési sebesség növekedésével? (56, 57. ábrák, valamint az irodalmi összefoglalóban szereplő 25. ábra) Az oldott hidrogén hatása endoterm és exoterm jellegű oldódási folyamatokban Kétféle módszerrel történt hidrogén bevitelről van szó a dolgozatban: elektrolitikus módszerrel és gáz fázisból történtek a H-oldási kísérletek. Ami a fémüvegekben az oldódási szabadentalpia változás előjelét illeti, azt a domináns módon az alapfém kémiai jellege határozza meg (dolgozatban 3. táblázat). Jól érthető ennek alapján, hogy miért különülnek el tendenciájukban egymástól a fémek, a H-oldódás hőmérsékletfüggését, ill. az oldott H mennyiségét illetően. Ezt mutatja a dolgozatban 34. ábra. A hőmérséklettel növekvő oldódás azt mutatja, hogy az oldódási hő vagy 0, vagy gyengén pozitív, és az oldódás tényével járó teljes szabadentalpia változás TS tagja, vagyis az entrópiaváltozás jelenti az oldódás hajtóerejét. Ezekben a fémekben ill. a belőlük készült (többnyire mágneses) ötvözetekben nincs, vagy nagyon csekély a matrix atomok és H-atomok között a kémiai kölcsönhatás, ezért az oldódási folyamatot követő hőmérséklet csökkenésével, az oldott H spontán módon eltávozik a fémes matrixból. A H atomok preferáltan foglalnak helyet a geometriailag kedvező környezetekben és tartózkodási idejük alatt feszültségnövelő hatást fejtenek ki, ami a feszültségre érzékeny mágneses jellemzőkben meg is nyilvánul (pl: koercitiv erő)(75, 76 ábrák). Minthogy a H diffúziósebessége szobahőmérséklet környezetében minimum 10 nagyságrenddel nagyobb, mint a matrix-atomok visszarendeződésének sebessége (öndiffúzió), a H teljes deszorpciója után (ami néhányszor 10 óra) a H által okozott feszültségállapotnövekedés egy része még mindig kimutatható a mágneses tulajdonságokban. Minthogy a feszültségállapot megváltozása csak a relaxálatlan fémüvegeken volt kimutatható, kézenfekvő a magyarázat, hogy jelentősen hozzájárulnak a H-atomok befogásához azok a feszültségcentrumok, amelyek egyébként is felelősek a koercitív erő növekedéséért az amorf állapotban. Ezek pedig a már többször tárgyalt -centrumok. Különösen tanulságosak azok a kísérletek, amelyek az abszorbeált H-atomok T c am -re gyakorolt hatásának kimutatására irányultak. Itt a kísérleti nehézséget a már említett mérési folyamattal járó relaxációs jelenségek és a H jelenlétéből következő hatások elkülönítése jelentette. Az erre vonatkozó eredmények a dolgozat ábráin kerültek ismertetésre. 15
16 Lényegesen különböznek az előzőektől azok a fémüveg-rendszerek, amelyekben legalább egy, jelentékeny stabilitású hidridet képző komponens is van. Ilyenek a vizsgált Ni-Zr-Cu üvegötvözetek is. Ezek vizsgálatára azért került sor, mert potenciális H-tárolók kifejlesztésére láttak bennük lehetőséget. Minthogy a komponensek és a H közötti affinitás igen eltérő, a ciklikus feltöltés és deszorpció során a H fokozatosan átrendezi a rövidtávú rendet (a 33 ábrából leolvasható trendnek megfelelően!). A ciklikus deszorpció-abszorpció során mikrofázisszeparáció alakul ki az ötvözetben még amorf állapotban, és ennek szerkezeti következményeit láthatjuk a 93. ábrán. Az ábrán (SAD felvételek) látható, hogy az eredetileg egyetlen az amorf szerkezetre tipikus diffúz diffrakciós gyűrű fokozatosan két diffrakciós gyűrűvé alakul át, jelezvén az amorf szerkezetben kialakult kémiai rendeződést (kémiai reakció indukált) mikro-fázisszeparációt. Összefoglalás Első pont: elnézést kérek, rossz fogalmazás Helyesen: átmenetifém ötvözőelemek hatásmechanizmusának értelmezésében A tézisekhez megadott közlemények felsorolása: Sajnos, igaza van, hogy a tézisekre vonatkozó irodalom csak a vastag betűs nyomtatásban különbözik a hivatkozásoktól, ill. azok az irodalmi hivatkozások között is szerepelnek esetenként. Így számbavételük nehézségeket okoz. Ennek ellenére: 154 = 12 (saját eredmények között hivatkozom) Tézispontok 1. tézispont anomális viselkedés nem definiált. Igaz ugyan, hogy elvben a téziseknek a disszertáció nélkül is érthetőnek kell lennie, azonban egyetlen bővített mondatban ez igen nehezen fogalmazható meg. Nem véletlen, hogy a tézispont mondanivalóját több alpontban fejtettem ki, amely kijelentések több, független módszerrel mért fizikai tulajdonság változására vonatkoznak. Ami az Egami- és Bethe Slater-összefüggésre vonatkozó hívatkozást illeti, a szerző nem állította hogy ezek saját eredményei, hanem a mágneses tulajdonságok általa meghatározott változását akként értelmezi, hogy ezek egyezésben vannak a két szerző állításaival, fenomenologiai megállapításaival. Tehát értelmezésről van szó: itt nem látom, hogy miért tulajdonítottam volna el a két szerző eredményeit. Ami a Bethe Slater-összefüggést illeti, itt a hívatkozás jellege még nyilvánvalóbb: az idézett közleménynek eredeti kijelentésében semmi köze sincs az amorf állapothoz (féművegekhez), amelyeket több évtizeddel később fedeztek fel, mint a hivatkozott összefüggést. Ami a c. pont kijelentését illeti, ismét hangsúlyozom, hogy több, párhuzamosan elkészített ötvözetrendszerről van szó a 47, 48 ábrákon. Bár az összetétel meghatározásnak is vannak hibái, a tendenciajellegű változások mind a kristályosodási entalpiában, mind a kristályosodási hőmérsékletben világosan kirajzolódnak. Ráadásul antikorrelált változásokról van szó a kristályosodási entalpiában és a kristályosodási hőmérsékletben, ami nem lehet véletlen. A tendenciajellegű antikorrelált kapcsolat létezését a két tulajdonság között Fe-B ötvözetekben, már a dolgozat 77 hivatkozásában is megállapították, így ez az eredmény alátámasztja a 47. és 48. ábra kijelentéseit. 16
17 A tézispont utolsó mondata egyébként rávilágít, hogy milyen értelemben beszél a szerző az anomális viselkedésről: Ennek alapján megállapítottam, hogy a tulajdonságok nem értelmezhetők az általánosan elfogadott homogén szerkezeti képben az átlagos elektronsűrűség (e/a) ötvözéssel történő változásának következményeként. Nem látom ezek után, hogy miért volnának pontatlanok a tézis kijelentése? 2. tézispont b. pont: A szerző válaszának korábbi részében már meggyőzően bizonyította kijelentését. Ennek tényszerűen indokolható oldékonysági okai vannak (47. ábra és a mellékelt Fe-Cu fázisdiagram) c. pont: Válaszom ugyanaz: a 47. ábra világosan mutatja a Cu adagolásának eredményét: ugyanaz a primer kristályosodási folyamat kristályos csíráinak (a.fe) aktiválási energiájának csökkentéséről van szó. 4/c tézispont Valóban nem teljesen pontos a fogalmazás: helyesen: Az irreverzibilis Curie-hőmérséklet növekedését a kvencseléskor befagyott fcc-jellegű klaszterek (fázis-emlékezések) fcc bcc irányú átalakulásával értelmeztem. 7/a tézispont Utolsó mondata: Köszönöm a figyelem felhívását! A hivatkozott saját publikáció valóban nem igazolja a kijelentést. A megfelelő szerkezetvizsgálati hivatkozások [47,48,49] 8. tézispont (A bíráló nem fogadta el) A tézis eredeti megfogalmazása: Hidrogén által keltett mikro-fázisszeparációt mutattam ki Ni-Zr és Ni-Cu-Zr fémüvegekben ciklikus telítési folyamatok után. VIII. a: A hidrogén oldódása nanométeres tartományokon koncentráció-fluktuációkat okoz az amorf közegben, egyes tartományokban a Cu-atomok feldúsulása mutatható ki, egyidejűleg a reverzibilisen oldódó hidrogén mennyisége csökken jeléül annak, hogy a hidrogén a kémiai rövidtávú rendet megváltoztatva spinodális jellegű bomlást eredményez az amorf mátrixban. VIII. b: A kémiai és topológiai rövidtávú környezetváltozás kvalitatív értelmezését adtam meg a Miedema által javasolt atomi cella modell alapján. Válasz: A szerző szerint a VIII tézispont a dolgozat legkoherensebb és talán legdokumentáltabb tézispontja. A megfelelő publikációk: J. Garaguly, A. Lovas, Á. Cziráki, M. Reybold, J. Takács, K. Wetzig Mater. Sci. Eng. A (1997) (195) J. Garaguly, A. Lovas, K. Tompa, J. Takács: Electrical resistance change during hydrogen charging and discharging in Ni67-xCuxZr33 glassy alloys Journal of Alloys and Compounds (1997) pp , Bemutatásra került az Int. Symp. on Metal-Hydrogen Systems; (Les Diablerets, Aug , 1996) konferencián 26 (198)- I. Nagy, I. Bakonyi, A. Lovas, E. Tóth-Kádár, K. Tompa, M. Hossó, Á. Cziráki, B. Fogarassy, J. of Less-Common Metals, 167 (1991) (tézispontokhoz nem rendelt publikáció) 17
18 201 I. Bakonyi, E. Tóth-Kádár, I. Nagy, J. Tóth, K. Tompa, A. Lovas, Zeitschrift für Phys. Chem Bd 183, s (1994) (tézispontokhoz nem rendelt, de tematikusan szorosan idetartozó publikáció) Az oldott H által keltett irreverzibilis elektromos ellenállás-változást több (biner és terner) amorf ötvözetben kimutattam. Ez kísérletileg teljesen egyértelmű és dokumentált állítás (lásd pl. disszertáció 92. ábrája, ahol látható módon az R/R o normált ellenállás nagyobb értékről indul, mint az első telítés során). A hidrogén által keltett ellenállás-növekedéshez az irodalomból egyértelmű, kísérletileg igazolt elektronszerkezeti változás rendelhető hozzá, amint ezt a 41.ábra igazolja. 41. ábra Hidrogénezetlen és hidrogénezett biner Ni-Zr amorf ötvözetek UPS spektrumai. Az egyes görbék azonos csúcsmagasságra vannak normálva [101] Az ellenállás-növekedés elektronszerkezeti oka az, hogy az oldott hidrogén az ötvözet hidridképző komponensének d-elektronjaival kötést létesít, emiatt ezek az elektronok (a Fermi-felület környezetében a d-elektronokról, mint a vezetésért felelős töltéshordozókról van szó) sűrűsége lecsökken. Ezzel egyidejűleg a nagyobb kötési energiájú elektronállapotok száma növekszik (sraffozott területek a 41. ábrán). Ebből egyértelmű, hogy a hidrogén atomok, oldódásuk során nem egyszerűen térkitöltő szerepet játszanak hanem ötvözőként viselkednek, kémiai kötést létesítenek. Az exoterm oldódási mechanizmusnak éppen az a termodinamikai jelentése, hogy a reakciópartnerek elektronrendszere egymással kölcsönhatásba kerül. A hidrogén által keltett rövidtávú atomi átrendeződést mutatja az is, hogy ismételt telítési kísérletek során, a telítési idő már a második ciklusban is lényegesen lerövidül, jeléül annak, hogy az általam térfogati aktiválás -nak nevezett folyamatban már megváltozott kémiai 18
19 környezeteken haladnak át az oldott H-atomok, vagyis a H-diffúzió elemi lépéseinek ideje lerövidül (a dolgozat 91. ábrája). A kémiai reakció ebben az esetben szelektív, vagyis az ötvözet komponensei közül csak a Zr-atomok reakciójáról beszélhetünk (ami következik a 90. ábra szelleméből). Analóg a jelenség, mint például a különböző fémek oxidjainak eltérő képződéshője (89. ábra [199]), vagyis reaktív gázok, reakciójuk során bizonyítottan a matrix-atomok térbeni átrendeződését okozzák. Az ismételt H-abszorpció-deszorpció eredményeként tehát az amorf matrix bizonyos esetekben újrarendeződik. Ennek következtében fordulhat az elő, hogy a fémüveg-matrixot jellemző diffúz gyűrű fokozatosan átalakul (a d-jelű mintán kettős diffúz gyűrűvé alakul át). 93. ábra. A telítési ciklusszám növekedésével előrehaladó klaszteresedési folyamat figyelhető meg amorf állapoton belül. A sötét színű klaszterekben a Cu komponens dúsul fel a SAD (Selected Area Electron Diffraction) vizsgálatok szerint a ciklikus telítési folyamat során Meg kell jegyeznem, hogy az ábra a 92. ábrán jelölt kezelések alapján válik érthetővé. 19
20 A következőkben a formai megjegyzéseire térek ki (melléklet) 1. A mellékletben összefoglalt nyomtatási és nyelvi észrevételeit köszönettel fogadom. Minden megjegyzése helytálló. Külön kitérek viszont az ábrák jelölésével kapcsolatos megjegyzéseire. Az irodalmi összefoglalóban idézett ábrák tekintélyes részét közvetlenül az irodalomból emeltem be a szövegbe. Az ábrák többnyire angol nyelvűek, ezeken az átjelölések rendkívül nagy munkát jelentett volna. Ilyen pl. a 6. ábra, amely ugyancsak irodalomból került átemelésre. Az X tengelyen valóban nincsenek rajta a mérőszámok. Köszönöm az észrevételt. Célja az üvegképző olvadékok két jellegzetes csoportjának elkülönítése. Az üvegátalakulási hőmérséklettel normált relatív hőmérsékleti skálán látható a kétféle olvadéktípus viszkozitásának hőmérsékletfüggése. Az Arrheniusz típusú T-függés, amely állandó aktiválási energiát tételez fel az olvadáspont és szobahőmérséklet között (E az 1. sz. egyenletben). E Aexp (1) kt (E - aktiválási energia, η - viszkozitás, A - állandó) Ezzel szemben, a 2. egyenletben, a T-től függő viszkozitást (η) a η o referenciaérték és a B konstans segítségével írják le, és a képletben szereplő T o nem más, mint az a referenciahőmérséklet. B 0 exp (2) ( T T0 ) 18. oldal: 12. ábra: X tengelye nem hőmérsékletet jelöl, hanem az olvadási hőmérséklethez kapcsolódó viszonyszámot (relatív hőmérsékletet). 22 oldal: 8 képlet: a és b dimenziónélküli paraméterek, amelyek olvadék/szilárd felület közötti hatásfelületi energiával függnek össze (köszönöm az észrevételt). 22. oldal: ábraszámozás hibás, köszönöm az észrevételt. 25. oldal: 14 képlet: B állandó 27. oldal: C f a gyorshűtéskor befagyott szabad térfogatra jellemző, atomi térfogat nagyságrendjébe eső u.n. folyási hiba, amely csak áttételes kapcsolatban van a makroszkóposan mérhető viszkozitással. 29 oldal: T a a hőkezelés hőmérséklete, T c helyesen: T c am az amorf Curie hőmérséklet, T c a gyakorlatilag végtelenül hosszú hőkezelési időhöz tartozó Curiehőmérséklet. 46. oldal 25. egyenlet: 20
Válasz Lovas Antal által benyújtott Akadémiai doktori értekezés bírálatára.
 Dr. Arató Péter (MTA doktor) Úrnak Válasz Lovas Antal által benyújtott Akadémiai doktori értekezés bírálatára. Tisztelt Bíráló! Megköszönöm a dolgozatom értékelésében nyújtott kritikai véleményét. Mindenekelőtt
Dr. Arató Péter (MTA doktor) Úrnak Válasz Lovas Antal által benyújtott Akadémiai doktori értekezés bírálatára. Tisztelt Bíráló! Megköszönöm a dolgozatom értékelésében nyújtott kritikai véleményét. Mindenekelőtt
dc_619_12 Klaszterjelenségek átmenetifém alapú, nem egyensúlyi ötvözetek tulajdonságaiban és átalakulásaiban Tézisfüzet Akadémiai doktori értekezés
 Klaszterjelenségek átmenetifém alapú, nem egyensúlyi ötvözetek tulajdonságaiban és átalakulásaiban Akadémiai doktori értekezés Tézisfüzet Készítette: Dr. Lovas Antal műszaki tudomány kandidátusa Budapest
Klaszterjelenségek átmenetifém alapú, nem egyensúlyi ötvözetek tulajdonságaiban és átalakulásaiban Akadémiai doktori értekezés Tézisfüzet Készítette: Dr. Lovas Antal műszaki tudomány kandidátusa Budapest
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások.
 Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
Kétalkotós ötvözetek. Vasalapú ötvözetek. Egyensúlyi átalakulások. dr. Fábián Enikő Réka fabianr@eik.bme.hu BMEGEMTAGM3-HŐKEZELÉS 2016/2017 Kétalkotós ötvözetrendszerekkel kapcsolatos alapfogalmak Az alkotók
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ
 TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
TANULÁSTÁMOGATÓ KÉRDÉSEK AZ 2.KOLLOKVIUMHOZ Vas-karbon diagram: A vas olvadáspontja: a) 1563 C. b) 1536 C. c) 1389 C. Mennyi a vas A1-el jelölt hőmérséklete? b) 1538 C. Mennyi a vas A2-el jelölt hőmérséklete?
Makroszkópos tulajdonságok, jelenségek, közvetlenül mérhető mennyiségek leírásával foglalkozik (például: P, V, T, összetétel).
 Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
Mire kell? A mindennapi gyakorlatban előforduló jelenségek (például fázisátalakulások, olvadás, dermedés, párolgás) értelmezéséhez, kvantitatív leírásához. Szerkezeti anyagok tulajdonságainak változása
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV.
 TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI IV. TÖBBFÁZISÚ, TÖBBKOMPONENS RENDSZEREK Kétkomponens szilárd-folyadék egyensúlyok Néhány fogalom: - olvadék - ötvözetek - amorf anyagok Állapotok feltüntetése:
KLASZTERJELENSÉGEK ÁTMENETIFÉM ALAPÚ, NEM EGYENSÚLYI ÖTVÖZETEK TULAJDONSÁGAIBAN ÉS ÁTALAKULÁSAIBAN. Akadémiai doktori értekezés.
 KLASZTERJELENSÉGEK ÁTMENETIFÉM ALAPÚ, NEM EGYENSÚLYI ÖTVÖZETEK TULAJDONSÁGAIBAN ÉS ÁTALAKULÁSAIBAN Akadémiai doktori értekezés Lovas Antal BME Közlekedésmérnöki és Járműmérnöki Kar Járműgyártás és-javítás
KLASZTERJELENSÉGEK ÁTMENETIFÉM ALAPÚ, NEM EGYENSÚLYI ÖTVÖZETEK TULAJDONSÁGAIBAN ÉS ÁTALAKULÁSAIBAN Akadémiai doktori értekezés Lovas Antal BME Közlekedésmérnöki és Járműmérnöki Kar Járműgyártás és-javítás
Al-Mg-Si háromalkotós egyensúlyi fázisdiagram közelítő számítása
 l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
l--si háromalkotós egyensúlyi fázisdiagram közelítő számítása evezetés Farkas János 1, Dr. Roósz ndrás 1 doktorandusz, tanszékvezető egyetemi tanár Miskolci Egyetem nyag- és Kohómérnöki Kar Fémtani Tanszék
2010. január 31-én zárult OTKA pályázat zárójelentése: K62441 Dr. Mihály György
 Hidrosztatikus nyomással kiváltott elektronszerkezeti változások szilárd testekben A kutatás célkitűzései: A szilárd testek elektromos és mágneses tulajdonságait az alkotó atomok elektronhullámfüggvényeinek
Hidrosztatikus nyomással kiváltott elektronszerkezeti változások szilárd testekben A kutatás célkitűzései: A szilárd testek elektromos és mágneses tulajdonságait az alkotó atomok elektronhullámfüggvényeinek
Anyagtudomány. Ötvözetek egyensúlyi diagramjai (állapotábrák)
 Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Anyagtudomány Ötvözetek egyensúlyi diagramjai (állapotábrák) Kétkomponensű fémtani rendszerek fázisai és szövetelemei Folyékony, olvadék fázis Színfém (A, B) Szilárd oldat (α, β) (szubsztitúciós, interstíciós)
Szilárdság (folyáshatár) növelési eljárások
 Képlékeny alakítás Szilárdság (folyáshatár) növelési eljárások Szemcseméret csökkentés Hőkezelés Ötvözés allotróp átalakulással rendelkező ötvözetek kiválásos nemesítés diszperziós keményítés interstíciós
Képlékeny alakítás Szilárdság (folyáshatár) növelési eljárások Szemcseméret csökkentés Hőkezelés Ötvözés allotróp átalakulással rendelkező ötvözetek kiválásos nemesítés diszperziós keményítés interstíciós
Vas- karbon ötvözetrendszer
 Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
Vas- karbon ötvözetrendszer Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos, és szaggatott vonallal is fel vannak
5 előadás. Anyagismeret
 5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
5 előadás Anyagismeret Ötvözet Legalább látszatra egynemű fémes anyag, amit két vagy több alkotó különböző módszerekkel való egyesítése után állítunk elő. Alapötvöző minden esetben fémes anyag. Ötvöző
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR ANYAGTUDOMÁNYI INTÉZET Miskolc, 2008. 1. TANTÁRGYLEÍRÁS Anyagszerkezettan II. kommunikációs
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR ANYAGTUDOMÁNYI INTÉZET Miskolc, 2008. 1. TANTÁRGYLEÍRÁS Anyagszerkezettan II. kommunikációs
Fázisátalakulások, avagy az anyag ezer arca. Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium
 Fázisátalakulások, avagy az anyag ezer arca Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium Atomoktól a csillagokig, Budapest, 2016. december 8. Fázisátalakulások Csak kondenzált anyag? A kondenzált
Fázisátalakulások, avagy az anyag ezer arca Sasvári László ELTE Fizikai Intézet ELTE Bolyai Kollégium Atomoktól a csillagokig, Budapest, 2016. december 8. Fázisátalakulások Csak kondenzált anyag? A kondenzált
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram)
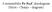 A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
A metastabilis Fe-Fe 3 C ikerdiagram (Heyn - Charpy - diagram) A vas-karbon egyensúlyi diagram alapvető fontosságú a vasötvözetek tárgyalásánál. Az Fe-C ötvözetekre vonatkozó ismereteket általában kettős
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Acélok nem egyensúlyi átalakulásai
 Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Acélok nem egyensúlyi átalakulásai Acélok egyensúlyitól eltérő átalakulásai Az ausztenit átalakulásai lassú hűtés Perlit diffúziós átalakulás α+fe 3 C rétegek szilárdság közepes martensit bainit finom
Szilárdságnövelés. Az előadás során megismerjük. Szilárdságnövelési eljárások
 Anyagszerkezettan és anyagvizsgálat 2015/16 Szilárdságnövelés Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti alapjait; Technológiai
Anyagszerkezettan és anyagvizsgálat 2015/16 Szilárdságnövelés Dr. Szabó Péter János szpj@eik.bme.hu Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti alapjait; Technológiai
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK. Anyagismeret 2016/17. Szilárdságnövelés. Dr. Mészáros István Az előadás során megismerjük
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2016/17 Szilárdságnövelés Dr. Mészáros István meszaros@eik.bme.hu 1 Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2016/17 Szilárdságnövelés Dr. Mészáros István meszaros@eik.bme.hu 1 Az előadás során megismerjük A szilárságnövelő eljárásokat; Az eljárások anyagszerkezeti
Fogorvosi anyagtan fizikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek
 Fémek törékeny/képlékeny nemesémek magas/alacsony o.p. Fogorvosi anyagtan izikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek ρ < 5 g cm 3 könnyűémek 5 g cm3 < ρ nehézémek 2 Fémek tulajdonságai
Fémek törékeny/képlékeny nemesémek magas/alacsony o.p. Fogorvosi anyagtan izikai alapjai 5. Általános anyagszerkezeti ismeretek Fémek, ötvözetek ρ < 5 g cm 3 könnyűémek 5 g cm3 < ρ nehézémek 2 Fémek tulajdonságai
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Spontaneitás, entrópia
 Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Spontaneitás, entrópia 6-1 Spontán folyamat 6-2 Entrópia 6-3 Az entrópia kiszámítása 6-4 Spontán folyamat: a termodinamika második főtétele 6-5 Standard szabadentalpia változás, ΔG 6-6 Szabadentalpia változás
Bevezetés a lézeres anyagmegmunkálásba
 Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
Bevezetés a lézeres anyagmegmunkálásba FBN332E-1 Dr. Geretovszky Zsolt 2010. október 6. Anyagcsaládok Fémek Kerámiák, üvegek Műanyagok Kompozitok A családok közti különbségek tárgyalhatóak: atomi szinten
Fémek és ötvözetek termikus viselkedése
 Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
Anyagtudomány és Technológia Tanszék Fémek és ötvözetek termikus viselkedése Dr. Szabó Péter János szpj@eik.bme.hu Anyagszerkezettan és anyagvizsgálat BMEGEMTBGA1 2018/2019/2 Az előadás során megismerjük
Polimerek fizikai, mechanikai, termikus tulajdonságai
 SZÉCHENYI ISTVÁN EGYETEM ANYAGISMERETI ÉS JÁRMŰGYÁRTÁSI TANSZÉK POLIMERTECHNIKA NGB_AJ050_1 Polimerek fizikai, mechanikai, termikus tulajdonságai DR Hargitai Hajnalka 2011.10.05. BURGERS FÉLE NÉGYPARAMÉTERES
SZÉCHENYI ISTVÁN EGYETEM ANYAGISMERETI ÉS JÁRMŰGYÁRTÁSI TANSZÉK POLIMERTECHNIKA NGB_AJ050_1 Polimerek fizikai, mechanikai, termikus tulajdonságai DR Hargitai Hajnalka 2011.10.05. BURGERS FÉLE NÉGYPARAMÉTERES
Fázisátalakulás Fázisátalakulások diffúziós (egyedi atomi mozgás) martenzites (kollektív atomi mozgás, diffúzió nélkül)
 ázisátalakulások, P, C változása új (egyensúlyi) állapot Új fázis(ok): stabil, metastabil ázisátalakulás: folyamat, amelynek során a régi fázis(ok)ból új, más szerkezetű (rács, szövet) vagy halmazállapotú
ázisátalakulások, P, C változása új (egyensúlyi) állapot Új fázis(ok): stabil, metastabil ázisátalakulás: folyamat, amelynek során a régi fázis(ok)ból új, más szerkezetű (rács, szövet) vagy halmazállapotú
Szilárdtestek mágnessége. Mágnesesen rendezett szilárdtestek
 Szilárdtestek mágnessége Mágnesesen rendezett szilárdtestek 2 Mágneses anyagok Permanens atomi mágneses momentumok: irány A kétféle spin-beállású elektronok betöltöttsége különbözik (spin-polarizáció)
Szilárdtestek mágnessége Mágnesesen rendezett szilárdtestek 2 Mágneses anyagok Permanens atomi mágneses momentumok: irány A kétféle spin-beállású elektronok betöltöttsége különbözik (spin-polarizáció)
N I. 02 B. Mágneses anyagvizsgálat G ép. 118 2011.11.30. A mérés dátuma: A mérés eszközei: A mérés menetének leírása:
 N I. 02 B A mérés eszközei: Számítógép Gerjesztésszabályzó toroid transzformátor Minták Mágneses anyagvizsgálat G ép. 118 A mérés menetének leírása: Beindítottuk a számtógépet, Behelyeztük a mintát a ferrotestbe.
N I. 02 B A mérés eszközei: Számítógép Gerjesztésszabályzó toroid transzformátor Minták Mágneses anyagvizsgálat G ép. 118 A mérés menetének leírása: Beindítottuk a számtógépet, Behelyeztük a mintát a ferrotestbe.
Kémiai reakciók mechanizmusa számítógépes szimulációval
 Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Kémiai reakciók mechanizmusa számítógépes szimulációval Stirling András stirling@chemres.hu Elméleti Kémiai Osztály Budapest Stirling A. (MTA Kémiai Kutatóközpont) Reakciómechanizmus szimulációból 2007.
Vas- karbon ötvözetrendszer. Összeállította: Csizmazia Ferencné dr.
 Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Vas- karbon ötvözetrendszer Összeállította: Csizmazia Ferencné dr. 1 Vas- Karbon diagram 2 Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
 Anyagos rész: Lásd: állapotábrás pdf. Ha többet akarsz tudni a metallográfiai vizsgálatok csodáiról, akkor: http://testorg.eu/editor_up/up/egyeb/2012_01/16/132671554730168934/metallografia.pdf
Anyagos rész: Lásd: állapotábrás pdf. Ha többet akarsz tudni a metallográfiai vizsgálatok csodáiról, akkor: http://testorg.eu/editor_up/up/egyeb/2012_01/16/132671554730168934/metallografia.pdf
HŐKEZELÉS FÉMTANI ALAPJAI
 HŐKEZELÉS FÉMTANI ALAPJAI ANYAGMÉRNÖK MESTERKÉPZÉS HŐKEZELŐ SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET
HŐKEZELÉS FÉMTANI ALAPJAI ANYAGMÉRNÖK MESTERKÉPZÉS HŐKEZELŐ SZAKIRÁNY TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás
 3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás 2018.02.05. A gyakorlat célja Ismerkedés a Fizikai Kémia II. laboratóriumi gyakorlatok légkörével A jegyzőkönyv
3. Az Sn-Pb ötvözetek termikus analízise, fázisdiagram megszerkesztése. Előkészítő előadás 2018.02.05. A gyakorlat célja Ismerkedés a Fizikai Kémia II. laboratóriumi gyakorlatok légkörével A jegyzőkönyv
Mikrohullámú abszorbensek vizsgálata 4. félév
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata 4. félév Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata 4. félév Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Katalízis. Tungler Antal Emeritus professzor 2017
 Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Katalízis Tungler Antal Emeritus professzor 2017 Fontosabb időpontok: sósav oxidáció, Deacon process 1860 kéndioxid oxidáció 1875 ammónia oxidáció 1902 ammónia szintézis 1905-1912 metanol szintézis 1923
Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása
 Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Oktatási Hivatal I. FELADATSOR Országos Középiskolai Tanulmányi Verseny 2009/2010. Kémia I. kategória II. forduló A feladatok megoldása 1. B 6. E 11. A 16. E 2. A 7. D 12. A 17. C 3. B 8. A 13. A 18. C
Anyagismeret. 3. A vas- karbon ötvözet
 Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Anyagismeret 3. A vas- karbon ötvözet A fémek és ötvözetek szerkezete Vas- Karbon diagram Eltérések az eddig tárgyalt diagramokhoz képest a diagramot csak 6,67 C %-ig ábrázolják, bizonyos vonalak folyamatos,
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján
 Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján Készítette: Zsélyné Ujvári Mária, Szalma József; 2012 Előadó: Zsély István Gyula, Javított valtozat 2016 Laborelőkészítő előadás,
Ón-ólom rendszer fázisdiagramjának megszerkesztése lehűlési görbék alapján Készítette: Zsélyné Ujvári Mária, Szalma József; 2012 Előadó: Zsély István Gyula, Javított valtozat 2016 Laborelőkészítő előadás,
Diffúzió. Diffúzió sebessége: gáz > folyadék > szilárd (kötőerő)
 Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Diffúzió Diffúzió - traszportfolyamat (fonon, elektron, atom, ion, hőmennyiség...) Elektromos vezetés (Ohm) töltés áram elektr. potenciál grad. Hővezetés (Fourier) energia áram hőmérséklet különbség Kémiai
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Modern Fizika Labor. 2. Elemi töltés meghatározása
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2011.09.27. A mérés száma és címe: 2. Elemi töltés meghatározása Értékelés: A beadás dátuma: 2011.10.11. A mérést végezte: Kalas György Benjámin Németh Gergely
Modern Fizika Labor Fizika BSC A mérés dátuma: 2011.09.27. A mérés száma és címe: 2. Elemi töltés meghatározása Értékelés: A beadás dátuma: 2011.10.11. A mérést végezte: Kalas György Benjámin Németh Gergely
Diffúzió. Diffúzió. Diffúzió. Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
 Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Anyagszerkezettan és anyagvizsgálat 5/6 Diffúzió Dr. Szabó Péter János szpj@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd
Jövônk anyagai, technológiái
 Jövônk anyagai, technológiái Rovatvezetôk: dr. Buzáné dr. Dénes Margit, dr. Klug Ottó GULYÁS CSABA LOVAS ANTAL BUZA GÁBOR Fe Ni-alapú ötvözetek néhány új alkalmazása Írásunkban Fe Ni-alapú amorf ötvözetek
Jövônk anyagai, technológiái Rovatvezetôk: dr. Buzáné dr. Dénes Margit, dr. Klug Ottó GULYÁS CSABA LOVAS ANTAL BUZA GÁBOR Fe Ni-alapú ötvözetek néhány új alkalmazása Írásunkban Fe Ni-alapú amorf ötvözetek
Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához
 Dr. Pósa Mihály Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához 1. Bevezetés Shillady Don professzor az Amerikai Kémiai Szövetség egyik tanácskozásán felhívta a figyelmet a
Dr. Pósa Mihály Megjegyzések (észrevételek) a szabad energia és a szabad entalpia fogalmához 1. Bevezetés Shillady Don professzor az Amerikai Kémiai Szövetség egyik tanácskozásán felhívta a figyelmet a
ANYAGSZERKEZETTAN II.
 ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc, 2013. 1. TANTÁRGYLEÍRÁS
ANYAGSZERKEZETTAN II. ANYAGMÉRNÖK ALAPKÉPZÉS TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR FÉMTANI, KÉPLÉKENYALAKÍTÁSI ÉS NANOTECHNOLÓGIAI INTÉZET Miskolc, 2013. 1. TANTÁRGYLEÍRÁS
ÖNTÖTT ÖTVÖZETEK FÉMTANA
 ÖNTÖTT ÖTVÖZETEK FÉMTANA ANYAGMÉRNÖK BSC KÉPZÉS JÁRMŰIPARI ÖNTÉSZETI SZAKIRÁNY (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR JÁRMŰIPARI ÖNTÉSZETI INTÉZETI
ÖNTÖTT ÖTVÖZETEK FÉMTANA ANYAGMÉRNÖK BSC KÉPZÉS JÁRMŰIPARI ÖNTÉSZETI SZAKIRÁNY (nappali munkarendben) TANTÁRGYI KOMMUNIKÁCIÓS DOSSZIÉ MISKOLCI EGYETEM MŰSZAKI ANYAGTUDOMÁNYI KAR JÁRMŰIPARI ÖNTÉSZETI INTÉZETI
Mérnöki anyagok Járműszerkezeti anyagok. Vas-karbon ötvözetrendszer Egyensúlyi átalakulások
 SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Mérnöki anyagok Járműszerkezeti anyagok Vas-karbon ötvözetrendszer Egyensúlyi átalakulások Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
SZÉCHENYI ISTVÁN EGYETEM Anyagtudományi és Technológiai Tanszék Mérnöki anyagok Járműszerkezeti anyagok Vas-karbon ötvözetrendszer Egyensúlyi átalakulások Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Egyensúlyitól eltérő átalakulások
 Egyensúlyitól eltérő átalakulások Egyensúlyitól eltérő átalakulások Az előzőekben láttuk, hogy az egyensúlyi diagramok alapján meg lehet határozni a kristályosodás, a fázis átalakulások stb. hőmérsékleteit.
Egyensúlyitól eltérő átalakulások Egyensúlyitól eltérő átalakulások Az előzőekben láttuk, hogy az egyensúlyi diagramok alapján meg lehet határozni a kristályosodás, a fázis átalakulások stb. hőmérsékleteit.
Határfelületi jelenségek. Fogorvosi anyagtan fizikai alapjai 3. Általános anyagszerkezeti ismeretek. N m J 2
 Határelületi jelenségek 1. Felületi eszültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagszerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eszültség adhézió nedvesítés ázis ázisdiagramm
Határelületi jelenségek 1. Felületi eszültség Fogorvosi anyagtan izikai alapjai 3. Általános anyagszerkezeti ismeretek Határelületi jelenségek Kiemelt témák: elületi eszültség adhézió nedvesítés ázis ázisdiagramm
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 8. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 8. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Anyagismeret 2016/17. Diffúzió. Dr. Mészáros István Diffúzió
 Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
Anyagismeret 6/7 Diffúzió Dr. Mészáros István meszaros@eik.bme.hu Diffúzió Különféle anyagi részecskék anyagon belüli helyváltoztatása Az anyag lehet gáznemű, folyékony vagy szilárd Diffúzió Diffúzió -
FOK Fogorvosi anyagtan fizikai alapjai tárgy kolokviumi kérdései 2012/13-es tanév I. félév
 FOK Fogorvosi anyagtan fizikai alapjai tárgy kolokviumi kérdései 2012/13-es tanév I. félév A kollokviumon egy-egy tételt kell húzni az 1-10. és a 11-20. kérdések közül. 1. Atomi kölcsönhatások, kötéstípusok.
FOK Fogorvosi anyagtan fizikai alapjai tárgy kolokviumi kérdései 2012/13-es tanév I. félév A kollokviumon egy-egy tételt kell húzni az 1-10. és a 11-20. kérdések közül. 1. Atomi kölcsönhatások, kötéstípusok.
Nagynyomású csavarással tömörített réz - szén nanocső kompozit mikroszerkezete és termikus stabilitása
 Nagynyomású csavarással tömörített réz - szén nanocső kompozit mikroszerkezete és termikus stabilitása P. Jenei a, E.Y. Yoon b, J. Gubicza a, H.S. Kim b, J.L. Lábár a,c, T. Ungár a a Anyagfizikai Tanszék,
Nagynyomású csavarással tömörített réz - szén nanocső kompozit mikroszerkezete és termikus stabilitása P. Jenei a, E.Y. Yoon b, J. Gubicza a, H.S. Kim b, J.L. Lábár a,c, T. Ungár a a Anyagfizikai Tanszék,
A II. kategória Fizika OKTV mérési feladatainak megoldása
 Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Kinetika. Általános Kémia, kinetika Dia: 1 /53
 Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Kinetika 15-1 A reakciók sebessége 15-2 Reakciósebesség mérése 15-3 A koncentráció hatása: a sebességtörvény 15-4 Nulladrendű reakció 15-5 Elsőrendű reakció 15-6 Másodrendű reakció 15-7 A reakció kinetika
Fázisátalakulások vizsgálata
 KLASSZIKUS FIZIKA LABORATÓRIUM 6. MÉRÉS Fázisátalakulások vizsgálata Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. szeptember 28. Szerda délelőtti csoport 1. A mérés célja A mérés
KLASSZIKUS FIZIKA LABORATÓRIUM 6. MÉRÉS Fázisátalakulások vizsgálata Mérést végezte: Enyingi Vera Atala ENVSAAT.ELTE Mérés időpontja: 2011. szeptember 28. Szerda délelőtti csoport 1. A mérés célja A mérés
MAGYAR TUDOMÁNYOS AKADÉMIA SZILÁRDTESTFIZIKAI ÉS OPTIKAI KUTATÓINTÉZET (MTA SZFKI)
 MTA SZFKI Fémkutatási Osztály (1972: Fémfizikai O.) Tudományos osztályvezető (1995 óta): BAKONYI Imre (MTA Doktora) Fő tevékenység: szilárdtestfizikai és anyagtudományi kísérleti alapkutatás fémek, fémhidridek,
MTA SZFKI Fémkutatási Osztály (1972: Fémfizikai O.) Tudományos osztályvezető (1995 óta): BAKONYI Imre (MTA Doktora) Fő tevékenység: szilárdtestfizikai és anyagtudományi kísérleti alapkutatás fémek, fémhidridek,
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Modern Fizika Labor. 11. Spektroszkópia. Fizika BSc. A mérés dátuma: dec. 16. A mérés száma és címe: Értékelés: A beadás dátuma: dec. 21.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. dec. 16. A mérés száma és címe: 11. Spektroszkópia Értékelés: A beadás dátuma: 2011. dec. 21. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
ACÉLOK MÉRNÖKI ANYAGOK
 ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
ACÉLOK MÉRNÖKI ANYAGOK 80%-a (5000 kg/fő/év) kerámia, kő, homok... Ebből csak kb. 7% a iparilag előállított cserép, cement, tégla, porcelán... 14%-a (870 kg/fő/év) a polimerek csoportja, melynek kb. 90%-a
Készítette: NÁDOR JUDIT. Témavezető: Dr. HOMONNAY ZOLTÁN. ELTE TTK, Analitikai Kémia Tanszék 2010
 Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
Készítette: NÁDOR JUDIT Témavezető: Dr. HOMONNAY ZOLTÁN ELTE TTK, Analitikai Kémia Tanszék 2010 Bevezetés, célkitűzés Mössbauer-spektroszkópia Kísérleti előzmények Mérések és eredmények Összefoglalás EDTA
TARTALOMJEGYZÉK. Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola. Készítette: Bán Krisztián okleveles gépészmérnök
 TARTALOMJEGYZÉK BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola Doktori tézisfüzet A SZERKEZETI RELAXÁCIÓ ÉS A HIDROGÉNABSZORPCIÓ
TARTALOMJEGYZÉK BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola Doktori tézisfüzet A SZERKEZETI RELAXÁCIÓ ÉS A HIDROGÉNABSZORPCIÓ
A nagytermi gyakorlat fő pontjai
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2008/09 Fe-C állapotábra Dr. Reé András ree@eik.bme.hu Fe-C 1 A nagytermi gyakorlat fő pontjai A Fe-C állapotábra felépítése Stabil (grafit) rendszer Metastabil
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Anyagismeret 2008/09 Fe-C állapotábra Dr. Reé András ree@eik.bme.hu Fe-C 1 A nagytermi gyakorlat fő pontjai A Fe-C állapotábra felépítése Stabil (grafit) rendszer Metastabil
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR. Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola
 BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola A SZERKEZETI RELAXÁCIÓ ÉS A HIDROGÉNABSZORPCIÓ ÚJ JELENSÉGEI, VALAMINT
BUDAPESTI MŰSZAKI ÉS GAZDASÁGTUDOMÁNYI EGYETEM KÖZLEKEDÉSMÉRNÖKI KAR Kandó Kálmán Multidiszciplináris Műszaki Tudományok Doktori Iskola A SZERKEZETI RELAXÁCIÓ ÉS A HIDROGÉNABSZORPCIÓ ÚJ JELENSÉGEI, VALAMINT
Kémiai átalakulások. A kémiai reakciók körülményei. A rendszer energiaviszonyai
 Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Kémiai átalakulások 9. hét A kémiai reakció: kötések felbomlása, új kötések kialakulása - az atomok vegyértékelektronszerkezetében történik változás egyirányú (irreverzibilis) vagy megfordítható (reverzibilis)
Az alakítással bevitt energia hatása az ausztenit átalakulási hőmérsékletére
 Az alakítással bevitt energia hatása az ausztenit átalakulási hőmérsékletére Csepeli Zsolt Bereczki Péter Kardos Ibolya Verő Balázs Workshop Miskolc, 2013.09.06. Előadás vázlata Bevezetés Vizsgálat célja,
Az alakítással bevitt energia hatása az ausztenit átalakulási hőmérsékletére Csepeli Zsolt Bereczki Péter Kardos Ibolya Verő Balázs Workshop Miskolc, 2013.09.06. Előadás vázlata Bevezetés Vizsgálat célja,
Anyagszerkezet és vizsgálat. 4. Előadás: Vas-karbon ötvözetrendszer
 SZÉCHENYI ISTVÁN EGYETEM Anyagismereti és Járműgyártási Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 4. Előadás: Vas-karbon ötvözetrendszer 2010. 10. 11. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
SZÉCHENYI ISTVÁN EGYETEM Anyagismereti és Járműgyártási Tanszék Anyagszerkezet és vizsgálat NGB_AJ021_1 4. Előadás: Vas-karbon ötvözetrendszer 2010. 10. 11. Dr. Hargitai Hajnalka (Csizmazia Ferencné dr.
Hőkezelő technológia tervezése
 Miskolci Egyetem Gépészmérnöki Kar Gépgyártástechnológiai Tanszék Hőkezelő technológia tervezése Hőkezelés és hegesztés II. című tárgyból Név: Varga András Tankör: G-3BGT Neptun: CP1E98 Feladat: Tervezze
Miskolci Egyetem Gépészmérnöki Kar Gépgyártástechnológiai Tanszék Hőkezelő technológia tervezése Hőkezelés és hegesztés II. című tárgyból Név: Varga András Tankör: G-3BGT Neptun: CP1E98 Feladat: Tervezze
Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam
 A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
A feladatokat írta: Kódszám: Harkai Jánosné, Szeged... Lektorálta: Kovács Lászlóné, Szolnok 2019. május 11. Curie Kémia Emlékverseny 2018/2019. Országos Döntő 7. évfolyam A feladatok megoldásához csak
1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai
 3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
Reakciókinetika. Általános Kémia, kinetika Dia: 1 /53
 Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Reakciókinetika 9-1 A reakciók sebessége 9-2 A reakciósebesség mérése 9-3 A koncentráció hatása: a sebességtörvény 9-4 Nulladrendű reakció 9-5 Elsőrendű reakció 9-6 Másodrendű reakció 9-7 A reakciókinetika
Melléklet. 4. Telep fluidumok viselkedésének alapjai Olajtelepek
 Melléklet 4. Telep fluidumok viselkedésének alapjai 4.1. Olajtelepek A nyersolaj fizikai tulajdonságok és kémiai összetétel alapján igen széles tartományt fednek le, ezért célszerű őket csoportosítani,
Melléklet 4. Telep fluidumok viselkedésének alapjai 4.1. Olajtelepek A nyersolaj fizikai tulajdonságok és kémiai összetétel alapján igen széles tartományt fednek le, ezért célszerű őket csoportosítani,
Reális kristályok, rácshibák. Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC
 Reális kristályok, rácshibák Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC Valódi, reális kristályok Reális rács rendezetlenségeket, rácshibákat tartalmaz Az anyagok tulajdonságainak bizonyos csoportja
Reális kristályok, rácshibák Anyagtudomány gyakorlat 2006/2007 I.félév Gépész BSC Valódi, reális kristályok Reális rács rendezetlenségeket, rácshibákat tartalmaz Az anyagok tulajdonságainak bizonyos csoportja
A fémek egyensúlyi viselkedése. A fémek kristályos szerkezete
 A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
A fémek egyensúlyi viselkedése A fémek kristályos szerkezete Kristályos szerkezet A kristályos szerkezetben az atomok szabályos geometriai rendben helyezkednek el. Azt a legkisebb - több atomból álló -
Kisciklusú fárasztóvizsgálatok eredményei és energetikai értékelése
 Kisciklusú fárasztóvizsgálatok eredményei és energetikai értékelése Tóth László, Rózsahegyi Péter Bay Zoltán Alkalmazott Kutatási Közalapítvány Logisztikai és Gyártástechnikai Intézet Bevezetés A mérnöki
Kisciklusú fárasztóvizsgálatok eredményei és energetikai értékelése Tóth László, Rózsahegyi Péter Bay Zoltán Alkalmazott Kutatási Közalapítvány Logisztikai és Gyártástechnikai Intézet Bevezetés A mérnöki
Természetes vizek, keverékek mindig tartalmaznak oldott anyagokat! Írd le milyen természetes vizeket ismersz!
 Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Összefoglalás Víz Természetes víz. Melyik anyagcsoportba tartozik? Sorolj fel természetes vizeket. Mitől kemény, mitől lágy a víz? Milyen okokból kell a vizet tisztítani? Kémiailag tiszta víz a... Sorold
Atomerőművi anyagvizsgálatok 4. előadás: Fémtan
 Budapesti Műszaki- és Gazdaságtudományi Egyetem (BME) Nukleáris Technikai Intézet (NTI) Atomerőművi anyagvizsgálatok 4. előadás: Fémtan Tárgyfelelős: Dr. Aszódi Attila Előadó: Kiss Attila 2012-2013. ősz
Budapesti Műszaki- és Gazdaságtudományi Egyetem (BME) Nukleáris Technikai Intézet (NTI) Atomerőművi anyagvizsgálatok 4. előadás: Fémtan Tárgyfelelős: Dr. Aszódi Attila Előadó: Kiss Attila 2012-2013. ősz
PhD DISSZERTÁCIÓ TÉZISEI
 Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
Budapesti Muszaki és Gazdaságtudományi Egyetem Fizikai Kémia Tanszék MTA-BME Lágy Anyagok Laboratóriuma PhD DISSZERTÁCIÓ TÉZISEI Mágneses tér hatása kompozit gélek és elasztomerek rugalmasságára Készítette:
5. előadás 12-09-16 1
 5. előadás 12-09-16 1 H = U + PV; U=Q-PV H = U + (PV); P= áll H = U + P V; U=Q-P V; U=Q-P V H = Q U= Q V= áll P= áll H = G + T S Munkává nem alakítható Hátalakulás = G + T S 2 3 4 5 6 7 Szilárd halmazállapot
5. előadás 12-09-16 1 H = U + PV; U=Q-PV H = U + (PV); P= áll H = U + P V; U=Q-P V; U=Q-P V H = Q U= Q V= áll P= áll H = G + T S Munkává nem alakítható Hátalakulás = G + T S 2 3 4 5 6 7 Szilárd halmazállapot
Folyadékszcintillációs spektroszkópia jegyz könyv
 Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
Folyadékszcintillációs spektroszkópia jegyz könyv Zsigmond Anna Julia Fizika MSc I. Mérés vezet je: Horváth Ákos Mérés dátuma: 2010. október 21. Leadás dátuma: 2010. november 8. 1 1. Bevezetés A mérés
5. Laboratóriumi gyakorlat
 5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
5. Laboratóriumi gyakorlat HETEROGÉN KÉMIAI REAKCIÓ SEBESSÉGÉNEK VIZSGÁLATA A CO 2 -nak vízben történő oldódása és az azt követő egyensúlyra vezető kémiai reakció az alábbi reakcióegyenlettel írható le:
Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban
 Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban A folyósító szerek viselkedése a kerámia anyagokban Bevezetés A kerámia masszák folyósításkor fő cél az anyag
Szakértesítő 1 Interkerám szakmai füzetek A folyósító szerek viselkedése a kerámia anyagokban A folyósító szerek viselkedése a kerámia anyagokban Bevezetés A kerámia masszák folyósításkor fő cél az anyag
Halmazállapotok. Gáz, folyadék, szilárd
 Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
Halmazállapotok Gáz, folyadék, szilárd A levegővel telt üveghengerbe brómot csepegtetünk. A bróm illékony, azaz könnyen alakul gázhalmazállapotúvá. A hengerben a levegő részecskéi keverednek a bróm részecskéivel
Mikrohullámú abszorbensek vizsgálata
 Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
Óbudai Egyetem Anyagtudományok és Technológiák Doktori Iskola Mikrohullámú abszorbensek vizsgálata Balla Andrea Témavezetők: Dr. Klébert Szilvia, Dr. Károly Zoltán MTA Természettudományi Kutatóközpont
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája
 ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÁTEDZHETŐ ÁTMÉRŐJÉNEK MEGHATÁROZÁSA Dr. Palotás Béla / Dr. Németh Árpád palotasb@eik.bme.hu A gyakorlat előkészítő előadás fő témakörei Az
ANYAGTUDOMÁNY ÉS TECHNOLÓGIA TANSZÉK Fémek technológiája ACÉLOK ÁTEDZHETŐ ÁTMÉRŐJÉNEK MEGHATÁROZÁSA Dr. Palotás Béla / Dr. Németh Árpád palotasb@eik.bme.hu A gyakorlat előkészítő előadás fő témakörei Az
NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen
 NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen Készítette: Battistig Nóra Környezettudomány mesterszakos hallgató A DOLGOZAT
NEHÉZFÉMEK ELTÁVOLÍTÁSA IPARI SZENNYVIZEKBŐL Modell kísérletek Cr(VI) alkalmazásával növényi hulladékokból nyert aktív szénen Készítette: Battistig Nóra Környezettudomány mesterszakos hallgató A DOLGOZAT
TÖBBKOMPONENS RENDSZEREK FÁZISEGYENSÚLYAI II. Ismerjük fel, hogy többkomponens fázisegyensúlyokban a folyadék fázisnak kitüntetett szerepe van!
 TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
TÖKOMPONENS RENDSZEREK FÁZISEGYENSÚLYI II Ismerjük fel hogy többkomonens fázisegyensúlyokban a folyadék fázisnak kitüntetett szeree van! Eddig: egymásban korátlanul oldódó folyadékok folyadék-gz egyensúlyai
Fluidum-kőzet kölcsönhatás: megváltozik a kőzet és a fluidum összetétele és új egyensúlyi ásványparagenezis jön létre Székyné Fux V k álimetaszo
 Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Hidrotermális képződmények genetikai célú vizsgálata Bevezetés a fluidum-kőzet kölcsönhatás, és a hidrotermális ásványképződési környezet termodinamikai modellezésébe Dr Molnár Ferenc ELTE TTK Ásványtani
Modern fizika laboratórium
 Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Modern fizika laboratórium 11. Az I 2 molekula disszociációs energiája Készítette: Hagymási Imre A mérés dátuma: 2007. október 3. A beadás dátuma: 2007. október xx. 1. Bevezetés Ebben a mérésben egy kétatomos
Reakciókinetika és katalízis
 Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Reakciókinetika és katalízis k 4. előadás: 1/14 Különbségek a gázfázisú és az oldatreakciók között: 1 Reaktáns molekulák által betöltött térfogat az oldatreakciónál jóval nagyobb. Nincs akadálytalan mozgás.
Számítástudományi Tanszék Eszterházy Károly Főiskola.
 Networkshop 2005 k Geda,, GáborG Számítástudományi Tanszék Eszterházy Károly Főiskola gedag@aries.ektf.hu 1 k A mérés szempontjából a számítógép aktív: mintavételezés, kiértékelés passzív: szerepe megjelenítés
Networkshop 2005 k Geda,, GáborG Számítástudományi Tanszék Eszterházy Károly Főiskola gedag@aries.ektf.hu 1 k A mérés szempontjából a számítógép aktív: mintavételezés, kiértékelés passzív: szerepe megjelenítés
Jegyzőkönyv. Konduktometria. Ungvárainé Dr. Nagy Zsuzsanna
 Jegyzőkönyv CS_DU_e 2014.11.27. Konduktometria Ungvárainé Dr. Nagy Zsuzsanna Margócsy Ádám Mihálka Éva Zsuzsanna Róth Csaba Varga Bence I. A mérés elve A konduktometria az oldatok elektromos vezetésének
Jegyzőkönyv CS_DU_e 2014.11.27. Konduktometria Ungvárainé Dr. Nagy Zsuzsanna Margócsy Ádám Mihálka Éva Zsuzsanna Róth Csaba Varga Bence I. A mérés elve A konduktometria az oldatok elektromos vezetésének
Színfémek és ötvözetek egyensúlyi lehőlése
 Színfémek és ötvözetek egyensúlyi lehőlése 1 Színfém lehőlési görbéje (nincs allotróp átalakulás) F + Sz = K + 1. K = 1 1. Szakasz F=1 olvadék Sz =1 T változhat 2. Szakasz F=2 olvadék + szilárd Sz= 0 T
Színfémek és ötvözetek egyensúlyi lehőlése 1 Színfém lehőlési görbéje (nincs allotróp átalakulás) F + Sz = K + 1. K = 1 1. Szakasz F=1 olvadék Sz =1 T változhat 2. Szakasz F=2 olvadék + szilárd Sz= 0 T
Fázisátalakulások vizsgálata
 Klasszikus Fizika Laboratórium VI.mérés Fázisátalakulások vizsgálata Mérést végezte: Vanó Lilla VALTAAT.ELTE Mérés időpontja: 2012.10.18.. 1. Mérés leírása A mérés során egy adott minta viselkedését vizsgáljuk
Klasszikus Fizika Laboratórium VI.mérés Fázisátalakulások vizsgálata Mérést végezte: Vanó Lilla VALTAAT.ELTE Mérés időpontja: 2012.10.18.. 1. Mérés leírása A mérés során egy adott minta viselkedését vizsgáljuk
A TÖMEGSPEKTROMETRIA ALAPJAI
 A TÖMEGSPEKTROMETRIA ALAPJAI web.inc.bme.hu/csonka/csg/oktat/tomegsp.doc alapján tömeg-töltés arány szerinti szétválasztás a legérzékenyebb módszerek közé tartozik (Nagyon kis anyagmennyiség kimutatására
A TÖMEGSPEKTROMETRIA ALAPJAI web.inc.bme.hu/csonka/csg/oktat/tomegsp.doc alapján tömeg-töltés arány szerinti szétválasztás a legérzékenyebb módszerek közé tartozik (Nagyon kis anyagmennyiség kimutatására
