DOKTORI (Ph.D.) ÉRTEKEZÉS. Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során
|
|
|
- Fruzsina Orbánné
- 6 évvel ezelőtt
- Látták:
Átírás
1 DOKTORI (Ph.D.) ÉRTEKEZÉS Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során dr. Viola Árpád Onkológia c. program keretében Témavezető: Programvezető: Készült: Dr. med. habil. Julow Jenő Prof. Dr. Kopper László Szent János Kórház, Budai Egészségügyi Regionális Centrum Idegsebészeti Osztály Doktori Iskola Semmelweis Egyetem, Budapest 2006
2 Tartalomjegyzék Összefoglalás 5 Summary..6 Rövidítések jegyzéke 7 I. Bevezetés...8 II. Célkitűzések..10 III. Irodalmi háttér...11 III.1. A sztereotaxiás sebészet..11 III.2. Brachytherápia a szövetközi besugárzás fejlődésének történeti áttekintése.12 III.3. A sztereotaxiás sugársebészeti eljárások fejlődésének történeti áttekintése 13 III.3.1 A gamma-kés sugársebészet 13 III.3.2. A LINAC sugársebészet...14 IV. Módszer és betegek 16 IV.1. A sztereotaxiás szövetközi besugárzás során alkalmazott sugárforrás jellemzői 16 IV.2. A sztereotaxiás koordináta rendszer és CT-MRI-PET képfúzió.16 IV.3. A szövetközi besugárzás 17 IV.3.1. A sztereotaxiás Jód-125 szövetközi besugárzás tervezése...17 IV.3.2. A Jód-125 sugárforrások sztereotaxiás beültetése 17 IV.3.3. A CT-CT intraoperatív képfúzió..18 IV A Jód-125 sugárforrások sztereotaxiás beültetését követő intraoperatív verifikáció.18 IV A CT-CT intraoperatív képfúzióval verifikált esetek 18 IV.3.4. A Jód-125 sztereotaxiás brachyterápia és LINAC sztereotaxiás sugársebészeti eljárások dóziseloszlásainak és sugárbiológiai hatásosságának összehasonlítása 20 IV Esetismertetés 20 IV Közös céltérfogat a sztereotaxiás szövetközi besugárzás és LINAC sugársebészeti tervekhez...20 IV A Jód-125 brachyterápiás tervek...21 IV A LINAC sugársebészeti tervek 21 IV A referenciadózis renormalizálása.23 2
3 IV Dozimetriai megfontolások...23 IV Térfogati indexek...25 IV.4. A Jód-125 szövetközi besugárzással kezelt esetek bemutatása...26 IV.4.1. Gliomák 26 IV.4.2. Meningeomák...28 IV.4.3. Pineoblastomák.29 IV.4.4. Akuszticus neurinomák 29 V. Eredmények...31 V.1. A CT-CT intraoperatív képfúzió...31 V.1.1. A kis és nagy daganatok csoportja.35 V.1.2. A szabályos és szabálytalan alakú daganatok csoportja 35 V.2. A Jód-125 sztereotaxiás brachyterápia és LINAC sztereotaxiás sugársebészeti eljárás dóziseloszlásainak és sugárbiológiai hatásosságának összehasonlítása...36 V.2.1. A szabályos és szabálytalan alakú daganatok csoportja.36 V.2.2. Dozimetriai megfontolások 37 V.3. A Jód-125 szövetközi besugárzás klinikai eredményei 43 V.3.1. Gliomák.43 V.3.2. Meningeomák 44 V.3.3. Pinealoblastomák...46 V.3.4. Akusztikus neurinomák..48 VI. Megbeszélés...51 VI.1. A CT-CT intraoperatív fúzió...51 VI.2. A Jód-125 sztereotaxiás brachyterápia és LINAC sztereotaxiás sugársebészeti eljárások dóziseloszlásainak és sugárbiológiai hatásosságának összehasonlítása 53 VI.3. A szövetközi besugárzás nemzetközi és a saját eredmények összehasonlítása...57 VI.3.1. Gliomák 57 VI.3.2. Meningeomák 62 VI Meningeomák LINAC sztereotaxiás sugársebészete 62 VI Meningeomák gamma-kés sztereotaxiás sugársebészete 62 VI Meningeomák Jód-125 szövetközi besugárzása 62 3
4 VI.3.3. Pinealis parenchymális daganatok (PPD) pinealoblastomák 66 VI.3.4. Akusztikus neurinomák 72 VI.4. Következtetések és az eredmények alkalmazhatósága a gyakorlatban...74 VII. Köszönetnyilvánítás 75 VIII. Irodalomjegyzék 77 4
5 Összefoglalás Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során dr. Viola Árpád Témavezető: Dr. med. habil. Julow Jenő Budapest, Semmelweis Egyetem Doktori Iskola, Onkológia program 2006 Az agydaganatok state-of-the art ellátása magában foglalja a multimodális képalkotók (CT, MR, PET) alkalmazását a tumorok lokalizálására és a 3D besugárzástervező szoftverek alkalmazását a célpont és a céltérfogat optimalizálás, dóziseloszlás és a besugárzás konformalitás optimalizálására. A brachyterápiás műtét kivitelezése során a katétereknek a tervezettől való néhány milliméteres eltérése is már jelentős különbséget okoz a céltérfogat és ép szövet sugárterhelésében. Több, a sztereotaxiás sugársebészeti eljárások technikájának összehasonlításával foglalkozó tanulmány jelent meg, azonban ezek egyike sem veti össze a sztereotaxiás szövetközi besugárzás és más sugársebészeti eljárások dóziseloszlásainak előnyeit és hátrányait, valamint kései sugárbiológiai hatásukat. A brachytherápiás műtétek után közvetlenül elvégzett CT vizsgálat képeit fuzionáltam a műtétek tervezésekor felhasznált CT képekkel, valamint a tervekben a referencia dózis renormalizálása után összehasonlítottam a brachyterápiás és LINAC tervek céltérfogatra és ép szövetre vonatkozó dózis-térfogat hisztogram paramétereit és a két terápiás eljárás kései sugárbiológiai hatását. Megállapítottam, hogy a szövetközi besugárzás CT-CT fúziós ellenőrzése lehetővé teszi a katéter dislokációjának felderítését és korrigálását, így az eljárás pontosabbá és megbízhatóbbá válik. Ugyanakkor alacsony implantációs kockázat mellett nagyon jó konformalitást sikerül elérni. A lineáris quadratikus modell alapján végzett számításaim szerint a Jód-125 szövetközi besugárzás összehasonlítva a LINAC sztereotaxiás besugárzással kisebb dózissal terheli meg a céltérfogat közvetlen és közvetett szomszédságában elhelyezkedő ép szöveteket. 5
6 Summary Intraoperative image fusion and linear-quadratic model for Iodine-125 interstitial irradiation of brain tumors dr. Viola Árpád Supervisor: Dr. med. habil. Julow Jenő Budapest, Semmelweis University Ph.D. School, Oncology program, 2006 State-of-th-art treatment involves the use of multimodal imaging (CT, MRI, PET) for tumor localization and use of modern 3D radiation treatment planning programs to determine optimal access points and a dose distribution conforming to the tumour. While implanting seeds during a brachytherapy operation, a few millimeter variances from the planning of the operation may cause considerable changes in the radioactive outcome of the tumor volume and the normal tissue. As far as we know, there is no study available investigeting both, the accuracy of the stereotactic brachytherapy implantation in brain tumours and the dosimetric consequences of deviations from the planned implantation site. A number of comparisons between difrent stereotactic radiosurgery treatment techniques have been published, but none of them compared their radiobiological advantages, disadvantages and late radiobiological effect with I-125 interstitial brachytherapy treatment. After the renormalization of LINAC and brachytherapy referential doses, using the dose volume histograms and the linear-quadratic model the brachytherapy doses were compared to the brachytherapy equivalent LINAC radiosurgery doses with respect to late effect of irradiations on normal brain tissue. It was found, that the application of the intraoperativ image fusion and linear quadratic model allows us to increase the quality of stereotactic interstitial irradiation, to choose the optimal stereotactic treatment method and to decrease the radiological exposure of normal tissue surrounding the target volume. 6
7 Rövidítések jegyzéke BT brachyterápia CI - lefedési index CT komputertomográf DVH - dózis-térfogat hisztogram EI - külső térfogati index HI - relatív dózis homogenitási index LINAC - lineáris gyorsítóval LQ modell lineáris quadratikus modell MR - mágneses magrezonancia PET - pozitron emissziós tomográf PPD - pinealis parenchymális daganat PRD - pinealis régió daganat PTV céltérfogat V ref - referenciadózis által körbefogott térfogat 3D három dimenzió 7
8 I. Bevezetés A természetes radioaktivitás 1896-os felfedezését követően rövid időn belül, már a 20. század első éveiben elkezdték terápiás céllal alkalmazni a radioaktív izotópokat. A kezelés egyik módja a szövetközi besugárzás - brachyterápia, melynek során a sugárzó izotópok a sebészi beavatkozást követően kerülnek a besugárzandó szövetbe (daganatba). Ezzel a lokális kezelési módszerrel a sugárforrások közelében nagy dózisok szolgáltathatók ki, a távolabb lévő ép szövetek relatív alacsony dózisterhelése mellett. Ezt a sugárforrások körül kialakuló kedvező tulajdonságú dózisviszonyok teszik lehetővé, amelyek alapvető geometriai és fizikai törvényszerűségből következnek. A brachyterápiás források közvetlen közelében kialakuló nagy dózisok csak kis térfogatra korlátozódnak, melyek általában nem okoznak késői komplikációkat. A megfelelő brachyterápiás kezelés követelménye a céltérfogat lehető legnagyobb részének az előírt dózissal történő besugárzása, éspedig a körülötte lévő ép szövetek dózisterhelésének minimalizálása mellett (1). A brachyterápia alkalmazási területe az agy-, fej-nyak-, lágyrész-, emlő- és prosztatadaganatok sugárterápiás kezelése, amely lehet a külső sugárterápiát kiegészítő ún. boost besugárzás vagy egyedüli brachyterápia. Az agydaganatok brachyterápiája során a besugárzás mindkét fajtáját, az állandó (permanens) besugárzást, v. a Curieterápiát és az időleges besugárzást, v. a brachy-curie terápiát is alkalmazzuk. A Curieterápia során a radioizotóp beültetése végleges, a besugárzási dózisteljesítmény alacsony, és az izotóp a tumoron belül - a daganat nagysága, alakja, szövettani típusa és a beültetésre kerülő izotóp aktivitása függvényében - néhány nap, vagy hónap alatt adja le a terápiás dózist. A brachy-curieterápia alkalmazásakor rövid ideig nagy intenzitású besugárzás történik, időlegesen beültetett radionuklidokkal, néhány nap vagy hét alatt leadva a terápiás dózist. Az agytumorok brachyterápiás kezelését az anatómiai viszonyok nehezítik. A daganat hozzáférhetőségének útjában gyakran létfontosságú agyi központok vannak, vagy ép maga a daganat a létfontosságú agyállományban foglal helyet. Párhuzamosan a brachyterápiás eljárások tökéletesítésével ugyancsak a 20. század első felében kezdtek intenzíven foglalkozni a későbbiekben sztereotaxiának nevezett eljárással, amely lehetővé tette a háromdimenziós koponyaűri tájékozódást. A brachyterápia és a 8
9 sztereotaxiás idegsebészet vívmányainak fuzionálásával alakult ki a sztereotaxiás brachyterápia. A konvergáló, több irányból egymást a célpontban keresztező, keskeny sugárnyalábokat alkalmazó eljárás és a sztereotaxiás technika együttes alkalmazása lehetővé tette a gamma-késsel és lineáris gyorsítóval (LINAC) végzett sztereotaxiás sugársebészeti eljárások kidolgozását. A modern metszetképalkotó eljárások és a sztereotaxiás készülékek integrálása lehetővé tette a craniotomia elhagyásával a sugárforrások seed -ek céltérfogatba történő biztonságos elhelyezését (2-7). A seed -ek beültetésekor a brachyterápiás műtét kivitelezése során a tervezettől a csupán néhány milliméteres eltérés is jelentős különbséget okoz a céltérfogat és az ép szövet sugárterhelésében. Több, a sztereotaxiás sugársebészeti eljárások technikájának összehasonlításával foglalkozó tanulmány jelent már meg (8-13), azonban ezek egyike sem tárgyalja a sztereotaxiás szövetközi besugárzás és a sugársebészeti eljárások dóziseloszlásainak előnyeit és hátrányait, valamint kései sugárbiológiai hatásukat. Ezért választottam célul az agydaganatok Jód-125 sztereotaxiás szövetközi besugárzás pontosságának CT-CT fúziós kvantitatív kiértékelését és a brachyterápia valamint a LINAC sugársebészeti eljárás dóziseloszlásainak és kései sugárbiológiai hatássosságának összehasonlítását. 9
10 II. Célkitűzések 1. A számítógép vezérelt intraoperatív CT-CT képfúzió használhatóságának vizsgálata az agydaganatok Jód-125 sztereotaxiás szövetközi besugárzásánál. 2. A számítógép vezérelt intraoperatív CT-CT képfúzióval verifikált tervek és kivitelezések dózis-térfogat hisztogram paramétereinek összehasonlítása különös tekintettel a daganat méretére és alakjára. 3. A számítógép vezérelt intraoperatív CT-CT képfúzióval feltárt kivitelezési pontatlanságok okainak feltárására és kiküszöbölésére vonatkozó korrekció kidolgozása. 4. A Jód-125 sztereotaxiás szövetközi besugárzás és a LINAC sztereotaxiás besugárzás dózis-térfogat paramétereinek öszehasonlítását lehetővé tevő eljárás kidolgozása és annak alkalmazása saját klinikai eseteinken. 5. A Jód-125 sztereotaxiás szövetközi besugárzás és a LINAC sztereotaxiás besugárzás ép szövetekre kifejtett késői sugárbiológiai hatásának összehasonlítása. 6. A Jód-125 sztereotaxiás szövetközi besugárzásban részesített betegek túlélési adatainak és a nemzetközi irodalomból vett klinikai adatainak az összevetése. 10
11 Irodalmi háttér III.1. A sztereotaxiás sebészet A Science folyóiratban 1947-ben megjelent rövid tanulmány számolt be a philadelphiai Temple Medical School két kutatóorvosa Ernst A. Spiegel és Henry T. Wycis által emberen elvégzett sikeres sztereotaxiás sebészeti beavatkozásról (14). Sztereotaxiás célzókészülék segítségével alkoholt injektáltak a globus pallidumba és ansa lenticularisba. Így sikeresen megszüntették egy Huntington-chorea-s beteg fej- és végtagtremorját. Azonban hosszú út vezetett az első sikeres, emberen elvégzett sztereotaxiás sebészeti beavatkozás kivitelezéséig. René Descartes a 17. században dolgozta ki a háromdimenziós (3D) tér pontjainak matematikai helymeghatározását lokalizálását (15). Horsley és Clarke 1907-ben a karteziánus elv alapján megépített sztereotaxiás célzókészülék segítségével végezték első állatkísérleteiket (16). A majmok kisagyi magjaira kifejtett minimális roncsolás következményeit tanulmányozták. A legtöbb neurofiziológiai ismeretre sztereotaxiás célzókészülékkel végzett kísérletek alapján tett szert az orvostudomány. Az első, emberen tervezett beavatkozás céljából 1918-ban megépített sztereotaxiás célzókészülék Aubrey Mussen nevéhez fűződik. Azonban ezt a célzókészüléket sohasem alkalmazták humán beavatkozásra, 1940-ben újságpapírba csomagolva egy csűrben találtak rá (15, 17). Spiegel és Wycis által kifejlesztett sztereotaxiás célzókészülék lényegében a Horsley- Clarke-féle kísérleti célzókészülék módosított, továbbfejlesztett változata (16). Mint általában a 20. század mérföldkövet jelentő felfedezéseinek, a sztereotaxiás célzókészülék továbbfejlesztésének és az ezzel kapcsolatos elektrofiziológiai kísérleteknek is van magyar vonatkozása. Székely Imre, második világháborús emigráns Spiegel kísérleti laboratóriumát vezette és részt vett a sztereotaxiás műtétek tervezésében és kivitelezésében is (18). A koponyaűri tájékozódás könnyítésére az első sztereotaxiás célzókészülékeket pneumoencefalográffal egy ülésben alkalmazták. A pneumoencefalográfon kirajzolódó Monro-nyílás, commissurák és a tobozmirigy tájékozódási pontként szolgáltak a 11
12 célterületek bemérésekor, a beavatkozást pedig pneumoencefalotomiának keresztelték. A sztereotaxiás idegsebészet európai fellegvárában, Jean Talairach párizsi klinikáján az 1970-es években egy újabb magyar emigráns, Szikla Gábor dolgozta ki a sztereotaxiás sztereoszkópiás angiografiát (19, 20). A vénák és artériák sztereoszkópiás angiografiás vizualizálása lehetővé tette a gyrusok és sulcusok pontos bemérését, és így a sztereotaxiás koponyaűri tájékozódást is. Óriási lendületet adott a sztereotaxiás műtétek kivitelezésének az, hogy a Hounsfield által ban kifejlesztett komputertomográfhoz (CT) (21), a Lauterbur és Mansfield által az 1980-as években bevezetett mágneses magrezonanciás (MR) (22, 23) készülékhez és a Phelps által 1973-ban kifejlesztett pozitron emissziós tomográfhoz (PET) (24) közvetlenül vagy közvetve hozzá lehetett kapcsolni a sztereotaxiás célzókészüléket. Patrick J. Kelly 1979-ben fiduciálisokkal kiegészített sztereotaxiás célzókészülékkel a világon elsőként végzett számítógép asszisztált és CT-vezérelt sztereotaxiás beavatkozást (25). III.2. Brachytherápia a szövetközi besugárzás fejlődésének történelmi áttekintése A radioizotópok szövetközi - interstitialis alkalmazása, a daganatszövet tűzdelése nem új keletű ben a Curie házaspár barátja, Danlos rádiummal végzett először ilyen tűzdelést nem daganatos bőrgyógyászati betegségek gyógykezelésére (26). Európában az első, Szentpéterváron elvégzett brachyterápiás kezelést már daganatos (arcbőr basalioma) betegeken alkalmazták 1903-ban (27). Hirsch 1912-ben az orron keresztül behelyezett rádiummal sugarazta be a török nyereg környékét (28). Agydaganatok, meningeomák első nem sztereotaxiás szövetközi, rádiummal történő besugárzásáról Frazier számolt be 1920 ban (29). Az 1950-es években Jean Talairach és munkatársai az agydaganatok szövetközi besugárzásának lehetőségét tanulmányozták. Jód-125, Ittrium-90, Arany-198 és Rénium- 186 radionuklidokkal végzett kísérleteik során elsőként számoltak be késői sugárnekrózisról (phenomenon of delayed radiation-induced necrosis) (30). Talairach kutatócsoportjához 1956-ban csatlakozó Szikla Gábor a sztereotaxiás szövetközi besugárzás úttörőjévé vált. Agyalapi mirigy besugárzására a kis dózisteljesítményű 12
13 Arany-198, gliomák besugárzására Irídium-192, cisztás tumorok falának besugárzására Ittrium-90 és Rénium-186 radionuklidot használtak. Az Európában történt első sztereotaxiás szövetközi besugárzást megelőzve az USA-ban 1953-ban Murtagh és társai elvégezték az első craniophryngeoma ciszta Foszfor-32 sztereotaxiás intracavitalis besugárzását (31). Amióta Mundinger és Szikla az agydaganatok kezelésében bevezették a radioaktív források sztereotaxiás intratumorális alkalmazását (32), több forradalmian új képalkotási eljárás született (CT, MRI, PET), melyek elősegítették a szövetközi besugárzás tökéletesítését. Hazánkban is nagy múltja van a brachyterápiának (Kisfaludy, 1932), a high dose rate utántöltéses eljárással végzett emlőtűzdelésekről elsőként Mayer és mtsai. számoltak be a 90-es évek elején (33). A craniopharyngeoma ciszták intracavitalis besugárzása 30 éves múltra tekint vissza (Julow, 1975), (34, 35), low grade gliomák és más agydaganatok low dose rate Jód-125 és high grade gliomák high dose rate Iridium-192 sztereotaxiás szövetközi besugárzása 9 éve folyik rutinszerűen (Julow, Major, 1997), (36). A világon elsőként végzett, számítógép asszisztált CT- és képfúzióvezérelt sztereotaxiás szövetközi besugárzás Julow Jenő nevéhez fűződik (37). A szövetközi besugárzás alkalmazásakor a tumorban az izotóp sugárforrások ( seed -ek) körül kialakuló sugárnekrózis következményeként csökken a daganatsejtek száma, maga után vonva a neurológiai tünetek enyhülését (38-45). Többféle izotóppal végeztek sztereotaxiás brachyterápiát, de leginkább az Ir-192 és a I-125 terjedt el. Az utóbbi izotóp előnye, hogy az alacsony energia (27-35 kev) miatt jelentős mértékű a szöveti gyengítés, ami lehetővé teszi, hogy a céltérfogat körüli ép szövetek dózisterhelése minimális legyen. Sugárvédelmi szempontból is kedvező az alacsony energia, mivel kisebb mértékű (lokális) sugárvédelmet igényel (46-48). III.3. A sztereotaxiás sugársebészeti eljárások fejlődésének történeti áttekintése III.3.1 A gamma-kés sugársebészet 13
14 A sztereotaxiás sugársebészetnek, melyet Lars Leksell definiált 1951-ben, legfőbb célja a kóros, vagy ép sejteket tartalmazó meghatározott céltérfogat teljes és pontos megsemmisítése egyszeri, nagydózisú sugárkezeléssel, a környező szövetek károsítása nélkül (49-51). Ez úgy érhető el, hogy több irányból, egymást a célpontban keresztező, keskeny sugárnyalábot használunk, így a metszéspontban nagy dózis alakul ki, ugyanakkor az ép szövetek sugárterhelése alacsony marad. Míg a hagyományos sugárkezelés hatékonysága a szövetek eltérő sugárérzékenységén alapul, addig a sugársebészetben a nagy pontossággal leadott szövetroncsoló sugárdózis miatt az eltérő sugárérzékenység kevésbé jelentős. Napjainkban különböző technikák alkalmazhatók erre a célra: gamma-kés, LINAC végzett fotonbesugárzás, proton besugárzás és a Cyberkés sugársebészet (8, 49-57). Az eredeti, Leksell által kidolgozott gamma-kés sugársebészeti rendszerben, egy félgömbpaláston elhelyezett 179 különálló, a gömb középpontjára fókuszált gammasugárzást emittáló Kobalt-60 izotóp volt a sugárforrás (50, 51). Előre meghatározott koordináták alapján a beteg feje a készülékben úgy helyezhető el, hogy a célpont a sugárfókuszba kerül. III.3.2. A LINAC sugársebészet A lineáris gyorsítót alkalmazó besugárzási rendszer egy körív mentén vertikális síkban mozgó sugárforrásból, és egy, az előbbire merőleges, horizontális síkban elhelyezkedő kezelőasztalból áll. Sugársebészeti beavatkozásnál a kezelendő elváltozást a két forgástengely metszéspontjába (izocentrum) állítjuk be. Mivel ez a pont a kezelőasztal és a sugárforrás forgatásával nem változik, így a több irányból történő besugárzás lehetővé válik. A pontos beállítást egy sztereotaxiás állvány teszi lehetővé, melyet a kezelőasztal folytatásaként annak forgó pódiumához rögzítünk. Az állványhoz kapcsolódik a beteg fejéhez rögzített sztereotaxiás keret, melyet az állvánnyal a tér három síkjában lehet elmozdítani. A rendszer úgy van összehangolva, hogy a lokalizálás során nyert koordinátákat az állványon beállítva a célpont a gyorsító izocentrumába kerül. A sugármező méreteit a sugárforrásra szerelt speciális szűkítőkkel (másodlagos kollimátorok) állítjuk be (55, 58, 59). 14
15 Az első hazai LINAC sugársebészeti rendszert 1991-ben Fedorcsák és mtsai. helyezték üzembe (60). 15
16 IV. Módszer és betegek IV.1. A sztereotaxiás szövetközi besugárzás során alkalmazott sugárforrás jellemzői A daganatok szövetközi besugárzását lágy gamma sugárzású radioaktív Jód-125 izotóprudacskákkal (Iodine 125 Seeds IMC6702, 6711 Nycomed, Amersham), úgynevezett seed -ekkel végezzük. A Modell es forrásban a radioaktív anyagot egy titán kapszula foglalja magába, amelynek hossza 4,5 mm, átmérője 0,8 mm, falvastagsága pedig 0,05 mm. A kapszula 3 műgyanta golyócskát tartalmaz, melyeknek a felszínén van az adszorbeált radioaktív anyag. A kapszulák kezdeti aktivitása 5-20 mci ( MBq). A radioaktív Jód-125 izotópnak három fő fotonenergiája van: a 27,4 kev és a 31,4 kev fékezési, valamint 35,5 kev gammasugárzás, 1,00, 0,25 és 0,06 relatív intenzitásokkal. A felezési ideje 59,6 nap, a felezőréteg vastagsága ólomban 0,025 mm. A kis energia hozzájárul ahhoz, hogy a kezelés során a céltérfogatot körülvevő ép szövetek dózisterhelése kicsi legyen (61). IV.2. A sztereotaxiás koordináta rendszer és CT-MRI-PET képfúzió A betegeket Fischer-Mundinger sztereotaxiás alapkerettel immobilizáljuk. A műtétek tervezéséhez és kivitelezéséhez a CT felvételeket Elscint Elite 2400 és Siemens Magneton Impact (Szent János Kórház, Budapest) képalkotóval végezzük. A daganat alsó határától számított 2 cm mélységből a koponyatetőig 1,5 mm szeletvastagsággal végezzük a CT vizsgálatokat és betegenként 100 ml Ultravist i.v. kontrasztanyagot alkalmazunk. A kontrasztanyagnak köszönhetően a daganat az ép szövetektől jobban elkülöníthetővé válik, és a brachyterápiás beavatkozásokkor az így láthatóvá tett erek sérülését is el tudjuk kerülni. Low grade gliomás betegeknél, elsősorban recidív gliomák és ismételt besugárzások esetén a műtétek tervezésekor felhasználjuk a rendelkezésünkre álló MRI (Siemens Magnetom Vision Plus 1,5 Tesla, Kaposvári Pannon Egyetem; General Electric, Sigma Infinity, Echospeed 1,5 T, LX 9.1, SE Szív és Érsebészeti Klinika, Budapest; Siemens, Magneton Symphony, Országos Onkológiai és Sugárterápiás Intézet, Budapest; Siemens, Magneton Symphony, Országos Idegsebészeti és 16
17 Tudományos Intézet, Budapest; Siemens Magneton Impact 1 T, Országos Pszichiátriai és Neurológiai Intézet, Radiológiai Osztály, Budapest) és PET (GE 4096 Plus, DOTE) vizsgálatok digitális képeit is. Az MRI vizsgálatok során 10 ml Magnevist i.v. kontrasztanyagot, míg PET vizsgálatkor 11 C-methionin tracert használunk. Ezt követően a CT képek 3 dimenziós koordináta rendszerében fuzionáljuk a CT, MRI és PET képeket, így az MRI és PET vizsgálat képi információiban is lehetővé tesszük a sztereotaxiás tájékozódást, ill. a brachyterápiás és LINAC sugársebészeti beavatkozást. A különböző képmodalitások képfúzióját a BrainLab cég (BrainLab AG, Kirchheim- Heimstetten, Németország) Target 1.19 besugárzás tervezőrendszerének pixel-to-pixel automata képfúziós szoftvermoduljával végezzük (37, 62, 63). A statisztikai számításokat a MedCalc és az MS Excel szoftverek felhasználásával végezzük. Szignifikánsnak véleményeztünk az eltérést, ha a Student-félr t-próba értéke p< IV.3. A szövetközi besugárzás IV.3.1. A sztereotaxiás Jód-125 szövetközi besugárzás tervezése A brachyterápiás műtétek tervezését a BrainLab cég Target 1.19 besugárzás-tervező szoftver moduljával végeztük. A keresztmetszeti képek tervező számítógépbe történő bevitele után a következő lépés a célterület, illetve az elokvens agyi struktúrák berajzolása minden egyes CT szeleten. A berajzolt kontúrokból 3D rekonstrukció segítségével a tumor térbeli alakja vizsgálható. Az így berajzolt céltérfogat nagyságától függően kell megválasztani a használandó katéterek számát, azok térbeli elhelyezkedését, a katéterekben levő izotópok aktivitását és egymáshoz viszonyított pozícióikat. A cél az, hogy referenciadózis-felület vegye körbe a céltérfogat alakját, de ugyanakkor ne alakuljanak ki nagy, túldozírozott térfogatok sem. Ehhez megfelelő geometriai elrendezésben kell elhelyezni a sugárforrásokat, mert a dózis közelítőleg a forrásoktól mért távolság négyzetével fordítottan arányos, ami kis távolságoknál mindig nagy elnyelt dózist eredményez. 17
18 IV.3.2. A Jód-125 sugárforrások sztereotaxiás beültetése A tervezés eredményeként meghatározásra kerülnek a célzóíven beállítandó paraméterek, melyeket felhasználva a katéterek pontosan beültethetők. A katétereket az implantáció előtt kell elkészíteni. A katéterek izotópokkal és a közöttük levő műanyag távtartókkal történő feltöltése sterilen és sugárvédett helyen történik. A Jód-125 pálcikákat tartalmazó katéterek implantációját sugárhigiéniás körülményeket biztosító idegsebészeti műtőben, steril körülmények között végezzük. A műtét során, helyi érzéstelenítés mellett, az alapkeretre pontosan illeszkedő célzókeret segítségével a koponyára a számításoknak megfelelő helyeken 3,2 mm átmérőjű fúrt lyukakat helyezünk fel. Ezeken a fúrt lyukakon át kerülnek bevezetésre az aktív izotópokat tartalmazó katéterek. A katétereket a koponya lamina externájához fém klippekkel rögzítjük. Közvetlen az implantáció után végzett CT-CT fúziós vizsgálat lehetőséget ad a verifikációra is, amely során ellenőrizzük az izotópok térbeli pozícióját. A katéterek eltávolítását a kiszámított besugárzási idő letelte után helyi érzéstelenítés mellett végezzük. IV.3.3. A CT-CT intraoperatív képfúzió IV A Jód-125 sugárforrások sztereotaxiás beültetését követő intraoperatív verifikáció Az implantáció után, a beteg koponyájához rögzített sztereotaxiás kerettel együtt újabb koponya CT vizsgálatot végzünk. Az így nyert újabb CT vizsgálati anyagot fuzionáljuk a tervezéshez felhasznált CT felvételi anyaggal. Ezáltal a műtét során végzett CT-CT fúzió lehetőséget ad a verifikációra, amely során ellenőrizzük az izotópokkal feltöltött katéterek térbeli pozícióit. Ha a fúziót követően a katéter valódi pozíciója nem egyezik a tervben meghatározottal, a katéter pozícióját korrigáljuk. IV A CT-CT intraoperatív képfúzióval verifikált esetek 18
19 Összesen 70 esetben végeztünk intraoperatív CT-CT fúziós verifikációt. A hetven eset során 116 katétert és 351 izotóp magot ültettünk be. A képfúziót követően 14 esetben (20 %) kellett a beültetett katéterek helyzetén változtatni (1. Táblázat). 1. Táblázat Tizennégy műtét adatai, melyeknél a katéterek helyzete eltért a tervezettől n Szövettan V (cm 3 ) Dózis (Gy) A ö (mci) T (h) n k n s 1. # A II 8, , HA 30, , PBL 1, , A II # GBL 20, , PBL 2,8 60 9, # A II 16, , # GBL 15, , CRF 7, , # AN 6, , A III 19, , A II 11, , # A II 30, , # M ca ov 3, Átlag 12,7 58,8 61,2 354,9 Medián 2 5 Jelmagyarázat: n esetszám, V a daganat térfogata, A ö a tumorba beültetett seedek összaktivitása, T besugárzási idő, h óra, n k a beültetett katéterek száma, n s a beültetett seedek száma, A II - astrocytoma grade II, A III - astrocytoma grade III, HA hipofízis adenoma, PBL pineoblastoma, GBM glioblastoma multiforne, CRF craniopharyngeoma, AN akusztikus neurinoma, M ca ov ovárium karcinóma metasztázis, # - szabálytalan (irreguláris) alakú daganatok 19
20 IV.3.4. A Jód-125 sztereotaxiás brachyterápia és LINAC sztereotaxiás sugársebészeti eljárások dóziseloszlásainak és sugárbiológiai hatásosságának összehasonlítása IV Esetismertetés Huszonnégy Jód-125 brachyterápiás (továbbiakban BT) és huszonnégy LINAC sugársebészeti besugárzási tervet készítettünk 22 beteg 24 intracranialis tumorának besugárzására (2. Táblázat). Minden tumor esetében elkészítettük a brachytherápiás és LINAC-os tervet is. Az esetben megterveztük, majd kiviteleztük a brachyterápiás kezelést, ezt követően visszamenőleg készítettük el a LINAC-os tervet. A esetekben először megterveztük, majd kiviteleztük a LINAC-os kezelést, és ezt követően készítettük el a brachyterápiás tervet. Két betegen egyenként két két sztereotaxiás besugárzást végeztünk. Az 5. számú betegen elvégeztünk egy brachyterápiás és egy LINAC-os (13. eset) besugárzást is, míg egy betegen (14. és 15. eset) két LINAC-os besugárzást hajtottunk végre. A daganatok átlag térfogata 12,7 cm 3 (tartomány: 1,3-30,5 cm 3 ) volt. Huszonnégy esetből 11 esetben (2. Táblázat) a daganatok szabálytalan alakúak voltak. A szabályos daganatok megközelítőleg gömb vagy forgási ellipszoid alakúak voltak, a szabálytalan alakú daganatokon egy vagy több kiemelkedés vagy bemélyedés volt. IV Közös céltérfogat a stereotaxiás szövetközi besugárzás és LINAC sugársebészeti tervekhez A brachyterápiás műtétek tervezését a BrainLab cég Target 1.19, a LINAC besugárzások tervezését pedig a BrainLab cég Target 4.03 besugárzás-tervező szoftver modullal végeztük. E szoftverek lehetővé teszik, hogy a céltérfogat és a védendő szervek berajzolását követően az adatok mindkét tervező szoftvermodul részére elérhetők legyenek. Így sikerült biztosítani, hogy egyszeri berajzolással ugyanazt a céltérfogatot használjuk a brachyterápiás és a LINAC-os besugárzási terv elkészítéséhez. 20
21 IV A Jód-125 brachyterápiás tervek Tumoronként a tumor nagyságától, alakjától és az izotópok aktivitásától függően a tervekben medián 1 katétert (1 3 db) és medián 5 seed -t (1 10 db) használtunk. Az izotópok aktivitásának medián értéke 10,3 mci (4,7 19,2 mci) volt. A tumor széli részeire tervezett referenciadózisnak medián értéke 60 Gy ( Gy) és a medián átlagos dózisteljesítmény 31,3 cgy/óra ( 12,5 83,3 cgy/óra ) volt. A brachyterápiás besugárzási idő medián értéke 192 óra ( óra) volt (2. Táblázat). A esetben a brachyterápiás tervezésnél 10,3 mci aktivitású seed -eket használtunk, ami megegyezik az közti időszakban elvégzett 70 brachyterápiás besugárzás során alkalmazott seed -ek átlagos aktivitásával. IV A LINAC sugársebészeti tervek A esetekben a besugárzást az Országos Onkológiai Intézet Sugárterápiás Osztályának 6 MV-s fotonenergiájú Siemens-Mevatron lineáris gyorsítójával végeztük. A LINAC-os besugárzások tervezése során tumoronként a tumor nagyságától és alakjától függően medián 1 izocentrumot (1 4 db), 7,5 30 mm közötti átmérőjű kör alakú kollimátort és 4 standard besugárzási ívet használtunk (2. Táblázat). A besugárzási ívek a következők voltak: 180 -s transverzális, 90 -s sagittalis és két 45 -s parasagittalis. A brachyterápiás és LINAC-os besugárzási terv elkészítése során törekedtünk a céltérfogat konformális besugárzására, az ép szövetek és védendő struktúrák (agyidegek különös tekintettel a látóidegre és agytörzsre) legkisebb sugárterhelése mellett. 21
22 2. Táblázat A Jód-125 brachyterápiás és LINAC sugársebészeti tervek adatai n Szövettan Dref (Gy) Jód-125 stereotaxiás brachyterápia LINAC SS D min (Gy) T (h) A S (mci) n k ; n S D at (cgy/h) D ref (Gy) D min (Gy) D max (Gy) n IC 1. AN ; , PBL 54 27, ,1 1 ; 1 28, , M ca t 80 66, ,8 1 ; 2 33, , * A II ,2 1 ; 3 35, , A II 60 37, ,8 1 ; 5 35, * MG 70 27, ,7 1 ; 2 20, , * A III 60 18, ,1 2 ; 10 31, * A III 60 25, ,3 2 ; 7 17, , CRF 50 34, ,4 1 ; 3 20, , * A II ,7 1 ; 7 12,5 16 7, * AI 60 58, ,6 1 ; 6 31,3 16 9, * A II 60 26, ,7 2 ; 6 12, A II 60 57, ,3 1 ; , A II ,3 1 ; 4 27, , A II ,3 1 ; 5 27, AN 60 52, ,3 1 ; 1 35, , * A II 60 52, ,3 3 ; 6 31, ,3 22, AN ,3 1 ; , M ca t 60 40, ,3 1 ; M mel ,3 1 ; 1 83, , * M ca t 80 53, ,3 2 ; 4 47, , * HN 60 26, ,3 1 ; 6 31,3 12 4, * MG , ,3 2 ; 6 33, EP ,3 1 ; 4 35,7 20 9, Medián 60 41, ,3 1; 5 31, , Jelmagyarázat: n- esetszám, * - szabálytalan alakú daganat, SS sztereotaxiás sugársebészet, AN akusztikus neurinoma, PBL pineoblastoma, M ca t tüdő karcinóma metasztázis, A II - astrocytoma grade II, MG meningeoma, A III - astrocytoma grade III, CRF craniopharyngeoma, A I - astrocytoma grade I, M mel melanoma metasztázis, HN hypoglossus neurinoma, EP ependymoma, D ref - referencia dózis, D min daganatra leadott minimális dózis, T besugárzási idő, h óra, A S - seed aktivitás, n k a katéterek száma, n S seed -ek száma, D at átlagos dózisteljesítmény, D max daganatra leadott maximális dózis, n IC - izocentrum 22
23 IV A referenciadózis renormalizálása A huszonnégy brachyterápiás és huszonnégy LINAC-os terv elkészítését követően a referenciadózist renormalizáltuk. Az új referenciadózist úgy választottuk meg, hogy az mindig a céltérfogat 95 % -át sugarazza be (9. Táblázat). Ezt követően meghatároztuk, hogy az új referenciadózissal a céltérfogat hány százalékának megfelelő ép agyszövetet sugaraztunk be. Így lehetővé vált a BT-s és a LINAC-os tervek céltérfogatra és ép szövetre vonatkozó DVH (dózis-térfogat hisztogram) paramétereinek összehasonlítása. Ezt követően az összehasonlítást elvégeztük az új referenciadózis 90 és 150 százalékára is (9. Táblázat). IV Dozimetriai megfontolások Minden egyes BT-s tervnél meghatároztuk, hogy a céltérfogat hány százalékának megfelelő ép agyszövet részesül 8, 12, Gy dózisban (1 11. csoportok), (10. és 11. Táblázat). Az azonos céltérfogatokhoz a LINAC-os tervekben visszakerestük a dózisértékeket. Ezt követően a LINAC-os dózisokat a Brenner és munkatársai által leírt linear-quadratic (LQ) modell dózis-idő összefüggése alapján átszámoltuk ekvivalens BT-s dózissá (Új BT dózis), (1. és 2. Ábra) (64). Számításainkban az alfa/beta hányadost az ép szövetekre 2 Gy-nek vettük (65, 66). A LINAC-os besugárzásoknál 30 perces kezelési időt és 45 perc felezési időt feltételeztünk a megújulásra (repair), a BT-s terveknél minden egyes dózisra az adott tervben szereplő besugárzási időt használtuk. Így minden egyes térfogatértékhez két BT-s dózist rendeltünk, ezáltal lehetővé vált a BT-s és a LINAC-os tervek ép szövetre gyakorolt (késői) sugárbiológiai hatásának összehasonlítása (10. és 11. Táblázat). 23
24 1. Ábra A 19. eset brachyterápiás műtéti tervének dóziseloszlása 3 ortogonális síkban. A referenciadózis 60 Gy. 2. Ábra A 19. eset LINAC-os műtéti tervének dóziseloszlása 3 ortogonális síkban. A referenciadózis 16 Gy. 24
25 IV Térfogati indexek A céltérfogat pontos térbeli ismeretében az intersticiális dóziseloszlások kvantitatív jellemzésére térfogati indexek használhatók: lefedési index ("coverage index", CI), relatív dózis homogenitási index ("homogeneity index", HI) és a külső térfogati index ("external volume index", EI) (67-70). A CI megadja a céltérfogatnak azt a hányadát, amelyen belül az elnyelt dózis nagyobb vagy egyenlő a referenciadózissal. A HI a céltérfogatnak azt a hányadát jelenti, amelyben az elnyelt dózis a referencia dózis 100 % -a és 150 %-a között van. Az EI a céltérfogaton kívüli ép szövetek azon térfogatának a céltérfogathoz viszonyított arányát jelenti, melyben a dózis nagyobb vagy egyenlő a referenciadózissal. Ideális esetben a CI = 1, a HI maximális és az EI = 0. Saw és mtsai. négyféle sztereotaxiás agytűzdelési technikát hasonlítottak össze dozimetriai szempontból, és megállapították, hogy a katéterek számának növelése javított a dózishomogenitáson (71). Baltas és mtsai. a CT képeken alapuló konformális brachyterápiás tűzdelések kiértékelésére definiálták a COIN konformalitási indexet (72). Definíció szerint, a COIN = c1 x c2, ahol c1 = PTVref/PTV és c2 = PTVref/Vref. A PTVref a céltérfogat (PTV) és a referenciadózis által körbefogott térfogatnak (Vref ) a közös része. A c1 együttható a céltérfogatnak az a hányada, amelyet a referencia dózis magában foglal (megegyezik CIvel), a c 2 együttható pedig a referenciadózis-felület által körbefogott térfogatnak az a hányada, amely a céltérfogaton belül van. Ez utóbbi együttható egyben azt is jellemzi, hogy a céltérfogaton kívüli ép szövetek mekkora része kapja meg a referenciadózist, mert a Vref -nek a PTV-n kívüli része már a normál szövethez tartozik. Ideális esetben mindkét együttható, és ezért a COIN értéke is egyenlő 1-el. Ez az eset akkor áll fenn, amikor a céltérfogat minden pontja úgy kapja meg a referenciadózist (vagy annál nagyobbat), hogy az ép szövetek minden pontjának a dózisterhelése kisebb mint a referenciadózis. Szemléletesen ez azt jelenti, hogy a referenciadózis-felület pontosan követi a céltérfogat térbeli alakját. Valódi tűzdeléseknél a konformalitás soha sem tökéletes, vagyis a COIN értéke mindig kisebb mint 1. A BrainLab besugárzástervező rendszerrel a CI-t közvetlenül, míg a COIN-t, HI-t és EI-t csak közvetetten lehet meghatározni. A DVH grafikonon tetszőleges dózis-értékhez tartozó térfogat érték egy mozgatható, a DVH görbét metsző egyenes vonal segítségével 25
26 határozható meg. Az így leolvasott értékekből a definíciók alapján manuálisan számoltuk ki a különböző paramétereket. A fenti paraméterek eredetileg brachyterápiás dóziseloszlások jellemzésére lettek definiálva, de értelemszerűen alkalmazhatók teleterápiás besugárzási tervek kiértékelésére is. Vizsgálataink során kétféle sugárterápiás eljárást hasonlítottunk össze, ezért azonos dozimetriai paramétereket használtunk mindkét módszernél. A BT-s és LINAC-os dóziseloszlások összehasonlítása a céltérfogat azonos dózislefedettségén alapult. A lefedési index mindig azonos volt, ami azt jelenti, hogy úgy választottuk meg a dóziselőírásra szolgáló referencia izodózis felületet, hogy az minden esetben 95 %-t foglaljon magába a céltérfogatból. IV.4. A Jód-125 szövetközi besugárzással kezelt esetek bemutatása Az közti időszakban 75 betegen 93 Jód-125 sztereotaxiás szövetközi besugárzást végeztünk. A rendszeres betegkövetés 64 esetben volt lehetséges, 11 beteg sorsa ismeretlen. A továbbiakban a rendszeres kontrollon megjelent és képalkotó eljárásokkal rendszeresen kontrollált betegek adatait tárgyaljuk. 48 daganat supratentorialis és 6 infratentorialis elhelyezkedésű volt; 42 glioma, 7 meningeoma, 3 akusztikus neurinoma, 2 pineoblastoma. IV.4.1. Gliomák Összesen 42 inoperabilis glioma 30 low grade és 12 high grade (8 A III astrocytoma és 4 glioblastoma multiforme) részesült szövetközi besugárzásban. A szövetközi besugárzást 16 esetben nem előzte meg műtét, míg 26 esetben a besugárzást recidív és reziduális gliomák kezelésére alkalmaztuk. A betegek 38 esetben egyszeri, 3 esetben kétszeri és 1 esetben háromszori besugárzásban részesültek. A gliomák elhelyezkedése 27 esetben lobalis, 15 esetben axialis volt. A betegek általános állapota Karnofsky 70 és 100 között változott (Medián 80) (3. és 4. Táblázat). 26
27 3. Táblázat Gliomás betegeink Jód-125 szövetközi besugárzásának adatai Átlag Medián Minimum Maximum Életkor Tumor térfogat (cm 3 ) Katéterek száma Seed -ek száma Aktivitás (mci) Besugárzási idő (nap) CI (%) EI (%) Referencia dózis (Gy) Dózis-teljesítménye (cgy/óra) Jelmagyarázat: CI dózis-térfogat hisztogram, EI - a daganat térfogatához viszonyított referencia dózissal besugarazott épp szövet aránya 4. Táblázat Gliomás betegeink Jód-125 szövetközi besugárzásának adatai BT mint adjuváns kezelés BT mint első beavatkozás LGG HGG GBM LGG HGG GBM Esetszám KPS Medián Tartomány Nemek megoszlása Férfi Nő Életkor (év) Átlag Szórás Lokalizáció Lobáris Axiális
28 Jelmagyarázat: LGG low grade gliomák, HG high grade gliomák, GBM glioblastoma multiforme, KPS Karnofsky skála IV.4.2. Meningeomák Öt betegen 7 meningeoma szövetközi besugárzását végeztük el. Egy betegen izotóp hiányában két ülésben 2, illetve 1 meningeoma besugárzását kiviteleztük. Egy esetben reziduális, hat esetben recidív ebből 4 malignus meningeomát sugaraztunk be. Daganatonként a daganat nagyságától, alakjától és a seed -ek aktivitásától függően medián 3 sugárforrást (2 6) használtunk. A meningeomák térfogata a terápiát megelőzően medián 4,5 cm 3 (1,3 9,1 cm 3 ), a felhasznált seed -ek medián aktivitása 9,7 mci (4 16,5 mci) volt (5. Táblázat). A betegek általános állapota Karnofsky 80 és 100 között változott (medián 90). 5. Táblázat Meningeomás betegeink Jód-125 szövetközi besugárzásának adatai Daganat V A n Év Szövettan lokalizációja (cm 3 n ) K /n S D ref S (mci) (Gy) , 1993 meningeoma jo. n. opticus 3,7 1/1, 1/1 12, , 2000 malignus meningeoma jo.frontolateralis 4,7 1/3 9, meningeoma bo. frontobasalis 5,0 1/3 16, meningeoma jo. sinus cavernosus 1,3 1/1, 1/ * jo parietooccipitalis 9,1 1/6 10, , malignus bo. parasagittalis 4,1 1/3 4, , meningeoma , 2002 jo. parasagittalis 4,5 1/5 4,6 120 Jelmagyarázat: n a beteg száma, Év a mikrosebészeti beavatkozás éve, V a daganat térfogata, n K a katéterek száma, n S a seedek száma, A S a seedek aktivitása, D ref - 28
29 referenciadózis, jo. jobb oldali, bo. bal oldali, * ben a szövettani eredmény benignus meningeoma volt IV.4.3. Pineoblastomák Két pineoblastomás beteget részesítettünk Jód-125 szövetközi besugárzásban. A daganatok besugárzására vonatkozó adatokat a 6. Táblázatban láthatók. A betegek általános állapota Karnofsky 90 és 100 volt. 6. Táblázat Pineoblastomás betegeink Jód-125 szövetközi besugárzásának adatai n Daganat lokalizációja V (cm 3 ) n K / n S A S (mci) D ref (Gy) 1 pinealis raegio 2,9 1/2 4, pinealis raegio 1,3 1/1 11,7 54 Jelmagyarázat: n a beteg száma, DT a daganat térfogata, n K a katéterek száma, n S a seedek száma, A S a seedek aktivitása, Dref - referenciadózis IV.4.4. Akusztikus neurinomák Három akusztikus neurinomás beteget részesítettünk Jód-125 szövetközi besugárzásban. A daganatok besugárzására vonatkozó adatokat a 7. Táblázatban láthatók. A betegek általános állapota Karnofsky 80, 80 és 90 volt. 29
30 7. Táblázat Akusztikus neurinomás betegeink Jód-125 szövetközi besugárzásának adatai Daganat V A n Év lokalizációja (cm 3 n ) K /n S D ref S (mci) (Gy) 1 - jobb oldal 6,7 1/3 7, jobb oldal 11,5 1/4 7, jobb oldal 10,0 1/5 17,0 50 Jelmagyarázat: n a beteg száma, Év a mikrosebészeti beavatkozás éve, V a daganat térfogata, n K a katéterek száma, n S a seedek száma, A S a seedek aktivitása, Dref - referenciadózis 30
31 V. Eredmények V.1. A CT-CT intraoperatív képfúzió A brachytherápiás műtétek után közvetlenül elvégzett CT felvételeket fuzionáltuk a műtétek tervezésekor felhasznált CT felvételekkel. A 70 esetben elvégzett képfúziót követően 14 esetben (20 %) kellett a beültetett katéterek helyzetét változtatni. A katéterek számát figyelembe véve a 70 esetben felhasznált 116 katéterből a kontroll képfúziót követően 16 katéter helyzetét (13,8 %) kellett korrigálni. A 14 eset mindegyikénél egy tumor besugárzását végeztük el. Összesen 22 katétert és 72 seed -t használtunk fel a 14 műtét során. A tizennégy eset során felhasznált 22 katéterből 16 katéter pozícióján kellett változtatni (8. Táblázat): a katéter vége 12 esetben volt túlnyomva a tervek alapján meghatározott célponton. Ezekben az esetekben a katétereket vissza kellett húzni (3. és 4. Ábra). 3. Ábra A 11. eset intraoperatív (műtét tervezéséhez használt és a katéter bevezetése utáni) CT-képeinek fúziója a bevezetett katéter síkjában. A sárga kontúr a daganatot, a zöld vonal a katétert, a sárga rudacskák a Jód 125 seed -ek tervezett helyét, míg a vastag fehér vonal a seed -ekkel feltöltött katéter valóságos helyzetét mutatja. A katéter vége 5 mm-el túl van nyomva a terv alapján meghatározott célponton (egyes számmal jelölt zöld kereszt). A katétert 5 mm rel vissza kellett húzni. 31
32 4. Ábra A 4. eset intraoperatív (műtét tervezéséhez használt és a katéter bevezetése utáni) CT-képeinek fúziója a bevezetett katéter síkjában. A sárga kontúr a daganatot, a zöld vonal a katétert, a sárga rudacskák a Jód 125 seed -ek tervezett helyét, míg a vastag fehér vonal a seed -ekkel feltöltött katéter valóságos helyzetét mutatja. A katéter vége 4 mm-el túl van nyomva a tervek alapján meghatározott célponton (egyes számmal jelölt zöld kereszt). A katétert 4 mm-rel vissza kellett húzni. 2 esetben volt a katéter egyidejűleg túlnyomva és oldalirányban eltolódva. A katétereket vissza kellett húzni, és korrigálni kellett a beültetés szögét (5. Ábra). 5. Ábra A 8. eset intraoperatív (műtét tervezéséhez használt és a katéter bevezetése utáni) axiális CT-képeinek fúziója. A sárga kontúr a daganatot, a zöld vonal a katétert, a sárga rudacskák a Jód 125 seed -ek tervezett helyét, míg a vastag fehér vonal a seed -ekkel 32
33 feltöltött katéter valóságos helyzetét mutatja. A katéter 3 mm el van tolódva oldal irányba és a vége 2 mm-el túl van nyomva a tervek alapján meghatározott célponton. Meg kellett változtatni a katéter dőlésszögét, és 2 mm rel vissza kellett húzni. 1 esetben a katéter vége nem érte el a tervek alapján meghatározott célpontot. A katétert beljebb kellett nyomni. 1 esetben a katéter vége nem érte el a terv alapján meghatározott célpontot és oldalirányban is el volt tolódva. A katétert beljebb kellett nyomni, és korrigálni kellett a beültetés szögét. Mind a 14 terven a tervezőrendszer DVH funkcióját használva meghatároztuk, hogy a referenciadózis a daganat térfogatának hány százalékát fedi, továbbá kiszámoltuk azt is, hogy az ép agyszövet mekkora része kapja meg ezt a referenciadózist. Ez utóbbi értéket is a daganat térfogatához viszonyítottuk (%). A postoperatív CT-CT fúziót követően a 14 esetben a katéterek valós helyzetének megfelelően újraszámoltuk a DVH értékeket, majd azokat összehasonlítottuk az eredeti terv megfelelő értékeivel (8. Táblázat). A katéter korrigálása előtti referenciadózis a daganattérfogatok átlag 75,8% -át (69,1 94%) fedte le, ami 16,6 %-kal elmaradt a tervezetthez képest (átlag: 92,4%, tartomány: 87,9 98,3%). Az átlagértékek között az eltérés szignifikáns volt (p = 0,01), (5. Táblázat). Az ép szövetek sugárterhelését tekintve a korrekció hiánya 10,4%-os túldozírozást eredményezett volna. A valódi forráspozíciókkal számolva az ép szövetből átlagosan a daganat 86,4%-nak (35 195%) megfelelő térfogat kapta volna meg a referenciadózist, szemben a terv alapján számolt 76%-kal (32,7 192,3%). A különbség itt is szignifikáns volt (p=0,01, 5. Táblázat). 33
34 5. Táblázat A tizennégy eset daganatra és ép agyszövetre vonatkozó dózis térfogat paraméterek, valamint a katéter pozícionálás pontatlanságainak adatai n CI (%) ÉI (%) KVH / eltérés Terv Valóság Terv Valóság (mm) 1. 89,5 77,1 34,5 45,6 A / 2, , ,4 50,9 A / ,7 56,7 104,4 125,5 A / ,9 71,2 32,7 35 A / ,7 70,1 58,4 82,5 A / ,9 57,6 32,7 63,2 A / 2, C / ,6 116,9 120,8 A / , ,3 195 A / 2, C / ,9 84,3 79,3 82 A / ,9 72,1 46,5 67 A / ,8 74,1 112,5 117 A / ,5 80,5 69,6 79,6 B / ,1 86,2 53,6 59,8 A / 2; B / 4, C / ,4 69,1 69,6 101,9 A / 4; A / 4 Átlag 92,4 75, ,8 A / 3,5, C / 2,7, B / 3 p < 0,0001 0,001 Jelmagyarázat: n esetszám, CI tumor dózis-térfogat hisztogram, EI ép szövet dózis-térfogat hisztogram, KVH a katéter valódi helyzete, A a katéter vége a célponthoz képest túl volt nyomva, B a katéter vége nem érte el a célpontot - a célponthoz képest sekélyebben volt, C a katéter dőlésszöge eltér a tervben szereplő dőlésszögtől ( a tervezett és a katéter végének valódi helyzete közti távolság) 34
35 V.1.1. A kis és nagy daganatok csoportja (1. Táblázat) A 14 esetet kis (<10 cm 3 ) és nagy ( 10 cm 3 ) térfogatú daganatok csoportjára választottuk szét. A kis daganatok csoportjában a kivitelezést követően a referenciadózis a daganattérfogat átlag 69,7 %-t (56,7 84,3 %) fedte le (CI=0,697), ami 22 % -kal elmaradt a terveknél mért átlagos 92,4 % - tól (87,9 94,4 %), (p = 0, 01). A nagy daganatok csoportjában a kivitelezést követően a referenciadózis a daganattérfogat átlag 81,8 % -át (70,1 94 %) fedte le (CI=0,818), ami 11,2 %-kal maradt el a terveknél mért átlagos 93 % - tól (88,7 98,3 %), (p = 0, 01). Az ép szövet referencia dózissal besugarazott térfogatának átlagértéke a kivitelezést követően a kis daganatok csoportjában 74,3 % (35 125,5 %) volt (EI=0,743), ami 17,2 %-kal meghaladta a tervek alapján meghatározott 57,1 % -ot,(32,7 104,4), (p = 0,01). A nagy tumoroknál az értékek 99,4 % (50,9 195), (EI=0,994) és 94,8 % (50,4 192,3 %), (EI=0,948), (p = 0,05) voltak. Az előbbi érték 4,6 % -kal haladta meg a tervek alapján meghatározott átlagértéket. V.1.2. A szabályos és szabálytalan alakú daganatok csoportja (1.sz. Táblázat) A daganatokat alakjuk szerint felosztottuk szabályos és szabálytalan alakú daganatokra. A szabályos daganatok gömb vagy forgási ellipszoid alakúak voltak, a szabálytalan alakú daganatokon egy vagy több kiemelkedés vagy bemélyedés volt. Vizsgáltuk a DVH daganatra és ép szövetre vonatkozó értékeit. A daganat térfogatának referenciadózis általi lefedettsége a szabálytalan alakú daganatok csoportjában a kivitelezést követően átlag 77,7 % (69,1 86,6 %) volt (CI=0,777), ami 13,8 % -kal elmaradt a terveknél mért átlagos 91,5 %-tól (88,7 94,8 %), (p < 0, 01). A szabályos alakú daganatok esetén a térfogatérték a kivitelezést követően 73,8 % (71,2 94 %) volt (CI=0,738). Ez az érték 19,5 % -kal volt kevesebb, mint a tervek alapján meghatározott átlag 93,3 % (87,9 98,3 %), (CI=0,933), (p < 0, 01). Az ép szövet térfogatának átlagértéke a kivitelezést követően a szabálytalan alakú daganatok csoportjában 103,2 % (45,6 195 %) volt (EI=1,032), ami 12,1 %-kal 35
36 meghaladta a tervek alapján meghatározott 91,1 %-t (34,5 192,3), (p=0,03). A szabályos alakú tumorok esetén a besugárzott ép szövet átlagértéke a kivitelezést követően 71,9 % (35 125,5) volt (EI=0,719), ami 12,5 %-kall haladta meg a tervek alapján meghatározott 59,4 % átlagértéket (32,7 104,4 %), (EI=0,594), (p=0,03). V.2. A Jód-125 sztereotaxiás brachyterápia és LINAC sztereotaxiás sugársebészeti eljárások dóziseloszlásainak és sugárbiológiai hatásának összehasonlítása Az új referenciadózis a brachyterápiás tervek esetén az eredeti átlag 64,3 Gy ről átlag 68,4 Gy re változott (9. Táblázat). A LINAC terveknél az új referenciadózis-átlag 16,9 Gy, ami megegyezik az eredeti referencia dózissal (6. Ábra). Az új referencia dózis az ép szövetből a brachyterápiás terveknél a céltérfogatnak átlagosan 127 % -át, a LINAC terveknél 141,3 % -át sugarazta be. Az új referenciadózis 90 százalékánál az ép szövetek DVH értéke a brachyterápiás és LINAC tervek esetén a céltérfogat átlag 159,1 % -a, illetve 201,6 % -a volt (9. Táblázat). A Student-féle t-próba a két eljárás között szignifikáns különbséget mutatott (p = 0,02). Az új referencia dózis 150 százalékánál mind a céltérfogatra, mind az ép szövetre vonatkozó DVH értékek a két eljárás közt szignifikáns eltérést jeleztek (7. Ábra), (p=0,01). A 1. és 2. csoportban a LINAC sztereotaxiás besugárzás az ép szövetre nézve kedvezőbbnek bizonyult, azonban szignifikáns különbség nem volt (10. Táblázat). A 3. és 4. csoportban a brachyterápiás besugárzás bizonyult kedvezőbbnek, azonban a különbség itt sem volt szignifikáns (10. Táblázat). A csoportban a brachyterápiás besugárzás szignifikánsan jobbnak bizonyult. A legnagyobb különbséget a két sztereotaxiás eljárás ép szövetre kifejtett biológiai hatása között a 7. (p = 0,0008) és 8. (p = 0,0006) csoportban mutattuk ki (11. Táblázat). V.2.1. A szabályos és szabálytalan alakú daganatok csoportja 36
37 A szabályos alakú daganatok 1. csoportjában a LINAC besugárzás az ép szövetekre nézve szignifikánsan kíméletesebbnek bizonyult, mint a brachyterápia.(p = 0,03). A 2. és 3. csoportban a LINAC besugárzás kíméletesebb volt, de szignifikáns eltérést nem találtunk. A szabályos alakú daganatok csoportjaiban a brachyterápiás besugárzás bizonyult kíméletesebbnek az ép szövetekre nézve, de szignifikáns különbség nem volt a két eljárás közt (11. Táblázat). A szabálytalan alakú daganatok 1 2. csoportjában a két eljárás ép szövetekre kifejtett késői sugárbiológiai hatásában eltérés nem mutatkozott. A 3 4. csoportban a brachyterápiás eljárás bizonyult jobbnak, szignifikáns különbség nélkül. A csoportban a brachyterápiás besugárzás a LINAC besugárzással összehasonlítva szignifikánsan jobbnak bizonyult (p = 0,001-0,03), (10. és 11.. Táblázat). V.2.2. Dozimetriai megfontolások A dóziseloszlások térfogati paramétereit összehasonlítva megállapíthatjuk, hogy a brachyterápiás besugárzásokkal konformálisabban sugározható be a daganat, mint a LINAC eljárással. Az előbbi COIN indexe átlagosan 0,45 volt, míg a LINAC besugárzásoké 0,42 (12. Táblázat). Az ép szövetek felesleges besugárzását jellemző EI index is kedvezőbb a brachyterápiánál (1,28 vs. 1,41). Ugyanakkor meg kell jegyezni, hogy a különbségek egyik paraméternél sem voltak statisztikailag szignifikánsak. A dóziseloszlások homogenitását nézve azonban a LINAC besugárzások bizonyultak kedvezőbbnek. A HI paraméter szignifikánsan nagyobb volt a sugársebészetnél, mint az intersticiális brachyterapiánál (0,8 vs. 0,19) (12. Táblázat). Ez az eredmény várható volt, mert a brachyterápiás dóziseloszlások a sugárforrások körüli meredek dózisesés miatt mindig inhomogén dózisviszonyokat eredményeznek. 37
38 BT LINAC Relatív térfogat (%) V90 V100 V Ábra A BT és LINAC stereotaxiás sugársebészeti tervek során a referenciadózis 90, 100 és 150 %-kával besugarazott daganattérfogatok százalékaránya a céltérfogathoz viszonyítva. Relatív térfogat (%) Vép90 Vép100 Vép150 BT LINAC 7. Ábra A BT és LINAC stereotaxiás sugársebészeti tervek során a referenciadózis 90, 100 és 150 %-kával besugarazott épszövettérfogatok százalékaránya a céltérfogathoz viszonyítva. 38
39 9. Táblázat Dózistérfogat adatok a refrenciadózis renormalizálása után n V D ref (Gy) D ref új (Gy) V ép 100 (%) V 90 (%) Vép 90 (%) V 150 (%) V ép 150 (%) ( cm 3 ) BT LSS BT LSS BT LSS BT LSS BT LSS BT LSS BT LSS 1. 9, ,5 13,1 170,3 43, ,9 203,5 67,6 75,7 0 85, , ,3 18,2 162,7 116,7 96,3 97,3 208,2 220,7 84, , ,2 29,5 29,9 98,8 98,2 46,3 57,7 70,5 0 1, , ,2 18,6 144,8 233,5 99,1 98,4 182,4 290,9 66,6 26,5 54, , ,8 22,4 68,7 130,2 97,6 98,4 89,9 183,5 75,2 0 17, , ,8 16, ,5 97,5 97,8 358, ,2 15,4 152,4 24, , ,8 18,8 124,4 103,4 96,4 97, ,4 82,9 33,4 44,3 3, , ,8 18,4 116,5 62,5 96,5 97,7 141, ,5 44,2 46,6 7,5 9. 4, ,4 49,7 63, , ,9 67,4 0 17, , ,2 15,3 71,4 125, ,2 92,2 160,3 77,5 24,2 21,7 8, , ,2 14,7 54, , ,2 78,6 39,8 11,7 5, , , ,4 119, ,7 129,6 178,1 84,9 0 32, , ,5 61,4 113,4 97, ,9 249,6 76,4 0 12, , , ,1 204, ,3 234,7 252,6 72,4 0 82, , , ,7 339, ,8 327, ,5 46,9 111, , ,7 153,9 96, ,7 296,2 83, , ,2 19,1 94, ,5 97,6 118,6 252, , ,9 129,6 270,8 96, ,2 439, , , ,6 93, ,4 41,4 110,8 68,8 0 3, , ,8 18, , , , , ,6 194, ,7 237,1 263,7 81,9 11,5 84,9 9, ,9 115,5 131, ,8 143,4 164,2 83,5 79,2 39,4 38, , ,2 19,6 112,1 115,7 98,3 99,3 147,7 169, ,7 28,5 2, , ,8 95,1 111,3 98,2 97,5 118,4 147,2 75,4 11,6 28,2 1,4 Átlag 5,6 64,3 16,9 68,4 16, ,3 97,8 98,2 159,1 201,6 76,3 14,4 50,1 7,6 p 0,3 0,07 0,02 0,01 0,01 Jelmagyarázat: n esetszám, V a daganat térfogata, D ref referenciadózis, BT brachyterápia, LSS LINAC sztreotaxiás sugársebészet, Vép 100 új referenciadózissal besugarazott ép agyszövet térfogata a daganat térfogatához ( céltérfogathoz ) viszonyítva, V 90 új referencia 90 százalékával besugarazott daganatrész (céltérfogat) térfogata százalékban kifejezve, Vép 90 új referenciadózis 90 százalékával besugarazott ép agyszövet térfogata a céltérfogathoz viszonyítva, V új referenciadózis 150 százalékával besugarazott daganatrész (céltérfogat) térfogata százalékban kifejezve, Vép 150 új referenciadózis 150 százalékával besugarazott ép agyszövet térfogata a céltérfogathoz viszonyítva, - nincs adat 39
40 10. Táblázat Jód-125 brachyterápiás és LINAC sugársebészeti dózisok összehasonlítása n 1. csoport (Gy) 2. csoport (Gy) 3. csoport (Gy) 4. csoport 30 (Gy) 5. csoport 40 (Gy) 6. csoport 50 (Gy) BT Új BT LSS BT Új BT LSS BT Új BT LSS BT Új BT LSS BT Új BT LSS BT Új BT LSS ,5 1, ,2 2, ,3 3, ,4 4, ,5 6, ,9 8, ,7 3, , ,8 8, ,7 13, , , ,2 2, , ,1 4, ,9 6, ,7 8, ,9 10, ,5 4, , ,3 7, ,4 10, , ,6 17, ,3 3, ,6 5, , ,2 11, ,2 16, , ,6 3, ,6 5, , ,5 11, ,7 15, ,4 17, , ,7 4, ,6 6, ,2 9, ,1 12, ,4 15, , , ,9 7, ,6 8, ,3 10, ,4 12, ,6 3, ,7 5, ,3 8, ,8 13, ,6 17, ,7 18, ,7 3, ,3 4, ,8 6, ,3 9, ,8 13, ,4 15, ,8 2, ,5 3, ,3 4, ,1 5, ,6 7, ,8 9, ,2 3, ,3 4, ,8 7, ,8 10, ,7 14, ,1 17, ,6 4, ,4 6, ,8 9, , ,5 20, ,7 22, , ,4 2,6 20 9,6 3, ,6 5, ,1 7, ,4 9, ,8 2, ,9 2, ,2 3, ,9 5, ,3 7, ,1 9, ,6 0, ,9 0, ,4 0, ,2 6, ,6 8, ,4 9, , ,4 4, ,3 6, ,7 9, ,7 13, ,4 16, ,4 1, ,4 2, ,8 4, ,2 6, ,4 8, ,4 10, ,4 3, ,2 4, ,8 6, , ,6 12, ,6 16, ,1 2,2 12 7,1 3, ,5 5, ,3 7, ,6 10, ,4 12, ,7 3, ,6 4, ,4 7, , , ,3 17, ,4 1, ,5 2,6 20 8,8 3, ,8 5, ,6 6, ,8 7, , ,8 2, , ,1 5, ,3 7, ,9 8, ,5 12 7,5 3, ,3 4, , ,3 9, ,2 11,75 Átlag 8 6,7 2, ,7 3, ,4 5, ,6 8, ,4 11, ,5 13,9 p 0,06 0,23 0,85 0,07 0,01 0,009 Jelmagyarázat: n esetszám, BT brachyterápia, LSS LINAC sztereotaxiás sugársebészet 40
41 11. Táblázat Jód-125 brachyterápiás és LINAC sugársebészeti dózisok összehasonlítása n 7. csoport (Gy) 8. csoport (Gy) 9. csoport (Gy) 10. csoport (Gy) 11. csoport (Gy) BT Új BT LRS BT Új BT LRS BT Új BT LRS BT Új BT LRS BT Új BT LRS ,2 9, ,1 10, ,2 11, ,5 12, ,6 12, , , ,1 19, ,7 19, ,3 19, ,8 13, , ,9 16, ,9 17, , ,4 21, ,1 22, ,1 23, , ,8 24, ,9 22, ,5 23, ,5 23, ,4 24, ,3 24, ,6 19, ,9 20, ,6 21, ,5 22, ,1 23, , , ,6 22, ,3 23, ,9 24, ,7 14, ,8 16, ,9 18, ,3 20, , ,8 19, ,3 19, , , , ,8 17, , ,3 19, ,8 20, ,1 21, ,4 11, , ,8 15, ,3 16, ,1 18, ,6 18, , ,4 19, ,7 19, ,8 19, ,3 23, , ,8 24, ,2 24, ,6 24, ,1 10, , ,7 15, ,6 16, , ,2 11, ,1 14, ,2 15, ,9 16, ,2 17, ,4 10, ,5 11, ,3 11, ,3 11, ,7 11, ,1 19, , ,6 21, ,2 21, , ,6 10, , ,4 11, ,1 11, ,8 11, , ,5 19, ,3 19, , , ,3 15, , ,8 16, ,1 16, ,1 16, , ,1 22, ,3 23, , ,6 24, ,2 9, ,7 11, , ,5 13, , ,6 10, , , ,3 15, ,2 16, ,7 13, ,7 14, ,8 15, ,5 16, ,2 16,5 Átlag 60 88,6 15, ,7 17, , ,2 18, ,2 19,2 p 0,0087 0,073 0,0089 0,009 0,03 Jelmagyarázat: n esetszám, BT brachyterápia, LSS LINAC sztereotaxiás sugársebészet 41
42 12. Táblázat Jód-125 brachyterápiás és LINAC sugársebészeti tervek térfogati indexei COIN HI EI n BT LSS BT LSS BT LSS 1. 0,34 0,65 0,19 0,95 1,7 0, ,35 0,43 0,11 0,95 1,63 1, ,73 0,72 0,25 0,95 0,3 0,3 4. 0,38 0,27 0,29 0,69 1,45 2, ,55 0,4 0,2 0,95 0,69 1,3 6. 0,22 0,31 0,16 0,8 3,07 1, ,41 0,46 0,12 0,46 1,24 1, ,43 0,57 0,11 0,51 1,17 0, ,62 0,57 0,28 0,95 0,5 0, ,54 0,41 0,17 0,71 0,71 1, ,6 0,55 0,16 0,55 0,55 0, ,46 0,42 0,1 0,95 1 1, ,58 0,43 0,19 0,95 0,61 1, ,3 0,3 0,23 0,95 2,02 2, ,25 0,21 0,25 0,48 2,63 3, ,36 0,36 0,12 0,95 1,77 1, ,48 0,3 x 0,95 0,95 2, ,4 0,25 x 0,95 1,3 2, ,73 0,48 0,26 0,95 0,28 0, ,32 0,35 0,25 0,95 1,9 1, ,31 0,31 0,13 0,84 2 1, ,43 0,4 0,11 0,16 1,16 1, ,44 0,43 0,27 0,83 1,12 1, ,48 0,44 0,2 0,83 0,95 1,11 Átlag 0,45 0,42 0,19 0,8 1,28 1,41 p 0,24 0,01 0,31 Jelmagyarázat: n esetszám, COIN konformalitási index, EI külső térfogati index, HI relatív homogenitási index, ST - standard deviáció, BT brachyterápia, LSS LINAC sztereotaxiás sugársebészet, x-nincs adat 42
43 V.3. A Jód-125 szövetközi besugárzás klinikai eredményei V.3.1. Gliomák A még életben lévő low grade gliómás betegek diagnózistól és brachyterápiától számított medián túlélése 51,7, illetve 31,2 hónap volt. Az elhunyt betegek esetében a diagnózistól számított medián túlélés 57,5 hónap, míg a brachyterápiától számított medián túlélés 47 hónap volt (13. Táblázat). Mivel az anaplasticus astrocytomás betegek csoportjában csak 8, míg a glioblastome multiformes betegek csoportjában csak 4 beteg volt, ezért a túlélés szempontjából a következőkben ezt a két csoportot együtt tárgyaljuk high grade glioma megjelöléssel. A még életben lévő high grade gliomás betegek diagnózistól és brachyterápiától számított túlélése 14, illetve 13,1 hónap volt. Az elhunyt betegek esetében a diagnózistól számított medián túlélés 22 hónap, míg a brachyterápiától számított medián túlélés 11,4 hónap volt (13. Táblázat). Két beteg esetében a 84, illetve 27 hónappal a brachyterápiát követően elvégzett PET 11 C Methionin vizsgálat tumort nem igazolt (8. és 9.sz. Ábra). 13. Táblázat Gliomás betegeink Jód-125 szövetközi besugárzásának eredményei Brachyterápiától számított túlélés Diagnózistól számított túlélés LGG HGG GBM LGG HGG GBM n Életben lévők túlélése (hónap) Medián 31,2 13,1 51,7 14 Tartomány Elhunytak túlélése (hónap) Medián 47 11,4 57,5 22 Tartomány Túlélési ráta (%) 1 éves éves éves éves
44 n esetszám, LGG low grade gliomas, HG high grade gliomas, GBM glioblastoma multiforme, Karnofsky Karnofsky skála, * - nincs elég beteg a statisztikai analízisre 8. Ábra 9. Ábra A 8. Ábra egy 51 éves férfi beteg műtéti terve látható. A zöld vonalak a katéterek, a sárga rudacskák a Jód-125 seed tervezett elhelyezését mutatják. A sárga kontúr a jobb oldali insularis daganat (Astrocytoma WHO Grade II.) határát jelöli a besugárzás előtt készült CT felvételen. A 9. Ábra a műtéti terv és 84 hónappal a besugárzás után készült kontroll PET 11 C- Methionine felvételének fúziója látható. A PET 11 C-Methionine vizsgálat tumort nem igazolt. V.3.2. Meningeomák Öt betegen hat alkalommal 7 meningeomát részesítettünk sztereotaxiás brachyterápiában (14. Táblázat). A 2. számú betegnél a kezelést követő tizenkettedik hónapban 2 új malignus meningeomát egy jobb oldalon frontobazálisan elhelyezkedő 9,1 cm 3 es, és a már előzőleg besugarazott meningeomától néhány milliméterre frontolateralisan lévő 29,1 cm 3 es meningeomát észleltünk. A jobb oldali új frontolaterális és a már besugarazott tumor mikrosebészeti eltávolítása után 6 nappal a beteg kardiális 44
45 insufficienciában elhunyt. Az elhunyt beteg brachyterápiásan kezelt malignus meningeomája 2 %-os zsugorodást mutatott. Az 5. számú betegnél júliusában izotóp hiányában csak a jobb oldali 9,1 cm 3 es parietooccipitalis és a bal oldali 4,1 cm 3 es parasagittalis tumorokat sugaraztuk be. A jobb oldali 2,2 cm 3 es paraszagittalis tumor brachytherapiájára nem állt rendelkezésünkre kellő számú izotóp rudacska. A jobb oldali paraszagittalis meningeoma besugárzására szeptemberében került sor. Ez a tumor két hónap alatt duplájára nőtt, a kezelés időpontjában már 4,5 cm 3 -es volt. Ugyancsak növekedést, a tumortérfogat 10 %-os duzzadását észleltük a besugárzáskor 9,1 cm 3 es jobb oldali parietooccipitalis és bal oldali 4,1 cm 3 es térfogatú paraszagittalis meningeomáknál. Ezt a besugárzás utáni átmeneti tumorduzzadással magyaráztuk, mely folyamatot acusticus neurinomák gamma-kés sugársebészetét követően már Kobayashi és Yu leírtak (73, 74 ). Az életben lévő négy beteg brachyterápiától számított medián követési ideje 54 (41 64 hónap). Az élő betegek tumorai medián 54 %-t ( %) zsugorodtak. Az összes meningeomára számított medián zsugorodás 52 % (2 100 % volt. 10. Ábra A 3. eset műtéti tervének és 54 hónappal a besugárzás után készült kontroll CT felvételének fúziója. A zöld vonal a katéter, a sárga rudacska a Jód-125 seed tervezett elhelyezését mutatja. A piros kontúr a daganat határát jelöli a besugárzás előtt készült CT felvételen, a sárga a besugárzás után 54 hónappal készült CT felvételen. A daganat zsugorodása 56 %-os. 45
46 14. Táblázat Meningeomás betegeink Jód-125 szövetközi besugárzásának eredményei V KI n V BT V T (cm 3 ) (cm 3 ) (%) (hónap) 1 3,7 2, ,7 4,6 2 elhalálozás 12 hónappal a szvb után 3 5,0 2, , ,1 4, ,1 2, ,5 2, Jelmagyarázat: n a beteg száma, V BT a tumor térfogata szövetközi besugárzáskor, V KI a tumor térfogata a megadott követési időben, V a tumor zsugorodása, T - a szövetközi besugárzástól számított követési idő V.3.3. Pinealoblastomák A két beteg esetében a brachyterápiától számított követési idő 62, illetve 59 hónap. Mindkét betegen többszöri kontroll CT, illetve MRI és PET vizsgálatot végeztünk. Az 1. esetben 58 hónappal a besugárzás után a kontroll MR felvételen mért tumortérfogat 0,76 cm 3 volt, amely 73 %-s zsugorodást jelentett a szövetközi besugárzás tervezésekor mért 2,87 cm 3 -es céltérfogathoz képest (15. Táblázat), (11. és 12. Ábra). A 2. esetben 56 hónappal a besugárzás után a kontroll MRI vizsgálaton mért tumortérfogat 0,29 cm 3 volt, amely a besugárzás tervezésekor mért 1,27 cm 3 -es céltérfogat 77 %-os zsugorodását igazolta (13. és 14. Ábra). Mindkét esetben végeztünk PET 11 C-Methionine vizsgálatot, ami élő tumorszövetet nem igazolt. 46
47 11. Ábra Az 1.eset CT műtéti tervének és 58 hónappal a besugárzás után készült kontroll MR felvételének fúziója. A zöld kontúr a daganat határát jelöli a besugárzás előtt, a sárga pedig besugárzás után 58 hónappal. A daganat térfogata 73 %-kal csökkent. 12. Ábra Az 1.eset CT műtéti tervének és dóziseloszlásának és 58 hónappal a besugárzás után készült kontroll MR felvételének fúziója. 13. Ábra A 2. eset CT műtéti tervének és 56 hónappal a besugárzás után készült kontroll MRI felvételének fúziója. Zöld szín a daganatot jelöli a besugárzás előtt készült CT felvételen, a narancssárga a besugárzás után 56 hónappal készült MRI felvételen. A daganatzsugorodás 77 %. 14. Ábra Az 2. eset CT műtéti tervének és dóziseloszlásának 56 hónappal a besugárzás után készült kontroll MR felvételének fúziója. 47
48 15. Táblázat Pineoblastomás betegeink Jód-125 szövetközi besugárzásának eredményei V BT n (cm 3 ) V KI V T (cm 3 ) (%) (hónap) 1 2,9 0, ,3 0, Jelmagyarázat: n a beteg száma, V BT a tumor térfogata szövetközi besugárzáskor, V KI a tumor térfogata a megadott követési időben, V a tumor zsugorodása, T - a szövetközi besugárzástól számított követési idő V.3.4. Akusztikus neurinomák Betegeink idősek, rossz általános állapotúak voltak. Csökkent műtéti teherbíró képességük miatt döntöttünk a shunt műtét, részleges tumoreltávolítás és interstitialis besugárzás mellett. Az életben lévő két beteg brachyterápiától számított követési ideje 88, illetve 71 hónap. A harmadik beteg a szövetközi besugárzást követő 13. hónapban légzési elégtelenségben elhunyt. Az audiometriai vizsgálat az első két esetben mérsékelt hallásjavulást állapított meg. A brachyterápiát követő hallásjavulás eredményeként az 1. esetben a beteg a hallásfunkció megítélésére szolgáló Gardner-Robertson 5 fokozatú skálán az V. fokozatból a IV. fokozatba, míg a 2. esetben az V. fokozatból a III. fokozatba volt besorolható (75). Az 1. esetben 85 hónappal a besugárzás után a kontroll CT felvételeken mért tumortérfogat 5,32 cm 3 volt, amely 21%-os zsugorodást jelentett a szövetközi besugárzás tervezésekor mért 6,74 cm 3 -es céltérfogathoz képest (15. Ábra). A 2. esetben a zsugorodás még látványosabb volt. Itt 68 hónappal a besugárzás után a kontroll MRI vizsgálaton mért tumortérfogat 6,64 cm 3 volt, mely a besugárzás tervezésekor mért 11,45 cm 3 -es céltérfogat 42%-os zsugorodását jelentette. A 3. esetben a kontroll MRI vizsgálatot a besugárzást követő 2. hónapban a daganat mérsékelt 5 %-os duzzadását találtuk, ugyanakkor a daganat belsejében a daganattérfogat 17 %-át kitevő postirradiatios ciszta alakult ki. A besugárzást követő nyolcadik hónapban a daganat térfogata 10 %-t zsugorodott és a cysta a térfogat 45 %-át tette ki (16. Táblázat), (16. Ábra). 48
49 A besugárzást követően facialis paresist, arczsibbadást, illetve hypaesthesiat egyik betegen sem észleltünk. 16. Táblázat Akusztikus neurinomás betegeink Jód-125 szövetközi besugárzásának eredményei V KI n V BT V T (cm 3 ) (cm 3 ) (%) (hónap) 1 6,7 5, ,5 6, , elhalálozás 12 hónappal a szvb után Jelmagyarázat: n a beteg száma, V BT a tumor térfogata szövetközi besugárzáskor, V KI a tumor térfogata a megadott követési időben, V a tumor zsugorodása, T - a szövetközi besugárzástól számított követési idő 15. Ábra A 1. eset műtéti tervének és 85 hónappal a besugárzás után készült kontroll CT felvételének fúziója. A zöld vonal a katéter, a sárga rudacska a Jód-125 seed tervezett elhelyezését mutatja. A külső piros kontúr a daganat határát jelöli a besugárzás előtt készült CT felvételen, a zöld a besugárzás után 85 hónappal készült CT felvételen. A daganat zsugorodása 21 %-os. 49
50 16. Ábra A 3. eset műtéti tervének és 8 hónappal a besugárzás után készült kontroll CT felvételének fúziója. A sárga kontúr a daganat határát jelöli a besugárzás előtt készült CT felvételen, a zöld a besugárzás után 8 hónappal készült CT felvételen. A lila kontúr a daganat 45 %-ot kitevő postirradiatios kontúrt jelöli. A daganat zsugorodása 10 %-os. 50
DOKTORI (Ph.D.) ÉRTEKEZÉS. Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során
 DOKTORI (Ph.D.) ÉRTEKEZÉS Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során dr. Viola Árpád Onkológia c. program keretében Témavezető:
DOKTORI (Ph.D.) ÉRTEKEZÉS Az intraoperatív képfúzió és a lineáris-quadratikus modell alkalmazása az agydaganatok Jód-125 szövetközi besugárzása során dr. Viola Árpád Onkológia c. program keretében Témavezető:
AZ AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA
 MTA DOKTORA PÁLYÁZAT DOKTORI ÉRTEKEZÉS AZ AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA DR. MED. HABIL. JULOW JEN Budapest 2007 TARTALOMJEGYZÉK 1. EL ZMÉNYEK ÉS CÉLKIT ZÉSEK 5 1.1 Tudományos el zmények:
MTA DOKTORA PÁLYÁZAT DOKTORI ÉRTEKEZÉS AZ AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA DR. MED. HABIL. JULOW JEN Budapest 2007 TARTALOMJEGYZÉK 1. EL ZMÉNYEK ÉS CÉLKIT ZÉSEK 5 1.1 Tudományos el zmények:
Az intraoperatív képfúzió jelentôsége a sztereotaxiás szövetközi besugárzás minôségi ellenôrzése során
 Az intraoperatív képfúzió jelentôsége a sztereotaxiás szövetközi besugárzás minôségi ellenôrzése során Dr. Viola Árpád, Dr. med. habil. Julow Jenô, Fôvárosi Önkormányzat, Szent János Kórház és Rendelô
Az intraoperatív képfúzió jelentôsége a sztereotaxiás szövetközi besugárzás minôségi ellenôrzése során Dr. Viola Árpád, Dr. med. habil. Julow Jenô, Fôvárosi Önkormányzat, Szent János Kórház és Rendelô
Szövetközi besugárzások - Emlőtűzdelések
 Szövetközi besugárzások - Emlőtűzdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Emlőtűzdelés Emlőtűzdelés
Szövetközi besugárzások - Emlőtűzdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Emlőtűzdelés Emlőtűzdelés
2. A BETEGEK ÉS A FELDOLGOZÁS MÓDSZEREI
 2. A BETEGEK ÉS A FELDOLGOZÁS MÓDSZEREI Értekezésemet 1975-2007 között végzett m téteimre és a betegek éveken (évtizedeken) át tartó klinikai és legalább 3 alkalommal végzett CT/MR, ritkábban CT/MR/PET
2. A BETEGEK ÉS A FELDOLGOZÁS MÓDSZEREI Értekezésemet 1975-2007 között végzett m téteimre és a betegek éveken (évtizedeken) át tartó klinikai és legalább 3 alkalommal végzett CT/MR, ritkábban CT/MR/PET
Dr. Fedorcsák Imre OITI
 Sztereotaxiás sugársebészeti fejlődése - lehetőségek Magyarországon Dr. Fedorcsák Imre OITI A sugársebészet definíciója: Egy pontosan meghatározott intracranialis céltérfogatot úgy tudunk nagy adott esetben
Sztereotaxiás sugársebészeti fejlődése - lehetőségek Magyarországon Dr. Fedorcsák Imre OITI A sugársebészet definíciója: Egy pontosan meghatározott intracranialis céltérfogatot úgy tudunk nagy adott esetben
Dr. Fröhlich Georgina
 Szövetk vetközi besugárz rzások - Emlőtűzdel zdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Emlőtűzdelés
Szövetk vetközi besugárz rzások - Emlőtűzdel zdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Emlőtűzdelés
Radioaktív izotópok a testünkben A prosztata belső sugárkezelése
 Radioaktív izotópok a testünkben A prosztata belső sugárkezelése A legtöbb embernek a háta is borsódzik, ha arra gondol, hogy sugárzó anyaggal kell kapcsolatba lépnie. Ennél is bizarrabbnak tűnhet, ha
Radioaktív izotópok a testünkben A prosztata belső sugárkezelése A legtöbb embernek a háta is borsódzik, ha arra gondol, hogy sugárzó anyaggal kell kapcsolatba lépnie. Ennél is bizarrabbnak tűnhet, ha
Minőségbiztosítás a sugárterápiában
 Minőségbiztosítás a sugárterápiában Dr. Szabó Imre DEOEC Onkológiai Intézet Sugárterápia Tanszék Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist
Minőségbiztosítás a sugárterápiában Dr. Szabó Imre DEOEC Onkológiai Intézet Sugárterápia Tanszék Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist
Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet)
 Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet) I. Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist az ép
Sugárterápia minőségbiztosításának alapelvei Dr. Szabó Imre (DE OEC Onkológiai Intézet) I. Irányelvek WHO 1988: Mindazon tevékenység, amely biztosítja a céltérfogatra leadott megfelelő sugárdózist az ép
Terápiás ablak. Ionizáló sugárzás. Sugárterápia. Röntgen sugárzás. Radioaktív izotópok
 Ionizáló sugárzás Sugárterápia Lövey József Országos Onkológiai Intézet SE Radiológiai és Onkoterápiás Klinika Budapest Az elnyelt sugárzás mértékegysége J/kg = Gray 100 % Terápiás ablak T C P N T C P
Ionizáló sugárzás Sugárterápia Lövey József Országos Onkológiai Intézet SE Radiológiai és Onkoterápiás Klinika Budapest Az elnyelt sugárzás mértékegysége J/kg = Gray 100 % Terápiás ablak T C P N T C P
Agydaganatok Sebészi neuroonkológia. Dr. Bagó Attila, Ph.D. Orsz. Klin. Idegtudományi Int. Neuroonkológiai Osztály Amerikai út.
 Agydaganatok Sebészi neuroonkológia Dr. Bagó Attila, Ph.D. Orsz. Klin. Idegtudományi Int. Neuroonkológiai Osztály Amerikai út. Neuro-onkológia Központi idegrendszeri daganatok komplex kezelése IDEGSEBÉSZET
Agydaganatok Sebészi neuroonkológia Dr. Bagó Attila, Ph.D. Orsz. Klin. Idegtudományi Int. Neuroonkológiai Osztály Amerikai út. Neuro-onkológia Központi idegrendszeri daganatok komplex kezelése IDEGSEBÉSZET
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél
 Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Eredményes temozolamid kezelés 2 esete glioblasztómás betegeknél Dr. Mangel László 1,2, Prof. Dr. Dóczi Tamás 3, Dr. Balogh Zsolt 4, Dr. Lövey József 2, Dr. Sipos László 5 Pécsi Tudományegyetem, Onkoterápiás
Szövetközi besugárzások - Prosztatatűzdelések
 Szövetközi besugárzások - Prosztatatűzdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Prosztatatűzdelés 4.
Szövetközi besugárzások - Prosztatatűzdelések Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Prosztatatűzdelés 4.
A sztereotaxiás sugárterápia
 A sztereotaxiás sugárterápia Dr. Jánváry Levente Országos Onkológiai Intézet, Sugárterápia Központ Szeged, 2018.09.13. Onkológia továbbképzés IGRT-Képvezérelt sugárterápia A kezelés pontosságának biztosítására,
A sztereotaxiás sugárterápia Dr. Jánváry Levente Országos Onkológiai Intézet, Sugárterápia Központ Szeged, 2018.09.13. Onkológia továbbképzés IGRT-Képvezérelt sugárterápia A kezelés pontosságának biztosítására,
I. Külső (teleterápiás) besugárzó-készülékek. 5 db lineáris gyorsító:
 I. Külső (teleterápiás) besugárzó-készülékek 5 db lineáris gyorsító: Varian TrueBeam 6, 10 és 18 MV foton, 6-18 MeV elektron, képvezérelt, intenzitás modulált, légzéskapuzott és sztereotaxiás sugárkezelés,
I. Külső (teleterápiás) besugárzó-készülékek 5 db lineáris gyorsító: Varian TrueBeam 6, 10 és 18 MV foton, 6-18 MeV elektron, képvezérelt, intenzitás modulált, légzéskapuzott és sztereotaxiás sugárkezelés,
AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA
 MTA DOKTORA PÁLYÁZAT DOKTORI ÉRTEKEZÉS TÉZISEI AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA DR. MED. HABIL. JULOW JEN Szent János Kórház Budapest 2007 TARTALOMJEGYZÉK 1. A KIT ZÖTT KUTATÁSI FELADAT ÖSSZEFOGLALÁSA
MTA DOKTORA PÁLYÁZAT DOKTORI ÉRTEKEZÉS TÉZISEI AGYDAGANATOK KÉPFÚZIÓ VEZÉRELT BRACHYTERÁPIÁJA DR. MED. HABIL. JULOW JEN Szent János Kórház Budapest 2007 TARTALOMJEGYZÉK 1. A KIT ZÖTT KUTATÁSI FELADAT ÖSSZEFOGLALÁSA
Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet
 Molekuláris Medicina Mindenkinek Semmelweis Egyetem, Neurológiai Klinika 2012. December 4. Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet Felosztás Neurofibromatózis I. (Recklinghausen
Molekuláris Medicina Mindenkinek Semmelweis Egyetem, Neurológiai Klinika 2012. December 4. Dr. Erőss Loránd, Dr. Entz László Országos Idegtudományi Intézet Felosztás Neurofibromatózis I. (Recklinghausen
Fejezetek a klinikai onkológiából
 Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. 1 SUGÁRTERÁPIA Technikai alapok Dr. Szil Elemér Bevezetés A daganatos betegek kezelésére
Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. 1 SUGÁRTERÁPIA Technikai alapok Dr. Szil Elemér Bevezetés A daganatos betegek kezelésére
Sugárterápia. Ionizáló sugárzások elnyelődésének következményei
 Sugárterápia Sugárterápia: ionizáló sugárzások klinikai alkalmazása malignus daganatok eltávolításában. A sugárkezelés során célunk az ionizáló sugárzás terápiás dózisának elérése a kezelt daganatban a
Sugárterápia Sugárterápia: ionizáló sugárzások klinikai alkalmazása malignus daganatok eltávolításában. A sugárkezelés során célunk az ionizáló sugárzás terápiás dózisának elérése a kezelt daganatban a
SZAKDOLGOZAT TÉMÁK. 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája.
 PTE ETK KAPOSVÁRI KÉPZÉSI KÖZPONT KÉPALKOTÓ DIAGNOSZTIKAI ANALITIKA SZAKIRÁNY SZAKDOLGOZAT TÉMÁK 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája. 2.) Az agy fejlődési rendellenességeinek
PTE ETK KAPOSVÁRI KÉPZÉSI KÖZPONT KÉPALKOTÓ DIAGNOSZTIKAI ANALITIKA SZAKIRÁNY SZAKDOLGOZAT TÉMÁK 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája. 2.) Az agy fejlődési rendellenességeinek
A képfúzió szerepe stereotaxiás agymûtéteknél
 A képfúzió szerepe stereotaxiás agymûtéteknél Dr. med. habil. Julow Jenô, Dr. Viola Árpád, Fôvárosi Önkormányzat Szent János Kórház Dr. Sági Sarolta, Fôvárosi Önkormányzat Szent János Kórház Dr. Major
A képfúzió szerepe stereotaxiás agymûtéteknél Dr. med. habil. Julow Jenô, Dr. Viola Árpád, Fôvárosi Önkormányzat Szent János Kórház Dr. Sági Sarolta, Fôvárosi Önkormányzat Szent János Kórház Dr. Major
Sugárterápia. Ionizáló sugárzások elnyelődésének következményei. Konzultáció: minden hétfőn 15 órakor. 1. Fizikai történések
 Sugárterápia 40% 35% 30% 25% 20% 15% % 5% 0% 2014/2015. tanév FOK biofizika kollokvium jegyspektruma 5 4,5 4 3,5 3 2,5 2 1,5 1 Konzultáció: minden hétfőn 15 órakor Ionizáló sugárzások elnyelődésének következményei
Sugárterápia 40% 35% 30% 25% 20% 15% % 5% 0% 2014/2015. tanév FOK biofizika kollokvium jegyspektruma 5 4,5 4 3,5 3 2,5 2 1,5 1 Konzultáció: minden hétfőn 15 órakor Ionizáló sugárzások elnyelődésének következményei
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3,
 Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Sarkadi Margit1, Mezősi Emese2, Bajnok László2, Schmidt Erzsébet1, Szabó Zsuzsanna1, Szekeres Sarolta1, Dérczy Katalin3, Molnár Krisztián3, Rostás Tamás3, Ritter Zsombor4, Zámbó Katalin1 Pécsi Tudományegyetem
Országos Onkológiai Intézet, Sugárterápiás Centrum 2. Országos Onkológiai Intézet, Nukleáris Medicina Osztály 4
 99m Tc-MDP hatására kialakuló dózistér mérése csontszcintigráfia esetén a beteg közvetlen közelében Király R. 1, Pesznyák Cs. 1,2,Sinkovics I. 3, Kanyár B. 4 1 Országos Onkológiai Intézet, Sugárterápiás
99m Tc-MDP hatására kialakuló dózistér mérése csontszcintigráfia esetén a beteg közvetlen közelében Király R. 1, Pesznyák Cs. 1,2,Sinkovics I. 3, Kanyár B. 4 1 Országos Onkológiai Intézet, Sugárterápiás
Brachyterápia. Dr. Fröhlich Georgina. Országos Onkológiai Intézet Sugárterápiás Központ Budapest
 Brachyterápia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés teleterápia: sugárzás forrása a betegen kívül
Brachyterápia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés teleterápia: sugárzás forrása a betegen kívül
besugárz Dr. Fröhlich Georgina Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Országos Onkológiai Intézet Sugárterápiás Központ Budapest
 Sugárter rterápiás besugárz rzás-tervezés Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Tervezőrendszerek (TPS)
Sugárter rterápiás besugárz rzás-tervezés Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Tervezőrendszerek (TPS)
DOKTORI ÉRTEKEZÉS. MTA Doktora pályázat. Major Tibor. Dóziseloszlások kvantitatív elemzése emlő- és prosztatadaganatok brachyterápiás.
 MTA Doktora pályázat DOKTORI ÉRTEKEZÉS Dóziseloszlások kvantitatív elemzése emlő- és prosztatadaganatok brachyterápiás tűzdeléseinél: a Párizs-i dozimetriai rendszertől a képvezérelt, inverz optimalizálásig
MTA Doktora pályázat DOKTORI ÉRTEKEZÉS Dóziseloszlások kvantitatív elemzése emlő- és prosztatadaganatok brachyterápiás tűzdeléseinél: a Párizs-i dozimetriai rendszertől a képvezérelt, inverz optimalizálásig
A sugárterápia szerepe a daganatok kezelésében
 A sugárterápia szerepe a daganatok kezelésében Dr. Horváth Ákos DEOEC Sugárterápia Tanszék A sugárterápia szerepe a daganatok kezelésében Onkoterápiás lehetőségek: Lokális: - sebészet - sugárterápia -
A sugárterápia szerepe a daganatok kezelésében Dr. Horváth Ákos DEOEC Sugárterápia Tanszék A sugárterápia szerepe a daganatok kezelésében Onkoterápiás lehetőségek: Lokális: - sebészet - sugárterápia -
Klinikai Központ Elnök. A Semmelweis Egyetem K l i n i k a i K ö z p o n t E l n ö k é n e k 1/2017. (I.30.) számú U T A S Í T Á S A
 Ikt.szám:10230/KLINK/2017 egészségügyi szolgáltató jellegére, társadalmi felelősségvállalására, valamint a lakosság egészségi állapota iránt érzett felelősségére tekintettel, orvosszakmai szempontok messze
Ikt.szám:10230/KLINK/2017 egészségügyi szolgáltató jellegére, társadalmi felelősségvállalására, valamint a lakosság egészségi állapota iránt érzett felelősségére tekintettel, orvosszakmai szempontok messze
Benignus agydaganat miatt operált betegek rehabilitációjának eredményei
 Benignus agydaganat miatt operált betegek rehabilitációjának eredményei Tarjányi Szilvia, Nagy Helga, Dénes Zoltán Országos Orvosi Rehabilitációs Intézet Semmelweis Egyetem Rehabilitációs Tanszéki Csoport
Benignus agydaganat miatt operált betegek rehabilitációjának eredményei Tarjányi Szilvia, Nagy Helga, Dénes Zoltán Országos Orvosi Rehabilitációs Intézet Semmelweis Egyetem Rehabilitációs Tanszéki Csoport
Atomfizika a gyászatban
 Atomfizika a gyógy gyászatban - Sugárter rterápia Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Nov. 8. Sugárterápia - Az egyik fő modalitás a daganatok kezelésében (+kemo,
Atomfizika a gyógy gyászatban - Sugárter rterápia Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Nov. 8. Sugárterápia - Az egyik fő modalitás a daganatok kezelésében (+kemo,
Vizsgálatok és módszerek Eredmények
 OPPONENSI VÉLEMÉNY Dr.Major Tibor: Dóziseloszlások kvantitatív elemzése emlő és prosztata daganatok brachyterápiás tűzdeléseinél: a Párizs-i dozimetriai rendszertől a képvezérelt, inverz optimalizálásig
OPPONENSI VÉLEMÉNY Dr.Major Tibor: Dóziseloszlások kvantitatív elemzése emlő és prosztata daganatok brachyterápiás tűzdeléseinél: a Párizs-i dozimetriai rendszertől a képvezérelt, inverz optimalizálásig
CT-képeken alapuló konformális brachyterápiás besugárzástervezés
 CT-képeken alapuló konformális brachyterápiás besugárzástervezés Eredeti közlemény Major Tibor, Polgár Csaba, Mangel László, Takácsi Nagy Zoltán, Somogyi András, Németh György Országos Onkológiai Intézet,
CT-képeken alapuló konformális brachyterápiás besugárzástervezés Eredeti közlemény Major Tibor, Polgár Csaba, Mangel László, Takácsi Nagy Zoltán, Somogyi András, Németh György Országos Onkológiai Intézet,
Daganatok sugárkezelése és radiokemoterápiája. Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék
 Daganatok sugárkezelése és radiokemoterápiája Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres szisztémás
Daganatok sugárkezelése és radiokemoterápiája Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres szisztémás
TEXTÚRA ANALÍZIS VIZSGÁLATOK LEHETŐSÉGEI A RADIOLÓGIÁBAN
 TEXTÚRA ANALÍZIS VIZSGÁLATOK LEHETŐSÉGEI A RADIOLÓGIÁBAN Monika Béres 1,3 *, Attila Forgács 2,3, Ervin Berényi 1, László Balkay 3 1 DEBRECENI EGYETEM, ÁOK Orvosi Képalkotó Intézet, Radiológia Nem Önálló
TEXTÚRA ANALÍZIS VIZSGÁLATOK LEHETŐSÉGEI A RADIOLÓGIÁBAN Monika Béres 1,3 *, Attila Forgács 2,3, Ervin Berényi 1, László Balkay 3 1 DEBRECENI EGYETEM, ÁOK Orvosi Képalkotó Intézet, Radiológia Nem Önálló
Intervenciós radiológia és sugárterápia
 Intervenciós radiológia és sugárterápia Hadjiev Janaki dr. Kaposvári Egyetem, Egészségügyi Centrum, Kaposvár A keresztmetszeti képalkotás forradalmi szerepe, a céltérfogat pontosabb meghatározása a CT-
Intervenciós radiológia és sugárterápia Hadjiev Janaki dr. Kaposvári Egyetem, Egészségügyi Centrum, Kaposvár A keresztmetszeti képalkotás forradalmi szerepe, a céltérfogat pontosabb meghatározása a CT-
DÓZISTELJESÍTMÉNY DILEMMA SUGÁRTERÁPIÁS BUNKEREK KÖRNYEZETÉBEN
 DÓZISTELJESÍTMÉNY DILEMMA SUGÁRTERÁPIÁS BUNKEREK KÖRNYEZETÉBEN dr. Ballay László OSSKI-AMOSSO A DÓZISTELJESÍTMÉNY DILEMMA FELVETÉSE SUGÁRVÉDELMI MÉRÉSEK: DÓZISTELJESÍTMÉNY MÉRÉSEK A helyszínen csak a dózisteljesítmény
DÓZISTELJESÍTMÉNY DILEMMA SUGÁRTERÁPIÁS BUNKEREK KÖRNYEZETÉBEN dr. Ballay László OSSKI-AMOSSO A DÓZISTELJESÍTMÉNY DILEMMA FELVETÉSE SUGÁRVÉDELMI MÉRÉSEK: DÓZISTELJESÍTMÉNY MÉRÉSEK A helyszínen csak a dózisteljesítmény
Orvosi biofizika képzk az ELTE-n
 Orvosi biofizika képzk pzés az ELTE-n Fröhlich Georgina Eötvös Loránd Tudományegyetem Természettudományi Kar Budapest Orvosi biofizika - Multidiszciplináris: fizika - mérnöki tudományok orvostudomány
Orvosi biofizika képzk pzés az ELTE-n Fröhlich Georgina Eötvös Loránd Tudományegyetem Természettudományi Kar Budapest Orvosi biofizika - Multidiszciplináris: fizika - mérnöki tudományok orvostudomány
3.3 A képfúzió vezérelt interstitialis besugárzás eredményei
 3.3 A képfúzió vezérelt interstitialis besugárzás eredményei A képfúzió vezérelt IB-kor a sztereotaxiás CT 3D rendszerében jelenítjük meg az agydaganatok 3D CT, MRI, PET képeit. Bármelyik modalitásra manuálisan
3.3 A képfúzió vezérelt interstitialis besugárzás eredményei A képfúzió vezérelt IB-kor a sztereotaxiás CT 3D rendszerében jelenítjük meg az agydaganatok 3D CT, MRI, PET képeit. Bármelyik modalitásra manuálisan
DIPLOMAMUNKA. Czermann Márton. klinikai sugárfizikus Országos Onkológiai Intézet
 DIPLOMAMUNKA Sztereotaxiás sugársebészet dóziseloszlásainak összehasonlító értékelése ívbesugárzásoknál és micromlc-vel végzett konformális technikánál Czermann Márton Témavezető: Tanszéki konzulens: Dr.
DIPLOMAMUNKA Sztereotaxiás sugársebészet dóziseloszlásainak összehasonlító értékelése ívbesugárzásoknál és micromlc-vel végzett konformális technikánál Czermann Márton Témavezető: Tanszéki konzulens: Dr.
Az informatika lehetséges szerepe a sugárterápiában II.
 Az informatika lehetséges szerepe a sugárterápiában II. Biológiai dóziseloszlási program létrehozása agydaganatok háromdimenziós besugárzás-tervezésénél Eredeti Mangel László, Kiss Tibor, Skriba Zoltán,
Az informatika lehetséges szerepe a sugárterápiában II. Biológiai dóziseloszlási program létrehozása agydaganatok háromdimenziós besugárzás-tervezésénél Eredeti Mangel László, Kiss Tibor, Skriba Zoltán,
Daganatok sugárkezelése és radiokemoterápiája. Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék
 Daganatok sugárkezelése és radiokemoterápiája Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres szisztémás
Daganatok sugárkezelése és radiokemoterápiája Polgár Cs. - Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres szisztémás
Speciális teleterápiás technikák
 Speciális teleterápiás technikák Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Teleterápia: - LinAc/ Co-ágyú
Speciális teleterápiás technikák Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Teleterápia: - LinAc/ Co-ágyú
Koch Zita BSc 4. évfolyam
 TDK 2011 Koch Zita BSc 4. évfolyam Témavezető: Dr. Fröhlich Georgina, Dr. Major Tibor Országos Onkológiai Intézet - Sugárterápiás Osztály Belső konzulens: Dr. Pesznyák Csilla BME - Nukleáris Technika Tanszék
TDK 2011 Koch Zita BSc 4. évfolyam Témavezető: Dr. Fröhlich Georgina, Dr. Major Tibor Országos Onkológiai Intézet - Sugárterápiás Osztály Belső konzulens: Dr. Pesznyák Csilla BME - Nukleáris Technika Tanszék
Intraoperatív és posztimplantációs dozimetria összehasonlítása permanens implantációs prosztata-brachyterápiával kezelt betegeknél
 148 Eredeti közlemény Intraoperatív és posztimplantációs dozimetria összehasonlítása permanens implantációs prosztata-brachyterápiával kezelt betegeknél Herein András 1,2, Ágoston Péter 1, Szabó Zoltán
148 Eredeti közlemény Intraoperatív és posztimplantációs dozimetria összehasonlítása permanens implantációs prosztata-brachyterápiával kezelt betegeknél Herein András 1,2, Ágoston Péter 1, Szabó Zoltán
Az elsô hazai sztereotaxiás agyi sugársebészeti rendszer továbbfejlesztése
 Az elsô hazai sztereotaxiás agyi sugársebészeti rendszer továbbfejlesztése Eredeti közlemény Kontra Gábor 1, Fedorcsák Imre 2, Bajcsay András 1 1 Országos Onkológiai Intézet, Sugárterápiás Osztály, 2 Országos
Az elsô hazai sztereotaxiás agyi sugársebészeti rendszer továbbfejlesztése Eredeti közlemény Kontra Gábor 1, Fedorcsák Imre 2, Bajcsay András 1 1 Országos Onkológiai Intézet, Sugárterápiás Osztály, 2 Országos
(intersticiális. brachyterápia) Dr. Fröhlich Georgina. Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest
 Szövetk vetközi besugárz rzások (intersticiális brachyterápia) Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest BT
Szövetk vetközi besugárz rzások (intersticiális brachyterápia) Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest BT
Cervixcarcinomadefinitív radiokemoterápia. Kahán Zsuzsanna
 Cervixcarcinomadefinitív radiokemoterápia Kahán Zsuzsanna SZTE Onkoterápiás Klinika, Szeged Méhnyakrák: definitív radiokemoterápia Igen sugár-és kemoszenzitívdaganat kemoradioterápia platina készítménnyel!
Cervixcarcinomadefinitív radiokemoterápia Kahán Zsuzsanna SZTE Onkoterápiás Klinika, Szeged Méhnyakrák: definitív radiokemoterápia Igen sugár-és kemoszenzitívdaganat kemoradioterápia platina készítménnyel!
KLINIKAI SUGÁRFIZIKA
 KLINIKAI SUGÁRFIZIKA Általános alapismeretek 1. A radioaktivitás alapjai 2. Elektromágneses sugárzás keletkezése, tulajdonságai 3. Ionizáló sugárzás és anyag kölcsönhatásai 4. Dózisfogalmak, egységek,
KLINIKAI SUGÁRFIZIKA Általános alapismeretek 1. A radioaktivitás alapjai 2. Elektromágneses sugárzás keletkezése, tulajdonságai 3. Ionizáló sugárzás és anyag kölcsönhatásai 4. Dózisfogalmak, egységek,
Radon leányelemek depozíciója és tisztulása a légzőrendszerből
 Radon leányelemek depozíciója és tisztulása a légzőrendszerből Füri Péter, Balásházy Imre, Kudela Gábor, Madas Balázs Gergely, Farkas Árpád, Jókay Ágnes, Czitrovszky Blanka Sugárvédelmi Továbbképző Tanfolyam
Radon leányelemek depozíciója és tisztulása a légzőrendszerből Füri Péter, Balásházy Imre, Kudela Gábor, Madas Balázs Gergely, Farkas Árpád, Jókay Ágnes, Czitrovszky Blanka Sugárvédelmi Továbbképző Tanfolyam
Seven implantátumok klinikai és radiológiai vizsgálata. Az osseointegráció mértéke és a csont szintjének stabilitása. Elsődleges eredmények.
 Seven implantátumok klinikai és radiológiai vizsgálata. Az osseointegráció mértéke és a csont szintjének stabilitása. Elsődleges eredmények. Zabaras D, Boubolis S, Spanos A, Petsinis V, Gisakis I G Bevezetés
Seven implantátumok klinikai és radiológiai vizsgálata. Az osseointegráció mértéke és a csont szintjének stabilitása. Elsődleges eredmények. Zabaras D, Boubolis S, Spanos A, Petsinis V, Gisakis I G Bevezetés
A FIZIKUS SZEREPE A DAGANATOS BETEGEK GYÓGYÍTÁSÁBAN
 A FIZIKUS SZEREPE A DAGANATOS BETEGEK GYÓGYÍTÁSÁBAN Balogh Éva Jósa András Megyei Kórház, Onkoradiológiai Osztály, Nyíregyháza Angeli István Debreceni Egyetem, Kísérleti Fizika Tanszék A civilizációs ártalmaknak,
A FIZIKUS SZEREPE A DAGANATOS BETEGEK GYÓGYÍTÁSÁBAN Balogh Éva Jósa András Megyei Kórház, Onkoradiológiai Osztály, Nyíregyháza Angeli István Debreceni Egyetem, Kísérleti Fizika Tanszék A civilizációs ártalmaknak,
Teleterápia Dr. Fröhlich Georgina
 Teleterápia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Sugárterápia: - az egyik fő modalitás a daganatok
Teleterápia Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Sugárterápia: - az egyik fő modalitás a daganatok
Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése
 Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése Doktori értekezés Fröhlich Georgina Semmelweis Egyetem Elméleti Orvostudományok Doktori
Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése Doktori értekezés Fröhlich Georgina Semmelweis Egyetem Elméleti Orvostudományok Doktori
Hivatalos Bírálat Dr. Gődény Mária
 Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Kiválósági ösztöndíjjal támogatott kutatások az Építőmérnöki Karon c. előadóülés
 Kiválósági ösztöndíjjal támogatott kutatások az Építőmérnöki Karon c. előadóülés Hazay Máté hazay.mate@epito.bme.hu PhD hallgató Budapesti Műszaki és Gazdaságtudományi Egyetem Tartószerkezetek Mechanikája
Kiválósági ösztöndíjjal támogatott kutatások az Építőmérnöki Karon c. előadóülés Hazay Máté hazay.mate@epito.bme.hu PhD hallgató Budapesti Műszaki és Gazdaságtudományi Egyetem Tartószerkezetek Mechanikája
Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése
 Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése Doktori tézisek Fröhlich Georgina Semmelweis Egyetem Elméleti Orvostudományok Doktori
Metszetképalkotó eljárásokon alapuló intersticiális konformális prosztata és emlő brachyterápia dozimetriai elemzése Doktori tézisek Fröhlich Georgina Semmelweis Egyetem Elméleti Orvostudományok Doktori
Konformális sztereotaxiás együléses sugársebészeti kezelés: tervértékelési módszerek és eredmények
 Eredeti közlemény 85 Konformális sztereotaxiás együléses sugársebészeti kezelés: tervértékelési módszerek és eredmények Kovács Péter 1, Sebestyén Zsolt 1, Farkas Róbert 1, Bellyei Szabolcs 1, Szigeti András
Eredeti közlemény 85 Konformális sztereotaxiás együléses sugársebészeti kezelés: tervértékelési módszerek és eredmények Kovács Péter 1, Sebestyén Zsolt 1, Farkas Róbert 1, Bellyei Szabolcs 1, Szigeti András
Röntgendiagnosztikai alapok
 Röntgendiagnosztikai alapok Dr. Voszka István A röntgensugárzás keltésének alternatív lehetőségei (röntgensugárzás keletkezik nagy sebességű, töltéssel rendelkező részecskék lefékeződésekor) Röntgencső:
Röntgendiagnosztikai alapok Dr. Voszka István A röntgensugárzás keltésének alternatív lehetőségei (röntgensugárzás keletkezik nagy sebességű, töltéssel rendelkező részecskék lefékeződésekor) Röntgencső:
Az Implantológia radiológiai vonatkozásai Dr. Ackermann Gábor gabor@dentesthic.hu www.fogaszati-radiologia.hu
 Az Implantológia radiológiai vonatkozásai Dr. Ackermann Gábor gabor@dentesthic.hu www.fogaszati-radiologia.hu Röntgenvizsgálat célja Diagnosztika/tervezés Műtét közben ellenőrzés Követéses vizsgálat Felvételi
Az Implantológia radiológiai vonatkozásai Dr. Ackermann Gábor gabor@dentesthic.hu www.fogaszati-radiologia.hu Röntgenvizsgálat célja Diagnosztika/tervezés Műtét közben ellenőrzés Követéses vizsgálat Felvételi
A SUGÁRVÉDELEM SZEREPE A BME ORVOSI FIZIKA MSC KÉPZÉSÉBEN
 A SUGÁRVÉDELEM SZEREPE A BME ORVOSI FIZIKA MSC KÉPZÉSÉBEN Pesznyák Cs 1,2, Légrády D 1, Osváth Sz 1, Zagyvai P 1,3 1 BME NTI 2 Országos Onkológiai Intézet 3 MTA EK ORVOSFIZIKUS Az orvosfizikus olyan fizikusi
A SUGÁRVÉDELEM SZEREPE A BME ORVOSI FIZIKA MSC KÉPZÉSÉBEN Pesznyák Cs 1,2, Légrády D 1, Osváth Sz 1, Zagyvai P 1,3 1 BME NTI 2 Országos Onkológiai Intézet 3 MTA EK ORVOSFIZIKUS Az orvosfizikus olyan fizikusi
Géresi Enikő Tel.: E-posta: Semmelweis Egyetem Továbbképzési Központ Akkr.pont. Tanfolyami órák
 Tanfolyam adatlap Alapadatok Kódszám Főcím Állapot Szervező Partner Célcsoport Szemeszter 2013.II.félév Jelleg Brachyterápia továbbképző tanfolyam Országos Onkológiai Intézet és Dr. Major (OOI) 1. sugárterápia
Tanfolyam adatlap Alapadatok Kódszám Főcím Állapot Szervező Partner Célcsoport Szemeszter 2013.II.félév Jelleg Brachyterápia továbbképző tanfolyam Országos Onkológiai Intézet és Dr. Major (OOI) 1. sugárterápia
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS
 KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS 1. Daganatos morbiditás és mortalitás Magyarországon 2. Kémiai és fizikai tényezők szerepe a daganatok kialakulásában
KLINIKAI ONKOLÓGIA ÁLTALÁNOS ONKOLÓGIA, EPIDEMIOLÓGIA, ETIOLÓGIA, DIAGNOSZTIKA ÉS SZŰRÉS 1. Daganatos morbiditás és mortalitás Magyarországon 2. Kémiai és fizikai tényezők szerepe a daganatok kialakulásában
II./3.4. fejezet: Daganatos betegségek sugárkezelésének alapelvei
 II./3.4. fejezet: Daganatos betegségek sugárkezelésének alapelvei Hideghéty Katalin A fejezet célja, hogy a hallgató megismerkedjen a sugárkezelés általános alapelveivel, és rálátást szerezzen a különböző
II./3.4. fejezet: Daganatos betegségek sugárkezelésének alapelvei Hideghéty Katalin A fejezet célja, hogy a hallgató megismerkedjen a sugárkezelés általános alapelveivel, és rálátást szerezzen a különböző
Emberi Erőforrások Minisztériuma
 Emberi Erőforrások Minisztériuma 55 725 20 Sugárterápiás szakasszisztens Komplex szakmai vizsga A vizsgafeladat időtartama: 45 perc (felkészülési idő 30 perc, válaszadási idő 15 perc) A vizsgafeladat értékelési
Emberi Erőforrások Minisztériuma 55 725 20 Sugárterápiás szakasszisztens Komplex szakmai vizsga A vizsgafeladat időtartama: 45 perc (felkészülési idő 30 perc, válaszadási idő 15 perc) A vizsgafeladat értékelési
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház. Emlő MR vizsgálatok korai eredményei kórházunkban
 DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
III./7.5. fejezet: Terápia. Tüneti kezelés
 III./7.5. fejezet: Terápia Bevezetés Az idegrendszeri tumorok kezelésének tárgyalása során szót ejtünk a tüneti eljárásokról, műtéti lehetőségekről, a sugárkezelés különböző módozatairól, a chemotherápiáról
III./7.5. fejezet: Terápia Bevezetés Az idegrendszeri tumorok kezelésének tárgyalása során szót ejtünk a tüneti eljárásokról, műtéti lehetőségekről, a sugárkezelés különböző módozatairól, a chemotherápiáról
MINŐSÉGBIZTOSÍTÁS SZEREPE A SUGÁRTERÁPIÁS SUGÁRBALESETEK MEGELŐZÉSÉBEN
 MINŐSÉGBIZTOSÍTÁS SZEREPE A SUGÁRTERÁPIÁS SUGÁRBALESETEK MEGELŐZÉSÉBEN A Nemzetközi Sugárbiztonsági Normák megfogalmazása szerint BALESETNEK tekinthető: Bármely nem szándékos esemény, beleértve az üzemeltetési
MINŐSÉGBIZTOSÍTÁS SZEREPE A SUGÁRTERÁPIÁS SUGÁRBALESETEK MEGELŐZÉSÉBEN A Nemzetközi Sugárbiztonsági Normák megfogalmazása szerint BALESETNEK tekinthető: Bármely nem szándékos esemény, beleértve az üzemeltetési
BESUGÁRZÁSTERVEZŐ RENDSZEREK MINŐSÉGBIZTOSÍTÁSA A SUGÁRTERÁPIÁBAN, 10 ÉV TAPASZTALATA. Pesznyák Csilla
 BESUGÁRZÁSTERVEZŐ RENDSZEREK MINŐSÉGBIZTOSÍTÁSA A SUGÁRTERÁPIÁBAN, 10 ÉV TAPASZTALATA Pesznyák Csilla Budapesti Műszaki és Gazdaságtudományi Egyetem Országos Onkológiai Intézet ELŐKÉSZÍTÉS RER/6/015 -
BESUGÁRZÁSTERVEZŐ RENDSZEREK MINŐSÉGBIZTOSÍTÁSA A SUGÁRTERÁPIÁBAN, 10 ÉV TAPASZTALATA Pesznyák Csilla Budapesti Műszaki és Gazdaságtudományi Egyetem Országos Onkológiai Intézet ELŐKÉSZÍTÉS RER/6/015 -
IV. Felkészítő feladatsor
 IV. Felkészítő feladatsor 1. Az A halmaz elemei a (-7)-nél nagyobb, de 4-nél kisebb egész számok. B a nemnegatív egész számok halmaza. Elemeinek felsorolásával adja meg az A \ B halmazt! I. 2. Adott a
IV. Felkészítő feladatsor 1. Az A halmaz elemei a (-7)-nél nagyobb, de 4-nél kisebb egész számok. B a nemnegatív egész számok halmaza. Elemeinek felsorolásával adja meg az A \ B halmazt! I. 2. Adott a
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia. Dr. Sáfrány Géza OKK - OSSKI
 Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
Sugárbiológiai ismeretek: LNT modell. Sztochasztikus hatások. Daganat epidemiológia Dr. Sáfrány Géza OKK - OSSKI Az ionizáló sugárzás biológiai hatásai Determinisztikus hatás Sztochasztikus hatás Sugársérülések
XVII. econ Konferencia és ANSYS Felhasználói Találkozó
 XVII. econ Konferencia és ANSYS Felhasználói Találkozó Hazay Máté, Bakos Bernadett, Bojtár Imre hazay.mate@epito.bme.hu PhD hallgató Budapesti Műszaki és Gazdaságtudományi Egyetem Tartószerkezetek Mechanikája
XVII. econ Konferencia és ANSYS Felhasználói Találkozó Hazay Máté, Bakos Bernadett, Bojtár Imre hazay.mate@epito.bme.hu PhD hallgató Budapesti Műszaki és Gazdaságtudományi Egyetem Tartószerkezetek Mechanikája
A II. kategória Fizika OKTV mérési feladatainak megoldása
 Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Nyomaték (x 0 Nm) O k t a t á si Hivatal A II. kategória Fizika OKTV mérési feladatainak megoldása./ A mágnes-gyűrűket a feladatban meghatározott sorrendbe és helyre rögzítve az alábbi táblázatban feltüntetett
Dr. Fröhlich Georgina
 Speciális teleterápi piás s technikák Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Teleterápia: - LinAc/
Speciális teleterápi piás s technikák Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest Ionizáló sugárzások a gyógyításban ELTE TTK, Budapest Bevezetés Teleterápia: - LinAc/
Daganatok sugárkezelésének és radio-kemoterápiájának alapjai
 Daganatok sugárkezelésének és radio-kemoterápiájának alapjai Polgár Cs. Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres
Daganatok sugárkezelésének és radio-kemoterápiájának alapjai Polgár Cs. Országos Onkológiai Intézet, Semmelweis Egyetem ÁOK Onkológiai Tanszék Daganatok komplex kezelése Sebészi kezelés Sugárkezelés Gyógyszeres
Miskolci Egyetem Egészségügyi Kar Klinikai Radiológiai Tanszék által a 2010/2011-es tanévre meghirdetésre leadott szakdolgozati és TDK témák
 Miskolci Egyetem Egészségügyi Kar Klinikai Radiológiai Tanszék által a 2010/2011-es tanévre meghirdetésre leadott szakdolgozati és TK témák V Védőnő szakirány GY Gyógytornász szakirány Képalkotó iagnosztikai
Miskolci Egyetem Egészségügyi Kar Klinikai Radiológiai Tanszék által a 2010/2011-es tanévre meghirdetésre leadott szakdolgozati és TK témák V Védőnő szakirány GY Gyógytornász szakirány Képalkotó iagnosztikai
Hadházi Dániel.
 Hadházi Dániel hadhazi@mit.bme.hu Orvosi képdiagnosztika: Szerepe napjaink orvoslásában Képszegmentálás orvosi kontextusban Elvárások az adekvát szegmentálásokkal szemben Verifikáció és validáció lehetséges
Hadházi Dániel hadhazi@mit.bme.hu Orvosi képdiagnosztika: Szerepe napjaink orvoslásában Képszegmentálás orvosi kontextusban Elvárások az adekvát szegmentálásokkal szemben Verifikáció és validáció lehetséges
Ionizáló sugárzások dozimetriája
 Ionizáló sugárzások dozimetriája A becsült átlagos évi dózis természetes és mesterséges forrásokból 3.6 msv. környezeti foglalkozási katonai nukleáris ipari orvosi A terhelés megoszlása a források között
Ionizáló sugárzások dozimetriája A becsült átlagos évi dózis természetes és mesterséges forrásokból 3.6 msv. környezeti foglalkozási katonai nukleáris ipari orvosi A terhelés megoszlása a források között
Modern Fizika Labor. 21. PET (Pozitron Annihiláció vizsgálata) Fizika BSc. A mérés száma és címe: A mérés dátuma: nov. 15.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 15. A mérés száma és címe: 21. PET (Pozitron Annihiláció vizsgálata) Értékelés: A beadás dátuma: 2011. nov. 30. A mérést végezte: Németh Gergely
Modern Fizika Labor Fizika BSc A mérés dátuma: 2011. nov. 15. A mérés száma és címe: 21. PET (Pozitron Annihiláció vizsgálata) Értékelés: A beadás dátuma: 2011. nov. 30. A mérést végezte: Németh Gergely
Korszerû brachyterápia
 Korszerû brachyterápia Dr. Polgár Csaba, Dr. Ágoston Péter, Dr. Takácsi-Nagy Zoltán, Dr. Kásler Miklós Országos Onkológiai Intézet, Budapest Rövidítések AL: utántöltés ( afterloading ) BT: brachyterápia
Korszerû brachyterápia Dr. Polgár Csaba, Dr. Ágoston Péter, Dr. Takácsi-Nagy Zoltán, Dr. Kásler Miklós Országos Onkológiai Intézet, Budapest Rövidítések AL: utántöltés ( afterloading ) BT: brachyterápia
SUGÁRTERÁPIA SZAKKÉPZÉS KÜLSŐ KÉPZŐHELYI REAKKREDITÁCIÓJA. Szegedi Tudományegyetem Általános Orvostudományi Kar Szak- és Továbbképzési Központ 2013.
 SUGÁRTERÁPIA SZAKKÉPZÉS KÜLSŐ KÉPZŐHELYI REAKKREDITÁCIÓJA Szegedi Tudományegyetem Általános Orvostudományi Kar Szak- és Továbbképzési Központ 2013. SUGÁRTERÁPIA BÁCS-KISKUN MEGYEI ÖNKORMÁNYZAT KÓRHÁZ,
SUGÁRTERÁPIA SZAKKÉPZÉS KÜLSŐ KÉPZŐHELYI REAKKREDITÁCIÓJA Szegedi Tudományegyetem Általános Orvostudományi Kar Szak- és Továbbképzési Központ 2013. SUGÁRTERÁPIA BÁCS-KISKUN MEGYEI ÖNKORMÁNYZAT KÓRHÁZ,
rzások a Dr. Fröhlich Georgina ELTE TTK, Budapest Országos Onkológiai Intézet Sugárterápiás Központ Budapest
 Ionizáló sugárz rzások a gyógy gyításban Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest ELTE TTK, Budapest chopin.web.elte.hu Bevezetés 1. A radioaktivitás alapjai (atomszerkezet,
Ionizáló sugárz rzások a gyógy gyításban Dr. Fröhlich Georgina Országos Onkológiai Intézet Sugárterápiás Központ Budapest ELTE TTK, Budapest chopin.web.elte.hu Bevezetés 1. A radioaktivitás alapjai (atomszerkezet,
(54) Radiográfus (52) Sugárterápiás szakasszisztens (54) Röntgenasszisztens Röntgenasszisztens (52)
 5. KÉPI DIAGNOSZTIKA SZAKMACSOPORT 5.A. Képi diagnosztika 5.E. Radiofarmakológia 5.3. Diagnosztikai képalkotó 5.4. Radio-farmakológiai szakasszisztens 5.5. Radio-farmakológiai szakasszisztens (egészségügyi
5. KÉPI DIAGNOSZTIKA SZAKMACSOPORT 5.A. Képi diagnosztika 5.E. Radiofarmakológia 5.3. Diagnosztikai képalkotó 5.4. Radio-farmakológiai szakasszisztens 5.5. Radio-farmakológiai szakasszisztens (egészségügyi
XIII./5. fejezet: Terápia
 XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
Korszerû sugárterápia: teleterápia
 Korszerû sugárterápia: teleterápia Dr. Fodor János, Dr. Major Tibor, Dr. Kásler Miklós Országos Onkológiai Intézet, Budapest magazin MOTESZ Rövidítések 2D: két dimenzió 3D: három dimenzió 4D: négy dimenzió
Korszerû sugárterápia: teleterápia Dr. Fodor János, Dr. Major Tibor, Dr. Kásler Miklós Országos Onkológiai Intézet, Budapest magazin MOTESZ Rövidítések 2D: két dimenzió 3D: három dimenzió 4D: négy dimenzió
JAVÍTÁSI-ÉRTÉKELÉSI ÚTMUTATÓ. Sugárterápiás szakasszisztens szakképesítés A besugárzás tervezése modul. 1. vizsgafeladat október 10.
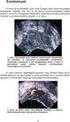 Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
Emberi Erőforrások Minisztériuma Korlátozott terjesztésű! Érvényességi idő: az interaktív vizsgatevékenység befejezésének időpontjáig A minősítő neve: Rauh Edit A minősítő beosztása: mb. főigazgató-helyettes
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában
 Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
3. VIZSGÁLATI EREDMÉNYEK ÉS KÖVETKEZTETÉSEK
 3. VIZSGÁLATI EREDMÉNYEK ÉS KÖVETKEZTETÉSEK 3.1 A craniopharyngeomás ciszták 9o Y besugárzásának eredményei: A craniopharyngeomás ciszták 9o Y besugárzása eredményeinek ismertetése el tt e daganatfajta
3. VIZSGÁLATI EREDMÉNYEK ÉS KÖVETKEZTETÉSEK 3.1 A craniopharyngeomás ciszták 9o Y besugárzásának eredményei: A craniopharyngeomás ciszták 9o Y besugárzása eredményeinek ismertetése el tt e daganatfajta
Koponyaalap-közeli daganatok frakcionált sztereotaxiás sugárkezelése (fsrt)
 Eredeti közlemény 251 Koponyaalap-közeli daganatok frakcionált sztereotaxiás sugárkezelése (fsrt) Horváth Zsolt 1, Bellyei Szabolcs 2, Farkas Róbert 2, Mangel László 2, Kovács Péter 2, Sebestyén Zsolt
Eredeti közlemény 251 Koponyaalap-közeli daganatok frakcionált sztereotaxiás sugárkezelése (fsrt) Horváth Zsolt 1, Bellyei Szabolcs 2, Farkas Róbert 2, Mangel László 2, Kovács Péter 2, Sebestyén Zsolt
PTE-Klinikai Központ- Radiologiai Klinika
 CT vizsgálati protokollok optimalizálásának hatása a diagnosztikus pontosságra és a pácienseket ért sugárterhelésre Dr. Szukits Sándor, Dr. Kékkői László, Dr. Dérczy Katalin PTE-Klinikai Központ- Radiologiai
CT vizsgálati protokollok optimalizálásának hatása a diagnosztikus pontosságra és a pácienseket ért sugárterhelésre Dr. Szukits Sándor, Dr. Kékkői László, Dr. Dérczy Katalin PTE-Klinikai Központ- Radiologiai
Szemeszter 2013.II.félé v. Géresi Enikő Semmelweis Egyetem Továbbképzés i Központ Akkr.pont 50 Országos Onkológiai Helyszíne
 Tanfolyam adatlap Alapadatok Kódszám SE- TK/2013.II/00274 Szemeszter 2013.II.félé v Jelleg Főcím Brachyterápia továbbképző tanfolyam Állapot A tanfolyam akkreditálásra került Szervező Partner Országos
Tanfolyam adatlap Alapadatok Kódszám SE- TK/2013.II/00274 Szemeszter 2013.II.félé v Jelleg Főcím Brachyterápia továbbképző tanfolyam Állapot A tanfolyam akkreditálásra került Szervező Partner Országos
Speciális sugárkezelési módszerek
 Speciális sugárkezelési módszerek Osztályunkon több olyan speciális sugárkezelési eljárást is alkalmazunk, amelyre Magyarországon jelenleg csak nálunk (vagy csak 1-2 intézetben) van lehetőség. Sztereotaxiás
Speciális sugárkezelési módszerek Osztályunkon több olyan speciális sugárkezelési eljárást is alkalmazunk, amelyre Magyarországon jelenleg csak nálunk (vagy csak 1-2 intézetben) van lehetőség. Sztereotaxiás
I. DOZIMETRIAI MENNYISÉGEK ÉS MÉRTÉKEGYSÉGEK
 1 I. DOZIMETRIAI MENNYISÉGEK ÉS MÉRTÉKEGYSÉGEK 1) Iondózis/Besugárzási dózis (ro: Doza de ioni): A leveg egy adott V térfogatában létrejött ionok Q össztöltésének és az adott térfogatban található anyag
1 I. DOZIMETRIAI MENNYISÉGEK ÉS MÉRTÉKEGYSÉGEK 1) Iondózis/Besugárzási dózis (ro: Doza de ioni): A leveg egy adott V térfogatában létrejött ionok Q össztöltésének és az adott térfogatban található anyag
FELSZÍN ALATTI VIZEK RADONTARTALMÁNAK VIZSGÁLATA ISASZEG TERÜLETÉN
 FELSZÍN ALATTI VIZEK RADONTARTALMÁNAK VIZSGÁLATA ISASZEG TERÜLETÉN Készítette: KLINCSEK KRISZTINA környezettudomány szakos hallgató Témavezető: HORVÁTH ÁKOS egyetemi docens ELTE TTK Atomfizika Tanszék
FELSZÍN ALATTI VIZEK RADONTARTALMÁNAK VIZSGÁLATA ISASZEG TERÜLETÉN Készítette: KLINCSEK KRISZTINA környezettudomány szakos hallgató Témavezető: HORVÁTH ÁKOS egyetemi docens ELTE TTK Atomfizika Tanszék
Izotópos méréstechnika, alkalmazási lehetőségek
 Radioizotópok orvosi, gyógyszerészi alkalmazása Izotópos méréstechnika, alkalmazási lehetőségek Dr. Voszka István Az alkalmazás alapja:- A radioaktív izotóp ugyanúgy viselkedik a szervezetben, mint stabil
Radioizotópok orvosi, gyógyszerészi alkalmazása Izotópos méréstechnika, alkalmazási lehetőségek Dr. Voszka István Az alkalmazás alapja:- A radioaktív izotóp ugyanúgy viselkedik a szervezetben, mint stabil
