Klasszikus zika Termodinamika I.
|
|
|
- Tibor Kiss
- 7 évvel ezelőtt
- Látták:
Átírás
1 Klasszikus zika Termodinamika I. Horváth András, SZE GIVK v 0.95 Oktatási célra szabadon terjeszthet Horváth András, SZE GIVK Termodinamika I. v / 35
2 A termodinamika tárgya A termodinamika a testek olyan állapotváltozásaival foglalkozik, melyek h átadáshoz, h mérséklet-változáshoz kapcsolódnak. Horváth András, SZE GIVK Termodinamika I. v / 35
3 A termodinamika tárgya A termodinamika a testek olyan állapotváltozásaival foglalkozik, melyek h átadáshoz, h mérséklet-változáshoz kapcsolódnak. Geometriai, mechanikai mennyiségek: (lásd korábban) térfogat (V ) tömeg (m) s r ség (ϱ) nyomás (p) Horváth András, SZE GIVK Termodinamika I. v / 35
4 A termodinamika tárgya A termodinamika a testek olyan állapotváltozásaival foglalkozik, melyek h átadáshoz, h mérséklet-változáshoz kapcsolódnak. Geometriai, mechanikai mennyiségek: (lásd korábban) térfogat (V ) tömeg (m) s r ség (ϱ) nyomás (p) H tani mennyiségek: h mérséklet (T ) bels energia (E b ) h kapacitás (C ) fajh (c) entrópia (S) A h tani mennyiségek értelmezhet k a részletek ismerete nélkül, de az anyag részecskéinek mozgásán keresztül is. (Pl. a bels energia a részecskék össz mozgási energiája.) Horváth András, SZE GIVK Termodinamika I. v / 35
5 A h mérséklet mérése H érzet: vannak hidegebb és melegebb tárgyak. Hogy lehet ezt mérhet vé, objektívvé tenni? (Ugyanaz az ember is máshogy érzi a h mérsékletet pl. a fáradtság függvényében!) Kis általánosítás: a t z nagyon meleg, mert melegíti a tárgyakat. (A h érzethez túl forró a t z!) Horváth András, SZE GIVK Termodinamika I. v / 35
6 A h mérséklet mérése H érzet: vannak hidegebb és melegebb tárgyak. Hogy lehet ezt mérhet vé, objektívvé tenni? (Ugyanaz az ember is máshogy érzi a h mérsékletet pl. a fáradtság függvényében!) Kis általánosítás: a t z nagyon meleg, mert melegíti a tárgyakat. (A h érzethez túl forró a t z!) Keresni kell tárgyakat, melyek mérhet tulajdonságukat változtatják, ha változik a h mérséklet. Els (és máig használt) ötlet: folyadékok h tágulása. Problémák: méréshatár, eltér ütemben táguló folyadékok. Horváth András, SZE GIVK Termodinamika I. v / 35
7 A h mérséklet mérése Kés bbi h mérsékletet-mérési elvek: gázok h tágulása szilárd testek h tágulása vezet képesség-változás termoelektromos hatás sugárzás intenzitása sugárzás színképe... A gyakorlatban az alkalmazáshoz megfelel en választjuk meg az eszközt. Horváth András, SZE GIVK Termodinamika I. v / 35
8 A h mérséklet mérése Kés bbi h mérsékletet-mérési elvek: gázok h tágulása szilárd testek h tágulása vezet képesség-változás termoelektromos hatás sugárzás intenzitása sugárzás színképe... A gyakorlatban az alkalmazáshoz megfelel en választjuk meg az eszközt. H mérséklet-fogalom pontosítása: Nem is egyszer. Az anyagi tulajdonságok (méret, vezet képesség,...) nem lineárisan függnek a h mérséklett l! Nem tárgyaljuk. Horváth András, SZE GIVK Termodinamika I. v / 35
9 Gyakori h mérséklet-skálák Sok skála volt a történelem során. A két túlél : Celsius-skála: ez a szabványos. A víz fagyáspontja: 0 C, forráspontja: 100 C. Fahrenheit-skála: sok helyen (pl. USA) még használják. Ammónium-klorid-víz keverék: 0 F, emberi testh mérséklet: 100 F. (0 F = 17,8 C, 100 F= 37,8 C.) Horváth András, SZE GIVK Termodinamika I. v / 35
10 Gyakori h mérséklet-skálák Sok skála volt a történelem során. A két túlél : Celsius-skála: ez a szabványos. A víz fagyáspontja: 0 C, forráspontja: 100 C. Fahrenheit-skála: sok helyen (pl. USA) még használják. Ammónium-klorid-víz keverék: 0 F, emberi testh mérséklet: 100 F. (0 F = 17,8 C, 100 F= 37,8 C.) Termodinamikai kutatások: Van legalacsonyabb h mérséklet! Abszolút h mérsékleti skála: Kelvin-skála 0 K: a legalacsonyabb h mérséklet 273,15 K: a víz fagyáspontja normál légköri nyomáson 1 K h mérséklet-változás megfelel 1 C változásnak. T [kelvin] = T [celsius] + 273,15 T [kelvin] = T [celsius] Horváth András, SZE GIVK Termodinamika I. v / 35
11 Mi is az a h mérséklet? Miben különbözik a meleg és a hideg test? Régi válasz: létezik egy folyadékszer h anyag, amib l ha sok van valahol, akkor meleg a test. Valódi válasz: a meleg testek részecskéi gyorsabban mozognak. (Nem volt egyszer rájönni!) Horváth András, SZE GIVK Termodinamika I. v / 35
12 Mi is az a h mérséklet? Miben különbözik a meleg és a hideg test? Régi válasz: létezik egy folyadékszer h anyag, amib l ha sok van valahol, akkor meleg a test. Valódi válasz: a meleg testek részecskéi gyorsabban mozognak. (Nem volt egyszer rájönni!) Egyszer érv: dörzsöléskor h keletkezik. Mechanikai munkavégzéssel h mérsékletet emelhetünk. Horváth András, SZE GIVK Termodinamika I. v / 35
13 Mi is az a h mérséklet? Miben különbözik a meleg és a hideg test? Régi válasz: létezik egy folyadékszer h anyag, amib l ha sok van valahol, akkor meleg a test. Valódi válasz: a meleg testek részecskéi gyorsabban mozognak. (Nem volt egyszer rájönni!) Egyszer érv: dörzsöléskor h keletkezik. Mechanikai munkavégzéssel h mérsékletet emelhetünk. Igaz a fordítottja? H mérséklet-csökkenéssel munkához juthatunk? Igen, de korlátokkal. Lásd a h er gépekr l szóló részt. Horváth András, SZE GIVK Termodinamika I. v / 35
14 A bels energia Tapasztalat: a testeken végzett munka a testek belsejében összegy lik. Egy test két állapota közti bels energiakülönbségnek nevezzük azt a munkamennyiséget, amellyel az egyikb l a másikba átvihet, ha közben a test a környezetével nem cserél h t. Horváth András, SZE GIVK Termodinamika I. v / 35
15 A bels energia Tapasztalat: a testeken végzett munka a testek belsejében összegy lik. Egy test két állapota közti bels energiakülönbségnek nevezzük azt a munkamennyiséget, amellyel az egyikb l a másikba átvihet, ha közben a test a környezetével nem cserél h t. Mikroszkopikusan: a bels energia a test mikroszkopikus részecskéinek összesített mozgási energiája. A bels energiát azért nem mechanikai energiaként észleljük, mert: túl kicsik a részecskék (atomok, molekulák) túl sok van bel lük a mozgás rendezetlen Horváth András, SZE GIVK Termodinamika I. v / 35
16 A h átadás Egy test bels energiáját úgy is növelhetjük, ha magasabb h mérséklet testtel hozzuk kapcsolatba. Ilyenkor makroszkópikus szinten nem látszik semmi, csak a melegebb test gyorsabban mozgó részecskéi rendezetlen mozgásukból adnak át energiát a hidegebbnek. Horváth András, SZE GIVK Termodinamika I. v / 35
17 A h átadás Egy test bels energiáját úgy is növelhetjük, ha magasabb h mérséklet testtel hozzuk kapcsolatba. Ilyenkor makroszkópikus szinten nem látszik semmi, csak a melegebb test gyorsabban mozgó részecskéi rendezetlen mozgásukból adnak át energiát a hidegebbnek. (A h átadás módjairól egy kés bbi fejezet szól.) Horváth András, SZE GIVK Termodinamika I. v / 35
18 A termodinamika I. f tétele Egy test bels energiájának megváltozása ( E ) a küls er k munkavégzésének (W ) és az átadott h nek (Q) az összege: E = Q + W Horváth András, SZE GIVK Termodinamika I. v / 35
19 A termodinamika I. f tétele Egy test bels energiájának megváltozása ( E ) a küls er k munkavégzésének (W ) és az átadott h nek (Q) az összege: E = Q + W El jel-konvenció: A mennyiségeket akkor vesszük pozitívnak, ha a test energiáját növelik. (Nem minden könyv veszi így!) Ez tulajdonképpen az energiamegmaradás egy olyan alakja, melyben a makroszkópikus és mikroszkópikus energiaátadás külön van választva. Horváth András, SZE GIVK Termodinamika I. v / 35
20 Ideális gázok állapotegyenlete Állapotegyenlet: termodinamikai változók közti kapcsolat. Meggyelés: ritka gázokra jó közelítéssel igaz, hogy pv = nrt ahol p a nyomás, V a térfogat, n a mólszám, R = 8,31 J/(mol K) az univerzális gázállandó, T a h mérséklet kelvinben. (Ezekb l a mérésekb l jöttek rá az abszolút 0 fok létezésére.) Horváth András, SZE GIVK Termodinamika I. v / 35
21 Ideális gázok állapotegyenlete Állapotegyenlet: termodinamikai változók közti kapcsolat. Meggyelés: ritka gázokra jó közelítéssel igaz, hogy pv = nrt ahol p a nyomás, V a térfogat, n a mólszám, R = 8,31 J/(mol K) az univerzális gázállandó, T a h mérséklet kelvinben. (Ezekb l a mérésekb l jöttek rá az abszolút 0 fok létezésére.) Az n mólszámot kémiai mérésekb l állapították meg. (A mól annak a rendszernek anyagmennyisége, amely annyi elemi egységet tartalmaz, mint ahány atom van 0,012 kg szén-12-izotópban.) Horváth András, SZE GIVK Termodinamika I. v / 35
22 Ideális gázok állapotegyenlete másképpen 1. A gázok kis részecskékb l (molekulák, atomok) állnak. 1 mól megfelel N A = 6, db részecskének. N A neve: Avogadro-szám. N = n N A Horváth András, SZE GIVK Termodinamika I. v / 35
23 Ideális gázok állapotegyenlete másképpen 1. A gázok kis részecskékb l (molekulák, atomok) állnak. 1 mól megfelel N A = 6, db részecskének. N A neve: Avogadro-szám. N = n N A Ezzel az ideális gázok állapotegyenlete: pv = nrt = N N A RT = N R N A T Horváth András, SZE GIVK Termodinamika I. v / 35
24 Ideális gázok állapotegyenlete másképpen 1. A gázok kis részecskékb l (molekulák, atomok) állnak. 1 mól megfelel N A = 6, db részecskének. N A neve: Avogadro-szám. N = n N A Ezzel az ideális gázok állapotegyenlete: pv = nrt = N N A RT = N R N A T pv = NkT ahol k = R/N A = 1, J/K a Boltzmann-állandó. Ez egyenérték a pv = nrt -vel, csak hol ezt, hol azt kényelmes használni. Horváth András, SZE GIVK Termodinamika I. v / 35
25 Ideális gázok állapotegyenlete másképpen 2. Érdemes lehet néha a gáz m tömegét direktbe bevezetni. Nyilván n = m/m, ahol M a relatív móltömeg, azaz 1 mol anyag tömege. Így az állapotegyenlet másik alakja: pv = m M RT vagy s r séggel: p = m V RT M = ϱrt M. Horváth András, SZE GIVK Termodinamika I. v / 35
26 Ideális gázok állapotegyenlete másképpen 2. Érdemes lehet néha a gáz m tömegét direktbe bevezetni. Nyilván n = m/m, ahol M a relatív móltömeg, azaz 1 mol anyag tömege. Így az állapotegyenlet másik alakja: pv = m M RT vagy s r séggel: p = m V RT M = ϱrt M. Az M relatív móltömeg táblázatokból vehet. Pl. H 2 gázra 2 g/mol, N 2 -re 28 g/mol,... Horváth András, SZE GIVK Termodinamika I. v / 35
27 Ideális gázok: egyszer sített törvények Az állapotegyenletb l következik, hogy: Állandó h mérsékleten, adott mennyiség gázra pv =áll. (Boyle-Mariotte-törvény.) Állandó térfogaton, adott mennyiség gázra p/t =áll. (Gay-Lussac I. törvénye.) Állandó nyomáson, adott mennyiség gázra V /T =áll. (Gay-Lussac II. törvénye.)... Mind következik az állapotegyenletb l. (Általános gáztörvény) Horváth András, SZE GIVK Termodinamika I. v / 35
28 Ideális gázok: egyszer sített törvények Az állapotegyenletb l következik, hogy: Állandó h mérsékleten, adott mennyiség gázra pv =áll. (Boyle-Mariotte-törvény.) Állandó térfogaton, adott mennyiség gázra p/t =áll. (Gay-Lussac I. törvénye.) Állandó nyomáson, adott mennyiség gázra V /T =áll. (Gay-Lussac II. törvénye.)... Mind következik az állapotegyenletb l. (Általános gáztörvény) Tipikus elrendezés: dugattyúval bezárt gáz változásai. Bezárt gáz mennyisége állandó. Nyomás, térfogat,...: a falaktól és a dugattyútól függ. Horváth András, SZE GIVK Termodinamika I. v / 35
29 Ideális gázok: fontos állapotváltozások 1. Izoterm állapotvált. Izo=azonos, term=h mérséklet. Jó h vezet falú tartály és kell en lassú változás esetén a bezárt gáz h mérséklete állandó marad. pv = áll. Változások oka: küls munkavégzés a dugattyún. Horváth András, SZE GIVK Termodinamika I. v / 35
30 Ideális gázok: fontos állapotváltozások 1. Izoterm állapotvált. Izo=azonos, term=h mérséklet. Jó h vezet falú tartály és kell en lassú változás esetén a bezárt gáz h mérséklete állandó marad. pv = áll. Változások oka: küls munkavégzés a dugattyún. Izobár állapotvált. bár=nyomás. Szabadon mozgó dugattyú esetén a bezárt gáz nyomása állandó marad. V /T = áll. Változások oka: küls h átadás. Horváth András, SZE GIVK Termodinamika I. v / 35
31 Ideális gázok: fontos állapotváltozások 2. Izochor állapotvált. chor=térfogat. Rögzített dugattyú esetén a gáz térfogata állandó marad. p/t = áll. Változások oka: küls h átadás. Horváth András, SZE GIVK Termodinamika I. v / 35
32 Ideális gázok: fontos állapotváltozások 2. Izochor állapotvált. chor=térfogat. Rögzített dugattyú esetén a gáz térfogata állandó marad. p/t = áll. Változások oka: küls h átadás. Adiabatikus állapotvált. h átadás nélküli. Jó h szigetel tartály, dugattyú és gyors változás esetén a gáz nem kap h t kívülr l. pv κ = áll. Változások oka: küls munkavégzés a dugattyún. Bizonyítás kés bb. Horváth András, SZE GIVK Termodinamika I. v / 35
33 Egyszer állapotváltozások a pv diagramon Igen fontos eszköz: térfogat függvényében ábrázolni a nyomást. Horváth András, SZE GIVK Termodinamika I. v / 35
34 Munkavégzés gázokon (Korábbról: párhuzamos er és elmozdulás esetén: W = F r.) Egyszer eset: dugattyúval lezárt tartály, állandó nyomás. Horváth András, SZE GIVK Termodinamika I. v / 35
35 Munkavégzés gázokon (Korábbról: párhuzamos er és elmozdulás esetén: W = F r.) Egyszer eset: dugattyúval lezárt tartály, állandó nyomás. A gáz munkája: W g = F x Horváth András, SZE GIVK Termodinamika I. v / 35
36 Munkavégzés gázokon (Korábbról: párhuzamos er és elmozdulás esetén: W = F r.) Egyszer eset: dugattyúval lezárt tartály, állandó nyomás. A gáz munkája: Er és gáz nyomás: W g = (pa) x = W g = F x F = pa Horváth András, SZE GIVK Termodinamika I. v / 35
37 Munkavégzés gázokon (Korábbról: párhuzamos er és elmozdulás esetén: W = F r.) Egyszer eset: dugattyúval lezárt tartály, állandó nyomás. A gáz munkája: Er és gáz nyomás: W g = F x F = pa W g = (pa) x = p(a x) = p V. A környezet ennek 1-szeresét végzi a gázon: W = p V Horváth András, SZE GIVK Termodinamika I. v / 35
38 Munkavégzés gázokon (Korábbról: párhuzamos er és elmozdulás esetén: W = F r.) Egyszer eset: dugattyúval lezárt tartály, állandó nyomás. A gáz munkája: Er és gáz nyomás: W g = F x F = pa W g = (pa) x = p(a x) = p V. A környezet ennek 1-szeresét végzi a gázon: W = p V Ha a nyomás nem állandó, akkor kis szakaszokra bontjuk és összegezzük: V2 W = p(v )dv V 1 Horváth András, SZE GIVK Termodinamika I. v / 35
39 Munkavégzés a pv diagramon Az el z egyenlet szemléletes jelentése: A munkavégzés nagysága a pv diagram grakon alatti területével egyezik meg. El jel rendben: ha V n, akkor tágul a gáz, tehát végez munkát a környezetén. Azaz: V > 0 azt eredményezi, hogy W < 0 lesz. Horváth András, SZE GIVK Termodinamika I. v / 35
40 H kapacitás, fajh, moláris h kapacitás Ha h t közlünk a gázzal, akkor annak h mérséklete emelkedni fog. A kett arányát fejezi ki a h kapacitás: C = Q T Horváth András, SZE GIVK Termodinamika I. v / 35
41 H kapacitás, fajh, moláris h kapacitás Ha h t közlünk a gázzal, akkor annak h mérséklete emelkedni fog. A kett arányát fejezi ki a h kapacitás: C = Q T A h kapacitás nyilván egyenesen arányos az anyagmennyiséggel. Érdemes az egységnyi mennyiségre vonatkozó h kapacitásokat elnevezni: Fajh : a h kapacitás és a tömeg hányadosa. c = C m = Q m T Moláris h kapacitás: (molh ) a h kapacitás és a mólszám hányadosa. c m = C n = Q n T Horváth András, SZE GIVK Termodinamika I. v / 35
42 H kapacitás: állandó nyomáson vagy térfogaton? Az I. f tétel miatt nem mindegy, hogy milyen körülmények közt történik a melegítés. Állandó térfogaton nincs tágulás: minden h a bels energiát növeli. Q V = E Állandó nyomáson a melegített gáz tágul: a h egy része tágulási munkává alakul. Q p = E W = E + p V Horváth András, SZE GIVK Termodinamika I. v / 35
43 H kapacitás: állandó nyomáson vagy térfogaton A h kapacitás is eltér a két esetben: C p = Q p T C V = Q V T = E T = E + p V T = C V + p V T Horváth András, SZE GIVK Termodinamika I. v / 35
44 H kapacitás: állandó nyomáson vagy térfogaton A h kapacitás is eltér a két esetben: C p = Q p T C V = Q V T = E T = E + p V T = C V + p V T Az állapotegyenletb l: V = nrt /p, ezért ha p állandó: V / T = nr/p Horváth András, SZE GIVK Termodinamika I. v / 35
45 H kapacitás: állandó nyomáson vagy térfogaton A h kapacitás is eltér a két esetben: C p = Q p T C V = Q V T = E T = E + p V T = C V + p V T Az állapotegyenletb l: V = nrt /p, ezért ha p állandó: V / T = nr/p Így az állandó nyomáson vett h kapacitás: C p = C V + nr = C V + Nk Horváth András, SZE GIVK Termodinamika I. v / 35
46 H kapacitás: állandó nyomáson vagy térfogaton A h kapacitás is eltér a két esetben: C p = Q p T C V = Q V T = E T = E + p V T = C V + p V T Az állapotegyenletb l: V = nrt /p, ezért ha p állandó: V / T = nr/p Így az állandó nyomáson vett h kapacitás: C p = C V + nr = C V + Nk Az eltérés érthet : ha állandó nyomáson melegítünk egy gázt, akkor az tágul, azaz a bevitt h egy része nem a bels energiát növeli, hanem melegít. (H b l munka! H er gép? :-) Csak a tágulás idejére... :-( ) Horváth András, SZE GIVK Termodinamika I. v / 35
47 Fajh és moláris fajh : állandó nyomáson vagy térfogaton Egységnyi tömegre: c p = c V + n m R = c V + R M Egy mólra: c m,p = c m,v + R Ezek a korábbiakból következnek, csak néha egyszer bb így számolni. Horváth András, SZE GIVK Termodinamika I. v / 35
48 További estek Állandó h mérsékleten vett h kapacitás? Nincs értelme! Fizikailag sem és matematikailag sem (nevez ben 0.) Horváth András, SZE GIVK Termodinamika I. v / 35
49 További estek Állandó h mérsékleten vett h kapacitás? Nincs értelme! Fizikailag sem és matematikailag sem (nevez ben 0.) Adiabatikus h kapacitás? 0, hisz Q = 0. Nincs értelme bevezetni. Horváth András, SZE GIVK Termodinamika I. v / 35
50 További estek Állandó h mérsékleten vett h kapacitás? Nincs értelme! Fizikailag sem és matematikailag sem (nevez ben 0.) Adiabatikus h kapacitás? 0, hisz Q = 0. Nincs értelme bevezetni. Speciális alkalmazások: Néha felmerül, hogy nem V vagy p állandó, hanem más mennyiség. Ilyenkor speciális h kapacitás, fajh, moláris fajh fogalmak jönnek el. Horváth András, SZE GIVK Termodinamika I. v / 35
51 Ideális gázok fajh értékei Pontos érték: méréssel. A legtöbb gáz esetén jó közelítés: c m,v = f 2 R, c m,p = f R Egyatomos gázok (He, Ne, Ar,...): f = 3 Kétatomos gázok (O 2, N 2, H 2,...): f = 5 Bonyolultabb molekulák (H 2 O, NH 3, diesel-üzemanyag): f 6 Ebb l a h kapacitás, fajh könnyen meghatározható. C = c m n, c = C m = c n m m = c m M Horváth András, SZE GIVK Termodinamika I. v / 35
52 Ideális gázok fajh értékei Pontos érték: méréssel. A legtöbb gáz esetén jó közelítés: c m,v = f 2 R, c m,p = f R Egyatomos gázok (He, Ne, Ar,...): f = 3 Kétatomos gázok (O 2, N 2, H 2,...): f = 5 Bonyolultabb molekulák (H 2 O, NH 3, diesel-üzemanyag): f 6 Ebb l a h kapacitás, fajh könnyen meghatározható. C = c m n, c = C m = c n m m = c m M Miért ilyen a törvény? Rövidesen meglátjuk... Horváth András, SZE GIVK Termodinamika I. v / 35
53 Az adiabatikus állapotváltozás Adiabatikus állapotvált. Q = 0, E = W Jó h szigetelés, gyors változás. Ha s rítjük, akkor az izoterm változáshoz képest gyorsabban n a nyomás. Ok: nemcsak kisebb helyre lesz szorítva a gáz, hanem a h mérséklete is n! Levezetés nélkül: pv κ = áll., TV κ 1 = áll., κ = c p c V adiabata κ neve: specikus fajh hányados. A fentiek alapján: izotermák κ = f + 2 f Horváth András, SZE GIVK Termodinamika I. v / 35
54 A politropikus állapotváltozás Gyakorlatban nincs ideális adiabatikus állapotváltozás: mindig van kicsi h csere. A változás hasonló az adiabatikushoz, de más a kitev : Sok korábbi esetet visszaad: n=1,2 pv n = áll., TV n 1 = áll. izochor n=-1/2 n=0 n=1.4 n=1 n=oo n=-1/2 n=1.2 n neve: politropikus index. n = 0: izobár n = 1: izoterm n = κ: adiabatikus n = : izochor adiabata izobár izoterm Vigyázat! Ne keverjük ezt az n-et a mólszámmal! Horváth András, SZE GIVK Termodinamika I. v / 35
55 Molekuláris modell A gázok f bb tulajdonságai megérthet k az alábbi feltevésekkel: A gázok kicsi részecskékb l (atomokból, molekulákból) állnak, melyek ritkán ütköznek a fallal és egymással. A falnak átadott lendületb l származik a gáz nyomása. A bels energia a gázrészecskék energiájának összege. Horváth András, SZE GIVK Termodinamika I. v / 35
56 Molekuláris modell A gázok f bb tulajdonságai megérthet k az alábbi feltevésekkel: A gázok kicsi részecskékb l (atomokból, molekulákból) állnak, melyek ritkán ütköznek a fallal és egymással. A falnak átadott lendületb l származik a gáz nyomása. A bels energia a gázrészecskék energiájának összege. A pontos tárgyalás a statisztikus zika eszköztárát igényli, de sok fontos összefüggés levezethet elemi eszközökkel. Csak az átlagos értékeket fogjuk kiszámolni. Horváth András, SZE GIVK Termodinamika I. v / 35
57 Molekuláris modell: a gáz (átlagos) nyomása Molekulák tömege m 1, átlagos sebességnagysága x irányban: v x Ütközés a falon: p l = 2m 1 v x lendületátadás. Két ütközés közti id : t = 2l x /v x. Horváth András, SZE GIVK Termodinamika I. v / 35
58 Molekuláris modell: a gáz (átlagos) nyomása Molekulák tömege m 1, átlagos sebességnagysága x irányban: v x Ütközés a falon: p l = 2m 1 v x lendületátadás. Két ütközés közti id : t = 2l x /v x. 1 molekula átlagos ereje a falra: F 1 = p l t = m 1v 2 x l x Horváth András, SZE GIVK Termodinamika I. v / 35
59 Molekuláris modell: a gáz (átlagos) nyomása Molekulák tömege m 1, átlagos sebességnagysága x irányban: v x Ütközés a falon: p l = 2m 1 v x lendületátadás. Két ütközés közti id : t = 2l x /v x. 1 molekula átlagos ereje a falra: F 1 = p l t = m 1v 2 x l x Ennek megfelel átlagnyomás: p 1 = F 1 A = m 1v 2 x l x A = m 1v 2 x V Horváth András, SZE GIVK Termodinamika I. v / 35
60 Molekuláris modell: a gáz (átlagos) nyomása Ha nem 1, hanem N db hasonló molekulánk van: azaz: p = p 1 N = N V m 1v 2 x pv = N m 1 v 2 x (Az átlagolást lehagytuk, mert a gyakorlatban N olyan nagy, hogy az átlagtól való eltérés elhanyagolható.) Horváth András, SZE GIVK Termodinamika I. v / 35
61 Molekuláris modell: a gáz (átlagos) nyomása Ha nem 1, hanem N db hasonló molekulánk van: azaz: p = p 1 N = N V m 1v 2 x pv = N m 1 v 2 x (Az átlagolást lehagytuk, mert a gyakorlatban N olyan nagy, hogy az átlagtól való eltérés elhanyagolható.) Ez nagyon hasonlít az egyetemes gáztörvényre! Ha a molekulák átlagos mozgássebessége állandó, akkor pv /N =állandó. Egyezés, ha: m 1 v 2 x = kt. A h mérséklet egyenesen arányos a molekulák átlagsebességének négyzetével. Horváth András, SZE GIVK Termodinamika I. v / 35
62 Az ekvipartíció tétele Az el z egyenletben a mozgási energiához hasonló fogalmat fedezhetünk fel: 1 2 kt = 1 2 m 1v 2 x = E 1,x azaz az x irányú mozgásban a molekula (átlagosan) kt /2 energiát tárol. Nyilván ugyanez van y és z irányban is. A molekulák azonban nemcsak mozoghatnak (transzláció), hanem foroghatnak (rotáció) is! Ezek egymástól függetlenül történnek. Horváth András, SZE GIVK Termodinamika I. v / 35
63 Az ekvipartíció tétele Az el z egyenletben a mozgási energiához hasonló fogalmat fedezhetünk fel: 1 2 kt = 1 2 m 1v 2 x = E 1,x azaz az x irányú mozgásban a molekula (átlagosan) kt /2 energiát tárol. Nyilván ugyanez van y és z irányban is. A molekulák azonban nemcsak mozoghatnak (transzláció), hanem foroghatnak (rotáció) is! Ezek egymástól függetlenül történnek. Fontos fogalom: Egy rendszer szabadsági fokainak nevezzük a többit l független energiatárolási lehet ségeket. (Példák kés bb.) Bebizonyítható az ekvipartíció tétele: A testek egyensúlyi állapotban minden szabadsági fokon átlagosan kt /2 energiát tárolnak. Horváth András, SZE GIVK Termodinamika I. v / 35
64 Az ekvipartíció tétele: szabadsági fokszámok A molekulák szabadsági fokszáma szerkezetükt l függ. Horváth András, SZE GIVK Termodinamika I. v / 35
65 Az ekvipartíció tétele: szabadsági fokszámok A molekulák szabadsági fokszáma szerkezetükt l függ. Molekulánként f szabadsági fok esetén az N atomos gáznak Nf szabadsági foka van, ezért össz bels energiája: E = Nf 1 2 kt = f 2 NkT = f 2 nrt így moláris h kapacitása állandó térfogaton: (ua., mint fentebb) c m,v = 1 n E T = f 2 R Most már értjük, hogy a korábbi f az 1 molekula szabadsági fokszáma. Horváth András, SZE GIVK Termodinamika I. v / 35
66 A szabadsági fokokról A legtöbb egyszer molekulánál a fenti 3, 5 vagy 6 érték valósul meg. Kvantummechanika: egy rezgés beindításának van egy minimális energiája. Ha ez a minimális energia meghaladja kt /2-t, az a rezgés nem indul be. Horváth András, SZE GIVK Termodinamika I. v / 35
67 A szabadsági fokokról A legtöbb egyszer molekulánál a fenti 3, 5 vagy 6 érték valósul meg. Kvantummechanika: egy rezgés beindításának van egy minimális energiája. Ha ez a minimális energia meghaladja kt /2-t, az a rezgés nem indul be. Általános név: A szabadsági fokok befagyása. Elmélete bonyolult. a transzlációs szab. fokok sosem fagynak be a rotációs szab. fokok többnyire K alatt fagynak be a rezgési szab. fokok K alatt fagynak be. A legtöbb molekula szobah mérsékleten csak transzlációban és rotációban tárol energiát. (De vannak kivételek és pár száz fokon már sok a rezgési szab. fok is.) Horváth András, SZE GIVK Termodinamika I. v / 35
68 Következmények Egy molekula átlagsebessége v, de ez 3 irányú transzlációból tev dik össze: v 2 = v 2 x + v 2 y + v 2 z. Ezért az (átlagos) össz mozgási energia az ekvipartíció tétel miatt: E 1 = 1 2 m 1v 2 = 1 2 m 1v 2 x m 1v 2 y m 1v 2 z = E 1,x + E 2,x + E 3,x = 3 2 kt Horváth András, SZE GIVK Termodinamika I. v / 35
69 Következmények Egy molekula átlagsebessége v, de ez 3 irányú transzlációból tev dik össze: v 2 = v 2 x + v 2 y + v 2 z. Ezért az (átlagos) össz mozgási energia az ekvipartíció tétel miatt: E 1 = 1 2 m 1v 2 = 1 2 m 1v 2 x m 1v 2 y m 1v 2 z = E 1,x + E 2,x + E 3,x = 3 2 kt Innen a molekulák átlagsebessége: 3kT 3RT v = = m 1 M Horváth András, SZE GIVK Termodinamika I. v / 35
70 A hangsebesség és a molekulák mozgása A fentieket N 2 molekulákra 300 K-en alkalmazva: v = 517 m/s. Ez nem véletlenül esik a 300 K-en érvényes hangsebesség nagyságrendjébe! A hangot, azaz a leveg beli s r södést-ritkulást a molekulák adják tovább. A hangsebesség azért kisebb ennél, mert a molekulák nem rendezetten, egy irányban haladnak. Horváth András, SZE GIVK Termodinamika I. v / 35
71 A hangsebesség és a molekulák mozgása A fentieket N 2 molekulákra 300 K-en alkalmazva: v = 517 m/s. Ez nem véletlenül esik a 300 K-en érvényes hangsebesség nagyságrendjébe! A hangot, azaz a leveg beli s r södést-ritkulást a molekulák adják tovább. A hangsebesség azért kisebb ennél, mert a molekulák nem rendezetten, egy irányban haladnak. Érdekesség: v = 3RT /M-b l látszik, hogy: v egyenesen arányos T -vel, azaz hidegben lassabban mennek a molekulák és kisebb a hangsebesség is. v fordítottan arányos M-mel, azaz nagyobb móltömeg gázban (nehezebb molekulák) kisebb a hangsebesség. Horváth András, SZE GIVK Termodinamika I. v / 35
72 A hangsebesség és az információ átadási sebesség A fentiek következménye: A gázon belül minden változás hangsebességgel adódik tovább. Horváth András, SZE GIVK Termodinamika I. v / 35
73 A hangsebesség és az információ átadási sebesség A fentiek következménye: A gázon belül minden változás hangsebességgel adódik tovább. Példák: Egy álló dugattyú megmozdításának hatása nem egyb l érz dik a tartályban, hanem hangsebességgel halad a változás. Egy nyíláson át vákuumba legfeljebb hangsebességgel áramlik ki a gáz. Ezek hatással vannak a mérnöki gyakorlatra: Gyors változások nem egyb l éreztetik hatásukat a rendszer távoli részein. Nyomáskülönbséggel csak hangsebességig tudom a gázt gyorsítani. (Bels égés motoroknál, kipufogórendszernél,... ezek jelentkeznek.) Horváth András, SZE GIVK Termodinamika I. v / 35
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
FIZIKA I. Ez egy gázos előadás lesz! (Ideális gázok hőtana) Dr. Seres István
 Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Ez egy gázos előadás lesz! ( hőtana) Dr. Seres István Kinetikus gázelmélet gáztörvények Termodinamikai főtételek fft.szie.hu 2 Seres.Istvan@gek.szie.hu Kinetikus gázelmélet Az ideális gáz állapotjelzői:
Digitális tananyag a fizika tanításához
 Digitális tananyag a izika tanításához Gázok állaotjelzői Adott mennyiségű gáz állaotjelzői: Nyomás: []=Pa=N/m Térogat []=m 3 Hőmérséklet [T]=K; A gázok állaotát megadó egyéb mennyiségek: tömeg: [m]=g
Digitális tananyag a izika tanításához Gázok állaotjelzői Adott mennyiségű gáz állaotjelzői: Nyomás: []=Pa=N/m Térogat []=m 3 Hőmérséklet [T]=K; A gázok állaotát megadó egyéb mennyiségek: tömeg: [m]=g
Klasszikus zika Termodinamika III.
 Klasszikus zika Termodinamika III. Horváth András, SZE GIVK v 0.9 Oktatási célra szabadon terjeszthet 1 / 24 Ismétlés Mi is az az entrópia? Alapötlet Egy izotermán belül mozogva nincs bels energia változás.
Klasszikus zika Termodinamika III. Horváth András, SZE GIVK v 0.9 Oktatási célra szabadon terjeszthet 1 / 24 Ismétlés Mi is az az entrópia? Alapötlet Egy izotermán belül mozogva nincs bels energia változás.
Hőtan I. főtétele tesztek
 Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan I. főtétele tesztek. álassza ki a hamis állítást! a) A termodinamika I. főtétele a belső energia változása, a hőmennyiség és a munka között állaít meg összefüggést. b) A termodinamika I. főtétele
Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői
 Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői Hőmérséklet Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála: 0 ºC pontja
Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői Hőmérséklet Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála: 0 ºC pontja
Mivel foglalkozik a hőtan?
 Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
Hőtan Gáztörvények Mivel foglalkozik a hőtan? A hőtan a rendszerek hőmérsékletével, munkavégzésével, és energiájával foglalkozik. A rendszerek stabilitása áll a fókuszpontjában. Képes megválaszolni a kérdést:
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK
 ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
ÖSSZEFOGLALÁS HŐTANI FOLYAMATOK HŐTÁGULÁS lineáris (hosszanti) hőtágulási együttható felületi hőtágulási együttható megmutatja, hogy mennyivel változik meg a test hossza az eredeti hosszához képest, ha
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (korlátok) Fókusz: a légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gázegyenlet és általánosított gázegyenlet 5-4 A tökéletes gázegyenlet alkalmazása 5-5 Gáz reakciók 5-6 Gázkeverékek
Gázok. 5-7 Kinetikus gázelmélet 5-8 Reális gázok (limitációk) Fókusz Légzsák (Air-Bag Systems) kémiája
 Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
Gázok 5-1 Gáznyomás 5-2 Egyszerű gáztörvények 5-3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet 5-4 A tökéletes gáz egyenlet alkalmazása 5-5 Gáz halmazállapotú reakciók
A gáz halmazállapot. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
A gáz halmazállapot A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 0 Halmazállapotok, állapotjelzők Az anyagi rendszerek a részecskék közötti kölcsönhatásoktól és az állapotjelzőktől függően
1. Feladatok a termodinamika tárgyköréből
 . Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással.. Feladat: (HN 9A-5) Egy épület téglafalának mérete: 4 m 0 m és, a fal 5 cm vastag. A hővezetési együtthatója λ = 0,8 W/m K. Mennyi
Termodinamika. Belső energia
 Termodinamika Belső energia Egy rendszer belső energiáját az alkotó részecskék mozgási energiájának és a részecskék közötti kölcsönhatásból származó potenciális energiák teljes összegeként határozhatjuk
Termodinamika Belső energia Egy rendszer belső energiáját az alkotó részecskék mozgási energiájának és a részecskék közötti kölcsönhatásból származó potenciális energiák teljes összegeként határozhatjuk
Belső energia, hőmennyiség, munka Hőtan főtételei
 Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
Belső energia, hőmennyiség, munka Hőtan főtételei Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak.
Termodinamika (Hőtan)
 Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Termodinamika (Hőtan) Termodinamika A hőtan nagyszámú részecskéből (pl. gázmolekulából) álló makroszkópikus rendszerekkel foglalkozik. A nagy számok miatt érdemes a mólt bevezetni, ami egy Avogadro-számnyi
Egy részecske mozgási energiája: v 2 3 = k T, ahol T a gáz hőmérséklete Kelvinben 2 2 (k = 1, J/K Boltzmann-állandó) Tehát a gáz hőmérséklete
 Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
Hőtan III. Ideális gázok részecske-modellje (kinetikus gázmodell) Az ideális gáz apró pontszerű részecskékből áll, amelyek állandó, rendezetlen mozgásban vannak. Rugalmasan ütköznek egymással és a tartály
Atomok. szilárd. elsődleges kölcsönhatás. kovalens ionos fémes. gázok, folyadékok, szilárd anyagok. ionos fémek vegyületek ötvözetek
 Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Légköri termodinamika
 Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Légköri termodinamika Termodinamika: a hőegyensúllyal, valamint a hőnek, és más energiafajtáknak kölcsönös átalakulásával foglalkozó tudományág. Meteorológiai vonatkozása ( a légkör termodinamikája): a
Termodinamika. 1. rész
 Termodinamika 1. rész 1. Alapfogalmak A fejezet tartalma FENOMENOLÓGIAI HŐTAN a) Hőmérsékleti skálák (otthoni feldolgozással) b) Hőtágulások (otthoni feldolgozással) c) A hőmérséklet mérése, hőmérők (otthoni
Termodinamika 1. rész 1. Alapfogalmak A fejezet tartalma FENOMENOLÓGIAI HŐTAN a) Hőmérsékleti skálák (otthoni feldolgozással) b) Hőtágulások (otthoni feldolgozással) c) A hőmérséklet mérése, hőmérők (otthoni
1. előadás. Gáztörvények. Fizika Biofizika I. 2015/2016. Kapcsolódó irodalom:
 1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
1. előadás Gáztörvények Kapcsolódó irodalom: Fizikai-kémia I: Kémiai Termodinamika(24-26 old) Chemical principles: The quest for insight (Atkins-Jones) 6. fejezet Kapcsolódó multimédiás anyag: Youtube:
Termodinamikai bevezető
 Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Termodinamikai bevezető Alapfogalmak Termodinamikai rendszer: Az univerzumnak az a részhalmaza, amit egy termodinamikai vizsgálat során vizsgálunk. Termodinamikai környezet: Az univerzumnak a rendszeren
Értékelési útmutató az emelt szint írásbeli feladatsorhoz
 Értékelési útmutató az emelt szint írásbeli feladatsorhoz 1. C 1 pont 2. B 1 pont 3. D 1 pont 4. B 1 pont 5. C 1 pont 6. A 1 pont 7. B 1 pont 8. D 1 pont 9. A 1 pont 10. B 1 pont 11. B 1 pont 12. B 1 pont
Értékelési útmutató az emelt szint írásbeli feladatsorhoz 1. C 1 pont 2. B 1 pont 3. D 1 pont 4. B 1 pont 5. C 1 pont 6. A 1 pont 7. B 1 pont 8. D 1 pont 9. A 1 pont 10. B 1 pont 11. B 1 pont 12. B 1 pont
Fizika feladatok. 1. Feladatok a termodinamika tárgyköréből november 28. Hővezetés, hőterjedés sugárzással. Ideális gázok állapotegyenlete
 Fizika feladatok 2014. november 28. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-23) Határozzuk meg egy 20 cm hosszú, 4 cm átmérőjű hengeres vörösréz
Fizika feladatok 2014. november 28. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-23) Határozzuk meg egy 20 cm hosszú, 4 cm átmérőjű hengeres vörösréz
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás Hőáramlás (konvekció) olyan folyamat,
 2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
2. A hőátadás formái és törvényei 2. A hőátadás formái Tapasztalat: tűz, füst, meleg edény füle, napozás. 2.1. Hőáramlás (konvekció) olyan folyamat, amelynek során a hő a hordozóközeg áramlásával kerül
Elméleti kérdések 11. osztály érettségire el ı készít ı csoport
 Elméleti kérdések 11. osztály érettségire el ı készít ı csoport MECHANIKA I. 1. Definiálja a helyvektort! 2. Mondja meg mit értünk vonatkoztatási rendszeren! 3. Fogalmazza meg kinematikailag, hogy mikor
Elméleti kérdések 11. osztály érettségire el ı készít ı csoport MECHANIKA I. 1. Definiálja a helyvektort! 2. Mondja meg mit értünk vonatkoztatási rendszeren! 3. Fogalmazza meg kinematikailag, hogy mikor
Az előadás vázlata: Állapotjelzők: Állapotjelzők: Állapotjelzők: Állapotjelzők: nagy közepes kicsi. Hőmérséklet, T tapasztalat (hideg, meleg).
 Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok
 Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Műszaki termodinamika I. 2. előadás 0. főtétel, 1. főtétel, termodinamikai potenciálok, folyamatok Az előadás anyaga pár napon belül pdf formában is elérhető: energia.bme.hu/~imreattila (nem kell elé www!)
Fizika feladatok. 1. Feladatok a termodinamika tárgyköréből. 2014. december 8. Hővezetés, hőterjedés sugárzással
 Fizika feladatok 014. december 8. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-3) Határozzuk meg egy 0 cm hosszú, 4 cm átmérőjű hengeres vörösréz rúdon
Fizika feladatok 014. december 8. 1. Feladatok a termodinamika tárgyköréből Hővezetés, hőterjedés sugárzással 1.1. Feladat: (HN 19A-3) Határozzuk meg egy 0 cm hosszú, 4 cm átmérőjű hengeres vörösréz rúdon
Értékelési útmutató az emelt szint írásbeli feladatsorhoz I.
 Értékelési útmutató az emelt szint írásbeli feladatsorhoz I. 1. C. B 3. B 4. C 5. B 6. A 7. D 8. D 9. A 10. C 11. C 1. A 13. C 14. B 15. B 16. B 17. D 18. B 19. C 0. B I. RÉSZ Összesen 0 pont 1 1. téma
Értékelési útmutató az emelt szint írásbeli feladatsorhoz I. 1. C. B 3. B 4. C 5. B 6. A 7. D 8. D 9. A 10. C 11. C 1. A 13. C 14. B 15. B 16. B 17. D 18. B 19. C 0. B I. RÉSZ Összesen 0 pont 1 1. téma
Atomok. szilárd. elsődleges kölcsönhatás. kovalens ionos fémes. gázok, folyadékok, szilárd anyagok. ionos fémek vegyületek ötvözetek
 Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
Atomok elsődleges kölcsönhatás kovalens ionos fémes véges számú atom térhálós szerkezet 3D ionos fémek vegyületek ötvözetek molekulák atomrácsos vegyületek szilárd gázok, folyadékok, szilárd anyagok Gázok
1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai
 3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
3.1. Ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és a zárt termodinamikai rendszer? Az anyagi valóság egy, általunk kiválasztott szempont vagy szempontrendszer
Axiomatikus felépítés az axiómák megalapozottságát a felépített elmélet teljesítképessége igazolja majd!
 Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
Hol vagyunk most? Definiáltuk az alapvet fogalmakat! - TD-i rendszer, fajtái - Környezet, fal - TD-i rendszer jellemzi - TD-i rendszer leírásához szükséges változók, állapotjelzk, azok csoportosítása -
A TERMODINAMIKA I. AXIÓMÁJA. Egyszerű rendszerek egyensúlya. Első észrevétel: egyszerű rendszerekről beszélünk.
 A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
A TERMODINAMIKA I. AXIÓMÁJA Egyszerű rendszerek egyensúlya Első észrevétel: egyszerű rendszerekről beszélünk. Második észrevétel: egyensúlyban lévő egyszerű rendszerekről beszélünk. Mi is tehát az egyensúly?
Ideális gáz és reális gázok
 Ideális gáz és reális gázok Fizikai kémia előadások 1. Turányi Tamás ELTE Kémiai Intézet Állaotjelzők állaotjelző: egy fizikai rendszer makroszkoikus állaotát meghatározó mennyiség egykomonensű gázok állaotjelzői:
Ideális gáz és reális gázok Fizikai kémia előadások 1. Turányi Tamás ELTE Kémiai Intézet Állaotjelzők állaotjelző: egy fizikai rendszer makroszkoikus állaotát meghatározó mennyiség egykomonensű gázok állaotjelzői:
Az energia bevezetése az iskolába. Készítette: Rimai Anasztázia
 Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
Az energia bevezetése az iskolába Készítette: Rimai Anasztázia Bevezetés Fizika oktatása Energia probléma Termodinamika a tankönyvekben A termodinamikai fogalmak kialakulása Az energia fogalom története
gáznál = 32, CO 2 gáznál 1+1=2, O 2 gáznál = 44)
 Hőtan - gázok Gázok állapotjelzői A gázok állapotát néhány jellemző adatával adhatjuk meg. Ezek: Térfogat Valójában a tartály térfogata, amelyben van, mivel a gáz kitölti a rendelkezésére álló teret, tehát
Hőtan - gázok Gázok állapotjelzői A gázok állapotát néhány jellemző adatával adhatjuk meg. Ezek: Térfogat Valójában a tartály térfogata, amelyben van, mivel a gáz kitölti a rendelkezésére álló teret, tehát
4. Jellegzetes állapotváltozások; leírásuk: p-v, T-S, H-S diagramokban
 Energetika 1 4. Jellegzetes állapotváltozások; leírásuk: p-v, T-S, H-S diagramokban Energodinamikai rendszerek vizsgálata során elsősorban gáznemű halmazállapot esetén lényeges az állapotváltozásokat megkülönböztetni.
Energetika 1 4. Jellegzetes állapotváltozások; leírásuk: p-v, T-S, H-S diagramokban Energodinamikai rendszerek vizsgálata során elsősorban gáznemű halmazállapot esetén lényeges az állapotváltozásokat megkülönböztetni.
Az előadás vázlata: Állapotjelzők: Állapotjelzők: Állapotjelzők: Állapotjelzők: nagy közepes kicsi. Hőmérséklet, T tapasztalat (hideg, meleg).
 Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Az előadás vázlata: I. A tökéletes gáz és állapotegyenlete. izoterm, izobár és izochor folyamatok. II. Tökéletes gázok elegyei, a móltört fogalma, a parciális nyomás, a Dalton-törvény. III. A reális gázok
Fizika. Fizika. Nyitray Gergely (PhD) PTE PMMIK március 6.
 Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 6. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 6. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
Gáztörvények tesztek
 Gáztörvények tesztek. Azonos fajtájú ideális gáz különböző mennyiségei töltenek ki két hőszigetelt tartályt. Az egyik gázmennyiség jellemzői,,, a másiké,,. A két tartályt összenyitjuk. Melyik állítás igaz?
Gáztörvények tesztek. Azonos fajtájú ideális gáz különböző mennyiségei töltenek ki két hőszigetelt tartályt. Az egyik gázmennyiség jellemzői,,, a másiké,,. A két tartályt összenyitjuk. Melyik állítás igaz?
Gáztörvények tesztek. 2. Azonos fajtájú ideális gáz különböző mennyiségei töltenek ki két hőszigetelt tartályt. Az egyik
 Gáztörvények tesztek. Azonos fajtájú ideális gáz különböző mennyiségei töltenek ki két hőszigetelt tartályt. Az egyik gázmennyiség jellemzői,,, a másiké,,. A két tartályt összenyitjuk. Melyik állítás igaz?
Gáztörvények tesztek. Azonos fajtájú ideális gáz különböző mennyiségei töltenek ki két hőszigetelt tartályt. Az egyik gázmennyiség jellemzői,,, a másiké,,. A két tartályt összenyitjuk. Melyik állítás igaz?
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1
 1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
1 Műszaki hőtan Termodinamika. Ellenőrző kérdések-02 1 Kérdések. 1. Mit mond ki a termodinamika nulladik főtétele? Azt mondja ki, hogy mindenegyes termodinamikai kölcsönhatáshoz tartozik a TDR-nek egyegy
Termodinamika. Gázok hőtágulása, gáztörvények. Az anyag gázállapota. Avogadro törvény Hőmérséklet. Tóth Mónika.
 Hőmérséklet ermodinamika Hőmérséklet: Egy rendszer részecskéinek átlagos mozgási energiájával arányos fizikai mennyiség. óth Mónika 203 monika.a.toth@aok.pte.hu Különböző hőmérsékleti skálák. Kelvin skálájú
Hőmérséklet ermodinamika Hőmérséklet: Egy rendszer részecskéinek átlagos mozgási energiájával arányos fizikai mennyiség. óth Mónika 203 monika.a.toth@aok.pte.hu Különböző hőmérsékleti skálák. Kelvin skálájú
Általános kémia képletgyűjtemény. Atomszerkezet Tömegszám (A) A = Z + N Rendszám (Z) Neutronok száma (N) Mólok száma (n)
 Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Általános kémia képletgyűjtemény (Vizsgára megkövetelt egyenletek a szimbólumok értelmezésével, illetve az egyenletek megfelelő alkalmazása is követelmény) Atomszerkezet Tömegszám (A) A = Z + N Rendszám
Feladatok gázokhoz (10. évfolyam) Készítette: Porkoláb Tamás
 Feladatok ázokhoz (10. évfolyam) Készítette: Porkoláb Tamás Elméleti kérdések 1. Ismertesd az ideális ázok modelljét! 2. Írd le az ideális ázok tulajdonsáait! 3. Mit nevezünk normálállapotnak? 4. Milyen
Feladatok ázokhoz (10. évfolyam) Készítette: Porkoláb Tamás Elméleti kérdések 1. Ismertesd az ideális ázok modelljét! 2. Írd le az ideális ázok tulajdonsáait! 3. Mit nevezünk normálállapotnak? 4. Milyen
f = n - F ELTE II. Fizikus 2005/2006 I. félév
 ELTE II. Fizikus 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 2. (X. 25) Gibbs féle fázisszabály (0-dik fıtétel alkalmazása) Intenzív állapotothatározók száma közötti összefüggés: A szabad intenzív paraméterek
ELTE II. Fizikus 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 2. (X. 25) Gibbs féle fázisszabály (0-dik fıtétel alkalmazása) Intenzív állapotothatározók száma közötti összefüggés: A szabad intenzív paraméterek
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 1. 2:24 Normál Magasabb hőmérsékleten a részecskék nagyobb tágassággal rezegnek, s így távolabb kerülnek egymástól. Magasabb hőmérsékleten a részecskék kisebb tágassággal rezegnek, s így távolabb kerülnek
1. 2:24 Normál Magasabb hőmérsékleten a részecskék nagyobb tágassággal rezegnek, s így távolabb kerülnek egymástól. Magasabb hőmérsékleten a részecskék kisebb tágassággal rezegnek, s így távolabb kerülnek
Feladatok gázokhoz. Elméleti kérdések
 Feladatok ázokhoz Elméleti kérdések 1. Ismertesd az ideális ázok modelljét! 2. Írd le az ideális ázok tulajdonsáait! 3. Mit nevezünk normálállapotnak? 4. Milyen tapasztalati tényeket használhatunk a hımérséklet
Feladatok ázokhoz Elméleti kérdések 1. Ismertesd az ideális ázok modelljét! 2. Írd le az ideális ázok tulajdonsáait! 3. Mit nevezünk normálállapotnak? 4. Milyen tapasztalati tényeket használhatunk a hımérséklet
gáznál 16+16 = 32, CO 2 gáznál 1+1=2, O 2 gáznál 12+16+16= 44)
 Hőtan - gázok Gázok állapotjelzői A gázok állapotát néhány jellemző adatával adhatjuk meg. Ezek: Térfogat Valójában a tartály térfogata, amelyben van, mivel a gáz kitölti a rendelkezésére álló teret, tehát
Hőtan - gázok Gázok állapotjelzői A gázok állapotát néhány jellemző adatával adhatjuk meg. Ezek: Térfogat Valójában a tartály térfogata, amelyben van, mivel a gáz kitölti a rendelkezésére álló teret, tehát
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 1. 2:29 Normál párolgás olyan halmazállapot-változás, amelynek során a folyadék légneművé válik. párolgás a folyadék felszínén megy végbe. forrás olyan halmazállapot-változás, amelynek során nemcsak a
1. 2:29 Normál párolgás olyan halmazállapot-változás, amelynek során a folyadék légneművé válik. párolgás a folyadék felszínén megy végbe. forrás olyan halmazállapot-változás, amelynek során nemcsak a
összetevője változatlan marad, a falra merőleges összetevő iránya ellenkezőjére változik, miközben nagysága ugyanakkora marad.
 A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
A termodinamika 2. főtétele kis rendszerekben Osváth Szabolcs Semmelweis Egyetem Statisztikus sokaságok Nyomás Nyomás: a tartály falával ütköző molekulák, a falra erőt fejtenek ki Az ütközésben a részecske
Műszaki hőtan I. ellenőrző kérdések
 Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
Alapfogalmak, 0. főtétel Műszaki hőtan I. ellenőrző kérdések 1. Mi a termodinamikai rendszer? Miben különbözik egymástól a nyitott és zárt termodinamikai rendszer? A termodinamikai rendszer (TDR) az anyagi
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 gázok hőtágulása függ: 1. 1:55 Normál de független az anyagi minőségtől. Függ az anyagi minőségtől. a kezdeti térfogattól, a hőmérséklet-változástól, Mlyik állítás az igaz? 2. 2:31 Normál Hőáramláskor
gázok hőtágulása függ: 1. 1:55 Normál de független az anyagi minőségtől. Függ az anyagi minőségtől. a kezdeti térfogattól, a hőmérséklet-változástól, Mlyik állítás az igaz? 2. 2:31 Normál Hőáramláskor
TestLine - Fizika 7. osztály Hőtan Témazáró Minta feladatsor
 Nézd meg a képet és jelöld az 1. igaz állításokat! 1:56 Könnyű F sak a sárga golyó fejt ki erőhatást a fehérre. Mechanikai kölcsönhatás jön létre a golyók között. Mindkét golyó mozgásállapota változik.
Nézd meg a képet és jelöld az 1. igaz állításokat! 1:56 Könnyű F sak a sárga golyó fejt ki erőhatást a fehérre. Mechanikai kölcsönhatás jön létre a golyók között. Mindkét golyó mozgásállapota változik.
71. A lineáris és térfogati hőtágulási tényező közötti összefüggés:
 Összefüggések: 69. Lineáris hőtágulás: Hosszváltozás l = α l 0 T Lineáris hőtágulási Kezdeti hossz Hőmérsékletváltozás 70. Térfogati hőtágulás: Térfogatváltozás V = β V 0 T Hőmérsékletváltozás Térfogati
Összefüggések: 69. Lineáris hőtágulás: Hosszváltozás l = α l 0 T Lineáris hőtágulási Kezdeti hossz Hőmérsékletváltozás 70. Térfogati hőtágulás: Térfogatváltozás V = β V 0 T Hőmérsékletváltozás Térfogati
Hőtágulás - szilárd és folyékony anyagoknál
 Hőtágulás - szilárd és folyékony anyagoknál Celsius hőmérsékleti skála: 0 ºC pontja a víz fagyáspontja 100 ºC pontja a víz forráspontja Kelvin hőmérsékleti skála: A beosztása 273-al van elcsúsztatva a
Hőtágulás - szilárd és folyékony anyagoknál Celsius hőmérsékleti skála: 0 ºC pontja a víz fagyáspontja 100 ºC pontja a víz forráspontja Kelvin hőmérsékleti skála: A beosztása 273-al van elcsúsztatva a
Termodinamika. Tóth Mónika
 Termodinamika Tóth Mónika 2012.11.26-27 monika.a.toth@aok.pte.hu Hőmérséklet Hőmérséklet: Egy rendszer részecskéinek átlagos mozgási energiájával arányos fizikai mennyiség. Különböző hőmérsékleti skálák.
Termodinamika Tóth Mónika 2012.11.26-27 monika.a.toth@aok.pte.hu Hőmérséklet Hőmérséklet: Egy rendszer részecskéinek átlagos mozgási energiájával arányos fizikai mennyiség. Különböző hőmérsékleti skálák.
Követelmények: f - részvétel az előadások 67 %-án - 3 db érvényes ZH (min. 50%) - 4 elfogadott laborjegyzőkönyv
 Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
Fizikai kémia és radiokémia B.Sc. László Krisztina 18-93 klaszlo@mail.bme.hu F ép. I. lépcsőház 1. emelet 135 http://oktatas.ch.bme.hu/oktatas/konyvek/fizkem/kornymern Követelmények: 2+0+1 f - részvétel
1. feladat Alkalmazzuk a mólhő meghatározását egy gázra. Izoterm és adiabatikus átalakulásokra a következőt kapjuk:
 Válaszoljatok a következő kérdésekre: 1. feladat Alkalmazzuk a mólhő meghatározását egy gázra. Izoterm és adiabatikus átalakulásokra a következőt kapjuk: a) zéró izoterm átalakulásnál és végtelen az adiabatikusnál
Válaszoljatok a következő kérdésekre: 1. feladat Alkalmazzuk a mólhő meghatározását egy gázra. Izoterm és adiabatikus átalakulásokra a következőt kapjuk: a) zéró izoterm átalakulásnál és végtelen az adiabatikusnál
8. Belső energia, entalpia és entrópia ideális és nem ideális gázoknál
 8. első energia, entalpia és entrópia ideális és nem ideális gázoknál első energia első energia (U): a vizsgált rendszer energiája, DE nem tartozik hozzá - a teljes rendszer együttes mozgásából adódó mozgási
8. első energia, entalpia és entrópia ideális és nem ideális gázoknál első energia első energia (U): a vizsgált rendszer energiája, DE nem tartozik hozzá - a teljes rendszer együttes mozgásából adódó mozgási
Molekuláris dinamika I. 10. előadás
 Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
Molekuláris dinamika I. 10. előadás Miről is szól a MD? nagy részecskeszámú rendszerek ismerjük a törvényeket mikroszkópikus szinten minden részecske mozgását szimuláljuk? Hogyan tudjuk megérteni a folyadékok,
Energia. Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia
 Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Kémiai változások Energia Energia: munkavégző, vagy hőközlő képesség. Kinetikus energia: a mozgási energia Potenciális (helyzeti) energia: a részecskék kölcsönhatásából származó energia. Energiamegmaradás
Feladatlap X. osztály
 Feladatlap X. osztály 1. feladat Válaszd ki a helyes választ. Két test fajhője közt a következő összefüggés áll fenn: c 1 > c 2, ha: 1. ugyanabból az anyagból vannak és a tömegük közti összefüggés m 1
Feladatlap X. osztály 1. feladat Válaszd ki a helyes választ. Két test fajhője közt a következő összefüggés áll fenn: c 1 > c 2, ha: 1. ugyanabból az anyagból vannak és a tömegük közti összefüggés m 1
Termodinamika. Tóth Mónika
 Termodinamika Tóth Mónika 2015 monika.a.toth@aok.pte.hu Termodinamika Hő Mozgás TERMODINAMIKA a világ egy jól körülhatárolt részének a RENDSZERnek és a rendszer KÖRNYEZETének kölcsönhatásával és a rendszer
Termodinamika Tóth Mónika 2015 monika.a.toth@aok.pte.hu Termodinamika Hő Mozgás TERMODINAMIKA a világ egy jól körülhatárolt részének a RENDSZERnek és a rendszer KÖRNYEZETének kölcsönhatásával és a rendszer
Műszaki hőtantermodinamika. Műszaki menedzsereknek. BME Energetikai Gépek és Rendszerek Tanszék
 Műszaki hőtantermodinamika Műszaki menedzsereknek Termodinamikai rendszer Meghatározott anyagmennyiség, agy/és Véges térrész. A termodinamikai rendszert a környezetétől tényleges agy elkézelt fal álasztja
Műszaki hőtantermodinamika Műszaki menedzsereknek Termodinamikai rendszer Meghatározott anyagmennyiség, agy/és Véges térrész. A termodinamikai rendszert a környezetétől tényleges agy elkézelt fal álasztja
Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői, állapotváltozásai Hőmérséklet Az anyagok melegségének
 Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői, állapotváltozásai Hőmérséklet Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála:
Hőtan ( első rész ) Hőmérséklet, szilárd tárgyak és folyadékok hőtágulása, gázok állapotjelzői, állapotváltozásai Hőmérséklet Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála:
Bevezetés és gyakorlati tanácsok Az első lépés minden tudomány elsajátítása felé az, hogy megértjük az alapjait, és megbízható tudást szerzünk
 Bevezetés és gyakorlati tanácsok Az első lépés minden tudomány elsajátítása felé az, hogy megértjük az alapjait, és megbízható tudást szerzünk belőle. A következő az, hogy a megszerzett tudást elmélyítjük.
Bevezetés és gyakorlati tanácsok Az első lépés minden tudomány elsajátítása felé az, hogy megértjük az alapjait, és megbízható tudást szerzünk belőle. A következő az, hogy a megszerzett tudást elmélyítjük.
Termokémia. Termokémia Dia 1 /55
 Termokémia 6-1 Terminológia 6-2 Hő 6-3 Reakcióhő, kalorimetria 6-4 Munka 6-5 A termodinamika első főtétele 6-6 Reakcióhő: U és H 6-7 H indirekt meghatározása: Hess-tétel 6-8 Standard képződési entalpia
Termokémia 6-1 Terminológia 6-2 Hő 6-3 Reakcióhő, kalorimetria 6-4 Munka 6-5 A termodinamika első főtétele 6-6 Reakcióhő: U és H 6-7 H indirekt meghatározása: Hess-tétel 6-8 Standard képződési entalpia
MŰSZAKI TERMODINAMIKA 1. ÖSSZEGZŐ TANULMÁNYI TELJESÍTMÉNYÉRTÉKELÉS
 MŰSZAKI TERMODINAMIKA. ÖSSZEGZŐ TANULMÁNYI TELJESÍTMÉNYÉRTÉKELÉS 207/8/2 MT0A Munkaidő: 90 perc NÉV:... NEPTUN KÓD: TEREM HELYSZÁM:... DÁTUM:... KÉPZÉS Energetikai mérnök BSc Gépészmérnök BSc JELÖLJE MEG
MŰSZAKI TERMODINAMIKA. ÖSSZEGZŐ TANULMÁNYI TELJESÍTMÉNYÉRTÉKELÉS 207/8/2 MT0A Munkaidő: 90 perc NÉV:... NEPTUN KÓD: TEREM HELYSZÁM:... DÁTUM:... KÉPZÉS Energetikai mérnök BSc Gépészmérnök BSc JELÖLJE MEG
Osztályozó vizsga anyagok. Fizika
 Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
Osztályozó vizsga anyagok Fizika 9. osztály Kinematika Mozgás és kölcsönhatás Az egyenes vonalú egyenletes mozgás leírása A sebesség fogalma, egységei A sebesség iránya Vektormennyiség fogalma Az egyenes
Az egyensúly. Általános Kémia: Az egyensúly Slide 1 of 27
 Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Az egyensúly 6'-1 6'-2 6'-3 6'-4 6'-5 Dinamikus egyensúly Az egyensúlyi állandó Az egyensúlyi állandókkal kapcsolatos összefüggések Az egyensúlyi állandó számértékének jelentősége A reakció hányados, Q:
Modern fizika vegyes tesztek
 Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
(2006. október) Megoldás:
 1. Állandó hőmérsékleten vízgőzt nyomunk össze. Egy adott ponton az edény alján víz kezd összegyűlni. A gőz nyomását az alábbi táblázat mutatja a térfogat függvényében. a)ábrázolja nyomás-térfogat grafikonon
1. Állandó hőmérsékleten vízgőzt nyomunk össze. Egy adott ponton az edény alján víz kezd összegyűlni. A gőz nyomását az alábbi táblázat mutatja a térfogat függvényében. a)ábrázolja nyomás-térfogat grafikonon
Szabadentalpia nyomásfüggése
 Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Égéselmélet Szabadentalpia nyomásfüggése G( p, T ) G( p Θ, T ) = p p Θ Vdp = p p Θ nrt p dp = nrt ln p p Θ Mi az a tűzoltó autó? A tűz helye a világban Égés, tűz Égés: kémiai jelenség a levegő oxigénjével
Abszolút jelleg skála : elvárásunk: anyagi min ségt l független, természeti törvények egyszer alakúak (Lord Kelvin, 1852). A T alapmennyiség (nem
 H tan el adás segédanyag, zika BSc, 2. félév Szabó Péter Imre, SZTE Kísérleti Fizika Tanszék http://titan.physx.u szeged.hu/~szabopeter CSAK SEGÉDANYAG! Javasolt tankönyv: Budó: Kísérleti Fizika I. kötet,
H tan el adás segédanyag, zika BSc, 2. félév Szabó Péter Imre, SZTE Kísérleti Fizika Tanszék http://titan.physx.u szeged.hu/~szabopeter CSAK SEGÉDANYAG! Javasolt tankönyv: Budó: Kísérleti Fizika I. kötet,
Általános Kémia. Dr. Csonka Gábor 1. Gázok. Gázok. 2-1 Gáznyomás. Barométer. 6-2 Egyszerű gáztörvények. Manométer
 Gázok -1 Gáznyoás - Egyszerű gáztörvények -3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet -4 tökéletes gáz egyenlet alkalazása -5 Gáz halazállapotú reakciók -6 Gázkeverékek
Gázok -1 Gáznyoás - Egyszerű gáztörvények -3 Gáztörvények egyesítése: Tökéletes gáz egyenlet és általánosított gáz egyenlet -4 tökéletes gáz egyenlet alkalazása -5 Gáz halazállapotú reakciók -6 Gázkeverékek
Fizika. Fizika. Nyitray Gergely (PhD) PTE PMMIK március 20.
 Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 20. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
Fizika Nyitray Gergely (PhD) PTE PMMIK 2017. március 20. A termodinamikai rendszer fogalma Termodinamika: Nagy részecskeszámú rendszerek fizikája. N A 10 23 db. A rendszer(r): A világ azon része, amely
Atomok és molekulák elektronszerkezete
 Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Atomok és molekulák elektronszerkezete Szabad atomok és molekulák Schrödinger egyenlete Tekintsünk egy kvantummechanikai rendszert amely N n magból és N e elektronból áll. Koordinátáikat jelölje rendre
Biofizika szeminárium. Diffúzió, ozmózis
 Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Biofizika szeminárium Diffúzió, ozmózis I. DIFFÚZIÓ ORVOSI BIOFIZIKA tankönyv: III./2 fejezet Részecskék mozgása Brown-mozgás Robert Brown o kísérlet: pollenszuszpenzió mikroszkópos vizsgálata o megfigyelés:
Kérdések Fizika112. Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika
 Kérdések Fizika112 Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika 1. Adjuk meg egy tömegpontra ható centrifugális erő nagyságát és irányát!
Kérdések Fizika112 Mozgás leírása gyorsuló koordinátarendszerben, folyadékok mechanikája, hullámok, termodinamika, elektrosztatika 1. Adjuk meg egy tömegpontra ható centrifugális erő nagyságát és irányát!
Zaj- és rezgés. Törvényszerűségek
 Zaj- és rezgés Törvényszerűségek A hang valamilyen közegben létrejövő rezgés. A vivőközeg szerint megkülönböztetünk: léghangot (a vivőközeg gáz, leggyakrabban levegő); folyadékhangot (a vivőközeg folyadék,
Zaj- és rezgés Törvényszerűségek A hang valamilyen közegben létrejövő rezgés. A vivőközeg szerint megkülönböztetünk: léghangot (a vivőközeg gáz, leggyakrabban levegő); folyadékhangot (a vivőközeg folyadék,
TestLine - Fizika hőjelenségek Minta feladatsor
 1. 2:29 Normál zt a hőmérsékletet, melyen a folyadék forrni kezd, forráspontnak nevezzük. Különböző anyagok forráspontja más és más. Minden folyadék minden hőmérsékleten párolog. párolgás gyorsabb, ha
1. 2:29 Normál zt a hőmérsékletet, melyen a folyadék forrni kezd, forráspontnak nevezzük. Különböző anyagok forráspontja más és más. Minden folyadék minden hőmérsékleten párolog. párolgás gyorsabb, ha
FIZIKA KÖZÉPSZINTŐ SZÓBELI FIZIKA ÉRETTSÉGI TÉTELEK Premontrei Szent Norbert Gimnázium, Gödöllı, 2012. május-június
 1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
1. Egyenes vonalú mozgások kinematikája mozgásokra jellemzı fizikai mennyiségek és mértékegységeik. átlagsebesség egyenes vonalú egyenletes mozgás egyenes vonalú egyenletesen változó mozgás mozgásokra
Csillapított rezgés. a fékező erő miatt a mozgás energiája (mechanikai energia) disszipálódik. kváziperiódikus mozgás
 Csillapított rezgés Csillapított rezgés: A valóságban a rezgések lassan vagy gyorsan, de csillapodnak. A rugalmas erőn kívül, még egy sebességgel arányos fékező erőt figyelembe véve: a fékező erő miatt
Csillapított rezgés Csillapított rezgés: A valóságban a rezgések lassan vagy gyorsan, de csillapodnak. A rugalmas erőn kívül, még egy sebességgel arányos fékező erőt figyelembe véve: a fékező erő miatt
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont)
 Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
Égés és oltáselmélet I. (zárójelben a helyes válaszra adott pont) 1. "Az olyan rendszereket, amelyek határfelülete a tömegáramokat megakadályozza,... rendszernek nevezzük" (1) 2. "Az olyan rendszereket,
3. Gyakorlat Áramlástani feladatok és megoldásuk
 3 Gyakorlat Áramlástani feladatok és megoldásuk 681 Feladat Adja meg Kelvin és Fahrenheit fokban a T = + 73 = 318 K o K T C, T = 9 5 + 3 = 113Fo F T C 68 Feladat Adja meg Kelvin és Celsius fokban a ( T
3 Gyakorlat Áramlástani feladatok és megoldásuk 681 Feladat Adja meg Kelvin és Fahrenheit fokban a T = + 73 = 318 K o K T C, T = 9 5 + 3 = 113Fo F T C 68 Feladat Adja meg Kelvin és Celsius fokban a ( T
Méréstechnika. Hőmérséklet mérése
 Méréstechnika Hőmérséklet mérése Hőmérséklet: A hőmérséklet a termikus kölcsönhatáshoz tartozó állapotjelző. A hőmérséklet azt jelzi, hogy egy test hőtartalma milyen szintű. Amennyiben két eltérő hőmérsékletű
Méréstechnika Hőmérséklet mérése Hőmérséklet: A hőmérséklet a termikus kölcsönhatáshoz tartozó állapotjelző. A hőmérséklet azt jelzi, hogy egy test hőtartalma milyen szintű. Amennyiben két eltérő hőmérsékletű
Általános Kémia Gyakorlat II. zárthelyi október 10. A1
 2008. október 10. A1 Rendezze az alábbi egyenleteket! (5 2p) 3 H 3 PO 3 + 2 HNO 3 = 3 H 3 PO 4 + 2 NO + 1 H 2 O 2 MnO 4 + 5 H 2 O 2 + 6 H + = 2 Mn 2+ + 5 O 2 + 8 H 2 O 1 Hg + 4 HNO 3 = 1 Hg(NO 3 ) 2 +
2008. október 10. A1 Rendezze az alábbi egyenleteket! (5 2p) 3 H 3 PO 3 + 2 HNO 3 = 3 H 3 PO 4 + 2 NO + 1 H 2 O 2 MnO 4 + 5 H 2 O 2 + 6 H + = 2 Mn 2+ + 5 O 2 + 8 H 2 O 1 Hg + 4 HNO 3 = 1 Hg(NO 3 ) 2 +
Gázok. Készítette: Porkoláb Tamás
 Gázok Készítette: Porkoláb Taás. Alapfogalak. Az ideális gáz nyoása, a Boyle-Mariotte törvény 3. A hıérséklet 4. Gay-Lussac I. törvénye 5. Gay-Lussac II. törvénye 6. Az állapotegyenlet 7. Az ideális gáz
Gázok Készítette: Porkoláb Taás. Alapfogalak. Az ideális gáz nyoása, a Boyle-Mariotte törvény 3. A hıérséklet 4. Gay-Lussac I. törvénye 5. Gay-Lussac II. törvénye 6. Az állapotegyenlet 7. Az ideális gáz
5. Állapotegyenletek : Az ideális gáz állapotegyenlet és a van der Waals állapotegyenlet
 5. Állapotegyenletek : Az ideális gáz állapotegyenlet és a van der Waals állapotegyenlet Ideális gáz Az ideális gáz állapotegyenlete pv=nrt empírikus állapotegyenlet, a Boyle-Mariotte (pv=konstans) és
5. Állapotegyenletek : Az ideális gáz állapotegyenlet és a van der Waals állapotegyenlet Ideális gáz Az ideális gáz állapotegyenlete pv=nrt empírikus állapotegyenlet, a Boyle-Mariotte (pv=konstans) és
Hőtan főtételei. (vázlat)
 Hőtan főtételei (vázlat) 1. Belső energia oka, a hőtan I. főtétele. Ideális gázok belső energiája 3. Az ekvipartíció elve 4. Hőközlés és térfogati munka, a hőtan I. főtétele ideális gázokra 5. A hőtan
Hőtan főtételei (vázlat) 1. Belső energia oka, a hőtan I. főtétele. Ideális gázok belső energiája 3. Az ekvipartíció elve 4. Hőközlés és térfogati munka, a hőtan I. főtétele ideális gázokra 5. A hőtan
A szilárd testek alakja és térfogata észrevehetően csak nagy erő hatására változik meg. A testekben a részecskék egymáshoz közel vannak, kristályos
 Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Az anyagok lehetséges állapotai, a fizikai körülményektől (nyomás, hőmérséklet) függően. Az anyagokat általában a normál körülmények között jellemző állapotuk alapján soroljuk be szilád, folyékony vagy
Reológia Mérési technikák
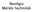 Reológia Mérési technikák Reológia Testek (és folyadékok) külső erőhatásra bekövetkező deformációját, mozgását írja le. A deformációt irreverzibilisnek nevezzük, ha a az erőhatás megszűnése után a test
Reológia Mérési technikák Reológia Testek (és folyadékok) külső erőhatásra bekövetkező deformációját, mozgását írja le. A deformációt irreverzibilisnek nevezzük, ha a az erőhatás megszűnése után a test
HŐTAN. Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki:
 Hőmérséklet HŐTAN Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála: 0 ºC pontja a víz fagyáspontja 100 ºC pontja a víz forráspontja Fahrenheit skála (angolszász országokban
Hőmérséklet HŐTAN Az anyagok melegségének mérésére hőmérsékleti skálákat találtak ki: Celsius-skála: 0 ºC pontja a víz fagyáspontja 100 ºC pontja a víz forráspontja Fahrenheit skála (angolszász országokban
1. SI mértékegységrendszer
 I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
I. ALAPFOGALMAK 1. SI mértékegységrendszer Alapegységek 1 Hosszúság (l): méter (m) 2 Tömeg (m): kilogramm (kg) 3 Idő (t): másodperc (s) 4 Áramerősség (I): amper (A) 5 Hőmérséklet (T): kelvin (K) 6 Anyagmennyiség
Fizika 1i (keresztfélév) vizsgakérdések kidolgozása
 Fizika 1i (keresztfélév) vizsgakérdések kidolgozása Készítette: Hornich Gergely, 2013.12.31. Kiegészítette: Mosonyi Máté (10., 32. feladatok), 2015.01.21. (Talapa Viktor 2013.01.15.-i feladatgyűjteménye
Fizika 1i (keresztfélév) vizsgakérdések kidolgozása Készítette: Hornich Gergely, 2013.12.31. Kiegészítette: Mosonyi Máté (10., 32. feladatok), 2015.01.21. (Talapa Viktor 2013.01.15.-i feladatgyűjteménye
Spontaneitás, entrópia
 Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Spontaneitás, entrópia 11-1 Spontán és nem spontán folyamat 11-2 Entrópia 11-3 Az entrópia kiszámítása 11-4 Spontán folyamat: a termodinamika második főtétele 11-5 Standard szabadentalpia változás, ΔG
Előszó.. Bevezetés. 1. A fizikai megismerés alapjai Tér is idő. Hosszúság- és időmérés.
 SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
SZABÓ JÁNOS: Fizika (Mechanika, hőtan) I. TARTALOMJEGYZÉK Előszó.. Bevezetés. 1. A fizikai megismerés alapjai... 2. Tér is idő. Hosszúság- és időmérés. MECHANIKA I. Az anyagi pont mechanikája 1. Az anyagi
ELTE II. Fizikus, 2005/2006 I. félév KISÉRLETI FIZIKA Hıtan 9. (XI. 23)
 ELE II. Fizikus, 005/006 I. félév KISÉRLEI FIZIKA Hıtan 9. (XI. 3) Kémiai reakciók Gázelegyek termodinamikája 1) Dalton törvény: Azonos hımérséklető, de eltérı anyagi minıségő és V térfogatú gázkeverékben
ELE II. Fizikus, 005/006 I. félév KISÉRLEI FIZIKA Hıtan 9. (XI. 3) Kémiai reakciók Gázelegyek termodinamikája 1) Dalton törvény: Azonos hımérséklető, de eltérı anyagi minıségő és V térfogatú gázkeverékben
A hőmérséklet változtatásával a szilárd testek hosszméretei megváltoznak, mégpedig melegítéskor általában növekednek. Ez azzal magyarázható, hogy a
 Kísérletek: 1 2 3 4 A hőmérséklet változtatásával a szilárd testek hosszméretei megváltoznak, mégpedig melegítéskor általában növekednek. Ez azzal magyarázható, hogy a szilárd testet alkotó molekulák rezgőmozgásának
Kísérletek: 1 2 3 4 A hőmérséklet változtatásával a szilárd testek hosszméretei megváltoznak, mégpedig melegítéskor általában növekednek. Ez azzal magyarázható, hogy a szilárd testet alkotó molekulák rezgőmozgásának
