Trendek és fejlemények az SPC-k és pediátriai hosszabbítások május Mátraháza, Hotel Residence Ózon Buzásné Nagy Zsuzsanna,
|
|
|
- György Nemes
- 8 évvel ezelőtt
- Látták:
Átírás
1 Trendek és fejlemények az SPC-k és pediátriai hosszabbítások területén május Mátraháza, Hotel Residence Ózon Buzásné Nagy Zsuzsanna, Szellemi itulajdon Nemzeti tihivatala 1
2 Prozac UK Sales Sales 8 Jan Year Forrás: IMS-Global.com 2
3 3
4 SPC bejelentések száma Magyarországon /2009/EK rendelet ( korábban 1768/92/EGK ) a gyógyszerek kiegészítő oltalmi tanúsítványáról ( május 6.) /96/EK rendelet a növényvédő szerek kieg.olt.tanúsítványáról (1996.július 23.) 1901/2006/EK rendelet a gyermekgyógyászati gyógyszerekről (2006.dec.2) 26/2004. Korm.rend. a végrehajtási szabályokról évi XXXIII törvény (Szt.) 22/A
5 Kiegészítő oltalom Szt. 22/A május 1-től (1) Az Európai Közösség rendeleteiben meghatározott esetben, feltételekkel és időtartamra a találmány tárgya kiegészítő oltalomban részesül azt követően, hogy a szabadalmi oltalom az oltalmi idő lejártával megszűnik. (2) Az (1) bekezdésben említett európai közösségi rendeletek végrehajtására vonatkozó részletes szabályokat külön jogszabály állapítja meg. (3) Az (1)bekezdésben említett európai közösségi rendeletek, illetve a (2) bekezdésben említett külön jogszabály eltérő rendelkezése hiányában a kiegészítő oltalmi tanúsítványokkal kapcsolatos ügyekben e törvény rendelkezéseit kell megfelelően alkalmazni. 5
6 1768/92/EGK gyógyszer 3. cikk A tanúsítvány megszerzésének feltételei A termékre tanúsítványt kell adni, ha abban a tagállamban, amelyben a bejelentést benyújtották, a bejelentés napján a) a termék hatályos alapszabadalom oltalma alatt áll; b) a termék gyógyszerként történő forgalomba hozatalát a megfelelő, érvényes irányelv szerint engedélyezték; c) a termékre még nem adtak tanúsítványt; d) a b) pontban említett engedély a termék gyógyszerként történő forgalomba hozatalára vonatkozó első engedély. 6
7 1610/96 EK rendelet (17) preambulum egyes szabályok megfelelően alkalmazandók a 1768/92/EGK tanácsi rendeletre is. 13. preambulum: a tanúsítvány kiterjed az alapszabadalom oltalmi körébe tartozó származékokra( sók, észterek) is. -enantiomerek? Polimorf kristályformák? 14. preambulum:a hatóanyag származékaira (sók, észterek) vonatkozó további tanúsítványok adhatók, feltéve, hogy a származékok külön szabadalmak a oltalma a alatt a állnak. - -kiválasztási találmányok További szabályok: 3.cikk (2) 17. cikk 2) 7
8 1610/96 3.cikk (2) bekezdése mindkét rendeletre alkalmazandó! 1 szabadalmasnak egy termékre csak 1 SPC adható Ha azonban ugyanarra a termékre különböző szabadalmasok tettek több SPC bejelentést, tanúsítvány adható a szabadalmasok mindegyike számára. ECJ C-482/07 (AHP Manufacturing BVBureau voor de Industriële Eigendom ) 8
9 7.Cikk A tanúsítvány iránti bejelentés határideje (1) A tanúsítvány iránti bejelentést a termék gyógyszerként történő forgalomba hozataláról szóló első belföldi engedély kiadásának napját követő hat hónapon bllkllb belül kell benyújtani. (2) Ha a termék forgalomba hozatalát az alapszabadalom megadása előtt engedélyezik, a tanúsítvány iránti bejelentést az (1) bekezdéstől eltérően léő a szabadalom bdl megadását dáákövető ő hat hónapon bllkll belül kell benyújtani. Általában a szabadalom kerül előbb megadásra! 9
10 19. Cikk Eljárási szabályok Ahol az európai közösségi rendelet eljárási szabályokat nem állapít meg, az alapszabadalomra irányadó eljárási szabályokat kell alkalmazni, feltéve, hogy a tagállam nem ír elő különleges eljárási szabályokat. 26/2004 Korm. rend A közösségi rendelet 7. cikkében megszabott határidők elmulasztása esetén igazolásnak nincs helye A bejelentés nem változtatható meg úgy, hogy más termékre, más forgalomba hozatali engedélyre vagy más alapszabadalomra vonatkozzon, mint amelyet a bejelentés benyújtásakor megjelöltek. Az SPC bejelentés a bejelentés benyújtásának napjától nyilvános 10
11 13.Cikk A tanúsítvány időtartama Szabadalom bjl bejelentési téinapja X év Közösségi első forg.h. eng. SPC kezdete SZABADALOM SPC ( x -5) +6 (20 év) De max 5 év hónap összesen legfeljebb tizenöt év kizárólagosságot kell biztosítani attól az időponttól számítva, amikor először engedélyezték az adott gyógyszer forgalomba hozatalát a Közösségben. 11
12 1610/ cikk 2) bekezdése mindkét rendeletre alkalmazandó! l Az oltalmi idő módosítása A tanúsítvány kiadásáról á szóló határozat ellen a tanúsítvány időtartamának helyesbítése iránt jogorvoslatnak van helye, ha a tanúsítvány iránti 8. cikk szerinti bejelentésben a Közösségen belüli első forgalomba hozatali engedély időpontja hibásan szerepel. De ECJ C-127/00 Aktiebolaget Hassle v Ratiopharm GmbH Ha egy kiegészítő oltalmi tanúsítvány a 19. cikk ( átmeneti rendelkezések) alapján nem lett volna megadható, mivel a közösségi első forgalomba hozatali engedély kiadásának dátuma az ott megjelölt dátum előtti, a 15. cikk alapján 12 érvénytelen.
13 13. cikk (3) új! A tanúsítvány időtartama (1) A tanúsítvány időtartama az alapszabadalom jogszabályban meghatározott oltalmi idejének lejártakor kezdődik, és az alapszabadalom iránti bejelentés benyújtásának napja és a termék Közösségen belüli forgalomba hozatalára vonatkozó első engedély keltezésének napja között eltelt időszak öt évvel csökkentett időtartamával megegyező ideig tart. (2) A tanúsítvány időtartama mindazonáltal az (1) bekezdésben foglaltaktól eltérően nem haladhatja meg a kezdetének napjától számított öt évet. (3) Az (1) és a (2) bekezdésben meghatározott időtartamot hat hónappal meg kell hosszabbítani az 1901/2006/EK rendelet 36. cikkének alkalmazása esetén. Ebben az esetben az e cikk (1) bekezdésében meghatározott időtartam csak egy ízben hosszabbítható
14 Az 1901/2006/EK rendelet (2006. december 12.) Miért volt szükség a szabályozásra? Az esetek több, mint 50%-ában olyan gyógyszerrel kezelték a gyermekeket, amelyet ezen a populáción ki sem próbáltak, mert klinikai vizsgálat gyermekeken csak a felnőtt-vizsgálat után lehetséges, akkor a gyógyszercég már forgalmazni akar a gyermek-indikáció sokszor nem hoz elegendően nagy profitot a gyermek-vizsgálat etikailag mindig problémásabb, nehezebb a protokollt összeállítani nehezebb kellő számú vizsgálati alanyt gyűjteni 14
15 Az 1901/2006/EK rendelet - Cél a gyermekgyógyászati kutatások ösztönzése. - A jóváhagyott gyermekgyógyászati vizsgálati terv(pip) végrehajtása, az információ beépítése a betegtájékoztatóba az összes tagállamban. - Az EMA Gyermekgyógyászati Bizottsága értékeli a vizsgálati tervet, dönt a mentességekről és halasztásokról, vagy véleményt ad más (nemzeti) hatóság kérésére. - Jutalmak és ösztönzők a költséges vizsgálatok elvégzéséért. - A jutalmat akkor is meg kell adni, ha a kutatás negatív eredménnyel zárul! 15
16 1901/2006/EK 7és8cikk A gyógyszer forgalomba hozatali engedély kiadásának feltételei Minden új, - hatályba lépésekor* - a Közösség területén még nem engedélyezett gyógyszerkészítmény forgalomba hozatali engedély kérelemnek tartalmaznia kell a jóváhagyott gyermekgyógyászati vizsgálati tervnek megfelelő vizsgálatok eredményeit is, vagy igazolni kell az e követelmény alól kapott mentesítést vagy halasztást. Ugyanez vonatkozik a már engedélyezett gyógyszerek új terápiás javallatainak, gyógyszerformáinak vagy új alkalmazásainak engedélyezése iránti kérelmekre is, amennyiben azok kiegészítő oltalmi tanúsítvánnyal vagy gypotenciálisan kiegészítő oltalmi tanúsítványra feljogosító szabadalommal védettek. * a 7. cikk esetében július 26 16
17 Mentességek és halasztások 17
18 1901/2006/EK Jutalmak és ösztönzők - Szabadalommal vagy kiegészítő oltalmi tanúsítvánnyal védett gyógyszertermék esetén az SPC oltalmi idejének 6 hónapos meghosszabbítása 36. cikk - Ritka betegségek gyógyszerei esetén a tíz éves piaci kizárólagosság tizenkét évre emelkedik 37. cikk - Szellemi tulajdonjog oltalma alatt (már) nem álló termékek, kizárólag gyermekgyógyászati célra kifejlesztett gyógyszerek esetén gyermekgyógyászati felhasználásra szolgáló forgalomba hozatali engedély (PUMA) adható +1 év adatkizárólagosság 38.cikk 18
19 Az iparjogvédelmi jutalom: 6 hónapos SPC meghosszabbítás Csak a 1768/92/EGK rendelet által bevezetett kiegészítő oltalmi tanúsítvány hosszabbítható meg. A nemzeti iparjogvédelmi hatóságnál kell kérelmezni új vagy folyamatban lévő SPC bejelentéssel együtt vagy már megadott tanúsítványra alapozva és benyújtani a bizonyítékokat. k t Csak akkor adható, ha a termék forgalomba hozatalát minden EU tagállamban engedélyezték (centralizált (EU) engedély vagy kölcsönös elismerésen alapuló nemzeti eljárással) és a forgalomba hozatali tliengedélyt déltkidóhtóá kiadó hatóság az engedélyben elismeri, i hogy a kérelem a jóváhagyott és végrehajtott gyermekgyógyászati vizsgálati tervnek megfelel. 19
20 Jóváhagyott... Gyermekgyógyászati vizsgálati terv (Pediatric Investigation Plan, PIP) Kutatási és fejlesztési program, amely meghatározza, milyen feltételek mellett engedélyezhető, hogy az adott gyógyszert gyermekek kezelésére használják. Ismertetni kell az elvégzendő vizsgálatokat, időbeli ütemezésüket valamint tjavaslatot tkell lltenni a gyermekpopuláció ióéi érintett tttcsoportjai tji (csecsemőtől a serdülőkorúig) számára megfelelő kiszerelési formákra. Ez után a Gyermekgyógyászati Bizottság 60 napon belül véleményt ad arról, hogy a javasolt vizsgálatokat jóváhagyja e. Az Európai Gyógyszerértékelő Ügynökség honlapján teszi közzé a gyermekgyógyászati vizsgálati tervek jóváhagyása, mentességek és halasztások engedélyezése tárgyában hozott döntéseit. 20
21 ..és végrehajtott Megfelelőségi nyilatkozat (compliance statement) Az EMA ( vagy a nemzeti törzskönyvezési hatóság) keretében működő Gyermekgyógyászati Bizottság ellenőrzi, hogy a gyermekgyógyászati vizsgálati tervben előirányzott valamennyi intézkedés teljesült-e (compliance check) Amennyiben a gyermekgyógyászati vizsgálati tervben előirányzott valamennyi intézkedés teljesült, ezt a tényt fel kell tüntetni a forgalomba hozatali engedélyben. 28 cikk (3) A forgalomba hozatali engedély jogosultja e pozitív vélemény alapján szerezheti meg a jutalmakat a megfelelésért (compliance statement) 21
22 ZOMETA Súlyos osteogenesis imperfecta kezelésében két klinikai vizsgálatban értékelték gyermekkorú betegek körében. A Zometa gyermekpopulációban nem alkalmazható, mert a biztonságosságot és hatásosságot gyermekekben nem igazolták Pozitív megfelelőségi nyilatkozat van: végrehajtották a gyermekgyógyászati vizsg tervet és a betegtájékoztatóban szerepel az eredmény! 22
23 469/2009/EK gyógyszer 7Cikk(3)-(5) 7.Cikk új! A meghosszabbítási kérelem benyújtásának határideje (3) A meghosszabbítás iránti kérelem a tanúsítvány iránti bejelentéssel egyidejűleg, vagy akkor nyújtható be, ha a tanúsítvány iránti bejelentés elbírálása folyamatban van, és a kérelem eleget tesz az adott esetnek megfelelően a 8. cikk (1) bekezdése d) pontjában vagy a 8. cikk ikk(2)b bekezdésében éb foglalt ltkövetelményeknek. k k (4) A már megadott tanúsítványra vonatkozó meghosszabbítás iránti kérelmet legkésőbb a tanúsítvány lejárta előtt két évvel kell benyújtani. (5) A (4) bekezdéstől eltérően, az 1901/2006/EK rendelet hatálybalépését követő öt éven* át a már megadott tanúsítványra vonatkozó meghosszabbítás iránti kérelmet legkésőbb a tanúsítvány lejárta előtt hat hónappal kell benyújtani. * január január 26 23
24 Milyen bizonyítékokat kell benyújtani a 6 hónapos hosszabbítás elnyeréséhez? 8.Cikk 1. d) Centralizált eljárással kiadott (EU) forgalomba hozatali engedély esetén Az Európai Gyógyszerügynökség (EMA) nyilatkozata, hogy az előzetesen jóváhagyott gyermekgyógyászati vizsgálati tervet végrehajtották és az eredményeket beépítették a betegtájékoztatóba. kölcsönös elismerésen alapuló vagy nemzeti eljárás (OGYI) keretén belül engedélyezett hatóanyag esetén: + Bizonyítani kell, hogy a termék az összes tagállam vonatkozásában forgalomba hozatali engedéllyel rendelkezik.! 24
25 469/2009/EK gyógyszer 8.Cikk 1.bekezdés d) új! d) amennyiben a tanúsítvány iránti bejelentés meghosszabbítás iránti kérelmet tartalmaz: i. az 1901/2006/EK rendelet 36. cikke (1) bekezdésében említett, a jóváhagyott és végrehajtott gyermekgyógyászati vizsgálati tervnek való megfelelésről szóló nyilatkozat másolata (compliance statement) ii. amennyiben szükséges (!), a b) pontban említett forgalomba hozatali engedély másolatán á felül bizonyíték arra vonatkozóan, hogy a termék az 1901/2006/EK rendelet 36. cikke (3) bekezdésében említettek szerint az összes többi tagállamra kiterjedő forgalomba hozatali engedéllyel rendelkezik. 25
26 A Gyermekgyógyászati Bizottsághoz 2011 márciusáig beérkezett kérelmek száma Összesen PIP értékelés vagy mentesség iránti kérelem Új gyógyszerkészítmény forgalomba hozatali engedély iránti kérelem Engedélyezett és szab. oltalom alatt álló gyógyszerek új terápiás javallatainak, gyógyszerformáinak stb.engedélyezése iránti kérelem % Gyermekgyógyászati felhasználásra szóló forgalomba hozatali engedély iránti kérelmek (off- patented ) óló f l b h t li dél Forrás: Paediatric i Committee (PDCO) Monthly report from the March 2011 meeting 26
27 A Gyermekgyógyászati Bizottság által 2011 márciusáig kiadott döntések száma Összesen Teljes mentesség Vizsgálati terv elfogadás halasztással Negatív vélemény Pozitív vélemény a megfelelőségről Negatív vélemény a megfelelőségről fllő ől Forrás: Paediatric Committee (PDCO) Monthly report from the March 2011 meeting 27
28 ticle_50_report2010.pdf 50. cikk Az EMA jelentése alapján és legalább évente egyszer a Bizottság nyilvánosságra hozza azon vállalatok és termékek jegyzékét,amelyek az ebben a rendeletben szereplő bármely jutalomban vagy ösztönzőben részesültek 28
29 29
30 Az EMEA Gyermekgyógyászati Bizottsága által kiadott pozitív megfelelőségi nyilatkozatok (2009 végéig): endokrinológia-nőgyógyászat: Anastrozole, Colesevelam hidroklorid, Dienogest, Nomegestrol acetát, 17 beta-estradiol, estradiol, onkológia: Aprepitant, Ipilimumab, Vandetanib kardiovaszkuláris betegségek: Losartan kálium, Valsartan, dermatológia: Ustekinumab, Nalfurafine hidroklorid, immunológia, reumatológia: Abatacept, Belatacept, hematológia: Eltrombopag láz- és fájdalomcsillapítás: j p Paracetamol,, 30
31 A következő gyógyszerhatóanyagok kiegészítő oltalma l jár le ban 2013 Magyarországon 2012 Duloxetin és gyógyászatilag elfogadható savaddíciós sói, különösen hidrokloridja Pioglitazon és sói Zoledronsav, gyógyászatilag alkalmazható sói és hidrátjai (2 SPC, eltérő jogosultak) + egyikre 6 hónapos hosszabbítási kérelem! Levodopa, carbidopa és entacapone valamint sóik óikkombinációja iój 2013 Nelarabin Dexmedetomidin-hidroklorid Ganirelix vag ggyógyászatilag gelfogadható sói 31
32 Kiegészítő oltalmi tanúsítványok lejárati idejének időbeli megoszlása Magyarországon 2011-ben SPC oltalmak száma Kiegészítő oltalom lejártának éve 32
33 Viszontlátásra az SZTNH-ban!
SEMMI, VAGY MÉG ANNYI SEM Zéró vagy negatív időtartamú SPC
 2008.06.25. SEMMI, VAGY MÉG ANNYI SEM Zéró vagy negatív időtartamú SPC Daróczi Klára iparjogvédelmi osztályvezető 1./ 1901/2006/EK rendelet a gyermekgyógyászati felhasználásra szánt gyógyszerekről - a
2008.06.25. SEMMI, VAGY MÉG ANNYI SEM Zéró vagy negatív időtartamú SPC Daróczi Klára iparjogvédelmi osztályvezető 1./ 1901/2006/EK rendelet a gyermekgyógyászati felhasználásra szánt gyógyszerekről - a
Az Európai Unió Hivatalos Lapja. 13/11. kötet
 200 31992R1768 1992.7.2. AZ EURÓPAI KÖZÖSSÉGEK HIVATALOS LAPJA L182/1 A TANÁCS 1768/92/EGK RENDELETE (1992. június 18.) a gyógyszerek kiegészítő oltalmi tanúsítványának bevezetéséről AZ EURÓPAI KÖZÖSSÉGEK
200 31992R1768 1992.7.2. AZ EURÓPAI KÖZÖSSÉGEK HIVATALOS LAPJA L182/1 A TANÁCS 1768/92/EGK RENDELETE (1992. június 18.) a gyógyszerek kiegészítő oltalmi tanúsítványának bevezetéséről AZ EURÓPAI KÖZÖSSÉGEK
(Az EK-Szerződés/Euratom-Szerződés alapján elfogadott jogi aktusok, amelyek közzététele kötelező) RENDELETEK
 2009.6.16. Az Európai Unió Hivatalos Lapja L 152/1 I (Az EK-Szerződés/Euratom-Szerződés alapján elfogadott jogi aktusok, amelyek közzététele kötelező) RENDELETEK AZ EURÓPAI PARLAMENT ÉS A TANÁCS 469/2009/EK
2009.6.16. Az Európai Unió Hivatalos Lapja L 152/1 I (Az EK-Szerződés/Euratom-Szerződés alapján elfogadott jogi aktusok, amelyek közzététele kötelező) RENDELETEK AZ EURÓPAI PARLAMENT ÉS A TANÁCS 469/2009/EK
SPC kiegészítő oltalmi tanúsítvány
 SPC kiegészítő oltalmi tanúsítvány MIE konferencia Mátraháza, 2011. május 26-27. Szentpéteri Zsolt szabadalmi ügyvivő SPC 1.) Forgalomba hozatali engedélyekkel kapcsolatos problémák 2.) Vizsgálattal kapcsolatos
SPC kiegészítő oltalmi tanúsítvány MIE konferencia Mátraháza, 2011. május 26-27. Szentpéteri Zsolt szabadalmi ügyvivő SPC 1.) Forgalomba hozatali engedélyekkel kapcsolatos problémák 2.) Vizsgálattal kapcsolatos
Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért
 1996R1610 HU 01.07.2013 003.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS 1610/96/EK RENDELETE
1996R1610 HU 01.07.2013 003.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS 1610/96/EK RENDELETE
Incyte from the inside EGY MAGYAR SPC ÜGY AZ EURÓPAI UNIÓ BÍRÓSÁGA ELŐTT
 Incyte from the inside EGY MAGYAR SPC ÜGY AZ EURÓPAI UNIÓ BÍRÓSÁGA ELŐTT Miről lesz szó? Kiegészítő oltalmi tanúsítványok időtartama (SPC) Seattle Genetics ügy (C-471/14.) Incyte Corp. ügy (C-492/16.)
Incyte from the inside EGY MAGYAR SPC ÜGY AZ EURÓPAI UNIÓ BÍRÓSÁGA ELŐTT Miről lesz szó? Kiegészítő oltalmi tanúsítványok időtartama (SPC) Seattle Genetics ügy (C-471/14.) Incyte Corp. ügy (C-492/16.)
VII. FEJEZET A gyógyszerek és a növényvédő szerek kiegészítő oltalmi tanúsítványával összefüggő ügyek
 VII. FEJEZET A gyógyszerek és a növényvédő szerek kiegészítő oltalmi tanúsítványával összefüggő ügyek I. A kiegészítő oltalmi tanúsítványokkal kapcsolatos ügyek intézésének általános rendje...3 1. Jogszabályi
VII. FEJEZET A gyógyszerek és a növényvédő szerek kiegészítő oltalmi tanúsítványával összefüggő ügyek I. A kiegészítő oltalmi tanúsítványokkal kapcsolatos ügyek intézésének általános rendje...3 1. Jogszabályi
Az Európai Unió Tanácsa Brüsszel, március 14. (OR. en)
 Az Európai Unió Tanácsa Brüsszel, 2017. március 14. (OR. en) Intézményközi referenciaszám: 2017/0005 (NLE) 5347/17 JOGALKOTÁSI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: AELE 5 EEE 2 N 3 ISL 2 FL 2 MI 41 ECO 6 SAN
Az Európai Unió Tanácsa Brüsszel, 2017. március 14. (OR. en) Intézményközi referenciaszám: 2017/0005 (NLE) 5347/17 JOGALKOTÁSI AKTUSOK ÉS EGYÉB ESZKÖZÖK Tárgy: AELE 5 EEE 2 N 3 ISL 2 FL 2 MI 41 ECO 6 SAN
Engedélyezési útmutató. I. A már létező ÁÉKBV-k és ABA-k PPA-ként történő engedélyezésének közös szabályai
 2018. november 12. Engedélyezési útmutató az Európai Parlament és a Tanács 2017. június 14-i (EU) 2017/1131 számú EU Rendelete által szabályozott pénzpiaci alapként (PPA) történő engedélyezésre irányuló
2018. november 12. Engedélyezési útmutató az Európai Parlament és a Tanács 2017. június 14-i (EU) 2017/1131 számú EU Rendelete által szabályozott pénzpiaci alapként (PPA) történő engedélyezésre irányuló
EURÓPAI PARLAMENT. Ülésdokumentum
 EURÓPAI PARLAMENT 2004 Ülésdokumentum 2009 C6-0087/2006 2004/0217(COD) 16/03/2006 Közös álláspont Az Európai Parlament és a Tanács 2006. március 10-i rendelete a gyermekgyógyászati felhasználásra szánt
EURÓPAI PARLAMENT 2004 Ülésdokumentum 2009 C6-0087/2006 2004/0217(COD) 16/03/2006 Közös álláspont Az Európai Parlament és a Tanács 2006. március 10-i rendelete a gyermekgyógyászati felhasználásra szánt
A Neurim döntés következményei, avagy a 469/2009/EK rendelet célkitűzéseinek megvalósulása a gyakorlatban Olyan bizonytalan vagyok, vagy mégsem?
 A Neurim döntés következményei, avagy a 469/2009/EK rendelet célkitűzéseinek megvalósulása a gyakorlatban Olyan bizonytalan vagyok, vagy mégsem? Buzásné Nagy Zsuzsanna Iparjogvédelmi Főosztály Richter
A Neurim döntés következményei, avagy a 469/2009/EK rendelet célkitűzéseinek megvalósulása a gyakorlatban Olyan bizonytalan vagyok, vagy mégsem? Buzásné Nagy Zsuzsanna Iparjogvédelmi Főosztály Richter
(Kötelezően közzéteendő jogi aktusok)
 2006.12.27. L 378/1 I (Kötelezően közzéteendő jogi aktusok) AZ EURÓPAI PARLAMENT ÉS A TANÁCS 1901/2006/EK RENDELETE (2006. december 12.) a gyermekgyógyászati felhasználásra szánt gyógyszerkészítményekről,
2006.12.27. L 378/1 I (Kötelezően közzéteendő jogi aktusok) AZ EURÓPAI PARLAMENT ÉS A TANÁCS 1901/2006/EK RENDELETE (2006. december 12.) a gyermekgyógyászati felhasználásra szánt gyógyszerkészítményekről,
I. fejezet. Általános rendelkezések. II. fejezet
 78/2004. (IV. 19.) Korm. rendelet a mezőgazdasági termékek és az élelmiszerek földrajzi árujelzőinek oltalmára vonatkozó részletes szabályokról 2005. november 1-jétől hatályos szöveg A védjegyek és a földrajzi
78/2004. (IV. 19.) Korm. rendelet a mezőgazdasági termékek és az élelmiszerek földrajzi árujelzőinek oltalmára vonatkozó részletes szabályokról 2005. november 1-jétől hatályos szöveg A védjegyek és a földrajzi
GYÓGYTERMÉKEK JELENE ÉS JÖVŐJE
 GYÓGYTERMÉKEK JELENE ÉS JÖVŐJE Sárvár 2011. március 24. Országos Gyógyszerészeti Intézet Dr. Szepezdi Zsuzsanna főigazgató A természetes anyagok (növényi szerek) szabályozására 1987-ben került sor elsőként
GYÓGYTERMÉKEK JELENE ÉS JÖVŐJE Sárvár 2011. március 24. Országos Gyógyszerészeti Intézet Dr. Szepezdi Zsuzsanna főigazgató A természetes anyagok (növényi szerek) szabályozására 1987-ben került sor elsőként
1995. évi XXXIII. törvény a találmányok szabadalmi oltalmáról
 A Szabadalom 1995. évi XXXIII. törvény a találmányok szabadalmi oltalmáról ELSŐ RÉSZ A TALÁLMÁNY ÉS A SZABADALOM I. A szabadalmi oltalom tárgya II. A találmányból és a szabadalmi oltalomból eredő jogok
A Szabadalom 1995. évi XXXIII. törvény a találmányok szabadalmi oltalmáról ELSŐ RÉSZ A TALÁLMÁNY ÉS A SZABADALOM I. A szabadalmi oltalom tárgya II. A találmányból és a szabadalmi oltalomból eredő jogok
Közbeszerzési Hatóság közleménye
 Közbeszerzési Hatóság közleménye A Közbeszerzési Hatóság - a közbeszerzésekről szóló 2015. évi CXLIII. törvény (a továbbiakban: Kbt.) 187. (2) bekezdésének ab) alpontjával, valamint az r) ponttal összhangban
Közbeszerzési Hatóság közleménye A Közbeszerzési Hatóság - a közbeszerzésekről szóló 2015. évi CXLIII. törvény (a továbbiakban: Kbt.) 187. (2) bekezdésének ab) alpontjával, valamint az r) ponttal összhangban
KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY ÉS ADATKIZÁRÓLAGOSSÁG MAGYARORSZÁGON GÁL MELINDA S. B. G. & K. SZABADALMI ÜGYVIVŐI IRODA
 KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY ÉS ADATKIZÁRÓLAGOSSÁG MAGYARORSZÁGON GÁL MELINDA S. B. G. & K. SZABADALMI ÜGYVIVŐI IRODA ÚJ OLTALMI FORMÁK AZ IPARJOGVÉDELEMBEN CSATLAKOZÁS AZ EU-HOZ 2004. MÁJUS 1. EU JOGANYAGÁNAK
KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY ÉS ADATKIZÁRÓLAGOSSÁG MAGYARORSZÁGON GÁL MELINDA S. B. G. & K. SZABADALMI ÜGYVIVŐI IRODA ÚJ OLTALMI FORMÁK AZ IPARJOGVÉDELEMBEN CSATLAKOZÁS AZ EU-HOZ 2004. MÁJUS 1. EU JOGANYAGÁNAK
SZLMK Gyógyszer. Közbeszerzési Értesítő száma: 2017/223. Eljárás fajtája: Közzététel dátuma: Iktatószám: 17822/2017 CPV Kód:
 SZLMK Gyógyszer Közbeszerzési Értesítő száma: 2017/223 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa: Helyesbítés/2015 EUHL Eljárás fajtája: Közzététel dátuma: 2017.12.08. Iktatószám: 17822/2017 CPV
SZLMK Gyógyszer Közbeszerzési Értesítő száma: 2017/223 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa: Helyesbítés/2015 EUHL Eljárás fajtája: Közzététel dátuma: 2017.12.08. Iktatószám: 17822/2017 CPV
Javaslat A BIZOTTSÁG /.../EK RENDELETE
 Javaslat A BIZOTTSÁG /.../EK RENDELETE [ ] a légi járművek és kapcsolódó termékek, alkatrészek és berendezések légialkalmassági és környezetvédelmi tanúsítása, valamint a tervező és gyártó szervezetek
Javaslat A BIZOTTSÁG /.../EK RENDELETE [ ] a légi járművek és kapcsolódó termékek, alkatrészek és berendezések légialkalmassági és környezetvédelmi tanúsítása, valamint a tervező és gyártó szervezetek
összefoglalás Hasznosítás? + Értékesítés Megadás/fenntart Publikáció Publikáció
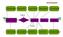 összefoglalás Technika állása Előzetes UV Írásos vélem. Újdonság kut. Érd.vizsg.kérés Publikáció Kutatás/fejlesztés - Hasznosítás? + Gyártáselők. Gyártás Értékesítés Publikáció Titokvédelem Hazai bejelentés
összefoglalás Technika állása Előzetes UV Írásos vélem. Újdonság kut. Érd.vizsg.kérés Publikáció Kutatás/fejlesztés - Hasznosítás? + Gyártáselők. Gyártás Értékesítés Publikáció Titokvédelem Hazai bejelentés
EURÓPAI BIZOTTSÁG EGÉSZSÉGÜGYI ÉS ÉLELMISZERBIZTONSÁGI FŐIGAZGATÓSÁG
 EURÓPAI BIZOTTSÁG EGÉSZSÉGÜGYI ÉS ÉLELMISZERBIZTONSÁGI FŐIGAZGATÓSÁG Brüsszel, 2019. február 18. REV2 A 2018. október 2-án közzétett kérdések és válaszok (REV1) helyébe lép KÉRDÉSEK ÉS VÁLASZOK AZ EGYESÜLT
EURÓPAI BIZOTTSÁG EGÉSZSÉGÜGYI ÉS ÉLELMISZERBIZTONSÁGI FŐIGAZGATÓSÁG Brüsszel, 2019. február 18. REV2 A 2018. október 2-án közzétett kérdések és válaszok (REV1) helyébe lép KÉRDÉSEK ÉS VÁLASZOK AZ EGYESÜLT
Az Európai Parlament és a Tanács 2004/24/EK irányelve. (2004. március 31.)
 Az Európai Parlament és a Tanács 2004/24/EK irányelve (2004. március 31.) az emberi felhasználásra szánt gyógyszerek közösségi kódexéről szóló 2001/83/EK irányelvnek a hagyományos növényi gyógyszerek tekintetében
Az Európai Parlament és a Tanács 2004/24/EK irányelve (2004. március 31.) az emberi felhasználásra szánt gyógyszerek közösségi kódexéről szóló 2001/83/EK irányelvnek a hagyományos növényi gyógyszerek tekintetében
Dr. Kőszeginé dr. Szalai Hilda Főigazgató-helyettes november
 Gyógyszerengedélyezés az Európai Unióban és hazánkban Dr. Kőszeginé dr. Szalai Hilda Főigazgató-helyettes 2014. november Témakörök A gyógyszerengedélyezés, mint a gyógyszerpiac szabályozásának kulcseleme
Gyógyszerengedélyezés az Európai Unióban és hazánkban Dr. Kőszeginé dr. Szalai Hilda Főigazgató-helyettes 2014. november Témakörök A gyógyszerengedélyezés, mint a gyógyszerpiac szabályozásának kulcseleme
Magyar joganyagok - 30/2005. (VIII. 2.) EüM rendelet - az emberi alkalmazásra kerül 2. oldal g) szükség esetén egyéb különleges figyelmeztetést; h) a
 Magyar joganyagok - 30/2005. (VIII. 2.) EüM rendelet - az emberi alkalmazásra kerül 1. oldal 30/2005. (VIII. 2.) EüM rendelet az emberi alkalmazásra kerülő gyógyszerek címkéjéről és betegtájékoztatójáról
Magyar joganyagok - 30/2005. (VIII. 2.) EüM rendelet - az emberi alkalmazásra kerül 1. oldal 30/2005. (VIII. 2.) EüM rendelet az emberi alkalmazásra kerülő gyógyszerek címkéjéről és betegtájékoztatójáról
Zsámbék Város Képviselő-testületének 22/2008. (VII.01.) számú R E N D E L E T E
 Zsámbék Város Képviselő-testületének 22/2008. (VII.01.) számú R E N D E L E T E Zsámbék Város közigazgatási területén működő üzletek éjszakai nyitva tartásának rendjéről Zsámbék Város Képviselő-testülete
Zsámbék Város Képviselő-testületének 22/2008. (VII.01.) számú R E N D E L E T E Zsámbék Város közigazgatási területén működő üzletek éjszakai nyitva tartásának rendjéről Zsámbék Város Képviselő-testülete
449/2017. (XII. 27.) Korm. rendelet a gyógyszerekkel folytatott nagykereskedelmi és párhuzamos importtevékenység végzésének engedélyezéséről
 449/2017. (XII. 27.) Korm. rendelet a gyógyszerekkel folytatott nagykereskedelmi és párhuzamos importtevékenység végzésének engedélyezéséről hatályos: 2018.01.01 - A Kormány az emberi alkalmazásra kerülő
449/2017. (XII. 27.) Korm. rendelet a gyógyszerekkel folytatott nagykereskedelmi és párhuzamos importtevékenység végzésének engedélyezéséről hatályos: 2018.01.01 - A Kormány az emberi alkalmazásra kerülő
Magyar joganyagok - 19/2005. (IV. 12.) GKM rendelet - a Magyar Szabadalmi Hivatal 2. oldal (6) Nukleotid- vagy aminosav-szekvenciák feltárását tartalm
 Magyar joganyagok - 19/2005. (IV. 12.) GKM rendelet - a Magyar Szabadalmi Hivatal 1. oldal 19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási
Magyar joganyagok - 19/2005. (IV. 12.) GKM rendelet - a Magyar Szabadalmi Hivatal 1. oldal 19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási
448/2017. (XII. 27.) Korm. rendelet az emberi felhasználásra kerülő gyógyszerek egyedi rendelésének és felhasználásának engedélyezéséről
 448/2017. (XII. 27.) Korm. rendelet az emberi felhasználásra kerülő gyógyszerek egyedi rendelésének és felhasználásának engedélyezéséről hatályos: 2018.01.01-2018.01.01 A Kormány az emberi alkalmazásra
448/2017. (XII. 27.) Korm. rendelet az emberi felhasználásra kerülő gyógyszerek egyedi rendelésének és felhasználásának engedélyezéséről hatályos: 2018.01.01-2018.01.01 A Kormány az emberi alkalmazásra
SPC, Bolar kivétel: forradalmi változások kezdete? Buzásné Nagy Zsuzsanna Richter Gedeon Nyrt.
 SPC, Bolar kivétel: forradalmi változások kezdete? Buzásné Nagy Zsuzsanna Richter Gedeon Nyrt. Iparjogvédelmi Konferencia 2018. május 10-11. Szilvásvárad SPC reform, gyártási kivétel bevezetése A kiegészítő
SPC, Bolar kivétel: forradalmi változások kezdete? Buzásné Nagy Zsuzsanna Richter Gedeon Nyrt. Iparjogvédelmi Konferencia 2018. május 10-11. Szilvásvárad SPC reform, gyártási kivétel bevezetése A kiegészítő
Járulékok, biztosítási kötelezettség
 Járulékok, biztosítási kötelezettség 1. Kérdés: Egy Magyarországon bejegyzett betéti társaság beltagja - aki a társaság tevékenységében személyesen közreműködik - román állampolgár, Romániában van munkaviszonyból
Járulékok, biztosítási kötelezettség 1. Kérdés: Egy Magyarországon bejegyzett betéti társaság beltagja - aki a társaság tevékenységében személyesen közreműködik - román állampolgár, Romániában van munkaviszonyból
A hazai K+F+I pályázatok iparjogvédelmi vonatkozásai
 A hazai K+F+I pályázatok iparjogvédelmi vonatkozásai Németh Gábor Szellemi Tulajdon Nemzeti Hivatala Múlt jelen jövő a szellemi tulajdon világában MIE szakmai konferencia, Visegrád, 2015. november 25.
A hazai K+F+I pályázatok iparjogvédelmi vonatkozásai Németh Gábor Szellemi Tulajdon Nemzeti Hivatala Múlt jelen jövő a szellemi tulajdon világában MIE szakmai konferencia, Visegrád, 2015. november 25.
A Kormány. Korm. rendelete. a rendvédelmi feladatokat ellátó szervek személyi állományának kártalanításáról
 TERVEZET! A Kormány /2016. ( ) Korm. rendelete a rendvédelmi feladatokat ellátó szervek személyi állományának kártalanításáról A Kormány a rendvédelmi feladatokat ellátó szervek hivatásos állományának
TERVEZET! A Kormány /2016. ( ) Korm. rendelete a rendvédelmi feladatokat ellátó szervek személyi állományának kártalanításáról A Kormány a rendvédelmi feladatokat ellátó szervek hivatásos állományának
A BIZOTTSÁG 712/2012/EU RENDELETE
 L 209/4 Az Európai Unió Hivatalos Lapja 2012.8.4. A BIZOTTSÁG 712/2012/EU RENDELETE (2012. augusztus 3.) az emberi, illetve állatgyógyászati felhasználásra szánt gyógyszerkészítmények forgalombahozatali
L 209/4 Az Európai Unió Hivatalos Lapja 2012.8.4. A BIZOTTSÁG 712/2012/EU RENDELETE (2012. augusztus 3.) az emberi, illetve állatgyógyászati felhasználásra szánt gyógyszerkészítmények forgalombahozatali
A TANULMÁNYOK ELISMERÉSÉRE VONATKOZÓ SZABÁLYOK AZ OKLEVELES KÖNYVVIZSGÁLÓI KÉPZÉSI PROGRAMBAN
 3. SZÁMÚ MELLÉKLET Az okleveles könyvvizsgálói szakképzési és vizsgaszabályzathoz A TANULMÁNYOK ELISMERÉSÉRE VONATKOZÓ SZABÁLYOK AZ OKLEVELES KÖNYVVIZSGÁLÓI KÉPZÉSI PROGRAMBAN [ Kkt. 95. (1) A szakképzést
3. SZÁMÚ MELLÉKLET Az okleveles könyvvizsgálói szakképzési és vizsgaszabályzathoz A TANULMÁNYOK ELISMERÉSÉRE VONATKOZÓ SZABÁLYOK AZ OKLEVELES KÖNYVVIZSGÁLÓI KÉPZÉSI PROGRAMBAN [ Kkt. 95. (1) A szakképzést
19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól
 19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól Az iparjogvédelmi eljárások igazgatási szolgáltatási díjáról szóló 1992. évi
19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól Az iparjogvédelmi eljárások igazgatási szolgáltatási díjáról szóló 1992. évi
NEMZETI TESTÜLET. Nemzeti Akkreditálási Rendszer. szervezetek minõsítési NAR-01M. Hatálybalépés: 2008. november 1. 3. kiadás
 NEMZETI AKKREDITÁLÓ TESTÜLET Nemzeti Akkreditálási Rendszer Vizsgáló, ellenõrzõ és tanúsító szervezetek minõsítési eljárása kijelöléshez NAR-01M 3. kiadás Hatálybalépés: 2008. november 1. Tartalomjegyzék
NEMZETI AKKREDITÁLÓ TESTÜLET Nemzeti Akkreditálási Rendszer Vizsgáló, ellenõrzõ és tanúsító szervezetek minõsítési eljárása kijelöléshez NAR-01M 3. kiadás Hatálybalépés: 2008. november 1. Tartalomjegyzék
Tájékoztató a jogszabályi kötelezettségen alapuló könyvvizsgálói tevékenység végzéséhez szükséges igazolásról
 1 Tájékoztató a jogszabályi kötelezettségen alapuló könyvvizsgálói tevékenység végzéséhez szükséges igazolásról A Magyar Könyvvizsgálói Kamaráról, a könyvvizsgálói tevékenységről, valamint a könyvvizsgálói
1 Tájékoztató a jogszabályi kötelezettségen alapuló könyvvizsgálói tevékenység végzéséhez szükséges igazolásról A Magyar Könyvvizsgálói Kamaráról, a könyvvizsgálói tevékenységről, valamint a könyvvizsgálói
az január 1 je elıtt benyújtott bejelentések alapján esedékessé vált díjakra vonatkozóan
 Az ipari és kereskedelmi miniszter 77/1995. (XII. 29.) IKM rendelete a Magyar Szabadalmi Hivatal elıtti iparjogvédelmi eljárások igazgatási szolgáltatási díjáról az 1996. január 1 je elıtt benyújtott bejelentések
Az ipari és kereskedelmi miniszter 77/1995. (XII. 29.) IKM rendelete a Magyar Szabadalmi Hivatal elıtti iparjogvédelmi eljárások igazgatási szolgáltatási díjáról az 1996. január 1 je elıtt benyújtott bejelentések
A gazdasági és közlekedési miniszter. /2006. (...) GKM rendelete. a kereskedelmi szakértői tevékenység engedélyezéséről
 A gazdasági és közlekedési miniszter /2006. (...) GKM rendelete a kereskedelmi szakértői tevékenység engedélyezéséről A kereskedelemről szóló 2005. évi CLXIV. törvény 12. -a (2) bekezdésének c) pontjában
A gazdasági és közlekedési miniszter /2006. (...) GKM rendelete a kereskedelmi szakértői tevékenység engedélyezéséről A kereskedelemről szóló 2005. évi CLXIV. törvény 12. -a (2) bekezdésének c) pontjában
Hatóanyag vs. adjuváns/excipiens. Avagy miért nem hatóanyag egy ható anyag?
 Hatóanyag vs. adjuváns/excipiens Avagy miért nem hatóanyag egy ható anyag? A kérdések A kezdetek C-431/04 MIT A gyógyszer hatóanyag-kombinációja fogalom megköveteli-e, hogy a kombináció alkotórészei mind
Hatóanyag vs. adjuváns/excipiens Avagy miért nem hatóanyag egy ható anyag? A kérdések A kezdetek C-431/04 MIT A gyógyszer hatóanyag-kombinációja fogalom megköveteli-e, hogy a kombináció alkotórészei mind
FT-1180/SZTE/ /T/2018/SZTE - Komplett Hibrid műtő kialakítása és szállítása - részvételi felhívás 2. korrigendum
 FT-1180/SZTE/2018-20/T/2018/SZTE - Komplett Hibrid műtő kialakítása és szállítása - részvételi felhívás 2. korrigendum Közbeszerzési Értesítő száma: 2018/105 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa:
FT-1180/SZTE/2018-20/T/2018/SZTE - Komplett Hibrid műtő kialakítása és szállítása - részvételi felhívás 2. korrigendum Közbeszerzési Értesítő száma: 2018/105 Beszerzés tárgya: Árubeszerzés Hirdetmény típusa:
19/2005. (IV. 12.) GKM rendelet. a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól
 19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól Az iparjogvédelmi eljárások igazgatási szolgáltatási díjáról szóló 1992. évi
19/2005. (IV. 12.) GKM rendelet a Magyar Szabadalmi Hivatal előtti iparjogvédelmi eljárások igazgatási szolgáltatási díjairól Az iparjogvédelmi eljárások igazgatási szolgáltatási díjáról szóló 1992. évi
A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK. Jobb gyermekgyógyszerek: az elképzeléstől a megvalósításig
 EURÓPAI BIZOTTSÁG Brüsszel, 2013.6.24. COM(2013) 443 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK Jobb gyermekgyógyszerek: az elképzeléstől a megvalósításig Általános jelentés a ti
EURÓPAI BIZOTTSÁG Brüsszel, 2013.6.24. COM(2013) 443 final A BIZOTTSÁG JELENTÉSE AZ EURÓPAI PARLAMENTNEK ÉS A TANÁCSNAK Jobb gyermekgyógyszerek: az elképzeléstől a megvalósításig Általános jelentés a ti
Szabadalmi bejelentési kérelem
 Szellemi Tulajdon Nemzeti Hivatala Budapest Garibaldi u. 2. 1054 A Hivatal tölti ki Szabadalmi bejelentési kérelem Kérem az alábbi találmányra a szabadalmi oltalom megadását az 1995. évi XXXIII. törvény
Szellemi Tulajdon Nemzeti Hivatala Budapest Garibaldi u. 2. 1054 A Hivatal tölti ki Szabadalmi bejelentési kérelem Kérem az alábbi találmányra a szabadalmi oltalom megadását az 1995. évi XXXIII. törvény
Az emberi erőforrások minisztere..../2013. ( ) EMMI rendelete
 A tervezetet a Kormány nem tárgyalta meg, ezért az nem tekinthető a Kormány álláspontjának. Az emberi erőforrások minisztere.../2013. ( ) EMMI rendelete a biocid termékek előállításának és forgalomba hozatalának
A tervezetet a Kormány nem tárgyalta meg, ezért az nem tekinthető a Kormány álláspontjának. Az emberi erőforrások minisztere.../2013. ( ) EMMI rendelete a biocid termékek előállításának és forgalomba hozatalának
1969. évi II. törvény
 1969. évi II. törvény a találmányok szabadalmi oltalmáról, egységes szerkezetben a végrehajtásáról szóló 4/1969. (XII. 28.) OMFB-IM együttes rendelettel, valamint a 9/1969. (XII. 28.) IM rendelettel [Vastag
1969. évi II. törvény a találmányok szabadalmi oltalmáról, egységes szerkezetben a végrehajtásáról szóló 4/1969. (XII. 28.) OMFB-IM együttes rendelettel, valamint a 9/1969. (XII. 28.) IM rendelettel [Vastag
MELLÉKLETEK. a következőhöz: A BIZOTTSÁG VÉGREHAJTÁSI RENDELETE
 EURÓPAI BIZOTTSÁG Brüsszel, 2018.4.4. C(2018) 1866 final ANNEES 1 to 3 MELLÉKLETEK a következőhöz: A BIZOTTSÁG VÉGREHAJTÁSI RENDELETE az (EU) 2016/797 európai parlamenti és tanácsi irányelv alapján a vasúti
EURÓPAI BIZOTTSÁG Brüsszel, 2018.4.4. C(2018) 1866 final ANNEES 1 to 3 MELLÉKLETEK a következőhöz: A BIZOTTSÁG VÉGREHAJTÁSI RENDELETE az (EU) 2016/797 európai parlamenti és tanácsi irányelv alapján a vasúti
I. A SZABADALMI JOG II.
 E-jog 2013 11. előad adás Iparjogvédelem 2. Áttekintés: I.1 A szabadalmi oltalom keletkezése és megszűnése I.2 A találmányhoz és szabadalomhoz fűződő jogok védelme I.3 Hatósági, bírósági eljárás szabadalmi
E-jog 2013 11. előad adás Iparjogvédelem 2. Áttekintés: I.1 A szabadalmi oltalom keletkezése és megszűnése I.2 A találmányhoz és szabadalomhoz fűződő jogok védelme I.3 Hatósági, bírósági eljárás szabadalmi
Gyógyszerengedélyezés hazánkban és az Európai Unióban. Dr. Kıszeginé dr. Szalai Hilda Fıigazgató-helyettes
 Gyógyszerengedélyezés hazánkban és az Európai Unióban Dr. Kıszeginé dr. Szalai Hilda Fıigazgató-helyettes Témakörök A gyógyszerengedélyezés, mint a gyógyszerpiac szabályozásának kulcseleme A gyógyszerengedélyezés
Gyógyszerengedélyezés hazánkban és az Európai Unióban Dr. Kıszeginé dr. Szalai Hilda Fıigazgató-helyettes Témakörök A gyógyszerengedélyezés, mint a gyógyszerpiac szabályozásának kulcseleme A gyógyszerengedélyezés
Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért
 2008R1234 HU 04.08.2013 002.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B A BIZOTTSÁG 1234/2008/EK RENDELETE (2008. november 24.)
2008R1234 HU 04.08.2013 002.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B A BIZOTTSÁG 1234/2008/EK RENDELETE (2008. november 24.)
A KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY HÁROM ÉVE MAGYARORSZÁGON
 Boros István, Buzásné Nagy Zsuzsanna, Csutorás Lászlóné A KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY HÁROM ÉVE MAGYARORSZÁGON A gyógyszerek és növényvédő szerek kiegészítő oltalmi tanúsítványának (SPC) mint új oltalmi
Boros István, Buzásné Nagy Zsuzsanna, Csutorás Lászlóné A KIEGÉSZÍTŐ OLTALMI TANÚSÍTVÁNY HÁROM ÉVE MAGYARORSZÁGON A gyógyszerek és növényvédő szerek kiegészítő oltalmi tanúsítványának (SPC) mint új oltalmi
ESPD és a nyilatkozati elv, öntisztázás. Soós Gábor LL.M. Magyar Fejlesztési Bank Zrt.
 ESPD és a nyilatkozati elv, öntisztázás Soós Gábor LL.M. Magyar Fejlesztési Bank Zrt. I. Egységes európai közbeszerzési dokumentum (ESPD) [nyilatkozati elv az uniós eljárásrendben] II. Öntisztázás (self-cleaning)
ESPD és a nyilatkozati elv, öntisztázás Soós Gábor LL.M. Magyar Fejlesztési Bank Zrt. I. Egységes európai közbeszerzési dokumentum (ESPD) [nyilatkozati elv az uniós eljárásrendben] II. Öntisztázás (self-cleaning)
Eger Megyei Jogú Város Önkormányzat Közgyűlése 4/1992. (II. 11.) önkormányzati rendelete Az Eger város nevének, címerének és zászlajának használatáról
 Eger Megyei Jogú Város Önkormányzat Közgyűlése 4/1992. (II. 11.) önkormányzati rendelete Az Eger város nevének, címerének és zászlajának használatáról Módosította: 33/2006. (IX.01.) önkormányzati rendelet
Eger Megyei Jogú Város Önkormányzat Közgyűlése 4/1992. (II. 11.) önkormányzati rendelete Az Eger város nevének, címerének és zászlajának használatáról Módosította: 33/2006. (IX.01.) önkormányzati rendelet
Részletes vitát lezáró bizottsági módosító javaslat
 Iromány száma: T/1659/2. Benyújtás dátuma: 2018-10-09 16:32 Az Országgyűlés Igazságügyi bizottsága Parlex azonosító: 1557DKFF0001 Címzett: Kövér László, az Országgyűlés elnöke Benyújtó: Dr. Vejkey Imre,
Iromány száma: T/1659/2. Benyújtás dátuma: 2018-10-09 16:32 Az Országgyűlés Igazságügyi bizottsága Parlex azonosító: 1557DKFF0001 Címzett: Kövér László, az Országgyűlés elnöke Benyújtó: Dr. Vejkey Imre,
Tanácsi ügyek felgyorsításának lehetőségei
 Tanácsi ügyek felgyorsításának lehetőségei Dr. Mikló Katalin SZTNH Szabadalmi Fórum 2014. április 23. Jogszabályi háttér Megsemmisítési eljárás - feltételei (Szt. 42. ) - eljárási szabályok (Szt. 80.,
Tanácsi ügyek felgyorsításának lehetőségei Dr. Mikló Katalin SZTNH Szabadalmi Fórum 2014. április 23. Jogszabályi háttér Megsemmisítési eljárás - feltételei (Szt. 42. ) - eljárási szabályok (Szt. 80.,
Az eredetmegjelölések oltalmára és nemzetközi lajstromozására vonatkozó Lisszaboni Megállapodáshoz kapcsolódó Végrehajtási Szabályzat. I.
 Az eredetmegjelölések oltalmára és nemzetközi lajstromozására vonatkozó Lisszaboni Megállapodáshoz I. fejezet ÁLTALÁNOS RENDELKEZÉSEK 1. szabály Rövidített kifejezések E Szabályzat alkalmazásában (i) Megállapodás:
Az eredetmegjelölések oltalmára és nemzetközi lajstromozására vonatkozó Lisszaboni Megállapodáshoz I. fejezet ÁLTALÁNOS RENDELKEZÉSEK 1. szabály Rövidített kifejezések E Szabályzat alkalmazásában (i) Megállapodás:
AZ EURÓPAI PARLAMENT ÉS A TANÁCS 141/2000/EK RENDELETE (1999. december 16.) a ritka betegségek gyógyszereiről (HL L 18., , 1. o.
 2000R0141 HU 07.08.2009 001.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS 141/2000/EK RENDELETE
2000R0141 HU 07.08.2009 001.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B AZ EURÓPAI PARLAMENT ÉS A TANÁCS 141/2000/EK RENDELETE
Lőrinci Város Önkormányzata Képviselőtestületének. 8/2006. (V. 25.) önkormányzati RENDELETE. A gyermekek védelméről. Rendelet-módosítási javaslat
 Jelenlegi szabályozás Lőrinci Város Önkormányzata Képviselő-testületének 8/2006. (V. 25.) önkormányzati RENDELETE A gyermekek védelméről Lőrinci Város Önkormányzatának Képviselő-testülete (továbbiakban:
Jelenlegi szabályozás Lőrinci Város Önkormányzata Képviselő-testületének 8/2006. (V. 25.) önkormányzati RENDELETE A gyermekek védelméről Lőrinci Város Önkormányzatának Képviselő-testülete (továbbiakban:
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA A BIZOTTSÁG HATÁROZATA
 AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 16.12.2008 C(2008)8731 NEM KÖZZÉTÉTELRE A BIZOTTSÁG HATÁROZATA 16.12.2008 a(z) "Onsior - Robenacoxib" állatgyógyászati készítmény forgalomba hozatalának a 726/2004/EK
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 16.12.2008 C(2008)8731 NEM KÖZZÉTÉTELRE A BIZOTTSÁG HATÁROZATA 16.12.2008 a(z) "Onsior - Robenacoxib" állatgyógyászati készítmény forgalomba hozatalának a 726/2004/EK
T/4818. számú törvényjavaslat. a géntechnológiai tevékenységről szóló 1998. évi XXVII. törvény módosításáról
 MAGYARORSZÁG KORMÁNYA T/4818. számú törvényjavaslat a géntechnológiai tevékenységről szóló 1998. évi XXVII. törvény módosításáról Előadó: Dr. Fazekas Sándor földművelésügyi miniszter Budapest, 2015. május
MAGYARORSZÁG KORMÁNYA T/4818. számú törvényjavaslat a géntechnológiai tevékenységről szóló 1998. évi XXVII. törvény módosításáról Előadó: Dr. Fazekas Sándor földművelésügyi miniszter Budapest, 2015. május
1 MUNKAANYAG A MINISZTÉRIUM VÉGSŐ ÁLLÁSPONTJÁT NEM TÜKRÖZI A földművelésügyi és vidékfejlesztési miniszter
 1 A földművelésügyi és vidékfejlesztési miniszter /2008. ( ) FVM rendelete a növényvédő szerek forgalomba hozatalának és felhasználásának engedélyezéséről, valamint a növényvédő szerek csomagolásáról,
1 A földművelésügyi és vidékfejlesztési miniszter /2008. ( ) FVM rendelete a növényvédő szerek forgalomba hozatalának és felhasználásának engedélyezéséről, valamint a növényvédő szerek csomagolásáról,
GYÓGYSZEREK FORGALOMBA HOZATALA
 GYÓGYSZEREK FORGALOMBA HOZATALA DR. ZELKÓ ROMÁNA EGYETEMI GYÓGYSZERTÁR GYÓGYSZERÜGYI SZERVEZÉSI INTÉZET 2015. 05. 04. KORÁBBAN: TÖRZSKÖNYVEZÉS Ma nem használjuk, mert az EU kizárólag a forgalomba hozatal
GYÓGYSZEREK FORGALOMBA HOZATALA DR. ZELKÓ ROMÁNA EGYETEMI GYÓGYSZERTÁR GYÓGYSZERÜGYI SZERVEZÉSI INTÉZET 2015. 05. 04. KORÁBBAN: TÖRZSKÖNYVEZÉS Ma nem használjuk, mert az EU kizárólag a forgalomba hozatal
Orgovány Nagyközség Önkormányzati Képviselőtestületének 11/2013.(IX.16.) önkormányzati rendelete
 Orgovány Nagyközség Önkormányzati Képviselőtestületének 11/2013.(IX.16.) önkormányzati rendelete A helyi civil szervezetek pénzügyi támogatásának rendjéről Orgovány Nagyközség Önkormányzati Képviselőtestülete
Orgovány Nagyközség Önkormányzati Képviselőtestületének 11/2013.(IX.16.) önkormányzati rendelete A helyi civil szervezetek pénzügyi támogatásának rendjéről Orgovány Nagyközség Önkormányzati Képviselőtestülete
II. Az import engedélyre vonatkozó tudnivalók
 This page can only be read in Magyar. II. Az import engedélyre vonatkozó tudnivalók 1.) Az import engedélyek kérelmezése Az AGRIM engedélyt kizárólag Behozatali kérelem adatlapon (AGRIM) lehet kérelmezni.
This page can only be read in Magyar. II. Az import engedélyre vonatkozó tudnivalók 1.) Az import engedélyek kérelmezése Az AGRIM engedélyt kizárólag Behozatali kérelem adatlapon (AGRIM) lehet kérelmezni.
TÁJÉKOZTATÓ A TŰZVÉDELMI TERVEZŐI JOGOSULTSÁGOKRÓL ÉS A JOGOSULTSÁG MEGÁLLAPÍTÁSÁNAK ELJÁRÁSÁRÓL. összeállította: Lengyelfi László
 TÁJÉKOZTATÓ A TŰZVÉDELMI TERVEZŐI JOGOSULTSÁGOKRÓL ÉS A JOGOSULTSÁG MEGÁLLAPÍTÁSÁNAK ELJÁRÁSÁRÓL összeállította: Lengyelfi László Az elmúlt időszakban a tervezői jogosultságok megszerzésével kapcsolatos
TÁJÉKOZTATÓ A TŰZVÉDELMI TERVEZŐI JOGOSULTSÁGOKRÓL ÉS A JOGOSULTSÁG MEGÁLLAPÍTÁSÁNAK ELJÁRÁSÁRÓL összeállította: Lengyelfi László Az elmúlt időszakban a tervezői jogosultságok megszerzésével kapcsolatos
Szellemitulajdon-védelem a K+F eredmények hasznosításában. ITD szeminárium Budapest, 2009 június 17
 Szellemitulajdon-védelem a K+F eredmények hasznosításában ITD szeminárium Budapest, 2009 június 17 Iparjogvédelmi oltalmi formák, szabadalom Szabadalom, publikálás vagy titoktartás Oltalomszerzés Magyarországon
Szellemitulajdon-védelem a K+F eredmények hasznosításában ITD szeminárium Budapest, 2009 június 17 Iparjogvédelmi oltalmi formák, szabadalom Szabadalom, publikálás vagy titoktartás Oltalomszerzés Magyarországon
E/1/2016. (VII.28.) számú H A T Á R O Z A T A
 A Semmelweis Egyetem Rektorának és Kancellárjának E/1/2016. (VII.28.) számú H A T Á R O Z A T A a Semmelweis Egyetem közalkalmazottainak külföldi tanulmányútjához, valamint munkavállalás és egyéb célból
A Semmelweis Egyetem Rektorának és Kancellárjának E/1/2016. (VII.28.) számú H A T Á R O Z A T A a Semmelweis Egyetem közalkalmazottainak külföldi tanulmányútjához, valamint munkavállalás és egyéb célból
A találmányok legrégibb hagyományokkal rendelkező jogi oltalmi formája a szabadalom.
 A találmányok legrégibb hagyományokkal rendelkező jogi oltalmi formája a szabadalom. A szabadalom jogintézménye a találmány alkotója, a feltaláló (illetve jogutódja) részére időleges és kizárólagos jellegű
A találmányok legrégibb hagyományokkal rendelkező jogi oltalmi formája a szabadalom. A szabadalom jogintézménye a találmány alkotója, a feltaláló (illetve jogutódja) részére időleges és kizárólagos jellegű
1991. évi XXXIX. törvény a mikroelektronikai félvezető termékek topográfiájának oltalmáról. I. Fejezet AZ OLTALOM TÁRGYA ÉS TARTALMA
 1991. évi XXXIX. törvény a mikroelektronikai félvezető termékek topográfiájának oltalmáról I. Fejezet AZ OLTALOM TÁRGYA ÉS TARTALMA Az oltalmazható topográfia 1. (1) Oltalomban részesülhet a mikroelektronikai
1991. évi XXXIX. törvény a mikroelektronikai félvezető termékek topográfiájának oltalmáról I. Fejezet AZ OLTALOM TÁRGYA ÉS TARTALMA Az oltalmazható topográfia 1. (1) Oltalomban részesülhet a mikroelektronikai
Originális és generikus gyógyszerek. Dr Szabó Mónika Bayer Hungária Kft 2014 március 19
 Originális és generikus gyógyszerek Dr Szabó Mónika Bayer Hungária Kft 2014 március 19 Gyógyszer életciklusa Originális és generikus K+F Originális kutatás-fejlesztés: 10-15 év, 300-1200M$ Felfedezés Preklinika
Originális és generikus gyógyszerek Dr Szabó Mónika Bayer Hungária Kft 2014 március 19 Gyógyszer életciklusa Originális és generikus K+F Originális kutatás-fejlesztés: 10-15 év, 300-1200M$ Felfedezés Preklinika
(Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL, SZERVEITŐL, HIVATALAITÓL ÉS ÜGYNÖKSÉGEITŐL SZÁRMAZÓ KÖZLEMÉNYEK EURÓPAI BIZOTTSÁG
 2013.8.2. Az Európai Unió Hivatalos Lapja C 223/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL, SZERVEITŐL, HIVATALAITÓL ÉS ÜGYNÖKSÉGEITŐL SZÁRMAZÓ KÖZLEMÉNYEK EURÓPAI BIZOTTSÁG Iránymutatás a különböző
2013.8.2. Az Európai Unió Hivatalos Lapja C 223/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL, SZERVEITŐL, HIVATALAITÓL ÉS ÜGYNÖKSÉGEITŐL SZÁRMAZÓ KÖZLEMÉNYEK EURÓPAI BIZOTTSÁG Iránymutatás a különböző
korrigendum - Könyvvizsgálati feladatok ellátása az állami egészségügyi ellátó központ kiemelt projektjei keretében 13 részben?.
 korrigendum - Könyvvizsgálati feladatok ellátása az állami egészségügyi ellátó központ kiemelt projektjei keretében 13 részben?. Közbeszerzési Értesítő száma: 2018/56 Beszerzés tárgya: Szolgáltatásmegrendelés
korrigendum - Könyvvizsgálati feladatok ellátása az állami egészségügyi ellátó központ kiemelt projektjei keretében 13 részben?. Közbeszerzési Értesítő száma: 2018/56 Beszerzés tárgya: Szolgáltatásmegrendelés
Ipolytölgyes községi Önkormányzat Képviselő-Testületének 7/2009.(V. 13.) számú rendelete a szociális ellátások helyi szabályozásáról.
 Ipolytölgyes községi Önkormányzat Képviselő-Testületének 7/2009.(V. 13.) számú rendelete a szociális ellátások helyi szabályozásáról. Ipolytölgyes község Önkormányzatának Képviselő-Testület a helyi önkormányzatokról
Ipolytölgyes községi Önkormányzat Képviselő-Testületének 7/2009.(V. 13.) számú rendelete a szociális ellátások helyi szabályozásáról. Ipolytölgyes község Önkormányzatának Képviselő-Testület a helyi önkormányzatokról
Javaslat A TANÁCS HATÁROZATA
 EURÓPAI BIZOTTSÁG Brüsszel, 2014.6.12. COM(2014) 351 final 2014/0179 (NLE) Javaslat A TANÁCS HATÁROZATA az Európai Unió által az EFTA Vegyes Bizottságban az EGT-megállapodás II. mellékletének módosításáról
EURÓPAI BIZOTTSÁG Brüsszel, 2014.6.12. COM(2014) 351 final 2014/0179 (NLE) Javaslat A TANÁCS HATÁROZATA az Európai Unió által az EFTA Vegyes Bizottságban az EGT-megállapodás II. mellékletének módosításáról
316/2013. (VIII. 28.) Korm. rendelet. a biocid termékek engedélyezésének és forgalomba hozatalának egyes szabályairól
 316/2013. (VIII. 28.) Korm. rendelet a biocid termékek engedélyezésének és forgalomba hozatalának egyes szabályairól Hatályos:2013. 09. 02-től A Kormány a kémiai biztonságról szóló 2000. évi XXV. törvény
316/2013. (VIII. 28.) Korm. rendelet a biocid termékek engedélyezésének és forgalomba hozatalának egyes szabályairól Hatályos:2013. 09. 02-től A Kormány a kémiai biztonságról szóló 2000. évi XXV. törvény
(az időközbeni módosításokkal egységes szerkezetben)
 Gárdony Város Önkormányzat Képviselő-testületének 39/2004. (IX. 29.) számú rendelete a személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12,13,14,15,
Gárdony Város Önkormányzat Képviselő-testületének 39/2004. (IX. 29.) számú rendelete a személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12,13,14,15,
1995R0297 HU
 1995R0297 HU 20.11.2005 003.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B A TANÁCS 297/95/EK RENDELETE (1995. február 10.) az
1995R0297 HU 20.11.2005 003.001 1 Ez a dokumentum kizárólag tájékoztató jellegű, az intézmények semmiféle felelősséget nem vállalnak a tartalmáért B A TANÁCS 297/95/EK RENDELETE (1995. február 10.) az
2. A rendelet célja a saját erőből történő lakáshoz jutás, a meglévő lakások szükség szerinti bővítésének, felújításának elősegítése.
 Csolnok Község Önkormányzata Képviselő-testületének 9/2005.(IX.23.) ökr. számú rendelete a lakáscélú helyi támogatásokról az azt módosító 11/2006. (V.05.) ökr. rendelettel egységes szerkezetben Csolnok
Csolnok Község Önkormányzata Képviselő-testületének 9/2005.(IX.23.) ökr. számú rendelete a lakáscélú helyi támogatásokról az azt módosító 11/2006. (V.05.) ökr. rendelettel egységes szerkezetben Csolnok
(Közlemények) BIZOTTSÁG (2008/C 243/01)
 2008.9.24. C 243/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ KÖZLEMÉNYEK BIZOTTSÁG A Bizottság közleménye Iránymutatás a gyermekgyógyászati vizsgálati terv jóváhagyásával vagy
2008.9.24. C 243/1 II (Közlemények) AZ EURÓPAI UNIÓ INTÉZMÉNYEITŐL ÉS SZERVEITŐL SZÁRMAZÓ KÖZLEMÉNYEK BIZOTTSÁG A Bizottság közleménye Iránymutatás a gyermekgyógyászati vizsgálati terv jóváhagyásával vagy
ELŐTERJESZTÉS. az egyes műszaki tárgyú miniszteri rendeletek módosításáról
 NEMZETI FEJLESZTÉSI ÉS GAZDASÁGI MINISZTÉRIUM NFGM/ /2009. ELŐTERJESZTÉS az egyes műszaki tárgyú miniszteri rendeletek módosításáról Budapest, 2009. augusztus 2 EGYEZTETÉSI LAP 1. Az egyeztetés alapadatai
NEMZETI FEJLESZTÉSI ÉS GAZDASÁGI MINISZTÉRIUM NFGM/ /2009. ELŐTERJESZTÉS az egyes műszaki tárgyú miniszteri rendeletek módosításáról Budapest, 2009. augusztus 2 EGYEZTETÉSI LAP 1. Az egyeztetés alapadatai
113/1996. (VII. 23.) Korm. rendelet az egészségügyi szolgáltatás nyújtására jogosító működési engedélyekről
 113/1996. (VII. 23.) Korm. rendelet az egészségügyi szolgáltatás nyújtására jogosító működési engedélyekről Az egészségügyi ellátási kötelezettségről és a területi finanszírozási normatívákról szóló 1996.
113/1996. (VII. 23.) Korm. rendelet az egészségügyi szolgáltatás nyújtására jogosító működési engedélyekről Az egészségügyi ellátási kötelezettségről és a területi finanszírozási normatívákról szóló 1996.
A BIZOTTSÁG VÉGREHAJTÁSI HATÁROZATA (EGT vonatkozású szöveg) (CSAK A DÁN NYELVŰ SZÖVEG HITELES)
 EURÓPAI BIZOTTSÁG Brüsszel, 29.6.2011 C(2011)4837 végleges A BIZOTTSÁG VÉGREHAJTÁSI HATÁROZATA 29.6.2011 az emberi felhasználásra szánt "Instanyl - Fentanil" gyógyszer számára a C(2009)5900 határozat alapján
EURÓPAI BIZOTTSÁG Brüsszel, 29.6.2011 C(2011)4837 végleges A BIZOTTSÁG VÉGREHAJTÁSI HATÁROZATA 29.6.2011 az emberi felhasználásra szánt "Instanyl - Fentanil" gyógyszer számára a C(2009)5900 határozat alapján
I. A rendelet célja. II. A rendelet hatálya
 Takácsi Község Önkormányzat Képviselő-testülete 5/2013. (II. 19.) önkormányzati rendelete a személyes gondoskodást nyújtó ellátásokról, azok igénybevételének rendjéről, a fizetendő térítési díjak megállapításáról
Takácsi Község Önkormányzat Képviselő-testülete 5/2013. (II. 19.) önkormányzati rendelete a személyes gondoskodást nyújtó ellátásokról, azok igénybevételének rendjéről, a fizetendő térítési díjak megállapításáról
A 32/2013. (XII.16.) MNB
 A Magyar Nemzeti Bank elnökének 32/2013. (XII.16.) MNB rendelete a kockázati tőkealapokkal, a kibocsátókkal és a nyilvános vételi ajánlatot tevő szervezetekkel összefüggő kötelező elektronikus kapcsolattartással
A Magyar Nemzeti Bank elnökének 32/2013. (XII.16.) MNB rendelete a kockázati tőkealapokkal, a kibocsátókkal és a nyilvános vételi ajánlatot tevő szervezetekkel összefüggő kötelező elektronikus kapcsolattartással
EURÓPAI BIZOTTSÁG VÁLLALKOZÁSPOLITIKAI ÉS IPARI FŐIGAZGATÓSÁG
 EURÓPAI BIZOTTSÁG VÁLLALKOZÁSPOLITIKAI ÉS IPARI FŐIGAZGATÓSÁG Fogyasztási cikkek Gyógyszerkészítmények Brüsszel, 9/1/2008 ENTR NR D(2007) Nyilvános pályázati felhívás az Európai Gyógyszerügynökség fejlett
EURÓPAI BIZOTTSÁG VÁLLALKOZÁSPOLITIKAI ÉS IPARI FŐIGAZGATÓSÁG Fogyasztási cikkek Gyógyszerkészítmények Brüsszel, 9/1/2008 ENTR NR D(2007) Nyilvános pályázati felhívás az Európai Gyógyszerügynökség fejlett
1.. A rendelet célja
 MIHÁLYFA KÖZSÉGI ÖNKORMÁNYZAT KÉPVISELŐ-TESTÜLETÉNEK 22/2013.(XII.13.)RENDELETE A személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről, valamint a fizetendő térítési díjáról. A Képviselő-testület
MIHÁLYFA KÖZSÉGI ÖNKORMÁNYZAT KÉPVISELŐ-TESTÜLETÉNEK 22/2013.(XII.13.)RENDELETE A személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről, valamint a fizetendő térítési díjáról. A Képviselő-testület
HU-Budapest: Diagnosztikumok 2012/S 149-248140
 1/7 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:248140-2012:text:hu:html HU-Budapest: Diagnosztikumok 2012/S 149-248140 Országos Vérellátó Szolgálat, Karolina út 19-21., attn:
1/7 Ez a hirdetmény a TED weboldalán: http://ted.europa.eu/udl?uri=ted:notice:248140-2012:text:hu:html HU-Budapest: Diagnosztikumok 2012/S 149-248140 Országos Vérellátó Szolgálat, Karolina út 19-21., attn:
Rákóczifalva Város Önkormányzata Képviselő-testületének 7/2019. (V. 24.) önkormányzati rendelete
 Rákóczifalva Város Önkormányzata Képviselő-testületének 7/2019. (V. 24.) önkormányzati rendelete az önkormányzati tulajdonú lakások és helyiségek bérletéről és elidegenítéséről Rákóczifalva Város Önkormányzatának
Rákóczifalva Város Önkormányzata Képviselő-testületének 7/2019. (V. 24.) önkormányzati rendelete az önkormányzati tulajdonú lakások és helyiségek bérletéről és elidegenítéséről Rákóczifalva Város Önkormányzatának
AZ EURÓPAI UNIÓ TANÁCSA. Brüsszel, január 25. (26.01) (OR. en) 5674/12 DENLEG 4 AGRI 38 FEDŐLAP
 AZ EURÓPAI UNIÓ TANÁCSA Brüsszel, 2012. január 25. (26.01) (OR. en) 5674/12 DENLEG 4 AGRI 38 FEDŐLAP Küldi: az Európai Bizottság Az átvétel dátuma: 2012. január 20. Címzett: Uwe CORSEPIUS, az Európai Unió
AZ EURÓPAI UNIÓ TANÁCSA Brüsszel, 2012. január 25. (26.01) (OR. en) 5674/12 DENLEG 4 AGRI 38 FEDŐLAP Küldi: az Európai Bizottság Az átvétel dátuma: 2012. január 20. Címzett: Uwe CORSEPIUS, az Európai Unió
A BIZOTTSÁG 1002/2005/EK RENDELETE
 2005.7.1. Az Európai Unió Hivatalos Lapja L 170/7 A BIZOTTSÁG 1002/2005/EK RENDELETE (2005. június 30.) az 1239/95/EK rendeletnek a kényszerengedély megadása és a Közösségi Növényfajta-hivatal birtokában
2005.7.1. Az Európai Unió Hivatalos Lapja L 170/7 A BIZOTTSÁG 1002/2005/EK RENDELETE (2005. június 30.) az 1239/95/EK rendeletnek a kényszerengedély megadása és a Közösségi Növényfajta-hivatal birtokában
Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé. Mifepristone Linepharma 200 mg Tafla
 I. melléklet A gyógyszerek neveinek, gyógyszerformáinak, erősségének felsorolása, az alkalmazási módok, a forgalomba hozatali engedély jogosultjai és kérelmezői a tagállamokban 1 EU/EKÜ tagállam Forgalomba
I. melléklet A gyógyszerek neveinek, gyógyszerformáinak, erősségének felsorolása, az alkalmazási módok, a forgalomba hozatali engedély jogosultjai és kérelmezői a tagállamokban 1 EU/EKÜ tagállam Forgalomba
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA A BIZOTTSÁG HATÁROZATA 11.2.2009
 AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 11.2.2009 C(2009)1056 NEM KÖZZÉTÉTELRE A BIZOTTSÁG HATÁROZATA 11.2.2009 a(z) "STARTVAC" állatgyógyászati készítmény forgalomba hozatalának a 726/2004/EK európai
AZ EURÓPAI KÖZÖSSÉGEK BIZOTTSÁGA Brüsszel, 11.2.2009 C(2009)1056 NEM KÖZZÉTÉTELRE A BIZOTTSÁG HATÁROZATA 11.2.2009 a(z) "STARTVAC" állatgyógyászati készítmény forgalomba hozatalának a 726/2004/EK európai
(EGT-vonatkozású szöveg)
 L 60/12 HU A BIZOTTSÁG (EU) 2019/337 VÉGREHAJTÁSI RENDELETE (2019. február 27.) a mefentriflukonazol hatóanyagnak a növényvédő szerek forgalomba hozataláról szóló 1107/2009/EK európai parlamenti és tanácsi
L 60/12 HU A BIZOTTSÁG (EU) 2019/337 VÉGREHAJTÁSI RENDELETE (2019. február 27.) a mefentriflukonazol hatóanyagnak a növényvédő szerek forgalomba hozataláról szóló 1107/2009/EK európai parlamenti és tanácsi
ORVOSBIOLÓGIAI, ORVOSTUDOMÁNYI KUTATÁSOK,ELJÁRÁSOK, TEVÉKENYSÉGEK SZAKMAI, ETIKAI VÉLEMÉNYEZÉSE, JÓVÁHAGYÁSA
 ORVOSBIOLÓGIAI, ORVOSTUDOMÁNYI KUTATÁSOK,ELJÁRÁSOK, TEVÉKENYSÉGEK SZAKMAI, ETIKAI VÉLEMÉNYEZÉSE, JÓVÁHAGYÁSA DR. TEMESI ALFRÉDA BIOL. TUD. KANDIDÁTUS C.E. DOCENS ETT-ESKI PÁLYÁZATI IRODA IGAZGATÓ FŐBB
ORVOSBIOLÓGIAI, ORVOSTUDOMÁNYI KUTATÁSOK,ELJÁRÁSOK, TEVÉKENYSÉGEK SZAKMAI, ETIKAI VÉLEMÉNYEZÉSE, JÓVÁHAGYÁSA DR. TEMESI ALFRÉDA BIOL. TUD. KANDIDÁTUS C.E. DOCENS ETT-ESKI PÁLYÁZATI IRODA IGAZGATÓ FŐBB
- aktív tagja a Személy-, Vagyonvédelmi és Magánnyomozói Szakmai Kamara
 Személy-, Vagyonvédelmi és Magánnyomozói Szakmai Kamara 1135 B u d a p e s t, Szegedi út 37-39. Telefon: 00-(36)-1-220-5690 FAX: 00-(36)-1-220-8921. A Személy-, Vagyonvédelmi és Magánnyomozói Szakmai Kamara
Személy-, Vagyonvédelmi és Magánnyomozói Szakmai Kamara 1135 B u d a p e s t, Szegedi út 37-39. Telefon: 00-(36)-1-220-5690 FAX: 00-(36)-1-220-8921. A Személy-, Vagyonvédelmi és Magánnyomozói Szakmai Kamara
Személyes gondoskodást nyújtó ellátási formák
 Apátfalva Község Önkormányzat Képviselő-testületének 16/2007. (VI.27.)Ör a személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről és a fizetendő térítési díjakról Apátfalva Község Önkormányzat
Apátfalva Község Önkormányzat Képviselő-testületének 16/2007. (VI.27.)Ör a személyes gondoskodást nyújtó ellátásokról, azok igénybevételéről és a fizetendő térítési díjakról Apátfalva Község Önkormányzat
(EGT-vonatkozású szöveg)
 L 77/6 2018.3.20. A BIZOTTSÁG (EU) 2018/456 VÉGREHAJTÁSI RENDELETE (2018. március 19.) az új élelmiszerré történő minősítésre irányuló, az új élelmiszerekről szóló (EU) 2015/2283 európai parlamenti és
L 77/6 2018.3.20. A BIZOTTSÁG (EU) 2018/456 VÉGREHAJTÁSI RENDELETE (2018. március 19.) az új élelmiszerré történő minősítésre irányuló, az új élelmiszerekről szóló (EU) 2015/2283 európai parlamenti és
A Mezőgazdasági és Vidékfejlesztési Hivatal. 62/2012. (IV. 27.) számú KÖZLEMÉNYE. a mezőgazdasági területek erdősítése támogatás igényléséről
 A Mezőgazdasági és Vidékfejlesztési Hivatal 62/2012. (IV. 27.) számú KÖZLEMÉNYE a mezőgazdasági területek erdősítése támogatás igényléséről Jelen Közlemény alapja az Európai Mezőgazdasági Vidékfejlesztési
A Mezőgazdasági és Vidékfejlesztési Hivatal 62/2012. (IV. 27.) számú KÖZLEMÉNYE a mezőgazdasági területek erdősítése támogatás igényléséről Jelen Közlemény alapja az Európai Mezőgazdasági Vidékfejlesztési
Helsinki, március 25. Dokumentum: MB/12/2008 végleges
 Helsinki, 2009. március 25. Dokumentum: MB/12/2008 végleges HATÁROZAT AZ EURÓPAI PARLAMENT, A TANÁCS ÉS A BIZOTTSÁG DOKUMENTUMAIHOZ VALÓ NYILVÁNOS HOZZÁFÉRÉSRŐL SZÓLÓ 1049/2001/EK EURÓPAI PARLAMENTI ÉS
Helsinki, 2009. március 25. Dokumentum: MB/12/2008 végleges HATÁROZAT AZ EURÓPAI PARLAMENT, A TANÁCS ÉS A BIZOTTSÁG DOKUMENTUMAIHOZ VALÓ NYILVÁNOS HOZZÁFÉRÉSRŐL SZÓLÓ 1049/2001/EK EURÓPAI PARLAMENTI ÉS
1.10. Adószáma (11 hosszan): - - 1.11. Pénzforgalmi (átutalási) számlaszáma(i) és a számlavezető pénzintézet(ek) megnevezése, fiókja, számlaszáma:
 Kérelem benyújtásának időpontja: Kérelmet átvevő vámszerv megnevezése, aláírása: KÉRELEM vámhatósági nyilvántartásba vételhez a kereskedelmi gázolaj utáni adó-visszaigénylés érvényesítéséhez Új kérelem
Kérelem benyújtásának időpontja: Kérelmet átvevő vámszerv megnevezése, aláírása: KÉRELEM vámhatósági nyilvántartásba vételhez a kereskedelmi gázolaj utáni adó-visszaigénylés érvényesítéséhez Új kérelem
