SZENT ISTVÁN EGYETEM ÁLLATORVOS-TUDOMÁNYI KAR Patológiai Tanszék. A kutyák gastrointestinalis stromalis tumorainak immunhisztokémiai vizsgálata
|
|
|
- András Varga
- 7 évvel ezelőtt
- Látták:
Átírás
1 SZENT ISTVÁN EGYETEM ÁLLATORVOS-TUDOMÁNYI KAR Patológiai Tanszék A kutyák gastrointestinalis stromalis tumorainak immunhisztokémiai vizsgálata Immunohistochemical investigation of the canine gastrointestinal stromal tumor Készítette: Nádasdi Péter Vilmos, VI. évf. hallgató Témavezető: Dr. Jakab Csaba, egyetemi adjunktus SzIE ÁOTK, Patológiai Tanszék Budapest,2015
2 TARTALOMJEGYZÉK 1. BEVEZETÉS IRODALMI ÁTTEKINTÉS A GIST-ről általában A GIST emberben A GIST kutyában Immunhisztokémia Kezelés ANYAG ÉS MÓDSZER Kórszövettan Immunhisztokémia EREDMÉNYEK MEGBESZÉLÉS ÖSSZEFOGLALÁS SUMMARY KÖSZÖNETNYILVÁNÍTÁS IRODALOMJEGYZÉK
3 Rövidítések GIST Gastrointestinalis stromalis tumor SMA smooth muscle actin (simaizom actin) LM Leomyoma LMS Leomyosarcoma NFS - Neurofibrosarcoma SI Simaizom NNL Nagy nagyítású látótér ir immunreakció IH - Immunhisztokémia mtsai - munkatársai 3
4 1. BEVEZETÉS Napjaink egyik legnagyobb félelmet keltő és egyben leggyakoribb kórképei a tumoros megbetegedések, mind a humán-, mind az állatorvoslás terén. Ebből kifolyólag egyre fontosabbá válik, hogy minél hamarabb, minél pontosabb képet kapjunk ezen elváltozások szerkezetéről, milyenségéről. Az utóbbi években a tumor diagnosztika robbanásszerű fejlődésen ment keresztül és köszönhetően a legújabb technikáknak egyre könnyebbé és gyorsabbá válik az osztályozás folyamata. A modern molekuláris patológia egyik leghasznosabb vívmánya az immunhisztokémiai vizsgálat. Segítségével lehetővé vált a kórszövettani vizsgálatokból egyértelműen meg nem állapítható sejteredet feltérképezése, mind az intact, mind a kórosan elváltozott (daganatos, gyulladásos) szövetekben. Az ezen vizsgálatokra épülő ismeretek segítenek a pontosabb és biztosabb diagnózis felállításában és célzott terápiás stratégiák kidolgozásában. Munkánk során célul tűztük ki, hogy a SZIE ÁOTK Patológiai Tanszékének szövetbankjából kiválasztott kutyák gyomrából, vékonybeléből és nyelőcsövéből származó, fénymikroszkóposan simaizom eredetűnek diagnosztizált tumorokat indirekt immunhisztokémiai vizsgálatnak vessük alá, anti-vimentin, anti-α-sma, anti-s-100 protein, anti-c-kit (CD117) ellenanyagok segítségével. Hazánkban ez az első ilyen jellegű, állatorvosi patológiai közlemény. 4
5 2. IRODALMI ÁTTEKINTÉS 2.1. A GIST-ről általában A gastrointestinalis stromalis tumor (GIST) az emésztőcső, kutyákban elsősorban a vakbél és a vastagbél, ún. Cajal-sejtjeiből kiinduló, fénymikroszkópos vizsgálattal orsósejtes megjelenésű daganata. A Cajal-sejtek, mint intestinalis pacemaker sejtek biztosítják élettani körülmények között a gyomor-bélcsatorna autonóm mozgását.(1. ábra) 1. ábra: A Cajal-sejtek helyeződése (Forrás: The life raft, megtekintés: ) Az immunhisztokémiai vizsgálatoknak köszönhetően a humánorvoslás területén írták le először (2, 4, 16), majd később kutyákban is azonosították (3, 9, 10). Kizárólag klinikai 5
6 tünetek és vizsgálatok, illetve a mikroszkópos lelet alapján a GIST nem különíthető el az emésztőtraktusban megjelenő más daganat típusoktól (leggyakrabban leomyoma, leomyosarcoma, ami a daganatok 10-30%-át teszi ki (3)). A leomyosarcoma ugyan gyakrabban fordul elő a gyomorban és a vékonybeleken, a GIST pedig a vastagbeleken, de mindkét daganattípust megtalálhatjuk a teljes emésztőcsőben, így a helyeződés nem szolgálhat a differenciáció alapjául. A GIST lehet malignus és benignus is, melynek elkülönítését hasonlóan a többi daganathoz - a mikroszkópos sejttani vizsgálat teszi lehetővé. Készült azonban egy tanulmány, melyben ultrahangos kép alapján határozták meg az áttétképződés lehetőségét. A szerzők megállapították, hogy a nagyobb átmérő, az egyenetlen szegély, a heterogén belső echogenitás nagy hypoechogen területekkel viszonylag pontosan jelzi előre a metastasis lehetőségét (29). A daganat pontos diagnózisához nélkülözhetetlen a megfelelő antitestekből álló immunhisztokémiai panel alkalmazása (15). A GIST emberekben és kutyákban a leggyakoribb, azonban leírták már főemlősökben és 2001-ben lovakban is, de sajnos náluk még nem alkalmazták a c-kitet, ami nélkül mai ismereteink szerint nem lehet pontosan diagnosztizálni a GIST-t (bővebben a 2.4.-es fejezetben). 10 ló és egy póni daganatos elváltozásaiból vettek mintát (2 esetben mutatkoztak klinikai tünetek, 9-nél csak, mint melléklelet vették észre az elváltozásokat). A daganatok helyeződés szerint a következőként oszlottak meg: 5 caecum, 3 ileum, 2 colon, 1 jejunum, 1 gyomor minta. Mindegyik elváltozás vimentin pozitivitást mutatott, 3 db S-100-zal és 2 alfa- SMA-val is festődött. Kutatásunk folyamán nem találtunk olyan cikket, mely lovakban is vizsgálta volna GIST-ek anti-c-kit festődését (25). 6
7 2.2. A GIST emberben A humán GIST leggyakrabban a gyomorban, majd a vékonybélben, ritkábban a rectumban, mesenteriumban, nyelőcsőben, colonban fejlődik ki, elsősorban az idősebb korosztályban. Az érintett betegek átlagos életkora a daganat észlelésekor 63 év. A GIST hányingert, hányást, hasi fájdalmat, testsúlycsökkenést, az evést követő túl korai teltségérzetet okozhat emberben, ill. vérzések is kísérhetik a betegséget, amelyek idővel vérszegénységhez és fáradékonysághoz vezetnek. Ezek a tünetek a betegség kezdeti megjelenésétől számítva átlagosan 4 6 hónapon belül jelennek meg. A daganat áttéteket legtöbbször a nyirokcsomóba, a hasüregbe (mesenteriumba) és a májba ad (2, 4, 8, 15, 22, 24). Hazánkban OROSZ és mtsai (2006) végeztek retrospek felmérést öt regionális centrumban azzal a céllal, hogy megállapítsák: a GIST-k 2004-től 1985-ig visszamenően milyen kórszövettani diagnózisokkal szerepeltek (15). A visszatekintő immunhisztokémiai vizsgálat során a c-kit-pozi GIST-nek bizonyult esetek első diagnózisai a következők voltak: leiomyoma, leiomyosarcoma, benignus schwannoma/neurinoma, neurofibroma, malignus schwannoma, GANT (gastrointestinalis autonóm idegtumor), fibroma, fibrosarcoma, fibromyoma, haemangiopericytoma, mesothelioma, lymphoma, malignus fibrosus histiocytoma. Munkájukkal felhívták a figyelmet arra, hogy a gyomor-bélrendszer daganatai esetében indokolt a szélesebb immunhisztokémiai paletta alkalmazása, a c-kit (CD117), a CD34, az S100 protein és a desmin immunhisztokémiai reakciók elvégzése (1, 13, 15). 7
8 2.3. A GIST kutyában Kutyákban a retrospek immunhisztokémiai vizsgálatoknak köszönhetően 1997-ben írták le először a GIST-t. Ebben a kutatásban azonban még nem alkalmazták a ma legmegbízhatóbbnak tartott c-kitet, illetve a GIST fogalma sem volt még teljes egészében tisztázott. 35 formalinban fixált mintát dolgoztak fel, melyek közül 14 LM, 18 LMS, 2 differenciálatlan sarcoma és egy NFS. Minden mintát négy markerre teszteltek (vimentin, S- 100, alfa-sma és desmin). 31/35 eset mutatott alfa-sma és/vagy desmin, 17 eset pedig S- 100 pozitivitást. A probléma az, hogy a GIST-k minden fent említett markerre lehetnek poziak és több más tumor típus is festődhet velük, így csupán a fentiek alapján nem lehet biztos diagnózist felállítani (9). A c-kit használatára kutyákban először 2003-ban került sor, amikor FROST és mtsai 50 leomyomának diagnosztizált daganatot vizsgáltak meg különböző immunhisztokémiai eljárásokkal. Az 50 esetből 21 lett GIST (42%), ebből pedig 11 tumor mutatott c-kit pozitivitást. Ugyan ez csak az esetek 52%-a, de a szerzők már ekkor feltételezték, hogy valószínűleg a többi próba fals nega és a legtöbb GIST pozi a C-Kit-re. 7 GIST ezen felül pozi lett alfa-sma-ra és egyik sem festődött desminnel vagy S-100-zal. A daganatot azonos arányban észlelték szuka és kan egyedekben, amelyek átlag életkora 11 év volt (5 14 év). Az esetek 24%-ában jelentkeztek klinikai tünetek, ill. 29%-ban már volt áttét a májban és a hasüregben. A GIST anatómiai megoszlása a következő volt: vastagbél (48%), vékonybél (29%), gyomor (19%), és mesenterium (5%) (3). Többnyire orsósejtes, hypercellularis típust észleltek vizsgálataik során, szemben a jóval kisebb számban előforduló epitheloid típussal. A mitoticus index 0 19 osztódó sejt/10 NNL volt. 29 tumornál maradtak az eredeti diagnózisnál, vagyis az LM-nél. Itt az ivararány eltolódott a hímek irányába (82%), de az átlag életkor itt is 11 év volt. 9 tumor okozott klinikai tüneteket, 22 a gyomorból, 4 a nyelőcsőből és 3 a belekből származott. 28 eset (97%) volt pozi alfa-sma-ra, 18 desminre, de egyik sem S-100-ra vagy c-kitre. Megállapították tehát, hogy a c-kit egy specifikus markere a GIST-nek (3). MAAS és mtsai 2007-ben 72 vékonybél és vakbél eredetű leiomyoma, leiomyosarcoma újraosztályozását végezték el α-sma, desmin, vimentin, S-100 protein és c-kit alapú immunhisztokémia segítségével. A reklasszifikáció kritériuma, hogy a mintának c-kit és vimentin pozinak kell lennie függetlenül a mikroszkópos látképtől és az α-sma, desmin, S-100 festődéstől. Ebben a tanulmányban használják a GIST-like kifejezést is. Ezen tumorok 8
9 tulajdonságai megegyeznek a GIST-ével, de nem poziak c-kitre. A 72 esetből 47 minta származott a vékonybélből, 25 pedig a caecumból. A vékonybél mintáknál 19 GIST és 17 GIST-like lett reklasszifikálva (2 maradt LM, 9 pedig LMS), a caecumban pedig az összes tumort újraosztályozták (23 GIST, 2 GIST like). A tanulmányban vizsgált esetek 85%-a, azaz 19 vékonybél és 23 caecum tumor bizonyult utólag GIST-nek. A szerzők eme tanulmány fontos eredményének tartják még, hogy hiába volt a legtöbb daganat malignus jellegű, a megfelelő sebészi eltávolítás után viszonylag hosszú volt a páciensek túlélési ideje. A vékonybél tumorosok közül 3 (446, 1093, 3491 nap), míg a vakbelesek közül 4 állat 1 év után is életben volt (470, 813, 823, 1393 nap), ezen felül mind a 7 kutya mentes volt klinikai tünetektől. A vékonybeles csoportban 12-nek (29%) maradt vissza tumor/tünet vagy alakult ki metastasis a műtét után, 3 közülük elaltatásra került. Ezen állatok átlagos túlélési ideje csupán 32 nap volt. A vakbeles csoportban 7-nél nem sikerült a teljes tumort eltávolítani és 2-t altattak el, az átlagos túlélési idő csupán 59 nap volt (10). A kutatásból kitűnik, hogy a sebészi eltávolítás nem mindig sikeres, így szükségessé válik a gyógyszeres kezelés mélyrehatóbb vizsgálata. 9
10 2.4. Immunhisztokémia A c-kit vagy CD117 egy tirozin-kináz aktivitású, transzmembrán receptorfehérje, amely élettani körülmények között a csontvelői myeloid haemopoeticus őssejtek, a bőrbeli melanocyták, a gyomorbélbeli Cajal-sejtek és a mastocyták (hízósejtek) membránjában fejeződik ki. Szerepet játszik a sejtnövekedésben, a proliferációban és a differenciálódásban (23). A c-kit kódoló génjében (protoonkogénben) bekövetkező mutáció alapvető szerepet játszik a következő daganatok kialakulásában: GIST, mastocytoma, seminoma, acut myeloid leukaemia, adenoid cysticus carcinoma. Ezekben a rosszindulatú daganatokban a mutáció miatti túlzott kifejeződés (overexpresszió), az immunhisztokémiai vizsgálat során intenzív c- Kit-pozitivitásként észlelhető, ill. perinuclearis jellegű (14, 20). A c-kit valószínűleg nem az egyetlen marker, amivel diagnosztizálni lehet a GIST-eket. Az egyik lehetséges alternaa a CD34 volt, amely humán esetek 60-80%-ában pozi eredményt ad. A CD34 egy sejtfelszíni fehérje, amely többek közt a sejtek közötti kapcsolatok kialakításában játszik fontos szerepet. Ezen fehérje markerként való használatának lehetőségét 2011-ben vizsgálták, de sajnos csak az esetek 14,8% lett pozi, így a CD34 egyelőre nem használható a GIST diagnosztikájában (30). Ígéretesebb lehetőséggel egy friss tanulmány szerint a DOG1 membrán fehérje kecsegtet, amely a kálcium dependens kloridion transzportért felel a GIST-ekben. A szerzők 55 tumormintát vetettek immunhisztokémiai vizsgálatok alá, amelyből 33-mat GIST-ként azonosítottak (15 szuka, 18 kan, 10,2 átlag életkor). Azokat a tumorokat jelölték GIST-nek, melyek c-kit vagy DOG1 poziak, illetve desmin negaak voltak (a desminnel való festődés leomyosarcomara, leomyomara utal). 32 eset pozi volt c-kit-re és DOG1-re is, 1 csak DOG1-re, egy pedig DOG1-re és desminre is (ez utóbbi tehát leomyosarcoma). Azt, hogy miért voltak c-kit nega GIST-k nem tudták megmagyarázni, de valamilyen daganat szubtípust vagy a kimutatási eljárás közben elkövetett hibát feltételeztek. Látható, hogy a DOG1 hasonlóan érzékeny markere lehet a GIST-eknek, mint a c-kit (26). Természetesen a leomyoma és leomyosarcoma is mutatnak immunhisztokémiai festődést. A leomyoma SMA és desmin pozi, de nega S-100-ra és c-kitre, ezen felül a mikroszkópos sejttani vizsgálat nem utal malignanciára. Az LMS hasonló kritériumok szerint festődik, mint az LM, de malignus jellegű (10). 10
11 2.5. Kezelés E daganattípusnál sem a korábbi kemo-, sem a radioterápia nem hozott számottevő eredményt. Az eddig klasszikusan alkalmazott módszer a sebészi eltávolítás, azonban a GIST gyakran képez áttéteket vagy van inoperábilis helyen. JOENSUU és mtsai 2001-ben, áttétes GIST-s betegnél tirozinkináz-gátlóval (STI571, imatinib mesylate, Glivec ) gyakorlatilag teljes gyógyulást értek el (6). Előrehaladott GIST esetén azonnali imatinib kezelés javasolható, napi 400 mg adaggal. A kezelést tumorprogresszióig (áttétképződésig), intoleranciáig vagy a beteg általi visszautasításig folytatni kell. Áttétek megjelenése esetén el kell különíteni a partialis vagy multifocalis rezisztenciát. Ez azt jelenti, hogy a Glivec terápia során csak egy vagy néhány áttét mutat növekedést, míg a többi tumor mérete változatlan (8) ban hasonló kutatást végeztek egy 10 év körüli kutyán, amelynek nem operábilis GISTje volt. Az imatinib hatására a tumor mérete csökkent a 67. napig, de ezután a kezelés 140. napjáig már nem. Emellett hepatotoxicitás is fellépett, mint mellékhatás (az ALT szint jelentősen emelkedett), de a szerzők feltételezik, hogy ez valószínűleg egyedi eset, mert az imatinib más kutatásokban nem okozott ilyen elváltozást. Hogy miért állt meg a tumor csökkenése a 67. napon nem bizonyított, de elképzelhető, hogy humán esetekhez hasonlóan a tumor rezisztenssé vált a tirozin-kináz gátlóra (28) ös tanulmány szerint egy 13 éves kutyát kezeltek imatinibbel, amelynek hasüregében eredeti tumorának műtéti eltávolítása után 5 hónappal újabb daganatokat észleltek. A diagnosztikai laparotómia során vett minták mindegyike pozitivitást mutatott c-kit-re. Ezután kezdték meg az imatinib-mesylate-os kezelést 10 mg/kg dózisban. 2 hét után látható méretcsökkenés, 2 hónap után teljes gyógyulás következett be. A kutya további 4 és fél évet élt, kiújulást nem észleltek, további kezelésre nem volt szükség ( a kimúlás oka nem köthető össze a GIST-tel) (27). 11
12 3. ANYAG ÉS MÓDSZER 3.1. Kórszövettan Munkánk során, a SZIE ÁOTK Patológiai Tanszékének szövetbankjából kiválasztottunk 15, kutya nyelőcsövéből (n = 1), gyomrából (n = 8) és vékonybeléből (n = 6) származó daganatmintát, amelyek kórszövettani első diagnózisa jóindulatú, ill. rosszindulatú simaizomszöveti daganat, ún. leiomyoma és leiomyosarcoma volt. Valamennyi gyomor eredetű minta kórszövettani vizsgálattal leiomyomának tűnt, amelyek közül két esetben multiplex megjelenést észleltük. A nyelőcső distalis szakaszán, valamint a vékonybélfalban észlelt daganatokat leiomyosarcomaként leleteztük. Egy esetben lépbeli, ill. egy esetben májbeli áttéteket is megfigyeltünk. A kórszövettani vizsgálathoz a mintákat előzetesen szobahőmérsékleten, 24 órán át, 8%-os pufferolt formaldehid oldatban konzerváltuk, majd szövetelőkészítő automatával tettük alkalmassá a további feldolgozásra. A beágyazást követően a paraffinos blokkokból 3 4 μm vastagságú metszeteket készítettünk, amelyeket hematoxilinnal és eozinnal festettünk meg. A metszeteket Nikon Optiphot-2 típusú fénymikroszkóppal vizsgáltuk. A daganat mitotikus indexének meghatározása során 50 különböző, nagynagyítású (200 ) látómezőben (NNL) észlelt osztódó (profázisban, metafázisban, anafázisban, telofázisban lévő) daganatsejtet megszámlálva átlagoltunk Immunhisztokémia Az indirekt immunhisztokémiai vizsgálatot Ventana-immunfestő automata segítségével végeztük. A felhasznált antitesteket az 1. táblázatban foglaltuk össze. Az immunhisztokémiai reakciókat avidin-biotin immunperoxidáz rendszerrel (DAKO LSAB2 Kit) és DAB (diaminobenzidin) chromogennel tettük láthatóvá. A kontrasztfestés hematoxilinnel történt. A nega kontroll metszeteket az elsődleges antitestek kihagyásával készítettük. Az immunhisztokémiai reakciók kiértékelése során külső pozi kontrollokat használtunk. Az immunhisztokémiai reakciók elemzésénél utalunk korábbi tanulmányunk adott fejezetére (5). 12
13 Antitest Külső pozi kontroll Immunreakció Vimentin (monoclonalis egér, 1:200, DAKO) kutya vaginalis fibroma cytoplasmaticus α-smooth muscle actin (α-sma) (monoclonalis egér, 1:8000, Sigma) kutya vaginalis leiomyoma cytoplasmaticus S-100 protein (polyclonalis nyúl, 1:50, DAKO) kutya perifériás ideghüvelytumor cytoplasmaticus c-kit/cd117 (polyclonalis nyúl, 1:100, DAKO) kutya grade I-es mastocytoma membrán-cytoplasmaticus 1.táblázat: Felhasznált antitestek 2. ábra: A szövetbank 13
14 3. ábra: A paraffinos minta szeletelése 4. ábra: A festőautomata 14
15 5. ábra: A festőtárcsa 15
16 4. EREDMÉNYEK A fénymikroszkópos vizsgálatok során a gyomorból származó minták esetén a monomorf, orsósejtes megjelenésű daganatokban osztódó sejteket csak elvétve figyeltünk meg (osztódó sejtszám: < 5/50 NNL). Ezen daganatok állományában mérsékelt tumorindukált érújdonképződés (neoangiogenesist) volt látható, ill. vérzés, elhalás jeleit nem tapasztaltuk. A vékonybélből származó minták esetén nagy mitoticus aktivitást (osztódó sejtszám: > 5/50 NNL), kifejezett, perifériás jellegű daganat indukálta érújdonképződést, ill. centrális vérzést, elhalást észleltünk. A nyelőcsődaganat a bélfali tumorokhoz hasonló kórszövettani jellemzőket mutatott, viszont elhalás, vérzés nem volt állományában. Tumor helyeződés Tum or átmé rő 1. Nyelőcs 5,5c ő m 2. Gyomor 1,5c m Osztó dó sejtsz ám (50N NL) Korábbi kórszövetta ni (első) diagnózis Vimen tin-ir. >5 Leiomyosar coma ív (5) <5 Leiomyoma ív (5) 3. Gyomor 1cm <5 Leiomyoma ív (5) 4. Gyomor 2,2c m 5. Gyomor 1,5c m 6. Gyomor 1,2c m 7. Gyomor 1,4c m 8. Gyomor 1,9c m 9. Gyomor 1,2c m 10. Vékony bél 11. Vékony bél 12. Vékony bél 13. Vékony bél <5 Leiomyoma ív (5) <5 Leiomyoma ív (5) <5 Leiomyoma ív (5) <5 Leiomyoma ív (5) <5 Leiomyoma ív (5) <5 Leiomyoma ív (5) 7,5c m >5 Leiomyosar coma 5cm >5 Leiomyosar coma 5,6c >5 Leiomyosar m coma 6,3c >5 Leiomyosar m coma ív (5) ív (5) ív (5) ív (5) α- SMA -ir. S 100 prot. -ir. ív (3) ív (3) ív (3) ív (3) ív (3) c- Kitir. Új diagnóz is GIST GIST GIST GIST Leiomy oma Leiomy oma GIST GIST GIST GIST GIST GIST GIST Rizik ó- csop ort Nagy Nagy on kis Nagy on kis Kis - - Nagy on kis Nagy on kis Nagy on kis Nagy Nagy Nagy Nagy 16
17 14. Vékony bél 8cm >5 Leiomyosar coma 15. Vékony 4,5c >5 Leiomyosar bél m coma 2.Táblázat: A vizsgálatok eredményei ív (5) ív (5) GIST GIST Nagy Nagy Immunhisztokémiai vizsgálataink eredményeit a 2. táblázatban foglaltuk össze, és azokat mikroszkópos felvételekkel mutatjuk be. 6. ábra: Szervminta formalinban 17
18 7. ábra: Solitaer gyomordaganat. A daganat állományában vérzés és elhalás nem látható. 8. ábra: Multiplex GIST a gyomor fundusi területén. 18
19 9. ábra: Solitaer nyelőcsődaganat a distalis szakaszon. 10. ábra: A nyelőcső GIST metszéslapja. Elhalás és vérzés nem látható, mérsékelt érújdonképződés. 19
20 11. ábra: Cseplesszel fedett daganat a jejunum falában. 12. ábra: A vékonybél daganat metszéslapja. Kifejezetten nagymértékű vérzés és elhalás látható. 20
21 13. ábra: Bél eredetű GIST lépáttéte Tanulmányunk során valamennyi daganat vimentin pozitivitást mutatott. Két gyomordaganat (az összes tumor 13,33%-a) volt α-sma-pozi, ill. S-100 protein- és c-kit (CD117)-nega. Ezeket a daganatokat, az eredeti kórszövettani diagnózissal megegyezően, leiomyomaként azonosítottuk. A többi bélfali tumor (13/15; 86,67%) α-sma-neganak, c-kit-pozinak, ill. egy kivételével (12/15; 80%) S-100 protein-pozinak bizonyult. A 13 c-kit-pozi daganatot, amelyek korábbi kórszövettani diagnózisa gastricus leiomyoma (n = 6), intestinalis leiomyosarcoma (n = 6) és oesophagealis leiomyosarcoma (n = 1) volt, újraosztályoztuk (reklasszifikáltuk) gastrointestinalis stromalis tumorként, valamint a humánorvosi rizikócsoportosítás alapján (2) különböző csoportokba soroltuk. 21
22 14. ábra: Mikroszkópos felvétel a vékonybél eredetű GIST-ről (SI= bélfali simaizomszövet), H.-E. 15. ábra: Nagy nagyítású felvétel a vékonybél eredetű GIST-ről (SI= bélfali simaizomszövet), H.-E. 400X 22
23 16. ábra: α-sma-negativitás a daganatban (GIST), ill. α-sma-pozitivitás a tunica muscularisban (SI: barna színreakció; belső pozi kontrol), IH., ábra: S-100 protein-pozitivitás a daganatban (GIST; barna színreakció), ill. S-100 protein-negativitás a tunica muscularisban (SI: belső nega kontroll), IH.,
24 18. ábra: c-kit (CD117)-pozitivitás a daganatban (GIST: barna színreakció), ill. c-kitnegativitás a tunica muscularisban (SI: belső nega kontrol), IH., ábra: Nagyobb nagyítású felvétel a c-kit-pozi GIST-ről, IH.,
25 Amint a 12-es és 13-as ábrán látható a GIST semmiféle specifikus tulajdonságot nem mutat H.-E. festéssel. Láthatóak elpusztult vagy az osztódás különböző fázisaiban lévő orsó alakú sejtek, de ez a mikroszkópos látlelet nem különbözik az LM-ától és LMS-étől. Az anti- α - SMA-val festett metszet már többet mutat, hiszen a daganat nem festődik bizonyítva azt, hogy nem simaizom eredetű. LM vagy LMS esetén a tumorszövet festődött volna α-sma-val. A GIST, ellentétben az SI-vel festődik S-100-zal is, ami neurogén eredetre utal. Önmagában sajnos ez az eljárás sem használható kizárólagosan a GIST diagnosztikában, hiszen a bélben előfordulhatnak más idegsejt eredetű tumorok (pl. schwannoma, neurofibroma, neurofibrosarcoma stb ), amik szintén poziak lennének S-100-ra. Biztos diagnózist tehát csak a c-kit pozitivitás ad, mellyel az emésztőtraktusban előforduló más tumorok és a simaizom is nega, a GIST viszont egyértelműen festődik. 25
26 5. MEGBESZÉLÉS A gastrointestinalis stromalis tumor először a humánorvosi területen felismert, ill. leírt, csak immunhisztokémiai vizsgálattal azonosítható, elsősorban a gyomor és bélrendszerben előforduló, a lágyszöveti sarcomák csoportjába tartozó daganat (4). E tumor olyan prekurzor őssejtekből fejlődik ki, amelyek ún. interstitialis Cajal-sejtekké differenciálódnak. A Cajalsejtek, mint intestinalis pacemaker sejtek biztosítják élettani körülmények között a gyomorbélcsatorna autonóm mozgását. Szövettanilag a bélfali izomrostok és az idegrostok között helyezkednek el, a plexus myentericusban és akörül (1, 7, 18, 21). Elnevezésüket SANTIAGO RAMON Y CAJAL ( ) spanyol patológusról kapták, aki kórszövettannal és idegkutatással foglalkozott (19). Hasonló megjelenésű, eltérő immunfenotípusú (CD34- pozi/c-kit-nega), a gyomor-bélrendszerben fellelhető sejtek a telocyták vagy interstitialis Cajal-sejt szerű sejtek (17). A gyomor-bélcsatorna mesenchymalis daganatait a fénymikroszkópos megjelenés jellegzetességei alapján a szakirodalomban hosszú időn keresztül leiomyogen (simaizom eredetű) vagy neurogen (idegszövet eredetű) daganatként osztályozták. MAZUR és CLARK 1983-ban vezette be a gastrointestinalis stromalis tumor (GIST) elnevezést az onkológiai diagnosztikába, utalva arra, hogy ezek a tumorok a plexus myentericusból indulnak ki (11). A közelmúltban leírt GIST-ben fontos a jó-, ill. a rosszindulatúság megítélése. Jelenleg a FLETCHER és mtsai (2002) által ajánlott besorolást alkalmazzák. A daganat méretének, az osztódó sejtek számának, a tumoron belüli elhalásnak, a szöveti atípiának együttes értékelésével 3 csoportot különítenek el (2): nagyon kis rizikójú (átmérő: < 2 cm; osztódó sejtek száma < 5/50 nagy nagyítású, 200 látótér [továbbiakban: NNL]); kis rizikójú (átmérő: 2 5 cm; osztódó sejtek száma < 5/50 NNL), közepes (átmérő: < 5 cm; osztódó sejtek száma 6 10/50 NNL, vagy átmérő: 5 10 cm; osztódó sejtek száma < 5/50 NNL); nagy rizikójú (átmérő: > 5 cm; osztódó sejtek száma > 5/50 NNL, vagy átmérő: > 10 cm; osztódó sejtek száma: bármennyi, vagy átmérő: bármekkora; osztódó sejtek száma > 10/50 NNL ). 26
27 Leírtak már a bélfodorból, a csepleszből, a retroperitoneumból kiinduló, extragastrointestinalis helyeződésű GIST-t is (16). A tumor kórszövettanilag lehet orsósejtes, epitheloid sejtes és kevert típusú. A GIST-t, az emésztőtraktus falában kialakuló egyéb orsósejtes tumoroktól, a leiomyomától, a leiomyosarcomától, a fibromától, a fibrosarcomától, a myxomától, a myxosarcomától, a fibromyxomától, a perifériás ideghüvely daganatoktól (a benignus schwannomától, a perineuriomától, a neurofibromától, a malignus schwannomától, a neurofibrosarcomától), az orsósejtes melanomától és carcinomától, az inflammatoricus myofibroblastos tumortól, a pericytomától, a differenciálatlan liposarcomától, a malignus fibrosus histiocytomától, a gastrointestinalis endocrin tumoroktól, a paragangliomától és a sclerotisáló mesenteritistől kell immunhisztokémia segítségével elkülöníteni (15). Az elkülönítő kórjelzést segítő ellenanyagok az anti-c-kit (CD117) és az anti-dog-1 (12). Jelen immunhisztokémiai vizsgálataink során 15, kutyából származó gyomor, vékonybél és egy nyelőcső eredetű, korábban kórszövettanilag leiomyomának, ill. leiomyosarcomának diagnosztizált daganatot vizsgáltunk meg anti-vimentin, anti-α-sma, anti-s-100 protein és anti-c-kit ellenanyagok segítségével. A sejteredetet megbízhatóan azonosító molekuláris patológiai módszer, az immunhisztokémia, a 15 megvizsgált daganatból a c-kit-pozitivitás miatt 13 eset újraosztályozását, a korábbi kórszövettani diagnózis (simaizom eredetű daganat), gastrointestinalis stromalis tumorrá történő módosítását eredményezte. Tapasztalataink felhívják a figyelmet arra, hogy a kutyák emésztőcsövének területéről származó, orsósejtes daganatok korrekt, patológiai vizsgálatához nem elegendő a hematoxilin és eozin alapú kórszövettani elemzés. Minden esetben a pontos sejteredet, a tumor szövettani típusának meghatározása legalább négy antitestből (anti-vimentinből, anti-α-sma-ból, anti-s- 100 proteinből és anti-c-kit-ből) álló immunhisztokémiai panelt igényel. Ezekre alapozva lehet színvonalas állatorvosi szakmai véleményt alkotni, elfogadható közleményt, ill. előadást bemutatni, amely alapot ad a gyakorló állatorvosi munkához is. 27
28 6. ÖSSZEFOGLALÁS Tanulmányunkban 15, kutyából származó, hematoxilin-eozin festés alapján leiomyomaként és leiomyosarcomaként leletezett (első diagnózis), gyomor (n = 8; leiomyoma), vékonybél (n = 6; leiomyosarcoma) és nyelőcső eredetű (n = 1; leiomyosarcoma), necropsiás lágyszöveti mintát vizsgáltunk meg indirekt immunhisztokémiai módszerrel. A felhasznált immunhisztokémiai panel a következő antitestekből állt: anti-vimentin, anti-sma, anti-s-100 protein, és anti-c-kit (CD117). Munkánk során valamennyi daganat vimentinpozitivitást mutatott. Két gyomordaganat (2/15; 13,33%) volt α-sma-pozi, ill. S-100 protein- és c-kitnega. Ezeket az első (kórszövettani) diagnózissal megegyezően, leiomyomának nyilvánítottuk. A többi tumor (13/15; 86,67%) c-kit-, egy kivételével (12/15; 80%) S-100 proteinpozinak, ill. α-sma-neganak (13/15; 86,67%) bizonyult. A c-kit-pozi 13 daganatot, amelyek első (kórszövettani) diagnózisa gyomor leiomyoma (n = 6), vékonybél leiomyosarcoma (n = 6) és nyelőcső leiomyosarcoma (n = 1) volt, újraosztályoztuk gastrointestinalis stromalis tumorként (GIST). A vizsgálat eredménye alapján javasoljuk a kutyák emésztőtraktusából származó sebészi vagy necropsiás, orsósejtes megjelenésű minták anti-vimentin, anti-α-sma, anti-s-100 protein és anti-c-kit ellenanyagokra alapozott immunhisztokémiai vizsgálatát a pontos diagnózis érdekében. 28
29 7. SUMMARY In the present immunohistochemical study the author reanalyses 15 gastric (n = 8), intestinal (n = 6), and oesophageal (n = 1) canine soft tissue necropsy samples (Figures 1-4.), which were initially diagnosed as leiomyoma (gastric), and leiomyosarcoma (intestinal, oesophageal), based on light microscopic analysis of the haematoxylin and eosin stained slides (Figure 5.). The immunohistochemical panel consisted of anti-vimentin, anti-α-smooth muscle actin (α-sma), anti-s-100 protein, anti-c-kit (CD117) (Table 1.). All tumours showed vimentin-positivity. Two gastric tumours (2/15; 13.33%) were positive for α-sma, and were negative for S-100 protein and c-kit. These tumours, according to the fi rst (histological) diagnosis, were histopathological declared leiomyoma. The other tumours (13/15; 86.67%) were c-kit-positive, and except for one (12/15; 80%) were S-100 protein-positive, furthermore all these tumours (13/15; 86.67%) were α-sma-negative (Figures 6 9.). Based on immunohistochemical analysis the defi nitive, revised diagnosis of the c-kit-positive 13 tumours ([fi rst, histological diagnosis was gastric leiomyoma, n = 6]; [first, histological diagnosis was intestinal leiomyosarcoma, n = 6]; [fi rst, histological diagnosis was oesophageal leiomyosarcoma, n = 1]) was gastrointestinal stromal tumour (Table 2.). The author suggests the immunohistochemical analysis, with anti-vimentin, anti-α-sma, anti-s- 100 protein, and anti-c-kit antibodies of the canine fusocellular soft tissue biopsy, necropsy samples, for the correct defi nitive diagnosis. 29
30 8. KÖSZÖNETNYILVÁNÍTÁS Szeretném elsősorban megköszönni témavezetőmnek Dr. Jakab Csabának a felajánlott témát, a sok közös kutatást és munkát, amely során sok, a jövőben is használható tudással gazdagodtam. Köszönöm Prof. Dr. Rusvai Miklósnak a Patológiai Tanszék vezetőjének, hogy engedélyével hozzájárult a tanszéken készített szakdolgozatomhoz. Szeretnék köszönetet mondani mindazoknak, akik munkájukkal és tanácsaikkal segítették jelen dolgozat elkészítését: Pekár Magdolnának és Gregor Viktóriának, akik az immunhisztkémiai vizsgálatokban adtak nélkülözhetetlen segítséget, ill. Pop Renátának aki a kórszövettani metszetek elkészítésében, festésében segített nekünk. 30
31 9. Irodalomjegyzék 1. CRETOIU, D. CRETOIU, S. M. ET AL.: TELOCYTES, A DISTINCT TYPE OF CELL AMONG THE STROMAL CELLS PRESENT IN THE LAMINA PROPRIA OF JEJUNUM. HISTOL. HISTOPATHOL., FLETCHER, C. D. M. BERMAN, J. J. ET AL.: DIAGNOSIS OF GASTROINTESTINAL STROMAL TUMORS: A CONSENSUS APPROACH. HUM. PATHOL., FROST, D. LASOTA, J. MIETTINEN, M.: GASTROINTESTINAL STROMAL TUMORS AND LEIOMYOMAS IN THE DOG: A HISTOPATHOLOGIC, IMMUNOHISTOCHEMICAL, AND MOLECULAR GENETIC STUDY OF 50 CASES.VET. PATHOL., HIROTA, S. ISOZAKI, K. ET AL.: GAIN-OF-FUNCTION MUTATIONS OF C-KIT IN HUMAN GASTROINTESTINAL STROMAL TUMORS. SCIENCE, JAKAB CS. SZABÁRA Á. BENDZSEL D.: A KUTYÁK GYULLADÁSOS MYOFIBROBLASTOS DAGANATÁNAK IMMUNHISZTOKÉMIAI VIZSGÁLATA. MAGY. ÁLLATORV. LAPJA, JOENSUU, H. ROBERTS, P. J. ET AL.: EFFECT OF THE TYROSINE KINASE INHIBITOR STI571 IN A PATIENT WITH AMETASTATIC GASTROINTESTINAL STROMAL TUMOR. N. ENGL. J. MED., KINDBLOM, L. G. REMOTTI, H. E. ET AL.: GASTROINTESTINAL PACEMAKER CELL TUMOR (GIPACT): GASTROINTESTINAL STROMAL TUMORS SHOW PHENOTYPIC CHARACTERISTICS OF THE INTERSTITIAL CELLS OF CAJAL. AM. J. PATHOL., LANDHERR L.: GASTROINTESTINÁLIS STROMÁLIS TUMOROK (GIST). GASTUPDATE, LAROCK, R. G. GINN, P. E.: IMMUNOHISTOCHEMICAL STAINING CHARACTERISTICS OF CANINE GASTROINTESTINAL STROMAL TUMORS. VET. PATHOL., MAAS, C. P. TER HAAR, G. ET AL.: RECLASSIFI CATION OF SMALL INTESTINAL AND CECAL SMOOTH MUSCLE TUMORS IN 72 DOGS: CLINICAL, HISTOLOGIC, AND IMMUNOHISTOCHEMICAL EVALUATION.VET. SURG., MAZUR, M. T. CLARK, H. B.: GASTRIC STROMAL TUMORS: REAPPRAISAL OF HISTOGENESIS. AM. J. SURG. PATHOL., MIETTINEN, M. WANG, Z. F. LASOTA, J.: DOG1 ANTIBODY IN THE DIFFERENTIAL DIAGNOSIS OF GASTROINTESTINAL STROMAL TUMORS: A STUDY OF 1840 CASES. AM. J. SURG. PATHOL.,
32 13. NANNINI, M. BIASCO, G. ET AL.: INSULIN-LIKE GROWTH FACTOR (IGF) SYSTEM AND GASTROINTESTINAL STROMAL TUMOURS (GIST): PRESENT AND FUTURE. HISTOL. HISTOPATHOL., NATALI, P. G. NICOTRA, M. R. ET AL.: EXPRESSION OF C-KIT RECEPTOR IN NORMAL AND TRANSFORMED HUMAN NONLYMPHOID TISSUES. CANCER RES., OROSZ ZS. BALÁZS D. SÁPI Z. TISZLAVICZ L. TORNÓCZKY T.: GASTROINTESTINALIS MESENCHYMALIS DAGANATOK ÚJRAOSZTÁLYOZÁSA. MAGYAR ONKOLÓGIA, REITH, J. D. GOLDBLUM, J. R. ET AL.: EXTRAGASTROINTESTINAL (SOFT TISSUE) STROMAL TUMORS: AN ANALYSIS OF 48 CASES WITH EMPHASIS ON HISTOLOGIC PREDICTORS OF OUTCOME. MOD. PATHOL., RUSU, M. C. POP, F. ET AL.: TELOCYTES FORM NETWORKS IN NORMAL CARDIAC TISSUES. HISTOL. HISTOPATHOL., SANDERS, K. M. KOH. S. D. WARD, S. M.: INTERSTITIAL CELLS OF CAJAL AS PACEMAKERS IN THE GASTROINTESTINAL TRACT. ANNU. REV. PHYSIOL., SHERRINGTON, C. S.: SANTIAGO RAMON Y CAJAL OBITUARY NOTICES OF FELLOWS OF THE ROYAL SOCIETY TSUJIMURA, T. FURITSU, T. ET AL.: LIGAND-INDEPENDENT ACTIVATION OF C-KIT RECEPTOR TYROSINE KINASE IN A MURINE MASTOCYTOMA CELL LINE P-815 GENERATED BY A POINT MUTATION. BLOOD, WU, B. LIU, L. ET AL.: DISTRIBUTION OF INTERSTITIAL CELLS OF CAJAL IN MERIONES UNGUICULATUS AND ALTERATIONS IN THE DEVELOPMENT OF INCOMPLETE INTESTINAL OBSTRUCTION. HISTOL. HISTOPATHOL., XU, C. LIU, Y. L. ET AL.: SYNCHRONOUS AND METACHRONOUS MULTIPLE GASTROINTESTINAL STROMAL TUMORS. HISTOL. HISTOPATHOL., YARDEN, Y. KUANG, W. J. ET AL.: HUMAN PROTOONCOGENE C-KIT: A NEW CELL SURFACE RECEPTOR TYROSINE KINASE FOR AN UNIDENTIFI ED LIGAND. EMBO J., AZ EGÉSZSÉGÜGYI MINISZTÉRIUM SZAKMAI PROTOKOLLJA: GASTROINTESTINÁLIS STROMÁLIS TUMOROK (GIST).KÉSZÍTETTE: A SEBÉSZETI SZAKMAI KOLLÉGIUM 32
33 25. F. DEL PIERO - B. A. SUMMERS - J. F. CUMMINGS - G. MANDELLI - E. A. BLOMME: Gastrointestinal Stromal Tumors in Equids. Vet Pathol Deanna D. Dailey. - E. J. Ehrhart - Dawn L. Duval - Todd Bass - B. E. Powers: DOG1 is a sensitive and specific immunohistochemical marker for diagnosis of canine gastrointestinal stromal tumors. Journal of Veterinary Diagnostic Investigation (3) M. IRIE Y. TAKEUCHI Y. OHTAKE H. SUZUKI N. NAGATA T. MIYOSHI Y. KAGAWA T. YAMAGAMI: Imatinib Mesylate Treatment in a Dog with Gastrointestinal Stromal Tumors with ac-kit mutation. The Journal of Veterinary Medical Science M. KOBAYASHI S. KUROKI K. ITO A. YASUDA H. SAWADA K. ONO T. WASHIZU M. ONKOBARA: Imatinib-associated tumour response in a dog with a nonresectable gastrointestinal stromal tumour harbouring a c-kit exon 11 deletion mutation. The Veterinary Journal K. HANAZONO S. FUKUMOTO K. HIRAYAMA K. TAKASHIMA Y. YAMANE M. NATSUHORI T. KADOSAWA T. UCHIDE: Predicting Metastatic Potential of Gastrointestinal Stromal Tumors in Dog by Ultrasonography. J. Vet. Med. Sci (11): V. Gillespie - K. Baer - J. Farrelly - D. Craft - R. Luong: Canine Gastrointestinal Stromal Tumors: Immunohistochemical Expression of CD34 and Examination of Prognostic Indicators Including Proliferation Markers Ki67 and AgNOR. Veterinary Pathology (1)
Gastrointestinalis mesenchymalis daganatok újraosztályozása
 Gastrointestinalis mesenchymalis daganatok újraosztályozása Összefoglaló Orosz Zsolt, Balázs Dezsô 1, Sápi Zoltán 2, Tiszlavicz lászló 3, Tornóczky Tamás 4 Országos Onkológiai Intézet, Daganatpathologiai
Gastrointestinalis mesenchymalis daganatok újraosztályozása Összefoglaló Orosz Zsolt, Balázs Dezsô 1, Sápi Zoltán 2, Tiszlavicz lászló 3, Tornóczky Tamás 4 Országos Onkológiai Intézet, Daganatpathologiai
Post mortem diagnosztizált GIST esetekről. Jäckel Márta HM Állami Egészségügyi Központ 2008. október 9-11.
 Post mortem diagnosztizált GIST esetekről Jäckel Márta HM Állami Egészségügyi Központ 2008. október 9-11. Mi a GIST? GIST (GastroIntestinális Stromális Tumor) G - 40-70 % gyomor I - 20-40 % vékonybél;
Post mortem diagnosztizált GIST esetekről Jäckel Márta HM Állami Egészségügyi Központ 2008. október 9-11. Mi a GIST? GIST (GastroIntestinális Stromális Tumor) G - 40-70 % gyomor I - 20-40 % vékonybél;
III./5. GIST. Bevezetés. A fejezet felépítése. A.) Panaszok. B.) Anamnézis. Pápai Zsuzsanna
 III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
III./5. GIST Pápai Zsuzsanna A fejezet célja: a GIST daganatok epidemiológiájának, tüneteinek, diagnosztikájának valamint, kezelési lehetőségeinek áttekintése egy beteg esetének bemutatásán keresztül.
patológi Klinikum Az emlımirigytumorok szövettani csoportosítása: Malignus tumorok Benignus tumorok Dysplasiák/hyperplasiák
 A kutyák emlıtumorainak patológi giája Dr. Jakab Csaba SZIE - ÁOTK Kórbonctani és Igazságügyi Állatorvostani Tanszék Budapest 1078 István u. 2. 2012 A kutyák emlıtumorainak patológi giája Klinikum Az emlımirigytumorok
A kutyák emlıtumorainak patológi giája Dr. Jakab Csaba SZIE - ÁOTK Kórbonctani és Igazságügyi Állatorvostani Tanszék Budapest 1078 István u. 2. 2012 A kutyák emlıtumorainak patológi giája Klinikum Az emlımirigytumorok
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján)
 pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
pt1 colorectalis adenocarcinoma: diagnózis, az invázió fokának meghatározása, a daganatos betegség ellátása (EU guideline alapján) Szentirmay Zoltán Országos Onkológiai Intézet Daganatpatológiai Centrum
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet. Frank Diagnosztika Szimpózium, DAKO workshop 2012.
 Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
Tóth Erika Sebészeti és Molekuláris Patológia Osztály Országos Onkológiai Intézet Frank Diagnosztika Szimpózium, DAKO workshop 2012.december 7 Follicularis hám eredetű daganatok Jól differenciált tumorok
A GYOMOR DAGANATOS MEGBETEGEDÉSEI
 A GYOMOR DAGANATOS MEGBETEGEDÉSEI DR. LÉNÁRT ZSUZSANNA SZEGEDI TUDOMÁNYEGYETEM I.SZ. BELGYÓGYÁSZATI KLINIKA A GYOMOR JÓINDULATÚ DAGANATAI ("protrudáló gyomorlaesiók", " gyomorpolypusok") eredetük szerint
A GYOMOR DAGANATOS MEGBETEGEDÉSEI DR. LÉNÁRT ZSUZSANNA SZEGEDI TUDOMÁNYEGYETEM I.SZ. BELGYÓGYÁSZATI KLINIKA A GYOMOR JÓINDULATÚ DAGANATAI ("protrudáló gyomorlaesiók", " gyomorpolypusok") eredetük szerint
Mit is csinál pontosan a patológus?
 Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
Szász A. Marcell Mit is csinál pontosan a patológus? Ceglédi Kossuth Lajos Gimnázium Cegléd, 2015. március 19. www.meetthescientist.hu 1 26 Google - patológus www.meetthescientist.hu 2 26 Google - patológia
A.) Biopsziás mintavétel lehetőségei és a biopsziás anyagok kezelésével kapcsolatos tudnivalók.
 II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
II./2.5. fejezet: Daganatok szövettani diagnosztikája Kulka Janina Ebben a fejezetben a daganatból történő szövettani mintavétel lehetőségeit és értékelését, illetve értékének korlátait, valamint a sebészeti
Epithelialis-mesenchymalis átmenet vastagbél daganatokban
 Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
Epithelialis-mesenchymalis átmenet vastagbél daganatokban Éles Klára Országos Onkológiai Intézet Sebészi és Molekuláris Daganatpatológiai Centrum Budapest, 2010. 12. 03. Epithelialis-mesenchymalis átmenet
A má m j á se s bé b sz s e z te A a n tó t mi m a i i i á tt t e t kin i t n é t s h l e y l e y ző d s A m áj s áj ebé b sze z te
 A máj sebészete Anatómiai áttekintés A máj sebészete Dr. Németh Tibor Ph.D egyetemi docens SzIE, ÁOTK Sebészeti és Szemészeti Tanszék és Klinika helyeződés (epigastrium) részei (lobus dext., sin. lat.
A máj sebészete Anatómiai áttekintés A máj sebészete Dr. Németh Tibor Ph.D egyetemi docens SzIE, ÁOTK Sebészeti és Szemészeti Tanszék és Klinika helyeződés (epigastrium) részei (lobus dext., sin. lat.
A GI daganatok onkológiai kezelésének alapelvei. dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika
 A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
A GI daganatok onkológiai kezelésének alapelvei dr Lohinszky Júlia SE II. sz Belgyógyászati Klinika Onkológiai ellátás Jelentősége Elvei Szemléletváltás szükségessége Klinikai onkológia Kemoterápia kit,
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK
 SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
SUPRACLAVICULARIS NYIROKCSOMÓ DAGANATOK DIFFERENCIÁLDIAGNOSZTIKÁJA CSAPDÁK Péter Ilona¹, Boér András² és Orosz Zsolt¹ Országos Onkológiai Intézet, Humán és Kísérletes Daganatpatológiai Osztály¹ és Fej-Nyak,
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr.
 Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
Célzott terápiás diagnosztika Semmelweis Egyetem I.sz. Pathologiai és Kísérleti Rákkutató Intézet, Budapest Tamási Anna, Dr. Krenács Tibor KROMAT Dako szeminárium 2017. Napjainkban egyre nagyobb teret
67. Pathologus Kongresszus
 A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
A kemoirradiáció okozta oncocytás átalakulás szövettani, immunhisztokémiai, ultrastruktúrális jellemzői és lehetséges prognosztikus jelentősége rectum adenocarcinomákban 67. Pathologus Kongresszus Bogner
Fejezetek a klinikai onkológiából
 Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
Fejezetek a klinikai onkológiából Előadás jegyzet Szegedi Tudományegyetem Általános Orvosi Kar Onkoterápiás Klinika 2012. A patológiai, képalkotó és laboratóriumi diagnosztika jelentősége az onkológiában.
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a PD-L1 és PD-1 fehérjék túlélésre gyakorolt hatása
 Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Tüdő adenocarcinomásbetegek agyi áttéteiben jelenlévő immunsejtek, valamint a és PD-1 fehérjék túlélésre gyakorolt hatása Téglási Vanda, MoldvayJudit, Fábián Katalin, Csala Irén, PipekOrsolya, Bagó Attila,
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása.
 Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
Kérdések és megoldások Immunhisztokémiai eljárások. Az eredmények interpretálása. Kerekasztal moderátor Péter Ilona Dako Workshop A Frank Diagnosztika Kft. és az Országos Onkológiai Intézet szervezésében
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
Esetbemutatás. Dr. Iván Mária Uzsoki Kórház 2013.11.07.
 Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Esetbemutatás Dr. Iván Mária Uzsoki Kórház 2013.11.07. Esetbemutatás I. 26 éves férfi 6 héttel korábban bal oldali herében elváltozást észlelt,majd 3 héttel később haemoptoe miatt kereste fel orvosát antibiotikumos
Dr Tóth László Országos Onkológiai Intázet Általános és Mellkassebészeti Osztály
 Primer retroperitonealis daganatok sebészi kezelése Dr Tóth László Országos Onkológiai Intázet Általános és Mellkassebészeti Osztály Sebészi anatómia Felül: rekeszkupola felső áthajlása Alul: diaphragma
Primer retroperitonealis daganatok sebészi kezelése Dr Tóth László Országos Onkológiai Intázet Általános és Mellkassebészeti Osztály Sebészi anatómia Felül: rekeszkupola felső áthajlása Alul: diaphragma
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében
 A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
A tüdőcitológia jelentősége a tüdődaganatok neoadjuváns kezelésének tervezésében Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató Intézet 70. Patológus Kongresszus Siófok 2011. szept. 29 - okt.1.
szerzett tapasztalataink néhány eset kapcsán
 Telkes Gábor 1. oldal 2008.02.02. A GastroIntestinalis Stroma Tumorok sebészi kezelésében szerzett tapasztalataink néhány eset kapcsán Our experiences with surgical treatment of gastrointestinal stromal
Telkes Gábor 1. oldal 2008.02.02. A GastroIntestinalis Stroma Tumorok sebészi kezelésében szerzett tapasztalataink néhány eset kapcsán Our experiences with surgical treatment of gastrointestinal stromal
Az Egészségügyi Minisztérium szakmai protokollja Gastrointestinális Stromális Tumorok (GIST) Készítette: A Sebészeti Szakmai Kollégium
 I. Alapvető megfontolások Az Egészségügyi Minisztérium szakmai protokollja Gastrointestinális Stromális Tumorok (GIST) Készítette: A Sebészeti Szakmai Kollégium 1. Definíció A Gastrointestinális stromális
I. Alapvető megfontolások Az Egészségügyi Minisztérium szakmai protokollja Gastrointestinális Stromális Tumorok (GIST) Készítette: A Sebészeti Szakmai Kollégium 1. Definíció A Gastrointestinális stromális
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei
 A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A keringı tumor markerek klinikai alkalmazásának aktuális kérdései és irányelvei A TM vizsgálatok alapkérdései A vizsgálatok célja, információértéke? Az alkalmazás területei? Hogyan válasszuk ki az alkalmazott
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet november 19., ÁOK, III.
 ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
ONKOLÓGIA Bödör Csaba I. sz. Patológiai és Kísérleti Rákkutató Intézet 2018. november 19., ÁOK, III. bodor.csaba1@med.semmelweis-univ.hu ONKOLÓGIA Daganatok általános jellemzése, benignus és malignus daganatok
Az Egészségügyi Minisztérium módszertani levele Lágyrésztumorok kórszövettani diagnosztikája
 Az Egészségügyi Minisztérium módszertani levele Lágyrésztumorok kórszövettani diagnosztikája Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium 1. Bevezetés Minthogy a lágyrésztumorok
Az Egészségügyi Minisztérium módszertani levele Lágyrésztumorok kórszövettani diagnosztikája Készítette: Az Országos Pathologiai Intézet és a Pathologus Szakmai Kollégium 1. Bevezetés Minthogy a lágyrésztumorok
Gastrointestinalis stromalis tumorok
 HASI DIAGNOSZTIKA Összefoglaló közlemény Gastrointestinalis stromalis tumorok Bahéry Mária A gastrointestinalis stromalis tumorok az emésztôrendszer leggyakoribb mesenchymalis daganatai. Differenciációs
HASI DIAGNOSZTIKA Összefoglaló közlemény Gastrointestinalis stromalis tumorok Bahéry Mária A gastrointestinalis stromalis tumorok az emésztôrendszer leggyakoribb mesenchymalis daganatai. Differenciációs
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése
 Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Colorectalis carcinomában szenvedő betegek postoperatív öt éves követése Kegyes Lászlóné 1, Némethné Lesó Zita 1, Varga Sándor Attiláné 1, Barna T. Katalin 1, Rombauer Edit 2 Dunaújvárosi Prodia Központi
Kettôs tumorok a gasztrointesztinális traktusban: szinkron és metakron stromális (GIST) és epiteliális/neuroendokrin daganatok
 Kettôs tumorok a gasztrointesztinális traktusban: szinkron és metakron stromális (GIST) és epiteliális/neuroendokrin daganatok Eredeti közlemény Kövér Erika, 1 Faluhelyi Zsolt, 1 Bogner Barna, 2 Kalmár
Kettôs tumorok a gasztrointesztinális traktusban: szinkron és metakron stromális (GIST) és epiteliális/neuroendokrin daganatok Eredeti közlemény Kövér Erika, 1 Faluhelyi Zsolt, 1 Bogner Barna, 2 Kalmár
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában
 Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
Lehetőségek és korlátok a core-biopszián alapuló limfóma diagnosztikában Strausz Tamás Tóth Erika Országos Onkológiai Intézet Sebészeti és Molekuláris Patológiai Osztály FiPaT 2012 Elvi alapok WHO klasszifikáció
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody
 CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
CONFIRM anti-estrogen Receptor (ER) (SP1) Rabbit Monoclonal Primary Antibody 790-4324 50 790-4325 250 FELHASZNÁLÁSI TERÜLET 1. ábra. CONFIRM anti-er (SP1) festés lobuláris emlőcarcinómában. Ez az antitest
A daganatok pathologiája. A daganatok pathológiája
 A daganatok pathologiája A daganatok pathológiája Alapfogalmak Neoplasia (új növedék) - daganat Rokonértelmű: tumor - duzzanat Oncologia (görög: onkos; duzzanat ) daganatos betegségek vizsgálatával foglalkozó
A daganatok pathologiája A daganatok pathológiája Alapfogalmak Neoplasia (új növedék) - daganat Rokonértelmű: tumor - duzzanat Oncologia (görög: onkos; duzzanat ) daganatos betegségek vizsgálatával foglalkozó
A göbös pajzsmirigy kivizsgálása, ellátása. Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika
 A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
A göbös pajzsmirigy kivizsgálása, ellátása Mészáros Szilvia dr. Semmelweis Egyetem I. sz. Belgyógyászati Klinika Pajzsmirigy göbök A lakosság 4-8%-ának van tapintható göbe. Ultrahanggal a lakosság közel
2355-06 Egyéb citológiai vizsgálatok követelménymodul szóbeli vizsgafeladatai
 1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
1. feladat Tájékoztassa a munkahelyére érkező vendégeket a különféle szervekből nyert citológiai anyagok feldolgozásáról, diagnosztikára való előkészítéséről! Tájékoztatója során az alábbi szempontokra
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata
 Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
Primer emlőcarcinomák és metasztázisaik immunfenotípusának vizsgálata Lukács Lilla Vanda, Szász A. Marcell, Tőkés Anna-Mária, Kiss Orsolya, Lőrincz Tamás, Kulka Janina Az emlőrákok újabban azonosított
M E G H Í V Ó. HSAVA őszi, háromnapos 39. országos konferenciája. meghívott külföldi előadó: Susan Little (Kanada) és Tim Hackett (USA)
 M E G H Í V Ó HSAVA őszi, háromnapos 39. országos konferenciája meghívott külföldi előadó: Susan Little (Kanada) és Tim Hackett (USA) MÁOK által elismert KIEMELT RENDEZVÉNY (legalább 2 napon történő részvétel
M E G H Í V Ó HSAVA őszi, háromnapos 39. országos konferenciája meghívott külföldi előadó: Susan Little (Kanada) és Tim Hackett (USA) MÁOK által elismert KIEMELT RENDEZVÉNY (legalább 2 napon történő részvétel
Diagnosztikai irányelvek Paget-kórban
 Diagnosztikai irányelvek Paget-kórban Dr. Donáth Judit Országos Reumatológiai és Fizioterápiás Intézet, Budapest HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012-2014 2015. ÁPRILIS 17.
Diagnosztikai irányelvek Paget-kórban Dr. Donáth Judit Országos Reumatológiai és Fizioterápiás Intézet, Budapest HALADÁS A REUMATOLÓGIA, IMMUNOLÓGIA ÉS OSTEOLÓGIA TERÜLETÉN 2012-2014 2015. ÁPRILIS 17.
II./3.3.2 fejezet:. A daganatok célzott kezelése
 II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
II./3.3.2 fejezet:. A daganatok célzott kezelése Kopper László A fejezet célja, hogy megismerje a hallgató a célzott terápiák lehetőségeit és a fejlesztés lényeges lépéseit. A fejezet teljesítését követően
Többes malignus tumoros eseteink elemzése. Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya
 Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Többes malignus tumoros eseteink elemzése Mihály O, Szűcs I, Almási K KEMÖ Szent Borbála Kórháza Tatabánya Szövettanilag bizonyított tumoros betegség Különböző szövettani típus Azonos vagy különböző szervek
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok
 Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Her2 fehérje overexpresszió gyomorrákokban: Hazai tapasztalatok Dr. Lotz Gábor, Dr. Szirtes Ildikó, Dr. Kiss András Prof. Tímár József, Prof. Kulka Janina Semmelweis Egyetem II. Pathologiai Intézet - Exophyticus
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával
 Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Szinoviális szarkómák patogenezisében szerepet játszó szignálutak jellemzése szöveti multiblokk technika alkalmazásával Fónyad László 1, Moskovszky Linda 1, Szemlaky Zsuzsanna 1, Szendrői Miklós 2, Sápi
Cutan lágyrészdaganatok. Sápi Zoltán SE I. Sz. Patológiai és Kísérleti Rákkutató Intézet
 Cutan lágyrészdaganatok Sápi Zoltán SE I. Sz. Patológiai és Kísérleti Rákkutató Intézet Bőr WHO, 2006 Fibrosus, fibrohistocytás, histiocytás tumorok Vascularis tumorok Lymphaticus tumorok Sima és harántcsíkolt
Cutan lágyrészdaganatok Sápi Zoltán SE I. Sz. Patológiai és Kísérleti Rákkutató Intézet Bőr WHO, 2006 Fibrosus, fibrohistocytás, histiocytás tumorok Vascularis tumorok Lymphaticus tumorok Sima és harántcsíkolt
Gasztrointesztinális tumorok. Esetbemutatások
 Gasztrointesztinális tumorok Esetbemutatások 1. Eset: 54 éves férfibeteg 1997 jul.-ban sigma tumor miatt sigma resectio. Szövettan: adenocc. G3, pt3, pn0 (5 nyirokcsomóból) pn0, kevés eltávolított nycs.
Gasztrointesztinális tumorok Esetbemutatások 1. Eset: 54 éves férfibeteg 1997 jul.-ban sigma tumor miatt sigma resectio. Szövettan: adenocc. G3, pt3, pn0 (5 nyirokcsomóból) pn0, kevés eltávolított nycs.
2354-06 Nőgyógyászati citodiagnosztika követelménymodul szóbeli vizsgafeladatai
 1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
1. feladat A laboratóriumba vendég érkezik. Tájékoztassa a rákmegelőzés lehetőségeiről! Ismertesse a citológiai előszűrő vizsgálatok lényegét! - a primer és szekunder prevenció fogalma, eszközei - a citológia
 Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia -cysta - tályog -daganat
Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia -cysta - tályog -daganat
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI
 DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
DIGITÁLIS MIKROSZKÓPIA AZ EMÉSZTŐRENDSZERI SZÖVETI MINTÁK DIAGNOSZTIKÁJÁBAN Doktori tézisek Ficsór Levente Semmelweis Egyetem, 2. sz. Belgyógyászati Klinika Klinikai Orvostudományok Doktori Iskola Programvezető:
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének vizsgálata
 Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
Az ABCG2 multidrog transzporter fehérje szerkezetének és működésének Kutatási előzmények Az ABC transzporter membránfehérjék az ATP elhasítása (ATPáz aktivitás) révén nyerik az energiát az általuk végzett
 Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
Sebész szerepe az axilla ellátásában Mersich Tamás Uzsoki utcai Kórház Sebészeti-onkosebészeti Osztály 2014. május 24. Kecskemét Bevezetés A nyirokcsomók sebészi eltávolítása felel a legtöbb szövődményért
A fasciitis nodularis ritka formája
 Az Országos Traumatológiai Intézet közleménye A fasciitis nodularis ritka formája DR. RÉKÓ GYULA, DR. LACZKÓ TIBOR Érkezett: 1999. február 22. ÖSSZEFOGLALÁS A szerzõk az agresszív fibromatosisok csoportjába
Az Országos Traumatológiai Intézet közleménye A fasciitis nodularis ritka formája DR. RÉKÓ GYULA, DR. LACZKÓ TIBOR Érkezett: 1999. február 22. ÖSSZEFOGLALÁS A szerzõk az agresszív fibromatosisok csoportjába
A fejezet felépítése. A.) Általános nevezéktan
 II./1.4. fejezet: Nevezéktan, stádiumbeosztás Torgyík László, Dank Magdolna A fejezet áttekintése során a hallgató megismerkedik az onkológiai kezelések során használatos kifejezések értemével és a TNM-osztályozás
II./1.4. fejezet: Nevezéktan, stádiumbeosztás Torgyík László, Dank Magdolna A fejezet áttekintése során a hallgató megismerkedik az onkológiai kezelések során használatos kifejezések értemével és a TNM-osztályozás
A születéskor gyűjthető. őssejtekről, felhasználási. lehetőségükről, valamint a KRIO Intézet. szolgáltatásairól
 A születéskor gyűjthető őssejtekről, felhasználási lehetőségükről, valamint a KRIO Intézet szolgáltatásairól krio Családi Őssejtbank A KRIO Intézet Sejt- és Szövetbank Zrt. 2004 óta végzi köldökzsinórvér
A születéskor gyűjthető őssejtekről, felhasználási lehetőségükről, valamint a KRIO Intézet szolgáltatásairól krio Családi Őssejtbank A KRIO Intézet Sejt- és Szövetbank Zrt. 2004 óta végzi köldökzsinórvér
Epithelioid lágyrészdaganatok differenciáldiagnosztikája
 DAKOCytomation Workshop Budapest Epithelioid lágyrészdaganatok differenciáldiagnosztikája dr. Orosz Zsolt 2008. december 05. Epithelioid sejttípus Resembling epithelium In a general sense, a cell that
DAKOCytomation Workshop Budapest Epithelioid lágyrészdaganatok differenciáldiagnosztikája dr. Orosz Zsolt 2008. december 05. Epithelioid sejttípus Resembling epithelium In a general sense, a cell that
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén
 Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Sentinel nyirokcsomó biopszia szájüregi laphámrák esetén Dr. Patkó Tamás, dr. Koltai Pál, dr. Remenár Éva, dr. Boér András Országos Onkológiai Intézet Fej-nyak-állcsont és Rekonstrukciós Sebészeti Osztály
Immunológia I. 4. előadás. Kacskovics Imre
 Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
Immunológia I. 4. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) 3.1. ábra A vérsejtek képződésének helyszínei az élet folyamán 3.2. ábra A hemopoetikus őssejt aszimmetrikus osztódása 3.3. ábra
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2.
 A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
A tananyag tanulási egységei I. Általános elméleti onkológia I/1. Jelátviteli utak szerepe a daganatok kialakulásában I/2. Vírusok szerepe a daganatok kialakulásában I/3. A környezet hatása a daganatok
Immunológia I. 2. előadás. Kacskovics Imre (imre.kacskovics@ttk.elte.hu)
 Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Immunológia I. 2. előadás Kacskovics Imre (imre.kacskovics@ttk.elte.hu) Az immunválasz kialakulása A veleszületett és az adaptív immunválasz összefonódása A veleszületett immunválasz mechanizmusai A veleszületett
Semmelweis Egyetem, Budapest, Onkológiai Tanszék, Országos Onkológiai Intézet, 1122 Ráth Gy. u. 7-9.
 Semmelweis Egyetem, Budapest, Onkológiai Tanszék, Országos Onkológiai Intézet, 1122 Ráth Gy. u. 7-9. Tanszékvezető: Prof. dr. Polgár Csaba, egyetemi tanár Tel.: +36-1-224-8690 E-mail: polgar@oncol.hu Web-site:
Semmelweis Egyetem, Budapest, Onkológiai Tanszék, Országos Onkológiai Intézet, 1122 Ráth Gy. u. 7-9. Tanszékvezető: Prof. dr. Polgár Csaba, egyetemi tanár Tel.: +36-1-224-8690 E-mail: polgar@oncol.hu Web-site:
A mellékvese és a retroperitoneum képalkotó diagnosztikája
 Dr. Palkó András A mellékvese és a retroperitoneum képalkotó diagnosztikája Vizsgáló módszerek: natív röntgen (felvétel, átvilágítás, tomogr.) kontrasztanyagos röntgen (incl. angiographia) ultrahang (b-mód,
Dr. Palkó András A mellékvese és a retroperitoneum képalkotó diagnosztikája Vizsgáló módszerek: natív röntgen (felvétel, átvilágítás, tomogr.) kontrasztanyagos röntgen (incl. angiographia) ultrahang (b-mód,
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek?
 Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Mit tud a tüdő-citológia nyújtani a klinikus igényeinek? XVI. Citológus Kongresszus és akkreditált tanfolyam Siófok, 2017. március 30-április 1. Pápay Judit SE, I.sz.Patológiai és Kísérleti Rákkutató intézet
Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi Tudományegyetemen
 SZEGEDI TUDOMÁNYEGYETEM Szent-Györgyi Albert Klinikai Központ Patológiai Intézet Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi
SZEGEDI TUDOMÁNYEGYETEM Szent-Györgyi Albert Klinikai Központ Patológiai Intézet Endoszkópos ultrahang vezérelt finomtű aspiráció intraabdominalis daganatok diagnosztikájában: 6 év tapasztalatai a Szegedi
1) A molekuláris módszerek alkalmazhatósága és haszna az aspirációs citológiai diagnosztikában
 1 Szegedi Tudományegyetem Általános Orvostudományi Kar Pathologiai Intézet Tanszékvezető: Dr. Iványi Béla egyetemi tanár, D. Sc. 6720 Szeged, Állomás u. 2. (6701 Szeged, Pf. 427.) Tel: 62-545 878, 62-545148
1 Szegedi Tudományegyetem Általános Orvostudományi Kar Pathologiai Intézet Tanszékvezető: Dr. Iványi Béla egyetemi tanár, D. Sc. 6720 Szeged, Állomás u. 2. (6701 Szeged, Pf. 427.) Tel: 62-545 878, 62-545148
KUTYÁK ÉS MACSKÁK EMLÔTUMORAI ÉS HAZAI ELÔFORDULÁS SAJÁT ESETEK KAPCSÁN OLÓGIA ONKOLÓGIA
 ONK KUTYÁK ÉS MACSKÁK EMLÔTUMORAI IRODALMI ÁTTEKINTÉS ÉS HAZAI ELÔFORDULÁS SAJÁT ESETEK KAPCSÁN DR. PERGE EDINA MÁTRIX Kórszövettani és Citológiai Szolgáltatás J elen közlemény célja, hogy tájékoztatást
ONK KUTYÁK ÉS MACSKÁK EMLÔTUMORAI IRODALMI ÁTTEKINTÉS ÉS HAZAI ELÔFORDULÁS SAJÁT ESETEK KAPCSÁN DR. PERGE EDINA MÁTRIX Kórszövettani és Citológiai Szolgáltatás J elen közlemény célja, hogy tájékoztatást
A prostata sebészete. A prostata sebészeti jelentőségű. középkorú, ill. idős kanokban
 Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia --cysta -- tályog --daganat
Sebészeti anatómia ( ) A prostata sebészete Dr. Németh Tibor, PhD egyetemi docens Sebészeti anatómia ( ) A prostata sebészeti jelentőségű betegségei Benignus prostata hyperplasia --cysta -- tályog --daganat
FOLYAMATOS ORVOSTOVÁBBKÉPZÉS. A méhtest mesenchymalis daganatai
 FOLYAMATOS ORVOSTOVÁBBKÉPZÉS A méhtest mesenchymalis daganatai MAGYAR ÉVA DR. 1, SALAMON FERENC DR. 1, VAJDA KATALIN DR. 2 Fôvárosi Uzsoki utcai Kórház, Patológiai Osztály 1, Fôvárosi Szent János Kórház,
FOLYAMATOS ORVOSTOVÁBBKÉPZÉS A méhtest mesenchymalis daganatai MAGYAR ÉVA DR. 1, SALAMON FERENC DR. 1, VAJDA KATALIN DR. 2 Fôvárosi Uzsoki utcai Kórház, Patológiai Osztály 1, Fôvárosi Szent János Kórház,
Hivatalos Bírálat Dr. Gődény Mária
 Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Hivatalos Bírálat Dr. Gődény Mária:,,Multiparametrikus MR vizsgálat prognosztikai és prediktív faktorokat meghatározó szerepe fej-nyaki tumoroknál, valamint a kismedence főbb daganat csoportjaiban című
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata
 Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
Lymphoma sejtvonalak és gyerekkori leukémia (ALL) sejtek mikro RNS (mir) profiljának vizsgálata Dr. Nemes Karolina, Márk Ágnes, Dr. Hajdu Melinda, Csorba Gézáné, Dr. Kopper László, Dr. Csóka Monika, Dr.
A vesedaganatok sebészi kezelése
 A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
A vesedaganatok sebészi kezelése Szendrői Attila Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum Az Európai Urológus Testület képzőhelye Robson elvek (1963) Nincs szisztémás kezelés -radikális
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése
 Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
Két kevéssé ismert humán ABCG fehérje expressziója és funkcionális vizsgálata: ABCG1 és ABCG4 jellemzése Doktori tézisek Dr. Cserepes Judit Semmelweis Egyetem Molekuláris Orvostudományok Doktori Iskola
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház. Emlő MR vizsgálatok korai eredményei kórházunkban
 DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
DR. HAJNAL KLÁRA / DR. NAHM KRISZTINA KÖZPONTI RÖNTGEN DIAGNOSZTIKA Uzsoki utcai kórház Emlő MR vizsgálatok korai eredményei kórházunkban 2015.01.01-2016.04.30 között kórházunkban végzett emlő MR vizsgálatok
Férfi emlő és vékonybél leiomyosarcomája
 A férfi emlő rosszindulatú daganata a ritkább megbetegedések közé tartozik, Magyarországon, mint Európában általában, 100 női emlőrákra esik egy férfi emlőrák. Az emlő sarcomája a női emlő rosszindulatú
A férfi emlő rosszindulatú daganata a ritkább megbetegedések közé tartozik, Magyarországon, mint Európában általában, 100 női emlőrákra esik egy férfi emlőrák. Az emlő sarcomája a női emlő rosszindulatú
I. melléklet. Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása
 I. melléklet Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések,
I. melléklet Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések, valamint az elutasítás indokolása Az Európai Gyógyszerügynökség által beterjesztett tudományos következtetések,
A pre-analitika szerepe a patológiai minták. Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet
 A pre-analitika szerepe a patológiai minták megőrz rzöttségében Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet A sebészeti anyagok útja Műtő OPTIMÁLIS HŐMÉRSÉKLET (20-22 C) IDŐFAKTOR (15
A pre-analitika szerepe a patológiai minták megőrz rzöttségében Dr. Lotz Gábor Semmelweis Egyetem, II. sz. Patológiai Intézet A sebészeti anyagok útja Műtő OPTIMÁLIS HŐMÉRSÉKLET (20-22 C) IDŐFAKTOR (15
HORMONKEZELÉSEK. A hormonkezelés típusai
 HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
HORMONKEZELÉSEK A prosztatarák kialakulásában és progressziójában kulcsszerepük van a prosztatasejtek növekedését, működését és szaporodását elősegítő férfi nemi hormonoknak, az androgéneknek. Az androgének
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában
 Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
Új lehetőségek a tumoros emlőanyagok patológiai feldolgozásában Dr. Lippai Norbert Hetényi Géza Kórház, Szolnok Múlt és jelen Szakmai irányelvek a műtéti preparátumot az eltávolítás után azonnal (maximum
Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió
 Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió összefüggései Szentmártoni Gy., Zergényi É., Torgyík L., Tóth A., Szita A., Dank M. SE Radiológiai és Onkoterápiás
Emlőtumor agyi áttéteinek korszerű kezelése: a tumorválasz és extracraniális progresszió összefüggései Szentmártoni Gy., Zergényi É., Torgyík L., Tóth A., Szita A., Dank M. SE Radiológiai és Onkoterápiás
Regionális onkológiai centrum fejlesztése a markusovszky kórházban
 Regionális onkológiai centrum fejlesztése a markusovszky kórházban Regionális onkológiai centrum fejlesztése TIOp-2.2.6-12/1a-2013-0002 A megvalósult Fejlesztés célja: olyan komprehenzív Regionális Onkológiai
Regionális onkológiai centrum fejlesztése a markusovszky kórházban Regionális onkológiai centrum fejlesztése TIOp-2.2.6-12/1a-2013-0002 A megvalósult Fejlesztés célja: olyan komprehenzív Regionális Onkológiai
A GYOMOR-BÉL RENDSZERI DAGANATOK DIAGNOSZTIKÁJÁNAK AKTUÁLIS KÉRDÉSEI A PATOLÓGIAI GYAKORLATBAN
 A GYOMOR-BÉL RENDSZERI DAGANATOK DIAGNOSZTIKÁJÁNAK AKTUÁLIS KÉRDÉSEI A PATOLÓGIAI GYAKORLATBAN PhD értekezés Dr. Gonda Gábor Országos Gyógyintézeti Központ Patológiai Osztály Témavezeto: Dr. Kopper László
A GYOMOR-BÉL RENDSZERI DAGANATOK DIAGNOSZTIKÁJÁNAK AKTUÁLIS KÉRDÉSEI A PATOLÓGIAI GYAKORLATBAN PhD értekezés Dr. Gonda Gábor Országos Gyógyintézeti Központ Patológiai Osztály Témavezeto: Dr. Kopper László
A klinikai citológia alapjai
 A klinikai citológia alapjai Vajdovich Péter Szent István Egyetem Állatorvos-tudományi Kar Belgyógyászati Tanszék és Klinika Budapest A citológiai vizsgálatok célja elváltozások: normál, hiperplasztikus
A klinikai citológia alapjai Vajdovich Péter Szent István Egyetem Állatorvos-tudományi Kar Belgyógyászati Tanszék és Klinika Budapest A citológiai vizsgálatok célja elváltozások: normál, hiperplasztikus
Engedélyszám: /2011-EAHUF Analitika követelménymodul szóbeli vizsgafeladatai
 1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
1. feladat A műtőből olyan szövettani minták kerülnek a patológiai osztályra, melyek nincsenek kellően előkészítve. Magyarázza el a főműtősnőnek a minta előkészítésének fontosságát! Hívja fel a figyelmét
Őssejtkezelés kardiovaszkuláris kórképekben
 Őssejtkezelés kardiovaszkuláris kórképekben Papp Zoltán Debreceni Egyetem Kardiológiai Intézet Klinikai Fiziológiai Tanszék Megmenthető a károsodott szív őssejtekkel? Funkcionális változások az öregedő
Őssejtkezelés kardiovaszkuláris kórképekben Papp Zoltán Debreceni Egyetem Kardiológiai Intézet Klinikai Fiziológiai Tanszék Megmenthető a károsodott szív őssejtekkel? Funkcionális változások az öregedő
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen
 Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Az orvosi biotechnológiai mesterképzés megfeleltetése az Európai Unió új társadalmi kihívásainak a Pécsi Tudományegyetemen és a Debreceni Egyetemen Azonosító szám: Az orvosi biotechnológiai mesterképzés
Vaginalis angiofibroma diagnózisa kutyában. Diagnosis of a vaginal angiofibroma in a dog
 Vaginalis angiofibroma diagnózisa kutyában Diagnosis of a vaginal angiofibroma in a dog Gargya Sándor 1, Nagy Péter Kristóf 2, Müller Linda 3 és Jakab Csaba 4 Esettanulmány 1] Magánállatorvos 2] Magánállatorvos
Vaginalis angiofibroma diagnózisa kutyában Diagnosis of a vaginal angiofibroma in a dog Gargya Sándor 1, Nagy Péter Kristóf 2, Müller Linda 3 és Jakab Csaba 4 Esettanulmány 1] Magánállatorvos 2] Magánállatorvos
A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei
 Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Tolna Megyei Önkormányzat Balassa János Kórháza Pathologiai Osztály A jól differenciált gastrointestinalis neuroendocrin tumorok prognosztikai lehetőségei rutin pathologiai feldolgozás során Cifra János
Leukocyta scintigraphia - a gyulladásos bélbetegségek noninvazív vizsgálómódszereinek gold standard - je?
 Leukocyta scintigraphia - a gyulladásos bélbetegségek noninvazív vizsgálómódszereinek gold standard - je? Bevezetés Dr. Salamon Ágnes Szekszárd A gyulladásos bélbetegségek (inflammatory bowel diseases,
Leukocyta scintigraphia - a gyulladásos bélbetegségek noninvazív vizsgálómódszereinek gold standard - je? Bevezetés Dr. Salamon Ágnes Szekszárd A gyulladásos bélbetegségek (inflammatory bowel diseases,
A lágyrészsarcomák patológiája
 Összefoglaló közlemény 11 A lágyrészsarcomák patológiája Sápi Zoltán Semmelweis Egyetem, I. Sz. Patológiai és Kísérleti Rákkutató Intézet, Budapest A lágyrészsarcomák az összes malignus daganatok mintegy
Összefoglaló közlemény 11 A lágyrészsarcomák patológiája Sápi Zoltán Semmelweis Egyetem, I. Sz. Patológiai és Kísérleti Rákkutató Intézet, Budapest A lágyrészsarcomák az összes malignus daganatok mintegy
Szemeszter 2015.I.félév Jelleg
 Tanfolyam adatlap Alapadatok Kódszám Főcím Állapot Szervező Partner Szemeszter 2015.I.félév Jelleg Szabadon választható SE- TK/2015.I./00099 Daganatok és komplex terápiája A tanfolyamot az EEKH elfogadta,
Tanfolyam adatlap Alapadatok Kódszám Főcím Állapot Szervező Partner Szemeszter 2015.I.félév Jelleg Szabadon választható SE- TK/2015.I./00099 Daganatok és komplex terápiája A tanfolyamot az EEKH elfogadta,
A bőrmelanoma kezelésének módjai. Dr. Forgács Balázs Bőrgyógyászati Osztály
 A bőrmelanoma kezelésének módjai Dr. Forgács Balázs Bőrgyógyászati Osztály Melanoma TNM (AJCC VIII.) A melanoma kezelés alapja (T:tumor, N:nyirokcsomó, M:metasztázis) T: Breslow érték a legközelebbi 0,1
A bőrmelanoma kezelésének módjai Dr. Forgács Balázs Bőrgyógyászati Osztály Melanoma TNM (AJCC VIII.) A melanoma kezelés alapja (T:tumor, N:nyirokcsomó, M:metasztázis) T: Breslow érték a legközelebbi 0,1
ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA. Péter Ilona. ziuma Budapest 2008.
 ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA Péter Ilona Az Országos Onkológiai Intézet és s a Dako közös s szimpóziuma ziuma Budapest 2008. Oncocyta a pajzsmirigyben Definíci
ONCOCYTÁS S PAJZSMIRIGY TUMOROK DIFFERENCIÁLDIAGNOSZTIK LDIAGNOSZTIKÁJA Péter Ilona Az Országos Onkológiai Intézet és s a Dako közös s szimpóziuma ziuma Budapest 2008. Oncocyta a pajzsmirigyben Definíci
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA. Dr. Kurgyis Zsuzsanna
 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA TUMOR-SZTRÓMA SEJTFÚZIÓ HATÁSÁRA PhD tézis Dr. Kurgyis Zsuzsanna Bőrgyógyászati és Allergológiai Klinika Szegedi Tudományegyetem Szeged 2017 2 TUMORSEJTEK FENOTÍPUS-VÁLTOZÁSA
SZAKDOLGOZAT TÉMÁK. 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája.
 PTE ETK KAPOSVÁRI KÉPZÉSI KÖZPONT KÉPALKOTÓ DIAGNOSZTIKAI ANALITIKA SZAKIRÁNY SZAKDOLGOZAT TÉMÁK 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája. 2.) Az agy fejlődési rendellenességeinek
PTE ETK KAPOSVÁRI KÉPZÉSI KÖZPONT KÉPALKOTÓ DIAGNOSZTIKAI ANALITIKA SZAKIRÁNY SZAKDOLGOZAT TÉMÁK 1.) A stroke képalkotó diagnosztikája és differenciál diagnosztikája. 2.) Az agy fejlődési rendellenességeinek
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában. Cifra János. Tolna Megyei Balassa János Kórház, Pathologia Osztály
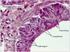 A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
A sejt és szövettani diagnosztika modern eszközei a diagnosztikában és terápiában Cifra János Tolna Megyei Balassa János Kórház, Pathologia Osztály Szekszárd 2016. Május 6. Patológus feladatai Preoperatív
Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában
 Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában G E LE N C S É R V I K TÓ R I A, B O É R K ATA LI N SZ E N T MA RGIT KÓ RH Á Z, O N KO LÓ GIA MAGYOT, 2016.05.05
Bevacizumab kombinációval elért hosszútávú remissziók metasztatikus colorectális carcinomában G E LE N C S É R V I K TÓ R I A, B O É R K ATA LI N SZ E N T MA RGIT KÓ RH Á Z, O N KO LÓ GIA MAGYOT, 2016.05.05
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend)
 A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
A nem világossejtes vesedaganatok diagnosztikájának és kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály
XIII./5. fejezet: Terápia
 XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
XIII./5. fejezet: Terápia A betegek kezelésekor a sebészi kezelés, a kemoterápia (klasszikus citotoxikus és a biológiai terápia), a radioterápia és ezek együttes alkalmazása egyaránt szóba jön. A gégének
Paradigmaváltás a daganatok patológiai diagnosztikájában: molekuláris alapú differenciáldiagnosztika, prognosztikus és prediktív patológia
 Paradigmaváltás a daganatok patológiai diagnosztikájában: molekuláris alapú differenciáldiagnosztika, prognosztikus és prediktív patológia Eredeti közlemény Orosz Zsolt 1, Sápi Zoltán 4, Szentirmay Zoltán
Paradigmaváltás a daganatok patológiai diagnosztikájában: molekuláris alapú differenciáldiagnosztika, prognosztikus és prediktív patológia Eredeti közlemény Orosz Zsolt 1, Sápi Zoltán 4, Szentirmay Zoltán
Tanfolyami órák Jelentkezési hat.idő 2013.01.11. www.oncol.hu. Sorsz. Nap Időpont Hossz Előadás címe Előadó Minősítése
 Tanfolyam adatlap Alapadatok Kódszám SE- TK/2013.I./00025 Szemeszter 2013.I.félév Jelleg Főcím Daganatok és komplex terápiája Állapot Tanfolyam adatok még változtathatóak a szervező által Szervező Országos
Tanfolyam adatlap Alapadatok Kódszám SE- TK/2013.I./00025 Szemeszter 2013.I.félév Jelleg Főcím Daganatok és komplex terápiája Állapot Tanfolyam adatok még változtathatóak a szervező által Szervező Országos
M E G H Í V Ó. Magyar Kisállatgyógyász Állatorvosok Egyesület (HSAVA), és a Federation of European Companion Animal Veterinary Associations (FECAVA)
 M E G H Í V Ó A Magyar Kisállatgyógyász Állatorvosok Egyesület (HSAVA), és a Federation of European Companion Animal Veterinary Associations (FECAVA) meghívja Önt a HSAVA és FECAVA tavaszi, háromnapos
M E G H Í V Ó A Magyar Kisállatgyógyász Állatorvosok Egyesület (HSAVA), és a Federation of European Companion Animal Veterinary Associations (FECAVA) meghívja Önt a HSAVA és FECAVA tavaszi, háromnapos
E4 A Gyermekkori szervezett lakossági emlőszűrések hatása az emlőműtétek
 08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
08.30-09.30 09.00-10.30 Pátria terem 2005. november 10. csütörtök E1 MEGNYITÓ E2 1.Nemzeti Üléselnökök: Rákkontroll Kovács Attila, Program Csonka I. Csaba, Ottó Szabolcs E3 Kásler Ottó jellegzetességei,
