PROTOKOLL A KRÓNIKUS VÍRUSHEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE
|
|
|
- Marcell Gál
- 9 évvel ezelőtt
- Látták:
Átírás
1 1. HÁTTÉR PROTOKOLL A KRÓNIKUS VÍRUSHEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE Az alábbi kezelési útmutatót a Gasztroenterológiai és Infektológiai Szakmai Kollégiumok által megbízott szakmai bizottság (aláírók) a krónikus vírushepatitis kezelésére az OEP által nevesített gasztroenterológusok és infektológusok részére állította össze és aktualizálta. A diagnosztikával kapcsolatos ajánlásokat az Orvosi Laboratóriumi Vizsgálatok Szakmai Kollégiuma is véleményezte. Az ajánlás felújított verziója a legújabb nemzetközi guide-line-ok alapján, a bizonyítékokon alapuló orvoslás tapasztalatai és a költség haszonszámítások, valamint a kezelésben gyakorlatot szerzett kollégák javaslatainak figyelembevételével készült, a szeptember 12-én, a hepatitis centrumok vezetői és a terápiás bizottság tagjai részvételével tartott kerekasztal megbeszélés alapján. Az ajánlásban leírtak nem helyettesítik az OGYI által elfogadott alkalmazási előiratokban foglaltakat! Ez az ajánlás az érintett Szakmai Kollégiumok által történő jóváhagyást és aláírást követően, az Egészségügyi Közlönyben történő megjelenés után válik hivatalos protokollá, és akkor lép érvénybe (addig szakmai ajánlásnak tekinthető). 2. KRÓNIKUS B HEPATITIS A kezelés feltételei HBsAg és HBV-DNS pozitivitás (mennyiségi PCR, akkreditált víruslaborban, CE jelzésű teszttel). HBV- DNS vizsgálat csak a kezelési indikáció felállításához szükséges, a fertőzőképességet a HBeAg pozitivitás igazolja. Hat hónapon belül 3 alkalommal emelkedett GPT érték, és/vagy szövettanilag igazolt krónikus hepatitis, hisztológiai aktivitással. (Konzekvensen emelkedett GPT és nagyobb, mint IU/ml feletti értékű HBV-DNS titer esetén a májbiopsiától el lehet tekinteni.) Kontraindikáció hiánya. Differenciáldiagnosztika: HBeAg, anti-hbe; HDAg, anti-hd-igm, totál anti-hd; anti-hcv. (Ezek eredménye a kezelési tervet befolyásolhatja.) A kezelést eldöntő vizsgálatok: HBV-DNS mennyiségi PCR, HBeAg, anti HDV IgM vagy HDV Ag. Májbiopsia: szövettanilag igazolt krónikus hepatitis. Hisztológiai aktivitási index, és/vagy fibroscan vizsgálat. Cirrhosis bármely stádiuma: HBV-DNS pozitivitás esetén a vírus titertől és a GPT től függetlenül kezelendő. Immunsupprimalt, szervtranszplantált beteg: HBsAg pozitivitás esetén a vírus titertől és a GPT től függetlenül kezelendő. Biológiai terápia előtt és csontvelő transzplantált betegben, ha a beteg antihbc pozitív, akkor HBV DNS javasolt, és pozitív lelelt esetén kezelendő. Cirrhosis Child A stádiuma: HDV Ag vagy anti-hdv IgM pozitivitás esetén a GPT-től függetlenül HBV- DNS negativitás esetén is IFN-nal kezelendő. Megjegyzés: anti-hdv IgM pozitivitás HBV-DNS negativitás esetén is a kezelés indikációja! A kezelést meghatározó eredmények: HBeAg pozitív, HBV-DNS IU/ml ( IU/ml = 10 5 copies/ml) felett, GPT emelkedett, vagy HBeAg negatív, HBV-DNS IU/ml ( IU/ml) felett, GPT emelkedett ha a GPT norm: májbiopsia. HAI >0 vagy fibroscan, ha a HBV-DNS fentinél alacsonyabb, de GPT emelkedett: májbiopsia, HAI>0 vagy fibroscan, ha a HBV-DNS fentinél alacsonyabb és a GPT norm.: nem kezelendő, obszerválandó. 1
2 2.2. Kezelési lehetőségek A kezelés megkezdése előtt a beteget tájékoztatni kell és a betegtől a tájékoztatásról írásos, aláírt, beleegyező nyilatkozat szükséges. A választható gyógyszerek rendelésének egyes szempontjait és a kontraindikációkat a 4. pont ismerteti (további részletek az alkalmazási előiratokban!). A kezelés előtt vagy alatt hepatitis A ellen vakcináció javasolt Pegilált interferonok Első választás a pegilált interferon (ellenjavallatainak hiánya esetén). Adagja heti mcg peginterferon alfa-2a. A és pontoknál részletezett kezelés is választható, az adott pont szerinti esetekben. A kezelés időtartama 1 év. Anti-HD-IgM pozitív esetekben a kezelés időtartama másfél év. A kezelés befejezése után, és 24 héttel később HBV-DNS mennyiségi PCR, HBsAg, HBeAg/anti HBe, GPT vizsgálat javasolt. Beszűkült veseműködés esetén a peginterferon alfa-2a adagja heti 135 μg. Lásd még 4.1 pont! Standard interferonok Alternatíva, 18 év alatti életkor, alacsony fvs és/vagy thrombocyta szám, anamnézisben cytopenia esetén: hetente ME/m 2 (9-10 ME) standard interferon alfa-2a vagy alfa-2b. Egyebekben, mint pont Nukleoz(t)id Analógok A terápia célja a B vírus szaporodás gátlása, a vírus nukleinsav szint alacsonyan tartása. Választhatók az alábbi esetekben: 12 hónapos interferon kezelésre nem reagáló beteg. Interferon kezelésre reagáló, de relapsust mutató beteg HBeAg negatív, de HBV-DNS pozitív, anti-hbc-igm negatív krónikus hepatitis (pre-core mutáns). Biológiai terápia előtt és csontvelő transzplantált betegben, ha a beteg antihbc pozitív, akkor HBV DNS javasolt, és pozitív lelet esetén kezelendő. Önállóan első szerként vagy gyógyszer-rezisztencia kialakulásakor második készítményként, utóbbi esetben kombinációban is. Szervtranszplantált HBV-DNS pozitív beteg. HBV-fertőzött transplantált beteg profilaktikus kezelése Immunszuppresszív vagy kemoterápiában részesülő HBsAg pozitív beteg. HBV okozta cirrhosis bármely stádiuma. Interferon bármely okból ellenjavallt. Anti-HDV IgM negatív Lásd még 4.2 pont. Diagnosztika: A kezelés során félévenként, valamint a kezelés alatt jelentkező GPT emelkedés esetén HBV-DNS vizsgálat (real-time mennyiségi PCR) ajánlott. Viraemia újbóli megjelenése vagy a titer 1 log emelkedése és/vagy jelentős GPT emelkedés gyógyszerrezisztens mutációra utal. Mutáns megjelenésekor gyógyszerváltás indokolt Lamivudin Kezelési mód: HBe-Ag pozitív és negatív krónikus B hepatitis: napi mg Beszűkült veseműködés esetén a GFR-től függően dóziscsökkentés javasolt. Lamivudin rezisztencia kialakulásakor a mutáció alapján hatékony másik nukleoz(t)id készítményre (adefovir dipivoxil hozzáadása, vagy entecavir, tenofovir önmagában) váltás szükséges. 2
3 Kezelés tartama: HBeAg pozitív esetben az anti-hbe szerokonverzió után minimum 6 hónapig. HBe-Ag negatív esetben a HBsAg/HBV DNS eltűnése, illetve az anti-hbs megjelenése után minimum 6 hónapig,. Egyéb indikáció esetén (HBV-cirrhosis, májtranszplantáció előtt és után, immun-kompromittált beteg krónikus B-hepatitise, illetve HBV aktív replikáció) a kezelés a beteg élete végéig, vagy a kezelés indikációjaként szolgáló állapot megszűnését követően legalább 6 hónapig folytatandó. A kezelés felfüggesztése esetén életveszélyes relapsus, fulmináns májelégtelenség léphet fel! Adefovir dipivoxil Kezelési mód: 1 10 mg naponta Nukleozid naiv betegnek eü. 100% pont módosítást igényel! Beszűkült vesefunkciók esetén a dózis a gyógyszer alkalmazási előiratában megadott séma szerint csökkentendő. Egyebekben ugyanúgy, mint kezelés esetén Entecavir Kezelési mód: Nukleozid naiv betegnek 1 0,5 mg naponta. (eü. 100% pont módosítást igényel!) Lamivudin rezisztens virus: napi 1 1,0 mg Beszűkült vesefunkciók esetén dózisa a gyógyszer alkalmazási előiratában megadott séma szerint csökkentendő. Egyebekben ugyanúgy, mint kezelés esetén Tenofovir Napi adagja mg. Rezisztens vírus esetén adható A kezelés befejezése A kezelés végén vérkép, májfunkciók, HBV-DNS, HBeAg, anti-hbe vizsgálat, 6 hónappal később ezek mellett HBsAg vizsgálat szükséges. 3. KRÓNIKUS C HEPATITIS 3.1. A diagnózis és a kezelés indikációja Érzékeny módszerrel (real time RT-PCR) HCV-RNS pozitivitás és vírus genotípus meghatározás OEP által akkreditált víruslaborban, CE jelzésű teszttel. (A beteg molekuláris diagnosztikai vizsgálatai az értékelhetőség és a követés érdekében a kezelés egész időtartama alatt azonos módszerrel és azonos laboratóriumban végzendők.) Amen nyiben a beteg kezelése várhatóan szükséges és lehetséges (anti-hcv pozitivitás, emelkedett GPT érték, nincs kontraindikáció), úgy csak mennyiségi HCV-RNS vizsgálat történjen a kezelés megkezdése előtt. Men nyisé gi HCV-RNS vizsgálat a HCV 1 és 4 genotípusok esetén a kezelés megkezdése előtt mindenképpen szükséges. Hat hónapon belül 3 alkalommal emelkedett GPT (ALT) érték és/vagy szövettanilag, vagy más módon igazolt krónikus hepatitis (aktivitás és/vagy fibrosis). A májbiopsiát kiválthatja non-invaziv fibrosis score vagy fibroscan vizsgálat. HCV-RNS pozitivitás esetén konzekvensen emelkedett GPT (ALT) és/vagy HCV 2/3 genotípusok esetén mellőzhető a májbiopsia. Jelentős szövettani aktivitás és/vagy fibrosis normál GPT (ALT) esetén is indokolja a kezelést, amennyiben annak egyéb feltételei adottak. Klinikailag manifest akut C hepatitis (icterus) vagy ismert dátumú expozició esetén, a 4-6. héten HCV-RNS vizsgálat végzendő; ha pozitív: a héten a HCV-RNS vizsgálat megismétlendő; pozitivitás esetén 6 hónapos pegilált interferon monoterápia javasolt. Három éves kor felett igen indokolt esetben gyermekgyógyász és hepatológus konzílium alapján javasolható interferon (és ribavirin) kezelés. Kontraindikácó hiánya. Megjegyzés: Olyan anti-hcv pozitív betegnél, akinél antivirális kezelés biztosan nem végezhető (pl. kontraindikált, vagy a kezelést a beteg nem vállalja), HCV-RNS vizsgálat végzése indokolatlan. 3
4 3.2. Kezelési lehetőségek A választható gyógyszerek rendelésének egyes szempontjait és a kontraindikációkat a 4. pont ismerteti (további részletek az alkalmazási előiratokban!). A legjobb eredmények krónikus C hepatitis kezelésében peginterferon + ribavirin kombinációval érhetők el, de a , a , és a pontoknál részletezett esetekben az ott megjelölt kezelések is választhatók. A kezelés előtt vagy alatt hepatitis A és hepatitis B ellen vakcináció javasolt Peginterferon + ribavirin Teljes kezdő dózis: Hetente 1 1,5 mcg/ttkg peginterferon-alfa-2b vagy hetente mcg peginterferonalfa-2a + napi mg ( 13,0 mg/ttkg) ribavirin. A kezelés időtartama függ a genotípustól és a kezelésre adott választól, lásd a Kezelési algoritmus diagrammot. A ribavirinnel kombinált, alacsonyabb keződózisú pegilált interferonnal (pl. heti 1 1,0 mcg/ttkg peginterferon-alfa-2b) végzett kezelés is hatékonynak bizonyult. Ilyen csökkentett kezdődózissal, igen nagy körültekintéssel végzett kezelés lehet indokolt pl. igazoltan májcirrhosisos (csak Child A stádium!) betegeknél, kifejezett thrombopenia vagy leukopenia esetén. A kockázat/várható haszon gondos elemzése szükséges ilyen betegeknél a kezelés megkezdése előtt. A két, több szempontból különböző pegilált interferon készítmény egymással történő helyettesíthetőségével kapcsolatban nem állnak rendelkezésre adatok Standard interferon + ribavirin Kifejezett thrombopenia vagy leukopenia hajlam esetén végezhető, heti ME standard interferon + fenti dózisú ribavirin Interferon monoterápia Ribavirin ellenjavallata esetén a fenti dózisú peginterferon, vagy standard interferon monoterápia javasolható Természetes interferon A STOP szabály alkalmazása során az interferon/peginterferon kezelésből kiesett betegek kezelése végezhető liofilizált természetes human leukocyta interferonnal, az eredetileg tervezett időtartamig. Dózis: heti 3 3 ME. Ribavirin együttes adása nem lehetséges. A kezelés a biokémiai remisszió fenntartása érdekében, vagy relapsus esetén - engedélyezést követően egy éven túl is folytatható, illetve ismételhető. Extrahepatikus manifesztáció (pl. cryoglobulinaemias vasculitis) esetén, ha a GPT érték és a szövettan alapján májérintettség nem bizonyítható, egy éves természetes interferon kezelés javasolt. (Indokolt esetben további kezelés kérvényezhető.) 3.3. Kezelési algoritmus, STOP szabály (l. folyamatábra) HCV 2-es és 3-as genotípus: a kezelés tartama általában 6 hónap. Amennyiben a kezelés megkezdését megelőzően végzett vizsgálat alacsony kiinduló vírustitert igazolt (LVL: HCV-RNS IU/ml), a kezelés 4. és 16. hetét követően qualitatív HCV-RNS vizsgálat végezhető. Amennyiben HCV-RNS ezekben az időpontokban real-time PCR módszerrel sem mutatható ki, a kezelés 16 hétre lerövidíthető. HCV1-es és 4-es genotípus: a kezelés tartama reagáló beteg esetén általában egy év, az alábbi lehetősége - ket mérlegelve: Alacsony kiinduló HCV-RNS titer ( IU/ml), valamint ún. rapid virológiai válasz esetén (RVR: 4 hét után real-time PCR módszerrel a HCV-RNS nem mutatható ki, a kezelés 6 hónap után befejezendő, rekurrencia esetén ismételt kezelés mérlegelhető. Olyan HCV 1-es vagy 4-es genotípusú betegnél, akinél rövidített, 24 hetes kezelés lehetősége nem merül fel, csak a kezelés 12. hetében szükséges HCV-RNS vizsgálat: Magas kiinduló HCV-RNS titer (> IU/ml), és/vagy a 4. hét után is detektálható HCV-RNS esetén a kezelés további 8 hétig folytatandó, majd a további kezelés a 12. hetet követő mennyiségi HCV- RNS vizsgálat eredményétől függ: Ha 12 hét kezelés után a HCV-RNS titer csökkenése kisebb, mint 2 log, és a GPT sem normalizálódott, a beteg nem-reagáló (NR), a kezelés a 12. heti PCR-lelet kézhezvételekor befejezendő (STOP szabály-1). 4
5 Ha 12 hét kezelés után real-time PCR módszerrel HCV-RNS nem mutatható ki (cevr), a kezelés további 36 hétig, összesen 1 évig végzendő. Minden egyéb esetben a kezelés még 3 hónapig folytatandó, majd a további kezelés a 24. héten végzett RNS vizsgálat eredményétől függ: Ha a 24. heti PCR negatív, a kezelés további 12 hónapig (összesen másfél évig) folytatható (lassú reagáló). Ha a 24. heti PCR pozitív, a beteg nem-reagáló (NR), a kezelés befejezendő (STOP szabály-2). A STOP szabály hatálya alá eső, nem reagáló beteg számára csak a korábbinál igazoltan hatékonyabb gyógyszeres kezelés, vagy természetes interferon rendelhető. (kivéve pont lásd ott!) A tartós vírusválasz (SVR) megítélésére a kezelés alatt HCV-RNS negatívvá vált betegeknél a kezelés befejezése után 6 hónappal HCV-RNS vizsgálat szükséges. A tartós vírusválaszt mutató betegeknél a HCV-RNS későbbi követése nem szükséges, relapsus gyanúja esetén (emelkedett GPT) lehet indokolt újabb HCV-RNS vizsgálat. A kezelést befejező betegeket a hematológiai paraméterek rendeződéséig havonta javasolt kontrollálni (vérkép), majd a kezelőorvos megítélése szerinti gyakorisággal (pl. cirrhosis esetén évente hasi ultrahang és AFP vizsgálat). Sikertelen kezelés után 1-6 havonta májenzimek, vérkép vizsgálata indokolt, évente hasi ultrahang, fibroscan és/vagy aktivitási index, valamint AFP vizsgálat javasolható. Vírusszám meghatározás csak esetleges ismételt kezelés előtt közvetlenül szükséges Speciális betegcsoportok Vesebetegek A kezelési mód megválasztása a szérum kreatinin szinttől és/vagy a kreatinin clearance-től függ. PegIntron + Rebetol 200 µmol/l feletti kreatinin és/vagy 50 ml/perc alatti kreatinin clearance esetén ellenjavallt. Pegintron monoterápia végezető beszűkült vesefunkció esetén (15-50 ml/perc creatinin clearance) az alkalmazási előiratban rögzített dóziscsökkentéssel. Pegasys+Copegus kombinált kezelés dóziscsökkentéssel beszűkült vesefunkciók esetén is alkalmazható megfelelő monitorozással. Hemodialysalt betegek esetén peginterferon alfa-2a javasolt, 135 µg/hét dózisban, nagy körültekintéssel másnaponta 200 mg Copegus adása mérlegelhető. A kezelés időtartamát a nem vesebetegekre vonatkozó szabályok határozzák meg Extrahepatikus manifesztáció (pl. cryoglobulinaemias vasculitis) Amennyiben májérintettség bizonyítható, akkor a kezelés megfelel az előzőekben leírtaknak. Ha a GPT érték és a szövettan alapján májérintettség nem bizonyítható, egy éves interferon kezelés végezhető. Természetes interferon adása javasolt, indokolt esetben meghosszabbított kezelés kérvényezhető. Interferon alapú kezelésre nem reagáló, súlyos cryoglobulinaemia eseteiben (membranoproliferatív glomerulonephritis, súlyos vasculitis) vagy interferon kontraindikációja esetén, haematológiai konsilium és rituximab kezelés jön szóba Gyermekek Az interferon alfa ill. peginterferon alfa készítmények felnőttek számára kerültek törzskönyvezésre az ellenjavallatok között a 3 év alatti életkor szerepel; a 3 és 18 év közötti betegeknél végzett kezelésről korlátozottan állnak rendelkezésre adatok. Három éves kor felett indokolt esetben gyermekgyógyász és hepatológus együttes javaslata alapján egy éves kombinált interferon alfa 2b és ribavirin kezelés javasolható. A pegilált interferonnal történő kezelés az indikáción túli gyógyszerrendelés szabályai szerint lehetségessé válhat. Dozírozás az alkalmazási előirat szerint Ismételt kezelés Rekurrens C hepatitis újrakezelése Előzőleg már interferon monoterápiában, vagy standard interferon + ribavirin kezelésben részesült, reagáló, de visszaeső betegeknél a peginterferon + ribavirin kezeléstől eredmény várható, ezért amennyiben az indikáció továbbra is fennáll, és nics kontraindikáció az előzőekben ismertetettek szerinti kombinált kezelés javasolt. 5
6 Peginterferon + ribavirin kezelést követő relapsus esetén a beteg újrakezelése a kezelés hatékonyságát ismerten csökkentő tényezők (pl. obesitas, vas túlterhelés, alkoholfogyasztás, depressio, stb.) rendezése után hatékony kezelési sémával (teljes dózisú pegilált interferon, maximálisan tolerálható dózisú ribavirin) végezhető és a kezelés időtartamának 72 hétre történő meghosszabbítása mérlegelhető.. Az ismételten kezelt betegeknél a STOP szabály alkalmazandó, amennyiben a 12. heti HCV PCR nem negatív! Nem reagáló betegek újrakezelése Előzőleg már interferon monoterápiában, vagy standard interferon + ribavirin kezelésben részesült, nem reagáló betegeknél a peginterferon + ribavirin kezeléstől várható csak eredmény. Három hónapig emelt dózisú pegilált interferonnal végzett indukciós kezelés (off-label alkalmazás), és 72 hétre meghosszabbított kezelés előnyösebbnek mutatkozott az első kezeléskor javasolt kezelési módnál Az individualizált kezelés elvének megfelelően a korábbi Peginterferon + ribavirin kezelés során a STOP szabály hatálya alá eső betegek esetében, vagy ha a beteg a kezelés ellenére sem vált vírusmentessé, a kezelőorvos egyéni mérlegelés alapján a kezelés megismétlése mellett dönthet Ha az első kezelés nem a jelenleg elfogadott séma szerint történt (pl. alacsony ribavirin dózis, nem kellő ideig végzett kezelés) vagy ha az előző kezelés során a kezelés nem kellő effektusát a tervezettnél alacsonyabb bevitt gyógyszerdózis (dóziscsökkentés, gyógyszerkihagyás) magyarázta, és ez olyan ok következménye volt, melynek ismétlődésére reálisan nem kell számítani (pl. interkurrens betegség), vagy amelynek kivédésére, megelőzésére az újabb kezelés során reális lehetőség van (pl. lehetőség van az anaemia erythropoietin kezelésére); ezekben az esetekben is, a beteg újrakezelésére a kezelés hatékonyságát ismerten csökkentő tényezők (pl. obesitas, vas túlterhelés, alkohol fogyasztás, depressio, stb.) rendezése után, hatékony kezelési sémával (teljes dózisú pegilált interferon, maximálisan tolerálható dózisú ribavirin) végezhető, és javasolt a kezelés időtartamának meghosszabbítása 72 hétre, ha megfelelő adherencia várható Az ismételten kezelt betegeknél a STOP szabály alkalmazandó, amennyiben a 12. heti HCV PCR nem negatív! Akut C hepatitis Akut C hepatitis, vagy ismert dátumú expozició esetén a 3. hónapban is fennálló HCV-RNS pozitivitás esetén 6 hónapos peginterferon monoterápia végezhető, ha az indikáció egyéb feltételei is adottak HIV és HCV coinfectio Heti 1 adott teljes dózisú peginterferon és napi 800 mg ribavirin javasolt 1 évig, genotípustól függetlenül. Aktív retrovirális kezelés ill. <200/μl CD4 sejtszám esetén fokozott ellenőrzés indokolt a tejsav acidosis ill. a cytopenia lehetősége miatt. 4. A KEZELÉS SORÁN HASZNÁLHATÓ GYÓGYSZEREK RENDELÉSÉNEK SZEMPONTJAI (további részletek az alkalmazási előiratokban!) Bármely kezelés feltétele az indikáció fennállása (l. kórképek)! Kontraindikáció esetén az adott kezelés nem kezdhető el, a zajló kezelés felfüggesztendő! A kezelés megkezdése előtt a beteget tájékoztatni kell a betegség és a terápia részleteiről. A tájékoztatás tudomásulvételéről és a kezelés vállalásáról a betegtől aláírt nyilatkozat szükséges! 4.1. Interferon/Peginterferon A készítmény rendelésének feltételei: A teljes interferon/peginterferon dózissal történő kezelés megkezdésének feltétele az 1,5 G/l absolut neutrophil granulocytaszám és a 75 G/l feletti thrombocytaszám. A kezelés és a választott kezdő dózis egyéni mérlegelése szükséges 0,75-1,5 G/l absolut neutrophyl granulocytaszám és G/l thrombocytaszám között. Az interferon dózis kihagyása szükséges, ha az abszolút neutrophil granculocytaszám 0,5 G/l alatti, vagy a thrombocytaszám 25 G/l alatti. Beszűkült veseműködés esetén a kezelési mód megválasztása a plazma kreatinin szinttől és/vagy a kreatinin clearance értékétől függ. 6
7 Pegasys: A vesebetegség végső fázisában lévő betegeknek 135 mikrogramm kezdő dózist kell adni. Pegintron: Peginterferon alpha 2b + ribavirin kombinált kezelés 50 ml/perc alatti kreatinin clearance esetén nem végezhető ml/perc közötti kreatinin clearance esetén peginterferon-alfa-2b monoterápia az alkalmazási előiratban előírt dóziscsökkentéssel végezhető. Gyermekkorban, 3 év felett, egy éves standard interferon és ribavirin kezelés adható egy évig. 65 év felett egyedi elbírálás szükséges Kontraindikációk Dekompenzált májcirrhosis (Child B és C). Aktív autoimmun betegség (1:300 feletti ANA, anti-dna, SMA, AMA pozitivitás) Cytopenia: 0,5 G/l alatti absolut neutrophyl granulocytaszám, 25 G/l alatti thrombocytaszám a kezelés során. Kezeletlen hyperthyreosis. Labilis, nehezen kontrollálható diabetes mellitus. Cardiorespiratoricus elégtelenség Kezeletlen pszichiátriai betegségek: major depresszió, súlyos szorongásos zavarok, pszichotikus állapot. Az interferon kezelés megkezdése előtt a pozitív addiktológiai anamnézisű betegeknél a manifest pszichiátriai zavar (különös tekintettel a depresszióra és a szorongásos kórképekre) kizárása szükséges. Neurológiai betegségek: konvulzióhajlam, cerebrovascularis betegség (neurológiai konsilium javasolt). Addiktológiai betegség: manifest fennálló drog- vagy alkohol dependencia. Intravénás szerhasználatra vonatkozóan pozitív addiktológiai anamnézisű betegeknél az interferon kezelés 3 hónapos legalább két negatív drogteszttel igazolt absztinencia után kezdhető meg. Az addiktológus által rendelt fenntartó suboxone vagy methadon kezelés nem minősül kontraindikációnak. Az interferon kezelés megkezdését követően észlelt pozitív drogteszttel igazolt intravénás kábítószerhasználat esetén az interferon-kezelés felfüggesztendő. A kezelés az előző pontban leírt feltételek teljesülése esetén folytatható. Terhesség, lactatio. Interferon allergia. Együttműködés (compliance) hiánya. A pozitív addiktológiai anamnézisű betegeknél a kezeléshez szükséges compliance felmérésére 3 hónapos (addiktológiai vagy hepatológiai) előgondozás, illetve a compliance-t kedvezőtlenül befolyásoló súlyos személyiségzavar szűrése javasolt. Gyermekkorban 3 év felett egyedi elbírálás 65 év felett egyedi elbírálás A beteg a kezelésbe nem egyezik bele Betegkövetés Havonta vérkép, vércukor, szérum bilirubin, májenzimek, KN, kreatinin. A vérkép vizsgálata az injekció beadása után 5-7 nappal történjen. Fogamzásképes korú nőknél a kezelés előtt, és a kezelés ideje alatt, majd az azt követő hat hónapban havonta terhességi próba végzendő, illetve menstruációs zavarok esetén soron kívül. A kezelés alatt és utána fél évig mindkét nemnél adekvát fogamzásgátló rendszabályok betartása szükséges. Három havonta TSH, sz.e. pajzsmirigyhormon szint. Javasolt a kezelés megkezdése előtt, és a héten, illetve ilyen irányú panaszok megjelenése esetén a szorongásos- és a hangulatzavarok szűrése, ilyen tünetek esetén megfelelő szorongásoldó, illetve antidepreszáns kezelés beállítása, amelyhez pszichiáter segítsége vehető igénybe. Veszélyeztető állapot szintjét elérő tünetek (leggyakrabban suicid késztetés) megjelenése esetén a kezelés felfüggesztése, és sürgős pszichiátriai konzílium szükséges Hematológiai szempontok Az interferon kihagyása szükséges, ha az absolut neutrophyl granulocytaszám 0,5 G/l alatti, vagy a thrombocytaszám 25 G/l alatti A 0,75 G/l alatti neutrofil granulocytaszám és/vagy 50 G/l alatti thrombocytaszám esetén az interferon dózisa csökkentendő 7
8 Ha a kezelhetőség feltételei visszaálltak, a kezelés csökkentett dózissal folytatható. (Egyes esetekben a kiinduló dózisra történő visszatérés is lehetségessé válhat.) Súlyos cytopenia esetén a hematológiai paraméterek hetente ellenőrzendők Hematológus javaslatára a kezelés kiegészíthető erythropoetinnel vagy granulocyta colonia stimuláló faktorral 4.2. Lamivudin A készítmény rendelésének feltételei A napi 100 mg teljes dózissal történő kezelés feltétele legalább 50 ml/perc kreatinin clearance. Beszűkült vesefunkció esetén, kreatinin clearance-tól függően, heti mg az alkalmazott dózis. Haemodialysis idején heti mg adható Kontraindikációk Allergia a készítményre Lactatio Betegkövetés Kéthavonta vérkép, szérum-bilirubin, májenzimek, KN, kreatinin, húgysav. Dóziscsökkentés a vesefunkciós értékek szerint lehet szükséges A kezelés során félévenként HBV-DNS vizsgálat (mennyiségi PCR) ajánlott (2.2.3.) 4.3. Ribavirin A készítmény rendelésének feltételei Krónikus vírushepatitis kezelésére csak interferonnal együtt alkalmazható 65 év felett egyedi elbírálás Fogamzóképes nőknél a ribavirin kezelés megkezdése előtt közvetlenül, és a kezelés során havonta terhességi tesztet kell végeztetni és csak ennek negatív eredménye esetén lehet a kezelést végezni! Rebetol: Azok a betegek, akiknél a kreatinin clearance < 50 ml/perc, nem kezelhetők Rebetollal. Copegus: Nincs elegendő adat a ribavirin biztonságosságáról és hatásosságáról olyan betegeken akik szérum kreatinin szintje >2 mg/dl, vagy a kreatinin clearance-e <50 ml/min függetlenül attól, hogy dializálják-e vagy nem, ezért az ilyen betegek számára nem adható meg módosított adagolás. Ezen betegek esetében tehát a ribavirint csak nagyon indokolt esetben szabad alkalmazni. A ribavirin szint monitorozása mellett igen alacsony dózisban (pl. másnaponta 200 mg) haemodyalizált betegknél Pegasyssel kombinálva előnyös lehet Kontraindikációk A készítmény hatóanyagával vagy bármely segédanyagával szembeni túlérzékenység Anaemia, anaemiára hajlamosító betegségek (pl. thalassemia, sarlósejtes vérszegénység). Coronaria betegség, vagy cerebrovascularis betegség esetén 120 g/l Hgb érték alatt, ezek nélkül 100 g/l Hgb alatt kezelés nem kezdhető. Az interferon + ribavirin kezelés alatt kialakult 85 g/l alatti Hgb esetén a kezelés felfüggesztése szükséges Súlyos szívbetegség az előző 6 hónapban, beleértve az instabil vagy kezeletlen szívbetegséget Súlyos májbetegség Krónikus veseelégtelenség (kreatinin clearance <50 ml/perc, szérum kreatinin > 200 µmol/l) és/vagy művesekezelés esetén a Rebetol ellenjavallt. Terhesség, lactatio Betegkövetés Az interferon kezelésnél leírt havonkénti követés + szérum húgysav vizsgálat Ribavirin kezelés során, vagy azt követően fél éven belül kialakult terhesség esetén a beteget figyelmeztetni kell a ribavirin rendkívül erős teratogén hatására, terhesség megszakítást indokolt javasolni! 8
9 Hematológiai szempontok A ribavirin kihagyása szükséges 85 g/l Hgb érték alatt; coronaria-,vagy cerebrovascularis betegségben szenvedőknél 100 g/l Hgb érték alatt. Ha a kezelhetőség feltételei visszaálltak, a kezelés csökkentett dózissal újra megkísérelhető A ribavirin dózisának 200 mg-os csökkentése szükséges 100 g/l Hgb érték alatt; coronaria-, vagy cerebrovascularis betegségben szenvedőknél 120 g/l Hgb érték alatt. További Hgb csökkenés esetén újabb dóziscsökkentés, vagy kihagyás lehet szükséges Súlyos cytopenia esetén a hematológiai paraméterek hetente ellenőrzendők Hematológus javaslatára a kezelés kiegészíthető erythropoetinnel Összeállították: Dr. Gervain Judit, Dr. Horváth Gábor, Prof. Dr. Hunyady Béla, Dr. Makara Mihály, Prof. Dr. Pár Alajos, Prof. Dr. Szalay Ferenc, Prof. Dr. Tornai István, Dr. Telegdy László 9
10 KRÓNIKUS C HEPATITIS KEZELÉSI ALGORITMUSA 10
Az Egészségügyi Minisztérium szakmai protokollja A krónikus vírushepatitisek antivirális kezeléséről
 Az Egészségügyi Minisztérium szakmai protokollja A krónikus vírushepatitisek antivirális kezeléséről Készítette: a Gasztroenterológiai Szakmai Kollégium és az Infektológiai Szakmai kollégium I. Alapvető
Az Egészségügyi Minisztérium szakmai protokollja A krónikus vírushepatitisek antivirális kezeléséről Készítette: a Gasztroenterológiai Szakmai Kollégium és az Infektológiai Szakmai kollégium I. Alapvető
PROTOKOLL A KRÓNIKUS VÍRUSHEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE
 PROTOKOLL A KRÓNIKUS VÍRUSHEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE Gasztroenterológiai Szakmai Kollégium 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai és az Infektológiai Szakmai Kollégium által
PROTOKOLL A KRÓNIKUS VÍRUSHEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE Gasztroenterológiai Szakmai Kollégium 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai és az Infektológiai Szakmai Kollégium által
PROTOKOLL A KRÓNIKUS C HEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE
 1. HÁTTÉR PROTOKOLL A KRÓNIKUS C HEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE Az alábbi kezelési útmutatót a Gasztroenterológiai és Infektológiai Szakmai Kollégiumok által megbízott szakmai bizottság (aláírók) a
1. HÁTTÉR PROTOKOLL A KRÓNIKUS C HEPATITISEK ANTIVIRÁLIS KEZELÉSÉRE Az alábbi kezelési útmutatót a Gasztroenterológiai és Infektológiai Szakmai Kollégiumok által megbízott szakmai bizottság (aláírók) a
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája
 A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. július 29. Azonosítószám:
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. július 29. Azonosítószám:
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja (eljárásrend)
 A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja
 A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és
PROTOKOLL A C HEPATITIS ANTIVIRÁLIS KEZELÉSÉRE
 1. HÁTTÉR PROTOKOLL A C HEPATITIS ANTIVIRÁLIS KEZELÉSÉRE Az alábbi kezelési útmutatót a Gasztroenterológiai és Infektológiai Szakmai Kollégiumok által megbízott szakmai bizottság (aláírók) a C vírushepatitis
1. HÁTTÉR PROTOKOLL A C HEPATITIS ANTIVIRÁLIS KEZELÉSÉRE Az alábbi kezelési útmutatót a Gasztroenterológiai és Infektológiai Szakmai Kollégiumok által megbízott szakmai bizottság (aláírók) a C vírushepatitis
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája
 A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010 február 15. 1.
A hepatitis B vírus okozta krónikus májgyulladás diagnosztikája és terápiája Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest, 2010 február 15. 1.
Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja
 Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
A hepatitis C vírus okozta krónikus májgyulladás diagnosztikájának és kezelésének finanszírozási eljárásrendje
 M A G Y A R K Ö Z L Ö N Y 2013. évi 71. szám 50719 Az emberi erőforrások minisztere 32/2013. (IV. 30.) EMMI rendelete a finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet módosításáról
M A G Y A R K Ö Z L Ö N Y 2013. évi 71. szám 50719 Az emberi erőforrások minisztere 32/2013. (IV. 30.) EMMI rendelete a finanszírozási eljárásrendekről szóló 31/2010. (V. 13.) EüM rendelet módosításáról
NEFMI szakmai protokoll. a C hepatitis antivirális kezeléséről 1
 1. oldal Készítette: az Infektológiai Szakmai Kollégium NEFMI szakmai protokoll a C hepatitis antivirális kezeléséről 1 I. Alapvető megfontolások 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai
1. oldal Készítette: az Infektológiai Szakmai Kollégium NEFMI szakmai protokoll a C hepatitis antivirális kezeléséről 1 I. Alapvető megfontolások 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai
Országos Egészségbiztosítási Pénztár. A Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja
 diagnosztikája és terápiájának finanszírozási protokollja 2013.05. 01. Országos Egészségbiztosítási Pénztár Egészség, biztonság! 1. Azonosítószám: a 32/2013. (IV. 30.) EMMI rendelet 1. melléklete 2. Az
diagnosztikája és terápiájának finanszírozási protokollja 2013.05. 01. Országos Egészségbiztosítási Pénztár Egészség, biztonság! 1. Azonosítószám: a 32/2013. (IV. 30.) EMMI rendelet 1. melléklete 2. Az
Hepatitis C diagnosztikája és kezelése
 Hepatitis C diagnosztikája és kezelése Finanszírozási protokoll háttéranyaga Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. július 29. Az
Hepatitis C diagnosztikája és kezelése Finanszírozási protokoll háttéranyaga Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. július 29. Az
Ajánlás a B-, a C- és a D-vírus hepatitisek diagnosztikájára és antivirális kezelésére
 AJÁNLÁS Ajánlás a B-, a C- és a D-vírus hepatitisek diagnosztikájára és antivirális kezelésére Makara Mihály dr.* 1 Horváth Gábor dr.* 2 Gervain Judit dr. 3 Pár Alajos dr. 4 Szalay Ferenc dr. 5 Telegdy
AJÁNLÁS Ajánlás a B-, a C- és a D-vírus hepatitisek diagnosztikájára és antivirális kezelésére Makara Mihály dr.* 1 Horváth Gábor dr.* 2 Gervain Judit dr. 3 Pár Alajos dr. 4 Szalay Ferenc dr. 5 Telegdy
A hepatitis C vírus okozta krónikus májgyulladás diagnosztikájának és kezelésének finanszírozási eljárásrendje
 17. melléklet a 31/2010. (V. 13.) EüM rendelethez 1 A hepatitis C vírus okozta krónikus májgyulladás diagnosztikájának és kezelésének finanszírozási eljárásrendje 1. Az eljárásrend tárgyát képező betegség,
17. melléklet a 31/2010. (V. 13.) EüM rendelethez 1 A hepatitis C vírus okozta krónikus májgyulladás diagnosztikájának és kezelésének finanszírozási eljárásrendje 1. Az eljárásrend tárgyát képező betegség,
Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja
 Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest,
Hepatitis C vírus okozta krónikus májgyulladás diagnosztikája és terápiájának finanszírozási protokollja Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértıi és Szakmai Ellenırzési Fıosztály Budapest,
32/2013. (IV. 30.) EMMI rendelet
 32/2013. (IV. 30.) EMMI rendelet a finanszírozási eljárásrendekrıl szóló 31/2010. (V. 13.) EüM rendelet módosításáról 1 hatályos: 2013.05.01-2013.05.02 A kötelezı egészségbiztosítás ellátásairól szóló
32/2013. (IV. 30.) EMMI rendelet a finanszírozási eljárásrendekrıl szóló 31/2010. (V. 13.) EüM rendelet módosításáról 1 hatályos: 2013.05.01-2013.05.02 A kötelezı egészségbiztosítás ellátásairól szóló
Hepatitis B diagnosztikája és kezelése
 Hepatitis B diagnosztikája és kezelése Finanszírozási protokoll háttéranyaga Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. augusztus 29.
Hepatitis B diagnosztikája és kezelése Finanszírozási protokoll háttéranyaga Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2009. augusztus 29.
a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek
 38/2015. (VIII. 17.) EMMI rendelet a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás
38/2015. (VIII. 17.) EMMI rendelet a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás
diagnosztikája és kezelési lehetõségei
 Dr. Telegdy László A vírushepatitisek epidemiológiája, diagnosztikája és kezelési lehetõségei Összefoglalás A szerzõ az akut és krónikus vírusos hepatitisek epidemiológiáját, klinikai és laboratóriumi
Dr. Telegdy László A vírushepatitisek epidemiológiája, diagnosztikája és kezelési lehetõségei Összefoglalás A szerzõ az akut és krónikus vírusos hepatitisek epidemiológiáját, klinikai és laboratóriumi
NEFMI szakmai protokoll. a B és D hepatitis antivirális kezeléséről 1
 1. oldal Készítette: az Infektológiai Szakmai Kollégium NEFMI szakmai protokoll a B és D hepatitis antivirális kezeléséről 1 I. Alapvető megfontolások 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai
1. oldal Készítette: az Infektológiai Szakmai Kollégium NEFMI szakmai protokoll a B és D hepatitis antivirális kezeléséről 1 I. Alapvető megfontolások 1. Háttér Az alábbi kezelési útmutatót a Gasztroenterológiai
ÚJ LEHETŐSÉGEK A HEPATITIS C KEZELÉSÉBEN
 ÚJ LEHETŐSÉGEK A HEPATITIS C KEZELÉSÉBEN Összefoglaló a Magyar Hemofília Egyesület rendezvényéről 2015. május 20. Dr. Kalász László, az egyesület korábbi alelnökének előadása Súlyos A hemofíliások kezelésének
ÚJ LEHETŐSÉGEK A HEPATITIS C KEZELÉSÉBEN Összefoglaló a Magyar Hemofília Egyesület rendezvényéről 2015. május 20. Dr. Kalász László, az egyesület korábbi alelnökének előadása Súlyos A hemofíliások kezelésének
A krónikus vírushepatitisek klinikuma és kezelése. Dr.Werling Klára Gaszroenterológiai fakultáció
 A krónikus vírushepatitisek klinikuma és kezelése Dr.Werling Klára Gaszroenterológiai fakultáció 2017.12.04. Mikor gondolunk krónikus vírus hepatitisre? Klinikai tünetek gyakran tünetmentes gyengeség,
A krónikus vírushepatitisek klinikuma és kezelése Dr.Werling Klára Gaszroenterológiai fakultáció 2017.12.04. Mikor gondolunk krónikus vírus hepatitisre? Klinikai tünetek gyakran tünetmentes gyengeség,
AZ EGÉSZSÉGÜGYI MINISZTÉRIUM HIVATALOS LAPJA
 LVIII. ÉVFOLYAM 10. SZÁM 2881-3112. OLDAL 2008. május 28. AZ EGÉSZSÉGÜGYI MINISZTÉRIUM HIVATALOS LAPJA ÁRA: 1365 FT TARTALOM I. RÉSZ Személyi rész II. RÉSZ Törvények, országgyûlési határozatok, köztársasági
LVIII. ÉVFOLYAM 10. SZÁM 2881-3112. OLDAL 2008. május 28. AZ EGÉSZSÉGÜGYI MINISZTÉRIUM HIVATALOS LAPJA ÁRA: 1365 FT TARTALOM I. RÉSZ Személyi rész II. RÉSZ Törvények, országgyûlési határozatok, köztársasági
A krónikus B hepatitis diagnosztikája és kezelése
 A krónikus B hepatitis diagnosztikája és kezelése Horváth Gábor dr. az orvostudomány kandidátusa Budai Hepatológiai Centrum Budapest Irodalom EASL Clinical Practice Guidelines: Management of chronic hepatitis
A krónikus B hepatitis diagnosztikája és kezelése Horváth Gábor dr. az orvostudomány kandidátusa Budai Hepatológiai Centrum Budapest Irodalom EASL Clinical Practice Guidelines: Management of chronic hepatitis
Néhány mondat a m á m j á b j e b t e eg e s g é s g é e g k e k g y g ó y g ó y g s y z s er e es e s k e k z e el e é l s é é s r é ől
 Néhány mondat a májbetegségek gyógyszeres kezeléséről dr. Pár Gabriella PTE I. Belgyógyászati Klinika, Pécs A fontosabb májbetegségek Alkoholos zsirmáj - hepatitis - cirrhosis Krónikus B és C virus hepatitis
Néhány mondat a májbetegségek gyógyszeres kezeléséről dr. Pár Gabriella PTE I. Belgyógyászati Klinika, Pécs A fontosabb májbetegségek Alkoholos zsirmáj - hepatitis - cirrhosis Krónikus B és C virus hepatitis
Hepatitises betegek. Makara Mihály dr.
 Hepatitises betegek felismerése, kivizsgálása Makara Mihály dr. Hepatitisvírusok A B C D E Inkubáció 15-45 (30) 45-180 (90) 15-90 (60) 20-90 (30) 15-60 (40) Típus RNS, DNS kettős, heptovirus hepadnavirus
Hepatitises betegek felismerése, kivizsgálása Makara Mihály dr. Hepatitisvírusok A B C D E Inkubáció 15-45 (30) 45-180 (90) 15-90 (60) 20-90 (30) 15-60 (40) Típus RNS, DNS kettős, heptovirus hepadnavirus
Az egészségügyi miniszter 8013/2007. (EüK. 19.) EüM. tájékoztatója
 Az egészségügyi miniszter 8013/2007. (EüK. 19.) EüM tájékoztatója az egészségügyi szakellátás társadalombiztosítási finanszírozásának egyes kérdéseirıl szóló 9/1993. (IV. 2.) NM rendelet 2. számú mellékletében
Az egészségügyi miniszter 8013/2007. (EüK. 19.) EüM tájékoztatója az egészségügyi szakellátás társadalombiztosítási finanszírozásának egyes kérdéseirıl szóló 9/1993. (IV. 2.) NM rendelet 2. számú mellékletében
A B- és D-vírus hepatitis diagnosztikája, antivirális kezelése
 A B- és D-vírus hepatitis diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Horváth Gábor dr. 1, 2 Hunyady Béla dr. 3, 4 Gervain Judit dr. 5 Lengyel Gabriella dr. 6 Makara Mihály dr. 7 Pár
A B- és D-vírus hepatitis diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Horváth Gábor dr. 1, 2 Hunyady Béla dr. 3, 4 Gervain Judit dr. 5 Lengyel Gabriella dr. 6 Makara Mihály dr. 7 Pár
Májenzim eltérések Psoriasis - szisztémás terápiák a hepatológus szemével
 Májenzim eltérések Psoriasis - szisztémás terápiák a hepatológus szemével Dr. Tornai István DEOEC, Belgyógyászati Intézet Gasztroenterológiai tanszék Debrecen, 2012. október 11. Psoriasis és májbetegség
Májenzim eltérések Psoriasis - szisztémás terápiák a hepatológus szemével Dr. Tornai István DEOEC, Belgyógyászati Intézet Gasztroenterológiai tanszék Debrecen, 2012. október 11. Psoriasis és májbetegség
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése
 A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Horváth Gábor dr. 1, 2 Gerlei Zsuzsanna dr. 3 Gervain Judit dr. 6 Lengyel Gabriella dr. 4 Makara Mihály
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Horváth Gábor dr. 1, 2 Gerlei Zsuzsanna dr. 3 Gervain Judit dr. 6 Lengyel Gabriella dr. 4 Makara Mihály
A KRÓNIKUS B ÉS C VÍRUSHEPATITISEK ANTIVIRÁLIS TERÁPIÁJÁT BEFOLYÁSOLÓ MOLEKULÁRIS DIAGNOSZTIKA. DR. GERVAIN JUDIT PhD
 A KRÓNIKUS B ÉS C VÍRUSHEPATITISEK ANTIVIRÁLIS TERÁPIÁJÁT BEFOLYÁSOLÓ MOLEKULÁRIS DIAGNOSZTIKA DR. GERVAIN JUDIT PhD Molekuláris Diagnosztikai Laboratórium rium és s IV. Belgyógy gyászat Fejér r Megyei
A KRÓNIKUS B ÉS C VÍRUSHEPATITISEK ANTIVIRÁLIS TERÁPIÁJÁT BEFOLYÁSOLÓ MOLEKULÁRIS DIAGNOSZTIKA DR. GERVAIN JUDIT PhD Molekuláris Diagnosztikai Laboratórium rium és s IV. Belgyógy gyászat Fejér r Megyei
A krónikus vírushepatitisek klinikuma és kezelése. Dr.Werling Klára Gaszroenterológiai fakultáció 2015.11.23.
 A krónikus vírushepatitisek klinikuma és kezelése Dr.Werling Klára Gaszroenterológiai fakultáció 2015.11.23. Mikor gondolunk krónikus vírus hepatitisre? Klinikai tünetek gyakran tünetmentes gyengeség,
A krónikus vírushepatitisek klinikuma és kezelése Dr.Werling Klára Gaszroenterológiai fakultáció 2015.11.23. Mikor gondolunk krónikus vírus hepatitisre? Klinikai tünetek gyakran tünetmentes gyengeség,
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA
 III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
III. MELLÉKLET AZ ALKALMAZÁSI ELŐÍRÁS ÉS BETEGTÁJÉKOZTATÓ MÓDOSÍTÁSA Az alkalmazási előírás és a betegtájékoztató módosításai a Bizottság Határozatával egyidőben lépnek érvénybe. A Bizottsági Határozat
Tudományos információk a hepatológia tárgyköréből
 Tudományos információk a hepatológia tárgyköréből INFO XII./42. 2010. Tisztelt Kollégák! A Fresenius Kabi gyógyszergyár immár 12. éve rendszeresen megjelenő tudományos információs periodikája most először
Tudományos információk a hepatológia tárgyköréből INFO XII./42. 2010. Tisztelt Kollégák! A Fresenius Kabi gyógyszergyár immár 12. éve rendszeresen megjelenő tudományos információs periodikája most először
A vírushepatítisek (HBV, HCV) kezelésének gyakorlati vonatkozásai
 320 Gastro Update 2008 Dr. Nemesánszky Elemér Szent János Kórház, I. sz. Belgyógyászat Budapest A vírushepatítisek (HBV, HCV) kezelésének gyakorlati vonatkozásai Az elmúlt évek irodalmi adatai szerint
320 Gastro Update 2008 Dr. Nemesánszky Elemér Szent János Kórház, I. sz. Belgyógyászat Budapest A vírushepatítisek (HBV, HCV) kezelésének gyakorlati vonatkozásai Az elmúlt évek irodalmi adatai szerint
Krónikus B-vírushepatitis antivirális kezelése során szerzett tapasztalataink
 Krónikus B-vírushepatitis antivirális kezelése során szerzett tapasztalataink Pocsay Réka, Lakatos Piroska, Martyin Tibor, Bányai Tivadar Békés Megyei Képviselőtestület Pándy Kálmán Kórháza, Gyula, Infektológiai
Krónikus B-vírushepatitis antivirális kezelése során szerzett tapasztalataink Pocsay Réka, Lakatos Piroska, Martyin Tibor, Bányai Tivadar Békés Megyei Képviselőtestület Pándy Kálmán Kórháza, Gyula, Infektológiai
program 18. Májnap Aesculap Akadémia 1115 Budapest, Halmi u. 20-22. 2013. május 10. péntek
 program program 18. Májnap Aesculap Akadémia 1115 Budapest, Halmi u. 20-22. 2013. május 10. péntek Üléselnök: dr. Telegdy László Egyesített Szent István és Szent László Kórház-Rendelőintézet, Hepatológiai
program program 18. Májnap Aesculap Akadémia 1115 Budapest, Halmi u. 20-22. 2013. május 10. péntek Üléselnök: dr. Telegdy László Egyesített Szent István és Szent László Kórház-Rendelőintézet, Hepatológiai
Hepatitis Regiszter Hunyady Béla Kaposi Mór Oktató Kórház, Kaposvár PTE KK I.sz. Belgyógyászati Klinika, Pécs
 Hepatitis Regiszter Hunyady Béla Kaposi Mór Oktató Kórház, Kaposvár PTE KK I.sz. Belgyógyászati Klinika, Pécs Hepatitis Regiszter (HepReg) o A vírushepatitises betegek interferon-alapú kezelésének nyilvántartására,
Hepatitis Regiszter Hunyady Béla Kaposi Mór Oktató Kórház, Kaposvár PTE KK I.sz. Belgyógyászati Klinika, Pécs Hepatitis Regiszter (HepReg) o A vírushepatitises betegek interferon-alapú kezelésének nyilvántartására,
Chronicus hepatitisek. Dr. Nagy István SZTE I. sz. Belgyógyászati Klinika
 Chronicus hepatitisek Dr. Nagy István SZTE I. sz. Belgyógyászati Klinika 2008 Chronicus hepatitis (CH) Definitio: a máj több, mint 6 hónapig fennálló, májsejtnecrosissal és szöveti gyulladással járó necroinflammatorikus
Chronicus hepatitisek Dr. Nagy István SZTE I. sz. Belgyógyászati Klinika 2008 Chronicus hepatitis (CH) Definitio: a máj több, mint 6 hónapig fennálló, májsejtnecrosissal és szöveti gyulladással járó necroinflammatorikus
Vírus hepatitisek (akut és krónikus) V. év gasztroenterológia. Dr. Tornai István DEOEC II. Belklinika
 Vírus hepatitisek (akut és krónikus) V. év gasztroenterológia Dr. Tornai István DEOEC II. Belklinika Az akut hepatitis syndroma Hirtelen kezdet Magas májenzimek (transzaminázok, ALT, AST) Sárgaság Etiológia?
Vírus hepatitisek (akut és krónikus) V. év gasztroenterológia Dr. Tornai István DEOEC II. Belklinika Az akut hepatitis syndroma Hirtelen kezdet Magas májenzimek (transzaminázok, ALT, AST) Sárgaság Etiológia?
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése
 A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2017. szeptember 22-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 3 Lengyel
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2017. szeptember 22-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 3 Lengyel
Országos Egészségbiztosítási Pénztár tájékoztatója a tételes elszámolás alá eső hatóanyagok körének bővítéséről
 Országos Egészségbiztosítási Pénztár tájékoztatója a tételes elszámolás alá eső hatóanyagok körének bővítéséről Az egészségügyért felelős miniszter 2011. december 23-i rendeletében módosította az egészségügyi
Országos Egészségbiztosítási Pénztár tájékoztatója a tételes elszámolás alá eső hatóanyagok körének bővítéséről Az egészségügyért felelős miniszter 2011. december 23-i rendeletében módosította az egészségügyi
hatályos: 2015.08.19-2015.08.31
 38/2015. (VIII. 17.) EMMI rendelet a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás
38/2015. (VIII. 17.) EMMI rendelet a törzskönyvezett gyógyszerek és a különleges táplálkozási igényt kielégítő tápszerek társadalombiztosítási támogatásba való befogadásának szempontjairól és a befogadás
Katasztrófális antifoszfolipid szindróma
 Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Katasztrófális antifoszfolipid szindróma Gadó Klára Semmelweis Egyetem, I.sz. Belgyógyászati Klinika Antifoszfolipid szindróma Artériás és vénás thrombosis Habituális vetélés apl antitest jelenléte Mi
Nemekre szabott terápia: NOCDURNA
 Nemekre szabott terápia: NOCDURNA Dr Jaczina Csaba, Ferring Magyarország Kft. Magyar Urológus Társaság XXI. Kongresszusa, Debrecen Régi és új megfigyelések a dezmopresszin kutatása során 65 év felett megnő
Nemekre szabott terápia: NOCDURNA Dr Jaczina Csaba, Ferring Magyarország Kft. Magyar Urológus Társaság XXI. Kongresszusa, Debrecen Régi és új megfigyelések a dezmopresszin kutatása során 65 év felett megnő
MAGYOT évi Tudományos Szimpóziuma Május 5-6, Budapest
 MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
MAGYOT 2017. évi Tudományos Szimpóziuma Május 5-6, Budapest A petefészekrákok kezelésében nem régen került bevezetésre egy újabb fenntartó kezelés BRCA mutációt hordozó (szomatikus vagy germinális) magas
az engedélyezésről amiatt, hogy a bizottság nem nézte át a kérvényt és nem adta meg az általa megadható +10 pontot. Bizottsági plusz pontot csak
 Várólista Magyarországon a krónikus hepatitis B és hepatitis C kezelése rendszeresen frissülő, a hazai hepatológus kezelőorvosok által összeállított szakmai kezelési protokollok szerint történik, országosan,
Várólista Magyarországon a krónikus hepatitis B és hepatitis C kezelése rendszeresen frissülő, a hazai hepatológus kezelőorvosok által összeállított szakmai kezelési protokollok szerint történik, országosan,
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése
 A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2015. szeptember 12-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 4 Lengyel
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2015. szeptember 12-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 4 Lengyel
KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN
 KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN Dr Haris Ágnes 1, Dr Polner Kálmán 1, Dr Arányi József 1, Dr Braunitzer Henrik 1, Bakonyvári
KÉT ÉVTIZED EREDMÉNYEI ANCA- ASSZOCIÁLT VASCULITISBEN SZENVEDŐ BETEGEINK KOMPLEX IMMUNSZUPPRESSZÍV KEZELÉSE KAPCSÁN Dr Haris Ágnes 1, Dr Polner Kálmán 1, Dr Arányi József 1, Dr Braunitzer Henrik 1, Bakonyvári
A plazmaferezis szerepe immunológiai. Dr. Haris Ágnes, Dr. Polner Kálmán Szent Margit Kórház, Budapest, Nephrológia Osztály Plazmaferezis Részlege
 A plazmaferezis szerepe immunológiai etiológiájú vesebetegségekben Dr. Haris Ágnes, Dr. Polner Kálmán Szent Margit Kórház, Budapest, Nephrológia Osztály Plazmaferezis Részlege 1189 PEX kezelés indikációja
A plazmaferezis szerepe immunológiai etiológiájú vesebetegségekben Dr. Haris Ágnes, Dr. Polner Kálmán Szent Margit Kórház, Budapest, Nephrológia Osztály Plazmaferezis Részlege 1189 PEX kezelés indikációja
Rovarméreg (méh, darázs) - allergia
 Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Rovarméreg (méh, darázs) - allergia Herjavecz Irén Országos Korányi TBC és Pulmonológiai Intézet Epidemiológia I. Prevalencia: - nagy helyi reakció: felnőtt 10-15 % - szisztémás reakció: gyerek 0.4-0.8
Dr. Makara Mihály Balatonfüred, 2011.
 A hepatitis C vírusfertőzés Dr. Makara Mihály Balatonfüred, 2011. Intravénás kábítószer 1992. előtti transfusio, vér-készítmény (haemophilia) Perinatális átvitel Haemodialysis, szervtranszplantáció Tűszúrás,
A hepatitis C vírusfertőzés Dr. Makara Mihály Balatonfüred, 2011. Intravénás kábítószer 1992. előtti transfusio, vér-készítmény (haemophilia) Perinatális átvitel Haemodialysis, szervtranszplantáció Tűszúrás,
Betegtájékoztató PEGINTRON 100 MIKROGRAMM POR ÉS OLDÓSZER OLDATOS INJEKCIÓHOZ. PegIntron 100 mikrogramm por és oldószer oldatos injekcióhoz
 PEGINTRON 100 MIKROGRAMM POR ÉS OLDÓSZER OLDATOS INJEKCIÓHOZ PegIntron 100 mikrogramm por és oldószer oldatos injekcióhoz peginterferon alfa-2b (rekombináns interferon alfa-2b és monometoxi-polietilénglikol
PEGINTRON 100 MIKROGRAMM POR ÉS OLDÓSZER OLDATOS INJEKCIÓHOZ PegIntron 100 mikrogramm por és oldószer oldatos injekcióhoz peginterferon alfa-2b (rekombináns interferon alfa-2b és monometoxi-polietilénglikol
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése
 A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2016. október 15-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 4 Lengyel Gabriella
A hepatitis B- és D-vírus-fertőzés diagnosztikája, antivirális kezelése Magyar konszenzusajánlás Érvényes: 2016. október 15-től Horváth Gábor dr. 1 Gerlei Zsuzsanna dr. 2 Gervain Judit dr. 4 Lengyel Gabriella
A C-vírus hepatitis diagnosztikája, antivirális kezelése, kezelés utáni gondozása
 A C-vírus hepatitis diagnosztikája, antivirális kezelése, kezelés utáni gondozása Magyar konszenzusajánlás Hunyady Béla dr. 1, 5 Gervain Judit dr. 2 Horváth Gábor dr. 3 Makara Mihály dr. 4 Pár Alajos dr.
A C-vírus hepatitis diagnosztikája, antivirális kezelése, kezelés utáni gondozása Magyar konszenzusajánlás Hunyady Béla dr. 1, 5 Gervain Judit dr. 2 Horváth Gábor dr. 3 Makara Mihály dr. 4 Pár Alajos dr.
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
IV. melléklet Tudományos következtetések 61 Tudományos következtetések Háttér-információ A ponatinib egy tirozin-kináz inhibitor (TKI), amelyet a natív BCR-ABL, valamint minden mutáns variáns kináz beleértve
A Kockázatkezelési Terv Összefoglalója
 1 A Kockázatkezelési Terv Összefoglalója Hatóanyag/hatóanyagcsoport paracetamol ATC N02BE01 Érintett készítmény(ek) Magyarországon Paracetamol Teva 10 mg/ml oldatos infúzió (MAH: Teva Gyógyszergyár Zrt.,
1 A Kockázatkezelési Terv Összefoglalója Hatóanyag/hatóanyagcsoport paracetamol ATC N02BE01 Érintett készítmény(ek) Magyarországon Paracetamol Teva 10 mg/ml oldatos infúzió (MAH: Teva Gyógyszergyár Zrt.,
Terápiás protokoll - Metotrexát
 Terápiás protokoll - Metotreát SZTE Bőrgyógyászati és Allergológiai Klinika Érvényesség kezdete: 2013. július Készítette: Dr. Kui Róbert, Prof. Kemény Lajos Bevezetés/általános információ A metotreátot
Terápiás protokoll - Metotreát SZTE Bőrgyógyászati és Allergológiai Klinika Érvényesség kezdete: 2013. július Készítette: Dr. Kui Róbert, Prof. Kemény Lajos Bevezetés/általános információ A metotreátot
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL
 MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
MELLÉKLET FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS ÉS HATÁSOS HASZNÁLATÁRA, MELYEKET A TAGÁLLAMOKNAK TELJESÍTENIÜK KELL FELTÉTELEK VAGY KORLÁTOZÁSOK, TEKINTETTEL A GYÓGYSZER BIZTONSÁGOS
Krónikus vírushepatitiszes betegek kezelésének várható lehetőségei Magyarországon 2015-ben
 Krónikus vírushepatitiszes betegek kezelésének várható lehetőségei Magyarországon 2015-ben Hunyady Béla Somogy Megyei Kaposi Mór Oktató Kórház, Kaposvár Pécsi Tudományegyetem, Pécs Budapest, 2012. október
Krónikus vírushepatitiszes betegek kezelésének várható lehetőségei Magyarországon 2015-ben Hunyady Béla Somogy Megyei Kaposi Mór Oktató Kórház, Kaposvár Pécsi Tudományegyetem, Pécs Budapest, 2012. október
A hepatitis C vírus okozta krónikus májgyulladás diagnosztikájának és kezelésének finanszírozási eljárásrendje
 M A G Y A R K Ö Z L Ö N Y 2017. évi 78. szám 7997 3. Az R2. 15. melléklet 7. pont 7.3. alpontjában foglalt táblázat a következő 15. sorral egészül ki: (1 ATC ATC megnevezése) 15 M05BX04 Denoszumab 7. melléklet
M A G Y A R K Ö Z L Ö N Y 2017. évi 78. szám 7997 3. Az R2. 15. melléklet 7. pont 7.3. alpontjában foglalt táblázat a következő 15. sorral egészül ki: (1 ATC ATC megnevezése) 15 M05BX04 Denoszumab 7. melléklet
Kryoglobulinaemia kezelése. Domján Gyula. Semmelweis Egyetem I. Belklinika. III. Terápiás Aferezis Konferencia, 2014. Debrecen
 Kryoglobulinaemia kezelése Domján Gyula Semmelweis Egyetem I. Belklinika Mi a kryoglobulin? Hidegben kicsapódó immunglobulin Melegben visszaoldódik (37 C-on) Klasszifikáció 3 csoport az Ig komponens
Kryoglobulinaemia kezelése Domján Gyula Semmelweis Egyetem I. Belklinika Mi a kryoglobulin? Hidegben kicsapódó immunglobulin Melegben visszaoldódik (37 C-on) Klasszifikáció 3 csoport az Ig komponens
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Baraclude 0,5 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg entekavir (monohidrát formájában) tablettánként. Ismert hatású segédanyagok:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Baraclude 0,5 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg entekavir (monohidrát formájában) tablettánként. Ismert hatású segédanyagok:
A hepatitis B- és D-vírus hepatitis diagnosztikája, antivirális kezelése. Magyar konszenzusajánlás.
 A hepatitis B- és D-vírus hepatitis diagnosztikája, antivirális kezelése. Magyar konszenzusajánlás. Horváth Gábor, Gerlei Zsuzsanna, Gervain Judit, Lengyel Gabriella, Makara Mihály, Pár Alajos, Rókusz
A hepatitis B- és D-vírus hepatitis diagnosztikája, antivirális kezelése. Magyar konszenzusajánlás. Horváth Gábor, Gerlei Zsuzsanna, Gervain Judit, Lengyel Gabriella, Makara Mihály, Pár Alajos, Rókusz
Dr Varga Márta Békéscsaba Réthy Pál Kórház,Gasztroenterológia. 2010.12.03. Tata
 Dr Varga Márta Békéscsaba Réthy Pál Kórház,Gasztroenterológia ANAMNESIS Emelkedett májenzimértékek esetén -beteg anamnézisében szerepel-e akut hepatitis, -sárgaság, -transzfúzió, -műtét, -alkoholfogyasztás
Dr Varga Márta Békéscsaba Réthy Pál Kórház,Gasztroenterológia ANAMNESIS Emelkedett májenzimértékek esetén -beteg anamnézisében szerepel-e akut hepatitis, -sárgaság, -transzfúzió, -műtét, -alkoholfogyasztás
II. melléklet. Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása
 II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 7 Tudományos következtetések A Cymevene i.v. és kapcsolódó nevek (lásd I. melléklet)
II. melléklet Tudományos következtetések és a forgalomba hozatali engedély feltételeit érintő változtatások indoklása 7 Tudományos következtetések A Cymevene i.v. és kapcsolódó nevek (lásd I. melléklet)
Visegrád, március
 Visegrád, 2017. március 23-25. A Magyar Gasztroenterológiai Társaság Hepatológiai Szekciója, a Májbetegekért Alapítvány és a Magyar Májkutatási Társaság közös rendezvénye 2017.03.23. Csütörtök 14.00 14.10
Visegrád, 2017. március 23-25. A Magyar Gasztroenterológiai Társaság Hepatológiai Szekciója, a Májbetegekért Alapítvány és a Magyar Májkutatási Társaság közös rendezvénye 2017.03.23. Csütörtök 14.00 14.10
Moderiba 200 mg filmtabletta 200 mg ribavirint tartalmaz filmtablettánként. Ismert hatású segédanyagok: 15 mg laktóz-monohidrát filmtablettánként.
 1. A GYÓGYSZER NEVE Moderiba 200 mg filmtabletta Moderiba 400 mg filmtabletta Moderiba 600 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Moderiba 200 mg filmtabletta 200 mg t tartalmaz filmtablettánként.
1. A GYÓGYSZER NEVE Moderiba 200 mg filmtabletta Moderiba 400 mg filmtabletta Moderiba 600 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Moderiba 200 mg filmtabletta 200 mg t tartalmaz filmtablettánként.
Visegrád, március
 Visegrád, 2018. március 22-24. Májbetegekért Alapítvány, Magyar Májkutatási Társaság, Magyar Gasztroenterológiai Társaság Hepatológiai Szekció szervezésében 2018.03.22. CSÜTÖRTÖK 14.00 14.10 MEGNYITÓ Makara
Visegrád, 2018. március 22-24. Májbetegekért Alapítvány, Magyar Májkutatási Társaság, Magyar Gasztroenterológiai Társaság Hepatológiai Szekció szervezésében 2018.03.22. CSÜTÖRTÖK 14.00 14.10 MEGNYITÓ Makara
40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban).
 1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
1. A GYÓGYSZER NEVE Zovirax 40 mg/ml belsőleges szuszpenzió 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 40,0 mg aciklovir 1 ml szuszpenzióban (200,0 mg aciklovir 5 ml 1 adag szuszpenzióban). Ismert hatású segédanyagok:
Adalimumab. Finanszírozott indikációk:
 Adalimumab Finanszírozott indikációk: 1. Felnőttkori súlyos luminaris Crohn-betegség (18 éves kor felett és CDAI > 300) kezelésére - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott
Adalimumab Finanszírozott indikációk: 1. Felnőttkori súlyos luminaris Crohn-betegség (18 éves kor felett és CDAI > 300) kezelésére - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott
Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek
 Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek Nagy V. Endre Endokrinológia Tanszék Debreceni Egyetem Orvos- és Egészségtudományi Centrum Belgyógyászati Intézet, I. Belklinika A pajzsmirigybetegségek
Mindennapi pajzsmirigy diagnosztika: antitestek, hormonszintek Nagy V. Endre Endokrinológia Tanszék Debreceni Egyetem Orvos- és Egészségtudományi Centrum Belgyógyászati Intézet, I. Belklinika A pajzsmirigybetegségek
Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye alapján jött létre.
 II. melléklet Az alkalmazási előírás és a betegtájékoztató módosítása az Európai Gyógyszerügynökség előterjesztésére Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye
II. melléklet Az alkalmazási előírás és a betegtájékoztató módosítása az Európai Gyógyszerügynökség előterjesztésére Ez az alkalmazási előírás és a betegtájékoztató az előterjesztési eljárás eredménye
MAGYAR KÖZLÖNY 117. szám
 MAGYAR KÖZLÖNY 117. szám MAGYARORSZÁG HIVATALOS LAPJA 2015. augusztus 17., hétfő Tartalomjegyzék 29/2015. (VIII. 17.) MNB rendelet A Mohácsi Nemzeti Emlékhely rézötvözetű emlékérme kibocsátásáról 18852
MAGYAR KÖZLÖNY 117. szám MAGYARORSZÁG HIVATALOS LAPJA 2015. augusztus 17., hétfő Tartalomjegyzék 29/2015. (VIII. 17.) MNB rendelet A Mohácsi Nemzeti Emlékhely rézötvözetű emlékérme kibocsátásáról 18852
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Pegasys 180 mikrogramm oldatos injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Pegasys 180 mikrogramm oldatos injekció Egy injekciós üveg 180 mikrogramm
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE Pegasys 180 mikrogramm oldatos injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Pegasys 180 mikrogramm oldatos injekció Egy injekciós üveg 180 mikrogramm
Tejkaramella színű, filmbevonatú, hosszúkás alakú, mindkét oldalán domború, megközelítőleg 11 mm x 5 mm-es, az egyik oldalán GX CG5 bevésettel.
 1. A GYÓGYSZER NEVE Zeffix 100 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg lamivudin filmtablettánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Filmtabletta
1. A GYÓGYSZER NEVE Zeffix 100 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 100 mg lamivudin filmtablettánként. A segédanyagok teljes listáját lásd a 6.1 pontban. 3. GYÓGYSZERFORMA Filmtabletta
III. melléklet. Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral eljárás eredményeként jöttek létre.
 III. melléklet Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak módosításai Megjegyzés: Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral
III. melléklet Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak módosításai Megjegyzés: Az alkalmazási előírás és a betegtájékoztató érintett szakaszainak ezen módosításai a referral
Infliximab. Finanszírozott indikációk:
 Infliximab Finanszírozott indikációk: 1. Felnőttkori súlyos luminaris Crohn-betegség (18 éves kor felett és CDAI > 300) kezelésére - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott
Infliximab Finanszírozott indikációk: 1. Felnőttkori súlyos luminaris Crohn-betegség (18 éves kor felett és CDAI > 300) kezelésére - a finanszírozási eljárásrendekről szóló miniszteri rendeletben meghatározott
CSALÁDTERVEZ TEKINTETTEL A PSZICHIÁTRIAI BETEGSÉGEKRE GEKRE. Dr. Erős s Erika
 CSALÁDTERVEZ DTERVEZÉS KÜLÖNÖS TEKINTETTEL A PSZICHIÁTRIAI BETEGSÉGEKRE GEKRE Dr. Erős s Erika A családtervez dtervezés s törtt rténete Magyarországon gon Veleszületett letett rendellenességek (CA) Jelenleg
CSALÁDTERVEZ DTERVEZÉS KÜLÖNÖS TEKINTETTEL A PSZICHIÁTRIAI BETEGSÉGEKRE GEKRE Dr. Erős s Erika A családtervez dtervezés s törtt rténete Magyarországon gon Veleszületett letett rendellenességek (CA) Jelenleg
III. melléklet. Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai. Megjegyzés:
 III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai Megjegyzés: Az alkalmazási előírás, a címke és a betegtájékoztató a referál eljárás eredménye. Lehetséges,
III. melléklet Az alkalmazási előírás és a betegtájékoztató vonatkozó fejezeteinek módosításai Megjegyzés: Az alkalmazási előírás, a címke és a betegtájékoztató a referál eljárás eredménye. Lehetséges,
Az új mérőeszközök felhasználási lehetőségei a gyakorlatban
 Az új mérőeszközök felhasználási lehetőségei a gyakorlatban Előadó: Dr. Hudák Aranka vezető főorvos Nemzeti Munkaügyi Hivatal Munkahigiénés és Foglalkozás-egészségügyi Főosztály Klinikai Laboratóriuma
Az új mérőeszközök felhasználási lehetőségei a gyakorlatban Előadó: Dr. Hudák Aranka vezető főorvos Nemzeti Munkaügyi Hivatal Munkahigiénés és Foglalkozás-egészségügyi Főosztály Klinikai Laboratóriuma
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil.
 1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
1998- ban először az Egyesült Államokban került bevezetésre az első nem amphetamin típusú ébrenlétet javító szer, a modafinil. Magyarországon egyedi gyógyszerrendelés alapján két éve adható (MODASOMIL,
IV. melléklet. Tudományos következtetések
 IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
IV. melléklet Tudományos következtetések 1 Tudományos következtetések 2017. június 7-én az Európai Bizottság (EB) halálos kimenetelű fulmináns májelégtelenségről értesült egy folyamatban lévő megfigyeléses
Visegrád, március
 Visegrád, 2018. március 22-24. Májbetegekért Alapítvány, Magyar Májkutatási Társaság, Magyar Gasztroenterológiai Társaság Hepatológiai Szekció szervezésében 2018.03.22. CSÜTÖRTÖK 14.00 14.10 MEGNYITÓ Makara
Visegrád, 2018. március 22-24. Májbetegekért Alapítvány, Magyar Májkutatási Társaság, Magyar Gasztroenterológiai Társaság Hepatológiai Szekció szervezésében 2018.03.22. CSÜTÖRTÖK 14.00 14.10 MEGNYITÓ Makara
Egynapos akkreditált továbbképző konferencia háziorvosok, gasztroenterológusok és minden érdeklődő számára
 MÁJBETEGEKÉRT ALAPÍTVÁNY PROGRAM 20. Májnap Dr. Telegdy László emlékére Egynapos akkreditált továbbképző konferencia háziorvosok, gasztroenterológusok és minden érdeklődő számára Időpont: 2015. május 08.
MÁJBETEGEKÉRT ALAPÍTVÁNY PROGRAM 20. Májnap Dr. Telegdy László emlékére Egynapos akkreditált továbbképző konferencia háziorvosok, gasztroenterológusok és minden érdeklődő számára Időpont: 2015. május 08.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend)
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest, 2013. június 26.
Kábítószer-fogyasztással összefüggő hepatitis C fertőzések antivirális kezelésének költségei
 Kábítószer-fogyasztással összefüggő hepatitis C fertőzések antivirális kezelésének költségei Horváth Gergely Csaba Tűcsere Szakmai találkozó NFP OEK 2009. NOVEMBER 25. Társadalmi célok Nemzeti Stratégia
Kábítószer-fogyasztással összefüggő hepatitis C fertőzések antivirális kezelésének költségei Horváth Gergely Csaba Tűcsere Szakmai találkozó NFP OEK 2009. NOVEMBER 25. Társadalmi célok Nemzeti Stratégia
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Sebivo 600 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 600 mg telbivudin filmtablettánként. A segédanyagok teljes listáját lásd a
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER MEGNEVEZÉSE Sebivo 600 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 600 mg telbivudin filmtablettánként. A segédanyagok teljes listáját lásd a
Férfiakban: RBC: < 4,4 T/l HGB: < 135 g/l PCV: < 0,40 l/l. Nőkben: RBC: < 3,8 T/l HGB: < 120 g/l PCV: < 0,37 l/l
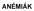 ANÉMIÁK Az anémia ritkán önálló megbetegedés, leggyakrabban valamilyen más egyéb betegség - pl: krónikus gyulladás, malignus megbetegedés kísérőjelensége, könnyen felismerhető tünete. Definíció: A keringő
ANÉMIÁK Az anémia ritkán önálló megbetegedés, leggyakrabban valamilyen más egyéb betegség - pl: krónikus gyulladás, malignus megbetegedés kísérőjelensége, könnyen felismerhető tünete. Definíció: A keringő
Molekuláris biológiai diagnosztika alkalmazása
 Molekuláris biológiai diagnosztika alkalmazása (HIV, HCV, HBV szabad vírus mennyiség meghatározás) a napi rutin diagnosztikában Reichenberger Anna Mária, Dr. Sárvári Csilla Dr. Ujhelyi Eszter Fıvárosi
Molekuláris biológiai diagnosztika alkalmazása (HIV, HCV, HBV szabad vírus mennyiség meghatározás) a napi rutin diagnosztikában Reichenberger Anna Mária, Dr. Sárvári Csilla Dr. Ujhelyi Eszter Fıvárosi
Hepatitis C-vírus-fertőzés: diagnosztika, antivirális terápia, kezelés utáni gondozás
 Hepatitis C-vírus-fertőzés: diagnosztika, antivirális terápia, kezelés utáni gondozás Magyar konszenzusajánlás Hunyady Béla dr. 1, 2 Gerlei Zsuzsanna dr. 3 Gervain Judit dr. 6 Horváth Gábor dr. 7 Lengyel
Hepatitis C-vírus-fertőzés: diagnosztika, antivirális terápia, kezelés utáni gondozás Magyar konszenzusajánlás Hunyady Béla dr. 1, 2 Gerlei Zsuzsanna dr. 3 Gervain Judit dr. 6 Horváth Gábor dr. 7 Lengyel
GNTP. Személyre Szabott Orvoslás (SZO) Munkacsoport. Kérdőív Értékelő Összefoglalás
 GNTP Személyre Szabott Orvoslás (SZO) Munkacsoport Kérdőív Értékelő Összefoglalás Választ adott: 44 fő A válaszok megoszlása a válaszolók munkahelye szerint Személyre szabott orvoslás fogalma Kérdőív meghatározása:
GNTP Személyre Szabott Orvoslás (SZO) Munkacsoport Kérdőív Értékelő Összefoglalás Választ adott: 44 fő A válaszok megoszlása a válaszolók munkahelye szerint Személyre szabott orvoslás fogalma Kérdőív meghatározása:
Olvassa el figyelmesen az alábbi betegtájékoztatót, mely az Ön számára fontos információkat tartalmaz.
 FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Plavix 75 mg filmtabletta BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
FIGYELEM!!! Az alábbi dokumentum csak tájékoztató jellegű, minden esetben olvassa el a termék dobozában található tájékoztatót! Plavix 75 mg filmtabletta BETEGTÁJÉKOZTATÓ: INFORMÁCIÓK A FELHASZNÁLÓ SZÁMÁRA
Oszteoporózis diagnózis és terápia Mikor, kinek, mit? Dr. Kudlák Katalin Somogy Megyei Kaposi Mór Oktató Kórház 2015.01.21.
 Oszteoporózis diagnózis és terápia Mikor, kinek, mit? Dr. Kudlák Katalin Somogy Megyei Kaposi Mór Oktató Kórház 2015.01.21. Diagnózis Osteodensitometria ( T- score:
Oszteoporózis diagnózis és terápia Mikor, kinek, mit? Dr. Kudlák Katalin Somogy Megyei Kaposi Mór Oktató Kórház 2015.01.21. Diagnózis Osteodensitometria ( T- score:
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE 135 mikrogramm oldatos injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 135 mikrogramm peginterferon alfa-2a* hatóanyagot tartalmaz
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1 1. A GYÓGYSZER NEVE 135 mikrogramm oldatos injekció 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL Egy injekciós üveg 135 mikrogramm peginterferon alfa-2a* hatóanyagot tartalmaz
Melléklet a./2008. (EüK..) EüM tájékoztatóhoz
 Melléklet a./2008. (EüK..) EüM tájékoztatóhoz A Szabálykönyv I. fejezetében: (A24) Amennyiben a járóbeteg-szakellátás szakorvosa a páciens számára további, más szolgáltató, szakrendelés által elvégezhetı
Melléklet a./2008. (EüK..) EüM tájékoztatóhoz A Szabálykönyv I. fejezetében: (A24) Amennyiben a járóbeteg-szakellátás szakorvosa a páciens számára további, más szolgáltató, szakrendelés által elvégezhetı
A krónikus myeloid leukémia kezelésének finanszírozási protokollja
 A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
A krónikus myeloid leukémia kezelésének finanszírozási protokollja (finanszírozási eljárásrend) Országos Egészségbiztosítási Pénztár Elemzési, Orvosszakértői és Szakmai Ellenőrzési Főosztály Budapest,
BÉCS-BUDAPEST TÜDŐ TRANSZPLANTÁCIÓS PROGRAM
 BÉCS-BUDAPEST TÜDŐ TRANSZPLANTÁCIÓS PROGRAM Verzió 1.0 2016. május Tisztelt Kolléga! Amennyiben Ön gondoz olyan tüdőbetegségben szenvedő beteget, akiről úgy gondolja, hogy tüdőátültetésre szorul, úgy olvassa
BÉCS-BUDAPEST TÜDŐ TRANSZPLANTÁCIÓS PROGRAM Verzió 1.0 2016. május Tisztelt Kolléga! Amennyiben Ön gondoz olyan tüdőbetegségben szenvedő beteget, akiről úgy gondolja, hogy tüdőátültetésre szorul, úgy olvassa
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS
 I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/51 1. A GYÓGYSZER NEVE Entecavir Mylan 0,5 mg filmtabletta Entecavir Mylan 1 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg entekavirral egyenértékű entekavir-monohidrát
I. MELLÉKLET ALKALMAZÁSI ELŐÍRÁS 1/51 1. A GYÓGYSZER NEVE Entecavir Mylan 0,5 mg filmtabletta Entecavir Mylan 1 mg filmtabletta 2. MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL 0,5 mg entekavirral egyenértékű entekavir-monohidrát
