Mágneses magrezonancia (NMR) spektroszkópiák
|
|
|
- Vilmos Fodor
- 8 évvel ezelőtt
- Látták:
Átírás
1 1 A szerves vegyületek szerkezetének meghatározására kezdetben az elemi analízist és az analógiákon alapuló szerkezetbizonyító szintézist illetve lebontást alkalmazták. Bonyolultabb vegyületek szerkezetének megállapítása ezen módszerek kombinálását igényelte: idő- és anyagigényes eljárás volt. Ugrásszerű fejlődést okozott a szerkezetmeghatározásban a különböző fizikai szerkezet- és tisztaságvizsgáló módszerek megjelenése és ezek megfelelő érzékenységűvé történt fejlesztése. A fejlesztések eredményeképpen a szerkezetvizsgálathoz szükséges idő- és anyagigény nagyságrendekkel csökkent, sőt a vizsgálatok végeztével bizonyos esetekben a minta változatlan állapotban visszanyerhető volt. A jelenlegi szerves kémiai gyakorlatban legelterjedtebben a mágneses magrezonancia jelenségén alapuló 1 H NMR- és 13 C NMR-spektroszkópiát, az infravörös sugárzás és az anyag kölcsönhatását kihasználó IR-spektroszkópiát, a röntgensugárzás kristályokon való szóródásán alapuló röntgendiffrakciós módszert, valamint a nagy energiájú elektronok szerves molekulákkal történő kölcsönhatását felhasználó tömegspektrometriát alkalmazzák. A gyakorló szerves kémikus önállóan leginkább az első három spektroszkópiás módszert használja, míg a tömegspektrometriai adatok kiértékelésekor a szakterület specialistáit hívja segítségül, a röntgendiffrakciós vizsgálatoknak pedig csak a végeredményéről kap tájékoztatást. Mágneses magrezonancia (NMR) spektroszkópiák A szerves kémikus számára az esetek többségében elegendő az atomokat kétféle elemi részecskéből álló képződményeknek tekinteni: ezek közül az egyik az elektron, ami valódi elemi részecske, a másik az atommag, ami izotóponként ismert szerkezetű összetett rendszer, de a szerves kémikus számára általában egységes egészként jelenik meg. A kvantummechanika szerint mind az elektronhoz, mind a különböző atommagokhoz tartozik saját impulzusmomentum, vagy más néven spinmomentum, amit röviden spinnek nevezünk. A spin kvantált vektormennyiség, azaz nem vehet fel tetszőleges értékeket. Lehetséges értékeit a spinkvantumszámok befolyásolják: ezek skaláris mennyiségek. A spinkvantumszámok egy-egy atommagra (izotópra) adott értékek és röviden magspinnek is nevezik őket: lehetséges értékük I = 0, ½, 1, 3/2, 2, 6. Mint ismeretes, mozgó elektromos töltések mágneses teret indukálnak, így az említett részecskék spinjéhez meghatározott összefüggés szerint az I = 0 eset kivételével nullától különböző mágneses momentum is rendelhető (az atommag mágneses térrel való kölcsönhatása során a mágneses momentum is szerepel a kölcsönhatást leíró egyenletekben, de mivel atomi állandókat tartalmazó egyenleteken keresztül egyértelmű összefüggésben van a spinkvantumszámokkal, a probléma mélyebb szintű tárgyalásától és a konkrét reakcióegyenletek felírásától eltekintünk, lévén ezek szükségtelenek az alapszintű alkalmazott NMR spektroszkópiához). Ennek megfelelően a nullától különböző spinkvantumszámmal rendelkező atommagok esetében van esély arra, hogy a mágneses magrezonancia spektroszkópiát szerkezetvizsgálat céljára felhasználhassuk. Legegyszerűbben tárgyalható az I = ½ spinkvantumszámmal rendelkező atommagok esete: szerencsére mind a protonnak ( 1 H), mind a szén egyik természetes izotópjának, a 13 C izotópnak spinkvantumszáma ½, így a szerves molekulák leggyakoribb összetevői NMR spektroszkópiával tanulmányozhatók. Erős homogén mágneses térben az I = ½ spinkvantumszámú magok, így a protonok és a 13 C atommagok két, egymástól kismértékben különböző energiájú állapotban létezhetnek: a kisebb energiájút alapállapotnak, a nagyobb energiájút gerjesztett állapotnak nevezzük (az alap- és a gerjesztett állapot közti energiakülönbség a mágneses tér erősségétől függ: erősebb mágneses térhez nagyobb
2 2 energiakülönbség tartozik). Amennyiben a rendszernek például elektromágneses sugárzás útján energiát adunk át, akkor az alap- és a gerjesztett állapot közötti energiakülönbségnek megfelelő frekvenciánál abszorpciót észlelünk: az alapállapotú magok meghatározott energia felvételével gerjesztett állapotba kerülnek (a környezettel való kölcsönhatás következtében bekövetkező energiavesztés miatt a gerjesztett magok előbb-utóbb alapállapotba jutnak vissza és a folyamat kezdődhet elölről). Mivel az elektromágneses sugárzás energiája egyértelmű összefüggésben van a frekvenciával, az abszorpció meghatározott frekvenciánál következik be: a frekvencia (adott mágneses tér esetén) jellemző az atommagra. Kiszámítható, hogy a protonok pl. 4,7 Tesla erősségű mágneses tér esetén 202,07006 MHz frekvenciájú sugárzással gerjeszthetők: eközben 1,9 x 10-5 kcal / mól energiát vesznek fel. A gerjesztési frekvenciák tehát atommag-fajtánként eltérőek: adott erősségű mágneses tér esetén a proton és a 13 C atommag, valamint a többi mágnesesen aktív mag teljesen más frekvenciájú elektromágneses sugárzást abszorbeál: az abszorpciók a jelenleg szokásos mágneses térerősségek esetén a MHz tartományba esnek. A szerves molekulákban az atommagok a molekula elektronrendszerén belül helyezkednek el és ezen keresztül kapcsolódnak egymáshoz. Az elektronrendszer szintén kölcsönhatásba lép a mágneses térrel, így a mágneses tér az elektronok közvetítésével fejti ki hatását az egyes atommagokra. Ez a hatás abban nyilvánul meg, hogy az elektronrendszer a kölcsönhatás eredményeképpen kismértékben gyengíti vagy erősíti a külső mágneses tér hatását, ennek következtében még az egy molekulán belüli azonos atommagok sem pontosan az adott magra számított frekvenciájú sugárzással gerjeszthetők: a frekvenciák a számítottól pozitív és negatív irányban egyaránt eltérhetnek. Egy adott atommag gerjesztési frekvenciája tehát attól függ, hogy pontosan milyen az elektronrendszer a környezetében, ez utóbbi pedig a kémiai szerkezet (kötéstípus, kötéspolaritás) függvénye: eltérő kémiai környezetű atommagok gerjesztési vagy más néven rezonanciafrekvenciája eltérő. A rutin NMR méréseket úgy végzik, hogy a vizsgálandó mintát feloldják olyan oldószerben, amelyik nem tartalmaz a minta méréstartományában abszorbeáló atommagokat: ez általában deuterált szerves oldószerek felhasználását jelenti. A szerves oldószer minden protonját deutériumra cserélik, mert a deutérium rezonanciafrekvenciája jelentősen eltér a protonétól, így a protonok mérését nem zavarja. A leggyakrabban használt deuterált oldószerek: deuterokloroform, CDCl 3, hexadeutero-dimetil-szulfoxid vagy DMSO-d 6, CD 3 -S(O)-CD 3. Az oldat a vizsgálandó mintán kívül kevés tetrametilszilánt -, Si(CH 3 ) 4 is tartalmaz. Az oldatot egy megfelelő üvegcsőbe töltik és behelyezik a készülékbe, ahol az erős homogén mágneses térben elvégzik a besugárzást és a különböző frekvenciákon bekövetkező abszorpciókat egy írószerkezet segítségével grafikusan megjelenítik. Az ábra vízszintes tengelyén nem abszolút frekvenciákat tüntetnek fel, hiszen ezek az alkalmazott mágneses tér erősségétől függenek, tehát készülékfüggők. A készüléktől való függetlenítést az alábbiak szerint érték el: - a mintával együtt feloldott tetrametilszilán protonjainak rezonanciafrekvenciáját választották a skála kezdőpontjának az 1 H NMR spektroszkópiában: a 12 azonos kémiai környezetű hidrogént tartalmaz, amelyek 1 rezonanciajelet adnak; a 13 C NMR spektroszkópiában a ( 13 C) szénjelét választották a skála kezdőpontjának: a 4 azonos kémiai környezetű szénatomot tartalmaz, amelyek 1 rezonanciajelet adnak. - a -től, mint 0-ponttól egy adott rezonanciajelnek hertzben mért távolságát elosztották a adott készüléken megahertzben mért rezonanciafrekvenciájával: adott jel távolsága a protonjelétől (Hz) δ= a adott készülékre jellemző frekvenciája (MHz)
3 3 Az így kapott δ érték az úgynevezett kémiai eltolódás, ppm egységekben kifejezve (ppm: part per million = milliomodrész; az, hogy a nevezőben a frekvenciáját MHz-ben és nem Hz-ben fejeztük ki, egymillióval való szorzásnak felel meg, a kémiai eltolódás tehát azt jelenti, hogy a kémiai környezet hány milliomodrészben változtatja meg az adott proton rezonanciafrekvenciáját a protonjainak rezonanciafrekvenciájához képest). Az NMR készüléket általában nem az általa generált mágneses tér erősségével jellemzik, hanem azzal, hogy a protonjai a készülék mágneses terében milyen frekvencián adnak rezonanciajelet: egy 90 MHz-es készülék esetében a protonjai 90 MHz-nél, míg egy 250 MHz-es készülék esetében a protonjai 250 MHz-nél adnak jelet. ν (Hz) CH 2 Br 2 CH 3 Br CHBr δ (ppm) A fenti ábrán a CH 3 Br, a CH 2 Br 2 és a CHBr 3 ekvimoláris elegyének 90 MHz-es készüléken felvett NMR spektruma látható (az NMR jeleknek vonalakat feleltettünk meg). A készüléken a protonjai Hz-nél, azaz 90 MHz-nél adnak jelet (ez a ppm-skála 0-pontja), a CH 3 Br protonjainak rezgési frekvenciája Hz, a CH 2 Br 2 protonjainak rezgési frekvenciája Hz, míg a CHBr 3 protonjának rezgési frekvenciája Hz. A fenti képlet szerinti ppm-ekben kifejezett kémiai eltolódások: CH 3 Br: 237 / 90 = 2,63 ppm, CH 2 Br 2 : 441 / 90 = 4,90 ppm, CHBr 3 : 614 / 90 = 6,82 ppm. A tetrametilszilánnak mind a protonjai, mind a szénmagjai viszonylag sűrű elektronfelhőben találhatók (a szilícium elektronegativitása kicsi): ez a sűrű elektronfelhő jelentősen árnyékolja a külső mágneses tér hatását. A legtöbb szerves vegyületben a protonok és a szénmagok árnyékoltsága a -ben tapasztaltaknál kisebb, így a szerves vegyületek túlnyomó többségének 1 H NMR és 13 C NMR jelei a spektrumokban hasonlóan a fenti 3 példához a -től balra, azaz pozitív δ-értékeknél találhatók, csak kevés vegyületnél figyelhetők meg negatív kémiai eltolódások. Mindezek alapján indokolt a -t a ppm-skála kiindulópontjának tekinteni.
4 4 A szerves vegyületekben található különböző kémiai környezetű 13 C magok kémiai eltolódása az esetek túlnyomó többségében ppm, míg a protonok kémiai eltolódása 0 13 ppm tartományba esik (megjegyzendő, hogy a két tartomány nem fed át egymással, mert a két mag gerjesztési frekvenciája távol van egymástól). Tipikus 13 C NMR eltolódások (az adatok tájékoztató jellegűek, csak a tendenciákat tükrözik): C = O, C = S C = C és aromás C telített C, oxigénhez kötve telített C, szénhez kötve ppm ppm ppm 50 0 ppm Az sp 3 hibridállapotú szenet tartalmazó CH 3 (metil), CH 2 (metilén) és CH (metin) csoportok protonjainak várható körülbelüli 1 H NMR kémiai eltolódását a következő durva becsléssel jósolhatjuk meg: - kiindulunk abból, hogy egy átlagos metilcsoport protonjainak kémiai eltolódása kb. 0,9 ppm, egy átlagos metiléncsoport protonjaié kb. 1,3 ppm, míg egy átlagos metincsoport protonjáé kb. 1,7 ppm; - ezekhez az eltolódásokhoz kb. 1 ppm-et kell hozzáadni, amennyiben az említett csoportokhoz a következők közül 1 kapcsolódik: -C=C, C CR, C N, -C=O, -SH, -SR; - az eltolódásokhoz kb. 1,5 ppm-et kell hozzáadni, amennyiben a fenti csoportokhoz a következők közül 1 kapcsolódik: -Ar (aromás), -NH 2, O - az eltolódásokhoz kb. 2 ppm-et kell hozzáadni, amennyiben a fenti csoportokhoz a következők közül 1 kapcsolódik: -OH, -OR, -NHC(O)R, -Cl, -Br, -I, -SO 2 R; - az eltolódásokhoz kb. 2,5 ppm-et kell hozzáadni, amennyiben a fenti csoportokhoz egy OAr csoport kapcsolódik; - az eltolódásokhoz kb. 3 ppm-et kell hozzáadni, amennyiben a fenti csoportokhoz a következők közül 1 kapcsolódik: -NO2, OC(O)R, -F. A közelítés csak durva becslést tesz lehetővé. Ha a CH 2 vagy CH csoportokhoz az említett funkciós csoportok közül több is kapcsolódik, a megadott tendenciák fokozottan érvényesülnek, de az eltolódás-változások nem additívak: lásd fentebb a CH 3 Br a CH 2 Br 2 és a CHBr 3 spektrumát. Olefinekben az sp 2 hibridállapotú szénatomokhoz közvetlenül kapcsolódó protonok hozzávetőleges eltolódás-tartománya 4,5 5,5 ppm, az aromás gyűrűhöz kapcsolódó protonok esetén ez az értéktartomány kb. 6,5 8 ppm, míg az acetilének sp hibridállapotú szénatomjához kapcsolódó proton rezonanciafrekvenciája kb. 2,5 ppm. A karbonilcsoporthoz közvetlenül kapcsolódó aldehidproton jele kb ppm között várható, míg a karboxilcsoport oxigénhez kapcsolódó protonja ppm közötti tartományban jelenhet meg. Általánosságban azt mondhatjuk, hogy egy molekula különböző kémiai környezetű 1 H vagy 13 C atommagjai a megadott tartományokon belül különböző helyeken adnak rezonanciajeleket (véletlen egybeesések időnként előfordulhatnak). A különböző kémiai környezetű magok számát egy molekulán belül a szerkezeti képlet szemrevételezésével, a molekula szimmetriaelemeinek alkalmazásával lehet megállapítani: ha az NMR felvétel körülményei között az egyszeres kötések körüli rotáció nem gátolt, elegendő a molekula legszimmetrikusabb (a gyakorlatban esetleg nem is megvalósuló) konformációját figyelembe venni. Az 1 H NMR spektroszkópiában egy molekula jeleinek integráljai arányosak az őket létrehozó protonok számával, így az 1 H NMR spektrumból megállapítható a különböző kémiai eltolódású jeleket létrehozó protonok számaránya. Ez a fajta integrálhatóság a 13 C NMR spektroszkópiában nem áll fenn. S R
5 5 Egy adott NMR-aktív mag megérzi a környezetében lévő NMR-aktív magok mágneses állapotát: a hatást a kötéseken keresztül az elektronrendszer közvetíti. Az egymással ilyen kapcsolatban lévő magokról azt mondjuk, hogy spin-spin csatolásban vannak. A csatolást a csatolási állandóval jellemezzük, aminek jele J. A csatolási állandó nagyságát hertzben adjuk meg. A csatolási állandókat aszerint is megkülönböztetjük, hogy hány kötésen át terjedő hatást írnak le. A CH 2 csoport azonos szénatomhoz kapcsolódó 2 protonja egymástól két kötésnyi távolságban van: H-C-H (geminális hidrogének). A csatolási állandó jelölése ez esetben: 2 J HH. A H-C-C-H szerkezeti részlet protonjai egymástól 3 kötésnyi távolságban vannak (vicinális hidrogének), csatolási állandójuk jelölése: 3 J HH. Konjugált vagy aromás rendszerek esetében a csatolás 3 kötésnél tovább is terjedhet. Hogyan értelmezhető a csatolás? Vegyünk pl. egymástól 3 kötésnyi távolságban levő két nagyon különböző kémiai környezetű protont, az egyiket jelöljük A, a másikat X betűvel(h A -C-C-H X ), utalva a jeleik kémiai eltolódása közötti nagy távolságra. Az A proton egy adott mágneses állapotához az X proton két lehetséges állapota tartozik: vagy az alapállapot, vagy a kicsit magasabb energiájú gerjesztett állapot. Attól függően, hogy az X proton melyik állapotban van, vagy egy kicsit erősíti, vagy egy kicsit gyengíti az A proton környezetében a külső mágneses tér hatását, ennek megfelelően az A proton X állapotától függően egy adott frekvencia helyett ennél vagy egy kicsit kisebb, vagy egy kicsit nagyobb frekvenciájú sugárzással gerjeszthető: így a spektrumban két egymáshoz közeli jelet kapunk az A protonra jellemző kémiai eltolódásnál. A jelek intenzitása 1 : 1, mivel annak a valószínűsége, hogy X proton alap- vagy gerjesztett állapotban van, gyakorlatilag 50 50% (az alap- és gerjesztett állapot közötti energiakülönbség olyan kicsi, hogy pl. 300 K hőmérsékleten 7,05 Tesla erősségű mágneses térben alapállapotú protonra gerjesztett állapotú proton jut: ez gyakorlatilag 1 : 1 arány). Az elmondottak az X proton vonatkozásában ugyanígy igazak, ennek megfelelően az X proton jele is megduplázódik.. AX- rendszer csatolásban 3 J AX 3 J AX AX- rendszer csatolás nélkül
6 6 Egyszerű kombinatorikai megfontolások alapján több protonból álló spinrendszerek csatolásai is jól leírhatók abban az esetben, ha a kémiai eltolódások elég messze vannak egymástól. Amennyiben a rezonanciafrekvenciákat az egyes protonokra hertzben adjuk meg, az egyes protonok hertzben kifejezett eltolódás-különbsége jóval nagyobb kell hogy legyen, mint az aktuális csatolási állandó: δ(hz) >> J(Hz). Ebben az esetben beszélünk elsőrendű csatolásról. Ha δ(hz) / J(Hz) < 5, a multiplikálódott jelek összecsúszhatnak, számítógép nélkül nehezen értelmezhető spektrumot adva. Elsőrendű csatolás esetén elmondhatjuk, hogy egy adott proton jele, ha az adott proton n darab azonos kémiai környezetű protonnal van csatolásban, (n + 1)-szeres felhasadást mutat. A felhasadt jelek intenzitásaránya I = ½ spinkvantumszámú magok ( 1 H, 13 C) esetén a Pascalháromszög segítségével vezethető le. A kiválasztott protonnal csatolásban lévő azonos kémiai A kiválasztott proton A felhasadt jel környezetű protonok jelének felhasadása részeinek intenzitásaránya száma (n + 1)-szeres n = 0 1 (szingulett, s ) 1 n = 1 2 (dublett, d ) 1 1 n = 2 3 (triplett, t ) n = 3 4 (kvartett, q ) n = 6 7 (szeptett) AX 2 - rendszer csatolásban AX 2 - rendszer csatolás nélkül
7 7 AX 3 - rendszer csatolásban AX 3 - rendszer csatolás nélkül A 2 X 2 - rendszer csatolásban A 2 X 2 - rendszer csatolás nélkül
8 8 A 2 X 3 - rendszer csatolásban A 2 X 3 - rendszer csatolás nélkül Elvileg heteroatomhoz kapcsolódó proton is lehet csatolásban szénhez kapcsolódó protonnal, pl. a következő szerkezeti részletben: H-O-C-H. Az ilyen csatolás kizárólag csak akkor valósul meg, ha a heteroatomhoz kapcsolódó proton nem vesz részt gyors kicserélődési folyamatokban (pl. az oldószer, vagy az oldószerben található víznyomok közreműködésével). Gyors protoncsere esetén csatolás nem észlelhető és a gyorsan cserélődő proton jele kiszélesedhet (mint pl. a karboxilcsoport protonjának 1 H NMR-jele. Az NMR spektroszkópiában nem csak azonos fajtájú NMR-aktív magok közötti úgynevezett homonukleáris csatolások képzelhetők el, megvalósulhatnak különböző fajtájú magok közötti úgynevezett heteronukleáris csatolások is. A természetes hidrogén 99,98%-ban 1 H izotópot, 0,016%-ban 2 H izotópot (deutériumot) tartalmaz. A deutérium is NMR-aktív, csatol is a protonokkal, de annak a valószínűsége igen csekély, hogy egy molekulában deutérium kerüljön megfelelő kötéstávolságra protontól, így az ehhez a heteronukleáris csatoláshoz tartozó jelek gyakorlatilag nem vehetők észre a rutin NMR spektrumban. A természetes szén 98,9%-ban tartalmazza az NMR-inaktív 12 C izotópot, míg az NMR-aktív 13 C izotóp 1,108%- ban fordul elő benne. Az előbbiekhez hasonlóan a 13 C izotóp kis százalékos aránya miatt a 13 C- 1 H csatolások csak igen kis intenzitású, alig észrevehető jelet adnak az 1 H NMR spektrumban. A 13 C NMR spektrumban a 13 C- 13 C homonukleáris csatolások hanyagolhatók el: kicsi a valószínűsége annak, hogy 1 molekulán belül két 13 C izotóp csatolási közelségbe kerüljön. A 13 C- 1 H heteronukleáris csatolásokat a 13 C NMR spektrum felvétele közben egy technikai trükkel kiküszöbölik. A fent elmondottaknak megfelelően tehát a rutin 13 C NMR spektrum annyi szingulettből áll, ahány különböző kémiai környezetű szénatomot tartalmaz a vizsgált molekula. A rutin 1 H NMR spektrumban viszont gyakorlatilag csak az 1 H- 1 H homonukleáris csatolások láthatók,
9 9 aminek következtében multiplettek jelennek meg. Elsőrendű csatolás esetén ha a kiválasztott proton több, de azonos kémiai környezetű protonnal áll kölcsönhatásban, a multiplettek alapján bizonyos csoportok könnyen azonosíthatók. Az alapképzés során csak ilyen egyszerű esetekkel foglalkozunk. Elsőrendű csatolás esetén: -CH 2 -CH 3 csoport (A 2 X 3 rendszer) kvartett-triplett -CH-CH 3 csoport (AX 3 rendszer) kvartett-dublett -CH 2 -CH 2 - csoport (A 2 X 2 rendszer) triplett-triplett -CH-CH 2 - csoport (AX 2 rendszer) triplett-dublett -CH(CH 3 ) 2 csoport (AX 6 rendszer) szeptett-dublett. Infravörös spektroszkópia A szerves molekulák az infravörös tartományba eső hullámhosszúságú elektromágneses sugárzással is kölcsönhatásba tudnak lépni. Ilyenkor a molekulák kvantált rezgési nívói gerjesztődnek (vegyértékrezgés és deformációs rezgés), ami azzal jár, hogy bizonyos frekvenciáknál a sugárzás abszorpciója következik be. Ez a spektrumokban (itt nem részletezett módon) elnyelési sávok megjelenéséhez vezet. Ezeknek a sávoknak a spektrumban elfoglalt helye bizonyos funkciós csoportok jelenlétére utal. A sávok helyét az IR spektrumban a hullámhossz reciprokában, hullámszámokban (cm -1 ) adják meg. Az IR spektrumok legintenzívebb sávjai a C = O csoport vegyértékrezgéséhez (kb cm -1 hullámszámnál), illetve az alkoholok, éterek, észterek és karbonsavak C O vegyértékrezgéséhez ( cm -1 ) köthetők. Jellegzetes még a karbonsavak O H vegyértékrezgésének cm -1 hullámszámok között megjelenő rendkívül széles, általában középerős sávja is. Tömegspektrometria A tömegspektrometriai mérések során a vizsgálandó mintát valamilyen módon ionizálják (a klasszikus elektron-impakt módszer esetén pl. nagy energiájú elektronokkal érik el az ionizációt) majd a keletkező molekulaiont (amennyiben ennek az élettartama elég hosszú) és / vagy az ennek szétesése során keletkező molekulatöredékeket, az úgynevezett fragmenseket detektálják tömegszám szerint. Szerkezet-meghatározás A szerkezet-meghatározás a tárgyalt 4 egymástól független vizsgálati módszer által szolgáltatott adatok összevetésén alapul: ha valakinek az egyik módszer adatai alapján kialakul egy hipotézise, meg kell vizsgálnia, hogy a többi független vizsgálatból nyert adatok ezt egyértelműen megerősítik-e. Ellentmondás-mentesség esetén valószínűsíthető egy szerkezet. A mellékelt spektrumokon a szerkezet-meghatározás az elmondottak alapján gyakorolható.
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
Műszeres analitika II. (TKBE0532) 7. előadás NMR spektroszkópia Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék NMR, Nuclear Magnetic
Spektroszkópiai módszerek 2.
 Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Spektroszkópiai módszerek 2. NMR spektroszkópia magspinek rendeződése külső mágneses tér hatására az eredő magspin nem nulla, ha a magot alkotó nukleonok közül legalább az egyik páratlan a szerves kémiában
Mi mindenről tanúskodik a Me-OH néhány NMR spektruma
 Mi mindenről tanúskodik a Me-OH néhány NMR spektruma lcélok és fogalmak: l- az NMR-rezonancia frekvencia (jel), a kémiai környezete, a kémiai eltolódás, l- az 1 H-NMR spektrum, l- az -OH és a -CH 3 csoportokban
Mi mindenről tanúskodik a Me-OH néhány NMR spektruma lcélok és fogalmak: l- az NMR-rezonancia frekvencia (jel), a kémiai környezete, a kémiai eltolódás, l- az 1 H-NMR spektrum, l- az -OH és a -CH 3 csoportokban
Mágneses módszerek a mőszeres analitikában
 Mágneses módszerek a mőszeres analitikában NMR, ESR: mágneses momentummal rendelkezı anyagok minıségi és mennyiségi meghatározására alkalmas analitikai módszer Atommag spin állapotok közötti energiaátmenetek:
Mágneses módszerek a mőszeres analitikában NMR, ESR: mágneses momentummal rendelkezı anyagok minıségi és mennyiségi meghatározására alkalmas analitikai módszer Atommag spin állapotok közötti energiaátmenetek:
Mágneses módszerek a műszeres analitikában
 Mágneses módszerek a műszeres analitikában NMR, ESR: mágneses momentummal rendelkező anyagok minőségi és mennyiségi meghatározására alkalmas Atommag spin állapotok közötti energiaátmenetek: NMR (magmágneses
Mágneses módszerek a műszeres analitikában NMR, ESR: mágneses momentummal rendelkező anyagok minőségi és mennyiségi meghatározására alkalmas Atommag spin állapotok közötti energiaátmenetek: NMR (magmágneses
Műszeres analitika II. (TKBE0532)
 Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Műszeres analitika II. (TKBE0532) 4. előadás Spektroszkópia alapjai Dr. Andrási Melinda Debreceni Egyetem Természettudományi és Technológiai Kar Szervetlen és Analitikai Kémiai Tanszék A fény elektromágneses
Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia?
 Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia? Prof. Túri László (ELTE, Kémiai Intézet) turi@chem.elte.hu 2012. november 19. Szent László Gimnázium Önképzőkör 1 Kapcsolódási pontok
Hogyan bírhatjuk szóra a molekulákat, avagy mi is az a spektroszkópia? Prof. Túri László (ELTE, Kémiai Intézet) turi@chem.elte.hu 2012. november 19. Szent László Gimnázium Önképzőkör 1 Kapcsolódási pontok
Elektronspinrezonancia (ESR) - spektroszkópia
 Elektronspinrezonancia (ESR) - spektroszkópia Paramágneses anyagok vizsgáló módszere. A mágneses momentum iránykvantáltságán alapul. A mágneses momentum energiája B indukciójú mágneses térben E m S μ z
Elektronspinrezonancia (ESR) - spektroszkópia Paramágneses anyagok vizsgáló módszere. A mágneses momentum iránykvantáltságán alapul. A mágneses momentum energiája B indukciójú mágneses térben E m S μ z
Tartalomjegyzék. Emlékeztetõ. Emlékeztetõ. Spektroszkópia. Fényelnyelés híg oldatokban 4/11/2016. A fény; Abszorpciós spektroszkópia
 Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2016 március 1.) Az abszorpció mérése;
Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2016 március 1.) Az abszorpció mérése;
Kémiai kötések. Kémiai kötések kj / mol 0,8 40 kj / mol
 Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Kémiai kötések A természetben az anyagokat felépítő atomok nem önmagukban, hanem gyakran egymáshoz kapcsolódva léteznek. Ezeket a kötéseket összefoglaló néven kémiai kötéseknek nevezzük. Kémiai kötések
Név... intenzitás abszorbancia moláris extinkciós. A Wien-féle eltolódási törvény szerint az abszolút fekete test maximális emisszióképességéhez
 A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
A Név... Válassza ki a helyes mértékegységeket! állandó intenzitás abszorbancia moláris extinkciós A) J s -1 - l mol -1 cm B) W g/cm 3 - C) J s -1 m -2 - l mol -1 cm -1 D) J m -2 cm - A Wien-féle eltolódási
Műszeres analitika. Abrankó László. Molekulaspektroszkópia. Kémiai élelmiszervizsgálati módszerek csoportosítása
 Abrankó László Műszeres analitika Molekulaspektroszkópia Minőségi elemzés Kvalitatív Cél: Meghatározni, hogy egy adott mintában jelen vannak-e bizonyos ismert komponensek. Vagy ismeretlen komponensek azonosítása
Abrankó László Műszeres analitika Molekulaspektroszkópia Minőségi elemzés Kvalitatív Cél: Meghatározni, hogy egy adott mintában jelen vannak-e bizonyos ismert komponensek. Vagy ismeretlen komponensek azonosítása
lásd: enantiotóp, diasztereotóp
 anizokrón anisochronous árnyékolási állandó shielding constant árnyékolási járulékok és empirikus értelmezésük shielding contributions diamágneses és paramágneses árnyékolás diamagnetic and paramagnetic
anizokrón anisochronous árnyékolási állandó shielding constant árnyékolási járulékok és empirikus értelmezésük shielding contributions diamágneses és paramágneses árnyékolás diamagnetic and paramagnetic
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 5. mérés: Elektronspin rezonancia. 2008. március 18.
 Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
Modern Fizika Labor Fizika BSc A mérés dátuma: 28. március 18. A mérés száma és címe: 5. mérés: Elektronspin rezonancia Értékelés: A beadás dátuma: 28. március 26. A mérést végezte: 1/7 A mérés leírása:
Kötések kialakítása - oktett elmélet
 Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek elsődleges kémiai kötések Kötések
Sugárzások kölcsönhatása az anyaggal
 Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Radioaktivitás Biofizika előadások 2013 december Sugárzások kölcsönhatása az anyaggal PTE ÁOK Biofizikai Intézet, Orbán József Összefoglaló radioaktivitás alapok Nukleononkénti kötési energia (MeV) Egy
Jegyzet. Kémia, BMEVEAAAMM1 Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens.
 Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Kémia, BMEVEAAAMM Műszaki menedzser hallgatók számára Dr Csonka Gábor, egyetemi tanár Dr Madarász János, egyetemi docens Jegyzet dr. Horváth Viola, KÉMIA I. http://oktatas.ch.bme.hu/oktatas/konyvek/anal/
Szerves vegyületek szerkezetfelderítése NMR spektroszkópia
 Szerves vegyületek szerkezetfelderítése NMR spektroszkópia Az anyag összeállításához Krajsovszky Gábor, Mátyus Péter és Perczel András diáit is felhasználtuk. 1 (hullámhossz) -sugárzás röntgensugárzás
Szerves vegyületek szerkezetfelderítése NMR spektroszkópia Az anyag összeállításához Krajsovszky Gábor, Mátyus Péter és Perczel András diáit is felhasználtuk. 1 (hullámhossz) -sugárzás röntgensugárzás
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel
 4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
4.2. Az Al(III) kölcsönhatása aszparaginsav-tartalmú peptidekkel A kisméretű peptidek közül az oldalláncban negatív töltésű karboxilcsoportokat tartalmazó AspAsp és AspAspAsp ligandumok komplexképződését
Kémiai kötések. Kémiai kötések. A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Kémiai kötések A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 Cl + Na Az ionos kötés 1. Cl + - + Na Klór: 1s 2 2s 2 2p 6 3s 2 3p 5 Kloridion: 1s2 2s2 2p6 3s2 3p6 Nátrium: 1s 2 2s
Bevezetés a modern fizika fejezeteibe. 4. (a) Kvantummechanika. Utolsó módosítás: november 15. Dr. Márkus Ferenc BME Fizika Tanszék
 Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Bevezetés a modern fizika fejezeteibe 4. (a) Kvantummechanika Utolsó módosítás: 2015. november 15. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Modern Fizika Labor. 12. Infravörös spektroszkópia. Fizika BSc. A mérés dátuma: okt. 04. A mérés száma és címe: Értékelés:
 Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor Fizika BSc A mérés dátuma: 011. okt. 04. A mérés száma és címe: 1. Infravörös spektroszkópia Értékelés: A beadás dátuma: 011. dec. 1. A mérést végezte: Domokos Zoltán Szőke Kálmán Benjamin
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia. 2008. május 6.
 Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia Értékelés: A beadás dátuma: 28. május 13. A mérést végezte: 1/5 A mérés célja A mérés célja az
Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 12. mérés: Infravörös spektroszkópia Értékelés: A beadás dátuma: 28. május 13. A mérést végezte: 1/5 A mérés célja A mérés célja az
Elektronegativitás. Elektronegativitás
 Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Általános és szervetlen kémia 3. hét Elektronaffinitás Az az energiaváltozás, ami akkor következik be, ha 1 mól gáz halmazállapotú atomból 1 mól egyszeresen negatív töltésű anion keletkezik. Mértékegysége:
Abszorpció, emlékeztetõ
 Hogyan készültek ezek a képek? PÉCI TUDMÁNYEGYETEM ÁLTALÁN RVTUDMÁNYI KAR Fluoreszcencia spektroszkópia (Nyitrai Miklós; február.) Lumineszcencia - elemi lépések Abszorpció, emlékeztetõ Energia elnyelése
Hogyan készültek ezek a képek? PÉCI TUDMÁNYEGYETEM ÁLTALÁN RVTUDMÁNYI KAR Fluoreszcencia spektroszkópia (Nyitrai Miklós; február.) Lumineszcencia - elemi lépések Abszorpció, emlékeztetõ Energia elnyelése
FELADATMEGOLDÁS. Tesztfeladat: Válaszd ki a helyes megoldást!
 FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
FELADATMEGOLDÁS Tesztfeladat: Válaszd ki a helyes megoldást! 1. Melyik sorozatban található jelölések fejeznek ki 4-4 g anyagot? a) 2 H 2 ; 0,25 C b) O; 4 H; 4 H 2 c) 0,25 O; 4 H; 2 H 2 ; 1/3 C d) 2 H;
Fizikai kémia Részecskék mágneses térben, ESR spektroszkópia. Részecskék mágneses térben. Részecskék mágneses térben
 06.08.. Fizikai kémia. 3. Részecskék mágneses térben, ESR spektroszkópia Dr. Berkesi Ottó SZTE Fizikai Kémiai és Anyagtudományi Tanszéke 05 Részecskék mágneses térben A részecskék mágneses térben ugyanúgy
06.08.. Fizikai kémia. 3. Részecskék mágneses térben, ESR spektroszkópia Dr. Berkesi Ottó SZTE Fizikai Kémiai és Anyagtudományi Tanszéke 05 Részecskék mágneses térben A részecskék mágneses térben ugyanúgy
Általános Kémia, BMEVESAA101
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Óravázlatok:
Fizikai kémia Mágneses magrezonancia spektroszkópia alapjai. Mágneses magrezonancia - NMR. Mágneses magrezonancia - NMR
 Fizikai kémia 2.. Mágneses magrezonancia spektroszkópia alapjai Dr. Berkesi Ottó SZTE Fizikai Kémiai és Anyagtudományi Tanszéke 205 Mágneses magrezonancia - NMR Amint azt a korábbiakban megismertük a molekulákban
Fizikai kémia 2.. Mágneses magrezonancia spektroszkópia alapjai Dr. Berkesi Ottó SZTE Fizikai Kémiai és Anyagtudományi Tanszéke 205 Mágneses magrezonancia - NMR Amint azt a korábbiakban megismertük a molekulákban
2, = 5221 K (7.2)
 7. Gyakorlat 4A-7 Az emberi szem kb. 555 nm hullámhossznál a Iegnagyobb érzékenységű. Adjuk meg annak a fekete testnek a hőmérsékletét, amely sugárzásának a spektrális teljesitménye ezen a hullámhosszon
7. Gyakorlat 4A-7 Az emberi szem kb. 555 nm hullámhossznál a Iegnagyobb érzékenységű. Adjuk meg annak a fekete testnek a hőmérsékletét, amely sugárzásának a spektrális teljesitménye ezen a hullámhosszon
A TÖMEGSPEKTROMETRIA ALAPJAI
 A TÖMEGSPEKTROMETRIA ALAPJAI web.inc.bme.hu/csonka/csg/oktat/tomegsp.doc alapján tömeg-töltés arány szerinti szétválasztás a legérzékenyebb módszerek közé tartozik (Nagyon kis anyagmennyiség kimutatására
A TÖMEGSPEKTROMETRIA ALAPJAI web.inc.bme.hu/csonka/csg/oktat/tomegsp.doc alapján tömeg-töltés arány szerinti szétválasztás a legérzékenyebb módszerek közé tartozik (Nagyon kis anyagmennyiség kimutatására
Tartalomjegyzék. Emlékeztetõ. Emlékeztetõ. Spektroszkópia. Fényelnyelés híg oldatokban A fény; Abszorpciós spektroszkópia
 Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2015 január 27.) Az abszorpció mérése;
Tartalomjegyzék PÉCS TUDOMÁNYEGYETEM ÁLTALÁNOS ORVOSTUDOMÁNY KAR A fény; Abszorpciós spektroszkópia Elektromágneses hullám kölcsönhatása anyaggal; (Nyitrai Miklós; 2015 január 27.) Az abszorpció mérése;
Fizikai kémia 2. ZH V. kérdések I. félévtől
 Fizikai kémia 2. ZH V. kérdések 2016-17 I. félévtől Szükséges adatok és állandók: k=1,38066 10-23 JK; c= 2,99792458 10 8 m/s; e= 1,602177 10-19 C; h=6,62608 10-34 Js; N A= 6,02214 10 23 mol -1 ; me= 9,10939
Fizikai kémia 2. ZH V. kérdések 2016-17 I. félévtől Szükséges adatok és állandók: k=1,38066 10-23 JK; c= 2,99792458 10 8 m/s; e= 1,602177 10-19 C; h=6,62608 10-34 Js; N A= 6,02214 10 23 mol -1 ; me= 9,10939
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár. Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár,
 Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Általános Kémia, BMEVESAA101 Dr Csonka Gábor, egyetemi tanár Az anyag Készítette: Dr. Csonka Gábor egyetemi tanár, csonkagi@gmail.com 1 Jegyzet Dr. Csonka Gábor http://web.inc.bme.hu/csonka/ Facebook,
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
A testek részecskéinek szerkezete
 A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
A testek részecskéinek szerkezete Minden test részecskékből, atomokból vagy több atomból álló molekulákból épül fel. Az atomok is összetettek: elektronok, protonok és neutronok találhatók bennük. Az elektronok
Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés
 Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés A gyakorlatra vigyenek magukkal pendrive-ot, amire a mérési adatokat átvehetik. Ajánlott irodalom: P. W. Atkins: Fizikai
Fizikai kémia és radiokémia labor II, Laboratóriumi gyakorlat: Spektroszkópia mérés A gyakorlatra vigyenek magukkal pendrive-ot, amire a mérési adatokat átvehetik. Ajánlott irodalom: P. W. Atkins: Fizikai
 http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
http://www.nature.com 1) Magerő-sugár: a magközéppontból mért távolság, ameddig a magerők hatótávolsága terjed. Rutherford-szórásból határozható meg. R=1,4 x 10-13 A 1/3 cm Az atommag terének potenciálja
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről
 A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
A kvantummechanika kísérleti előzményei A részecske hullám kettősségről Utolsó módosítás: 2016. május 4. 1 Előzmények Franck-Hertz-kísérlet (1) A Franck-Hertz-kísérlet vázlatos elrendezése: http://hyperphysics.phy-astr.gsu.edu/hbase/frhz.html
Az NMR spektroszkópia alapjai Dr. Rohonczy János ELTE Szervetlen Kémiai Tanszék
 Az NMR spektroszkópia alapjai Dr. Rohonczy János ELTE Szervetlen Kémiai Tanszék A mágneses magrezonancia spektroszkópia (röviden NMR angolul Nuclear Magnetic Resonace) egyike azon modern kémiai szerkezetvizsgálati
Az NMR spektroszkópia alapjai Dr. Rohonczy János ELTE Szervetlen Kémiai Tanszék A mágneses magrezonancia spektroszkópia (röviden NMR angolul Nuclear Magnetic Resonace) egyike azon modern kémiai szerkezetvizsgálati
Modern Fizika Labor Fizika BSC
 Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. március 2. A mérés száma és címe: 5. Elektronspin rezonancia Értékelés: A beadás dátuma: 2009. március 5. A mérést végezte: Márton Krisztina Zsigmond
Modern Fizika Labor Fizika BSC A mérés dátuma: 2009. március 2. A mérés száma és címe: 5. Elektronspin rezonancia Értékelés: A beadás dátuma: 2009. március 5. A mérést végezte: Márton Krisztina Zsigmond
Feladatok haladóknak
 Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
Feladatok haladóknak Szerkesztő: Magyarfalvi Gábor és Varga Szilárd (gmagyarf@chem.elte.hu, szilard.varga@bolyai.elte.hu) Feladatok A formai követelményeknek megfelelő dolgozatokat a nevezési lappal együtt
Szacharóz OH HO O O OH HO O OH HO OH HO 1
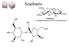 Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
Szacharóz 1 A jelek átfedése miatt oldószer váltás DMS helyett D2 Measured by... Evaluated by... NMR-01 Bruker Avance-500 103.59 92.08 81.28 DEPTq 300K ns=1k D2 115 110 105 100 95 90 85 80 75 70 65 60
Mézerek és lézerek. Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19.
 és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
és lézerek Berta Miklós SZE, Fizika és Kémia Tsz. 2006. november 19. Fény és anyag kölcsönhatása 2 / 19 Fény és anyag kölcsönhatása Fény és anyag kölcsönhatása E 2 (1) (2) (3) E 1 (1) gerjesztés (2) spontán
Dr. JUVANCZ ZOLTÁN Óbudai Egyetem Dr. FENYVESI ÉVA CycloLab Kft
 Dr. JUVANCZ ZOLTÁN Óbudai Egyetem Dr. FENYVESI ÉVA CycloLab Kft Atom- és molekula-spektroszkópiás módszerek Módszer Elv Vizsgált anyag típusa Atom abszorpciós spektrofotometria (AAS) A szervetlen Lángfotometria
Dr. JUVANCZ ZOLTÁN Óbudai Egyetem Dr. FENYVESI ÉVA CycloLab Kft Atom- és molekula-spektroszkópiás módszerek Módszer Elv Vizsgált anyag típusa Atom abszorpciós spektrofotometria (AAS) A szervetlen Lángfotometria
Abszorpciós fotometria
 A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
A fény Abszorpciós fotometria Ujfalusi Zoltán PTE ÁOK Biofizikai ntézet 2011. szeptember 15. E B x x Transzverzális hullám A fény elektromos térerősségvektor hullámhossz Az elektromos a mágneses térerősség
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések
 Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Sillabusz orvosi kémia szemináriumokhoz 1. Kémiai kötések Pécsi Tudományegyetem Általános Orvostudományi Kar 2010-2011. 1 A vegyületekben az atomokat kémiai kötésnek nevezett erők tartják össze. Az elektronok
Az atom- olvasni. 1. ábra Az atom felépítése 1. Az atomot felépítő elemi részecskék. Proton, Jele: (p+) Neutron, Jele: (n o )
 Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Az atom- olvasni 2.1. Az atom felépítése Az atom pozitív töltésű atommagból és negatív töltésű elektronokból áll. Az atom atommagból és elektronburokból álló semleges kémiai részecske. Az atommag pozitív
Az anyagi rendszerek csoportosítása
 Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
Kémia 1 A kémiai ismeretekről A modern technológiai folyamatok és a környezet védelmére tett intézkedések alig érthetőek kémiai tájékozottság nélkül. Ma már minden mérnök számára alapvető fontosságú a
1. mérés: Benzolszármazékok UV spektrofotometriás vizsgálata
 1. mérés: Benzolszármazékok UV spektrofotometriás vizsgálata A vegyi anyagok (atomok és molekulák) és az elektromágneses sugárzás kölcsönhatásának vizsgálata jelentős szerepet játszik ezen anyagok mind
1. mérés: Benzolszármazékok UV spektrofotometriás vizsgálata A vegyi anyagok (atomok és molekulák) és az elektromágneses sugárzás kölcsönhatásának vizsgálata jelentős szerepet játszik ezen anyagok mind
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését!
 I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
I. Atomszerkezeti ismeretek (9. Mozaik Tankönyv:10-30. oldal) 1. Részletezze az atom felépítését! Az atom az anyagok legkisebb, kémiai módszerekkel tovább már nem bontható része. Az atomok atommagból és
Abszorpciós spektroszkópia
 Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Tartalomjegyzék Abszorpciós spektroszkópia (Nyitrai Miklós; 2011 február 1.) Dolgozat: május 3. 18:00-20:00. Egész éves anyag. Korábbi dolgozatok nem számítanak bele. Felmentés 80% felett. A fény; Elektromágneses
Az atommag összetétele, radioaktivitás
 Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Az atommag összetétele, radioaktivitás Az atommag alkotórészei proton: pozitív töltésű részecske, töltése egyenlő az elektron töltésével, csak nem negatív, hanem pozitív: 1,6 10-19 C tömege az elektron
Kémiai kötés. Általános Kémia, szerkezet Dia 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Az elektromágneses hullámok
 203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
203. október Az elektromágneses hullámok PTE ÁOK Biofizikai Intézet Kutatók fizikusok, kémikusok, asztronómusok Sir Isaac Newton Sir William Herschel Johann Wilhelm Ritter Joseph von Fraunhofer Robert
Az Ampère-Maxwell-féle gerjesztési törvény
 Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
Az Ampère-Maxwell-féle gerjesztési törvény Maxwell elméleti meggondolások alapján feltételezte, hogy a változó elektromos tér örvényes mágneses teret kelt (hasonlóan ahhoz ahogy a változó mágneses tér
7. osztály Hevesy verseny, megyei forduló, 2003.
 Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
Figyelem! A feladatokat ezen a feladatlapon oldd meg! Megoldásod olvasható és áttekinthető legyen! A feladatok megoldásában a gondolatmeneted követhető legyen! A feladatok megoldásához használhatod a periódusos
KÉMIA FELVÉTELI DOLGOZAT
 KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
KÉMIA FELVÉTELI DOLGOZAT I. Egyszerű választásos teszt Karikázza be az egyetlen helyes, vagy egyetlen helytelen választ! 1. Hány neutront tartalmaz a 127-es tömegszámú, 53-as rendszámú jód izotóp? A) 74
Szilárdtestek sávelmélete. Sávelmélet a szabadelektron-modell alapján
 Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
Szilárdtestek sávelmélete Sávelmélet a szabadelektron-modell alapján A Fermi Dirac statisztika alapjai Nagy részecskeszámú rendszerek fizikai jellemzéséhez statisztikai leírást kell alkalmazni. (Pl. gázokra
OPTIKA. Fénykibocsátás mechanizmusa fényforrás típusok. Dr. Seres István
 OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
OPTIKA Fénykibocsátás mechanizmusa Dr. Seres István Bohr modell Niels Bohr (19) Rutherford felfedezte az atommagot, és igazolta, hogy negatív töltésű elektronok keringenek körülötte. Niels Bohr Bohr ezt
Energiaminimum- elve
 Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
Energiaminimum- elve Minden rendszer arra törekszi, hogy stabil állapotba kerüljön. Milyen kapcsolat van a stabil állapot, és az adott állapot energiája között? Energiaminimum elve Energiaminimum- elve
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyző jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyző jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
Az anyagi rendszer fogalma, csoportosítása
 Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Az anyagi rendszer fogalma, csoportosítása A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 1 1 A rendszer fogalma A körülöttünk levő anyagi világot atomok, ionok, molekulák építik
Szerves Kémiai Problémamegoldó Verseny
 Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Szerves Kémiai Problémamegoldó Verseny 2015. április 24. Név: E-mail cím: Egyetem: Szak: Képzési szint: Évfolyam: Pontszám: Név: Pontszám: / 3 pont 1. feladat Egy C 4 H 10 O 3 összegképletű vegyület 0,1776
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet
 Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
Atommodellek de Broglie hullámhossz Davisson-Germer-kísérlet Utolsó módosítás: 2016. május 4. 1 Előzmények Az atomok színképe (1) A fehér fény komponensekre bontható: http://en.wikipedia.org/wiki/spectrum
5.4. Elektronspektroszkópia
 5.4. Elektronspektroszkópia Két módszer: UV-VIS spektroszkópia: M + hν M PES, XPS (ESCA): M + hν M + + e 5.4.1. UV-VIS ultraibolya-látható spektroszkópia Alapelvek: l. fizikai kémia és műszeres analitika
5.4. Elektronspektroszkópia Két módszer: UV-VIS spektroszkópia: M + hν M PES, XPS (ESCA): M + hν M + + e 5.4.1. UV-VIS ultraibolya-látható spektroszkópia Alapelvek: l. fizikai kémia és műszeres analitika
Minta feladatsor. Az ion neve. Az ion képlete O 4. Szulfátion O 3. Alumíniumion S 2 CHH 3 COO. Króm(III)ion
 Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
Minta feladatsor A feladatok megoldására 90 perc áll rendelkezésére. A megoldáshoz zsebszámológépet használhat. 1. Adja meg a következő ionok nevét, illetve képletét! (8 pont) Az ion neve.. Szulfátion
6. változat. 3. Jelöld meg a nem molekuláris szerkezetű anyagot! A SO 2 ; Б C 6 H 12 O 6 ; В NaBr; Г CO 2.
 6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
6. változat Az 1-től 16-ig terjedő feladatokban négy válaszlehetőség van, amelyek közül csak egy helyes. Válaszd ki a helyes választ és jelöld be a válaszlapon! 1. Jelöld meg azt a sort, amely helyesen
Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei
 Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Gazdálkodási modul Gazdaságtudományi ismeretek I. Közgazdasá Adatgyűjtés, mérési alapok, a környezetgazdálkodás fontosabb műszerei KÖRNYEZETGAZDÁLKODÁSI
4.3. Az AcLysSerProValValGluGly heptapeptid Al(III)-kötő sajátságának jellemzése
 4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
4.3. Az AcLysProValValGly heptapeptid Al(III)-kötő sajátságának jellemzése Az Al(III)fehérje kölcsönhatás megismerése céljából olyan neurofilamentum peptidfragmenst vizsgáltunk, mely az oldalláncban oxigén
Modern fizika vegyes tesztek
 Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
Modern fizika vegyes tesztek 1. Egy fotonnak és egy elektronnak ugyanakkora a hullámhossza. Melyik a helyes állítás? a) A foton lendülete (impulzusa) kisebb, mint az elektroné. b) A fotonnak és az elektronnak
MÁGNESES MAGREZONANCIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN
 MÁGNESES MAGREZONANIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN 1) A jelenség 2) Nuclear Magnetic Resonance (NMR) 3) Magnetic Resonance Imaging (MRI) 4) Magnetic Resonance Spectroscopy (MRS) NMR
MÁGNESES MAGREZONANIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN 1) A jelenség 2) Nuclear Magnetic Resonance (NMR) 3) Magnetic Resonance Imaging (MRI) 4) Magnetic Resonance Spectroscopy (MRS) NMR
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben?
 Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
Szentjánosbogár, trópusi halak, sarki fény Mi a közös a természet fénytüneményeiben? Szalay Péter egyetemi tanár ELTE, Kémiai Intézet Elméleti Kémiai Laboratórium Van közös bennük? Egy kis történelem
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
A kémiai kötés magasabb szinten 13-1 Mit kell tudnia a kötéselméletnek? 13- Vegyérték kötés elmélet 13-3 Atompályák hibridizációja 13-4 Többszörös kovalens kötések 13-5 Molekulapálya elmélet 13-6 Delokalizált
Atomfizika. Az atommag szerkezete. Radioaktivitás Biofizika, Nyitrai Miklós
 Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
Atomfizika. Az atommag szerkezete. Radioaktivitás. 2010. 10. 13. Biofizika, Nyitrai Miklós Összefoglalás Atommag alkotói, szerkezete; Erős vagy magkölcsönhatás; Tömegdefektus. A kölcsönhatások világképe
1. feladat. Versenyző rajtszáma:
 1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
1. feladat / 4 pont Válassza ki, hogy az 1 és 2 anyagok közül melyik az 1,3,4,6-tetra-O-acetil-α-D-glükózamin hidroklorid! Rajzolja fel a kérdésben szereplő molekula szerkezetét, és értelmezze részletesen
Heterociklusos vegyületek
 Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Szerves kémia A gyűrű felépítésében más atom (szénatomon kívül!), ún. HETEROATOM is részt vesz. A gyűrűt alkotó heteroatomként leggyakrabban a nitrogén, oxigén, kén szerepel, (de ismerünk arzént, szilíciumot,
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008.
 Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Radiokémia vegyész MSc radiokémia szakirány Kónya József, M. Nagy Noémi: Izotópia I és II. Debreceni Egyetemi Kiadó, 2007, 2008. Kiss István,Vértes Attila: Magkémia (Akadémiai Kiadó) Nagy Lajos György,
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
Kémiai kötés 12-1 Lewis elmélet 12-2 Kovalens kötés: bevezetés 12-3 Poláros kovalens kötés 12-4 Lewis szerkezetek 12-5 A molekulák alakja 12-6 Kötésrend, kötéstávolság 12-7 Kötésenergiák Általános Kémia,
R nem hidrogén, hanem pl. alkilcsoport
 1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
1 Minimumkövetelmények C 4 metán C 3 - metilcsoport C 3 C 3 C 3 metil kation metilgyök metil anion C 3 -C 3 C 3 -C 2 - C 3 -C 2 C 3 -C 2 C 3 -C 2 C 2 5 - C 2 5 C 2 5 C 2 5 etán etilcsoport etil kation
Termokémia. Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011
 Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
Termokémia Hess, Germain Henri (1802-1850) A bemutatót összeállította: Fogarasi József, Petrik Lajos SZKI, 2011 A reakcióhő fogalma A reakcióhő tehát a kémiai változásokat kísérő energiaváltozást jelenti.
MÁGNESES MAGREZONANCIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN
 MÁGNESES MAGREZONANIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN 1) A jelenség 2) Nuclear Magnetic Resonance (NMR) 3) Magnetic Resonance Imaging (MRI) 4) Magnetic Resonance Spectroscopy (MRS) NMR
MÁGNESES MAGREZONANIA A KÉMIÁBAN, GYÓGYSZERÉSZETBEN, ORVOSTUDOMÁNYBAN 1) A jelenség 2) Nuclear Magnetic Resonance (NMR) 3) Magnetic Resonance Imaging (MRI) 4) Magnetic Resonance Spectroscopy (MRS) NMR
Kémiai kötés. Általános Kémia, szerkezet Slide 1 /39
 Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Kémiai kötés 4-1 Lewis elmélet 4-2 Kovalens kötés: bevezetés 4-3 Poláros kovalens kötés 4-4 Lewis szerkezetek 4-5 A molekulák alakja 4-6 Kötésrend, kötéstávolság 4-7 Kötésenergiák Általános Kémia, szerkezet
Abszorpciós fotometria
 abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
abszorpció Abszorpciós fotometria Spektroszkópia - Színképvizsgálat Spektro-: görög; jelente kép/szín -szkópia: görög; néz/látás/vizsgálat Ujfalusi Zoltán PTE ÁOK Biofizikai Intézet 2012. február Vizsgálatok
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS
 Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
Kémiai kötések és kristályrácsok ISMÉTLÉS, GYAKORLÁS Milyen képlet adódik a következő atomok kapcsolódásából? Fe - Fe H - O P - H O - O Na O Al - O Ca - S Cl - Cl C - O Ne N - N C - H Li - Br Pb - Pb N
A kémiai kötés magasabb szinten
 A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
A kémiai kötés magasabb szinten 11-1 Mit kell tudnia a kötéselméletnek? 11- Vegyérték kötés elmélet 11-3 Atompályák hibridizációja 11-4 Többszörös kovalens kötések 11-5 Molekulapálya elmélet 11-6 Delokalizált
Abszorpciós spektrometria összefoglaló
 Abszorpciós spektrometria összefoglaló smétlés: fény (elektromágneses sugárzás) tulajdonságai, kettős természet fény anyag kölcsönhatás típusok (reflexió, transzmisszió, abszorpció, szórás) Abszorpció
Abszorpciós spektrometria összefoglaló smétlés: fény (elektromágneses sugárzás) tulajdonságai, kettős természet fény anyag kölcsönhatás típusok (reflexió, transzmisszió, abszorpció, szórás) Abszorpció
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK. Kalocsai Angéla, Kozma Enikő
 ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
ATOMMODELLEK, SZÍNKÉP, KVANTUMSZÁMOK Kalocsai Angéla, Kozma Enikő RUTHERFORD-FÉLE ATOMMODELL HIBÁI Elektromágneses sugárzáselmélettel ellentmondásban van Mivel: a keringő elektronok gyorsulnak Energiamegmaradás
T I T - M T T. Hevesy György Kémiaverseny. A megyei forduló feladatlapja. 7. osztály. A versenyz jeligéje:... Megye:...
 T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
T I T - M T T Hevesy György Kémiaverseny A megyei forduló feladatlapja 7. osztály A versenyz jeligéje:... Megye:... Elért pontszám: 1. feladat:... pont 2. feladat:... pont 3. feladat:... pont 4. feladat:...
2. ZH IV I.
 Fizikai kémia 2. ZH IV. kérdések 2018-19. I. félévtől Szükséges adatok és állandók: k=1,38066 10-23 JK; c= 2,99792458 10 8 m/s; e= 1,602177 10-19 C; h=6,62608 10-34 Js; N A= 6,02214 10 23 mol -1 ; me=
Fizikai kémia 2. ZH IV. kérdések 2018-19. I. félévtől Szükséges adatok és állandók: k=1,38066 10-23 JK; c= 2,99792458 10 8 m/s; e= 1,602177 10-19 C; h=6,62608 10-34 Js; N A= 6,02214 10 23 mol -1 ; me=
Alkalmazás a makrókanónikus sokaságra: A fotongáz
 Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
Alkalmazás a makrókanónikus sokaságra: A fotongáz A fotonok az elektromágneses sugárzás hordozó részecskéi. Spinkvantumszámuk S=, tehát kvantumstatisztikai szempontból bozonok. Fotonoknak habár a spinkvantumszámuk,
Adatgyőjtés, mérési alapok, a környezetgazdálkodás fontosabb mőszerei
 GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
GazdálkodásimodulGazdaságtudományismeretekI.Közgazdaságtan KÖRNYEZETGAZDÁLKODÁSIMÉRNÖKIMScTERMÉSZETVÉDELMIMÉRNÖKIMSc Tudományos kutatásmódszertani, elemzési és közlési ismeretek modul Adatgyőjtés, mérési
Általános és szervetlen kémia 3. hét Kémiai kötések. Kötések kialakítása - oktett elmélet. Lewis-képlet és Lewis szerkezet
 Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Általános és szervetlen kémia 3. hét Kémiai kötések Az elemek és vegyületek halmazai az atomok kapcsolódásával - kémiai kötések kialakításával - jönnek létre szabad atomként csak a nemesgázatomok léteznek
Modern Fizika Labor. A mérés száma és címe: A mérés dátuma: Értékelés: Infravörös spektroszkópia. A beadás dátuma: A mérést végezte:
 Modern Fizika Labor A mérés dátuma: 2005.10.26. A mérés száma és címe: 12. Infravörös spektroszkópia Értékelés: A beadás dátuma: 2005.11.09. A mérést végezte: Orosz Katalin Tóth Bence 1 A mérés során egy
Modern Fizika Labor A mérés dátuma: 2005.10.26. A mérés száma és címe: 12. Infravörös spektroszkópia Értékelés: A beadás dátuma: 2005.11.09. A mérést végezte: Orosz Katalin Tóth Bence 1 A mérés során egy
Stern Gerlach kísérlet. Készítette: Kiss Éva
 Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Stern Gerlach kísérlet Készítette: Kiss Éva Történelmi áttekintés 1890. Thomson-féle atommodell ( mazsolás puding ) 1909-1911. Rutherford modell (bolygó hasonlat) Bohr-féle atommodell Frank-Hertz kísérlet
Modern Fizika Labor. Fizika BSc. Értékelés: A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n. 2008. április 29.
 Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
Modern Fizika Labor Fizika BSc A mérés dátuma: A mérés száma és címe: 13. mérés: Molekulamodellezés PC-n Értékelés: A beadás dátuma: 2008. május 6. A mérést végezte: 1/5 A mérés célja A mérés célja az
Kormeghatározás gyorsítóval
 Beadás határideje 2012. január 31. A megoldásokat a kémia tanárodnak add oda! 1. ESETTANULMÁNY 9. évfolyam Olvassa el figyelmesen az alábbi szöveget és válaszoljon a kérdésekre! Kormeghatározás gyorsítóval
Beadás határideje 2012. január 31. A megoldásokat a kémia tanárodnak add oda! 1. ESETTANULMÁNY 9. évfolyam Olvassa el figyelmesen az alábbi szöveget és válaszoljon a kérdésekre! Kormeghatározás gyorsítóval
Mit tanultunk kémiából?2.
 Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
Mit tanultunk kémiából?2. Az anyagok rendkívül kicsi kémiai részecskékből épülnek fel. Több milliárd részecske Mól az anyagmennyiség mértékegysége. 1 mol atom= 6. 10 23 db atom 600.000.000.000.000.000.000.000
Lumineszcencia. Lumineszcencia. mindenütt. Lumineszcencia mindenütt. Lumineszcencia mindenütt. Alapjai, tulajdonságai, mérése. Kellermayer Miklós
 Alapjai, tulajdonságai, mérése Kellermayer Miklós Fotolumineszcencia Radiolumineszcencia Fotolumineszcencia Radiolumineszcencia Aurora borrealis (sarki fény) Biolumineszcencia GFP-egér Biolumineszcencia
Alapjai, tulajdonságai, mérése Kellermayer Miklós Fotolumineszcencia Radiolumineszcencia Fotolumineszcencia Radiolumineszcencia Aurora borrealis (sarki fény) Biolumineszcencia GFP-egér Biolumineszcencia
Orvosi Biofizika I. 12. vizsgatétel. IsmétlésI. -Fény
 Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
Orvosi iofizika I. Fénysugárzásanyaggalvalókölcsönhatásai. Fényszóródás, fényabszorpció. Az abszorpciós spektrometria alapelvei. (Segítséga 12. tételmegértéséhezésmegtanulásához, továbbá a Fényabszorpció
